1. Кислотно-основные свойства веществ
1.1. Оксиды
Оксидами называются сложные вещества, состоящие из двух элементов, одним из которых является кислород.
Название оксида составляют из слова «оксид» и названия элемента в родительном падеже. Если элемент, образующий оксид, имеет постоянную степень окисления, то ее не указывают в названии оксида. Например, MgO – оксид магния, Al2O3 – оксид алюминия. Если элемент образует несколько оксидов, то после названия оксида в скобках римской цифрой указывают степень окисления элемента: SnO – оксид олова (II), SnO2 – оксид олова (IV).
По числу атомов кислорода в молекуле оксиды иногда называют: PbO2 – диоксид свинца, SO3 – триоксид серы.
Особую группу составляют пероксиды,
которые содержат пероксидную группу
–О–О–: Н
Оксиды делятся на несолеобразующие и солеобразующие.
Несолеобразующие оксиды (безразличные или индифферентные) – это оксиды, которым в качестве гидроксидов не соответствуют ни основания, ни кислоты. Например: СО, NO, N2O.
Солеобразующие оксиды делятся на основные, кислотные и амфотерные. Солеобразующие оксиды обладают способностью образовывать соли.
Основные оксиды
Основными называются оксиды, которым в качестве гидроксидов соответствуют основания:
К2О КОН, СаО Са(ОН)2.
Основные оксиды обычно образованы типичными металлами со степенями окисления:
+1: K2O, Li2O, Na2O, Rb2O, Cs2O, Cu2O, Ag2
O, Tl2O;+2: CaO, BaO, SrO, MnO, FeO, MgO, NiO, TiO;
+3: (иногда) Bi2O3, La2O3, Ti2O3.
Способы получения основных оксидов:
— окислением металлов
2Fe + O2 = 2FeO;
— разложением оснований и солей при нагревании
Ca(OH)2 = CaO + H2O;
MgCO3 = MgO + CO2↑;
— оксиды серебра и ртути получают разложением их гидроксидов в момент образования:
2AgNO3 + 2NaOH = Ag2O + H2O + 2NaNO3;
Hg(NO3)2 + 2NaOH = HgO + H2O + 2NaNO3.
Химические свойства основных оксидов:
— взаимодействие с водой оксидов щелочных (Li, Na, K, Rb, Cs) и щелочноземельных металлов (Ca, Sr, Ba) с образованием щелочей:
СаО + Н2О = Са(ОН)2;
К2О + Н2О = 2КОН;
— взаимодействие с кислотами
MgO + H2SO4 = MgSO4 + H2O;
— взаимодействие с кислотными оксидами
ВаО + СО2 = ВаСО3.
Кислотные оксиды
Кислотными называются оксиды, которым в качестве гидроксидов соответствуют кислоты:
N2O5 HNO3; CO2 H2CO3.
Кислотные оксиды – это оксиды неметаллов (P2O5, B2O3, Cl2O7) и некоторых металлов, проявляющих высокие степени окисления:
+5, +6, +7 (Nb 2O5, MoO3, Mn2O7).
Способы получения кислотных оксидов:
— окислением неметаллов и сложных веществ:
S + O2 = SO2;
CH4 + 2O2 = CO2 + 2H2O;
— разложением кислот и солей:
BaCO3 = BaO + CO2;
H2CO3 = H2O + CO2;
Химические свойства кислотных оксидов:
— взаимодействие с водой
P2O5 + 3H2O = 2H3PO4.
Некоторые кислотные оксиды с водой не взаимодействуют, например, SiO2;
— взаимодействие со щелочами
СО2 + Ва(ОН)
— взаимодействие с основными оксидами
СаО + СО2 = СаСО3.
Амфотерные оксиды
Амфотерными называются оксиды, которым в качестве гидроксидов соответствуют и основания, и кислоты, например
H2ZnO2 ZnO Zn(OH)2
кислота оксид цинка основание
H2[Zn(OH)4]
Амфотерные оксиды – это оксиды металлов со степенями окисления:
+2: BeO, ZnO, SnO, PbO, CuO, GeO;
+3: Al2O3, Sb2O3, Cr2O3, Fe2O3, Ga2O3;
+4: SnO2, PbO2, GeO2.
Амфотерные оксиды взаимодействуют:
— с кислотами и кислотными оксидами, проявляя основные свойства:
PbO + 2HNO3 = Pb(NO3)2 + H2O;
PbO + CO2 = PbCO3;
— со щелочами и основными оксидами, проявляя кислотные свойства:
Al2O3 + 2NaOH = 2NaAlO2 + H2O;
Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4];
Al2O3 + BaO = Ba(AlO2)2.
Амфотерность — Википедия
Амфоте́рность (от др.-греч. ἀμφότεροι «двоякий, двойственный; обоюдный») — способность некоторых химических веществ и соединений проявлять в зависимости от условий как кислотные, так и осно́вные свойства.
Понятие амфоте́рность как характеристика двойственного поведения вещества было введено в 1814 г. Ж. Гей-Люссаком и Л. Тенаром. А. Ганч в рамках общей химической теории кислотно-основных взаимодействий (1917-1927 гг.) определил амфоте́рность как «
Амфотерны гидроксиды таких элементов главных подгрупп, как бериллий, алюминий, галлий, мышьяк, сурьма, селен и др., таких элементов побочных подгрупп как хром, цинк, молибден, вольфрам и многих других. Обычно в химическом поведении гидроксидов преобладает или кислотный, или основный характер[2].
Амфотерность как химическое свойство[править | править код]
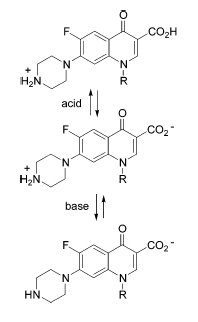
Амфотерность как химическое свойство вещества может проявляться по-разному:
1. В рамках теории электролитической диссоциации это способность вещества к электролитической диссоциации как по механизму кислот (с отщеплением ионов гидроксония, H + ), так и по механизму оснований (отщепление гидроксид-ионов, OH– ). Электролиты, которые в растворе ионизируются одновременно по кислотному и основному типам называются амфолитами[3]. Если обозначить амфотерный электролит формулой XOH, то его диссоциацию можно описать схемой:
- H++XO−⇄XOH⇄X++OH−{\displaystyle {\mathsf {H^{+}+XO^{-}\rightleftarrows XOH\rightleftarrows X^{+}+OH^{-}}}}
Например, кислотно-основные свойства азотистой кислоты определяются равновесными процессами диссоциации с образованием нитрит-аниона и нитрозильного катиона:
- HNO2⇄H++NO2− Ka≈10−5{\displaystyle {\mathsf {HNO_{2}\rightleftarrows H^{+}+NO_{2}^{-}\ \ K_{a}\approx 10^{-5}}}}
- HNO2⇄NO++OH− Kb≈10−7{\displaystyle {\mathsf {HNO_{2}\rightleftarrows NO^{+}+OH^{-}\ \ K_{b}\approx 10^{-7}}}}
Идеальным амфолитом будет вода:
- h3O⇄H++OH−{\displaystyle {\mathsf {H_{2}O\rightleftarrows H^{+}+OH^{-}}}}
Также к числу идеальных амфолитов относят гидроксид галлия Ga(OH)3, вторые и третьи константы диссоциации которого по кислотному и основному типам практически одинаковы[2].
2. В рамках протолитической теории Брёнстеда-Лоури проявление амфотерности рассматривается как способность протолита выступать донором и акцептором протона. Например, для воды амфотерность проявляется как автопротолиз[4]:
- 2h3O→h4O++OH−{\displaystyle {\mathsf {2H_{2}O\rightarrow H_{3}O^{+}+OH^{-}}}}
Амфолитами также будут вещества, имеющие в своём составе функциональные группы, способные быть донорами и акцепторами протонов. Например, к амфотерным органическим электролитам относятся белки, пептиды и аминокислоты. Так аминокислоты имеют в своём составе, по крайней мере, карбоксильную группу –COOH и аминогруппу –NH2. В растворе эти группы подвергаются частичной ионизации:
- h3N-CH(R)-COOH+h3O⇄h3N-CH(R)-COO−+h4O+{\displaystyle {\mathsf {H_{2}N{\text{-}}CH(R){\text{-}}COOH+H_{2}O\rightleftarrows H_{2}N{\text{-}}CH(R){\text{-}}COO^{-}+H_{3}O^{+}}}}
- h3N-CH(R)-COOH+h3O⇄[h4N-CH(R)-COOH]++OH−{\displaystyle {\mathsf {H_{2}N{\text{-}}CH(R){\text{-}}COOH+H_{2}O\rightleftarrows [H_{3}N{\text{-}}CH(R){\text{-}}COOH]^{+}+OH^{-}}}}
Таким образом, молекула аминокислоты находится в двух равновесных формах, заряженной (цвиттер-ион) и незаряженной. В этих комбинациях R–COOH и R–NH3+ являются потенциальными кислотами (донорами протонов, катионов), а R–COO– и R–NH2 – сопряженными потенциальными основаниями (акцепторами протонов, катионов).
3. Амфотерность может проявляться как способность вещества к взаимодействию как с кислотами, так и с основаниями. Это характерно для оксидов, гидроксидов и комплексных соединений некоторых p-элементов и большинства d-элементов в промежуточных степенях окисления. Амфотерность в той или иной степени является общим свойством гидроксидов[3]. Например, для соединений хрома (III) известны реакции[5]:
- Cr(OH)3+3HCl→CrCl3+3h3O{\displaystyle {\mathsf {Cr(OH)_{3}+3HCl\rightarrow CrCl_{3}+3H_{2}O}}}
- Cr(OH)3+3NaOH→Na3[Cr(OH)6]{\displaystyle {\mathsf {Cr(OH)_{3}+3NaOH\rightarrow Na_{3}[Cr(OH)_{6}]}}}
- Cr2O3+6HCl→2CrCl3+3h3O{\displaystyle {\mathsf {Cr_{2}O_{3}+6HCl\rightarrow 2CrCl_{3}+3H_{2}O}}}
- Cr2O3+2NaOH→ot2NaCrO2+h3O{\displaystyle {\mathsf {Cr_{2}O_{3}+2NaOH{\xrightarrow[{}]{^{o}t}}2NaCrO_{2}+H_{2}O}}}
Не соответствуют действительности традиционные представления о проявлении амфотерности гидроксидов как диссоциации по кислотному и основному типам[2]. В общем виде амфотерное поведение нерастворимых гидроксидов хрома (III), алюминия, цинка может быть описано как реакции ионного обмена ионов среды с лигандами H2O и OH–. Например, для Al(OH)3 ионные равновесия могут быть записаны следующим образом:
- [Al(OH)3(h3O)3]+3h4O+⇄[Al(h3O)6]3++3h3O{\displaystyle {\mathsf {[Al(OH)_{3}(H_{2}O)_{3}]+3H_{3}O^{+}\rightleftarrows [Al(H_{2}O)_{6}]^{3+}+3H_{2}O}}}
- [Al(OH)3(h3O)3]+3OH−⇄[Al(OH)6]3−+3h3O{\displaystyle {\mathsf {[Al(OH)_{3}(H_{2}O)_{3}]+3OH^{-}\rightleftarrows [Al(OH)_{6}]^{3-}+3H_{2}O}}}
4. В ряде случаев важным косвенным признаком амфотерности является способность элемента образовывать два ряда солей, катионного и анионного типа[6]. Например, для цинка: ZnCl2, [Zn(H2O)4]SO4 (катионные) и Na2ZnO2, Na2(Zn(OH)4) (анионные).
- Амфотерные гидроксиды и их поведение в водных растворах / Корольков Д. В. Основы неорганической химии. — М.: Просвещение, 1982. — 271 с.
- Кислотные и основные свойства / Общая химия. Под ред. Е. М. Соколовской и Л. С. Гузея. — М.: Изд-во Моск. ун-та, 1989. — 640 с. ун-та, 1989. — 640 с
- ↑ Танганов Б.Б. Химические методы анализа. — Улан-Удэ, 2005.- 550 с.
- ↑ 1 2 3 Амфотерные гидроксиды и их поведение в водных растворах / Корольков Д. В. Основы неорганической химии. — М.: Просвещение, 1982. — 271 с.
- ↑ 1 2 Угай Я. А. Общая и неорганическая химия. — М.: Высшая школа, 1997. — 527 с.
- ↑ Автопротолиз воды / Жуков С. Т. Химия. 8-9 класс
- ↑ Лидин Р. А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ. – М.: Химия, 2000. – 480 с.: ил.
- ↑ Кислотные и основные свойства / Общая химия. Под ред. Е. М. Соколовской и Л. С. Гузея. — М.: Изд-во Моск. ун-та, 1989. — 640 с. ун-та, 1989. — 640 с .
Амфотерные соединения | Дистанционные уроки
05-Дек-2014 | комментария 4 | Лолита Окольнова
и их свойства

Автор статьи — Саид Лутфуллин
Химия – это всегда единство противоположностей.
Посмотрите на периодическую систему.
Некоторые элементы (почти все металлы, проявляющие степени окисления +1 и +2) образуют основные оксиды и гидроксиды. Например, калий образует оксид K2O, и гидроксид KOH. Они проявляют основные свойства, например взаимодействуют с кислотами.
K2O + HCl → KCl + h3O
Некоторые элементы (большинство неметаллов и металлы со степенями окисления +5, +6, +7) образуют кислотные оксиды и гидроксиды. Кислотные гидроксиды – это кислородсодержащие кислоты, их называют гидроксидами, потому что в строении есть гидроксильная группа, например, сера образует кислотный оксид SO3 и кислотный гидроксид H2SO4 (серную кислоту):

Такие соединения проявляют кислотные свойства, например они реагируют с основаниями:
h3SO4 + 2KOH → K2SO4 + 2h3O
А есть элементы, образующие такие оксиды и гидроксиды, которые проявляют и кислотные, и основные свойства. Это явление называется амфотерностью. Таким оксидам и гидроксидам и будет приковано наше внимание в этой статье. Все амфотерные оксиды и гидроксиды — твердые вещества, нерастворимые в воде.
Для начала, как определить является ли оксид или гидроксид амфотерным? Есть правило, немного условное, но все-таки пользоваться им можно:
Амфотерные гидроксиды и оксиды образуются металлами, в степенях окисления +3 и +4, например (Al2O3, Al(OH)3, Fe2O3, Fe(OH)3)
И четыре исключения: металлы Zn, Be, Pb, Sn образуют следующие оксиды и гидроксиды: ZnO, Zn(OH)2, BeO, Be(OH)2, PbO, Pb(OH)2, SnO, Sn(OH)2, в которых проявляют степень окисления +2, но не смотря на это, эти соединения проявляют амфотерные свойства.
Наиболее часто встречающиеся амфотерные оксиды (и соответствующие им гидроксиды): ZnO, Zn(OH)2, BeO, Be(OH)2, PbO, Pb(OH)2, SnO, Sn(OH)2, Al2O3, Al(OH)3, Fe2O3, Fe(OH)3, Cr2O3, Cr(OH)3.
Свойства амфотерных соединений запомнить не сложно: они взаимодействуют с кислотами и щелочами.
- с взаимодействием с кислотами все просто, в этих реакциях амфотерные соединения ведут себя как основные:
Оксиды:
Al2O3 + 6HCl → 2AlCl3 + 3H2O
ZnO + H2SO4 → ZnSO4 + H2O
BeO + HNO3 → Be(NO3)2 + H2O
Точно так же реагируют гидроксиды:
Fe(OH)3 + 3HCl → FeCl3 + 3H2O
Pb(OH)2 + 2HCl → PbCl2 + 2H2O
- С взаимодействием со щелочами немного сложнее. В этих реакциях амфотерные соединения ведут себя как кислоты, и продукты реакции могут быть различными, все зависит от условий.
Или реакция происходит в растворе, или реагирующие вещества берутся твердые и сплавляются.
Разберем на примере гидроксида цинка. Как уже говорилось ранее, амфотерные соединения взаимодействуя с основными, ведут себя как кислоты. Вот и запишем гидроксид цинка Zn(OH)2 как кислоту. У кислоты водород спереди, вынесем его: H2ZnO2. И реакция щелочи с гидроксидом будет протекать как будто он – кислота. «Кислотный остаток» ZnO22- двухвалентный:
2KOH(тв.) + H2ZnO2(тв.) (t,сплавление)→ K2ZnO2 + 2H2O
Полученное вещество K2ZnO2 называется метацинкат калия (или просто цинкат калия). Это вещество – соль калия и гипотетической «цинковой кислоты» H2ZnO2 (солями такие соединения называть не совсем правильно, но для собственного удобства мы про это забудем). Только гидроксид цинка записывать вот так: H2ZnO2 – нехорошо. Пишем как обычно Zn(OH)2, но подразумеваем (для собственного удобства), что это «кислота»:
2KOH(тв.) + Zn(OH)2(тв.) (t,сплавление)→ K2ZnO2 + 2H2O
С гидроксидами, в которых 2 группы ОН, все будет так же как и с цинком:
Be(OH)2(тв.) + 2NaOH(тв.) (t,сплавление)→ 2H2O + Na2BeO2 (метабериллат натрия, или бериллат)
Pb(OH)2(тв.) + 2NaOH(тв.) (t,сплавление)→ 2H2O + Na2PbO2 (метаплюмбат натрия, или плюмбат)
С амфотерными гидроксидов с тремя группами OH (Al(OH)3, Cr(OH)3, Fe(OH)3) немного иначе.
Разберем на примере гидроксида алюминия: Al(OH)3, запишем в виде кислоты: H3AlO
H3AlO3 – H2O → HAlO2 + H2O.
Вот с этой «кислотой» (HAlO2) мы и работаем:
HAlO2 + KOH → H2O + KAlO2 (метаалюминат калия, или просто алюминат)
Но гидроксид алюминия вот так HAlO2 записывать нельзя, записываем как обычно, но подразумеваем там «кислоту»:
Al(OH)3(тв.) + KOH(тв.) (t,сплавление)→ 2H2O + KAlO2(метаалюминат калия)
То же самое и с гидроксидом хрома:
Cr(OH)3 → H3CrO3 → HCrO2
Cr(OH)3(тв.) + KOH(тв.) (t,сплавление)→ 2H 2O + KCrO2(метахромат калия,
НО НЕ ХРОМАТ, хроматы – это соли хромовой кислоты).
С гидроксидами содержащими четыре группы ОН точно так же: выносим вперед водород и убираем воду:
Sn(OH)4 → H4SnO4 → H2SnO3
Pb(OH)4 → H4PbO4 → H2PbO3
Следует помнить, что свинец и олово образуют по два амфотерных гидроксида: со степенью окисления +2 (Sn(OH)2, Pb(OH)2), и +4 (Sn(OH)4, Pb(OH)4).
И эти гидроксиды будут образовывать разные «соли»:
Степень окисления | +2 | +4 | ||
Формула гидроксида |
|
|
|
|
Формула гидроксида в виде кислоты | H2SnO2 | H2PbO2 | H2SnO3 | H2PbO3 |
Соль (калиевая) | K2SnO2 | K2PbO2 | K2SnO3 | K2PbO3 |
Название соли | станнИТ | блюмбИТ | метастаннАТ | метаблюмбАТ |
Те же принципы, что и в названиях обычных «солей», элемент в высшей степени окисления – суффикс АТ, в промежуточной – ИТ.
Такие «соли» (метахроматы, метаалюминаты, метабериллаты, метацинкаты и т.д.) получаются не только в результате взаимодействия щелочей и амфотерных гидроксидов. Эти соединения всегда образуются, когда соприкасаются сильноосновный «мир» и амфотерный (при сплавлении). То есть точно так же как и амфотерные гидроксиды со щелочами будут реагировать и амфотерные оксиды, и соли металлов, образующих амфотерные оксиды (соли слабых кислот). И вместо щелочи можно взять сильноосновный оксид, и соль металла, образующего щелочь (соль слабой кислоты).

Взаимодействия:
Запомните, реакции, приведенные ниже, протекают при сплавлении.
Амфотерного оксида с сильноосновным оксидом:
ZnO(тв.) + K2O(тв.) (t,сплавление)→ K2ZnO2 (метацинкат калия, или просто цинкат калия)
Амфотерного оксида со щелочью:
ZnO(тв.) + 2KOH(тв.) (t,сплавление)→ K2ZnO2 + H2O↑
Амфотерного оксида с солью слабой кислоты и металла, образующего щелочь:
ZnO(тв.)+ K2CO3(тв.) (t,сплавление)→ K2ZnO2 + CO2↑
Амфотерного гидроксида с сильноосновным оксидом:
Zn(OH)2(тв.) + K2O(тв.) (t,сплавление)→ K2ZnO2 + H2O↑
Амфотерного гидроксида со щелочью:
Zn(OH)2(тв.) + 2KOH(тв.) (t,сплавление)→ K2ZnO2 + 2H2O↑
Амфотерного гидроксида с солью слабой кислоты и металла, образующего щелочь:
Zn(OH)2(тв.) + K2CO3(тв.) (t,сплавление)→ K2ZnO2 + CO2↑ + H2O↑
Соли слабой кислоты и металла, образующего амфотерные соединение с сильноосновным оксидом:
ZnCO3(тв.) + K2O(тв.) (t,сплавление)→ K2ZnO2 + CO2↑
Соли слабой кислоты и металла, образующего амфотерные соединение со щелочью:
ZnCO3(тв.) + 2KOH(тв.) (t,сплавление)→ K2ZnO2 + CO2↑ + H2O↑
Соли слабой кислоты и металла, образующего амфотерные соединение с солью слабой кислоты и металла, образующего щелочь:
ZnCO3(тв.)+ K2CO3(тв.) (t,сплавление)→ K2ZnO2 + 2CO2↑
Ниже представлена информация по солям амфотерных гидроксидов, красным помечены наиболее встречающиеся в ЕГЭ.
Оксид | Гидроксид | Гидроксид в виде кислоты | Кислотный остаток | Соль | Название соли |
BeO | Be(OH)2 | H2BeO2 | BeO22- | K2BeO2 | Метабериллат (бериллат) |
ZnO | Zn(OH)2 | H2ZnO2 | ZnO22- | K2ZnO2 | Метацинкат (цинкат) |
Al2O3 | Al(OH)3 | HAlO2 | AlO2— | KAlO2 | Метаалюминат (алюминат) |
Fe2O3 | Fe(OH)3 | HFeO2 | FeO2— | KFeO2 | Метаферрат (НО НЕ ФЕРРАТ) |
SnO | Sn(OH)2 | H2SnO2 | SnO22- | K2SnO2 | СтаннИТ |
PbO | Pb(OH)2 | H2PbO2 | PbO22- | K2PbO2 | БлюмбИТ |
SnO2 | Sn(OH)4 | H2SnO3 | SnO32- | K2SnO3 | МетастаннАТ (станнат) |
PbO2 | Pb(OH)4 | H2PbO3 | PbO32- | K2PbO3 | МетаблюмбАТ (плюмбат) |
Cr2O3 | Cr(OH)3 | HCrO2 | CrO2— | KCrO2 | Метахромат (НО НЕ ХРОМАТ) |
В ЕГЭ это называют «растворением гидроксида алюминия (цинка, бериллия и т.д.) щелочи». Это обусловлено способностью металлов в составе амфотерных гидроксидов в присутствии избытка гидроксид-ионов (в щелочной среде) присоединять к себе эти ионы. Образуется частица с металлом (алюминием, бериллием и т.д.) в центре, который окружен гидроксид-ионами. Эта частица становится отрицательно-заряженной (анионом) за счет гидроксид-ионов, и называться этот ион будет гидроксоалюминат, гидроксоцинкат, гидроксобериллат и т.д.. Причем процесс может протекать по-разному металл может быть окружен разным числом гидроксид-ионов.
Мы будем рассматривать два случая: когда металл окружен четырьмя гидроксид-ионами, и когда он окружен шестью гидроксид-ионами.
Запишем сокращенное ионное уравнение этих процессов:
Al(OH)3 + OH— → Al(OH)4—
Образовавшийся ион называется Тетрагидроксоалюминат-ион. Приставка «тетра-» прибавляется, потому что гидроксид-иона четыре. Тетрагидроксоалюминат-ион имеет заряд -, так как алюминий несет заряд 3+, а четыре гидроксид-иона 4-, в сумме получается -.
Al(OH)3 + 3OH— → Al(OH)63-
Образовавшийся в этой реакции ион называется гексагидроксоалюминат ион. Приставка «гексо-» прибавляется, потому что гидроксид-иона шесть.
Прибавлять приставку, указывающую на количество гидроксид-ионов обязательно. Потому что если вы напишете просто «гидроксоалюминат», не понятно, какой ион вы имеете в виду: Al(OH)4— или Al(OH)63-.
При взаимодействии щелочи с амфотерным гидроксидом в растворе образуется соль. Катион которой – это катион щелочи, а анион – это сложный ион, образование которого мы рассмотрели ранее. Анион заключается в квадратные скобки.
Al(OH)3 + KOH → K[Al(OH)4] (тетрагидроксоалюминат калия)
Al(OH)3 + 3KOH → K3[Al(OH)6] (гексагидроксоалюминат калия)
Какую именно (гекса- или тетра-) соль вы напишете как продукт – не имеет никакого значения. Даже в ответниках ЕГЭ написано: «…K3[Al(OH)6] (допустимо образование K[Al(OH)4]». Главное не забывайте следить, чтобы все индексы были верно проставлены. Следите за зарядами, и имейте ввиду, что сумма их должна быть равна нулю.
Кроме амфотерных гидроксидов, со щелочами реагируют амфотерные оксиды. Продукт будет тот же. Только вот если вы запишете реакцию вот так:
Al2O3 + NaOH → Na[Al(OH)4]
Al2O3 + NaOH → Na3[Al(OH)6]
Но эти реакции у вас не уравняются. Надо добавить воду в левую часть, взаимодейтсиве ведь происходит в растворе, воды там дотаточно, и все уравняется:
Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4]
Al2O3 + 6NaOH + 3H2O → 2Na3[Al(OH)6]
Помимо амфотерных оксидов и гидроксидов, с растворами щелочей взаимодействуют некоторые особо активные металлы, которые образуют амфотерные соединения. А именно это: алюминий, цинк и бериллий. Чтобы уравнялось, слева тоже нужна вода. И, кроме того, главное отличие этих процессов – это выделение водорода:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2↑
2Al + 6NaOH + 6H2O → 2Na3[Al(OH)6] + 3H2↑
В таблице ниже приведены наиболее распространенные в ЕГЭ примеры свойства амфотерных соединений:
Амфотерное вещество | Соль | Название соли | Реакции |
Al Al2O3 Al(OH)3 | Na[Al(OH)4] | Тетрагидроксоалюминат натрия | Al(OH)3 + NaOH → Na[Al(OH)4] Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4] 2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2↑ |
Na3[Al(OH)6] | Гексагидроксоалюминат натрия | Al(OH)3 + 3NaOH → Na3[Al(OH)6] Al2O3 + 6NaOH + 3H2O → 2Na3[Al(OH)6] 2Al + 6NaOH + 6H2O → 2Na3[Al(OH)6] + 3H2↑ | |
Zn ZnO Zn(OH)2 | K2[Zn(OH)4] | Тетрагидроксоцинкат натрия | Zn(OH)2 + 2NaOH → Na2[Zn(OH)4] ZnO + 2NaOH + H2O → Na2[Zn(OH)4] Zn + 2NaOH + 2H2O → Na2[Zn(OH)4]+ H2↑ |
K4[Zn(OH)6] | Гексагидроксоцинкат натрия | Zn(OH)2 + 4NaOH → Na4[Zn(OH)6] ZnO + 4NaOH + H2O → Na4[Zn(OH)6] Zn + 4NaOH + 2H2O → Na4[Zn(OH)6]+ H2↑ | |
Be BeO Be(OH)2 | Li2[Be(OH)4] | Тетрагидроксобериллат лития | Be(OH)2 + 2LiOH → Li2[Be(OH)4] BeO + 2LiOH + H2O → Li2[Be(OH)4] Be + 2LiOH + 2H2O → Li2[Be(OH)4]+ H2↑ |
Li4[Be(OH)6] | Гексагидроксобериллат лития | Be(OH)2 + 4LiOH → Li4[Be(OH)6] BeO + 4LiOH + H2O → Li4[Be(OH)6] Be + 4LiOH + 2H2O → Li4[Be(OH)6]+ H2↑ | |
Cr2O3 Cr(OH)3 | Na[Cr(OH)4] | Тетрагидроксохромат натрия | Cr(OH)3 + NaOH → Na[Cr(OH)4] Cr2O3 + 2NaOH + 3H2O → 2Na[Cr(OH)4] |
Na3[Cr(OH)6] | Гексагидроксохромат натрия | Cr(OH)3 + 3NaOH → Na3[Cr(OH)6] Cr2O3 + 6NaOH + 3H2O → 2Na3[Cr(OH)6] | |
Fe2O3 Fe(OH)3 | Na[Fe(OH)4] | Тетрагидроксоферрат натрия | Fe(OH)3 + NaOH → Na[Fe(OH)4] Fe2O3 + 2NaOH + 3H2O → 2Na[Fe(OH)4] |
Na3[Fe(OH)6] | Гексагидроксоферрат натрия | Fe(OH)3 + 3NaOH → Na3[Fe(OH)6] Fe2O3 + 6NaOH + 3H2O → 2Na3[Fe(OH)6] |
Полученные в этих взаимодействиях соли реагируют с кислотами, образуя две другие соли (соли данной кислоты и двух металлов):
2Na3[Al(OH)6] + 6H2SO4 → 3Na2SO4 + Al2(SO4)3 + 12H2O
Вот и все! Ничего сложного. Главное не путайте, помните что образуется при сплавлении, что в растворе. Очень часто задания по этому вопросу попадаются в B части.