Горение свечи это физическое или химическое явление ? Раскрываем тайну огня
В этой статье мы рассмотрим вопрос о том, горение свечи – это физическое или химическое явление, обоснуем свою точку зрения и докажем ее верность. Однако для начала мы уделим внимание общим сведениям о том, что представляет собой процесс горения. Также поговорим, из-за чего его сложно отнести к конкретно физическим или химическим процессам.
Горение – что это с точки зрения науки
Горение – сложный процесс с физическими и химическими реакциями, при котором исходные вещества превращаются в продукты сгорания. Происходит это из-за экзотермической реакции, которая сопровождается обильным выделением тепловой энергии. Из этого определения уже понятно, почему четко разобраться в том, горение свечи – это физическое или химическое явление, довольно сложно.
Отдельно стоит поговорить о таком термине, как «пламя». Это образованная в результате реакций горения зона, от которой исходят свет и тепло. Температура пламени зависит от условий, при которых происходит само горение, а также от смесей, участвующих в этом процессе.
Температура пламени зависит от условий, при которых происходит само горение, а также от смесей, участвующих в этом процессе.
Что представляет собой горение свечи
Теперь, когда мы знаем немного теории, можно плавно переходить к вопросу о том, горение свечи – это физическое или химическое явление, и почему сложно разобраться в этом вопросе. На основе приведенных выше фактов, мы можем с уверенностью утверждать, что горение – это смесь из химических и физических явлений. Если отбросить в сторону сам момент, когда свеча поджигается, то при горении можно обозначить несколько моментов.
Первым делом, происходит физический процесс. От горячего пламени во все стороны исходит тепло, в том числе и в нижнюю часть. Излучение, попадающее на саму парафиновую свечу (возьмем в качестве примера самый простой вариант этого изделия), нагревает ее материал.
Далее происходит расплавление парафина, который под воздействием капиллярных сил равномерно идет вдоль фитиля прямо к его горящей части. В этом месте происходит испарение парафина.
В этом месте происходит испарение парафина.
Пары парафина подхватываются восходящим воздухом и смешиваются с ним.
Однако это далеко не вся информация о том, горение свечи – это физическое или химическое явление, ведь дальше в дело вступает химический процесс, а именно, начинается окисление парафина. Говоря иными словами, происходит распадение его молекул, если не вдаваться в подробности, вплоть до самих атомов. Парафины представляют собой углеводороды, чьи молекулы составлены из атомов C и H. Они соединяются с кислородом, вследствие чего появляются вода и углекислый газ. А в результате окисления идет выделение энергии, относящееся к химическим процессам.
Еще недавно лечение разного рода нарушений кожного покрова производилось с помощью многочисленных перевязочных материалов: ваты, бинтов, тампонов или марли. Современная медицина предполагает использование более современных и технологичных способов — стерильных послеоперационных повязок. В статье вы найдете информацию о популярных товарах этой категории и их особенностях.
На этом можно было бы остановиться и закрыть вопрос о том, горение свечи – это физическое или химическое явление, ведь мы наглядно видим, что здесь происходят сразу оба процесса. Однако давайте рассмотрим процесс горения до конца. За окислением снова начинается физическая часть процесса. Образовавшаяся энергия поступает ко всем задействованным в работе молекулам, благодаря чему повышается их кинетическая сила. Иногда часть этой силы выделяется в качестве света или обычного свечения. Затем поднимающиеся потоки горячих газов способствуют образованию пламени свечи.
Подводим итоги
Выходит, что споры о том, горение свечи – это физическое или химическое явление, наблюдения, о чем ведутся уже очень давно, можно смело закрывать. В горении свечи присутствуют и химические, и физические процессы одновременно.
Физические и химические явления. — химия, презентации
Физические и химические явления. Сущность и признаки химических реакций.
Сущность и признаки химических реакций.
Задачи: Обучающие : Изучить сущность химических реакций. Научиться различать физические и химические явления по определенным признакам. Изучить классификацию химических реакций по признаку выделения и поглощения энергии. Развивающие: Развивать интеллектуальные и практические умения ( умение анализировать, сравнивать, делать выводы). Воспитательные: Воспитывать культуру химического эксперимента: соблюдение правил технике безопасности при работе, поведение в кабинете химии.
Физические явления
Физика изучает движение тел в пространстве, оптические и тепловые процессы, гравитацию, электричество и многие другие явления, не связанные с превращением одних веществ в другие. Свойства веществ, проявляющиеся при этом, относят к физическим свойствам.
Химические явления
- Химия изучает строение материи, ее состав, получение и превращение веществ.

- Свойства веществ, проявляющиеся при их получении и превращениях, относят к химическим свойствам веществ.
- Явления, которые сопровождают получение и превращение веществ, называются химическими явлениями.
Химические свойства веществ не претерпевают никаких изменений при физических процессах.
В результате химического превращения — химической реакции — образуются новые вещества с другими свойствами.
Дробление вещества и кристаллизация
- Сравните степень дробления при измельчении в ступке и при растворении соли.
- Выпарьте несколько капель раствора в фарфоровой чашке.
- Отнесите данные явления (измельчение, растворение, выпаривание и кристаллизацию) к физическим или химическим явлениям.
Испарение и конденсация
- Можно ли утверждать, что бензин исчез?
- К какому типу явлений отнесете процесс, имевший место в данном опыте?
- Возможно ли вновь собрать пары этого бензина в капли жидкости?
- Можно ли считать появление, исчезновение инея в зимнее время примером конденсации и испарения вещества воды?
Физическое явление: замерзший водяной пар образует иней на деревьях
Иней на листве – это замерзший водяной пар. Растаяв, он вновь превратится в жидкость, затем в пар.
Растаяв, он вновь превратится в жидкость, затем в пар.
Гидроксид натрия, только что взятый из контейнера
Гидроксид натрия, пролежавший на воздухе некоторое время. Произошло физическое явление –притягивание паров воды из воздуха.
Перманганат калия – кристаллическое твердое вещество темно-серого цвета с металлическим блеском
Перманганат калия растворим в воде. Получаем раствор этого же вещества – перманганата калия.
Растворение сахара – тоже физическое явление
Давайте теперь найдем отличия между явлениями разрезания и сжигания бумаги. Мы можем видеть, что каждый кусок разрезанной бумаги сохраняет ее свойства. Процесс измельчения бумаги – физическое явление . В случае сжигания бумаги полученные нами почерневшие клочки рассыпаются от прикосновения. Образовавшееся вещество — пепел — имеет другие свойства, отличные от свойств исходного вещества. В процессе горения одно вещество превратилось в другое. Значит, горение бумаги –
В процессе горения одно вещество превратилось в другое. Значит, горение бумаги –
Каждый кусочек бумаги имеет те же свойства, что и целый лист
Пепел обладает совсем другими свойствами, чем бумага
Плавление и горение парафина
Плавление парафина, как и разрезание бумаги, — физическое явление, тогда как горение этих веществ — химическое явление.
Сравните эти два явления по внешним признакам и по их сущности? Сделайте вывод о классификации этих явлений? Произошло ли образование новых веществ в ходе этих опытов?
Разрезание и горение магния
Отрезанный кусок магния имеет те же свойства, что и целая лента магния. При поджигании с помощью газовой горелки магний горит с интенсивным свечением. Блестящее, серебристое вещество превращается в белый порошок — оксид магния. Поскольку образовавшееся вещество имеет другие свойства, мы можем сказать, что произошло химическое превращение
Отрезанный кусочек магния имеет те же свойства, что и целая лента до разрезания
При горении магния образуется новое вещество с другими свойствами
Сравните яркость горения магния с яркостью обычной электрической лампочки? Относится ли горения магния и «горение» электролампочки к одному типу явлений? К какому типу явлений относятся горение дров, свечение насекомых или глубоководных рыб?
Экзо- и эндотермические реакции
Экзотермические реакции
- Исходные вещества = Продукты реакции + Q
- Эндотермические реакции
- Исходные вещества = Продукты реакции -Q
Признаки химических реакций
- Растворение и появление осадка.

- Выделение газа.
- Изменение цвета.
- Выделение света.
- Выделение или поглощение тепла.
- Запах.
Условия течения реакций
- Подача тепла.
- Дробление.
- Перемешивание.
- Применение катализатора.
- Время.
Вопросы для систематизации и обобщения темы.
- Можно ли на основании только лишь внешних признаков точно определить, к какому типу явлений относится данный процесс?
- Для получения краски нужного цвета и оттенка художники, рисуя картины, смешивают различные краски. Например, при смешивании желтого и синего получается зеленый цвет. К какому типу явлений относится такое превращение?
О каких явлениях идет речь в высказываниях поэтов?
Унылая пора! Очей очарованье! Приятна мне твоя прощальная краса – люблю я пышное природы увяданье,
В багрец и золото одетые леса!
А.С.Пушкин.
И трещат сухие сучья, Разгораясь жарко, Освещая тьму ночную Далеко и ярко!
 Суриков . В декабре, в декабре Все деревья в серебре, Нашу речку, словно в сказке, За ночь вымостил мороз… С. Маршак.
Суриков . В декабре, в декабре Все деревья в серебре, Нашу речку, словно в сказке, За ночь вымостил мороз… С. Маршак.
Вывод
- Согласно атомно-молекулярному учению при химических реакциях молекулы разрушаются, а атомы сохраняются; в процессе реакции происходит перегруппировка атомов.
- В соответствии с теорией химической связи происходит разрыв химических связей в исходных веществах и образование новых в продуктах реакции.
Домашнее задание
- Обязательный уровень.
- П. 25-26. упражнение 1 страница 95
- Тренировочный уровень.
- Подобрать примеры экзо- и эндотермических реакций, с которыми вы встречаетесь в повседневной жизни.
- Творческое задание.
- Разработать плакаты – опорные конспекты по теме сегодняшнего урока.
Торбеевская средняя общеобразовательная школа №3.
Автор презентации
Учитель химии высшей категории
Дудорова Е. В.
В.
2015г.
Химические явления. Реакция горения. | Презентация к уроку по природоведению (5 класс) по теме:
Слайд 1
Химические явления. Горение. Презентация по природоведению для 5 класса Подготовила Шашлова Т.А.Слайд 2
Цель урока Познакомиться с новыми понятиями: химические явления, химические реакции; Познакомиться с реакцией горения; Определить значение горения для человека.
Слайд 3
Химическое явление (реакция) – явление, при котором образуются новые вещества. Литье металлов Обжигание глины Получение мыла
Слайд 4
А по каким признакам можно определить, что произошла химическая реакция ? При некоторых химических реакциях происходит выпадение осадка; Другие реакции сопровождаются изменением цвета исходного вещества; В третьих происходит изменение его вкуса; В четвертых – выделение газа, выделение или поглощение тепла и света.
Слайд 5
Признаки химических реакций Изменение цвета исходного вещества Изменение вкуса исходного вещества Выпадение осадка Выделение газа Появление запаха
Слайд 6
Изменение цвета Изменение вкуса Выделение газа Раствор крахмала йод
Слайд 7
Реакция горения Реакцию, сопровождающуюся выделением тепла и света, называют горением.
Слайд 8
Строение пламени свечи Менее яркое пламя Яркое пламя Темное пламя
Слайд 9
Как погасить пламя? — п рекратить доступ воздуха Можно гасить водой: древесину; уголь. Нельзя гасить водой: бензин; нефть; керосин.
Слайд 10
Горючие материалы, сжигаемые для использования выделяющейся теплоты, называют топливом .
Слайд 11
Твердое топливо торф Каменный уголь
Слайд 12
Жидкое топливо Бензин Керосин
Слайд 13
Газообразное топливо Природный газ
Слайд 14
Значение горения: обеспечивает движение транспорта; обогревает жилища; применяется во всех отраслях промышленности; применяется в сельском хозяйстве; используется на тепловых электростанциях.
Слайд 16
Закрепление почему при протапливании печей открывают трубы? к какой группе явлений можно отнести: гниение листьев; скисание молока; таяние льда; журчание ручья; сгорание дров.
Слайд 17
Домашнее задание прочитать параграф 14 ответить на вопросы 4, 6 (стр. 62) письменно.
62) письменно.
Слайд 18
Спасибо за внимание!
Основные явления горения — Справочник химика 21
После завершающих экспериментальных доказательств того, что кислород есть субстанция, которая порождает горение горючих тел и которая в процессе дыхания животных выполняет аналогичную функцию, можно утверждать, по мнению Лавуазье, что теория флогистона не отвечает экспериментальным данным и поэтому должна быть отброшена. Его статья Соображения о флогистоне относится к 1783 г. В ней о флогистоне сказано Но если в химии все объясняется удовлетворительным образом без помощи флогистона, то одно это означает бесконечно большую вероятность того, что такое начало не существует и что оно представляет собой гипотетическую субстанцию, неосновательное предположение… В эпоху, когда писал Шталь, основные явления горения еще не были известны. Об этом явлении он знал лишь то, что поражает сознание — выделение света и тепла… Ои предположил, что посредником нри соединении огня с горючими телами служит некое землистое начало, и он назвал горючим началом или флогистоном результат этого соеди-нения.
Состав, агрегатное состояние и другие свойства горючих веществ различны, однако основные явления, протекающие при возникновении горения, одинаковы. [c.6]
ОСНОВНЫЕ ЯВЛЕНИЯ ГОРЕНИЯ [c.260]
Горение жидкого топлива представляет весьма сложный процесс. Многочисленные работы различных авторов освеш.ают природу явлений, объединяемых понятием — горение. Поскольку этими работами уточняется, но в основном не опровергается изложенная выше схема горения и поскольку в нашу задачу входит лишь рассмотрение условий наиболее эффективной работы форсунок, остановимся на основных стадиях горения, в той или иной мере зависящих от работы форсунок. [c.27]
Для дизельного топлива изменение температурных условий (температуры потока) в исследованной области практически не сказывается ни на суммарной длительности процесса горения, ни на длительности собственно горения. Это обстоятельство позволяет сделать вывод, что общая длительность процесса горения тяжелых остаточных топлив по сравнению с легкими, полностью испаряющимися, будет определяться длительностью процессов подготовки топлива и выгорания коксового остатка. Изменение условий обтекания капли, выражающееся в изменении температуры и скорости, не изменяло общей последовательности и характера развития процесса горения (рис. 23). Скорость обдувания варьировалась в интервале 3,3—6,5 м/сек. В этом случае сравнение соответствующих значений времени полного сгорания одиночной капли мазута (т ) при различных условиях обдува показывает, что величина Т2 остается примерно постоянной. Одновременно с этим время горения жидкой фазы возрастает с увеличением относительной скорости. Причина этого явления в том, что с увеличением скорости обдувания пламя смещается относительно капли и основной очаг горения располагается в следе за каплей.
Это обстоятельство позволяет сделать вывод, что общая длительность процесса горения тяжелых остаточных топлив по сравнению с легкими, полностью испаряющимися, будет определяться длительностью процессов подготовки топлива и выгорания коксового остатка. Изменение условий обтекания капли, выражающееся в изменении температуры и скорости, не изменяло общей последовательности и характера развития процесса горения (рис. 23). Скорость обдувания варьировалась в интервале 3,3—6,5 м/сек. В этом случае сравнение соответствующих значений времени полного сгорания одиночной капли мазута (т ) при различных условиях обдува показывает, что величина Т2 остается примерно постоянной. Одновременно с этим время горения жидкой фазы возрастает с увеличением относительной скорости. Причина этого явления в том, что с увеличением скорости обдувания пламя смещается относительно капли и основной очаг горения располагается в следе за каплей.
Основная особенность явлений горения заключается в том, что условия, необходимые для быстрого протекания реакции, созданы ею самою. Эти условия заключаются либо в высокой температуре, либо в высокой концентрации активных продуктов, ускоряющих (катализирующих) реакцию (переносчики реакционных цепей свободные атомы, радикалы, органические перекиси и т. п.). Если сама реакция создает условия для своего собственного быстрого протекания, то возникает то, что в кибернетике называется обратной связью. При малом изменении внешних условий возможен пе- [c.258]
Эти условия заключаются либо в высокой температуре, либо в высокой концентрации активных продуктов, ускоряющих (катализирующих) реакцию (переносчики реакционных цепей свободные атомы, радикалы, органические перекиси и т. п.). Если сама реакция создает условия для своего собственного быстрого протекания, то возникает то, что в кибернетике называется обратной связью. При малом изменении внешних условий возможен пе- [c.258]
Наиболее изученной реакцией с разветвленными цепями является реакция водорода с кислородом [40]. Кинетике и явлениям горения гремучей смеси (как принято называть смесь водорода с кислородом) посвящено громадное количество работ. Это — основная модельная разветвленная цепная реакция. [c.275]
Вблизи температуры формула (VI,23) представляет хорошее приближение к закону Аррениуса, в котором сохраняются все основные особенности явлений горения. В то же время она гораздо проще в математическом отношении. Важно не только то, что метод разложения экспонента позволяет получать в замкнутом виде приближенные решения ряда задач, для которых при [c. 291]
291]
Это позволяет охватить основные стороны взаимодействия явлений горения и газификации и выявить динамические характеристики процесса в различных формах и аппаратах. [c.5]
Для точного расчета выгорания топлива и распределения температур по длине факела необходимо совместное рассмотрение системы уравнений, описывающих основные явления в процессе горения потока топлива, а именно [c.187]
В [5.68, 5.69] изложена теория горения и комплексный анализ процесса горения потока топлива в неизотермических условиях. Рассмотрены системы уравнений, отражающих основные явления в процессе горения потока топлива движение газа и топлива, диффузия и конвективный перенос реагирующих компонент, кинетика химических реакций, выгорание компонент, выделение и поглощение тепла, теплообмен с окружающей средой. Такая постановка задачи связана с теорией необратимых процессов и механикой реагирующих сред, хотя основные положения теории горения топлива разработаны независимо от указанных более общих теорий. [c.446]
[c.446]
Горение газообразных сред в емкостях редко переходит в детонацию. В основном, явление детонации проявляется в трубах. Это связано с тем, что для возникновения детонации необходимо наличие так называемого преддетонационного расстояния, т. е. расстояния от места воспламенения до места возникновения детонации. Это расстояние в каждом конкретном случае зависит от диаметра труб, их шероховатости, от места поджога — у открытого или закрытого конца трубы. Чрезвычайную опасность представляет переход детонационной волны из трубопровода в закрытую систему (автоклавы, ресиверы) или полуоткрытую систему (производственные помещения, вен- [c.291]
Вот почему теория флогистона при всей ошибочности и нелепости ее основных положений не могла воспрепятствовать дальнейшему, постепенно убыстряющемуся развитию химии. Можно сказать, даже наоборот, эта теория, охватив единой общей точкой зрения различные химические явления и, прежде всего, явления горения и кальцинации металлов, содействовала их изучению путем сопоставлений и сравнений.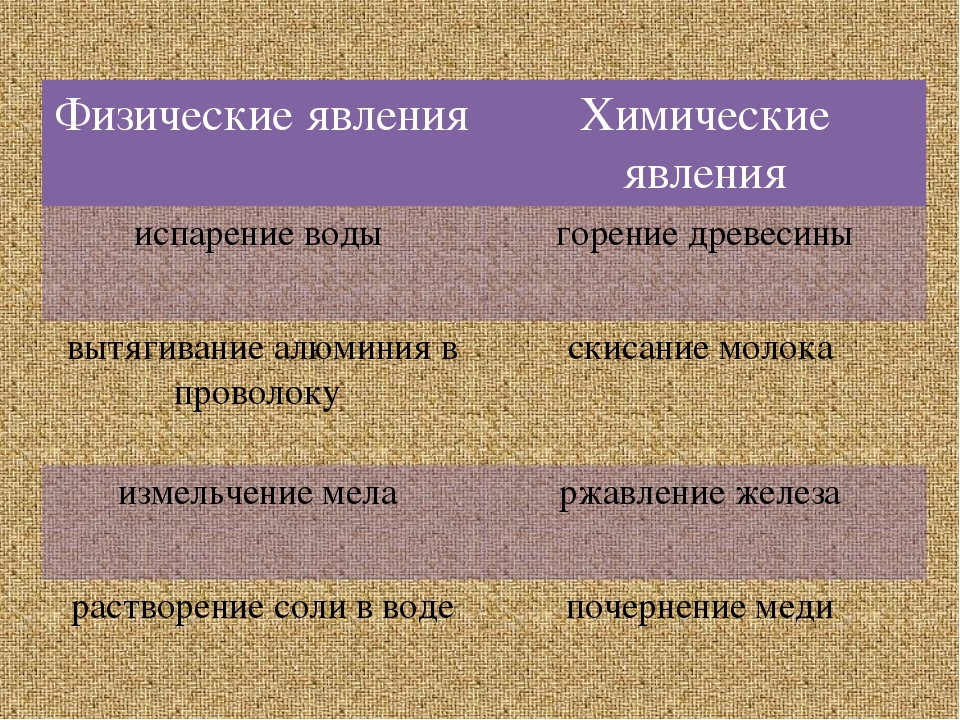 [c.250]
[c.250]
По-видимому, в середине 1780-х годов у Лавуазье возникла мысль обобщить все полученные им ранее результаты исследований и объяснений разнообразных явлений и изложить их в систематизированном виде в курсе элементарной химии. Основной материал для такого курса уже имелся. Принципы кислородной теории, рационально объяснившие явления горения, обжига металлов, физиологию дыхания и другие явления, оказались ключом для разрешения многих других неясных вопросов, связанных с трактовкой химических явлений. [c.361]
В одной из предыдущих лекций уже разбиралось явление горения водорода, но, изучив основное направление этой реакции, мы тогда оставили в стороне многие важные ее подробности, в частности совершенно не коснулись той роли, которую играют при горении водорода пергидроксил и перекись водорода. Теперь после подробного ознакомления со свойствами перекиси мы можем вернуться к рассмотрению цепи последовательных стадий реакции [c. 108]
108]
В данной статье мы смогли изложить лишь немногие результаты применения современных физико-хими-ческих методов исследования к изучению наиболее древнего явления — горения. Приведенные примеры отнюдь не исчерпывают ни того, что уже было открыто, ни тем более того, что еще может быть открыто. Они лишь иллюстрируют сложную природу явлений горения, при изучении которых необходимо использовать богатый арсенал методов химии, физики, гидродинамики и, в первую очередь, одну из основных идей современной химии — учение о цепной теории химических реакций. [c.164]
Вся многообразная область явлений горения может быть разделена на три основные группы [c.292]
С другой стороны, поскольку основной упор в книге делается на применение спектроскопии к изучению пламен, она может оказаться весьма полезно как для изучающих химию процессов горения, так и для тех, кто интересуется различными особенностями явления горения. Сюда относится вопрос о температуре пламени, которая может быть довольно точно оценена с помощью спектроскопического метода, вопрос о термодинамическом состоянии горящей смеси на различных стадиях реакции, вопрос о природе стука и детонации в двигателе и т. д. [c.6]
д. [c.6]
История открытия основных законов химии. Свойства газов. Явления горения. [c.168]
Настоящая книга является первой из семи намеченных к изданию книг по химмотологии. В ней изложены основные представления о химмотологии как новой научной дисциплине и ее роли в народном хозяйстве. Рассмотрены теоретические основы окисления углеводородов и горения жидких топлив, теория поверхностных явлений в двигателях и механизмах с участием ПАВ, основы трения и износа, механизм действия противоизносных и противозадирных присадок к топливам и маслам. Даны теоретические представления о коррозии конструктивных материалов в контакте с нефтепродуктами, описаны мероприятия по защите от коррозии. [c.2]
Условия появления оксида углерода при горении природного газа, содержащего в основном метан, упрощенно можно рассматривать как стадии последовательных превращений метан — формальдегид — оксид углерода—диоксид углерода. При неблагоприятных условиях цепная реакция может оборваться и в продуктах горения будут содержаться оксид углерода и альдегиды.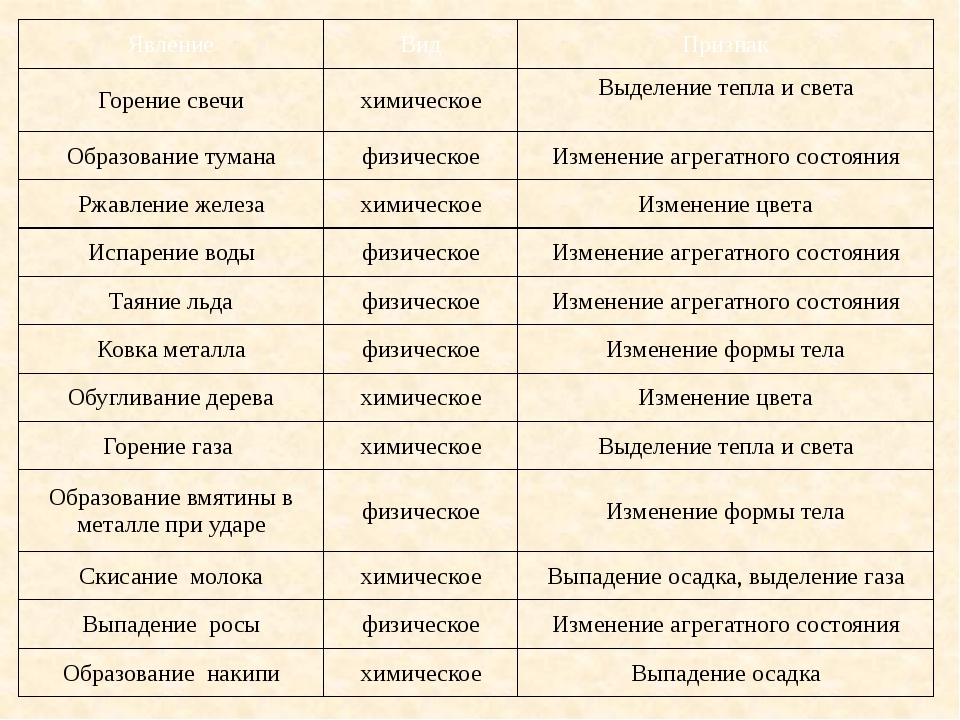 Подобные явления происходят и с другими горючими газами при недостатке окислителя. То же наблюдается при охлаждении зоны горения. [c.292]
Подобные явления происходят и с другими горючими газами при недостатке окислителя. То же наблюдается при охлаждении зоны горения. [c.292]
Суммируя все вышесказанное, можно определить основные химические опасности как опасности, присущие условиям и промышленного предприятия, и транспорта быстроразвивающиеся (острые) и дающие в типичных своих проявлениях свыше десяти несчастных случаев, обусловленных действием поражающих факторов явлений аварии — пожаров, взрывов или токсических выбросов. В определенных условиях (например, при вовлечении в реализацию опасности достаточно большого количества опасных веществ) возможно появление и других поражающих факторов — переохлаждения, удушья, интенсивного горения в перенасыщенном кислородом воздухе или рассеяния разъедающих ткани веществ. [c.67]
Химическая кинетика приобретает большое значение при изучении сложных явлений, включаюш,их химическое превращение в качестве одного из основных элементов (процессы горения, биологические процессы). [c.4]
[c.4]
Техническая необходимость более глубокого понимания хода процесса горения в энергетических и транспортных агрегатах, а также необходимость проведения практических расчетов горения на разных его стадиях требуют детального изучения курса теории горения студентами энергетических специальностей. Курс теории горения в значительной степени синтезирует сведения основных теплотехнических и физико-химических дисциплин, учит последовательному анализу весьма сложных явлений. Важно при этом заметить, что такой анализ обычно слагается из ряда приближений, в которых выясняются главные соотношения процесса и области его протекания. [c.3]
Задачи горения, следовательно, можно охарактеризовать как нестационарные задачи турбулентной массо- и теплопроводности при наличии динамических источников вещества и тепла. Но хотя такое представление и определяет пути анализа процессов горения, конкретное решение задач теории горения при этом затруднено. Исследование процессов горения должно развиваться по пути составления систем интегро-дифференциальных уравнений, соответствие которых истинному ходу процесса следует проверять сопоставлением результатов решений этих систем с данными эксперимента. Именно так и развивается ныне теория горения, причем наиболее подробно исследуются крайние случаи, когда в сложном комплексе вопросов можно абстрагироваться от некоторых из них. В частности, установилось деление процессов горения на области протекания. Так, при анализе явлений термического распада природных топлив для мелких частиц при низких температурах можно пренебречь временем прогрева и рассматривать процесс как чисто кинетический распад сложного вещества на более простые соединения. Наоборот, при прогреве крупных кусков топлива в среде высокой температуры основным является ход нагрева. Можно принять, что сам термический распад происходит мгновенно. Появляется деление процесса на крайние области — кинетическую и тепловую, в каждой процесс может быть описан более простыми уравнениями, чем в общем случае протекания процесса в промежуточной области. [c.5]
Именно так и развивается ныне теория горения, причем наиболее подробно исследуются крайние случаи, когда в сложном комплексе вопросов можно абстрагироваться от некоторых из них. В частности, установилось деление процессов горения на области протекания. Так, при анализе явлений термического распада природных топлив для мелких частиц при низких температурах можно пренебречь временем прогрева и рассматривать процесс как чисто кинетический распад сложного вещества на более простые соединения. Наоборот, при прогреве крупных кусков топлива в среде высокой температуры основным является ход нагрева. Можно принять, что сам термический распад происходит мгновенно. Появляется деление процесса на крайние области — кинетическую и тепловую, в каждой процесс может быть описан более простыми уравнениями, чем в общем случае протекания процесса в промежуточной области. [c.5]
В 1777 г. А. Лавуазье указал на то, что хотя теория флогистона и объясняет кое-что из явлений горения и кальцинации, но возможность понять их, не прибегая к флогистону, колеблет до основания эту теорию. Таким образом, в начале своей борьбы с флогистоном он выступал очень осторожно, ограничиваясь указанием, что иззгчаемые явления могут быть объяснены и на основании новой теории. В том же году А. Лавуазье сформулировал следующие основные положения новой теории горения [c.89]
Таким образом, в начале своей борьбы с флогистоном он выступал очень осторожно, ограничиваясь указанием, что иззгчаемые явления могут быть объяснены и на основании новой теории. В том же году А. Лавуазье сформулировал следующие основные положения новой теории горения [c.89]
Подобного рода соображения заставляют предполагать, что после достижения известного температурного уровня суммарная итоговая реакция, которая носит название горения углерода, начинает в основном определяться скоростью протекания восстановительной пеакции ССО2 —> 2С0, которая из побочной становится основной. Явление это впервые отмечено и косвенно наблюдалось на опыте Хитриным [Л. 69, 76], который указал, что ничем другим нельзя удовлетворительно объяснить вторичный подъем К ривой А» =[(Т), который отчетливо наблюдается в зоне высоких температур, особенно если в опыте приблизится к достаточно строгим изотермическим условиям. Иллюстрацией к этому может служить фиг. 8-6. Еще более ярким примером неизбежности такого подъема скорости является фиг. 8-11, 11зображаю-щая результаты опытов того же автора с частицами электродного угля (2=15 мм). Как видно из приведенных иллюстраций, вторичный подъем начинается за пределами 1 100- — 1 300°, т. е. уже в зоне таких значительных темпера- [c.81]
8-11, 11зображаю-щая результаты опытов того же автора с частицами электродного угля (2=15 мм). Как видно из приведенных иллюстраций, вторичный подъем начинается за пределами 1 100- — 1 300°, т. е. уже в зоне таких значительных темпера- [c.81]
В отчете [Stahl, 1949] представлено описание последовательности событий, составленное на основе свидетельских показаний, в которых отмечались свистящий звук, характерный для пара, выпускаемого локомотивом, и появление коричнево-белого облака перед основным взрывом. Авторы отчета считают, что имели место два химических взрыва. Первый — незначительный — произошел снаружи и перевернул цистерну, вызвав ее разрушение, после чего последовал основной взрыв. Имеющийся опыт показывает, что цистерна не обязательно должна быть перевернута в результате химического взрыва. Свистящий звук может объясняться начальным образованием трещины, а разрушение цистерны обусловлено последующим ее разрывом под действием давления. Однако необходимо отметить, что, хотя в отчете проведен детальный анализ по многим аспектам, в нем отсутствуют какие-либо попытки проанализировать само явление взрыва. Это явление сравнивают со взрывом фугасного снаряда, несмотря на то, что при этом не образуется воронки. Как отмечалось выше, в работе [Giesbre ht,1981] проведен анализ модели разрушения для данного случая аварии (в [Stahl,1949] приводится большой объем информации по данному вопросу), представленной на рис. 4.7 цитируемой работы согласно модели, тепловая энергия в процессе горения составила 854 ГДж. Сделан вывод о том, что максимальный уровень избыточного давления в ходе ава)5ии не превышал 0,05 МПа. [c.321]
Это явление сравнивают со взрывом фугасного снаряда, несмотря на то, что при этом не образуется воронки. Как отмечалось выше, в работе [Giesbre ht,1981] проведен анализ модели разрушения для данного случая аварии (в [Stahl,1949] приводится большой объем информации по данному вопросу), представленной на рис. 4.7 цитируемой работы согласно модели, тепловая энергия в процессе горения составила 854 ГДж. Сделан вывод о том, что максимальный уровень избыточного давления в ходе ава)5ии не превышал 0,05 МПа. [c.321]
Две основные особенности явлений горения заключаются, во-первых, в наличии критических условий, о которых мы уже говорили, и, во-вторых, в способности процесса к пространственному распространению. При тепловом горении распространение происходит посредством передачи тепла, при цепном или автокатали-тическом посредством передачи активных веществ, т. е. диффузии. По этой причине второй вид называют иногда диффузионным горением. [c.259]
Г>се разнообразие проявлений горения может быть отнесено к двум основным явлениям — возникновениш и распространению пламени. [c.5]
[c.5]
В работе Зельдовича 1948 г. [13] были изложены основы общего метода численного интегрирования уравнений пламени без ограничивающих предположений нн о зависимости скорости реакции от температуры, ни о соотношении между О и (Х/срр). Большое число опубликованных за последнее десятилетие теоретических работ содержит различные варианты решения уравнений пламени как приближенными методами, так н численным интегрированием с определением как собственного значения, удовлетворяющего уравнениям пламени в заданных граничных условиях. Оставляя вне рассмотрения математическую сторону этих работ, мы коснемся их в дальнейшем лишь в той части, в которой они связаны с кинетической стороной явлений горения — основным предметом настоящего исследования. [c.184]
Вторая, более тонкая экспериментальная методика состояла в горении графитовой нити в сильно разреженной атмосфере (работы Дюваля [1], Буланжье [2]) этот метод является наиболее удобным для изучения основных явлений. Однако он не позволяет изучать горение при температурах ниже 800—900°. По третьей методике (работа Боннетена, 1958) графит в виде калиброванных зерен с большой поверхностью реагирует в сильно разреженной атмосфере в пределах температур 500— 900°. Используя данные, полученные методом нити в области низких температур, этот метод непосредственно [c.127]
Однако он не позволяет изучать горение при температурах ниже 800—900°. По третьей методике (работа Боннетена, 1958) графит в виде калиброванных зерен с большой поверхностью реагирует в сильно разреженной атмосфере в пределах температур 500— 900°. Используя данные, полученные методом нити в области низких температур, этот метод непосредственно [c.127]
Не все химики сразу признали учение Шталя. Некоторые из них принимали его лишь частично, другие же совершенно отвергали, предпочитая оставаться на позициях иатрохимиков и алхимиков. Возникновение теории флогистона не вызвало революционных изменений в теоретических взглядах но основным вопросам химии. Объяснения флогистиками явлений горения и кальцинации металлов, казавшиеся новыми, прекрасно сочетались со старыми алхимическими верованиями и скорее закрепляли установившиеся в XVI и XVII вв. традиции, нежели разрушали их. Да и сама теория флогистона не получала какого-либо заметного развития, оставаясь в течение ряда десятилетий в том же самом виде, в каком была предложена Шталем. Все это следует объяснять крайней ограниченностью фактического материала, которым располагала химия в начале XVIII в. Положение изменилось лишь во второй половине XVIII в., когда на основе нового экспериментального материала стали возможными действительно революционные преобразования. [c.242]
Все это следует объяснять крайней ограниченностью фактического материала, которым располагала химия в начале XVIII в. Положение изменилось лишь во второй половине XVIII в., когда на основе нового экспериментального материала стали возможными действительно революционные преобразования. [c.242]
Не рассматривая подробно явление горения, укажем основные реакщ1и, происходящие при горении. При самых низких температурах идет окисление по реакции С4-02 = СОг далее к ней прибавляется реакция СОг + С = 2С0 и в системе С — СО — СОг З стававливается равповесие, которое можно характеризовать следующими цифрами [c.281]
Основными особенностями горения являются, во-первых, наличие критических условий, когда нри малом изменении внешних условий имеют место явления ]зезкого изменеиия режима протекания процесса, и, во-вторых, способность процесса к пространственному распространению, которое в тепловом горении достигается посредством передачи тепла. Внешним проявлением горения, что отличает его от протекания обычной химической реакции, является появление пламени Р ]. Правда, в болоо поздиих работах ио гетерогенному горению приводятся примеры и беспламенного горения. Однако это но исключает основного внешнего признака теплового горения, а только расширяет диапазон процессов, протекание которых может быть отнесено к тепловому горению. [c.324]
Правда, в болоо поздиих работах ио гетерогенному горению приводятся примеры и беспламенного горения. Однако это но исключает основного внешнего признака теплового горения, а только расширяет диапазон процессов, протекание которых может быть отнесено к тепловому горению. [c.324]
Перечисленные задачи химмотологии как науки не исчерпывают всего многочисленного перечня нерешенных еще вопросов теории и практики рационального применения ГСМ, они скорее отражают лишь основные научные направления, по которым химмотологи должны проводить работы в ближайшем будущем. Важное место в этих работах должны занять теоретические исследования, например установление механизма действия многочисленных присадок и их композиций в топливах, смазочных материалах и специальных жидкостях разработка научно-теоретических основ подбора присадок, особенно их синергических смесей установление важнейших закономерностей самоорганизующихся процессов в двигателях и механизмах при применении ГСМ (например, при воспламенении и горении топлив) дальнейшее развитие и углубление теории поверхностных явлений в двигателях и механизмах, в частности в условиях граничного трения, при каталитических превращениях топлив и масел в контакте с нагретыми поверхностями металлов, при протекании электрохимических процессов на границе раздела металл — нефтепродукт, а также в условиях одновременного действия всех перечисленных факторов. [c.12]
[c.12]
Хотя за последние годы в литературе и появились словари специальных терминов, например [Stull,1977 Gugan,1979 АСМН,1979 anvey,1981],автор не смог найти какой-либо удовлетворительной систематической классификации различных явлений, составляющих пожар и возникающих при реализации основных химических опасностей. После рассмотрения существа дела будет сделана попытка построить такую таксономию по крайней мере в отношении горения жидкостей, газов и паров. [c.138]
При горении в узких каналах теплопые потери имеют в основном механизм кондуктивной теплопроводности к стенкам капала. Здесь охлаждается зона реакции заведомо взрывчатых газовых систем. В достаточно узких каналах возможны гасящие тепловые потери даже для наиболее быстрогорящих взрывчатых систем. Это явление используется при применении огнепреградителей с узкими каналами, отделяющими опасный аппарат от защищаемого огнепреградителем окружающего про-страпства, потенциально заполненного взрывчатой средой. Другого выхода из опасного аппарата газ и пламя не имеют. [c.42]
Другого выхода из опасного аппарата газ и пламя не имеют. [c.42]
1
Первый слайд презентации: Химические явления. Горение
Презентация по природоведению для 5 класса Подготовила Шашлова Т.А.
Изображение слайда
2
Слайд 2: Цель урока
Познакомиться с новыми понятиями: химические явления, химические реакции;
Познакомиться с реакцией горения;
Определить значение горения для человека.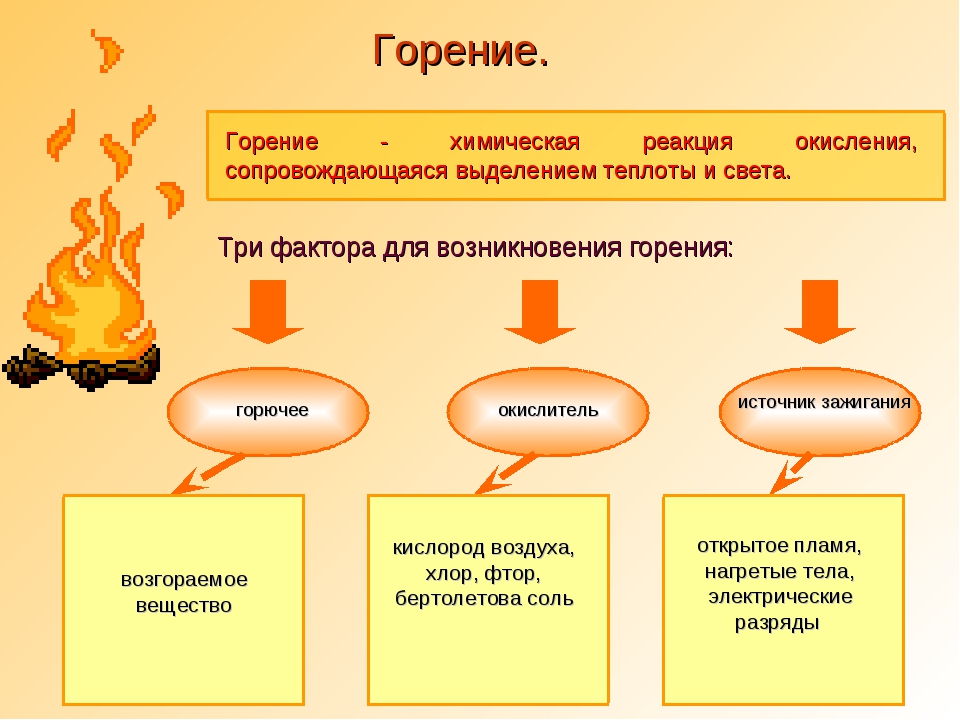
Изображение слайда
3
Слайд 3
Химическое явление (реакция) – явление, при котором образуются новые вещества. Литье металлов Обжигание глины Получение мыла
Изображение слайда
4
Слайд 4: А по каким признакам можно определить, что произошла химическая реакция ?
При некоторых химических реакциях происходит выпадение осадка;
Другие реакции сопровождаются изменением цвета исходного вещества;
В третьих происходит изменение его вкуса;
В четвертых – выделение газа, выделение или поглощение тепла и света.
Изображение слайда
5
Слайд 5
Признаки химических реакций Изменение цвета исходного вещества Изменение вкуса исходного вещества Выпадение осадка Выделение газа Появление запаха
Изображение слайда
6
Слайд 6
Изменение цвета Изменение вкуса Выделение газа Раствор крахмала йод
Изображение слайда
7
Слайд 7: Реакция горения
Реакцию, сопровождающуюся выделением тепла и света, называют горением.
Изображение слайда
8
Слайд 8: Строение пламени свечи
Менее яркое пламя Яркое пламя Темное пламя
Изображение слайда
9
Слайд 9: Как погасить пламя? — п рекратить доступ воздуха
Можно гасить водой:
древесину;
уголь. Нельзя гасить водой:
бензин;
нефть;
керосин.
Нельзя гасить водой:
бензин;
нефть;
керосин.
Изображение слайда
10
Слайд 10: Горючие материалы, сжигаемые для использования выделяющейся теплоты, называют топливом
Изображение слайда
11
Слайд 11
Изображение слайда
12
Слайд 12
Изображение слайда
13
Слайд 13
Изображение слайда
14
Слайд 14: Значение горения:
обеспечивает движение транспорта;
обогревает жилища;
применяется во всех отраслях промышленности;
применяется в сельском хозяйстве;
используется на тепловых электростанциях.
Изображение слайда
15
Слайд 15
Изображение слайда
16
Слайд 16: Закрепление
почему при протапливании печей открывают трубы?
к какой группе явлений можно отнести: гниение листьев; скисание молока; таяние льда; журчание ручья; сгорание дров.
Изображение слайда
17
Слайд 17: Домашнее задание
прочитать параграф 14 ответить на вопросы 4, 6 (стр. 62) письменно.
Изображение слайда
18
Последний слайд презентации: Химические явления. Горение: Спасибо за внимание!
Изображение слайда
Горение свечи это физическое или химическое явление ? Раскрываем тайну огня
В этой статье мы рассмотрим вопрос о том, горение свечи – это физическое или химическое явление, обоснуем свою точку зрения и докажем ее верность. Однако для начала мы уделим внимание общим сведениям о том, что представляет собой процесс горения. Также поговорим, из-за чего его сложно отнести к конкретно физическим или химическим процессам.
Однако для начала мы уделим внимание общим сведениям о том, что представляет собой процесс горения. Также поговорим, из-за чего его сложно отнести к конкретно физическим или химическим процессам.
Горение – что это с точки зрения науки
Горение – сложный процесс с физическими и химическими реакциями, при котором исходные вещества превращаются в продукты сгорания. Происходит это из-за экзотермической реакции, которая сопровождается обильным выделением тепловой энергии. Из этого определения уже понятно, почему четко разобраться в том, горение свечи – это физическое или химическое явление, довольно сложно.
Отдельно стоит поговорить о таком термине, как «пламя». Это образованная в результате реакций горения зона, от которой исходят свет и тепло. Температура пламени зависит от условий, при которых происходит само горение, а также от смесей, участвующих в этом процессе.
Что представляет собой горение свечи
Теперь, когда мы знаем немного теории, можно плавно переходить к вопросу о том, горение свечи – это физическое или химическое явление, и почему сложно разобраться в этом вопросе. На основе приведенных выше фактов, мы можем с уверенностью утверждать, что горение – это смесь из химических и физических явлений. Если отбросить в сторону сам момент, когда свеча поджигается, то при горении можно обозначить несколько моментов.
На основе приведенных выше фактов, мы можем с уверенностью утверждать, что горение – это смесь из химических и физических явлений. Если отбросить в сторону сам момент, когда свеча поджигается, то при горении можно обозначить несколько моментов.
Первым делом, происходит физический процесс. От горячего пламени во все стороны исходит тепло, в том числе и в нижнюю часть. Излучение, попадающее на саму парафиновую свечу (возьмем в качестве примера самый простой вариант этого изделия), нагревает ее материал.
Далее происходит расплавление парафина, который под воздействием капиллярных сил равномерно идет вдоль фитиля прямо к его горящей части. В этом месте происходит испарение парафина.
Пары парафина подхватываются восходящим воздухом и смешиваются с ним.
Однако это далеко не вся информация о том, горение свечи – это физическое или химическое явление, ведь дальше в дело вступает химический процесс, а именно, начинается окисление парафина. Говоря иными словами, происходит распадение его молекул, если не вдаваться в подробности, вплоть до самих атомов. Парафины представляют собой углеводороды, чьи молекулы составлены из атомов C и H. Они соединяются с кислородом, вследствие чего появляются вода и углекислый газ. А в результате окисления идет выделение энергии, относящееся к химическим процессам.
Парафины представляют собой углеводороды, чьи молекулы составлены из атомов C и H. Они соединяются с кислородом, вследствие чего появляются вода и углекислый газ. А в результате окисления идет выделение энергии, относящееся к химическим процессам.
Еще недавно лечение разного рода нарушений кожного покрова производилось с помощью многочисленных перевязочных материалов: ваты, бинтов, тампонов или марли. Современная медицина предполагает использование более современных и технологичных способов — стерильных послеоперационных повязок. В статье вы найдете информацию о популярных товарах этой категории и их особенностях.
На этом можно было бы остановиться и закрыть вопрос о том, горение свечи – это физическое или химическое явление, ведь мы наглядно видим, что здесь происходят сразу оба процесса. Однако давайте рассмотрим процесс горения до конца. За окислением снова начинается физическая часть процесса. Образовавшаяся энергия поступает ко всем задействованным в работе молекулам, благодаря чему повышается их кинетическая сила. Иногда часть этой силы выделяется в качестве света или обычного свечения. Затем поднимающиеся потоки горячих газов способствуют образованию пламени свечи.
Иногда часть этой силы выделяется в качестве света или обычного свечения. Затем поднимающиеся потоки горячих газов способствуют образованию пламени свечи.
Подводим итоги
Выходит, что споры о том, горение свечи – это физическое или химическое явление, наблюдения, о чем ведутся уже очень давно, можно смело закрывать. В горении свечи присутствуют и химические, и физические процессы одновременно.
Горение: реакция, виды и характеристики
Горение – это совокупность одновременно протекающих физических процессов (плавление, испарение, ионизация) и химических реакций окисления горючего вещества и материала, сопровождающееся, как правило, световым и тепловым излучением и выделением дыма. В основе горения лежит взаимодействие горючего вещества с окислителем, преимущественно с кислородом воздуха.
Однако горения может осуществляться без доступа воздуха (кислорода), если в состав горючей массы (среды) входит окислитель в виде примеси или составной части молекулы. В производственных условиях или ракетной технике горения может осуществляться в атмосфере таких окисляющих газов, как фтор, хлор, окислы азота и другие.
В производственных условиях или ракетной технике горения может осуществляться в атмосфере таких окисляющих газов, как фтор, хлор, окислы азота и другие.
Процесс горения
Некоторые вещества (порошкообразные титан и цирконий) способны гореть в атмосфере азота, двуокиси углерода, не относящимся к традиционным окислителям.
В зависимости от способа подвода окислителя различают:
- диффузионное горение, когда реагенты (горючее и окислитель) перед началом горения не были перемешаны, а их смешение происходит в процессе горения за счет диффузии;
- гомогенное горение, когда реагенты перед началом горения были перемешаны без поверхности раздела фаз;
- гетерогенное горение, когда реагенты находятся в разных агрегатах состояния (твердое + газ, твердое + жидкость) или между ними имеется поверхность раздела (твердое + твердое, несмешивающиеся жидкость + жидкость). Гетерогенное горение часто относят к диффузионному горению.

- горение, скорость которого лимитирована скоростью химической реакции, называют кинетическим горением. Так как скорость химического взаимодействия, как правило, выше скорости диффузии, кинетическое горение протекает с максимальной для данной системы скоростью (дефлаграция, детонация).
При пожаре отмечается смешанный тип горения. В зависимости от скорости горение может быть медленным (тление), нормальным (дефлаграция) и взрывообразным (взрыв), переходящим в детонационное (детонация).
По внешнему проявлению горение может быть пламенным или беспламенным.
Беспламенное горение может возникнуть в результате дефицита окислителя (тление) или при низком давлении насыщенных паров горючего вещества (горение тугоплавких металлов и кокса).
По механизму развития горение может быть тепловым, при котором причиной самоускорения реакций окисления является повышение температуры, и автокаталитическим (цепным), когда ускорение процесса достигается накоплением промежуточных катализирующих продуктов (активных центров). Автокаталитическое горение осуществляется при сравнительно низких температурах. При достижении определенных концентраций промежуточных каталитических продуктов автокаталитическое горение может переходить в тепловое. При этом температура горения резко возрастает.
Горение может возникать и развиваться спонтанно, стихийно (пожар), но может быть специально организованным, целесообразным: энергетическое горение (в целях получения тепловой или электрической энергии) и технологическое горение (доменный процесс, металлотермия, синтез тугоплавких неорганических соединений и т. д.).
д.).
Горение характеризуется такими величинами, как: температура, скорость, полнота, состав продуктов. Располагая данными о механизме горения и его характерных особенностях, можно увеличивать скорость и температуру горения (промотирование горения) или снижать их вплоть до прекращения горения (ингибирование горения).
Источники: Основные характеристики горения. Мальцев В.М., Мальцев М.И., Кашпоров Л.Я. —М., 1977; Процессы горения в химической технологии и металлургии. Мержанов А.Г. —Черноголовка, 1975; Физика горения и взрыва. Хитрин Л.Н. —М., 1957.
youtube.com/embed/ZMb76Sbr9aI?autohide=2&autoplay=0&mute=0&controls=1&fs=1&loop=0&modestbranding=0&playlist=&rel=0&showinfo=1&theme=light&wmode=&playsinline=0″ frameborder=»0″ allowfullscreen=»» allow=»autoplay; encrypted-media; picture-in-picture» title=»»/>
горения | Определение, реакция, анализ и факты
Горение , химическая реакция между веществами, обычно включающими кислород, обычно сопровождающаяся выделением тепла и света в виде пламени. Скорость или скорость объединения реагентов высока, отчасти из-за природы самой химической реакции, а отчасти из-за того, что генерируется больше энергии, чем может уйти в окружающую среду, в результате чего температура реагентов повышается. чтобы еще больше ускорить реакцию.
Британская викторина
Типы химических реакций
Можете ли вы определить, какой тип химической реакции показан? Проверьте свои знания с помощью этой викторины!
Знакомый пример реакции горения — зажженная спичка. Когда зажигается спичка, трение нагревает голову до температуры, при которой химические вещества вступают в реакцию и выделяют больше тепла, чем может уйти в воздух, и они горят пламенем.Если ветер уносит тепло или химикаты влажные и трение не повышает температуру в достаточной степени, спичка гаснет. При правильном зажигании тепло от пламени повышает температуру соседнего слоя спички и кислорода в прилегающем к ней воздухе, и древесина и кислород вступают в реакцию сгорания. Когда достигается равновесие между общей тепловой энергией реагентов и общей тепловой энергией продуктов (включая фактическое количество тепла и излучаемого света), горение прекращается.Пламя имеет определенный состав и сложную структуру; Говорят, что они разнообразны и способны существовать как при довольно низких, так и при чрезвычайно высоких температурах. Излучение света в пламени происходит из-за присутствия возбужденных частиц и, как правило, заряженных атомов и молекул, а также электронов.
Когда зажигается спичка, трение нагревает голову до температуры, при которой химические вещества вступают в реакцию и выделяют больше тепла, чем может уйти в воздух, и они горят пламенем.Если ветер уносит тепло или химикаты влажные и трение не повышает температуру в достаточной степени, спичка гаснет. При правильном зажигании тепло от пламени повышает температуру соседнего слоя спички и кислорода в прилегающем к ней воздухе, и древесина и кислород вступают в реакцию сгорания. Когда достигается равновесие между общей тепловой энергией реагентов и общей тепловой энергией продуктов (включая фактическое количество тепла и излучаемого света), горение прекращается.Пламя имеет определенный состав и сложную структуру; Говорят, что они разнообразны и способны существовать как при довольно низких, так и при чрезвычайно высоких температурах. Излучение света в пламени происходит из-за присутствия возбужденных частиц и, как правило, заряженных атомов и молекул, а также электронов.
Горение охватывает большое количество разнообразных явлений, широко применяемых в промышленности, науке, профессии и в быту, и его применение основано на знаниях физики, химии и механики; их взаимосвязь становится особенно очевидной при рассмотрении распространения пламени.
В общем, горение является одной из наиболее важных химических реакций и может считаться завершающей стадией окисления определенных видов веществ. Хотя когда-то считалось, что окисление представляет собой простую комбинацию кислорода с любым соединением или элементом, значение этого слова было расширено и теперь включает любую реакцию, в которой атомы теряют электроны, тем самым становясь окисленными. Как уже указывалось, в любом процессе окисления окислитель забирает электроны у окисляемого вещества, тем самым становясь восстановленным (приобретая электроны).Окислителем может быть любое вещество. Но эти определения, достаточно ясные в применении к атомной структуре для объяснения химических реакций, не так четко применимы к горению, которое, вообще говоря, остается типом химической реакции с участием кислорода в качестве окислителя, но осложняется тем фактом, что процесс включает а также другие виды реакций и тем, что это происходит в необычно быстром темпе. Более того, большинство пламен имеет в своей структуре участок, в котором вместо окисления протекают реакции восстановления. Тем не менее, главным событием при горении часто является соединение горючего материала с кислородом.
Тем не менее, главным событием при горении часто является соединение горючего материала с кислородом.
горения | Определение, реакция, анализ и факты
Горение , химическая реакция между веществами, обычно включающими кислород, обычно сопровождающаяся выделением тепла и света в виде пламени. Скорость или скорость объединения реагентов высока, отчасти из-за природы самой химической реакции, а отчасти из-за того, что генерируется больше энергии, чем может уйти в окружающую среду, в результате чего температура реагентов повышается. чтобы еще больше ускорить реакцию.
Британская викторина
Типы химических реакций
Можете ли вы определить, какой тип химической реакции показан? Проверьте свои знания с помощью этой викторины!
Знакомый пример реакции горения — зажженная спичка. Когда зажигается спичка, трение нагревает голову до температуры, при которой химические вещества вступают в реакцию и выделяют больше тепла, чем может уйти в воздух, и они горят пламенем.Если ветер уносит тепло или химикаты влажные и трение не повышает температуру в достаточной степени, спичка гаснет. При правильном зажигании тепло от пламени повышает температуру соседнего слоя спички и кислорода в прилегающем к ней воздухе, и древесина и кислород вступают в реакцию сгорания. Когда достигается равновесие между общей тепловой энергией реагентов и общей тепловой энергией продуктов (включая фактическое количество тепла и излучаемого света), горение прекращается.Пламя имеет определенный состав и сложную структуру; Говорят, что они разнообразны и способны существовать как при довольно низких, так и при чрезвычайно высоких температурах. Излучение света в пламени происходит из-за присутствия возбужденных частиц и, как правило, заряженных атомов и молекул, а также электронов.
Когда зажигается спичка, трение нагревает голову до температуры, при которой химические вещества вступают в реакцию и выделяют больше тепла, чем может уйти в воздух, и они горят пламенем.Если ветер уносит тепло или химикаты влажные и трение не повышает температуру в достаточной степени, спичка гаснет. При правильном зажигании тепло от пламени повышает температуру соседнего слоя спички и кислорода в прилегающем к ней воздухе, и древесина и кислород вступают в реакцию сгорания. Когда достигается равновесие между общей тепловой энергией реагентов и общей тепловой энергией продуктов (включая фактическое количество тепла и излучаемого света), горение прекращается.Пламя имеет определенный состав и сложную структуру; Говорят, что они разнообразны и способны существовать как при довольно низких, так и при чрезвычайно высоких температурах. Излучение света в пламени происходит из-за присутствия возбужденных частиц и, как правило, заряженных атомов и молекул, а также электронов.
Горение охватывает большое количество разнообразных явлений, широко применяемых в промышленности, науке, профессии и в быту, и его применение основано на знаниях физики, химии и механики; их взаимосвязь становится особенно очевидной при рассмотрении распространения пламени.
В общем, горение является одной из наиболее важных химических реакций и может считаться завершающей стадией окисления определенных видов веществ. Хотя когда-то считалось, что окисление представляет собой простую комбинацию кислорода с любым соединением или элементом, значение этого слова было расширено и теперь включает любую реакцию, в которой атомы теряют электроны, тем самым становясь окисленными. Как уже указывалось, в любом процессе окисления окислитель забирает электроны у окисляемого вещества, тем самым становясь восстановленным (приобретая электроны).Окислителем может быть любое вещество. Но эти определения, достаточно ясные в применении к атомной структуре для объяснения химических реакций, не так четко применимы к горению, которое, вообще говоря, остается типом химической реакции с участием кислорода в качестве окислителя, но осложняется тем фактом, что процесс включает а также другие виды реакций и тем, что это происходит в необычно быстром темпе. Более того, большинство пламен имеет в своей структуре участок, в котором вместо окисления протекают реакции восстановления. Тем не менее, главным событием при горении часто является соединение горючего материала с кислородом.
Тем не менее, главным событием при горении часто является соединение горючего материала с кислородом.
От чего горит огонь? Почему один огонь — ревущий ад, в то время как другой едва ползет? Огонь — это химическая реакция, в которой энергия в виде тепла выделяется. произведено. Когда лесное топливо горит, есть химическое соединение кислорода воздуха с древесным материалом, смола и другие горючие элементы, встречающиеся в лесной среде. Этот процесс известен как возгорание. Горение — это цепная реакция, химически подобная фотосинтезу в обеспечить регресс. Фотосинтез требует большого количества тепла, которое выделяется
солнце. Процесс горения
высвобождает это тепло. Огромный
количество тепла, которое выделяется в процессе горения, является основной причиной того, что
тушение лесных пожаров — такая сложная задача, и почему использование
предписанный пожар — сложный и требовательный процесс, требующий знающих и
опытные люди. Процесс горения или возгорания иногда называют быстрым. окисление. Это похоже на образование ржавчины на железе или гниение мертвой древесины в лесу, кроме процесс резко ускоряется. Пожар начинается с возгорания. В спичка — обычное устройство зажигания. Трение создает достаточно тепла для воспламенения фосфора в конце спички. Произойдет возгорание, и спичка загорится. Для начала процесса сгорания необходимо тепло. Однажды начавшись, огонь производит собственное тепло.Пожары на дикой земле возникают от таких источников тепла, как спички, угли. от сигарет, сигар или трубок, костров, мусорных костров, выхлопных искр от железнодорожные локомотивы, искры от тормозных колодок или горячих ящиков железнодорожных вагонов. молния, самовозгорание, раскаленный пепел и поджоги. Огненный треугольникТребуются три вещи в правильном сочетании прежде, чем произойдет возгорание и горение — Heat, Oxygen and Fuel .
Тепло — это энергия Источники тепла:
Солнце — главный источник тепла. С непрерывной подачей тепла (от сам процесс горения) воспламенение дополнительного топлива будет продолжаться как пока присутствует достаточно кислорода. Таким образом очевидно, что эти три элемента должны присутствовать и удовлетворительно вместе до того, как горение может произойти и продолжиться Для простоты мы называем это Треугольником Огня. Удалите любую из трех сторон или элементов.
и огонь перестанет гореть. Ослабить
любой, и огонь ослабнет.Увеличивать
любой один или несколько элементов, и огонь усилится. Демонстрация ВНИМАНИЕ: банка сильно нагревается! Не трогай это без защиты. Маленьким детям не следует выполнять это упражнение. без присмотра взрослых. Есть несколько способов сломать или изменить огненный треугольник. Один из примеров того, как можно сломать треугольник, можно сделать с помощью короткого свеча и банка.Зажечь свечу и поставьте на ровную поверхность. После хорошо горит, переверните банку на свечу. Через некоторое время свеча погаснет. Это происходит из-за того, что весь кислород внутри емкости был израсходован горящая свеча и дополнительный кислород не может попасть в свечу из-за банка. Прежде чем поставить банку горящая свеча, у вас были все ингредиенты, необходимые для горения; нагревать от спички, топливо в свече и кислород из воздуха. Зажгите свечу заново.Этот раз,
возьмите ножницы, отрежьте фитиль под пламенем и удалите
свеча. При тушении пожара цель состоит в том, чтобы остановить возгорание путем удаления или изменение одной или нескольких сторон треугольника. Стадии горения: пламя этапы (см. рисунки из лаборатории) Температура предварительного подогрева топлива повышена до точки, при которой газы начать улетучиваться Испаряются летучие вещества в топливе до воспламенения Пламя достигается температура воспламенения топлива и сгорание начинается Переходное топливо частично расходуется при сгорании, в то время как пламя продолжается в порциях топлива, приводящих к возникновению тления и дыма поколение Тлеющее сгорание топлива практически завершено при наличии кислорода. Раскаленная ступень горения с ограниченным содержанием кислорода Четыре наиболее важные стадии сгорания для предписанных горелок: предварительное воспламенение (топливо готово загореться) пламенное активное горение Начало переходного дыма тление остаточного дыма Тушение огня и дыма поколение (сегмент по подавлению) Когда начался лесной пожар, мы пытаемся удалить кислородную сторону треугольника.
тушив огонь антипиреном, пеной, грязью или водой в мелком
спрей или туман.Они заменят
кислород вокруг топлива воздействует на одну сторону огненного треугольника.
Они также поглощают тепло и, таким образом, изменяют тепловую сторону треугольника.
Замедлители покроют топливо и защитят его от тепла даже после
вода испарилась. Они также
подавить горение пламенем химическим действием.
Пена также покрывает топливо и служит дольше, чем вода. Вода поглощает огромное количество тепла, особенно при нанесении в виде тумана. Каждая капля поглощает большое количество тепла, что превращает воду в горячий газ или пар (пар). Горячий пар затем рассеивается ветром в атмосферу. Однако вода тяжелая и ее сложно доставить на линию огня. в труднодоступных местах. А также есть возможность выбежать в самый неподходящий момент и потерять Пожар. В условиях леса один из наиболее важных подходов к подавлению
Wildfires — это удаление третьей стороны треугольника — топлива.
Топливо удаляется путем создания пожарной линии, разделяющей топливо.
Когда лесной пожар горит до линии огня, топлива больше нет и
огонь гаснет. Линия огня
обычно изготавливается агрегатом трактор-плуг или вручную.
(В западной части США
используются бульдозеры и ручные инструменты из-за крутых каменистых условий. Удаление топлива Удаление источника топлива — это самый распространенный метод борьбы с лесными пожарами. Этот метод не тушит огонь. Огонь продолжает гореть до тех пор, пока топливо внутри линии огня не сгорит. потребляется. Удаление топлива в путь огня предотвращает распространение огня. Медленно продвигающийся огонь, горит разреженная земля Топливо можно проверить, проложив пожарный трубопровод до минерального грунта. Горячий, быстроразвивающийся огонь может потребовать нескольких линий огня, выжигающих топливо между линиями огня и огнем или их комбинация. Хорошая процедура тушения пожара часто представляет собой умелую комбинацию удаления топлива, тепло и кислород.Поэтому, когда вы при тушении пожара следует подумать о том, как лучше всего использовать персонал и оборудование для удаления одной или всех сторон огненного треугольника 1. Огонь — это — выберите ответ -a. химическая реакцияb. молекулярная реакцияc. надуманный ответ на определенные условияd. атомная реакция
2.
Тепловую энергию, выделяемую огнем, можно рассматривать как запасенную энергию от
— выберите ответ -a. неизвестные источники b. продукт фотосинтезаc. атомное действиеd. солнце
3.
Три ножки огненного треугольника — это
— выберите ответ -a.огонь, солнце, атмосфераb. тепло, топливо, энергияc. температура воспламенения, кислород, заправлен. спичка, листья, ветер
4.
Огонь — это
— выберите ответ -a. взрывb. цепная реакцияc. загадочное явление. результат клеточного сбоя
5.
Огненные стадии огня, пламенеющие стадии — это
— выберите ответ -a. предварительный нагрев, предварительное зажигание, пламя, горение, накал b. предварительное зажигание, пламя, горение, остаточное, тлеющееc. предварительный нагрев, пламя, горение, тление, тление. предварительный нагрев, предварительное зажигание, пламя, переход, тление, тление
6.
Двумя наиболее важными стадиями пламени для предписанных горелок являются:
— выберите ответ -a. химическая реакцияb. молекулярная реакцияc. надуманный ответ на определенные условияd. атомная реакция
2.
Тепловую энергию, выделяемую огнем, можно рассматривать как запасенную энергию от
— выберите ответ -a. неизвестные источники b. продукт фотосинтезаc. атомное действиеd. солнце
3.
Три ножки огненного треугольника — это
— выберите ответ -a.огонь, солнце, атмосфераb. тепло, топливо, энергияc. температура воспламенения, кислород, заправлен. спичка, листья, ветер
4.
Огонь — это
— выберите ответ -a. взрывb. цепная реакцияc. загадочное явление. результат клеточного сбоя
5.
Огненные стадии огня, пламенеющие стадии — это
— выберите ответ -a. предварительный нагрев, предварительное зажигание, пламя, горение, накал b. предварительное зажигание, пламя, горение, остаточное, тлеющееc. предварительный нагрев, пламя, горение, тление, тление. предварительный нагрев, предварительное зажигание, пламя, переход, тление, тление
6.
Двумя наиболее важными стадиями пламени для предписанных горелок являются:
— выберите ответ -a. пылающий, тлеющийb. пылающий, переходныйc. переходный, тлеющий. тлеющий, светящийся
7.
Тушение или удержание установленного огня состоит из:
— выберите ответ -a. снижение температуры или ограничение кислорода b. удушение или охлаждениеc. охлаждение или ограничение кислорода. ограничение топлива или охлаждения пылающий, тлеющийb. пылающий, переходныйc. переходный, тлеющий. тлеющий, светящийся
7.
Тушение или удержание установленного огня состоит из:
— выберите ответ -a. снижение температуры или ограничение кислорода b. удушение или охлаждениеc. охлаждение или ограничение кислорода. ограничение топлива или охлаждения |
Что такое огонь? — Science Learning Hub
Огонь — это видимый эффект процесса горения — особого типа химической реакции.Это происходит между кислородом в воздухе и каким-то топливом. Продукты химической реакции полностью отличаются от исходного материала.
Топливо должно быть нагрето до температуры воспламенения, чтобы произошло сгорание. Реакция будет продолжаться, пока есть достаточно тепла, топлива и кислорода. Это известно как огненный треугольник.
Горение — это реакция топлива с кислородом с выделением тепловой энергии. Горение может быть медленным или быстрым в зависимости от количества доступного кислорода.Возгорание, в результате которого возникает пламя, происходит очень быстро и называется горением. Горение может происходить только между газами.
Горение может происходить только между газами.
Химическая реакция в процессе горения
Топливо может быть твердым, жидким или газообразным. Во время химической реакции, приводящей к возгоранию, топливо нагревается до такой степени, что (если это уже не газ) оно выделяет газы со своей поверхности.
При горении могут вступать в реакцию только газы. Газы состоят из молекул (групп атомов). Когда эти газы достаточно горячие, молекулы в газах распадаются, и фрагменты молекул воссоединяются с кислородом из воздуха, образуя новые молекулы продукта — молекулы воды (H 2 O) и молекулы диоксида углерода (CO 2 ) — и другие продукты, если сжигание не завершено.
Тепло, выделяемое в результате реакции, поддерживает огонь. Тепло пламени удерживает оставшееся топливо при температуре воспламенения. Пламя воспламеняет выделяющиеся газы, и огонь распространяется. Пока есть достаточно топлива и кислорода, огонь продолжает гореть.
Топливо + кислород (из воздуха) = продукты сгорания (в основном CO 2 + H 2 O) + тепловая энергия.
Полное сгорание
При полном сгорании топливо производит только воду и углекислый газ (без дыма или других продуктов).Пламя обычно синее. Для этого должно быть достаточно кислорода, чтобы полностью соединиться с топливным газом.
Многие из нас используют метан (CH 4 ), широко известный как природный газ, дома для приготовления пищи. Когда газ нагревается (пламенем или искрой) и если в атмосфере достаточно кислорода, молекулы распадаются и полностью преобразуются в воду и углекислый газ.
| CH 4 (г) | + | 2O 2 (г) | + | тепло | → | CO 2 (г) | + | 2H O (г) | + | тепло | |
| метан | + | кислород | + | тепло | → | диоксид углерода | + | вода | + | тепло |
Неполное сгорание
Если во время химической реакции не хватает кислорода, происходит неполное сгорание и образуются такие продукты, как углерод (C) и монооксид углерода (CO), а также вода и диоксид углерода. При неполном сгорании выделяется меньше тепловой энергии, чем при полном сгорании.
При неполном сгорании выделяется меньше тепловой энергии, чем при полном сгорании.
При неполном сгорании горящее пламя обычно желтого или оранжевого цвета и присутствует дым.
Связанное содержание
Изучите еще несколько важных научных идей и концепций, связанных с огнем:
- Что такое дым? объясняет неполное сгорание и опасности, которые представляет дым.
- Тепловая энергия учитывает теплопередачу — конвекцию, теплопроводность и излучение.
- Поведение при пожаре исследует переменные, влияющие на пожар.
Лесные пожары — что это такое? Что их вызывает? Как пожары влияют на нас и влияет ли на них климат?
Идеи действий
Драма в микромире — использование драмы для моделирования атомов, молекул, теплопередачи и горения.
Зажгите свечу — наблюдайте и исследуйте пламя свечи и процесс горения.
Тушение пожара — исследуйте способы тушения пожара, используя знания о пожарном треугольнике и химии пожара.
Взрывающаяся мука — наблюдение за горением.
Самовозгорание — обзор
6 Самовозгорание
Самовозгорание — это явление, при котором углеводородное (или химическое вещество) вещество неожиданно воспламеняется без видимой причины. При обычном горении углеводород намеренно нагревается до точки воспламенения, чтобы заставить его гореть. Во время этого процесса многие углеводороды подвергаются медленному окислению, которое, как и быстрое окисление при горении, выделяет тепло.Если выделяемое таким образом тепло не может уйти, температура углеводорода повышается до тех пор, пока не произойдет возгорание. Самовозгорание часто происходит в кучах тряпок, пропитанных углеводородом (маслянистых), и может представлять серьезную опасность возгорания.
Пожары, возникающие в результате самовозгорания, вызываются следующими механизмами: (1) самопроизвольное нагревание, (2) пирофорность и (3) гиперголические реакции.
Самопроизвольное нагревание — это медленное окисление элемента или соединения, которое вызывает повышение общей температуры элемента или соединения без добавления внешнего источника тепла.Самопроизвольное нагревание может быть результатом прямого окисления углеводородов (например, масел и растворителей) или может происходить из-за действия микроорганизмов в органических материалах.
Насыщенные углеводороды (например, алканы) не склонны к самовозгоранию, тогда как ненасыщенные углеводороды имеют тенденцию к самовозгоранию.
Пирофорные вещества мгновенно воспламеняются при контакте с воздухом (атмосферный кислород). Пирофорное вещество может быть твердым, жидким или газообразным.Большинство материалов не являются пирофорными, если они не находятся в очень мелкодисперсном состоянии. Хотя есть некоторые пирофорные жидкости и газы, большинство пирофорных материалов — это металлы. Пирофорность является частным случаем гиперголической реакции , потому что окислитель ограничен атмосферным кислородом.
Если пирофорность касается только самовозгорания материала при контакте с воздухом (кислородом воздуха), гиперголическая реакция описывает способность материала самовоспламеняться или взрываться при контакте с любым окислителем .
Некоторые углеводороды способны самопроизвольно нагреваться и воспламеняться при надлежащих условиях. Самопроизвольное нагревание углеводородов обычно связано с контактом горючего жидкого углеводорода с горючими материалами. Примером может служить горючая ветошь, пропитанная маслами или растворителями. Приведет ли самопроизвольный нагрев к воспламенению или нет, зависит от нескольких факторов: (1) скорости, с которой тепло выделяется и удаляется из окисляемого материала; (2) температура воспламенения волокнистого горючего материала, углеводорода или любых газов, выделяемых при окислении; (3) удельная площадь (см 2 / г, определенная ниже) углеводорода, подверженного действию окислителя; и (4) количество влаги, присутствующей в атмосфере и волокнистом материале.
Чтобы произошло самовозгорание, скорость выделения тепла в результате окисления должна превышать скорость отвода тепла за счет теплопроводности, конвекции и излучения (теплового). Когда температура материала начинает повышаться, скорость тепловыделения часто увеличивается. Результатом является реакция неуправляемого разгона , которая в конечном итоге вызывает возгорание. Если скорость отвода тепла превышает скорость генерации, материал остывает и не воспламеняется. Скорость отвода тепла может быть увеличена за счет физического контакта с теплопроводной поверхностью, вращения стопок горючих материалов для охлаждения горячих точек и циркуляции инертных газов через груды для охлаждения горячих точек и вытеснения кислорода.
Температура воспламенения материалов, очевидно, вызывает беспокойство и сильно варьируется в зависимости от материала. Гораздо более строгий контроль должен применяться к материалам с более низкими температурами воспламенения и тем, которые выделяют взрывоопасные газы. Хотя большинство материалов с высокими температурами воспламенения вызывают меньшее беспокойство, некоторые из них более взрывоопасны, чем материалы с более низкими температурами воспламенения.
Хотя большинство материалов с высокими температурами воспламенения вызывают меньшее беспокойство, некоторые из них более взрывоопасны, чем материалы с более низкими температурами воспламенения.
Удельная площадь горючего вещества — это мера площади поверхности материала, подверженной воздействию окислительной атмосферы, на грамм материала и выражается в единицах см 2 / г.Материалы с высокой удельной площадью более склонны к нагреванию и самовозгоранию.
Например, горючие жидкости на волокнистом материале представляют опасность самопроизвольного возгорания, поскольку волокна материала позволяют жидкости распространяться по большей площади поверхности, обеспечивая больший контакт с кислородом и, следовательно, пористые горючие материалы с большей вероятностью воспламеняются. чем плотно упакованные твердые материалы.
Важно, чтобы потенциально самопроизвольно нагревающиеся компаунды оставались как можно более сухими.Высокая температура окружающей среды усугубляет проблемы с влажностью. По мере повышения температуры окружающей среды скорость самопроизвольного тепловыделения также увеличивается. Высокие температуры окружающей среды также снижают скорость отвода тепла, приближая углеводород к температуре воспламенения.
По мере повышения температуры окружающей среды скорость самопроизвольного тепловыделения также увеличивается. Высокие температуры окружающей среды также снижают скорость отвода тепла, приближая углеводород к температуре воспламенения.
Самовозгорание может происходить в кучах влажного органического материала, где на ранних стадиях выделяется тепло в результате дыхания бактерий, плесени и микроорганизмов. Для активной деятельности требуется высокое содержание влаги, и нагревание обычно регулируется путем поддержания содержания влаги ниже заданного уровня.Этот тип нагрева может только нагреть материал до температуры 50–75 ° C (122–167 ° F), при которой живые организмы погибают.
За пределами этой точки должны вступить в действие реакции окисления, если должно произойти возгорание. Существование биологического обогрева требует тщательного контроля влажности, притока воздуха и находящихся поблизости горючих или легковоспламеняющихся материалов. Если горячая точка в куче органического материала вступит в контакт с легковоспламеняющейся жидкостью или газом, может произойти пожар или взрыв. Тепло, генерируемое биологическим действием, также может действовать как катализатор для других реакций, которые происходят только при повышенных температурах.
Тепло, генерируемое биологическим действием, также может действовать как катализатор для других реакций, которые происходят только при повышенных температурах.
Вероятность биологического нагрева можно снизить следующими мерами: (1) обеспечить соответствующую вентиляцию органического материала для удаления влаги, тепла и частиц пыли; (2) ограничить время хранения органического материала, используя практическое правило «первым пришел — первым ушел»; и (3) циркуляция больших количеств органических материалов для рассеивания зон локального нагрева.
Что такое горение? | Обзор химии [видео]
Combustion
Привет, ребята! Добро пожаловать в этот видеоролик о горении.Вы, наверное, уже знакомы с этим словом из таких фраз, как «самовозгорание» и «двигатель внутреннего сгорания». Вы, вероятно, ассоциируете это с горением, и это здорово, потому что общее определение горения — это просто «процесс сжигания предметов». В этом видео мы выйдем за рамки этого простого определения и поймем химические и физические явления, лежащие в основе горения.
Прежде чем делать что-либо еще, давайте составим общее химическое уравнение для горения и пару важных терминов:
топливо + кислород (O2) -> отходы + энергия
Поскольку можно использовать разные виды топлива, существует множество вариантов горения, но это основная формула.
Во всех химических реакциях участвуют реагентов и продуктов . Реагенты — это вещества, которые запускают реакцию, а продукты — это вещества, образующиеся в результате реакции.
Поскольку энергия вырабатывается, горение является экзотермической реакцией. Это означает, что химические связи продуктов более стабильны (с меньшей энергией), чем химические связи реагентов. Когда происходит реакция горения, разница в энергии между реагентами и продуктами высвобождается в виде комбинации тепла и света, иначе говоря, огня!
Так почему же дрова (обычное топливо для сжигания) просто не загораются? В конце концов, в воздухе есть кислород, поэтому кажется, что у нас есть все необходимое для реакции горения. Что ж, причина того, что дрова не загораются самопроизвольно в присутствии кислорода, заключается в том, что требуется некоторая энергия активации. Например, мы должны использовать спичку, чтобы разжечь костры. Но как только реакция горения началась, она сама производит достаточно энергии, чтобы преодолеть барьер и самоподдержаться.
Что ж, причина того, что дрова не загораются самопроизвольно в присутствии кислорода, заключается в том, что требуется некоторая энергия активации. Например, мы должны использовать спичку, чтобы разжечь костры. Но как только реакция горения началась, она сама производит достаточно энергии, чтобы преодолеть барьер и самоподдержаться.
Итак, что же является хорошим топливом для реакции горения? Что ж, глядя на общее уравнение, мы видим, что кислород является другим реагентом, что дает нам ключ к разгадке. Если топливо вступает в реакцию с кислородом, мы можем сделать вывод, что горение является типом реакции окисления.Это говорит нам о том, что если топливо будет окисляться в реакции, оно должно начинаться без окисления. Обычным топливом в реакциях горения являются углеводороды, такие как метан, этан и пропан. Все они содержат простые углеродные цепи, насыщенные водородом. Фактически, если вы использовали газовый гриль, вы, вероятно, использовали пропан в качестве топлива в реакции сгорания для приготовления пищи.
Рассмотрим конкретный пример, в котором метан \ ((CH_4) \) является топливом.
\ (CH_4 + 2O_2 -> CO_2 + 2H_2O + energy \)Здесь метан соединяется с кислородом с образованием энергии и двух побочных продуктов, двуокиси углерода и воды.Реагенты метан и кислород имеют более высокую энергию, чем продукты диоксида углерода и воды. Хотя диоксид углерода и вода являются очень стабильными соединениями, основной причиной большой разницы в энергии является относительная нестабильность одинарных и двойных связей в кислороде.
Сжигание метана, как показано, является примером полного сгорания. Атом углерода в метане полностью окисляется, когда он превращается в диоксид углерода, что приводит к высвобождению максимально возможного количества энергии.Однако при недостаточном количестве кислорода реакция может быть неполной. Это означает, что атомы углерода реагентов не полностью окисляются в процессе. Это не только приводит к сокращению производства энергии, но и создает нежелательные отходы, которые могут быть опасными для окружающей среды и здоровья человека.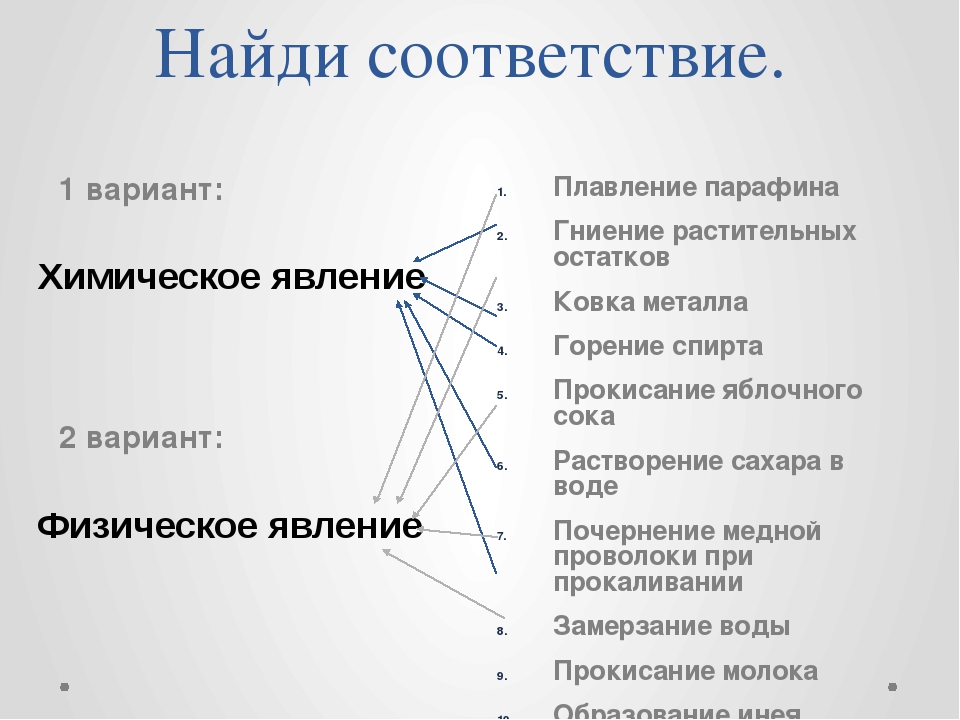 Вот химическое уравнение, показывающее пример неполного сгорания метана:
Вот химическое уравнение, показывающее пример неполного сгорания метана:
Обратите внимание, что вместо образования диоксида углерода, как при полном сгорании, метан превращается в углерод. монооксид и углерод (сажа).Поскольку мы часто используем воздух в качестве источника кислорода, который составляет всего 21% кислорода, неполное сгорание более распространено, чем полное сгорание.
Метан — лишь один из примеров горючего. Другие углеводороды, такие как этан и пропан, также горючие. При наличии достаточного количества кислорода углеводороды могут полностью сгорать, что часто называют «чистым сгоранием». Другие виды топлива, такие как древесина, бумага, уголь, бензин и т. Д., Горючие, но имеют более сложный химический состав и часто подвергаются неполному сгоранию.Следовательно, эти реакции менее энергоэффективны и, как правило, хуже для окружающей среды из-за токсичных отходов.
Хорошо, давайте рассмотрим: горение — это общий класс экзотермических реакций окисления, когда топливо вступает в реакцию с кислородом с образованием отходов и большого количества энергии, обычно характеризующихся возгоранием. Большинство реакций горения требует немного энергии для преодоления начального активационного барьера, поэтому мы запускаем газовые грили с помощью спички или искры. Большинство реакций горения являются неполными, что означает, что углерод в реагентах не окисляется полностью, что приводит к меньшему количеству производимой энергии и токсичным отходам, таким как окись углерода и сажа.Хотя использование сжигания для производства энергии имеет жизненно важное значение для развития общества, огромное количество образовавшихся отходов представляет собой серьезную угрозу для окружающей среды и здоровья человека.
Большинство реакций горения требует немного энергии для преодоления начального активационного барьера, поэтому мы запускаем газовые грили с помощью спички или искры. Большинство реакций горения являются неполными, что означает, что углерод в реагентах не окисляется полностью, что приводит к меньшему количеству производимой энергии и токсичным отходам, таким как окись углерода и сажа.Хотя использование сжигания для производства энергии имеет жизненно важное значение для развития общества, огромное количество образовавшихся отходов представляет собой серьезную угрозу для окружающей среды и здоровья человека.
Спасибо за просмотр. Мы надеемся, что это видео о горении поможет вам подготовиться и укрепить свои силы.
Избранные механизмы образования пламени, Propagat
Содержание
Проблемы горения, Йозеф Яросински и Бернар Вейсьер
Измерения для определения химического состава горения, Катарина Козе-Хёингхаус
Пределы воспламеняемости, воспламеняемость горючей смеси Пределы воспламеняемости Предел воспламеняемости и предел воспламеняемости 9010 История воспламеняемости Flame Extinction, Jozef Jarosinski
Зажигание электрическими искрами и механизм образования пламени, Michikata Kono and Mitsuhiro Tsue
Влияние граничных условий на распространение пламени
Распространение противоточного пламени
Распространение в вихрях: скорость распространения по ядру вихря, Satoru Ishizuka
Edge Flames, Suk Ho Chung
Явления нестабильности во время распространения пламени
Неустойчивости распространения пламени, Geoff Searby Устическая нестабильность, Себастьян Кандель, Даниэль Дюрокс и Тьерри Шуллер
Пламя тюльпанов: форма дефлаграции в закрытых трубах, Дерек Данн-Ранкин
Различные методы тушения пламени
Узкие каналы распространения пламени и его распространение Quenching, Artur Gutkowski and Jozef Jarosinski
Тушение пламени турбулентностью: критерии тушения пламени, Shenqyang S. Shy
Shy
Тушение противоточного предварительно смешанного пламени, Chih-Jen Sung
Распространение пламени во вращающемся цилиндрическом сосуде: механизм тушения пламени, Jerzy Chomiak and Jozef Jarosinski
Roland Borderlands Turbulent Flames
Turbulent Flames
Арно Мура и Алексей А. Бурлука
Турбулентное горение без предварительного смешивания, Джонатан Х. Франк и Роберт С. Барлоу
Моделирование турбулентного горения с высоким разрешением, Лоран Селле и Тьерри Пуансо Другие интересные случаи горения и пламени Formation
Свеча и диффузионное пламя струи: механизм горения в условиях гравитации и микрогравитации, Фумиаки Такахаси
Горение в двигателях с искровым зажиганием, Джеймс Д.Smith and Volker Sick
Сгорание в двигателях с воспламенением от сжатия, Зоран Филипи и Фолкер Больной
Переход от дефлаграции к детонации, Анджей Теодорчик
Детонации, Bernard Veyssiere
Index .


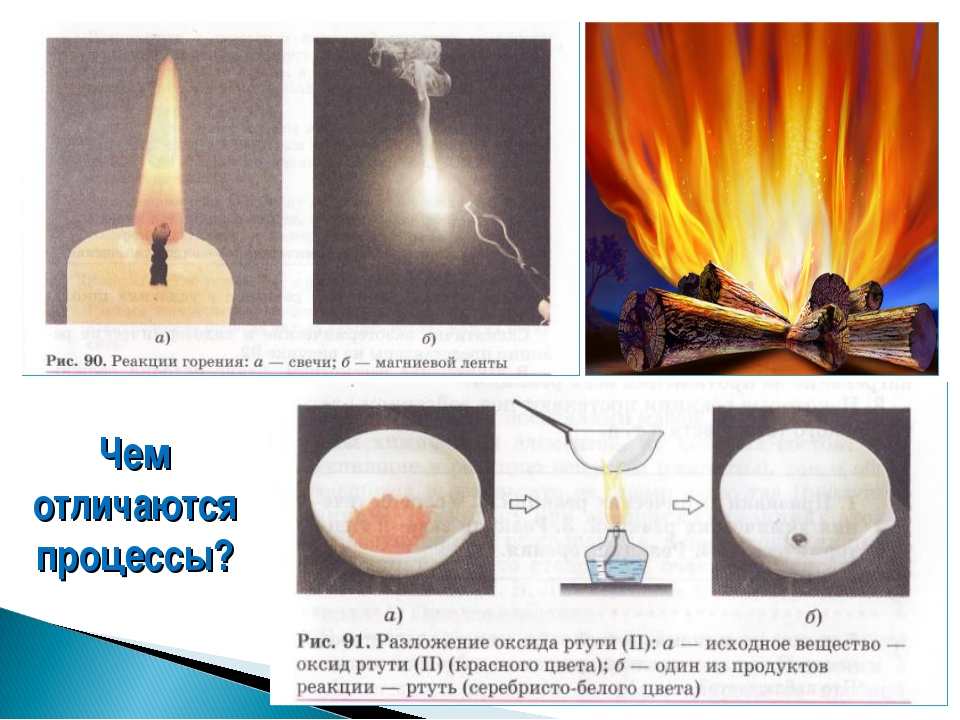



 Вооруженный
с этими знаниями пожарный или назначенная горелка могут многое сделать, чтобы
управлять огнем.
Вооруженный
с этими знаниями пожарный или назначенная горелка могут многое сделать, чтобы
управлять огнем. Опять огонь погаснет
через короткий промежуток времени, когда остаток фитиля, оставшийся на ножницах,
потребляется. На этот раз у тебя было много
кислорода в воздухе, но вы удалили топливо.
Тот же принцип используется при борьбе с лесными пожарами.
Удалите тепло, кислород или топливо, и огонь погаснет.
Опять огонь погаснет
через короткий промежуток времени, когда остаток фитиля, оставшийся на ножницах,
потребляется. На этот раз у тебя было много
кислорода в воздухе, но вы удалили топливо.
Тот же принцип используется при борьбе с лесными пожарами.
Удалите тепло, кислород или топливо, и огонь погаснет. имеется в наличии, тление продолжается, что приводит к образованию дыма
имеется в наличии, тление продолжается, что приводит к образованию дыма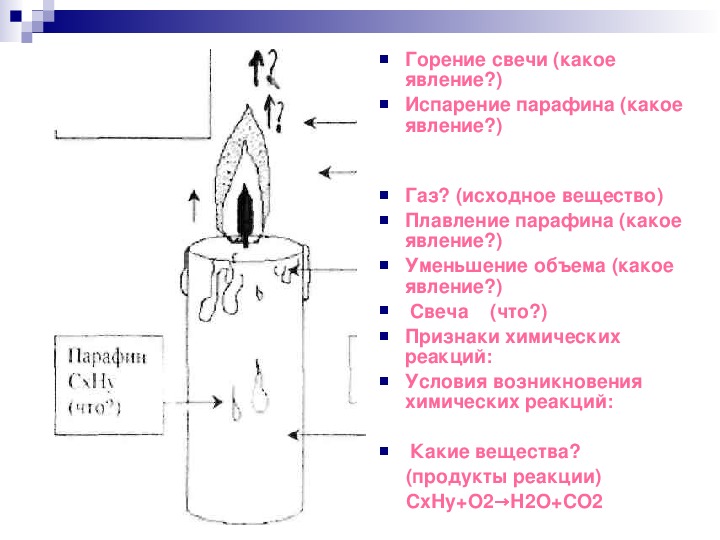 Они уменьшают тепло, а также подачу кислорода к топливу.
Они будут придерживаться вертикального топлива и могут легко наноситься по земле.
единицы измерения.
Они уменьшают тепло, а также подачу кислорода к топливу.
Они будут придерживаться вертикального топлива и могут легко наноситься по земле.
единицы измерения. )
На некоторых участках используются вертолетные экипажи и специализированная наземная техника.
)
На некоторых участках используются вертолетные экипажи и специализированная наземная техника.