Реакции конпропорционирования
ОПЫТ 10 . К содержимому пробирки ( из опыта 9) прибавить 2 мл 1М раствора серной кислоты до появления бурой окраски раствора. Пользуясь раствором крахмала, доказать, что бурая окраска вызвана процессом образования свободного иода:
NaIO3 + NaI + H2SO4 → I2 + ….
К раствору добавить несколько капель бензола (толуола). Пробирку встряхнуть и наблюдать изменение окраски бензольного кольца, обусловленного экстракцией иода (переход иода из водной фазы в органическую).
Составьте полное уравнение, используя метод ионно-электронных уравнений, укажите окислитель и восстановитель.
ОПЫТ 11 . К 1 мл
раствора сульфата марганца (MnSO4)
прибавить по каплям раствор перманганата
калия (KMnO
Составьте полное уравнение реакции, используя метод ионно-электронных уравнений, укажите окислитель и восстановитель.
33
Окислительно-восстановительная двойственность веществ
ОПЫТ 12. В одну пробирку налейте 3-5 капель 1 М KI и столько же 2н H2SO4, а в другую – 2-3 капли 1 М KMnO4 и 2-3 капли концентрированной H2SO4. В каждую пробирку добавьте по 3-5 капель пероксида водорода H2O2. Что наблюдаете? Схемы реакций:
H2O2 + I— → I2 + H2O;
H2O2 + MnO4— → Mn2+ + O2↑ + H2O.
Составьте полные уравнения реакций, используя ионно-электронный метод. Сделайте вывод об окислительно-восстановительных свойствах
H2O2.ОПЫТ 13. Какие окислительно-восстановительные свойства характерны для нитрита натрия NaNO2? Может ли он быть восстановителем? Если да, выберите на основании стандартных электродных потенциалов в ряду веществ подходящий окислитель: KMnO4, KI, KNO3. Налейте в пробирку 2мл раствора NaNO2, добавьте 1 мл разбавленной серной кислоты и добавьте раствор выбранного восстановителя. Опыт проводите под тягой. Объясните свои наблюдения. Составьте полные уравнения реакций, используя ионно-электронный метод.
Может ли NaNO2 быть окислителем?
Если да, выберите на основании стандартных
электродных потенциалов в ряду веществ
подходящий восстановитель: FeCl3,
KI,
H2O2.
В пробирку налейте 2 мл раствора выбранного
восстановителя, добавьте 1 мл раствора
H2SO4 и несколько кристаллов соли NaNO
Влияние рН на окислительные свойства
ОПЫТ 14. Налейте в две пробирки по 1 мл раствора бихромата калия
34
K2Cr2O7, в первую добавьте 3-5 капель разбавленной серной кислоты, а во вторую – 3-5 капель разбавленного раствора NaOH. Обратите внимание на изменение цвета во второй пробирке (бихромат переходит в хромат). Добавьте в обе пробирки по нескольку кристаллов соли КNO2. Объясните наблюдаемое. Запишите уравнения реакций, считая, что бихромат переходит в соединения хрома (III), а хромат (вторая пробирка) взаимодействует по схеме
CrO42- + NO2— → [Cr(OH)6]3- + NO3—.
Составьте полные уравнения реакций, используя ионно-электронный метод. Определите окислитель и восстановитель.
ОПЫТ 15 . Налейте в 3 пробирки по 3-4 капли водного раствора KMnO4, добавьте в одну разбавленной серной кислоты, во вторую – концентрированный раствор щелочи NaOH) (20%), в третью – немного дистиллированной воды. Затем в каждую пробирку добавьте несколько кристаллов сульфита натрия Na2SO3. Объясните свои наблюдения, если в кислой среде ионы MnO4— восстанавливаются до Mn2+, в нейтральной – до MnO2, в щелочной – до MnO42-. Выпишите значения стандартных окислительно-восстановительных потенциалов этих процессов. В какой среде окислительные свойства MnO4— выражены сильнее?
35
ВАРИАНТЫ ЗАДАНИЙ
Вариант | Задачи | Вариант | Задачи |
1 | 1, 45, 46(1), 47(1), 48(1) | 16 | 16, 40, 46(16), 47(16), 48(16) |
2 | 2, 44, 46(2), 47(2), 48(2) | 17 | 17, 32, 46(17), 47(17), 48(17) |
3 | 3, 43, 46(3), 47(3), 48(3) | 18 | 18, 39, 46(18), 47(18), 48(18) |
4 | 4, 39, 46(4),47(4) 48(4) | 19 | 19, 34, 46(19), 47(19), 48(19) |
| 5 | 5, 41, 46(5), 47(5), 48(5) | 20 | 20, 38, 46(20), 47(20), 48(20) |
6 | 6, 42, 46(6), 47(6), 48(6) | 21 | 21, 37, 46(21), 47(21), 48(21) |
7 | 7, 36, 46(7), 47(7), 48(7) | 22 | 22, 36, 46(22), 47(22), 48(22) |
8 | 8, 33, 46(8), 47(8), 48(8) | 23 | 23, 33, 46(23), 47(23), 48(23) |
9 | 9, 40, 46(9), 47(9), 48(9) | 24 | 24, 40, 46(24), 47(24), 48(24) |
10 | 10, 35, 46(10), 47(10), 48(10) | 25 | 25,41, 46(25), 47(25), 48(25) |
11 | 11, 36 46(11), 47(11), 48(11) | 26 | 26, 43, 46(26), 47(26), 48(26) |
12 | 12, 37, 46(12), 47(12), 48(12) | 27 | 27, 37, 46(27), 47(27), 48(27) |
13 | 13, 43, 46(13), 47(13), 48(13) | 28 | 28,35, 46(28), 47(28), 48(28) |
14 | 14, 39, 46(14), 47(14), 48(14) | 29 | 29, 45, 46(29), 47(29), 48(29) |
15 | 15, 31, 46(15), 47(15), 48(15) | 30 | 30, 44, 46(30), 47(30), 48(30) |
36
Классификация окислительно-восстановительных реакций
Основой для классификации ОВР служит местоположение окислителя и восстановителя.
1. Межатомные (а) или межмолекулярные (б) ОВР. Окислитель и восстановитель входят в состав разных веществ.
а) 2 +
+ = 2
= 2
б) 
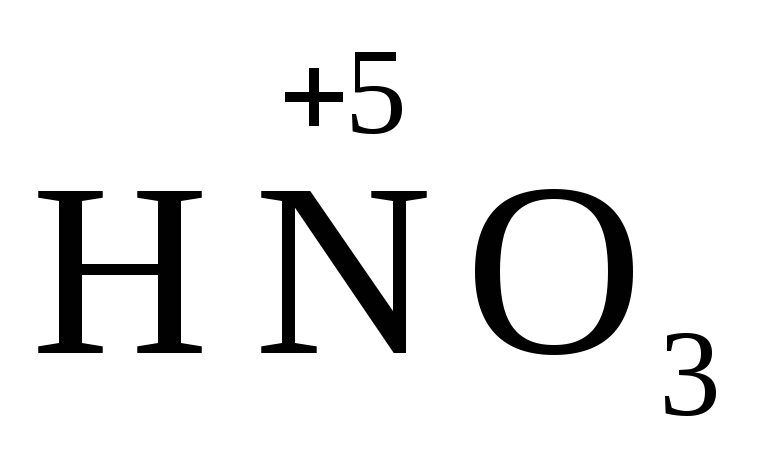 =
=  + 2
+ 2 + 2H2O
+ 2H2O2. Внутримолекулярные ОВР. Окислитель и восстановитель входят в состав одного вещества.
2 = 2
= 2 + 3
+ 3
3. Реакции диспропорционирования (дисмутации, самоокисления-самовосстановления). Окислителем и восстановителем являются атомы одного и того же элемента, находящиеся в промежуточной степени окисления и входящие в состав одного вещества. Часть атомов повышает свою степень окисления, а другая часть ее понижает.
3 =
= + 2
+ 2 +H2O
+H2O
4. Реакции конпропорционирования – это реакции, в которых атомы одного и того же элемента имеют разные степени окисления, переходят к промежуточной степени окисления.
7
Реакции конпропорционирования могут быть:
а) внутримолекулярными (в соединении имеется элемент с разными степенями окисления):
 =
= 
б) межмолекулярными (в разных соединениях имеется один и тот же элемент с разными степенями окисления)
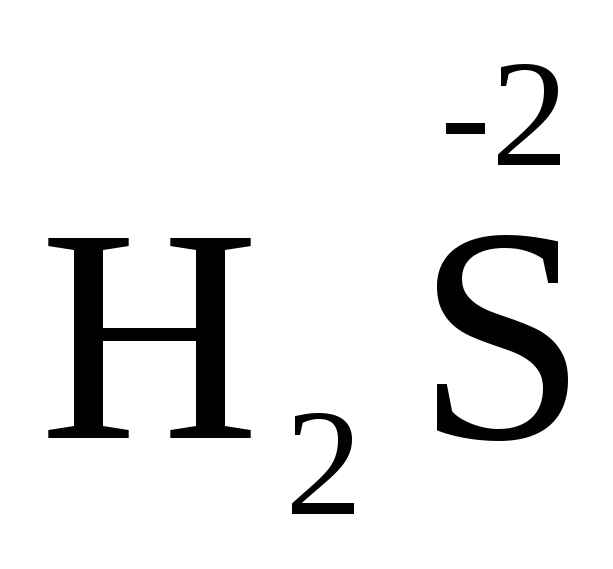 +
+ 
3 S0 + 2 H2O
3 S0 + 2 H2O
Составление уравнений окислительно-восстановительных реакций
При составлении уравнений ОВР нужно учесть, что число электронов, отданных восстановителем, равно числу электронов, принятых окислителем.
В химии условный
заряд электрона принят за «-1» и
обозначается  Для подбора стехиометрических
коэффициентов можно использовать
несколько методов, из которых наиболее
распространены два: метод электронного
баланса и метод электронно-ионных
уравнений (метод полуреакций).
Для подбора стехиометрических
коэффициентов можно использовать
несколько методов, из которых наиболее
распространены два: метод электронного
баланса и метод электронно-ионных
уравнений (метод полуреакций).
1.Метод электронного баланса является наиболее универсальным методом, и применим для любых окислительно-восстановительных процессов, протекающих в любых системах (растворы, расплавы, газы). В основе метода лежит принцип сравнения степеней окисления атомов в исходных веществах и в продуктах реакции с последующим составлением схемы электронного баланса.
В качестве примера рассмотрим реакцию взаимодействия дихромата калия с сероводородом в кислой среде:
 +
+  +
+ →
→ +
+ +
+  +
+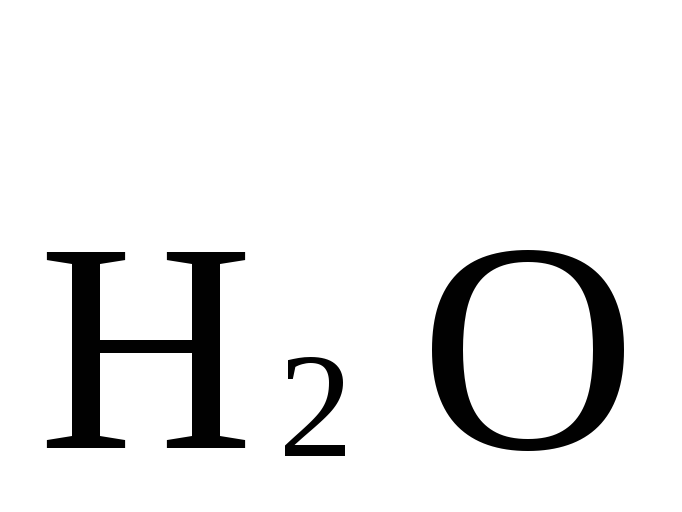
Для расстановки коэффициентов выполняем следующие действия.
1.1. Определяем элементы, атомы которых изменяют степень окисления:
8
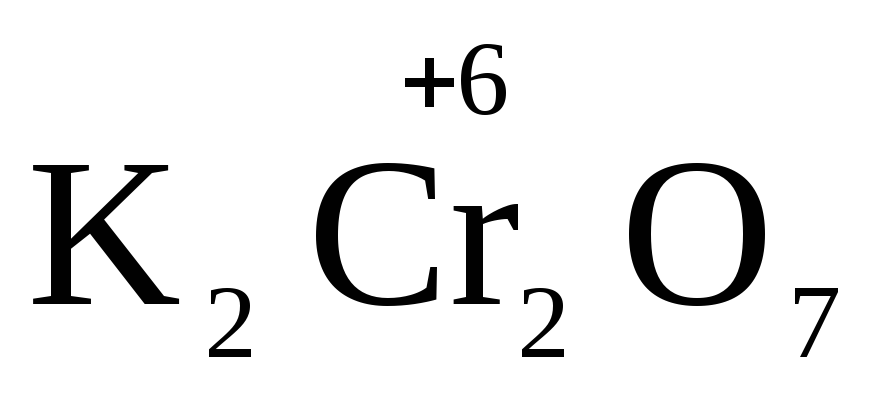 +
+  +
+ →
→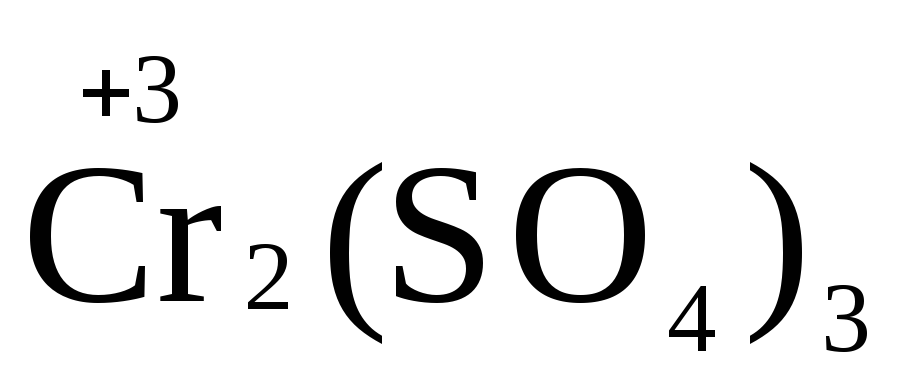 +
+ +
+  +
+
1.2. Находим
окислитель и восстановитель в данной
ОВР, составляем схему перехода электронов
от восстановителя к окислителю и пишем
отдельно электронные уравнения процессов
окисления и восстановления, с учетом
того, что количество атомов, входящих
в соединение, должно сохраняться.
Например, в  имеется два атомаCr,
следовательно, в схеме они должны
присутствовать:
имеется два атомаCr,
следовательно, в схеме они должны
присутствовать:
+5ē


 -2ē
-2ē



 +
+  +
+ →
→ +
+ +
+ 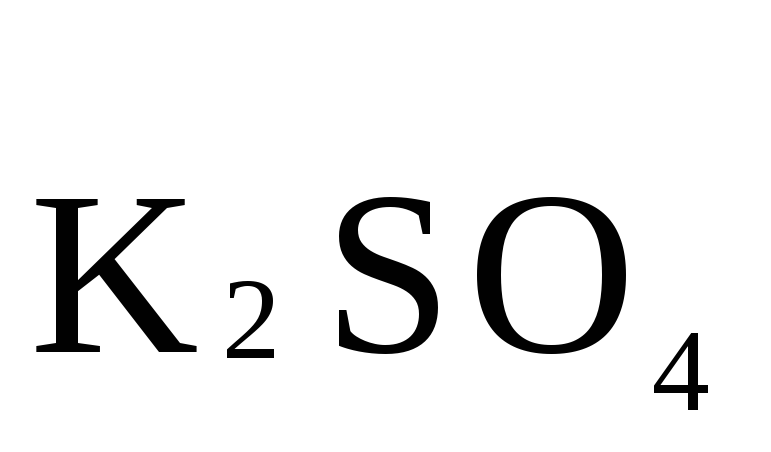 +
+
окислитель восстановитель
2Cr+6 + 6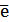 = 2Cr+3 (а) —
восстановление
= 2Cr+3 (а) —
восстановление
S-2 — 2 =
S0 (б) — окисление
=
S0 (б) — окисление
1.3. Уравниваем число электронов в процессе окисления и восстановления (электронный баланс). В приведенной схеме необходимо уравнение (б) умножить на 3, тогда будет принято и отдано по 6 электронов. После умножения уравнения складываются как обычные алгебраические, а электроны сокращаются.
2
 Cr+6 + 6
Cr+6 + 6 = 2Cr+3 1
= 2Cr+3 1
+
S-2 — 2 =
S0 3
=
S0 3

2Cr+6 +3S-2 = 2Cr+3 + 3 S0
1.4. Полученные коэффициенты называют основными. Они переносятся в молекулярную схему реакции и ставятся перед соответствующими веществами. Так как в молекулах дихромата калия и сульфата хрома содержится по два атома хрома, двойки перед этими веществами опускаются.
K2Cr2O7 + 3H2S + H2SO4 = Cr2(SO4)3 + 3S+ K2SO4 + H2O
1.5. Окончательно уравниваем число атомов каждого элемента в обеих частях молекулярного уравнения. Продукты реакции (Cr2(SO4)3, K2SO4),
9
имеющие коэффициенты по единице, содержат 4 моль сульфат-ионов (SO42-), которые содержатся в серной кислоте, следовательно, перед ней ставится коэффициент 4. Чтобы количество атомов водорода было одинаково в левой и правой части уравнения, перед водой ставится коэффициент 7:
K2Cr2O7 + 3H2S + 4H2SO4 = Cr2(SO4)3 + 3S+ K2SO4 + 7H2O
Проверка количества остальных атомов показывает, что все коэффициенты подобраны.
2. Метод электронно-ионных уравнений (метод полуреакций) применяется для подбора коэффициентов в уравнениях реакций, протекающих в растворах. Метод оперирует с реально существующими в растворах частицами и позволяет учитывать влияние среды раствора (т.е. рН) на процессы окисления и восстановления частиц. В качестве частиц среды в водных растворах могут принимать участие следующие частицы.
Таблица 1
Кислотность (рН) | Исходные частицы | Продукты |
Кислая среда (рН<7) | Н+и Н2О | Н2О и ОН— |
Нейтральная среда (рН = 7) | Н2О | Н+и ОН— |
Щелочная среда (рН>7) | Н2О и ОН— | Н2О и ОН— |
В качестве примера рассмотрим ту же реакцию.
2.1. Молекулярная схема реакции:
K2Cr2O7 + H2S + H2SO4 → Cr2(SO4)3 + S+ K2SO4 + H2O
2.2. Записываем это уравнение в ионно-молекулярной форме. Для этого необходимо все сильные электролиты представить в виде ионов, а слабые электролиты, газы и малорастворимые вещества оставляем в виде молекул. К сильным электролитам относятся все хорошо растворимые соли, часть кислот (HCl, HNO3, H2SO4 и др.), щелочи (LiOH, NaOH, KOH и др.). Степень окисления атомов не используют, а учитывают заряды реальных ионов и характер среды, в которой идет окислительно-восстановительный процесс.
10
2K+ + Cr2O7-2 + H2S + 2H++ SO4-2 = 2Cr+3+3SO4-2 + S0 + 2K+ +SO4-2 + H2O
кислая среда
2.3. Определяем частицы, изменившие свой заряд или состав:
Cr2O7-2→ 2Cr+3и H2S → S0
2.4. На основании этих превращений составляем полуреакции окисления и восстановления с участием частиц среды (см. табл.1). Анион дихромата потерял 7 моль атомов кислорода, которые в кислой среде связываются 14 моль ионами водорода и превращаются в воду. Молекула сероводорода потеряла 2 моль ионов водорода.
C r2O7-2 + 14Н+ →
2Cr+3+
7Н2О
r2O7-2 + 14Н+ →
2Cr+3+
7Н2О
H2S → S0 + 2Н+
2.5. Полученные полуреакции необходимо уравнять по зарядам. В первом уравнении слева суммарный заряд равен (+12), а справа – (+6), значит, дихромат-ион присоединил 6 электронов и восстанавливается. Во втором уравнении слева (0), а справа – (+2). Молекула сероводорода потеряла 2 электрона и окислилась.
C r2O7-2 + 14Н+ +6
r2O7-2 + 14Н+ +6 → 2Cr+3+
7Н2О
→ 2Cr+3+
7Н2О
H2S
— 2 → S0 + 2Н+
→ S0 + 2Н+
2.6. Для соблюдения электронного баланса второе уравнение необходимо умножить на 3, после чего просуммировать уравнения.
C
 r2O7-2 + 14Н+ +6
r2O7-2 + 14Н+ +6 → 2Cr+3+
7Н2О
1
→ 2Cr+3+
7Н2О
1
+
H2S
— 2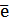 → S0 + 2Н+ 3
→ S0 + 2Н+ 3

Cr2O7-2 + 14Н+ + 3H2S = 2Cr+3+ 7Н2О + 3S0 + 6Н+
После сокращения подобных частиц в левой и правой частях уравнения получим суммарное ионно-молекулярное уравнение, которое отражает смысл произошедшей реакции.
Cr2O7-2 + 8Н+ + 3H2S = 2Cr+3+ 7Н2О + 3S0
Перенос полученных коэффициентов в молекулярную схему реакции позволяет получить ее полное уравнение:
11
K2Cr2O7 + 3H2S + 4H2SO4 = Cr2(SO4)3 + 3S+ K2SO4 + 7H2O
Иногда в реакции окислитель является одновременно и средой. Например, в реакции:
I2 + HNO3® HIO3 +NO2 +H2O
азотная кислота HNO3 одновременно содержит окислитель ион NO3— и создает кислую среду (наличие ионов Н+).
Представим молекулярное уравнение в ионно-молекулярном виде:
I2 + H+ + NO3—® IO3— +NO2 +H2O
Далее составим полуреакции окисления и восстановления с участием частиц среды (см.табл.1) и для соблюдения электронного баланса умножим первое уравнение на 10, а затем полуреакции просуммируем :
N
 O3— + 2H+ +ē®NO2 +H2O
10
O3— + 2H+ +ē®NO2 +H2O
10
 I2 + 6H2O
— 10ē ®
2IO3— + 12H+
I2 + 6H2O
— 10ē ®
2IO3— + 12H+
10NO3— + 20 H+ + I2 + 6H2O®10NO2 +10 H2O + 2 IO3— + 12H+
После сокращения подобных частиц в левой и правой частях уравнения получим суммарное ионно-молекулярное уравнение:
10NO3— + 8 H+ + I2 ®10NO2 +4 H2O + 2 IO3—
Затем полученные коэффициенты перенесем в молекулярную схему реакции. Учитывая, что ионы NO3— и H+ входят в состав одного и того же соединения, а количество их разное, перед HNO3 ставится максимальный коэффициент, так как. часть азотной кислоты расходуется на создание кислой среды. Таким образом, полное уравнение:
I2 + 10HNO3®2HIO3 +10NO2 +4H2O
Метод полуреакций позволяет определить коэффициенты перед всеми веществами, участвующими в реакции, что значительно упрощает подбор дополнительных коэффициентов.
12
Реакции конпропорционирования
ОПЫТ 10 . К содержимому пробирки ( из опыта 9) прибавить 2 мл 1М раствора серной кислоты до появления бурой окраски раствора. Пользуясь раствором крахмала, доказать, что бурая окраска вызвана процессом образования свободного иода:
NaIO3 + NaI + H2SO4 → I2 + ….
К раствору добавить несколько капель бензола (толуола). Пробирку встряхнуть и наблюдать изменение окраски бензольного кольца, обусловленного экстракцией иода (переход иода из водной фазы в органическую).
Составьте полное уравнение, используя метод ионно-электронных уравнений, укажите окислитель и восстановитель.
ОПЫТ 11 . К 1 мл раствора сульфата марганца (MnSO4) прибавить по каплям раствор перманганата калия (KMnO4). Наблюдать образование бурого осадка MnO2.
Составьте полное уравнение реакции, используя метод ионно-электронных уравнений, укажите окислитель и восстановитель.
33
Окислительно-восстановительная двойственность веществ
ОПЫТ 12. В одну пробирку налейте 3-5 капель 1 М KI и столько же 2н H2SO4, а в другую – 2-3 капли 1 М KMnO4 и 2-3 капли концентрированной H2SO4. В каждую пробирку добавьте по 3-5 капель пероксида водорода H2O2. Что наблюдаете? Схемы реакций:
H2O2 + I— → I2 + H2O;
H2O2 + MnO4— → Mn2+ + O2↑ + H2O.
Составьте полные уравнения реакций, используя ионно-электронный метод. Сделайте вывод об окислительно-восстановительных свойствах H2O2.
ОПЫТ 13. Какие окислительно-восстановительные свойства характерны для нитрита натрия NaNO2? Может ли он быть восстановителем? Если да, выберите на основании стандартных электродных потенциалов в ряду веществ подходящий окислитель: KMnO4, KI, KNO3. Налейте в пробирку 2мл раствора NaNO2, добавьте 1 мл разбавленной серной кислоты и добавьте раствор выбранного восстановителя. Опыт проводите под тягой. Объясните свои наблюдения. Составьте полные уравнения реакций, используя ионно-электронный метод.
Может ли NaNO2 быть окислителем? Если да, выберите на основании стандартных электродных потенциалов в ряду веществ подходящий восстановитель: FeCl3, KI, H2O2. В пробирку налейте 2 мл раствора выбранного восстановителя, добавьте 1 мл раствора H2SO4 и несколько кристаллов соли NaNO2. Опыт проводите под тягой. Объясните свои наблюдения. Составьте полные уравнения реакций, используя ионно-электронный метод.
Влияние рН на окислительные свойства
ОПЫТ 14. Налейте в две пробирки по 1 мл раствора бихромата калия
34
K2Cr2O7, в первую добавьте 3-5 капель разбавленной серной кислоты, а во вторую – 3-5 капель разбавленного раствора NaOH. Обратите внимание на изменение цвета во второй пробирке (бихромат переходит в хромат). Добавьте в обе пробирки по нескольку кристаллов соли КNO2. Объясните наблюдаемое. Запишите уравнения реакций, считая, что бихромат переходит в соединения хрома (III), а хромат (вторая пробирка) взаимодействует по схеме
CrO42- + NO2— → [Cr(OH)6]3- + NO3—.
Составьте полные уравнения реакций, используя ионно-электронный метод. Определите окислитель и восстановитель.
ОПЫТ 15 . Налейте в 3 пробирки по 3-4 капли водного раствора KMnO4, добавьте в одну разбавленной серной кислоты, во вторую – концентрированный раствор щелочи NaOH) (20%), в третью – немного дистиллированной воды. Затем в каждую пробирку добавьте несколько кристаллов сульфита натрия Na2SO3. Объясните свои наблюдения, если в кислой среде ионы MnO4— восстанавливаются до Mn2+, в нейтральной – до MnO2, в щелочной – до MnO42-. Выпишите значения стандартных окислительно-восстановительных потенциалов этих процессов. В какой среде окислительные свойства MnO4— выражены сильнее?
35
ВАРИАНТЫ ЗАДАНИЙ
Вариант | Задачи | Вариант | Задачи |
1 | 1, 45, 46(1), 47(1), 48(1) | 16 | 16, 40, 46(16), 47(16), 48(16) |
2 | 2, 44, 46(2), 47(2), 48(2) | 17 | 17, 32, 46(17), 47(17), 48(17) |
3 | 3, 43, 46(3), 47(3), 48(3) | 18 | 18, 39, 46(18), 47(18), 48(18) |
4 | 4, 39, 46(4),47(4) 48(4) | 19 | 19, 34, 46(19), 47(19), 48(19) |
5 | 5, 41, 46(5), 47(5), 48(5) | 20 | 20, 38, 46(20), 47(20), 48(20) |
6 | 6, 42, 46(6), 47(6), 48(6) | 21 | 21, 37, 46(21), 47(21), 48(21) |
7 | 7, 36, 46(7), 47(7), 48(7) | 22 | 22, 36, 46(22), 47(22), 48(22) |
8 | 8, 33, 46(8), 47(8), 48(8) | 23 | 23, 33, 46(23), 47(23), 48(23) |
9 | 9, 40, 46(9), 47(9), 48(9) | 24 | 24, 40, 46(24), 47(24), 48(24) |
10 | 10, 35, 46(10), 47(10), 48(10) | 25 | 25,41, 46(25), 47(25), 48(25) |
11 | 11, 36 46(11), 47(11), 48(11) | 26 | 26, 43, 46(26), 47(26), 48(26) |
12 | 12, 37, 46(12), 47(12), 48(12) | 27 | 27, 37, 46(27), 47(27), 48(27) |
13 | 13, 43, 46(13), 47(13), 48(13) | 28 | 28,35, 46(28), 47(28), 48(28) |
14 | 14, 39, 46(14), 47(14), 48(14) | 29 | 29, 45, 46(29), 47(29), 48(29) |
15 | 15, 31, 46(15), 47(15), 48(15) | 30 | 30, 44, 46(30), 47(30), 48(30) |
36
Классификация окислительно-восстановительных реакций
Основой для классификации ОВР служит местоположение окислителя и восстановителя.
1. Межатомные (а) или межмолекулярные (б) ОВР. Окислитель и восстановитель входят в состав разных веществ.
а) 2 +
+ = 2
= 2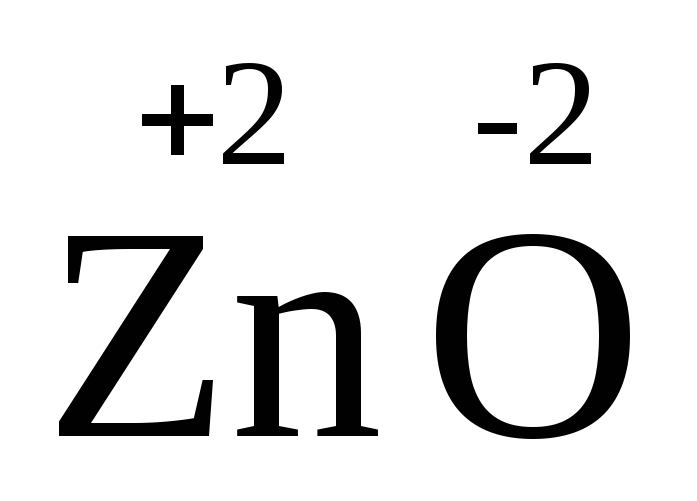
б)  + 2
+ 2 =
=  + 2
+ 2 + 2H2O
+ 2H2O
2. Внутримолекулярные ОВР. Окислитель и восстановитель входят в состав одного вещества.
2 = 2
= 2 + 3
+ 3
3. Реакции диспропорционирования (дисмутации, самоокисления-самовосстановления). Окислителем и восстановителем являются атомы одного и того же элемента, находящиеся в промежуточной степени окисления и входящие в состав одного вещества. Часть атомов повышает свою степень окисления, а другая часть ее понижает.
3 =
= + 2
+ 2 +H2O
+H2O
4. Реакции конпропорционирования – это реакции, в которых атомы одного и того же элемента имеют разные степени окисления, переходят к промежуточной степени окисления.
7
Реакции конпропорционирования могут быть:
а) внутримолекулярными (в соединении имеется элемент с разными степенями окисления):
 =
=  + 2H2O
+ 2H2O
б) межмолекулярными (в разных соединениях имеется один и тот же элемент с разными степенями окисления)
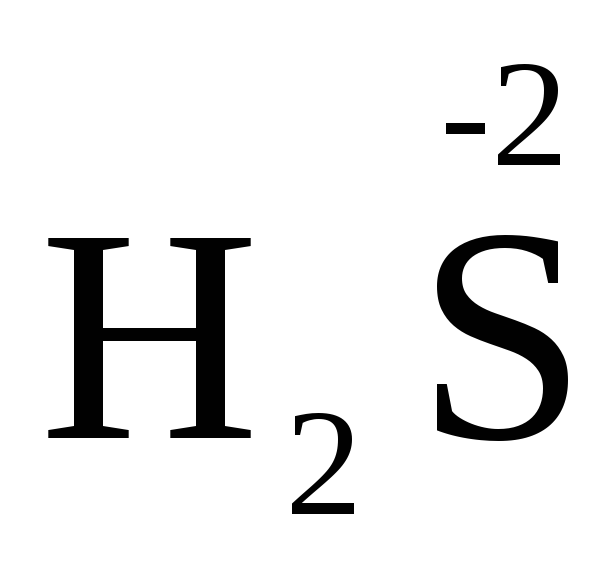 +
+ 
3 S0 + 2 H2O
3 S0 + 2 H2O
Составление уравнений окислительно-восстановительных реакций
При составлении уравнений ОВР нужно учесть, что число электронов, отданных восстановителем, равно числу электронов, принятых окислителем.
В химии условный
заряд электрона принят за «-1» и
обозначается  Для подбора стехиометрических
коэффициентов можно использовать
несколько методов, из которых наиболее
распространены два: метод электронного
баланса и метод электронно-ионных
уравнений (метод полуреакций).
Для подбора стехиометрических
коэффициентов можно использовать
несколько методов, из которых наиболее
распространены два: метод электронного
баланса и метод электронно-ионных
уравнений (метод полуреакций).
1.Метод электронного баланса является наиболее универсальным методом, и применим для любых окислительно-восстановительных процессов, протекающих в любых системах (растворы, расплавы, газы). В основе метода лежит принцип сравнения степеней окисления атомов в исходных веществах и в продуктах реакции с последующим составлением схемы электронного баланса.
В качестве примера рассмотрим реакцию взаимодействия дихромата калия с сероводородом в кислой среде:
 +
+  +
+ →
→ +
+ +
+  +
+
Для расстановки коэффициентов выполняем следующие действия.
1.1. Определяем элементы, атомы которых изменяют степень окисления:
8
 +
+  +→
+→ +
+ +
+  +
+
1.2. Находим
окислитель и восстановитель в данной
ОВР, составляем схему перехода электронов
от восстановителя к окислителю и пишем
отдельно электронные уравнения процессов
окисления и восстановления, с учетом
того, что количество атомов, входящих
в соединение, должно сохраняться.
Например, в  имеется два атомаCr,
следовательно, в схеме они должны
присутствовать:
имеется два атомаCr,
следовательно, в схеме они должны
присутствовать:
+5ē


 -2ē
-2ē
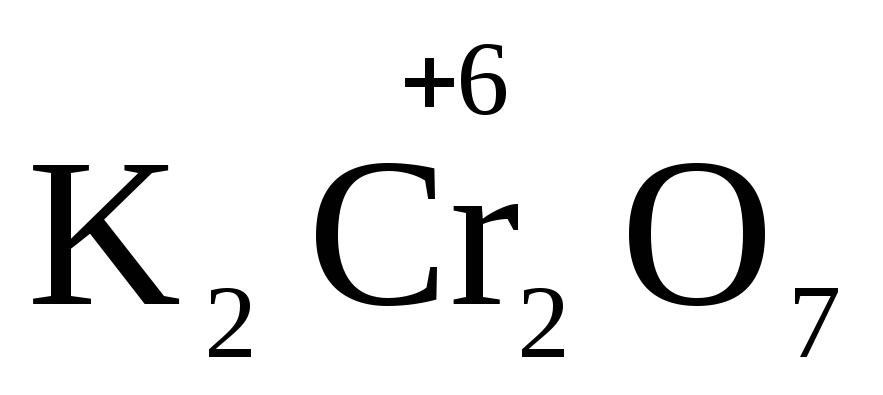


 +
+ 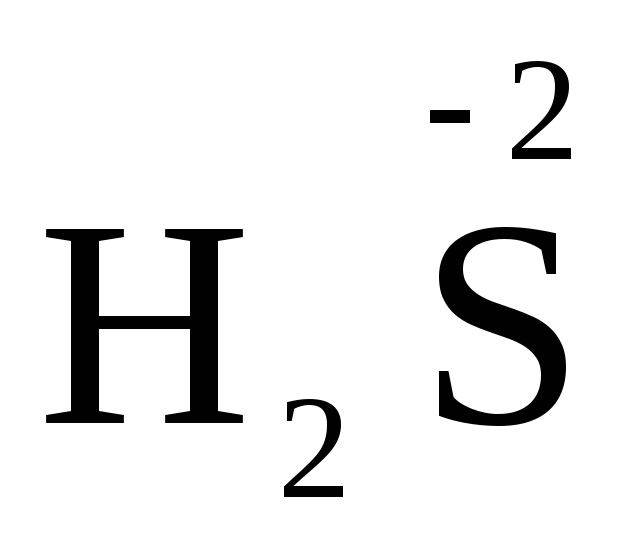 +
+ →
→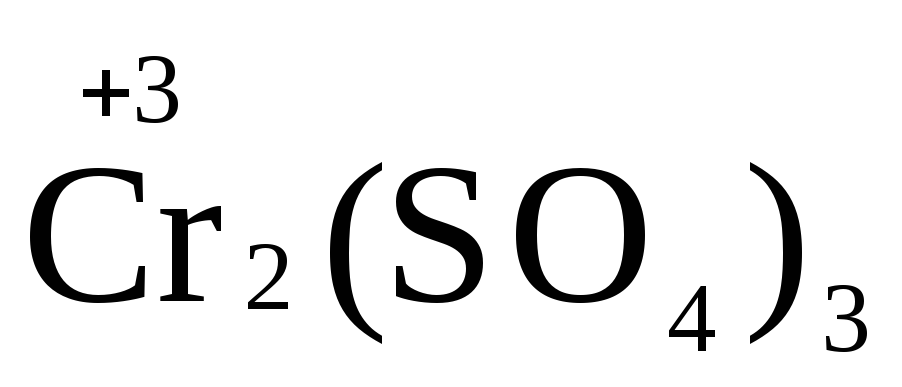 +
+ +
+  +
+
окислитель восстановитель
2Cr+6 + 6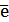 = 2Cr+3 (а) —
восстановление
= 2Cr+3 (а) —
восстановление
S-2 — 2 =
S0 (б) — окисление
=
S0 (б) — окисление
1.3. Уравниваем число электронов в процессе окисления и восстановления (электронный баланс). В приведенной схеме необходимо уравнение (б) умножить на 3, тогда будет принято и отдано по 6 электронов. После умножения уравнения складываются как обычные алгебраические, а электроны сокращаются.
2
 Cr+6 + 6
Cr+6 + 6 = 2Cr+3 1
= 2Cr+3 1
+
S-2 — 2 =
S0 3
=
S0 3

2Cr+6 +3S-2 = 2Cr+3 + 3 S0
1.4. Полученные коэффициенты называют основными. Они переносятся в молекулярную схему реакции и ставятся перед соответствующими веществами. Так как в молекулах дихромата калия и сульфата хрома содержится по два атома хрома, двойки перед этими веществами опускаются.
K2Cr2O7 + 3H2S + H2SO4 = Cr2(SO4)3 + 3S+ K2SO4 + H2O
1.5. Окончательно уравниваем число атомов каждого элемента в обеих частях молекулярного уравнения. Продукты реакции (Cr2(SO4)3, K2SO4),
9
имеющие коэффициенты по единице, содержат 4 моль сульфат-ионов (SO42-), которые содержатся в серной кислоте, следовательно, перед ней ставится коэффициент 4. Чтобы количество атомов водорода было одинаково в левой и правой части уравнения, перед водой ставится коэффициент 7:
K2Cr2O7 + 3H2S + 4H2SO4 = Cr2(SO4)3 + 3S+ K2SO4 + 7H2O
Проверка количества остальных атомов показывает, что все коэффициенты подобраны.
2. Метод электронно-ионных уравнений (метод полуреакций) применяется для подбора коэффициентов в уравнениях реакций, протекающих в растворах. Метод оперирует с реально существующими в растворах частицами и позволяет учитывать влияние среды раствора (т.е. рН) на процессы окисления и восстановления частиц. В качестве частиц среды в водных растворах могут принимать участие следующие частицы.
Таблица 1
Кислотность (рН) | Исходные частицы | Продукты |
Кислая среда (рН<7) | Н+и Н2О | Н2О и ОН— |
Нейтральная среда (рН = 7) | Н2О | Н+и ОН— |
Щелочная среда (рН>7) | Н2О и ОН— | Н2О и ОН— |
В качестве примера рассмотрим ту же реакцию.
2.1. Молекулярная схема реакции:
K2Cr2O7 + H2S + H2SO4 → Cr2(SO4)3 + S+ K2SO4 + H2O
2.2. Записываем это уравнение в ионно-молекулярной форме. Для этого необходимо все сильные электролиты представить в виде ионов, а слабые электролиты, газы и малорастворимые вещества оставляем в виде молекул. К сильным электролитам относятся все хорошо растворимые соли, часть кислот (HCl, HNO3, H2SO4 и др.), щелочи (LiOH, NaOH, KOH и др.). Степень окисления атомов не используют, а учитывают заряды реальных ионов и характер среды, в которой идет окислительно-восстановительный процесс.
10
2K+ + Cr2O7-2 + H2S + 2H++ SO4-2 = 2Cr+3+3SO4-2 + S0 + 2K+ +SO4-2 + H2O
кислая среда
2.3. Определяем частицы, изменившие свой заряд или состав:
Cr2O7-2→ 2Cr+3и H2S → S0
2.4. На основании этих превращений составляем полуреакции окисления и восстановления с участием частиц среды (см. табл.1). Анион дихромата потерял 7 моль атомов кислорода, которые в кислой среде связываются 14 моль ионами водорода и превращаются в воду. Молекула сероводорода потеряла 2 моль ионов водорода.
C r2O7-2 + 14Н+ →
2Cr+3+
7Н2О
r2O7-2 + 14Н+ →
2Cr+3+
7Н2О
H2S → S0 + 2Н+
2.5. Полученные полуреакции необходимо уравнять по зарядам. В первом уравнении слева суммарный заряд равен (+12), а справа – (+6), значит, дихромат-ион присоединил 6 электронов и восстанавливается. Во втором уравнении слева (0), а справа – (+2). Молекула сероводорода потеряла 2 электрона и окислилась.
C r2O7-2 + 14Н+ +6
r2O7-2 + 14Н+ +6 → 2Cr+3+
7Н2О
→ 2Cr+3+
7Н2О
H2S
— 2 → S0 + 2Н+
→ S0 + 2Н+
2.6. Для соблюдения электронного баланса второе уравнение необходимо умножить на 3, после чего просуммировать уравнения.
C r2O7-2 + 14Н+ +6
r2O7-2 + 14Н+ +6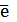 → 2Cr+3+
7Н2О
1
→ 2Cr+3+
7Н2О
1
+
H2S
— 2 → S0 + 2Н+ 3
→ S0 + 2Н+ 3

Cr2O7-2 + 14Н+ + 3H2S = 2Cr+3+ 7Н2О + 3S0 + 6Н+
После сокращения подобных частиц в левой и правой частях уравнения получим суммарное ионно-молекулярное уравнение, которое отражает смысл произошедшей реакции.
Cr2O7-2 + 8Н+ + 3H2S = 2Cr+3+ 7Н2О + 3S0
Перенос полученных коэффициентов в молекулярную схему реакции позволяет получить ее полное уравнение:
11
K2Cr2O7 + 3H2S + 4H2SO4 = Cr2(SO4)3 + 3S+ K2SO4 + 7H2O
Иногда в реакции окислитель является одновременно и средой. Например, в реакции:
I2 + HNO3® HIO3 +NO2 +H2O
азотная кислота HNO3 одновременно содержит окислитель ион NO3— и создает кислую среду (наличие ионов Н+).
Представим молекулярное уравнение в ионно-молекулярном виде:
I2 + H+ + NO3—® IO3— +NO2 +H2O
Далее составим полуреакции окисления и восстановления с участием частиц среды (см.табл.1) и для соблюдения электронного баланса умножим первое уравнение на 10, а затем полуреакции просуммируем :
N
 O3— + 2H+ +ē®NO2 +H2O
10
O3— + 2H+ +ē®NO2 +H2O
10
 I2 + 6H2O
— 10ē ®
2IO3— + 12H+
I2 + 6H2O
— 10ē ®
2IO3— + 12H+
10NO3— + 20 H+ + I2 + 6H2O®10NO2 +10 H2O + 2 IO3— + 12H+
После сокращения подобных частиц в левой и правой частях уравнения получим суммарное ионно-молекулярное уравнение:
10NO3— + 8 H+ + I2 ®10NO2 +4 H2O + 2 IO3—
Затем полученные коэффициенты перенесем в молекулярную схему реакции. Учитывая, что ионы NO3— и H+ входят в состав одного и того же соединения, а количество их разное, перед HNO3 ставится максимальный коэффициент, так как. часть азотной кислоты расходуется на создание кислой среды. Таким образом, полное уравнение:
I2 + 10HNO3®2HIO3 +10NO2 +4H2O
Метод полуреакций позволяет определить коэффициенты перед всеми веществами, участвующими в реакции, что значительно упрощает подбор дополнительных коэффициентов.
12
Реакции конпропорционирования
ОПЫТ 10 . К содержимому пробирки ( из опыта 9) прибавить 2 мл 1М раствора серной кислоты до появления бурой окраски раствора. Пользуясь раствором крахмала, доказать, что бурая окраска вызвана процессом образования свободного иода:
NaIO3 + NaI + H2SO4 → I2 + ….
К раствору добавить несколько капель бензола (толуола). Пробирку встряхнуть и наблюдать изменение окраски бензольного кольца, обусловленного экстракцией иода (переход иода из водной фазы в органическую).
Составьте полное уравнение, используя метод ионно-электронных уравнений, укажите окислитель и восстановитель.
ОПЫТ 11 . К 1 мл раствора сульфата марганца (MnSO4) прибавить по каплям раствор перманганата калия (KMnO4). Наблюдать образование бурого осадка MnO2.
Составьте полное уравнение реакции, используя метод ионно-электронных уравнений, укажите окислитель и восстановитель.
33
Окислительно-восстановительная двойственность веществ
ОПЫТ 12. В одну пробирку налейте 3-5 капель 1 М KI и столько же 2н H2SO4, а в другую – 2-3 капли 1 М KMnO4 и 2-3 капли концентрированной H2SO4. В каждую пробирку добавьте по 3-5 капель пероксида водорода H2O2. Что наблюдаете? Схемы реакций:
H2O2 + I— → I2 + H2O;
H2O2 + MnO4— → Mn2+ + O2↑ + H2O.
Составьте полные уравнения реакций, используя ионно-электронный метод. Сделайте вывод об окислительно-восстановительных свойствах H2O2.
ОПЫТ 13. Какие окислительно-восстановительные свойства характерны для нитрита натрия NaNO2? Может ли он быть восстановителем? Если да, выберите на основании стандартных электродных потенциалов в ряду веществ подходящий окислитель: KMnO4, KI, KNO3. Налейте в пробирку 2мл раствора NaNO2, добавьте 1 мл разбавленной серной кислоты и добавьте раствор выбранного восстановителя. Опыт проводите под тягой. Объясните свои наблюдения. Составьте полные уравнения реакций, используя ионно-электронный метод.
Может ли NaNO2 быть окислителем? Если да, выберите на основании стандартных электродных потенциалов в ряду веществ подходящий восстановитель: FeCl3, KI, H2O2. В пробирку налейте 2 мл раствора выбранного восстановителя, добавьте 1 мл раствора H2SO4 и несколько кристаллов соли NaNO2. Опыт проводите под тягой. Объясните свои наблюдения. Составьте полные уравнения реакций, используя ионно-электронный метод.
Влияние рН на окислительные свойства
ОПЫТ 14. Налейте в две пробирки по 1 мл раствора бихромата калия
34
K2Cr2O7, в первую добавьте 3-5 капель разбавленной серной кислоты, а во вторую – 3-5 капель разбавленного раствора NaOH. Обратите внимание на изменение цвета во второй пробирке (бихромат переходит в хромат). Добавьте в обе пробирки по нескольку кристаллов соли КNO2. Объясните наблюдаемое. Запишите уравнения реакций, считая, что бихромат переходит в соединения хрома (III), а хромат (вторая пробирка) взаимодействует по схеме
CrO42- + NO2— → [Cr(OH)6]3- + NO3—.
Составьте полные уравнения реакций, используя ионно-электронный метод. Определите окислитель и восстановитель.
ОПЫТ 15 . Налейте в 3 пробирки по 3-4 капли водного раствора KMnO4, добавьте в одну разбавленной серной кислоты, во вторую – концентрированный раствор щелочи NaOH) (20%), в третью – немного дистиллированной воды. Затем в каждую пробирку добавьте несколько кристаллов сульфита натрия Na2SO3. Объясните свои наблюдения, если в кислой среде ионы MnO4— восстанавливаются до Mn2+, в нейтральной – до MnO2, в щелочной – до MnO42-. Выпишите значения стандартных окислительно-восстановительных потенциалов этих процессов. В какой среде окислительные свойства MnO4— выражены сильнее?
35
ВАРИАНТЫ ЗАДАНИЙ
Вариант | Задачи | Вариант | Задачи |
1 | 1, 45, 46(1), 47(1), 48(1) | 16 | 16, 40, 46(16), 47(16), 48(16) |
2 | 2, 44, 46(2), 47(2), 48(2) | 17 | 17, 32, 46(17), 47(17), 48(17) |
3 | 3, 43, 46(3), 47(3), 48(3) | 18 | 18, 39, 46(18), 47(18), 48(18) |
4 | 4, 39, 46(4),47(4) 48(4) | 19 | 19, 34, 46(19), 47(19), 48(19) |
5 | 5, 41, 46(5), 47(5), 48(5) | 20 | 20, 38, 46(20), 47(20), 48(20) |
6 | 6, 42, 46(6), 47(6), 48(6) | 21 | 21, 37, 46(21), 47(21), 48(21) |
7 | 7, 36, 46(7), 47(7), 48(7) | 22 | 22, 36, 46(22), 47(22), 48(22) |
8 | 8, 33, 46(8), 47(8), 48(8) | 23 | 23, 33, 46(23), 47(23), 48(23) |
9 | 9, 40, 46(9), 47(9), 48(9) | 24 | 24, 40, 46(24), 47(24), 48(24) |
10 | 10, 35, 46(10), 47(10), 48(10) | 25 | 25,41, 46(25), 47(25), 48(25) |
11 | 11, 36 46(11), 47(11), 48(11) | 26 | 26, 43, 46(26), 47(26), 48(26) |
12 | 12, 37, 46(12), 47(12), 48(12) | 27 | 27, 37, 46(27), 47(27), 48(27) |
13 | 13, 43, 46(13), 47(13), 48(13) | 28 | 28,35, 46(28), 47(28), 48(28) |
14 | 14, 39, 46(14), 47(14), 48(14) | 29 | 29, 45, 46(29), 47(29), 48(29) |
15 | 15, 31, 46(15), 47(15), 48(15) | 30 | 30, 44, 46(30), 47(30), 48(30) |
36
Диспропорционирование — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 28 октября 2016; проверки требует 1 правка. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 28 октября 2016; проверки требует 1 правка.Диспропорциони́рование (дисмутация) — химическая реакция, в которой один и тот же элемент выступает и в качестве окислителя, и в качестве восстановителя, причём в результате реакции образуются соединения, которые содержат один и тот же элемент в разных степенях окисления.
Примером может служить реакция взаимодействия оксида азота(IV) с водой:
2N+4O2+h3O ⇆ HN+5O3+HN+3O2{\displaystyle 2{\stackrel {+4}{\mbox{N}}}{\mbox{O}}_{2}+{\mbox{H}}{_{2}}{\mbox{O}}~\leftrightarrows ~{\mbox{H}}{\stackrel {+5}{\mbox{N}}}{\mbox{O}}_{3}+{\mbox{H}}{\stackrel {+3}{\mbox{N}}}{\mbox{O}}_{2}}или реакция разложения хлората калия :
4KCl+5O3 →t∘ KCl−1+3KCl+7O4{\displaystyle 4{\mbox{K}}{\stackrel {+5}{\mbox{Cl}}}{\mbox{O}}_{3}~{\stackrel {t^{\circ }}{\rightarrow }}~{\mbox{K}}{\stackrel {-1}{\mbox{Cl}}}+3{\mbox{K}}{\stackrel {+7}{\mbox{Cl}}}{\mbox{O}}_{4}}Некоторые реакции диспропорционирования идут только при определенном рН среды. Например, иод, также как и сера, диспропорционирует только в щелочной среде:
3I02+6OH− → 5I−1−+I+5O3−+3h3O{\displaystyle 3{\stackrel {0}{\mbox{I}}}_{2}+6{\mbox{OH}}^{{}-{}}~\rightarrow ~{5}{\stackrel {-1}{\mbox{I}}}{}^{{}-{}}+{}{\stackrel {+5}{\mbox{I}}}{\mbox{O}}_{3}^{{}-{}}+{3}{{\mbox{H}}_{2}}{\mbox{O}}}Реакция диспропорционирования обратна реакции конпропорционирования. Чтобы понять, при каких условиях возможна реакция диспропорционирования, можно использовать диаграмму Фроста, диаграмму Пурбе или таблицу окислительно-восстановительных потенциалов.
- ДИСПРОПОРЦИОНИРОВАНИЕ / Химическая Энциклопедия
- [1]
Реакции конпропорционирования
ОПЫТ 10 . К содержимому пробирки ( из опыта 9) прибавить 2 мл 1М раствора серной кислоты до появления бурой окраски раствора. Пользуясь раствором крахмала, доказать, что бурая окраска вызвана процессом образования свободного иода:
NaIO3 + NaI + H2SO4 → I2 + ….
К раствору добавить несколько капель бензола (толуола). Пробирку встряхнуть и наблюдать изменение окраски бензольного кольца, обусловленного экстракцией иода (переход иода из водной фазы в органическую).
Составьте полное уравнение, используя метод ионно-электронных уравнений, укажите окислитель и восстановитель.
ОПЫТ 11 . К 1 мл раствора сульфата марганца (MnSO4) прибавить по каплям раствор перманганата калия (KMnO4). Наблюдать образование бурого осадка MnO2.
Составьте полное уравнение реакции, используя метод ионно-электронных уравнений, укажите окислитель и восстановитель.
33
Окислительно-восстановительная двойственность веществ
ОПЫТ 12. В одну пробирку налейте 3-5 капель 1 М KI и столько же 2н H2SO4, а в другую – 2-3 капли 1 М KMnO4 и 2-3 капли концентрированной H2SO4. В каждую пробирку добавьте по 3-5 капель пероксида водорода H2O2. Что наблюдаете? Схемы реакций:
H2O2 + I— → I2 + H2O;
H2O2 + MnO4— → Mn2+ + O2↑ + H2O.
Составьте полные уравнения реакций, используя ионно-электронный метод. Сделайте вывод об окислительно-восстановительных свойствах H2O2.
ОПЫТ 13. Какие окислительно-восстановительные свойства характерны для нитрита натрия NaNO2? Может ли он быть восстановителем? Если да, выберите на основании стандартных электродных потенциалов в ряду веществ подходящий окислитель: KMnO4, KI, KNO3. Налейте в пробирку 2мл раствора NaNO2, добавьте 1 мл разбавленной серной кислоты и добавьте раствор выбранного восстановителя. Опыт проводите под тягой. Объясните свои наблюдения. Составьте полные уравнения реакций, используя ионно-электронный метод.
Может ли NaNO2 быть окислителем? Если да, выберите на основании стандартных электродных потенциалов в ряду веществ подходящий восстановитель: FeCl3, KI, H2O2. В пробирку налейте 2 мл раствора выбранного восстановителя, добавьте 1 мл раствора H2SO4 и несколько кристаллов соли NaNO2. Опыт проводите под тягой. Объясните свои наблюдения. Составьте полные уравнения реакций, используя ионно-электронный метод.
Влияние рН на окислительные свойства
ОПЫТ 14. Налейте в две пробирки по 1 мл раствора бихромата калия
34
K2Cr2O7, в первую добавьте 3-5 капель разбавленной серной кислоты, а во вторую – 3-5 капель разбавленного раствора NaOH. Обратите внимание на изменение цвета во второй пробирке (бихромат переходит в хромат). Добавьте в обе пробирки по нескольку кристаллов соли КNO2. Объясните наблюдаемое. Запишите уравнения реакций, считая, что бихромат переходит в соединения хрома (III), а хромат (вторая пробирка) взаимодействует по схеме
CrO42- + NO2— → [Cr(OH)6]3- + NO3—.
Составьте полные уравнения реакций, используя ионно-электронный метод. Определите окислитель и восстановитель.
ОПЫТ 15 . Налейте в 3 пробирки по 3-4 капли водного раствора KMnO4, добавьте в одну разбавленной серной кислоты, во вторую – концентрированный раствор щелочи NaOH) (20%), в третью – немного дистиллированной воды. Затем в каждую пробирку добавьте несколько кристаллов сульфита натрия Na2SO3. Объясните свои наблюдения, если в кислой среде ионы MnO4— восстанавливаются до Mn2+, в нейтральной – до MnO2, в щелочной – до MnO42-. Выпишите значения стандартных окислительно-восстановительных потенциалов этих процессов. В какой среде окислительные свойства MnO4— выражены сильнее?
35
ВАРИАНТЫ ЗАДАНИЙ
Вариант | Задачи | Вариант | Задачи |
1 | 1, 45, 46(1), 47(1), 48(1) | 16 | 16, 40, 46(16), 47(16), 48(16) |
2 | 2, 44, 46(2), 47(2), 48(2) | 17 | 17, 32, 46(17), 47(17), 48(17) |
3 | 3, 43, 46(3), 47(3), 48(3) | 18 | 18, 39, 46(18), 47(18), 48(18) |
4 | 4, 39, 46(4),47(4) 48(4) | 19 | 19, 34, 46(19), 47(19), 48(19) |
5 | 5, 41, 46(5), 47(5), 48(5) | 20 | 20, 38, 46(20), 47(20), 48(20) |
6 | 6, 42, 46(6), 47(6), 48(6) | 21 | 21, 37, 46(21), 47(21), 48(21) |
7 | 7, 36, 46(7), 47(7), 48(7) | 22 | 22, 36, 46(22), 47(22), 48(22) |
8 | 8, 33, 46(8), 47(8), 48(8) | 23 | 23, 33, 46(23), 47(23), 48(23) |
9 | 9, 40, 46(9), 47(9), 48(9) | 24 | 24, 40, 46(24), 47(24), 48(24) |
10 | 10, 35, 46(10), 47(10), 48(10) | 25 | 25,41, 46(25), 47(25), 48(25) |
11 | 11, 36 46(11), 47(11), 48(11) | 26 | 26, 43, 46(26), 47(26), 48(26) |
12 | 12, 37, 46(12), 47(12), 48(12) | 27 | 27, 37, 46(27), 47(27), 48(27) |
13 | 13, 43, 46(13), 47(13), 48(13) | 28 | 28,35, 46(28), 47(28), 48(28) |
14 | 14, 39, 46(14), 47(14), 48(14) | 29 | 29, 45, 46(29), 47(29), 48(29) |
15 | 15, 31, 46(15), 47(15), 48(15) | 30 | 30, 44, 46(30), 47(30), 48(30) |
36