28. Опыт Резерфорда. Планетарная модель атома.
Масса электронов в несколько тысяч раз меньше массы атомов. Так как атом в целом нейтрален, то, следовательно, основная масса атома приходится на его положительно заряженную часть.
Для экспериментального исследования распределения положительного заряда, а значит, и массы внутри атома Резерфорд предложил в 1906 г. применить зондирование атома с помощьюα-частиц. Эти частицы возникают при распаде радия и некоторых других элементов. Их масса примерно в 8000 раз больше массы электрона, а положительный заряд равен по модулю удвоенному заряду электрона. Это не что иное, как полностью ионизированные атомы гелия. Скорость α-частиц очень велика: она составляет 1/15 скорости света.
Этими частицами Резерфорд бомбардировал атомы тяжелых элементов. Электроны вследствие своей малой массы не могут заметно изменить траекторию α-частицы, подобно тому как камушек в несколько десятков граммов при столкновении с автомобилем не в состоянии заметно изменить его скорость. Рассеяние (изменение направления движения)
Радиоактивный препарат, например радий, помещался внутри свинцового цилиндра 1, вдоль которого был высверлен узкий канал. Пучок α-частиц из канала падал на тонкую фольгу 2 из исследуемого материала (золото, медь и пр.). После рассеяния α-частицы попадали на полупрозрачный экран 3, покрытый сульфидом цинка. Столкновение каждой частицы с экраном сопровождалось вспышкой света (сцинтилляцией), которую можно было наблюдать в микроскоп 4. Весь прибор размещался в сосуде, из которого был откачан воздух.
При хорошем вакууме внутри прибора в отсутствие фольги на экране возникал светлый кружок, состоящий из сцинтилляций, вызванных тонким пучком α-частиц. Но когда на пути пучка помещали фольгу, α-частицы из-за рассеяния распределялись на экране по кружку большей площади. Модифицируя экспериментальную установку, Резерфорд попытался обнаружить отклонение α-частиц на большие углы. Совершенно неожиданно оказалось, что небольшое число α-частиц (примерно одна из двух тысяч) отклонилось на углы, большие 90°. Позднее Резерфорд признался, что, предложив своим ученикам эксперимент по наблюдению рассеяния α-частиц на большие углы, он сам не верил в положительный результат. «Это почти столь же невероятно, — говорил Резерфорд, — как если бы вы выстрелили 15-дюймовым снарядом в кусок тонкой бумаги, а снаряд возвратился бы к вам и нанес вам удар». В самом деле, предвидеть этот результат на основе модели Томсона было нельзя. При распределении по всему атому положительный заряд не может создать достаточно интенсивное электрическое поле, способное отбросить а-частицу назад. Максимальная сила отталкивания определяется по закону Кулона:
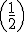

где qα — заряд α-частицы; q — положительный заряд атома; r — его радиус; k — коэффициент пропорциональности. Напряженность электрического поля равномерно заряженного шара максимальна на поверхности шара и убывает до нуля по мере приближения к центру. Поэтому, чем меньше радиус r, тем больше сила, отталкивающаяα-частицы.
 ,
(1)
,
(1)
Определение размеров атомного ядра. Резерфорд понял, что α-частица могла быть отброшена назад лишь в том случае, если положительный заряд атома и его масса сконцентрированы в очень малой области пространства. Так Резерфорд пришел к идее атомного ядра — тела малых размеров, в котором сконцентрированы почти вся масса и весь положительный заряд атома.
Планетарная модель атома, или модель Резерфорда, — историческая модель строения атома, которую предложил Эрнест Резерфорд в результате эксперимента с рассеянием альфа-частиц. По этой модели атом состоит из небольшого положительно заряженного ядра, в котором сосредоточена почти вся масса атома, вокруг которого движутся электроны, — подобно тому, как планеты движутся вокруг Солнца. Планетарная модель атома соответствует современным представлениям о строении атома с учётом того, что движение электронов имеет квантовый характер и не описывается законами классической механики. Исторически планетарная модель Резерфорда пришла на смену «модели сливового пудинга»Джозефа Джона Томсона, которая постулирует, что отрицательно заряженные электроны помещены внутрь положительно заряженного атома.
Планетарная модель атома Резерфорда
«Каждый, кто надеется, что преобразования атомных ядер станут источником энергии, исповедует вздор.»
Эрнест Резерфорд
Модель Томсона была первым пробным шагом в познании микромира. Однако она не отвечала на многие вопросы. Требовался новый нестандартный взгляд для создания модели, способной разрешить возникшие противоречия.
Модель атома, предложенная Томсоном, давала только общее представление о строении атома и не согласовывалась со все новыми данными экспериментов и теоретических вычислений. Настало время создания другой модели, способной согласовать теорию и эксперимент.
Этого не может быть… Или факты — упрямая вещь
К 1904 году японский физик Хантаро Нагаока разработал раннюю «планетарную модель» атома — так называемый «атом типа Сатурна». Модель была разработана по аналогии с расчетами устойчивости колец Сатурна. И хотя впоследствии модель и оказалась ошибочной, два следствия из нее все-таки оказались пророческими:
- ядро атома действительно очень массивно;
- электроны удерживаются на орбите электростатическими силами.
Годом раньше немецкий физик Филипп фон Ленард попытался создать модель, которая не предполагала раздельное существование в атоме противоположных зарядов. Атом, согласно модели Ленарда, состоит из нейтральных частиц — динамид, каждая из которых является электрическим дуплетом. Расчеты, выполненные Ленардом, показали, что эти частицы должны иметь очень маленькие размеры, то есть большая часть объема атома представляет собой пустоту.

Эрнест Резерфорд (1871-1937) — британский физик новозеландского происхождения. Известен как отец ядерной физики. Лауреат Нобелевской премии по химии 1908 года
В 1909 году Ганс Гейгер и Эрнест Марсден под руководством Эрнеста Резерфорда решили попытаться найти экспериментальное подтверждение модели Томсона и провели ставшие классическими опыты по рассеиванию альфа-частиц на тонкой золотой фольге. Альфа-частицы были выбраны благодаря своей большей массе (в 7350 раз больше массы электрона), поэтому они не должны претерпевать сколь-нибудь заметного отклонения при взаимодействии с электронами. Это позволяет исследовать только положительную составляющую атома. Источником альфа-частиц послужил радий. Частицы, проходящие через золотую фольгу, рассеивались, и это рассеяние регистрировалось по сцинтилляционным вспышкам на экране из сульфида цинка.
В начале эксперимента исследовались только малые углы отклонения альфа-частицы. И тут выяснилось, что подавляющее большинство частиц проходили сквозь фольгу, как раскаленная дробинка через кусок масла, словно мишень была прозрачна для бомбардирующих ее частиц. Наблюдалось лишь весьма незначительное отклонение порядка одного градуса.
Затем Резерфорд поручил молодому сотруднику Марсдену выяснить, могут ли частицы рассеиваться на большие углы. В частности, до 180°. И вот зимним днем 1909 года Марсден остановил на университетской лестнице Резерфорда и сказал: «Вы были правы, профессор: они возвращаются». Это было невероятно и противоречило существующей модели атома. Таким образом, вместо доказательства правоты Томсона эксперименты Резерфорда доказали ее несостоятельность.
Тот факт, что альфа-частицы возвращались, говорил о том, что они столкнулись с преградой — очень массивной положительно заряженной частицей, но эти столкновения происходили очень редко, в среднем — одно на восемь тысяч. А это уже свидетельство о том, что… Впрочем, именно над этим и задумался Резерфорд.
Альфа-частица (а-частица)— положительно заряженная частица, образованная двумя протонами и двумя нейтронами, по сути это ядро атома гелия. Поток альфа-частиц называют альфа-лучами, или альфа-излучением.
И все-таки он вертится!
И задумался он на целых два года. К 1911 году результатом его раздумий явилась новая модель строения атома. Однако обо всем по порядку.
Альфа-частицы, проходя через фольгу, проходят сквозь атомы золота в большинстве случаев без отклонений.
Из этого следуют два вывода. Первый: легкие электроны практически не влияют на движение тяжелой альфа-частицы. Вывод второй: так как альфа-частицы в большинстве случаев отклоняются на малые углы, атом в большей части своего объема пустой.
Небольшая часть альфа-частиц все же отклоняется на значительные углы. А значит, вывод третий такой: центральная часть атома очень маленьких размеров, но в ней сосредоточена почти вся масса атома, и эта центральная часть имеет положительный заряд. Она и получила название ядра атома.

Планетарная модель атома Резерфорда: вокруг ядра вращаются электроны
Согласно Резерфорду, атом состоит из массивного положительного ядра и вращающихся по определенным орбитам вокруг него электронов, что само по себе напомнило Солнечную систему, поэтому модель и получила название планетарной.
Если представить атом в виде сферы диаметром один километр — его ядро будет размером с мелкую монету.
По соотношению между общим числом альфа-частиц и количеством отклонившихся на определенные углы можно рассчитать размер ядра и его заряд. Оказалось, что радиус ядра имеет порядок 10-14 м. Заряд же ядра, как было сказано выше, положителен и определяется формулой q=Z *e, где Z — порядковый номер элемента в периодической системе элементов Менделеева, а е — модуль заряда электрона. Но эту связь установил Генри Мозли в экспериментах, выполненных в 1913 году.
Однако и эта модель атома оказалась в противоречии с классической физикой. Согласно теории Максвелла, любой ускоренно движущийся заряд должен непрерывно излучать электромагнитные волны. Поскольку электроны, вращаясь вокруг ядра, движутся с центростремительным ускорением, они должны непрерывно излучать электромагнитные волны. На самом же деле в нормальном состоянии атомы не излучают!
Благодаря излучению электромагнитных волн энергия электронов должна непрерывно уменьшаться, и они должны приближаться к ядру и, в конце концов, непременно «упасть» на него. Согласно расчетам, время «падения» должно составить 10-8 с. Однако опыты показывают, что атомы существуют довольно продолжительное время.
Таким образом, эти факты были несовместимы с планетарной моделью атома Резерфорда, если рассматривать ее с позиции классической электродинамики.
Разрешения этих противоречий были еще впереди. Пока же количество вопросов значительно превышало число удобоваримых объяснений. Тем не менее, это был значительный шаг на пути понимания устройства мира. Добавим лишь, что рассеяние микрочастиц на других частицах или атомных ядрах — это квантовый процесс, а для его описания необходимо уравнение Шредингера, которого в 1911 году еще попросту не было.
Поделиться ссылкой
sitekid.ru
Модель строения атома э. Резерфорда
В начале XXв. опытами по облучению тонкой фольги α-частицами Э. Резерфорд определил структуру атома. Он показал, что атом имеет планетарную модель (рис. 3), то есть состоит из плотного положительно заряженного ядра, вокруг которого обращается рыхлая электронная оболочка.
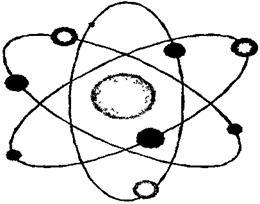
Рис. 3.Планетарная модель строения атома Э. Резерфорда
В целом атом является электронейтральной элементарной структурой химического элемента. Физический смысл порядкового номера Z-элемента в периодической системе элементов был установлен в планетарной модели атома Резерфорда. Z совпадает с числом положительных элементарных зарядов в ядре, закономерно возрастающих на единицу при переходе от предыдущего элемента к последующему. Химические свойства элементов и ряд их физических свойств объясняются поведением внешних, так называемых валентных электронов их атомов.
Поэтому периодичность свойств химических элементов должна быть связана с определенной периодичностью в расположении электронов в атомах различных элементов. Теория периодической системы основывается на следующих положениях:
а) порядковый номер химического элемента равен общему числу электронов в атоме данного элемента;
б) состояние электронов в атоме определяется набором их квантовых чисел п, l, m и ms. Распределение электронов в атоме по энергетическим состояниям должно удовлетворять принципу минимума потенциальной энергии: с возрастанием числа электронов каждый следующий электрон должен занять возможное энергетическое состояние с наименьшей энергией;
в) заполнение электронами энергетических состояний в атоме должно происходить в соответствии с принципом Паули.
(Подробнее об этом можно прочитать в теме 2.6.)
Электроны в атоме, занимающие совокупность состояний с одинаковым значением главного квантового числа п, образуют электронную оболочку, или электронный слой. В зависимости от значенийnразличают следующие оболочки:К прип = 1,Lприп = 2,Мприn= 3,N прип = 4,Оприп = 5 и т. д. Максимальное число электронов, которые могут находиться в оболочках согласно принципу Паули: вК-оболочке – 2 электрона, в оболочкахL,М,N иОсоответственно 8, 18, 32 и 50 электронов. В каждой из оболочек электроны распределяются по подгруппам или подоболочкам, каждая из которых соответствует определенному значению орбитального квантового числа. В атомной физике принято обозначать электронное состояние в атоме символомпl, указывающим значение двух квантовых чисел. Электроны, находящиеся в состояниях, характеризуемых одинаковыми квантовыми числамиnиl, называются эквивалентными. ЧислоZ-эквивалентных электронов указывается показателем степени в символеnlz. Если электроны находятся в некоторых состояниях с определенными значениями квантовых чиселп иl, то считается заданной так называемая электронная конфигурация. Например, основное состояние атома кислорода можно выразить следующей символической формулой: 1s2, 2s2, 2p4. Она показывает, что два электрона находятся в состояниях сn= 1 иl= 0, два электрона имеют квантовые числаn= 2 иl= 0 и четыре электрона занимают состоянияc n = 2 иl= 1.
Порядок заполнения электронных состояний в оболочках атомов, а в пределах одной оболочки – в подгруппах (подоболочках) должен соответствовать последовательности расположения энергетических уровней с данными п иl. Сначала заполняются состояния с наименьшей возможной энергией, а затем состояния со все более высокой энергией. Для легких атомов этот порядок соответствует тому, что сначала заполняется оболочка с меньшимп и лишь затем должна заполняться электронами следующая оболочка. В пределах однойоболочки сначала заполняются состояния с l = 0, а затем состояния с большими l, вплоть доl=п – 1. Взаимодействие между электронами приводит к тому, что для достаточно больших главных квантовых чиселnсостояния с большимnи малымlмогут иметь меньшую энергию, то есть быть энергетически более выгодными, чем состояния с меньшимп, но с большимl. Из изложенного следует, что периодичность химических свойств элементов объясняется повторяемостью электронных конфигураций во внешних электронных подгруппах у атомов родственных элементов.
studfile.net
Модели атомов. Опыт Резерфорда. Видеоурок. Физика 9 Класс
На предыдущем уроке мы обсудили, что в результате радиоактивности образуются различные виды излучений: a-, b-, и g-лучи. Появился инструмент, при помощи которого можно было изучать строение атома.
После того, как стало ясно, что атом тоже имеет сложную структуру, как-то по-особенному устроен, необходимо было исследовать само строение атома, объяснить, как он устроен, из чего состоит. И вот ученые приступили к этому изучению.
Первые идеи о сложном строении были высказаны Томсоном, который в 1897 году открыл электрон. В 1903 году Томсон впервые предложил модель атома. По теории Томсона, атом представлял собой шар, по всему объему которого «размазан» положительный заряд. А внутри, как плавающие элементы, находились электроны. В целом, по Томсону, атом был электронейтрален, т. е. заряд такого атома был равен 0. Отрицательные заряды электронов компенсировали положительный заряд самого атома. Размер атома составлял приблизительно 10-10м. Модель Томсона получила название «пудинг с изюмом»: сам «пудинг» – это положительно заряженное «тело» атома, а «изюм» – это электроны (рис. 1).

Рис. 1. Модель атома Томсона («пудинг с изюмом»)
Первый достоверный опыт по определению строения атома удалось провести Э. Резерфорду. На сегодняшний день мы твердо знаем, что атом представляет собой структуру, напоминающую планетную солнечную систему. В центре находится массивное тело, вокруг которого вращаются планеты. Такая модель атома получила название планетарной модели.
Давайте обратимся к схеме опыта Резерфорда (рис. 2) и обсудим результаты, которые привели к созданию планетарной модели.

Рис. 2. Схема опыта Резерфорда
Внутрь свинцового цилиндра с узким отверстием был заложен радий. При помощи диафрагмы создавался узкий пучок a-частиц, которые, пролетая через отверстие диафрагмы, попадали на экран, покрытый специальным составом, при попадании возникала микро-вспышка. Такое свечение при попадании частиц на экран называется «сцинтиляционная вспышка». Такие вспышки наблюдались на поверхности экрана при помощи микроскопа. В дальнейшем до тех пор, пока в схеме не было золотой пластины, все частицы, которые вылетали из цилиндра, попадали в одну точку. Когда же внутрь экрана на пути летящих a-частиц была поставлена очень тонкая пластинка из золота, стали наблюдаться совершенно непонятные вещи. Как только была поставлена золотая пластина, начались отклонения a-частиц. Были замечены частицы, которые отклонялись от своего первоначального прямолинейного движения и уже попадали в совершенно другие точки этого экрана.
Более того, когда экран сделали почти замкнутым, выяснилось, что есть частицы, которые каким-то образом летят в обратную сторону. Они отклоняются под углом 90° и больше. Эти наблюдения были проанализированы Резерфордом, и выяснилась следующая довольно любопытная вещь.
В первую очередь здесь потерпела крах теория Томсона. По теории Томсона, атом представляет собой шар размером 10-10м, в котором положительный заряд размазан и есть электрон. Так вот, электроны – это очень маленькие частицы, они не могут препятствовать a-частицам, летящим с приличной скоростью. Скорость a-частиц в данном случае составляла около 10000 км/с.
Представьте себе ситуацию, когда грузовик столкнется с игрушечным автомобилем. Понятно, что грузовик даже не заметит такого автомобиля. Это мы можем привести как аналогию столкновения электрона с a-частицей. Значит, необходимо было сделать вывод, что атом устроен иначе, не так, как утверждал Томсон. И, видимо, в атоме золота есть объект более массивный, чем a-частица, имеющий положительный заряд.
Давайте посмотрим еще одну картину, которая характеризует рассеивание a-частиц на той массивной частице, наличие которой предсказал Резерфорд в атоме (рис. 3).

Рис. 3. Рассеивание альфа-частиц По результатам опытов можно было говорить, что в атоме есть массивный положительно заряженный объект. a-частица, сталкиваясь с этой большой частицей, может отразиться обратно. Те частицы, которые пролетают рядом, отклоняются на разные углы. Чем дальше a-частица пролетает от этого объекта, тем на меньший угол они отклоняются. Такое явление получило название «рассеивание a-частиц».
Крупную частицу, которая находится внутри атома, Резерфорд назвал ядром. И даже оценил его размеры. По оценке Резерфорда, размеры ядра составили 10-14–10-15м. Этот объект был очень и очень мал по своим размерам по сравнению с атомом. Атом имеет размер порядка 10-10м. При этом практически вся масса атома была сосредоточена именно в ядре. И именно вокруг ядра обращаются электроны.
Отсюда следует планетарная модель Резерфорда, которая утверждает, что атом представляет собой массивное положительно заряженное ядро, вокруг которого по своим орбитам обращаются электроны (рис. 4). В целом атом электронейтрален, т. е. заряд атома равен нулю. Если у атома избыток или недостаток электронов, то его называют ион.
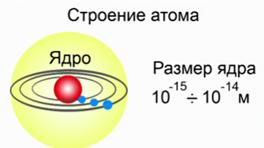
Рис. 4. Планетарная модель атома
Конечно, были и другие теории, представляющие интерес. На сегодняшний день общепринятой, с некоторыми оговорками, о которых поговорим позднее, является именно планетарная модель атома, предложенная Эрнестом Резерфордом.
Список литературы
- Бронштейн М.П. Атомы и электроны. «Библиотечка “Квант”». Вып. 1. – М.: Наука, 1980.
- Кикоин И.К., Кикоин А.К. Физика: Учебник для 9 класса средней школы. – М.: «Просвещение».
- Китайгородский А.И. Физика для всех. Фотоны и ядра. Книга 4. – М.: Наука.
- Мякишев Г.Я., Синякова А.З. Физика. Оптика Квантовая физика. 11 класс: учебник для углубленного изучения физики. – М.: Дрофа.
- Ньютон И. Математические начала натуральной философии. – М.: Наука, 1989.
- Резерфорд Э. Избранные научные труды. Радиоактивность. – М.: Наука.
- Резерфорд Э. Избранные научные труды. Строение атома и искусственное превращение элементов. – М.: Наука.
- Эйнштейн А., Инфельд Л. Эволюция физики. Развитие идей от первоначальных понятий до теории относительности и квантов. – М.: Наука, 1965.
interneturok.ru
Планетарная модель атома — Википедия
Материал из Википедии — свободной энциклопедии
Планетарная модель атома: ядро (красное) и электроны (зелёные)Планета́рная моде́ль а́тома, или модель атома Резерфо́рда, — исторически важная модель строения атома, предложенная Эрнстом Резерфордом в классической статье[1], опубликованной в 1911 г. на основании анализа и статистической обработки результатов экспериментов по рассеиванию альфа-частиц в тонкой золотой фольге, выполненных Гейгером и Марсденом в 1909 г.
В этой модели Резерфорд описывает строение атома состоящим из крохотного положительно заряженного ядра, в котором сосредоточена почти вся масса атома, вокруг которого вращаются электроны, — подобно тому, как планеты движутся вокруг Солнца.
Планетарная модель атома соответствует современным представлениям о строении атома с уточнениями, что движение электронов не может быть описано законами классической механики и имеет квантовомеханическое описание.
Исторически планетарная модель Резерфорда пришла на смену «модели сливового пудинга» Джозефа Джона Томсона, которая предполагает, что отрицательно заряженные электроны помещены внутрь положительно заряженного атома с распределённым по всему объёму атома положительным зарядом, подобно изюминкам в пудинге.
Предыстория
Схема модели атома Томсона. В модели Томсона «корпускулы» (электроны) расположены внутри облака положительного заряда, а не вокруг положительно заряженного ядра.К 1904 году японский физик Нагаока разработал раннюю, как оказалось впоследствии, ошибочную «планетарную модель» атома («атом типа Сатурна»)[2]. Модель была построена на аналогии с расчётами устойчивости колец Сатурна (кольца уравновешены из-за очень большой массы планеты). Модель Нагаоки была неверна, но два следствия из неё оказались пророческими:
Новую модель строения атома Резерфорд предложил в 1911 году на основе анализа экспериментов по рассеиванию альфа-частиц в золотой фольге, проведённых в 1909 г. под его руководством[1].
При этом рассеянии большое, неожиданно статистически необъяснимое, количество альфа-частиц рассеивалось на большие углы, что свидетельствовало о том, что центр рассеяния имеет небольшие размеры, в нём сосредоточен значительный электрический заряд и масса атома.
Расчёты Резерфорда показали, что рассеивающий центр, заряженный положительно или отрицательно, должен быть по крайней мере в 3000 раз меньше размера атома, который в то время уже был известен и оценивался как примерно 10−10 м. Поскольку в то время электроны уже были известны, а их масса и заряд определены, то рассеивающий центр, который позже назвали ядром, должен был иметь противоположный электронам заряд. Резерфорд не связал величину заряда с атомным номером. Этот вывод был сделан позже. А сам Резерфорд предположил, что заряд ядра пропорционален атомной массе. Связь электрического заряда ядра с атомным номером химического элемента установил Генри Мозли в экспериментах, выполненных в 1913 г.
Недостатком планетарной модели была невозможность объяснения ею устойчивости атомов. Из классической электродинамики следует, что так как электроны движутся вокруг ядра, испытывая при этом центростремительное ускорение как планеты вокруг Солнца, то они по законам классической электродинамики должны излучать электромагнитные волны, теряя при этом на излучение кинетическую энергию орбитального движения и в результате «упасть» на ядро. Расчёты, выполненные с помощью методов классической электродинамики показывают, что электроны должны «упасть» на ядро за время порядка 10−11 с.
Это противоречие было снято последующим развитием планетарной модели в модели атома Бора, постулирующая другие, отличные от классических законы орбитального движения электронов на основе волн де Бройля. Полностью противоречащие эксперименту выводы классической электродинамики смогло объяснить развитие квантовой механики.
Примечания
wikipedia.green
Строение атома. Опыты Резерфорда — Класс!ная физика
Строение атома. Опыты Резерфорда
«Физика — 11 класс»
Открытие сложного строения атома — важнейший этап становления современной физики, наложивший отпечаток на все ее дальнейшее развитие.
В процессе создания количественной теории строения атома, позволившей объяснить атомные спектры, были открыты новые законы движения микрочастиц — законы квантовой механики.
Модель Томсона
Первая модель атома была предложена английским физиком Дж. Дж. Томсоном, открывшим электрон.
По мысли Томсона, положительный заряд атома занимает весь объем атома и распределен в этом объеме с постоянной плотностью.
Простейший атом (атом водорода) представляет собой положительно заряженный шар радиусом около 10-8 см, внутри которого находится электрон.
У более сложных атомов в положительно заряженном шаре находится несколько электронов, так что атом подобен кексу, в котором роль изюминок выполняют электроны.
Однако модель атома Томсона оказалась в полном противоречии с известными уже к тому времени свойствами атома, главным из которых является устойчивость.
Опыты Резерфорда
Масса электронов в несколько тысяч раз меньше массы атомов.
Так как атом в целом нейтрален, то, следовательно, основная масса атома приходится на его положительно заряженную часть.
Для экспериментального исследования распределения положительного заряда, а значит, и массы внутри атома Эрнест Резерфорд предложил в 1906 г. применить зондирование атома с помощью α-частиц.
Эти частицы возникают при распаде радия и некоторых других элементов.
Их масса примерно в 8000 раз больше массы электрона, а положительный заряд равен по модулю удвоенному заряду электрона.
Это не что иное, как полностью ионизированные атомы гелия.
Скорость α-частиц очень велика: она составляет 1/15 скорости света.
Этими частицами Резерфорд бомбардировал атомы тяжелых элементов.
Электроны вследствие своей малой массы не могут заметно изменить траекторию а-частицы, подобно тому как камушек в несколько десятков граммов при столкновении с автомобилем не может значительно изменить его скорость.
Рассеяние (изменение направления движения) α-частиц может вызвать только положительно заряженная часть атома.
Таким образом, по рассеянию α-частиц можно определить характер распределения положительного заряда и массы внутри атома.
Схема опытов Резерфорда:
Радиоактивный препарат, например радий, помещался внутри свинцового цилиндра 1, вдоль которого был высверлен узкий канал.
Пучок -частиц из канала падал на тонкую фольгу 2 из исследуемого материала (золото, медь и пр.).
После рассеяния α-частицы попадали на полупрозрачный экран 3, покрытый сульфидом цинка.
Столкновение каждой частицы с экраном сопровождалось вспышкой света (сцинтилляцией), которую можно было наблюдать в микроскоп 4.
Весь прибор размещался в сосуде, из которого был откачан воздух.
При хорошем вакууме внутри прибора в отсутствие фольги на экране возникал светлый кружок, состоящий из сцинтилляций, вызванных тонким пучком α-частиц.
Но когда на пути пучка помещали фольгу, α-частицы из-за рассеяния распределялись на экране по кружку большей площади.
Модифицируя экспериментальную установку, Резерфорд попытался обнаружить отклонение α-частиц на большие углы.
Для этого он окружил фольгу сцинтилляциоными экранами и определил число вспышек на каждом экране.
Совершенно неожиданно оказалось, что небольшое число α-частиц (примерно одна из двух тысяч) отклонилось на углы, большие 90°.
Позднее Резерфорд признался, что, предложив своим ученикам провести эксперимент по наблюдению за рассеянием α-частиц на большие углы, он сам не верил в положительный результат.
В самом деле, предвидеть этот результат на основе модели Томсона было нельзя.
При распределении по всему атому положительный заряд не может создать достаточно сильное электрическое поле, способное отбросить α-частицу назад.
Максимальная сила отталкивания может быть определена по закону Кулона:
где
qα — заряд α-частицы;
q — положительный заряд атома;
R — его радиус;
k — коэффициент пропорциональности.
Напряженность электрического поля равномерно заряженного шара максимальна на поверхности шара и убывает до нуля по мере приближения к центру.
Поэтому чем меньше радиус R, тем больше сила, отталкивающая α-частицы.
Определение размеров атомного ядра
Резерфорд понял, что α-частица могла быть отброшена назад лишь в том случае, если положительный заряд атома и его масса сконцентрированы в очень малой области пространства.
Так Резерфорд пришел к мысли о существовании атомного ядра — тела малых размеров, в котором сконцентрированы почти вся масса и весь положительный заряд атома.
На рисунке показаны траектории α-частиц, пролетающих на различных расстояниях от ядра.
Подсчитывая число α-частиц, рассеянных на различные углы, Резерфорд смог оценить размеры ядра.
Оказалось, что ядро имеет диаметр порядка 10-12—10-13 см (у разных ядер диаметры различны).
Размер же самого атома 10-8 см, т. е. в 10—100 тысяч раз превышает размеры ядра.
Впоследствии удалось определить и заряд ядра.
При условии, что заряд электрона принят за единицу, заряд ядра в точности равен номеру данного химического элемента в периодической системе Д. И. Менделеева.
Планетарная модель атома
На основе своих опытов Резерфорд создал планетарную модель атома.
В центре атома расположено положительно заряженное ядро, в котором сосредоточена почти вся масса атома.
В целом атом нейтрален.
Поэтому число внутриатомных электронов, как и заряд ядра, равно порядковому номеру элемента в периодической системе.
Ясно, что покоиться электроны внутри атома не могут, так как они упали бы на ядро.
Они движутся вокруг ядра, подобно тому как планеты обращаются вокруг Солнца.
Такой характер движения электронов определяется действием кулоновских сил притяжения со стороны ядра.
В атоме водорода вокруг ядра обращается всего лишь один электрон.
Ядро атома водорода имеет положительный заряд, равный по модулю заряду электрона, и массу, примерно в 1836,1 раза бо́льшую массы электрона.
Это ядро было названо протоном и стало рассматриваться как элементарная частица.
Размер атома водорода — это радиус орбиты его электрона.
Простая и наглядная планетарная модель атома имеет прямое экспериментальное обоснование.
Она кажется совершенно необходимой для объяснения опытов по рассеиванию α-частиц.
Но на основе этой модели нельзя объяснить факт существования атома, его устойчивость.
Ведь движение электронов по орбитам происходит с ускорением, причем весьма немалым.
Ускоренно движущийся заряд по законам электродинамики Максвелла должен излучать электромагнитные волны с частотой, равной частоте его обращения вокруг ядра.
Излучение сопровождается потерей энергии.
Теряя энергию, электроны должны приближаться к ядру, подобно тому как спутник приближается к Земле при торможении в верхних слоях атмосферы.
Как показывают расчеты, основанные на механике Ньютона и электродинамике Максвелла, электрон за ничтожно малое время (порядка 10-8 с) должен упасть на ядро.
Атом должен прекратить свое существование.
В действительности ничего подобного не происходит.
Атомы устойчивы и в невозбужденном состоянии могут существовать неограниченно долго, совершенно не излучая электромагнитные волны.
Не согласующийся с опытом вывод о неизбежной гибели атома вследствие потери энергии на излучение — это результат применения законов классической физики к явлениям, происходящим внутри атома.
Отсюда следует, что к таким явлениям законы классической физики неприменимы.
Резерфорд создал планетарную модель атома: электроны обращаются вокруг ядра, подобно тому как планеты обращаются вокруг Солнца.
Эта модель проста, обоснована экспериментально, но не позволяет объяснить устойчивость атома.
Источник: «Физика — 11 класс», учебник Мякишев, Буховцев, Чаругин
Атомная физика. Физика, учебник для 11 класса — Класс!ная физика
Строение атома. Опыты Резерфорда — Квантовые постулаты Бора. Модель атома водорода по Бору. Трудности теории Бора. Квантовая механика — Лазеры — Краткие итоги главы
class-fizika.ru
Планетарная модель Резерфорда, атом в модели Резерфорда
Открытия в области строения атома стали важным шагом в развитии физики. Огромное значение имела модель Резерфорда. Атом как система и частицы, его составляющие, был изучен более точно и подробно. Это привело к успешному становлению такой науки, как ядерная физика.
Античные представления о строении вещества
Предположение о том, что окружающие тела состоят из мельчайших частиц, были высказаны еще в античные времена. Мыслители того времени представляли атом в виде мельчайшей и неделимой частицы любого вещества. Они утверждали, что нет во Вселенной ничего меньшего по размеру, чем атом. Таких взглядов придерживались великие древнегреческие ученые и философы – Демокрит, Лукреций, Эпикур. Гипотезы этих мыслителей сегодня объединены под названием «античный атомизм».

Средневековые представления
Времена античности прошли, и в средние века также были ученые, которые высказывали различные предположения о строении веществ. Однако преобладание религиозных философских взглядов и власть церкви в тот период истории на корню пресекали любые попытки и стремления человеческого разума к материалистическим научным выводам и открытиям. Как известно, средневековая инквизиция весьма недружелюбно вела себя с представителями научного мира того времени. Остается сказать, что у тогдашних светлых умов было пришедшее из античности представление о неделимости атома.
Исследования 18-19 веков
18 столетие было отмечено серьезными открытиями в области элементарного строения вещества. Во многом благодаря стараниям таких ученых, как Антуан Лавуазье, Михаил Ломоносов и Джон Дальтон. Независимо друг от друга они сумели доказать, что атомы действительно существуют. Но вопрос об их внутреннем строении оставался открытым. Конец 18 века был отмечен таким знаменательным событием в научном мире, как открытие Д. И. Менделеевым периодической системы химических элементов. Это стало по-настоящему мощным прорывом того времени и приоткрыло завесу над пониманием того, что все атомы имеют единую природу, что они родственны друг другу. В дальнейшем, в 19 веке, еще одним важным шагом на пути к разгадке строения атома стало доказательство того, что в составе любого из них присутствует электрон. Работа ученых этого периода подготовила благодатную почву для открытий 20-го века.
Эксперименты Томсона
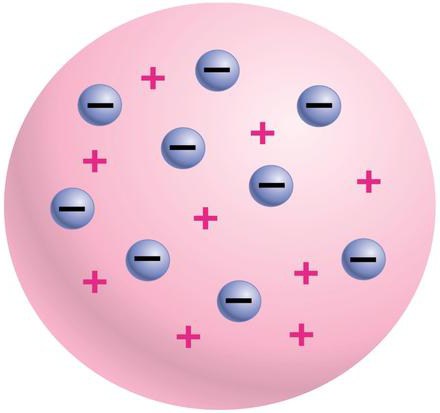
Английский физик Джон Томсон в 1897 году доказал, что в состав атомов входят электроны с отрицательным зарядом. На этом этапе ложные представления о том, что атом – предел делимости любого вещества, были окончательно разрушены. Как же Томсон сумел доказать существование электронов? Ученый в своих опытах помещал в сильно разреженные газы электроды и пропускал электрический ток. В результате возникали катодные лучи. Томсон тщательно изучил их особенности и обнаружил, что они являются потоком заряженных частиц, которые движутся с огромной скоростью. Ученый сумел высчитать массу этих частиц и их заряд. Он также выяснил, что их нельзя преобразовать в нейтральные частицы, поскольку электрический заряд – это основа их природы. Так были открыты электроны. Томсон является и создателем первой в мире модели строения атома. Согласно ей, атом – это сгусток положительно заряженной материи, в которой равномерно распределены отрицательно заряженные электроны. Такое строение объясняет общую нейтральность атомов, так как противоположные заряды уравновешивают друг друга. Опыты Джона Томсона стали неоценимо важными для дальнейшего изучения строения атома. Однако многие вопросы оставались без ответа.

Исследования Резерфорда
Томсон открыл существование электронов, но он не сумел найти в атоме положительно заряженных частиц. Эрнест Резерфорд исправил это недоразумение в 1911 году. Во время экспериментов, изучая активность альфа-частиц в газах, он обнаружил, что в атоме присутствуют частицы, положительно заряженные. Резерфорд увидел, что при прохождении лучей сквозь газ или через тонкую металлическую пластину происходит резкое отклонение незначительного количества частиц от траектории движения. Их буквально отбрасывало назад. Ученый догадался, что такое поведение объясняется столкновением с положительно заряженными частицами. Такие эксперименты позволили физику создать модель строения атома Резерфорда.

Планетарная модель
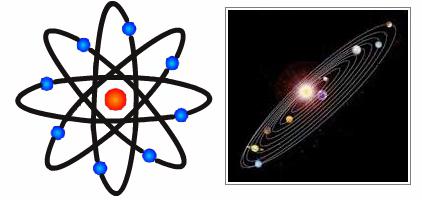
Теперь представления ученого несколько отличались от предположений, высказанных Джоном Томсоном. Разными стали и их модели атомов. Опыт Резерфорда позволил ему создать совершенно новую теорию в этой области. Открытия ученого имели решающее значение для дальнейшего развития физики. Модель Резерфорда описывает атом как ядро, расположенное в центре, и движущиеся вокруг него электроны. Ядро обладает положительным зарядом, а электроны – отрицательным. Модель атома по Резерфорду предполагала вращение электронов вокруг ядра по определенным траекториям – орбитам. Открытие ученого помогло объяснить причину отклонения альфа-частиц и стало толчком к развитию ядерной теории атома. В модели атома Резерфорда прослеживается аналогия с движением планет Солнечной системы вокруг Солнца. Это очень точное и яркое сравнение. Поэтому модель Резерфорда, атом в которой движется вокруг ядра по орбите, была названа планетарной.
Работы Нильса Бора
Двумя годами позже датский физик Нильс Бор попытался объединить представления о строении атома с квантовыми свойствами светового потока. Ядерная модель атома Резерфорда была положена ученым в основу его новой теории. По предположению Бора, атомы вращаются вокруг ядра по круговым орбитам. Такая траектория движения приводит к ускорению электронов. Кроме того, кулоновское взаимодействие этих частиц с центром атома сопровождается созданием и расходованием энергии для поддержания пространственного электромагнитного поля, возникающего из-за движения электронов. При таких условиях отрицательно заряженные частицы должны когда-нибудь упасть на ядро. Но этого не происходит, что указывает на большую устойчивость атомов как систем. Нильс бор понял, что законы классической термодинамики, описанные уравнениями Максвелла, не работают во внутриатомных условиях. Поэтому ученый поставил перед собой задачу вывести новые закономерности, которые были бы справедливы в мире элементарных частиц.
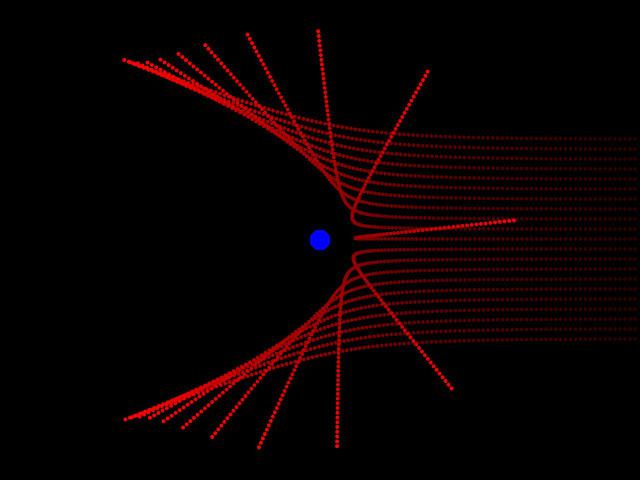
Постулаты Бора
Во многом благодаря тому, что существовала модель Резерфорда, атом и его составляющие были неплохо изучены, Нильс Бор смог подойти к созданию своих постулатов. Первый из них гласит о том, что атом имеет стационарные состояния, при которых он не изменяет свою энергию, а электроны при этом движутся по орбитам, не меняя своей траектории. Согласно второму постулату, при переходе электрона с одной орбиты на другую происходит выделение или поглощение энергии. Она равна разности энергий предшествующего и последующего состояний атома. При этом, если электрон перепрыгивает на более близкую к ядру орбиту, то происходит излучение энергии (фотона), и наоборот. Несмотря на то что движение электронов мало напоминает орбитальную траекторию, расположенную строго по окружности, открытие Бора позволило получить великолепное объяснение существованию линейчатого спектра атома водорода. Приблизительно в это же время ученые-физики Герц и Франк, жившие в Германии, подтвердили учение Нильса Бора о существовании стационарных, стабильных состояний атома и возможность изменения значений атомной энергии.

Сотрудничество двух ученых
Кстати, Резерфорд длительное время не мог определить заряд ядра. Ученые Марсден и Гейгер попытались осуществить перепроверку утверждений Эрнеста Резерфорда и в результате подробных и тщательных экспериментов и расчетов пришли к выводу о том, что именно ядро является важнейшей характеристикой атома, и в нем сосредоточен весь его заряд. В дальнейшем было доказано, что значение заряда ядра численно равно порядковому номеру элемента в периодической системе элементов Д. И. Менделеева. Интересно, что Нильс Бор вскоре познакомился с Резерфордом и полностью согласился с его взглядами. В последующем ученые длительно работали вместе в одной лаборатории. Модель Резерфорда, атом как система, состоящая из элементарных заряженных частиц, – все это Нильс Бор посчитал справедливым и навсегда отложил в сторону свою электронную модель. Совместная научная деятельность ученых была очень успешной и принесла свои плоды. Каждый из них углубился в изучение свойств элементарных частиц и сделал значимые для науки открытия. Позже Резерфорд обнаружил и доказал возможность разложения ядра, но это уже тема другой статьи.
fb.ru