Развитие в науке представлений о простом и сложном веществе. Химические элементы. Символы химических элементов.
Тема: Первоначальные химические представления
Урок: Развитие в науке представлений о простом и сложном веществе. Химические элементы
Вам уже знакомо имя английского исследователя Р. Бойля. Именно он предложил опыты по определению состава веществ. Рассмотрим суть таких опытов.
Чтобы установить состав вещества (проанализировать вещество) часто используют реакцию разложения, в результате которой из одного исходного вещества получается несколько продуктов реакции.
ОПЫТ 1. Разложение сахара при нагревании.
Поместим в пробирку несколько крупинок сахара и нагреем ее в пламени спиртовки. В результате прокаливания на стенках пробирки появляются капельки прозрачной жидкости, а на месте крупинок сахара образуется вещество черного цвета (Рис. 1). Если продолжать нагревание и дальше, то с черным веществом ничего не происходит. Это вещество – сажа (уголь). Его нельзя разложить ни при каких условиях.
Прозрачная жидкость на стенках пробирки — это вода. Воду можно разложить на два вещества с помощью электрического тока.

Рис. 1. Разложение сахара при нагревании
ОПЫТ 2. Разложение воды.
Заполним водой электролизер. На электроды надеваем пробирки, заполненные водой. При пропускании электрического тока через воду на электродах начнут выделяться газы, которые вытеснят воду из пробирок. Газы получатся чистыми, потому что воздуха в пробирках, заполненных водой, нет.

Рис. 2. Разложение воды под действием электрического тока
Итак, при разложении сахара образуется два вещества – вода и сажа (или уголь). Сажа не подвергается дальнейшему разложению. Вода же разлагается на водород и кислород. Водород и кислород дальше не разлагаются.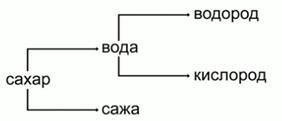
Рис. 3. Результаты опытов по разложению сахара и воды
За многие годы исследований ученые обнаружили немало веществ, которые не подвергаются разложению ни при каких условиях. Это сажа, железо, сера, медь, кислород, водород и другие. Вещества, которые не удавалось разложить, стали называть простыми веществами. Если вещество удавалось разложить, его считали сложным веществом.
Долгое время к простым веществам относили и воду, потому что не могли подобрать условия ее разложения. Ошибочно также простыми считали кварц и корунд. В состав минерала кварца входят атомы кремния и кислорода. А корунд, отличающийся большой твердостью, содержит атомы алюминия и кислорода.
По мнению Р. Бойля, простое вещество оттого нельзя разложить, что оно состоит из отличного от других элемента. Что же такое химический элемент?
Химический элемент – это разновидность атомов.
Тогда сформулируем определения простого и сложного веществ.
Простое вещество состоит из одного химического элемента (из атомов одного вида).
Сложное вещество состоит из различных химических элементов (из атомов разных видов).
Важно отметить, что из одного простого вещества нельзя в ходе химической реакции получить вещество, образованное другим химическим элементом, т.к. в ходе химических реакций атомы не изменяются.
Проиллюстрируем данные определения. Молекула водорода состоит из двух атомов одного химического элемента, тоже называемого водородом. Молекула кислорода тоже состоит из двух атомов одного химического элемента, называемого кислородом. Сажа состоит только из атомов углерода. Молекула воды состоит из двух атомов водорода и одного атома кислорода, т.е. включает в себя два различных химических элемента.
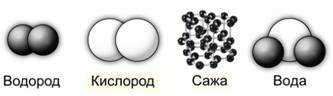
Рис. 4. Модели строения некоторых веществ
Названия многих химических элементов не отличаются от названий простых веществ, образованных этими элементами. Например, простое вещество водород состоит из химического элемента водорода. Простое вещество кислород состоит из химического элемента кислорода. Простое вещество железо состоит из атомов железа. Поэтому очень важно научиться различать понятия «простое вещество» и «химический элемент».
Приведем примеры двух высказываний о кислороде, в одном из которых речь идет о химическом элементе, а в другом – о простом веществе.
Первое: «Рыбы дышат кислородом, растворенным в воде.» Второе: «В состав молекулы воды входит кислород.» Говоря о кислороде, который растворен в воде, мы имеем в виду вещество, для которого характерны определенные свойства – например, растворимость в воде.Кислород, входящий в состав молекулы воды, — это химический элемент. Т.е мы можем сказать, что атом кислорода входит в состав молекулы воды.
Есть химические элементы, которые образуют несколько различных простых веществ. Например, химический элемент углерод образует графит (тоже, что и сажа, уголь) и алмаз. Графит – нетвердое вещество серого цвета с металлическим блеском. Из него делают стержни простых карандашей.
Алмаз — минерал, имеющий самую большую твердость. Ограненный алмаз называют бриллиантом. Несмотря на то, что эти простые вещества состоят только из атомов углерода, они очень различаются по свойствам.
Свойство химического элемента, образовывать несколько простых веществ, называют аллотропией. А простые вещества, образованные одним химическим элементом, называют
аллотропическими модификациями.
Список рекомендованной литературы
1. Сборник задач и упражнений по химии: 8-й класс: к учебнику П.А. Оржековского и др. «Химия, 8 класс» / П.А. Оржековский, Н.А. Титов, Ф.Ф. Гегеле. – М.: АСТ: Астрель, 2006.
2. Ушакова О.В. Рабочая тетрадь по химии: 8-й кл.: к учебнику П.А. Оржековского и др. «Химия. 8 класс» / О.В. Ушакова, П.И. Беспалов, П.А. Оржековский; под. ред. проф. П.А. Оржековского — М.: АСТ: Астрель: Профиздат, 2006. (с.17-19)
3. Химия: 8-й класс: учеб. для общеобр. учреждений / П.А. Оржековский, Л.М. Мещерякова, Л.С. Понтак. М.: АСТ: Астрель, 2005.(§7)
4. Химия: неорг. химия: учеб. для 8 кл. общеобр. учреждений / Г.Е. Рудзитис, ФюГю Фельдман. – М.: Просвещение, ОАО «Московские учебники», 2009. (§§5,6)
5. Энциклопедия для детей. Том 17. Химия / Глав. ред.В.А. Володин, вед. науч. ред. И. Леенсон. – М.: Аванта+, 2003.
1. Единая коллекция цифровых образовательных ресурсов (Источник).
2. Электронная версия журнала «Химия и жизнь» (Источник).
3. Тесты по химии (онлайн) (Источник).
Домашнее задание
с. 17 №№ 4, 5 из Рабочей тетради по химии: 8-й кл.: к учебнику П.А. Оржековского и др. «Химия. 8 класс» / О.В. Ушакова, П.И. Беспалов, П.А. Оржековский; под. ред. проф. П.А. Оржековского — М.: АСТ: Астрель: Профиздат, 2006.
interneturok.ru
«Простые и сложные вещества. Состав вещества. Химическая формула».
Задания для итоговой оценки достижения планируемых результатов
Тема: «Простые и сложные вещества.
Состав вещества. Химическая формула».
Планируемый результат: характеризовать вещества по составу и свойствам:
I. Различать простые и сложные вещества на основании их химических формул;
II. Характеризоваться состав веществ по их химическим формулам и составлять формулы, зная состав веществ.
Умение: различать простые и сложные вещества на основании их химических формул.
Примеры заданий
I. Задание 1 (базовый уровень)
В каком ряду приведены формулы только сложных веществ?
CO2, O3, HCl, KOH
NaOH, Hl, H2, HNO3
CO, SO2, NaCl, SiO2
NH3, H2O, CO2, O3
Ответ: 3
Задание 2 (повышенный уровень)
Определите, какие из веществ, о которых говорилось при описании природных процессов, являются простыми либо сложными, и выпишите отдельно химические формулы веществ каждой группы.
В листья зеленых растений на свету углекислый газ (CO2), поступающий в растения из воздуха, и вода (H2O), поступающая из почвы, превращаются в глюкозу (С6Н12О6) и кислород (О2).
Азот (N2), содержащийся в воздухе, способны усваивать клубеньковые бактерии бобовых растений. При гниении этих растений в почве образуются различные органические вещества, мочевина ((NН2)2СО) и нередко аммиак (NH3).
Элементы ответа:
Определены формулы простых веществ: О2 и N2
Определены формулы сложных веществ: CO2, H2O, С
6Н12О6, ((NН2)2СО, NH3.
Умение: характеризоваться состав веществ по их химическим формулам и составлять формулы, зная состав веществ.
Примеры заданий
Задание 1(базовый уровень)
Сложное вещество образовано двумя химическими элементами – азотом и кислородом, при этом на каждый атом азота приходится один атом кислорода. Химическая формула этого вещества:
N2O3
NO2
NO
N2O5
Ответ: 3
Задание 2 (повышенный уровень)
Установите соответствие между химической формулой вещества и числом атомов кислорода в составе этого вещества.
А) NH4NO3B) Ca(NO3)2
12
3
2
6
infourok.ru
Урок на тему «Простые и сложные вещества». 8-й класс, химия
Цель урока:
- Знать определение атома, молекулы, простого и сложного вещества.
- Уметь различать простые и сложные вещества; смеси и сложные вещества.
- Знать отличие смеси и сложного вещества.
Оборудование: Шаровые модели молекул воды, Штатив с пробирками, реактивы (железо, вода, сера, карбонат кальция).
демонстрация соединение железа с серой.
Лабораторные опыты: Ознакомление с образцами простых и сложных веществ.
Ход урока
1. Повторение и обобщение знаний.
1) Проверка домашнего задания:
Упражнение упр. 8, 9, 10, на стр. 22. (Взаимопроверка).
2) Выполните тестовое задание. Подберите соответствие: термин – определение понятия.
(Приложение №1). Самопроверка.
3) Приведите примеры смесей (не менее двух), которые можно разделить:
1 вариант:
А) фильтрованием————————————————————————————-
Б) отстаиванием—————————————————————————————-
2 вариант:
А) выпариванием—————————————————————————————
Б) дистилляцией——————————————————————————————
2. Изучение нового материала
1. Фронтальный опрос:
Какие виды смесей вам известны?
Какие смеси называются однородными, неоднородными?
Какое вещество называется чистым? Что такое «вещество»? Из курса физики вам известно, что многие вещества состоят из молекул.
Дайте определения понятиям «молекула» и «атом». (Приложение №2).
Рассмотрите шаровые модели некоторых веществ, укажите состав данного вещества. Чем молекула озона отличается от молекулы оксида кальция? Чем водород отличается от соляной кислоты? Учащиеся могут ответить, что молекулы водорода, фосфора, азота образованы атомами одного вида. – Простые вещества.
Вещества соляная кислота, оксид кальция, метан, оксид натрия образованы атомами разного вида. Сложные вещества.
Выпишите в словарь новые понятия, со страниц 15,16.
Заполните схему:
2. Лабораторный опыт.
Инструкция к лабораторному опыту.
- Прослушайте инструктаж по охране труда.
- Выполните опыт: рассмотрите выданные вам образцы веществ: железо, вода, сера, карбонат кальция.
- Опишите их физические свойства.
- Оформите результаты в таблицу. (Приложение №3).
| Физические свойства | железо |
вода |
сера |
Карбонат кальция |
Агрегатное состояние (твердое, жидкое, газообразное) |
|
|
|
|
Цвет |
|
|
|
|
Блеск |
|
|
|
|
Растворимость в воде |
|
|
|
|
Хрупкость (пластичность) |
|
|
|
|
Теплоэлектропроводность |
|
|
|
|
Температура кипения, температура плавления. |
|
|
|
|
Простое (сложное) вещество |
|
|
|
|
Вывод к работе: о физических свойствах веществ, о составе простых и сложных веществах.
3. Чем смесь отличается от сложного вещества.
Напомнив, как готовиться смесь железа и серы, учитель отмечает, что сера — простое вещество, молекулы ее состоят из одинаковых атомов одного вида, железо тоже простое вещество, состоящее из одинаковых атомов другого вида. Можно ли назвать то, что получилось при перемешивании порошков, сложным веществом? Разделим смесь при помощи магнита. После обсуждения делаем вывод, что смесь можно разделить физическими способами и получить чистые вещества, из которых она состояла. Нагреваем железо с опилками. Образовалось новое вещество, которое невозможно разделить, не действует на него магнит. Сульфид железа – это чистое сложное вещество.
Таблица №1. Сравнение смесей и сложных веществ.
Смесь |
Сложное вещество |
1. Вещества сохраняют свои свойства. |
1. Свойства исходных веществ не сохраняются. |
2. Вещества можно разделить физическими методами. |
2. Сложное вещество нельзя разделить физическими методами. |
3. Количественный состав может быть произвольным. |
3. Количественный состав химического соединения всегда одинаков независимо от места нахождения и способа получения. |
3. Закрепление.
1. Выпишите простые вещества: сталь, чугун, железо, морская вода, дистиллированная вода, алюминий, лимонад, спиртовая настойка йода, нефть, глюкоза, поваренная соль, воздух, кислород, бронза.
2. Простые вещества состоят из атомов … химического элемента.
Сложные вещества состоят из атомов … Химических элементов. Сложные вещества иначе называют … .
Простое вещество, в отличие от сложного, нельзя … .
3. Чем морская вода отличается от дистиллированной воды?
4. Сравнить смесь со сложным веществом.
Вопросы и задания |
Вещества |
|
вода |
Водород и кислород (смесь) |
|
Можно ли разделить эти вещества на более простые компоненты. Не разрушая молекул? Почему? |
|
|
Сохраняется ли способность молекул кислорода поддерживать горение? Почему? |
|
|
Рефлексия и подведение итогов.
Что нового узнали на уроке?
Какие вопросы вызвали затруднение?
Какие знания вы сегодня приобрели?
Домашнее задание: Читать стр. 15-17.
Выполнить упражнения 11-13 на стр.22.
Литература: Г.Е. Рудзитис, Ф.Г. Фельдман. «Химия 8 класс».
urok.1sept.ru
«Предмет химии. Простые и сложные вещества. Свойства веществ».
Урок по химии для 8 класса.
Презентация на тему: « «Предмет химии. Простые и сложные вещества. Свойства веществ».
Химия – это одна из интереснейших, загадочных и опасных наук. Все, что нас с вами окружает, -люди, животные, растения, моря, бытовые предметы – имеет непосредственное отношение к химии.
Химия является опасной наукой, так как все взрывчатые вещества, пиротехника, патроны, ядерные бомбы, химическое оружие. Все это разработано на основе знаний по химии. Для защиты населения и объектов тыла от радиационной, химической и биологической опасности были созданы «химические войска» во время 1-й мировой войны. Сейчас они называются войска радиационной, химической и биологической защиты Вооружённых сил Российской Федерации (с 1992 г).
В определение химии было мы с вами употребили понятие вещество.
Вещество – это то, из чего состоят физические тела.
Физические тела – это все что нас с вами окружает.
Определенный вид атомов – химический элемент.
Каждый химический элемент что каждый химический элемент имеет
три формы существования:
1. Свободные атомы.
2. Простые вещества.
3. Сложные вещества.
На слайде приведены формы существования химического элементы на примере водорода
Давайте разберем, что это значит.
При соединении атомов одного химического элемента образуется простые вещества.
Простые вещества – вещества, образованные атомами одного химического элемента.
При соединении атомов разных химических элементов образуются сложные вещества.
Сложные вещества — вещества, образованные атомами разных химических элементов.
infourok.ru
Простые и сложные вещества — методическая рекомендация. Химия, 8–9 класс.
| 1. | Названия простых веществ | 1 вид — рецептивный | лёгкое | 1 Б. | Требуется выбрать названия простых веществ. |
| 2. | Названия сложных веществ | 1 вид — рецептивный | лёгкое | 1 Б. | Надо выбрать названия сложных веществ. |
| 3. | Формулы простых веществ | 1 вид — рецептивный | лёгкое | 1 Б. | Надо выбрать формулы простых веществ. |
| 4. | Простое вещество и химический элемент | 2 вид — интерпретация | среднее | 2 Б. | Требуется выбрать утверждения, в которых речь идёт о простом веществе. |
| 5. | Состав и строение веществ | 2 вид — интерпретация | среднее | 2 Б. | Надо выбрать верные утверждения о составе и строении простых и сложных веществ. |
| 6. | Отличия металлов от неметаллов | 2 вид — интерпретация | среднее | 2 Б. | Требуется определить особенности свойства металлов и выбрать их формулы. |
| 7. | Формулы простых и сложных веществ | 3 вид — анализ | сложное | 3 Б. | Требуется установить соответствие между типами веществ и их формулами. |
| 8. | Аллотропия кислорода | 3 вид — анализ | сложное | 4 Б. | Задание на установление соответствия между простыми веществами (кислородом и озоном) и их характеристиками. |
| 9. | Установи формулу сложного вещества | 3 вид — анализ | сложное | 4 Б. | Задача на определение формулы вещества по известным массам составляющих его элементов. |
www.yaklass.ru