Кремниевые кислоты — это… Что такое Кремниевые кислоты?
Кремниевые кислоты — очень слабые, малорастворимые в воде кислоты. Известны соли метакремниевой кислоты Н2SiO3 (SiO2•H2О) — силикаты, ортокремниевой кислоты H4SiO4 (SiO2•2H2O) — ортосиликаты и других кислот с различным числом SiO2•nH2О. Гидраты кремнезема с содержанием более 2Н2О на каждую молекулу SiO2 в индивидуальном состоянии, по-видимому, не существуют, однако известны многие их соли. В воде кремниевые кислоты образуют коллоидные растворы.Соли кремниевых кислот называют силикатами (силикаты широко распространены в природе)[1].
Строение
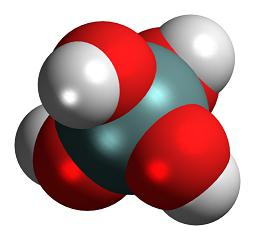
Метакремниевая (Н2SiO3) кислота состоит из структурных звеньев, имеющих тетраэдрическое строение. Звенья соединяются в цепи, образуя поликремниевые кислоты (Н2SiO3)n[1].
Получение
Na2SiO3 + 2HCl = H2SiO3 + 2NaCl.
- При высокой температуре вода выпаривается:
H2SiO3 = SiO2 + H2O
В этой реакции оксид кремния(IV) выделяется в виде силикагеля[1].
Применение
Соли кремниевых кислот применяют в производстве бумаги, в текстильной промышленности, для обработки воды, как связующие материалы. Гели кремниевых кислот (силикагели) используют как адсорбенты и как отбеливающие материалы[1].
Литература
- Капуцкий Ф. Н., Тикавый В. Ф. Пособие по химии для поступающих в вузы. — Минск: Выш. школа, 1979. — С. 384.
- Хомченко Г. П. Химия для поступающих в вузы. — М.: Высшая школа, 1994. — С. 447.
Примечания
- ↑ 1 2 3 4 Кнунянц И. Л. и др. т.2 Даффа-Меди // Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5
dic.academic.ru
подскажите в HSiO3 скольки валентен силициум о три.. и как правильно записать эту формулу
Валентность это свойство атома — говорить о «валентности» кислотного остатка как-то некомильфо. Число свободных связей, степень окисления.. . Но уж никак не валентность. В мое время например за подобный пассаж по голове не гладили Силициум — четвертая группа. h3SiO3 У водорода +1 У кислорода -2 В сумме ноль, то есть степень окисления силициума +4 Валентность четыре само-собой Структурная формула В центре кремний — от него 4 связи (2 одинарные, одна двойная) — валентность 4 Два водорода — от каждого одна связь — валентность 1 Три кислорода — от каждого две связи (или одна двойная) — валентность 2 направо от него двойная связь с кислородом Влево-вверх и влево-вниз связи еще с двумя кислородами ОТ каждого из этих двух кислородов влево по связи и на конце водород SiO3 обладает степенью окисления -2, но назвать ЭТО валентностью у меня язык не поворачивается
Вообще-то (SiO3) двухвалентный, а формула кремниевой кислоты h3SiO3.
Мне знакома только метакремниевая кислота Н2SiO3 (SiO2•h3О) и ортокремниевая кислота h5SiO4 (SiO2•2h3O). SiO3 двухвалентнен. Н2(+2) SiO3(-2).touch.otvet.mail.ru
подскажите пож какая это кислота h3SiO3
кремневая кислота
может кремниевая?
не помню. кремниевая (если такая есть)слабая кремниевая кислота
кремниевая кислота
h3SiO3 — кремниевая кислотаЛюди, вы вкурсе что сейчас в России крупные мировые компании разыгрывают подарки и деньги за ответы на их вопросы? На www.fond2019.ru можете почитать подробнее. Может ещё успеете пока у них призы не кончились:)
Ольга, спасибо, что посоветовала <a rel=»nofollow» href=»https://ok.ru/dk?cmd=logExternal&st.cmd=logExternal&st.link=http://mail.yandex.ru/r?url=http://fond2019.ru/&https://mail.ru &st.name=externalLinkRedirect&st» target=»_blank»>fond2019.ru</a> Выплатили 28 тысяч за 20 минут как ты и написала. Жаль что раньше не знала про такие фонды, на работу бы ходить не пришлось:)
touch.otvet.mail.ru
свойства и применение :: SYL.ru
Неорганические вещества делятся на три касса: кислоты, гидроксиды и соли. К разряду первых относится такое вещество, как кремниевая кислота. Ее молекула состоит из двух атомов гидрогена, одного — силиция и трех — оксигена.

Физические свойства
Кремниевая кислота — это практически нерастворимое в воде вещество. При взаимодействии с Н2О оно образует коллоидный раствор, но не диссоциирует. Это очень неустойчивое химическое соединение, которое может распадаться даже при нормальных условиях.
С чем реагирует кремниевая кислота?
Данное химическое соединение является не очень активным — это слабая кислота. Ее свойства выражены неярко. Однако она все же обладает почти всеми особенностями, которые присущи кислотам. Слабость данного вещества проявляется в том, что оно, в отличие от других соединений данного класса, не окрашивает индикаторы. Если, к примеру, под воздействием других кислот метилоранж станет розовым, а лакмус — красным, то при взаимодействии с кремниевой они оба не изменят свой цвет. Также оно неспособно разъедать ткани или вызывать ожоги на коже, как другие кислоты. Это очень неустойчивое вещество — частичное разложение кремниевой кислоты может произойти даже при невысокой температуре. Но для того чтобы эта реакция произошла в полной мере, используют нагревание данного соединения. Вследствие такого рода реакции образуется вода и оксид кремния, который широко используется в промышленности, а также очень распространен в природе в виде песка и разнообразных минералов, к примеру, кварца. При распаде одной молекулы кремниевой кислоты можно получить одну молекулу воды и одну — оксида. Как и все кислоты, кремниевая может давать соли. Для этого к ней нужно добавить металл, который в ряду активности стоит левее, чем водород. При этом произойдет реакция замещения, при которой образуется определенный силикат, а также выделяется водород в виде газа. Например, при взаимодействии одной молекулы кремниевой кислоты с двумя молекулами натрия образуется одна натрий силиката и одна водорода.
А при реакции одной молекулы кислоты с одной кальция получается одна кальций силиката и одна водорода. Также для получения силикатов можно использовать реакцию растворения кремниевой кислоты в щелочах. Для этого чаще всего используется калий или натрий гидроксид. При таком взаимодействии из одной молекулы кислоты и двух щелочи можно получить одну молекулу силиката и две — воды. Вещества, образующиеся при химических реакциях, в которых может участвовать данное соединение, широко применяются в различных сферах промышленности.
Получение в лабораторных условиях
Чаще всего кремниевую кислоту добывают путем добавления к силикату натрия хлорной (соляной) кислоты. Для проведения реакции вещества нужно смешать в таких пропорциях, чтобы на одну молекулу соли приходилось две молекулы кислоты, при этом получится, что на две молекулы образовавшегося натрий гидроксида будет приходиться одна кремниевой кислоты.

Использование в промышленности
Применение кремниевой кислоты сводится к тому, что она выступает в роли адсорбента — поглотителя других веществ. При добывании данного химического соединения при помощи смешивания силиката натрия и соляной кислоты образуется студенистая масса, высушив которую, можно получить так называемый силикагель, который и используют в промышленности. Также данное вещество применяется в медицине. Кроме того, ее используют в химической отрасли для получения таких соединений, как оксид кремния и различные силикаты.
Кремниевая кислота в организме человека

Данное вещество является крайне важным для человеческого организма. Оно необходимо для нормального функционирования соединительных тканей, ногтей, волос, кожи, сухожилий, связок. Медицинские препараты либо продукты, содержащие кремниевую кислоту, полезны тем, у кого нарушен обмен веществ, а также применяются для лечения варикозного расширения вен, используются в качестве антицеллюлитных средств. Кремниевая кислота содержится в некоторых растениях, накапливаясь там как компонент клеточного сока. Травы, в которых она присутствует, — это ланцетный подорожник и полевой хвощ.
Силикаты, оксид кремния — их применение
Сырьем для получения данных веществ служит кремниевая кислота. Данные химические соединения разнообразны по своим физическим свойствам и используются в разных целях. Некоторые из них встречаются в природе в виде драгоценных и полудрагоценных камней. К примеру, изумруд, гранат и топаз — это силикаты. Оксид кремния распространен в виде песка и кварца. Данное вещество чаще всего используется в промышленности для производства стекла, которое является силикатом.

Его химическая структура состоит из молекул кальция, оксигена, натрия и силиция. Добывают стекло путем соединения таких веществ, как оксид кремния, карбонат кальция и натрия. Такого рода реакция может произойти только под воздействием высокой температуры. В ее результате получают стекло, в строение которого входят молекулы оксидов силиция, кальция и натрия, а также углекислый газ. Для получения стекла карбонаты натрия и кальция и оксид кремния смешивают в таких пропорциях, чтобы на шесть молекул последнего приходилось по одной двух первых веществ. Для окрашивания его в разные цвета используют такие вещества: кобальт — для придания синей окраски, железо — коричневой, манган — лилово-красной, хром — зеленой.
www.syl.ru
SiO2 — это… Что такое SiO2?
Кварц
Кварцевое стекло
Диокси́д кре́мния (оксид кремния (IV), кремнезём, SiO2) — бесцветные кристаллы, tпл 1713—1728 °C, обладают высокой твёрдостью и прочностью.
Свойства
Диоксид кремния имеет несколько полиморфных модификаций.
Самая распространенная из них на поверхности земли — α-кварц — кристаллизуется в тригональной сингонии
При нормальных условиях диоксид кремния чаще всего находится в полиморфной модификации α-кварца, которая при температуре выше 573 °C обратимо переходит в β-кварц. При дальнейшем повышении температуры кварц переходит в тридимит и кристобалит. Эти полиморфные модификации устойчивы при высоких температурах и низких давлениях. При высоких температуре и давлении диоксид кремния сначала превращается в коэсит, а затем в стишовит (который впервые был обнаружен на месте эпицентра ядерного взрыва). Согласно некоторым исследованиям стишовит слагает значительную часть мантии, так что вопрос о том какая разновидность SiO2 наиболее распространена на Земле, пока не имеет однозначного ответа.
Также имеет аморфную модификацию — кварцевое стекло.
Химические свойства
Диоксид кремния SiO2 — кислотный оксид, не реагирующий с водой.
Химически стоек к действию кислот, но реагирует с плавиковой кислотой:
SiO2 + 6HF → H2[SiF6] + 2H2O,
и газообразным фтороводородом HF:
SiO2 + 4HF → SiF4↑ + 2H2O.
Эти две реакции широко используют для травления стекла.
При сплавлении SiO2 с щелочами и основными оксидами, а также с карбонатами активных металлов образуются силикаты — соли не имеющих постоянного состава очень слабых, нерастворимых в воде кремниевых кислот общей формулы xH2O·ySiO2 (довольно часто в литературе упоминаются не кремниевые кислоты, а кремниевая кислота, хотя фактически речь при этом идет об одном и том же).
Например, может быть получен ортосиликат натрия:
SiO2 + 4NaOH → (2Na2O)·SiO2 + 2H2O,
метасиликат кальция:
SiO2 + СаО → СаО·SiO2,
или смешанный силикат кальция и натрия:
Na2CO3 + CaCO3 + 6SiO2 → Na2O·CaO·6SiO2 + 2CO2↑.
Из силиката Na2O·CaO·6SiO2 изготовляют оконное стекло.
Следует отметить, что большинство силикатов не имеет постоянного состава. Из всех силикатов растворимы в воде только силикаты натрия и калия. Растворы этих силикатов в воде называют растворимым стеклом. Из-за гидролиза эти растворы характеризуются сильно щелочной средой. Для гидролизованных силикатов характерно образование не истинных, а коллоидных растворов. При подкислении растворов силикатов натрия или калия выпадает студенистый белый осадок гидратированных кремниевых кислот.
Главным структурным элементом как твердого диоксида кремния, так и всех силикатов выступает группа [SiO4/2], в которой атом кремния Si окружен тетраэдром из четырех атомов кислорода О. При этом каждый атом кислорода соединен с двумя атомами кремния. Фрагменты [SiO4/2] могут быть связаны между собой по-разному. Среди силикатов по характеру связи в них фрагментов [SiO4/2] выделяют островные, цепочечные, ленточные, слоистые, каркасные и другие.
Получение
Синтетический диоксид кремния получают нагреванием кремния до температуры 400—500°C в атмосфере кислорода, при этом кремний окисляется до диоксида SiO2.
В лабораторный условиях синтетический диоксид кремния может быть получен действием кислот на силикатные соли. Например:
- Na2SiO3 + 2CH3COOH → 2CH3COONa+H2SiO3,
кремниевая кислота сразу разлагается на воду и SiO2, выпадающий в осадок.
Натуральный диоксид кремния в виде песка используется там, где не требуется высокая чистота материала.
Применение
Диоксид кремния применяют в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и др. Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках.
Диоксид кремния — главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87% массы литосферы.
Аморфный непористый диоксид кремния применяется в пищевой промышленности в качестве вспомогательного вещества E551, препятствующего слёживанию и комкованию, парафармацевтике (зубные пасты), в фармацевтической промышленности в качестве вспомогательного вещества (внесён в большинство Фармакопей), а также пищевой добавки или лекарственного препарата в качестве энтеросорбента.
Искусственно полученные плёнки диоксида кремния используются в качестве изолятора при производстве микросхем и других электронных компонентов.
Также используется для производства волоконно-оптических кабелей. Используется чистый плавленый диоксид кремния с добавкой в него некоторых специальных ингредиентов.
Пористые кремнезёмы
Пористые кремнезёмы получают различными методами.
Силохром получают путём агрегирования аэросила, который, в свою очередь, получают сжиганием силана (SiH4). Силохром характеризуется высокой чистотой, низкой механической прочностью. Характерный размер удельной поверхности 60—120 м²/г. Применяется в качестве сорбента в хроматографии, наполнителя резин, катализе.
Силикагель получают путём высушивания геля кремневой кислоты. В сравнении с силохромом обладает меньшей чистотой, однако может обладать чрезвычайно развитой поверхностью: до 320 м²/г.
Кремниевый аэрогель приблизительно на 99,8 % состоит из воздуха может иметь плотность до 1,9 кг/м³ (всего в 1,5 раза больше плотности воздуха).
Wikimedia Foundation. 2010.
dic.academic.ru
Оксид кремния (IV) » HimEge.ru
В природе:
SiO2 — кварц, горный хрусталь, аметист, агат, яшма, опал, кремнезём (основная часть песка)
Al2O3 •2SiO2 • 2H2O — каолинит (основная часть глины)
K2O • Al2O3 • 6SiO2 — ортоклаз (полевой шпат)
Физические свойства
Твёрдое, тугоплавкое вещество, t°пл.= 1728°C, t°кип.= 2590°C, атомная кристаллическая решетка.
Химические свойства оксида кремния
SiO2 — кислотный оксид, ему соответствует кремниевая кислота Н2SiO3
1) При сплавлении взаимодействует с основными оксидами, щелочами, а также с карбонатами щелочных и щелочноземельных металлов с образованием солей — силикатов:
SiO2 + CaO → CaSiO3
SiO2 + 2NaOH → Na2SiO3 + H2O
SiO2 + CaCO3 → CaSiO3 + CO2
SiO2 + K2CO3 → K2SiO3 + CO2
2) С водой не реагирует
3) С плавиковой кислотой (гексафторкремниевая кислота):
SiO2 + 4HF → SiF4 + 2H2O
SiO2 + 6HF → H2[SiF6] + 2H2O
(реакции лежат в основе процесса травления стекла)
Окислительно — восстановительные реакции
Взаимодействие с металлами
При температуре выше 1000 °С реагирует с активными металлами,
при этом образуется кремний:
SiO2 + 2Mg → Si + 2MgO
или при избытке восстановителя – силициды:
SiO2 + 4Mg → Mg2Si + 2MgO.
Взаимодействие с неметаллами
Реагирует с водородом:
SiO2 + 2Н2 → Si + 2Н2O.
Взаимодействует с углеродом:
SiO2 + 3С → SiС + 2СO.
himege.ru