Соли — Википедия
Со́ли — сложные вещества, состоящие из катионов металлов и анионов кислотных остатков. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов[1]. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды[2].
Кроме катионов металлов, в солях могут находиться катионы аммония NH4+, фосфония PH4+ и их органические производные, а также комплексные катионы и т. д. Анионами в солях выступают анионы кислотного остатка различных кислот Брёнстеда — как неорганических, так и органических, включая карбанионы и комплексные анионы[3].
М. В. Ломоносов в своих Трудах по химии и физике так описывал понятие «соль»[4][5]:
Названием солей обозначают хрупкие тела, которые растворяются в воде, причем она остается прозрачной; они не загораются, если в чистом виде подвергаются действию огня. Их виды: купорос и все другие металлические соли, квасцы, бура, винный камень, существенные соли растений, соль винного камня и поташ, летучая мочевая соль, селитра, обыкновенная соль родниковая, морская и каменная, нашатырь, английская соль и другие соли, полученные в результате химических работ.
Если рассматривать соли как продукты замены катионов в кислотах или гидроксогрупп в основаниях, то можно выделить следующие типы солей[3]:
- Средние (нормальные) соли — продукты замещения всех катионов водорода в молекулах кислоты на катионы металла (Na2CO3, K3PO4).
- Кислые соли — продукты частичного замещения катионов водорода в кислотах на катионы металла (NaHCO3, K2HPO4). Они образуются при нейтрализации основания избытком кислоты (то есть в условиях недостатка основания или избытка кислоты).
- Осно́вные соли — продукты неполного замещения гидроксогрупп основания (OH —) кислотными остатками ((CuOH)2CO3). Они образуются в условиях избытка основания или недостатка кислоты.
- Комплексные соли (Na2[Zn(OH)4])
По числу присутствующих в структуре катионов и анионов выделяют следующие типы солей[6]:
- Простые соли — соли, состоящие из одного вида катионов и одного вида анионов (NaCl)
- Двойные соли — соли, содержащие два различных катиона (KAl(SO4)2·12 H2O).
- Смешанные соли — соли, в составе которых присутствует два различных аниона (Ca(OCl)Cl).
Также различают гидратные соли (кристаллогидраты), в состав которых входят молекулы кристаллизационной воды, например, Na2SO4·10 H2O, и комплексные соли, содержащие комплексный катион или комплексный анион (K4[Fe(CN)6], [Cu(NH3)
Номенклатура солей кислородсодержащих кислот[править | править код]
Названия солей, как правило, связаны с названиями соответствующих кислот. Поскольку многие кислоты в русском языке носят тривиальные, или традиционные, названия, подобные названия (нитраты, фосфаты, карбонаты и др.) также сохраняются и для солей[8].
Традиционные названия солей состоят из названий анионов в именительном падеже и названий катионов в родительном падеже[9]. Названия анионов строятся на основе русских или латинских названий кислотообразующих элементов. Если кислотообразующий элемент может иметь одну степень окисления, то к его названию добавляют суффикс —ат:
- CO32- — карбонат,
- GeO32- — германат.
Если кислотообразующий элемент может принимать две степени окисления, то для аниона, образованного этим элементом в более высокой степени окисления, применяют суффикс — ат, а для аниона с элементом в меньшей степени окисления — суффикс —ит:
- SO42- — сульфат,
- SO32- — сульфит.
Если элемент может принимать три степени окисления, то для высшей, средней и низшей степени окисления используют соответственно суффиксы —ат, —ит и суффикс —ит с приставкой гипо-:
- NO3— — нитрат,
- NO2— — нитрит,
- NO22- — гипонитрит.
Наконец, в случае элементов, принимающих четыре степени окисления, для высшей степени окисления применяют приставку пер— и суффикс —ат, далее (в порядке понижения степени окисления) суффикс —ат, суффикс —ит и суффикс —ит с приставкой гипо-:
- ClO4— — перхлорат,
- ClO3— — хлорат,
- ClO2— — хлорит,
- ClO— — гипохлорит[10].
Приставки мета-, орто-, поли-, ди-, три-, пероксо— и т. п., традиционно присутствующие в названиях кислот, сохраняются также и в названиях анионов[9].
Названия катионов соответствуют названиям элементов, от которых они образованы: при необходимости указывается число атомов в катионе (катион диртути(2+) Hg22+, катион тетрамышьяка(2+) As42+) и степень окисления атома, если она переменная[11].
Названия кислых солей образуются путём добавления приставки гидро— к названию аниона. Если на один анион приходится больше одного атома водорода, то его количество указывают при помощи умножающей приставки (NaHCO3 — гидрокарбонат натрия, NaH2PO4 — дигидрофосфат натрия). Аналогично, для образования названий основных солей используются приставки гидроксо— ((FeOH)NO3 — гидроксонитрат железа(II))[12].
Кристаллогидратам дают названия, добавляя слово гидрат к традиционному или систематическому названию соли (Pb(BrO3)2·H2O — гидрат бромата свинца(II), Na2CO3·10 H2O — декагидрат карбоната натрия). Если известна структура кристаллогидрата, то может применяться номенклатура комплексных соединений ([Be(H2O)4]SO4 — сульфат тетрааквабериллия(II))[13].
Для некоторых классов солей существуют групповые названия, например, квасцы — для двойных сульфатов общего вида MIMIII(SO4)2·12 H2O, где MI — катионы натрия, калия, рубидия, цезия, таллия или аммония, а MIII — катионы алюминия, галлия, индия, таллия, титана, ванадия, хрома, марганца, железа, кобальта, родия или иридия
Для более сложных или редких солей применяются систематические названия, образующиеся по правилам номенклатуры комплексных соединений[8]. Согласно данной номенклатуре, соль подразделяется на внешнюю и внутреннюю сферы (катион и анион): последняя состоит из центрального атома и лигандов — атомов, связанных с центральным атомом. Название соли формируют следующим образом. Вначале записывают название внутренней сферы (аниона) в именительном падеже, состоящее из названий лигандов (приставок) и центрального элемента (корня) с суффиксом —ат и указанием его степени окисления. Затем к названию добавляют названия атомов внешней сферы (катионов) в родительном падеже[15].
- LiBO3 — триоксоборат(III) лития
- Na2Cr2O7 — гептаоксодихромат(VI) натрия
- NaHSO4 — тетраоксосульфат(VI) водорода-натрия
Номенклатура солей бескислородных кислот[править | править код]
Для образования названий солей бескислородных кислот пользуются общими правилами составления названий бинарных соединений: применяются либо универсальные номенклатурные правила с указанием числовых приставок, либо способ Штока с указанием степени окисления, причём второй способ является предпочтительным.
Названия галогенидов составляются из названия галогена с суффиксом —ид и катиона (NaBr — бромид натрия, SF6 — фторид серы(VI), или гексафторид серы, Nb6I11 — ундекаиодид гексаниобия). Кроме того, существует класс псевдогалогенидов — солей, которые содержат анионы с галогенидоподобными свойствами. Их названия образуются подобным образом (Fe(CN)2 — цианид железа(II), AgNCS — тиоцианат серебра(I))[16].
Халькогениды, содержащие в качестве аниона серу, селен и теллур, называют сульфидами, селенидами и теллуридами. Сероводород и селеноводород могут образовывать кислые соли, которые называют гидросульфидами и гидроселенидами соответственно (ZnS — сульфид цинка, SiS
Физические свойства и строение солей[править | править код]
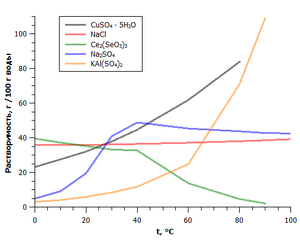 Зависимость растворимости некоторых солей от температуры
Зависимость растворимости некоторых солей от температурыКак правило, соли представляют собой кристаллические вещества с ионной кристаллической решёткой. Например, кристаллы галогенидов щелочных и щёлочноземельных металлов (NaCl, CsCl, CaF2) построены из анионов, расположенных по принципу плотнейшей шаровой упаковки, и катионов, занимающих пустоты в этой упаковке. Ионные кристаллы солей могут быть построены также из кислотных остатков, объединённых в бесконечные анионные фрагменты и трёхмерные каркасы с катионами в полостях (силикаты). Подобное строение соответствующим образом отражается на их физических свойствах: они имеют высокие температуры плавления, в твёрдом состоянии являются диэлектриками [18].
Известны также соли молекулярного (ковалентного) строения (например, хлорид алюминия AlCl3). У многих солей характер химических связей является промежуточным между ионным и ковалентным[7].
Особый интерес представляют ионные жидкости — соли с температурой плавления ниже 100 °С. Кроме аномальной температуры плавления ионные жидкости имеют практически нулевое давление насыщенного пара и высокую вязкость. Особые свойства этих солей объясняются низкой симметрией катиона, слабым взаимодействием между ионами и хорошим распределением заряда катиона[19].
Важным свойством солей является их растворимость в воде. По данному критерию выделяют растворимые, мало растворимые и нерастворимые соли.
Многие минералы — соли, образующие залежи (например, галит NaCl{\displaystyle {\mathsf {NaCl}}}, сильвин KCl{\displaystyle {\mathsf {KCl}}}, флюорит CaF2{\displaystyle {\mathsf {CaF_{2}}}}).
Существуют различные методы получения солей:
h3SO4+Mg⟶MgSO4+h3↑{\displaystyle {\mathsf {H_{2}SO_{4}+Mg\longrightarrow MgSO_{4}+H_{2}\uparrow }}}
h3SO4+MgO⟶MgSO4+h3O{\displaystyle {\mathsf {H_{2}SO_{4}+MgO\longrightarrow MgSO_{4}+H_{2}O}}}
3h3SO4+Al2O3⟶Al2(SO4)3+3 h3O{\displaystyle {\mathsf {3H_{2}SO_{4}+Al_{2}O_{3}\longrightarrow Al_{2}(SO_{4})_{3}+3\ H_{2}O}}}
Ca(OH)2+CO2⟶CaCO3↓+h3O{\displaystyle {\mathsf {Ca(OH)_{2}+CO_{2}\longrightarrow CaCO_{3}\downarrow +H_{2}O}}}
CaO+SiO2⟶CaSiO3{\displaystyle {\mathsf {CaO+SiO_{2}\longrightarrow CaSiO_{3}}}}
Al2O3+3 SO3⟶Al2(SO4)3{\displaystyle {\mathsf {Al_{2}O_{3}+3\ SO_{3}\longrightarrow Al_{2}(SO_{4})_{3}}}}
Mg(OH)2+CO2⟶MgCO3↓+h3O{\displaystyle {\mathsf {Mg(OH)_{2}+CO_{2}\longrightarrow MgCO_{3}\downarrow +H_{2}O}}}
Zn(OH)2+SO3⟶ZnSO4+h3O{\displaystyle {\mathsf {Zn(OH)_{2}+SO_{3}\longrightarrow ZnSO_{4}+H_{2}O}}}
- Взаимодействие солей c кислотами, другими солями (если образуется выходящий из сферы реакции продукт):
CaCO3+2HCl⟶CaCl2+h3O+CO2↑{\displaystyle {\mathsf {CaCO_{3}+2HCl\longrightarrow CaCl_{2}+H_{2}O+CO_{2}\uparrow }}}
CuCl2+Na2S⟶2NaCl+CuS↓{\displaystyle {\mathsf {CuCl_{2}+Na_{2}S\longrightarrow 2NaCl+CuS\downarrow }}}
2Na2CO3+2MgCl2+h3O⟶[Mg(OH)]2CO3+CO2↑+4NaCl{\displaystyle {\mathsf {2Na_{2}CO_{3}+2MgCl_{2}+H_{2}O\longrightarrow [Mg(OH)]_{2}CO_{3}+CO_{2}\uparrow +4NaCl}}}
- Взаимодействие простых веществ:
Fe+S⟶FeS{\displaystyle {\mathsf {Fe+S\longrightarrow FeS}}}
Ca(OH)2+Cl2⟶Ca(OCl)Cl+h3O{\displaystyle {\mathsf {Ca(OH)_{2}+Cl_{2}\longrightarrow Ca(OCl)Cl+H_{2}O}}}
Кристаллогидраты обычно получают при кристаллизации соли из водных растворов, однако известны также кристаллосольваты солей, выпадающие из неводных растворителей (например, CaBr2·3 C2H5OH)
История соли от древности до наших дней
Люди настолько привыкли к соли, что есть ощущение, будто она была на столах всегда. О ней известно то, что этот продукт помогает сохранить продукты, в том числе мясо, более долгое время, и этим с успехом пользовались древние люди, чтобы обеспечить пропитание на зимний период времени. Кроме того, соль — природный усилитель вкуса и аромата блюд. Но что такое соль, как и где она появилась, какие таит в себе загадки?
Что говорят геологи?
Существует мнение, что соль имеет океаническое происхождение.Геология еще не сформировалась как наука, а жаркие споры о происхождении соли уже велись многие годы. По мнению Рене Декарта (17 век), механизм происхождения этого минерала заключается в проникновении сквозь трещины в поверхности земли воды океана, которая со временем превращается в соль. Позднее в научном мире геологов произошел раскол, часть ученых стали нептунистами, а другие — плутонистами.
Первая группа придерживалась мнения, что все коренные породы, и соль в том числе, имеют океаническое происхождение. Вторая группа считала, что эти вещества имеют вулканическое происхождение. Когда люди овладели технологией глубинного бурения, выяснилось, что соль попадается практически повсеместно. Это обстоятельство натолкнуло известного ученого-геолога В. Строганова на мысль объединить обе теории для получения правдоподобной картины. Согласно его версии, энергия, которая необходима для выпаривания океанской воды, появлялась в результате тектонических процессов. Таким образом, время возникновения всех солеродных бассейнов совпадает с моментом образования гор.
Историческая роль соли
Соленый Праокеан — место рождения всего живого на планете, поэтому человек неразрывно связан с солью. В определенные исторические моменты соль имела такую ценность, что служила денежной единицей. Повышение налогообложения на этот продукт приводило к соляным бунтам.
Эти белые кристаллы стали частью народного эпоса, поэтому имеется большое количество различных легенд и сказок, связанных с солью. Само слово получило иносказательное значение и вошло в специфический лексикон представителей различных профессий.
Отношение к соли у наших предков выражается даже в том, на каком расстоянии были рассажены гости от ладьи, в которой она находится. Знатные гости на царских пирах усаживались так, чтобы они возвышались над этим предметом, а остальные — в соответствии с рангом, ниже его.
В рацион не только людей, но и животных, а также растений обязательно должна входить поваренная соль. Этот минерал широко используется как наиболее распространенный консервант.
Попытки разобраться, когда человечество познакомилось с солью и стало приправлять ею пищу, ученые оставили, так как история уходит далеко вглубь веков. Например, египетские рабы не только трудились при строительстве величественных пирамид, но и занимались выпариванием из морской воды соли.
Известен труд китайских ученых, касающийся фармакологии под названием «Пень-Цао-Кан-Му», который датируется 2700 г. до н.э. Показателен тот факт, что в нем представлено более сорока видов соли. Кроме этого трактат описывает и методы ее получения, коих насчитывается несколько сотен. По объему эта информация занимает большую часть книги.
Китайцы одни из первых правильно оценили важность этого продукта, и также в числе первых придумали пополнять государственный бюджет за счет введения налога на соль. Многие правители в разных странах поступали точно также, не зная об опыте своих китайских коллег.
Исторические уроки римских правителей
В Древнем Риме не утруждали себя поиском сложных путей получения продукта, а поступали предельно просто. Производство ее заключалось в сборе концентрированного раствора соли в его естественных источниках и последующем выпаривании с помощью огня.
Соляная дорога — одна из первых дорог, имела стратегическое значение и была сооружена для транспортировки результата деятельности солеваров по Апеннинскому полуострову. Продажа соли в Римской Империи происходила в соответствии с законами рынка, но полностью этот процесс на самотек не отпускался. При необходимости власти влияли на ценообразование.
Правители нередко заигрывали со своими гражданами и делали своеобразные подарки, например, уменьшали цены на соль. В качестве примера можно привести поступок императора Августа перед решающим боем против Антония и Клеопатры. Он поступил мудро и раздал людям большое количество соли и оливкового масла, что и привело к победе.
Ведение войны — дорогое удовольствие в любые времена. В период ведения Пунических войн Рим остро нуждался в средствах, и ему приходилось манипулировать ценами так, чтобы и казна не была пустой, и люди не роптали. Было решено сделать цену на соль в столице минимальной, а по мере удаления от солеварен ее цена пропорционально возрастала.
Как мы уже отмечали, в соли нуждаются и люди, и животные, поэтому определенную порцию ее обязательно получали и солдаты, и их лошади. От латинского наименования этого рациона пошло английское слово, означающее жалование, а во французском языке появилось слово «платить». От этих слов произошло понятие soldier — солдат. Кроме этого, слово «салат» пошло от латинского salad, что означает соленый, так как римские кулинары обязательно солили овощи перед подачей.
Кристаллы ценного минерала были обязательным атрибутом стола. У простых граждан римской империи использовалась в качестве посуды для соли морская раковина, а патриции могли себе позволить красивую солонку, выполненную из серебра. Соль служила символом дружбы, поэтому, если ее не было на столе во время трапезы, то это означало неприязненные отношение к гостю.
Торговля и соль
Производством соли занимались в Венеции, начиная с 9 века, однако размер ее был небольшой, поэтому более крупную завозили из других мест. Город на воде постоянно подвержен атакам морской стихии, но в 12 столетии произошло наводнение такой силы, что половина солеварен была уничтожена водой и доля импорта увеличилась.
Именно такие неблагоприятные обстоятельства натолкнули венецианцев на мысль, что проще и выгоднее скупать соль и перепродавать ее, чем самим заниматься производством. Венецианские купцы значительно обогатились на этом предприятии и расширили его, скупая прочие товары. В результате Венеция стала торговым центром, через который шли все поставки на Европейский континент. В объеме всего товарооборота соль составляла порядка 30-50%.
Влияние Венеции постепенно увеличивалось, и практически весь рынок соли находился в ее руках. Экспансия купцов продвигалась по Средиземноморскому побережью, что привело к скупке запасов соли и по возможности приобретались и сами производства в Северной Африке и Крыму. Процветание Венеции, строительство сложных гидротехнических сооружений и величественных зданий стало возможно именно благодаря торговле солью. Можно сказать, что город построен не на воде, а на соли.
Опора короны
Матиасом Шлайденом, ученым из Германии, в 19 веке было сделано предположение, что между налогообложением и тиранией существует прямая связь. Бюджет древних цивилизаций Греции и Рима не строился на взимании налогов с соли, а при монархиях наблюдается обратная картина.
Налог на соль был опорой благосостояния монархов в Британии. Множество подданных в этой стране поплатились свободой за нежелание платить эту подать.
Во Франции габель (соляной налог) сначала имел незначительный размер. Однако расточительность монархов и постоянные войны были верной дорогой к финансовому кризису, поэтому прибегали к проверенному способу поправить положение дел — увеличивали габель. Среди всех французских правителей династия Валуа — выдающаяся, так как налог на соль был практически единственным источником пополнения казны. Был издан закон, согласно которому предписывалось всем французам по достижении восьмилетнего возраста приобретать каждый год 7 кг соли по государственным ценам. Такое количество соли израсходовать было очень сложно, даже при значительных объемах засолки продуктов впрок.
Терпение у французского народа иногда заканчивалось, что выливалось в бунты. Один из них поднял более сорока тысяч недовольных крестьян в юго-восточных провинциях, причем они не были против короля, а выступали за снижение габеля. Масштаб протеста привел властителей в ужас, и им пришлось отступить.
По статистике 18 столетия, тысячи французов, среди которых были дети и женщины, заключались под стражу или были казнены за неуплату габеля. Только после победы французской революции ненавистный налог был отменен.
Но с приходом к власти Наполеона Бонапарта Франция постоянно вела войны, поэтому потребовались дополнительные средства. Источником их, как нетрудно догадаться, стал габель, который шел на нужды армии. Однако соли удалось отомстить новоявленному императору и его солдатам. При отступлении в 1812 году из России огромное количество раненых французов погибали, так как недостаток соли в их организме стал причиной плохой заживляемости ран.
Соль правит миром
В Новом Свете опорой властей было солеварение. Работал тот же принцип удержания власти, что и в Старом Свете: кто контролирует производство соли, тот имеет колоссальное влияние на людей. Такая формула работала и до начала колонизации континента, и после этого. Ярким примером может служить захват городка под названием Солтвилль, который поставлял соль для Южан. После того, как поставки соли в армию Гранта прекратились, исход противостояния был предрешен.
Все города и поселения в обеих Америках возникали в местах, которые имели доступ к соли. Вблизи Куско находились источники к стратегическому продукту. На территории нынешней Колумбии аборигены-кочевники устраивали поселения рядом с природными солонцами. Племя чичба, обитавшее в высокогорных районах, смогло достичь господствующего положения за счет незаурядного умения варить соль.
У ацтеков не было собственных источников соли, поэтому в критических случаях им приходилось добывать соль, выпаривая ее из своей мочи. Племенам, обитавшим на территории Гондураса, было проще, так как у них был доступ к океану. Для получения соли их технология получения соли заключалась в погружении горячих палок в волны прибоя и дальнейшего удаления с них кристаллов вещества.
Соль всегда была гордостью тех стран, у которых наблюдался ее избыток. Например, в Боливии, в месте, где происходит добыча этого продукта, возведен отель, материалом которого служит соль.
Если перенестись в Европу, то и здесь имеются отголоски прошлого величия солеваров. Например, Зальцбург в буквальном переводе означает город соли.
Полезное видео по теме
Битва за соль: документальный фильм об этом продукте.
https://www.youtube.com/watch?v=im3O0vrQmrQ
ОТКУДА ВЗЯЛАСЬ КАМЕННАЯ СОЛЬ? | Наука и жизнь
Принципиально новая концепция появления на Земле каменной соли выдвинута кандидатом геолого-минералогических наук В. Строгановым.
Автор отвергает общепринятое представление о том, что все известные на Земле запасы соли (24х1015 тонн) могли образоваться в результате выпаривания ее из Мирового океана. Ведь это означало бы, что Мировому океану за время его существования приходилось неоднократно и весьма основательно опресняться, тогда как соленость его, по геологическим данным, всегда оставалась стабильной.
Между тем для накопления солей в одном только Прикаспийском соленосном бассейне пришлось бы выпарить за относительно короткий срок воду в количестве, содержащемся в Северном Ледовитом океане, и притом исключительно за счет тепла солнечного излучения. Автор находит это предположение неправдоподобным.
Существует, впрочем, и еще одна - менее распространенная — гипотеза происхождения соли: ее могло образовать соединение вынесенных из далеких земных глубин хлора и натрия. При этом якобы образовывались лиманы и соленые озера, из которых затем соль выпаривалась под действием того же солнечного излучения. Тем самым предполагается, что во времена эпохи интенсивного накопления соли климат на Земле был чрезвычайно жарким и сухим, тогда как палеоклиматология такое допущение отрицает. Напротив, установлено, что 70 % всех мировых запасов соли образовалось в те времена, когда климат на Земле был умеренно теплым.
Автор опубликованной статьи полагает, что необходимое для выпаривания соли тепло было тектонического происхождения, и основывает свое предположение на том, что все солеродные бассейны образовались во время или после формирования близлежащих гор, когда на поверхность земли изливалась магма и действовали геотермальные источники.
Аналогичным образом объясняет он появление месторождений каменного угля (бурого или антрацита — в зависимости от окружающей температуры), а также сланцев и нефти, утверждая, что не случайно все эти месторождения, как правило, располагаются неподалеку одно от другого. А насколько реалистична эта гипотеза, покажут время и дальнейшие исследования.
Как образуется соль? | Kratkoe.com


Как образуется соль в природе, Вы узнаете из этой статьи.
Как образуется соль?
Жизнь человека неразрывно связана с солью. Даже в некоторые исторические периоды она выступала денежной единицей. Но думали ли Вы над тем, как образовалось это ископаемое в земле, в толще пород? Для этого необходимо обратить внимание на геологическое прошлое нашей планеты.
Земной шар с момента возникновения медленно менял свой внутренний и внешний лик. Миллиарды лет тому назад его окружала непроницаемая густая завеса из водяных паров. Постепенно охлаждаясь, они превращались в облака и выпадали ливнями. Вода заполнила поверхностные впадины, образовав лагуны и моря. В них продолжали вливаться потоки дождя, вода с горных цепей и горячие изверженные воды.
Из горных пород и атмосферы вместе с водой на поверхность попадали химические соединения. Возможно, так соль попала в океан. Когда начался постоянный кругооборот воды на планете, все новые запасы соли попадали в океаны и моря.
Когда на Земле началось распределение океанов и материков на планете, то вследствие медленных колебаний коры, а также горообразовательных процессов в разных местах земля то опускалась (и море заливало сушу), то поднималась, обнажая морское дно. Так соль проникала в земную кору, образовывая там целые пласты. Почва просто пропиталась солью древнего моря.
Подземные давления время от времени сминали земную кору в складки. Горные цепи выпячивались, опускались и провались. В процессе данных смещений на поверхность выходили осадочные породы, отложившиеся на дне древних морей. Вместе с ними выходили залежи каменной соли, а в других местах она оставалась лежать на огромной глубине.
Разное вертикальное давление и пластичность соли способствовали образованию соляных куполов – мощных месторождений этого ископаемого. Она очень пластична и под давлением может течь. Так и зарождаются куполы, достигавшие километры в высоту.
Кроме подземных залежей соль находиться еще в лагунах, соляных озерах и минеральных водах. Пласты солей могут достигать в толщину десятки метров.
Надеемся, что из этой статьи Вы узнали, как в природе образуется соль.