| 1. | Природные и синтетические вещества | 1 вид — рецептивный | лёгкое | 1 Б. | Закрепляются знания о природных и синтетических органических веществах. |
| 2. | Свойства органических веществ | 1 вид — рецептивный | лёгкое | 1 Б. | Закрепляются знания состава, строения и свойств органических соединений. |
| 3. | Формулы органических веществ | 1 вид — рецептивный | лёгкое | 1 Б. | Отрабатывается умение узнавать формулы органических веществ. |
| 4. | Вид формулы | 1 вид — рецептивный | лёгкое | 1 Б. | Закрепляются знания способов изображения органических соединений (молекулярных, структурных и электронных формул. |
| 5. | Массовая доля углерода | 2 вид — интерпретация | среднее | 1 Б. | Закрепляется умение вычислять массовую долю углерода по формуле органического соединения. |
| 6. | Классификация | 2 вид — интерпретация | среднее | 2 Б. | Отрабатываются навыки классификации веществ. |
| 7. | Число электронов | 3 вид — анализ | среднее | 2 Б. | Закрепляются знания электронного строения атомов углерода и водорода, совершенствуется умение определять общее число электронов в молекуле и число электронов, участвующих в образовании ковалентных связей. |
| 8. | Не существуют вещества | 3 вид — анализ | среднее | 3 Б. | Отрабатываются навыки анализа структурных формул веществ и определения по ним валентности атомов. |
| 9. | Определи формулу | 3 вид — анализ | сложное | 3 Б. | Отрабатывается умение устанавливать формулу углеводорода по массовым долям элемента и относительной молекулярной массе вещества. |
Лекция 9 органическая химия
13
Органическая химия изучает органические вещества и их преобразования.
Органические вещества – имеют свои особенности в составе, строении и свойствах.
Состав органических веществ:
1. Качественный состав – из атомов каких элементов состоит вещество
Органические вещества – это соединения атомов Углерода. Кроме атомов Углерода, в органические соединения могут входить атомы Серы, Азота, Кислорода, Фосфора. Эти элементы называются элементами-органогенами (90% состава органических веществ). Атомы других элементов встречаются редко.
Особенности органических веществ:
Атомы Углерода могут соединятся не только с атомами других элементов, но и между собой, образуя углеродные цепи с одинарными или двойными связями.
Атомы Углерода в органических веществах всегда четырехвалентны.
атомы элементов-органогенов небольшие по размерам, поэтому могут образовывать компактные молекулы.
органогены имеют невысокую токсичность.
атомы биогенных элементов могут образовывать макроэргические связи – связи ковалентного типа, при разрыве которых выделяется 25 кДж/моль энергии.
На сегодняшний день известно около 300 тыс. неорганических и 5млн органических веществ.
Количественный состав – отображается общей формулой для каждого класса – количество атомов, входящих в состав молекулы.
Строение органических веществ
Различают строение
— структурное;
— стереохимическое;
— электронное.
Структурное – последовательность связей атомов в молекуле. Отображается с помощью связей в формулах.
Атомы Углерода в органических соединениях могут соединяться между собой, образуя цепи или циклы:
О рганическая
химия
рганическая
химия
Нециклические соединения (цепь) Циклические соединения
СН3-СН2-СН3
карбоциклические гетероциклические
алицикличесике ароматические
одноядерные многоядерные

В органической химии существует понятие «функциональная группа»– группа атомов, по которой соединение проявляет наиболее характерные свойства.
По наличию функциональной группы органические вещества делятся:
І .
УГЛЕВОДОРОДЫ (СхНу)
.
УГЛЕВОДОРОДЫ (СхНу)
Нециклические Циклические
насыщенные ненасыщенные алициклические ароматические
алкены алкины диены насыщенные ненасыщенные
алкены диены
І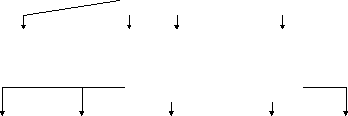 І.КИСЛОРОДСОДЕРЖАЩИЕ
УГЛЕВОДОРОДЫ
І.КИСЛОРОДСОДЕРЖАЩИЕ
УГЛЕВОДОРОДЫ
-оксо- простые эфиры -окси— карбоновые кислоты и их производные
кетоны фенолы хлорангидриды
ІІІ. Азотсодержащие органические соединения
амины нитрилы соли диазония диазосоединения гетероциклы
Органические вещества могут образовывать гомологические ряды– это ряд веществ одного класса, молекулы которых отличаются между собой на одну или несколько гомологических разниц (СН2)
В гомологических рядах происходит закономерное изменение физических свойств. Гомологи имеют одинаковый качественный, но различный количественный состав.
Органические вещества могут образовывать изомеры. Изомеры–это вещества, которые имеют одинаковый количественный и качественный состав, но различное строение.
Структурная изомерия
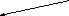

изомерия углеводородного скелета изомерия положения функциональной группы
| 1. |
Природные и синтетические вещества
Сложность: лёгкое |
1 |
| 2. |
Свойства органических веществ
Сложность: лёгкое |
1 |
| 3. |
Формулы органических веществ
Сложность: лёгкое |
1 |
| 4. |
Вид формулы
Сложность: лёгкое |
1 |
| 5. |
Массовая доля углерода
Сложность: среднее |
1 |
| 6. |
Классификация
Сложность: среднее |
2 |
| 7. |
Число электронов
Сложность: среднее |
2 |
| 8. |
Не существуют вещества
Сложность: среднее |
3 |
| 9. |
Определи формулу
Сложность: сложное |
3 |
Химическое строение органических веществ
К созданию теории химического строения органических веществ приложили руки и умы Э.Франкланд, Ф.Кекуле, Ш.Жерар и другие химики. Но особую роль сыграл Александр Михайлович Бутлеров (1828-1886). Он установил, что порядок связи атомов в молекуле играет важнейшую роль в его свойствах и даже предсказании тех веществ, которые еще могут быть открыты.
Эта теория позволила химии стать одной из величайших наук, быстро стать отдельной отраслью и двигателем производства.
Основные идеи теории А.М.Бутлерова:
1. Все атомы в молекуле связываются, согласно их валентностям (химическое строение по Бутлерову).
Строение соединения (геометрическое расположение его атомов) отражается в его структурной формуле.
2. Свойства веществ зависят не только от входящих в него атомов, но и от их порядка соединения.
Это объясняет существование изомеров (от греч. равный + доля) — т.е. два (и более) вещества одинаковые по массе, по атомам, но имеют абсолютно разные свойства.
3. Свойства вещества позволяют определить молекулу, и, наоборот: по молекуле можно определить свойство вещества.
Это открытие позволило (и до сих пор позволяет) создать много новых полезных веществ (лекарств, красителей, пищевых заменителей…).
4. Атомы и группы атомов влияют друг на друга в молекулах.
Редактировать этот урок и/или добавить задание и получать деньги постоянно* Добавить свой урок и/или задания и получать деньги постоянноДобавить новость и получить деньги
Добавить анкету репетитора и получать бесплатно заявки на обучение от учеников
Органическая химия
ЛЕКЦИЯ 1
1. Предмет органической химии.
1. ПРЕДМЕТ ОРГАНИЧЕСКОЙ ХИМИИ
1.1.ПОНЯТИЕ ОБ ОРГАНИЧЕСКОМ ВЕЩЕСТВЕ И ОРГАНИЧЕСКОЙ ХИМИИ.
Органические вещества — класс химических соединений, в состав которых входит углерод
Органические соединения — самый обширный класс химических соединений. Многообразие органических соединений связано с уникальным свойством углерода образовывать цепочки из атомов, что в свою очередь обусловлено высокой стабильностью (то есть энергией) углерод-углеродной связи. Связь углерод-углерод может быть как одинарной, так и кратной — двойной, тройной. При увеличении кратности углерод-углеродной связи возрастает её энергия, то есть стабильность, а длина уменьшается. Высокая валентность углерода — 4, а также возможность образовывать кратные связи, позволяет образовывать структуры различной размерности (линейные, плоские, объёмные).
1.2.ВИТАЛИЗМ И ЕГО КРУШЕНИЕ.
Название органические вещества появилось на ранней стадии развития химии во время господства виталистических воззрений, продолжавших традицию Аристотеля и Плиния Старшего о разделении мира на живое и неживое. Вещества при этом разделялись на минеральные — принадлежащие царству минералов, и органические — принадлежащие царствам животных и растений. Считалось, что для синтеза органических веществ необходима особая «жизненная сила» (лат. vis vitalis), присущая только живому, и поэтому синтез органических веществ из неорганических невозможен.
Витали́зм (от лат. vitalis — «жизненный») — учение о наличии в живых организмах нематериальной сверхъестественной силы, управляющей жизненными явлениями — «жизненной силы» (лат. vis vitalis) («души», «энтелехии», «археи» и проч.).
Это представление было опровергнуто Фридрихом Вёлером в 1828 году путём синтеза «органической» мочевины из «минерального» цианата аммония, однако деление веществ на органические и неорганические сохранилось в химической терминологии и по сей день.
Количество из
План-конспект на тему Первоначальные сведения о строении органических веществ. Основные положения теории строения органических соединений А.М. Бутлерова. Изомерия. Упрощенная классификация органических соединений.
Тема. Первоначальные сведения о строении органических веществ. Основные положения теории строения органических соединений А.М. Бутлерова. Изомерия. Упрощенная классификация органических соединений.
Цели: дать краткую историческую справку о развитии органической химии; формировать понятия о сущности теории химического строения органических веществ, опираясь на знания учащихся об электронном строении атомов элементов, их положении в Периодической системе Д.И. Менделеева, о степени окисления, природе химической связи; ввести понятие изомерия; рассмотреть классификацию органических веществ.
Развивать мыслительные приемы анализа, сравнения, обобщения; тренировать внимание учащихся при восприятии большого по объему материала;
Воспитывать интерес к предмету.
Тип урока: усвоение новых знаний.
Ход урока
Организационный момент
Вступительное слово учителя.
Актуализация опорных знаний
Проходит в виде беседы.
С курса химии 8 класса вам известно, что все вещества делятся на 2 группы. Какие? (органические и неорганические)
Какие органические соединения вам известны? (сахар, спирт, белки, жиры, углеводы и др.).
Где чаще всего встречаются органические вещества? (в животных и растительных организмах)
Изучение нового материала
До начала XIX века все вещества делились по происхождению на минеральные, животные и растительные. Впервые термин «органические вещества» был применен шведским ученым Й. Берцелиусом. Существовали взгляды, что органические вещества возникают только в живых организмах и их невозможно получить искусственно. Ошибочность этого представления была доказана синтезами органических веществ в лабораторных условиях:
1828 г. Ф. Вёлер синтезировал мочевину;
1845 г. А.В.Кольбе получил уксусную кислоту;
1854 г. П.Э.Бертло синтезировал жир;
1861 г.А.М. Бутлеров получил сахаристое вещество.
Оказалось, что резкой границы между органическими и неорганическими веществами не существуют и они могут быть превращены друг в друга.
Обратите внимание на доску, там изображены формулы некоторых органических веществ.
Глицерин
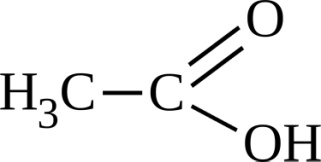
Уксусная кислота

Ацетон

Сахар
На каком основании все эти вещества можно отнести к органическим? Что общего вы заметили в составе этих веществ? (наличие в них атомов углерода, водорода и кислорода).
Можем ли мы уже дать определение органической химии? Что является предметом ее изучения? (варианты учащихся)
Органическая химия – наука об органических веществах, их составе, строении, свойствах и способах применения.
Органические вещества – это соединения углерода.
На 2000 год загеристрировано более 18 млн. органических веществ.
В следствии быстрого развития органическая химия в первые десятилетия XIX века стала самостоятельной наукой. Было открыто и исследовано много новых органических веществ. Среди них были и такие, которые при одинаковом химическом составе и одинаковой молекулярной формуле имели разные свойства. Теории, которые существовали в те времена, не в состоянии были объяснить исследуемые материалы и наблюдения. Отсутствие объединяющей научной теории тормозила развитие органической химии. С этой теоретической безысходности ее вывела теория химического строения органических соединений, создана великим русским ученным О.М.Бутлеровым (1861 г). Эта теория положила научные основы органической химии и объяснила ее важнейшие закономерности.
Основные положения теории А.М.Бутлерова о строении органических соединений:
Все атомы, образующие молекулы органических веществ, связаны в определенной последовательности согласно их валентностям.
Порядок связи атомов называется химическим строением. Атом углерода в органических соединениях проявляет валентность 4, может соединятся друг с другом простыми (С-С) или кратными ковалентными связями – двойными (С=С), тройными (С≡С), образовывать неразветвленные, разветвленные и замкнутые цепи.
СН3 – СН2 – СН2 – СН3 СН3 – СН2– СН3
СН3
Свойства веществ зависят не только от качественного и количественного состава, но и от порядка соединения атомов в молекуле.
До А.М.Бутлерова не могли объяснить, почему одинаковые по составу вещества имеют разные свойства. Так, состав этилового спирта и диметилового эфира выражается одной молекулярной формулой С2Н6О, но свойства их разные: этиловый спирт – жидкость с tкип 78,3 0С, а диметиловый эфир – газ. Правильное объяснение этому явлению, названому изомерией, дает теория О.М.Бутлерова.
Изомеры – вещества с одинаковым составом и одинаковой молекулярной формулой, но с разным строением молекул, что вызывает разные свойства.
Изомеры бутана:
н-бутан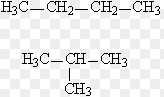
изобутан
По свойствам данного вещества можно определить строение его молекулы, а по строению молекулы предвидеть свойства.
Атомы и группы атомов в молекулах веществ взаимно влияют друг на друга.
Классификацию органических веществ можно представить в виде схемы:
Ациклическими называют соединения с открытой цепью атомов углерода, циклическими – с замкнутой. В гетероциклических соединениях цикл образуют наряду с атомами углерода и атомы других элементов (N, O, S).
Закрепление изученного материала
Проходит в виде беседы.
Что изучает органическая химия?
Перечислите основные положения ТХС органических соединений.
В чем особенность химического строения органических соединений?
Как называются соединения, в которых цепь атомов углерода незамкнутая?
Как называются соединения, в которых цепь атомов углерода замкнутая?
На какие группы делятся ациклические соединения?
На какие группы делятся циклические соединения?
Домашнее задание
§________________
Подведение итогов урока. Рефлексия.
Прием «Незаконченное предложение»
сегодня я узнал…
было интересно…
было трудно…
я понял, что…
я почувствовал, что…
3. Общая характеристика органических соединений
Вещества, в состав которых входят атомы углерода, называются органическими. Многообразие органических веществ обусловлено строением атома углерода и его химическими свойствами, способного образовывать химические связи различного типа между собой и атомами O, N, H. Атомы углерода способны образовывать стабильные цепи и кольца, служащие скелетами макромолекул. Среди органических веществ наибольшее биологическое значение имеют белки, нуклеиновые кислоты, углеводы, жиры и витамины.
Белки – это природные биополимеры, продукты реакции поликонденсации аминокислот. Аминокислота – полифункциональное органическое вещество, имеющее в своем составе две функциональные группы: аминогруппу (–NH2) и карбоксильную группу (–СООН), соединенных с радикалом, также содержащим различные функциональные группы атомов. Природных аминокислот 18-23, их сочетание образует большое количество разновидностей молекул белков. По характеру влияния аминокислот на обмен веществ их разделяют на заменимые и незаменимые. Незаменимые аминокислоты должны обязательно поступать в организм с пищей.
При образовании молекул белков между аминокислотами образуется «пептидная» связь (–C–N–). Белки кроме сложного состава характеризуются и сложным строением белковых молекул. Различают четыре вида структур белковых молекул. Первичная структура – порядок расположения остатков аминокислот в полипептидной цепи. Вторичная структура – пространственное расположение полипептидной цепи (спираль или линейные структуры). Устойчивость молекуле обеспечивается различными химическими связями (водородной, ионной и других видов связи) между отдельными витками спирали. Третичная структура – пространственные расположением спирали, или иной структуры. Четвертичная структура – пространственное расположение субъединиц молекул белка, характерна для сложных белков, например гемоглобина.
Белок в живом веществе по структуре отличается от белка, подвергшегося воздействию, при котором он теряет структуру (четвертичную или третичную структуру белковой молекулы) и свойства живого белка. Неглубокое воздействие называют денатурацией, при которой свойства белка могут восстанавливаться. Одним из видов денатурации является обратимая коагуляция. При необратимой коагуляции нативный белок превращается в «мертвый белок».
По составу различают две группы белков: протеины и протеиды. Протеины – простые белки, молекула образована только белком, например яичный альбумин. Протеиды – сложные белки, молекулы которых состоят из белковой и небелковой составляющих. Протеиды подразделяются на несколько групп, важнейшими из которых являются: гликопротеиды (сложное соединение белка и углевода), липопротеиды (комплекс молекул белка и липидов), нуклеопротеиды (комплекс белков и молекул нуклеиновых кислот).
По форме молекулы среди белков различают две группы: глобулярные и фибриллярные. Молекулы глобулярных белков имеют шарообразную форму, например у яичного альбумина. Такие белки растворимы в воде, способны к образованию коллоидных растворов. Фибриллярные белки имеют молекулы в форме нитей (фибрилл), например, миозин мышц, фиброин шелка. Фибриллярные белки нерастворимы в воде. По растворимости в различных растворителях белки разделяют на водорастворимые и жирорастворимые.
Функции белков в клетке: структурная, реагентная, каталитическая, энергетическая, запасающая. Функции белков в организме: воспринимающая, проводящая, сократительная, трофическая.
Жиры – органические соединения, являющиеся сложными эфирами, образованными остатками высших жирных кислот и спиртов, например глицерина. Липиды – жироподобные вещества. Среди жиров большое значение имеют глицериды – сложные эфиры глицерина и высших жирных кислот. В молекулах жиров могут содержаться одинаковые или разные остатки жирных кислот. Глицериды в своем составе содержащие остатки фосфорной кислоты называют фосфоглицеридами.
По характеру углеводородного радикала жирные кислоты бывают предельными (масляная, пальмитиновая, стеариновая) и непредельными (олеиновая, линолевая, линоленовая). По агрегатному состоянию различают твердые и жидкие жиры. Примером твердого жира является тристеарин, жидкого – триолеин. Жидкие и твердые жиры отличаются по составу: в состав жидких жиров входят остатки непредельных жирных кислот, а в состав твердых – предельных жирных кислот.
Функции жиров в организме: строительная, запасная, запасание воды, терморегуляционная, энергетическая, трофическая, защитная.
Углеводы – это органические вещества, состоящие из углерода, водорода и кислорода, имеющие общую формулу Сn(Н2O)m. Углеводы подразделяют на моносахариды, олигосахариды и полисахариды.
Моносахариды – это углеводы, общая формула которых Сn(Н2О)n. Моносахариды по числу атомов углерода, содержащихся в молекуле, различают на тетрозы, пентозы, гексозы, гептозы. Наибольшее биологическое значение имеют пентозы и гексозы.
Пентозы – это моносахариды, молекула которых содержит 5 атомов углерода. Среди них важное биологическое значение имеют рибоза и дезоксирибоза. Формула рибозы – С5Н10С5. Рибоза входит в состав рибонуклеотидов, структурных единиц рибонуклеиновой кислоты (РНК). Формула дезоксирибозы – С5Н10O4. Дезоксирибоза участвует в образовании дезоксирибонуклеотидов, мономеров дезоксирибонуклеиновой кислоты (ДНК).
Гексозы – это моносахариды, молекулы которых содержат шесть атомов углерода. Общая формула гексоз С6(Н2O)6. Наибольшее значение в природе имеет глюкоза, используемая организмом в качестве универсального питательного вещества и легкодоступного источника энергии.
Дисахариды образуются в резудьтате взаимодействия двух молекул моносахаридов. Важнейшим представителем дисахаридов является сахароза – продукт взаимодействия глюкозы и фруктозы. Ее формула в общем виде C12H22O11. Для человека сахароза является источник глюкозы.
Полисахариды – это природные полимеры, образующиеся в результате взаимодействия большого количества молекул моносахаридов. Полисахариды на основе гексоз имеют общую формулу (С6Н10O5)n. Наиболее важными из полисахаридов являются крахмал, гликоген и целлюлоза (клетчатка).
Крахмал – это полисахарид, продукт реакции поликонденсации глюкозы. Крахмал выступает основным запасным веществом в растительных клетках, у животных и грибов запасным веществом является гликоген.
Молекулы крахмала имеют две разновидности, одна из которых называется амилоза (в этой молекуле нет боковых цепей), а другая – амилопектин, молекулы которых имеют боковые цепи. Гликоген по строению молекул подобен амилопектину. Важнейшим химическим свойством, обусловливающим биолого-экологическую роль крахмала и гликогена, является их способность подвергаться гидролизу с образованием глюкозы. Для животных крахмал – важнейший пищевой продукт.
Целлюлоза (клетчатка) – полисахарид, являющийся продуктом реакции поликонденсации глюкозы. Ее общая формула (С6Н10O5)n. В отличие от крахмала молекулы целлюлозы строго линейны и имеют фибриллярную («нитчатую») структуру. Целлюлоза образует механически прочные нитчатые структуры, обеспечивающие защиту отдельных органоидов клетки и механическую прочность различных растительных тканей.
В природных условиях клетчатка (после отмирания растений) подвергается разложению, в результате которого возможно образование гумуса, нефти, различных видов каменного угля.