Типы кристаллических решеток. Видеоурок. Химия 11 Класс
На уроке будут рассмотрены типы кристаллических решеток, типы агрегатных состояний вещества и твердые тела с кристаллической структурой. Вводится понятие полиморфизма и аллотропии.
В зависимости от давления и температуры, все вещества могут существовать в различных агрегатных состояниях: твердом, жидком, газообразном или в виде плазмы. При низких температурах и высоком давлении все вещества существуют в твёрдом агрегатном состоянии. Твердое и жидкое состояние вещества называют конденсированным.
В твердых телах частицы располагаются компактно, в определенном порядке. В зависимости от степени упорядоченности частиц в твердых телах определяют 2 фазовых состояния: кристаллическое и аморфное. Если частицы располагаются таким образом, что между соседними частицами есть некоторая упорядоченность в расположении, а именно: постоянное расстояние и углы между ними, такое явление называют наличие ближнего порядка в расположении. Рис. а.
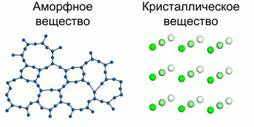
a b
Рис. 1. Наличие ближнего и дальнего порядка в расположении частиц
Если же частицы расположены таким образом, что упорядоченность наблюдается и между ближайшими соседями, и на гораздо больших расстояниях, это называют наличие дальнего порядка. Рис. б.
Аморфное тело (от греч А – не, morfe – форма) – бесформенные вещества. В них существует только ближний порядок и нет дальнего порядка.
Примеры аморфных тел приведены на рис. 2.

Рис. 2. Аморфные тела
Это воск, стекло, пластилин, смола, шоколад.
Свойства аморфных веществ
- Имеют только ближний порядок (как в жидкостях).
- Твердое агрегатное состояние при нормальных условиях.
- Нет четкой температуры плавления. Плавятся в интервале температур.
В кристаллическом теле существует и ближний, и дальний порядок. Если мысленно соединить точки, обозначающие линии, получится пространственный каркас, который называется кристаллической решеткой. Точки, в которых размещены частицы – ионы, атомы или молекулы – называют узлами кристаллической решетки (рис. 3). Частицы не жестко фиксированы в узлах, они могут немного колебаться, не убегая из этих точек. В зависимости от того, какие частицы находятся в узлах кристаллической решетки, выделяют её типы (табл. 1).
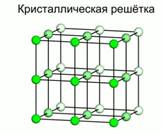
Рис. 3. Кристаллическая решетка
Физические свойства веществ с различными типами кристаллических решеток
Табл.1. Физические свойства веществ
Существует несколько подтипов кристаллических решеток, различающихся расположением атомов в пространстве.
В веществах с атомной, ионной, металлической кристаллической решетками нет молекул – это немолекулярные вещества.Молекулярные вещества – с молекулярной кристаллической решеткой.
Полиморфизм — это явление, при котором сложные вещества одинакового состава имеют разные кристаллические решетки.
Например, пирит и марказит. Их формула – FeS2.Но они и выглядят по-разному, и обладают различными физическими свойствами. Аналогично, различными физическими свойствами обладают минералы состава CaCO3: арагонит, мрамор, исландский шпат, мел.
Явление существования химических элементов в виде нескольких простых веществ называется аллотропией, а вещества – аллотропными модификациями. Это объясняется различным составом вещества или различием в их кристаллической решетке. Кислород и озон – аллотропные модификации химического элемента кислорода. Углерод образует графит, алмаз, фуллерен, карбин. Расположение атомов в их кристаллических решетках разное, и поэтому они проявляют разные свойства. У фосфора аллотропные вещества – красный, белый и черный фосфор. Аллотропия характерна и для металлов. Например, железо может существовать в виде α, β, δ, γ.
Текучесть аморфных веществ
Одним из свойств, по которым отличаются аморфные тела от жидких, является их текучесть. Если положить кусочек смолы на нагретую поверхность, то он постепенно растечется по этой поверхности.
Вязкость – это способность сопротивляться перемещению одних частей тела относительно других для жидкостей и газов: чем она выше, тем сложнее изменить форму тела. Оконные стекла – это типичные аморфные вещества. Теоретически они должны постепенно стекать вниз. Но вязкость стекла высокая, и его деформацией можно пренебречь. Вязкость стекла примерно в 1000 раз выше вязкости смолы. За год деформация стекла составляет 0,001%. За 1000 лет деформация стекла составляет 1%.
Подведение итога урока
На уроке рассмотрены типы кристаллических решеток, типы агрегатных состояний вещества, твердые тела с кристаллической структурой. Введено понятие полиморфизма и аллотропии. Объяснялась зависимость физических и химических свойств от разных типов кристаллических решеток в веществе.
Список литературы
- Рудзитис Г.Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф.Г. Фельдман. – 14-е издание. – М.: Просвещение, 2012.
- Попель П.П. Химия: 11 кл.: учебник для общеобразовательных учебных заведений / П.П. Попель, Л.С. Кривля. – К.: ИЦ «Академия», 2008. – 240 с.: ил.
- Габриелян О.С.Химия. 11 класс. Базовый уровень. 2-е изд., стер. – М.: Дрофа, 2007. – 220 с.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- Interneturok.ru (Источник).
- Hemi.nsu.ru (Источник).
- Chemport.ru (Источник).
- Химик.ру (Источник).
Домашнее задание
- №№ 7, 8, 9 (с. 41) Рудзитис Г.Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г.Е. Рудзитис, Ф.Г. Фельдман. – 14-е издание. – М.: Просвещение, 2012.
- Приведите примеры веществ молекулярного строения.
- Что такое полиморфизм?
interneturok.ru
Кристаллическая решетка
Твердые кристаллы можно представить как трехмерные конструкции, в которых четко повторяется один и тот же элемент структуры во всех направлениях. Геометрически правильная форма кристаллов обусловлена их строго закономерным внутренним строением. Если центры притяжения атомов, ионов или молекул в кристалле изобразить в виде точек, то получим трехмерное регулярное распределение таких точек, которое называется кристаллической решеткой, а сами точки — узлы кристаллической решетки. Определенная внешняя форма кристаллов является следствием их внутренней структуры, которая связана именно с кристаллической решеткой.
Кристаллическая решетка — это воображаемый геометрический образ для анализа строения кристаллов, который представляет собой объемно-пространственную сетчатую структуру, в узлах которой располагаются атомы, ионы или молекулы вещества.
Для характеристики кристаллической решетки используют следующие параметры:
- Энергия кристаллической решетки Екр [КДж / моль] — это энергия, выделяющаяся при образовании 1 моля кристалла из микрочастиц (атомов, молекул, ионов), которые находятся в газообразном состоянии и удалены друг от друга на такое расстояние, что исключается возможность их взаимодействия.
- Константа кристаллической решетки d [A0] — наименьшее расстояние между центрами двух частиц в соседних узлах кристаллической решетки, соединенных химической связью.
- Координационное число — количество ближайших частиц, окружающих в пространстве центральную частицу и сочетаются с ней химической связью.
Основой кристаллической решетки является элементарная ячейка, которая повторяется в кристалле бесконечное количество раз.
Элементарная ячейка — это наименьшая структурная единица кристаллической решетки, которая обнаруживает все свойства ее симметрии.
Упрощенно элементарную ячейку можно определить как малую часть кристаллической решетки, которая еще выявляет характерные особенности ее кристаллов. Признаки элементарной ячейки описываются с помощью трех правил Бреве :
- симметрия элементарной ячейки должна соответствовать симметрии кристаллической решетки;
- элементарная ячейка должна иметь максимальное количество одинаковых ребер а, b, с и одинаковых углов между ними a, b, g. ;
- при условии соблюдения первых двух правил элементарная ячейка должна занимать минимальный объем.
Для описания формы кристаллов используют систему трех кристаллографических осей а, b, с, которые отличаются от обычных координатных осей тем, что они являются отрезками определенной длины, углы между которыми a, b, g могут быть как прямыми, так и непрямыми.

 Модель кристаллической структуры: а) кристаллическая решетка с выделенной элементарной ячейкой; б) элементарная ячейка с обозначениями гранных углов Форму кристалла изучает наука геометрическая кристаллография, одним из основных положений которой является закон постоянства гранных углов: для всех кристаллов данного вещества углы между соответствующими гранями всегда остаются одинаковыми.
Модель кристаллической структуры: а) кристаллическая решетка с выделенной элементарной ячейкой; б) элементарная ячейка с обозначениями гранных углов Форму кристалла изучает наука геометрическая кристаллография, одним из основных положений которой является закон постоянства гранных углов: для всех кристаллов данного вещества углы между соответствующими гранями всегда остаются одинаковыми.Если взять большое количество элементарных ячеек и заполнить ими плотно друг к другу определенный объем, сохраняя параллельность граней и ребер, то образуется монокристалл идеальной строения. Но на практике чаще всего встречаются поликристаллов, в которых регулярные структуры существуют в определенных пределах, по которым ориентация регулярности резко меняется.
В зависимости от соотношения длин ребер а, b, с и углов a, b, g между гранями элементарной ячейки различают семь систем — так называемых сингоний кристаллов. Однако элементарная ячейка может быть построенной и таким образом, что она имеет дополнительные узлы, которые размещаются внутри ее объема или на всех ее гранях — такие решетки называются соответственно объемноцентрированными и гранецентрированными. Если дополнительные узлы находятся только на двух противоположных гранях (верхний и нижний), то это базоцентрированная решетка. С учетом возможности дополнительных узлов существует всего 14 типов кристаллических решеток.
Внешняя форма и особенности внутреннего строения кристаллов определяются принципом плотной «упаковки»: наиболее устойчивой, а потому и наиболее вероятной структурой будет такая, которая соответствует наиболее плотному расположению частиц в кристалле и в которой остается наименьшее по объему свободное пространство.
Типы кристаллических решеток
В зависимости от природы частиц, содержащихся в узлах кристаллической решетки, а также от природы химических связей между ними, различаются четыре основных типа кристаллических решеток.
Ионные решетки
Ионные решетки построены из разноименных ионов, расположенных в узлах решетки и связанные силами электростатического притяжения. Поэтому структура ионной кристаллической решетки должна обеспечить ее электронейтральность. Ионы могут быть простыми (Na+, Cl—) или сложными (NH4+, NO3—). Вследствие ненасыщенности и ненаправленности ионной связи ионные кристаллы характеризуются большими координационными числами. Так, в кристаллах NaCl координационные числа ионов Na+ и Cl— равна 6, а ионов Cs+ и Cl— в кристалле CsCl — 8, поскольку один ион Cs+ окружен восемью ионами Cl—, а каждый ион — Cl — соответственно восемью ионами Cs+. Ионные кристаллические решетки образуются большим количеством солей, оксидов и оснований.

 Примеры ионных кристаллических решеток: а) NaCl; б) CsCl
Примеры ионных кристаллических решеток: а) NaCl; б) CsClВещества с ионными кристаллическими решетками имеют сравнительно высокую твердость, они достаточно тугоплавкие, нелетучие. В отличие от металлов ионные соединения очень хрупкие, поэтому даже небольшой сдвиг в кристаллической решетке приближает друг к другу одноименно заряженные ионы, отталкивания между которыми приводит к разрыву ионных связей и как следствие — к появлению в кристалле трещин или к его разрушению. В твердом состоянии вещества с ионной кристаллической решеткой относятся к диэлектрикам и не проводят электрический ток. Однако при расплавлении или растворении в полярных растворителях нарушается геометрически правильная ориентировка ионов относительно друг друга, сначала ослабляются, а затем разрушаются химические связи, поэтому меняются и свойства. Как следствие, электрический ток начинают проводить как расплавы ионных кристаллов, так и их растворы.
Атомные решетки
Эти решетки построены из атомов, соединенных между собой ковалентной связью. Они, в свою очередь, делятся на три типа: каркасные, слоистые и цепочечные структуры.
Каркасную структуру имеет, например, алмаз — одно из самых твердых веществ. Благодаря sp3 -гибридизации атома углерода строится трехмерная решетка, которая состоит исключительно из атомов углерода, соединенных ковалентными неполярными связями, оси которых размещаются под одинаковыми валентными углами (109,5o).

 Каркасная структура атомной кристаллической решетки алмаза
Каркасная структура атомной кристаллической решетки алмазаСлоистые структуры можно рассматривать как огромные двумерные молекулы. Для слоистых структур присущи ковалентные связи внутри каждого слоя и слабое вандерваальсовское взаимодействие между соседними слоями.

 Слоистые структуры атомных кристаллических решеток: а) CuCl2 ; б) PbO. На моделях с помощью очертаний параллелепипедов выделены элементарные ячейки
Слоистые структуры атомных кристаллических решеток: а) CuCl2 ; б) PbO. На моделях с помощью очертаний параллелепипедов выделены элементарные ячейкиКлассическим примером вещества со слоистой структурой является графит, в котором каждый атом углерода находится в состоянии sp2 -гибридизации и образует в одной плоскости три ковалентные s-связи с тремя другими атомами С. Четвертые валентные электроны каждого атома углерода являются негибридизированными, за их счет образуются очень слабые вандерваальсовские связи между слоями. Поэтому при приложении даже небольшого усилия, отдельные слои легко начинают скользить друг вдоль друга. Этим объясняется, например, свойство графита писать. В отличие от алмаза графит хорошо проводит электричество: под воздействием электрического поля нелокализованные электроны могут перемещаться вдоль плоскости слоев, и, наоборот, в перпендикулярном направлении графит почти не проводит электрического тока.

 Слоистая структура атомной кристаллической решетки графита
Слоистая структура атомной кристаллической решетки графита
Цепочечные структуры характерны, например, для оксида серы (SO3)n , киновари HgS, хлорида бериллия BeCl2, а также для многих аморфных полимеров и для некоторых силикатных материалов, таких, как асбест.

 Цепная структура атомной кристаллической решетки HgS: а) проекция сбоку б) фронтальная проекция
Цепная структура атомной кристаллической решетки HgS: а) проекция сбоку б) фронтальная проекцияВеществ с атомной строением кристаллических решеток сравнительно немного. Это, как правило, простые вещества, образованные элементами IIIА- и IVA-подгрупп (Si, Ge, B, C). Нередко соединения двух разных неметаллов имеют атомные решетки, например, некоторые полиморфные модификации кварца (оксид кремния SiO2 ) и карборунда (карбид кремния SiC).
Все атомные кристаллы отличаются высокой прочностью, твердостью, тугоплавкостью и нерастворимостью практически ни в одном растворителе. Такие свойства обусловлены прочностью ковалентной связи. Вещества с атомной кристаллической решеткой имеют широкий диапазон электрической проводимости от изоляторов и полупроводников до электронных проводников.

 Атомные кристаллические решетки некоторых полиморфных модификации карборунда — карбида кремния SiC
Атомные кристаллические решетки некоторых полиморфных модификации карборунда — карбида кремния SiCМеталлические решетки
Эти кристаллические решетки содержат в узлах атомы и ионы металлов, между которыми свободно движутся общие для них всех электроны (электронный газ), которые образуют металлическую связь. Особенность кристаллических решеток металлов заключается в больших координационных числах (8-12), которые свидетельствуют о значительной плотность упаковки атомов металлов. Это объясняется тем, что «остовы» атомов, лишены внешних электронов, размещаются в пространстве как шарики одинакового радиуса. Для металлов чаще всего встречаются три типа кристаллических решеток: кубическая гранецентрированная с координационным числом 12 кубическая объемноцентрированная с координационным числом 8 и гексагональная, плотной упаковки с координационным числом 12.
Особые характеристики металлического связи и металлических решеток обусловливают такие важнейшие свойства металлов, как высокие температуры плавления, электро- и теплопроводность, ковкость, пластичность, твердость.

 Металлические кристаллические решетки: а) кубическая объемноцентрированная (Fe, V, Nb, Cr) б) кубическая гранецентрированная (Al, Ni, Ag, Cu, Au) в) гексагональная (Ti, Zn, Mg, Cd)
Металлические кристаллические решетки: а) кубическая объемноцентрированная (Fe, V, Nb, Cr) б) кубическая гранецентрированная (Al, Ni, Ag, Cu, Au) в) гексагональная (Ti, Zn, Mg, Cd)Молекулярные решетки
Молекулярные кристаллические решетки содержат в узлах молекулы, соединенные между собой слабыми межмолекулярными силами — вандерваальсовскими или водородными связями. Например, лед состоит из молекул воды, удерживающихся в кристаллической решетке водородными связями. К тому же типу относятся кристаллические решетки многих веществ, переведенных в твердое состояние, например: простые вещества Н2, О2, N2, O3, P4, S8, галогены (F2, Cl2, Br2, I2), «сухой лед» СО2, все благородные газы и большинство органических соединений.

 Молекулярные кристаллические решетки: а) йод I2 ; б) лед Н2О
Молекулярные кристаллические решетки: а) йод I2 ; б) лед Н2ОПоскольку силы межмолекулярного взаимодействия слабее, чем силы ковалентной или металлической связи, молекулярные кристаллы имеют небольшую твердость; они легкоплавкие и летучие, нерастворимые в воде и не проявляют электропроводности.
www.polnaja-jenciklopedija.ru
Свойства кристаллических решеток
Тип кристаллической решетки | Характеристика |
Ионные | Состоят из ионов. Образуют вещества с ионной связью. Обладают высокой твердостью, хрупкостью, тугоплавки и малолетучи, легко растворяются в полярных жидкостях, являются диэлектриками. Плавление ионных кристаллов приводит к нарушению геометрически правильной ориентации ионов относительно друг друга и ослаблению прочности связи между ними. Поэтому их расплавы (растворы) проводят электрический ток. Ионные кристаллические решетки образуют многие соли, оксиды, основания. |
Атомные (ковалентные) | В узлах находятся атомы, которые соединены между собой ковалентными связями. Атомных кристаллов много. Все они имеют высокую температуру плавления, не растворимы в жидкостях, обладают высокой прочностью, твердостью, имеют широкий диапазон электропроводимости. Атомные кристаллические решетки образуют элементы III и IV групп главных подгрупп (Si, Ge, B, C). |
Продолжение табл. З4
Молекулярные | Состоят из молекул (полярных и неполярных), которые соединены между собой слабыми водородными, межмолекулярными и электростатическими силами. Поэтому молекулярные кристаллы имеют малую твердость, низкие температуры плавления, малорастворимы в воде, не проводят электрический ток и обладают высокой летучестью. Молекулярную решетку образует лед, твердый углекислый газ («сухой лед»), твердые галогенводороды, твердые простые вещества, образованные одно- (благородные газы), двух- (F2, Cl2, Br2, J2, H2, N2, O2), трех- (O3), четырех- (P4), восьми- (S8) атомными молекулами, многие кристаллические органические соединения. |
Металлические | Состоят из атомов или ионов металлов, соединенных металлической связью. Узлы металлических решеток заняты положительными ионами, между которыми перемещаются валентные электроны, находящиеся в свободном состоянии (электронный газ). Металлическая решетка является прочной. Этим объясняются свойственные большинству металлов твердость, малая летучесть, высокая температура плавления и кипения. Она же обусловливает такие характерные свойства металлов как электро- и теплопроводность, блеск, ковкость, пластичность, непрозрачность, фотоэффект. Металлической кристаллической решеткой обладают чистые металлы и сплавы. |
Кристаллы по величине электропроводности делятся на три класса:
Проводники I рода – электропроводность 104 — 106 (Омсм)-1–вещества с металлической кристаллической решеткой, характеризующиеся наличием «переносчиков тока» — свободно перемещающихся электронов (металлы, сплавы).
Диэлектрики (изоляторы) – электропроводность 10-10-10-22 (Омсм)-1 – вещества с атомной, молекулярной и реже ионной решеткой, обладающие большой энергией связи между частицами (алмаз, слюда, органические полимеры и др.).
Полупроводники – электропроводность 104-10-10 (Омсм)-1 – вещества с атомной или ионной кристаллической решеткой, обладающие более слабой энергией связи между частицами, чем изоляторы. С ростом температуры электропроводность у полупроводников возрастает (серое олово, бор, кремний и др.)
studfile.net
Типы кристаллических решеток и свойства веществ
По характеру структуры кристаллические решетки всех веществ относят к одному из четырех основных типов:
а) молекулярная решетка,
б) атомная,
в) ионная,
г) металлическая.
В основу этой классификации положен род структурных частиц (молекулы-атомы-ионы), находящихся в узлах кристаллической решетки.
Молекулярная решетка
В узлах молекулярной решетки находятся полярные или неполярные молекулы, связанные между собой слабыми силами межмолекулярного взаимодействия (силами Ван-дер-Ваальса). Молекулы в кристалле способны совершать незначительные колебания различного характера. Вещества с молекулярным типом решетки, например, органические вещества, кристаллы инертных газов и большинства неметаллов, сухой лед (СО2 тверд.) обладают малой твердостью, низкими температурами плавления и кипения. Эти характеристики объясняются тем, что при приложении незначительной энергии межмолекулярные связи разрываются и кристалл разрушается с образованием отдельных молекул, что и наблюдается при плавлении и при испарении кристаллов. Внутри отдельных молекул атомы связаны значительно более прочными связями (ковалентными полярными или неполярными). Эти связи разрушаются при более высокой температуре, и молекулы распадаются на составляющие их атомы (происходит термическая диссоциация).
Атомная решетка
В узлах атомной кристаллической решетки находятся атомы. Роль сил межмолекулярного взаимодействия здесь играют достаточно прочные ковалентные связи. Выделить из общей массы атомов один невозможно. Вещества с атомным типом кристаллической решетки (алмаз, бор, кремний, карборунд SiC, нитрид алюминия и другие) характеризуются очень большой твердостью, иногда сочетающейся с хрупкостью, нерастворимостью в обычных растворителях, очень высокими температурами плавления и кипения. Все связи в кристалле равноценны. При разрыве этих связей, достигаемом лишь при высокой температуре, кристалл диссоциирует на отдельные атомы: плавление, кипение и термическая диссоциация практически совпадают.
Ионная (координационная) решетка
В узлах ионной кристаллической решетки находятся чередующиеся положительные и отрицательные ионы, связанные между собой силами кулоновского взаимодействия. Особенностью этих сил является их ненасыщаемость. Это приводит к тому, что отдельный ион координирует вокруг себя несколько ионов противоположного заряда. Ионы в кристаллах совершают упорядоченные колебания. Энергия связей между противоположно заряженными ионами очень велика, и такие кристаллы, казалось бы, должны обладать наиболее высокой твердостью и высокими температурами плавления и кипения. На самом деле эти свойства у них ниже, чем у кристаллов с атомной структурой. Причина заключается в том, что наряду с силами притяжения в кристалле действуют силы отталкивания между одноименно заряженными ионами, причем соотношение этих сил приводит к определенному равновесному состоянию. Вещества с ионной решеткой растворимы в той или иной степени в полярных растворителях.
Металлическая решетка
В узлах металлической решетки находятся положительно заряженные ионы металлов, окруженные электронами. Эти электроны, связанные отчасти с ионами силами электростатического взаимодействия, являются «полусвободными», иначе говоря «не прикреплены» к отдельным ионам, а более или менее свободно перемещаются между ними. Этот «электронный газ» обусловливает типичные для металлов свойства: тепло- и электропроводность, серовато-серебристый (у большинства металлов) цвет, металлический блеск (отражательную способность), способность отражать радиоволны, пластичность, ковкость и в то же время достаточную прочность (результат обволакивания ионов «электронным газом»). Подходя к катиону металла, электроны образуют с ним на мгновение электронейтральную частицу, которая быстро разрушается и через мгновение такой же непрочный «атом» образуется с этим или другим электроном и другим ионом металла. Между «атомами» возникают мгновенные ковалентные связи. Это и приводит к возникновению особой металлической связи, промежуточной по характеру между ионной и ковалентной, качественно отличающейся от той и другой и наблюдаемой лишь в куске металла. Энергия электронов в металле недостаточна, чтобы они могли «оторваться» от катионов металла и самопроизвольно покинуть металлическую решетку. Но при подведении энергии извне выход электронов наблюдается: фотоэлектрический эффект, термоэлектронная эмиссия. Прочность и температуры плавления и кипения у металлов не всегда имеют промежуточные значения между этими же свойствами у веществ с атомными и ионными решетками. Это зависит от природы металла. Интересно, что заряд ионов в металлах не всегда отвечает номеру группы периодической системы, в которой металл находится. Например, в кристаллической решетке алюминия ионы имеют средний заряд +2. Это можно объяснить двумя способами:
а) все атомы алюминия отдали по два электрона в «электронный газ»;
б) все атомы отдали по три электрона, но в среднем одна треть образовавшихся ионов Al+3 снова образует «атомы», поэтому средний заряд всех структурных частиц +2.
Таким образом, металлическое состояние в упрощенном представлении подобно атомарному ввиду его суммарной электронейтральности; это сосуществование и взаимосвязь «атомов»-ионов-электронов.
Типы кристаллических решеток и свойства веществ
№ | Тип кристаллической решетки | Структурные частицы кристалла | Характер связи между структурными частицами кристалла | Характер связи в молекулах | Примеры кристаллических веществ | Характерные свойства |
1. | Молекулярная | Полярные молекулы – диполи | 1. Электростатическое взаимодействие диполей. | Ковалентные полярные | HF, H2O, HCl, H2S, PCl3, NH3 (твердые) | Межмолекулярное взаимодействие средней силы. |
| Неполярные молекулы | Силы Ван-дер-Ваальса (слабые) | Ковалентные неполярные и ковалентные полярные | H2, Cl2, O2, N2, F2, СО2, SO3 (образованы молекулами симметричного строения) | Межмолекулярное взаимодействие слабое. Растворимы в неполярных растворителях, очень малая термическая устойчивость, очень слабая электропроводность, легкая летучесть (очень низкие температуры плавления и кипения), очень слабые механические свойства. | ||
2. | Атомная | Атомы | Ковалентные связи | — | C, Si, SiC, AlN, ВеО (образованы элементами, среднее арифметическое номеров групп которых равно 4) | Нерастворимы в обычных растворителях, термически устойчивы, неэлектропроводны, температуры плавления и кипения очень высокие; твердые, но хрупкие, прочность связей между частицами очень высокая. |
3. | Ионная | Ионы: катионы, анионы | 1. Электростатическое взаимодействие. | — | CsF, KCl, CaF2, CsH, NaF, ВаCl2 | Растворимы в полярных растворителях, термическая устойчивость высокая, большая электропроводность в растворах и расплавах, высокие температуры плавления; вещества твердые, но хрупкие, прочность связей между частицами высокая. |
4. | Металлическая | Катионы, «атомы», электроны | 1. Электростатическое притяжение ионов и электронов. | — | Na, K, Cu, Zn, Fe, Pt, Pb | Растворимы в расплавленных металлах, термическая устойчивость различная, электропроводность высокая, температуры плавления и кипения лежат в широких пределах; вещества пластичные, твердость, как и прочность связей между частицами, различная. |
urok.1sept.ru
Типы кристаллических решеток. Типы кристаллических решеток металлов :: SYL.ru
При осуществлении многих физических и химических реакций вещество переходит в твердое агрегатное состояние. При этом молекулы и атомы стремятся расположиться в таком пространственном порядке, при котором силы взаимодействия между частицами вещества были бы максимально сбалансированы. Этим и достигается прочность твердого вещества. Атомы, однажды заняв определенное положение, совершают небольшие колебательные движения, амплитуда которых зависит от температуры, но положение их в пространстве остается фиксированным. Силы притяжения и отталкивания уравновешивают друг друга на определенном расстоянии.
Современные представления о строении вещества
Современная наука утверждает, что атом состоит из заряженного ядра, несущего положительный заряд, и электронов, несущих заряды отрицательные. Со скоростью несколько тысяч триллионов оборотов в секунду электроны вращаются по своим орбитам, создавая вокруг ядра электронное облако. Положительный заряд ядра численно равен отрицательному заряду электронов. Таким образом, атом вещества остается электрически нейтральным. Возможные взаимодействия с другими атомами происходят тогда, когда электроны отсоединяются от родного атома, тем самым нарушая электрический баланс. В одном случае атомы выстраиваются в определенном порядке, который и называется кристаллической решеткой. В другом – за счет сложного взаимодействия ядер и электронов соединяются в молекулы различного вида и сложности.
Определение кристаллической решетки
В совокупности различные типы кристаллических решеток веществ представляют собой сетки с различной пространственной ориентацией, в узлах которых располагаются ионы, молекулы или атомы. Это стабильное геометрическое пространственное положение и называется кристаллической решеткой вещества. Расстояние между узлами одной кристаллической ячейки называется периодом идентичности. Пространственные углы, под которыми расположены узлы ячейки, называются параметрами. По способу построения связей кристаллические решетки могу быть простыми, базоцентрированными, гранецентрированными и объемно-центрированными. Если частицы вещества расположены лишь в углах параллелепипеда, такая решетка называется простой. Пример такой решетки показан ниже:
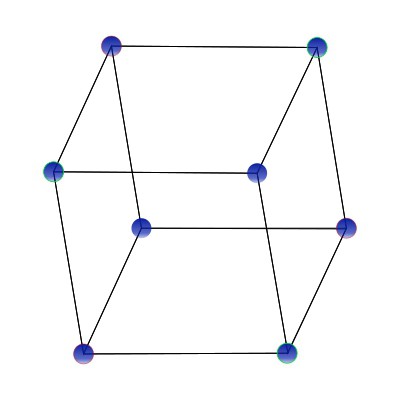
Если, кроме узлов, частицы вещества расположены и в середине пространственных диагоналей, то такое построение частиц в веществе имеет название объемно-центрированной кристаллической решетки. На рисунке этот тип показан наглядно.
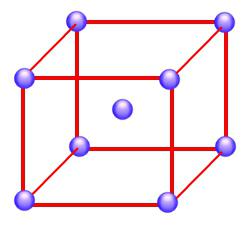
Если кроме узлов в вершинах решетки имеется узел и в месте, где пересекаются воображаемые диагонали параллелепипеда, то перед вами — гранецентрированный тип решетки.
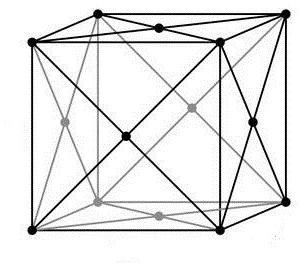
Виды кристаллических решеток
Различные микрочастицы, из которых состоит вещество, определяют различные типы кристаллических решеток. Они могут определять принцип построения связи между микрочастицами внутри кристалла. Физические типы кристаллических решеток — ионные, атомные и молекулярные. Сюда же относятся различные типы кристаллических решеток металлов. Изучением принципов внутреннего строения элементов занимается химия. Типы кристаллических решеток подробнее представлены ниже.
Ионные кристаллические решетки
Данные типы кристаллических решеток присутствуют в соединениях с ионным типом связи. В этом случае узлы решетки содержат ионы, обладающие противоположным электрическим зарядом. Благодаря электромагнитному полю, силы межионного взаимодействия оказываются достаточно сильными, и это обуславливает физические свойства вещества. Обычными характеристиками являются тугоплавкость, плотность, твердость и возможность проводить электрический ток. Ионные типы кристаллических решеток имеются у таких веществ, как поваренная соль, нитрат калия и прочие.
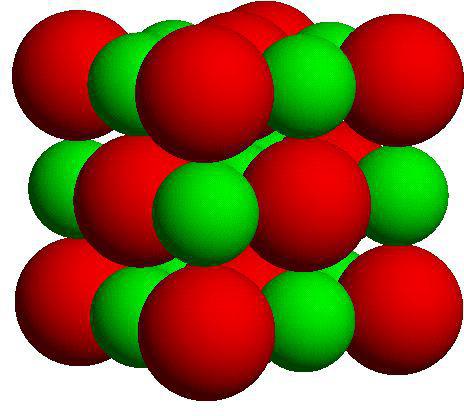
Атомные кристаллические решетки
Этот тип строения вещества присущ элементам, структуру которых определяет ковалентная химическая связь. Типы кристаллических решеток подобного рода содержат в узлах отдельные атомы, связанные между собой крепкими ковалентными связями. Подобный тип связи возникает тогда, когда два одинаковых атома «делятся» электронами, тем самым образуют общую пару электронов для соседних атомов. Благодаря такому взаимодействию ковалентные связи равномерно и сильно связывают атомы в определенном порядке. Химические элементы, которые содержат атомные типы кристаллических решеток, обладают твердостью, высокой температурой плавления, плохо проводят электрический ток и химически неактивны. Классическими примерами элементов с подобным внутренним строением можно назвать алмаз, кремний, германий, бор.
Молекулярные кристаллические решетки
Вещества, имеющие молекулярный тип кристаллической решетки, представляют собой систему устойчивых, взаимодействующих, плотноупакованных между собой молекул, которые расположены в узлах кристаллической решетки. В подобных соединениях молекулы сохраняют свое пространственное положение в газообразной, жидкой и твердой фазе. В узлах кристалла молекулы удерживаются слабыми ван-дер-ваальсовыми силами, которые в десятки раз слабее сил ионного взаимодействия.
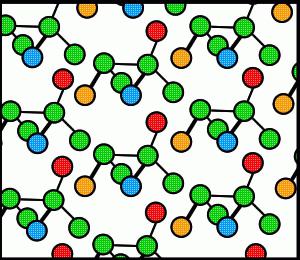
Образующие кристалл молекулы могут быть как полярными, так и неполярными. Из-за спонтанного движения электронов и колебания ядер в молекулах электрическое равновесие может смещаться – так возникает мгновенный электрический момент диполя. Соответствующим образом ориентированные диполи создают силы притяжения в решетке. Двуокись углерода и парафин являются типичными примерами элементов с молекуляной кристаллической решеткой.
Металлические кристаллические решетки
Металлическая связь гибче и пластичней ионной, хотя может показаться, что обе они базируются на одном и том же принципе. Типы кристаллических решеток металлов объясняют их типичные свойства – такие, например, как механическая прочность, тепло- и электропроводность, плавкость.
Отличительной особенностью металлической кристаллической решетки является наличие положительно заряженных ионов металла (катионов) в узлах этой решетки. Между узлами находятся электроны, которые непосредственно участвуют в создании электрического поля вокруг решетки. Количество электронов, перемещающихся внутри этой кристаллической решетки, называется электронным газом.
 При отсутствии электрического поля свободные электроны совершают хаотическое движение, беспорядочно взаимодействуя с ионами решетки. Каждое такое взаимодействие меняет импульс и направление движения отрицательно заряженной частицы. Своим электрическим полем электроны притягивают к себе катионы, уравновешивая их взаимное отталкивание. Хотя электроны считаются свободными, их энергии не хватает для того, чтобы покинуть кристаллическую решетку, поэтому эти заряженные частицы постоянно находятся в ее пределах.
При отсутствии электрического поля свободные электроны совершают хаотическое движение, беспорядочно взаимодействуя с ионами решетки. Каждое такое взаимодействие меняет импульс и направление движения отрицательно заряженной частицы. Своим электрическим полем электроны притягивают к себе катионы, уравновешивая их взаимное отталкивание. Хотя электроны считаются свободными, их энергии не хватает для того, чтобы покинуть кристаллическую решетку, поэтому эти заряженные частицы постоянно находятся в ее пределах.Присутствие электрического поля придает электронному газу дополнительную энергию. Соединение с ионами в кристаллической решетке металлов не является прочным, поэтому электроны легко покидают ее пределы. Электроны двигаются по силовым линиям, оставляя позади положительно заряженные ионы.
Выводы
Огромное значение изучению внутреннего строения вещества уделяет химия. Типы кристаллических решеток различных элементов определяют практически весь спектр их свойств. Воздействуя на кристаллы и меняя их внутренне строение, можно добиться усиления нужных свойств вещества и удалить нежелательные, преобразовывать химические элементы. Таким образом, изучение внутренней структуры окружающего мира может помочь познать суть и принципы устройства мироздания.
www.syl.ru
Кристаллические решетки
Как мы уже знаем, вещество может существовать в трех агрегатных состояниях: газообразном, твердом и жидком. Кислород, который при обычных условиях находится в газообразном состоянии, при температуре -194° С преобразуется в жидкость голубоватого цвета, а при температуре -218,8° С превращается в снегообразную массу с кристаллами синего цвета.
Температурный интервал существования вещества в твердом состоянии определяется температурами кипения и плавления. Твердые вещества бывают кристаллическими и аморфными.
У аморфных веществ нет фиксированной температуры плавления – при нагревании они постепенно размягчаются и переходят в текучее состояние. В таком состоянии, например, находятся различные смолы, пластилин.
 Кристаллические вещества отличаются закономерным расположением частиц, из которых они состоят: атомов, молекул и ионов, – в строго определенных точках пространства. Когда эти точки соединяются прямыми линиями, создается пространственный каркас, его называют кристаллической решеткой. Точки, в которых находятся частицы кристалла, называют узлами решетки.
Кристаллические вещества отличаются закономерным расположением частиц, из которых они состоят: атомов, молекул и ионов, – в строго определенных точках пространства. Когда эти точки соединяются прямыми линиями, создается пространственный каркас, его называют кристаллической решеткой. Точки, в которых находятся частицы кристалла, называют узлами решетки.
В узлах воображаемой нами решетки могут находиться ионы, атомы и молекулы. Эти частицы совершают колебательные движения. Когда температура увеличивается, размах этих колебаний тоже возрастает, что приводит к тепловому расширению тел.
В зависимости от разновидности частиц, находящихся в узлах кристаллической решетки, и характера связи между ними различают четыре типа кристаллических решеток: ионные, атомные, молекулярные и металлические.
Ионными называют такие кристаллические решетки, в узлах которых расположены ионы. Их образуют вещества с ионной связью, которой могут быть связаны как простые ионы Na+, Cl- , так и сложные SO24-, OH-. Таким образом, ионные кристаллические решетки имеют соли, некоторые оксиды и гидроксилы металлов, т.е. те вещества, в которых существует ионная химическая связь. Рассмотрим кристалл хлорида натрия, он состоит из положительно чередующихся ионов Na+ и отрицательных CL-, вместе они образуют решетку в виде куба. Связи между ионами в таком кристалле чрезвычайно устойчивы. Из-за этого вещества с ионной решеткой обладают сравнительно высокой прочностью и твердостью, они тугоплавки и нелетучи.
Атомными кристаллическими решетками называют такие кристаллические решетки, в узлах которых находятся отдельные атомы. В подобных решетках атомы соединяются между собой очень крепкими ковалентными связями. К примеру, алмаз – одно из аллотропных видоизменений углерода.
Вещества с атомной кристаллической решеткой не сильно распространены в природе. К ним относятся кристаллический бор, кремний и германий, а также сложные вещества, например такие, в составе которых есть оксид кремния (IV) – SiO2: кремнезем, кварц, песок, горный хрусталь.
 Подавляющее большинство веществ с атомной кристаллической решеткой имеют очень высокие температуры плавления (у алмаза она превышает 3500° С), такие вещества прочны и тверды, практически не растворимы.
Подавляющее большинство веществ с атомной кристаллической решеткой имеют очень высокие температуры плавления (у алмаза она превышает 3500° С), такие вещества прочны и тверды, практически не растворимы.
Молекулярными называют такие кристаллические решетки, в узлах которых расположены молекулы. Химические связи в этих молекулах могут быть также, как полярными (HCl, H20), так и неполярными (N2, O3). И хотя атомы внутри молекукл связаны очень крепкими ковалентными связями, между самими молекулами действует слабые силы межмолекулярного притяжения. Именно поэтому вещества с молекулярными кристаллическими решетками характеризуются малой твердостью, низкой температурой плавления, летучестью.
Примерами таких веществ могут послужить твердая вода – лед, твердый оксид углерода (IV) – «сухой лед», твердые хлороводород и сероводород, твердые простые вещества, образованные одно – (благородные газы), двух – (H2, O2, CL2, N2, I2), трех – (O3), четырех – (P4), восьмиатомными (S8) молекулами. Подавляющее большинство твердых органических соединений обладают молекулярными кристаллическими решетками (нафталин, глюкоза, сахар).
© blog.tutoronline.ru, при полном или частичном копировании материала ссылка на первоисточник обязательна.
blog.tutoronline.ru
Кристаллические решетки
Внимание! Предварительный просмотр слайдов используется исключительно в ознакомительных целях и может не давать представления о всех возможностях презентации. Если вас заинтересовала данная работа, пожалуйста, загрузите полную версию.
Тип урока: Комбинированный.
Основная цель урока: Дать учащимся конкретные представления об аморфных и кристаллических веществах, типах кристаллических решеток, установить взаимосвязь между строением и свойствами веществ.
Задачи урока.
Образовательная: сформировать понятия о кристаллическом и аморфном состоянии твердых тел, ознакомить учащихся с различными типами кристаллических решеток, установить зависимость физических свойств кристалла от характера химической связи в кристалле и типа кристаллической решетки, дать учащимся основные представления о влиянии природы химической связи и типов кристаллических решеток на свойства вещества, дать учащимся представление о законе постоянства состава.
Воспитательная: продолжить формирование мировоззрения учащихся, рассмотреть взаимное влияние компонентов целого- структурных частиц веществ, в результате которого появляются новые свойства, воспитывать умения организовать свой учебный труд, соблюдать правила работы в коллективе.
Развивающая: развивать познавательный интерес школьников, используя проблемные ситуации; совершенствовать умения учащихся устанавливать причинно-следственную зависимость физических свойств веществ от химической связи и типа кристаллической решетки, предсказывать тип кристаллической решетки на основе физических свойств вещества.
Оборудование: Периодическая система Д.И.Менделеева, коллекция “Металлы”, неметаллы: сера, графит, красный фосфор, кислород; Презентация “Кристаллические решетки”, модели кристаллических решеток разных типов (поваренной соли, алмаза и графита, углекислого газа и йода, металлов), образцы пластмасс и изделий из них, стекло, пластилин, смолы, воск, жевательная резинка, шоколад, компьютер, мультимедийная установка, видеопыт “Возгонка бензойной кислоты”.
Ход урока
1. Организационный момент.
Учитель приветствует учеников, фиксирует отсутствующих.
Затем сообщает тему урока и цель урока. Учащиеся записывают тему урока в тетрадь. (Cлайд 1, 2).
2. Проверка домашнего задания
(2 ученика у доски: Определить вид химической связи для веществ с формулами:
1) NaCl, CO2, I2 ; 2) Na, NaOH, H2S (записывают ответ на доске и включаются в опрос).
3. Анализ ситуации.
Учитель: Что изучает химия? Ответ: Химия — это наука о веществах, их свойствах и превращениях веществ.
Учитель: Что же такое вещество? Ответ: Вещество — это то, из чего состоит физическое тело. (Cлайд 3).
Учитель: Какие агрегатные состояния веществ вы знаете?
Ответ: Существует три агрегатных состояния: твердое, жидкое и газообразное. (Cлайд 4).
Учитель: Приведите примеры веществ, которые при различных температурах могут существовать во всех трех агрегатных состояниях.
Ответ: Вода. При обычных условиях вода находится в жидком состоянии, при понижении температуры ниже 00С вода переходит в твердое состояние — лед, а при повышении температуры до 1000С мы получим водяной пар (газообразное состояние).
Учитель (дополнение): Любое вещество можно получить в твердом, жидком и газообразном виде. Кроме воды – это металлы, которые при нормальных условиях находятся в твердом состоянии, при нагревании начинают размягчаться, и при определенной температуре(tпл) переходят в жидкое состояние — плавятся. При дальнейшем нагревании, до температуры кипения, металлы начинают испаряться, т.е. переходить в газообразное состояние. Любой газ можно перевести в жидкое и твердое состояние, понижая температуру: например, кислород, который при температуре (-1940С) превращается в жидкость голубого цвета, а при температуре (-218,80С) затвердевает в снегообразную массу, состоящую из кристаллов синего цвета. Сегодня на уроке мы будем рассматривать твердое состояние вещества.
Учитель: Назовите, какие твердые вещества находятся у вас на столах.
Ответ: Металлы, пластилин, поваренная соль: NaCl, графит.
Учитель: Как вы думаете? Какое из этих веществ лишнее?
Ответ: Пластилин.
Учитель: Почему?
Делаются предположения. Если ученики затрудняются, то с помощью учителя приходят к выводу, что пластилин в отличие от металлов и хлорида натрия не имеет определенной температуры плавления — он (пластилин) постепенно размягчается и переходит в текучее состояние. Таков, например, шоколад, который тает во рту, или жевательная резинка, а также стекло, пластмассы, смолы, воск (при объяснении учитель демонстрирует классу образцы этих веществ). Такие вещества называют аморфными. (слайд 5), а металлы и хлорид натрия — кристаллические. (Cлайд 6).
Таким образом, различают два вида твердых веществ: аморфные и кристаллические. (слайд7).
1) У аморфных веществ нет определенной температуры плавления и расположение частиц в них строго не упорядочено.
Кристаллические вещества имеют строго определенную температуру плавления и, главное, характеризуются правильным расположением частиц, из которых они построены: атомов, молекул и ионов. Эти частицы расположены в строго определенных точках пространства, и, если эти узлы соединить прямыми линиями, то образуется пространственный каркас — кристаллическая решетка.
(Cлайд 8)
Учитель задает проблемные вопросы
Как объяснить существование твердых веществ со столь различными свойствами?
2) Почему кристаллические вещества при ударе раскалываются в определенных плоскостях, а аморфные вещества этим свойством не обладают?
Выслушать ответы учеников и подвести их к выводу:
Свойства веществ в твердом состоянии зависят от типа кристаллической решетки (прежде всего от того, какие частицы находятся в ее узлах), что, в свою очередь, обусловлено типом химической связи в данном веществе.
(Cлайд 9).
Проверка домашнего задания:
1) NaCl – ионная связь,
СО2 – ковалентная полярная связь
I2 – ковалентная неполярная связь
2) Na – металлическая связь
NаОН — ионная связь между Na+иОН— (О и Н ковалентная)
Н2S — ковалентная полярная
Фронтальный опрос.
- Какая связь называется ионной?
- Какая связь называется ковалентной?
- Какая связь называется ковалентной полярной? неполярной?
- Что называется электроотрицательностью?
Вывод: Прослеживается логическая последовательность, взаимосвязь явлений в природе: Строение атома—>ЭО—>Виды химической связи—>Тип кристаллической решетки—>Свойства веществ. (слайд 10).
Учитель: В зависимости от вида частиц и от характера связи между ними различают четыре типа кристаллических решеток: ионные, молекулярные, атомные и металлические. (Cлайд 11).
Далее идет рассмотрение типов кристаллических решеток. Особое внимание уделяется взаимосвязи типа кристаллической решетки, вида химической связи и свойств твердых веществ.
Результаты оформляются в следующую таблицу-образец таблицы у учеников на парте. (см. Приложение 1). (Cлайд 12).
Ионные кристаллические решетки
(Cлайд13)
Учитель: Как вы думаете? Для веществ с каким видом химической связи будет характерен такой вид решетки?
Ответ: Для веществ с ионной химической связью будет характерна ионная решетка.
Учитель: Какие частицы будут находиться в узлах решетки?
Ответ: Ионы.
Учитель: Какие частицы называются ионами?
Ответ: Ионы-это частицы, имеющие положительный или отрицательный заряд.
Учитель: Какие ионы бывают по составу?
Ответ: Простые и сложные.
Демонстрация — модель кристаллической решетки хлорида натрия (NaCl).
Объяснение учителя: В узлах кристаллической решетки хлорида натрия находятся ионы натрия и хлора.
В кристаллах NaCl отдельных молекул хлорида натрия не существует. Весь кристалл следует рассматривать как гигантскую макромолекулу, состоящую из равного числа ионов Na+ и Cl—, NanCln, где n – большое число.
Связи между ионами в таком кристалле очень прочные. Поэтому вещества с ионной решеткой обладают сравнительно высокой твердостью. Они тугоплавки, нелетучи, хрупки. Расплавы их проводят электрический ток (Почему?), легко растворяются в воде.
Ионные соединения — это бинарные соединения металлов (I А и II A), соли, щелочи.
Атомные кристаллические решетки
(Слайд 14)
Демонстрация кристаллических решеток алмаза и графита.
У учеников на столе образцы графита.
Учитель: Какие частицы будут находиться в узлах атомной кристаллической решетки?
Ответ: В узлах атомной кристаллической решетки находятся отдельные атомы.
Учитель: Какая химическая связь между атомами будет возникать?
Ответ: Ковалентная химическая связь.
Объяснения учителя.
Действительно, в узлах атомных кристаллических решеток находятся отдельные атомы, связанные между собой ковалентными связями. Так как атомы, подобно ионам, могут по-разному располагаться в пространстве, то образуются кристаллы разной формы.
Атомная кристаллическая решетка алмаза
В данных решетках молекулы отсутствуют. Весь кристалл следует рассматривать как гигантскую молекулу. Примером веществ с таким типом кристаллических решеток могут служить аллотропные модификации углерода: алмаз, графит; а также бор, кремний, красный фосфор, германий. Вопрос: Какие эти вещества по составу? Ответ: Простые по составу.
Атомные кристаллические решетки имеют не только простые, но и сложные. Например, оксид алюминия, оксид кремния. Все эти вещества имеют очень высокие температуры плавления (у алмаза свыше 35000С), прочны и тверды, нелетучи, практически нерастворимы в жидкостях.
Металлические кристаллические решетки
(Слайд15)
Учитель: Ребята, у вас на столах коллекция металлов, рассмотрим эти образцы.
Вопрос: Какая химическая связь характерна для металлов?
Ответ: Металлическая. Связь в металлах между положительными ионами посредством обобществленных электронов.
Вопрос: Какие общие физические свойства для металлов характерны?
Ответ: Блеск, электропроводность, теплопроводность, пластичность.
Вопрос: Объясните, в чем причина того, что у такого числа разнообразных веществ одинаковые физические свойства?
Ответ: Металлы имеют единое строение.
Демонстрация моделей кристаллических решеток металлов.
Объяснение учителя.
Вещества с металлической связью имеют металлические кристаллические решетки
В узлах таких решеток находятся атомы и положительные ионы металлов, а в объеме кристалла свободно перемещаются валентные электроны. Электроны электростатически притягивают положительные ионы металлов. Этим объясняется стабильность решетки.
Молекулярные кристаллические решетки
(Слайд16)
Учитель демонстрирует и называет вещества: йод, сера.
Вопрос: Что объединяет эти вещества?
Ответ: Эти вещества являются неметаллами. Простые по составу.
Вопрос: Какая химическая связь внутри молекул?
Ответ: Химическая связь внутри молекул ковалентная неполярная.
Вопрос: Какие физические свойства для них характерны?
Ответ: Летучие, легкоплавкие, малорастворимые в воде.
Учитель: Давайте сравним свойства металлов и неметаллов. Ученики отвечают, что свойства принципиально отличаются.
Вопрос: Почему свойства неметаллов сильно отличаются от свойств металлов?
Ответ: У металлов связь металлическая, а у неметаллов ковалентная неполярная.
Учитель: Следовательно, и тип решетки другой. Молекулярная.
Вопрос: Какие частицы находятся в узлах решетки?
Ответ: Молекулы.
Демонстрация кристаллических решеток углекислого газа и йода.
Объяснение учителя.
Молекулярная кристаллическая решетка
Как видим, молекулярную кристаллическую решетку могут иметь не только твердые простые вещества: благородные газы, H2,O2,N2, I2, O3, белый фосфор Р4, но и сложные: твердая вода, твердые хлороводород и сероводород. Большинство твердых органических соединений имеют молекулярные кристаллические решетки (нафталин, глюкоза, сахар).
В узлах решеток находятся неполярные или полярные молекулы. Несмотря на то, что атомы внутри молекул связаны прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного взаимодействия.
Вывод: Вещества непрочные, имеют малую твердость, низкую температуру плавления, летучи, способны к возгонке.
Вопрос: Какой процесс называется возгонкой или сублимацией?
Ответ: Переход вещества из твердого агрегатного состояния сразу в газообразное, минуя жидкое, называется возгонкой или сублимацией.
Демонстрация опыта: возгонка бензойной кислоты (видеоопыт).
Работа с заполненной таблицей.
Приложение 1. (Слайд 17)
Кристаллические решетки, вид связи и свойства веществ
urok.1sept.ru