Методическая разработка по математике (9 класс): Частная методика решения задач на смеси, растворы и сплавы.
МУНИЦИПАЛЬНОЕ АВТОНОМНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
«СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА № 11»
Методика
решения задач на смеси, растворы и сплавы.
Материал подготовила: Скляр Галина Александровна
учитель математики
МАОУ СОШ №11 г. Тамбов
2018 г
Аннотация.
Данная методика посвящена проблеме подготовки к ОГЭ и ЕГЭ по математике по теме: «Решение задач на смеси, растворы и сплавы». В нее входят подобные экзаменационным, подготовительные задания для отработки элементов этой темы, задания для самостоятельного выполнения. Данная методика поможет обучающимся эффективнее подготовиться к сдаче экзамена.
Пояснительная записка
Данная методика предназначена для обучающихся 9-х-11-х классов общеобразовательных учреждений. Она предназначена для повышения эффективности подготовки обучающихся по теме «Решение задач на смеси, растворы и сплавы» к экзамену по математике за курс основной школы и предусматривает их подготовку к дальнейшему обучению в средней школе.
Методика сочетается с любым УМК, рекомендованным к использованию в образовательном процессе, согласована с требованиями государственного образовательного стандарта и содержанием основных программ курса математики основной школы.
Программой школьного курса математики не предусмотрены обобщение и систематизация знаний по теме решение текстовых задач и в частности решение задач на смеси, сплавы и растворы, а с этим видом задач у учащихся часто возникают сложности. Изучив алгоритм решения задач, учащиеся смогут легко решать задачи этого типа и даже более сложные нестандартные задания, выходящие за рамки школьной программы, которые встречаются на олимпиадах. Знание этого материала и умение его применять в практической деятельности позволит школьникам подготовиться к успешной сдаче экзамена.
Цель:
систематизация знаний по решению задач на смеси, сплавы и растворы, подготовка обучающихся к основному государственному экзамену по математике.
Задачи:
Формирование «базы знаний» по данной теме, позволяющей беспрепятственно оперировать математическим материалом вне зависимости от способа проверки знаний.
Развить навыки решения задач данного типа.
Функции методики:
ориентация на совершенствование навыков познавательной, организационной деятельности;
компенсация недостатков знаний, умений, навыков по математике.
Новизна:
Используя алгоритм решения задач на смеси, растворы и сплавы можно решать и задачи, в которых говорится о высушенных фруктах.
ОСНОВНОЕ СОДЕРЖАНИЕ.
Алгоритм решения задач на сплавы, растворы и смеси:
- Изучить условия задачи.
- Выбрать неизвестные величины и обозначить их буквами х, у и т.д.
- Используя условия задачи, определить все взаимосвязи между данными величинами.
- Составить математическую модель задачи и решить ее.
- Изучить полученное решение, провести критический анализ результата.
При решении задач на смеси, сплавы, растворы используем формулу m=M٠α , m — масса чистого вещества, M – масса всей смеси (сплава, раствора), α – концентрация, т.е. доля чистого вещества.
В большинстве случаев задачи на смеси и сплавы становятся нагляднее, если при их решении использовать схемы, иллюстративные рисунки или вспомогательные таблицы.
Пример:
1)Имеется два сплава с 20 %-ым и 40 %-ым содержанием олова. Из них получили новый сплав, найти процентное содержание олова в этом сплаве, если масса первого сплава 300 г, а масса второго сплава 200г.
Решение.
m (г) | M (г) | α | |
1 сплав | 0,2·300 | 300 | 0,2 |
2 сплав | 0,4·200 | 200 | 0,4 |
новый сплав | 60+80 | 500 | х |
Используя формулу m=M٠α, получаем уравнение
60+80=500х
х=140: 500
х= 0,28.
0,28 концентрация нового сплава, выразим в процентах. Ответ: 28%.
2) В 2 литра 10% раствора уксусной кислоты добавили 8 литров чистой воды. Определить процентное содержание уксусной кислоты в полученном растворе.
Решение.
m (л) | M (л) | α | |
1 раствор | 0,1·2 | 2 | 0,1 |
2 раствор | 0·8 | 8 | 0 |
новый раствор | 0,2 | 10 | х |
Используя формулу m=M٠α, получаем уравнение
0,2=10х
x=0,2: 10
х= 0,02
0,02 концентрация нового сплава, выразим в процентах. Ответ: 2%.
3) Если смешать 2 кг и 8кг растворов серной кислоты разной концентрации, то получим 12% раствор кислоты. При смешивании двух одинаковых масс тех же растворов получим 15% раствор. Определите первоначальную концентрацию каждого раствора.
Решение.
1 процесс
m (кг) | M (кг) | α | |
1 раствор | 0,01х·2=0,02х | 2 | 0,01х |
2 раствор | 0,01у·8=0,08у | 8 | 0,01у |
новый раствор | 0,02х+0,08у | 10 | 0,12 |
Используя формулу m=M٠α, получаем первое уравнение с двумя неизвестными 0,02х+0,08у=10٠0,12
2 процесс
m (кг) | M (кг) | α | |
1 раствор | 0,01х·1=0,01х | 1 | 0,01х |
2 раствор | 0,01у·1=0,01у | 1 | 0,01у |
новый раствор | 0,01х+0,01у | 2 | 0,15 |
Используя формулу m=M٠α, получаем второе уравнение с двумя неизвестными 0,01х+0,01у=2٠0,15
Решим эти уравнения в системе
Ответ: 10%; 20%.
4) В колбе было 800г 80% спирта. Провизор отлил из колбы 200г этого спирта и добавил в неё 200г воды. Определите концентрацию ( в %) полученного спирта.
Решение
m (г) | M (г) | α | |
было | 0,8٠800=640 | 800 | 0,8 |
отлил | 0,8·200=160 | 200 | 0,8 |
стало | 640-160=480 | 600 | 0,8 |
долил | 0 | 200 | 0 |
стало | 480 | 800 | х |
Используя формулу m=M٠α, получаем уравнение
480=800х
х=480:800
х=0,6
Выразим в процентах.
Ответ: 60%.
Этим же способом можно решить и такую задачу.
5) Свежие грибы содержали по массе 90% воды, а сухие 12%. Сколько получится сухих грибов из 22 кг свежих?
Решение.
За чистое вещество примем воду.
m (кг) | M (кг) | α | |
свежие грибы | 0,9·22=19,8 | 22 | 0,9 |
вода | (22-х)·1 | 22-х | 1 |
сухие грибы | 19,8-(22-х) | х | 0,12 |
Используя формулу m=M٠α, получаем уравнение
19,8-(22-х)=0,12х
х-2,2=0,12х
0,88х=2,2
х=2,2:0,88
х=2,5
Ответ: 2,5 кг
Задания для самостоятельного решения:
1. Смешали 300 г. 50%-го и 100 г. 30%-го раствора кислоты. Определите процентное содержание кислоты в полученной смеси.
2. Сколько нужно взять 10% — го и 30% – го растворов марганцовки, чтобы получить 200 г 16 % — го раствора марганцовки?
3. В 2 литра водного раствора, содержащего 60% кислоты, добавили 4 литра чистой воды. Определите процентное содержание кислоты в новом растворе.
4. Имеется два сплава. Первый сплав содержит 10% меди, второй — 40% меди. Масса второго сплава больше массы первого на 3 кг. Из этих двух сплавов получили третий сплав, содержащий 30% меди. Найдите массу третьего сплава. Ответ дайте в килограммах.
5. В сосуд, содержащий 5литров 14-процентного водного раствора некоторого вещества, добавили 5литров воды. Сколько процентов составляет концентрация получившегося раствора?
6. Смешав 30-процентный и 60-процентный растворы кислоты и добавив 10 кг чистой воды, получили 36-процентный раствор кислоты. Если бы вместо 10 кг воды добавили 10 кг 50-процентного раствора той же кислоты, то получили бы 41-процентный раствор кислоты. Сколько килограммов 30-процентного раствора использовали для получения смеси?
7. В 5% раствор кислоты массой 3,8 кг добавили 1,2 кг чистой воды. Чему стала равна концентрация раствора (в процентах)?
8. Чернослив содержит 25% влаги. Его получают из сливы, содержащей 90% влаги, путем сушки. Сколько нужно килограмм сливы, для получения 55 кг чернослива?
9. Имеются два сплава серебра с медью. В первом содержится 10% серебра, во втором — 25%. Сколько килограмм второго сплава нужно добавить 10кг первого, чтобы получить сплав 20% содержанием серебра?
10. Сергей смешал раствор, содержащий 20% кислоты и раствор, содержащий 40% той же кислоты. В итоге у него получился раствор, содержащий 32,5% кислоты, причём объём полученного раствора 4 литра. Сколько литров раствора, содержащего 20% кислоты, использовал Сергей при смешивании?
11. Один газ в сосуде А содержал 21% кислорода, второй газ в сосуде В содержал 5% кислорода. Масса первого газа в сосуде А была больше массы второго газа в сосуде В на 300 г. Перегородку между сосудами убрали так, что газы перемешались и получившийся третий газ теперь содержит 14,6% кислорода. Найдите массу третьего газа. Ответ дайте в граммах.
12. В сосуде А содержится 3 литра 17-процентного водного раствора вещества Х. Из сосуда В в сосуд А перелили 7 литров 19-процентного водного раствора вещества Х. Сколько процентов составляет концентрация полученного в сосуде А раствора?
13.Во сколько раз больше должен быть объём 5-процентного раствора кислоты, чем объём 10-процентного раствора той же кислоты, чтобы при смешивании получить 7-процентный раствор?
14. Во сколько раз больше должен быть объём 20-процентного раствора кислоты, чем объём 14-процентного раствора той же кислоты, чтобы при смешивании получить 18-процентный раствор?
15. Смешав 25-процентный и 95-процентный растворы кислоты и добавив 20 кг чистой воды, получили 40-процентный раствор кислоты. Если бы вместо 20 кг воды добавили 20 кг 30-процентного раствора той же кислоты, то получили бы 50-процентный раствор кислоты. Сколько килограммов 25-процентного раствора использовали для получения смеси?
16. Иван случайно смешал молоко жирностью 2,5% и молоко жирностью 6%. В итоге у него получилось 5 литров молока жирностью 4,6%. Сколько литров молока жирностью 2,5% было у Ивана до смешивания? Показать решение
Источник: https://shkolkovo.net/catalog/syuzhetnye_tekstovye_zadachi/na_rastvory_smesi_i_splavy © shkolkovo.net
Различные способы решения задач на смеси, сплавы , растворы

Различные способы решения задач на смеси, сплавы, растворы
Вайланд Анна Павловна, учитель математики МАОУ «Средняя общеобразовательная школа №3»
Балаково – 201 5 2

Проблема и гипотеза
- Рассматривая учебники по математике разных авторов, я увидела несколько совершенно разных по типу задач на растворы, а решения одних и тех же задач в одних учебниках были совершенно другими, нежели в других. Поэтому выдвинула свою гипотезу:
- Гипотеза: все задачи на растворы, сплавы и смеси делятся на несколько типов, а каждый из типов имеет конкретный способ решения.

Цели и задачи
- Систематизировать задачи на растворы, смеси и сплавы;
- Найти единый алгоритм решения этих задач;
- Научиться решать задачи по заданной теме.

ЕГЭ и межпредметная связь
- Созданный мною проект содержит материал по теме «Проценты» из курса математики, который может помочь также и при решении заданий на проценты не только в тестах ЕГЭ по математике за курс основной и средней школы, а так же при изучении химии, биологии, физики и других предметов.

Анализ ситуации
- В ходе проектной деятельности я проводила опрос «Можете ли вы решать задачи на растворы?». Вот результаты первого:
Конечно!
Скорее всего
Затруднились ответить
Нет
3
6
5
10

Введение
Для решения задач на концентрации нужно уметь рассуждать и решать задачи на дроби и проценты, на составление уравнений и их систем. Эти задачи решаются арифметически, применением линейного уравнения и их систем, и другие способы.

Основные понятия
- «Чистое вещество»
- «Примесь»
- Доли чистого вещества в смеси – « a »
- Чистое вещество – « m »
- Общее количество – « М »
a = m : M m = a M M = m : a

Классификация задач
На переливание
На понижение и повышение концентрации
На «высушивание»
На смешивание растворов разных концентраций

Задачи на понижение и повышение концентрации
Задача №1: сироп содержит 18% сахара. Сколько кг воды нужно добавить к 40 кг сиропа, чтобы содержание сахара составило 15% ?
Задача №2: сплав массой 36 кг содержит 45% меди. Сколько меди нужно добавить, чтобы новый сплав содержал 60% меди?

Решение задачи №1
II . Правило «креста»
18 15
15
0 3
I . Пусть надо добавить х кг воды. Заполним таблицу по условию задачи.
Значит, 40 кг – 15 частей тогда, чтобы получить 15% р-р нужно добавить 3 части воды
40:15 · 3=8 кг.
Ответ: 8 кг
Составим и решим уравнение:
0,15(40+х)=0,18*40
х =8
Ответ: 8 кг.
Было
α
18%=0,18
М(кг)
Стало
т (кг)
40
15%=0,15
0,18*40
40+ х
0,15(40+ х )

Задачи на высушивание
Задача №3:
Пчелы перерабатывают цветочный нектар в мёд, освобождая его от воды. Нектар содержит 84% воды, а полученный мёд — 20%. Сколько кг нектара нужно переработать пчелам для получения 1 кг мёда?

Решение задачи №3
- При решении таких задач надо разделять вещество на воду и «сухой остаток», масса которого не меняется в условиях задачи
1. Арифметический
1) 100-20=80% — составляет основное вещество от полученного мёда.
2) 1*0,8=0,8 кг – масса основное вещество в 1 кг.
3) 100-84 = 16% — составляет основное вещество от собранного нектара.
4) 0,8:0,16 = 5 кг нектара.
Ответ: 5 кг нектара нужно переработать пчелам для получения 1 кг мёда.
2. Правило «креста»
84 80
100
20 16
Значит, 1 кг составляет 16 частей, тогда 80 частей:
1 : 16 * 80 = 5 кг.
Ответ: 5 кг

Задачи, которые решаются с помощью систем линейных уравнений.
Имеется 2 раствора поваренной соли разной концентрации. Если слить вместе 100г первого раствора и 200г второго раствора, то получится 50%-ный раствор. Если же слить вместе 300г первого раствора и 200 г второго, то получится 42%-ный раствор. Найти концентрацию второго раствора.

Решение задачи №4
- Пусть процентное содержание соли в первом и втором растворах p% и q% соответственно, тогда по условиям задачи можно составить два уравнения:
100 p/100 + 200 q/100=50*(100+200)/100
300 p/100 + 200 q/100=42*(300+200)/100.
Упростив эти уравнения и решив систему, получим p=30 и q=60.
Следовательно, концентрация второго раствора равна 60%
Ответ. 60%

40-30
30-5
Старинная схема решения подобных задач
- Смешивая 5% и 40% растворы кислот, необходимо получить 30% раствор. В каком соотношении их необходимо взять?
Доли исходных продуктов в
конечном продукте
Параметры
исходных
продуктов
5%
40%
Параметры
конечного
продукта
30%
1-ый продукт
2-ой продукт
10 частей
25 частей
Ответ:
Соотношение первого и второго растворов – 10:25

Задачи на переливание
При решении этих задач выполняются следующие допущения: «закон сохранения масс» и «закон сохранения объёмов», как для всей смеси, так и для каждого её компонента. При этом плотности растворов изменяются не значительно и примерно равны плотности воды.

Теперь покажу, как графические иллюстрации к условию задач помогают найти правильный путь к ответу на вопрос задачи

Задача №5
Сначала приготовили 25%-ый водный раствор поваренной соли. Затем одну треть воды выпарили. Найти концентрацию получившегося раствора.

Решение задачи №5
До выпаривания:
NaCl
Н 2 О
Н 2 О
Н 2 О
25% 25% 25% 25%
После выпаривания:
NaCl
Н 2 О
Н 2 О
Сейчас соль стала составлять одну треть всего раствора или
Ответ:

Задача №6
Имеется два сплава золота и серебра. В одном количество этих металлов находится в отношении 1:9, а в другом 2:3. Сколько нужно взять каждого сплава, чтобы получить 15 кг нового сплава, в котором золота и серебро относилось бы как 1:4?

Решение задачи №6
НОВЫЙ СПЛАВ
Золота в нём 1/5 или 0,2
I СПЛАВ
Золота в нём 0,1 доля
II СПЛАВ
Золота в нём 2 / 5 или 0,4
1:9
2:3
1:4

Внесём данные в таблицу:
- Имеется два сплава золота и серебра. В одном количество этих металлов находится в отношении 1:9, а в другом 2:3. Сколько нужно взять каждого сплава, чтобы получить 15 кг нового сплава, в котором золота и серебро относилось бы как 1:4?
Название
элементов
Первый сплав
золото
серебро
Масса каждого элемента в сплаве
Второй сплав
золото
серебро
Общая масса сплава
0,1х кг
Новый сплав
X кг
Массовая доля элемента
0,4(15-х) кг
золото
серебро
(15- X) кг
0,1
0,2*15=3 кг
0,4
15 кг
0,2
Решение
0,1х + 0,4(15-х) =3
X =10
m (I сплава) =10 (кг)
m (II сплава) =15 – 10 =5 (кг) Ответ: 10 кг, 5 кг.

Вывод
При решении задач следует руководствоваться тем, что при соединении (разъединении) смесей с одним и тем же чистым веществом количества чистого вещества и общие количества смесей складываются (вычитаются). Складывать и вычитать доли и процентные содержания нельзя .

Вывод
- В ходе проектной деятельности я разделила задачи на растворы и смеси по типам и нашла единый алгоритм решения для каждого из типов, следовательно, моя гипотеза подтвердилась .

Повторный опрос «Можете ли вы решать задачи на растворы?»
ДО:
ПОСЛЕ:
1
3
6
5
14
9
10
Да!
Скорее всего
Затруднились ответить
Конечно!
Скорее всего
Затруднились ответить
Нет

Рефлексия
- Как видно из результатов опросов, проектная деятельность помогла мне лучше понять сущность процентных задач на растворы и смеси и научила правильно оценивать свои силы.

Список литературы
- М.В. Лурье и др. Задачи на составление уравнений, изд-во «Наука», М., 1976 г.
- Н.А. Терёшин Прикладная направленность школьного курса математики, «Просвещение», М., 1990 г.
- А.В. Шевкин Школьные математические олимпиады, изд-во «Русское слово», 2002г.
- О. Городнова Статья «Учимся решать задачи на «смеси и сплавы», г-та «Математика» №36 за 2004 г.

Интернет-ресурсы
1. Открытый банк заданий ЕГЭ по математике
http://www.mathege.ru
2. Шабон оформления презентации
http://www.pedsovet.su
Урок по теме: «Решение задач на растворы»
Решение задач на растворы
Уметь решать задачи есть искусство,
приобретающееся практикой.
Дьёрдь Пойа
(швейцарский математик)
Цель урока:
Задачи:
1. Образовательные:
освоить приемы решения задач по теме «Растворы»;
отработать умения и навыки учащихся при решении расчетных задач.
2. Воспитательные:
воспитывать умение контролировать внимание на всех этапах урока;
продолжить эстетическое воспитание через оформление доски, записей в тетради, использование наглядностей;
способствовать развитию коммуникативных качеств учащихся.
3. Развивающие:
развивать познавательные процессы, операции логического мышления (анализ, прогнозирование, умение делать выводы) при решении задач, через преобразование формул и подставления известных величин в конечную формулу или алгебраическое уравнение;
развивать познавательный интерес к предмету через решение задач, имеющих важное практическое значение;
способствовать развитию математической речи учащихся;
развивать самостоятельность учащихся при решении задач.
Тип урока: совершенствования знаний, умений, навыков
Методы обучения: наглядно-иллюстративный, частично-поисковый
Формы организации учебной деятельности:
Сколько ложек сахара ты кладешь в чай? Дома две, в гостях восемь. Шутка известная, но посмотрим на нее глазами химика. Вряд ли вам понравится в гостях такой чай слишком он сладкий, из-за неумеренного содержания сахара. Содержание сахара в растворе называется концентрацией. Ее можно выражать различными способами. Кстати, число ложек на стакан воды – способ вполне приемлемый, но только для кухни. Трудно представить себе химика, приготавливающего раствор таким способом. Один из самых распространенных способов выражения концентрации – это массовая доля вещества в растворе.
Общего рецепта для решения любой задачи нет, но целесообразно придерживаться определённой схемы её решения. Давайте уточним их.
Внимательно прочитать условие задачи.
Решение задачи всегда следует начать с анализа условия, и составления плана её решения.
Определить числовые данные задачи, которые при необходимости приводят в единую систему единиц (количественная сторона задачи).
Определить перечень химических веществ и явлений в их взаимосвязи, основные теоретические положения, необходимые для решения задачи (качественная сторона задачи).
Определить соотношения между качественными и количественными данными задачи в виде формул, уравнений, пропорций, законов.
Определить алгоритм решения задачи, т.е. последовательность её решения, начиная с конечного вопроса задачи до данных по условию.
Записываем краткое «дано».
1)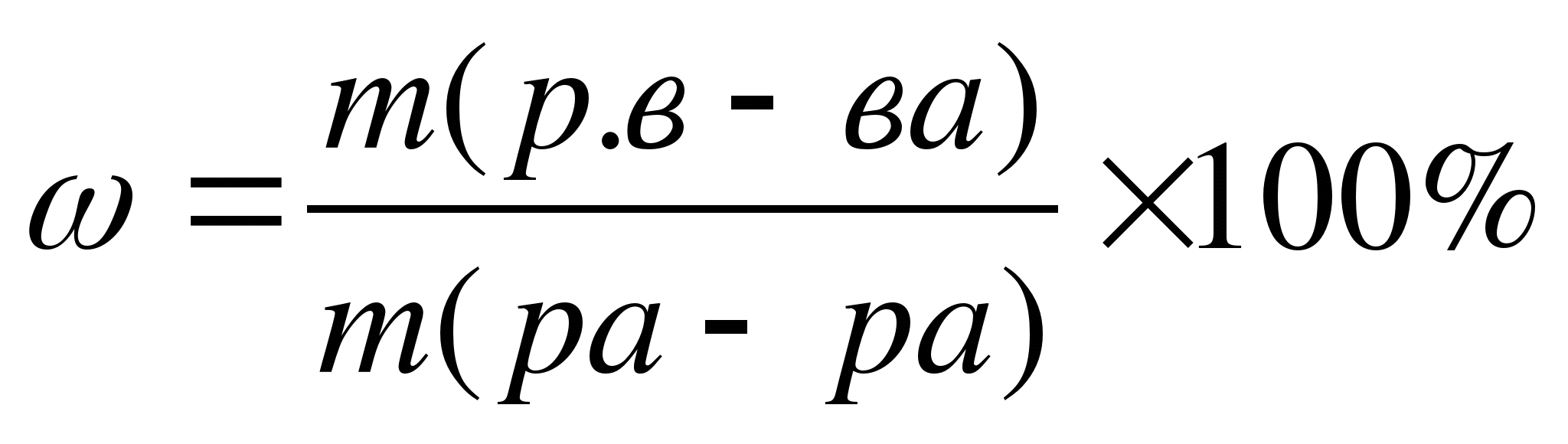 2)
2) 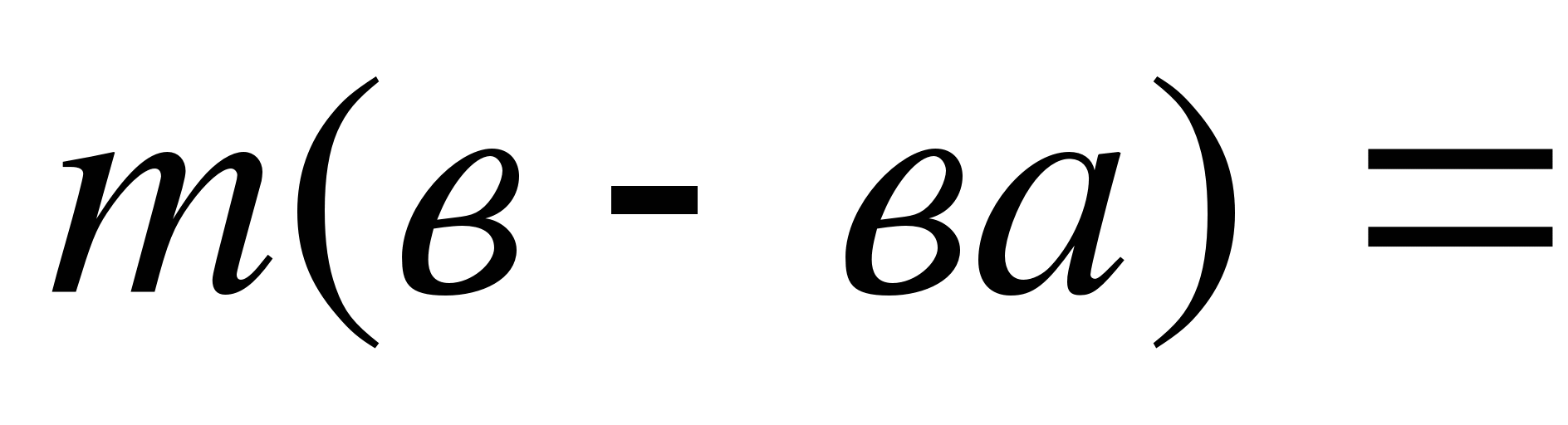
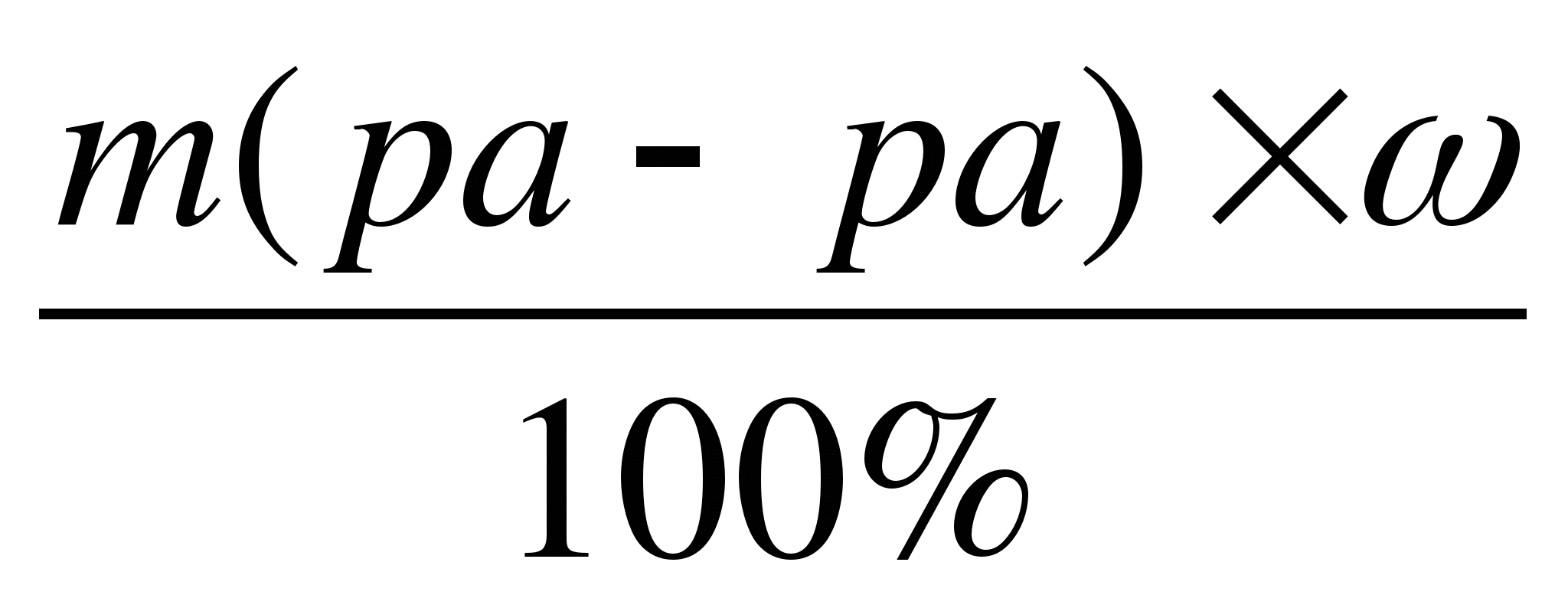 3)
3) 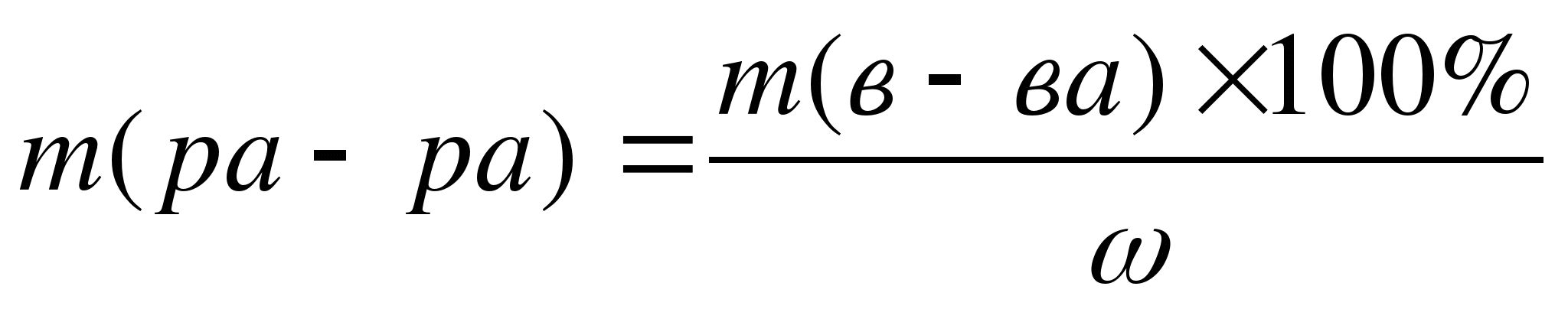
Удачи Вам пытливые умы!
На приготовление растворов
Задача №1.Смешали 200 г воды и 50 г гидроксида натрия. Определить массовую долю вещества в растворе.
1 способ – последовательный (формульный)
1.Использованные формулы.
1)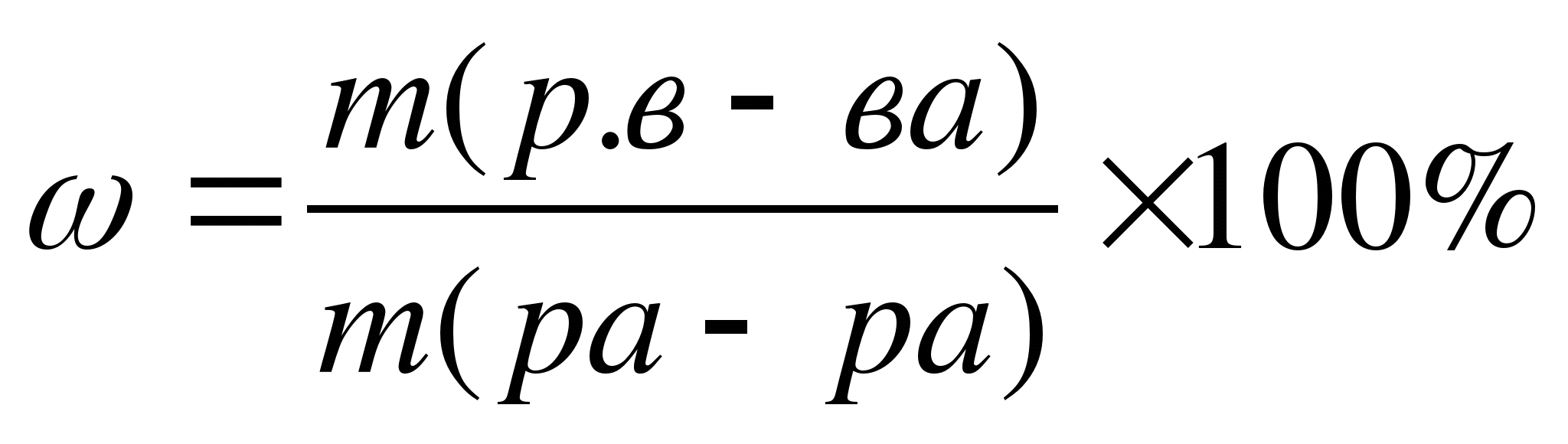 2)
2) 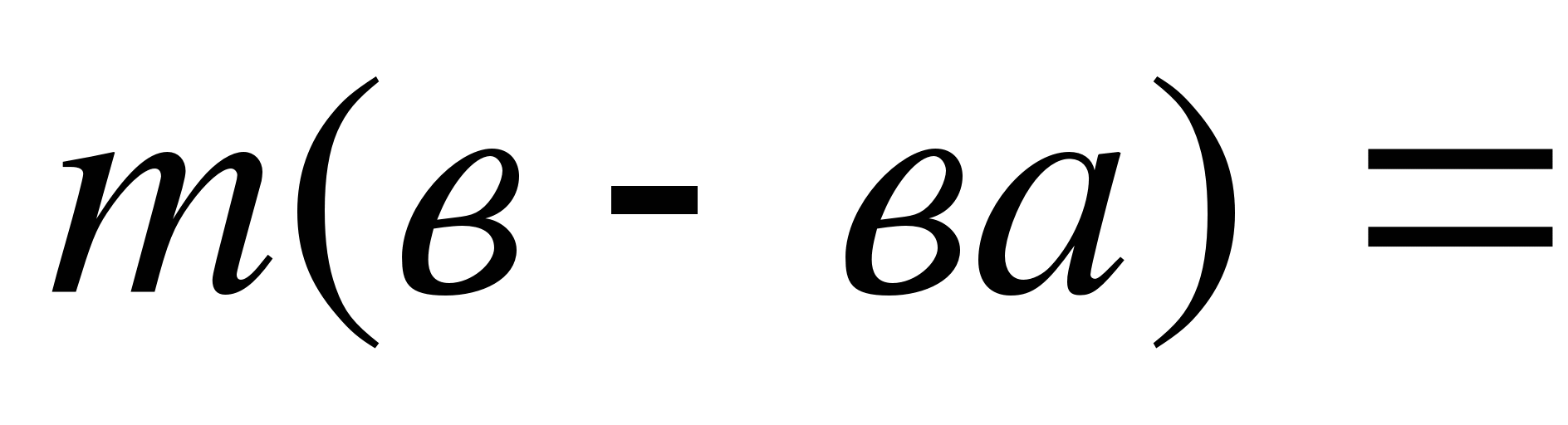
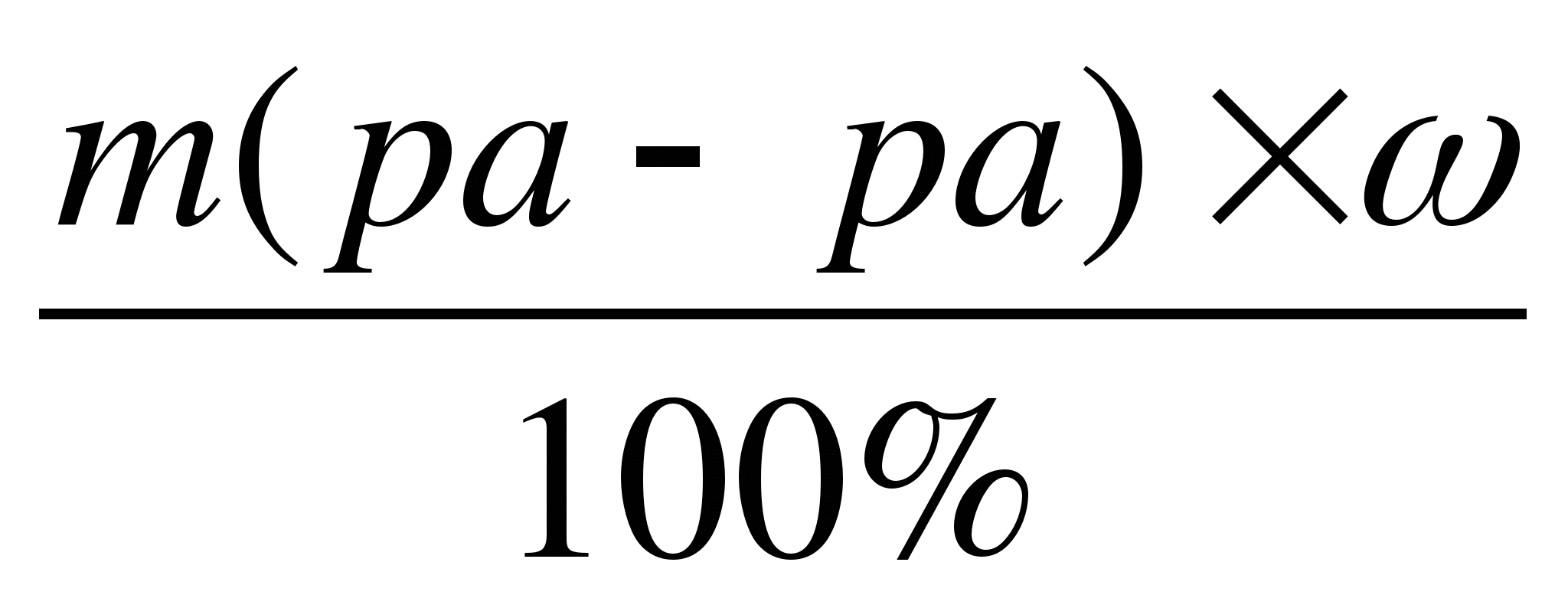 3)
3) 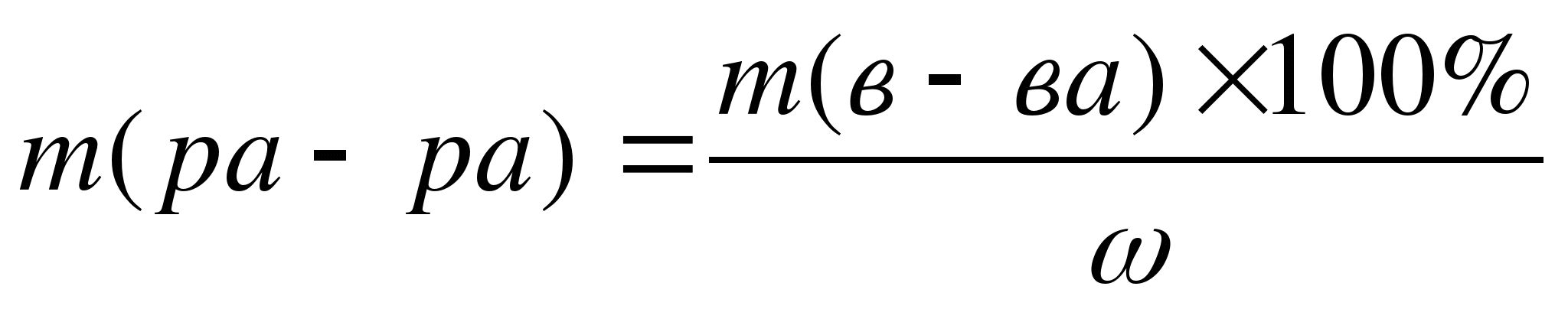
2. Если дается объем раствора, его надо пересчитать на массу. m(р-ра)= V×ρ.
3. Если надо рассчитать объем раствора, сначала рассчитывается масса, а затем объем. 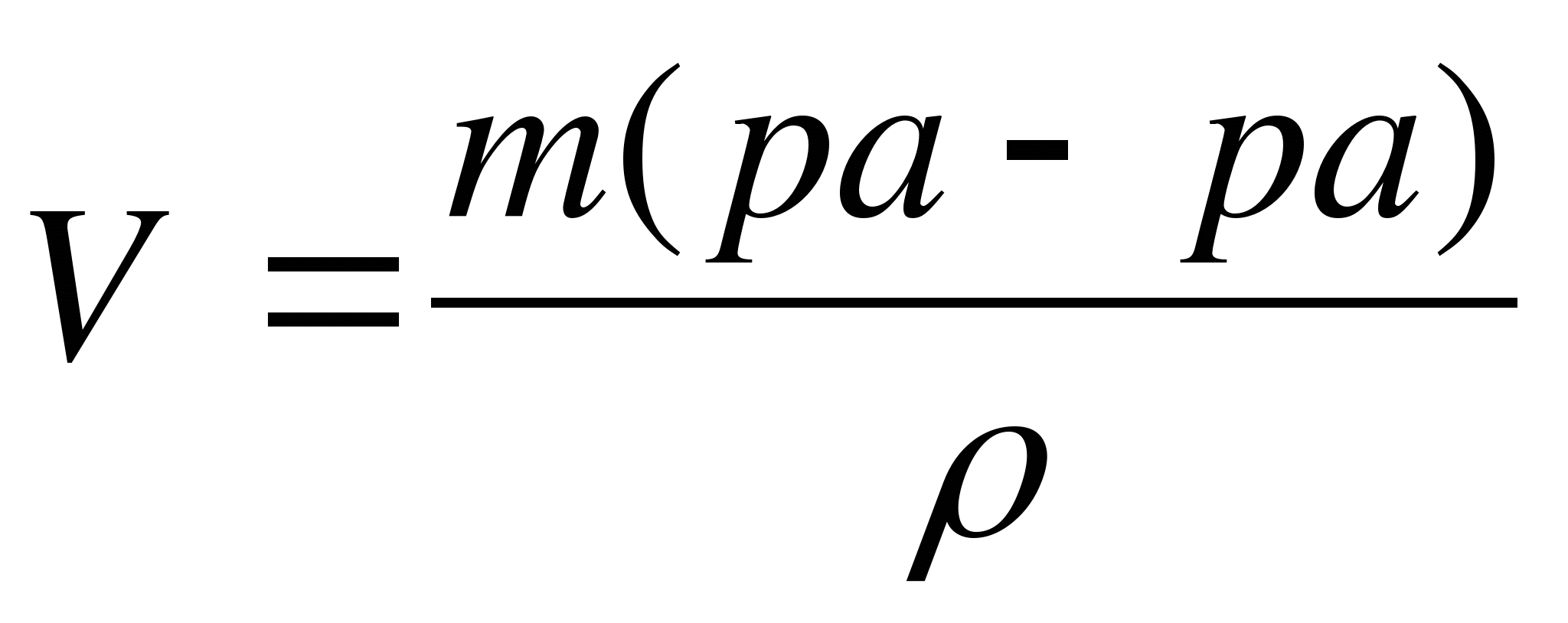
4.Если не известна масса раствора, и масса вещества, но известна массовая доля, (например она = 20%),
тогда масса раствора выражается через X; m(р-ра) = X;====>m(в-ва) = m(р-ра) × W в данном случае m (в-ва) = X× 0,2
Дано:
Решение
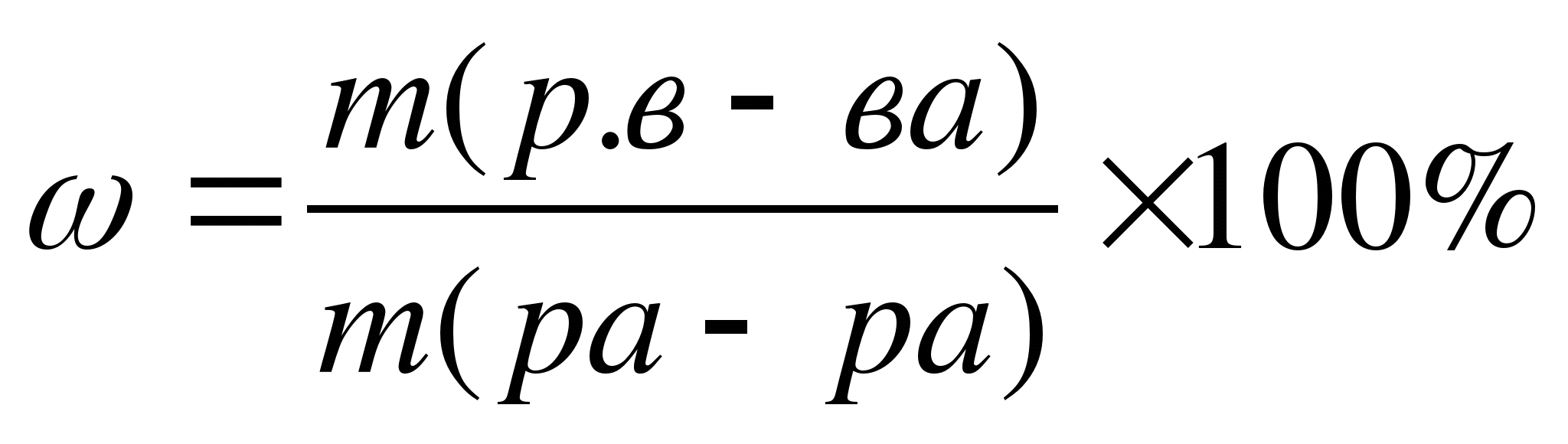
m(H2O)= 200г
m(NaOH)= 50г
т(р-ра) =m(в-ва) +m(H2O)
m(р-ра) = 50+ 200 = 250
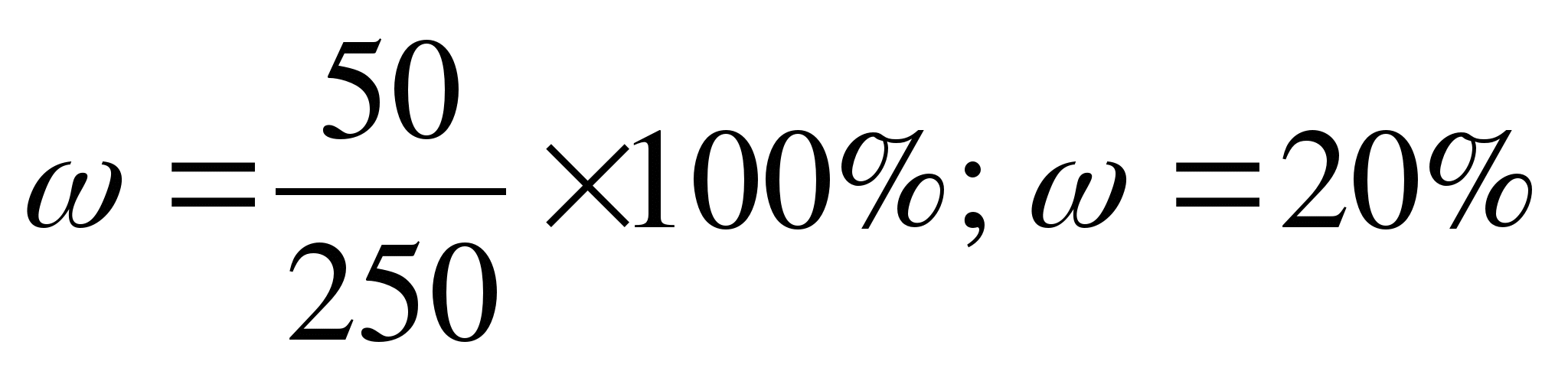
ω % =?
Ответ:ω=20%
2 способ — алгебраический
1.Исходим из того, что массы веществ исходных растворов равны массе вещества конечного раствора.
m(р-ра)1× ω1 + m( р-ра)2× ω2 =m(р-ра)3 × ω3
2. Масса вещества рассматривается как произведение массы раствора и массовой доли вещества в растворе.
3.ω удобнее выразить от единицы в долях.
4. в чистом веществе массовая доля равна 100% или 1.
5. массовая доля воды равна 0% или 0.
Составим схему согласно условию задачи.
РЕШЕНИЕ
3 способ — правило креста или конверт Пирсона
В данном случае массовые доли располагаются следующим образом:
слева сверху самая большая из приведённых в условии,
под ней самая маленькая,
в центре средняя,
по диагонали вычитаем от большей массовой доли меньшую, записываем результат
параллельно массовым долям на расстоянии от диагонали указываем соответствующие массы растворов.
ω берется в процентах.
в правой части диагонали получились три % отношения, мы выбираем наиболее удобное, так как при расчете любого отношения получим одинаковый результат.
Дано:
Предполагаем значение Х0<Х<100
m(в-ва)50г ————-100%
m(р-ра)250г————x%
3 способ — креста
В данном случае массовые доли располагаются следующим образом:
РЕШЕНИЕ
ω=20%0%
100-Х
___200
100
250
На смешивание растворов
Задача №1. Смешали 250г 30% и 150г 20% растворов серной кислоты. Выразите содержание вещества в процентах в приготовленном растворе.
2 Способ РЕШЕНИЕ
75+30 = 400x; x=0,26 или 26%
Ответ. W% = 26%
3 Способ
Предполагаем значение Х30>x>20
m(р-ра №1)250г ———30%
m(р-ра №2)150г———-20%
m(р-ра №3)400г———-x%
РЕШЕНИЕ
Ответ. W% = 26%
Х %
%
+
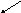
20%
30-Х
______150
10
400
Задача №2. Определите массу и концентрацию раствора, который нужно добавить к 13г 8% раствора, чтобы получить 40г 14% раствора.
2 способ РЕШЕНИЕ
Ответ. W% = 16,9%
3 Способ
Дано:
Предполагаем значение Х14< x >8
m(р-ра2)40-13——x%
m(р-ра3)40г——-14%
РЕШЕНИЕ
(× — 8)×27 =6×40; 27x -216 =240;27x =240-216; 27x =456; x =16,9%
Ответ: W% = 16,9%
1 4%
4%
+
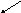
8%
Х-14
_____13г
Х-8
40г
На упаривание
Задача №1. 180г 15%-ного раствора хлорида бария выпарили до массы раствора 145г. Какова стала процентная концентрация раствора?
2 способ РЕШЕНИЕ
3 способ
Дано:
Предполагаем значение Х15 0
m(воды)180-145г—0%
m(р-ра3)145г——-x
РЕШЕНИЕ
Ответ: ω=18,6%
15%
+
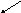

0%
Х-15
______35
Х
180
Действия с одним известным раствором
Задача №1. Определить массу 10% раствора карбоната натрия, который нужно добавить к 1020г 2%-ного раствора, чтобы получить 3%-ный раствор.
1Способ
Решениеm(р-ра) = 1020г
W%(1) =2%
W%(2) =10%
W%(3) =3%
1.рассчитаем массу вещества в 2-х%-ном растворе
m(в-ва) =1020×0,02 = 20,4г
2.выразим массу 10%-ного раствора через х
m10%-ного р-ра =х тогда m(в-ва) =Х× 0,1
3.выразим массу 3-х%-ного раствора
m 3-х%-ного =1020 + Х
m(в-ва) =(1020+Х) × 0,03
∑m(в-в) исходных растворов = m(в-ва) конечного раствора
20,4 + 0,1Х = (1020+Х)× 0,03; 20,4 +0,1Х = 30,6 +0,03Х; 0,1Х – 0,03Х =30,6- 20,4;
0,07Х =10,2; Х = 145,7(10%)
m 3%-ного р-ра = 1020+145,7 = 1165,7г
Ответ. m 10% = 145,7г
m 10%-?
2 способ РЕШЕНИЕ.
1020×0,02 +Х×0,1 =(1020 +Х)×0,03
20,4 + 0,1Х =30,6 + 0,03Х; 0,1Х – 0,03Х =10,2; Х = 145,7г.
3 способ
Дано:
Предполагаем значение Х0<Х<100
m (р-ра2)Хг ————-10%
m(р-ра3)1020+Х———3%
РЕШЕНИЕ
7
_____1020г
8
1020+Х
Задача №2. Определить массу 7%-ного раствора соли, в котором необходимо растворить ещё 20г этой соли, чтобы получить 12 %-ный раствор.
1 Способ
Решениеm(в-ва)=20г
W%=7%
W%=12%
m 7%=Х тогда m(в-ва)=Х×0,07
m 12% =Х+ 20 тогда m(в-ва) =(Х+ 20) ×0,12
∑m(в-в) исходных растворов = m(в-ва) конечного раствора
20 + 0,07Х=(Х+20)×0,12
17,6 =0,05Х; Х =352г
m7%- ?
Ответ:m 7% = 352г
2 Способ РЕШЕНИЕ.
3 Способ
Дано:
РЕШЕНИЕ88
_____Х
93
20+Х
Задача №3. Определить массу 20%-ного раствора соли, который нужно добавить к 40г 10%-ного раствора той же соли, чтобы получить 17%-ный раствор.
1Способ
Решениеm(р-ра) = 40г
W%= 10%
W% = 20%
W% =17%
m(в-ва) = 40× 0,1 =4г
m(20%) =Х тогда m(в-ва) =Х×0,2
m(17%)= 40 +Х тогда m(в-ва) =(40 + Х) × 0,17
40 +Х тогда m(в-ва) =(40 + Х) × 0,17
∑m(в-в) исходного раствора = m(в-в) нового раствора
4 + 0,2Х =(40+Х)× 0,17
4+ 0,2Х =6,8 + 0,17Х; 0,2Х – 0,17Х =6,8 – 4; 0,03Х = 2,8; Х =93,3г
m(20%) = ?
Ответ: m 20% = 93,3г
2 способ РЕШЕНИЕ.
3 способ Дано:
РЕШЕНИЕ
Ответ:93,3г
1 7%
7%
+
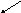
10%
3
_____40
10
40+Х
Задача №4. Рассчитайте массы 10 и 50%-ных растворов гидроксида калия, необходимых для приготовления 400г 25%-ного раствора.
1Способ РЕШЕНИЕ.
Решениеm(р-ра)=400г
W% =25%
W% =10%
W% =50%
m(в-ва) = 400 ×0,25 =100г
m(р-ра 10%) = Х тогда m(в-ва) =0,1Х
m(р-ра50%) =400-Х тогда m(в-ва) =(400-Х)× 0,5 = 200 – 0,5Х
∑веществ исходных растворов =массе вещества в новом растворе.
0,1Х+ 200 – 0,5Х = 100
100 = 0,4Х; Х = 250г(это 10%)
m(20%) =400 – 250 =150г
Ответ: m 10% =250г, m 50% = 150г
m(10%)=?
m(50%)=?
2 способ РЕШЕНИЕ.
3 способ Дано:
РЕШЕНИЕ
400 – 250 = 150(50%)
Ответ: m 10% =250г, m 50% = 150г
2 5%
5%
+
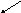
10%
25
____Хг
40
400г
Задачи на дом
1.Лимонная кислота содержится не только в лимонах, но также в незрелых яблоках, вишнях, ягодах смородины. Лимонная кислота часто используется в кулинарии и в домашнем хозяйстве (например, для выведения ржавых пятен с ткани). Определите, какая масса 10% и 70% раствора лимонной кислоты потребуется для приготовления 100 г 20% раствора?
2.Для засола огурцов используют 7% водный раствор поваренной соли (хлорида натрия NaCl). Именно такой раствор в достаточной мере подавляет жизнедеятельность болезнетворных микроорганизмов и плесневого грибка, и в то же время не препятствует процессам молочнокислого брожения. Рассчитайте массу соли и массу воды для приготовления 1 кг такого раствора.
Вариант 1.
Определите массы 10%-го и 90%-го растворов уксусной кислоты, необходимые для приготовления 500 г 30%-го раствора?
Сколько грамм йода и спирта нужно взять аптекарю, для приготовления 500 г 5% раствора йодной настойки?
Вариант 2.
Нужно приготовить 500 г столового уксуса (3%-раствор уксусной кислоты). Какое количество 90%-го раствора уксусной кислоты следует взять для этого?
В аптеке имеются растворы аммиака 5% и 25% . Как из них приготовить 1 кг нашатырного спирта (10% раствор аммиака).
1) Растения усваивают вещества в виде растворов;
2) Усвоение пищи связано с переводом питательных веществ в раствор;
3) Все природные воды являются растворами;
4) Растворами являются важнейшие физиологические жидкости – кровь, лимфа и т.д.
5) Многие технологические процессы в химической и других отраслях промышленности, например получение соды, удобрений, кислот, металлов, бумаги, протекают в растворах.
6) На лабораторных занятиях вы тоже работали в основном с растворами.
.
«Задачи на проценты и концентрацию».
Внеклассное мероприятие по математике
в 6 классе по теме «Задачи на смеси и сплавы»
Тема урок: «Задачи на проценты и концентрацию».
Цели: Формировать умение решать задачи на концентрацию, смеси и сплавы.
Задачи:
1.обобщить способы и методы решения задач на данную тематику;
2. развивать умения применять ранее изученные нестандартные методы для решения данного типа задач;
3.воспитание уверенности в себе, активности, умения работать в коллективе, стремление достигать поставленной цели.
План урока:
Организационный момент. (1 минута).
Подготовка учащихся к сознательному усвоению нового материала (5 минут).
1.Изучение нового материала (12 минут)
2.Решение задач на отработку формул (10 мин).
3.Физминутка (1 минута).
4.Самостоятельная работа (13минут).
5.Рефлексия (1 минута).
6.Подведение итогов. Домашнее задание (2 минуты).
Ход урока.
I. Организационный момент.
Задачи, которые мы будем решать, относятся к традиционным задачам математики. Они охватывают большой круг ситуаций: смешение товаров разной цены, жидкостей с различным содержанием соли, кислот разной концентрации, сплавление металлов с различным содержанием некоторого металла. Когда-то они имели исключительно практическое значение. В настоящее время эти задачи часто встречаются в тестах на выпускных экзаменах и на вступительных экзаменах в вузы.
Практическая деятельность.
1.Устная работа.
Найдите:
а) 50% от 80; б) 10% от 300 в) 1% от 30 г) 20% от 25
д)25% от 400 е) 5% от 200; ж) 50% от 17 з) 40% от 10
и) 70% от 30 к) 9% от 500.
2. Выразить десятичной дробью, а потом обыкновенной:
1.25%, 10%, 50%, 75%, 125%.
3.Указать в виде процентов: 0,7; 0,04; 1,3.
4.Найти число, 15% которого равны 30.
5.Из 25 семян взошло 24 семени. Найдите процент всхожести.
Изучение нового материала.
(Формирование умений и навыков.)
Задача . Имеются 3 раствора морской соли в воде: первый раствор содержит 10% соли, второй содержит 15 % соли и третий – 20% соли. Смешали 130 мл первого раствора, 200 мл второго раствора и 170 мл третьего раствора.
Определите, сколько процентов составляет морская соль в полученном растворе
Решение:
130 × 0,1 = 13 (г) столько морской соли содержится в 130 мл первого раствора .
200 × 0,15 = 30 (г) морской соли содержится в 170 мл второго раствора.
170 × 0,2 = 34 (г) морской соли содержится в 200 мл третьего раствора
После того, как эти растворы смешали, получили 130 + 200 + 170 = 500 (мл) нового раствора, который содержит 13 + 30 + 34 = 77 (г) морской соли.
Найдем, сколько процентов составляют 77 (г) морской соли от 500 мл раствор
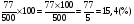 .
.
Ответ: 15,4 %
Задачи по данной теме (смешение жидкостей, товаров, сплавление металлов) имеют однотипные решения.
Масса соли в первом растворе равна( р1*V1)/100
Масса соли во втором растворе равна (р2*V2)/100
Масса соли в третьем растворе равна (р3*V3)/100
Процентное содержание соли в растворе равно
р =( ( (p1V1+p2V2+p3V3)/(V1+V2+V3))/100
Задача. Сколько граммов воды надо добавить к 50 г раствора, содержащего
8 % соли, чтобы получить 5 % — ный раствор?
Заметим, что задачи на концентрацию вызывают наибольшие затруднения у учащихся. Поэтому следует подробнее остановиться на решении данной задачи, начав не с составления уравнения, а с вопросов, которые помогут учащимся уяснить условие и осознанно подойти к её решению.
Вопросы учащимся:
1) Сколько граммов соли содержится в имеющемся растворе?
(50×0,08 = 4 г).
2) Если к имеющемуся раствору добавить воды, изменится ли массовая составляющая соли? (Нет.)
3) При добавлении воды изменится ли процентное содержание соли в растворе? (Да.)
4) Если к имеющемуся раствору добавить х г воды, какова станет масса всего раствора? (50 + х). Сколько граммов соли в нем будет? (4г).
5) Каково процентное содержание соли в новом растворе? (5%.)
6) Какую пропорцию, согласно полученным результатам, можно составить?
4 г соли – 5%
(50 + х) г раствора – 100%.
Имеем уравнение:
5(50 + х) = 400, откуда х = 30.
Ответ: 30г.
Работа над задачей.
Задача №1.
Сколько граммов воды надо добавить к 180 г сиропа, содержащего 25% сахара, чтобы получить 20%-ый сироп?
Решение.
Веществом, которое не меняет своей массы в новом растворе, является сахар. Поэтому найдем его массу.
180×0,25 = 45 г.
После добавления воды 45 г сахара в новом растворе будут составлять 20 % от всей массы. Пусть х г воды надо добавить, тогда масса нового раствора составляет (180 + х) г.
Имеем пропорцию:
45 г сахара – 20%;
(180 + х) г сиропа – 100%.
Из пропорции составим уравнение:
20(180 + х)= 4500, откуда х = 45.
Ответ: 45г.
Самостоятельная работа и осуществление контроля (работа в группах)
Задача №1
Сколько литров воды нужно добавить в 2л водного раствора, содержащего 60% кислоты, чтобы получить 20% раствор кислоты?
Решение:
60 : 20 = 3(раза) уменьшиться процентное содержание кислоты в растворе
2*3 = 6(л) , значит надо добавить 4(л) воды.
Ответ: 4л.
Задача № 2
В сосуд, содержащий 5 литров 12-процентного водного раствора некоторого вещества, добавили 7 литров воды. Сколько процентов составляет концентрация получившегося раствора?
Решение:
5+ 7 =12(л) стало.
(5 * 12%) : 12 = 5%
Ответ: 5%
Задача № 3
Смешали 4 литра 15-процентного водного раствора некоторого вещества с 6 литрами 25-процентного водного раствора этого же вещества. Сколько процентов составляет концентрация получившегося раствора?
Решение:
Р = (0.25* 6 + 0.15 * 4)/(4+6) = 0.21 = 21%
Ответ: 21 %
2-ой способ
15% = 0,15
0,15
 4 = 0,6(л) вещества в I сосуде
4 = 0,6(л) вещества в I сосуде25% = 0,25
0,25
 6 = 1,5(л) вещества во II сосуде
6 = 1,5(л) вещества во II сосуде0,6 + 1,5 = 2,1 (л) – количество вещества в полученном растворе
4 + 6 = 10(л) – количество полученного раствора
 — концентрация полученного раствора.
— концентрация полученного раствора.
Ответ: 21%
Рефлексия
Вопросы учащимся:
— Как найти процент от величины?
— Как найти величину по ее проценту?
— Как найти, сколько процентов одна величина составляет от другой величины?
— Каков алгоритм решения задач на концентрацию, в которых к имеющемуся раствору добавляют одно из составляющих его веществ?
— По какому плану решаются задачи на смешивание нескольких растворов
Домашние задание стр 90 № 1330,1363 ,1336
Задачи на концентрацию, смеси, сплавы.
Задачи на концентрацию традиционно являются слабым звеном в подготовке школьников и абитуриентов, кажутся многим из них довольно сложными. Обучение решению этих задач начинается с 6 класса и продолжается на продолжении всей основной школы. Однако, в 11 классе эти задачи у большинства вызывают затруднения. При повторении можно начинать с решения самых простых задач, взятых из учебника математики для 6 класса. В таких задачах речь обычно идет о растворах некоторого вещества в другом веществе и об изменении концентрации этого вещества после каких-либо манипуляций. При этом водные растворы, смеси, сплавы играют сходные роли и позволяют лишь несколько разнообразить сюжеты задач без изменения математического содержания. Ключевой при решении таких задач является идея отслеживания изменений, происходящих с «чистым» веществом.
Анализ.
Урок проводила в 5 А – классе.
На уроке присутствовало- 21 уч
Самостоятельная работа проводилась в группах. В группе – по 7 уч.
Самые лучшие результаты показала – 1гр (решили все три задания верно),
2 группа – верно решила 2-е и 3-е задание
3группа –решила все три задания но были допущены ошбка при вычислениях.
На 5 – 2уч
На 4 – 5уч
Так как тема новая -неудовлетворительные оценки не выстовляла.
Вывод – продолжить работу по теме «Задачи на концентрацию, смеси, сплавы» в следующем учебном году.
Текстовые задачи: проценты, сплавы, растворы
Цели: Оказать методическую помощь при подготовке выпускников к ЕГЭ по математике; проработать алгоритм решения химических задач.
Задачи.
Обучающие:
- активизировать знания учащихся по теме «Массовая доля вещества в растворе»;
- познакомить учащихся с алгоритмом решения задач на растворы и сплавы «методом стаканчиков»;
- закрепить умение решать задачи на растворы и сплавы;
- продолжить подготовку учащихся к сдаче ЕГЭ.
Развивающие:
- развивать познавательный интерес, реализуя межпредметные связи курсов химии и математики;
- развивать алгоритмический стиль мышления.
Воспитательные:
- продолжать формирование мотивации учебной деятельности, положительного отношения к знаниям;
- формировать информационную и коммуникативную культуру.
Оборудование. Компьютер, экран, мультимедийный проектор, презентация с алгоритмами решения задач на массовую долю вещества в растворе «методом стаканчиков», многовариантная проверочная работа с задачами трёх уровней сложности (10 вариантов), ключ к ответам.
Методы. Объяснительно-иллюстративный, репродуктивный.
План урока
1. Вводная часть:
– организационный момент;
– мотивация познавательной деятельности;
– сообщение темы и постановка целей урока.
2. Активизация знаний по теме «Массовая доля вещества в растворе».
3. Знакомство учащихся с алгоритмом решения задач на растворы и сплавы «методом стаканчиков».
4. Закрепление умения решать задачи на растворы и сплавы при помощи многовариантной проверочной работы с задачами трёх уровней сложности.
5. Самопроверка. Самооценка. Рефлексия.
6. Домашнее задание.
7. Подведение итогов.
Приложение 4
Ход урока
1. Вводная часть.
Проверка готовности класса к уроку, приветствие.
Учитель. У нас на уроке химии сегодня гости – это учителя математики. Как вы считаете, какая связь существует между учениками 11 класса, учителями математики и уроком химии?…. Да, это ЕГЭ по математике, в котором имеют место и химические задачи. С этими задачами вы уже встречались в 9 классе при сдаче экзаменов по химии и математике. А также умение решать эти задачи вам понадобится при подготовке к ЕГЭ по химии ( это задание В 9) и к ЕГЭ по математике (задание В 13). Поэтому закономерна тема нашего урока.
«Текстовые задачи: проценты, сплавы, растворы».
Далее учитель подводит учащихся к постановке целей урока.
- Повторить понятие массовой доли.
- Познакомиться с алгоритмом решения задач на растворы и сплавы методом стаканчиков».
- Отработать умение решать задачи на растворы и сплавы.
2. Активизация знаний по теме «Массовая доля вещества в растворе».
Как найти массу раствора?
– Надо сложить массу вещества и массу растворителя.
р-ра = т в-ва + т р-ля (запись на доске)т
Демонстрация приготовления раствора медного купороса (Приложение 1).
Что является основной характеристикой растворов?
– Массовая доля растворенного вещества.
Как вычислить массовую долю?
– Надо найти отношение массы растворенного вещества к массе раствора.
ω = т в-ва : т р-ра ۰ 100% (запись на доске)
В каких единицах измерения выражается массовая доля вещества?
– В процентах или долях единицы.
Это основные теоретические сведения, необходимые для успешного решения задач на растворы и сплавы.
3. Знакомство учащихся с алгоритмом решения задач на растворы и сплавы «методом стаканчиков»
Схема и уравнение для решения задач с процентами.
Главное правило в задачах с растворами.
Решение задачи №1.
Составляется схема приготовления раствора. Затем составляется уравнение решается относительно х.
Решение задачи № 2.
Решение задачи №3.
Решение задачи №4.
4. Закрепление умения решать задачи на растворы и сплавы при помощи многовариант-ной проверочной работы с задачами трёх уровней сложности (Приложение 2).
5. Двое учащихся с заданием 3-го уровня работают у доски. Остальные выполняют решение задач на листочках самостоятельно. Ученики оценивают свою работу, сверив ответы с матрицей.
- За правильное решение задачи первого уровня – «3» .
- За правильное решение задачи второго уровня – «4».
- За правильное решение задач первого и второго уровня -«5».
- За правильное решение задачи третьего уровня –«5».
Матрица ответов для самопроверки.
Рефлексия.
6. Домашнее задание.
Поменяться с соседом вариантом и решить его дома.
7. Подведение итогов урока (Приложение 3).
 4 = 0,6(л) вещества в I сосуде
4 = 0,6(л) вещества в I сосуде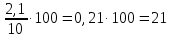 — концентрация полученного раствора.
— концентрация полученного раствора.