Периодический закон Менделеева Википедия
 Памятник на территории Словацкого технологического университета (Братислава), посвящённый Д. И. Менделееву
Памятник на территории Словацкого технологического университета (Братислава), посвящённый Д. И. МенделеевуПериодический закон — фундаментальный закон природы, открытый Д. И. Менделеевым в 1869 году при сопоставлении свойств известных в то время химических элементов и величин их атомных масс.
Определения[ | ]
После открытия периодического закона Д. И. Менделеев два года совершенствовал его формулировку и окончательно оформил её в следующем виде (1871):
 | Свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса[1]. |  |
С развитием атомной физики и квантовой химии Периодический закон получил строгое теоретическое обоснование. Благодаря классическим работам Й. Ридберга (1897), А. Ван-ден-Брука (1913), Г. Мозли (1913) был раскрыт физический смысл порядкового (атомного) номера элемента. Позднее была создана квантово-механическая модель периодического изменения электронного строения атомов химических элементов по мере возрастания зарядов их ядер (Н. Бор, В. Паули, Э. Шрёдингер,
ru-wiki.ru
ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА — это… Что такое ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА?
- ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА
ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА
, в химии — закон, сформулированный Дмитрием Ивановичем МЕНДЕЛЕЕВЫМ в 1869 г., согласно которому свойства химических ЭЛЕМЕНТОВ находятся в периодической зависимости от их ОТНОСИТЕЛЬНОЙ АТОМНОЙ МАССЫ. Объединение химических элементов в группы на основании этого закона предшествовало созданию ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ. На основе пробелов в этих группах Менделеев смог предсказать существование и свойства неоткрытых элементов. Однако в его таблице были некоторые отклонения от правила, объяснения которым смогли найти, лишь когда Генри МОЗЛИ в своей работе о РЕНТГЕНОВСКИХ ЛУЧАХ открыл, что периодичность связана с атомным номером (в большей степени, чем с атомной массой), а затем, несколько позже, были открыты ИЗОТОПЫ.
Научно-технический энциклопедический словарь.
- ПЕРИОДИЧЕСКАЯ ТАБЛИЦА
- ПЕРИСКОП
Смотреть что такое «ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА» в других словарях:
ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА
периодический закон Менделеева — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN periodic law … Справочник технического переводчика
периодический закон Менделеева — см. Периодическая система химических элементов. * * * ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА, см. Периодическая система элементов Менделеева (см. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ МЕНДЕЛЕЕВА) … Энциклопедический словарь
периодический закон Менделеева — Mendelejevo periodinis dėsnis statusas T sritis fizika atitikmenys: angl. periodic law of Mendeleef vok. Periodengesetz von Mendelejew, n rus. периодический закон Менделеева, m pranc. loi périodique de Mendéléev, f … Fizikos terminų žodynas
Периодический закон Менделеева
— фундаментальный закон, устанавливающий периодическое изменение свойств химических элементов в зависимости от увеличения зарядов ядер их атомов. Открыт Д. И. Менделеевым в 1869 при сопоставлении свойств всех известных в то время элементов… … Большая советская энциклопедияПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА — Открыт Д. И. Менделеевым в процессе работы над учебником Основы химии (1868 1871). Первоначально была разработана (1 марта 1869) таблица Опыт системы элементов, основанной на их атомном весе и химическом сходстве (см. Периодическая система… … Химическая энциклопедия
ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА — см. Периодическая система химических элементов … Естествознание. Энциклопедический словарь
Периодический закон — Памятник на территории Словацкого технологического университета (Братислава), посвященный Д. И. Менделееву Периодический закон фундаментальный закон природы, открытый Д. И. Ме … Википедия
ЗАКОН МЕНДЕЛЕЕВА (ПЕРИОДИЧЕСКИЙ ЗАКОН Д И МЕНДЕЛЕЕВА) — ЗАКОН МЕНДЕЛЕЕВА (ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА) в 1869 г. русский учёный открыл и сформулировал фундаментальный закон природы. Современная формулировка периодического закона: «Свойства простых тел, формы и свойства соединений элементов… … Большая политехническая энциклопедия
МЕНДЕЛЕЕВА ПЕРИОДИЧЕСКИЙ ЗАКОН — см. Периодическая система элементов Менделеева … Большой энциклопедический политехнический словарь
dic.academic.ru
Ответы@Mail.Ru: Что такое периодический закон?
Периодический закон Д. И. Менделеева — фундаментальный закон, устанавливающий периодическое изменение свойств химических элементов в зависимости от увеличения зарядов ядер их атомов. Открыт Д. И. Менделеевым в марте 1869 года при сопоставлении свойств всех известных в то время элементов и величин их атомных масс (весов) . Термин «периодический закон» Менделеев впервые употребил в ноябре 1870, а в октябре 1871 дал окончательную формулировку Периодического закона: «…свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса». [1] Графическим (табличным) выражением периодического закона является разработанная Менделеевым периодическая система элементов.
Периодический закон — фундаментальный закон природы, открытый Д. И. Менделеевым в 1869 году при сопоставлении свойств известных в то время химических элементов и их величин атомных масс.
touch.otvet.mail.ru
Периодический закон Менделеева — Большая советская энциклопедия
Периоди́ческий закон Менделеева
Фундаментальный закон, устанавливающий периодическое изменение свойств химических элементов в зависимости от увеличения зарядов ядер их атомов. Открыт Д. И. Менделеевым в 1869 при сопоставлении свойств всех известных в то время элементов и величин их атомных весов. Термин «периодический закон» Менделеев впервые употребил в ноябре 1870, а в октябре 1871 дал окончательную формулировку П. з.: «… свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса» («Периодический закон. [Основные статьи]», 1958, с. 111). Графическим (табличным) выражением П. з. явилась разработанная Менделеевым Периодическая система элементов.
Физический смысл П. з. был вскрыт лишь после выяснения того, что заряд ядра атома возрастает при переходе от одного химического элемента к соседнему (в периодической системе) на единицу элементарного заряда. Численно заряд ядра равен порядковому номеру (атомному номеру Z) соответствующего элемента в периодической системе, то есть числу протонов в ядре, в свою очередь равному числу электронов соответствующего нейтрального атома (см. Атом). Химические свойства атомов определяются структурой их внешних электронных оболочек, периодически изменяющейся с увеличением заряда ядра, и, следовательно, в основе П. з. лежит представление об изменении заряда ядра атомов, а не атомной массы элементов. Наглядная иллюстрация П. з.— кривые периодические изменения некоторых физических величин (ионизационных потенциалов, атомных радиусов, атомных объёмов) в зависимости от Z (см. Атомная физика). Какого-либо общего математического выражения П. з. не существует.
П. з. имеет огромное естественнонаучное и философское значение. Он позволил рассматривать все элементы в их взаимной связи и прогнозировать свойства неизвестных элементов. Благодаря П. з. многие научные поиски (например, в области изучения строения вещества — в химии, физике, геохимии, космохимии, астрофизике) получили целенаправленный характер. П. з.— яркое проявление действия общих законов диалектики, в частности закона перехода количества в качество.
Лит. см. при ст. Периодическая система элементов.
Источник: Большая советская энциклопедия на Gufo.me
Значения в других словарях
- ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА — ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА, в химии — закон, сформулированный Дмитрием Ивановичем МЕНДЕЛЕЕВЫМ в 1869 г., согласно которому свойства химических ЭЛЕМЕНТОВ находятся в периодической зависимости от их ОТНОСИТЕЛЬНОЙ АТОМНОЙ МАССЫ. Научно-технический словарь
- ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА — ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА — см. Периодическая система элементов Менделеева. Большой энциклопедический словарь
- периодический закон Менделеева — ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА Открыт Д. И. Менделеевым в процессе работы над учебником «Основы химии» (1868–1871). Первоначально была разработана (1 Марта 1869) таблица «Опыт системы элементов, основанной на их атомном весе и химическом сходстве» (см. Химическая энциклопедия

gufo.me
Периодический закон Менделеева — это… Что такое Периодический закон Менделеева?
- Периодический закон Менделеева
- фундаментальный закон, устанавливающий периодическое изменение свойств химических элементов в зависимости от увеличения зарядов ядер их атомов. Открыт Д. И. Менделеевым в 1869 при сопоставлении свойств всех известных в то время элементов и величин их атомных весов. Термин «периодический закон» Менделеев впервые употребил в ноябре 1870, а в октябре 1871 дал окончательную формулировку П. з.: «… свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса» («Периодический закон. [Основные статьи]», 1958, с. 111). Графическим (табличным) выражением П. з. явилась разработанная Менделеевым Периодическая система элементов.
Физический смысл П.
з. был вскрыт лишь после выяснения того, что заряд ядра атома возрастает при переходе от одного химического элемента к соседнему (в периодической системе) на единицу элементарного заряда. Численно заряд ядра равен порядковому номеру (атомному номеру Z) соответствующего элемента в периодической системе, то есть числу протонов в ядре, в свою очередь равному числу электронов соответствующего нейтрального атома (см. Атом). Химические свойства атомов определяются структурой их внешних электронных оболочек, периодически изменяющейся с увеличением заряда ядра, и, следовательно, в основе П. з. лежит представление об изменении заряда ядра атомов, а не атомной массы элементов. Наглядная иллюстрация П. з.— кривые периодические изменения некоторых физических величин (ионизационных потенциалов, атомных радиусов, атомных объёмов) в зависимости от Z (см. Атомная физика). Какого-либо общего математического выражения П. з. не существует.
П. з. имеет огромное естественнонаучное и философское значение. Он позволил рассматривать все элементы в их взаимной связи и прогнозировать свойства неизвестных элементов. Благодаря П. з. многие научные поиски (например, в области изучения строения вещества — в химии, физике, геохимии, космохимии, астрофизике) получили целенаправленный характер. П. з.— яркое проявление действия общих законов диалектики, в частности закона перехода количества в качество.
Большая советская энциклопедия. — М.: Советская энциклопедия. 1969—1978.
- Периодические решения
- Периодичность плодоношения
Смотреть что такое «Периодический закон Менделеева» в других словарях:
ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА — см. Периодическая система элементов Менделеева … Большой Энциклопедический словарь
ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА — ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА, в химии закон, сформулированный Дмитрием Ивановичем МЕНДЕЛЕЕВЫМ в 1869 г., согласно которому свойства химических ЭЛЕМЕНТОВ находятся в периодической зависимости от их ОТНОСИТЕЛЬНОЙ АТОМНОЙ МАССЫ. Объединение… … Научно-технический энциклопедический словарь
периодический закон Менделеева — — [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN periodic law … Справочник технического переводчика
периодический закон Менделеева — см. Периодическая система химических элементов. * * * ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА, см. Периодическая система элементов Менделеева (см. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ МЕНДЕЛЕЕВА) … Энциклопедический словарь
периодический закон Менделеева — Mendelejevo periodinis dėsnis statusas T sritis fizika atitikmenys: angl. periodic law of Mendeleef vok. Periodengesetz von Mendelejew, n rus. периодический закон Менделеева, m pranc. loi périodique de Mendéléev, f … Fizikos terminų žodynas
ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА — Открыт Д. И. Менделеевым в процессе работы над учебником Основы химии (1868 1871). Первоначально была разработана (1 марта 1869) таблица Опыт системы элементов, основанной на их атомном весе и химическом сходстве (см. Периодическая система… … Химическая энциклопедия
ПЕРИОДИЧЕСКИЙ ЗАКОН МЕНДЕЛЕЕВА — см. Периодическая система химических элементов … Естествознание. Энциклопедический словарь
Периодический закон — Памятник на территории Словацкого технологического университета (Братислава), посвященный Д. И. Менделееву Периодический закон фундаментальный закон природы, открытый Д. И. Ме … Википедия
ЗАКОН МЕНДЕЛЕЕВА (ПЕРИОДИЧЕСКИЙ ЗАКОН Д И МЕНДЕЛЕЕВА) — ЗАКОН МЕНДЕЛЕЕВА (ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА) в 1869 г. русский учёный открыл и сформулировал фундаментальный закон природы. Современная формулировка периодического закона: «Свойства простых тел, формы и свойства соединений элементов… … Большая политехническая энциклопедия
МЕНДЕЛЕЕВА ПЕРИОДИЧЕСКИЙ ЗАКОН — см. Периодическая система элементов Менделеева … Большой энциклопедический политехнический словарь
dal.academic.ru
Периодический закон Менделеева
Утверждение атомно-молекулярной теории на рубеже XVIII–XIX вв. сопровождалось бурным ростом числа известных химических элементов. Только за первое десятилетие XIX в. было открыто 14 новых элементов. Английский химик Г. Дэви (1778–1829) за один год с помощью электролиза получил шесть новых элементов– натрий, калий, магний, кальций, стронций, барий. К 1830 г. число известных элементов достигло 55.
Существование такого количества элементов, весьма разнообразных по свойствам, озадачивало химиков и требовало систематизации элементов. Некоторые ученые, заметив сходства нескольких элементов, объединяли их в отдельные группы, однако причины заметного изменения свойств не были установлены. Периодический закон химических элементов– фундаментальный закон природы – был открыт великим русским химиком Д.И. Менделеевым в 1869 г. в результате систематизации химических элементов в зависимости от их атомных весов: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
Несмотря на огромную значимость открытия Менделеева, оно представляло лишь гениальное эмпирическое обобщение фактов, а их физический смысл долго оставался непонятным. Причина заключалась в том, что в XIX в. отсутствовали какие-либо представления о сложном строении атома. Сам Менделеев по этому поводу писал: «Периодическая изменяемость простых и сложных тел подчиняется некоторому высшему закону, природу которого, а тем более причину еще нет средств охватить. По всей вероятности, она кроется в основных началах внутренней механики атомов и частиц».
Данные о строении атомного ядра и распределении электронов в атомах позволяют по-новому рассмотреть периодический закон, который в современной формулировке гласит: свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости от заряда ядра атомов (порядкового номера).
Такая формулировка закона не противоречит формулировке, данной Менделеевым. Она только базируется на новых данных, которые придают закону физическую обоснованность, и подтверждают его правильность. Примерами, иллюстрирующим проявление периодического закона химических элементов, может служить периодическая зависимость плотности простых веществ в твердом состоянии от порядкового номера элемента (заряда ядра), или же такие характеристики атома как его размер, энергия ионизации, электроотрицательность, степень окисления, имеющие периодическую зависимость от заряда атомного ядра (рис. 4.3).
Табличной формой представления периодического закона является периодическая система химических элементов, разработанная Менделеевым в 1869–1871 гг.
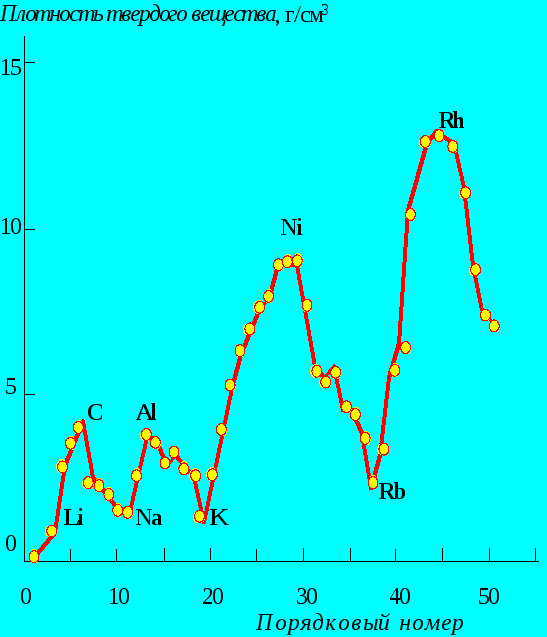
Рис. 4.3.Зависимость плотности простых веществ в твердом состоянии от порядкового номера.
В периодической системе химических элементов все известные в настоящее время химические элементы расположены в порядке возрастания зарядов их атомных ядер, численно равных порядковому номеру элемента, и образуют 7 горизонтальных периодов, каждый из которых, за исключением первого, начинается щелочным металлом и заканчивается инертным газом, причем, седьмой период является незавершенным. Первые три периода, состоящие из одного ряда, называются малыми, остальные – большими.
 По
вертикали химические элементы
располагаются в 8 вертикальных
столбцах-группах, причем каждая группа
делится на две подгруппы – главную,
состоящую из элементов второго и третьего
периодов и сходных с ними элементов
больших периодов, и – побочную, состоящую
из металлов больших периодов. Отдельно
внизу таблицы помещены элементы с
порядковыми номерами 58–71, называемые
лантаноидами, и – элементы с порядковыми
номерами 90–103, называемые актиноидами.
В каждой клетке периодической системы
химических элементов, помимо наименования
элемента и его порядкового номера,
приведено значение относительной
атомной массы элемента и показано
распределение электронов по энергетическим
уровням (рис. 4.4).
По
вертикали химические элементы
располагаются в 8 вертикальных
столбцах-группах, причем каждая группа
делится на две подгруппы – главную,
состоящую из элементов второго и третьего
периодов и сходных с ними элементов
больших периодов, и – побочную, состоящую
из металлов больших периодов. Отдельно
внизу таблицы помещены элементы с
порядковыми номерами 58–71, называемые
лантаноидами, и – элементы с порядковыми
номерами 90–103, называемые актиноидами.
В каждой клетке периодической системы
химических элементов, помимо наименования
элемента и его порядкового номера,
приведено значение относительной
атомной массы элемента и показано
распределение электронов по энергетическим
уровням (рис. 4.4).



Рис. 4.4. Фрагмент периодической системы химических элементов.
На основе периодического закона химических элементов и периодической таблицы Менделеев пришел к выводу о существовании новых элементов, свойства которых он подробно описал и дал им условные названия – экабор, экаалюминий и экасилиций. Предсказания Менделеева блестяще подтвердились, – все три элемента были открыты и получили названия тех стран, где были сделаны открытия и найдены минералы, содержащие эти элементы: галлий,скандий,германий. Таким образом, Менделеев провел блестящий теоретический анализ огромного числа экспериментальных данных, синтезировал свои результаты в виде общего закона и сделал на его основе предсказания, которые вскоре были подтверждены экспериментально. Эта работа является классическим примером научного подхода к познанию окружающего мира.
studfile.net
Периодический закон Менделеева и его применение
Нг1 основании периодического закона сформировалось учение о периодичности, которое складывается из трех основных направлений. Первое устанавливает связь макроскопических свойств простых и сложных веществ со строением и свойствами атомов, составляющих эти вещества. Эта сторона учения о периодичности получила развитие с созданием теории строения атома. Второе направление связано со способом выражения закона в виде периодической системы элементов важнейшими в этой системе являются представления об индивидуальных свойствах, специфических (элементы — аналоги по группе, по ряду, по диагонали) свойствах и общих свойствах (формы соединений), а также о месте элемента в системе. Это направление нашло выражение в сравнительном методе изучения свойств элементов и их соединений. Им широко пользовался Д. И. Менделеев, оно применяется до сих пор. Третье направление — применение идеи периодичности к другим объектам ядрам атомов, элементарным частицам и т. д. [c.44]В 1867 году становится широко известной работа Менделеева О современном развитии некоторых химических производств в применении к России… Через два года появляется первая формулировка периодического закона, Менделеев приступает к созданию капитального труда Основы химии . [c.9]
В соответствии с этим, как только в процессе открытия периодического закона Менделеев приходил путем применения индукции к некоторому обобщению, он тут же по ходу составления общей таблицы элементов прибегал к дедуктивным заключениям, извлекая их из только что найденного обобщения и проверяя тут же на фактах. В связи с этим находится его замечание о рефлексах закона на факты [9а, стр. 43]. [c.88]
В ходе открытия периодического закона Менделеев руководился идеей, что качество элементов обусловлено количеством их атомного веса и что количественное нарастание атомного веса в последовательном ряду элементов должно вызывать переход от одного качественно-определённого элемента к другому. На философском языке это означает не что иное, как конкретное применение закона о переходе количественных изменений в качественные. [c.20]
Идея о сложности атомов химических элементов привела к другому очень важному для нас предвидению — возможности превращения элементов. Ведь признание единства и сложности атомов различных по своим свойствам элементов неизбежно влечет за собой признание единства их происхождения и возможности превращения. В статье Естественная система элементов и применение ее к указанию свойств некоторых элементов в ноябре 1870 г. Д. И. Менделеев писал, что все (в природе) сводится на элементы, все учение химии состоит в учении о свойствах элементов — цель и задача — превратить один в другой . Следовательно, только после открытия периодического закона об изменении свойств химических элементов идея превращаемости элементов, о претворении которой люди мечтали много веков, впервые получила теоретическую основу. [c.14]
Периодический закон (Д, Менделеев, 1869) свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости от заряда ядра элемента. Существует ряд частных законов химии, которые имеют ограниченную область применения. [c.8]
Возглавив кафедру общей химии университета, Менделеев принял решение написать руководство к химии — Основы химии . Этот замечательный труд призван был познакомить публику и учащихся с достижениями химии, ее применением в технике, сельском хозяйстве и т. д. Именно в Основах химии Менделеев впервые предложил (17 февраля, или 1 марта по новому стилю, 1869 г.) таблицу расположения элементов в соответствии с принципом периодичности. Периодический закон также изложен Менделеевым в классическом учебнике Основы химии , опубликованном в 1868—1871 гг. [c.161]
Дмитрий Иванович Менделеев (1834 — 1907) — великий русский ученый — один из основоположников современной химии. Открыл периодический закон и периодическую систему химических элементов. Создал фундаментальный труд — учебник Основы химии , в котором впервые вся неорганическая хи.мия изложена на основе периодического закона. Д. И. Менделеев — автор химической теории растворов. В своих трудах много внимания уделял развитию отечественной промышленности и химизации сельского хозяйства. Он доказывал необходимость создания химических производств соды, серной кислоты, минеральных удобрений. Обосновал идеи подземной газификации угля и применения кислорода в металлургической промышленности. Предложил способ непрерывной переработки нефти, дал оригинальную теорию ее происхождения. Идеи Д. И. Менделеева осуществились только после Великой Октябрьской революции. [c.36]
Но предсказание, открытие и изучение свойств элементов — только первый результат применения периодического закона. Этот закон будил мысль исследователей, звал их дальше. Как и предвидел Менделеев, ученые неизбежно должны были притти к вопросу — почему свойства атомов изменяются так закономерно Не говорит ли это о внутренней сложности атомов [c.195]
В статье Периодическая законность химических элементов , написанной летом 1871 г., Менделеев выделил специальный раздел, в котором освещалось применение закона периодичности к исправлению величины атомных весов [44, с. 157]. В практическом и теоретическом отношении, — говорилось здесь, — конечно, гораздо важнее найти руководящее начало для открытия грубых погрешностей в определении атомных весов, получить понятия о крупных числах, и если для них откроется истинная законность, нет сомнения, что откроется со временем законность и для более точного, детального теоретического определения величины атомных весов. В той форме, какая свойственна ныне закону периодичности, он может служить к открытию грубых неточностей в определении атомных весов… [44, с. 158]. [c.41]
Теперь короткая таблица была превращена в систему прямоугольных координат и каждое место в системе могло быть определено двумя координатами — абсциссой, указывающей группу, к которой принадлежит данный элемент (обозначалась римскими цифрами), и ординатой, указывающей ряд, в который этот элемент входит. После этого и на основе столь глубоко и всесторонне разработанной короткой таблицы, в которой предположительно заняли место все восемь элементов, стоявших до тех пор вне системы, Менделеев мог приступить к подробному предсказанию необходимости крупного, а затем для некоторых элементов и мелкого изменения их атомного веса. Эти прогнозы были выдвинуты им в двух статьях, написанных в конце 1870 г. О месте церия в системе элементов и Естественная система элементов и применение ее к указанию свойств неоткрытых элементов , и особенно подробно в статье, написанной летом 1871 г. Периодическая законность химических элементов . В этой последней статье интересующему нас сейчас вопросу специально посвящены разд. 3 Применение закона периодичности к определению атомных весов мало исследованных элементов и разд. 5 Применение закона периодичности к исправлению атомных весов .
www.chem21.info