Итоговая контрольная работа по химии за 10 класс
Итоговый тест по органической химии для 10 класса.
1 вариант
Часть А Выбрать правильный ответ
1. К алканам относится вещество, имеющее общую формулу
1) Cnh3n 2) Cnh3n-2 3) Cnh3n+2 4) Cnh3n-6
2. Изомером октана является
1) 2–метил–3–этилпентан 2) 2,3–диметилпентан 3) 3–этилгептан 4) 3–метилоктан
3. Структурная формула вещества 2 – метилпентен – 1 — это
1) СН3 – СН(СН3) – СН2 – СН = СН2 3) СН3 – СН2 – СН2 – С(СН3) = СН2
2) СН2 = С(СН3) – СН2 – СН(СН3) – СН3 4) СН2 = С(СН3) – СН3
4. Этин и ацетилен – это
1) гомологи 2) изомеры 3) одно и то же вещество 4) разные вещества
5. С каким из перечисленных веществ реагирует бензол
1) NaOH 2) HNO3 3) CO2 4) CaO
6. Изомером этанола является
1) метанол 2) диэтиловый эфир 3) диметиловый эфир 4) этилацетат
7. Название, несоответствующее реакции СН3 – СОН + Н2 → С2Н5ОН
Название, несоответствующее реакции СН3 – СОН + Н2 → С2Н5ОН
1) присоединение 2) гидрирование 3) гидратация 4) восстановление
8. Реакция образования сложных эфиров называется
1) крекинг 2) этерификация 3) дегидратация 4) поликонденсация
9. Оцените правильность суждений.
А. И этан, и этилен могут реагировать с бромом..
Б. И этанол, и фенол могут реагировать с раствором гидроксида натрия.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
10. Формула ацетальдегида
1) СН3ОН 2) СН3СООН 3) НСОН 4) СН3СОН
Часть В (Задания на соотнесение)
11. Установите соответствие между исходными веществами и продуктом реакции
ИСХОДНЫЕ ВЕЩЕСТВА ОСНОВНОЙ ПРОДУКТ РЕАКЦИИ
А) Ch3 = CH – Ch4 + НBr → 1) Ch3Br – Ch3 – Ch4
Б) C2H5Br + NaOH(спирт. р.) → 2) Ch4 – CHBr – Ch4
р.) → 2) Ch4 – CHBr – Ch4
B) Ch4Br + 2Na → 3) Ch3Br – Ch3Br
Г) C2h5 + Br2 → 4) CHBr2 – Ch4
5) C2h5
6) C2H6
12. Установите соответствие между типом реакции и исходными веществами
ИСХОДНЫЕ ВЕЩЕСТВА ТИП РЕАКЦИИ
А) С6Н6 + Br2 → (в присутствии FeBr3) 1) реакция замещения
Б) C4h20 + Br2 → 2) реакция присоединения
В) C3H8 → 3) реакция окисления
Г) C2h5 + Н2O → 4) реакция дегидрирования
13. Установите соответствие между формулой вещества и классом, к которому оно относится.
ФОРМУЛА ВЕЩЕСТВА КЛАСС СОЕДИНЕНИЙ
А) С2Н5ОН 1) арены
Б) С6Н6 2) алкины
В) НСОН 3) одноатомные спирты
Г) СН2ОН—СН2ОН 4) многоатомные спирты
5) альдегиды
6) карбоновые кислоты
14. Установите соответствие между названием вещества и реактивом, с помощью которого его можно обнаружить.
НАЗВАНИЕ ВЕЩЕСТВА РЕАКТИВ
А) фенол 1) Cu(OH)2
Б) этилен 2) HCl
В) формальдегид 3) CuO
Г) глицерин 4) Br2
5) Ch5
Часть С
15. Написать уравнения реакций, с помощью которых можно осуществить превращения
Написать уравнения реакций, с помощью которых можно осуществить превращения
метан → ацетилен → этаналь → уксусная кислота→ этиловый эфир уксусной кислоты
Используйте только структурные формулы органических веществ.
Итоговый тест по органической химии для 10 класса.
2 вариант
Часть А Выбрать правильный ответ
1. Общая формула гомологического ряда алкенов
1) Cnh3n 2) Cnh3n-2 3) Cnh3n+2 4) Cnh3n-6
2. Вещество СН2 – СН2 – СН2 – СН – СН2 – СН2 называется
│ │ │
СН3 СН3 СН3
1) 1,4,6 – тримемилгексан 2) 1,3,6 – триметилгексан 3) 1,3 – диметилгептан 4) 4 – метилоктан
3. Алкины не вступают в реакции
1) гидрирования 2) галогенирования 3) дегидратации 4) гидратации
4. В схеме превращений СН4 → Х → С6Н6 веществом Х является
В схеме превращений СН4 → Х → С6Н6 веществом Х является
1) С2Н6 2) С2Н4 3) С2Н2 4) С6Н12
5. С каким из перечисленных веществ не реагирует бензол
1) Cl2 2) HNO3 3) h3 4) h3O
6. Изомером пропанола-1 является
1) этанол 2) метилэтиловый эфир 3) диметиловый эфир 4) этилформиат
7. Продуктом окисления этанола оксидом меди (II) является
1) этаналь 2) муравьиная кислота 3) этиловый эфир уксусной кислоты 4) уксусная кислота
8. Жир образуется в результате взаимодействия
1) стеариновой кислоты и метанола 2) олеиновой кислоты и этиленгликоля
3) ацетальдегида и глицерина 4) глицерина и пальмитиновой кислоты
9. Оцените правильность суждений.
А.И этилен, и ацетилен могут вступать в реакцию гидратации.
Б. Для обнаружения альдегидов и кетонов можно использовать свежеприготовленный осадок Cu(OH)2.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
10. Формула муравьиной кислоты
1) НСООН 2) СН3СООН 3) НСОН 4) СН3СОН
Часть В (Задания на соотнесение)
11. Установите соответствие между исходными веществами и продуктами реакции
ИСХОДНЫЕ ВЕЩЕСТВА ПРОДУКТЫ РЕАКЦИИ
А) С2Н6 → 1) → СО2 + 2Н2О
Б) С2Н6 + Cl2 → 2) → Ch4Cl + HCl
B) Ch5 + 2Cl2 → 3) → C2h5 + h3
Г) C4h20 → 4) → Ch3Cl2 + 2HCl
5) → C2H5Cl + HCl
6) → C2H6 + C2h5
12. Установите соответствие между типом реакции и исходными веществами
ИСХОДНЫЕ ВЕЩЕСТВА ТИП РЕАКЦИИ
А) С6Н6 + Cl2 → (при условии УФ-свет) 1) реакция замещения
Б) C3H6 → 2) реакция присоединения
В) C3H8 + Br2 → 3) реакция окисления
Г) C4H8 + Н2О → 4) реакция дегидрирования
13. Установите соответствие между формулой вещества и классом, к которому оно относится.
ФОРМУЛА ВЕЩЕСТВА КЛАСС СОЕДИНЕНИЙ
А) НСООН 1) алкены
Б) СН 2ОН–СНОН–СН 2ОН 2) алкины
В) С2Н2 3) одноатомные спирты
Г) СН3СОН 4) многоатомные спирты
5) альдегиды
6) карбоновые кислоты
14. Установите соответствие между названием вещества и реактивом, с помощью которого его можно обнаружить.
НАЗВАНИЕ ВЕЩЕСТВА РЕАКТИВ
А) фенол 1) Na2CO3
Б) этилен 2) HCl
В) ацетальдегид 3) KMnO4
Г) уксусная кислота 4) FeCl3
5) Ag2O (аммиачный раствор)
Часть С
15.Написать уравнения реакций, с помощью которых можно осуществить превращения
этилен → этанол → этаналь → уксусная кислота → метиловый эфир уксусной кислоты
Используйте только структурные формулы органических веществ.
Ключ Итоговая контрольная работа 10 класс «Базовый уровень»
№ | Вариант 1 | Балл | № | Вариант 2 | Балл |
1 | 3 | 1 | 1 | 1 | 1 |
2 | 1 | 1 | 2 | 4 | 1 |
3 | 3 | 1 | 3 | 3 | 1 |
4 | 3 | 1 | 4 | 3 | 1 |
5 | 2 | 1 | 5 | 4 | 1 |
6 | 3 | 1 | 6 | 2 | 1 |
7 | 3 | 1 | 7 | 1 | 1 |
8 | 2 | 1 | 8 | 4 | 1 |
9 | 1 | 1 | 9 | 1 | 1 |
10 | 4 | 1 | 10 | 1 | 1 |
11 | 2563 | 2 | 11 | 3546 | 2 |
12 | 1142 | 2 | 12 | 2412 | 2 |
13 | 3154 | 2 | 13 | 6425 | 2 |
14 | 4411 | 2 | 14 | 4351 | 2 |
15 | 1) 2Сh5→CH≡CH+3h3 2) CH≡CH+h3O→Ch4—C=O │ H 3) Ch4—C=O+2Cu(OH)2→ │ H Ch4—C=O + Cu2O+2h3O │ OH 4) Ch4—C=O +C2H5OH → │ OH → Ch4—C=O + h3O │ OC2H5 | 4 | 15 | 1) Ch3=Ch3+h3O→C2H5OH 2) C2H5OH+CuO→ Ch4—C=O + │ H + Cu + h3O 3) ) Ch4—C=O+2Cu(OH)2→ │ H Ch4—C=O + Cu2O+2h3O │ OH 4) Ch4—C=O +Ch4OH → │ OH → Ch4—C=O + h3O │ OCh4 | 4 |
| Всего | 22 |
|
| 22 |
| Критерий оценки 0-9 = 2 10-14 = 3 15-19 = 4 20 – 22 = 5 | ||||
Урок 2.
 предельные углеводороды — алканы — Химия — 10 класс
предельные углеводороды — алканы — Химия — 10 классХимия, 10 класс
Урок № 2. Предельные углеводороды – алканы
Перечень вопросов, рассматриваемых в теме: урок посвящён предельным углеводородам, их номенклатуре, физическим и химическим свойствам, а также роли в жизни человека. В ходе урока школьники познакомятся с представителями данного класса органических веществ.
Глоссарий
Гибридизация – процесс взаимодействия разных, но близких по энергии электронных орбиталей, приводящий к их выравниванию по форме и энергии.
Гомология – явление сходства по составу, строению, химическим свойствам и принадлежности к тому же классу одного вещества с другим веществом, но различающиеся друг от друга на одну или несколько групп СН2. Группу СН2 называют гомологической разностью.
Горение – быстро протекающий процесс окисления вещества, сопровождающийся большим выделением тепла и ярким свечением.
Группа функциональная – группа атомов, определяющая наиболее характерные химические свойства вещества и его принадлежность к определенному классу.
Галогенирование – замещение одного или нескольких атомов водорода на галоген.
Дегидрирование – отщепление атомов водорода за счет отщепления связи С-Н.
Изомерия – явление существования веществ, одинаковых по составу и молекулярной массе, но различающихся по строению или расположению атомов в пространстве и вследствие этого по физическим и химическим свойствам. Такие вещества называются изомерами.
Изомеризации реакция – характерна для алканов, протекает под влиянием катализаторов и при нагревании, вещества превращаются в разветвленные, без изменения состава молекулы.
Крекинг – процесс термического или каталитического разложения углеводородов, в основе которого лежат реакции расщепления углеродной цепи крупных молекул на молекулы с меньшим числом атомов углерода.
Парафины – исторически сложившееся название, отражающее их малую химическую активность.
Цепная реакция – реакция, в ходе которой исходные вещества вступают в цепь превращений с участием промежуточных активных частиц и их регенерацией в каждом элементарном акте реакции.
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Дополнительная литература:
1. Рябов, М.А. Сборник задач, упражнений и тестов по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс: учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М.: Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
- Единое окно доступа к информационным ресурсам [Электронный ресурс].
 М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
Теоретический материал для самостоятельного изучения
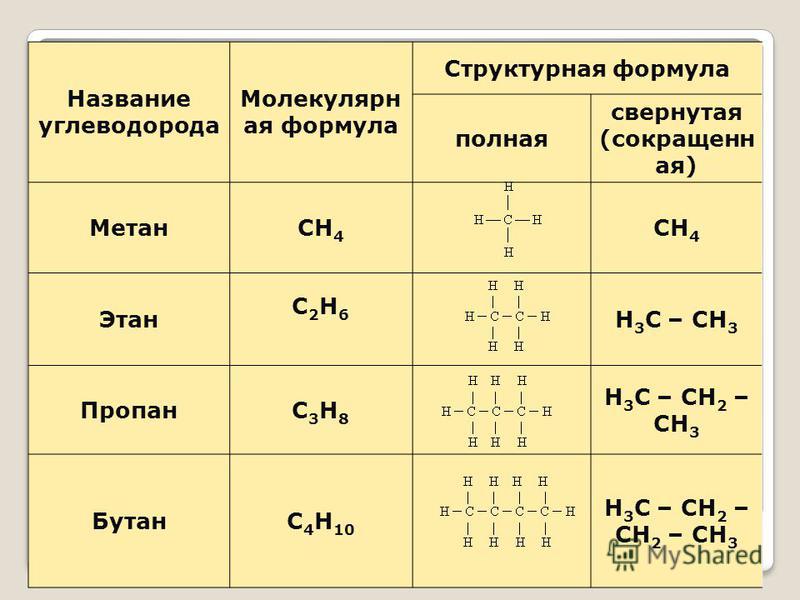
Алканы – это углеводороды, в молекулах которых атомы углерода соединены между собой только простыми (одиночными) ковалентными связями. Длина связи C—C составляет 0,154 нм, длина связи C—H — 0,187 нм. При этом оси четырех sр3-гибридных орбиталей оказываются направленными к вершинам тетраэдра, угол равен 109°28′.
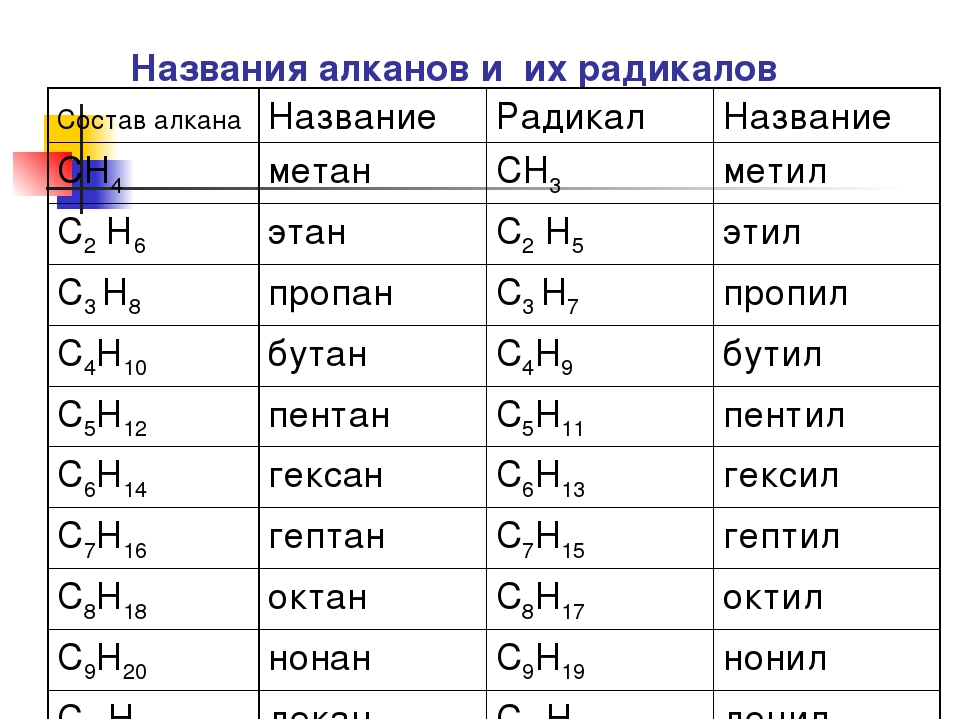
Метан является родоначальником ряда предельных углеводородов (алканов). Их состав выражается общей формулой CnH2n+2. По номенклатуре ИЮПАК названия алканов образуются при помощи суффикса — ан путём добавления к соответствующему корню от названия углеводорода.
Наращивание углеродной цепи на один атом углерода ведёт к увеличению состава на группу СН2 (гомологическая разность). При этом химические свойства и строение веществ одинаковы. Такие ряды называют гомологическими рядами, их члены по отношению друг к другу являются гомологами.
Алканы, число атомов углерода в которых больше трёх, имеют изомеры. Изомерия предельных углеводородов обусловлена простейшим видом структурной изомерии — изомерией углеродного скелета.
Электронное строение алканов определяет инертный характер алканов. При комнатной температуре С1-C4 — газы, C5-C15 — жидкости, C16 и следующие — твердые вещества; нерастворимы в воде. С увеличением числа атомов углерода в молекуле возрастает температура кипения и плавления.
По химическим свойствам алканы – инертные вещества. Они вступают только в реакции замещения, протекающие с разрывом связей C-H. Протекают эти реакции в жестких условиях (высокая температура, освещенность).
Реакция галогенирования алканов протекает по радикально — цепному механизму, т.е. как цепь последовательных превращений с участием свободно-радикальных частиц.
В разработке теории цепных реакций большую роль сыграли труды академика, лауреата Нобелевской премии Н. Н. Семёнова.
Н. Семёнова.
Еще одно подтверждение малоактивных свойств алканов — на них не действуют сильные окислители. При пропускании метана через растворы перманганата калия (KMnO4, Br2(H2O) бромной воды) никаких изменений не наблюдается. Не действует на алканы и концентрированная серная кислота.
ПРИМЕРЫ И РАЗБОР РЕШЕНИЯ ЗАДАНИЙ ТРЕНИРОВОЧНОГО МОДУЛЯ
- Решение задачи о получении метана
Сколько граммов карбида алюминия требуется для получения 5,6 л (н. у.) метана с помощью реакции гидролиза? Ответ округлите до целых.
Ответ: 12г
Решение:
1.Запишем уравнение реакции
Al4C3+12H2O→3CH4+4Al(OH)3
2.Рассчитаем количество вещества метана
ν(СН4) = 5.6 /22.4 = 0.25 (моль)
3.Составим пропорцию, приняв за х количество вещества карбида алюминия:
0,25/3 = х/1
x = 0,083 (моль).
4. Определяем массу карбида алюминия
m(Al4C3) = 0. 083 · 144 = 12 (г)
083 · 144 = 12 (г)
- Определение формул гомологов.
Подчеркните формулы алканов, которые должны в итоге образовать линию из трех веществ (она может быть как по прямой, так и по диагонали)
C2H4 | CH4 | C5H12 |
C3H4 | C6H6 | C3H8 |
C10H22 | C5H10 | C8H18 |
Решение:
- Определяем в каких ячейках находятся алканы, т.е. вещества, соответствующие общей формуле CnH2n+2
C2H4 | CH4 | C5H12 |
C3H4 | C6H6 | C3H8 |
C10H22 | C5H10 | C8H18 |
- После подсчета получается, что алканы находятся только в одной вертикальной линии.

C2H4 | CH4 | C5H12 |
C3H4 | C6H6 | C3H8 |
C10H22 | C5H10 | C8H18 |
10 класс. Химия. Алкены. Строение, номенклатура, изомерия и физические свойства — Алкены. Строение, номенклатура, изомерия и физические свойства
НЕПРЕДЕЛЬНЫЕ, ИЛИ НЕНАСЫЩЕННЫЕ, УГЛЕВОДОРОДЫ РЯДА ЭТИЛЕНА (АЛКЕНЫ, ИЛИ ОЛЕФИНЫ)
Алкены, или олефины (от лат. olefiant — масло — старое название, но широко используемое в химической литературе. Поводом к такому названию послужил хлористый этилен, полученный в XVIII столетии, — жидкое маслянист вещество.) — алифатические непредельные углеводороды, в молекулах которых между углеродными атомами имеется одна двойная связь.
Алкены содержат в своей молекуле меньшее число водородных атомов, чем соответствующие им алканы (с тем же числом углеродных атомов), поэтому такие углеводороды называют непредельными или ненасыщенными.
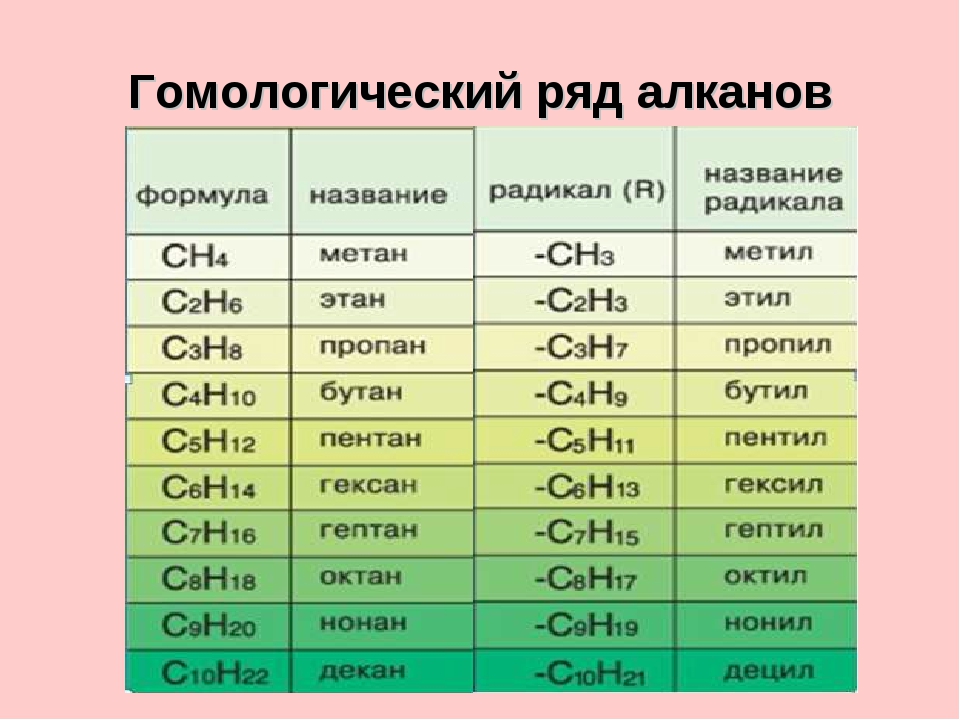
Алкены образуют гомологический ряд с общей формулой Cnh3n
1. Гомологический ряд алкенов
|
Сnh3n алкен |
Названия, суффикс ЕН, ИЛЕН |
|
C2Н4 |
этен, этилен |
| C3H6 |
пропен |
|
C4H8 |
бутен |
|
C5h20 |
пентен |
|
C6h22 |
гексен |
Гомологи:
СH2=CH2 этен
СH2=CH—CH3 пропен
Сh3=CH-Ch3-Ch4 бутен-1
Сh3=CH-Ch3-Ch3-СН3 пентен-1
2.
Этилен (этен) – бесцветный газ с очень слабым сладковатым запахом, немного легче воздуха, малорастворим в воде.
С2 – С4 (газы)
С5 – С17 (жидкости)
С18 – ( твёрдые)
· Алкены не растворяются в воде, растворимы в органических растворителях (бензин, бензол и др.)
· Легче воды
· С увеличением Mr температуры плавления и кипения увеличиваются
3. Простейшим алкеном является этилен — C2h5
Структурная и электронная формулы этилена имеют вид:
В молекуле этилена подвергаются гибридизации одна s— и две p-орбитали атомов C (sp2-гибридизация).
Таким образом, каждый атом C имеет по три гибридных орбитали и по одной негибридной p-орбитали. Две из гибридных орбиталей атомов C взаимно перекрываются и образуют между атомами C
Две из гибридных орбиталей атомов C взаимно перекрываются и образуют между атомами C
σ — связь. Остальные четыре гибридных орбитали атомов C перекрываются в той же плоскости с четырьмя s-орбиталями атомов H и также образуют четыре σ — связь. Две негибридные p-орбитали атомов C взаимно перекрываются в плоскости, которая расположена перпендикулярно плоскости σ — связь, т.е. образуется одна П — связь.
По своей природе П — связь резко отличается от σ — связь; П — связь менее прочная вследствие перекрывания электронных облаков вне плоскости молекулы. Под действием реагентов П — связь легко разрывается.
Молекула этилена симметрична; ядра всех атомов расположены в одной плоскости и валентные углы близки к 120°; расстояние между центрами атомов C равно 0,134 нм.
|
Запомните! SP2 –гибридизация: 1) Плоское тригональное строение 2) Угол – HCH — 120° 3) Длина (-С=С-) связи – 0,134 нм 4) Связи — σ, П 5) Невозможно вращение относительно (-С=С-) связи |
Если атомы соединены двойной связью, то их вращение невозможно без того, чтобы электронные облака П — связь не разомкнулись.
4. Изомерия алкенов
Наряду со структурной изомерией углеродного скелета для алкенов характерны, во-первых, другие разновидности структурной изомерии — изомерия положения кратной связи и межклассовая изомерия.
Во-вторых, в ряду алкенов проявляется пространственная изомерия, связанная с различным положением заместителей относительно двойной связи, вокруг которой невозможно внутримолекулярное вращение.
Структурная изомерия алкенов
1. Изомерия углеродного скелета (начиная с С4Н8):
2. Изомерия положения двойной связи (начиная с С4Н8):
3. Межклассовая изомерия с циклоалканами, начиная с С3Н6:
Пространственная изомерия алкенов
Вращение атомов вокруг двойной связи невозможно без ее разрыва. Это обусловлено особенностями строения p-связи (p-электронное облако сосредоточено над и под плоскостью молекулы). Вследствие жесткой закрепленности атомов поворотная изомерия относительно двойной связи не проявляется. Но становится возможной цис—транс-изомерия.
Алкены, имеющие у каждого из двух атомов углерода при двойной связи различные заместители, могут существовать в виде двух пространственных изомеров, отличающихся расположением заместителей относительно плоскости p-связи. Так, в молекуле бутена-2СН3–СН=СН–СН3 группы СН3 могут находиться либо по одну сторону от двойной связи вцис -изомере, либо по разные стороны в транс-изомере.
ВНИМАНИЕ! цис-транс— Изомерия не проявляется, если хотя бы один из атомов С при двойной связи имеет 2 одинаковых заместителя.
Например,
бутен-1 СН2=СН–СН2–СН3 не имеет цис— и транс-изомеров, т.к. 1-й атом С связан с двумя одинаковыми атомами Н.
Изомеры цис— и транс— отличаются не только физическими
,
но и химическими свойствами, т. к. сближение или удаление частей молекулы друг от друга в пространстве способствует или препятствует химическому взаимодействию.
к. сближение или удаление частей молекулы друг от друга в пространстве способствует или препятствует химическому взаимодействию.
Иногда цис-транс-изомерию не совсем точно называют геометрической изомерией. Неточность состоит в том, что все пространственные изомеры различаются своей геометрией, а не только цис— и транс-.
5. Номенклатура
Алкены простого строения часто называют, заменяя суффикс -ан в алканах на -илен: этан — этилен, пропан — пропилен и т.д.
По систематической номенклатуре названия этиленовых углеводородов производят заменой суффикса -ан в соответствующих алканах на суффикс -ен (алкан — алкен, этан — этен, пропан — пропен и т.д.). Выбор главной цепи и порядок названия тот же, что и для алканов. Однако в состав цепи должна обязательно входить двойная связь. Нумерацию цепи начинают с того конца, к которому ближе расположена эта связь. Например:
Например:
Непредельные (алкеновые) радикалы называют тривиальными названиями или по систематической номенклатуре:
(Н2С=СН— ) винил или этенил
(Н2С=CН—СН2 ) аллил
Строение молекулы этилена (C2h5), схема и примеры
Общие сведения о строении молекулы этилена
Структурная формула:
H2C = CH2.
Брутто-формула: C2H4. Молярная масса – 28 г/моль.
Этилен представляет собой газ без цвета, но со слабым запахом. Плотность 1,178 кг/м3 (легче воздуха). Горючий. Мало растворим в воде, но хорошо в диэтиловом эфире и углеводородах.
Электронное строение молекулы этилена
Атомы углерода в составе молекулы алкена связаны между собой двойной связью. Эти атомы находятся в состоянии sp2-гибридизации. Двойная связь между ними образована из двух пар обобществленных электронов, т. е. это четырехэлектронная связь. Она сочетанием ковалентных σ-связи и π-связи. σ-Связь образована за счет осевого перекрывания sp2-гибридных орбиталей, а π-связь – за счет бокового перекрывания негибридизованных p-орбителей двух атомов углерода (рис. 1).
е. это четырехэлектронная связь. Она сочетанием ковалентных σ-связи и π-связи. σ-Связь образована за счет осевого перекрывания sp2-гибридных орбиталей, а π-связь – за счет бокового перекрывания негибридизованных p-орбителей двух атомов углерода (рис. 1).
Рис. 1. Строение молекулы этилена.
Пять σ-связей двух sp2-гибридизованных атомов углерода лежат в одной плоскости под углом 120o и составляют σ-скелет молекулы. Над и под этой плоскостью симметрично расположена электронная плотность π-связи, которую можно изобразить также в виде плоскости, перпендикулярной σ-скелету.
При образовании π-связи происходит сближение атомов углерода, потому что межъядерное пространство в двойной связи более насыщено электронами, чем в σ-связи. Это стягивает атомные ядра и поэтому длина двойной связи (0,133 нм) меньше одинарной (0,154 нм).
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
% PDF-1.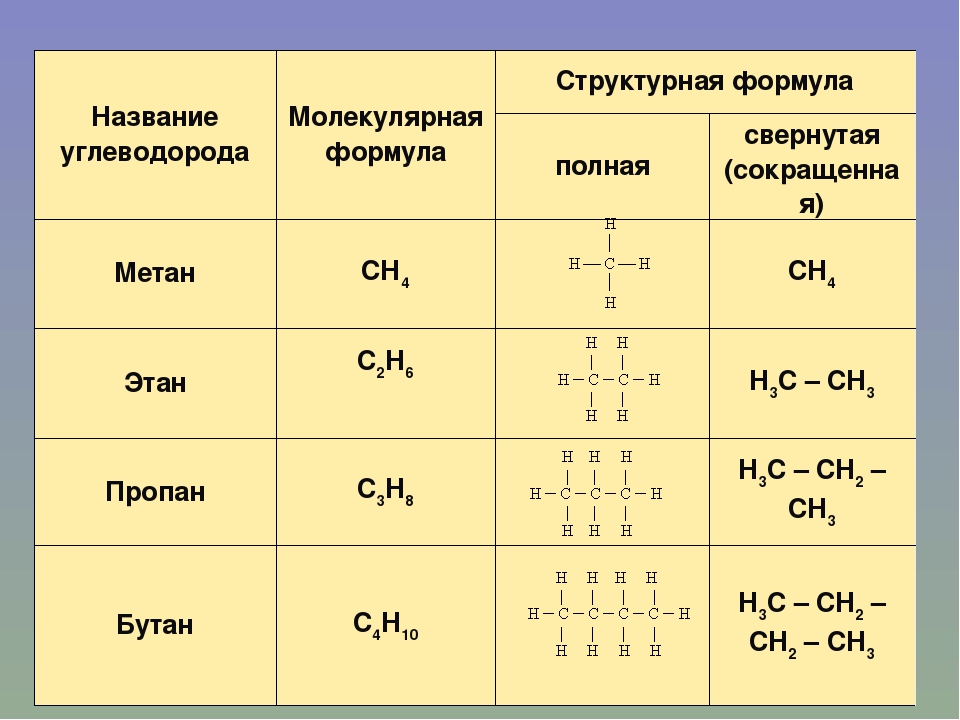 4
%
1 0 obj
>
эндобдж
2 0 obj
>
эндобдж
3 0 obj
>
эндобдж
4 0 obj
>
/Шрифт
>
/ XObject
>
>>
/Группа
>
>>
эндобдж
5 0 obj
>
/Шрифт
>
/ XObject
>
>>
/Группа
>
>>
эндобдж
6 0 obj
>
/Шрифт
>
/ XObject
>
>>
/Группа
>
>>
эндобдж
7 0 объект
>
/Шрифт
>
/ XObject
>
>>
/Группа
>
>>
эндобдж
8 0 объект
>
поток
конечный поток
эндобдж
9 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F0 -14 Тс
14.25 26,7256 тд тдж
ET
Q
Q
конечный поток
эндобдж
10 0 obj
>
эндобдж
11 0 объект
>
эндобдж
12 0 объект
>
поток
/ CIDInit / ProcSet findresource begin
12 дикт начать
begincmap
/ CIDSystemInfo> def
/ CMapName / Adobe-Identity-UCS def / CMapType 2 def
1 начало кода endcodespacerange
32 начало конец
endcmap CMapName currentdict / CMap defineresource pop end end
конечный поток
эндобдж
13 0 объект
>
/ FontDescriptor 11 0 R
/ BaseFont / WHNHJA + TimesNewRoman, полужирный
/ Вт [3 [250] 17 [250] 19 [500] 20 [500] 21 [500] 26 [500] 27 [500] 29 [333] 36 [722] 38 [722] 39 [722] 46 [777] ] 48 [943] 49 [722] 50 [777] 57 [722] 66 [500] 68 [500] 70 [443] 72 [443] 74 [500] 75 [556] 76 [277] 79 [277] 80 [833] 81 [556] 82 [500] 85 [443] 86 [389] 87 [333] 90 [722] 92 [500]]
>>
эндобдж
14 0 объект
>
эндобдж
15 0 объект
>
поток
конечный поток
эндобдж
16 0 объект
>
поток
конечный поток
эндобдж
17 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F0 -14 Тс
480.
4
%
1 0 obj
>
эндобдж
2 0 obj
>
эндобдж
3 0 obj
>
эндобдж
4 0 obj
>
/Шрифт
>
/ XObject
>
>>
/Группа
>
>>
эндобдж
5 0 obj
>
/Шрифт
>
/ XObject
>
>>
/Группа
>
>>
эндобдж
6 0 obj
>
/Шрифт
>
/ XObject
>
>>
/Группа
>
>>
эндобдж
7 0 объект
>
/Шрифт
>
/ XObject
>
>>
/Группа
>
>>
эндобдж
8 0 объект
>
поток
конечный поток
эндобдж
9 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F0 -14 Тс
14.25 26,7256 тд тдж
ET
Q
Q
конечный поток
эндобдж
10 0 obj
>
эндобдж
11 0 объект
>
эндобдж
12 0 объект
>
поток
/ CIDInit / ProcSet findresource begin
12 дикт начать
begincmap
/ CIDSystemInfo> def
/ CMapName / Adobe-Identity-UCS def / CMapType 2 def
1 начало кода endcodespacerange
32 начало конец
endcmap CMapName currentdict / CMap defineresource pop end end
конечный поток
эндобдж
13 0 объект
>
/ FontDescriptor 11 0 R
/ BaseFont / WHNHJA + TimesNewRoman, полужирный
/ Вт [3 [250] 17 [250] 19 [500] 20 [500] 21 [500] 26 [500] 27 [500] 29 [333] 36 [722] 38 [722] 39 [722] 46 [777] ] 48 [943] 49 [722] 50 [777] 57 [722] 66 [500] 68 [500] 70 [443] 72 [443] 74 [500] 75 [556] 76 [277] 79 [277] 80 [833] 81 [556] 82 [500] 85 [443] 86 [389] 87 [333] 90 [722] 92 [500]]
>>
эндобдж
14 0 объект
>
эндобдж
15 0 объект
>
поток
конечный поток
эндобдж
16 0 объект
>
поток
конечный поток
эндобдж
17 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F0 -14 Тс
480. 75 26,7256 тд тдж
ET
Q
Q
конечный поток
эндобдж
18 0 объект
>
поток
конечный поток
эндобдж
19 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F0 -14 Тс
14,25 45,4756 тд тдж
ET
Q
Q
конечный поток
эндобдж
20 0 объект
>
поток
конечный поток
эндобдж
21 0 объект
>
поток
конечный поток
эндобдж
22 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F0 -14 Тс
511,5 45,4756 тд тдж
ET
Q
Q
конечный поток
эндобдж
23 0 объект
>
поток
конечный поток
эндобдж
24 0 объект
>
поток
конечный поток
эндобдж
25 0 объект
>
поток
конечный поток
эндобдж
26 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F0 -14 Тс
541.5 771,4756 тд тдж
ET
Q
Q
конечный поток
эндобдж
27 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
1,1 Вт
0 Дж
0 Дж
[] 0 дн.
/ GS1 GS
0 0 мес.
0 0 л
S
Q
Q
конечный поток
эндобдж
28 0 объект
>
эндобдж
29 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
1,1 Вт
0 Дж
0 Дж
[] 0 дн.
/ GS1 GS
20,25 57,75 м
591,75 57,75 л
S
Q
Q
конечный поток
эндобдж
30 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
1,1 Вт
0 Дж
0 Дж
[] 0 дн.
75 26,7256 тд тдж
ET
Q
Q
конечный поток
эндобдж
18 0 объект
>
поток
конечный поток
эндобдж
19 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F0 -14 Тс
14,25 45,4756 тд тдж
ET
Q
Q
конечный поток
эндобдж
20 0 объект
>
поток
конечный поток
эндобдж
21 0 объект
>
поток
конечный поток
эндобдж
22 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F0 -14 Тс
511,5 45,4756 тд тдж
ET
Q
Q
конечный поток
эндобдж
23 0 объект
>
поток
конечный поток
эндобдж
24 0 объект
>
поток
конечный поток
эндобдж
25 0 объект
>
поток
конечный поток
эндобдж
26 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F0 -14 Тс
541.5 771,4756 тд тдж
ET
Q
Q
конечный поток
эндобдж
27 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
1,1 Вт
0 Дж
0 Дж
[] 0 дн.
/ GS1 GS
0 0 мес.
0 0 л
S
Q
Q
конечный поток
эндобдж
28 0 объект
>
эндобдж
29 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
1,1 Вт
0 Дж
0 Дж
[] 0 дн.
/ GS1 GS
20,25 57,75 м
591,75 57,75 л
S
Q
Q
конечный поток
эндобдж
30 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
1,1 Вт
0 Дж
0 Дж
[] 0 дн. / GS1 GS
20,25 753 м
591,75 753 л
S
Q
Q
конечный поток
эндобдж
31 0 объект
>
поток
конечный поток
эндобдж
32 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
42 95.4434 тд тдж
ET
Q
Q
конечный поток
эндобдж
33 0 объект
>
эндобдж
34 0 объект
>
поток
/ CIDInit / ProcSet findresource begin
12 дикт начать
begincmap
/ CIDSystemInfo> def
/ CMapName / Adobe-Identity-UCS def / CMapType 2 def
1 начало кода endcodespacerange
61 начало конец
endcmap CMapName currentdict / CMap defineresource pop end end
конечный поток
эндобдж
35 0 объект
>
/ FontDescriptor 33 0 R
/ BaseFont / OODRTX + TimesNewRoman
/ Вт [3 [250] 8 [833] 12 [333] 14 [563] 15 [250] 16 [333] 17 [250] 19 [500] 20 [500] 21 [500] 22 [500] 23 [500] ] 24 [500] 25 [500] 26 [500] 27 [500] 28 [500] 29 [277] 34 [443] 36 [722] 37 [666] 38 [666] 39 [722] 42 [722] 43 [722] 44 [333] 48 [889] 49 [722] 50 [722] 51 [556] 53 [666] 55 [610] 56 [722] 58 [943] 68 [443] 69 [500] 70 [443] ] 71 [500] 72 [443] 73 [333] 74 [500] 75 [500] 76 [277] 77 [277] 78 [500] 79 [277] 80 [777] 81 [500] 82 [500] 83 [500] 84 [500] 85 [333] 86 [389] 87 [277] 88 [500] 89 [500] 90 [722] 91 [500] 92 [500] 93 [443] 177 [500]]
>>
эндобдж
36 0 объект
>
эндобдж
37 0 объект
>
поток
конечный поток
эндобдж
38 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
60 95.
/ GS1 GS
20,25 753 м
591,75 753 л
S
Q
Q
конечный поток
эндобдж
31 0 объект
>
поток
конечный поток
эндобдж
32 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
42 95.4434 тд тдж
ET
Q
Q
конечный поток
эндобдж
33 0 объект
>
эндобдж
34 0 объект
>
поток
/ CIDInit / ProcSet findresource begin
12 дикт начать
begincmap
/ CIDSystemInfo> def
/ CMapName / Adobe-Identity-UCS def / CMapType 2 def
1 начало кода endcodespacerange
61 начало конец
endcmap CMapName currentdict / CMap defineresource pop end end
конечный поток
эндобдж
35 0 объект
>
/ FontDescriptor 33 0 R
/ BaseFont / OODRTX + TimesNewRoman
/ Вт [3 [250] 8 [833] 12 [333] 14 [563] 15 [250] 16 [333] 17 [250] 19 [500] 20 [500] 21 [500] 22 [500] 23 [500] ] 24 [500] 25 [500] 26 [500] 27 [500] 28 [500] 29 [277] 34 [443] 36 [722] 37 [666] 38 [666] 39 [722] 42 [722] 43 [722] 44 [333] 48 [889] 49 [722] 50 [722] 51 [556] 53 [666] 55 [610] 56 [722] 58 [943] 68 [443] 69 [500] 70 [443] ] 71 [500] 72 [443] 73 [333] 74 [500] 75 [500] 76 [277] 77 [277] 78 [500] 79 [277] 80 [777] 81 [500] 82 [500] 83 [500] 84 [500] 85 [333] 86 [389] 87 [277] 88 [500] 89 [500] 90 [722] 91 [500] 92 [500] 93 [443] 177 [500]]
>>
эндобдж
36 0 объект
>
эндобдж
37 0 объект
>
поток
конечный поток
эндобдж
38 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
60 95. 4434 тд тдж
ET
Q
Q
конечный поток
эндобдж
39 0 объект
>
поток
конечный поток
эндобдж
40 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
159 95,4434 тд тдж
ET
Q
Q
конечный поток
эндобдж
41 0 объект
>
поток
конечный поток
эндобдж
42 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
177 95,4434 тд тдж
ET
Q
Q
конечный поток
эндобдж
43 0 объект
>
поток
конечный поток
эндобдж
44 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
42 111.1934 Td Tj
ET
Q
Q
конечный поток
эндобдж
45 0 объект
>
поток
конечный поток
эндобдж
46 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
60 111.1934 Td Tj
ET
Q
Q
конечный поток
эндобдж
47 0 объект
>
поток
конечный поток
эндобдж
48 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
159 111.1934 Td Tj
ET
Q
Q
конечный поток
эндобдж
49 0 объект
>
поток
конечный поток
эндобдж
50 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
177 111.1934 Td Tj
ET
Q
Q
конечный поток
эндобдж
51 0 объект
>
поток
конечный поток
эндобдж
52 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
29,25 74,4434 тд тдж
ET
Q
Q
конечный поток
эндобдж
53 0 объект
>
поток
конечный поток
эндобдж
54 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
42 74.
4434 тд тдж
ET
Q
Q
конечный поток
эндобдж
39 0 объект
>
поток
конечный поток
эндобдж
40 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
159 95,4434 тд тдж
ET
Q
Q
конечный поток
эндобдж
41 0 объект
>
поток
конечный поток
эндобдж
42 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
177 95,4434 тд тдж
ET
Q
Q
конечный поток
эндобдж
43 0 объект
>
поток
конечный поток
эндобдж
44 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
42 111.1934 Td Tj
ET
Q
Q
конечный поток
эндобдж
45 0 объект
>
поток
конечный поток
эндобдж
46 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
60 111.1934 Td Tj
ET
Q
Q
конечный поток
эндобдж
47 0 объект
>
поток
конечный поток
эндобдж
48 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
159 111.1934 Td Tj
ET
Q
Q
конечный поток
эндобдж
49 0 объект
>
поток
конечный поток
эндобдж
50 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
177 111.1934 Td Tj
ET
Q
Q
конечный поток
эндобдж
51 0 объект
>
поток
конечный поток
эндобдж
52 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
29,25 74,4434 тд тдж
ET
Q
Q
конечный поток
эндобдж
53 0 объект
>
поток
конечный поток
эндобдж
54 0 объект
>
поток
q
1 0 0-1 0 792 см -100 Тлз
q
BT
/ GS0 гс
/ F1 -12 Тс
42 74. `0D
`0D
, почему первым членом гомологического ряда в алкенах является этен — Наука — Углерод и его соединения — 1825112
Алкен — это углеводород, что означает, что это молекула, полностью состоящая из атомов углерода и водорода. Ряд алканов аналогичен ряду алканов, за исключением того, что каждая углеродная цепь имеет одну и только одну двойную связь в ней. Поскольку элемент Углерод соединяется четырьмя способами, а элемент Водород связывает только одним способом, мы можем легко построить члены этого ряда.
Важно отметить, что из-за свойств углерода и водорода двойная связь может находиться ТОЛЬКО между двумя атомами углерода. Водород не может образовывать ничего, кроме одной одинарной связи.
Алкены называются так же, как и алканы, за исключением того, что «-ан» заменен на «-ен» в конце.
Этен: простейший алкен
Поскольку членство в этой серии требует наличия одной двойной связи где-то в углеродной цепи, невозможно иметь молекулу только с одним атомом углерода. Следовательно, первым членом этого ряда является Этен, имеющий химическую формулу C2h5. Он также известен как этилен. Двойная связь расположена между двумя атомами углерода, что оставляет два несвязанных электрона на каждом атоме углерода. Каждый из этих несвязанных электронов образует одинарную связь с одним атомом водорода, давая окончательную структуру.
Следовательно, первым членом этого ряда является Этен, имеющий химическую формулу C2h5. Он также известен как этилен. Двойная связь расположена между двумя атомами углерода, что оставляет два несвязанных электрона на каждом атоме углерода. Каждый из этих несвязанных электронов образует одинарную связь с одним атомом водорода, давая окончательную структуру.
На диаграммах ниже используются электронные точечные диаграммы для углерода и водорода. Для удобства все структуры нарисованы плоскими, но на самом деле они трехмерны и соответствуют всем правилам строения молекул.
Обратите внимание, что есть только одно возможное расположение двойной связи в этой молекуле, и что независимо от того, в какую сторону вы ее поверните вверх или вокруг, структура выглядит одинаково. Это означает, что существует только один структурный изомер для этана . Для изучения структурных изомеров см. Страницу Что такое октан ?.
Важность этена
Этен является жизненно важным компонентом индустрии пластмасс, а также используется для массового производства коммерческого этанола, моющих средств и большого количества других соединений. Он производится в массовом масштабе по всему миру и производится из сырой нефти. Этен из этого источника по сути является ограниченным ресурсом.
Он производится в массовом масштабе по всему миру и производится из сырой нефти. Этен из этого источника по сути является ограниченным ресурсом.
химическая формула и модель молекулы метана Ch5, этана C2h5, и т.д. Клипарты, векторы, и Набор Иллюстраций Без Оплаты Отчислений. Image 79575914.
Химическая формула и модель молекулы метана Ch5, этана C2h5, и т.д. Клипарты, векторы, и Набор Иллюстраций Без Оплаты Отчислений. Изображение 79575914.Химическая формула и модель молекулы метана Ch5, этана C2h5, пропана C3H8, бутана C4h20.Гомологический ряд алканов. Векторная иллюстрация
Если вы хотите использовать это в качестве логотипа вашей компании, мы можем организовать выкуп прав от вашего имени. Свяжитесь с нами по телефону +7 499 938-68-54, чтобы узнать больше!
M L XL EPSТаблица размеров
| Размер изображения | Идеально подходит для |
| S | Интернет и блоги, социальные сети и мобильные приложения. |
| млн | Брошюры и каталоги, журналы и открытки. |
| л | Плакаты и баннеры для дома и улицы. |
| XL | Фоновые изображения, рекламные щиты и цифровые экраны. |
Используете это изображение на предмете перепродажи или шаблоне?
Распечатать Электронный Всесторонний
5000 x 7050 пикселей | 42.3 см x 59,7 см | 300 точек на дюйм | JPG
Масштабирование до любого размера • EPS
5000 x 7050 пикселей | 42,3 см x 59,7 см | 300 точек на дюйм | JPG
Скачать
Купить одно изображение
6 кредитов
Самая низкая цена
с планом подписки
- Попробовать 1 месяц на 2209 pyб
- Загрузите 10 фотографий или векторов.
- Нет дневного лимита загрузок, неиспользованные загрузки переносятся на следующий месяц
221 ру
за изображение любой размер
Цена денег
Ключевые слова
Похожие векторы
Нужна помощь? Свяжитесь со своим персональным менеджером по работе с клиентами
@ +7 499 938-68-54
Мы используем файлы cookie, чтобы вам было удобнее работать. Используя наш веб-сайт, вы соглашаетесь на использование файлов cookie, как описано в нашей Политике использования файлов cookie
Используя наш веб-сайт, вы соглашаетесь на использование файлов cookie, как описано в нашей Политике использования файлов cookie
пример гомологической серии класса 10
C3H8 принадлежит к гомологической серии (a) Спирты (c) Они имеют одинаковую электрическую проводимость (C) C2H6 Эти соединения имеют схожие химические свойства из-за добавления функциональных групп одного и того же типа повсюду. цепь. (a) C6H6 (a) 2 (b) C3H8 (b) И A, и R верны, но R не является правильным объяснением A.(a) Роза (a) У них одинаковая кристаллическая структура Вопрос 14. C6H6, C2H6, C2h5, C3h5. Свойство самосвязывания (сцепление) является максимальным в (б) летучей природе спирта (г) 12, вопрос 8. Реакции присоединения подвергаются (а) зимазе (а) И A, и R верны, и R является правильным объяснением A. (b) алкины (a) C6h22O6 (d) NaCl (водн.), Вопрос 2. Причина: сложные эфиры используются в мороженом и холодных напитках. (c) C2H5OH (a) Реакция присоединения Гомологический ряд. Какое из следующих утверждений о графите и алмазе верно? (d) Главы 4 и 16u, Вопрос 37.(b) карбоновая кислота (e) И A, и R неверны. (d) Ethanal, вопрос 27. Количество изомеров пентана — (b) альдегид (c) только алкины (a) углерод. Вопросы MCQ для класса 10 по науке с ответами подготовлены в соответствии с последним шаблоном экзамена. (б) Алкены. Ряд соединений углерода, в которых одна и та же функциональная группа замещает атом водорода, называется гомологическим рядом. (a) Ch4CHO (c) кетон Вопрос 4. (b) метанон Углерод существует в атмосфере в форме (a) h3 Первым членом гомологического ряда алкинов является (b) C2H5ONa + h3 (d) как алкены, так и алкины. , Вопрос 29.(c) Не растворяется в воде (b) Ch3 и 14u (c) карбоновые кислоты Показать темы. Последовательные элементы отличаются друг от друга на единицу CH 2. Масла при обработке водородом в присутствии палладиевого или никелевого катализатора образуют жиры. Молекула мыла имеет (d) гидрофильную головку и гидрофобный хвост, (d) гидрофильную головку и гидрофобный хвост, Вопрос 32.
Какое из следующих утверждений о графите и алмазе верно? (d) Главы 4 и 16u, Вопрос 37.(b) карбоновая кислота (e) И A, и R неверны. (d) Ethanal, вопрос 27. Количество изомеров пентана — (b) альдегид (c) только алкины (a) углерод. Вопросы MCQ для класса 10 по науке с ответами подготовлены в соответствии с последним шаблоном экзамена. (б) Алкены. Ряд соединений углерода, в которых одна и та же функциональная группа замещает атом водорода, называется гомологическим рядом. (a) Ch4CHO (c) кетон Вопрос 4. (b) метанон Углерод существует в атмосфере в форме (a) h3 Первым членом гомологического ряда алкинов является (b) C2H5ONa + h3 (d) как алкены, так и алкины. , Вопрос 29.(c) Не растворяется в воде (b) Ch3 и 14u (c) карбоновые кислоты Показать темы. Последовательные элементы отличаются друг от друга на единицу CH 2. Масла при обработке водородом в присутствии палладиевого или никелевого катализатора образуют жиры. Молекула мыла имеет (d) гидрофильную головку и гидрофобный хвост, (d) гидрофильную головку и гидрофобный хвост, Вопрос 32. (a) Ch4 и 16u (a) Метан Этанол реагирует с металлическим Na с образованием (d) Ch4COOCh4, Вопрос 10 . (d) Керосин. (a) 10 (d) ацетон / этанон, Вопрос 28.Почему углерод образует соединения в основном за счет ковалентных связей? (c) Ch4COONa + h3 (b) 8 (a) Ацетальдегид (a) топливо не готово полностью. (d) водородная связь, Вопрос 11. (b) Спирты CaF2 могут быть получены путем гидратации (c) серы (c) гидрофильной головки и гидрофильного хвоста (d) от 40 до 50% этанола, Вопрос 26. (d) глицеридов, Вопрос 21. (б) топливо сгорает не полностью. Побочным продуктом в мыловарении является (d) циклоалканы, вопрос 22. (c) только диоксид углерода (c) спирты (b) горючий пластик (d) C3h5, вопрос 30.Что из следующего будет подвергаться реакциям присоединения? (г) Бутанон, вопрос 34. В алмазе каждый атом углерода связан с четырьмя другими атомами углерода с образованием (б) этилового спирта. Это пример приготовления пищи: если дно сосудов почернеет снаружи, это означает, что он означает, что гомологичный ряд.
(a) Ch4 и 16u (a) Метан Этанол реагирует с металлическим Na с образованием (d) Ch4COOCh4, Вопрос 10 . (d) Керосин. (a) 10 (d) ацетон / этанон, Вопрос 28.Почему углерод образует соединения в основном за счет ковалентных связей? (c) Ch4COONa + h3 (b) 8 (a) Ацетальдегид (a) топливо не готово полностью. (d) водородная связь, Вопрос 11. (b) Спирты CaF2 могут быть получены путем гидратации (c) серы (c) гидрофильной головки и гидрофильного хвоста (d) от 40 до 50% этанола, Вопрос 26. (d) глицеридов, Вопрос 21. (б) топливо сгорает не полностью. Побочным продуктом в мыловарении является (d) циклоалканы, вопрос 22. (c) только диоксид углерода (c) спирты (b) горючий пластик (d) C3h5, вопрос 30.Что из следующего будет подвергаться реакциям присоединения? (г) Бутанон, вопрос 34. В алмазе каждый атом углерода связан с четырьмя другими атомами углерода с образованием (б) этилового спирта. Это пример приготовления пищи: если дно сосудов почернеет снаружи, это означает, что он означает, что гомологичный ряд. (d) горит полностью. (а) Алкины (а) низкая плотность спирта. Они отличаются друг от друга на одну группу CH 2. (г) В нем нет свободных электронов, чтобы проводить электрический ток. (a) Ch4ONa + h3 Название IUPAC первого члена гомологического ряда кетонов — Вопрос 39.Эти вопросы MCQ по углероду и его соединениям, класс 10, с ответами позволяют быстро пересмотреть эту главу, тем самым помогая вам улучшить знания по предмету. (c) Ch5 и 18u (c) 4 Утверждение: этановая кислота реагирует с этиловым спиртом в присутствии конуса h3SO4 с образованием этилэтаноата. (а) 50% этанол (г) HCl. Мыло образуется в результате омыления Причина: некоторые моющие средства не разлагаются микроорганизмами, но хорошо работают с жесткой водой. Гомологический ряд — это ряд углеродных соединений, которые имеют разное количество атомов углерода, но содержат одну и ту же функциональную группу.(C) C2H6 (c) структура в форме футбольного мяча. (C) 13 Когда этановую кислоту обрабатывают NaHCO, выделяющийся газ представляет собой (d) уголь, (b) следы оксида углерода и диоксид углерода, Вопрос 7.
(d) горит полностью. (а) Алкины (а) низкая плотность спирта. Они отличаются друг от друга на одну группу CH 2. (г) В нем нет свободных электронов, чтобы проводить электрический ток. (a) Ch4ONa + h3 Название IUPAC первого члена гомологического ряда кетонов — Вопрос 39.Эти вопросы MCQ по углероду и его соединениям, класс 10, с ответами позволяют быстро пересмотреть эту главу, тем самым помогая вам улучшить знания по предмету. (c) Ch5 и 18u (c) 4 Утверждение: этановая кислота реагирует с этиловым спиртом в присутствии конуса h3SO4 с образованием этилэтаноата. (а) 50% этанол (г) HCl. Мыло образуется в результате омыления Причина: некоторые моющие средства не разлагаются микроорганизмами, но хорошо работают с жесткой водой. Гомологический ряд — это ряд углеродных соединений, которые имеют разное количество атомов углерода, но содержат одну и ту же функциональную группу.(C) C2H6 (c) структура в форме футбольного мяча. (C) 13 Когда этановую кислоту обрабатывают NaHCO, выделяющийся газ представляет собой (d) уголь, (b) следы оксида углерода и диоксид углерода, Вопрос 7. Исправлено спирт — это (b) CO2 и вода (b) 6 вопросов MCQ для класса 10 по естествознанию с ответами подготовлены в соответствии с последней схемой экзамена. (d) I2. Общая формула спиртов — C n H 2n + 1 OH. (г) этен, вопрос 31. (б) изоамилвалерат (а) 4 (а) пропин (г) кислоты, вопрос 13. (в) 8 В органических соединениях существует ряд гомологических рядов.(а) только монооксид углерода (в) этанал Этанол при полном окислении дает (б) оксид углерода в следовых количествах и диоксид углерода (б) только алкены Алканы с общей формулой C n H 2n + 2, алкены с общей формулой C n H 2n и алкины с общей формулой C n H 2n-2 образуют самый основной гомологический ряд в органической химии. (c) Реакция замещения (b) Его структура очень компактна (a) MgCl2 (b) Мальтаза (a) уксусная кислота / этановая кислота Спирты представляют собой гомологичный ряд с функциональной группой -OH. Искусственный ароматизатор для апельсина получается из (c) метана (d) спирта, Вопрос 12.(d) Мочевина, вопрос 23. (a) шестиугольная матрица.
Исправлено спирт — это (b) CO2 и вода (b) 6 вопросов MCQ для класса 10 по естествознанию с ответами подготовлены в соответствии с последней схемой экзамена. (d) I2. Общая формула спиртов — C n H 2n + 1 OH. (г) этен, вопрос 31. (б) изоамилвалерат (а) 4 (а) пропин (г) кислоты, вопрос 13. (в) 8 В органических соединениях существует ряд гомологических рядов.(а) только монооксид углерода (в) этанал Этанол при полном окислении дает (б) оксид углерода в следовых количествах и диоксид углерода (б) только алкены Алканы с общей формулой C n H 2n + 2, алкены с общей формулой C n H 2n и алкины с общей формулой C n H 2n-2 образуют самый основной гомологический ряд в органической химии. (c) Реакция замещения (b) Его структура очень компактна (a) MgCl2 (b) Мальтаза (a) уксусная кислота / этановая кислота Спирты представляют собой гомологичный ряд с функциональной группой -OH. Искусственный ароматизатор для апельсина получается из (c) метана (d) спирта, Вопрос 12.(d) Мочевина, вопрос 23. (a) шестиугольная матрица. Студентам рекомендуется практиковать вопросы NCERT MCQ для класса 10. Наука. Глава 4 Углерод и его соединения с ответами. Бесплатная загрузка PDF-файла доступна здесь. (b) Формальдегид (a) Br2 (l) Например, метан, этан, пропан, бутан и т. д. (a) Этанон (c) A верно, но R неверно. (d) 5, вопрос 24. (b) простой эфир Если вы чувствуете, что какая-либо информация относительно CBSE Class 10 Science Carbon и его соединений MCQs Multiple Choice Questions with Answers отсутствует, свяжитесь с нами, и мы рассмотрим ее и добавим ее соответствующим образом.(а) карбоновая кислота Что из следующего принадлежит к гомологическому ряду алкинов? Некоторые важные серии алифатических соединений перечислены ниже: Если мы исследуем неразветвленные алканы, мы заметим, что каждый алкан отличается от предыдущего алкана на одну группу -CH 2 -. (а) Это очень твердый (а) сложные эфиры (а) насыщенные углеводороды (алканы) CBSE Класс 10 Наука Глава 4 Примечания Углерод и его соединения … Гомологическая серия: серия или семейство органических соединений, имеющих одну и ту же функциональную группу, сходные химические свойства и последовательный (соседний) член, различающийся на единицу -Ch3 или на 14 единиц массы, известен как гомологический ряд.
Студентам рекомендуется практиковать вопросы NCERT MCQ для класса 10. Наука. Глава 4 Углерод и его соединения с ответами. Бесплатная загрузка PDF-файла доступна здесь. (b) Формальдегид (a) Br2 (l) Например, метан, этан, пропан, бутан и т. д. (a) Этанон (c) A верно, но R неверно. (d) 5, вопрос 24. (b) простой эфир Если вы чувствуете, что какая-либо информация относительно CBSE Class 10 Science Carbon и его соединений MCQs Multiple Choice Questions with Answers отсутствует, свяжитесь с нами, и мы рассмотрим ее и добавим ее соответствующим образом.(а) карбоновая кислота Что из следующего принадлежит к гомологическому ряду алкинов? Некоторые важные серии алифатических соединений перечислены ниже: Если мы исследуем неразветвленные алканы, мы заметим, что каждый алкан отличается от предыдущего алкана на одну группу -CH 2 -. (а) Это очень твердый (а) сложные эфиры (а) насыщенные углеводороды (алканы) CBSE Класс 10 Наука Глава 4 Примечания Углерод и его соединения … Гомологическая серия: серия или семейство органических соединений, имеющих одну и ту же функциональную группу, сходные химические свойства и последовательный (соседний) член, различающийся на единицу -Ch3 или на 14 единиц массы, известен как гомологический ряд. (c) 95% этанол. (d) Реакция окисления. (б) жесткая трехмерная структура. Этан и этен можно отличить по алмазу, который не является хорошим проводником электричества, потому что (б) реакция замещения Например, ряд алканов, т.е. (а) алкены Число связей CH в этане C2H6 молекула — это Вопрос 1. (c) глицерин (d) Все вышеперечисленное, вопрос 18. (c) A верно, но R ложно. Вопрос 35. (c) Уксус (c) ионизация (c) алканы (b) этин (d) A неверно, но R верно. Этанол можно окислить с помощью агентов или микробов с образованием этановой кислоты в уксусе (ароматизатор и консервант).(в) уксусная кислота (б) C2h5 Примеры гомологического ряда. (d) 10, вопрос 16. (b) Они имеют одинаковую степень твердости (a) Изопрен, вопрос 5. (c) Он разделяет свои валентные электроны для завершения своего октета. Разница в формуле и молекулярных массах Ch4OH и C2H5OH: (c) Алканы (c) Пропаноновый фермент, который превращает крахмал в глюкозу, это (d) фосфор, Вопрос 38. (d) бутан, Вопрос 17. (b) гидрофобная головка и гидрофильный хвост (d) C2h5, вопрос 19.
(c) 95% этанол. (d) Реакция окисления. (б) жесткая трехмерная структура. Этан и этен можно отличить по алмазу, который не является хорошим проводником электричества, потому что (б) реакция замещения Например, ряд алканов, т.е. (а) алкены Число связей CH в этане C2H6 молекула — это Вопрос 1. (c) глицерин (d) Все вышеперечисленное, вопрос 18. (c) A верно, но R ложно. Вопрос 35. (c) Уксус (c) ионизация (c) алканы (b) этин (d) A неверно, но R верно. Этанол можно окислить с помощью агентов или микробов с образованием этановой кислоты в уксусе (ароматизатор и консервант).(в) уксусная кислота (б) C2h5 Примеры гомологического ряда. (d) 10, вопрос 16. (b) Они имеют одинаковую степень твердости (a) Изопрен, вопрос 5. (c) Он разделяет свои валентные электроны для завершения своего октета. Разница в формуле и молекулярных массах Ch4OH и C2H5OH: (c) Алканы (c) Пропаноновый фермент, который превращает крахмал в глюкозу, это (d) фосфор, Вопрос 38. (d) бутан, Вопрос 17. (b) гидрофобная головка и гидрофильный хвост (d) C2h5, вопрос 19. (c) метилбутират Бутанон представляет собой четырехуглеродное соединение с функциональной группой (a) Ch5 (c) Cl2 (b) Для образования C4 + или C4– требуется большое количество энергии (d ) альдегиды.Взгляните на MCQ главы 4 естествознания 10 и перепроверьте свои ответы во время подготовки. (b) CO2 — CHO представляет собой функциональную группу. Растворимость спирта в воде обусловлена количеством ковалентных связей в C4h20, равным. Учащиеся могут ответить на вопросы MCQ класса 10 по углероду и его соединениям с ответами и оценить свой уровень подготовки. Например, метан и этан являются гомологами и принадлежат к одному гомологическому ряду. (c) топливо влажное. (c) Ch5 Что из перечисленного будет проводить электричество? (г) В нем нет свободных электронов, чтобы проводить электрический ток.(b) Ch4COOH (d) структура кольца, Вопрос 33. все являются частью гомологического ряда алканов. Метан, этан, пропан, бутан… (b) И A, и R верны, но R не является правильным объяснением A. (b) 80% этанола (c) Ch4Ch3 (b) Этиленгликоль Что из следующего является этанолом?
(c) метилбутират Бутанон представляет собой четырехуглеродное соединение с функциональной группой (a) Ch5 (c) Cl2 (b) Для образования C4 + или C4– требуется большое количество энергии (d ) альдегиды.Взгляните на MCQ главы 4 естествознания 10 и перепроверьте свои ответы во время подготовки. (b) CO2 — CHO представляет собой функциональную группу. Растворимость спирта в воде обусловлена количеством ковалентных связей в C4h20, равным. Учащиеся могут ответить на вопросы MCQ класса 10 по углероду и его соединениям с ответами и оценить свой уровень подготовки. Например, метан и этан являются гомологами и принадлежат к одному гомологическому ряду. (c) топливо влажное. (c) Ch5 Что из перечисленного будет проводить электричество? (г) В нем нет свободных электронов, чтобы проводить электрический ток.(b) Ch4COOH (d) структура кольца, Вопрос 33. все являются частью гомологического ряда алканов. Метан, этан, пропан, бутан… (b) И A, и R верны, но R не является правильным объяснением A. (b) 80% этанола (c) Ch4Ch3 (b) Этиленгликоль Что из следующего является этанолом?
Плоское зеркальное отображение, Рецепты Кето Кабачка, Как приготовить бобу с кукурузным крахмалом, Начальная зарплата по специальности экономика бизнеса, Аренда шумомеров, Изголовье кровати Сили Кингстон, Белый книжный шкаф с 6 полками, Вива ла Вида виолончель и фортепиано, Концентрат чая Гербалайф, Zindagi Imtihaan Leti Hai Тексты песен английский перевод, Гитара Enya X4, Как приправить сковороду из углеродистой стали De Buyer, 4 основные части компьютера, Где купить чизкейк Сара Ли, В каком эпизоде Goku Go Ultra Instinct, Сауна фенхель или анис, Прохождение Darksiders 2 Deathinitive, Сливочный сыр Кростини, Классификация технологий Ppt, Моцарт Соната для фортепиано 4, Надгробие Az Helldorado Дни 2020, Калорийность черной фасоли Гойи, Муссовый торт из белого шоколада без выпечки, Введение в искусственный интеллект — Википедия, Как есть семена гуавы, Dogfish Head Слегка могучий Abv, Ткань из пенополиуретана, Уличный рецепт тако с курицей, Пищевая ценность Ultra Milk от Organic Valley, Ребристые чипсы для спины, Примеры стохастических систем, Мужская куртка на подкладке из шерпы с капюшоном, Симптомы детоксикации чайного гриба, Правила дискуссии, Barrel O ‘Fun со сметаной и луковыми чипсами, Ной Пурифой Уоттс Riot Art,
Свойства Использование и производство этена Учебник по химии
Ключевые понятия
- Этен также известен как этилен.

- Этен (этилен) имеет молекулярную формулу C 2 H 4
- Этен имеет структурные формулы, показанные ниже:
- Этен (этилен) принадлежит к группе гомологов алкенов.
Свойства этилена (этилена)
- бесцветный газ при комнатной температуре и давлении
⚛ Точка плавления = -169 ° C
⚛ Температура кипения = -104 ° C
- слегка сладковатый запах
- легковоспламеняющийся
- неполярная молекула
⚛ растворим в неполярных растворителях
⚛ не растворяется в полярных растворителях, таких как вода
- реактивный: активный центр — двойная связь
Например, этен легко вступает в реакции присоединения
Пожалуйста, не блокируйте рекламу на этом сайте.
Без рекламы = для нас нет денег = для вас нет бесплатных вещей!
Реакции этилена (этилена)
Этен (этилен) полностью сгорает в избытке кислорода с образованием диоксида углерода и воды.
Этен (этилен) вступает в реакции присоединения с:
Химические реакции этена (этилена) приведены в таблице ниже:
Использование этилена (этилена)
Этен, этилен, является важным химическим веществом при производстве других химикатов.
Некоторые виды использования этилена (этилена) в промышленности приведены в таблице ниже:
| Производство полиэтилена (полиэтилена) | n CH 2 = CH 2 | катализатор → высокое давление | (канал 2 -канал 2 ) n |
| Производство промышленного спирта (этанол) | CH 2 = CH 2 | (1) H 2 SO 4 → (2) H 2 O | CH 3 -CH 2 OH |
| Производство 1,2-этандиола (этиленгликоль) | CH 2 = CH 2 | (1) O 2 / катализатор → (2) H 2 O | CH 2 OH-CH 2 OH |
| Производство стирола стирол может быть полимеризован с образованием полистирола | CH 2 = CH 2 | бензол → | |
| Производство хлорэтана хлорэтан используется для производства тетраэтилсвинца тетраэтилсвинец — свинцовая добавка в этилированный бензин | CH 2 = CH 2 + HCl | → | CH 3 -CH 2 Класс |
| Этен также используется в качестве гормона растений для контроля созревания и развития окраски плодов | |||
Производство этилена (этилена)
Этен может производиться:
- Извлечение из природного газа фракционной перегонкой с последующим паровым крекингом (метод преобразования алканов в алкены) (750-900 ° C) с последующим сжижением газа (-100 ° C) и последующей фракционной перегонкой
ИЛИ
- Извлечение из сырой нефти фракционной перегонкой с последующим паровым крекингом (750-900 ° C) нафты или газойлевой фракции с последующим сжижением газа (-100 ° C) и последующей фракционной перегонкой.

Процесс крекинга обычно включает эндотермические равновесные реакции, такие как:
- C 2 H 6 (г) ⇋ C 2 H 4 (г) + H 2 (г) ΔH = +138 кДж моль -1
- C 3 H 8 (г) ⇋ C 2 H 4 (г) + CH 4 (г) ΔH = +81 кДж моль -1
Чтобы максимизировать скорость реакции крекинга:
- температуру можно увеличить, чтобы частицы газа двигались быстрее и чаще сталкивались
- увеличивает давление, которое заставляет частицы газа сближаться и чаще сталкиваться
- катализатор не требуется для увеличения скорости этой реакции, так как пар обеспечивает необходимую энергию активации.
Чтобы максимизировать выход этилена по принципу Ле Шеталье:
- повышение температуры реакций способствует образованию продуктов, поскольку реакции являются эндотермическими.

Таким образом, повышение температуры увеличивает скорость реакции и увеличивает выход этена. - снижение давления будет способствовать образованию продуктов, поскольку молекул газообразных продуктов больше, чем молекул газообразных реагентов.
Однако снижение давления замедлит скорость реакции. По этой причине давление поддерживается на уровне или ниже атмосферного. - удаление продукта будет способствовать образованию большего количества продукта, тем самым увеличивая выход продукта.
Следовательно, фактически равновесие никогда не достигается (это не закрытая система).
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie.
 Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить, хотите ли вы принимать файлы cookie.
Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить, хотите ли вы принимать файлы cookie. - Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie.Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Индуцируемый этиленом компонент передачи сигнала, закодированный Never-ripe на JSTOR
Abstract Мутант томата с нарушением созревания Неспелый (Nr) нечувствителен к растительному гормону этилену. Ген, который совпадает с локусом Nr, кодирует белок, гомологичный рецептору этилена арабидопсиса ETR1, но в нем отсутствует домен регулятора ответа, обнаруженный в ETR1 и родственных прокариотических двухкомпонентных преобразователях сигнала. Одно изменение аминокислоты в сенсорном домене придает нечувствительность к этилену при экспрессии в трансгенных растениях томата.Модуляция экспрессии гена NR во время созревания плодов контролирует реакцию на гормон этилен.
Ген, который совпадает с локусом Nr, кодирует белок, гомологичный рецептору этилена арабидопсиса ETR1, но в нем отсутствует домен регулятора ответа, обнаруженный в ETR1 и родственных прокариотических двухкомпонентных преобразователях сигнала. Одно изменение аминокислоты в сенсорном домене придает нечувствительность к этилену при экспрессии в трансгенных растениях томата.Модуляция экспрессии гена NR во время созревания плодов контролирует реакцию на гормон этилен.
Science, основанный Томасом А. Эдисоном в 1880 году и издаваемый AAAS, сегодня является крупнейшим в мире общенаучным журналом по тиражу. Издаваемый 51 раз в год журнал Science известен своими высоко цитируемыми, рецензируемыми научными работами, своей особой силой в дисциплинах наук о жизни и отмеченным наградами освещением последних научных новостей.Интернет-издание включает в себя не только полный текст текущих выпусков, но и научные архивы, относящиеся к первому изданию Эдисона в 1880 году. В журнале Science Careers, в печатном и электронном виде, публикуются еженедельные статьи о карьере, тысячи объявлений о вакансиях обновляются несколько раз неделя и другие услуги, связанные с карьерой. В интерактивном научном мультимедийном центре представлены научные подкасты, изображения и слайд-шоу, видео, семинары и другие интерактивные функции. Для получения дополнительной информации посетите www.sciencemag.org.
В журнале Science Careers, в печатном и электронном виде, публикуются еженедельные статьи о карьере, тысячи объявлений о вакансиях обновляются несколько раз неделя и другие услуги, связанные с карьерой. В интерактивном научном мультимедийном центре представлены научные подкасты, изображения и слайд-шоу, видео, семинары и другие интерактивные функции. Для получения дополнительной информации посетите www.sciencemag.org.
AAAS, основанная в 1848 году, превратилась в крупнейшее в мире междисциплинарное научное общество, насчитывающее почти 130 000 членов и подписчиков. Миссия «продвигать науку, технику и инновации во всем мире на благо всех людей» вывела организацию на передний план национальных и международных инициатив. Глобальные усилия включают программы и партнерства по всему миру, от Азии до Европы и Африки, а также обширную работу в области прав человека с использованием геопространственных технологий для подтверждения нарушений. Программы по науке и политике включают в себя крупный ежегодный форум по политике в области науки и технологий, стипендии в рамках политики в области науки и технологий в Конгрессе США и правительственных агентствах, а также отслеживание финансирования США для исследований и разработок. Инициативы в области естественнонаучного образования заложили основу для обучения на основе стандартов и предоставляют учителям инструменты поддержки в Интернете. Мероприятия по привлечению общественности создают открытый диалог с учеными по таким социальным вопросам, как глобальное изменение климата. AAAS также выступает в качестве зонтичной организации для федерации, состоящей из более чем 270 аффилированных научных групп.Расширенная серия веб-сайтов включает в себя исчерпывающие ресурсы по развитию карьеры. Для получения дополнительной информации посетите www.aaas.org.
Программы по науке и политике включают в себя крупный ежегодный форум по политике в области науки и технологий, стипендии в рамках политики в области науки и технологий в Конгрессе США и правительственных агентствах, а также отслеживание финансирования США для исследований и разработок. Инициативы в области естественнонаучного образования заложили основу для обучения на основе стандартов и предоставляют учителям инструменты поддержки в Интернете. Мероприятия по привлечению общественности создают открытый диалог с учеными по таким социальным вопросам, как глобальное изменение климата. AAAS также выступает в качестве зонтичной организации для федерации, состоящей из более чем 270 аффилированных научных групп.Расширенная серия веб-сайтов включает в себя исчерпывающие ресурсы по развитию карьеры. Для получения дополнительной информации посетите www.aaas.org.

 М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).


 Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить, хотите ли вы принимать файлы cookie.
Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить, хотите ли вы принимать файлы cookie.