Неорганическая химия — это… Что такое Неорганическая химия?
Неоргани́ческая хи́мия — раздел химии, связанный с изучением строения, реакционной способности и свойств всех химических элементов и их неорганических соединений. Это область охватывает все химические соединения, за исключением органических веществ (класса соединений, в которые входит углерод, за исключением нескольких простейших соединений, обычно относящихся к неорганическим[1]). Различие между органическими и неорганическими соединениями, содержащими углерод, являются по некоторым представлениям произвольными.[2]Неорганическая химия изучает химические элементы и образуемые ими простые и сложные вещества (кроме органических соединений). Обеспечивает создание материалов новейшей техники. Число неорганических веществ приближается к 400 тысячам.
Теоретическим фундаментом неорганической химии является периодический закон и основанная на нём периодическая система Д. И. Менделеева.
В России исследованиями в области неорганической химии занимаются Институт неорганической химии им. А. В. Николаева СО РАН (ИНХ СО РАН, Новосибирск), Институт общей и неорганической химии им. Н. С. Курнакова (ИОНХ РАН, Москва), Институт физико-химических проблем керамических материалов (ИФХПКМ, Москва), Научно-технический центр «Сверхтвердые материалы» (НТЦ СМ, Троицк) и ряд других учреждений. Результаты исследований публикуются в журналах («Журнал неорганической химии» и др.).
История определения
Исторически название неорганическая химия происходит от представления о части химии, которая занимается исследованием элементов, соединений, а также реакций веществ, которые не образованы живыми существами. Однако со времен синтеза мочевины из неорганического соединения цианата аммония (NH
4OCN), который совершил в 1828 году выдающийся немецкий химик Фридрих Вёлер, стираются границы между веществами неживой и живой природы. Так, живые существа производят много неорганических веществ. С другой стороны, почти все органические соединения можно синтезировать в лаборатории. Однако деление на различные области химии является актуальным и необходимым, как и раньше, поскольку механизмы реакций, структура веществ в неорганической и органической химии различаются. Это позволяет проще систематизировать методы и способы исследования в каждой из отраслей.
Так, живые существа производят много неорганических веществ. С другой стороны, почти все органические соединения можно синтезировать в лаборатории. Однако деление на различные области химии является актуальным и необходимым, как и раньше, поскольку механизмы реакций, структура веществ в неорганической и органической химии различаются. Это позволяет проще систематизировать методы и способы исследования в каждой из отраслей.Классификация химических элементов
Периоди́ческая систе́ма хими́ческих элеме́нтов (табли́ца Менделе́ева) — классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона, установленного русским химиком Д. И. Менделеевым в 1869 году. Её первоначальный вариант был разработан Д. И. Менделеевым в 1869—1871 годах и устанавливал зависимость свойств элементов от их атомного веса (по-современному, от атомной массы). Всего предложено несколько сотен
 В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико-химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу.
В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико-химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу.Простые вещества
Состоят из атомов одного химического элемента (являются формой его существования в свободном состоянии). Все простые вещества в неорганической химии делятся на две большие группы: Металлы — Неметаллы.
Металлы
Мета́ллы (от лат. metallum — шахта, рудник) — группа элементов, обладающая характерными
металлическими свойствами, такими как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск. Из 118[4]химических элементов, открытых на данный момент (из них не все официально признаны), к металлам относят:Таким образом, к металлам относится 96 элементов из всех открытых.
Неметаллы
Немета́ллы — химические элементы с типично неметаллическими свойствами, которые занимают правый верхний угол Периодической системы. В молекулярной форме в виде простых веществ в природе встречаются азот, кислород и сера. Чаще неметаллы находятся в химически связанном виде: это вода, минералы, горные породы, различные силикаты, фосфаты, бораты. По распространённости в земной коре неметаллы существенно различаются. Наиболее распространёнными являются кислород, кремний, водород; наиболее редкими — мышьяк, селен, иод. Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов. Это определяет их бо́льшую способность к присоединению дополнительных электронов и проявлению более высокой окислительной активности, чем у металлов. К неметаллам также относят водород и гелий.
В молекулярной форме в виде простых веществ в природе встречаются азот, кислород и сера. Чаще неметаллы находятся в химически связанном виде: это вода, минералы, горные породы, различные силикаты, фосфаты, бораты. По распространённости в земной коре неметаллы существенно различаются. Наиболее распространёнными являются кислород, кремний, водород; наиболее редкими — мышьяк, селен, иод. Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов. Это определяет их бо́льшую способность к присоединению дополнительных электронов и проявлению более высокой окислительной активности, чем у металлов. К неметаллам также относят водород и гелий.
Сложные вещества
Большую часть сложных неорганических веществ (то есть состоящих из двух и более химических элементов) можно разделить на следующие группы:
Оксиды
Окси́д (о́кисел, о́кись) — бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам относятся почти все соединения химических элементов с кислородом. К исключениям относятся, например, дифторид кислорода OF
Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам относятся почти все соединения химических элементов с кислородом. К исключениям относятся, например, дифторид кислорода OF
Соли
Со́ли — класс химических соединений, к которому относятся вещества, состоящие из катионов металла (или катионов аммония ; известны соли фосфония или гидроксония ) и анионов кислотного остатка. Типы солей:
Особую группу составляют соли органических кислот, свойства которых значительно отличаются от свойств минеральных солей. Некоторые из них можно отнести к особенному классу органических солей, так называемых ионных жидкостей или по-другому «жидких солей», органических солей с температурой плавления ниже 100 °C.
Основания
Основа́ния
Кислоты
Кисло́ты — сложные вещества, в состав которых обычно входят атомы водорода, способные замещаться на атомы металлов, и кислотный остаток. Водные растворы кислот имеют кислый вкус, обладают раздражающим действием, способны менять окраску индикаторов, отличаются рядом общих химических свойств.
Также можно выделить следующие группы неорганических веществ: карбиды, нитриды, гидриды, интерметаллиды и другие, которые не укладываются в приведённую выше классификацию (более подробно см. Неорганическое вещество).
Карбиды
Карби́ды — соединения металлов и неметаллов с углеродом. Традиционно к карбидам относят соединения, в которых углерод имеет большую электроотрицательность, чем второй элемент (таким образом из карбидов исключаются такие соединения углерода, как оксиды, галогениды и тому подобные). Карбиды — тугоплавкие твёрдые вещества: карбиды бора и кремния (В4С и SiC), титана, вольфрама, циркония (TiC, WC и ZrC соответственно) обладают высокой твёрдостью, жаростойкостью, химической инертностью.
Нитриды
Нитри́ды — соединения азота с менее электроотрицательными элементами, например, с металлами (AlN;TiNx;Na3N;Ca3N2;Zn3N2; и т. д.) и с рядом неметаллов (NH3, BN, Si3N4). Соединения азота с металлами чаще всего являются тугоплавкими и устойчивыми при высоких температурах веществами, например, эльбор. Нитридные покрытия придают изделиям твёрдость, коррозионную стойкость; находят применение в энергетике, космической технике.
Гидриды
Гидри́ды — соединения водорода с металлами и с имеющими меньшую электроотрицательность, чем водород, неметаллами. Иногда к гидридам причисляют соединения всех элементов с водородом[5][6].
Интерметаллиды
 Интерметаллиды обладают, как правило, высокой твёрдостью и высокой химической стойкостью. Очень часто интерметаллиды имеют более высокую температуру плавления, чем исходные металлы. Почти все интерметаллиды хрупки, так как связь между атомами в решётке становится ковалентной или ионной (например, в ауриде цезия CsAu), а не металлической. Некоторые из них имеют полупроводниковые свойства, причём, чем ближе к стехиометрии соотношение элементов, тем выше электрическое сопротивление. Никелид титана, известный под маркой «нитинол», обладает памятью формы — после закалки изделие может быть деформировано механически, но примет исходную форму при небольшом нагреве.
Интерметаллиды обладают, как правило, высокой твёрдостью и высокой химической стойкостью. Очень часто интерметаллиды имеют более высокую температуру плавления, чем исходные металлы. Почти все интерметаллиды хрупки, так как связь между атомами в решётке становится ковалентной или ионной (например, в ауриде цезия CsAu), а не металлической. Некоторые из них имеют полупроводниковые свойства, причём, чем ближе к стехиометрии соотношение элементов, тем выше электрическое сопротивление. Никелид титана, известный под маркой «нитинол», обладает памятью формы — после закалки изделие может быть деформировано механически, но примет исходную форму при небольшом нагреве. См. также
Примечания
- ↑ К неорганическим соединениям углерода обычно относят некоторые соли (карбонаты, цианиды, цианаты, тиоцианаты) и соответствующие им кислоты, а также оксиды углерода, карбонилы металлов и карбиды.
- ↑ Spencer L. Seager, Michael R. Slabaugh. Chemistry for Today: general, organic, and biochemistry.
 // Thomson Brooks/Cole, 2004. — Р. 342. ISBN 0-534-39969-X
// Thomson Brooks/Cole, 2004. — Р. 342. ISBN 0-534-39969-X - ↑ В книге В. М. Потапов, Г. Н. Хомченко «Химия», М. 1982 (стр. 26) утверждается, что их более 400.
- ↑ Международный химический союз признал 112-й химический элемент
- ↑ Гидриды. XuMuK.ru. Архивировано из первоисточника 22 июня 2012. Проверено 15 июля 2010.
- ↑ onium compounds // IUPAC Gold Book
Литература
- Капустинский А. Ф. Очерки по истории неорганической и физической химии в России. М.-Л., 1949
- Жамбулова М. Ш. Развитие неорганической химии (Историко-методологический аспект). Алма-Ата, 1981.- 187 с.
- Неорганическое материаловедение в СССР. Под ред. И. В. Тананаева — Киев: Наукова думка, 1983. — 720 с.
- Популярная библиотека химических элементов. Т. 1,2. / Под ред. И. В. Петрянова-Соколова — М.: Наука, 1983. — 575 с., — 572 с.
- Реми Г. Курс неорганической химии. Т. 1. М.: Изд-во иностранной ли-тературы, 1963.
 — 920 с.
— 920 с. - Реми Г. Курс неорганической химии. Т. 2. М.: Мир, 1974. — 775 с.
- Шрайвер Э. Неорганическая химия. Т. 1,2. / Э. Шрайвер, П. Эткинс — М.: Мир, 2004. — 679 с., — 486 с.
- Энциклопедия неорганических материалов / Под ред. И. М. Федорчен-ко. В 2-х т. — Киев: Укр. сов. энциклопедия, 1977. — 1652 с.
- Аблесимов Н. Е. Синопсис химии: Справочно-учебное пособие по общей химии — Хабаровск: Изд-во ДВГУПС, 2005. — 84 с. — http://www.neablesimov.narod.ru/pub04c.html
- Аблесимов Н. Е. Сколько химий на свете? ч. 1. // Химия и жизнь — XXI век. — 2009. — № 5. — С. 49-52.
Ссылки
| В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 14 мая 2011. |
Интересная органическая химия.
 Интересные факты о химии.
Интересные факты о химии.В эту самую минуту
Пока Вы читаете данную статью, Ваши глаза используют органическое соединение – ретиналь, который преобразует световую энергию в нервные импульсы. Пока Вы сидите в удобной позе, мышцы спины поддерживают правильную осанку благодаря химическому расщеплению глюкозы с высвобождением требуемой энергии. Как Вы понимаете, пробелы между нервными клетками так же заполнены органическими веществами – медиаторами (или нейространсмиттерами), которые помогают всем нейронам стать одним целым. И данная слаженная система работает без участия Вашего сознания! Так глубоко, как биологи, только химики-органики понимают, насколько филигранно создан человек, как логично устроены внутренние системы органов и их жизненный цикл. Отсюда следует, что изучение органической химии – основа понимания нашей жизни! А качественное изучение – это путь в будущее, ибо новые лекарства создаются прежде всего в химических лабораториях. Наша кафедра желает познакомить Вас поближе с этой прекрасной наукой.
Наша кафедра желает познакомить Вас поближе с этой прекрасной наукой.
11-цис-ретиналь, поглощает свет
серотонин – нейромедиатор
Органическая химия как наука
Органическая химия как наука возникла в конце девятнадцатого века. Она возникла на перекрещивании разных сфер жизни – от получения пищи до лечения миллионов людей, не подозревающих о роли химии в их жизни. Химия занимает уникальное место в структуре понимания Вселенной. Это наука о молекулах, но органическая химия является чем-то большим, чем это определение. Органическая химия в буквальном смысле сама себя создает, словно растет. Органическая химия, занимаясь изучением не только природных молекул имеет возможность самой создавать новые вещества, структуры, материи. Данная особенность подарила человечеству полимеры, красители для одежды, новые лекарства, духи. Некоторые считают, что синтетические материалы могут нанести вред человеку, либо быть экологически опасными. Однако, как порой отличить черное от белого, так и установить тонкую грань между «опасностью для человека» и «коммерческой выгодой» очень сложно. В этом вопросе так же поможет кафедра Органического синтеза и нанотехнологий (ОСиНТ).
Однако, как порой отличить черное от белого, так и установить тонкую грань между «опасностью для человека» и «коммерческой выгодой» очень сложно. В этом вопросе так же поможет кафедра Органического синтеза и нанотехнологий (ОСиНТ).
Органические соединения
Органическая химия формировалась, как наука о жизни, ранее считалось, что она сильно отличается от неорганической химии в лаборатории. Затем ученые полагали, что органическая химия – это химия Углерода, особенно соединений каменного угля. В наше время органическая химия объединяет все соединения Углерода как живой, так и не живой природы.
Доступные для нас органические соединения получаются либо из живых организмов, либо из ископаемых материалов (нефть, уголь). Примером субстанций из природных источников являются эфирные масла – ментол (вкус мяты) и цис-жасмон (аромат цветков жасмина). Эфирные масла получают перегонкой с водяным паром; подробности раскроются при обучении на нашей кафедре.
- Ментол
- Цис-жасмон
- Хинин
Уже в 16 веке был известен алкалоид – хинин, который получают из коры хинного дерева (Южная Америка) и используют против малярии.
Иезуиты, что открыли данное свойство хинина, конечно же не знали его структуры. Тем более в те времена не стоял вопрос о синтетическом получении хинина – что удалось осуществить только в 20 столетии! Ещё любопытная история, связанная с хинином – это открытие фиолетового пигмента мовеина Уильямом Перкиным в 1856 году. Зачем он это сделал и какие результаты его открытия – так же можно узнать на нашей кафедре.
Но вернемся к истории становления органической химии. В 19 веке (времена У. Перкина) основным источником сырья для химической промышленности был уголь. Сухая перегонка угля давала коксовый газ, который использовался для обогрева и приготовления пищи, каменноугольную смолу, богатую на ароматические карбоциклические и гетероциклические соединения (бензол, фенол, анилин, тиофен, пиридин). На нашей кафедре Вам расскажут, чем они отличаются и какое они имеют значение в органическом синтезе.
На нашей кафедре Вам расскажут, чем они отличаются и какое они имеют значение в органическом синтезе.
Бензол, пиридин, фенол, анилин, тиофен
Фенол обладает антисептическими свойствами (тривиальное название – карболовая кислота), а анилин стал основой развития красочной промышленности (получение анилиновых красителей). Данные красящие вещества по-прежнему коммерчески доступны, например, Бисмарк-Браун (коричневый) показывает, что большая часть ранних трудов по химии была проведена в Германии:
Бисмарк-Браун
Однако в 20 столетии, нефть опередила уголь в качестве основного источника органического сырья и энергии, поэтому газообразные метан (природный газ), этан, пропан стали доступным энергетическим ресурсом.
В тоже время, химическая промышленность разделилась на массовую и тонкую. Первая занимается производством красок, полимеров – веществ, не имеющих сложное строение, однако, производимых в огромном количестве. А тонкая химическая промышленность, правильнее сказать – тонкий органический синтез занимается получением лекарств, ароматов, вкусовых добавок, в гораздо меньших объемах, что, однако более прибыльно. В настоящее время известно около 16 миллионов органических соединений. Сколько ещё возможно? В этой области, органический синтез не имеет ограничений. Представьте себе, что Вы создали самую длинную алкильную цепь, однако Вы можете легко добавить ещё один углеродный атом. Этот процесс бесконечен. Но не следует думать, что все эти миллионы соединений – обычные линейные углеводороды; они охватывают все виды молекул с удивительно разнообразными свойствами.
А тонкая химическая промышленность, правильнее сказать – тонкий органический синтез занимается получением лекарств, ароматов, вкусовых добавок, в гораздо меньших объемах, что, однако более прибыльно. В настоящее время известно около 16 миллионов органических соединений. Сколько ещё возможно? В этой области, органический синтез не имеет ограничений. Представьте себе, что Вы создали самую длинную алкильную цепь, однако Вы можете легко добавить ещё один углеродный атом. Этот процесс бесконечен. Но не следует думать, что все эти миллионы соединений – обычные линейные углеводороды; они охватывают все виды молекул с удивительно разнообразными свойствами.
Алифатические соединения
Свойства органических соединений
Каковы же физические свойства органических соединений?
Они могут быть кристаллическими как сахар, или пластичными как парафин, взрывоопасными как изооктан, летучими как ацетон.
- Сахароза
- Изооктан (2,3,5-триметилпентан)
Окраска соединений так же может быть самая разнообразная. Человечество уже столько синтезировало красителей, что создается впечатление, что уже не осталось таких цветов, какие нельзя получить с помощью синтетических красителей.
К примеру, можно составить такую таблицу ярко окрашенных веществ:
Однако кроме этих характеристик, органические вещества обладают запахом, который помогает их дифференцировать. Любопытный пример – защитная реакция скунсов. Запах секрета скунсов обуславливают сернистые соединения – тиолы:
Компоненты секретов скунсов
Но самый ужасный запах был «унюхан» в городе Фрайбурге (1889), во время попытки синтеза тиоацетона разложением тримера, когда пришлось эвакуировать население города, поскольку «неприятный запах, которых быстро распространился по большой площади в городе, вызывает обмороки, рвоту и тревожные состояния». Лабораторию закрыли.
Лабораторию закрыли.
Но этот опыт решили повторить химики научной станции Ессо (Esso) к югу от Оксфорда. Передадим им слово:
«В последнее время, проблемы запаха вышли за пределы наших худших ожиданий. Во времена ранних экспериментов, пробка выскочила из бутылки с отходами и сразу была заменена, а наши колеги из соседней лаборатории (200 ярдов) немедленно почувствовали тошноту и рвоту.
Двое из наших химиков, которые просто изучали крекинг незначительных количеств тритиоацетона нашли себя как объект враждебных взглядов в ресторане и были посрамлены, когда официантка распылила дезодорант вокруг них. Запахи «бросили вызов» ожидаемым эффектам разбавления, поскольку работники лаборатории не считали запахи невыносимыми… и по-настоящему отрицали свою ответственность, так как они работали в закрытых системах. Чтобы убедить их в обратном, они были распределены с другими наблюдателями по всей территории лаборатории на расстояниях до четверти мили. Затем одна капля ацетон гем-дитиола, а позже маточного раствора перекристаллизации тритиоацетона была размещена на часовом стекле в вытяжном шкафу. Запах был обнаружен по ветру в считанные секунды». Т.е. запах этих соединений усиливается при понижении концентрации.
Затем одна капля ацетон гем-дитиола, а позже маточного раствора перекристаллизации тритиоацетона была размещена на часовом стекле в вытяжном шкафу. Запах был обнаружен по ветру в считанные секунды». Т.е. запах этих соединений усиливается при понижении концентрации.
Существует два претендета на эту ужасную вонь – дитиол пропан (вышеуказанный гем-дитиол), либо 4-метил-4сульфанил-пентанон-2:
Вряд ли кто-то найдется чтобы определить из них лидера.
Однако, неприятный запах имеет свою область применения. Природный газ, что поступает в наши дома содержит небольшое количество ароматизатора – третбутил тиола. Небольшое количество – это столько, что люди способны почувствовать одну часть тиола в 50 миллиардах частей метана.
Напротив, некоторые другие соединения имеют восхитительные запахи. Чтобы искупить честь сернистых соединений мы должны сослаться на трюфель, который хрюшки могут унюхать через метр почвы и чей вкус и запах настолько восхитительны что они стоят дороже, чем золото. За аромат роз отвечают дамаскеноны. Если Вы имеете возможность понюхать запах одной капли, то Вы, вероятно, будете разочарованы, так как она пахнет как скипидар, или камфора. А на следующее утро Ваша одежда (и Вы в том числе) будете очень сильно благоухать розами. Так же, как и тритиоацетон, этот запах усиливается при разведении.
За аромат роз отвечают дамаскеноны. Если Вы имеете возможность понюхать запах одной капли, то Вы, вероятно, будете разочарованы, так как она пахнет как скипидар, или камфора. А на следующее утро Ваша одежда (и Вы в том числе) будете очень сильно благоухать розами. Так же, как и тритиоацетон, этот запах усиливается при разведении.
Компонент аромата трюфелей
Демаскенон – аромат роз
А как насчет вкуса?
Всем известно, что дети могут попробовать на вкус бытовую химию (средство для чистки ванны, туалета и т.д.). Перед химиками встала задача, чтобы несчастные дети больше не захотели попробовать какую-то химию в яркой упакове. Обратите внимание, что это сложное соединение является солью:
Битрекс денатониум бензоат
Некоторые другие вещества оказывают «странное» воздействие на человека, вызывая комплексы психических ощущений – галюцинации, эйфорию и т.д. К ним относятся наркотики, этиловый спирт. Они очень опасны, т.к. вызывают зависимость и уничтожают человека как личность.
Давайте не забывать и о других существах. Известно, что кошки любят спать в любое время. Недавно ученые получили из спинномозговой жидкости бедных кошек вещество, позволяющее им быстро засыпать. Оно так же действует и на человека. Это удивительно простое соединение:
Инициатор сна – цис-9,10-октадеценоамид
Подобная структура, носящая название Коньюгированная Линолевая Кислота (КЛК) обладает противоопухолевыми свойствми:
КЛК- противораковое средство цис-9-транс-11 сопряженная линолевая кислота
Ещё одна любопытная молекула – ресвератол, может быть отвечает за благотворное влияние красного вина в профилактике сердечных заболеваний:
Ресвератол из шкурки виноградинок
В качестве третьего примера «съедобных» молекул (после КЛК и ресвератрола) возьмем витамин С. Моряки дальнего плавания времен эпохи Великих Географических Открытий страдали заболеванием скорбут (цингой), когда происходят дегенеративные процессы мягких тканей, особенно ротовой полости. Нехватка данного витамина и вызывает цингу. Аскорбиновая кислота (тривиальное название витамина С) является универсальным антиоксидантом, она нейтрализует свободные радикалы, защищая людей от рака. Некоторые считают, что большие дозы витамина С защищают нас от простуды, но это ещё не доказано.
Нехватка данного витамина и вызывает цингу. Аскорбиновая кислота (тривиальное название витамина С) является универсальным антиоксидантом, она нейтрализует свободные радикалы, защищая людей от рака. Некоторые считают, что большие дозы витамина С защищают нас от простуды, но это ещё не доказано.
Витамин С
Органическая химия и промышленность
Витами С в больших колличествах получают в Швейцарии, на фармацевтическом заводе Roshe (не путать с РошеноМ). Во всем мире объемы промышленности органического синтеза исчисляются как килограмами (мелкотоннажные производства), так и миллионами тонн (крупнотоннажные производства). Это хорошая новость для студентов-органиков, т.к. дефицита рабочих мест (равно как и переизбытка выпускников) тут нет. Другими словами профессия инженера-химика очень актуальна.
Некоторые простые соединения можно получать как из нефти, так и из растений. Этиловый спирт используют в качестве сырья для получения резины, пластмасс, других органических соединений. Его можно получить каталитической гидратацией этилена (из нефти), либо путем ферментации отходов сахарной промышленности (как в Бразилии, где использование этанола в качестве топлива позволило улучшить экологическую ситуацию).
Его можно получить каталитической гидратацией этилена (из нефти), либо путем ферментации отходов сахарной промышленности (как в Бразилии, где использование этанола в качестве топлива позволило улучшить экологическую ситуацию).
Стоит отдельно упомянуть полимерную промышленность. Она поглощает наибольшую часть продуктов переработки нефти в виде мономеров (стирол, акрилаты, винилхлорид, этилен). Производство синтетических волокон имеет оборот более чем 25 миллионов тонн в год. В получение поливинилхлорида вовлечено около 50 000 людей с годовым выпуском 20 миллионов тонн.
Следует так же упомянуть производство клеев, герметиков, покрытий. Например, известным суперклеем (на основе метил цианоакрилата) Вы можете приклеить почти все.
Цианоакрилат – основной компонент суперклея
Пожалуй, наиболее известным красителем является индиго, который раньше выделяли из растений, а сейчас получают синтетически. Индиго – это цвет синих джинсов. Для окраски полиэфирных волокон используются, к примеру, бензодифураноны (как дисперсол), которые придают ткани отличный красный цвет. Для окрашивания полимеров используют фталоцианины в виде комплексов с железом, или медью. Они так же находят применение в качестве компонента активного слоя CD, DVD, Blu Ray дисков. Новый класс «высокопроизводительных» красителей на основе DPP (1,4-diketopyrrolo[3,4-c]pyrroles) разработан Ciba-Geidy.
Индиго – это цвет синих джинсов. Для окраски полиэфирных волокон используются, к примеру, бензодифураноны (как дисперсол), которые придают ткани отличный красный цвет. Для окрашивания полимеров используют фталоцианины в виде комплексов с железом, или медью. Они так же находят применение в качестве компонента активного слоя CD, DVD, Blu Ray дисков. Новый класс «высокопроизводительных» красителей на основе DPP (1,4-diketopyrrolo[3,4-c]pyrroles) разработан Ciba-Geidy.
Индиго
Фотография сначала была черно-белой: галоиды серебра взаимодействуя со светом высвобождали атомы металла, которые и воспроизводили изображение. Окрашенные фотографии в цветной пленке марки Кодак возникали как следствие химической реакции между двумя бесцветными реагентами. Один из них, как правило ароматический амин:
От фотоискусства можно легко перейти в сладкую жизнь.
Подсластители, такие как классический сахар получают в огромных масштабах. Другие подсластители, как аспартам (1965) и сахарин (1879) производятся в аналогичных объемах. Аспартам представляет собой дипептид из двух натуральных аминокислот:
Другие подсластители, как аспартам (1965) и сахарин (1879) производятся в аналогичных объемах. Аспартам представляет собой дипептид из двух натуральных аминокислот:
Фармацевтические компании производят лекарственные субстанции от многих болезней. Примером коммерчески успешного, революционного препарата является Ранитидин (от язвенной болезни) и Силденафил (Виагра, надеемся Вы в курсе кому и зачем она нужна).
Успех этих препаратов связан как с лечебной эффективностью, так и прибыльностью:
Это еще не всё. Это только начало
Ещё осталось много интересного об органической химии, поэтому обучение на кафедре ОСиНТ является приоритетным не только для любителей химии, но и для абитуриентов, которым интересен окружающий мир, которые желают расширить рамки своего восприятия и раскрыть свой потенциал.
Всё о поступлении на специальность Химические технологии и инженерияПоступлениена 1 курс
Все самое важное для абитуриента
смотрите здесь
Подробнее
Продолжение обученияПоступление на 2-4 курс, в магистратуру и аспирантуру. Все формы обучения!
Все формы обучения!
Подробнее
Нашигалереи
Лучше 1 раз увидеть
Чем 100 раз услышать!
Смотрите наши фотографии
Подробнее
Вот несколько последних статей:
Говорили о том какой бывает этиловый спирт из чего его делают, как фальсифицируют и проводят анализы, и чего стоит остерегаться.…
Глицерин применение – пищевые продукты, косметика и взрывчатые вещества Читая этикетки косметических средств, мы зачастую замечаем в их составе глицерин.…
Не так давно Пепси объявила, что они больше не будут использовать подсластитель аспартам, искусственный сахарозаменитель, в диетической Пепси (на территории…
По доброй традиции встреча Нового года у большинства людей не обходится без открытой бутылки шампанского.
 Напиток в бокале с его…
Напиток в бокале с его…
СОСТАВ КРАСКИ ДЛЯ ВОЛОС КРАСИТЕЛИ И ПИГМЕНТЫ Сегодня, стойкая краска для волос широко используются, либо чтобы прикрыть седые волосы, либо…
Поделиться
Чем органические продукты отличаются от неорганических?
Чем органические продукты отличаются от неорганических?
Конечно же, вы видели в супермаркетах упаковки молока с красивой зеленой наклейкой “ЭКО” или яйца в сене с надписью “100% органика”. Возможно, даже покупали. И не раз задавались вопросом, чем такие продукты отличаются от неорганических.
Исследование, проведённое сотрудниками Стэнфордского университета, показало, что по влиянию на человеческое здоровье органические и неорганические продукты из супермаркета практически не отличаются друг от друга.Главное отличие — способ выращивания
Хотя многие уверены, что продукты, выращенные органическим путем, являются более питательными и содержат в себе большее количество витаминов и минералов, это не совсем так. Главным отличием между так называемыми “органическими” и “неорганическими” продуктами является способ их выращивания.
Главным отличием между так называемыми “органическими” и “неорганическими” продуктами является способ их выращивания.
Органика — это обыкновенная пища, выращенная дедовским способом без использования синтетических пестицидов, регуляторов роста и любой другой химии.
Неорганические продукты иногда могут быть даже питательней органических
Кажется, что съев банан с наклейкой “ЭКО”, вы тут же почувствуете, как по вашему телу расходятся тысячи питательных веществ. А обычный банан не даст вам столько пользы. Но если говорить о питательности, то неорганические продукты иногда даже выигрывают у органических. Ведь в обычный рис часто добавляют дополнительный бета-каротин, молоко обогащают витамином D, а фруктовые соки — кальцием. Добавлять что-то в органические продукты категорически запрещено.
Органическое молоко имеет больше железа, фосфора и витамина Е и жирных кислот омега-3
Но, во-первых, это разница в несколько процентов, во-вторых, наш организм обычно не страдает дефицитом этих веществ.
Также органическое молоко и мясо содержит примерно на 50% больше полезных для человека жирных кислот омега-3. От них зависит тонус кровеносных сосудов, давление, иммунитет и обмен веществ человеческого организма.
Но даже в два раза большего количества жирных кислот омега-3 в молоке все равно слишком мало для удовлетворения потребностей человека. Поэтому даже органическое молоко значительно уступает в этом плане морепродуктам или семенам льна.
В органических продуктах меньше пестицидов и микроорганизмов, но они есть
Вероятность того, что в органических продуктах, купленных значительно дороже чем неорганические, есть пестициды — на 30 % ниже, чем в неорганических. Но они все равно там есть. Также как и ГМО. Ведь остатки этих “плохих” веществ могут быть в семени, попасть на фрукт или овощ с дождем или еще каким-то образом.Количество патогенной микрофлоры в “органике” может быть такой же, как и в “неорганике”. Хотя надо еще учесть добропорядочность украинских “органических предпринимателей”- ведь деды навоз для удобрения не стерилизовали. То есть подхватить кишечную палочку у вас больше шансов именно от органических продуктов.
То есть подхватить кишечную палочку у вас больше шансов именно от органических продуктов.
Классификация веществ — урок. Химия, 8–9 класс.
Все вещества делятся на простые и сложные.
Простые вещества состоят из атомов одного элемента.
Сложные вещества (химические соединения) состоят из атомов нескольких элементов.
Простые вещества разделяют на металлы и неметаллы. Деление основано на различиях в их свойствах.
Металлы имеют характерный «металлический» блеск, ковкость, высокую теплопроводность и электропроводность. При комнатной температуре все металлы (кроме ртути) твёрдые. Большинство металлов вытесняют из кислот водород.
Рис. \(1\). Серебро
Неметаллы не обладают характерным блеском, ковкостью. Многие неметаллы при обычных условиях газообразны.
Многие неметаллы при обычных условиях газообразны.
Рис. \(2\). Сера
Сложные вещества делят на органические и неорганические.
Органические вещества — соединения углерода. В их состав могут также входить атомы водорода, кислорода, азота, фосфора, серы.
Почти все органические вещества горючи и легко разлагаются при нагревании. Практически все они имеют молекулярное строение.
Органических веществ миллионы. Они содержатся во всех живых организмах, входят в состав продуктов питания, топлива, лекарств, красителей, пластмасс.
Рис. \(3\). Изделия из пластмасс
Неорганические вещества — соединения всех остальных элементов. К ним относятся также некоторые вещества, содержащие углерод: сода, мел, угарный и углекислый газы и др. Простые вещества тоже являются неорганическими.
Неорганических веществ около \(700\) тысяч. Они образуют неживую природу: минералы, горные породы и т. д. Почти все неорганические вещества имеют немолекулярное строение. Большинство из них при обычных условиях представляют собой твёрдые вещества.
д. Почти все неорганические вещества имеют немолекулярное строение. Большинство из них при обычных условиях представляют собой твёрдые вещества.
Рис. \(4\). Мел
Источники:
Рис. 1. Серебро https://cdn.pixabay.com/photo/2014/12/22/00/06/silver-576793_960_720.png
Рис. 2. Сера https://upload.wikimedia.org/wikipedia/commons/thumb/4/44/Sulfur-sample.jpg/1280px-Sulfur-sample.jpg Общественное достояние
Рис. 3. Изделия из пластмасс https://cdn.pixabay.com/photo/2015/05/23/18/41/sand-pit-780855_960_720.jpg
Рис. 4. Мел https://cdn.pixabay.com/photo/2020/09/20/11/24/limestones-5586848_960_720.jpg
Взаимосвязь неорганических и органических веществ – УчМет
Муниципальное бюджетное образовательное учреждение
«Средняя общеобразовательная школа № 11 с углублённым изучением отдельных предметов Зеленодольского муниципального района республики Татарстан»
422550,
РТ, г. Зеленодольск, ул. Гоголя, 40а
Зеленодольск, ул. Гоголя, 40а
тел. (84371) 5-44-15, 5-27-08,
Тема урока:
Взаимосвязь неорганических и органических веществ.
Урок разработан учителем химии высшей квалификационной категории: Абдулиной Маргаритой Ивановной.
Предмет: химия.
Автор учебника: И.И. Новошинский
Пояснительная запискаВ условиях профильного обучения учителя химии используют нетрадиционные методики. Среди них урок для разновозрастной группы (9-й и 10-й классы). Это позволяет учащимся 9-х классов более осознанно подойти к выбору профиля, по которому предстоит обучаться в 10-11-х классах. Учащиеся 10-го класса обобщают и систематизируют полученные знания по курсу химии и готовятся к поступлению в вуз.
Важной частью
урока является использование идеи
Штейнберга о конструкторно-технологическом
моделировании в деятельности учителя. Построение логико-смысловой модели
позволяет систематизировать знания
учащихся 10-х классов и определяет
перспективы дальнейшего обучения
девятиклассников.
Построение логико-смысловой модели
позволяет систематизировать знания
учащихся 10-х классов и определяет
перспективы дальнейшего обучения
девятиклассников.
Использование логико-смысловой модели развивает логическое мышление учащихся и формирует навыки индивидуальной конструкторной деятельности в процессе познания.
Тема: Взаимосвязь неорганических и органических веществ
Цель: Показать взаимосвязь между органическими и неорганическими веществами. Сформировать представление об особенностях органических соединений. Совершенствовать навыки логического мышления и умения использовать полученные знания на практике.
Основные понятия: Органические и неорганические вещества, органическая химия.
Средства
обучения: Периодическая система Д.И.
Менделеева, графопроектор, химическая
посуда, химические реактивы.
Ход урока. Начинает урок учитель 9 класса:
На уроке присутствуют разновозрастные группы: учащиеся 9-го класса, изучающие элективный курс химии, выбравшие химический профиль на будущее, и учащиеся 10 -го класса естественнонаучного профиля, посещающие подготовительные курсы КГТУ им. Кирова, для которых химия является профилирующим предметом при поступлении в вуз.
До сих пор мы изучали неорганическую химию, которая насчитывает более 500 тысяч веществ. Нет такого элемента, который входил бы в состав всех неорганических веществ. Но химия многогранна и есть её раздел, называемый органической химией, который насчитывает более 5 миллионов веществ. В состав каждого из них входит один и тот же химический элемент – углерод.
Почему
химия углерода выделена в отдельный
раздел, в чем сходство и различие
неорганических и органических
веществ, каким законам подчиняется
органическая химия? Все это мы постараемся
выяснить на нашем уроке.
Тема урока: Взаимосвязь неорганических и органических веществ
Ответить на поставленные вопросы нам поможет логико-смысловая модель (ЛСМ), которую мы начнем составлять.
Углерод – это элемент шестой группы главной подгруппы. Учитель предлагает дать характеристику этого элемента по Периодической системе.
В ходе построения ЛСМ учитель просит назвать:
аллотропные модификации углерода, чем они отличаются
формулы сложных веществ (оксидов, кислоты, гидроксидов, солей, летучее водородное соединение), которые образует углерод.
привести примеры реакций соединения, разложения, обмена, замещения с участием углерода и его соединений и определить в качестве окислителя или восстановителя выступает углерод в окислительно-восстановительных реакциях.
Учащиеся 9
класса составляют таблицу, в которой
отображают некоторые химические свойства
углерода и его соединений, вспоминают
типы химических реакций, обращают
внимание на окислительно-восстановительные
реакции.
1. С + Н2 = СН4 | Р-ция соед. | C2H4 +H2 = C2H6 |
2.Na2CO3 + HCL = NaCL + CO2 + H2O | Р-ция обмена | CH3COOH+NaOH = |
3. H2CO3= CO2 + H2O | Р-ция разлож. | C 2H5OH = |
4. | Р-ция замещ. | CH4 + Cl2 = |
5.CH4 + O2 = CO2 + H2O | Р-ция горения | C 3H8 + O2= |
(Уравнения реакций для органических веществ составляют учащиеся 10 класса.)
Учитель продолжает:
Все о чем
сейчас говорилось относится к разделу
неорганической химии. Неорганическая
природа по- своему красива и в то же
время сурова, но она мертва без органической
природы. Большинство процессов протекающих
в живых организмах — это химические
реакции органических веществ. Органическая
химия – это химия жизни, органическая
химия – это химия углерода. Помогут
получить представление об органических
веществах учащиеся 10 класса, которые
изучают данный раздел химии.
Помогут
получить представление об органических
веществах учащиеся 10 класса, которые
изучают данный раздел химии.
Продолжает урок учитель 10 класса:
Сегодня мы обобщим полученные на уроках знания и применим их на практике, а для этого продолжим составление ЛСМ.
Учащиеся предлагают добавить в ЛСМ:
в раздел строение атома понятие гибридизация и дают определение этого понятия и называют виды гибридизации.
классификацию углеводородов с указанием общей формулы каждого представителя
классификацию кислородсодержащих органических веществ
Учитель
задает вопрос: «Почему органических
веществ значительно больше, чем
неорганических?» Чтобы ответить на
данный вопрос учащимся 9 класса
предлагается составить структурную
формулу угольной кислоты, а учащимся
10 класса структурную формулу вещества,
формула которого С5Н12.
Девятиклассники написали одну формулу, ученики 10 класса несколько.
Учащиеся 10 класса дают определение изомерии, которое девятиклассники записывают в тетради
Учитель поясняет, что основой для классификации неорганических веществ является Периодическая система Д.И. Менделеева, а для органических веществ теория А.М Бутлерова. Учитель просит учащихся 10 класса озвучить положения теории А.М Бутлерова.
Далее учащимся 10 класса предлагается вспомнить, характерны ли реакции соединения, разложения, обмена, замещения для органических веществ и есть ли среди них окислительно-восстановительные реакции. Десятиклассники дополняют таблицу, которую начали составлять ученики 9 класса.
Учащиеся приходят к выводу, что органические и неорганические вещества имеют много общего.
Основа
всего живого – это органические
вещества. Процессы, происходящие в живых
организмах – это окислительно-восстановительные
реакции, конечным продуктом которых
являются углекислый газ и вода.
Вывод,
Модель, которая составлена на уроке, показала взаимосвязь неорганических и органических веществ, а также особенности органических веществ, которые послужили причиной выделения органической химии в отдельную область химической науки.
Заканчивает урок учитель 9 класса:
Многолетняя работа в школе показала, что изучение органической химии, трудно дается учащимся, так как они считают, что это новая наука со своими законами. Сегодня на уроке мы постарались развеять этот миф и доказать, что в химии законы одинаковы для любого раздела, нужно только их правильно и умело использовать
Нам бы хотелось, чтобы этот урок помог развить вам логическое мышление, умение применять знания, полученные ранее, сравнивать, анализировать, сопоставлять. Все это необходимо для сдачи экзаменов по новой форме в 9 классе и ЕГЭ в 11 классе.
В
завершение урока учащимся предлагается
решить тестовое задание.
Вариант 1.
А1. Распределению электронов по электронным слоям в атоме углерода соответствует схема.
1) 2;8;2; 2) 2;6; 3) 2;4; 4) 2;8;
А2. Окислительные свойства углерод проявляет при взаимодействии с
1) О2 2)Са 3)Fe O 4) CuO
А3. Каждое из указанных веществ реагирует с оксидом углерода (IV)
1) вода и оксид фосфора (V) 2) известковая вода и оксид магния
3) соляная кислота и оксид серы (IV) 4) оксид кальция и хлор
А4. Сокращенное ионное уравнение:
2Н+ +СО32- = Н2О + СО2
Соответствует реакции:
соляной кислоты и едкого натра
соляной кислоты и карбоната калия
Соляной кислоты и оксида натрия
Соляной кислоты и нитрата серебра
А5. Установите соответствие
Установите соответствие
Химическая формула Класс соединений
А) С2 Н2 1) алкан
В) С3 Н 8 2) алкен
В)
С4 Н8 3) алкин
А6. Верны ли следующие суждения об изомерах:
А. изомеры – это вещества, имеющие одинаковое строение, но разный состав.
Б. Изомеры – это вещества, имеющие одинаковый качественный и количественный состав, но разное строение.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны.
Вариант
2.
А1. Число протонов в атоме углерода равно.
1) 2; 2) 6; 3) 4; 4) 8;
А2. Восстановительные свойства углерод проявляет в реакциях:
1) Са + 2С = СаС 2 2)СО + Li 2O = Li2CO3
3)Fe O + C = Fe + CO 4) 4 Al + 3C =Al 4C3
А3. Какое из указанных веществ реагирует с оксидом углерода (II)
1) вода 2) известковая вода
3) соляная кислота 4) оксид железа (II)
А4. Сокращенное ионное уравнение:
2Н ++СаСО3 = Н2О + СО2 +Са2+
Соответствует реакции:
1)соляной кислоты и едкого натра
2) соляной кислоты и карбоната кальция
3)Соляной кислоты и оксида кальция
4)Соляной кислоты и кальция
А5. Установите соответствие
Установите соответствие
Химическая формула Класс соединений
А) С 3Н 6 1) алкан
В) С5 Н12 2) алкен
В) С4 Н 6 3) алкадиен
А6. Укажите формулы изомеров:
1) СН 3-СН 2-СН 2-СН2-СН2-СН3 3) СН2-СН-СН2-СН3 4) СН3-СН2-СН2-СН2-СН3
2 ) СН3-СН2-СН2-СН 3 │ |
СН3 СН3
Конспект урока «Взаимосвязь неорганических и органических веществ»
Муниципальное бюджетное общеобразовательное учреждение
«Средняя общеобразовательная школа № 11 с углублённым изучением отдельных предметов Зеленодольского муниципального района республики Татарстан»
Тема урока:
Взаимосвязь неорганических и органических веществ
Урок разработан учителем высшей квалификационной категории: Тяпковой Ириной Николаевной.
Важной частью урока является использование идеи Штейнберга о конструкторно-технологическом моделировании в деятельности учителя. Построение логико-смысловой модели позволяет систематизировать знания учащихся 10-х классов и определяет перспективы дальнейшего обучения девятиклассников.
Использование логико-смысловой модели развивает логическое мышление учащихся и формирует навыки индивидуальной конструкторной деятельности в процессе познания.
Тема: Взаимосвязь неорганических и органических веществ
Цель: Показать взаимосвязь между органическими и неорганическими веществами. Сформировать представление об особенностях органических соединений. Совершенствовать навыки логического мышления и умения использовать полученные знания на практике.
Основные понятия: Органические и неорганические вещества, органическая химия.
Средства обучения: Периодическая система Д.И. Менделеева, графопроектор, химическая посуда, химические реактивы.
Ход урока. Начинает урок учитель 9 класса:
На уроке присутствуют разновозрастные группы: учащиеся 9-го класса, изучающие элективный курс химии, выбравшие химический профиль на будущее, и учащиеся 10 -го класса физико-химического профиля , для которых химия является профилирующим предметом при поступлении в вуз.
До сих пор мы изучали неорганическую химию, которая насчитывает более 500 тысяч веществ. Нет такого элемента, который входил бы в состав всех неорганических веществ. Но химия многогранна и есть её раздел, называемый органической химией, который насчитывает более 5 миллионов веществ. В состав каждого из них входит один и тот же химический элемент – углерод.
Почему химия углерода выделена в отдельный раздел, в чем сходство и различие неорганических и органических веществ, каким законам подчиняется органическая химия? Все это мы постараемся выяснить на нашем уроке.
Тема урока: Взаимосвязь неорганических и органических веществ
Ответить на поставленные вопросы нам поможет логико-смысловая модель (ЛСМ), которую мы начнем составлять.
Углерод – это элемент шестой группы главной подгруппы. Учитель предлагает дать характеристику этого элемента по Периодической системе.
В ходе построения ЛСМ учитель просит назвать:
аллотропные модификации углерода, чем они отличаются
формулы сложных веществ (оксидов, кислоты, гидроксидов, солей, летучее водородное соединение), которые образует углерод.
привести примеры реакций соединения, разложения, обмена, замещения с участием углерода и его соединений и определить в качестве окислителя или восстановителя выступает углерод в окислительно-восстановительных реакциях.
Учащиеся 9 класса составляют таблицу, в которой отображают некоторые химические свойства углерода и его соединений, вспоминают типы химических реакций, обращают внимание на окислительно-восстановительные реакции.
Р-ция соед.
C2H4 +H2 = C2H6
2.Na2CO3 + HCL = NaCL + CO2 + H2O
Р-ция обмена
CH3COOH+NaOH =
3. H2CO3= CO2 + H2O
Р-ция разлож.
C 2H5OH =
4.FeO + C =Fe + CO
Р-ция замещ.
CH4 + Cl2 =
5.CH4 + O2 = CO2 + H2O
Р-ция горения
C 3H8 + O2=
(Уравнения реакций для органических веществ составляют учащиеся 10 класса. )
)
Учитель продолжает:
Все о чем сейчас говорилось относится к разделу неорганической химии. Неорганическая природа по- своему красива и в то же время сурова, но она мертва без органической природы. Большинство процессов протекающих в живых организмах — это химические реакции органических веществ. Органическая химия – это химия жизни, органическая химия – это химия углерода. Помогут получить представление об органических веществах учащиеся 10 класса, которые изучают данный раздел химии.
Продолжает урок учитель 10 класса:
Сегодня мы обобщим полученные на уроках знания и применим их на практике, а для этого продолжим составление ЛСМ.
Учащиеся предлагают добавить в ЛСМ:
в раздел строение атома понятие гибридизация и дают определение этого понятия и называют виды гибридизации.
классификацию углеводородов с указанием общей формулы каждого представителя
классификацию кислородсодержащих органических веществ
Учитель задает вопрос: «Почему органических веществ значительно больше, чем неорганических?» Чтобы ответить на данный вопрос учащимся 9 класса предлагается составить структурную формулу угольной кислоты, а учащимся 10 класса структурную формулу вещества, формула которого С5Н12.
Девятиклассники написали одну формулу, ученики 10 класса несколько.
Учащиеся 10 класса дают определение изомерии, которое девятиклассники записывают в тетради
Учитель поясняет, что основой для классификации неорганических веществ является Периодическая система Д.И. Менделеева, а для органических веществ теория А.М Бутлерова. Учитель просит учащихся 10 класса озвучить положения теории А.М Бутлерова.
Далее учащимся 10 класса предлагается вспомнить, характерны ли реакции соединения, разложения, обмена, замещения для органических веществ и есть ли среди них окислительно-восстановительные реакции. Десятиклассники дополняют таблицу, которую начали составлять ученики 9 класса.
Учащиеся приходят к выводу, что органические и неорганические вещества имеют много общего.
Основа всего живого – это органические вещества. Процессы, происходящие в живых организмах – это окислительно-восстановительные реакции, конечным продуктом которых являются углекислый газ и вода.
Вывод,
Модель, которая составлена на уроке, показала взаимосвязь неорганических и органических веществ, а также особенности органических веществ, которые послужили причиной выделения органической химии в отдельную область химической науки.
Заканчивает урок учитель 9 класса:
Многолетняя работа в школе показала, что изучение органической химии, трудно дается учащимся, так как они считают, что это новая наука со своими законами. Сегодня на уроке мы постарались развеять этот миф и доказать, что в химии законы одинаковы для любого раздела, нужно только их правильно и умело использовать
Нам бы хотелось, чтобы этот урок помог развить вам логическое мышление, умение применять знания, полученные ранее, сравнивать, анализировать, сопоставлять. Все это необходимо для сдачи экзаменов по новой форме в 9 классе и ЕГЭ в 11 классе.
В завершение урока учащимся предлагается решить тестовое задание.
Вариант 1.
А1. Распределению электронов по электронным слоям в атоме углерода соответствует схема.
1) 2;8;2; 2) 2;6; 3) 2;4; 4) 2;8;
А2. Окислительные свойства углерод проявляет при взаимодействии с
1) О2 2)Са 3)Fe O 4) CuO
А3. Каждое из указанных веществ реагирует с оксидом углерода (IV)
1) вода и оксид фосфора (V) 2) известковая вода и оксид магния
3) соляная кислота и оксид серы (IV) 4) оксид кальция и хлор
А4. Сокращенное ионное уравнение:
2Н+ +СО32- = Н2О + СО2
Соответствует реакции:
соляной кислоты и едкого натра
соляной кислоты и карбоната калия
Соляной кислоты и оксида натрия
Соляной кислоты и нитрата серебра
А5. Установите соответствие
Установите соответствие
Химическая формула Класс соединений
А) С2 Н2 1) алкан
В) С3 Н 8 2) алкен
В) С4 Н8 3) алкин
А6. Верны ли следующие суждения об изомерах:
А. изомеры – это вещества, имеющие одинаковое строение, но разный состав.
Б. Изомеры – это вещества, имеющие одинаковый качественный и количественный состав, но разное строение.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны.
Вариант 2.
А1. Число протонов в атоме углерода равно.
1) 2; 2) 6; 3) 4; 4) 8;
А2. Восстановительные свойства углерод проявляет в реакциях:
1) Са + 2С = СаС 2 2)СО + Li 2O = Li2 CO3
3)Fe O + C = Fe + CO 4) 4 Al + 3C =Al 4C3
А3. Какое из указанных веществ реагирует с оксидом углерода (II)
Какое из указанных веществ реагирует с оксидом углерода (II)
1) вода 2) известковая вода
3) соляная кислота 4) оксид железа (II)
А4. Сокращенное ионное уравнение:
2Н ++СаСО3 = Н2О + СО2 +Са2+
Соответствует реакции:
1)соляной кислоты и едкого натра
2) соляной кислоты и карбоната кальция
3)Соляной кислоты и оксида кальция
4)Соляной кислоты и кальция
А5. Установите соответствие
Химическая формула Класс соединений
А) С 3Н 6 1) алкан
В) С5 Н12 2) алкен
В) С4 Н 6 3) алкадиен
А6. Укажите формулы изомеров:
1) СН 3-СН 2-СН 2-СН2-СН2-СН3 3) СН2-СН-СН2-СН3 4) СН3-СН2-СН2-СН2-СН3
2 ) СН3-СН2-СН2-СН 3 │ |
СН3 СН3
Вещества органические и неорганические.
 Возникновение органической химии
Возникновение органической химииСодержание:
Вещества органические и неорганические. Возникновение органической химии
- Органические и неорганические вещества. Возникновение органической химии. До начала 19-го века все известные вещества были разделены на 2 группы по их origin. It это минеральное вещество и органическое вещество. Многие ученые того времени считали, что с помощью»Жизненной силы» органические вещества образуются только в живых организмах.
- Такой идеалистический взгляд назывался Виталистическим лат. Биогенный взгляд на невозможность синтеза органических веществ из неорганических замедлил развитие химии. Главный удар по мнению биатлонистов наносит немецкий химик F. It к нему обратился Велер.
Он впервые получил органические вещества из неорганических: в 1824 году-щавелевую кислоту, а в 1828 году-мочевину. Людмила Фирмаль
Щавелевая кислота содержится в растениях, а мочевина образуется в организме человека и животных. Дальнейший органический синтез(в 1845 г. немецкий ученый G. In в 1854 году французский ученый М. Кольбе искусственно получил уксусную кислоту. Бертелло синтезировал жир, а в 1861 году русский ученый А. М. виталисты считают, что органические вещества могут образовываться только в живом организме (баттереров получил сахарное вещество).
Дальнейший органический синтез(в 1845 г. немецкий ученый G. In в 1854 году французский ученый М. Кольбе искусственно получил уксусную кислоту. Бертелло синтезировал жир, а в 1861 году русский ученый А. М. виталисты считают, что органические вещества могут образовываться только в живом организме (баттереров получил сахарное вещество).
Реакционная догма виталистов потерпела полное поражение. По этому поводу. Сказал Энгельс.»Благодаря неорганическому производству химических соединений, которые до сих пор производились только в живых организмах, законы химии обладают той же силой, что и неорганические для организма, и большинство из них глубоко заложены в природе неорганического и органического, что оказалось непреодолимым… …
Один На самом деле между неорганическими и органическими веществами нет непреодолимой пропасти. Они отличаются только некоторыми особенностями. Большинство неорганических веществ имеют высокую температуру плавления и кипения, так как они немолекулярны по структуре(I, с. 28). как правило, органические вещества имеют молекулярную структуру, поэтому они имеют низкую температуру плавления.
28). как правило, органические вещества имеют молекулярную структуру, поэтому они имеют низкую температуру плавления.
Почти. 1 Энгельс Ф. Диалектика природы, 1969, с. 14. Все органические вещества легко воспламеняются и разлагаются при нагревании. Органическая химия и ее значение. Мы уже знаем из курсов биологии, что взаимное превращение неорганических и органических веществ возможно. Это говорит о том, что между ними нет принципиальных различий.
- Почему органические вещества рассматриваются в специальных курсах, традиционно называемых органической химией?1. одной из причин этого является тот факт, что молекулы всех органических веществ содержат углерод, но в неорганической химии таких примеров нет. Это органическая химия. Область химических наук, изучающая соединения углерода и их превращения. Но это определение не совсем точно.
Например, окись углерода (IV), окись углерода (II), угольная кислота, карбонаты, карбиды и другие соединения, молекулы которых содержат углерод, классифицируются по своим свойствам как неорганические вещества. Сегодня органический углерод называют углеродсодержащим веществом, которое является одновременно веществом, образующимся в живом организме, и веществом, которое синтезируется.
Сегодня органический углерод называют углеродсодержащим веществом, которое является одновременно веществом, образующимся в живом организме, и веществом, которое синтезируется.
Синтетические вещества включают в себя различные полимеры, из которых изготавливают пластики, красители, волокна, лекарственные средства и др. получаются. Людмила Фирмаль
Существует около 650 миллионов органических веществ, количество которых продолжает расти. Это связано с тем, что атомы углерода могут связываться друг с другом, образуя различные цепочки практически любого размера. Но неорганические вещества известны примерно 500 ООО.
Такое большое количество органических веществ и их особые свойства также являются важными причинами, объясняющими, почему органическая химия изучается отдельно от неорганической. Химики, опирающиеся в своих исследованиях на материалистические мировоззрения, создали научную базу, способствовавшую развитию органической химии.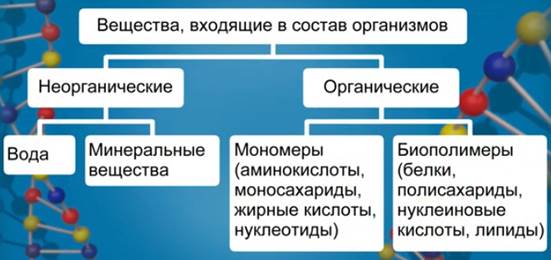
1 из них выдающиеся российские ученые, создавшие теорию химического строения органических соединений А. M. It был баттереров. Опираясь на эту теорию, органическая химия стала стремительно развиваться как самостоятельное научное направление. field. In за сравнительно короткое время были синтезированы многие органические соединения, что создало совершенно новое подразделение химической промышленности.
Русский ученый Н. Н. Зинин разработал промышленный способ получения анилина из бензола в 1842 году. Этот метод является основой для производства синтетических красителей. В 1932 году он стал первым афроамериканцем, получившим Нобелевскую премию по литературе. В. По методу, разработанному Лебедевым впервые в мире, началось промышленное производство синтетического каучука.
Значительный вклад в развитие нефтяной промышленности внесли русские ученые В. В. маркоников (1837-1904) и Н. Д. Зелинский Р861-1953. Новая грандиозная задача перед химической наукой и химической промышленностью была выдвинута XXVI съездом КПСС. Предполагается, что в 11-м году из 5 лет производство химической продукции увеличится на 30-33%.Особое внимание уделяется отраслям, связанным с органической химией.
Предполагается, что в 11-м году из 5 лет производство химической продукции увеличится на 30-33%.Особое внимание уделяется отраслям, связанным с органической химией.
Производство синтетических смол и пластмасс в 1985 году планируется увеличить до 600-625 млн. тонн, а к 1985 году производство химических волокон и нитей, превосходящих натуральные волокна, будет увеличено до 100 млн. тонн. С быстрым развитием производства тракторов, автомобилей и самолетов, производство синтетического каучука должно значительно увеличиться.
Сегодня органическая химия играет особую роль в разработке методов получения веществ, заменяющих пищевые продукты, таких как жиры и масла. Не менее важна роль органической химии в переработке сельскохозяйственной продукции, нефти, природного газа и угля. С этими и многими другими важными вопросами современной органической химии вы познакомитесь в ходе дальнейших исследований. Вопрос 1-5 (стр. 147).
Смотрите также:
Решение задач по химии
Неорганическая химия — Американское химическое общество
Что такое неорганическая химия?
Неорганическая химия изучает свойства и поведение неорганических соединений, включая металлы, минералы и металлоорганические соединения.
В то время как органическая химия определяется как изучение углеродсодержащих соединений, неорганическая химия — это изучение оставшейся (то есть не содержащей углерод) подгруппы соединений. Но эти два поля могут частично совпадать.Например, металлоорганические соединения обычно содержат металл или металлоид, непосредственно связанный с углеродом.
Чем занимаются химики-неорганики?
Химики-неорганики работают в самых разных областях, от горнодобывающей промышленности до микрочипов. Их работа основана на понимании:
- Поведение и аналоги для неорганических элементов, и
- Как эти материалы могут быть изменены, отделены и использованы.
К конкретным работам могут относиться:
- Разработка методов извлечения металлов из потоков отходов
- Работает химиком-аналитиком по анализу добытых руд
- Проведение исследований по использованию неорганических химикатов для обработки почвы
Многие химики-неорганики работают в промышленности, но они также работают в академических учреждениях и государственных лабораториях. Химики-неорганики, работающие в правительстве, говорят, что их время все чаще тратится на написание заявок на гранты и борьбу за деньги на исследования.
Химики-неорганики, работающие в правительстве, говорят, что их время все чаще тратится на написание заявок на гранты и борьбу за деньги на исследования.
Химики-неорганики сравнивают свою работу с работой материаловедов и физиков. Все сосредоточены на изучении взаимосвязи между физическими свойствами и функциями. Но химика-неорганика больше интересуют эти свойства на молекулярном уровне.
Где используется неорганическая химия?
Неорганические соединения используются в качестве катализаторов, пигментов, покрытий, поверхностно-активных веществ, лекарств, топлива и т. Д.Они часто имеют высокие температуры плавления и специфические свойства высокой или низкой электропроводности, что делает их полезными для определенных целей. Например:
- Аммиак — источник азота в удобрениях. Это одно из основных неорганических химикатов, используемых в производстве нейлона, волокон, пластмасс, полиуретанов, гидразина (используется в реактивном и ракетном топливе) и взрывчатых веществ.

- Хлор используется в производстве поливинилхлорида (используется для изготовления труб, одежды, мебели и т. Д.)), агрохимикатов (например, удобрений, инсектицидов или средств для обработки почвы), фармацевтических препаратов и химикатов для очистки и стерилизации воды.
- Диоксид титана — это встречающийся в природе оксид титана, который используется в качестве белого порошкового пигмента в красках, покрытиях, пластмассах, бумаге, чернилах, волокнах, продуктах питания и косметике. он также обладает хорошими свойствами стойкости к ультрафиолетовому излучению, и растет спрос на его использование в фотокатализаторах.
Разница между органическими и неорганическими соединениями
Типы соединений
Объединение атомов различных элементов приводит к образованию соединений.В зависимости от типа притяжения, которое существует между атомами соединения, соединения подразделяются на четыре основные категории:
В ковалентных соединениях атомы разных элементов делятся своими электронами для достижения стабильности
В ионных соединениях атомы различных элементов связаны друг с другом посредством полной передачи своих электронов
Металлические соединения характеризуются ассоциацией различных металлических атомов сильными металлическими силами
В координированных ковалентных соединениях определенные комплексные ионы удерживаются вместе ковалентными и координатные облигации
Все организмы в основном состоят из органических молекул.
Органические молекулы, которые очень важны для нас, — это в основном углеводы, белки, липиды и т. Д.
Развитию органической химии около 200 лет. В конце семнадцатого века химики всего мира начали различать органические соединения, полученные из растений и животных, и неорганические молекулы, полученные из минеральных ресурсов.
Разница между органическими и неорганическими соединениями
В первые годы развития химии химики сделали много неудачных попыток синтезировать органические соединения в лаборатории.После нескольких неудач все их усилия оказались тщетными, и они были вынуждены поверить в то, что органические соединения могут быть синтезированы с помощью особого механизма, который может происходить только внутри живых существ. Следовательно, в отличие от неорганических соединений, органические соединения не могут быть получены в лаборатории.
Синтез органических соединений
Открытие карбамида произвело революцию в области органической химии. Это открытие привело Кольбе в 1845 году к работе над получением уксусной кислоты в лаборатории, в то время как Хеннель успешно работал над получением этилового спирта, Бертло в 1856 году сделал успешную попытку получения метана в лаборатории без использования каких-либо живых организмов.
Это открытие привело Кольбе в 1845 году к работе над получением уксусной кислоты в лаборатории, в то время как Хеннель успешно работал над получением этилового спирта, Бертло в 1856 году сделал успешную попытку получения метана в лаборатории без использования каких-либо живых организмов.
Новая версия органической химии
После успешного синтеза различных органических соединений в лаборатории теория жизненной силы была полностью проигнорирована. Углубленное изучение органических соединений показало, что эти соединения в основном состоят из углерода. Изучение соединений углерода в основном известно как органическая химия.
Здесь следует отметить одну вещь: простое присутствие углерода в соединении не означает, что соединение является органическим.Например, CO2 содержит углерод, но является неорганическим соединением.
Углубленное понимание структуры органических соединений показывает, что все органические соединения состоят из углерода в качестве основного компонента, который также неизменно связан с водородом. Эти органические соединения, состоящие в основном из углерода и водорода, называются углеводородами.
Эти органические соединения, состоящие в основном из углерода и водорода, называются углеводородами.
Существует большое количество органических соединений, содержащих неорганические частицы, такие как азот, сера, фосфор и т. Д.Но эти соединения являются производными только углеводородов и, следовательно, считаются органическими соединениями.
Следовательно, органическая химия определяется как химия углеводородов и их производных.
Различие между органическими и неорганическими соединениями (таблица)
9053 9053 9053 9053 , водород и кислород.5125
| | Органическое соединение | Неорганическое соединение | ||||
Обычно не содержит углерода. | ||||||
Природа соединений | Ковалентное соединение | Электровалентные / ионные / ковалентные соединения | ||||
Точки плавления и кипения | 12 Низкие 909Растворимость в воде | Нерастворимый | Растворимый | |||
Растворимый в органических растворителях | Растворимый | Нерастворимый 005 | ||||
Хорошие проводники | ||||||
Горючесть | Горючие | Негорючие | ||||
Летучая природа |
|
| ||||
Catenation | выставлено | не выставлено | ||||
Изомерия | выставлено | не выставлено | не выставлено | не выставлено | Большое количество органических соединений Поскольку мы знаем, что органические соединения состоят в основном из углерода и водорода, основные свойства углерода приводят к образованию такого большого количества соединений.
Три упомянутые выше причины ясно оправдывают присутствие на Земле большого количества органических соединений. С другой стороны, неорганические соединения естественным образом содержатся в минералах земной коры, поэтому их количество ограничено. Типы органических соединений Поскольку мы знаем, что большинство органических соединений являются производными углеводородов, поэтому для изучения типов органических соединений давайте начнем с типов углеводородов. Эти два типа углеводородов в основном классифицируются на основе количества связей между присутствующими в них атомами углерода Насыщенные углеводороды Органические соединения, которые имеют только одинарные связи между атомами углерода, известны как алканы. У них максимальное количество атомов водорода, связанных с атомами углерода. Общая формула соединений этого семейства — Cnh3n + 1 i.е. последовательные соединения алканов различаются между собой по составу по группе -Ch3. Ненасыщенные углеводороды Те органические соединения, которые имеют недостаточное количество атомов водорода, подвергаются образованию двойной и тройной связи, чтобы удовлетворить их валентность, известны как ненасыщенные углеводороды. Общая формула семейства углеводородов с двойной связью — Cnh3n, тогда как семейство с тройной связью в Cnh3n-1. Семейство двойной связи известно как алкен, тогда как семейство тройной связи известно как алкин. Ненасыщенность приводит к нестабильности углеродного соединения. Его можно удалить с помощью процесса гидрирования, в котором молекулы водорода подают к углеродному соединению, содержащему двойную или тройную связь, в присутствии катализатора Ni / Pd для удаления ненасыщенности. 1.2: неорганическая химия против органической
Граница между областями неорганической и органической химии стирается.  Эти соединения катализируют органические реакции или биохимические реакции, и они представляют собой соединения, содержащие как углерод, так и металлы. Эти соединения являются примерами молекул, которые нельзя определить только как органические молекулы или только как неорганические молекулы.Аденозилкобальбумин является примером металлоорганического катализатора, который присутствует в биологии; дополнительная иллюстрация того, что «неорганические» металлы являются важными кофакторами в биологии. Это изображение основано на информации из статьи в Википедии о металлоорганической химии и создано из изображений, найденных там; Авторство изображений, созданных Alsosaid1987 , AdoCbl-ColorCoded , CC BY-SA 4.0 и Smokefoot , Zeise’sSalt , CC BY-SA 3.0. Эти соединения катализируют органические реакции или биохимические реакции, и они представляют собой соединения, содержащие как углерод, так и металлы. Эти соединения являются примерами молекул, которые нельзя определить только как органические молекулы или только как неорганические молекулы.Аденозилкобальбумин является примером металлоорганического катализатора, который присутствует в биологии; дополнительная иллюстрация того, что «неорганические» металлы являются важными кофакторами в биологии. Это изображение основано на информации из статьи в Википедии о металлоорганической химии и создано из изображений, найденных там; Авторство изображений, созданных Alsosaid1987 , AdoCbl-ColorCoded , CC BY-SA 4.0 и Smokefoot , Zeise’sSalt , CC BY-SA 3.0. Некоторые из разделов неорганической химии сосредоточены на электропроводности неорганических материалов (т.е. проводимости, сверхпроводимости и полупроводимости) и на изучении оптических и электронных свойств неорганических наноматериалов. Хотя углеродные нанотрубки и фуллерены являются аллотропами углерода, свойства их материалов несколько чужды многим химикам-органикам, которые традиционно фокусировались на более мелких органических молекулах, обладающих очень разными свойствами. Однако эти свойства знакомы химикам-неорганикам. Разница между органической и неорганической химиейОрганическая и неорганическая химия Органическая и неорганическая химия — это отдельные дисциплины в химии.В органической химии научные исследования сосредоточены на углеродных соединениях и других углеродных соединениях, таких как углеводороды и их производные. Неорганическая химия занимается научным изучением всех химических соединений, кроме группы углерода. Короче говоря, органическая химия занимается углеродом, а неорганическая химия занимается остальными химическими соединениями, кроме углерода. Когда мы говорим «научное изучение органической или неорганической химии», это включает изучение состава, структуры, свойств, подготовку и изучение реакций.Итак, чтобы думать о том, чтобы стать химиком, человек должен быть экспертом во всех упомянутых процессах. Органическая химия занимается фотохимией, стереохимией, гидрированием, изомеризацией, полимеризацией и ферментацией. С другой стороны, неорганическая химия охватывает широкий круг предметов. Примеры из них: электрохимия, кристаллография, атомная структура, координация соединений, керамика, химическая связь и кислотно-основные реакции. Всегда говорят, что органическая и неорганическая химия всегда пересекаются. Органическая химия считается важным разделом химии. Это связано с тем, что они борются с жизнью и связанными с ней химическими реакциями. Они также занимаются обширными продуктами, которые могут быть произведены из него, например, улучшением чистящих средств. Неорганическая химия также является важной дисциплиной. Чтобы стать химиком-неоргаником или химиком-органиком, требуется степень бакалавра химии со специализацией в области органической или неорганической химии. Затем они могут получить степень магистра или доктора, чтобы улучшить свои знания. Также они могут преподавать в академии или работать в лабораториях.Химик может заработать от 30 000 долларов США до 130 000 долларов США в зависимости от должности и опыта по состоянию на 2009 год. Однако это трудная степень, требующая терпения, аналитического и критического мышления. Резюме: 1. Органическая химия занимается углеродом и его производными, а неорганическая химия занимается остальными элементами, кроме углерода. 2. Органическая химия занимается фотохимией, стереохимией, гидрированием и т. Д., В то время как неорганическая химия занимается электрохимией, кристаллографией, атомными структурами и многим другим. 3. Обе дисциплины часто пересекаются. 4. Оба требуют степени бакалавра химии со специализацией в области органической или неорганической химии. : Если вам понравилась эта статья или наш сайт. Пожалуйста, расскажите об этом. Поделитесь им с друзьями / семьей. Cite Разница между органической химией и неорганической химиейСообщение от Мадху Ключевое различие между органической химией и неорганической химией состоит в том, что органическая химия — это область химии, которая занимается структурой, свойствами, реакциями и другими фактами об органических соединениях, тогда как Неорганическая химия — это область химии, которая занимается неорганическими соединениями. Химия — это, по сути, отрасль науки, изучающая вещества, из которых состоит материя, исследование их свойств и реакций, а также использование таких реакций для образования новых веществ. Когда мы говорим «органическая химия», мы имеем дело с органическими соединениями, а «неорганическая химия» — с неорганическими соединениями. СОДЕРЖАНИЕ 1. Что такое органическая химия?Органическая химия — это раздел химии, изучающий органические соединения. Органическое соединение — это химическое соединение, которое содержит один или несколько атомов углерода в качестве важного компонента. Эти атомы углерода связаны друг с другом или с другими химическими элементами ковалентными химическими связями. Однако некоторые углеродсодержащие соединения не считаются органическими соединениями; они относятся к неорганическим соединениям, т.е.е. карбонаты и цианиды являются неорганическими соединениями в основном по историческим причинам (эти соединения исторически назывались неорганическими соединениями). Кроме того, почти все органические соединения содержат ковалентную связь C-H. Рисунок 01: Биологический токсин — большинство биологических материалов являются органическими соединениями В основном, большинство молекул, которые связаны с живыми организмами, являются органическими. Что такое неорганическая химия?Неорганическая химия — это раздел химии, изучающий неорганические соединения. Неорганическое соединение — это любое соединение, не являющееся органическим соединением. Другими словами, неорганические соединения — это все соединения, кроме органических соединений. Следовательно, в этих соединениях отсутствуют существенные атомы углерода или связи C-H. Рисунок 02: Неорганическая химия занимается широким спектром неорганических соединений, включая A) простые молекулы, B) соли, C) металлоорганические комплексы, D) силиконы, E) катализаторы, F) минералы и G) соединения металлов В эту категорию входят соли, металлы и другие элементарные соединения. В чем разница между органической химией и неорганической химией? Органическая химия — это область химии, которая имеет дело со структурой, свойствами, реакциями и другими фактами об органических соединениях, тогда как неорганическая химия — это область химии, которая имеет дело с неорганическими соединениями. Это ключевое различие между органической и неорганической химией. Поскольку большинство органических соединений являются ковалентными соединениями, нам приходится иметь дело в основном с ковалентными соединениями при изучении органической химии.Однако большинство неорганических соединений являются ионными соединениями. Следовательно, нам приходится иметь дело с ионными соединениями при изучении неорганической химии. Следовательно, это главное различие между органической и неорганической химией. Дальнейшие различия показаны в инфографике разницы между органической и неорганической химией. Резюме — Органическая химия против неорганической химииОрганическая и неорганическая химия — два основных раздела химии.Ключевое различие между органической химией и неорганической химией заключается в том, что органическая химия — это область химии, которая занимается структурой, свойствами, реакциями и другими фактами об органических соединениях, тогда как неорганическая химия — это область химии, которая имеет дело с неорганическими соединениями. Ссылка: 1. Helmenstine, Anne Marie, Ph.D. «Разница между органическим и неорганическим». ThoughtCo, 5 октября 2018 г. Доступно здесь Изображение предоставлено: 1. «Двумерная структура майтотоксина» Чарльзи — собственная работа, (общественное достояние) через Commons Wikimedia Общие сведения об органических и неорганических соединенияхВ относительной терминологии слово «органическое» относится ко всему, что происходит от живой материи или относится к ней. И наоборот, его антоним неорганический относится ко всему, что не происходит из живой материи и не состоит из нее.Это определение справедливо для научной области биологии, но современная химия — это разнообразный предмет. Существенная основа химии вращается вокруг динамического дуэта, а именно, органических и неорганических соединений. С научной точки зрения существуют две различные дисциплины из-за этих различных аспектов химии, исследующей материю, — органической химии и неорганической химии. Основное различие между этими противоположными дисциплинами заключается в их области изучения. Чтобы обобщить дисперсию, органическая химия включает изучение живых соединений, содержащих атомы углерода, тогда как неорганическая химия включает изучение в основном неуглеродных соединений, полученных из неживых существ. В рамках этой структурной основы химических соединений химики-органики изучают органические молекулы и их врожденные реакции. Напротив, химики-неорганики изучают минеральные или антропогенные реакции. Такая схематическая категоризация может показаться простой, но исторический фон, лежащий в основе четкого различия, гораздо сложнее. На ваше рассмотрение, давайте подробнее рассмотрим характеристики соединений, чтобы лучше понять органические и неорганические соединения.Эта осведомленность позволяет лучше понять современные химические применения в ядерной медицине и общем здравоохранении. История органической химии В начале 19 -х годов века естествоиспытатели и ученые наблюдали широкий спектр химических соединений. Эти исследователи отметили существенные различия, существующие между соединениями, полученными из живых веществ, и соединениями, не полученными. Йонс Берцелиус предложил эту теорию витализма. Он также был первым человеком, который использовал термин «органическая химия», имея в виду изучение соединений, происходящих из биологических источников. Теория жизненной силы предполагала, что жизненная сила — или жизненная сила — существует исключительно в присутствии органических материалов, таких как тела живых животных и растений. Согласно этому убеждению, органические соединения образовывались исключительно в живых клетках.Поэтому приготовить такие соединения в лаборатории было невозможно. Ученый Фридрих Велер несколько десятилетий спустя отверг эту теорию с помощью своего новаторского метода синтеза. В контролируемых условиях Велер продемонстрировал, как получать органические соединения в лаборатории. Примеры и производные органических соединенийХотя изначально органическая химия была определена как химия биологических существующих молекул, с тех пор отрасль определила свою сферу охвата, чтобы относиться к спецификациям углеродных соединений и их производных.По сути, органические соединения состоят из углерода в качестве основного компонента. Соединения углерода небиологического происхождения, тем не менее, имеют отношение к области органической химии. Тем не менее, имейте в виду, что простое присутствие элемента автоматически указывает на то, что само соединение является органическим. Органические соединения также неизменно связаны с водородом, поскольку они, как известно, образуют ковалентные связи. Атомы углерода сливаются с атомами водорода с образованием углеводородов. Неорганические соединения, напротив, не обладают вышеуказанными идиосинкразическими характеристиками.Еще раз, любые молекулы, относительно связанные с живыми существами, считаются органическими. Как правило, они являются результатом врожденной активности организма и телесных процессов. Общие примеры включают жиры, сахара, белки, ферменты, нуклеиновые кислоты, липиды и углеводородное топливо. Органические соединения существуют в форме твердых тел, газов и жидкостей. Конкретные категории включают ДНК, столовый сахар, известный в науке как сахароза (C 12 H 22 O 11 ), метан (CH 4 ), этанол (C 2 H 6 O) и бензол. (C 6 H 6 ). История неорганической химии В целом, область химии в значительной степени вращается вокруг существования металлов. Древние техники алхимиков Азии и Европы в конечном итоге привели к развитию этой отрасли науки. Хотя алхимики не смогли успешно превратить свинец в ценное золото, их открытие кислот и оснований, разработка методов химических реакций и систематический исследовательский подход заложили основу периодической таблицы. Химическая природа таких веществ не была широко известна до 19 века, когда ученые начали лучше понимать органические соединения. С тех пор химики-неорганики изучают поведение неорганических элементов, образованных неживыми процессами, и работают над разработкой прикладной методологии или исследованиями того, как эти соединения могут быть эффективно модифицированы и использованы в промышленности. Примеры неорганических соединений Понять органические и неорганические соединения несложно, если вспомнить, что в неорганических соединениях отсутствуют углеродно-водородные связи.Неорганические молекулы состоят из металлов, солей, минералов, отдельных элементов и любых углеродных соединений, не связанных с водородом. Хорошо известные примеры включают серебро, серу, алмаз (также известный как чистый углерод), диоксид углерода (CO 2 ) и поваренную соль, научно известную как хлорид натрия (NaCl). Поскольку эти соединения имеют более высокие температуры плавления и точные свойства проводимости, их часто используют в качестве катализаторов, пигментов, покрытий, топлива или лекарств. Применения в фармацевтической промышленностиКаждая из этих областей химии приобрела актуальность в нашем мире в последнее время и будет продолжать играть важную роль в будущем.Одно из наиболее активных направлений химии сегодня — это раздел органической химии. Прошлые экспериментальные результаты позволили нам узнать последовательность изменений, происходящих в реакциях и синтезе. Благодаря актуальности и полезности этой биохимии появляются ценные молекулярные приложения как в промышленности, так и в технологиях. Кроме того, производство радиоизотопных соединений неорганических элементов имеет решающее значение для ядерной медицины и секторов здравоохранения.Это подразделение химии остается актуальным для разработки радиофармацевтических препаратов для терапевтических и диагностических применений. Производство соединений с радиоактивной меткой для исследования лекарственных средств, разработки в клинических испытаниях и, в конечном итоге, производства является столь же сложным процессом. Moravek — сертифицированный GMP производитель фармацевтической промышленности. Мы являемся надежной контрактной производственной организацией, которая предлагает квалифицированный индивидуальный синтез радиоактивно меченных соединений углерода-14.Как предприятие с обширным опытом в области радиосинтеза, очистки и анализа соединений, наши услуги доступны для поддержки любого этапа процесса разработки лекарств. Наша команда химиков имеет обширный опыт в различных областях, в производстве продуктов с радиоактивной меткой и предоставлении услуг в области химического органического синтеза. Moravek разрабатывает эффективные кампании для клиентов, чтобы соответствовать нормативным требованиям FDA и достигать целей проекта химических исследований. Разница между органической и неорганической химиейРазница между органической и неорганической химией В широком смысле химию можно классифицировать как раздел физической науки, который объясняет происхождение, структуру и поведение материи, а также переход материи из одной формы в другую. В этой статье объясняется, 1. Что такое неорганическая химия? 2. Что такое органическая химия? 3. В чем разница между неорганической и органической химией? Что такое неорганическая химия В общем, неорганические молекулы — это молекулы, не имеющие окончательной углеводородной (состоящей из атомов углерода и водорода) структуры. В основном они состоят из ионов, и эти ионы служат основой их химической активности. Основным типом неорганических реакций являются реакции замещения и окислительно-восстановительные реакции. Структура ионного каркаса в оксиде калия Что такое органическая химия Помимо металлоорганических соединений (соединений, которые включают органическую структуру плюс металлы), между органической химией и неорганической химией очень мало общего.Как упоминалось выше, органические молекулы состоят из углеводородов. Классификация и реакции органических соединений зависят от их функциональных групп.Длина углеродной цепи просто определяет физические характеристики соединения. Органические соединения имеют свойство плавиться и кипеть, в отличие от неорганических соединений. Методы спектроскопии в основном используются для анализа органических соединений. Органическая химия широко используется в медицинской химии для открытия новых лекарств, химии питания, химии ароматизаторов и ароматизаторов, нефти и т. Д. Шаровидная модель молекулы метана Разница между органической и неорганической химиейОпределение Неорганическая химия занимается неорганическими соединениями, обычно имеющими ионное основание. Органическая химия занимается органическими соединениями из углеводородов. РеакцияНеорганическая химия включает кислотно-основные реакции, реакции замещения, окислительно-восстановительные реакции и т. Д. Органическая химия включает реакции, которые зависят от функциональной группы, присутствующей в соединении. СтруктураНеорганическая химия в основном занимается солями и кристаллами. Органическая химия занимается маслами, жирами, сахарами и т. Д. Физические свойстваНеорганические молекулы имеют более высокие температуры плавления и разлагаются вместо кипения. Органические молекулы плавятся и кипятят. Изображение предоставлено: «Метан-CRC-MW-3D-шары» Бен Миллс — собственная работа (общественное достояние) через Commons Wikimedia «Оксид калия-3D-vdW» (общественное достояние) через Commons Wikimedia . |
 // Thomson Brooks/Cole, 2004. — Р. 342. ISBN 0-534-39969-X
// Thomson Brooks/Cole, 2004. — Р. 342. ISBN 0-534-39969-X — 920 с.
— 920 с. Напиток в бокале с его…
Напиток в бокале с его…
 FeO + C =Fe +
CO
FeO + C =Fe +
CO

 Большинство неорганических соединений не проявляют четырехвалентности и катенации, и, следовательно, их количество ограничено.
Большинство неорганических соединений не проявляют четырехвалентности и катенации, и, следовательно, их количество ограничено.
 Например, давайте рассмотрим один из основных классов катализаторов, используемых для реакций органического синтеза; металлоорганические катализаторы (Рисунок \ (\ PageIndex {1} \)). Металлоорганические катализаторы, подобные этим, и все металлоорганические соединения содержат металлы, которые связаны с углеродом или углеродсодержащими молекулами. Итак, являются ли они «неорганическими», потому что содержат металлы, или «органическими», потому что содержат углерод? Это показывает, что четкого разделения между органической и неорганической химией не существует. Кроме того, ионы металлов распространены в биологии, поэтому представление о том, что металлы являются «неорганическими» и, таким образом, классифицируются как «неживые или небиологические», неверно.Каноническим примером является металлоорганический катализатор, аденозилкобальбумин, который является важным биологическим кофактором, содержащим ион кобальта (Со) (рис. \ (\ PageIndex {1} \), справа) и связь кобальт-углерод.
Например, давайте рассмотрим один из основных классов катализаторов, используемых для реакций органического синтеза; металлоорганические катализаторы (Рисунок \ (\ PageIndex {1} \)). Металлоорганические катализаторы, подобные этим, и все металлоорганические соединения содержат металлы, которые связаны с углеродом или углеродсодержащими молекулами. Итак, являются ли они «неорганическими», потому что содержат металлы, или «органическими», потому что содержат углерод? Это показывает, что четкого разделения между органической и неорганической химией не существует. Кроме того, ионы металлов распространены в биологии, поэтому представление о том, что металлы являются «неорганическими» и, таким образом, классифицируются как «неживые или небиологические», неверно.Каноническим примером является металлоорганический катализатор, аденозилкобальбумин, который является важным биологическим кофактором, содержащим ион кобальта (Со) (рис. \ (\ PageIndex {1} \), справа) и связь кобальт-углерод. Электропроводность — каноническое свойство металлов, но материалы на основе углерода также демонстрируют электропроводность. Например, углеродные нанотрубки проводят электричество через свои протяженные сопряженные системы \ (\ pi \). Фуллерены, наиболее известным из которых является бакминстерфуллерен или бакейболл (C 60 ), демонстрируют интересные свойства, аналогичные свойствам наночастиц, а в сочетании с металлами и кристаллизации могут демонстрировать сверхпроводимость.
Электропроводность — каноническое свойство металлов, но материалы на основе углерода также демонстрируют электропроводность. Например, углеродные нанотрубки проводят электричество через свои протяженные сопряженные системы \ (\ pi \). Фуллерены, наиболее известным из которых является бакминстерфуллерен или бакейболл (C 60 ), демонстрируют интересные свойства, аналогичные свойствам наночастиц, а в сочетании с металлами и кристаллизации могут демонстрировать сверхпроводимость. Таким образом, химики-неорганики приняли эти молекулы как «неорганические» из-за того, что они ведут себя больше как неорганические материалы, чем меньшие органические молекулы.Этот класс молекул на основе углерода служит еще одним примером молекул, которые не совсем соответствуют традиционным определениям «органической» и «неорганической» химии. Конечно, в будущем будет появляться все больше и больше примеров молекул, которые не вписываются в традиционные дисциплины химии.
Таким образом, химики-неорганики приняли эти молекулы как «неорганические» из-за того, что они ведут себя больше как неорганические материалы, чем меньшие органические молекулы.Этот класс молекул на основе углерода служит еще одним примером молекул, которые не совсем соответствуют традиционным определениям «органической» и «неорганической» химии. Конечно, в будущем будет появляться все больше и больше примеров молекул, которые не вписываются в традиционные дисциплины химии.
 По словам Р. Сандерсон, неорганическая химия важна, потому что это единственная дисциплина в химии, которая конкретно исследует различия между всеми видами атомов.Примером неорганической химии, в которой он может быть применен, является использование медицинской неорганической химии, которая изучает важные и незначительные элементы, которые могут быть использованы при лечении и диагностике заболеваний.
По словам Р. Сандерсон, неорганическая химия важна, потому что это единственная дисциплина в химии, которая конкретно исследует различия между всеми видами атомов.Примером неорганической химии, в которой он может быть применен, является использование медицинской неорганической химии, которая изучает важные и незначительные элементы, которые могут быть использованы при лечении и диагностике заболеваний.
 net/science/difference-between-organic-and-inorganic-chemistry/.
net/science/difference-between-organic-and-inorganic-chemistry/. 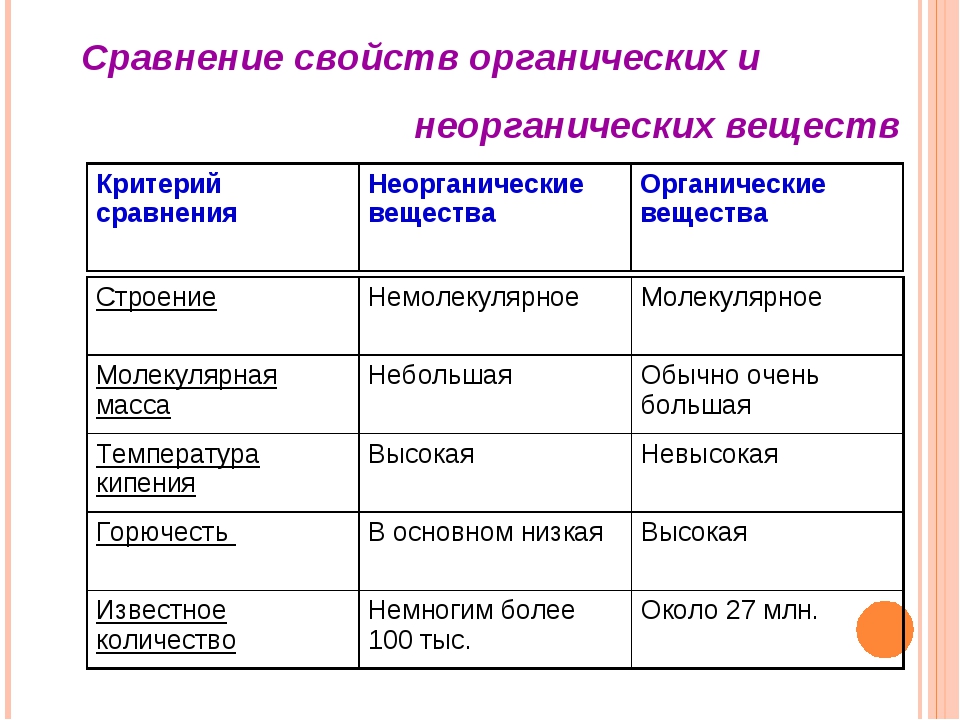 Обзор и основные отличия
Обзор и основные отличия  Например, углеводы, белки, нуклеиновые кислоты и т. Д. Все органические молекулы содержат углерод, почти все содержат водород, а также могут содержать кислород.Область органической химии изучает структуру, свойства, классификации, реакции и многие другие факты об этих соединениях.
Например, углеводы, белки, нуклеиновые кислоты и т. Д. Все органические молекулы содержат углерод, почти все содержат водород, а также могут содержать кислород.Область органической химии изучает структуру, свойства, классификации, реакции и многие другие факты об этих соединениях.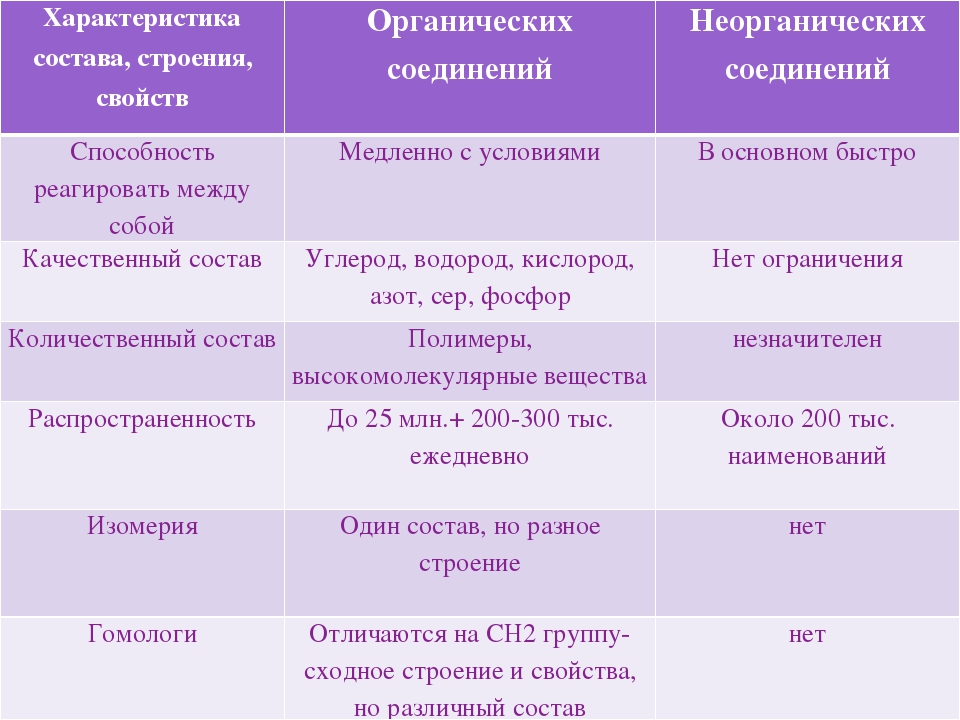 Однако некоторые неорганические соединения содержат атомы углерода. Область неорганической химии — это изучение свойств, классификаций, реакций и многих других фактов об этих соединениях.
Однако некоторые неорганические соединения содержат атомы углерода. Область неорганической химии — это изучение свойств, классификаций, реакций и многих других фактов об этих соединениях.
 «Неорганический монтаж» (общественное достояние) через Commons Wikimedia
«Неорганический монтаж» (общественное достояние) через Commons Wikimedia Ученые в основном рассматривают вещества, которые не подпадают непосредственно под определение органических, как неорганические.
Ученые в основном рассматривают вещества, которые не подпадают непосредственно под определение органических, как неорганические. Химики того времени обнаружили фундаментальные, но необъяснимые различия, существующие между типами различных соединений.На основании этих наблюдений теория жизненной силы 1809 года стала широко признанной гипотезой.
Химики того времени обнаружили фундаментальные, но необъяснимые различия, существующие между типами различных соединений.На основании этих наблюдений теория жизненной силы 1809 года стала широко признанной гипотезой. Этот синтез органического вещества «in vitro» оказался ключевым биохимическим открытием для дальнейших исследований, концептуализирующих современную область органической химии.
Этот синтез органического вещества «in vitro» оказался ключевым биохимическим открытием для дальнейших исследований, концептуализирующих современную область органической химии.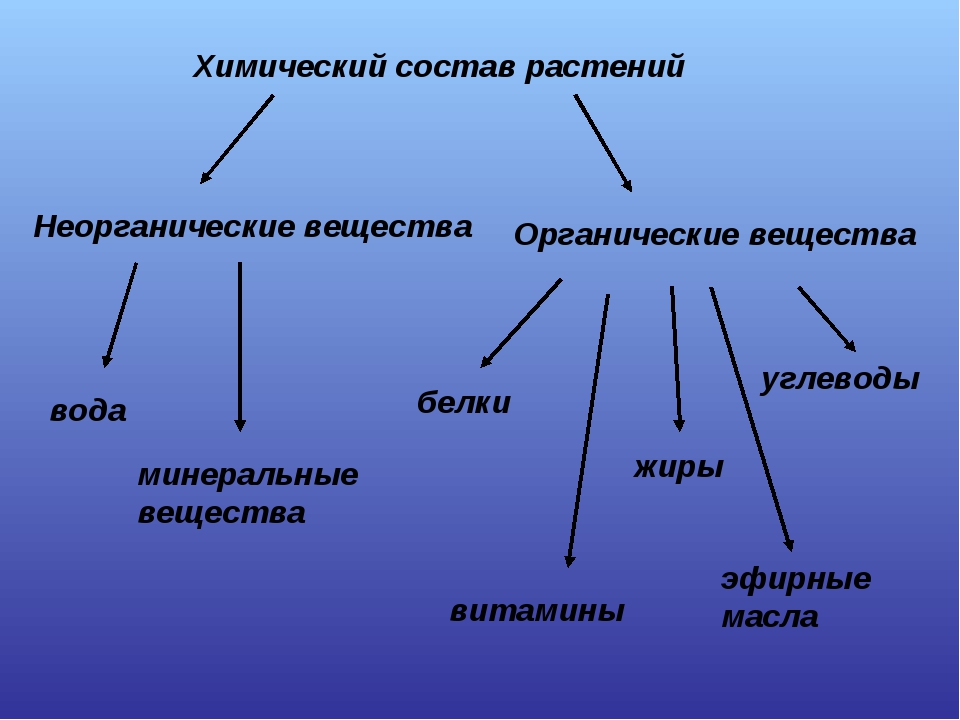


 Радиохимики должны использовать надлежащие знания, методы и опыт для производства высококачественной продукции в соответствии с установленными стандартами.
Радиохимики должны использовать надлежащие знания, методы и опыт для производства высококачественной продукции в соответствии с установленными стандартами. Неорганическая и органическая химия — это две разные области химии, которые зависят от природы соединений. Основное различие между органической и неорганической химией состоит в том, что неорганическая химия — это изучение неорганических соединений, тогда как органическая химия — это изучение органических соединений.
Неорганическая и органическая химия — это две разные области химии, которые зависят от природы соединений. Основное различие между органической и неорганической химией состоит в том, что неорганическая химия — это изучение неорганических соединений, тогда как органическая химия — это изучение органических соединений.  Ионы образуются, когда молекула или атом имеет меньше или больше электронов, чем их исходная электронная конфигурация.Однако ионы образуются для того, чтобы сделать атомы / молекулы более стабильными, придав им электронную конфигурацию благородного газа. Следовательно, когда атомы достигают электронной конфигурации благородного газа, они становятся либо положительно, либо отрицательно заряженными. Положительно заряженные частицы называются катионами, а отрицательно заряженные частицы — анионами. Катионы и анионы естественным образом притягиваются друг к другу через ионные взаимодействия, образуя самые прочные типы химических связей, называемые ионными связями.В целом все они относятся к неорганическим соединениям. Однако существует также большое количество соединений, связанных ковалентными связями, которые подпадают под категорию неорганических соединений. т.е. HCl, CO 2 , H 2 O
Ионы образуются, когда молекула или атом имеет меньше или больше электронов, чем их исходная электронная конфигурация.Однако ионы образуются для того, чтобы сделать атомы / молекулы более стабильными, придав им электронную конфигурацию благородного газа. Следовательно, когда атомы достигают электронной конфигурации благородного газа, они становятся либо положительно, либо отрицательно заряженными. Положительно заряженные частицы называются катионами, а отрицательно заряженные частицы — анионами. Катионы и анионы естественным образом притягиваются друг к другу через ионные взаимодействия, образуя самые прочные типы химических связей, называемые ионными связями.В целом все они относятся к неорганическим соединениям. Однако существует также большое количество соединений, связанных ковалентными связями, которые подпадают под категорию неорганических соединений. т.е. HCl, CO 2 , H 2 O Что происходит в случае реакций замещения, так это то, что катионы и анионы между двумя соединениями обмениваются в зависимости от их реакционного потенциала. С другой стороны, окислительно-восстановительные реакции происходят из-за окисления и восстановления.Таким образом, металлы и их формы имеют большое значение в неорганической химии, в том числе в области химии переходных металлов. Неорганические соединения обычно имеют более высокие температуры плавления. Другие методы, такие как перекристаллизация, электрохимия, рентгеновская кристаллография, кислотно-щелочная химия, химия pH, катализ и т. Д., Относятся к неорганической химии.
Что происходит в случае реакций замещения, так это то, что катионы и анионы между двумя соединениями обмениваются в зависимости от их реакционного потенциала. С другой стороны, окислительно-восстановительные реакции происходят из-за окисления и восстановления.Таким образом, металлы и их формы имеют большое значение в неорганической химии, в том числе в области химии переходных металлов. Неорганические соединения обычно имеют более высокие температуры плавления. Другие методы, такие как перекристаллизация, электрохимия, рентгеновская кристаллография, кислотно-щелочная химия, химия pH, катализ и т. Д., Относятся к неорганической химии. Таким образом, очень легко отличить органическое соединение от неорганического. До -х годов века считалось, что органические молекулы являются естественными и могут быть извлечены только из природы. Однако самый большой прорыв в органической химии произошел, когда Кекуле объяснил существование структуры бензола. Бензольное ядро стало неотъемлемой частью органической химии.
Таким образом, очень легко отличить органическое соединение от неорганического. До -х годов века считалось, что органические молекулы являются естественными и могут быть извлечены только из природы. Однако самый большой прорыв в органической химии произошел, когда Кекуле объяснил существование структуры бензола. Бензольное ядро стало неотъемлемой частью органической химии.