Воздух — Википедия
Материал из Википедии — свободной энциклопедии
Во́здух — смесь газов главным образом азота и кислорода — 98—99 % в сумме и зависит от влажности (концентрации водяного пара), а также аргона, углекислого газа, водорода, образующая земную атмосферу. Воздух необходим для нормального существования на Земле живых организмов. Кислород, содержащийся в воздухе, в процессе дыхания поступает в клетки организма и используется в процессе окисления, в результате которого происходит выделение необходимой для жизни энергии (метаболизм, аэробы). В промышленности и в быту кислород воздуха используется для сжигания топлива с целью получения тепла и механической энергии в двигателях внутреннего сгорания. Из воздуха, используя метод сжижения, добывают инертные газы. В соответствии с федеральным законом РФ «Об охране атмосферного воздуха» под атмосферным воздухом понимается «жизненно важный компонент окружающей среды, представляющий собой естественную смесь газов атмосферы, находящуюся за пределами жилых, производственных и иных помещений».
Доказательства зонального распределения температуры воздуха: она понижается от экватора к полюсам. В этом направлении угол падения солнечных лучей уменьшается, что приводит к снижению нагревания земной поверхности. Средняя годовая температура на всей земной поверхности +14 °C. Южное полушарие холоднее Северного.
 Состав воздуха
Состав воздухаВ 1754 году Джозеф Блэк экспериментально доказал, что воздух представляет собой смесь газов, а не простое вещество[1].
| Вещество | Обозначение | По объёму, % | По массе, % |
|---|---|---|---|
| Азот | N2 | 78,084 | 75,5 |
| Кислород | O2 | 20,9476 | 23,15 |
| Аргон | Ar | 0,934 | 1,292 |
| Углекислый газ | CO2 | 0,03 | 0,046 |
| Неон | Ne | 0,001818 | 0,0014 |
| Криптон | Kr | 0,000114 | 0,003 |
| Метан | CH4 | 0,0002 | 0,000084 |
| Гелий | He | 0,000524 | 0,000073 |
| Водород | H2 | 0,00005 | 0,00008 |
| Ксенон | Xe | 0,0000087 | 0,00004 |
Состав воздуха может меняться в небольших пределах: в крупных городах содержание углекислого газа немного выше, чем в лесах; в высокогорье и на больших высотах концентрация кислорода немного ниже вследствие того, что молекулы кислорода тяжелее молекул азота, и поэтому концентрация кислорода с высотой уменьшается быстрее.
Существенное влияние на концентрацию газов в воздухе вносит водяной пар, концентрация которого зависит от температуры, влажности, времени года, климата. Так, при температуре 0 °C 1 м³ воздуха может содержать максимально 5 г воды, а при температуре +10 °C — уже 10 г.
| Параметр | Значение | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Средняя молярная масса | 28,98 г/моль | ||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| Средняя удельная теплоёмкость при постоянном давлении cp | 1,006 кДж/(кг·К) | ||||||||||||||||||||||||||||||||
| Средняя удельная теплоёмкость при постоянном объёме cv | 0,717 кДж/(кг·К) | ||||||||||||||||||||||||||||||||
| Показатель адиабаты | 1,40 | ||||||||||||||||||||||||||||||||
| Скорость звука (при н. у.) | 331 м/с (1193 км/ч)[2] | ||||||||||||||||||||||||||||||||
| Средний коэффициент теплового расширения в интервале температур 0—100 °C | 3,67⋅10−3 1/К | ||||||||||||||||||||||||||||||||
| Коэффициент динамической вязкости воздуха (при н. у.) | 17,2 мкПа·с | ||||||||||||||||||||||||||||||||
| Растворимость воздуха в воде | 29,18 см3/л | ||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| Показатель преломления (при стандартных условиях) | 1,0002926 | ||||||||||||||||||||||||||||||||
| Коэффициент изменения показателя преломления | 2,8⋅10−9 1/Pa | ||||||||||||||||||||||||||||||||
| Средняя поляризуемость молекулы | 1,7⋅10−30 | ||||||||||||||||||||||||||||||||
| Константа Сатерленда Sat | 171⋅10−7 | ||||||||||||||||||||||||||||||||
В философии Эмпедокла воздух (аэр) — это одна из четырех стихий космоса, наряду с огнём, землей и водой. В философии Аристотеля воздух относится к подлунным легким элементам.
Немецкий мыслитель Фридрих Вильгельм Ницше писал о воздухе, что это наивысшая и самая тонкая из материй. Из воздуха соткана свобода человека. Поэтому символ воздуха в первую очередь — это символ свободы. Это свобода, для которой нет никаких преград, ведь воздух нельзя ограничить, нельзя поймать и придать ему форму[3][4].
Это символ не только физической, но и духовной свободы, свободы мысли. Поэтому присутствие символов воздуха на какой-либо поверхности говорит о легкости мышления, свободе и непредсказуемости
- ↑ Gribbin, John. Science. A History (1543-2001). — L.: Penguin Books, 2003. — 648 с. — ISBN 978-0-140-29741-6.
- ↑ Скорость звука // Физическая энциклопедия / под. ред. А. М. Прохорова. — М.: «Советская энциклопедия», 1988. — Т. 4.
- ↑ Ковальчук Т. Ю. Структура художественного пространства в лирике Д. С. Мережковского 1880—1900-х годов // Вестник Челябинского государственного университета. Филология. Искусствоведение. — Вып. 49.— 2010. — № 34 (215). — С. 58.
- ↑ Энциклопедия символов, знаков, эмблем. / авт.-сост. В. Андреева и др. — М. : МИФ : АСТ, 2001. — С. 96—97.
- ↑ Воздух // Символы, знаки, эмблемы: Энциклопедия / авт.-сост. В. Э. Багдасарян, И. Б. Орлов, В. Л. Телицын; под общ. ред. В. Л. Телицына. — 2-е изд. — М.: ЛОКИД-ПРЕСС, 2005. — 495 с.
Природный газ, это смесь или чистое вещество: свойства, состав
Многие люди не раз слышали словосочетание «природный газ» и даже пользовались им, но до конца не понимают, что это такое. Прежде всего стоит разобраться, природный газ это смесь или чистое вещество. Исходя из того, что в различных местах зарождения имеются различные сочетания данного вещества, то это смесь нескольких газов. Они обрезаются в недрах планеты во время анаэробного разложения органических веществ, которые находятся под ее поверхностью. Это натуральное природное ископаемое, которое добывается в том же виде, в котором и используется. В пластовых условиях вещество находится в газообразном состоянии. Также встречаются газовые шапки в месте рождения нефти. В растворенном состоянии вещество может находиться в воде или нефти.
Преимущественно в таких газах содержится метан. Его соотношения в различных случаях может достигать, примерно, 82-98%. Практически всегда в таких газах есть примесь в виде азота, углекислого газа и водяных паров. Водорода в примесях встречается очень редко. Это минимизирует количество сжимающихся составляющих в смеси.
Область применения 
Данное вещество применяется в сварочной сфере достаточно активно. Его можно встретить при поверхностной кислородной и разделительной резке. Также им производится непосредственное сваривание стальных деталей. С учетом того, что природный газ не обеспечивает столь высокую температуру, как остальные защитные газы, его можно применять для заготовок, толщина которых не превышает 5 мм. Больше всего он востребован при сварке легкоплавких сплавов и металлов. Помимо этого, его применяют в пайке. Практически все процессы газопламенной обработки, где используется данное вещество, не имеют потребности в высокой температуре пламени. Здесь же могут использоваться смеси природного газа с генераторным или коксовым. Свойства смеси, предназначенной для использования в сварке, регламентируется ГОСТ 5542-87.
Благодаря своей относительно невысокой стоимости, для самых простых процедур, чтобы понизить себестоимость шва, специалисты стараются использовать именно этот расходный материал. Он хранится в баллонах при меньшем давлении чем другие защитные газы, поэтому, если использование является более безопасным.
Природный газ — это вещество или смесь? 
Природный газ — это смесь из нескольких газов. Естественною, что при наличии такого термина многие люди могут подумать, что это отдельное образование, которое имеет свою формулу и так далее. Но на самом деле это несколько газов, зародившихся в одном месте при весьма схожих условиях. Даже с учетом того, что в некоторых случаях состав может отличаться более чем на 10%, основные свойства газа остаются почти одинаковыми, за некоторыми исключениями. Для промышленности подобные отклонения не имеют большого значения, так как во время ответственных работ такое вещество не применяется.
Определением того, что именно из себя представляет природный газ, задались еще в позапрошлом веке. В 1813 году Гемфри Деви определил, что газ с рудников и с болот имеет очень схожий состав и является смесью нескольких газов. Так было открыто понятие природного газа и создана отдельная его классификация.
Физические и химические свойства 
Физические характеристики во многом определяются составом, но в среднем параметры выглядят следующим образом:
- Температура самовозгорания – 650 градусов Цельсия;
- Плотность вещества – 0,73 кг/м2;
- Удельная теплота при сгорании – 38 МДж/м3;
- Масса вещества легче воздуха в 1,8 раз;
- Октановое число (если газ применяется в двигателях внутреннего сгорания) – 125;
- Соотношение газа с воздухом для создания взрывоопасной смеси – 15%.
Состав природного газа 
Основную часть вещества составляет метан, содержание которого колеблется от 70 до 98%. Вместе с ним в составе содержатся тяжелые углероды, такие как:
- Бутан;
- Пропан;
- Этан.
Помимо этого, в составе встречаются те вещества, которые не относятся к углеводородам. Среди них:
- Азот;
- Диоксид углерода;
- Сероводород;
- Водород;
- Гелий.

Состав природного газа
В техническом газе порой встречаются еще одоранты, вещества, которые придают запах. Это обусловлено тем, что в природном состоянии природный газ не имеет запаха и цвета.
Инструкция по использованию природного газа при сварке 
Использование природного газа в сварке встречается довольно часто. Принципиальных отличий в использовании его от других защитных газов в сварке не наблюдается. Он применяется для самых простых работ, но здесь также нужно применять правила безопасности. Когда проведены все подготовительные операции, следует включить горелку и продуть ее при помощи этого вещества. Когда будет слышен запах с горелки, то можно поджигать и подавать кислород.
«Важно!
Баллон от источника тепла должен находиться на расстоянии от 5 метров и дальше.»
Для каждого типа сварки нужно применять свои режимы. Они выставляются заранее, согласно требуемой технологии и только после этого начинается непосредственное сваривание. В некоторых случаях, когда нужно подогревать металл до и после создания шва, горелка ставится на режим с более низкой температурой
Углекислый газ — вещество или смесь? 
По аналогии с природным, некоторые люди задаются вопросом, углекислый газ чистое вещество или смесь. Здесь ответ будет более простым, так как для обозначения данного расходного материала имеется формула СО2. Это показывает, что углекислота является отдельным веществом с постоянной формулой. Природный газ не имеет постоянной формулы, что характеризует его как смесь.
Заключение
Природный газ знаком практически всем, а не только сварщикам, так как сфера его применения очень широка. Он встречается не только в области сварки, но и в отоплении, приготовлении пищи и так далее. Для сваривания металлов требуется качественная смесь с определенным соотношением, благодаря чему и существуют различные государственные стандарты по применению.
Воздух с точки зрения химии, его основные свойства
На страницах блога мы много рассказываем о самых разных химических веществах и смесях, но у нас еще не было рассказа об одном из важнейших сложных веществ — о воздухе. Исправим это и расскажем о воздухе. В первой статье: немного истории изучения воздуха, его химический состав и основные факты о нем.
Немного истории изучения воздуха
В настоящее время под воздухом понимают смесь газов,  образующих атмосферу нашей планеты. Но так было не всегда: долгое время ученые думали, что воздух — это простое вещество, целостная субстанция. И хотя многие ученые высказывали гипотезы о сложном составе воздуха, дальше догадок дело не шло до XVIII века. Кроме того, воздуху придавали философское значение. В Древней Греции воздух считался одной из основополагающих космических стихий, наряду с землей, огнем, землей и водой образующих все сущее. Аристотель относил воздух к подлунным легким элементам, олицетворяющим влажность и тепло. Ницше в своих трудах писал о воздухе, как о символе свободы, как о наивысшей и самой тонкой форме материи, для которой не существует преград.
образующих атмосферу нашей планеты. Но так было не всегда: долгое время ученые думали, что воздух — это простое вещество, целостная субстанция. И хотя многие ученые высказывали гипотезы о сложном составе воздуха, дальше догадок дело не шло до XVIII века. Кроме того, воздуху придавали философское значение. В Древней Греции воздух считался одной из основополагающих космических стихий, наряду с землей, огнем, землей и водой образующих все сущее. Аристотель относил воздух к подлунным легким элементам, олицетворяющим влажность и тепло. Ницше в своих трудах писал о воздухе, как о символе свободы, как о наивысшей и самой тонкой форме материи, для которой не существует преград.
В XVII веке было доказано, что воздух — это материальная сущность, вещество, свойства которого, например, плотность и вес, можно измерить.
В XVIII веке ученые проводили в запаянных химических сосудах реакции воздуха с различными веществами. Так было установлено, что поглощается примерно пятая часть объема воздуха, а оставшаяся часть горения и дыхания не поддерживают. В результате был сделан вывод, что воздух вещество сложное, состоящее из двух составляющих, одна из которых, кислород — поддерживает горение, а вторая — азот, «испорченный воздух», не поддерживает горение и дыхание. Так был открыт кислород. Чуть позднее получен в чистом виде азот. И только в самом конце XIX века были открыты аргон, гелий, криптон, ксенон, радон и неон, тоже имеющиеся в составе воздуха.
Химический состав
Воздух состоит из смеси примерно двадцати семи различных газов. Примерно на 99% — это смесь кислорода и азота. В составе оставшегося процента: водяной пар, углекислый газ, метан, водород, озон, инертные газы (аргон, ксенон, неон, гелий, криптон) и другие. Например, в воздухе часто можно обнаружить сероводород, угарный газ, йод, оксиды азота, аммиак.
 Считается, что в чистом воздухе при нормальных условиях содержится 78,1% азота и 20,93% кислорода. Однако в зависимости от географического положения и высоты над уровнем моря состав воздуха может различаться.
Считается, что в чистом воздухе при нормальных условиях содержится 78,1% азота и 20,93% кислорода. Однако в зависимости от географического положения и высоты над уровнем моря состав воздуха может различаться.
Существует еще такое понятие, как загрязненный воздух, то есть воздух, состав которого отличается от природного атмосферного за счет наличия загрязняющих веществ. Эти вещества бывают:
• естественного происхождения (вулканические газы и пыль, морская соль, дымы и газы от природных пожаров, растительная пыльца, пыль от эрозии почв и т.п.).
• антропогенного происхождения — возникшие в результате промышленной и бытовой деятельностью человека (выбросы соединений углерода, серы, азота; угольной и другой пыли от горнодобычи и промышленных предприятий; отходы сельскохозяйственного производства, промышленные и бытовые свалки, аварийные разливы нефти и других опасных для окружающей среды веществ; газовые выхлопы транспортных средств и т.п.).
Свойства
Чистый атмосферный воздух не имеет цвета и запаха, он невидим, хотя его можно ощутить. Физические параметры воздуха определяются следующими характеристиками:
• массой;
• температурой;
• плотностью;
• атмосферным давлением;
• влажностью;
• теплоемкостью;
• теплопроводностью;
• вязкостью.
Большая часть параметров воздуха зависят от его температуры, поэтому существует множество таблиц параметров воздуха для различных температур. Температуру воздуха измеряют с помощью метеорологического термометра, а влажность — с помощью гигрометра.
Воздух проявляет окислительные свойства (за счет большого содержания кислорода), поддерживает горение и дыхание; плохо проводит тепло, хорошо растворяется в воде. Его плотность уменьшается по мере увеличения температуры, а вязкость увеличивается.
Из следующей статьи вы узнаете о несколько несколько интересных фактов о воздухе и его применении.
Тест для 8 класса «Чистые вещества и смеси».
Самостоятельная работа по теме «Чистые вещества и смеси».
Вариант 1.
Часть А.
А1. Чистым (индивидуальным) веществом является:
1) стекло 2) речная вода 3) кислород 4) сталь
А2. Неоднородная смесь – это
1) молоко 2) раствор сахара 3) воздух 4) стекло
А3. Химический анализ состава смесей не проводят
геологи при разведке полезных ископаемых
продавцы хозяйственных магазинов
криминалисты
лаборанты химических лабораторий
А4. Смесь медных и железных опилок может быть разделена методом
1) отстаивания 2) фильтрования 3) кристаллизации 4) действия магнита
А5. Для очистки воды от растворённых в ней минеральных солей используют
1) центрифугирование 2) отстаивание 3) дистилляцию 4) фильтрование
А6. Способ разделения неоднородных смесей – это
1) дистилляция 2) выпаривание 3) хроматография 4) отстаивание
А7. Масса хлорида натрия, полученная при выпаривании 100 г 5%-го раствора NaCl
1) 2г 2) 3г 3) 5г 4) 10г
А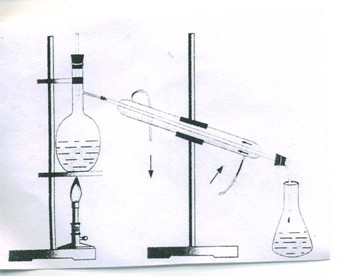 8. На рисунке показан способ разделения смеси
8. На рисунке показан способ разделения смеси
дистилляция
Выпаривание
Хроматография
Делительная воронка
А9. Газообразная смесь – это
1) природный газ 2) латунь 3) углекислый газ 4) кислород
А10. Газ, который не входит в состав воздуха
1) O2 2)Cl2 3) N2 4) CO2
А11. Признак или свойство, на основе которого можно разделить смесь растительного масла с водой: 1) цвет 2) плотность 3) запах 4) агрегатное состояние
А12. Нефтепродуктом является
1) природный газ 2) кокс 3) бензол 4) мазут
А13. Для разделения смеси сахарного песка с водой используют
чашку для выпаривания
воронку с фильтром
Делительную воронку
Прибор для дистилляции
А14. Масса сахара, необходимая для приготовления 200 г 5%-ного раствора сахара
1) 2г 2) 4г 3) 10 г 4) 20г
А15. Верны ли суждения о способах разделения смесей?
1)верно только А
2)верно только Б
3) верны оба суждения
4) оба суждения неверны
Часть В.
В1. Однородной смесью являются
воздух
цементный раствор
молоко
раствор уксусной кислоты
смесь глины с водой
В2. Установите соответствие между следующими понятиями.
1) раствор сахара в воде
6) кислород
Б) смеси
2) железная скрепка
7) магний
В) чистые вещества
3) алюминий
8) яблочный сок
4) дистиллированная вода
9) стеклянный цилиндр
5) речная вода
10) медная проволока
Часть С.
С1. Рассчитайте массовую долю соды в растворе, полученном при добавлении 20 г воды к 60 г 20%-ного раствора соды.
Самостоятельная работа по теме «Чистые вещества и смеси».
Вариант 2.
Часть А.
А1. Смесью является: 1) водопроводная вода 2) углекислый газ 3) кислород 4) азот
А2. Однородная смесь – это: 1) молоко 2) раствор этилового спирта 3) смесь мела с водой 4) нефть
А3. Фильтрованием можно разделить смесь воды и
1) сахарного песка 2) машинного масла 3) бензина 4) почвы
А4. Меньше всего растворённых солей содержит вода
1) морская 2) дождевая 3) дистиллированная 4) колодезная
А5. Водная смесь зубного порошка и поваренной соли может быть разделена
1) выпариванием 2) отстаиванием 3) перегонкой 4) кристаллизацией
А6. Способ разделения однородных смесей
1) выпаривание 2) отстаивание 3) фильтрование 4) действие магнитом
А7. Масса нитрата калия, образующегося при выпаривании 200 г 10%-ного раствора KNO3
1) 20г 2) 25г 3) 30г 4) 40г
А8. Верны ли суждения о чистых веществах и смесях?
А. Виноградный сок – это чистое вещество.
Б. Раствор сахара в воде является неоднородной смесью.
1)верно только А
2)верно только Б
3) верны оба суждения
4) оба суждения неверны
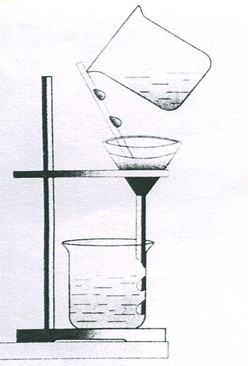
А9. На рисунке показан способ разделения смеси
м
 едных и древесных опилок
едных и древесных опилокРаствора мела в воде
Раствора столового уксуса
Воды и растительного масла
А10. К твёрдой смеси относится: 1) природный газ 2) нефть 3) бензин 4) чугун
А11. Газ, который преобладает в воздухе: 1) O2 2) Ar 3) N2 4) CO2
А12. Смесь порошков железа и серы можно разделить с помощью
1) возгонки 2) дистилляции 3) действия магнита 4) фильтрования
А13. Для очистки питьевой воды на водозаборной станции используют
речной песок 2) бумажный фильтр 3) матерчатый фильтр 4) вату
А14. Для разделения смеси подсолнечного масла и воды используют
чашку для выпаривания
делительную воронку
прибор для фильтрования
прибор для дистилляции
А15. Масса соли, полученная при выпаривании 300 г её раствора с массовой долей 0,15
1) 15г 2) 20 г 3) 30 г 4) 45 г
Часть В.
В1. Правильные суждения о чистых веществах и смесях.
при растворении мела в воде образуется неоднородная смесь
в однородных смесях частицы компонентов можно обнаружить невооружённым глазом
при растворении в воде поваренной соли образуется неоднородная смесь
смесь воды и сахара можно разделить выпариванием
однородные смеси при хранении самопроизвольно разделяются
В2. Установите соответствие между следующими понятиями.
1) фосфор
6) молоко
Б) смеси
2) воздух
7) азот
В) чистые вещества
3) чашка
8) цемент
4) сахарный песок
9) гвоздь
5) водопроводная вода
10) сладкий чай
Часть С.
С1. К 200 г 15%-ного раствора сахара добавили 15 г сахара. Какова массовая доля сахара в полученном растворе?

 едных и древесных опилок
едных и древесных опилок