Дихромат калия — Википедия
Материал из Википедии — свободной энциклопедии
У этого термина существуют и другие значения, см. хромпик.| Дихромат калия | |||
|---|---|---|---|
| |||
({{{изображение}}}) | |||
| Систематическое наименование | Дихромат калия | ||
| Традиционные названия | Бихромат калия, двухромовокислый калий, хромпик | ||
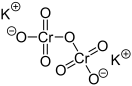
| Хим. формула | K2Cr2O7 | ||
| Состояние | оранжевые кристаллы | ||
| Молярная масса | 294,19 г/моль | ||
| Плотность | 2,676 г/см³ | ||
| Температура | |||
| • плавления | 396 °C | ||
| • кипения | 500 °C | ||
| • разложения | 500 °C | ||
| Энтальпия | |||
| • образования | −2033 кДж/моль | ||
| Растворимость | |||
| • в воде | 4,9 г/100 мл | ||
| Координационная геометрия | Тетраэдральная | ||
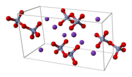
| Кристаллическая структура | Триклинная | ||
| Рег. номер CAS | 7778-50-9 | ||
| PubChem | 24502 | ||
| Рег. номер EINECS | 231-906-6 | ||
| SMILES | |||
| InChI | |||
| RTECS | HX7680000 | ||
| ChEBI | 53444 | ||
| ChemSpider | 22910 | ||
| ЛД50 | 25 мг/кг (крысы, орально) | ||
| Токсичность | высокотоксичен, канцероген, мутаген, аллерген, сильный окислитель | ||
| Пиктограммы СГС |      | ||
| NFPA 704 |  | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |||
Дихрома́т ка́лия (двухромовокислый калий, бихромат калия, техн.
хро́мпик) — неорганическое соединение, калиевая соль дихромовой кислоты с химической формулой K2Cr2O7, имеет вид оранжевых кристаллов. Обладает сильными окислительными свойствами, в связи с чем широко применяется в химии, фотографии, пиротехнике и различных областях промышленности. Высокотоксичен и канцерогенен.Иногда хромпиком также называют дихромат натрия (Na2Cr2O7).
Оранжевые кристаллы с температурой плавления 396 °C. Разлагается при нагреве выше 500 °C. Растворим в воде (г / 100 г): 4,6 (0 °C), 15,1 (25 °C), 37,7 (50 °C), незначительно растворим в этаноле. Сильный окислитель[1].
В кислой среде восстанавливается до солей хрома (III)[1]. Например, он окисляет галогенид-ионы галогенводородных кислот до свободных галогенов:
- K2Cr2O7+14HCl→2CrCl3+3Cl2+2KCl+7h3O{\displaystyle {\mathsf {K_{2}Cr_{2}O_{7}+14HCl\rightarrow 2CrCl_{3}+3Cl_{2}+2KCl+7H_{2}O}}}
Также в кислой среде при pH 3,0—3,5 обладает способностью окислять металлическое серебро[2]:
- 6Ag+Cr2O72−+14H+→−6e−6Ag++2Cr3++7h3O{\displaystyle 6Ag+Cr_{2}O_{7}^{2-}+14H^{+}{\ce {->[-6e^-]}}6Ag^{+}+2Cr^{3+}+7H_{2}O}
Кристаллический дихромат калия при нагревании с серой и углеродом восстанавливается до оксида хрома (III)[1]:
- K2Cr2O7+S→Cr2O3+K2SO4{\displaystyle {\mathsf {K_{2}Cr_{2}O_{7}+S\rightarrow Cr_{2}O_{3}+K_{2}SO_{4}}}}
- 2K2Cr2O7+3C→2Cr2O3+2K2CO3+CO2{\displaystyle {\mathsf {2K_{2}Cr_{2}O_{7}+3C\rightarrow 2Cr_{2}O_{3}+2K_{2}CO_{3}+CO_{2}}}}
Водные растворы дихромата калия обладают дубящими свойствами, в частности, задубливают желатину[2].
Получают действием хлорида калия на дихромат натрия:
- 2KCl+Na2Cr2O7→K2Cr2O7+2NaCl{\displaystyle {\mathsf {2KCl+Na_{2}Cr_{2}O_{7}\rightarrow K_{2}Cr_{2}O_{7}+2NaCl}}}
Применяется при производстве красителей, при дублении кож и овчин, как окислитель в спичечной промышленности, пиротехнике, фотографии, живописи. Раствор хромпика в серной кислоте (т. н. хромовую смесь) применяют для мытья стеклянной посуды в лабораториях. В лабораторной практике используется в качестве окислителя, в том числе в аналитической химии (хроматометрия).
В чёрно-белой фотографии применяется в качестве отбеливателя для удаления металлического серебра из эмульсии. Не применяется в цветной фотографии, так как для отбеливания требует кислой среды, а при pH ⩽ 4 красители, образовавшиеся в эмульсии при цветном проявлении, обесцвечиваются. Вместо этого в цветной фотографии для отбеливания используются составы на основе гексацианоферрата(III) калия и железной соли трилона Б[2].
Высокотоксичен[1], канцерогенен, аллерген, брызги его раствора разрушают кожные покровы, дыхательные пути и хрящевые ткани. Среди соединений шестивалентного хрома наиболее токсичен. ПДК составляет 0,01 мг/м³ (в пересчёте на CrO3)[1]. При работе с дихроматом калия необходимо применять защиту органов дыхания и кожи.
- Егоров А.С. Химия: современный курс для подготовки к ЕГЭ. — Ростов-на-Дону: Феникс, 2013. — 699 с. — ISBN 978-5-222-21137-3.
- Лидин Р. А., Андреева Л. Л., Молочко В. А. Химические свойства неорганических веществ: Учеб. пособие для вузов — 3-е изд., испр — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0
- Редько А. В. Химия фотографических процессов. — СПб. : НПО «Профессионал», 2006. — С. 837—954. — 1464 с. — (Новый справочник химика и технолога / ред. Москвин А. В. ; вып. Общие сведения. Строение вещества. Физические свойства важнейших веществ. Ароматические соединения. Химия фотографических процессов. Номенклатура органических соединений. Техника лабораторных работ. Основы технологии.). — ISBN 978-5-91259-013-9.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.-Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Степин Б. Д. Калия дихромат : статья // Химическая энциклопедия / Редкол.: Кнунянц И. Л. и др.. — М. : Советская энциклопедия, 1990. — Т. 2: Даффа—Меди. — С. 287—288. — 671 с. — ISBN 5-85270-035-5.
Хроматы — Википедия
Материал из Википедии — свободной энциклопедии
Хроматы — соли хромовой кислоты H2CrO4. Устойчивы в нейтральной и щелочной среде, в кислой среде обратимо переходят в дихроматы — соли дихромовой кислоты H2Cr2O7.
Хроматы получают путём сплавления CrO3 с основными оксидами:
- CrO3+ZnO→ZnCrO4{\displaystyle {\mathsf {CrO_{3}+ZnO\rightarrow ZnCrO_{4}}}}
Более распространено окисление соединений Cr3+ в щелочных растворах:
- 2KCrO2+3h3O2+2KOH→2K2CrO4+4h3O{\displaystyle {\mathsf {2KCrO_{2}+3H_{2}O_{2}+2KOH\rightarrow 2K_{2}CrO_{4}+4H_{2}O}}}
- 2K3[Cr(OH)6]+3Br2+4KOH→2K2CrO4+6KBr+8h3O{\displaystyle {\mathsf {2K_{3}[Cr(OH)_{6}]+3Br_{2}+4KOH\rightarrow 2K_{2}CrO_{4}+6KBr+8H_{2}O}}}
При этом происходит переход зелёной окраски раствора (ион Cr3+) в жёлтую (ион CrO42−).
Хромат-ион при подкислении переходит в дихромат-ион (при этом окраска раствора становится оранжевой), в растворах существует равновесие между хромат- и дихромат-ионами:
- 2CrO42−+2H+⇄2HCrO4−⇄Cr2O72−+h3O{\displaystyle {\mathsf {2CrO_{4}^{2-}+2H^{+}\rightleftarrows 2HCrO_{4}^{-}\rightleftarrows Cr_{2}O_{7}^{2-}+H_{2}O}}}
Хроматы устойчивы в нейтральной и щелочной среде, а дихроматы — в кислой.
Большинство дихроматов имеет оранжево-красную окраску. Растворимость их, как правило, выше, чем соответствующих хроматов. Почти все дихроматы щелочных, щелочноземельных и тяжёлых металлов хорошо растворимы в воде, малорастворимы дихроматы таллия и серебра.
Дихроматы, как и хроматы, в кислой среде являются сильными окислителями за счёт восстановления Cr(VI) до Cr(III), например:
- K2Cr2O7+14HCl→2KCl+2CrCl3+3Cl2↑+7h3O{\displaystyle {\mathsf {K_{2}Cr_{2}O_{7}+14HCl\rightarrow 2KCl+2CrCl_{3}+3Cl_{2}\uparrow +7H_{2}O}}}
При нагревании дихроматы малоустойчивы:
- 2K2Cr2O7→4KCrO2+3O2{\displaystyle {\mathsf {2K_{2}Cr_{2}O_{7}\rightarrow 4KCrO_{2}+3O_{2}}}}
Хроматы применяют в качестве сильных окислителей, как красящие вещества. Также хроматы используются в качестве средства для мытья лабораторной посуды, так называемая «хромовая смесь». Хроматы калия и натрия применяют в качестве консервантов древесины, как протраву при хранении тканей. Нерастворимые хроматы некоторых металлов обладают яркими, насыщенными цветами, поэтому на их основе делают краски: жёлтые кроны (PbCrO4, ZnCrO4, SrCrO4), красный свинцово-молибденовый крон (PbCrO4 и MoCrO4), создающий гамму оттенков от розового до фиолетового SnCrO4.
Обладающая очень сильным окислительным действием смесь равных объёмов насыщенного на холоду раствора K2Cr2O7 и концентрированной H2SO4 (хромовая смесь) применяется в лабораториях для мытья химической посуды.
Все соединения шестивалентного хрома, в том числе хроматы и дихроматы, токсичны и канцерогенны.
- Химическая энциклопедия / Редкол.: Зефиров Н.С. и др.. — М.: Большая Российская энциклопедия, 1998. — Т. 5 (Три-Ятр). — 783 с. — ISBN 5-85270-310-9.
Cr2O3 + HCl = ? уравнение реакции
В результате взаимодействия оксида хрома (III) с хлороводородной кислотой (Cr2O3 + HCl = ?) происходит образование хлорида хрома (III) и воды. Молекулярное уравнение реакции имеет вид:
Запишем ионные уравнения, учитывая, что оксиды и вода на ионы не распадаются, т.е. не диссоциируют.
Первое уравнение называют полным ионным, а второе – сокращенным ионным.
Хлорид хрома (III) представляет собой тугоплавкие кристаллы фиолетово-красного цвета, разлагающиеся при прокаливании и сублимирующиеся при нагревании в потоке хлора. Хорошо растворяется в холодной воде (но чрезвычайно медленно, растворение ускоряется в присутствии), гидролизуется по катиону. Образует кристаллогидраты состава и .
Хлорид хрома (III) реагирует со щелочами, гидратом аммиака. Слабый окислитель, в растворе восстанавливается атомным водородом, при высокой температуре — водородом, кальцием, хромом. Слабый восстановитель, в растворе окисляется хлорноватой кислотой, перманганатом калия, галогенами, при высокой температуре — фтором. Вступает в реакции обмена и комплексообразования.
Хлорид хрома (III) в промышленных масштабах получают путем хлорирования оксида хрома (III) в присутствии углерода при температуре :
 (
(