a) Zn+CL2 = ZNCl2; б) Zn+2HCl = ZnCl2 + h3↑ Проставьте над знаками соответствующих химических элементов степени их окисления и покажите переход электронов.
Источник:  Решебник
по
химии
за 9 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 1999 год),
Решебник
по
химии
за 9 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 1999 год),
задача №6
к главе «Глава I §§ 4-6 стр. 20».
Все задачи >
Даны уравнения реакций:Проставьте над знаками соответствующих химических элементов степени их окисления и покажите переход электронов. Ответ:
восстановитель, окисляется
окислитель, восстанавливается
восстановитель, окисляется —
окислитель, восстанавливается —
← Вопрос № 5 Даны уравнения реакций: a)h30 → 2h3↑+O2↑ б)Cu(OH)2 → CuO + h3O в)N2O5+h3O → 2HNO3 г)CuSO4+Fe → FeSO4+Cu д)2Fe+3Cl2 → 2FeCl3 Какие из этих реакций являются окислительно-восстановительными и почему? Укажите окисВопрос № 7 Даны схемы уравнений реакций: a) CuS + HNO3(разб) → Cu(NO3)2 + S + NO + h30; б) K2SO3 + h3SO4 + KMnO4 → K2SO4 + MnSO4 + h3O Составьте уравнения окислительно-восстановительных реакций, пользуясь рекомендацией, приведенной на стр. 17 →
- Вконтакте
5terka.com
a) Zn+CL2 = ZNCl2; б) Zn+2HCl = ZnCl2 + h3↑ Проставьте над… решение задачи
даны уравнения реакций:

 проставьте над знаками соответствующих химических элементов степени их окисления и покажите переход электронов. ответ:
проставьте над знаками соответствующих химических элементов степени их окисления и покажите переход электронов. ответ:
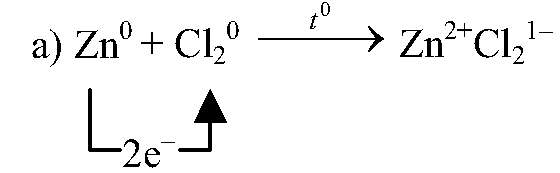
 восстановитель, окисляется
восстановитель, окисляется
 окислитель, восстанавливается
окислитель, восстанавливается

 восстановитель, окисляется —
восстановитель, окисляется —



davay5.com
§1. Окислительно-восстановительные реакции | 9 класс
1. Определите степени окисления элементов в следующих соединениях:
Li+12O-2, Na+12O-12, H+12S-2, Li+1H-1, P+52O-25, K+12Cr+62O-27.
2. Докажите, что реакция
2Fe + 3Cl2 = 2FeCl3 является окислительно-восстановительной. Укажите окислитель и восстановитель.
Fe0 – 3e– = Fe+III восстановитель
Cl02 + 2e– = 2Cl–I окислитель
3. Заполните таблицу, приведя по два примера реакций соединения и разложения, которые не являются окислительно-восстановительными. Обсудите таблицу с соседом о парте. Проверьте друг у друга заполненную таблицу.
4. Даны схемы реакций.
Zn+Cl2=ZnCl2
Zn+2HCl=ZnCl2+H2
Поставьте над знаками соответствующих химических элементов степени окисления, покажите переход электронов и расставьте коэффициенты.
Ответ:
Zn0+Cl02=Zn+2Cl-12
Zn0 – 2e– = Zn +II восстановитель, окисление
Cl02 + 2e– = 2Cl–I окислитель, восстановление
Zn0+2H+1
Cl-1=Zn+2Cl-12+H02Zn0 – 2e– = Zn +II восстановитель, окисление
2H+ + 2e– = H20 окислитель, восстановление
5. Даны схемы окислительно-восстановительных реакций.
А) CuS + HNO3 = Cu(NO3)2 + S + NO + H2O
Б) K2SO3+ H2SO4+KMnO4 = K2SO4 + MnSO4 + H2O
Составьте уравнения этих реакций, пользуясь алгоритмом, приведенном в параграфе.
Ответ:
6. В схеме реакции HNO3 → H2O + NO2 + Q
Расставьте коэффициенты методом электронного баланса.
Ответ:
4HN⁺⁵O₃ = 2H₂O + 4N⁺⁴O₂ + O₂°
N⁺⁵ + 1e⁻ = N⁺⁴ /4 окислитель
2O⁻² — 4e⁻ = O₂° /1 восстановитель
Тестовые задания.
1. 2)
2. 1)б
2) д
3) а
4) г
superhimik.ru
a)h30 → 2h3↑+O2↑ б)Cu(OH)2 → CuO + h3O в)N2O5+h3O → 2HNO3 г)CuSO4+Fe → FeSO4+Cu д)2Fe+3Cl2 → 2FeCl3 Какие из этих реакций являются окислительно-восстановительными и почему? Укажите окис
Источник:  Решебник
по
химии
за 9 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 1999 год),
Решебник
по
химии
за 9 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 1999 год),
задача №5
к главе «Глава I §§ 4-6 стр. 20».
Все задачи >
Даны уравнения реакций:Какие из этих реакций являются окислительно-восстановительными и почему? Укажите окислитель и восстановитель. Ответ: Окислительно-восстановительными являются следующие реакции:
восстановитель, окисляется
окислитель, восстанавливается
восстановитель, окисляется
окислитель, восстанавливается
восстановитель, окисляется
окислитель, восстанавливается Во всех реакциях атомы элементов меняют свою степень окисления, в отличие от двух остальных реакция, где степень окисления остается прежней:
← Вопрос № 4 Даны схемы a) 2H+ + CO32- →; б) 2H+ + S2- →; в) 2H+ + SO32- →. Составьте уравнения реакций в молекулярном виде. Вопрос № 6 Даны уравнения реакций: a) Zn+CL2 = ZNCl2; б) Zn+2HCl = ZnCl2 + h3↑ Проставьте над знаками соответствующих химических элементов степени их окисления и покажите переход электронов. →
- Вконтакте
5terka.com