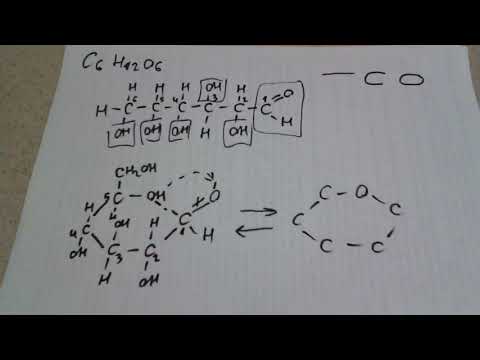
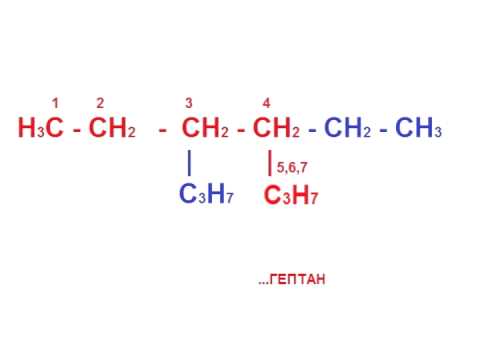
Необходимо выучить наизусть первые 10 представителей алкинов .Суффикс –ан в главной цепи меняется на –ин. Правила такие же, каку алкенов
Номенклатура органических соединений
№1 номенклатура предельных углеводородов
Необходимо сначала выучить наизусть первые 10 представителей алканов и некоторые их (алкильные) радикалы.
Алканы: (СnH2n+2)
СН4-метан С2Н6-этан С3Н8-пропан С4Н10-бутан
С5Н12-пентан С6Н14-гексан С7Н16-гептан С8Н18-октан
С9Н20-нонан С10Н22-декан
Радикалы:
СН3— метил С2Н5— этил СН3-CH 2-CH 2— пропилСН3-CH-CH 3 изопропил СН3-CH 2-CH 2-CH 2— бутил
СН3-CH-CH2-СH3 изобутил СН3-CH 2-CH 2-CH 2-СН2— амил
Правила номенклатуры:
1) выбираем самую длинную углеродную цепь в молекуле, пишем ее горизонтально. Это главная структура.
2) нумеруем атомы углерода в главной цепи. Начало нумерации там, где:
а) ближе «веточка»- радикал
б) больше радикалов
в) при одном атоме углерода 2 радикала(заместителя).В этом случае № атома «С» указываем дважды.
3) называем радикалы по старшинству, указывая перед ними № атома «С» в главной структуре(цепи).Старшинство радикалов — по алфавиту(чья начальная буква раньше, тот и старше).
4)
называем соответствующий углеводород главной цепи. Примеры:№1 изобутан СH3-CH-CH3
№2 изопентан
№3 неопентан
| |||||||||
Примечание: если в молекуле несколько одинаковых радикалов, то перечисляются все № атомов «С» с этими радикалами и соответствующие приставки:
2- ди, 3- три, 4- тетра, 5- пента, 6- гекса- и т.д.
№4
|
№5
5изопропил-2,4диметил-2этилгептан
№2 номенклатура алкенов ( углеводородов с 1 двойной связью)
Необходимо выучить наизусть первые 10 представителей алкенов .Суффикс –ан в главной цепи меняется на –ен(-илен). Правила такие же, как у алканов, только нумеруют главную цепь с того места, где ближе двойнаясвязь и в конце названия указывают № атома»С» , при котором двойная связь.
Алкены: (СnH2n) С2Н4-этен С3Н6-пропен С4Н8-бутен
С5Н10-пентен С6Н12-гексен С7Н14-гептен С8Н16-октен
С9Н18-нонен С10Н20-децен .
№1
бутен-1
№2
бутен-2
№3
2этилбутен-2
№4
4,6диметил-3,5диэтилгептен-1
№3 номенклатура алкинов ( углеводородов с 1 тройной связью)
Необходимо выучить наизусть первые 10 представителей алкинов .Суффикс –ан в главной цепи меняется на –ин. Правила такие же, каку алкенов.
Алкины: (СnH2n-2) С2Н2-этин(ацетилен) С3Н4-пропин С4Н6-бутин С5Н8-пентин С6Н10-гексин С7Н12-гептин С8Н14-октин С9Н16-нонин С10Н18-децин .
№1
3метилпентин-1
№2
5метил-4этилгексин-2
Правила номенклатуры как у алкенов, лишь перед –ен ставим префикс ди-. В конце главной цепи указываются № атомов «С», где имеются двойные связи.
Диены: (СnH2n-2)
№1
3метил-4,6диэтилгептадиен-1,6
№2
4изопропил-3метил-6этилгептадиен-1,6
№5 номенклатура циклоалканов
Здесь родоначальной структурой является цикл. В случае разветвленных циклоалканов атом «С» №1 тот, при котором есть радикал или старший радикал. Если радикалов несколько, то нумерация атомов углерода в цикле идет в том направлении, где радикалы друг к другу ближе.
Циклоалканы: (СnH2n)
циклопропан циклобутан
циклопентан циклогексан циклооктан №1
метилциклобутан №2
1,3диметилциклогексан
№3
1метил3этилциклогексан
№5 номенклатура аренов
Родоначальная структура-бензол. Правила похожи на номенклатуру циклоалканов, а можно еще по-другому указать ориентацию заместителей в бензольном кольце.
орто-положение мета-положение пара-положение
1,2-положение 1,3-положение 1,4-положение
№1
1,4диметилбензол
(парадиметилбензол)
№2
1,2диметил-3этилбензол
№3
1метил-2пропил-5этилбензол
№6 номенклатура спиртов
Спирты содержат 1 или несколько функциональных групп ОН-. Родоначальная структура – соответствующий углеводород ( предельный, непредельный, циклический, ароматический)+ суффикс ОЛ-. Если спирт многоатомный, то перед ол- указываем соответствующее числительное и № атомов «С», где есть ОН- группы. Нумерация углеводородной цепи с того места, где ближе ОН- группа.
Одноатомные предельные спирты
№1
Бутанол-1
№2
Бутанол-2
№3
4этилпентанол-2
№4
2метил-4этилпентанол-3
|
Одноатомные непредельные спирты
№1
пентен-4-ол-2
№2
3метилгексен-4-ол-2
Одноатомные циклические спирты
№1
циклобутанол
№2
3метилциклогексанол
Одноатомные ароматические спирты
У ароматических спиртов гидроксогруппа не соединена непосредственно с бензольным кольцом. Простейший из таких спиртов – бензиловый спирт.
Примеры:
А)
2,3-диметилбензиловый спирт
Б) 2-метил-3этилбензиловый спирт
Многоатомные предельные спирты
Примеры:
А)
Бутандиол-2,3 (молекула симметрична, Þ нумеруем цепь с любого конца).
Б)
4-метил-5 -пропилгептантриол-2,3,6
Молекула несимметрична, нумеруем цепь с того места, где больше ОН- групп, так как в номенклатуре они старше углеводородных радикалов.
№7 номенклатура фенолов
Фенолы ( гидроксибензолы) – соединения, где гидроксогруппа непосредственно соединена с бензольным кольцом. Простейший представитель- моногидроксибензол или просто фенол.
Примеры:
А) Б)
фенол
ортодигидроксибензол
В)
метадигидроксибензол
Г)
2,4-диметилдигидроксибензол-1,3
Нумерация атомов в кольце ведется со старшей ОН- группы и в том направлении, где больше заместителей и радикалов ( в данном случае по часовой стрелке).
Д)
3-изопропил-2,4-диметилфенол
№8 номенклатура альдегидов
Альдегиды имеют на конце цепи функциональную альдегидную группу (она состоит из карбонильной группы и атома водорода).
По составу углеводородного остатка альдегиды бывают предельные, непредельные, циклические, ароматические. Родовой суффикс — аль.
Предельные альдегиды.
Примеры:
А)
бутаналь
б)
3-метилбутаналь
в)
3-метил-4-этил-пентаналь
Урок 18. Алканы – HIMI4KA

Понятие об алканах
Алканы — это углеводороды незамкнутого (нециклического) строения, в молекулах которых атомы углерода соединены только простыми связями. Например:


Задание 18.1. Допишите атомы водорода и попробуйте ответить на вопрос: существует ли углеводород, имеющий большее число атомов водорода в молекуле?
Поэтому-то алканы обычно называют предельными углеводородами, то есть содержащими максимально возможное (предельное) число атомов водорода в молекуле.


Гомологический ряд, номенклатура, изомерия
Алканы образуют гомологический ряд с общей формулой
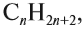
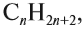
где n — число атомов углерода в молекуле. Если
- n = 1 → СН4, это метан;
- n = 2 → С2Н6, это этан;
- n = 3 → С3Н8, или СН3–СН2–СН3, это пропан.
Начиная с n = 4 для алканов возможна изомерия, то есть для вещества состава C4H10 существуют два соединения различного строения, а значит, различные по свойствам:


Следующий гомолог с n = 5 имеет уже три изомера, один из них н-пентан, то есть пентан нормального (неразветвлённого) строения.
Задание 18.2. Составьте графические формулы всех изомеров пентана (их три). Назовите эти изомеры.


Строение молекул
Атомы углерода и водорода в молекулах алканов соединены только простыми связями. Это ковалентные, слабо полярные связи.
Все С–Н связи в молекуле метана равноценны и направлены в пространстве к вершинам тетраэдра. Это σ-связи (сигма-связи), очень прочные. Поэтому метан и другие алканы с трудом вступают в химические реакции (на разрыв σ-связей нужно затратить много энергии). Все химические реакции алканов идут в особых условиях (нагревание, присутствие катализатора, освещение и др.), то есть при обычных условиях реакции алканов невозможны.


Свойства алканов
Физические свойства
Поскольку все связи в молекулах алканов слабо полярны, то в молекулах отсутствуют какие-либо значительные заряды. Поэтому молекулы алканов слабо притягиваются друг к другу. В результате все алканы — это либо газы, либо летучие жидкости, либо твёрдые легкоплавкие вещества (табл. 8).


Смесь газообразных углеводородов образует природный газ. Начиная с n = 16, алканы являются твёрдыми веществами. Очищенные твёрдые предельные углеводороды называют парафином.
Неполярные углеводороды практически нерастворимы в полярном растворителе, например в воде, но прекрасно растворяются в неполярных растворителях. Таким растворителем является смесь жидких алканов (бензин, керосин). Природная смесь твёрдых, жидких и газообразных углеводородов называется нефтью. Нефть в основном состоит из алканов и циклоалканов. При переработке нефти получают: попутный нефтяной газ, смесь жидких алканов (бензин, керосин), твёрдых алканов (асфальт, парафин) и другие нефтепродукты. Такой способ переработки нефти называется нефтеперегонкой и осуществляется при её нагревании в специальных ректификационных колоннах.
Задание 18.3. Бензин представляет собой смесь алканов с числом атомов углерода от 5 до 9. Составьте их молекулярные формулы.
Химические свойства
Алканы, в принципе, не способны к реакциям присоединения, так как имеют максимально возможное число атомов водорода. Поэтому их называют насыщенными углеводородами.
Для алканов наиболее характерна реакция замещения. В результате такой реакции происходит замещение одного атома водорода алкана на новую группу или на атом (на каждой стадии). Характер химической связи при этом не изменяется.
К таким реакциям относятся:
- Реакция хлорирования, которая происходит под действием солнечного света:
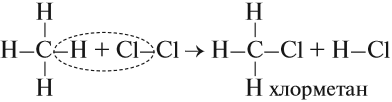
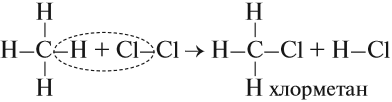
- Реакция нитрования, которая происходит при нагревании:


Обратите внимание: молекулу азотной кислоты в органических реакциях рекомендуется записывать как НО–NO2, так как в результате реакций с ней в молекуле исходного вещества появляется нитрогруппа –NО2.
Для алканов возможны реакции окисления. В растворе они не происходят. Но в присутствии катализаторов алканы окисляются до кислот:
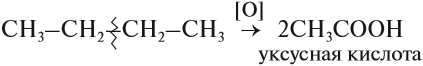
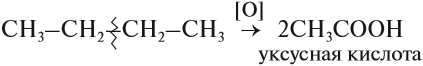
Обратите внимание! Знак [О] означает, что происходит неполное (мягкое) окисление. Окислителями могут быть разные вещества, не только кислород, например, перманганат калия KMnO4.
При полном окислении (горении) любой алкан (и любой углеводород!) превращается в углекислый газ и воду:


Газообразные алканы горят бесцветным пламенем, т. е. сгорают полностью! При этом выделяется много теплоты, поэтому алканы применяются в качестве топлива: природный газ, бензин, керосин, мазут и т. д.
Задание 18.4. Расставьте коэффициенты в уравнении реакции горения.
При нагревании до очень высоких температур в отсутствии кислорода происходит разрушение (крекинг) молекулы углеводорода:


При этом образуются и непредельные углеводороды.
Задание 18.5. Укажите формулы непредельных углеводородов.
Процессы крекинга используют при переработке нефти.
Задание 18.6. Напишите уравнения реакций:
- хлорирования этана;
- нитрования метана;
- горения пентана.


Получение и применение алканов
Алканы широко распространены в природе. Простейший алкан — метан — образуется в результате разложения без доступа воздуха остатков растительных и животных организмов, этот газ выделяется на болотах, поэтому он так и называется: «болотный газ». Метан накапливается в шахтах, где добывают каменный уголь, из-за этого на шахтах иногда бывают взрывы, так как смесь метана с воздухом взрывоопасна. Это следует учитывать и в быту, так как природный газ является источником тепла в газовых плитах. Метан составляет 95–97 % природного газа.
Алканы — ценное сырьё для получения смазочных масел, пластмасс, красок, стиральных порошков и т. д. Смеси алканов — бензин, керосин — топливо для автомобилей, тракторов, ракет, самолётов. Поэтому их получают в больших количествах в основном при переработке нефти и газа.
В лаборатории в небольших количествах алканы можно получить нагреванием соли карбоновой кислоты со щёлочью:


Внимание! Здесь и далее буквой R обозначается любой углеводородный радикал.
Так, метан получают нагреванием ацетата натрия в присутствии щёлочи:
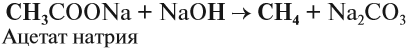
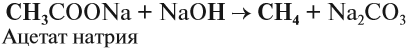
Метан можно получить гидролизом карбида алюминия (см. урок 13.1):


Кроме того, в лаборатории алканы получают синтезом Вюрца из галогенпроизводных под действием натрия:
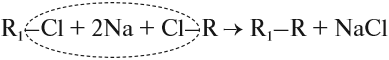
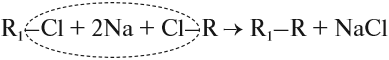
где R и R1 — предельные радикалы.


Выводы
Алканы — предельные, насыщенные углеводороды, в молекулах которых имеется максимально возможное (предельное) числа атомов углерода. Поэтому состав всех алканов СnH2n+2 и они не способны вступать в реакции присоединения. Все связи в молекулах алканов — неполярные, простые, очень прочные, поэтому алканы с трудом вступают в химические реакции. Это реакции замещения, крекинга, горения и каталитического окисления.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||