Хром — Вікіпедія
| Хром (Cr) | |
|---|---|
| Атомний номер | 24 |
| Зовнішній вигляд простої речовини | дуже твердий метал сірого кольору  |
| Властивості атома | |
| Атомна маса (молярна маса) | 51,9961 а.о.м. (г/моль) |
| Радіус атома | 130 пм |
| Енергія іонізації (перший електрон) | 652,4(6,76) кДж/моль (еВ) |
| Електронна конфігурація | [Cr] 3d5 4s1 |
| Хімічні властивості | |
| Ковалентний радіус | 118 пм |
| Радіус іона | (+6e)52 (+3e)63 пм |
| Електронегативність (за Полінгом) | 1,66 |
| Електродний потенціал | 0 |
| Ступені окиснення | 6, 3, 2, 0 |
| Термодинамічні властивості | |
| Густина | 7,18 г/см³ |
| Молярна теплоємність | 23,35 Дж/(К·моль) |
| Теплопровідність | 93,9 Вт/(м·К) |
| Температура плавлення | 2130 К |
| Теплота плавлення | 21 кДж/моль |
| Температура кипіння | 2945 К |
| Теплота випаровування | 342 кДж/моль |
| Молярний об’єм | 7,23 см³/моль |
| Кристалічна ґратка | |
| Структура ґратки | кубічна об’ємноцентрована |
| Період ґратки | 2,880 Å |
| Відношення с/а | n/a |
| Температура Дебая | 630[1] К |
| Хром у Вікісховищі? | |
Хром — хімічний елемент, із символом Cr і атомним номером 24, перший елемент шостої групи.
У 1766 році в околицях Єкатеринбурга був виявлений мінерал, який отримав назву «сибірський червоний свинець», PbCrO4. Сучасна назва — крокоїт. У 1797 французький хімік Л. Н. Воклен виділив з нього новий тугоплавкий метал (швидше за все Л. Н. Воклен отримав карбід хрому).
Назва походить від грец. χρωμα — колір, завдяки яскравій забарвленості його сполук.
Хром — це сталево-сірий, блискучий, твердий та крихкий метал[2], що має високу температуру плавлення. Назва елемента походить від грецького слова «chrōma» (χρώμα), що означає кольоровий[3], оскільки багато його сполук інтенсивно забарвлені.
Оксид хрому використовували китайці в династії Цінь ще 2000 років тому для покриття металевої зброї. Хром був виявлений як елемент після того, як у поле зору західного світу потрапив червоний кристалічний мінерал крокоїт (хромат свинцю (II) хромату), виявлений у 1761 році. Спочатку використовувався як пігмент. Луї Ніколя Воклен першим виділив металевий хром з мінералу в 1797 році.
Металічний хром та сплав ферохрому добувається з хромітів силікотермічною чи алюмінотермічною реакцію. Хром має високий корозійний опір і твердість. Його додають при виробництві нержавіючої сталі. Цей процес, разом з хромуванням, складають 85 % комерційного використання елемента.
Тривалентний іон Хрому, можливо, знаходиться у слідових кількостях в ліпідіах, хоча це питання залишається в дебатах[4]. У великих кількостях сполуки металу можуть бути токсичними та канцерогенними. Найвідомішим прикладом токсичної сполуки є шестивалентний хром (Cr(VI)).


Хром — 24-й елемент за поширеністю самих у земній корі із середньою концентрацію 100 частин на мільйон.[5] Сполуки хрому перебувають в навколишньому середовищі внаслідок ерозії хромсовмісних порід або вивержень вулканів. Діапазон концентрацій у ґрунті становить від 1 до 300 мг/кг, у морській воді від 5 до 800 мкг/л, у річках та озерах 26 мкг/літр до 5.2 мг/л.[6]
Метал видобувають з хроміту(FeCr2O4)[7]. Близько двох п’ятих хромітових руд і концентратів у світі виробляються в Південній Африці. Видобуванням хромітів також займається Казахстан, Індія, Росія і Туреччина. Нерозвинені родовища хромітів зосереджені в Казахстані та Південній Африці.[8]
Хоч і рідко, існують поклади самородного хрому[9]
У вільному вигляді хром — сірий метал з кубічною об’ємно-центрованою ґраткою, а = 0,28845 нм. Це єдина елементарна тверда сполука, яка виявляє антиферомагнітні властивості при кімнатній температурі (і нижче). При температурі вище 38 °C він перетворюється в парамагнетик.
Хром має твердість за шкалою Мооса 5[12], найтвердіший із чистих металів. Дуже чистий хром достатньо добре піддається механічній обробці.
Металічний хром на повітрі пасивує під дією кисню, утворюючи тонкий захисний шар поверхневого оксиду. Шар, що складається лише з кількох атомів завтовшки, є дуже щільним і, на відміну від заліза або нелегованої сталі, запобігає дифузії кисню в матеріал та виникненню іржі[13]. Пасивація може бути підвищена шляхом короткочасного контакту з такою кислотою-окисником як азотна. Протилежний ефект досягається при обробці сильним відновником, який руйнує захисний оксидний шар на металі. Хром, оброблений таким способом, легко розчиняється в навіть в слабких кислотах.
Природний хром складається з трьох стабільних ізотопів: 52Cr, 53Cr і 54Cr; 52 Cr є найбільш поширеним (83.789 %). Із 19 досліджених радіоізотопів найбільш стабільним є 50Cr з періодом напіврозпаду більше 1.8×1017 років, а для 51Cr період напіврозпаду становить 27,7 днів. Усі інші радіоактивні ізотопи мають періоди напіврозпаду менше 24 годин, більшість з них мають — менше 1 хвилини. Цей елемент також має 2 метастани.[14]
Всього відомо 25 ізотопів хрому з 42Cr по 67Cr.
Хром є елементом перехідних металів, перший елемент шостої групи. Хром (0) має електронну конфігурацію 4s13d5. Метал володіє широким спектром можливих окиснення, де +3 є найбільш енергетично стабільним, тому сполуки Хрому +3 і +6 більш характерні, у той час як +1, +4 і +5 — рідкісні.
| Ступені окиснення | |
|---|---|
| 0 | Cr(C6H6)2 |
| +1 | K3[Cr(CN)5NO] |
| +2 | CrCl2 |
| +3 | CrCl3 |
| +4 | K2CrF6 |
| +5 | K3CrO8 |
| +6 | K2CrO4 |
Нижче наведена Діаграма Пурбе для хрому в чистій воді, соляній кислоті або гідроксиді натрію:
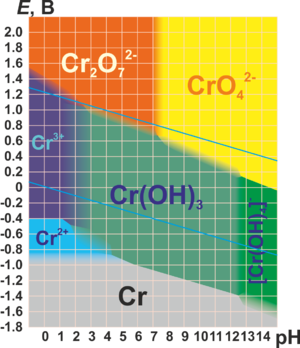
Проста речовина[ред. | ред. код]
Стійкий на повітрі за рахунок пасивації, не реагує з нітратною кислотою. З хлоридною кислотою в інертному середовищі взаємодіє, окиснюючись до двохвалентного хлориду. Реакція з концентрованою сульфатною кислотою протікає наступним чином:
- 2 Cr+6 h3SO4⟶{\displaystyle \mathrm {2\ Cr+6\ H_{2}SO_{4}\longrightarrow } } Cr2(SO4)3+2 SO2+6 h3O {\displaystyle \mathrm {\ Cr_{2}(SO_{4})_{3}+2\ SO_{2}+6\ H_{2}O\ } }
При 2000 ° C згоряє з утворенням зеленого оксиду хрому(III) Cr2O3, що володіє амфотерними властивостями. Синтезовано сполуки хрому з бором (бориди Cr2B, CrB, Cr3B4, CrB2, CrB4 та Cr5B3), з вуглецем (карбіди Cr23C6, Cr7C3 та Cr3C2), c кремнієм (силіциди Cr3Si, Cr5Si3 і CrSi) і азотом (нітриди CrN і Cr2N).
Сполуки Хрому (+2)[ред. | ред. код]
Ступені окиснення +2 відповідає основний оксид CrO чорного кольору. Солі Cr2+ (розчини блакитного кольору) утворюються при відновленні солей Cr
- 2Cr3+→Zn,HCl[H]2Cr2+{\displaystyle \mathrm {2Cr^{3+}{\xrightarrow[{Zn,HCl}]{[H]}}2Cr^{2+}} }
Солі Cr2+ — сильні відновники, при стоянні витісняють водень із води[15]. Киснем повітря, особливо в кислому середовищі, Cr2+ окиснюється, внаслідок чого блакитний розчин швидко зеленіє: 4 CrSO4+2 h3SO4+O2⟶{\displaystyle \mathrm {4\ CrSO_{4}+2\ H_{2}SO_{4}+O_{2}\longrightarrow } } Cr2(SO4)3+2 h3O {\displaystyle \mathrm {\ Cr_{2}(SO_{4})_{3}+2\ H_{2}O\ } }
Коричневий або жовтий гідроксид Cr(OH)2 осідає при додаванні лугів до розчинів солей хрому(II).
Синтезовано дигалогеніди CrF2, CrCl2, CrBr2 та CrI2.
Сполуки Хрому (+3)[ред. | ред. код]
Ступені окиснення +3 відповідає амфотерний оксид Cr2O3 та гідроксид Cr(OH)3 (обидва зеленого кольору). Це найбільш стійка ступінь окиснення для хрому. Його сполуки мають колір від брудно-лілового (іон [Cr(H2O) 6]3+) до зеленого (в координаційній сфері присутні аніони).
Cr3+ схильний до утворення подвійних сульфатів виду MICr(SO4) 2·12H2O (галунів)
Гідроксид хрому(III) отримують, діючи амоніаком на розчини солей хрому(III) :
- Cr3++3Nh4+3h3O→Cr(OH)3↓+3Nh5+{\displaystyle \mathrm {Cr^{3+}+3NH_{3}+3H_{2}O\rightarrow Cr(OH)_{3}\downarrow +3NH_{4}^{+}} }
Можна використовувати розчини лугів, але при їх надлишку утворюється розчинний гідроксокомплекс:
- Cr3++3OH−→Cr(OH)3↓{\displaystyle \mathrm {Cr^{3+}+3OH^{-}\rightarrow Cr(OH)_{3}\downarrow } }
- Cr(OH)3+3OH−→[Cr(OH)6]{\displaystyle \mathrm {Cr(OH)_{3}+3OH^{-}\rightarrow [Cr(OH)_{6}]} }
Сплавлені Cr2O3 з лугами отримують хроміти:
- Cr2O3+2NaOH→2NaCrO2+h3O{\displaystyle \mathrm {Cr_{2}O_{3}+2NaOH\rightarrow 2NaCrO_{2}+H_{2}O} }
Непрожарений оксид хрому(III) розчиняється в лужних розчинах і в кислотах:
- Cr2O3+6HCl→2CrCl3+3h3O{\displaystyle \mathrm {Cr_{2}O_{3}+6HCl\rightarrow 2CrCl_{3}+3H_{2}O} }
При окисненні сполук хрому(III) в лужному середовищі утворюються сполуки хрому(VI) :
- 2Na3[Cr(OH)6]+3h3O2→2Na2CrO4+2NaOH+8h3O{\displaystyle \mathrm {2Na_{3}[Cr(OH)_{6}]+3H_{2}O_{2}\rightarrow 2Na_{2}CrO_{4}+2NaOH+8H_{2}O} }
Те ж саме відбувається при сплавленні оксиду хрому(III) з лугом та окислювачами, або з лугом на повітрі (розплав при цьому набуває жовтого забарвлення):
- 2Cr2O3+8NaOH+3O2→4Na2CrO4+4h3O{\displaystyle \mathrm {2Cr_{2}O_{3}+8NaOH+3O_{2}\rightarrow 4Na_{2}CrO_{4}+4H_{2}O} }
Сполуки Хрому (+4)[ред. | ред. код]
При обережному розкладанні оксиду хрому(VI) CrO3 в гідротермальних умовах отримують хром(IV) оксид CrO2, який є феромагнетиком і має металеву провідність.
Серед тетрагалогенідів хрому стійким є флуорид CrF4, а тетрахлорид хрому CrCl4 існує лише в парах.
Сполуки Хрому (+6)[ред. | ред. код]
Ступені окислення +6 відповідає кислотний оксид хрому(VI) CrO3 та цілий ряд кислот, між якими існує рівновага. Найпростіші з них — хроматна H2CrO4 та дихроматна H2Cr2O7. Вони утворюють два ряди солей: жовті хромати та помаранчеві дихромати відповідно.
Оксид хрому(VI) CrO3 утворюється при взаємодії концентрованої сірчаної кислоти з розчинами дихроматів. Типовий кислотний оксид, при взаємодії з водою він утворює сильні нестійкі хромові кислоти: хромову H2CrO4, дихромову H2Cr2O7 та інші ізополікислоти із загальною формулою H2CrnO3n+1. Збільшення ступеня полімеризації відбувається зі зменшенням рН, тобто збільшенням кислотності:
- 2CrO42−+2H+→Cr2O72−+h3O{\displaystyle \mathrm {2CrO_{4}^{2-}+2H^{+}\rightarrow Cr_{2}O_{7}^{2-}+H_{2}O} }
Але якщо до помаранчевого розчину K2Cr2O7 прилити розчин лугу, забарвлення знову переходить в жовте, оскільки знову утворюється хромат K2CrO4:
- Cr2O72−+2OH−→2CrO42−+h3O{\displaystyle \mathrm {Cr_{2}O_{7}^{2-}+2OH^{-}\rightarrow 2CrO_{4}^{2-}+H_{2}O} }
До високого ступеня полімеризації, як це відбувається у вольфраму та молібдену, не доходить, оскільки поліхромова кислота розпадається на оксид хрому(VI) і воду:
- h3CrnO3n+1→h3O+nCrO3{\displaystyle \mathrm {H_{2}Cr_{n}O_{3n+1}\rightarrow H_{2}O+nCrO_{3}} }
Розчинність хроматів приблизно відповідає розчинності сульфатів. Зокрема, жовтий хромат барію BaCrO4 випадає при додаванні солей барію як до розчинів хроматів, так і до розчинів дихроматів:
- Ba2++CrO42−→BaCrO4↓{\displaystyle \mathrm {Ba^{2+}+CrO_{4}^{2-}\rightarrow BaCrO_{4}\downarrow } }
- 2Ba2++Cr2O72−+h3O→2BaCrO4↓+2H+{\displaystyle \mathrm {2Ba^{2+}+Cr_{2}O_{7}^{2-}+H_{2}O\rightarrow 2BaCrO_{4}\downarrow +2H^{+}} }
Відомі пентафлуорид хрому CrF5 та малостійкий гексафлуорид хрому CrF6. Також отримані леткі оксогалогеніди хрому CrO2F2 та CrO2Cl2.
Сполуки хрому(VI) — сильні окисники, наприклад:
- K2Cr2O7+14HCl→2CrCl3+2KCl+3Cl2↑+7h3O{\displaystyle \mathrm {K_{2}Cr_{2}O_{7}+14HCl\rightarrow 2CrCl_{3}+2KCl+3Cl_{2}\uparrow +7H_{2}O} }
Додавання до дихромату перекису водню, сірчаної кислоти та органічного розчинника (етеру) призводить до утворення синього пероксиду хрому CrO5L (L — молекула розчинника), який екстрагується в органічний шар; ця реакція використовується як аналітична.
- K2Cr2O7+4 h3O2+ h3SO4⟶{\displaystyle \mathrm {\ K_{2}Cr_{2}O_{7}+4\ H_{2}O_{2}+\ H_{2}SO_{4}\longrightarrow } } 2 CrO5⋅(C2H5)2O+ K2SO4+5 h3O{\displaystyle \mathrm {2\ CrO_{5}\cdot (C_{2}H_{5})_{2}O+\ K_{2}SO_{4}+5\ H_{2}O} }
 Злиток хрому добутий алюмотермічно
Злиток хрому добутий алюмотермічноХроміт заліза (хромистий залізняк) при 1200 °C перетворюють в хромат:
- 4 FeCr2O4+8 Na2CO3+7 O2⟶{\displaystyle \mathrm {4\ FeCr_{2}O_{4}+8\ Na_{2}CO_{3}+7\ O_{2}\longrightarrow } } 8 Na2CrO4+2 Fe2O3+8 CO2 {\displaystyle \mathrm {8\ Na_{2}CrO_{4}+2\ Fe_{2}O_{3}+8\ CO_{2}\ } }
Хромат розчиняють у воді і сірчаною кислотою переводять у дихромат:
- 2 Na2CrO4+h3SO4⟶{\displaystyle \mathrm {2\ Na_{2}CrO_{4}+H_{2}SO_{4}\longrightarrow } } Na2Cr2O7+Na2SO4+h3O {\displaystyle \mathrm {Na_{2}Cr_{2}O_{7}+Na_{2}SO_{4}+H_{2}O\ } }
Дихромат натрію кристалізується при охолоджені як дигідрат. При наступному відновленні вуглецем отримують Хром(III) оксид:
- Na2Cr2O7⋅2 h3O+2 C⟶{\displaystyle \mathrm {Na_{2}Cr_{2}O_{7}\cdot 2\ H_{2}O+2\ C\longrightarrow } } Cr2O3+Na2CO3+2 h3O+CO {\displaystyle \mathrm {Cr_{2}O_{3}+Na_{2}CO_{3}+2\ H_{2}O+CO\ } }
У кінцеві стадії відновлюють хром алюмотермічно:
- Cr2O3+2 Al⟶Al2O3+2 Cr {\displaystyle \mathrm {Cr_{2}O_{3}+2\ Al\longrightarrow Al_{2}O_{3}+2\ Cr\ } }
На початку ХIX ст. сполуки хрому використовувалися як вогнетривкий матеріал для фу
uk.wikipedia.org
хром — это… Что такое хром?
ХРОМ -а; м. [от греч. chrōma — цвет, краска]
1. Химический элемент (Сr), твёрдый металл серо-стального цвета (используется при изготовлении твёрдых сплавов и для покрытия металлических изделий).
2. Мягкая тонкая кожа, выдубленная солями этого металла. Сапоги из хрома.
◁ Хро́мовый (см.).
ХРОМ (лат. chromium, от греческого хрома — цвет, окраска, для соединений хрома характерна широкая цветовая палитра), Cr (читается «хром»), химический элемент с атомным номером 24, атомная масса 51,9961. Расположен в группе VIB в 4 периоде периодической системы элементов.Природный хром состоит из смеси четырех стабильных нуклидов: 50Cr (содержание в смеси 4,35%), 52Cr (83,79%), 53Cr (9,50%) и 54Cr (2,36%). Конфигурация двух внешних электронных слоев 3s2р6d54s1. Степени окисления от 0 до +6 , наиболее характерны +3 (самая устойчивая) и +6 (валентности III и VI).
Радиус нейтрального атома 0,127 нм, радиус ионов (координационное число 6): Cr2+ 0,073 нм, Cr3+ 0,0615 нм, Cr4+ 0,055 нм, Cr5+ 0,049 нм и Cr6+0,044 нм. Энергии последовательной ионизации 6,766, 16,49, 30,96, 49,1, 69,3 и 90,6 эВ. Сродство к электрону 1,6 эВ. Электроотрицательность по Полингу (см. ПОЛИНГ Лайнус) 1,66.
История открытия
В 1766 в окрестностях Екатеринбурга был обнаружен минерал, который получил название «сибирский красный свинец», PbCrO4. Современное название — крокоит. В 1797 французский химик Л. Н. Воклен (см. ВОКЛЕН Луи Никола) выделил из него новый тугоплавкий металл (скорее всего Воклен получил карбид хрома).
Нахождение в природе
Содержание в земной коре 0,035 % по массе. В морской воде содержание хрома 2·10-5 мг/л. В свободном виде хром практически не встречается. Входит в состав более 40 различных минералов (хромит FeCr2O4, волконскоит, уваровит, вокеленит и др.). Некоторые метеориты содержат сульфидные соединения хрома.
Получение
Промышленным сырьем при производстве хрома и сплавов на его основе служит хромит. Восстановительной плвкой хромита с коксом (восстановителем), железной рудой и другими компонентами получают феррохром с содержанием хрома до 80% (по массе).
Для получения чистого металлического хрома хромит с содой и известняком обжигают в печах:
2Cr2O3 + 2Na2CO3+ 3O2 = 4Na2CrO4 + 4CO2
Образующийся хромат натрия Na2CrO4 выщелачивают водой, раствор фильтруют, упаривают и обрабатывают кислотой. При этом хромат Na2CrO4 переходит в дихромат Na2Cr2O7:
2Na2CrO4 + H2SO4 = Na2Cr2O7 + Na2SO4 + H2O
Полученный дихромат восстанавливают серой:
Na2Cr2O7 + 3S = Na2S + Cr2O3 + 2SO2,
Образующийся чистый оксид хрома(III) Cr2O3 подвергают алюминотермии:
Cr2O3 + 2Al = Al2O3 + 2Cr.
Также используют кремний:
2Cr2O3 + 3Si = 3SiO2 + 4Cr
Для получения хрома высокой чистоты, технический хром электрохимически очищают от примесей.
Физические и химические свойства
В свободном виде — голубовато-белый металл с кубической объемно-центрированной решеткой, а = 0,28845 нм. При температуре 39°C переходит из парамагнитного состояния в антиферромагнитное (точка Нееля). Температура плавления 1890°C, температура кипения 2680°C. Плотность 7,19 кг/дм3.
Устойчив на воздухе. При 300°C сгорает с образованием зеленого оксида хрома (III) Cr2O3, обладающего амфотерными свойствами. Сплавляя Cr2O3 со щелочами получают хромиты:
Cr2O3 + 2NaOH = 2NaCrO2 + H2O
Непрокаленный оксид хрома (III) легко растворяется в щелочных растворах и в кислотах:
Cr2O3 + 6НСl = 2CrСl3 + 3Н2О
При термическом разложении карбонила хрома Cr(OH)6 получают красный основной оксид хрома(II) CrO. Коричневый или желтый гидроксид Cr(OН)2 со слабоосновными свойствами осаждается при добавлении щелочей к растворам солей хрома(II).
При осторожном разложении оксида хрома(VI) CrO3 в гидротермальных условиях получают диоксид хрома(IV) CrO2, который является ферромагнетиком и обладает металлической проводимостью.
При взаимодействии концентрированной серной кислоты с растворами дихроматов образуются красные или фиолетово-красные кристаллы оксида хрома(VI) CrO3. Типично кислотный оксид, при взаимодействии с водой он образует сильные неустойчивые хромовые кислоты: хромовая H2CrO4, дихромовая H2Cr2O7 и другие.
Известны галогениды, соответствующие разным степеням окисления хрома. Синтезированы дигалогениды хрома CrF2, CrCl2, CrBr2 и СrI2 и тригалогениды CrF3, CrCl3, CrBr3 и СrI3. Однако, в отличие от аналогичных соединений алюминия и железа, трихлорид CrCl3 и трибромид CrBr3 хрома нелетучи.
Среди тетрагалогенидов хрома устойчив CrF4, тетрахлорид хрома CrCl4 существует только в парах. Известен гексафторид хрома CrF6.
Получены и охарактеризованы оксигалогениды хрома CrO2F2 и CrO2Cl2.
Синтезированы соединения хрома с бором (бориды Cr2B, CrB, Cr3B4, CrB2, CrB4 и Cr5B3), с углеродом (карбиды Cr23C6, Cr7C3 и Cr3C2), c кремнием (силициды Cr3Si, Cr5Si3 и CrSi) и азотом (нитриды CrN и Cr2N).
В растворах наиболее устойчивы соединения хрома(III). В этой степени окисления хрому соответствуют как катионная форма, так и анионные формы, например, существующий в щелочной среде анион [Cr(OH)6]3-.
При окислении соединений хрома(III) в щелочной среде образуются соединения хрома(VI):
2Na3[Cr(OH)6] + 3H2O2 = 2Na2CrO4+ 2NaOH + 8H2O
Cr (VI) отвечает ряд существующих только в водных растворах кислот: хромовая H2CrO4, дихромовая H2Cr2O7, трихромовая H3Cr3O10 и другие, которые образуют соли — хроматы, дихроматы, трихроматы и т. д.
В зависимости от кислотности среды анионы этих кислот легко превращаются друг в друга. Например, при подкислении желтого раствора хромата калия K2CrO4 образуется оранжевый дихромат калия K2Cr2O7:
2K2CrO4 + 2НСl = K2Cr2O 7 + 2КСl + Н2О
Но если к оранжевому раствору K2Cr2O7 прилить раствор щелочи, как окраска вновь переходит в желтую т. к. снова образуется хромат калия K2CrO4:
K2Cr2O7 + 2КОН = 2K2CrO4 + Н2О
При добавлении к желтому раствору, содержащему хромат-ионы, раствора соли бария выпадает желтый осадок хромата бария BаCrO4:
Bа2+ + CrO42- = BаCrO4
Соединения хрома(III)— сильные окислители, например:
K2Cr2O7 + 14 НСl = 2CrCl3+ 2KCl + 3Cl2 + 7H2O
Применение
Использование хрома основано на его жаропрочности, твердости и устойчивости к коррозии. Применяют для получения сплавов: нержавеющей стали, нихрома и др. Большое количество хрома идет на декоративные коррозионно-стойкие покрытия. Соединения хрома — огнеупорные материалы. Оксид хрома (III) — пигмент зеленой краски, также входит в состав абразивных материалов (паст ГОИ). Изменение окраски при восстановлении соединений хрома(VI) применяют для проведения экспресс-анализа на содержание алкоголя в выдыхаемом воздухе.
Физиологическое действие
Хром — один из биогенных элементов, постоянно входит в состав тканей растений и животных. У животных хром участвует в обмене липидов, белков (входит в состав фермента трипсина), углеводов. Снижение содержания хромма в пище и крови приводит к уменьшению скорости роста, увеличению холестерина в крови.
Металлический хром практически нетоксичен, но металлическая пыль хрома раздражает ткани легких. Соединения хрома(III) вызывают дерматиты. Соединения хрома(VI) приводят к разным заболеваниям человека, в том числе и онкологическим. ПДК хрома(VI) в атмосферном воздухе 0,0015 мг/м3.
dic.academic.ru
Характеристика и качества хрома
Хром (Cr), химический элемент VI группы периодической системы Менделеева. Относится к переходным металлом с атомным номером 24 и атомной массой 51,996. В переводе с греческого, название металла означает «цвет». Такому названию металл обязан разнообразной цветовой гамме, которая присуща его различным соединениям.
Физические характеристики хрома
Металл обладает достаточной твердостью и хрупкостью одновременно. По шкале Мооса твердость хрома оценивается в 5,5. Этот показатель означает, что хром имеет максимальную твердость из всех известных на сегодня металлов, после урана, иридия, вольфрама и бериллия. Для простого вещества хрома характерен голубовато-белый окрас.
| Атомный номер | 24 |
| Атомная масса | 51,996 |
| Плотность, кг/м³ | 7190 |
| Температура плавления, °С | 1856 |
| Теплоемкость, кДж/(кг·°С) | 0,46 |
| Электроотрицательность | 1,6 |
| Ковалентный радиус, Å | 1,18 |
| 1-й ионизац. потенциал, эв | 6,76 |
Металл не относится к редким элементам. Его концентрация в земной коре достигает 0,02% масс. долей. В чистом виде хром не встречается никогда. Он содержится в минералах и рудах, которые являются главным источником добычи металла. Хромит (хромистый железняк, FeO*Cr2O3) считается основным соединением хрома. Еще одним достаточно распространенным, однако менее важным минералом, является крокоит PbCrO4.
Металл легко поддается плавке при температуре 19070С (21800К или 34650F). При температуре в 26720С – закипает. Атомная масса металла составляет 51,996 г/моль.
Хром является уникальным металлом благодаря своим магнитным свойствам. В условиях комнатной температуры ему присуще антиферромагнитное упорядочение, в то время, как другие металлы обладают им в условиях исключительно пониженных температур. Однако, если хром нагреть выше 370С, физические свойства хрома изменяются. Так, существенно меняется электросопротивление и коэффициент линейного расширения, модуль упругости достигает минимального значения, а внутреннее трение значительно увеличивается. Такое явление связано с прохождением точки Нееля, при которой антиферромагнитные свойства материала способны изменяться на парамагнитные. Это означает, что первый уровень пройден, и вещество резко увеличилось в объеме.
Строение хрома представляет собой объемно-центрированную решетку, благодаря которой металл характеризуется температурой хрупко-вязкого периода. Однако, в случае с данным металлом, огромное значение имеет степень чистоты, поэтому, величина находится в пределах -500С — +3500С. Как показывает практика, раскристаллизированный металл не имеет никакой пластичности, но мягкий отжиг и формовка делают его ковким.
Химические свойства хрома
Атом имеет следующую внешнюю конфигурацию: 3d54s1. Как правило, в соединениях хром имеет следующие степени окисления: +2, +3, +6, среди которых наибольшую устойчивость проявляет Сr3+.Кроме этого существуют и другие соединения, в которых хром проявляет совершенно иную степень окисления, а именно: +1, +4, +5.
Металл не отличается особой химической активностью. Во время нахождения хрома в обычных условиях, металл проявляет устойчивость к влаге и кислороду. Однако, данная характеристика не относится к соединению хрома и фтора – CrF3, которое при воздействии температур, превышающих 6000С, взаимодействует с парами воды, образуя в результате реакции Сr2О3, а также азотом, углеродом и серой.
Во время нагревания металлического хрома, он взаимодействует с галогенами, серой, кремнием, бором, углеродом, а также некоторыми другими элементами, в результате чего получаются следующие химические реакции хрома:
Cr + 2F2 = CrF4 (с примесью CrF5)
2Cr + 3Cl2 = 2CrCl3
2Cr + 3S = Cr2S3
Хроматы можно получить, если нагреть хром с расплавленной содой на воздухе, нитратами или хлоратами щелочных металлов:
2Cr + 2Na2CO3 + 3O2 = 2Na2CrO4 + 2CO2.
Хром не обладает токсичностью, чего нельзя сказать о некоторых его соединениях. Как известно, пыль данного металла, при попадании в организм, может раздражать легкие, через кожу она не усваивается. Но, поскольку в чистом виде он не встречается, то его попадание в человеческий организм является невозможным.
Трехвалентный хром попадает в окружающую среду во время добычи и переработки хромовой руды. В человеческий организм попадание хрома вероятно в виде пищевой добавки, используемой в программах по похудению. Хром с валентностью, равной +3, является активным участником синтеза глюкозы. Ученые установили, что излишнее употребление хрома особого вреда человеческому организму не наносит, поскольку не происходит его всасывание, однако, он способен накапливаться в организме.
Соединения, в котором участвует шестивалентный металл, являются крайне токсичными. Вероятность их попадания в человеческий организм появляется во время производства хроматов, хромирования предметов, во время проведения некоторых сварочных работ. Попадание такого хрома в организм чревато серьезными последствиями, так как соединения, в которых присутствует шестивалентный элемент, представляют собой сильные окислители. Поэтому, могут вызвать кровотечение в желудке и кишечнике, иногда с прободением кишечника. При попадании таких соединений на кожу возникают сильные химические реакции в виде ожогов, воспалений, возникновения язв.
В зависимости от качества хрома, которое необходимо получить на выходе, существует несколько способов производства металла: электролизом концентрированных водных растворов оксида хрома, электролизом сульфатов, а также восстановлением оксидом кремния. Однако, последний способ не очень популярен, так как при нем на выходе получается хром с огромным количеством примесей. Кроме того, он также является экономически невыгодным.
| Степень окисления | Оксид | Гидроксид | Характер | Преобладающие формы в растворах | Примечания |
| +2 | CrO (чёрный) | Cr(OH)2 (желтый) | Основный | Cr2+ (соли голубого цвета) | Очень сильный восстановитель |
|
+3 |
Cr2O3 (зелёный) | Cr(OH)3 (серо-зеленый) | Амфотерный |
Cr3+ (зеленые или лиловые соли) |
|
| +4 | CrO2 | не существует | Несолеобразующий | — |
Встречается редко, малохарактерна |
| +6 | CrO3 (красный) |
h3CrO4 |
Кислотный |
CrO42- (хроматы, желтые) |
Переход зависит от рН среды. Сильнейший окислитель, гигроскопичен, очень ядовит. |
mining-prom.ru
Хром — это… Что такое Хром?
| Внешний вид простого вещества | |
|---|---|
 Твёрдый металл голубовато-белого цвета | |
| Свойства атома | |
| Имя, символ, номер | Хром / Chromium (Cr), 24 |
| Атомная масса (молярная масса) | 51,9961 а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d5 4s1 |
| Радиус атома | 130 пм |
| Химические свойства | |
| Ковалентный радиус | 118 пм |
| Радиус иона | (+6e)52 (+3e)63 пм |
| Электроотрицательность | 1,66 (шкала Полинга) |
| Электродный потенциал | -0.74 |
| Степени окисления | 6, 3, 2, 0 |
| Энергия ионизации (первый электрон) | 652,4 (6,76) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 7,19 г/см³ |
| Температура плавления | 2130 K |
| Температура кипения | 2945 K |
| Теплота плавления | 21 кДж/моль |
| Теплота испарения | 342 кДж/моль |
| Молярная теплоёмкость | 23,3[1] Дж/(K·моль) |
| Молярный объём | 7,23 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая |
| Параметры решётки | 2,885 Å |
| Температура Дебая | 460 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 93,9 Вт/(м·К) |
Хром — элемент побочной подгруппы шестой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 24. Обозначается символом Cr (лат. Chromium). Простое вещество хром (CAS-номер: 7440-47-3) — твёрдый металл голубовато-белого цвета.
История
В 1766 году в окрестностях Екатеринбурга был обнаружен минерал, который получил название «сибирский красный свинец», PbCrO4. Современное название — крокоит. В 1797 французский химик Л. Н. Воклен выделил из него новый тугоплавкий металл (скорее всего Воклен получил карбид хрома).
Происхождение названия
Название элемент получил от греч. χρῶμα — цвет, краска — из-за разнообразия окраски своих соединений.
Нахождение в природе
Хром является довольно распространённым элементом (0,02 масс. долей, %). Основные соединения хрома — хромистый железняк (хромит) FeO·Cr2O3. Вторым по значимости минералом является крокоит PbCrO4.
Месторождения
Самые большие месторождения хрома находятся в ЮАР (1 место в мире), Казахстане, России, Зимбабве, Мадагаскаре. Также есть месторождения на территории Турции, Индии, Армении[2], Бразилии, на Филиппинах[3].
Главные месторождения хромовых руд в РФ известны на Урале (Донские и Сарановское).
Разведанные запасы в Казахстане составляют свыше 350 миллионов тонн (2 место в мире)[3].
Геохимия и минералогия
Среднее содержание хрома в различных изверженных породах резко непостоянно. В ультраосновных породах (перидотитах) оно достигает 2 кг/т, в основных породах (базальтах и др.) — 200 г/т, а в гранитах десятки г/т. Кларк хрома в земной коре 83 г/т. Он является типичным литофильным элементом и почти весь заключен в минералах типа хромшпинелидов. Хром вместе с железом, титаном, никелем, ванадием и марганцем составляют одно геохимическое семейство.
Различают три основных минерала хрома: магнохромит (Mn, Fe)Cr2O4, хромпикотит (Mg, Fe)(Cr, Al)2O4 и алюмохромит (Fe, Mg)(Cr, Al)2O4. По внешнему виду они неразличимы и их неточно называют «хромиты». Состав их изменчив:
- Cr2O3 18—62 %,
- FeO 1—18 %,
- MgO 5—16 %,
- Al2O3 0,2 — 0,4 (до 33 %),
- Fe2O3 2 — 30 %,
- примеси TiO2 до 2 %,
- ZnO до 5 %,
- MnO до 1 %; присутствуют также Co, Ni и др.
Собственно хромит, то есть FeCr2O4 сравнительно редок. Помимо различных хромитов, хром входит в состав ряда других минералов — хромовой слюды (фуксита), хромового хлорита, хромвезувиана, хромдиопсида, хромтурмалина, хромового граната (уваровита) и др., которые нередко сопровождают руды, но сами промышленного значения не имеют. В экзогенных условиях хром, как и железо, мигрирует в виде взвесей и может накапливаться в глинах. Наиболее подвижной формой являются хроматы.
Получение
Хром встречается в природе в основном в виде хромистого железняка Fe(CrO2)2 (хромит железа). Из него получают феррохром восстановлением в электропечах коксом (углеродом):
Феррохром применяют для производства легированных сталей.
Чтобы получить чистый хром, реакцию ведут следующим образом:
1) сплавляют хромит железа с карбонатом натрия (кальцинированная сода) на воздухе:
2) растворяют хромат натрия и отделяют его от оксида железа;
3) переводят хромат в дихромат, подкисляя раствор и выкристаллизовывая дихромат;
4) получают чистый оксид хрома восстановлением дихромата натрия углём:
5) с помощью алюминотермии получают металлический хром:
6) с помощью электролиза получают электролитический хром из раствора хромового ангидрида в воде, содержащего добавку серной кислоты. При этом на катодах совершаются в основном 3 процесса:
- восстановление шестивалентного хрома до трехвалентного с переходом его в раствор;
- разряд ионов водорода с выделением газообразного водорода;
- разряд ионов, содержащих шестивалентный хром, с осаждением металлического хрома;
Физические свойства
В свободном виде — голубовато-белый металл с кубической объемно-центрированной решеткой, а = 0,28845 нм. При температуре 39 °C переходит из парамагнитного состояния в антиферромагнитное (точка Нееля).
Хром имеет твердость по шкале Мооса 5.[4] Очень чистый хром достаточно хорошо поддаётся механической обработке.
Химические свойства
Характерные степени окисления
Для хрома характерны степени окисления +2, +3 и +6. (см. табл.) Практически все соединения хрома окрашены[5].
| Степень окисления | Оксид | Гидроксид | Характер | Преобладающие формы в растворах | Примечания |
|---|---|---|---|---|---|
| +2 | CrO (чёрный) | Не существует | Основный | Cr2+ (соли голубого цвета) | Очень сильный восстановитель |
| +3 | Cr2O3(зелёный) | Cr(OH)3 | Амфотерный | Cr3+ (зеленые или лиловые соли) [Cr(OH)4]— (зелёный) | |
| +4 | CrO2 | не существует | Несолеобразующий | — | Встречается редко, малохарактерна |
| +6 | CrO3(красный) | H2CrO4 H2Cr2O7 | Кислотный | CrO42- (хроматы, желтые) Cr2O72- (дихроматы, оранжевые) | Переход зависит от рН среды. Сильнейший окислитель, гигроскопичен, очень ядовит. |
Простое вещество
Устойчив на воздухе за счёт пассивирования. По этой же причине не реагирует с серной и азотной кислотами. При 2000 °C сгорает с образованием зелёного оксида хрома(III) Cr2O3, обладающего амфотерными свойствами.
Синтезированы соединения хрома с бором (бориды Cr2B, CrB, Cr3B4, CrB2, CrB4 и Cr5B3), с углеродом (карбиды Cr23C6, Cr7C3 и Cr3C2), c кремнием (силициды Cr3Si, Cr5Si3 и CrSi) и азотом (нитриды CrN и Cr2N).
Соединения Cr(+2)
Степени окисления +2 соответствует основный оксид CrO (чёрный). Соли Cr2+ (растворы голубого цвета) получаются при восстановлении солей Cr3+ или дихроматов цинком в кислой среде («водородом в момент выделения»):
Все эти соли Cr2+ — сильные восстановители вплоть до того, что при стоянии вытесняют водород из воды[6]. Кислородом воздуха, особенно в кислой среде, Cr2+ окисляется, в результате чего голубой раствор быстро зеленеет.
Коричневый или желтый гидроксид Cr(OH)2 осаждается при добавлении щелочей к растворам солей хрома(II).
Синтезированы дигалогениды хрома CrF2, CrCl2, CrBr2 и CrI2
Соединения Cr(+3)
Степени окисления +3 соответствует амфотерный оксид Cr2O3 и гидроксид Cr(OH)3 (оба — зелёного цвета). Это — наиболее устойчивая степень окисления хрома. Соединения хрома в этой степени окисления имеют цвет от грязно-лилового (ион [Cr(H2O)6]3+ до зелёного (в координационной сфере присутствуют анионы).
Cr3+ склонен к образованию двойных сульфатов вида MICr(SO4)2·12H2O (квасцов)
Гидроксид хрома (III) получают, действуя аммиаком на растворы солей хрома (III):
Можно использовать растворы щелочей, но в их избытке образуется растворимый гидроксокомплекс:
Сплавляя Cr2O3 со щелочами получают хромиты:
Непрокаленный оксид хрома(III) растворяется в щелочных растворах и в кислотах:
При окислении соединений хрома(III) в щелочной среде образуются соединения хрома(VI):
То же самое происходит при сплавлении оксида хрома (III) со щелочью и окислителями, или со щелочью на воздухе (рассплав при этом приобретает жёлтую окраску):
Соединения хрома (+4)
При осторожном разложении оксида хрома(VI) CrO3 в гидротермальных условиях получают оксид хрома(IV) CrO2, который является ферромагнетиком и обладает металлической проводимостью.
Среди тетрагалогенидов хрома устойчив CrF4, тетрахлорид хрома CrCl4 существует только в парах.
Соединения хрома (+6)
Степени окисления +6 соответствует кислотный оксид хрома (VI) CrO3 и целый ряд кислот, между которыми существует равновесие. Простейшие из них — хромовая H2CrO4 и двухромовая H2Cr2O7. Они образуют два ряда солей: желтые хроматы и оранжевые дихроматы соответственно.
Оксид хрома (VI) CrO3 образуется при взаимодействии концентрированной серной кислоты с растворами дихроматов. Типичный кислотный оксид, при взаимодействии с водой он образует сильные неустойчивые хромовые кислоты: хромовую H2CrO4, хромат K2CrO4:
До высокой степени полимеризации, как это происходит у вольфрама и молибдена, не доходит, так как полихромовая кислота распадается на оксид хрома(VI) и воду:
Растворимость хроматов примерно соответствует растворимости сульфатов. В частности, желтый хромат бария BaCrO4 выпадает при добавлении солей бария как к растворам хроматов, так и к растворам дихроматов:
Образование кроваво-красного малорастворимого хромата серебра используют для обнаружения серебра в сплавах при помощи пробирной кислоты.
Известны пентафторид хрома CrF5 и малоустойчивый гексафторид хрома CrF6. Также получены летучие оксигалогениды хрома CrO2F2 и CrO2Cl2 (хромилхлорид).
Соединения хрома(VI) — сильные окислители, например:
Добавление к дихроматам перекиси водорода, серной кислоты и органического растворителя (эфира) приводит к образованию синего пероксида хрома CrO5L (L — молекула растворителя), который экстрагируется в органический слой; данная реакция используется как аналитическая.
Применение
Хром — важный компонент во многих легированных сталях (в частности, нержавеющих), а также и в ряде других сплавов. Используется в качестве износоустойчивых и красивых гальванических покрытий (хромирование). Хром применяется для производства сплавов: хром-30 и хром-90, незаменимых для производства сопел мощных плазмотронов и в авиакосмической промышленности.
Биологическая роль и физиологическое действие
Хром — один из биогенных элементов, постоянно входит в состав тканей растений и животных. У животных хром участвует в обмене липидов, белков (входит в состав фермента трипсина), углеводов. Снижение содержания хрома в пище и крови приводит к уменьшению скорости роста, увеличению холестерина в крови.
В чистом виде хром довольно токсичен, металлическая пыль хрома раздражает ткани лёгких. Соединения хрома(III) вызывают дерматиты. Соединения хрома(VI) приводят к разным заболеваниям человека, в том числе и онкологическим. ПДК хрома(VI) в атмосферном воздухе 0,0015 мг/м³.
Интересные факты
- Основанный на реальных событиях фильм «Эрин Брокович» режиссёра Стивена Содерберга рассказывает о крупном судебном процессе, связанном с загрязнением окружающей среды шестивалентным хромом, в результате которого у многих людей развились серьёзные заболевания.[7]
См. также
Примечания
Ссылки
 Электрохимический ряд активности металлов Электрохимический ряд активности металлов | |
|---|---|
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na, Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu, Th, Np, U, Hf, Be, Al, Ti, Zr, Yb, Mn, V, Nb, Pa, Cr, Zn, Ga, Fe, Cd, In, Tl, Co, Ni, Te, Mo, Sn, Pb, H2, W, Sb, Bi, Ge, Re, Cu, Tc, Te, Rh, Po, Hg, Ag, Pd, Os, Ir, Pt, Au |
academic.ru
описание, свойства, формула и характеристика
Хром – химический элемент с атомным номером 24. Это твердый, блестящий, серо-стального цвета металл, который хорошо полируется и не тускнеет. Используется в сплавах, таких как нержавеющая сталь, и в качестве покрытия. Организму человека требуются небольшие количества трехвалентного хрома для метаболизма сахара, но Cr (VI) очень токсичен.
Различные соединения хрома, такие как окись хрома (III) и хромат свинца, ярко окрашены и используются в красках и пигментах. Красный цвет рубина обусловлен наличием этого химического элемента. Некоторые вещества, особенно бихромат калия и натрия, являются окислителями, используемыми для окисления органических соединений и (вместе с серной кислотой) для очистки лабораторной посуды. Кроме того, окись хрома (VI) применяется в производстве магнитной ленты.

Открытие и этимология
История открытия химического элемента хром такова. В 1761 году Иоганн Готлоб Леман нашел в Уральских горах оранжево-красный минерал и назвал его «сибирским красным свинцом». Хотя он ошибочно был идентифицирован как соединение свинца с селеном и железом, материал на самом деле являлся хроматом свинца с химической формулой PbCrO4. Сегодня он известен как минерал кроконт.
В 1770 году Петр Симон Паллас посетил то место, где Леман нашел красный свинцовый минерал, который имел очень полезные свойства пигмента в красках. Использование сибирского красного свинца в качестве краски получило быстрое развитие. Кроме того, ярко-желтый цвет из кроконта стал модным.
В 1797 году Николя-Луи Воклен получил образцы красной свинцовой руды. Путем смешивания кроконта с соляной кислотой он получил оксид CrO3. Хром как химический элемент был выделен в 1798 году. Воклен получил его при нагревании окисла с древесным углем. Он также смог обнаружить следы хрома в драгоценных камнях, таких как рубин и изумруд.
В 1800-х годах Cr в основном применялся в составе красок и кожевенных солей. Сегодня 85% металла используется в сплавах. Остальная часть применяется в химической промышленности, производстве огнеупорных материалов и литейной промышленности.
Произношение химического элемента хром соответствует греческому χρῶμα, что означает «цвет», из-за множества цветных соединений, которые из него можно получить.

Добыча и производство
Элемент производят из хромита (FeCr2O4). Примерно половина этой руды в мире добывается в Южной Африке. Кроме того, Казахстан, Индия и Турция являются его крупными производителями. Разведанных месторождений хромита достаточно, но географически они сконцентрированы в Казахстане и на юге Африки.
Залежи самородного металлического хрома встречаются редко, но они есть. Например, его добывают на шахте «Удачная» в России. Она является кимберлитовой трубкой, богатой алмазами, и восстановительная среда помогла образоваться чистому хрому и алмазам.
Для промышленного производства металла хромитовые руды обрабатывают расплавленной щелочью (едким натром, NaOH). При этом образуется хромат натрия (Na2CrO4), который восстанавливается углеродом до оксида Сг2O3. Металл получают при нагревании окисла в присутствии алюминия или кремния.
В 2000 году было добыто около 15 млн т хромитовой руды, которая была переработана в 4 млн т феррохрома, на 70% состоящего из сплава хрома с железом, приблизительная рыночная стоимость которых составила 2,5 млрд долларов США.

Основные характеристики
Характеристика химического элемента хрома обусловлена тем, что он является переходным металлом четвертого периода таблицы Менделеева и расположен между ванадием и марганцем. Входит в VI группу. Плавится при температуре 1907 °С. В присутствии кислорода хром быстро образует тонкий слой оксида, который защищает металл от дальнейшего взаимодействия с кислородом.
Как переходный элемент, он реагирует с веществами в различных соотношениях. Таким образом он образует соединения, в которых имеет различные степени окисления. Хром – химический элемент с основными состояниями +2, +3 и +6, из которых +3 является наиболее устойчивым. Кроме того, в редких случаях наблюдаются состояния +1, +4 и +5. Соединения хрома в степени окисления +6 представляют собой сильные окислители.
Какого цвета хром? Химический элемент придает анодированному алюминию рубиновый оттенок. Сг2O3, используемый для полировки металла, также применяется в качестве пигмента под названием «хромовая зелень». Его соли окрашивают стекло в изумрудно-зеленый цвет. Хром – химический элемент, присутствие которого делает рубин красным. Поэтому он используется в производстве синтетических рубинов.

Изотопы
Изотопы хрома обладают атомным весом от 43 до 67. Обычно данный химический элемент состоит из трех стабильных форм: 52Cr, 53Cr и 54Cr. Из них наиболее распространен 52Cr (83,8% всего природного хрома). Кроме того, описаны 19 радиоизотопов, из которых наиболее стабильным является 50Cr с периодом полураспада, превышающим 1,8×1017 лет. У 51Cr период полураспада – 27,7 дней, а у всех остальных радиоактивных изотопов он не превышает 24 ч, причем у большинства из них он длится менее одной минуты. Элемент также имеет два метасостояния.
Изотопы хрома в земной коре, как правило, сопутствуют изотопам марганца, что находит применение в геологии. 53Cr образуется при радиоактивном распаде 53Mn. Соотношение изотопов Mn/Cr подкрепляет другие сведения о ранней истории Солнечной системы. Изменения в соотношениях 53Cr/52Cr и Mn/Cr из разных метеоритов доказывает то, что новых атомные ядра были созданы непосредственно перед формированием Солнечной системы.

Химический элемент хром: свойства, формула соединений
Оксид хрома (III) Сг2O3, также известный как полуторная окись, является одним из четырех окислов этого химического элемента. Его получают из хромита. Соединение зеленого цвета обычно называют «хромовой зеленью», когда используют в качестве пигмента для живописи по эмали и стеклу. Оксид может растворяться в кислотах, образуя соли, а в расплавленной щелочи – хромиты.
Бихромат калия
K2Cr2O7 является мощным окислителем и ему отдается предпочтение в качестве средства для очистки лабораторной посуды от органики. Для этого используется его насыщенный раствор в концентрированной серной кислоте. Иногда, однако, его заменяют бихроматом натрия, исходя из более высокой растворимости последнего. Кроме того, он может регулировать процесс окисления органических соединений, преобразуя первичный спирт в альдегид, а затем в углекислоту.
Бихромат калия способен вызвать хромовый дерматит. Хром, вероятно, является причиной сенсибилизации, ведущей к развитию дерматита, особенно рук и предплечий, который носит хронический характер и трудно излечим. Как и другие соединения Cr (VI), бихромат калия канцерогенен. С ним нужно обращаться в перчатках и соответствующими средствами защиты.

Хромовая кислота
Соединение обладает гипотетической структурой H2CrO4. Ни хромовая, ни дихромовая кислоты не встречаются в природе, но их анионы находят в различных веществах. «Хромовая кислота», которую можно встретить в продаже, на самом деле является ее кислотным ангидридом – триоксидом CrO3.
Хромат свинца (II)
PbCrO4 обладает ярко-желтой окраской и практически не растворим в воде. По этой причине он нашел применение в качестве красящего пигмента под названием «желтый крон».
Cr и пятивалентная связь
Хром отличается своей способностью образовывать пятивалентные связи. Соединение создается Cr (I) и углеводородным радикалом. Пятивалентная связь формируется между двумя атомами хрома. Его формула может быть записана как Ar–Cr–Cr–Ar, где Ar представляет собой специфическую ароматическую группу.

Применение
Хром – химический элемент, свойства которого обеспечили ему множество различных вариантов применения, некоторые из которых приведены ниже.
Металлам он придает устойчивость к коррозии и глянцевую поверхность. Поэтому хром входит в состав таких сплавов, как нержавеющая сталь, используемых, например, в столовых приборах. Он также применяется для нанесения хромированного покрытия.
Хром является катализатором различных реакций. Из него делают формы для обжига кирпича. Его солями дубят кожу. Бихромат калия применяют для окисления органических соединений, таких как спирты и альдегиды, а также для очистки лабораторной посуды. Он служит фиксирующим агентом для окрашивания ткани, а также используется в фотографии и фотопечати.
CrO3 применяется для изготовления магнитных лент (например, для аудиозаписи), которые обладают лучшими характеристиками, чем пленки с оксидом железа.
Роль в биологии
Трехвалентный хром – химический элемент, необходимый для метаболизма сахара в организме человека. Напротив, шестивалентный Cr очень токсичен.
Меры предосторожности
Металлический хром и соединения Cr (III), как правило, не считаются опасными для здоровья, но вещества, содержащие Cr (VI), могут быть токсичными, если их принимать внутрь или вдыхать. Большинство таких веществ оказывают раздражающее действие на глаза, кожу и слизистые оболочки. При постоянном воздействии соединения хрома (VI) могут вызвать повреждение глаз, если их не лечить должным образом. Кроме того, это признанный канцероген. Смертельная доза данного химического элемента – около половины чайной ложки. Согласно рекомендациям Всемирной организации здравоохранения, предельно допустимая концентрация Cr (VI) в питьевой воде составляет 0,05 мг на литр.
Так как соединения хрома используются в красителях и для дубления кожи, они часто встречаются в почве и грунтовых водах заброшенных промышленных объектов, требующих экологической очистки и восстановления. Грунтовка, содержащая Cr (VI), до сих пор широко применяется в аэрокосмической промышленности и автомобилестроении.
Свойства элемента
Основные физические свойства хрома следующие:
- Атомное число: 24.
- Атомный вес: 51,996.
- Температура плавления: 1890 °C.
- Температура кипения: 2482 °C.
- Степень окисления: +2, +3, +6.
- Конфигурация электронов: [Ar]3d54s1.
fb.ru
Свойства и применения хрома
Подробности- Подробности
- Опубликовано 14.09.2016 12:14
- Просмотров: 21005
Хром, переходный метал, который широко используется в промышленности благодаря своей прочности и устойчивости к нагреву и коррозии. Эта статья даст вам понимание некоторых важных свойств и возможностей использования этого переходного металла.
Хром относится к категории переходных металлов. Это твердый, но хрупкий металл серо-стального цвета с атомным номером 24. Этот блестящий металл помещают в группы 6 периодической таблицы, и обозначают символом «Cr».
Имя хромий является производным от греческого слова хрома, что означает цвет.
Верный своему имени, хром образует несколько интенсивно окрашенных соединений. Сегодня практически весь коммерчески используемый хром извлекается из руды хромита железа или окиси хрома (FeCr2O4).
Свойства хрома
- Хром является наиболее распространенным элементом на земной коре, но он никогда не происходит в чистом виде. В основном добывается из шахт, таких как хромитовые рудники.
- Расплавляют хром при температуре 2180 K или 3465°F, а температура кипения составляет 2944 K или 4840°F. его атомный вес 51.996 г/моль, и по шкале Мооса составляет 5,5.
- Хром встречается во многих окислительных состояниях, таких как +1, +2, +3, +4, +5, и +6, из которых +2, +3 и +6 являются наиболее распространенными, а +1, +4, А +5-это редкое окисление. В +3 степени окисления является наиболее стабильным состоянием хрома. Хром (III) может быть получен растворением элементарного хрома в соляной или серной кислоте.
- Этот металлический элемент известен своими уникальными магнитными свойствами. При комнатной температуре, он обладает антиферромагнитным упорядочением, которое показано на других металлах при относительно низких температурах.
- Антиферромагнетизм — это где соседние ионы, которые ведут себя как магниты присоединяются к противоположным или антипараллельным механизмам через материал. В результате, магнитное поле, создаваемое магнитными атомами или ионами, ориентируются в одном направлении отменяя магнитные атомы или ионы, выстроенные в противоположном направлении, так, что материал не проявляет никаких грубых внешних магнитных полей.
- При температуре выше 38°C, хром становится парамагнетиком, т. е. его привлекает внешне приложенное магнитное поле. Другими словами, хром привлекает внешнее магнитное поле при температуре выше 38°С.
- Хром не подвергается водородному охрупчиванию, т. е. не становятся хрупкими при воздействии атомарного водорода. Но при воздействии азота, он теряет свою пластичность и становится хрупким.
- Хром обладает высокой устойчивостью к коррозии. Тонкая защитная оксидная пленка образуется на поверхности металла, когда он вступает в контакт с кислородом в воздухе. Этот слой препятствует диффузии кислорода в основной материал и таким образом, защищает его от дальнейшей коррозии. Этот процесс называется пассивация, пассивация хромом дает устойчивость к воздействию кислот.
- Существует три основных изотопа хрома, которые называются 52Cr, 53Cr, 54Cr и, из которых 52 CR является наиболее распространенным изотопом. Хром реагирует с большинством кислот, но не взаимодействует с водой. При комнатной температуре он реагирует с кислородом, образуя оксид хрома.
Применение
Производство нержавеющей стали
Хром нашел широкий спектр применения благодаря своей твердости и устойчивости к коррозии. Он используется в основном в трех отраслях промышленности ― металлургической, химической и огнеупорной. Он широко используется для производства нержавеющей стали, так как это предотвращает коррозию. Сегодня это очень важный легирующий материал для сталей. Он также используется для изготовления нихрена, что используется в нагревательных элементах сопротивления из-за его способности выдерживать высокие температуры.
Покрытие поверхностей
Кислый хромат или дихромат используется также для покрытия поверхностей. Обычно это делается с помощью метода гальваники, в котором тонкий слой хрома наносится на металлическую поверхность. Другой способ — это хромирование деталей, через который хроматы используются для нанесения защитного слоя на определенные металлы, такие как алюминий (Al), кадмий (CD), цинк (Zn), серебро, а также магний (MG).
Сохранение древесины и дубление кож
Соли хрома (VI) являются токсичными, поэтому они используются для сохранения древесины от повреждения и разрушения грибком, насекомыми и термитами. Хром (III), особенно хромовые квасцы или сульфат калия используется в кожевенной промышленности, так как он помогает стабилизировать кожу.
Красители и пигменты
Хром также используется для изготовления пигментов или красителей. Желтый хром и хромат свинца, широко использовались в качестве пигмента в прошлом. Из-за экологических проблем, его использование существенно снизилось, а затем, наконец, его заменили свинец и хромовые пигменты. Другие пигменты на основе хрома, красного хрома, оксида зеленого хрома, которые является смесью желтой и Берлинской лазури. Окись хрома используется для придания зеленоватого цвета стекла.
Синтез искусственных рубинов
Изумруды обязаны своим зеленым оттенком хрому. Окись хрома применяется также для производства синтетических рубинов. Естественные рубины корунды или кристаллы оксида алюминия, которые обретают красный оттенок из-за присутствия хрома. Синтетические или искусственные рубины сделаны легированием хрома (III) на синтетических кристаллах корунда.
Биологические функции
Хрома (III) или трехвалентный хром, необходим в организме человека, но в очень небольших количествах. Это, как полагают, играет важную роль в липиде и метаболизме сахара. В настоящее время он используется во многих диетических добавках, которые как утверждают, имеют несколько преимуществ для здоровья, однако, это является спорным вопросом. Биологическая роль хрома не была должным образом проверена, и многие эксперты считают, что это не важно для млекопитающих, в то время как другие рассматривают его как важнейший микроэлемент для человека.
Другое использование
Высокая температура плавления и теплостойкость сделать хром идеальным огнеупорным материалом. Он нашел себе применение в доменных печах, цементных печах, и металлических. Многие соединения хрома применяются в качестве катализаторов для переработки углеводородов. Хром (IV) используется, чтобы произвести магнитные ленты, используемые в аудио и видеокассетах.
Шестивалентный хром или хром (VI) называется токсическим и мутагенным веществом, а хром (IV) является известным своими канцерогенными свойствами. Хромат соли также вызывает аллергические реакции у некоторых людей. Благодаря заботе о здравоохранении и экологическим проблемам, некоторые ограничения были наложены на использование соединений хрома в различных частях мира.
Читайте также
Добавить комментарий
electrowelder.ru
Хром — Википедия
| Внешний вид простого вещества | |
|---|---|
| Твёрдый металл голубовато-белого цвета | |
| Свойства атома | |
| Название, символ, номер | Хром / Chromium (Cr), 24 |
| Атомная масса (молярная масса) | 51,9961(6)[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d5 4s1 |
| Радиус атома | 130 пм |
| Химические свойства | |
| Ковалентный радиус | 118 пм |
| Радиус иона | (+6e)52 (+3e)63 пм |
| Электроотрицательность | 1,66 (шкала Полинга) |
| Электродный потенциал | −0,74 |
| Степени окисления | 6, 3, 2, 0 |
| Энергия ионизации (первый электрон) | 652,4 (6,76) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 7,19 г/см³ |
| Температура плавления | 2130 K |
| Температура кипения | 2945 K |
| Уд. теплота плавления | 21 кДж/моль |
| Уд. теплота испарения | 342 кДж/моль |
| Молярная теплоёмкость | 23,3[2] Дж/(K·моль) |
| Молярный объём | 7,23 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объёмноцентрированая |
| Параметры решётки | 2,885 Å |
| Температура Дебая | 460 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 93,9 Вт/(м·К) |
| Номер CAS | 7440-47-3 |
Хром — элемент побочной подгруппы 6-й группы 4-го периода периодической системы химических элементов Д. И. Менделеева с атомным номером 24. Обозначается символом Cr (лат. Chromium). Простое вещество хром — твёрдый металл голубовато-белого цвета. Хром иногда относят к чёрным металлам.
История
Происхождение названия
Название элемент получил от греч. χρῶμα — цвет, краска — из-за разнообразия окраски своих соединений.
История
Открыт на Среднем Урале, в Березовском золоторудном месторождении. Впервые упоминается в труде М. В. Ломоносова «Первые основания металлургии» (1763 год), как красная свинцовая руда, PbCrO4. Современное название — крокоит. В 1797 году французский химик Л. Н. Воклен выделил из него новый тугоплавкий металл (скорее всего, Воклен получил карбид хрома).
Нахождение в природе
Хром является довольно распространённым элементом в земной коре (0,012 % по массе)[3]. Основные соединения хрома — хромистый железняк (хромит) FeO·Cr2O3. Вторым по значимости минералом является крокоит PbCrO4.
Месторождения
Самые большие месторождения хрома находятся в ЮАР (1-е место в мире), Казахстане, России, Зимбабве, Мадагаскаре. Также есть месторождения на территории Турции, Индии, Армении[4], Бразилии, на Филиппинах[5].
Главные месторождения хромовых руд в РФ известны на Урале (Донские и Сарановское).
Разведанные запасы в Казахстане составляют свыше 350 миллионов тонн (2-е место в мире)[5].
Геохимия и минералогия
Среднее содержание хрома в различных изверженных породах резко непостоянно. В ультраосновных породах (перидотитах) оно достигает 2 кг/т, в основных породах (базальтах и др.) — 200 г/т, а в гранитах десятки г/т. Кларк хрома в земной коре 83 г/т. Он является типичным литофильным элементом и почти весь заключен в минералах типа хромшпинелидов. Хром вместе с железом, титаном, никелем, ванадием и марганцем составляют одно геохимическое семейство.
Различают три основных минерала хрома: магнохромит (Mg, Fe)Cr2O4, хромпикотит (Mg, Fe)(Cr, Al)2O4 и алюмохромит (Fe, Mg)(Cr, Al)2O4. По внешнему виду они неразличимы, и их неточно называют «хромиты». Состав их изменчив:
- Cr2O3 18—62 %,
- FeO 1—18 %,
- MgO 5—16 %,
- Al2O3 0,2 — 0,4 (до 33 %),
- Fe2O3 2 — 30 %,
- примеси TiO2 до 2 %,
- V2O5 до 0,2 %,
- ZnO до 5 %,
- MnO до 1 %; присутствуют также Co, Ni и др.
Собственно, хромит, то есть FeCr2O4 сравнительно редок. Помимо различных хромитов, хром входит в состав ряда других минералов — хромовой слюды (фуксита), хромового хлорита, хромвезувиана, хромдиопсида, хромтурмалина, хромового граната (уваровита) и др., которые нередко сопровождают руды, но сами промышленного значения не имеют. В экзогенных условиях хром, как и железо, мигрирует в виде взвесей и может накапливаться в глинах. Наиболее подвижной формой являются хроматы.
Получение
Хром встречается в природе в основном в виде хромистого железняка Fe(CrO2)2 (хромит железа). Из него получают феррохром восстановлением в электропечах коксом (углеродом):
- Fe(CrO2)2+4C→Fe+2Cr+4CO{\displaystyle {\mathsf {Fe(CrO_{2})_{2}+4C\rightarrow Fe+2Cr+4CO}}}
Феррохром применяют для производства легированных сталей.
Чтобы получить чистый хром, реакцию ведут следующим образом:
1) сплавляют хромит железа с карбонатом натрия (кальцинированная сода) на воздухе:
- 4Fe(CrO2)2+8Na2CO3+7O2→8Na2CrO4+2Fe2O3+8CO2{\displaystyle {\mathsf {4Fe(CrO_{2})_{2}+8Na_{2}CO_{3}+7O_{2}\rightarrow 8Na_{2}CrO_{4}+2Fe_{2}O_{3}+8CO_{2}}}}
2) растворяют хромат натрия и отделяют его от оксида железа;
3) переводят хромат в дихромат, подкисляя раствор и выкристаллизовывая дихромат;
4) получают чистый оксид хрома восстановлением дихромата натрия углём:
- Na2Cr2O7+2C→Cr2O3+Na2CO3+CO{\displaystyle {\mathsf {Na_{2}Cr_{2}O_{7}+2C\rightarrow Cr_{2}O_{3}+Na_{2}CO_{3}+CO}}}
5) с помощью алюминотермии получают металлический хром:
- Cr2O3+2Al→Al2O3+2Cr+130kcal{\displaystyle {\mathsf {Cr_{2}O_{3}+2Al\rightarrow Al_{2}O_{3}+2Cr+130kcal}}}
6) с помощью электролиза получают электролитический хром из раствора хромового ангидрида в воде, содержащего добавку серной кислоты. При этом на катодах совершаются в основном 3 процесса:
- восстановление шестивалентного хрома до трехвалентного с переходом его в раствор;
- разряд ионов водорода с выделением газообразного водорода;
- разряд ионов, содержащих шестивалентный хром, с осаждением металлического хрома;
- Cr2O72−+14H++12e−→2Cr+7h3O{\displaystyle {\mathsf {Cr_{2}O_{7}^{2-}+14H^{+}+12e^{-}\rightarrow 2Cr+7H_{2}O}}}
Физические свойства
В свободном виде — голубовато-белый металл с кубической объёмноцентрированной решёткой, a = 0,28845 нм. Ниже температуры 38 °C является антиферромагнетиком, выше переходит в парамагнитное состояние (точка Нееля).
Хром имеет твёрдость по шкале Мооса 5[6], один из самых твёрдых чистых металлов (уступает только иридию, бериллию, вольфраму и урану). Очень чистый хром достаточно хорошо поддаётся механической обработке.
Химические свойства
Характерные степени окисления
Для хрома характерны степени окисления +2, +3 и +6 (см. табл.). Практически все соединения хрома окрашены[7].
| Степень окисления | Оксид | Гидроксид | Характер | Преобладающие формы в растворах | Примечания |
|---|---|---|---|---|---|
| +2 | CrO (чёрный) | Cr(OH)2 (жёлтый) | Основный | Cr2+ (соли голубого цвета) | Очень сильный восстановитель |
| +3 | Cr2O3 (зелёный) | Cr(OH)3 (серо-зелёный) | Амфотерный | Cr3+ (зелёные или лиловые соли) [Cr(OH)4]− (зелёный) | |
| +4 | CrO2 | не существует | Несолеобразующий | — | Встречается редко, малохарактерна |
| +6 | CrO3 (красный) | H2CrO4 H2Cr2O7 | Кислотный | CrO42− (хроматы, желтые) Cr2O72− (дихроматы, оранжевые) | Переход зависит от рН среды. Сильнейший окислитель, гигроскопичен, очень ядовит. |
Простое вещество
Устойчив на воздухе за счёт пассивирования. По этой же причине не реагирует с серной и азотной кислотами. При 2000 °C сгорает с образованием зелёного оксида хрома(III) Cr2O3, обладающего амфотерными свойствами.
Синтезированы соединения хрома с бором (бориды Cr2B, CrB, Cr3B4, CrB2, CrB4 и Cr5B3), с углеродом (карбиды Cr23C6, Cr7C3 и Cr3C2), c кремнием (силициды Cr3Si, Cr5Si3 и CrSi) и азотом (нитриды CrN и Cr2N).
Соединения Cr(+2)
Степени окисления +2 соответствует основный оксид CrO (чёрный). Соли Cr2+ (растворы голубого цвета) получаются при восстановлении солей Cr3+ или дихроматов цинком в кислой среде («водородом в момент выделения»):
- 2Cr3+→Zn,HCl[H]2Cr2+{\displaystyle {\mathsf {2Cr^{3+}{\xrightarrow[{Zn,HCl}]{[H]}}2Cr^{2+}}}}
Все эти соли Cr2+ — сильные восстановители вплоть до того, что при стоянии вытесняют водород из воды[8]. Кислородом воздуха, особенно в кислой среде, Cr2+ окисляется, в результате чего голубой раствор быстро зеленеет.
Коричневый или жёлтый гидроксид Cr(OH)2 осаждается при добавлении щелочей к растворам солей хрома(II).
Синтезированы дигалогениды хрома CrF2, CrCl2, CrBr2 и CrI2
Соединения Cr(+3)
Степени окисления +3 соответствует амфотерный оксид Cr2O3 и гидроксид Cr(OH)3 (оба — зелёного цвета). Это — наиболее устойчивая степень окисления хрома. Соединения хрома в этой степени окисления имеют цвет от грязно-лилового (в водных растворах ион Cr3+ существует в виде аквакомплексов [Cr(H2O)6]3+) до зелёного (в координационной сфере присутствуют анионы).
Cr3+ склонен к образованию двойных сульфатов вида MICr(SO4)2·12H2O (квасцов)
Гидроксид хрома (III) получают, действуя аммиаком на растворы солей хрома (III):
- Cr3++3Nh4+3h3O→Cr(OH)3↓+3Nh5+{\displaystyle {\mathsf {Cr^{3+}+3NH_{3}+3H_{2}O\rightarrow Cr(OH)_{3}\downarrow +3NH_{4}^{+}}}}
Можно использовать растворы щелочей, но в их избытке образуется растворимый гидроксокомплекс:
- Cr3++3OH−→Cr(OH)3↓{\displaystyle {\mathsf {Cr^{3+}+3OH^{-}\rightarrow Cr(OH)_{3}\downarrow }}}
- Cr(OH)3+3OH−→[Cr(OH)6]3−{\displaystyle {\mathsf {Cr(OH)_{3}+3OH^{-}\rightarrow [Cr(OH)_{6}]^{3-}}}}
Сплавляя Cr2O3 со щелочами, получают хромиты:
- Cr2O3+2NaOH→2NaCrO2+h3O{\displaystyle {\mathsf {Cr_{2}O_{3}+2NaOH\rightarrow 2NaCrO_{2}+H_{2}O}}}
Непрокаленный оксид хрома(III) растворяется в щелочных растворах и в кислотах:
- Cr2O3+6HCl→2CrCl3+3h3O{\displaystyle {\mathsf {Cr_{2}O_{3}+6HCl\rightarrow 2CrCl_{3}+3H_{2}O}}}
При окислении соединений хрома(III) в щелочной среде образуются соединения хрома(VI):
- 2Na3[Cr(OH)6]+3h3O2→2Na2CrO4+2NaOH+8h3O{\displaystyle {\mathsf {2Na_{3}[Cr(OH)_{6}]+3H_{2}O_{2}\rightarrow 2Na_{2}CrO_{4}+2NaOH+8H_{2}O}}}
То же самое происходит при сплавлении оксида хрома (III) со щелочью и окислителями, или со щелочью на воздухе (расплав при этом приобретает жёлтую окраску):
- 2Cr2O3+8NaOH+3O2→4Na2CrO4+4h3O{\displaystyle {\mathsf {2Cr_{2}O_{3}+8NaOH+3O_{2}\rightarrow 4Na_{2}CrO_{4}+4H_{2}O}}}
Соединения хрома (+4)
При осторожном разложении оксида хрома(VI) CrO3 в гидротермальных условиях получают оксид хрома(IV) CrO2, который является ферромагнетиком и обладает металлической проводимостью.
Среди тетрагалогенидов хрома устойчив CrF4, тетрахлорид хрома CrCl4 существует только в парах.
Соединения хрома (+6)
Степени окисления +6 соответствует кислотный оксид хрома (VI) CrO3 и целый ряд кислот, между которыми существует равновесие. Простейшие из них — хромовая H2CrO4 и двухромовая H2Cr2O7. Они образуют два ряда солей: желтые хроматы и оранжевые дихроматы соответственно.
Оксид хрома (VI) CrO3 образуется при взаимодействии концентрированной серной кислоты с растворами дихроматов. Типичный кислотный оксид, при взаимодействии с водой он образует сильные неустойчивые хромовые кислоты: хромовую H2CrO4, дихромовую H2Cr2O7 и другие изополикислоты с общей формулой H2CrnO3n+1. Увеличение степени полимеризации происходит с уменьшением рН, то есть увеличением кислотности:
- 2CrO42−+2H+→Cr2O72−+h3O{\displaystyle {\mathsf {2CrO_{4}^{2-}+2H^{+}\rightarrow Cr_{2}O_{7}^{2-}+H_{2}O}}}
Но если к оранжевому раствору K2Cr2O7 прилить раствор щёлочи, как окраска вновь переходит в жёлтую, так как снова образуется хромат K2CrO4:
- Cr2O72−+2OH−→2CrO42−+h3O{\displaystyle {\mathsf {Cr_{2}O_{7}^{2-}+2OH^{-}\rightarrow 2CrO_{4}^{2-}+H_{2}O}}}
До высокой степени полимеризации, как это происходит у вольфрама и молибдена, не доходит, так как полихромовая кислота распадается на оксид хрома(VI) и воду:
- h3CrnO3n+1→h3O+nCrO3{\displaystyle {\mathsf {H_{2}Cr_{n}O_{3n+1}\rightarrow H_{2}O+nCrO_{3}}}}
Растворимость хроматов примерно соответствует растворимости сульфатов. В частности, жёлтый хромат бария BaCrO4 выпадает при добавлении солей бария как к растворам хроматов, так и к растворам дихроматов:
- Ba2++CrO42−→BaCrO4↓{\displaystyle {\mathsf {Ba^{2+}+CrO_{4}^{2-}\rightarrow BaCrO_{4}\downarrow }}}
- 2Ba2++Cr2O72−+h3O→2BaCrO4↓+2H+{\displaystyle {\mathsf {2Ba^{2+}+Cr_{2}O_{7}^{2-}+H_{2}O\rightarrow 2BaCrO_{4}\downarrow +2H^{+}}}}
Образование кроваво-красного малорастворимого хромата серебра используют для обнаружения серебра в сплавах при помощи пробирной кислоты.
Известны пентафторид хрома CrF5 и малоустойчивый гексафторид хрома CrF6. Также получены летучие оксигалогениды хрома CrO2F2 и CrO2Cl2 (хромилхлорид).
Соединения хрома(VI) — сильные окислители, например:
- K2Cr2O7+14HCl→2CrCl3+2KCl+3Cl2↑+7h3O{\displaystyle {\mathsf {K_{2}Cr_{2}O_{7}+14HCl\rightarrow 2CrCl_{3}+2KCl+3Cl_{2}\uparrow +7H_{2}O}}}
Добавление к дихроматам перекиси водорода, серной кислоты и органического растворителя (эфира) приводит к образованию синего монопероксида хрома(VI) CrO5 (CrO(O2)2), который экстрагируется в органический слой; данная реакция используется как аналитическая.
Применение
Хром — важный компонент во многих легированных сталях (в частности, нержавеющих), а также и в ряде других сплавов. Добавка хрома существенно повышает твердость и коррозийную стойкость сплавов.
Используется в качестве износоустойчивых и красивых гальванических покрытий (хромирование).
Хром применяется для производства сплавов: хром-30 и хром-90, незаменимых для производства сопел мощных плазмотронов и в авиакосмической промышленности.
Биологическая роль и физиологическое действие
Хром — один из биогенных элементов, постоянно входит в состав тканей растений и животных. У животных хром участвует в обмене липидов, белков (входит в состав фермента трипсина), углеводов. Снижение содержания хрома в пище и крови приводит к уменьшению скорости роста, увеличению холестерина в крови.
В чистом виде хром довольно токсичен[9], металлическая пыль хрома раздражает ткани лёгких. Соединения хрома(III) вызывают дерматиты.
Соединения хрома в степени окисления +6 особо токсичны. Практически вся хромовая руда обрабатывается через преобразование в дихромат натрия. В 1985 году было произведено примерно 136 000 тонн шестивалентного хрома.[10] Другими источниками шестивалентного хрома являются триоксид хрома и различные соли — хроматы и дихроматы. Шестивалентный хром используется при производстве нержавеющих сталей, текстильных красок, консервантов для дерева, при хромировании и пр.
Шестивалентный хром является признанным канцерогеном при вдыхании.[11] На многих рабочих местах сотрудники подвержены воздействию шестивалентного хрома, например, при гальваническом хромировании или сварке нержавеющих сталей.[11] В Европейском союзе использование шестивалентного хрома существенно ограничено директивой RoHS.
Шестивалентный хром транспортируется в клетки человеческого организма с помощью сульфатного транспортного механизма благодаря своей близости к сульфатам по структуре и заряду. Трёхвалентный хром, более часто встречающийся, не транспортируется в клетки.
Внутри клетки Cr(VI) восстанавливается до метастабильного пятивалентного хрома (Cr(V)), затем до трехвалентного хрома (Cr(III)). Трехвалентный хром, присоединяясь к протеинам, создает гаптены, которые включают иммунную реакцию. После их появления чувствительность к хрому не пропадает. В этом случае даже контакт с текстильными изделиями, окрашенными хромсодержащими красками или с кожей, обработанной хромом, может вызвать раздражение кожи. Витамин C и другие агенты реагируют с хроматами и образуют Cr(III) внутри клетки.[12]
Продукты шестивалентного хрома являются генотоксичными канцерогенами. Хроническое вдыхание соединений шестивалентного хрома увеличивает риск заболеваний носоглотки, риск рака лёгких. (Лёгкие особенно уязвимы из-за большого количества мелких капилляров). Видимо, механизм генотоксичности запускается пяти- и трёхвалентным хромом.
В США предельно допустимая концентрация шестивалентного хрома в воздухе составляет 5 мкг/м³ (0,005 мг/м³).[13][14] В России предельно допустимая концентрация хрома (VI) существенно ниже — 1,5 мкг/м³ (0,0015 мг/м³).[15]
Одним из общепризнанных методов избежания шестивалентного хрома является переход от технологий гальванического хромирования к газотермическому и вакуумному напылению.
Основанный на реальных событиях фильм «Эрин Брокович» режиссёра Стивена Содерберга рассказывает о крупном судебном процессе, связанном с загрязнением окружающей среды шестивалентным хромом, в результате которого у многих людей развились серьёзные заболевания.[16]
См. также
Примечания
- ↑ Michael E. Wieser, Norman Holden, Tyler B. Coplen, John K. Böhlke, Michael Berglund, Willi A. Brand, Paul De Bièvre, Manfred Gröning, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O’Connor, Thomas Walczyk, Shige Yoneda, Xiang‑Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. — 2013. — Vol. 85, no. 5. — P. 1047-1078. — DOI:10.1351/PAC-REP-13-03-02.
- ↑ Редкол.:Зефиров Н. С. (гл. ред.). Химическая энциклопедия: в 5 т. — Москва: Большая Российская энциклопедия, 1999. — Т. 5. — С. 308.
- ↑ 1. Дроздов А. А. и др. Неорганическая химия: В 3 т./Под ред. ЮД Третьякова. T. 2: Химия переходных металлов. – 2004. 2. Greenwood N. N., Earnshaw A. Chemistry of the Elements. – 1984.
- ↑ статья «Минеральные ресурсы». Энциклопедия «Кругосвет». Архивировано 21 августа 2011 года.
- ↑ 1 2 ХРОМ | Онлайн Энциклопедия Кругосвет.
- ↑ Поваренных А. С. Твердость минералов. — АН УССР, 1963. — С. 197—208. — 304 с.
- ↑ Реми Г. Курс неорганической химии. Т. 2. М., Мир, 1966. С. 142—180.
- ↑ Некрасов Б. В. Курс общей химии. М:, ГНХТИ, 1952, С. 334
- ↑ Хром // Большая медицинская энциклопедия : в 30 т. / гл. ред.Б.В. Петровский. — 3 изд. — Москва : Советская энциклопедия, 1986. — Т. 27. Хлоракон — Экономика здравоохранения. — 576 с. — 150 000 экз.
- ↑ Gerd Anger, Jost Halstenberg, Klaus Hochgeschwender, Christoph Scherhag, Ulrich Korallus, Herbert Knopf, Peter Schmidt, Manfred Ohlinger, «Chromium Compounds» in Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005.
- ↑ 1 2 IARC. Volume 49: Chromium, Nickel, and Welding. — Lyon : International Agency for Research on Cancer, 1999-11-05. — «There is sufficient evidence in humans for the carcinogenicity of chromium[VI] compounds as encountered in the chromate production, chromate pigment production and chromium plating industries.». — ISBN 92-832-1249-5.
- ↑ Salnikow, K. and Zhitkovich, A., «Genetic and Epigenetic Mechanisms in Metal Carcinogenesis and Cocarcinogenesis: Nickel, Arsenic, and Chromium», Chem. Res. Toxicol., 2008, 21, 28-44. DOI:10.1021/tx700198a
- ↑ OSHA: Small Entity Compliance Guide for the Hexavalent Chromium Standards
- ↑ David Blowes (2002). «Tracking Hexavalent Cr in Groundwater». Science 295: 2024–25. DOI:10.1126/science.1070031. PMID 11896259.
- ↑ ПДК воздуха населенных мест
- ↑ Официальный сайт Эрин Брокович, страница, посвящённая фильму
Ссылки
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na, Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu, | |
wikipedia.green