|
1. Металлы |
Реагируют только металлы, которые находятся до водорода в ряду напряжений металлов: Fe + 2HCl → FeCl2 + H2 Fe + H2SO4(р) → FeSO4 + H2 Cu + HCl → реакция не идет |
Реагируют со всеми металлами кроме Au и Pt). Cu + 2H2SO4(к) → CuSO4 + SO2 + 2H2O 2Fe + 6H2SO4(к) (t → Fe2(SO4)3 + 3SO2 + 6H2O 3Cu + 8HNO3(р) → 3Сu(NO3)2 + 2NO + 4H2O Cu + 4HNO3(к) → Сu(NO3)2 + 2NO2 + 2H2O |
|
2. Неметаллы |
– |
Образование оксидов, кислот: 2H2SO4 (к) + S → 3SO2 + 2H2O 2H2SO4 (к) + C → CO2 + 2SO2 + 2H2O 4HNO3(р) + 3C → 3CO2 + 4NO + 2H2O 4HNO3(к, гор.) + C → CO2 + 4NO2 + 2H2O |
|
3. Оксиды:
1) Основные 2) Амфотерные 3) Кислотные |
CaO + HCl → CaCl 2 + H2O ZnO + H2SO4(р) → ZnSO4 + H2O – |
Обычные реакции обмена, так как металл уже окислен: CaO + H2SO4(к) → CaSO4 + H2O ZnO + H2SO4(к) → ZnSO4 + H2O – |
|
4. Основания: 1) Растворимые (щелочи)
2)Нерастворимые |
Реакция нейтрализации: HCl + NaOH → NaCl + H2O
3HCl + Al(OH)3 → AlCl3 + 3H2O |
Ca(OH)2 + H2SO4(к) → CaSO4 + 2H2O
Zn(OH)2 + H2SO4(к) → ZnSO4 + 2H2O |
|
5. Кислоты: 1) неокислители 2) окислители |
– – |
– – |
|
6. Соли:
2) нерастворимые |
Na 2CO3 + 2HCl → 2NaCl + CO2 + H2O
MgS + 2HCl → MgCl2 + H2S |
Если образуется осадок, газ или более слабая кислота: H2SO4 + Ba(NO3)2 → BaSO4 + 2HNO3
H2SO4 + CaCO3 → CaSO4 + CO2 + H2O |
|
7. Разложение при нагревании |
H2CO3 → CO2 + H2O H2SO3 → SO2 + H2O H2SiO3 → SiO2 + H2 |
– |
Химические свойства кислот – HIMI4KA

Кислотами называют класс химических соединений, которые содержат в своём составе один или несколько катионов водорода, способных замещаться на атомы металлов, и анионов кислотных остатков. Классификация кислот и способы их получения были рассмотрены ранее в уроке 6.
Все кислоты вступают в реакцию с основаниями с образованием солей и воды (реакция нейтрализации), с основными и амфотерными оксидами с образованием солей и воды, например:


Водные растворы сильных кислот вступают в реакцию с металлами, которые стоят в ряду напряжений металлов левее водорода с образованием соли и выделением водорода:
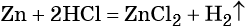
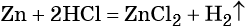
Исключением является азотная кислота в любой концентрации и концентрированная серная кислота. В этих случаях водород не выделяется, а происходит восстановление атомов азота и серы соответственно.
Сильные кислоты вытесняют более слабые кислоты из их солей. При этом образуется новая кислота и новая соль:
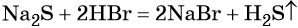
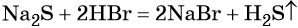
Тренировочные задания
1. Фтороводородная (плавиковая) кислота вступает в реакцию с
1) нитратом натрия
2) нитратом аммония
3) карбонатом натрия
4) сульфатом бария
2. Фтороводородная (плавиковая) кислота реагирует со всеми веществами набора
1) SO3, KCl
2) SiO2, KOH
3) NaOH, NaBr
4) SiO2, KCl
3. Верны ли следующие суждения о фтороводородной (плавиковой) кислоте?
А. Это сильная кислота.
Б. Растворы плавиковой кислоты нельзя хранить в стеклянной посуде.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
4. Соляная кислота вступает в реакцию с
1) сульфатом бария
2) сульфатом лития
3) гидроксидом аммония
4) оксидом серы (IV)
5. Соляная кислота реагирует со всеми веществами набора
1) AgNO3, NO
2) AgNO3, CaO
3) CaCO3, Hg
4) MgCO3, SO3
6. Верны ли следующие суждения о соляной кислоте?
А. Концентрация хлороводорода в соляной кислоте может достигать 60%.
Б. Соляная кислота растворяет алюминий.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
7. Бромоводородная кислота вступает в реакцию с
1) нитратом кальция
2) сульфатом аммония
3) сульфатом железа (II)
4) сульфидом натрия
8. Бромоводородная кислота реагирует со всеми веществами набора
1) BaO, ZnO
2) Na2O, Au
3) Al2O3, CO
4) ZnO, SiO2
9. Верны ли следующие суждения о бромоводородной кислоте?
А. Бромоводородная кислота вступает в реакции с металлами, расположенными в ряду напряжения металлов после водорода.
Б. Бромоводородная кислота сильнее уксусной.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
10. Сероводородная кислота вступает в реакцию с
1) ацетатом натрия
2) ацетатом свинца
3) хлоридом натрия
4) ацетатом лития
11. Сероводородная кислота реагирует со всеми веществами набора
1) Fe(CH3COO)2, NaOH
2) FeCl2, Au
3) SiO2, NaOH
4) SO2, N2
12. Верны ли следующие суждения о сероводородной кислоте?
А. Это слабая кислота.
Б. Она образует два ряда солей: средние и кислые.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
13. Фосфорная кислота вступает в реакцию с
1) ацетатом натрия
2) ацетатом калия
3) нитратом натрия
4) нитратом кальция
14. Фосфорная кислота реагирует со всеми веществами набора
1) NO, CaO
2) Na2O, K2O
3) SO3, N2
4) SO2, CO2
Ответ:
15. Верны ли следующие суждения о фосфорной кислоте?
А. Это твёрдое вещество, хорошо растворимое в воде.
Б. Фосфорная кислота вступает в реакцию обмена с хлоридом кальция.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
16. Азотная кислота в растворе вступает в реакцию с
1) ацетатом натрия
2) ацетатом свинца
3) хлоридом кальция
4) карбонатом калия
17. Азотная кислота реагирует со всеми веществами набора
1) K2CO3, LiOH
2) KOH, NaCl
3) K3PO4, CO2
4) SO3, N2O
18. Верны ли следующие суждения об азотной кислоте?
А. Это слабая одноосновная кислота.
Б. Разбавленная азотная кислота вступает в реакцию с медью.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
19. Серная кислота вступает в реакцию с
1) нитратом лития
2) нитратом калия
3) нитратом бария
4) нитратом железа (II)
20. Серная кислота реагирует со всеми веществами набора
1) NO, P2O5
2) Cr2O3, NO
3) Al2O3, ZnO
4) SO2, CO
21. Верны ли следующие суждения о серной кислоте?
А. Концентрированная серная кислота является сильным водоотнимающим средством.
Б. Серная кислота вытесняет угольную кислоту из её солей.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
22. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) HBr + Fe →
Б) HBr + CaO →
В) HBr (изб.) + K[Al(OH)4] →
ПРОДУКТЫ РЕАКЦИЙ
1) KBr + AlBr3 + H2O
2) KBr + Al(OH)3
3) FeBr3 + H2
4) CaBr2 + H2O
5) FeBr2 + H2
23. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) HCl + Na2CO3 →
Б) HCl + Cr →
В) HCl + KMnO4 →
ПРОДУКТЫ РЕАКЦИЙ
1) CrCl3 + H2
2) NaCl + CO2
3) Cl2 + MnCl2 + KCl + H2O
4) CrCl2 + H2
5) NaCl + CO2 + H2O
24. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) H2SO4 + NaOH (изб.) →
Б) H2SO4 (изб.) + NaOH →
В) H2SO4 (разб.) + Al →
ПРОДУКТЫ РЕАКЦИЙ
1) Al2(SO4)3 + H2
2) NaHSO4
3) Na2SO4 + H2O
4) NaHSO4 + H2O
5) Al2(SO4)3 + H2O
25. Дана схема превращений:


Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
26. Дана схема превращений:


Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
Ответы




Химические свойства карбоновых кислот | CHEMEGE.RU
| Карбоновые кислоты – это вещества, в молекулах которых содержится одна или несколько карбоксильных групп СООН. |
Общая формула предельных одноосновных карбоновых кислот: СnH2nO2
Строение, изомерия и гомологический ряд карбоновых кислот
Химические свойства карбоновых кислот
Способы получения карбоновых кислот
.
Для карбоновых кислот характерны следующие свойства:
|
1. Кислотные свойства
| Кислотные свойства карбоновых кислот возникают из-за смещения электронной плотности к карбонильному атому кислорода и вызванной этим дополнительной (по сравнению со спиртами и фенолами) поляризацией связи О–Н. |
| Карбоновые кислоты – кислоты средней силы. В водном растворе карбоновые кислоты частично диссоциируют на ионы: R–COOH ⇆ R-COO– + H+ |
1.1. Взаимодействие с основаниями
Карбоновые кислоты реагируют с большинством оснований. При взаимодействии карбоновых кислот с основаниями образуются соли карбоновых кислот и вода.
CH3COOH + NaOH = CH3COONa + H2
Карбоновые кислоты реагируют с щелочами, амфотерными гидроксидами, водным раствором аммиака и нерастворимыми основаниями.
| Например, уксусная кислота растворяет осадок гидроксида меди (II) |
Видеоопыт взаимодействия уксусной кислоты с гидроксидом натрия можно посмотреть здесь.
| Например, уксусная кислота реагирует с водным раствором аммиака с образованием ацетата аммония |
CH3COOH + NH3 = CH3COONH4
1.2. Взаимодействие с металлами
Карбоновые кислоты реагируют с активными металлами. При взаимодействии карбоновых кислот с металлами образуются соли карбоновых кислот и водород.
| Например, уксусная кислота взаимодействует с кальцием с образованием ацетата кальция и водорода. |

Видеоопыт взаимодействия уксусной кислоты с магнием и цинком можно посмотреть здесь.
1.3. Взаимодействие с основными оксидами
Карбоновые кислоты реагируют с основными оксидами с образованием солей карбоновых кислот и воды.
| Например, уксусная кислота взаимодействует с оксидом бария с образованием ацетата бария и воды. |

| Например, уксусная кислота реагирует с оксидом меди (II) |
2СН3СООН + CuO = H2О + ( CH3COO)2 Cu
Видеоопыт взаимодействия уксусной кислоты с оксидом меди (II) можно посмотреть здесь.
1.4. Взаимодействие с с солями более слабых и летучих (или нерастворимых) кислот
Карбоновые кислоты реагируют с солями более слабых, нерастворимых и летучих кислот.
| Например, уксусная кислота растворяет карбонат кальция |

| Качественная реакция на карбоновые кислоты: взаимодействие с содой (гидрокарбонатом натрия) или другими гидрокарбонатами. В результате наблюдается выделение углекислого газа |

2. Реакции замещения группы ОН
| Для карбоновых кислот характерны реакции нуклеофильного замещения группы ОН с образованием функциональных производных карбоновых кислот: сложных эфиров, амидов, ангидридов и галогенангидридов. |
2.1. Образование галогенангидридов
Под действием галогенагидридов минеральных кислот-гидроксидов (пента- или трихлорид фосфора) происходит замещение группы ОН на галоген.
| Например, уксусная кислота реагирует с пентахлоридом фосфора с образованием хлорангидрида уксусной кислоты |

2.2. Взаимодействие с аммиаком
При взаимодействии аммиака с карбоновыми кислотами образуются соли аммония:

При нагревании карбоновые соли аммония разлагаются на амид и воду:

2.3. Этерификация (образование сложных эфиров)
Карбоновые кислоты вступают в реакции с одноатомными и многоатомными спиртами с образованием

| Например, этанол реагирует с уксусной кислотой с образованием этилацетата (этилового эфира уксусной кислоты): |

2.4. Получение ангидридов
С помощью оксида фосфора (V) можно дегидратировать (то есть отщепить воду) карбоновую кислоту – в результате образуется ангидрид карбоновой кислоты.
| Например, при дегидратации уксусной кислоты под действием оксида фосфора образуется ангидрид уксусной кислоты |

3. Замещение атома водорода при атоме углерода, ближайшем к карбоксильной группе
| Карбоксильная группа вызывает дополнительную поляризацию связи С–Н у соседнего с карбоксильной группой атома углерода (α-положение). Поэтому атом водорода в α-положении легче вступает в реакции замещения по углеводородному радикалу. |
В присутствии красного фосфора карбоновые кислоты реагируют с галогенами.
| Например, уксусная кислота реагирует с бромом в присутствии красного фосфора |

4. Свойства муравьиной кислоты
| Особенности свойств муравьиной кислоты обусловлены ее строением, она содержит не только карбоксильную, но и альдегидную группу и проявляет все свойства альдегидов. |

4.1. Окисление аммиачным раствором оксида серебра (I) и гидроксидом меди (II)
Как и альдегиды, муравьиная кислота окисляется аммиачным раствором оксида серебра. При этом образуется осадок из металлического серебра.

При окислении муравьиной кислоты гидроксидом меди (II) образуется осадок оксида меди (I):

4.2. Окисление хлором, бромом и азотной кислотой
Муравьиная кислота окисляется хлором до углекислого газа.

4.3. Окисление перманганатом калия
Муравьиная кислота окисляется перманганатом калия до углекислого газа:
5HCOOH + 2KMnO4 + 3H2SO4 → 5CO2 + 2MnSO4 + K2SO4 + 8H2O
Видеоопыт взаимодействия муравьиной кислоты с перманганатом калия можно посмотреть здесь.
4.4. Разложение при нагревании
При нагревании под действием серной кислоты муравьиная кислота разлагается с образованием угарного газа:

Видеоопыт разложения муравьиной кислоты можно посмотреть здесь
5. Особенности бензойной кислоты
5.1. Разложение при нагревании
При нагревании бензойная кислота разлагается на бензол и углекислый газ:

4.2. Реакции замещения в бензольном кольце
| Карбоксильная группа является электроноакцепторной группой, она уменьшает электронную плотность бензольного кольца и является мета-ориентантом. |

6. Особенности щавелевой кислоты
6.1. Разложение при нагревании
При нагревании щавелевая кислота разлагается на угарный газ и углекислый газ:

6.2. Окисление перманганатом калия
Щавелевая кислота окисляется перманганатом калия до углекислого газа:

7. Особенности непредельных кислот (акриловой и олеиновой)
7.1. Реакции присоединения
Присоединение воды и бромоводорода к акриловой кислоте происходит против правила Марковникова, т.к. карбоксильная группа является электроноакцепторной:

К непредельным кислотам можно присоединять галогены и водород. Например, олеиновая кислота присоединяет водород:

6.2. Окисление непредельных карбоновых кислот
Непредельные кислоты обесцвечивают водный раствор перманганатов. При этом окисляется π-связь и у атомов углерода при двойной связи образуются две гидроксогруппы:

С чем реагируют кислоты
Ответ на вопрос «с чем реагируют кислоты» довольно прост:
— с основаниями, что приводит к образованию солей и воды
— с основными и амфотерными оксидами:
— с металлами, стоящими в ряду активности до водорода:
— с солями более слабых кислот:
В первом приближении, влияние химической структуры на температуру плавления гомополимеров аналогично ее влиянию на температуру стеклования, Так, например, хорошо известна корреляция температур стеклования и плавления 2/3 (правило «двух третей»). Это эмпирическое соотношение показывает, что температуры стеклования и плавления изменяются параллельно при любых изменениях химической структуры гомополимера.
Обе эти температуры определяются, во-первых, гибкостью макромолекул: чем выше гибкость, тем ниже температуры стеклования и плавления. Во-вторых, объемные боковые группы и наличие разветвлений приводят к понижению температуры плавления вследствие разрыхления кристаллической структуры. Например, для полиэтилена высокой плотности степень разветвленности составляет 1-5 боковых цепей на 1000 атомов углерода основной цепи, и температура плавления ПЭВП достигает 415К. Для полиэтилена низкой плотности характерна более высокая степень разветвленности (15-30), и, как результата, его температура плавления не превышает 390 К.
В-третьих, наличие полярных групп в основной цепи приводит к росту межмолекулярного взаимодействия и повышению температуры плавления.
О едком и не очень / Хабр
– Эти идиоты поместили фарфоровый контейнер со «студнем» в специальную камеру, предельно изолированную… То есть это они думали, что камера предельно изолирована, но когда они открыли контейнер манипуляторами, «студень» пошел через металл и пластик, как вода через промокашку, вырвался наружу, и все, с чем он соприкасался, превращалось опять же в «студень». Погибло тридцать пять человек, больше ста изувечено, а все здание лаборатории приведено в полную негодность. Вы там бывали когда-нибудь? Великолепное сооружение! А теперь «студень» стек в подвалы и нижние этажи… Вот вам и прелюдия к контакту.
— А. Стругацкий, Б. Стругацкий «Пикник на обочине»
Привет, %username%!
В том, что я всё ещё что-то пишу — вините вот этого человека. Он навеял идею.
Просто, немного поразмыслив, я решил, что небольшой экскурс по едким веществам получится относительно быстро. Может кому-то будет и интересно. А кому-то — и полезно.
Поехали.
Сразу определимся с понятиями.
Едкий — 1. Разъедающий химически. 2. Резкий, вызывающий раздражение, боль. 3. Язвительный, колкий.
Ожегов С.И. Словарь русского языка. — М.: Рус.яз., 1990. — 921 с.
Итак, отбрасываем сразу два последних значения слова. Также отбрасываем «едкие» лакриматоры — которые не столько едкие, сколько вызывают слезотечение, и стерниты — которые вызывают кашель. Да, ниже будут вещества, которые обладают и этими свойствами, но они — что главное! — действительно разъедают материалы, а иногда и плоть.
Мы не будем рассматривать вещества, едкие только для человека и подобных — в виду специфического разрушения мембран клеток. А потому иприты останутся не у дел.
Мы будем рассматривать соединения, которые в комнатных условиях — жидкости. Поэтому жидкий кислород и азот, а также газы типа фтора рассматривать не будем, хотя их можно считать едкими, да.
Как обычно, взгляд будет исключительно субъективным, основанным на собственном опыте. И да — вполне возможно, что кого-то я и не упомню — пиши комментарии, %username%, в течение трёх суток с момента публикации я буду дополнять статью тем, что забылось с самого начала!
И да — у меня нет времени и сил строить «хит-парад», поэтому будет сборная солянка. И со всеми исключениями — она вышла довольно короткой.
Едкие щелочи
А конкретно — гидроксиды щелочных металлов: лития, натрия, калия, рубидия, цезия, франция, гидроксид таллия (I) и гидроксид бария. Но:
- Литий, цезий, рубидий и барий отбрасываем — дорого и редко встретишь
- Если ты, %username%, встретишь гидроксид франция, то едкость тебя будет волновать в последнюю очередь — он жутко радиоактивный
- То же и с таллием — он ядовит до жути.
А потому остались натрий и калий. Но будем откровенны — свойства у всех едких щелочей очень схожие.
Гидроксид натрия известен всем как «каустическая сода» (не путать с пищевой, кальцинированной и другими содами, а также поташем). Гидроксид калия как пищевая добавка Е525 — тоже. По свойствам оба похожи: сильно гигроскопичны, то бишь тянут воду, на воздухе «расплываются». Хорошо растворяются в воде, при этом выделяется большое количество теплоты.
«Расплывание» на воздухе — по сути образование очень концентрированных растворов щелочей. А потому, если положить кусочек едкой щёлочи на бумагу, кожу, некоторые металлы (тот же алюминий) — то по прошествии времени обнаружится, что материал хорошо подъело! То, что показывали в «Бойцовском клубе» — очень похоже на правду: действительно, потные руки — да в щёлочь — будет больно! Лично мне показалось больнее, чем от соляной кислоты (о ней ниже).
Впрочем, если руки очень сухие — скорее всего в именно сухой щёлочи ничего и не почувствуешь.
Едкие щёлочи отлично разваливают жиры на глицерин и соли жирных кислот — так и варят мыло (привет, «Бойцовский клуб!») Чуть дольше, но так же действенно расщепляются белки — то есть в принципе щёлочи плоть растворяют, особенно крепкие растворы — да при нагревании. Недостатком в сравнении с той же хлорной кислотой (о ней тоже ниже) является то, что все щёлочи тянут углекислый газ из атмосферы, а потому сила будет постепенно снижаться. Кроме того, щёлочи реагируют и с компонентами стекла — стекло мутнеет, хотя, чтобы его растворить целиком — тут, конечно, надо постараться.
К едким щелочам иногда относят и тетраалкиламмоний гидроксиды, например
Гидроксид тетраметиламмонияНа самом деле в этих веществах объединились свойства катионных поверхностно-активных веществ (ну это как обычное мыло — только катионное: тут активная дифильная частица — с зарядом «+», а в мыле — с зарядом «-«) и относительно высокая основность. Если попадёт на руки — можно намылить в воде и помыть, как мылом, если в водном растворе погреть волосы, кожу или ногти — растворятся. «Едкость» на фоне гидроксидов натрия и калия — так себе.
Серная кислота
H2SO4
Самая популярная, наверное, во всех историях. Не самая едкая, но достаточно неприятная: концентрированная серная кислота (которая 98%) — маслянистая жидкость, которая очень любит воду, а потому у всех её отнимает. Отнимая воду у целлюлозы и сахара, обугливает их. Точно так же она радостно отнимет воду и у тебя, %username%, особенно если налить её на нежную кожу лица или в глаза (ну в глаза на самом деле всё будет попадать с приключениями). Особо добрые люди мешают серную кислоту с маслом, чтобы труднее смывалась и лучше впитывалась в кожу.
Кстати, забирая воду, серная кислота здорово разогревается, что делает картину ещё больше сочной. А потому смывать её водой — очень плохая идея. Лучше — маслом (смывать, а не втирать — а потом уже смыть водой). Ну или большим потоком воды, чтобы сразу и охлаждать.
«Сначала вода, а потом кислота — иначе случится большая беда!» — это именно про серную кислоту, хотя почему-то все считают, что про любую кислоту.
Будучи окислителем, серная кислота окисляет поверхность металлов до оксидов. А поскольку взаимодействие оксидов с кислотами проходит при участии воды как катализатора — а воду серная кислота не отдаёт — то происходит эффект, называемый пассивацией: плотная, нерастворимая и непроницаемая плёнка оксида металла защищает его от дальнейшего растворения.
По этому механизму концентрированную серную кислоту посылают в далёкие дали железо, алюминий. Примечательно, что если кислоту разбавить — появляется вода, и посылать не получается — металлы растворяются.
Кстати, оксид серы SO3 растворяется в серной кислоте и получается олеум — который иногда ошибочно пишут как H2S2O7, но это не совсем верно. У олеума тяга к воде ещё больше.
Собственные ощущения от попадания серной кислоты на руку: немного тепло, потом чуток печёт — смыл под краном, ничего страшного. Фильмам не верьте, но на лицо капать не советую.
Органики часто пользуются хромпиком или «хромовой смесью» — это бихромат калия, растворённый в серной кислоте. По сути это — раствор хромовой кислоты, он хорош для мытья посуды от остатков органики. При попадании на руку тоже жжётся, но по сути — серная кислота плюс токсичный шестивалентный хром. Дырок в руке не дождёшься, разве что на одежде.
Автор этих строк знаком с идиотом, который вместо бихромата калия использовал перманганат калия. При контакте с органикой немножко жахнуло. Присутствующие обделались отделались лёгким испугом.
Кстати, раз уж вспомнили хромпик — немного отвлечёмся от темы кислот и
Хлористый хромил
CrO2Cl2
По сути своей — лютое соединение шестивалентного хрома и соляной кислоты. Тёмно-красная жидкость, которая тянет воду, гидролизуется — и в итоге дымит этой самой соляной кислотой. Едкость — итог этого братского единения: хром — окисляет, соляная кислота — растворяет: воспламеняет некоторые органические растворители (спирт, скипидар), однако в некоторых растворяется (четыреххлористый углерод, дихлорметан, сероуглегод). Подъедает металлы, но не настолько хорошо, как кислоты — опять дело в пассивации. например, сталь при воздействии приобретает красивую тёмно-синию поверхность.
Кожу — понятно — изъязвляет, при чём в этом сильнее хромпика, поскольку лучше проникает в кожу как в неполярную органическую ткань. Но дело даже не в этом, а в шестивалентном хроме, который вообще-то канцероген, а потому глубже проникнет — больше проблем. Ну и конечно надышаться куда опаснее.
Соляная кислота
HCl
Выше 38% в воде не бывает. Одна из самых популярных кислот для растворения — в этом она покруче остальных, потому что технологически может быть очень чистой, а кроме действия, как кислота, ещё и образует комплексные хлориды, которые повышают растворимость. Кстати, именно по этой причине нерастворимый хлорид серебра очень даже растворим в концентрированной соляной кислоте.
Эта при попадании на кожу жжётся чуток сильнее, субъективно — ещё и зудит, к тому же воняет: если в лаборатории с плохой вытяжкой работать много с концентрированной соляной кислотой — твой стоматолог скажет тебе «спасибо»: ты его озолотишь на пломбах. Кстати, помогает жвачка. Но не сильно. Лучше — вытяжка.
Поскольку не маслянистая и с водой сильно не разогревается, то едкость — только к металлам, и то не ко всем. Кстати, сталь в концентрированной соляной кислоте пассивируется и говорит ей «не-а!». Чем и пользуются при транспортировке.
Азотная кислота
HNO3
Тоже очень популярная, её тоже почему-то боятся — а зря. Концентрированная — это которая до 70% — она самая популярная, выше — это «дымящая», чаще всего никому не нужная. Есть ещё безводная — так та ещё и взрывается.
Будучи окислителем, пассивирует многие металлы, которые покрываются нерастворимой плёнкой и говорят: «до свидания» — это хром, железо, алюминий, кобальт, никель и другие.
С кожей моментально реагирует по принципу ксантопротеиновой реакции — будет жёлтое пятно, что означает, что ты, %username%, всё-таки состоишь из белка! Через какое-то время жёлтая кожа слезет, как при ожоге. При этом щиплет меньше соляной, хотя воняет не хуже — и на этот раз токсичнее: летящие окислы азота не очень хороши для организма.
В химии используют так называемую «нитрующую смесь» — самая популярная состоит из серной и азотной кислот. Используется в синтезах, в частности в получении весёлого вещества — пироксилина. По едкости — тот же хромпик плюс красивая жёлтая кожа.
Так же есть «царская водка» — это часть азотной кислоты на три части соляной. Используется для растворения некоторых металлов, в основном — драгоценных. На разном соотношении и добавлении воды основан капельный метод проверки пробы золотых изделий — кстати, специалистов по этому методу очень сложно надурить с подделкой. По едкости для кожи — та же «нитрующая смесь» плюс воняет отменно, запах не спутаешь ни с чем, он тоже довольно токсичный.
Есть ещё «обратная царская водка» — когда соотношение наоборот, но это редкая специфика.
Кстати, о той самой «дымящей», которая красная, злая и окислитель — цитирую рассказ хорошего друга, который мне вот прямо сейчас прислал.
Гнал я эту самую 98% азотку. То ли просто перегонял для очистки, то ли из меланжа, уже не помню. Нагнал литра два, снимаю приемник. Прошу лаборантку дать чистую колбу на 2 литра — перелить. Она мне и дала сухую, чистую, но из под спирта — и с закрытой пробкой. То есть пары были и накопились. Я туда воронку и переливаю. Я ее туда — а она обратно. Хорошо брызнула на руки, на рожу и ниже шеи. Ощущение — как орел в морду вцепился. Плюс руки, шея, под носом ну и т.д. по мелочи. В руках, напоминаю, два литра того же добра. Глаза закрыты, естественно. Понимаю, что бросить колбу нельзя, будет сразу сильно хуже. Аккуратно ставлю колбу на резиновую подставку, перемещаюсь к мойке, разворачиваю гусак себе в морду и включаю полный напор. Секунд за пять управился. До подкожной клетчатки не добралась. А то все было бы намного хуже. Видел у другого мужика, что бывает через 10-15 сек. Труднозаживающие багровые рубцы на половину руки. Потом понял, почему она такая злая. Мало того, что довольно сильная кислота и окислитель, она еще и чудесный растворитель. Неограниченно смешивается с водой, но неограниченно смешивается и с, например, дихлорэтаном. Такая себе бифильная дрянь.
Фосфорная кислота
H3PO4
На самом деле я привёл формулу ортофосфорной кислоты — самой распространённой. А есть ещё метафосфорная, полифосфорные, ультрафосфорные — короче, хватает, но неважно.
Концентрированная ортофосфорная кислота (85%) — это такой сиропчик. Кислота она сама по себе средняя, её часто используют в пищевой промышленности, кстати — когда тебе ставят пломбы, то поверхность зуба предварительно протравливают фосфорной кислотой.
Коррозионность у неё так себе, но есть неприятный нюанс: этот сиропчик хорошо впитывается. Поэтому если капнет на вещи — впитается, а потом будет потихоньку разъедать. И если от азотной и соляной кислоты будет пятно или дырка — то от фосфорной вещь будет разлазиться, особенно это красочно на обуви, когда дырка как бы крошится, пока не получится насквозь.
Ну а вообще едкой её назвать сложно.
Плавиковая кислота
HF
Концентрированная плавиковая кислота — это примерно 38%, хотя и бывают странные исключения.
Слабенькая кислота, которая берёт яростной любовью фторид-ионов образовывать стойкие комплексы со всем, с кем можно. Поэтому на удивление растворяет то, что другие, более сильные подруги — не могут, а потому очень часто используется в разных смесях для растворения. При попадании на руку ощущения будут больше от других компонентов таких смесей, но есть нюанс.
Плавиковая кислота растворяет SiO2. То есть песок. То есть стекло. То есть кварц. Ну и так далее. Нет, если ты плеснёшь на окно этой кислотой — оно не растворится, но мутное пятно останется. Чтобы растворить — нужно долго держать, а ещё лучше — нагреть. При растворении выделяется SiF4, который так полезен для здоровья, что лучше это делать под вытяжкой.
Маленький, но приятный нюанс: кремний содержится у тебя, %username%, в ногтях. Так вот, если плавиковая кислота попадёт под ногти — ты ничего не заметишь. Но ночью спать не сможешь — болеть будет ТАК, что иногда возникает желание оторвать палец. Поверь, друг — я знаю.
И вообще плавиковая кислота токсична, канцерогенна, впитывается через кожу и масса всего — но мы-то сегодня про едкость, правда?
Помнишь, мы договаривались в самом начале, что фтора не будет? Его и не будет. Но будут…
Фториды инертных газов
На самом деле фтор — суровый парень, с ним особо не повыпендриваешься, а потому некоторые инертные газы образуют с ним фториды. Известны такие стабильные фториды: KrF2, XeF2, XeF4, XeF6. Всё это — кристаллы, которые на воздухе с разной скоростью и охотой разлагаются влагой до плавиковой кислоты. Едкость — соответствующая.
Иодоводородная кислота
HI
Самая сильная (по степени диссоциации в воде) бинарная кислота. Сильный восстановитель, чем пользуются химики-органики. На воздухе окисляется и становится бурой, чем и пачкает при контакте. Ощущения при контакте — как от соляной. Всё.
Хлорная кислота
HClO4
Одна из самых сильных (по степени диссоциации в воде) кислот вообще (с ней конкурируют суперкислоты — о них ниже) — функция кислотности Гаммета (численное выражение способности среды быть донором протонов по отношению к произвольному основанию, чем меньше — тем сильнее кислота) составляет -13. Безводная — сильный окислитель, любит взрываться, да и вообще неустойчива. Концентрированная (70%-72%) — окислитель не хуже, часто используют в разложении биологических объектов. Разложение интересно и захватывающе тем, что может взрываться в процессе: нужно следить, чтобы не было частиц угля, чтобы не кипело слишком бурно и т.д. Хлорная кислота к тому же довольно грязная — её невозможно очистить субперегонкой, взрывается зараза! Поэтому используют её нечасто.
При попадании на кожу жжётся, ощущения как от соляной. Воняет. Когда видите в фильмах, что кто-то кинул труп в ёмкость с хлорной кислотой — и он растворился, то да, такое возможно — но долго или греть. Если греть — может рвануть (см. выше). Так что будьте критичны к кинематографу (я, кажется, видел это в «Кловерфилд, 10»).
Кстати, едкость оксида хлора (VII) Cl2O7 и оксида хлора (VI) Cl2O6 — это итог того, что с водой эти оксиды образуют хлорную кислоту.
А теперь представим, что мы решили в одном соединении объединить сильную кислотность — и едкость фтора: возьмём молекулу хлорной или серной кислоты — и заменим на ней все гидроксильные группы на фтор! Дрянь получится редкостная: она будет взаимодействовать с водой и подобными соединениями — и будет в месте реакции сразу получаться сильная кислота и плавиковая кислота. А?
Фториды серы, брома и иода
Помните, мы договорились рассматривать только жидкости? По этой причине в нашу статью не попал трифторид хлора ClF3, который кипит при +12 °C, хотя все страшилки о том, что он жутко токсичен, воспламеняет стекло, противогаз и при разливании 900 килограммов — проедает 30 см бетона и метр гравия — всё это правда. Но мы же договорились — жидкости.
Однако есть жёлтая жидкость — пентафторид иода IF5, бесцветная жидкость — трифторид брома BrF3, светло-жёлтая — пентафторид брома BrF5, которые не хуже. BrF5, к примеру, тоже растворяет стекло, металлы и бетон.
Аналогично — среди всех фторидов серы жидким является только декафторид дисеры (иногда её называют ещё пятифтористой серой) — бесцветная жидкость с формулой S2F10. Но это соединение при обычных температурах достаточно стабильно, не разлагается водой — а потому не особо и едко. Правда, в 4 раза токсичнее фосгена с аналогичным механизмом действия.
Кстати, говорят, что пентафторид иода был «специальным газом» для заполнения атмосферы в спасательном шаттле в последних кадрах фильма «Чужой» 1979 года. Ну не помню, честно. Напомнился! Блин, там настолько круто, что я не удержался — и посвятил этому отдельную статью.
Суперкислоты
Термин «суперкислота» введён Джеймсом Конантом в 1927 году для классификации более сильных кислот, чем обычные минеральные кислоты. В некоторых источниках хлорную кислоту относят к суперкислоте, хотя это не так — она обычная минеральная.
Ряд суперкислот — это минеральные, к которым подцепили галоген: галоген тянет на себя электроны, все атомы очень сильно гневаются, а достаётся всё как обычно водороду: тот отваливается в виде Н+ — бабах: вот и кислота стала сильнее.
Примеры — фторсерная и хлорсерная кислотыУ фторсерной кислоты функция Гаммета -15,1, кстати, благодаря фтору, эта кислота постепенно растворяет пробирку, в которой хранится.
Потом кто-то из умных подумал: а давайте возьмём кислоту Льюиса (вещество, способное принять пару электронов другого вещества) и смешаем с кислотой Бренстеда (веществом, которое способно отдавать протон)! Смешали пентафторид сурьмы с плавиковой кислотой — получили гексафторсурьмяную кислоту HSbF6. В этой системе плавиковая кислота выделяет протон (H+), а сопряжённое основание (F−) изолируется координационной связью с пентафторидом сурьмы. Так образуется большой октаэдрический анион (SbF6−), являющийся очень слабым нуклеофилом и очень слабым основанием. Став «свободным», протон обусловливает сверхкислотность системы — функция Гаммета -28!
А потом пришли другие и сказали, а чего это кислоту Бернстеда взяли слабую — и придумали вот что.
Трифторметансульфоновая кислота— сама по себе уже суперкислота (функция Гаммета -14,1). Так вот, к ней добавили опять пентафторид сурьмы — получили снижение до -16,8! Такой же фокус с фторсерной кислотой дал снижение до -23.
А потом группа ученых с химической кафедры американского университета Калифорнии под управлением профессора Кристофера Рида затусила с коллегами из Института катализа СО РАН (Новосибирск) и придумали карборановую кислоту H(CHB11Cl11). Ну «карборановой» её назвали для обычных людей, а если хочешь почувствовать себя учёным — произнеси «2,3,4,5,6,7,8,9,10,11,12-ундекахлор-1-карба-клозо-додекаборан(12)» три раза и быстро.
Так выглядит эта красоткаЭто — сухой порошочек, который растворим в воде. Это и есть Самая Сильная Кислота на текущий момент. Карборановая кислота приблизительно в миллион раз сильнее концентрированной серной кислоты. В обычных шкалах измерить силу кислоты не удается, так как кислота протонирует все известные слабые основания и все растворители, в которых она растворяется, включая воду, бензол, фуллерен-60, диоксид серы.
Впоследствии Кристофер Рид в интервью службе новостей Nature сказал: «Идея синтеза карборановой кислоты родилась из фантазий «о молекулах, никогда прежде не создаваемых». Вместе с коллегами он хочет использовать карборановую кислоту для окисления атомов инертного газа ксенона — просто потому, что никто прежде этого не делал. Оригинально, что сказать.
Ну поскольку суперкислоты — это обычные кислоты, то и действуют они обычно, только немного сильнее. Ясно, что кожу будут жечь, но это не значит — что растворять. Фторсульфоновая — отдельный случай, но там всё благодаря фтору, как и в плавиковой.
Тригалогенуксусные кислоты
А конкретно — трифторуксусная и трихлоруксусная кислота
Милы и приятны сочетанием свойств органического полярного растворителя и достаточно сильной кислоты. Воняют — похоже на уксус.
Самая няшка — трифторуксусная кислота: 20%-ный раствор разрушает металлы, пробку, резину, бакелит, полиэтилен. На коже жжётся и образует сухие язвы, доходящие до мышечного слоя.
Трихлоруксусная в этом плане — младший брат, но тоже ничего. Кстати, аплодисменты слабому полу: в погоне за красотой, некоторые идут на так называемую процедуру ТСА-пилинга (ТСА — это TetraChloroAcetate) — когда этой самой трихлоруксусной кислотой растворяют верхний огрубевший слой кожи.
Уксусная кислота
СН3СООН
Скорее всего, у тебя на кухне есть эта кислота — и да, она используется как пищевая добавка Е260. Но также она бывает и покрепче — 70-80%-й водный раствор уксусной кислоты называют уксусной эссенцией, а если концентрация близка к 100% — ледяной уксусной кислотой (потому что она может замерзать и образовывать нечто похожее на лёд.
Уксусная кислота не так едка по отношению к металлам, как минеральные кислоты, но поскольку и не так полярна, а в какой-то степени даже дифильна (сочетание гидрофобной и гидрофильной части в одной молекуле — как в поверхностно-активных веществах) — то она здорово всасывается кожей. Опасными считаются растворы с концентрацией уксусной кислоты больше 30%. Особенность ожогов в том, что также инициируется развитие коагуляционных некрозов прилегающих тканей различной протяженности и глубины — если не смыть, то будут долго заживающие язвы и рубцы.
Ну и воняет она, конечно, знатно.
Муравьиная кислота
НСООН
Мы уже обсуждали, что муравьиная кислота, образующаяся в организме после принятия метанола, — одна из основных причин его токсичности. Так вот, муравьиная кислота извне вовсе не так опасна, поскольку быстро метаболизируется и выводится организмом. Токсичность довольно низка — для крыс LD50 порядка 1,8 г/кг, а потому муравьиную кислоту тоже часто используют, в том числе и как пищевую добавку — и этого бояться не стоит.
»Едкость» муравьиной кислоты зависит от концентрации. Согласно классификации Европейского союза, концентрация до 10% обладает раздражающим эффектом, больше 10% — разъедающим. И речь опять не о металлах и стекле — а об организме. При контакте с кожей 100%-я жидкая муравьиная кислота вызывает сильные химические ожоги. Попадание даже небольшого её количества на кожу причиняет сильную боль, поражённый участок сначала белеет, как бы покрываясь инеем, потом становится похожим на воск, вокруг него появляется красная кайма. Кислота легко проникает через жировой слой кожи, поэтому промывание поражённого участка раствором соды необходимо произвести немедленно. Так что муравьи действительно что-то знают.
Бром
Br2
Тяжёлая едкая жидкость красно-бурого цвета с сильным неприятным запахом, отдалённо напоминающим запах одновременно иода и хлора. Кстати, название «бром» от греческого βρῶμος — «вонючка», «вонючий».
Бром — типичный галоген, по химической активности бром занимает промежуточное положение между хлором и иодом. То есть не такой прыткий, как фтор — но поживее скучного иода. И да, до хлора тоже не дотягивает.
Немного растворим в воде, хорошо — в некоторых органических растворителях. Бромная вода — реактив на непредельные углеводороды — воняет, но вполне себе мирная и ничего сильно не растворяет.
Чистый бром могуч, вонюч и волосат, а также токсичен. При попадании на кожу вызывает ожоги: неприятность в том, что молекулы брома неполярны, а потому хорошо проникают в гидрофобную человеческую кожу и плоть — а потому ожоги действительно болезненны, долго заживают, почти всегда оставляют на память шрам. Алюминий вспыхивает при контакте с бромом, остальные металлы более воздержаны, но в виде порошка — некоторые реагируют, например, железо.
Бетон и стекло к брому достаточно устойчивы. Органические соединения бромом — что? — правильно! — бромируются при наличии ненасыщенной связи. По этой причине устойчивость полимеров зависит от их типа, к примеру полиэтилен и полипропилен — плевать хотели на бром при комнатных условиях.
Пероксид водорода
H2O2
Нестабильное соединение, которое постоянно постепенно разваливается на кислород и воду. Чем выше концентрация — тем нестабильнее, что постепенно превращается во взрывоопасность. Для стабилизации технического пероксида водорода в него добавляют пирофосфат или станнат натрия; при хранении в алюминиевых емкостях используют ингибитор коррозии — нитрат аммония.
Пероксид водорода в лаборатории обычно представляет собой раствор 38%. При попадании на кожу оказывает химический ожог с характерным белым окрашиванием. Ожог болезненный, особенно на тонкой коже, побелевшая ороговевшая кожа потом часто трескается и зудит.
В медицине используют 3% пероксид водорода для очистки глубоких ран сложного профиля, гнойных затёков, флегмон и других гнойных ран, санация которых затруднена — так вещество обладает не только антисептическим эффектом, но и создаёт большое количество пены при взаимодействии с ферментом каталазой. Это в свою очередь позволяет размягчить и отделить от тканей некротизированные участки, сгустки крови, гноя, которые будут легко смыты последующим введением в полость раны антисептического раствора. Кстати, перекись водорода нежелательна в других случаях ран: обладая хорошими очищающими свойствами, это вещество на самом деле не ускоряет процесс заживления, поскольку повреждает прилегающие к ране клетки, равно как и молодые, новообразующиеся ткани — а это ещё и чревато образованием рубцов.
Кроме как ожогов на коже — ничего не разъедает и не растворяет. Металлы, стекло и пластики устойчивы к пероксиду водорода.
А ещё пероксид водорода подарил миру много уникальных натуральных блондинок с чёрными корнями волос!
Близки к пероксиду водорода так называемые надкислоты — кислоты, в которых присутствуют пероксидные группы. Пример: надуксусная кислота СН3СОООН — вещество, напоминающее по свойствам пероксид водорода, а потому и использующееся точно в таких же сферах. Есть «первомур» или «С-4» (нет, это не тот С-4, о котором ты подумал) — это пермуравьиная кислота HCOOOН, которая ещё слабее надуксусной, а потому хирируги моют ей руки перед операцией. И наконец — трифторперуксусная кислота СF3СОООН — лютый, бешеный окислитель, на который с восхищением смотрят химики-органики за возможность окисления анилина до нитробензола, получения гипервалентного иода в органических соединениях, реакцию Байера-Виллигера и другие малопонятные нормальным людям вещи. По едкости — трифторуксусная кислота, смешанная с перекисью водорода, чем, собственно, и является, а потому для рук представляет особую опасность, да. В виду своей высокой окислительной способности, трифторперуксусная кислота не продаётся, а обычно получается восхищающимися химиками-органиками прямо там, где необходимо, взаимодействием трифторуксусного ангидрида с пероксидом водорода.
Ну вот примерно так, если говорить про жидкость и про едкость. Будут ещё дополнения?
кислотно-основных реакций | Типы реакций
13.2 Кислотно-основные реакции (ESBQY)
Реакция между кислотой и основанием известна как реакция с нейтрализацией . Часто, когда кислота и основание вступают в реакцию, образуются соль и вода. Мы рассмотрим несколько примеров кислотно-основных реакций.
В химии слово соль не означает белое вещество, которое вы опрыскиваете в пищу (это белое вещество — соль, но не единственная соль). Соль (для химиков) является продуктом кислотно-щелочной реакции и состоит из катиона из основания и аниона из кислоты.{-} \) ионы. Соль все еще образуется как единственный продукт, но вода не производится.
Важно понять, насколько полезны эти реакции нейтрализации. Ниже приведены некоторые примеры:
Бытовое использование
Оксид кальция (\ (\ text {CaO} \)) является основанием (все оксиды металлов являются основаниями), которое наносится на слишком кислую почву. Порошковый известняк \ ((\ text {CaCO} _ {3}) \) также можно использовать, но его действие намного медленнее и менее эффективно.Эти вещества могут также использоваться в более широком масштабе в сельском хозяйстве и в реках.
Известняк (белый камень или карбонат кальция) используется в выгребных ямах (или длинных каплях). Известняк является основой, которая помогает нейтрализовать кислотные отходы.
Биологическое использование
Кислоты в желудке (например, соляная кислота) играют важную роль в переваривании пищи. Однако, когда у человека есть язва желудка или когда в желудке слишком много кислоты, эти кислоты могут вызывать сильную боль. Антациды используются для нейтрализации кислот, чтобы они не горели так сильно. Антациды — это основания, которые нейтрализуют кислоту. Примерами антацидов являются гидроксид алюминия, гидроксид магния («магнезиальное молоко») и бикарбонат натрия («бикарбонат соды»). Антациды также могут быть использованы для облегчения изжоги.
Промышленное использование
Основной гидроксид кальция (известковая вода) может использоваться для поглощения вредного кислого \ (\ text {SO} _ {2} \) газа, который выделяется на электростанциях и при сжигании ископаемого топлива.
Пчелиные укусы кислые и имеют рН между \ (\ text {5} \) и \ (\ text {5,5} \). Их можно успокоить, используя такие вещества, как бикарбонат соды и магнезиальное молоко. Обе основы помогают нейтрализовать кислотный укус пчелы и снять зуд!
Кислотно-основные реакции
Цель
Изучить кислотно-основные реакции.
Приборы и материалы
- Колба мерная
- конических колб
- раствор гидроксида натрия
- раствор соляной кислоты
- пипетка
- индикатор
Метод
Используйте пипетку для добавления \ (\ text {20} \) \ (\ text {ml} \) раствора гидроксида натрия в мерную колбу.Залейте водой до отметки и хорошо встряхните.
Поместите \ (\ text {20} \) \ (\ text {ml} \) раствора гидроксида натрия в коническую колбу. Добавьте несколько капель индикатора.
Медленно добавляйте \ (\ text {10} \) \ (\ text {ml} \) соляной кислоты. Если есть изменение цвета, остановитесь. Если нет, добавьте еще один \ (\ text {5} \) \ (\ text {ml} \). Продолжайте добавлять \ (\ text {5} \) \ (\ text {ml} \), пока не заметите изменение цвета.
Наблюдения
Раствор меняет цвет после добавления заданного количества соляной кислоты.
В приведенном выше эксперименте вы использовали индикатор, чтобы увидеть, когда кислота нейтрализовала основание. Индикаторы — это химические соединения, которые меняют цвет в зависимости от того, находятся ли они в кислоте или в основе.
Включен рекомендуемый эксперимент для неформальной оценки по выявлению природных показателей. Учащиеся могут протестировать различные красочные растения, чтобы увидеть, что происходит с каждым растением при смешивании с кислотой или основанием.Основная идея заключается в том, чтобы учащиеся извлекали цвет растения путем кипячения растительного вещества, а затем слива жидкости. Для таких веществ, как порошок карри, учащиеся могут растворить это в воде, а для чая они могут заварить чашку чая и затем вынуть пакетик перед тестированием. Затем полученную жидкость можно проверить, чтобы определить, является ли она индикатором. Альтернативой смешиванию кислоты или основания с жидкостью является замачивание полосок бумаги в жидкости и затем нанесение капли кислоты или основания на бумагу.Эксперимент ниже также охватывает некоторые другие вещества, такие как разрыхлитель, эссенция ванили и лук. Разрыхлитель расщепляется в кислотах, но не в основаниях. Лук и ванильная эссенция теряют свой характерный запах в основном растворе.
Важно, чтобы учащиеся не помещали свои лица или носы прямо над или в стакан, когда нюхали лук и ванильную эссенцию. Они должны держать мензурку в одной руке и использовать другую руку, чтобы поднять (то есть взмахнуть рукой взад и вперед) запах к лицу.
Кислоты и основания едкие и могут вызвать серьезные ожоги, поэтому с ними следует обращаться осторожно.
Показатели
Цель
Чтобы определить, какие растения и продукты могут выступать в качестве индикаторов.
Аппаратура и материалы
- Возможные показатели: красная капуста, свекла, ягоды (например, шелковица), порошок карри, красный виноград, лук, чай (ройбуш или обычный), разрыхлитель, ванильная эссенция
- кислот (например, уксус, соляная кислота), основания (например,грамм. аммиак (во многих бытовых чистящих средствах)) для теста
- мензурки
Метод
Возьмите небольшое количество первого возможного индикатора (не используйте лук, ванильную эссенцию и разрыхлитель). Вскипятите вещество до тех пор, пока вода не сменит цвет.
Отфильтруйте полученный раствор в мензурку, следя за тем, чтобы в мензурку не попало растительных веществ. (Вы также можете налить воду через дуршлаг или сито.)
Вылейте половину полученного окрашенного раствора во второй стакан.
Поставьте один стакан на лист бумаги формата А4 с надписью «кислоты». Поместите другой стакан на лист бумаги с надписью «основы».
Повторите все остальные возможные показатели (кроме лука, ванильной эссенции и разрыхлителя).
Во все мензурки на кислотном листе осторожно налейте \ (\ text {5} \) \ (\ text {ml} \) кислоты.Запишите ваши наблюдения.
Во все мензурки на базовом листе осторожно налейте \ (\ text {5} \) \ (\ text {ml} \) основы. Запишите ваши наблюдения.
Если у вас более одной кислоты или основания, вам нужно будет повторить вышеописанные шаги, чтобы получить свежие образцы индикаторов для вашей второй кислоты или основания. Или вы можете использовать меньше полученного окрашенного раствора для каждой кислоты и основания, которое вы хотите проверить.
Соблюдайте запах лука и ванильной эссенции.Поместите маленький кусочек лука в стакан. Это для тестирования с кислотой. Налейте \ (\ text {5} \) \ (\ text {ml} \) кислоты. Проведите рукой по стакану, чтобы подуть воздух к носу. Что ты замечаешь о запахе лука? Повторите с ванильной эссенцией.
Поместите маленький кусочек лука в стакан. Это для тестирования с базой. Залейте \ (\ text {5} \) \ (\ text {ml} \) базы. Проведите рукой по стакану, чтобы подуть воздух к носу.Что ты замечаешь о запахе лука? Повторите с ванильной эссенцией.
Наконец поместите чайную ложку разрыхлителя в стакан. Аккуратно налейте \ (\ text {5} \) \ (\ text {ml} \) кислоты в стакан. Запишите ваши наблюдения. Повторите, используя базу.
Наблюдения
Вещество 9000 990 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 9 8 9 8 9 8 9 9 9 902 901 9 9 9 9 9 9 9 90 9 9 9 9 8 9 9 9 8 9 9 9 9 9 9 8 9 9 9 8 9 9 9 9 9 8 9 9 9 9 8 9 999 9 дл | Свекла | |||
Ягоды | ||||
Карри порошок | ||||
Чай | ||||
Красный виноград | ||||
Лук | ||||
Ванильная эссенция | ||||
Разрыхлитель |
Следует отметить, что некоторые вещества меняют цвет в присутствии кислоты или основания.Разрыхлитель пенится, когда он находится в растворе кислоты, но никакой реакции не наблюдается, когда он находится в основном растворе. Ванильная эссенция и лук должны потерять свой характерный запах, когда в основе.
Ваниль и лук известны как обонятельные (запах) показатели. Обонятельные показатели теряют свой характерный запах при смешивании с кислотами или основаниями.
Теперь мы рассмотрим три конкретных типа кислотно-основных реакций. В каждом из этих типов кислотно-основных реакций кислота остается той же самой, но вид основания изменяется.Мы рассмотрим, какие продукты производятся, когда кислоты реагируют с каждым из этих оснований, и как выглядит общая реакция.
Кислота и гидроксид металла (ESBQZ)
Когда кислота реагирует с гидроксидом металла, образуются соль и вода . Мы уже кратко объяснили это. Вот некоторые примеры:
- \ (\ text {HCl (aq)} + \ text {NaOH (aq)} \ rightarrow \ text {H} _ {2} \ text {O (l)} + \ text {NaCl (aq)} \)
- \ (2 \ text {HBr (aq)} + \ text {Mg (OH)} _ {2} \ text {(aq)} \ rightarrow 2 \ text {H} _ {2} \ text {O (l) } + \ text {MgBr} _ {2} \ text {(aq)} \)
- \ (3 \ text {HCl (aq)} + \ text {Al (OH)} _ {3} \ text {(aq)} \ rightarrow 3 \ text {H} _ {2} \ text {O (l) } + \ text {AlCl} _ {3} \ text {(aq)} \)
Мы можем написать общее уравнение для этого типа реакции: \ [n \ text {H} ^ {+} \ text {(aq)} + \ text {M (OH)} _ {n} \ text {(aq)} \ rightarrow n \ text {H} _ {2 } \ text {O (l)} + \ text {M} ^ {n +} \ text {(aq)} \] Где \ (n \) — номер группы металла, а \ (\ text {M} \) — металл.
Практика Siyavula дает вам доступ к неограниченным вопросам с ответами, которые помогут вам учиться. Практика в любом месте, в любое время и на любом устройстве!
Зарегистрируйтесь сейчас на практике Упражнение 13.3Напишите сбалансированное уравнение для реакции между \ (\ text {HNO} _ {3} \) и \ (\ text {KOH} \).
\ (\ text {HNO} _ {3} \ text {(aq)} + \ text {KOH (aq)} \ rightarrow \ text {KNO} _ {3} \ text {(aq)} + \ text {H } _ {2} \ text {O (l)} \)
Кислота и оксид металла (ESBR2)
Когда кислота реагирует с оксидом металла, образуются также соль и вода .Вот некоторые примеры:
- \ (2 \ text {HCl (aq)} + \ text {Na} _ {2} \ text {O (aq)} \ rightarrow \ text {H} _ {2} \ text {O (l)} + 2 \ текст {NaCl} \)
- \ (2 \ text {HBr (aq)} + \ text {MgO} \ rightarrow \ text {H} _ {2} \ text {O (l)} + \ text {MgBr} _ {2} \ text {( водно)} \)
- \ (6 \ text {HCl (aq)} + \ text {Al} _ {2} \ text {O} _ {3} \ text {(aq)} \ rightarrow 3 \ text {H} _ {2} \ text {O (l)} + 2 \ text {AlCl} _ {3} \ text {(aq)} \)
Мы можем написать общее уравнение для реакции оксида металла с кислотой: \ [2y \ text {H} ^ {+} \ text {(aq)} + \ text {M} _ {x} \ text {O} _ {y} \ text {(aq)} \ rightarrow y \ text {H} _ {2} \ text {O (l)} + x \ text {M} ^ {n +} \ text {(aq)} \] Где \ (n \) — номер группы металла.\ (X \) и \ (y \) представляют отношение, в котором металл соединяется с оксидом, и зависит от валентности металла.
Практика Siyavula дает вам доступ к неограниченным вопросам с ответами, которые помогут вам учиться. Практика в любом месте, в любое время и на любом устройстве!
Зарегистрируйтесь сейчас на практике Упражнение 13.4Напишите сбалансированное уравнение для реакции между \ (\ text {HBr} \) и \ (\ text {K} _ {2} \ text {O} \).
\ (2 \ text {HBr (aq)} + \ text {K} _ {2} \ text {O (aq)} \ rightarrow 2 \ text {KBr (aq)} + \ text {H} _ {2} \ text {O (l)} \)
Кислота и карбонат металла (ESBR3)
Реакция кислот с карбонатами
Аппаратура и материалы
- Небольшие количества разрыхлителя (бикарбонат натрия)
- соляная кислота (разбавленная) и уксус
- ретортный стенд
- две пробирки
- одна резиновая пробка для пробирки
- трубка доставки
- известковая вода (гидроксид кальция в воде)
Эксперимент должен быть организован, как показано ниже.
Метод
Осторожно проденьте трубку подачи через резиновую пробку.
Налейте известковую воду в одну из пробирок.
Осторожно налейте небольшое количество соляной кислоты в другую пробирку.
Добавьте небольшое количество карбоната натрия в кислоту и закройте пробирку резиновой пробкой.Поместите другой конец подающей трубки в пробирку с известковой водой.
Посмотрите, что происходит с цветом известковой воды.
Повторите вышеуказанные шаги, на этот раз с использованием уксуса.
Наблюдения
Чистая известковая вода становится молочной, что означает, что углекислый газ был произведен. Вы можете не увидеть это для соляной кислоты, так как реакция может произойти быстро.
Когда кислота реагирует с карбонатом металла, образуется соль , диоксид углерода и вода . Посмотрите на следующие примеры:
Азотная кислота реагирует с карбонатом натрия с образованием нитрата натрия, углекислого газа и воды.
\ [2 \ text {HNO} _ {3} \ text {(aq)} + \ text {Na} _ {2} \ text {CO} _ {3} \ text {(aq)} \ rightarrow 2 \ text {NaNO} _ {3} \ text {(aq)} + \ text {CO} _ {2} \ text {(g)} + \ text {H} _ {2} \ text {O (l)} \]
Серная кислота вступает в реакцию с карбонатом кальция с образованием сульфата кальция, диоксида углерода и воды.
\ [\ text {H} _ {2} \ text {SO} _ {4} \ text {(aq)} + \ text {CaCO} _ {3} \ text {(aq)} \ rightarrow \ text { CaSO} _ {4} \ text {(s)} + \ text {CO} _ {2} \ text {(g)} + \ text {H} _ {2} \ text {O (l)} \]
Соляная кислота реагирует с карбонатом кальция с образованием хлорида кальция, диоксида углерода и воды.
\ [2 \ text {HCl (aq)} + \ text {CaCO} _ {3} \ text {(s)} \ rightarrow \ text {CaCl} _ {2} \ text {(aq)} + \ text {CO} _ {2} \ text {(g)} + \ text {H} _ {2} \ text {O (l)} \]
Напишите сбалансированное уравнение для реакции между \ (\ text {HCl} \) и \ (\ text {K} _ {2} \ text {CO} _ {3} \).
\ (2 \ text {HCl (aq)} + \ text {K} _ {2} \ text {CO} _ {3} \ text {(aq)} \ rightarrow 2 \ text {KCl (aq)} + \ text {H} _ {2} \ text {O (l)} + \ text {CO} _ {2} \ text {(g)} \)
Используя то, что мы узнали о кислотах и основаниях, мы можем теперь взглянуть на приготовление некоторых солей.
Создание солей
Цель
Для приготовления некоторых солей используют кислотно-основные реакции.{-3} $} \)), серная кислота (разбавленная), гидроксид натрия, оксид меди (II), карбонат кальция
мензурки, массометр, воронки, фильтровальная бумага, бунзеновская горелка, мерные цилиндры
Метод
Носите перчатки и защитные очки при работе с серной кислотой. Работа в хорошо проветриваемом помещении.
часть 1
- Отмерить \ (\ text {20} \) \ (\ text {ml} \) соляной кислоты в стакан.
- Отмерьте \ (\ text {20} \) \ (\ text {ml} \) гидроксида натрия и осторожно добавьте его в химический стакан, содержащий соляную кислоту.
- Осторожно нагрейте полученный раствор, пока вся вода не испарится. У вас должен остаться белый порошок.
часть 2
- Осторожно добавьте \ (\ text {25} \) \ (\ text {ml} \) серной кислоты в чистый стакан.
- Добавьте около небольшого количества (около \ (\ text {0,5} \) \ (\ text {g} \)) оксида меди (II) в стакан, содержащий серную кислоту.Размешайте раствор.
- Как только весь оксид меди (II) растворится, добавьте еще небольшое количество оксида меди (II). Повторяйте, пока твердое вещество не растворится и не останется небольшое количество нерастворенного твердого вещества.
- Отфильтруйте этот раствор и утилизируйте фильтровальную бумагу.
- Осторожно нагрейте полученную жидкость. Вы должны получить небольшое количество твердого вещества.
часть 3
- Отмерить \ (\ text {20} \) \ (\ text {ml} \) соляной кислоты в новый стакан.
- Добавить небольшое количество (около \ (\ text {0,5} \) \ (\ text {g} \)) карбоната кальция в стакан, содержащий соляную кислоту. Размешайте раствор.
- Как только весь карбонат кальция растворится, добавьте еще небольшое количество карбоната кальция. Повторяйте, пока твердое вещество не растворится и не останется небольшое количество нерастворенного твердого вещества.
- Отфильтруйте этот раствор и утилизируйте фильтровальную бумагу.
- Осторожно нагрейте полученную жидкость. Вы должны получить небольшое количество твердого вещества.
Наблюдения
В первой реакции (соляная кислота с гидроксидом натрия) полученный раствор был прозрачным. Когда этот раствор нагревали, было отмечено небольшое количество белого порошка. Этот порошок — хлорид натрия.
Во второй реакции (серная кислота с оксидом меди (II)) полученный раствор был синего цвета. Когда этот раствор нагревали, было отмечено небольшое количество белого порошка. Этот порошок сульфат меди.
В третьей реакции (соляная кислота с карбонатом кальция) полученный раствор был прозрачным.Когда этот раствор нагревали, было отмечено небольшое количество белого порошка. Этот порошок сульфат кальция.
Попробуйте написать уравнения реакций для трех реакций выше.
Заключение
Мы использовали кислотно-основные реакции для получения различных солей.
Кислоты и основания
Упражнение 13.6\ (\ text {HNO} _ {3} \) и \ (\ text {Ca} (\ text {OH}) _ {2} \)
Кислота и гидроксид металла
\ (2 \ text {HNO} _ {3} \ text {(aq)} + \ text {Ca (OH)} _ {2} \ text {(aq)} \ rightarrow \ text {Ca (NO} _ {3} \ text {)} _ {2} \ text {(aq)} + 2 \ text {H} _ {2} \ text {O (l)} \)
\ (\ text {HCl} \) и \ (\ text {BeO} \)
Кислота и оксид металла
\ (2 \ text {HCl (aq)} + \ text {BeO (aq)} \ rightarrow \ text {BeCl} _ {2} \ text {(aq)} + \ text {H} _ {2} \ текст {O (l)} \)
\ (\ text {HI} \) и \ (\ text {K} _ {2} \ text {CO} _ {3} \)
Кислота и карбонат
\ (2 \ text {HI (aq)} + \ text {K} _ {2} \ text {CO} _ {3} \ text {(aq)} \ rightarrow 2 \ text {KI (aq)} + \ text {H} _ {2} \ text {O (l)} + \ text {CO} _ {2} \ text {(g)} \)
\ (\ text {H} _ {3} \ text {PO} _ {4} \) и \ (\ text {KOH} \)
Кислота и гидроксид металла
\ (\ text {H} _ {3} \ text {PO} _ {4} \ text {(aq)} + 3 \ text {KOH (aq)} \ rightarrow \ text {K} _ {3} { PO} _ {4} \ text {(aq)} + 3 \ text {H} _ {2} \ text {O (l)} \)
\ (\ text {HCl} \) и \ (\ text {MgCO} _ {3} \)
Кислота и карбонат
\ (2 \ text {HCl (aq)} + \ text {MgCO} _ {3} \ text {(aq)} \ rightarrow \ text {MgCl} _ {2} \ text {(aq)} + \ text {H} _ {2} \ text {O (l)} + \ text {CO} _ {2} \ text {(g)} \)
\ (\ text {HNO} _ {3} \) и \ (\ text {Al} _ {2} \ text {O} _ {3} \)
Кислота и оксид металла
\ (6 \ text {HNO} _ {3} \ text {(aq)} + \ text {Al} _ {2} \ text {O} _ {3} \ text {(aq)} \ rightarrow 2 \ text {Al (NO} _ {3} \ text {)} _ {3} \ text {(aq)} + 3 \ text {H} _ {2} \ text {O (l)} \)
,Кислотно-основная реакция , тип химического процесса, характеризуемого обменом одного или нескольких ионов водорода, H + , между разновидностями, которые могут быть нейтральными (молекулы, такие как вода , H 2 O или уксусная кислота, CH 3 CO 2 H) или электрически заряженные (ионы, такие как аммоний, NH 4 + ; гидроксид, OH — или карбонат CO (3 ( (2-)).Это также включает аналогичное поведение молекул и ионов, которые являются кислотными, но не выделяют ионы водорода (хлорид алюминия, AlCl 3 и ион серебра AG + ).
сульфат натрия Сульфат натрия, также называемый глауберовой солью, является, как и другие соли, продуктом кислотно-щелочной реакции. Мартин УокерПопулярные вопросы
Что такое кислоты и основания?
Кислоты — это вещества, которые содержат один или несколько атомов водорода, которые в растворе выделяются в виде положительно заряженных ионов водорода.Кислота в водном растворе имеет кислый вкус, меняет цвет голубой лакмусовой бумаги на красный, реагирует с некоторыми металлами (например, железом) с выделением водорода, реагирует с основаниями с образованием солей и способствует определенным химическим реакциям (кислотный катализ). Основы — это вещества, которые имеют горький вкус и меняют цвет красной лакмусовой бумаги на синий. Основания реагируют с кислотами с образованием солей и способствуют определенным химическим реакциям (базовый катализ).
Как измеряются кислоты и основания?
Кислоты и основания имеют значение от 0 до 14, значение pH, в соответствии с их относительной силой.Чистая вода, которая является нейтральной, имеет рН 7. Раствор с рН менее 7 считается кислотным, а раствор с рН более 7 считается щелочным или щелочным. Сильные кислоты имеют более высокую концентрацию ионов водорода, и им присвоены значения ближе к 0. И наоборот, сильные основания имеют более высокие концентрации гидроксид-ионов, и им присвоены значения ближе к 14. Более слабые кислоты и основания ближе к значению pH 7, чем их более сильные аналоги.
Что происходит во время кислотно-щелочной реакции?
Кислотно-щелочная реакция представляет собой тип химической реакции, которая включает обмен одним или несколькими ионами водорода, H + , между видами, которые могут быть нейтральными (молекулы, такие как вода, H 2 O) или электрически заряженный (ионы, такие как аммоний, NH 4 + ; гидроксид, OH — ; или карбонат, CO 3 2-).Он также включает в себя аналогичные процессы, которые происходят в молекулах и ионах, которые являются кислыми, но не отдают ионы водорода.
Как кислоты и основания нейтрализуют друг друга (или нейтрализуют друг друга)?
Различные реакции дают разные результаты. Реакции между сильными кислотами и сильными основаниями разлагаются более полно на ионы водорода (протоны, положительно заряженные ионы) и анионы (отрицательно заряженные ионы) в воде. Для слабой кислоты и слабого основания более подходящим считается нейтрализация, включающая прямой перенос протона из кислоты в основание.Если один из реагентов присутствует в большом избытке, реакция может дать соль (или ее раствор), которая может быть кислотной, основной или нейтральной в зависимости от силы кислот и оснований, взаимодействующих друг с другом.
Кислоты — это химические соединения, которые в водном растворе проявляют острый вкус, коррозионное воздействие на металлы и способность окрашивать некоторые синие растительные красители в красный. Основы — это химические соединения, которые в растворе становятся мыльными на ощупь и окрашивают красными растительными красителями в синий. При смешивании кислоты и основания нейтрализуют друг друга и образуют соли, вещества с соленым вкусом и без характерных свойств кислот или оснований.
Идея о том, что некоторые вещества являются кислотами, тогда как другие являются основаниями, почти так же стара, как химия, и термины кислота , основание и соль встречаются очень рано в трудах средневековых алхимиков. Кислоты, вероятно, были первыми из них, очевидно, из-за их кислого вкуса. Английское слово acid , французское acide , немецкое Säure и русское kislota все происходят от слов, означающих кислый (латинский acidus , немецкий sauer , древнескандинавский sūur , и Русская кислая ).Другими свойствами, связанными с кислотами на раннем этапе, были их растворяющее или коррозийное действие; их влияние на растительные красители; и вспенивание, возникающее при нанесении на мел (образование пузырьков углекислого газа). Основания (или щелочи) характеризовались, главным образом, своей способностью нейтрализовать кислоты и образовывать соли, причем последние довольно слабо характеризуются как кристаллические вещества, растворимые в воде и имеющие солевой вкус.
Несмотря на их неточную природу, эти идеи послужили корреляцией значительного диапазона качественных наблюдений, и многие из наиболее распространенных химических материалов, с которыми сталкивались ранние химики, могли быть классифицированы как кислоты (соляная, серная, азотная и углекислота), основания (сода, калий, известь, аммиак) или соли (поваренная соль, аммиачная соль, селитра, квасцы, бура).Отсутствие какой-либо видимой физической основы для рассматриваемых явлений затрудняло количественный прогресс в понимании кислотно-основного поведения, но способность фиксированного количества кислоты нейтрализовать фиксированное количество основания была одним из самых ранних примеров химической эквивалентности : идея, что определенная мера одного вещества в некотором химическом смысле равна другому количеству второго вещества. Кроме того, довольно рано было обнаружено, что одна кислота может быть вытеснена из соли другой кислотой, и это позволило расположить кислоты в приблизительном порядке силы.Вскоре также стало ясно, что многие из этих смещений могут иметь место в любом направлении в соответствии с условиями эксперимента. Это явление указывает на то, что кислотно-основные реакции являются обратимыми, то есть продукты реакции могут взаимодействовать для регенерации исходного материала. Он также ввел концепцию равновесия в кислотно-щелочной химии: эта концепция утверждает, что обратимые химические реакции достигают точки равновесия, или равновесия, при котором исходные материалы и продукты каждый регенерируют в одной из двух реакций так же быстро, как и они. потребляются другим.
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 года с вашей подпиской. Подпишитесь сегодняПомимо теоретического интереса, кислоты и основания играют большую роль в промышленной химии и в повседневной жизни. Серная кислота и гидроксид натрия относятся к числу продуктов, производимых в больших количествах химической промышленностью, и большой процент химических процессов включает кислоты или основания в качестве реагентов или катализаторов. Почти каждый биологический химический процесс тесно связан с кислотно-основным равновесием в клетке или в организме в целом, а кислотность или щелочность почвы и воды имеют большое значение для растений или животных, живущих в них.И идеи, и терминология кислотно-щелочной химии проникли в повседневную жизнь, и термин соль особенно распространен.

