Оксид хрома(III), химические свойства, получение
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s 2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s 1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t° кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
ICSC 1531 — ОКСИД ХРОМА (III)
ICSC 1531 — ОКСИД ХРОМА (III)| ОКСИД ХРОМА (III) | ICSC: 1531 (Октябрь 2004) |
| CAS #: 1308-38-9 |
| EINECS #: 215-160-9 |
| ОСОБЫЕ ОПАСНОСТИ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ТУШЕНИЕ ПОЖАРА | |
|---|---|---|---|
| ПОЖАР И ВЗРЫВ | Не горючее. |
В случае возникновения пожара в рабочей зоне, использовать надлежащие средства пожаротушения. |
| НЕ ДОПУСКАТЬ ОБРАЗОВАНИЕ ПЫЛИ! | |||
|---|---|---|---|
| СИМПТОМЫ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ПЕРВАЯ ПОМОЩЬ | |
| Вдыхание | Кашель. | Применять местную вытяжку или средства защиты органов дыхания. | Свежий воздух, покой. |
| Кожа | Защитные перчатки. | Промыть кожу большим количеством воды или принять душ. | |
| Глаза | Покраснение. | Использовать защитные очки. | Прежде всего промыть большим количеством воды в течение нескольких минут (снять контактные линзы, если это возможно сделать без затруднений), затем обратится за медицинской помощью. |
| Проглатывание | Не принимать пищу, напитки и не курить во время работы. | Прополоскать рот. | |
| ЛИКВИДАЦИЯ УТЕЧЕК | КЛАССИФИКАЦИЯ И МАРКИРОВКА |
|---|---|
| Индивидуальная защита: Респиратор с сажевым фильтром, подходящий для концентрации вещества в воздухе. Смести просыпанное вещество в закрытые контейнеры. При необходимости, сначала намочить, чтобы избежать появления пыли. |
Согласно критериям СГС ООН Транспортировка |
| ХРАНЕНИЕ | |
| УПАКОВКА | |
Исходная информация на английском языке подготовлена группой международных экспертов, работающих от имени МОТ и ВОЗ при финансовой поддержке Европейского Союза. |
| ОКСИД ХРОМА (III) | ICSC: 1531 |
| ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА | |
|---|---|
|
Агрегатное Состояние; Внешний Вид
Физические опасности
Химические опасности
|
Формула: Cr2O3 |
| ВОЗДЕЙСТВИЕ НА ОРГАНИЗМ И ЭФФЕКТЫ ОТ ВОЗДЕЙСТВИЯ | |
|---|---|
|
Пути воздействия
Эффекты от кратковременного воздействия
|
Риск вдыхания
Эффекты от длительного или повторяющегося воздействия
|
| Предельно-допустимые концентрации |
|---|
|
TLV: (как Cr(III), ингаляционная фракция): 0.003 mg/m3, как TWA. EU-OEL: (как Cr(III)): 2 mg/m3 как TWA |
| ОКРУЖАЮЩАЯ СРЕДА |
|---|
| ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ |
|---|
|
Классификация ЕС |
| (ru) | Ни МОТ, ни ВОЗ, ни Европейский Союз не несут ответственности за качество и точность перевода или за возможное использование данной информации. © Версия на русском языке, 2018 |
Оксид хрома 3 валентный г. Казань — ПО Трубное решение
Оксид хрома 3
Оксид хрома 3 – это бинарное соединение положительно заряженного металла хрома со степенью окисления 3 и отрицательно заряженного аниона кислорода со степенью окисления 2. Внешне вещество представляет собой кристаллы хаотичной формы светло-зеленого цвета (при недостаточной степени очистки вещество может иметь темный оттенок зеленого).
Вещество не растворяется в воде, нерастворимо в спиртах (этиловый и метиловый спирт), в ацетоне вещество также не растворяется. Оксид хрома 3 достаточно активно реагирует с кислотами и щелочами. Вещество относят к третьему классу опасности (вещество представляет малую опасность для живых организмов). Единственное, что нужно учитывать при работе с веществом, так это то, что если оно попадет в пищевод в концентрации более 5 грамма, оно вызовет химическое отравление (повышение температуры тела, рвота, диарея). Поэтому следует иметь защитные перчатки при работе с порошком вещества.
Поэтому следует иметь защитные перчатки при работе с порошком вещества.
Химические характеристики
Оксид хрома 3 встречается в природной среде в виде минералов под названиями: калит, нитрит, магнитит (концентрация вещества в минералах порядка 1-3 процентов, остальное примеси других химических элементов). В искусственных условиях вещество получают посредством термического разложения дихромата аммония, также вещество можно получить посредством термического разложения дихромата калия или натрия. Молекулярная масса вещества составляет 152 грамма на моль, плотность вещества составляет 5,2-5,25 грамма на кубический сантиметр. Температура плавления вещества составляет 2450 градусов, температура разложения вещества составляет 4100-4200 градусов (вещество разлагается на металлический хром и молекулярный кислород).
Применение
Вещество активно применяется в качестве пигмента при производстве зеленой краски. Вещество применяют в качестве абразива при производстве полирующих паст. Оксид хрома применяется в производстве пиротехнических смесей (ускоряет протекание реакции окисления топлива в составе и придает пламени зеленоватый оттенок). Также вещество используется при производстве ракетного топлива в качестве катализаторов окисления топлива.
Оксид хрома применяется в производстве пиротехнических смесей (ускоряет протекание реакции окисления топлива в составе и придает пламени зеленоватый оттенок). Также вещество используется при производстве ракетного топлива в качестве катализаторов окисления топлива.
Условия доставки продукции: «Оксид хрома 3» в Казани
- Доставка по Татарстану и в другие регионы РФ осуществляется транспортными компаниями на выгодных для заказчика условиях.
- Доставка в Казани осуществляется с ближайшего к заказчику склада.
- Есть возможность самовывоза приобретенной продукции.
Условия реализации в Казани
- Компания «Трубное Решение» может поставить оптом и в розницу практически все позиции из каталога.
- Оплата осуществляется как безналичным способом, так и наличными средствами.
- Постоянным клиентам можем предложить отсрочку.
- Если вам нужна металлопродукция нестандартных размеров или редких марок стали, можем организовать производство.

- Организуем упаковку товара по стандартам.
Гарантии
- Продукция имеет все необходимые сертификаты.
- Соответствует нормативным документам.
- Гарантируем возврат товара в случае обнаружения факта поставки брака.
Получение и свойства оксида хрома
Получение и свойства оксида хрома (VI). 1. В стакан вместимостью 50 мл поместите 5 г дихромата калия и растворите его в 12—13 мл воды. В мерный цилиндр осторожно налейте 20 мл концентрированной серной кислоты и при [c.151]Получение и свойства оксида хрома (П1). 1. Приготовьте смесь, состоящую из измельченных дихромата калия (2,5 г) и серы (0,5 г). Смесь насыпьте в фарфоровый тигель, установите его в фарфоровый треугольник в вытяжном шкафу и нагрейте на пламени газовой горелки. Реакция взаимодействия К2СГ2О7 с серой экзотермична, поэтому, когда [c.149]
ПОЛУЧЕНИЕ И СВОЙСТВА ОКСИДА ХРОМА (III) [c.
 332]
332]Опыт 2. Получение и свойства оксида хрома (111) [c.229]
III). Гидроксиды железа (II) и (III). Их свойства. Комплексные соединения железа. Химические реакции, лежащие в основе получения чугуна и стали. Роль железа и его сплавов в технике. Хром, электронная формула, степени окисления. Получение, физические и химические свойства хрома. Оксиды хрома (II) и (III). Гидроксиды хрома (II) и (III). Их свойства. Оксид хрома (VI). Хромовая и дихромовая кислоты. Дихромат калия как окислитель. Марганец, злектронная формула, степени окисления. Получение, физические и химические свойства марганца. Кислотно-основные и окислительно-восстановительные свойства соединений марганца. Оксиды марганца (II) и [c.9]
Каковы физические свойства и способы получения оксида хрома (VI) [c.259]
Получение оксида хрома (IV) проводят осторожным окислением Сгг(3з под давлением кислорода. Диоксид хрома проявляет способность сохранять однажды сообщенную ему намагниченность (ферромагнитные свойства). [c.451]
[c.451]
Указать способы получения и свойства оксидов и гидроксидов хрома.. [c.261]
Опыт 4. Получение оксида хрома (III) и его свойства (ТЯГА ). [c.132]
Общая характеристика металлов физические и химические свойства. Общие способы получения металлов. Электрохимический ряд напряжений металлов. Общая характеристика 1А-и ПА-групп периодической системы. Свойства натрия, калия, кальция и магния и их соединений. Жесткость воды и способы ее устранения. Свойства алюминия и его соединений. Свойства оксидов и гидроксидов хрома (+2), (+3), хроматов и дихроматов. Свойства перманганата калия восстановление перманганат-иона в кислой, нейтральной и щелочной средах. Свойства железа, оксидов и гидроксидов железа (+2) и (+3). Свойства соединений меди (+1) и (+2). Свойства оксида и гидроксида цинка. Медико-биоло-гическое значение соединений указанных металлов. [c.757]
Пигментный оксид хрома По химическому составу этот пигмент представляет собой оксид хрома СггОз Цвет — оливково-зеленый с оттенками от желтоватого до синеватого Цвет и пигментные свойства зависят от условий получения [c. 320]
320]
Процесс получения новых носителей включал ряд операций осаждения и гелеобразования, которые широко применимы к оксидной системе или системе смешанных оксидов. В процессе золь — гель [23] коллоидальный золь оксидов или гидроксидов металлов превращается в полутвердый гель удалением воды, нейтрализацией основанием или экстракцией кислого компонента растворителем. Затем гель сушат и прокаливают с получением оксида металла. На стадии гелеобразования определяется конечная поверхность, распределение пор по радиусам и структура. В последние годы активно исследуется применимость технологии золь — гель для получения оксидов металлов [24, 35], используемых в топливных элементах (стержнях) или других ядерных материалах. В результате этой работы в настоящее время возможно изготовление оксидов алюминия, титана, циркония, хрома, железа, редкоземельных элементов и их смесей с хорошо контролируемыми физическими свойствами. [c.52]
Простое вещество.
 Белый, легкий, пластичный. Пассивируется в воде и концентрированной азотной кислоте из-за образования устойчивой оксидной пленки. Амальгамированный металл энергично реагирует с водой. Реакционноспособный, в ряду напряжений стоит значительно левее водорода. Проявляет амфотерные свойства, реагирует с кислотами и щелочами. Сильный восстановитель, реагирует с неметаллами, оксидами металлов. Катион А1 + в растворе — бесцветный аквакомплекс [Al(h30)ef+. Применяется как компонент легких и электропроводящих сплавов, реагент в алюминотермических методах получения металлов (хром, ванадий и др.) и термитной сварке стальных конструкций. [c.137]
Белый, легкий, пластичный. Пассивируется в воде и концентрированной азотной кислоте из-за образования устойчивой оксидной пленки. Амальгамированный металл энергично реагирует с водой. Реакционноспособный, в ряду напряжений стоит значительно левее водорода. Проявляет амфотерные свойства, реагирует с кислотами и щелочами. Сильный восстановитель, реагирует с неметаллами, оксидами металлов. Катион А1 + в растворе — бесцветный аквакомплекс [Al(h30)ef+. Применяется как компонент легких и электропроводящих сплавов, реагент в алюминотермических методах получения металлов (хром, ванадий и др.) и термитной сварке стальных конструкций. [c.137] В книге излагаются теоретические основы процессов получения комбинированных (композиционных) электрохимических покрытий, которые состоят из металла и оксидов, боридов и других включений.. Приведены формулы для расчета состава суспензий, типовые рецептуры и описаны свойства комбинированных покрытий на основе цинка, кадмия, олова, свинца, хрома, кобальта, железа, никеля, меди, серебра и золота. [c.2]
[c.2]
Взаимодействие хрома с кислотами. 2. Получение и свойства оксида хрома (III). 3. Полученйе и свойства гидроксида хроиа (III). [c.10]
В связи с этим свойства окислов металлов часто меняются в зависимости от того, берется ли для реакции свежеприготоалгнний окисел, полученный разложением веществ и не имеющий упорядоченной кристаллической структуры, или же окисел, который был расплавлен и затем закристаллизован. Так, кристаллический оксид алюминия или оксид хрома (111), железа (III) практически нерастворимы пи в кислотах, ни в щелочах, хотя полученные в мелкокристаллическом или аморфном виде довольно легко вступают в эти реакции. [c.224]
Этот тип сырья получают в ходе трех основных процессов, один из которых использует природную основу, а два других — нефтехимическую. Метиловые эфиры, выделяемые непосредственно из жиров и масел, в промышленности восстанавливаются до жирных спиртов гидрированием (с использованием оксидамеди(П)/хромита меди(П) в качестве катализатора) при повышенной температуре и давлении (290 °С, 20,7 МПа) [21-23]. При таких условиях процесса ненасыщенность исходных метиловых эфиров не сохраняется — конечными продуктами являются насыщенные спирты. Интерес для производства ПАВ представляют условия, ири которых ненасыщенные эфиры могли бы быть восстановлены до ненасыщенных спиртов без потери непредельности. Были специально смоделированы кадмиймодифицированные катализаторы. Так, например, с использованием комплексного катализатора высокой активности алюминий/кадмий/ хром оксидов при температуре 270-290 °С и давлении 19,3 МПа с высоким выходом был получен спирт из сложного эфира, с практически полным сохранением исходной непредельности [21]. При этом встал вопрос об использовании шестивалентного хрома в составе комплексного катализатора, поскольку из-за токсичности возникли серьезные проблемы при его производстве, использовании и продаже. Они были решены разработкой катализатора металлическая медь/железо/оксид алюминия, который обладает такой же активностью и лучшими технологическими фильтрационными свойствами [24].
При таких условиях процесса ненасыщенность исходных метиловых эфиров не сохраняется — конечными продуктами являются насыщенные спирты. Интерес для производства ПАВ представляют условия, ири которых ненасыщенные эфиры могли бы быть восстановлены до ненасыщенных спиртов без потери непредельности. Были специально смоделированы кадмиймодифицированные катализаторы. Так, например, с использованием комплексного катализатора высокой активности алюминий/кадмий/ хром оксидов при температуре 270-290 °С и давлении 19,3 МПа с высоким выходом был получен спирт из сложного эфира, с практически полным сохранением исходной непредельности [21]. При этом встал вопрос об использовании шестивалентного хрома в составе комплексного катализатора, поскольку из-за токсичности возникли серьезные проблемы при его производстве, использовании и продаже. Они были решены разработкой катализатора металлическая медь/железо/оксид алюминия, который обладает такой же активностью и лучшими технологическими фильтрационными свойствами [24]. [c.14]
[c.14]
Порошок карбида вольфрама W , по твердости близкого к алмазу, служит для получения металлокерамических пластинок с кобальтом в качестве связующего. Такие пластинки (марка WK-6) употребляют для изготовления режущего инструмента (резцов, сверл, фрез), способных обрабатывать самые твердые материалы. Карбид хрома СгдСг в сплаве с никелем тоже обладает высокими режущими свойствами. Поверхность стали, содержащей хром, сильно упрочняется за счет образования на ней карбидов или нитридов. Оксид хрома (И1) служит для полирования и шлифования различных изделий, употребляется в производстве искусственных рубинов (гл. XI, 3). Хроматы и бихроматы используются в качестве окислителей. Смесь бихромата калия с серной кислотой (хромовая смесь) применяется для очистки химической посуды от загрязнений. [c.340]
Оксиды. Марганец образует большой набор оксидов МпО, МП3О4, Мп Оз, МпО , МП2О7. Все оксиды, кроме Мп Оу, представляют собой кристаллические соединения, практически нерастворимые в воде. В целом оксиды марганца похожи на оксиды хрома, и мы не будем останавливаться на них подробно, но отметим некоторые свойства высших оксидов. Два высших оксида МпО и МП2О7 обладают сильными окислительными свойствами. Диоксид марганца — устойчивое малорастворимое вещество темно-бурого цвета — часто используется в лабораторной практике как сильный окислитель, например, для получения хлора при взаимодействии с соляной кислотой [c.351]
В целом оксиды марганца похожи на оксиды хрома, и мы не будем останавливаться на них подробно, но отметим некоторые свойства высших оксидов. Два высших оксида МпО и МП2О7 обладают сильными окислительными свойствами. Диоксид марганца — устойчивое малорастворимое вещество темно-бурого цвета — часто используется в лабораторной практике как сильный окислитель, например, для получения хлора при взаимодействии с соляной кислотой [c.351]
СТЕКЛО (обыкновенное, неорганическое, силикатное) — прозрачный аморфный сплав смеси различных силикатов или силикатов с диоксидом кремния. Сырье для производства стекла должно содержать основные стеклообразующие оксиды 510а, В Оз, Р2О5 и дополнительно оксиды щелочных, щелочноземельных и других металлов. Необходимые для производства С. материалы — кварцевый песок, борная кислота, известняк, мел, сода, сульфат натрия, поташ, магнезит, каолин, оксиды свинца, сульфат или карбонат бария, полевые шпаты, битое стекло, доменные шлаки и др. Кроме того, при варке стекла вводят окислители — натриевую селитру, хлорид аммония осветлители — для удаления газов — хлорид натрия, триоксид мышьяка обесцвечивающие вещества — селен, соединения кобальта и марганца, дополняющие цвет присутствующих оксидов до белого для получения малопрозрачного матового, молочного, опалового стекла или эмалей — криолит, фторид кальция, фосфаты, соединения олова красители — соединения хрома, кадмия, селена, никеля, кобальта, золота и др. Общий состав обыкновенного С. можно выразить условно формулой N3,0-СаО X X65102. Свойства С. зависят от химического состава, условий варки и дальнейшей обработки. [c.237]
Кроме того, при варке стекла вводят окислители — натриевую селитру, хлорид аммония осветлители — для удаления газов — хлорид натрия, триоксид мышьяка обесцвечивающие вещества — селен, соединения кобальта и марганца, дополняющие цвет присутствующих оксидов до белого для получения малопрозрачного матового, молочного, опалового стекла или эмалей — криолит, фторид кальция, фосфаты, соединения олова красители — соединения хрома, кадмия, селена, никеля, кобальта, золота и др. Общий состав обыкновенного С. можно выразить условно формулой N3,0-СаО X X65102. Свойства С. зависят от химического состава, условий варки и дальнейшей обработки. [c.237]
В смешанных катализаторах, в которых компоненты находятся в соизмеримых количествах, могут образоваться новые, более активные соединения. При этом свойства смешанного катализатора не являются простой суммой свойств его компонентов. К числу модификаторов можно отнести и носители (трегеры), особенно часто применяемые для получения дорогостоящих металлических катализаторов (Р1, Р(1, N1, Со).
 Роль носителей состоит в повышении активной поверхностп, увеличении термостойкости и механической прочности катализатора и т. п. В качестве носителей используют алюмосиликаты, оксиды алюминия, хрома или кремния, активированный уголь, пемзу, кизельгур и другие природные и синтетические материалы. Так, например, дегидрирование метилциклопен-тана платиной, нанесенной на активированный уголь, ведет к образованию метилциклопентана и пентадиена, а при дегидрировании на Р1-А120з образуются бензол и циклогексан. Носители могут изменять активность и избирательность катализатора и т. п. Следовательно, роль носителя как модификатора свойств катализатора может быть очень большой, и его выбор является существенным при создании оптимального катализатора для данного процесса. [c.442]
Роль носителей состоит в повышении активной поверхностп, увеличении термостойкости и механической прочности катализатора и т. п. В качестве носителей используют алюмосиликаты, оксиды алюминия, хрома или кремния, активированный уголь, пемзу, кизельгур и другие природные и синтетические материалы. Так, например, дегидрирование метилциклопен-тана платиной, нанесенной на активированный уголь, ведет к образованию метилциклопентана и пентадиена, а при дегидрировании на Р1-А120з образуются бензол и циклогексан. Носители могут изменять активность и избирательность катализатора и т. п. Следовательно, роль носителя как модификатора свойств катализатора может быть очень большой, и его выбор является существенным при создании оптимального катализатора для данного процесса. [c.442] Сульфид-ионы, как уже было упомянуто, редко используют в качестве осадителей в весовом анализе из-за их неспецифического осаждающего действия, а также из-за неподходящих для целей весового анализа свойств. Осаждение ионов металлов в виде гидроксидов в большой степени страдает теми же недостатками, но все же находит применение. Примером служит осаждение Ре + и аммиаком. Метод считается наиболее точным для определения этих металлов. Использование аммиака в качестве осадителя имеет то-преимущество, что большая часть двухвалентных катионов, таких, как Си +, N12+, 2п +, 0(1 +, в аммиачной среде образует устойчивые комплексы, которые остаются в растворе. Употребление аммиака, однако, не предотвращает осаждения других трех- и четырехвалентных ионов (Сг +, Т1 +), а при определенных условиях даже и некоторых двухвалентных [например, осаждение Mg(0H)2 в отсутствие избытка солей аммония в растворе]. Иногда при анализе пород и минералов на определенном этапе производится осаждение соответствующих гидроксидов при помощи аммиака, их прокаливание и совместное взвешивание. Полученный результат обозначается как РгОз и представляет собой сумму нескольких оксидов, обычно РегОз + АЬОзТ102-Ь Р2О5, а при наличии в пробе хрома и циркония —еще и оксидов этих, элементов.
Осаждение ионов металлов в виде гидроксидов в большой степени страдает теми же недостатками, но все же находит применение. Примером служит осаждение Ре + и аммиаком. Метод считается наиболее точным для определения этих металлов. Использование аммиака в качестве осадителя имеет то-преимущество, что большая часть двухвалентных катионов, таких, как Си +, N12+, 2п +, 0(1 +, в аммиачной среде образует устойчивые комплексы, которые остаются в растворе. Употребление аммиака, однако, не предотвращает осаждения других трех- и четырехвалентных ионов (Сг +, Т1 +), а при определенных условиях даже и некоторых двухвалентных [например, осаждение Mg(0H)2 в отсутствие избытка солей аммония в растворе]. Иногда при анализе пород и минералов на определенном этапе производится осаждение соответствующих гидроксидов при помощи аммиака, их прокаливание и совместное взвешивание. Полученный результат обозначается как РгОз и представляет собой сумму нескольких оксидов, обычно РегОз + АЬОзТ102-Ь Р2О5, а при наличии в пробе хрома и циркония —еще и оксидов этих, элементов. При необходимости отдельные компоненты смеси оксидов можно определять раздельно. [c.221]
При необходимости отдельные компоненты смеси оксидов можно определять раздельно. [c.221]
Применение. РЗЭ широко применяются в металлургии в качестве раскислителей, дегазаторов и десульфаторов. Введение долей процента мишметалла (52 % Се, 24 % La, 5 % Рг, 18 % Nd и др.) в стали различных марок способствует их очищению от примесей, повышает жаропрочность и сопротивление корро-зи. Сплавы S , легкие и обладающие высокой температурой плавления, служат конструкционными материалами в ракето-и самолетостроении. Сплавы Се с железом, магнием и алюминием отличаются малым коэффициентом расширения и используются в машиностроении при производстве деталей поршневых двигателей. Присадка РЗЭ к чугунам улучшает их механические свойства добавка РЗЭ к сплавам из хрома, никеля и железа практикуется в производстве нагревательных элементов промышленных электропечей. РЗЭ применяются также при изготовлении регулирующих стержней, поглощающих избыточные тепловые нейтроны в ядерных реакторах Gd, Sm, Eu имеют аномально высокие значения сечения захвата нейтронов. Соединения S используются при изготовлении люминофоров, в качестве катализаторов в химической промышленности, в химической технологии ядерного топлива, в нефтеперерабатывающей промышленности для получения катализаторов крекинга нефти, для производства синтетических волокон, пластмасс, для синтеза жидких углеводородов, в цветной металлургии. РЗЭ употребляются для полировки стекла (в виде полирита, состоящего из оксидов Се, La, Nd и Рг), в силикатной промышленности для окрашивания и обесцвечивания стекол, для производства химически- и жаростойких, оптических, устойчивых к рентгеновскому облучению, высокоэлектропроводных и высокопрочных стекол, для окраски фарфора и керамики. рЗЭ применяются также в светотехнике, электронике, радиотехнике, в текстильной и кожевенной промышленности, в производстве ЭВМ, в медицине, рентгенотехнике и т. д. [c.253]
Соединения S используются при изготовлении люминофоров, в качестве катализаторов в химической промышленности, в химической технологии ядерного топлива, в нефтеперерабатывающей промышленности для получения катализаторов крекинга нефти, для производства синтетических волокон, пластмасс, для синтеза жидких углеводородов, в цветной металлургии. РЗЭ употребляются для полировки стекла (в виде полирита, состоящего из оксидов Се, La, Nd и Рг), в силикатной промышленности для окрашивания и обесцвечивания стекол, для производства химически- и жаростойких, оптических, устойчивых к рентгеновскому облучению, высокоэлектропроводных и высокопрочных стекол, для окраски фарфора и керамики. рЗЭ применяются также в светотехнике, электронике, радиотехнике, в текстильной и кожевенной промышленности, в производстве ЭВМ, в медицине, рентгенотехнике и т. д. [c.253]
Таким образом, следует считать, что шероховатость является необходимым, но недостаточным условием получения высокой адгезии металлического покрытия к пластмассе. Надо учитывать влияние на адгезию следующих факторов прочности самой пластмассы, так как разрушение обычно происходит в поверхностном слое пластмассы наличия благоприятных функциональных групп на поверхности присутствия различных промоторов адгезии неорганических, например соединений хрома, и органических, таких, как полярные низкомолекулярные соединения. Кроме того, на адгезию со временем могут оказать отрицательное влияние некоторые вещества, которые, диффундируя к промежуточному слою из глубины пластмассы, разрушают или ослабляют его (например, оксиды азота, если пластмассу травили в азотной кислоте). Существенное влияние имеют природа и условия осаждения металлического покрытия. Благородные металлы (Аи, Ад) образуют слабо связанные с пластмассой покрытия. Медь и никель при больших скоростях осаждения дают прочные сцепления, а при малых — слабо связанные осадки. В итоге можно сказать, что адгезионные и другие физико-мехакическпе свойства металлизированных пластмасс как композицпонного материала зависят от структуры и свойств промежуточного слоя, который играет роль связки.
Надо учитывать влияние на адгезию следующих факторов прочности самой пластмассы, так как разрушение обычно происходит в поверхностном слое пластмассы наличия благоприятных функциональных групп на поверхности присутствия различных промоторов адгезии неорганических, например соединений хрома, и органических, таких, как полярные низкомолекулярные соединения. Кроме того, на адгезию со временем могут оказать отрицательное влияние некоторые вещества, которые, диффундируя к промежуточному слою из глубины пластмассы, разрушают или ослабляют его (например, оксиды азота, если пластмассу травили в азотной кислоте). Существенное влияние имеют природа и условия осаждения металлического покрытия. Благородные металлы (Аи, Ад) образуют слабо связанные с пластмассой покрытия. Медь и никель при больших скоростях осаждения дают прочные сцепления, а при малых — слабо связанные осадки. В итоге можно сказать, что адгезионные и другие физико-мехакическпе свойства металлизированных пластмасс как композицпонного материала зависят от структуры и свойств промежуточного слоя, который играет роль связки. Рен- [c.18]
Рен- [c.18]
Оксид хрома 3 химические свойства. Способ получения оксида хрома (iii)
Гидроксид хрома (II) Cr(ОН) 2 получают в виде желтого осадка, обрабатывая растворы солей хрома (II) щелочами в отсутствие кислорода:
CrСl 2 +2NaOH=Cr(OH) 2 ¯+2NaCl
Cr(OH) 2 обладает типичными основными свойствами и является сильным восстановителем:
2Cr(OH) 2 +H 2 O+1/2O 2 =2Cr(OH) 3 ¯
Водные растворы солей хрома (II) получают без доступа воздуха растворением металлического хрома в разбавленных кислотах в атмосфере водорода или восстановлением цинком в кислой среде солей трехвалентного хрома. Безводные соли хрома (II) белого цвета, а водные растворы и кристаллогидраты — синего цвета.
По своим химическим свойствам соли хрома (II) похожи на соли двухвалентного железа, но отличаются от последних более ярко выраженными восстановительными свойствами, т.е. легче, чем соответствующие соединения двухвалентного железа, окисляются. Именно поэтому очень трудно получать и хранить соединения двухвалентного хрома.
Гидроксид хрома (III) Cr(ОН) 3 — студнеобразный осадок серо-зеленого цвета, его получают при действии щелочей на растворы солей хрома (III):
Cr 2 (SO 4) 3 +6NaOH=2Cr(OH) 3 ¯+3Na 2 SO 4
Гидроксид хрома (III) обладает амфотерными свойствами, растворяясь как в кислотах с образованием солей хрома (III):
2Cr(ОН) 3 +3H 2 SO 4 =Cr 2 (SO 4) 3 +6Н 2 О так и в щелочах с образованием гидроксихромитов: Cr(OH) 3 +NaOH=Na 3
При сплавлении Cr(ОН) 3 с щелочами образуются метахромиты и ортохромиты:
Cr(ОН) 3 +NaOH=NaCrO 2 +2Н 2 O Cr(ОН) 3 +3NaOH=Na 3 CrO 3 +3Н 2 О
При прокаливании гидроксида хрома (III) образуется оксид хрома (III):
2Cr(ОН) 3 =Cr 2 O 3 +3Н 2 O
Соли трехвалентного хрома как в твердом состоянии, так и в водных растворах окрашены. Например, безводный сульфат хрома (III) Cr 2 (SO 4) 3 фиолетово-красного цвета, водные растворы сульфата хрома (III) в зависимости от условий могут менять цвет от фиолетового до зеленого. Это объясняется тем, что в водных растворах катион Cr 3+ существует только в виде гидратированного иона 3+ благодаря склонности трехвалентного хрома к образованию комплексных соединений. Фиолетовый цвет водных растворов солей хрома (III) обусловлен именно катионом 3+ . При нагревании комплексные соли хрома (III) могут
Фиолетовый цвет водных растворов солей хрома (III) обусловлен именно катионом 3+ . При нагревании комплексные соли хрома (III) могут
частично терять воду, образуя соли различного цвета, вплоть до зеленого.
Соли трехвалентного хрома сходны с солями алюминия по составу, строению кристаллической решетки, по растворимости; так, для хрома (III) так же, как и для алюминия, типично образование хромокалиевых квасцов KCr(SO 4) 2 12Н 2 О, их применяют для дубления кож и в качестве протравы в текстильном деле.
Соли хрома (III)Cr 2 (SО 4) 3 , CrСl 3 и т.д. при хранении на воздухе устойчивы, а в растворах подвергаются гидролизу:
Cr 3+ +3Сl — +НОН«Cr(ОН) 2+ +3Сl — +Н +
Гидролиз идет по I ступени, но есть соли, которые гидролизуются нацело:
Cr 2 S 3 +Н 2 O=Cr(OH) 3 ¯+H 2 S
В окислительно-восстановительных реакциях в щелочной среде соли хрома (III) ведут себя как восстановители:
Следует отметить, что в ряду гидроксидов хрома различных степеней окисления Cr(ОН) 2 — Cr(ОН) 3 — Н 2 CrО 4 закономерно происходит ослабление основных свойств и усиление кислотных. Такое изменение свойств обусловлено увеличением степени окисления и уменьшением ионных радиусов хрома. В этом же ряду последовательно усиливаются окислительные свойства. Соединения Cr (II) — сильные восстановители, легко окисляются, превращаясь в соединения хрома (III). Соединения хрома(VI) — сильные окислители, легко восстанавливаются в соединения хрома (III). Соединения с промежуточной степенью окисления, т.е. соединения хрома (III), могут при взаимодействии с сильными восстановителями проявлять окислительные свойства, переходя в соединения хрома (II), а при взаимодействии с сильными окислителями проявлять восстановительные свойства, превращаясь в соединения хрома (VI).
Такое изменение свойств обусловлено увеличением степени окисления и уменьшением ионных радиусов хрома. В этом же ряду последовательно усиливаются окислительные свойства. Соединения Cr (II) — сильные восстановители, легко окисляются, превращаясь в соединения хрома (III). Соединения хрома(VI) — сильные окислители, легко восстанавливаются в соединения хрома (III). Соединения с промежуточной степенью окисления, т.е. соединения хрома (III), могут при взаимодействии с сильными восстановителями проявлять окислительные свойства, переходя в соединения хрома (II), а при взаимодействии с сильными окислителями проявлять восстановительные свойства, превращаясь в соединения хрома (VI).
«Национальный исследовательский Томский политехнический Университет»
Институт природных ресурсов Геоэкология и геохимия
Хром
По дисциплине:
Химия
Выполнил:
студент группы 2Г41 Ткачева Анастасия Владимировна 29.10.2014
Проверил:
преподаватель Стась Николай Федорович
Положение в периодической системе
Хром — элемент
побочной
подгруппы 6-ой группы 4-го периода
периодической
системы химических
элементов Д. И. Менделеева с атомным
номером 24.
Обозначается символом Cr (лат. Chromium ). Простое
вещество хром —
твёрдый металлголубовато-белого цвета.
Хром иногда относят к чёрным
металлам.
И. Менделеева с атомным
номером 24.
Обозначается символом Cr (лат. Chromium ). Простое
вещество хром —
твёрдый металлголубовато-белого цвета.
Хром иногда относят к чёрным
металлам.
Строение атома
17 Cl)2)8)7 — схема строения атома
1s2s2p3s3p- электронная формула
Атом располагается в III периоде, и имеет три энергетических уровня
Атом располагается в VII в группе, в главной подгруппе – на внешнем энергетическом уровне 7 электронов
Свойства элемента
Физические свойства
Хром
— белый блестящий металл
с кубической объемно-центрированной решеткой,
а = 0,28845 нм,
отличающийся твердостью и хрупкостью,
с плотностью 7,2 г/см 3 ,
один из
самых твердых чистых металлов (уступает
только бериллию, вольфраму
и урану),
с температурой плавления 1903 град. И с
температурой кипения около 2570 град. С.
На воздухе поверхность хрома покрывается
оксидной пленкой, которая предохраняет
его от дальнейшего окисления. Добавка
углерода к хрому еще больше увеличивает
его твердость.
Хром при обычных условиях – инертный металл, при нагревании становится довольно активным.
Взаимодействие с неметаллами
При нагревании выше 600°С хром сгорает в кислороде:
4Cr + 3O 2 = 2Cr 2 O 3 .
С фтором реагирует при 350°С, с хлором – при 300°С, с бромом – при температуре красного каления, образуя галогениды хрома (III):
2Cr + 3Cl 2 = 2CrCl 3 .
С азотом реагирует при температуре выше 1000°С с образованием нитридов:
2Cr + N 2 = 2CrN
или 4Cr + N 2 = 2Cr 2 N.
2Cr + 3S = Cr 2 S 3 .
Реагирует с бором, углеродом и кремнием с образованием боридов, карбидов и силицидов:
Cr + 2B = CrB 2 (возможно образование Cr 2 B, CrB, Cr 3 B 4 , CrB 4),
2Cr + 3C = Cr 2 C 3 (возможно образование Cr 23 C 6 , Cr 7 B 3),
Cr + 2Si = CrSi 2 (возможно образование Cr 3 Si, Cr 5 Si 3 , CrSi).
С водородом непосредственно не взаимодействует.
Взаимодействие с водой
В тонкоизмельченном раскаленном состоянии хром реагирует с водой, образуя оксид хрома (III) и водород:
2Cr + 3H 2 O = Cr 2 O 3 + 3H 2
Взаимодействие с кислотами
В электрохимическом ряду напряжений металлов хром находится до водорода, он вытесняет водород из растворов неокисляющих кислот:
Cr + 2HCl = CrCl 2 + H 2 ;
Cr
+ H 2 SO 4 =
CrSO 4 +
H 2 .
В присутствии кислорода воздуха образуются соли хрома (III):
4Cr + 12HCl + 3O 2 = 4CrCl 3 + 6H 2 O.
Концентрированная азотная и серная кислоты пассивируют хром. Хром может растворяться в них лишь при сильном нагревании, образуются соли хрома (III) и продукты восстановления кислоты:
2Cr + 6H 2 SO 4 = Cr 2 (SO 4) 3 + 3SO 2 + 6H 2 O;
Cr + 6HNO 3 = Cr(NO 3) 3 + 3NO 2 + 3H 2 O.
Взаимодействие с щелочными реагентами
В водных растворах щелочей хром не растворяется, медленно реагирует с расплавами щелочей с образованием хромитов и выделением водорода:
2Cr + 6KOH = 2KCrO 2 + 2K 2 O + 3H 2 .
Реагирует с щелочными расплавами окислителей, например хлоратом калия, при этом хром переходит в хромат калия:
Cr + KClO 3 + 2KOH = K 2 CrO 4 + KCl + H 2 O.
Восстановление металлов из оксидов и солей
Хром
– активный металл, способен вытеснять
металлы из растворов их солей:
2Cr + 3CuCl 2 =
2CrCl 3 +
3Cu.
Свойства простого вещества
Устойчив на воздухе за счёт пассивирования. По этой же причине не реагирует с серной и азотной кислотами. При 2000 °C сгорает с образованием зелёного оксида хрома(III) Cr 2 O 3 , обладающего амфотерными свойствами.
Синтезированы соединения хрома с бором (бориды Cr 2 B, CrB, Cr 3 B 4 , CrB 2 , CrB 4 и Cr 5 B 3), с углеродом (карбиды Cr 23 C 6 , Cr 7 C 3 и Cr 3 C 2), c кремнием (силициды Cr 3 Si, Cr 5 Si 3 и CrSi) и азотом (нитриды CrN и Cr 2 N).
Соединения Cr(+2)
Степени окисления +2 соответствует основный оксид CrO (чёрный). Соли Cr 2+ (растворы голубого цвета) получаются при восстановлении солей Cr 3+ или дихроматов цинком в кислой среде («водородом в момент выделения»):
Все эти соли Cr 2+ — сильные восстановители вплоть до того, что при стоянии вытесняют водород из воды. Кислородом воздуха, особенно в кислой среде, Cr 2+ окисляется, в результате чего голубой раствор быстро зеленеет.
Коричневый
или желтый гидроксид Cr(OH) 2 осаждается
при добавлении щелочей к растворам
солей хрома(II).
Синтезированы дигалогениды хрома CrF 2 , CrCl 2 , CrBr 2 и CrI 2
Соединения Cr(+3)
Степени окисления +3 соответствует амфотерный оксид Cr 2 O 3 и гидроксид Cr(OH) 3 (оба — зелёного цвета). Это — наиболее устойчивая степень окисления хрома. Соединения хрома в этой степени окисления имеют цвет от грязно-лилового (ион 3+) до зелёного (в координационной сфере присутствуют анионы).
Cr 3+ склонен к образованию двойных сульфатов вида M I Cr(SO 4) 2 ·12H 2 O (квасцов)
Гидроксид хрома (III) получают, действуя аммиаком на растворы солей хрома (III):
Cr+3NH+3h3O→Cr(OH)↓+3NH
Можно использовать растворы щелочей, но в их избытке образуется растворимый гидроксокомплекс:
Cr+3OH→Cr(OH)↓
Cr(OH)+3OH→
Сплавляя Cr 2 O 3 со щелочами получают хромиты:
Cr2O3+2NaOH→2NaCrO2+h3O
Непрокаленный оксид хрома(III) растворяется в щелочных растворах и в кислотах:
Cr2O3+6HCl→2CrCl3+3h3O
При окислении соединений хрома(III) в щелочной среде образуются соединения хрома(VI):
2Na+3HO→2NaCrO+2NaOH+8HO
То же самое происходит при сплавлении оксида хрома (III) со щелочью и окислителями, или со щелочью на воздухе (расплав при этом приобретает жёлтую окраску):
2Cr2O3+8NaOH+3O2→4Na2CrO4+4h3O
Соединения хрома (+4) [
При
осторожном разложении оксида
хрома(VI) CrO 3 в
гидротермальных условиях получают оксид
хрома(IV) CrO 2 ,
который является ферромагнетикоми
обладает металлической проводимостью.
Среди тетрагалогенидов хрома устойчив CrF 4 , тетрахлорид хрома CrCl 4 существует только в парах.
Соединения хрома (+6)
Степени окисления +6 соответствует кислотный оксид хрома (VI) CrO 3 и целый ряд кислот, между которыми существует равновесие. Простейшие из них — хромовая H 2 CrO 4 и двухромовая H 2 Cr 2 O 7 . Они образуют два ряда солей: желтые хроматы и оранжевые дихроматы соответственно.
Оксид хрома (VI) CrO 3 образуется при взаимодействии концентрированной серной кислоты с растворами дихроматов. Типичный кислотный оксид, при взаимодействии с водой он образует сильные неустойчивые хромовые кислоты: хромовую H 2 CrO 4 , дихромовую H 2 Cr 2 O 7 и другие изополикислоты с общей формулой H 2 Cr n O 3n+1 . Увеличение степени полимеризации происходит с уменьшением рН, то есть увеличением кислотности:
2CrO+2H→Cr2O+h3O
Но если к оранжевому раствору K 2 Cr 2 O 7 прилить раствор щёлочи, как окраска вновь переходит в жёлтую так как снова образуется хромат K 2 CrO 4:
Cr2O+2OH→2CrO+HO
До высокой степени полимеризации, как это происходит у вольфрама и молибдена, не доходит, так как полихромовая кислота распадается на оксид хрома(VI) и воду:
h3CrnO3n+1→h3O+nCrO3
Растворимость
хроматов примерно соответствует
растворимости сульфатов. В частности,
желтый хромат бария BaCrO 4 выпадает
при добавлении солей бария, как к
растворам хроматов, так и к растворам
дихроматов:
В частности,
желтый хромат бария BaCrO 4 выпадает
при добавлении солей бария, как к
растворам хроматов, так и к растворам
дихроматов:
Ba+CrO→BaCrO↓
2Ba+CrO+h3O→2BaCrO↓+2H
Образование кроваво-красного малорастворимого хромата серебра используют для обнаружения серебра в сплавах при помощи пробирной кислоты.
Известны пентафторид хрома CrF 5 и малоустойчивый гексафторид хрома CrF 6 . Также получены летучие оксигалогениды хрома CrO 2 F 2 и CrO 2 Cl 2 (хромилхлорид).
Соединения хрома(VI) — сильные окислители, например:
K2Cr2O7+14HCl→2CrCl3+2KCl+3Cl2+7h3O
Добавление к дихроматам перекиси водорода, серной кислоты и органического растворителя (эфира) приводит к образованию синего пероксида хрома CrO 5 L (L — молекула растворителя), который экстрагируется в органический слой; данная реакция используется как аналитическая.
Хром — элемент побочной подгруппы 6-ой группы 4-го периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 24. Обозначается символом Cr (лат. Chromium). Простое вещество хром- твёрдый металл голубовато-белого цвета.
Обозначается символом Cr (лат. Chromium). Простое вещество хром- твёрдый металл голубовато-белого цвета.
Химические свойства хрома
При обычных условиях хром реагирует только со фтором. При высоких температурах (выше 600°C) взаимодействует с кислородом, галогенами, азотом, кремнием, бором, серой, фосфором.
4Cr + 3O 2 – t° →2Cr 2 O 3
2Cr + 3Cl 2 – t° → 2CrCl 3
2Cr + N 2 – t° → 2CrN
2Cr + 3S – t° → Cr 2 S 3
В раскалённом состоянии реагирует с парами воды:
2Cr + 3H 2 O → Cr 2 O 3 + 3H 2
Хром растворяется в разбавленных сильных кислотах (HCl, H 2 SO 4)
В отсутствии воздуха образуются соли Cr 2+ , а на воздухе – соли Cr 3+ .
Cr + 2HCl → CrCl 2 + H 2
2Cr + 6HCl + O 2 → 2CrCl 3 + 2H 2 O + H 2
Наличие защитной окисной плёнки на поверхности металла объясняет его пассив-ность по отношению к концентрированным растворам кислот – окислителей.
Соединения хромаОксид хрома (II) и гидроксид хрома (II) имеют основной характер.
Cr(OH) 2 + 2HCl → CrCl 2 + 2H 2 O
Соединения хрома (II) — сильные восстановители; переходят в соединения хрома (III) под действием кислорода воздуха.
2CrCl 2 + 2HCl → 2CrCl 3 + H 2
4Cr(OH) 2 + O 2 + 2H 2 O → 4Cr(OH) 3
Оксид хрома (III) Cr 2 O 3 – зелёный, нерастворимый в воде порошок. Может быть получен при прокаливании гидроксида хрома (III) или дихроматов калия и аммония:
2Cr(OH) 3 – t° → Cr 2 O 3 + 3H 2 O
4K 2 Cr 2 O 7 – t° → 2Cr 2 O 3 + 4K 2 CrO 4 + 3O 2
(NH 4) 2 Cr 2 O 7 – t° → Cr 2 O 3 + N 2 + 4H 2 O (реакция «вулканчик»)
Амфотерный оксид. При сплавлении Cr 2 O 3 со щелочами, содой и кислыми солями получаются соединения хрома со степенью окисления (+3):
Cr 2 O 3 + 2NaOH → 2NaCrO 2 + H 2 O
Cr 2 O 3 + Na 2 CO 3 → 2NaCrO 2 + CO 2
При сплавлении со смесью щёлочи и окислителя получают соединения хрома в степени окисления (+6):
Cr 2 O 3 + 4KOH + KClO 3 → 2K 2 CrO 4 + KCl + 2H 2 O
Гидроксид хрома (III) С r (ОН) 3 . Амфотерный гидроксид. Серо-зеленый, разлагается при нагревании, теряя воду и образуя зеленый метагидроксид СrО(ОН). Не растворяется в воде. Из раствора осаждается в виде серо-голубого и голубовато-зеленого гидрата. Реагирует с кислотами и щелочами, не взаимодействует с гидратом аммиака.
Амфотерный гидроксид. Серо-зеленый, разлагается при нагревании, теряя воду и образуя зеленый метагидроксид СrО(ОН). Не растворяется в воде. Из раствора осаждается в виде серо-голубого и голубовато-зеленого гидрата. Реагирует с кислотами и щелочами, не взаимодействует с гидратом аммиака.
Обладает амфотерными свойствами — растворяется как в кислотах, так и в щелочах:
2Cr(OH) 3 + 3H 2 SO 4 → Cr 2 (SO 4) 3 + 6H 2 O Сr(ОН) 3 + ЗН + = Сr 3+ + 3H 2 O
Cr(OH) 3 + KOH → K , Сr(ОН) 3 + ЗОН — (конц.) = [Сr(ОН) 6 ] 3-
Cr(OH) 3 + KOH → KCrO 2 +2H 2 O Сr(ОН) 3 + МОН = МСrO 2(зел.) + 2Н 2 O (300-400 °С, М = Li, Na)
Сr(ОН) 3 →(120 o C – H 2 O ) СrO(ОН) →(430-1000 0 С – H 2 O ) Cr 2 O 3
2Сr(ОН) 3 + 4NаОН (конц.) + ЗН 2 O 2(конц.) =2Na 2 СrO 4 + 8Н 2 0
Получение : осаждение гидратом аммиака из раствора солей хрома(Ш):
Сr 3+ + 3(NH 3 Н 2 O) = С r (ОН) 3 ↓ + ЗNН 4+
Cr 2 (SO 4) 3 + 6NaOH → 2Cr(OH) 3 ↓+ 3Na 2 SO 4 (в избытке щелочи — осадок растворяется)
Соли хрома (III) имеют фиолетовую или тёмно-зелёную окраску. По химическим свойствам напоминают бесцветные соли алюминия.
По химическим свойствам напоминают бесцветные соли алюминия.
Соединения Cr (III) могут проявлять и окислительные, и восстановительные свойства:
Zn + 2Cr +3 Cl 3 → 2Cr +2 Cl 2 + ZnCl 2
2Cr +3 Cl 3 + 16NaOH + 3Br 2 → 6NaBr + 6NaCl + 8H 2 O + 2Na 2 Cr +6 O 4
Соединения шестивалентного хрома
Оксид хрома (VI) CrO 3 — ярко-красные кристаллы, растворимые в воде.
Получают из хромата (или дихромата) калия и H 2 SO 4 (конц.).
K 2 CrO 4 + H 2 SO 4 → CrO 3 + K 2 SO 4 + H 2 O
K 2 Cr 2 O 7 + H 2 SO 4 → 2CrO 3 + K 2 SO 4 + H 2 O
CrO 3 — кислотный оксид, со щелочами образует жёлтые хроматы CrO 4 2- :
CrO 3 + 2KOH → K 2 CrO 4 + H 2 O
В кислой среде хроматы превращаются в оранжевые дихроматы Cr 2 O 7 2- :
2K 2 CrO 4 + H 2 SO 4 → K 2 Cr 2 O 7 + K 2 SO 4 + H 2 O
В щелочной среде эта реакция протекает в обратном направлении:
K 2 Cr 2 O 7 + 2KOH → 2K 2 CrO 4 + H 2 O
Дихромат калия – окислитель в кислой среде:
К 2 Сr 2 O 7 + 4H 2 SO 4 + 3Na 2 SO 3 = Cr 2 (SO 4) 3 + 3Na 2 SO 4 + K 2 SO 4 + 4H 2 O
K 2 Cr 2 O 7 + 4H 2 SO 4 + 3NaNO 2 = Cr 2 (SO 4) 3 + 3NaNO 3 + K 2 SO 4 + 4H 2 O
K 2 Cr 2 O 7 + 7H 2 SO 4 + 6KI = Cr 2 (SO 4) 3 + 3I 2 + 4K 2 SO 4 + 7H 2 O
K 2 Cr 2 O 7 + 7H 2 SO 4 + 6FeSO 4 = Cr 2 (SO 4) 3 + 3Fe 2 (SO 4) 3 + K 2 SO 4 + 7H 2 O
Хромат калия К 2 Cr О 4 . Оксосоль. Желтый, негигроскопичный. Плавится без разложения, термически устойчивый. Хорошо растворим в воде (желтая окраска раствора отвечает иону СrO 4 2-), незначительно гидролизуется по аниону. В кислотной среде переходит в К 2 Cr 2 O 7 . Окислитель (более слабый, чем К 2 Cr 2 O 7). Вступает в реакции ионного обмена.
Оксосоль. Желтый, негигроскопичный. Плавится без разложения, термически устойчивый. Хорошо растворим в воде (желтая окраска раствора отвечает иону СrO 4 2-), незначительно гидролизуется по аниону. В кислотной среде переходит в К 2 Cr 2 O 7 . Окислитель (более слабый, чем К 2 Cr 2 O 7). Вступает в реакции ионного обмена.
Качественная реакция на ион CrO 4 2- — выпадение желтого осадка хромата бария, разлагающегося в сильнокислотной среде. Применяется как протрава при крашении тканей, дубитель кож, селективный окислитель, реактив в аналитической химии.
Уравнения важнейших реакций:
2K 2 CrO 4 +H 2 SO 4(30%)= K 2 Cr 2 O 7 +K 2 SO 4 +H 2 O
2K 2 CrO 4(т) +16HCl (кон ц., гор.) =2CrCl 3 +3Cl 2 +8H 2 O+4KCl
2K 2 CrO 4 +2H 2 O+3H 2 S=2Cr(OH) 3 ↓+3S↓+4KOH
2K 2 CrO 4 +8H 2 O+3K 2 S=2K[Сr(ОН) 6 ]+3S↓+4KOH
2K 2 CrO 4 +2AgNO 3 =KNO 3 +Ag 2 CrO 4(красн.) ↓
Качественная реакция:
К 2 СгO 4 + ВаСl 2 = 2КСl + ВаCrO 4 ↓
2ВаСrO 4 (т)+ 2НСl (разб. ) = ВаСr 2 O 7(p) + ВаС1 2 + Н 2 O
) = ВаСr 2 O 7(p) + ВаС1 2 + Н 2 O
Получение : спекание хромита с поташом на воздухе:
4(Сr 2 Fe ‖‖)O 4 + 8К 2 CO 3 + 7O 2 = 8К 2 СrO 4 + 2Fе 2 O 3 + 8СO 2 (1000 °С)
Дихромат калия K 2 Cr 2 O 7 . Оксосоль. Техническое название хромпик . Оранжево-красный, негигроскопичный. Плавится без разложения, при дальнейшем нагревании разлагается. Хорошо растворим в воде (оранжевая окраска раствора отвечает иону Сr 2 O 7 2-). В щелочной среде образует К 2 CrO 4 . Типичный окислитель в растворе и при сплавлении. Вступает в реакции ионного обмена.
Качественные реакции — синее окрашивание эфирного раствора в присутствии Н 2 O 2 , синее окрашивание водного раствора при действии атомарного водорода.
Применяется как дубитель кож, протрава при крашении тканей, компонент пиротехнических составов, реагент в аналитической химии, ингибитор коррозии металлов, в смеси с Н 2 SO 4 (конц. ) — для мытья химической посуды.
) — для мытья химической посуды.
Уравнения важнейших реакций:
4К 2 Cr 2 O 7 =4K 2 CrO 4 +2Cr 2 O 3 +3O 2 (500-600 o C)
K 2 Cr 2 O 7 (т) +14HCl (кон ц) =2CrCl 3 +3Cl 2 +7H 2 O+2KCl (кипячение)
K 2 Cr 2 O 7 (т) +2H 2 SO 4(96%) ⇌2KHSO 4 +2CrO 3 +H 2 O (“хромовая смесь”)
K 2 Cr 2 O 7 +KOH (конц) =H 2 O+2K 2 CrO 4
Cr 2 O 7 2- +14H + +6I — =2Cr 3+ +3I 2 ↓+7H 2 O
Cr 2 O 7 2- +2H + +3SO 2(г) =2Cr 3+ +3SO 4 2- +H 2 O
Cr 2 O 7 2- +H 2 O +3H 2 S (г) =3S↓+2OH — +2Cr 2 (OH) 3 ↓
Cr 2 O 7 2- (конц) +2Ag + (разб.) =Ag 2 Cr 2 O 7 (т. красный) ↓
Cr 2 O 7 2- (разб.) +H 2 O +Pb 2+ =2H + + 2PbCrO 4 (красный) ↓
K 2 Cr 2 O 7(т) +6HCl+8H 0 (Zn)=2CrCl 2(син) +7H 2 O+2KCl
Получение: обработка К 2 СrO 4 серной кислотой:
2К 2 СrO 4 + Н 2 SO 4 (30%) = К 2 Cr 2 O 7 + К 2 SO 4 + Н 2 O
Открытие хрома относится к периоду бурного развития химико-аналитических исследований солей и минералов.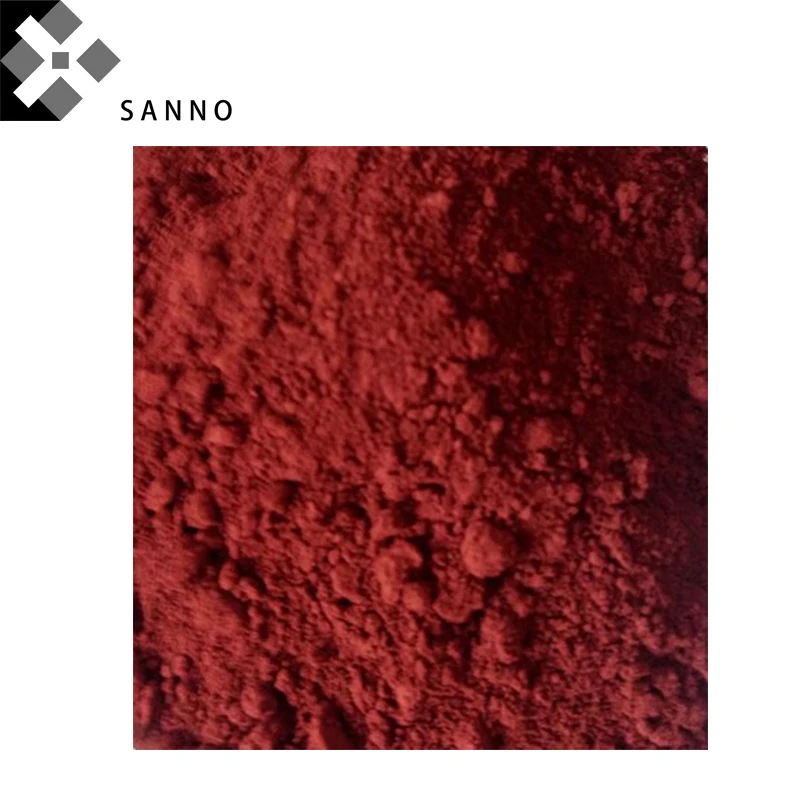 В России химики проявляли особый интерес к анализу минералов, найденных в Сибири и почти неизвестных в Западной Европе. Одним из таких минералов была сибирская красная свинцовая руда (крокоит), описанная еще Ломоносовым. Минерал исследовался, но ничего, кроме окислов свинца, железа и алюминия в нем не было найдено. Однако в 1797 году Вокелен, прокипятив тонко измельченный образец минерала с поташом и осадив карбонат свинца, получил раствор, окрашенный в оранжево – красный цвет. Из этого раствора он выкристаллизовал рубиново-красную соль, из которой выделили окисел и свободный металл, отличный от всех известных металлов. Вокелен назвал его Хром ( Chrome
) от греческого слова — окраска, цвет; правда здесь имелось в виду свойство не металла, а его ярко окрашенных солей
.
В России химики проявляли особый интерес к анализу минералов, найденных в Сибири и почти неизвестных в Западной Европе. Одним из таких минералов была сибирская красная свинцовая руда (крокоит), описанная еще Ломоносовым. Минерал исследовался, но ничего, кроме окислов свинца, железа и алюминия в нем не было найдено. Однако в 1797 году Вокелен, прокипятив тонко измельченный образец минерала с поташом и осадив карбонат свинца, получил раствор, окрашенный в оранжево – красный цвет. Из этого раствора он выкристаллизовал рубиново-красную соль, из которой выделили окисел и свободный металл, отличный от всех известных металлов. Вокелен назвал его Хром ( Chrome
) от греческого слова — окраска, цвет; правда здесь имелось в виду свойство не металла, а его ярко окрашенных солей
.
Нахождение в природе.
Важнейшей рудой хрома, имеющей практическое значение, является хромит, приблизительный состав которого отвечает формуле FeCrO 4.
Он встречается в Малой Азии, на Урале, в Северной Америке, на юге Африки. Техническое значение имеет также вышеназванный минерал крокоит – PbCrO 4 . В природе встречаются также оксид хрома (3) и некоторые другие его соединения. В земной коре содержание хрома в пересчете на металл составляет 0,03%. Хром обнаружен на Солнце, звездах, метеоритах.
Техническое значение имеет также вышеназванный минерал крокоит – PbCrO 4 . В природе встречаются также оксид хрома (3) и некоторые другие его соединения. В земной коре содержание хрома в пересчете на металл составляет 0,03%. Хром обнаружен на Солнце, звездах, метеоритах.
Физические свойства .
Хром – белый, твердый и хрупкий металл, исключительно химически стойкий к воздействию кислот и щелочей. На воздухе он окисляется, имеет на поверхности тонкую прозрачную пленку оксида. Хром имеет плотность 7,1 г/см 3 , его температура плавления составляет +1875 0 С.
Получение.
При сильном нагреве хромистого железняка с углем происходит восстановление хрома и железа:
FeO * Cr 2 O 3 + 4C = 2Cr + Fe + 4CO
В результате этой реакции образуется сплав хрома с железом, отличающийся высокой прочностью. Для получения чистого хрома, его восстанавливают из оксида хрома(3) алюминием:
Cr 2 O 3 + 2Al = Al 2 O 3 + 2Cr
В данном процессе обычно используют два оксида – Cr 2 O 3 и CrO 3
Химические свойства.
Благодаря тонкой защитной пленке оксида, покрывающей поверхность хрома, он весьма устойчив к воздействию агрессивных кислот и щелочей. Хром не реагирует с концентрированными азотной и серной кислотами, а также с фосфорной кислотой. Со щелочами хром вступает во взаимодействие при t = 600-700 о C. Однако хром взаимодействует с разбавленными серной и соляной кислотами, вытесняя водород:
2Cr + 3H 2 SO 4 = Cr 2 (SO 4) 3 + 3H 2
2Cr + 6HCl = 2CrCl 3 + 3H 2
При высокой температуре хром горит в кислороде, образуя оксид(III).
Раскаленный хром реагирует с парами воды:
2Cr + 3H 2 O = Cr 2 O 3 + 3H 2
Хром при высокой температуре реагирует также с галогенами, галоген — водородами, серой, азотом, фосфором, углем, кремнием, бором, например:
Cr + 2HF = CrF 2 + H 2
2Cr + N2 = 2CrN
2Cr + 3S = Cr 2 S 3
Cr + Si = CrSi
Вышеуказанные физические и химические свойства хрома нашли свое применение в различных областях науки и техники. Так, например, хром и его сплавы используются для получения высокопрочных, коррозионно-стойких покрытий в машиностроении. Сплавы в виде феррохрома используются в качестве металлорежущих инструментов. Хромированные сплавы нашли применение в медицинской технике, при изготовлении химического технологического оборудования.
Сплавы в виде феррохрома используются в качестве металлорежущих инструментов. Хромированные сплавы нашли применение в медицинской технике, при изготовлении химического технологического оборудования.
Положение хрома в периодической системе химических элементов:
Хром возглавляет побочную подгруппу VI группы периодической системы элементов. Его электронная формула следующая:
24 Cr IS 2 2S 2 2P 6 3S 2 3P 6 3d 5 4S 1
В заполнении орбиталей электронами у атома хрома нарушается закономерность, согласно которой сначала должна была бы заполнятся 4S – орбиталь до состояния 4S 2 . Однако, вследствие того, что 3d – орбиталь занимает в атоме хрома более выгодное энергетическое положение, происходит ее заполнение до значения 4d 5 . Такое явление наблюдается у атомов некоторых других элементов побочных подгрупп. Хром может проявлять степени окисления от +1 до +6. Наиболее устойчивыми являются cоединения хрома со степенями окисления +2, +3, +6.
Соединения двухвалентного хрома.
Оксид хрома (II) CrO – пирофорный черный порошок (пирофорность – способность в тонкораздробленном состоянии воспламенятся на воздухе). CrO растворяется в разбавленной соляной кислоте:
CrO + 2HCl = CrCl 2 + H 2 O
На воздухе при нагревании свыше 100 0 С CrO превращается в Cr 2 O 3 .
Соли двухвалентного хрома образуются при растворении металлического хрома в кислотах. Эти реакции проходят в атмосфере малоактивного газа (например H 2), т.к. в присутствии воздуха легко происходит окисление Cr(II) до Cr(III).
Гидроксид хрома получают в виде желтого осадка при действии раствора щелочи на хлорид хрома (II):
CrCl 2 + 2NaOH = Cr(OH) 2 + 2NaCl
Cr(OH) 2 обладает основными свойствами, является восстановителем. Гидратированный ион Cr2+ окрашен в бледно – голубой цвет. Водный раствор CrCl 2 имеет синюю окраску. На воздухе в водных растворах соединения Cr(II) переходят в соединения Cr(III). Особенно это ярко выражается у гидроксида Cr(II):
4Cr(OH) 2 + 2H 2 O + O 2 = 4Cr(OH) 3
Соединения трехвалентного хрома.
Оксид хрома (III) Cr 2 O 3 – тугоплавкий порошок зеленого цвета. По твердости близок к корунду. В лаборатории его можно получить нагреванием дихромата аммония:
(NH 4) 2 Cr 2 O 7 = Cr 2 O 3 + N 2 + 4H 2
Cr 2 O 3 – амфотерный оксид, при сплавлении со щелочами образует хромиты: Cr 2 O 3 + 2NaOH = 2NaCrO 2 + H 2 O
Гидроксид хрома также является амфотерным соединением:
Cr(OH) 3 + HCl = CrCl 3 + 3H 2 O
Cr(OH) 3 + NaOH = NaCrO 2 + 2H 2 O
Безводный CrCl 3 имеет вид листочков темно-фиолетового цвета, совершенно нерастворим в холодной воде, при кипячении он растворяется очень медленно. Безводный сульфат хрома (III) Cr 2 (SO 4) 3 розового цвета, также плохо растворим в воде. В присутствии восстановителей образует фиолетовый сульфат хрома Cr 2 (SO 4) 3 *18H 2 O. Известны также зеленые гидраты сульфата хрома, содержащие меньшее количество воды. Хромовые квасцы KCr(SO 4) 2 *12H 2 O выкристаллизовываются из растворов, содержащих фиолетовый сульфат хрома и сульфат калия. Раствор хромовых квасцов при нагревании становится зеленым благодаря образованию сульфатов.
Раствор хромовых квасцов при нагревании становится зеленым благодаря образованию сульфатов.
Реакции с хромом и его соединениями
Почти все соединения хрома и их растворы интенсивно окрашены. Имея бесцветный раствор или белый осадок, мы можем с большой долей вероятности сделать вывод об отсутствии хрома.
- Сильно нагреем в пламени горелки на фарфоровой чашке такое количество бихромата калия, которое поместится на кончике ножа. Соль не выделит кристаллизационной воды, а расплавится при температуре около 400 0 С с образование темной жидкости. Погреем ее еще несколько минут на сильном пламени. После охлаждения на черепке образуется зеленый осадок. Часть его растворим в воде (она приобретает желтый цвет), а другую часть оставим на черепке. Соль при нагревании разложилась, в результате образовался растворимый желтый хромат калия K 2 CrO 4 и зеленый Cr 2 O 3 .
- Растворим 3г порошкообразного бихромата калия в 50мл воды. К одной части добавим немного карбоната калия.
 Он растворится с выделением CO 2 , а окраска раствора станет светло – желтой. Из бихромата калия образуется хромат. Если теперь по порциям добавить 50% раствор серной кислоты, то снова появится красно – желтая окраска бихромата.
Он растворится с выделением CO 2 , а окраска раствора станет светло – желтой. Из бихромата калия образуется хромат. Если теперь по порциям добавить 50% раствор серной кислоты, то снова появится красно – желтая окраска бихромата. - Нальем в пробирку 5мл. раствора бихромата калия, прокипятим с 3мл концентрированной соляной кислоты под тягой. Из раствора выделяется желто-зеленый ядовитый газообразный хлор, потому, что хромат окислит HCl до Cl 2 и H 2 O. Сам хромат превратится в зеленый хлорид трехвалентного хрома. Его можно выделить выпариванием раствора, а потом, сплавив с содой и селитрой, перевести в хромат.
- При добавлении раствора нитрата свинца выпадает желтый хромат свинца; при взаимодействии с раствором нитрата серебра образуется красно – коричневый осадок хромата серебра.
- Добавим пероксид водорода к раствору бихромата калия и подкислим раствор серной кислотой. Раствор приобретает глубокий синий цвет благодаря образованию пероксида хрома. Пероксид при взбалтывании с некоторым количеством эфира перейдет в органический растворитель и окрасит его в голубой цвет.
 Данная реакция специфична для хрома и очень чувствительна. С ее помощью можно обнаружить хром в металлах и сплавах. Прежде всего необходимо растворить металл. При длительном кипячении с 30% — ной серной кислотой (можно добавить и соляную кислоту) хром и многие стали частично растворяются. Полученный раствор содержит сульфат хрома (III). Чтобы можно было провести реакцию обнаружения, сначала нейтрализуем его едким натром. В осадок выпадает серо-зеленый гидроксид хрома (III), который растворится в избытке NaOH и образует зеленый хромит натрия. Профильтруем раствор и добавим 30% -ый пероксид водорода. При нагревании раствор окрасится в желтый цвет, так как хромит окислится до хромата. Подкисление приведет к появлению голубой окраски раствора. Окрашенное соединение можно экстрагировать, встряхивая с эфиром.
Данная реакция специфична для хрома и очень чувствительна. С ее помощью можно обнаружить хром в металлах и сплавах. Прежде всего необходимо растворить металл. При длительном кипячении с 30% — ной серной кислотой (можно добавить и соляную кислоту) хром и многие стали частично растворяются. Полученный раствор содержит сульфат хрома (III). Чтобы можно было провести реакцию обнаружения, сначала нейтрализуем его едким натром. В осадок выпадает серо-зеленый гидроксид хрома (III), который растворится в избытке NaOH и образует зеленый хромит натрия. Профильтруем раствор и добавим 30% -ый пероксид водорода. При нагревании раствор окрасится в желтый цвет, так как хромит окислится до хромата. Подкисление приведет к появлению голубой окраски раствора. Окрашенное соединение можно экстрагировать, встряхивая с эфиром.
Аналитические реакции на ионы хрома.
- К 3-4 каплям раствора хлорида хрома CrCl 3 прибавьте 2М раствор NaOH до растворения первоначально выпавшего осадка.
 Обратите внимание на цвет образовавшегося хромита натрия. Нагрейте полученный раствор на водяно бане. Что при этом происходит?
Обратите внимание на цвет образовавшегося хромита натрия. Нагрейте полученный раствор на водяно бане. Что при этом происходит? - К 2-3 каплям р-ра CrCl 3 прибавьте равный объем 8М раствора NaOH и 3-4 капли 3% р-ра H 2 O 2 . Нагрейте реакционную смесь на водяной бане. Что при этом происходит? Какой осадок образуется, если полученный окрашеный раствор нейтрализовать, добавить к нему CH 3 COOH, а затем Pb(NO 3) 2 ?
- Налейте в пробирку по 4-5 капель растворов сульфата хрома Cr 2 (SO 4) 3 , IMH 2 SO 4 и KMnO 4 . Нагрейте реакционную смест в течение нескольких минут на водяной бане. Обратите внимание на изменение окраски раствора. Чем оно вызвано?
- К 3-4 каплям подкисленного азотной кислотой раствора K 2 Cr 2 O 7 прибавьте 2-3 капли раствора H 2 O 2 и перемешайте. Появляющиеся синее окрашивание раствора обусловлено возникновением надхромовой кислоты H 2 CrO 6:
Cr 2 O 7 2- + 4H 2 O 2 + 2H + = 2H 2 CrO 6 + 3H 2 O
Обратите внимание на на быстрое разложение H 2 CrO 6:
2H 2 CrO 6 + 8H+ = 2Cr 3+ + 3O 2 + 6H 2 O
синий цвет зеленый цвет
Надхромовая кислота значительно более устойчива в органических растворителях.
- К 3-4 каплям подкисленного азотной кислотой раствора K 2 Cr 2 O 7 прибавьте 5 капель изоамилового спирта, 2-3 капли раствора H 2 O 2 и взболтайте реакционную смесь. Всплывающий на верх слой органического растворителя окрашен в ярко-синий цвет. Окраска исчезает очень медленно. Сравните устойчивость H 2 CrO 6 в органической и водных фазах.
- При взаимодействии CrO 4 2- и ионами Ba 2+ выпадает желтый осадок хромата бария BaCrO 4 .
- Нитрат серебра образует с ионами CrO 4 2- осадок хромата серебра кирпично-красного цвета.
- Возьмите три пробирки. В одну из них поместите 5- 6 капель раствора K 2 Cr 2 O 7 , во вторую – такой же объем раствора K 2 CrO 4 , а в третью – по три капли обоих растворов. Затем добавте в каждую пробирку по три капли раствора иодида калия. Объясните полученный результат. Подкислите раствор во второй пробирке. Что при этом происходит? Почему?
Занимательные опыты с соединениями хрома
- Смесь CuSO 4 и K 2 Cr 2 O 7 при добавлении щелочи становится зеленой, а в присутствии кислоты становится желтой.
 Нагревая 2мг глицерина с небольшим количеством (NH 4) 2 Cr 2 O 7 с последующим добавлением спирта, после фильтрования получается ярко-зеленый раствор, который при добавлении кислоты становится желтым, а в нейтральной или щелочной среде становится зеленым.
Нагревая 2мг глицерина с небольшим количеством (NH 4) 2 Cr 2 O 7 с последующим добавлением спирта, после фильтрования получается ярко-зеленый раствор, который при добавлении кислоты становится желтым, а в нейтральной или щелочной среде становится зеленым. - Поместить в центр консервной банки с термитом «рубиновую смесь» — тщательно растертый и помещенный в алюминиевую фольгу Al 2 O 3 (4,75г) с добавкой Cr 2 O 3 (0,25г). Чтобы банка подольше не остывала, необходимо закопать под верхний обрез в песок, а после поджигания термита и начала реакции, накрыть ее железным листом и засыпать песком. Банку выкопать через сутки. В итоге образуется красно – рубиновый порошок.
- 10г бихромата калия растирают с 5г нитрата натрия или калия и 10г сахара. Смесь увлажняют и смешивают с коллодием. Если порошок спрессовать в стеклянной трубке, а затем вытолкнуть палочку и поджечь ее с торца, то начнет выползать «змея», сначала черная, а после охлаждения — зеленая. Палочка диаметром 4 мм горит со скоростью около 2мм в секунду и удлиняется в 10 раз.

- Если смешать растворы сульфата меди и дихромата калия и добавить немного раствора аммиака, то выпадет аморфный коричневый осадок состава 4СuCrO 4 * 3NH 3 * 5H 2 O, который растворяется в соляной кислоте с образованием желтого раствора, а в избытке аммиака получается зеленый раствор. Если далее к этому раствору добавить спирт, то выпадет зеленый осадок, который после фильтрации становится синим, а после высушивания – сине-фиолетовым с красными блестками, хорошо видимыми при сильном освещении.
- Оставшийся после опытов «вулкан» или «фараоновы змеи» оксид хрома можно регенерировать. Для этого надо сплавить 8г Cr 2 O 3 и 2г Na 2 CO 3 и 2,5г KNO 3 и обработать остывший сплав кипятком. Получается растворимый хромат, который можно превратить и в другие соединения Cr(II) и Cr(VI), в том числе и исходный дихромат аммония.
Примеры окислительно – восстановительных переходов с участием хрома и его соединений
1. Cr 2 O 7 2- — Cr 2 O 3 — CrO 2 — — CrO 4 2- — Cr 2 O 7 2-
a) (NH 4) 2 Cr 2 O 7 = Cr 2 O 3 + N 2 + 4H 2 Oб) Cr 2 O 3 + 2NaOH = 2NaCrO 2 + H 2 O
в) 2NaCrO 2 + 3Br 2 + 8NaOH = 6NaBr +2Na 2 CrO 4 + 4H 2 O
г) 2Na 2 CrO 4 + 2HCl = Na 2 Cr 2 O 7 + 2NaCl + H 2 O
2. Cr(OH) 2 — Cr(OH) 3 — CrCl 3 — Cr 2 O 7 2- — CrO 4 2-
Cr(OH) 2 — Cr(OH) 3 — CrCl 3 — Cr 2 O 7 2- — CrO 4 2-
а) 2Cr(OH) 2 + 1/2O 2 + H 2 O = 2Cr(OH) 3
б) Cr(OH) 3 + 3HCl = CrCl 3 + 3H 2 O
в) 2CrCl 3 + 2KMnO 4 + 3H 2 O = K 2 Cr 2 O 7 + 2Mn(OH) 2 + 6HCl
г) K 2 Cr 2 O 7 + 2KOH = 2K 2 CrO 4 + H 2 O
3. CrO — Cr(OH) 2 — Cr(OH) 3 — Cr(NO 3) 3 — Cr 2 O 3 — CrO — 2
Cr 2+
а) CrO + 2HCl = CrCl 2 + H 2 O
б) CrO + H 2 O = Cr(OH) 2
в) Cr(OH) 2 + 1/2O 2 + H 2 O = 2Cr(OH) 3
г) Cr(OH) 3 + 3HNO 3 = Cr(NO 3) 3 + 3H 2 O
д) 4Сr(NO 3) 3 = 2Cr 2 O 3 + 12NO 2 + O 2
е) Cr 2 O 3 + 2 NaOH = 2NaCrO 2 + H 2 O
Элемент хром в роли художника
Химики довольно часто обращались к проблеме создания искусственных пигментов для живописи. В XVIII-XIXвв была разработана технология получения многих живописных материалов. Луи Никола Воклен в 1797г., обнаруживший в сибирской красной руде ранее неизвестный элемент хром, приготовил новую, замечательно устойчивую краску – хромовую зелень. Хромофором ее является водный оксид хрома (III). Под названием « изумрудная зеленая» ее начали выпускать в 1837 году. Позже Л.Вокелен предложил несколько новых красок: баритовую, цинковую и хромовые желтые. Со временем они были вытеснены более стойкими желтыми, оранжевыми пигментами на основе кадмия.
Хромофором ее является водный оксид хрома (III). Под названием « изумрудная зеленая» ее начали выпускать в 1837 году. Позже Л.Вокелен предложил несколько новых красок: баритовую, цинковую и хромовые желтые. Со временем они были вытеснены более стойкими желтыми, оранжевыми пигментами на основе кадмия.
Зеленая хромовая – самая прочная и светостойкая краска, не поддающаяся воздействию атмосферных газов. Растертая на масле хромовая зелень обладает большой кроющей силой и способна к быстрому высыханию, поэтому с XIX в. ее широко применяют в живописи. Огромное значение она имеет в росписи фарфора. Дело в том, что фарфоровые изделия могут декорироваться как подглазурной, так и надглазурной росписью. В первом случае краски наносят на поверхность лишь слегка обожженного изделия, которое затем покрывают слоем глазури. Далее следует основной, высокотемпературный обжиг: для спекания фарфоровой массы и оплавления глазури изделия нагревают до 1350 – 1450 0 С. Столь высокую температуру без химических изменений выдерживают очень немногие краски, а в старину таких вообще было только две – кобальтовая и хромовая. Черный оксид кобальта, нанесенный на поверхность фарфорового изделия, при обжиге сплавляется с глазурью, химически взаимодействуя с ней. В результате образуются ярко-синие силикаты кобальта. Такую декарированную кобальтом синюю фарфоровую посуду все хорошо знают. Оксид хрома (III) не взаимодействует химически с компонентами глазури и просто залегает между фарфоровыми черепками и прозрачной глазурью «глухим» слоем.
Черный оксид кобальта, нанесенный на поверхность фарфорового изделия, при обжиге сплавляется с глазурью, химически взаимодействуя с ней. В результате образуются ярко-синие силикаты кобальта. Такую декарированную кобальтом синюю фарфоровую посуду все хорошо знают. Оксид хрома (III) не взаимодействует химически с компонентами глазури и просто залегает между фарфоровыми черепками и прозрачной глазурью «глухим» слоем.
Помимо хромовой зелени художники применяют краски, полученные из волконскоита. Этот минерал из группы монтмориллонитов (глинистый минерал подкласса сложных силикатов Na(Mo,Al), Si 4 O 10 (OH) 2 был обнаружен в 1830г. русским минералогом Кеммерером и назван в честь М.Н Волконской – дочери героя битвы при Бородино генерала Н.Н. Раевского, жены декабриста С.Г.Волконского. Волконскоит представляет собой глину, содержащую до 24% оксида хрома, а так же оксиды аллюминея и железа (III). Непостоянство состава минерала, встечающегося на Урале, в Пермской и Кировской областях, обусловливает его разнообразную окраску – от цвета зимней потемневшей пихты до ярко-зеленого цвета болотной лягушки.
Пабло Пикассо обращался к геологам нашей страны с просьбой изучить запасы волконскоита, дающего краску неповторимо свежего тона. В настоящее время разработан способ получения искусственного волконскоита. Интересно отметить, что по данным современных исследований, русские иконописцы использовали краски из этого материала еще в средние века, задолго до его «официального» открытия. Известной популярностью пользовалась у художников и зелень Гинье (создана в 1837г.), хромоформ которой является гидрат окиси хрома Cr 2 O 3 * (2-3) H 2 O, где часть воды химически связана, а часть адсорбирована. Этот пигмент придает краске изумрудный оттенок.
сайт, при полном или частичном копировании материала ссылка на первоисточник обязательна.
Хром, железо и медь, подготовка к ЕГЭ по химии
Хром
Твердый металл голубовато-белого цвета. Этимология слова «хром» берет начало от греч. χρῶμα — цвет, что связано с большим
разнообразием цветов соединений хрома. Массовая доля этого элемента в земной коре составляет 0.02% по массе.
Массовая доля этого элемента в земной коре составляет 0.02% по массе.
Для хрома характерны степени окисления +2, +3 и +6. У соединений, где хром принимает степень окисления +2, свойства основные, +3 — амфотерные, +6 — кислотные.
В природе хром встречается в виде следующих соединений.
- Fe(CrO2)2 — хромистый железняк, хромит
- (Mg, Fe)Cr2O4 — магнохромит
- (Fe, Mg)(Cr, Al)2O4 — алюмохромит
Получение
В промышленности хром получают прокаливанием хромистого железняка с углеродом. Также применяют алюминотермию для вытеснения хрома из его оксида.
Fe(CrO2)2 + C = Fe + Cr + CO
Cr2O3 + Al = Al2O3 + Cr
Химические свойства
- Реакции с неметаллами
- Реакция с водой
- Реакции с кислотами
- Реакции с солями менее активных металлов
Уже на воздухе вступает в реакцию с кислородом: на поверхности металла образуется пленка из оксида хрома (III) — Cr2O3 —
происходит пассивирование. Реагирует с неметаллами при нагревании.
Реагирует с неметаллами при нагревании.
Cr + O2 = (t) Cr2O3
Cr + S = (t) Cr2S3
Cr + N2 = (t) CrN
Cr + C = Cr2C3
Протекает в раскаленном состоянии.
Cr + H2O = (t) Cr(OH)3 + H2↑
Cr + HCl = CrCl2 + H2↑
Cr + H2SO4(разб.) = CrSO4 + H2↑
С холодными концентрированными серной и азотной кислотой реакция не идет. Она начинается только при нагревании.
Cr + H2SO4 = (t) Cr2(SO4)3 + SO2↑ + H2O
Хром способен вытеснить из солей металлы, стоящие в ряду напряжений правее него.
Cr + CuSO4 = CrSO4 + Cu
Соединения хрома (II)
Соединение хрома (II) носят основный характер. Оксид хрома (II) окисляется кислородом воздуха до более устойчивой формы — оксида хрома (III), реагирует с кислотами, кислотными оксидами.
CrO + O2 = Cr2O3
CrO + H2SO4 = CrSO4 + H2O
CrO + SO3 = CrSO4
Гидроксид хрома (II), как нерастворимый гидроксид, легко разлагается при нагревании на соответствующий оксид и воду, реагирует с кислотами, кислотными оксидами.
Cr(OH)2 = (t) CrO + H2O
Cr(OH)2 + HCl = CrCl2 + H2O
Cr(OH)2 + SO3 = CrSO4 + H2O
Соединения хрома (III)
Это наиболее устойчивые соединения, которые носят амфотерный характер. К ним относятся оксид хрома (III) гидроксид хрома (III).
К ним относятся оксид хрома (III) гидроксид хрома (III).
Оксид хрома (III) реагирует как с щелочами, так и с кислотами. В реакциях с щелочами при нормальной температуре (в растворе) образуются комплексные соли, при прокаливании — смешанные оксиды. С кислотами оксид хрома (III) образует различные соли.
H2O + NaOH + Cr2O3 → Na3[Cr(OH)6] (в растворе, гексагидроксохромат натрия)
Cr2O3 + Ba(OH)2 → (t°) Ba(CrO2)2 + H2O (прокаливание, хромит бария)
Cr2O3 + 2NaOH → (t°) 2NaCrO2 + H2O (прокаливание, хромит натрия)
Cr2O3 + HCl = CrCl3 + H2O (сохраняем степень окисления Cr+3)
Оксид хрома (III) реагирует с более активными металлами (например, при алюминотермии).
Cr2O3 + Al = Al2O3 + Cr
При окислении соединение хрома (III) получают соединения хрома (VI) (в щелочной среде).
K3[Cr(OH)6] + H2O2 = K2CrO4 + KOH + H2O
Cr2O3 + 8NaOH + O2 = (t) Na2CrO4 + H2O
Соединения хрома (VI)
В этой степени окисления хром проявляет кислотные свойства. К ним относится оксид хрома (VI) — CrO3, и две кислоты, находящиеся в растворе в состоянии равновесия: хромовая — H2CrO4 и дихромовая кислоты — H2Cr2O7.
Принципиально важно помнить окраску хроматов и дихроматов (часто она бывает дана в заданиях в качестве подсказки). Хроматы окрашивают
раствор в желтый цвет, а дихроматы — в оранжевый цвет.
Хроматы окрашивают
раствор в желтый цвет, а дихроматы — в оранжевый цвет.
Хроматы переходят в дихроматы с увеличением кислотности среды (часто в реакциях с кислотами). Цвет раствора меняется с желтого на оранжевый.
Na2CrO4 + H2SO4 = Na2Cr2O7 + Na2SO4 + H2O
Если же оранжевому раствору дихромата прилить щелочь, то он сменит свой цвет на желтый — образуется хромат.
Na2Cr2O7 + NaOH = Na2CrO4 + H2O
Разложение дихромата аммония выглядит очень эффектно и носит название «вулканчик» :)
(NH4)2Cr2O7 = (t) Cr2O3 + N2↑ + H2O
В степени окисления +6 соединения хрома проявляют выраженные окислительные свойства.
K2Cr2O7 + HCl = CrCl3 + KCl + Cl2↑ + H2O
Железо
Является одним из самых распространенных элементов в земной коре (после алюминия), составляет 4,65% ее массы.
Для железа характерны две основные степени окисления +2, +3, +6.
В природе железо встречается в виде следующих соединений:
- Fe2O3 — красный железняк, гематит
- Fe3O4 — магнитный железняк, магнетит
- Fe2O3*H2O — бурый железняк, лимонит
- FeS2 — пирит, серый или железный колчедан
- FeCO3 — сидерит
Получение
Получают железо восстановлением из его оксида — руды. Восстанавливают с помощью угарного газа, водорода.
Восстанавливают с помощью угарного газа, водорода.
CO + Fe2O3 = Fe + CO2↑
H2 + Fe2O3 = Fe + H2O
Основными сплавами железа являются чугун и сталь. В стали содержание углерода менее 2%, меньше содержится P, Mn, Si, S. Чугун отличается бо́льшим содержанием углерода (2-6%), содержит больше P, Mn, Si, S.
Химические свойства
- Реакции с неметаллами
- Реакции с кислотами
- Реакции с солями
- Восстановительные свойства
Fe + S = FeS (t > 700°C)
Fe + S = FeS2 (t
Fe + O2 = Fe3O4 (при горении железа образуется железная окалина — Fe3O4 — смесь двух оксидов FeO*Fe2O3)
При нагревании железо взаимодействует с галогенами, азотом, фосфором, углеродом, кремнием и другими.
Fe + Cl2 = (t) FeCl3
Fe + P = (t) FeP
Fe + C = (t) Fe3C
Fe + Si = (t) FeSi
Железо активнее водорода, способно вытеснить его из кислот.
Fe + HCl = FeCl2 + H2↑
На воздухе железо покрывается пленкой оксида, из-за чего пассивируется во многих реакциях, в том числе с концентрированными холодными серной и азотной кислотами.
Fe + H2SO4(разб.) = FeSO4 + H2↑
Реакция с концентрированными кислотами идет только при нагревании. В холодных серной и азотной кислотах железо пассивируется.
Fe + H2SO4(конц.) = Fe2(SO4)3 + SO2↑ + H2O
Железо способно вытеснить из солей металлы, стоящие в ряду напряжений правее железа.
CuCl2 + Fe = FeCl2 + Cu
Железо способно восстанавливать соединения железа +3 до +2.
Fe + Fe2O3 = (t) FeO
Fe + FeCl3 = (t) FeCl2
Соединения железа (II) проявляют основные свойства. Реагируют c кислотами. При разложении гидроксид железа (II) распадается на соответствующий оксид и воду.
FeO + H2SO4 = FeSO4 + H2O
Fe(OH)2 + HCl = FeCl2 + H2O
Fe(OH)2 = (t) FeO + H2O
При хранении на открытом воздухе соли железа (II) приобретают коричневый цвет из-за окисления до железа +3.
FeCl2 + H2O + O2 = Fe(OH)Cl2
Качественной реакцией на ионы Fe2+ в растворе является реакция с красной кровяной солью — K3[Fe(CN)6] — гексацианоферратом (III) калия. В результате реакции образуется берлинская лазурь (прусский синий).
FeCl2 + K3[Fe(CN)6] = KFe[Fe(CN)6] + KCl
Качественной реакцией на ионы Fe2+ также является взаимодействие с щелочью (гидроксидом натрия). В результате выпадает осадок зеленого цвета.
FeCl2 + NaOH = Fe(OH)2 + NaCl
Соединения железа (III) проявляют амфотерные свойства. Оксид и гидроксид железа (III) реагирует и с кислотами, и с щелочами.
Fe(OH)3 + H2SO4 = Fe2(SO4)3 + H2O
Fe(OH)3 + KOH = K3[Fe(OH)6] (гексагидроксоферрат калия)
При сплавлении комплексные соли не образуются из-за испарения воды.
Fe(OH)3 + KOH = (t) KFeO2 + H2O
Гидроксид железа (III) — ржавчина, образуется на воздухе в результате взаимодействия железа с водой в присутствии кислорода. При нагревании легко распадается на воду и соответствующий оксид.
Fe + H2O + O2 = Fe(OH)3
Fe(OH)3 = (t) Fe2O3 + H2O
Качественной реакцией на ионы Fe3+ является взаимодействие с желтой кровяной солью K4[Fe(CN)6]. В результате реакции образуется берлинская лазурь (прусский синий).
FeCl3 + K4[Fe(CN)6] = KFe[Fe(CN)6] + KCl
Реакция хлорида железа (III) с роданидом калия также является качественной, в результате нее образуется характерный раствор ярко
красного цвета.
FeCl3 + KCNS = Fe(CNS)3 + KCl
И еще одна качественная реакция на ионы Fe3+ — взаимодействие с щелочью (гидроксидом натрия). В результате выпадает осадок бурого цвета.
FeCl3 + NaOH = Fe(OH)3 + NaCl
Соединения железа (VI) — ферраты — соли несуществующей в свободном виде железной кислоты. Обладают выраженными окислительными свойствами.
Ферраты можно получить в ходе электролизом щелочи на железном аноде, а также действием хлора на взвесь Fe(OH)3 в щелочи.
Fe + KOH + H2O = (электролиз) K2FeO4 + H2↑
Fe(OH)3 + Cl2 + KOH = K2FeO4 + KCl + H2O
Медь
Один из первых металлов, освоенных человеком вследствие низкой температуры плавления и доступности получения руды.
Основные степени окисления меди +1, +2.
Медь встречается в самородном виде и в виде соединений, наиболее известные из которых:
- CuFeS2 — медный колчедан, халькопирит
- Cu2S — халькозин
- Cu2CO3(OH)2 — малахит
Получение
Пирометаллургический метод получения основан на получении меди путем обжига халькопирита, который идет в несколько этапов.
CuFeS2 + O2 = Cu2S + FeS + SO2↑
Cu2S + O2 = Cu2O + SO2
Cu2O + Cu2S = Cu + SO2
Гидрометаллургический метод заключается в растворении минералов меди в разбавленной серной кислоте и дальнейшем вытеснении меди
более активными металлами, например — железом.
CuSO4 + Fe = Cu + FeSO4
Медь, как малоактивный металл, выделяется при электролизе солей в водном растворе на катоде.
CuSO4 + H2O = Cu + O2 + H2SO4 (медь — на катоде, кислород — на аноде)
Химические свойства
- Реакции с неметаллами
- Реакции с кислотами
- С оксидами неметаллов
Во влажном воздухе окисляется с образованием основного карбоната меди.
Cu + CO2 + H2O + O2 = (CuOH)2CO3
При нагревании реагирует с кислородом, селеном, серой, при комнатной температуре с: хлором, бромом и йодом.
4Cu + O2 = (t) 2Cu2O (при недостатке кислорода)
2Cu + O2 = (t) 2CuO (в избытке кислорода)
Cu + Se = (t) Cu2Se
Cu + S = (t) Cu2S
Медь способна реагировать с концентрированными серной и азотной кислотами. С разбавленной серной не реагирует, с разбавленной азотной
— реакция идет.
С разбавленной серной не реагирует, с разбавленной азотной
— реакция идет.
Cu + H2SO4(конц.) = (t) CuSO4 + SO2↑ + H2O
Cu + HNO3(конц.) = Cu(NO3)2 + NO2↑ + H2O
Cu + HNO3(разб.) = Cu(NO3)2 + NO↑ + H2O
Реагирует с царской водкой — смесью соляной и азотной кислот в соотношении 1 объем HNO3 к 3 объемам HCl.
Cu + HCl + HNO3 = CuCl2 + NO + H2O
Медь способна восстанавливать неметаллы из их оксидов.
Cu + SO2 = (t) CuO + S
Cu + NO2 = (t) CuO + N2↑
Cu + NO = (t) CuO + N2↑
Соединения меди I
В степени окисления +1 медь проявляет основные свойства. Соединения меди (I) можно получить путем восстановления соединений меди (II).
Соединения меди (I) можно получить путем восстановления соединений меди (II).
CuCl2 + Cu = CuCl
CuO + Cu = Cu2O
Оксид меди (I) можно восстановить до меди различными восстановителями: угарным газом, алюминием (алюминотермией), водородом.
Cu2O + CO = (t) Cu + CO2
Cu2O + Al = (t) Cu + Al2O3
Cu2O + H2 = (t) Cu + H2O
Оксид меди (I) окисляется кислородом до оксида меди (II).
Cu2O + O2 = (t) CuO
Оксид меди (I) вступает в реакции с кислотами.
Cu2O + HCl = CuCl + H2O
Гидроксид меди CuOH неустойчив и быстро разлагается на соответствующий оксид и воду.
CuOH → Cu2O + H2O
Соединения меди (II)
Степень окисления +2 является наиболее стабильной для меди. В этой степени окисления у меди есть оксид CuO и гидроксид Cu(OH)2. Данные соединения проявляют преимущественно основные свойства.
Оксид меди (II) получают в реакциях термического разложения гидроксида меди (II), реакцией избытка кислорода с медью при нагревании.
Cu(OH)2 = (t) CuO + H2O
Cu + O2 = (t) CuO
Химические свойства
Гидроксид меди (II) — Cu(OH)2 — получают в реакциях обмена между растворимыми солями меди и щелочью.
CuSO4 + KOH = K2SO4 + Cu(OH)2↓
- Разложение
- Реакции с кислотами
- Реакции с щелочами
- Реакции с кислотными оксидами
При нагревании гидроксид меди (II), как нерастворимое основание, легко разлагается на соответствующий оксид и воду.
Cu(OH)2 = (t) CuO + H2O
Cu(OH)2 + HNO3 = Cu(NO3)2 + H2O
Cu(OH)2 + HCl = CuCl2 + H2O
Как сказано выше, гидроксид меди (II) носит преимущественно основный характер, однако способен проявлять и амфотерные свойства. В растворе концентрированной щелочи он растворяется, образуя гидроксокомлпекс.
Cu(OH)2 + LiOH = Li2[Cu(OH)4]
Cu(OH)2 + CO2 = (CuOH)2CO3 + H2O (дигидроксокарбонат меди (II) — (CuOH)2CO3)
Обратите особое внимание на реакцию взаимодействия соли меди (II) — сульфата меди (II), карбоната натрия и воды.
CuSO4 + Na2CO3 + H2O = (CuOH)2CO3 + Na2SO4 + CO2
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Оксид хрома(III) | AMERICAN ELEMENTS®
РАЗДЕЛ 1. ИДЕНТИФИКАЦИЯ
Наименование продукта: Оксид хрома(III)
Номер продукта: CR3-OX-02 , CR3-OX-03 , CR3-OX-04 , CR3-OX-05
Номер CAS: 1308-38-9
Соответствующие установленные области применения вещества: Научные исследования и разработки
Информация о поставщике:
American Elements
- 4
- 2 CH 3 COONa → (CH 3 ) 2 CO + Na 2 CO 3
- CH 3 COONa + CH 3 CH 2 COONa → (CH 3 )CO(CH 3 CH 2 ) + Na 902 4 3 3 3 9043 2
3- CH 3 CHONALE + C 6 H 5 H 5 H 5 COONA → (CH 3 ) CO (C 6 H 5 ) + Na 2 CO 3
- Из-за своей стабильности оксид хрома (iii) используется в качестве зеленого пигмента в чернилах, стеклах и красках, а также в качестве красителя для керамики, а также для придания слабого зеленого оттенка глазури [8] .
- Служит абразивом для полировки или зачистки лезвий бритв, ножей и поверхностей оптических устройств [9] .
- Оксид хрома (III) – Pubchem.ncbi.nlm.nih.gov
- Порошок оксида хрома (Cr 2 O 3 ) – Читать.ком
- Оксид хрома (III) — Americanelements.com
- Химия хрома – Chem.libretexts.org
- Оксид хрома (III) — Chemspider.com
- Химические уравнения – Chemequations.com
- Стехиометрия разложения дихромата аммония – Dartmouth.edu
- Оксид хрома – Chromestarchemicals.com
- 5 интересных фактов о зеленом оксиде хрома — Basstechintl.com
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.

- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Los Angeles, CA
Тел.
 : +1 310-208-0551
: +1 310-208-0551 Факс: +1 310-208-0351
Телефон службы экстренной помощи:
Внутренний, Северная Америка: +1 800-424-9300
Международный: +1 703-527-3887
РАЗДЕЛ 2. ИДЕНТИФИКАЦИЯ ОПАСНОСТИ
Классификация вещества или смеси
Классификация в соответствии с Регламентом (ЕС) № 1272/2008
GHS07
Acute Tox. 4 h402 Вреден при проглатывании.
Острый токсикоз. 4 h432 Вреден при вдыхании.
Датчик кожи.1 ч417 Может вызывать кожную аллергическую реакцию.
Классификация согласно Директиве 67/548/ЕЭС или Директиве 1999/45/ЕС
Xn; Вреден для здоровья
R20/22: Вреден при вдыхании и проглатывании.
Си; Сенсибилизация
R43: Может вызвать сенсибилизацию при контакте с кожей.
Информация об особых опасностях для человека и окружающей среды:
Н/Д
Опасности, не классифицированные иначе
Нет данных
Элементы маркировки
Маркировка в соответствии с Регламентом (ЕС) № 1272/2008
Вещество классифицируется и маркируется в соответствии с Регламентом CLP .
Пиктограммы, обозначающие опасности
GHS07
Сигнальное слово: Осторожно
Краткая характеристика опасности
h402+h432 Вреден при проглатывании или при вдыхании.
h417 Может вызывать кожную аллергическую реакцию.
Меры предосторожности
P261 Избегать вдыхания пыли/дыма/газа/тумана/паров/аэрозолей.
P280 Пользоваться защитными перчатками/защитной одеждой/средствами защиты глаз/лица.
P304+P340 ПРИ ВДЫХАНИИ: Вынести пострадавшего на свежий воздух и обеспечить комфорт для дыхания.
P301+P312 ПРИ ПРОГЛАТЫВАНИИ: Обратитесь в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР/к врачу/…/если вы плохо себя чувствуете.
P312 Обратитесь в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР/к врачу/…/, если вы плохо себя чувствуете.
P501 Утилизируйте содержимое/контейнер в соответствии с местными/региональными/национальными/международными нормами.
Классификация WHMIS
D2B — Токсичный материал, вызывающий другие токсические эффекты
Система классификации
Оценки HMIS (шкала 0–4)
(Система идентификации опасных материалов) 2
Воспламеняемость = 0
Физическая опасность = 1
Другие опасности
Результаты оценки PBT и vPvB
PBT: Н/Д
vPvB: Н/Д
РАЗДЕЛ 3.
 СОСТАВ/ИНФОРМАЦИЯ О КОМПОНЕНТАХ
СОСТАВ/ИНФОРМАЦИЯ О КОМПОНЕНТАХ Вещества
Номер CAS / Название вещества:
1308-38-9 Оксид хрома(III)
Идентификационный номер(а):
Номер ЕС: 215-160-9
3 РАЗДЕЛ МЕРЫ ПОМОЩИ
Описание мер первой помощи
При вдыхании:
Обеспечить пострадавшего свежим воздухом. Если не дышит, сделайте искусственное дыхание. Держите пациента в тепле.
Немедленно обратитесь к врачу.
При попадании на кожу:
Немедленно промыть водой с мылом; тщательно промыть.
Немедленно обратитесь к врачу.
При попадании в глаза:
Промыть открытые глаза в течение нескольких минут под проточной водой. Проконсультируйтесь с врачом.
При проглатывании:
Обратиться за медицинской помощью.
Информация для врача
Наиболее важные симптомы и эффекты, как немедленные, так и замедленные
Нет данных
Указание на необходимость немедленной медицинской помощи и специального лечения
Нет данных
РАЗДЕЛ 5.
 МЕРЫ ПОЖАРОТУШЕНИЯ
МЕРЫ ПОЖАРОТУШЕНИЯ Средства пожаротушения
Подходящие средства пожаротушения
Продукт негорючий.Используйте меры пожаротушения, подходящие для окружающего огня.
Особые опасности, исходящие от вещества или смеси
Если этот продукт вовлечен в пожар, могут быть выделены следующие вещества:
Пар оксида металла
Рекомендации для пожарных
Защитное снаряжение:
Надеть автономный респиратор.
Носите полностью защитный непроницаемый костюм.
РАЗДЕЛ 6. МЕРЫ ПРИ СЛУЧАЙНОМ ВЫБРОСЕ
Меры предосторожности для персонала, защитное снаряжение и порядок действий в чрезвычайных ситуациях
Использовать средства индивидуальной защиты.Держите незащищенных людей подальше.
Обеспечьте достаточную вентиляцию.
Меры предосторожности по охране окружающей среды:
Не допускайте попадания продукта в канализацию, канализационные системы или другие водотоки.
Не допускайте проникновения материала в землю или почву.
Методы и материалы для локализации и очистки:
Утилизировать загрязненный материал как отходы в соответствии с разделом 13.
Обеспечить достаточную вентиляцию.
Предотвращение вторичных опасностей:
Никаких специальных мер не требуется.
Ссылка на другие разделы
См. Раздел 7 для информации о безопасном обращении
См. Раздел 8 для информации о средствах индивидуальной защиты.
Информацию об утилизации см. в Разделе 13.
РАЗДЕЛ 7. ОБРАЩЕНИЕ И ХРАНЕНИЕ
Обращение
Меры предосторожности для безопасного обращения
Держите контейнер плотно закрытым.
Хранить в прохладном, сухом месте в плотно закрытой таре.
Обеспечьте хорошую вентиляцию на рабочем месте.
Информация о защите от взрывов и пожаров:
Продукт не воспламеняется
Условия безопасного хранения, включая любые несовместимости
Требования, которым должны соответствовать складские помещения и емкости:
Особых требований нет.
Информация о хранении в одном общем хранилище:
Хранить вдали от окислителей.
Дополнительная информация об условиях хранения:
Хранить контейнер плотно закрытым.
Хранить в прохладном сухом месте в хорошо закрытых контейнерах.
Конкретное конечное применение
Данные отсутствуют
РАЗДЕЛ 8. КОНТРОЛЬ ВОЗДЕЙСТВИЯ ВОЗДЕЙСТВИЯ/СРЕДСТВА ИНДИВИДУАЛЬНОЙ ЗАЩИТЫ
Дополнительная информация о конструкции технических систем: не менее 100 футов в минуту.
Параметры контроля
Компоненты с предельными значениями, требующими контроля на рабочем месте:
1308-38-9 Оксид хрома(III) (100,0%)
PEL (США) Длительное значение: 0,5 мг/м 3 как Cr
REL (США) Долговременное значение: 0,5 мг/м 3 в виде Cr; См. приложение «Карманный справочник». C
TLV (США) Долговременное значение: 0,5 мг/м 3 как Cr
EL (Канада) Долгосрочное значение: 0,5 мг/м 3 как Cr
Дополнительная информация: Нет данных
Средства контроля воздействия
Личное защитное оборудование
Соблюдайте стандартные меры защиты и гигиены при обращении с химическими веществами.
Хранить вдали от пищевых продуктов, напитков и кормов.
Немедленно снимите всю испачканную и загрязненную одежду.
Мыть руки перед перерывами и по окончании работы.
Поддерживайте эргономически подходящую рабочую среду.
Дыхательное оборудование:
Используйте подходящий респиратор при наличии высоких концентраций.
Рекомендуемое фильтрующее устройство для краткосрочного использования:
Используйте респиратор с картриджами типа P100 (США) или P3 (EN 143) в качестве резервного средства технического контроля. Необходимо провести оценку риска, чтобы определить, подходят ли респираторы для очистки воздуха.Используйте только оборудование, проверенное и одобренное в соответствии с соответствующими государственными стандартами.
Защита рук:
Непроницаемые перчатки
Осмотрите перчатки перед использованием.
Пригодность перчаток должна определяться как материалом, так и качеством, последнее из которых может варьироваться в зависимости от производителя.
Время проникновения материала перчаток (в минутах): Данные отсутствуют
Защита глаз: Защитные очки
Защита тела: Защитная рабочая одежда.
РАЗДЕЛ 9. ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
Информация об основных физических и химических свойствах
Внешний вид:
Форма: Различные формы (порошок/чешуйки/кристаллы/гранулы и т.д.)
Цвет: от светло-зеленого до темно-зеленого
Запах: без запаха
Порог восприятия запаха: Данные отсутствуют.
pH: неприменимо
Точка плавления/диапазон плавления: 2435 °C (4415 °F)
Точка/диапазон кипения: 3000 °C (5432 °F) газ): нет данных.
Температура воспламенения: Данные отсутствуют.
Температура разложения: Данные отсутствуют.
Самовоспламенение: Данные отсутствуют.
Опасность взрыва: Данные отсутствуют.
Пределы взрываемости:
Нижний: Данные отсутствуют
Верхний: Данные отсутствуют
Давление паров при 20 °C (68 °F): 0 гПа
Плотность при 20 °C (68 °F): 5,22 г/см 3 (43,561 фунта/гал)
Относительная плотность: Данные отсутствуют.
Плотность паров: N/A
Скорость испарения: N/A
Растворимость в воде (H 2 O): нерастворим
Коэффициент распределения (н-октанол/вода): Данные отсутствуют.
Вязкость:
Динамическая: Н/Д
Кинематика: Н/Д
Другая информация
Данные отсутствуют
РАЗДЕЛ 10.СТАБИЛЬНОСТЬ И РЕАКЦИОННАЯ СПОСОБНОСТЬ
Реакционная способность
Данные отсутствуют
Химическая стабильность
Стабилен при соблюдении рекомендуемых условий хранения.
Термическое разложение / условия, которых следует избегать:
Разложение не происходит, если используется и хранится в соответствии со спецификациями.
Возможность опасных реакций.
Реагирует с сильными окислителями.ТОКСИКОЛОГИЧЕСКАЯ ИНФОРМАЦИЯ
Информация о токсикологическом воздействии
Острая токсичность:
Вреден при вдыхании.
Вреден при проглатывании.
Реестр токсического воздействия химических веществ (RTECS) содержит данные об острой токсичности этого вещества.
Значения LD/LC50, важные для классификации: Нет данных
Раздражение или коррозия кожи: Может вызывать раздражение
Раздражение или коррозия глаз: Может вызывать раздражение
Сенсибилизация: Может вызывать аллергическую кожную реакцию.
Мутагенность зародышевых клеток:
Реестр токсических эффектов химических веществ (RTECS) содержит данные о мутациях для этого вещества.
Канцерогенность:
EPA-D: Канцерогенность для человека не классифицируется: неадекватные доказательства канцерогенности для людей и животных или данные отсутствуют.
EPA-CBD: канцерогенный потенциал не может быть определен.
IARC-3: Канцерогенность для человека не классифицируется.
ACGIH A4: Не классифицируется как канцероген для человека: Недостаточно данных для классификации агента с точки зрения его канцерогенности для людей и/или животных.
Реестр токсических эффектов химических веществ (RTECS) содержит данные об онкогенности, и/или канцерогенности, и/или новообразованиях для этого вещества.
Репродуктивная токсичность: Эффекты неизвестны.
Специфическая токсичность для системы органов-мишеней — многократное воздействие: Эффекты неизвестны.
Специфическая системная токсичность на орган-мишень — однократное воздействие: Эффекты неизвестны.
Опасность при вдыхании: Эффекты неизвестны.
От подострой до хронической токсичности:
Реестр токсических эффектов химических веществ (RTECS) содержит данные о токсичности при многократном приеме этого вещества.
Дополнительная токсикологическая информация:
Насколько нам известно, острая и хроническая токсичность этого вещества полностью не известна.
Раздел 12. Экологическая информация
Toxicity
Водная токсичность:
Нет данных Доступны
Устойчивость и деградальность
Нет данных Доступны
Биоаккумулятивный потенциал
Нет данных NO Data
Мобильность в почве
Нет данных Доступны
Дополнительная экологическая информация:
Избегайте передачи. в окружающую среду.
в окружающую среду.
Результаты оценки PBT и vPvB
PBT: н/д
vPvB: н/д
Другие неблагоприятные воздействия
Данные отсутствуют
РАЗДЕЛ 13. СООБРАЖЕНИЯ ПО УТИЛИЗАЦИИ
Методы обработки отходов
Рекомендация
См. официальные правила
Рекомендация
.
Неочищенная упаковка:
Рекомендация:
Утилизация должна производиться в соответствии с официальными правилами.
РАЗДЕЛ 14. ИНФОРМАЦИЯ О ТРАНСПОРТИРОВКЕ
Номер ООН
DOT, ADN, IMDG, IATA
N/A
Надлежащее отгрузочное наименование ООН
DOT, ADN, IMDG, IATA
N/A
DOT, ADR, ADN, IMDG, IATA
Class
N/A
Группа упаковки
DOT, IMDG, IATA
N/A
Опасность для окружающей среды:
N/A
Специальные меры предосторожности для пользователя
N/A
к Приложению II к MARPOL73/78 и IBC Code
N/A
Транспорт/Дополнительная информация:
DOT
Морской загрязнитель (DOT):
№
РАЗДЕЛ 15.
 НОРМАТИВНАЯ ИНФОРМАЦИЯ
НОРМАТИВНАЯ ИНФОРМАЦИЯ Нормы/законодательные акты по безопасности, охране здоровья и окружающей среды, относящиеся к данному веществу или смеси
Национальные нормативы
Все компоненты этого продукта перечислены в Реестре химических веществ Агентства по охране окружающей среды США.
Все компоненты этого продукта перечислены в Канадском перечне веществ для внутреннего потребления (DSL).
Раздел 313 SARA (списки конкретных токсичных химических веществ)
1308-38-9 Оксид хрома (III)
Предложение 65 штата Калифорния
Предложение 65 — Химические вещества, вызывающие рак
Вещество не указано в списке.
Prop 65 — Токсичность для развития
Вещество не указано.
Prop 65 — Токсичность для развития, женщины
Вещество не указано.
Prop 65 — Токсичность для развития, мужчины
Вещество не указано.
Информация об ограничении использования:
Только для использования технически квалифицированными лицами.
Другие правила, ограничения и запретительные положения
Вещество, вызывающее особую озабоченность (SVHC) в соответствии с Регламентом REACH (ЕС) № 1907/2006.
Вещество не указано.
Необходимо соблюдать условия ограничений согласно Статье 67 и Приложению XVII Регламента (ЕС) № 1907/2006 (REACH) для производства, размещения на рынке и использования.
Вещество не указано.
Приложение XIV Регламента REACH (требуется разрешение на использование)
Вещество не указано.
REACH — Предварительно зарегистрированные вещества
Вещество указано.
Оценка химической безопасности:
Оценка химической безопасности не проводилась.
РАЗДЕЛ 16.ПРОЧАЯ ИНФОРМАЦИЯ
Паспорт безопасности в соответствии с Регламентом (ЕС) № 1907/2006 (REACH). Приведенная выше информация считается верной, но не претендует на полноту и должна использоваться только в качестве руководства. Информация в этом документе основана на современном уровне наших знаний и применима к продукту с учетом соответствующих мер предосторожности. Это не является гарантией свойств продукта. American Elements не несет ответственности за любой ущерб, возникший в результате обращения или контакта с вышеуказанным продуктом. Дополнительные условия продажи см. на обратной стороне счета-фактуры или упаковочного листа. АВТОРСКИЕ ПРАВА 1997-2021 АМЕРИКАНСКИЕ ЭЛЕМЕНТЫ. ПРЕДОСТАВЛЯЕТСЯ ЛИЦЕНЗИЯ НА ИЗГОТОВЛЕНИЕ НЕОГРАНИЧЕННОГО БУМАЖНОГО КОПИЯ ТОЛЬКО ДЛЯ ВНУТРЕННЕГО ИСПОЛЬЗОВАНИЯ.
Дополнительные условия продажи см. на обратной стороне счета-фактуры или упаковочного листа. АВТОРСКИЕ ПРАВА 1997-2021 АМЕРИКАНСКИЕ ЭЛЕМЕНТЫ. ПРЕДОСТАВЛЯЕТСЯ ЛИЦЕНЗИЯ НА ИЗГОТОВЛЕНИЕ НЕОГРАНИЧЕННОГО БУМАЖНОГО КОПИЯ ТОЛЬКО ДЛЯ ВНУТРЕННЕГО ИСПОЛЬЗОВАНИЯ.
Кетоны — Sciencemadness Wiki
Кетоны представляют собой органические соединения, имеющие по крайней мере одну группу RC(=O)R’ , где R и R’ могут быть различными углеродсодержащими заместителями, такими как алканы. , алкены, алкины или ароматические соединения. Соединения с неуглеродными заместителями, такие как H, OH, NH 2 или галогены, являются не кетонами, а альдегидами, карбоновыми кислотами, амидами или ацилгалогенидами соответственно.
Свойства
Кетоны — бесцветные жидкости со слегка приятным запахом. Из всех кетонов только ацетон смешивается с водой, остальные растворимы или смешиваются с различными органическими растворителями.
Кетоны реакционноспособны как непосредственно в карбонильных, так и в их альфа-углеродных положениях. Нуклеофильное присоединение к карбонилу является обычным явлением, как в реакции реактивов Гриньяра с кетонами. Они образуют аддукты с бисульфитом и гидроксиламином, свойство, полезное для их выделения (вместе с альдегидами) из биологических образцов и других нечистых источников.
Нуклеофильное присоединение к карбонилу является обычным явлением, как в реакции реактивов Гриньяра с кетонами. Они образуют аддукты с бисульфитом и гидроксиламином, свойство, полезное для их выделения (вместе с альдегидами) из биологических образцов и других нечистых источников.
Подготовка
Кетоны могут быть легко получены окислением вторичных спиртов Джонсом с использованием триоксида хрома или дихромата калия, растворенных в разбавленной серной кислоте. Также можно использовать перманганат калия.
Более удобный способ включает пиролиз солей карбоновых кислот, процесс, известный как кетоновое декарбоксилирование. Однако этот процесс приводит к смешанным продуктам. Несколько примеров ниже:
Другие маршруты синтеза гидратация алкинов, реакция реактивов Гриньяра с нитрилами с последующим гидролизом, декарбоксилирование ангидридов карбоновых кислот, окисление аминов хлоридом железа(III), ацилирование по Фриделю-Крафтсу и др.
Безопасность
В отличие от альдегидов кетоны обладают низкой токсичностью и низким канцерогенным потенциалом. Однако они очень легко воспламеняются.
Ссылки
Соответствующие темы Sciencemadness
Факты об оксиде хрома III, формула, свойства, использование, данные о безопасности
Оксид хрома (iii), обычно называемый хромом и обозначаемый как оксо(оксохромиоокси)хром в номенклатуре ИЮПАК, представляет собой неорганическое соединение, содержащее хром и кислород, представленное химической формулой Cr 2 O 3 [1] .Он встречается в природе в виде минерального эсколаита и представляет собой труднорастворимое соединение с высокой термической стабильностью, обладающее свойствами как кислоты, так и основания [2, 3, 4] .
Оксид хрома (III) Идентификация | |
| Номер CAS | 1308-38-9 [1] |
| Идентификационный номер PubChem | 517277 [1] |
| ChemSpider ID | 451305 [5] |
| Номер ООН | 3077 [1] |
| Номер ЕС | 215-160-9 [1] |
| Номер RTECS | ГБ6475000 [1] |
| Ключ ИнЧИ | QDOXWKRWXJOMAK-UHFFFAOYSA-N [1] |
Оксид хрома (III) Формула
Как получают оксид хрома (III)
Его получают восстановлением дихромата натрия с помощью серы при высоких температурах, на что указывает окислительно-восстановительная реакция [6] :
Na 2 Cr 2 O 7 + S → Na 2 SO 4 + Cr 2 O 3
Дихромат аммония при нагревании разлагается на оксид хрома (iii), воду и азот [7] :
(NH 4 ) 2 Cr 2 O 7 → Cr 2 O 3 + N 2 + 3 O 4H 2
4 8 04Карбонат хрома (iii) нагревают с образованием оксида хрома (iii) и диоксида углерода:
Cr 2 (CO 3 ) 3 → Cr 2 O 3 + 3CO 2
Реакция с другими соединениями
Оксид хрома (III) с соляной кислотой
Реагирует с разбавленной соляной кислотой с образованием хлорида хрома (iii) и воды [8] :
Cr 2 O 3 + 6HCl → 2CrCl 3 + 3H 2 O
Оксид хрома (III) с сероводородом
При взаимодействии оксида хрома (iii) с газообразным сероводородом образуется сульфид хрома (iii) и вода:
Cr 2 O 3 + 3H 2 S → Cr 2 S 3 + 3H 2 O
Свойства и характеристики оксида хрома (III)
Общие свойства | |
| Молярная масса/молекулярная масса | 151. 989 г/моль [1, 3] 989 г/моль [1, 3] |
Физические свойства | |
| Цвет и внешний вид | Сухой мелкокристаллический порошок светло- или темно-зеленого цвета [1, 3] |
| Температура плавления | 2435 °C, 4415 °F [1] |
| Температура кипения | 4000 °C, 7230 °F [1] |
| Плотность | 5.22 г см -3 [1, 3] |
| Состояние вещества при комнатной температуре | Твердый [1, 3] |
| Растворимость | Нерастворим в ацетоне и спирте, очень мало растворим в щелочах и кислотах [1] |
| Растворимость в воде | Практически нерастворим, 2,96 мкг/л (20 °C, pH 8), 3,13 мкг/л (20 °C, pH 6) [1] |
| Магнитная восприимчивость ( χ ) | 1960. 0 X 10 -6 см 3 /моль 0 X 10 -6 см 3 /моль |
Атомные свойства | |
| Кристаллическая структура | Шестигранник |
Оксид хрома (III)
Использование
Безопасно ли это
Воздействие оксида хрома (iii) через рот и кожу может вызвать острую токсичность [1] . Это может вызвать аллергическую кожную реакцию и серьезное повреждение глаз [1] . Он также может вызывать репродуктивную токсичность и вреден для будущего ребенка [1] .
Каталожные номера
Какова химическая формула оксида хрома (III)?
Первое, на что следует обратить внимание, это то, что вы имеете дело с ионным соединением , которое содержит хром , #»Cr»#, переходный металл , и кислород, #»O»#, не -металл .
Самое интересное в этом соединении то, что оно содержит переходный металл в качестве катиона , т. цвет(красный)(2-)] -> » Cr «_ цвет (красный) (2) «O» _ цвет (синий) (3) #
цвет(красный)(2-)] -> » Cr «_ цвет (красный) (2) «O» _ цвет (синий) (3) #
Таким образом, химическая формула оксида хрома (III) будет
.#color(green)(|bar(ul(color(white)(a/a)color(black)(«Cr»_2″O»_3)color(white)(a/a)|)))#
Оксид хрома – обзор
8.1.2 Фазовые равновесия с оксидом хрома
В системе Cr 2 O 3 -Al 2 O 3 оксид хрома не образует промежуточных фаз с оксидом алюминия, поскольку ниже линия солидуса, по крайней мере, выше 1500 К. При более низких температурах твердый раствор имеет тенденцию к распаду на два изоморфных раствора, богатых хромом и глиноземом. Область сосуществования этих двух растворов составляет примерно от 15% до 25% до 50-70 мол.% Cr 2 O 3 , но точное положение фазовых границ остается предметом обсуждения.
Достоверные данные о фазовых равновесиях в системе хром-кремнезем и наличии металлического хрома в контакте с силикатными расплавами важны для оптимизации шлаковых режимов восстановительных процессов при производстве хромовых ферросплавов.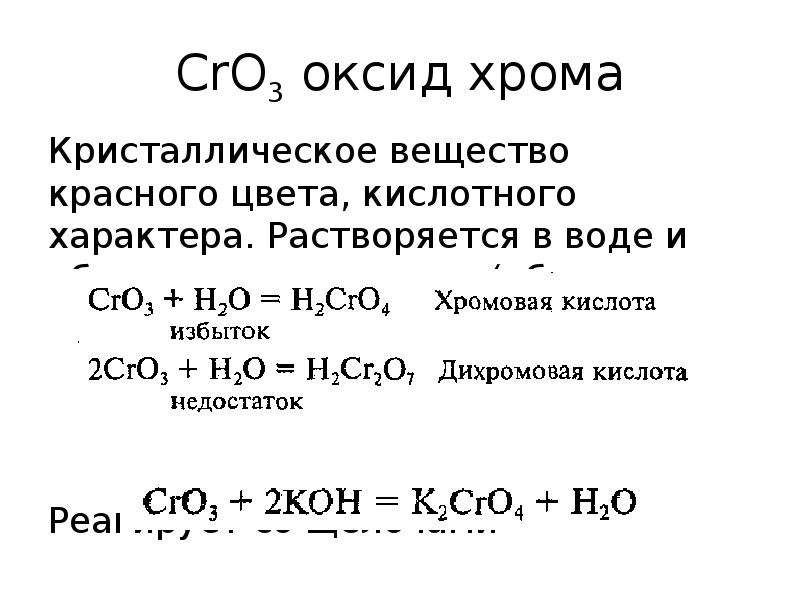 Эти данные представляют большой теоретический и практический интерес для производства хромсодержащих сталей и окислительного обезуглероживания высокоуглеродистого феррохрома в конвертерах.В условиях высокого окислительного потенциала газовой фазы и отсутствия металлического хромсодержащего расплава кремнезем не реагирует с Cr 2 O 3 .
Эти данные представляют большой теоретический и практический интерес для производства хромсодержащих сталей и окислительного обезуглероживания высокоуглеродистого феррохрома в конвертерах.В условиях высокого окислительного потенциала газовой фазы и отсутствия металлического хромсодержащего расплава кремнезем не реагирует с Cr 2 O 3 .
В восстановительных условиях (низкий окислительный потенциал газовой фазы и наличие металлического хрома) взаимодействие кремнезема с оксидом хрома (Cr 2 O 3 ) сопровождается восстановлением Cr 3+ → Cr 2+ с последующим образованием силикатного расплава «CrO»-SiO 2 .Здесь гипотетическая фазовая диаграмма (рис. 8.10) показывает, где вместо Cr 2 O 3 используется оксид «CrO». Как показано для системы Cr-O, в чисто кислых (богатых кремнеземом) средах соотношение Cr 3+ / Cr 2+ существенно снижается, что приводит к тому, что форма Cr 2+ находится в равновесии с кремнеземом. -богатые расплавы. Поскольку CrO не является самостоятельной стабильной фазой при нормальных условиях, он описывается составом Cr 2 O 3 + Cr в областях с низким содержанием кремнезема.На рис. 8.10 также показана область существования силиката хрома Cr 2 SiO 4 . Хотя и приблизительный, он объясняет некоторые технологические приемы, применяемые при производстве хромистых ферросплавов и сталей.
-богатые расплавы. Поскольку CrO не является самостоятельной стабильной фазой при нормальных условиях, он описывается составом Cr 2 O 3 + Cr в областях с низким содержанием кремнезема.На рис. 8.10 также показана область существования силиката хрома Cr 2 SiO 4 . Хотя и приблизительный, он объясняет некоторые технологические приемы, применяемые при производстве хромистых ферросплавов и сталей.
РИСУНОК 8.10. Фазовая диаграмма «CrO»-SiO 2 .
В отличие от кремнезема, кальций как основной оксид сдвигает равновесие в сторону более высоких валентностей хрома в присутствии кислорода. CaO образует хромит кальция (CaCr 2 O 4 ) с Cr 2 O 3 при высоких температурах в области, богатой хромом (рис.8.11). Этот хромит не стабилен при более низких температурах, и его состав также известен как (Ca 2 Cr 3 )Cr 10 O 20 , то есть как смешанный хромит кальция (Decterov and Pelton, 1997).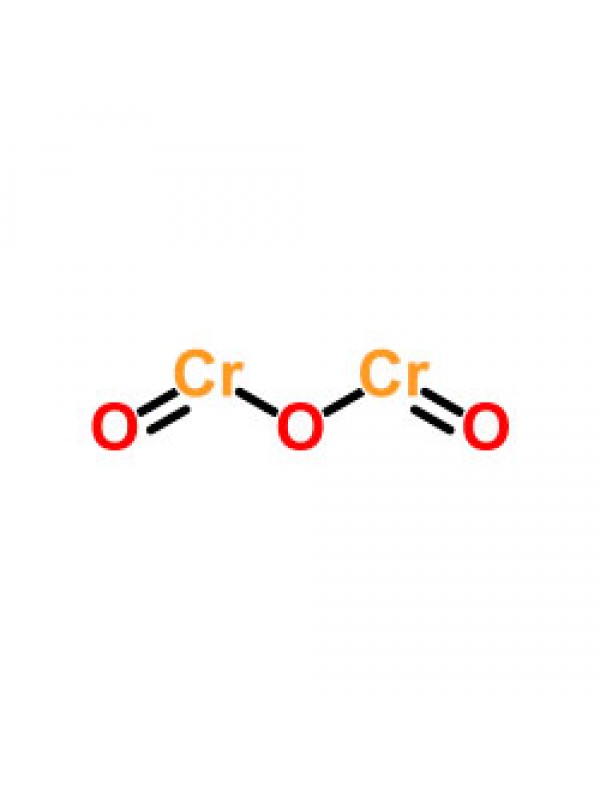 ). При увеличении содержания CaO соотношение Cr 6+ /Cr 3+ становится выше и образуется хромат кальция CaCrO 4 . Далее идентифицированы еще два комплексных соединения (хромит-хроматы кальция) состава 9CaO·4CrO 3 ·Cr 2 O 3 и 3CaO·2CrO 3 ·Cr 2 O 3 .Предлагалось также рассматривать эту диаграмму как часть тройного равновесия CaO-Cr 2 O 3 -CrO 3 (Kaiser et al., 1992; Лякишев, Гасик, 1998). Например, Kaiser et al. (1992) определили, что композиции Ca 5 (CrO 4 ) 3 O стабильны на воздухе при температуре от 776° до 959°C, Ca 3 (CrO 4 ) 2 между 882° и 1253°С и Ca 5 (CrO 4 ) 3 между 1140°С и 1297°С, но неустойчивы в восстановительных условиях.
). При увеличении содержания CaO соотношение Cr 6+ /Cr 3+ становится выше и образуется хромат кальция CaCrO 4 . Далее идентифицированы еще два комплексных соединения (хромит-хроматы кальция) состава 9CaO·4CrO 3 ·Cr 2 O 3 и 3CaO·2CrO 3 ·Cr 2 O 3 .Предлагалось также рассматривать эту диаграмму как часть тройного равновесия CaO-Cr 2 O 3 -CrO 3 (Kaiser et al., 1992; Лякишев, Гасик, 1998). Например, Kaiser et al. (1992) определили, что композиции Ca 5 (CrO 4 ) 3 O стабильны на воздухе при температуре от 776° до 959°C, Ca 3 (CrO 4 ) 2 между 882° и 1253°С и Ca 5 (CrO 4 ) 3 между 1140°С и 1297°С, но неустойчивы в восстановительных условиях.
РИСУНОК 8.11. Фазовая диаграмма CaO-Cr 2 O 3 .
Существенное снижение температуры ликвидуса (<1775°C) в диапазоне составов (от 30% до 60% Cr 2 O 3 ) используется для переработки известково-хромовых расплавов при производстве низкоуглеродистого FeCr путем смешение FeSiCr и CaO-Cr 2 O 3 расплавов.
Помимо равновесий хрома с CaO и SiO 2 , система Cr 2 O 3 -MgO является одной из важнейших систем в производстве ферросплавов и сталей.В этой системе образуется только одно соединение (магниевая шпинель MgCr 2 O 4 ), но MgO имеет широкую область растворимости, уменьшающуюся с понижением температуры (рис. 8.12). Сообщалось также, что хромит магния имеет некоторый диапазон гомогенности.
РИСУНОК 8.12. Фазовая диаграмма MgO-Cr 2 O 3 при P O 2 = 0,2 атм.
Обсуждавшиеся ранее бинарные системы с Cr 2 O 3 не проявляются как таковые в ферросплавных процессах, но они образуют основу для тройных и более сложных комбинаций.Наиболее важные из них кратко представлены в этой главе.
В тройной системе Cr 2 O 3 -Al 2 O 3 -SiO 2 большая область твердых растворов корунда, а также узкое протяженное поле муллита (2Al 3
) 3 ·2SiO 2 ) (Лякишев, Гасик, 1998). Состав тройной эвтектической жидкости имеет 6% мас. Al 2 O 3 и 1% масс. Cr 2 O 3 .В конце концов, здесь не оказывается равновесных тройных соединений. Из-за взаимной растворимости оксида алюминия и хрома (корундовая фаза) оксид алюминия, возможно, не так сильно влияет на соотношение Cr 2+ /Cr 3+ , как кремнезем.
Состав тройной эвтектической жидкости имеет 6% мас. Al 2 O 3 и 1% масс. Cr 2 O 3 .В конце концов, здесь не оказывается равновесных тройных соединений. Из-за взаимной растворимости оксида алюминия и хрома (корундовая фаза) оксид алюминия, возможно, не так сильно влияет на соотношение Cr 2+ /Cr 3+ , как кремнезем.Напротив, в тройной системе Cr 2 O 3 -CaO-SiO 2 имеется тройное соединение 3CaO·Cr 2 O 3 ·3SiO , природный минерал уваровит (Ca 3 Cr 2 Si 3 O 12 ), относящийся к группе гранатов.Если хром находится в окисленном состоянии 3+ (кислородный потенциал в газовой фазе достаточно высок), жидкая фаза имеет разрыв в смешиваемости двух жидкостей: почти чистого кремнезема и высококремнеземистого расплава с массовой долей 27%. СаО и ~1% мас. Cr 2 O 3 .
Однако, как было отмечено для бинарных систем, уровень кислородного потенциала, наличие металлического хрома и основность шлака (соотношение CaO/SiO 2 ) оказывают сильное влияние на степень окисления хрома, которая может изменяться от + 2 («CrO») до +6 (CrO 3 ). Экспериментальные исследования (Villiers and Muan, 1992; Xiao and Holappa, 1993) подтвердили, что для реалистичных условий можно было бы достичь более правильных равновесий ликвидуса и твердых тел, если рассматривать эту систему как четвертичную: CaO-CrO-Cr 2 O 3 -SiO 2 .
Экспериментальные исследования (Villiers and Muan, 1992; Xiao and Holappa, 1993) подтвердили, что для реалистичных условий можно было бы достичь более правильных равновесий ликвидуса и твердых тел, если рассматривать эту систему как четвертичную: CaO-CrO-Cr 2 O 3 -SiO 2 .
Для системы Cr 2 O 3 -MgO-SiO 2 о тройных соединениях не сообщалось, но был обнаружен большой разрыв в смешиваемости. Основными фазами в этой системе являются в основном хром, MgO и MgCr 2 O 4 , соседствующие с двойной Cr 2 O 3 -SiO 2 .
Замена различными оксидами по-разному влияет на активность хрома (Xiao and Holappa, 1993). Как и следовало ожидать, замена CaO в шлаках на MgO снижает активность оксидов хрома, но не оказывает существенного влияния на соотношение Cr 2+ /Cr 3+ . Незначительные добавки оксида алюминия повышают активность оксидов хрома, тогда как более высокие количества не дают такого эффекта. Это показывает, что шлаки переработки феррохрома могут вести себя весьма по-разному, если их состав меняется в процессе.
Это показывает, что шлаки переработки феррохрома могут вести себя весьма по-разному, если их состав меняется в процессе.
Оксид хрома(III) Хром для керамики Fantastic Glaze
Что делает оксид хрома в глазури? Как вы используете оксиды в керамике? Что означает оксид в керамике? Является ли оксид хрома таким же, как оксид хрома
Cr 2 O 3
Из-за своей значительной стабильности хром является широко используемым пигментом. Первоначально он назывался виридиан. Он используется в красках, чернилах и стеклах. Это краситель в «хромовом зеленом» и «институциональном зеленом».Оксид хрома (III) является предшественником магнитного пигмента диоксида хрома, по следующей реакции: Наряду со многими другими оксидами он используется в качестве соединения при полировке (также называемой строганием) лезвий ножей, бритв, поверхностей оптических устройства и т. д. на куске кожи, бальзы, ткани или другого материала. Он доступен в виде порошка или воска и в этом контексте известен как «зеленое соединение»
Оксид хрома (III) — применение in Pottery
Оксид хрома является очень тугоплавким красителем для керамики (даже 50% смесь с фриттой с высоким содержанием буры даже не начнет плавить его в тигле). Оксид хрома является единственным стабильным оксидом металлического хрома. Это кристаллический порошок от светло- до темно-зеленого цвета, нерастворимый в щелочах и кислотах. Он производится из минерала хромита, добываемого в Южной Африке, Азии, Турции и на Кубе. Как и в случае с другими сильными красителями, хром необходимо измельчать достаточно тонко, чтобы исключить образование пятен на стекле или глазури. Хром является «быстрым» красителем, что означает, что он может давать сильный зеленый цвет при любых условиях печи, медленных или быстрых, восстановительных или окислительных. Это также плоский краситель (из-за его тугоплавкости), он обычно дает непрозрачный зеленый цвет для армейских шлемов.Он мощный, обычно только 2% дают темный цвет. Его нельзя использовать для изготовления металлической глазури. Оксид хрома обычно используется в сырых глазурях, тогда как дихромат калия используется в фритте. Поскольку Cr2O3 превращается в 2CrO3, кислород поглощается из окружающей среды, поэтому процент (или коэффициент преобразования) превышает 100.
Оксид хрома является единственным стабильным оксидом металлического хрома. Это кристаллический порошок от светло- до темно-зеленого цвета, нерастворимый в щелочах и кислотах. Он производится из минерала хромита, добываемого в Южной Африке, Азии, Турции и на Кубе. Как и в случае с другими сильными красителями, хром необходимо измельчать достаточно тонко, чтобы исключить образование пятен на стекле или глазури. Хром является «быстрым» красителем, что означает, что он может давать сильный зеленый цвет при любых условиях печи, медленных или быстрых, восстановительных или окислительных. Это также плоский краситель (из-за его тугоплавкости), он обычно дает непрозрачный зеленый цвет для армейских шлемов.Он мощный, обычно только 2% дают темный цвет. Его нельзя использовать для изготовления металлической глазури. Оксид хрома обычно используется в сырых глазурях, тогда как дихромат калия используется в фритте. Поскольку Cr2O3 превращается в 2CrO3, кислород поглощается из окружающей среды, поэтому процент (или коэффициент преобразования) превышает 100. Металлические оксиды с 50% феррофритт 3134 в тиглях при конусе 6ox. Хром и рутил не плавятся, медь и кобальт чрезвычайно активны в плавке. Кобальт и медь кристаллизовались при охлаждении, марганец образовал радужное стекло.
Металлические оксиды с 50% феррофритт 3134 в тиглях при конусе 6ox. Хром и рутил не плавятся, медь и кобальт чрезвычайно активны в плавке. Кобальт и медь кристаллизовались при охлаждении, марганец образовал радужное стекло.
Формула: Cr 2 O 3
Молекулярный вес: 151,9904 г/моль
Форма: порошок Триоксид дихрома, хромия, полуторный оксид хрома
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только та информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
.



 Данная реакция специфична для хрома и очень чувствительна. С ее помощью можно обнаружить хром в металлах и сплавах. Прежде всего необходимо растворить металл. При длительном кипячении с 30% — ной серной кислотой (можно добавить и соляную кислоту) хром и многие стали частично растворяются. Полученный раствор содержит сульфат хрома (III). Чтобы можно было провести реакцию обнаружения, сначала нейтрализуем его едким натром. В осадок выпадает серо-зеленый гидроксид хрома (III), который растворится в избытке NaOH и образует зеленый хромит натрия. Профильтруем раствор и добавим 30% -ый пероксид водорода. При нагревании раствор окрасится в желтый цвет, так как хромит окислится до хромата. Подкисление приведет к появлению голубой окраски раствора. Окрашенное соединение можно экстрагировать, встряхивая с эфиром.
Данная реакция специфична для хрома и очень чувствительна. С ее помощью можно обнаружить хром в металлах и сплавах. Прежде всего необходимо растворить металл. При длительном кипячении с 30% — ной серной кислотой (можно добавить и соляную кислоту) хром и многие стали частично растворяются. Полученный раствор содержит сульфат хрома (III). Чтобы можно было провести реакцию обнаружения, сначала нейтрализуем его едким натром. В осадок выпадает серо-зеленый гидроксид хрома (III), который растворится в избытке NaOH и образует зеленый хромит натрия. Профильтруем раствор и добавим 30% -ый пероксид водорода. При нагревании раствор окрасится в желтый цвет, так как хромит окислится до хромата. Подкисление приведет к появлению голубой окраски раствора. Окрашенное соединение можно экстрагировать, встряхивая с эфиром. Обратите внимание на цвет образовавшегося хромита натрия. Нагрейте полученный раствор на водяно бане. Что при этом происходит?
Обратите внимание на цвет образовавшегося хромита натрия. Нагрейте полученный раствор на водяно бане. Что при этом происходит? Нагревая 2мг глицерина с небольшим количеством (NH 4) 2 Cr 2 O 7 с последующим добавлением спирта, после фильтрования получается ярко-зеленый раствор, который при добавлении кислоты становится желтым, а в нейтральной или щелочной среде становится зеленым.
Нагревая 2мг глицерина с небольшим количеством (NH 4) 2 Cr 2 O 7 с последующим добавлением спирта, после фильтрования получается ярко-зеленый раствор, который при добавлении кислоты становится желтым, а в нейтральной или щелочной среде становится зеленым.
