Кислоты и основания — это… Что такое Кислоты и основания?
классы химических соединений. Обычно кислотами называют вещества, содержащие водород (HCl, HNO3, H2SO4, CH3COOH и т.д.) и диссоциирующие в воде с образованием ионов Н+ (точнее, ионов гидроксония H3O+). Присутствие этих ионов обусловливает характерный острый вкус водных растворов кислот, а также их способность изменять окраску индикаторов химических (См. Индикаторы химические). По числу отщепляющихся протонов различают кислоты одноосновные (например, азотная HNO3, соляная HCl, уксусная CH3COOH), двухосновные (серная H2SO4, угольная H2CO3), трехосновные (ортофосфорная H3PO4). Чем больше ионов гидроксония присутствует в водном растворе кислоты, т. е. чем выше степень диссоциации последней, тем кислота сильнее. Кислоты, полностью диссоциированные в разбавленных растворах, называют сильными. К слабым относятся кислоты с константой ионизации (характеризующей степень диссоциации кислоты в растворе, например, при 25 °С) ниже 10
где BF3 — кислота, а NH3 — основание. Важная особенность кислотно-основных реакций, по Льюису, состоит в обобществлении электронной пары основания. Этим они отличаются от окислительно-восстановительных реакций, в ходе которых молекулы окислителя полностью отбирают по одному или несколько электронов у молекул восстановителя; никаких обобществленных орбит при этом не возникает. В отличие от Брёнстеда, Льюис связывает кислотно-основные свойства не с наличием определенных химических элементов (в частности, водорода), а исключительно со строением внешних электронных оболочек атомов. В то же время между обеими концепциями имеется внутренняя связь, основанная на том, что для иона Н
Я. М. Варшавский.
Принцип жёстких и мягких кислот и оснований — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 17 января 2017; проверки требуют 3 правки. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 17 января 2017; проверки требуют 3 правки.Принцип жёстких и мягких кислот и оснований (принцип ЖМКО, принцип ЖМКО Пирсона, англ. HSAB theory) — в химии принцип, качественно описывающий способность кислот и оснований Льюиса к эффективному взаимодействию. Данный принцип был предложен американским химиком-неоргаником Ральфом Пирсоном[en] в 1963 году[1][2][3]. В соответствии с данным принципом, кислоты и основания Льюиса делятся на жёсткие и мягкие, причём мягкие кислоты преимущественно реагируют с мягкими основаниями, а жёсткие кислоты — с жёсткими основаниями[4].
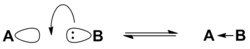
Принцип ЖМКО касается взаимодействий, рассматриваемых в теории кислот и оснований Льюиса. Согласно этой теории, основание Льюиса B отдаёт электронную пару на образование ковалентной связи с кислотой Льюиса A, которая имеет вакантную орбиталь. Эффективность такого взаимодействия зависит от химического состава и электронного строения реагирующих кислоты и основания. Данные параметры учтены Пирсоном при классификации кислот и оснований на мягкие и жёсткие.
Согласно Пирсону, жёсткие кислоты — это акцепторы электронной пары, обладающие малым размером, большим положительным зарядом, большой электроотрицательностью и низкой поляризуемостью. Молекулярная орбиталь, на которую переходит электронная пара, у жёстких кислот имеет низкую энергию. Соответственно, жёсткие основания — это доноры с аналогичными свойствами (с большим отрицательным зарядом, большой электроотрицательностью и низкой поляризуемостью). Их орбиталь, с которой отдаётся электронная пара, также имеет низкую энергию. Мягкие кислоты — это кислоты Льюиса с малым положительным зарядом, большим размером, низкой электроотрицательностью и высокой поляризуемостью. Мягкие основания — это основания Льюиса с теми же свойствами. Как у мягких кислот, так и у мягких оснований энергия орбиталей, участвующих в реакции высока. Поскольку такие свойства как заряд, электроотрицательность и поляризуемость изменяются плавно, существует ряд кислот и оснований Льюиса, которые занимают промежуточное положение между жёсткими и мягкими[5].
Жёсткость кислоты или основания означает его склонность образовывать связи преимущественно ионного характера, а мягкость кислоты или основания — склонность к образованию связей ковалентного характера[6].
| Жёсткие кислоты | Промежуточные кислоты | Мягкие кислоты |
|---|---|---|
| H+, Li+, Na+, K+, Mg2+, Ca2+, Al3+, Cr3+, Fe3+, BF3, B(OR)3, AlR3, AlCl3, SO3, -RCO+, CO2, RSO2+ | Cu2+, Fe2+, Zn2+, SO2, R3C+, C6H5+, NO+ | Ag+, Cu+, Hg2+, RS+, I+, Br+, Pb2+, BH3, карбены |
| Жёсткие основания | Промежуточные основания | Мягкие основания |
| OH—, RO—, F—, Cl—, RCOO—, NO3—, NH3, RNH2, H2O, ROH, SO42-, CO32-, R2O, NR2—, NH2— | Br—, C6H5NH2, NO2—, C5H5N | RS—, RSH, I—, H—, R3C—, алкены, C6H6, R3P, (RO)3P |
Помимо условного деления на три типа, можно также проследить зависимость жёсткости или мягкости в рядах отдельных кислот и оснований Льюиса. Например, при движении по группе периодической системы сверху вниз жёсткость оснований уменьшается[7]:
F−>Cl−>Br−>I−.{\displaystyle {\mathsf {F^{-}>Cl^{-}>Br^{-}>I^{-}.}}}
Для изоэлектронных соединений жёсткость возрастает при движении по периоду слева направо[7]:
Nh3−<OH−<F−.{\displaystyle {\mathsf {NH_{2}^{-}<OH^{-}<F^{-}.}}}
Жёсткость кислот уменьшается при движении по группе сверху вниз[7]:
Li+>Na+>K+;{\displaystyle {\mathsf {Li^{+}>Na^{+}>K^{+};}}}
Zn2+>Cd2+>Hg2+.{\displaystyle {\mathsf {Zn^{2+}>Cd^{2+}>Hg^{2+}.}}}
В органической химии принцип ЖМКО широко применяется для предсказания или объяснения протекания химических реакций.
Например, реакцию между тиоэфиром CH3COSR и алкоголят-ионом RO— можно представить как переход ацильного катиона CH3CO+ (жёсткой кислоты Льюиса) от мягкого основания Льюиса RS— к жёсткому основанию Льюиса RO—. Согласно принципу ЖМКО, аддукт жёсткой кислоты и жёсткого основания более устойчив, поэтому равновесие в реакции сдвинуто вправо[7].

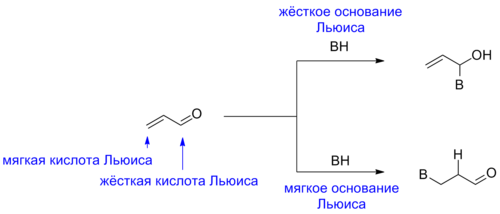
Принцип Пирсона также полезен для предсказания реакционной способности соединений с двумя реакционными центрами, например, енолят-ионов или α,β-ненасыщенных соединений. Последние, например, склонны к реакциям с нуклеофилами по двум положениям, причём преимущественное направление реакции зависит от жёсткости нуклеофила как основания Льюиса[7].
- ↑ Pearson в JACS, 1963.
- ↑ Pearson в JCE 1, 1968.
- ↑ Pearson в JCE 2, 1968.
- ↑ Химическая энциклопедия / Под ред. И. Л. Кнунянца. — М: Большая Российская энциклопедия, 1992. — Т. 2. — С. 145. — ISBN 5-85270-039-8.
- ↑ 1 2 Москва В. В. Понятие кислоты и основания в органической химии // Соросовский образовательный журнал. — 1996. — № 12. — С. 33—40.
- ↑ 1 2 Золотов Ю. А., Дорохова Е. Н., Фадеева В. И. и др. Основы аналитической химии. Книга 1. Общие вопросы. Методы разделения / Под ред. Ю. А. Золотова. — 2-е изд., перераб. и доп. — М: Высшая школа, 1999. — С. 152—153. — ISBN 5-06-003558-1.
- ↑ 1 2 3 4 5 Реутов О. А., Курц А. Л., Бутин К. П. Органическая химия. — 3-е изд.. — М: Бином. Лаборатория знаний, 2010. — Т. 1. — С. Глава 3. — ISBN 978-5-94774-614-9.
Оригинальные работы[править | править код]
- Pearson R. G. Hard and Soft Acids and Bases (англ.) // J. Am. Chem. Soc. — 1963. — Vol. 85, no. 22. — P. 3533—3539. — DOI:10.1021/ja00905a001.
- Pearson R. G. Hard and soft acids and bases, HSAB, part 1: Fundamental principles (англ.) // J. Chem. Educ. — 1968. — Vol. 45, no. 9. — P. 581—586. — DOI:10.1021/ed045p581.
- Pearson R. G. Hard and soft acids and bases, HSAB, part II: Underlying theories (англ.) // J. Chem. Educ. — 1968. — Vol. 45, no. 10. — P. 643—648. — DOI:10.1021/ed045p643.
Обзоры[править | править код]
Теории кислот и оснований — это… Что такое Теории кислот и оснований?
Теории кислот и оснований — совокупность фундаментальных физико-химических представлений, описывающих природу и свойства кислот и оснований. Все они вводят определения кислот и оснований — двух классов веществ, реагирующих между собой. Задача теории — предсказание продуктов реакции между кислотой и основанием и возможности её протекания, для чего используются количественные характеристики силы кислоты и основания. Различия между теориями лежат в определениями кислот и оснований, характеристики их силы и, как следствие — в правилах предсказания продуктов реакции между ними. Все они имеют свою область применимости, каковые области частично пересекаются.
Кислотно-основные взаимодействия чрезвычайно распространенены в природе и находят широкое применение в научной и производственной практике. Теоретические представления о кислотах и основаниях имеют важное значение в формировании всех концептуальных систем химии и оказывают разностороннее влияние на развитие многих теоретических концепций во всех основных химических дисциплинах.
На основе современной теории кислот и оснований разработаны такие разделы химических наук, как химия водных и неводных растворов электролитов, рН-метрия в неводных средах, гомо- и гетерогенный кислотно-основный катализ, теория функций кислотности и многие другие.
Эволюция представлений о кислотно-основных взаимодействиях

Представления о кислотно-основных взаимодействиях относятся к числу фундаментальных химических положений. Понятия «кислота» и «основание» сформировались еще в XVII веке, однако их содержание неоднократно пересматривалось и уточнялось.
Образная теория кислот и оснований была предложена Н. Лемери. В своем «Курсе химии» (1675) он попытался объяснить физические и химические свойства веществ на языке их формы и структуры. Согласно представлениям Лемери кислоты на своей поверхности имеют острые шипы, вызывающие на коже колющие ощущения. Основания, названные им щелочами, состоят из пористых тел. «Шипы» кислот проникают в «поры», при этом они ломаются или притупляются, и кислоты превращаются в нейтральные соли[1].
Научные представления о природе кислот и оснований начали формироваться в конце XVIII в. В работах А. Лавуазье кислотные свойства связывались с наличием в составе вещества атомов кислорода. Известные тогда минеральные и органические кислоты, действительно, содержали кислород. Эта гипотеза быстро показала свою несостоятельность, когда благодаря работам Г. Дэви и Ж. Гей-Люссака стал известен целый ряд кислот, не содержащих кислорода (например, галогеноводороды, синильные кислоты), в то время, как многие кислородсодержащие соединения не проявляют кислотных свойств.
С начала XIX века кислотами стали считать вещества, способные к взаимодействию с металлам с выделением водорода (Ю. Либих, 1839). Примерно в это же время Й. Берцелиус выдвинул идею, объясняющую кислотно-основные свойства веществ их электрической «дуалистической» природой. Так, к кислотам он относил электроотрицательные оксиды неметаллов и некоторых металлов (например, хрома, марганца и др.), а электроположительные оксиды металлов считал основаниями. Таким образом, кислотность или основность Берцелиусом рассматривается как функциональное, а не абсолютное свойство соединения. Берцелиус впервые сделал попытку количественной оценки и предсказания силы кислот и оснований[2].
C появлением теории электролитической диссоциации С. Аррениуса (1887) возникла возможность описания кислотно-основных свойств исходя из продуктов ионизации электролита. Благодаря работам В. Оствальда теория получила развитие для слабых электролитов.
В начале XX в. американские химики Г. Кэди, Э. Франклин и Ч. Краус создали теорию сольвосистем, распространившую положения теории Аррениуса-Освальда на все растворители, способные к самодиссоциации.
В основу современных теорий кислот и оснований положены представления Й. Брёнстеда и Г. Льюиса. Имеются вполне успешные попытки создать обобщенные теории (М. Усанович, 1939), но они не находят широкого применения[3].
Водородная теория Либиха
Определения. Кислота — вещество, способное реагировать с металлом с выделением водорода. Понятие «основание» в этой теории отсутствует.
Продукты реакции. При реакции кислоты с металлом образуется соль и водород.
Примеры. Кислота — HCl.
Реакция 2HCl + Zn = ZnCl2 + H2↑
Критерии протекания реакции. С сильными кислотами реагируют металлы, стоящие в ряду активностей левее водорода. Чем слабее кислота, тем более активный металл нужен для реакции между ними. Количественные характеристики. Поскольку теория используется редко, количественные характеристики силы кислоты (а значит, и предсказания направления реакции) в рамках данной теории не разработаны.
Область применимости. Предсказание взаимодействия водородсодержащих веществ с металлами в любых растворителях.
Специфические черты. В соответствии с этой теорией этиловый спирт и аммиак являются слабыми кислотами, так как способны реагировать со щелочными металлами:
- 2C2H5OH + 2Na = 2C2H5ONa + H2↑
- 2NH3 + 2Na = 2NaNH2 + H2↑
Теория электролитической диссоциации Аррениуса-Оствальда

Основная статья: Теория электролитической диссоциации
Определения. Кислоты — это вещества, образующие в водном растворе ионы гидратированные катионы водорода Н+ (ионы гидроксония) и анионы кислотного остатка.
Основания — вещества, диссоциирующие в водном растворе с образованием катионов металла и гидроксид-анионов ОН−.
Соли — вещества, диссоциирующие с образованием катиона металла и аниона кислотного остатка.
Продукты реакции. В реакции кислоты с основанием (реакция нейтрализации образуется соль и соли и воды.
Примеры. Кислота — HCl (кислотный остаток Cl—):
- HCl + H2O ↔ H3O+ + Cl—
Основание — NaOH:
- NaOH ↔ Na+ + OH—
Реакция нейтрализации (соль — NaCl):
- HCl + NaOH = NaCl + H2O
Критерии протекания реакции. Сильные кислоты реагируют с сильными основаниями. Чем слабее кислота, тем более сильное основание нужно для реакции.
Количественные характеристики Сила кислоты и основания характеризуются их константами диссоциации K.
- Для кислоты HA K = [H+]·[A—]/[HA]
- Для основания MOH K = [M+]·[OH—]/[MOH]
Чтобы прошла реакция между кислотой и основанием, произведение их констант диссоциации должно быть больше, чем 10-14 (ионное произведение воды).
Область применимости. Она вполне удовлетворительно описывает реакции достаточно сильных кислот и оснований друг с другом и свойства их водных растворов. На основе представлений о степени и константе диссоциации было закреплено деление электролитов на сильные и слабые, введено понятие водородного показателя, распространение которого на щелочные среды требует, однако, дополнительных допущений (введения ионного произведения воды).
Теорию можно применять для описания гидролиза солей и реакции кислот и оснований с солями, однако при этом требуется весьма громоздкий аппарат — протонная теория (см. ниже) гораздо удобнее.
Применимость теории Аррениуса-Оствальда ограничивается водными растворами. кроме того, она не позволяет объяснить наличие основных свойств аммиака, фосфина и других соединений, не содержащих гидроксогрупп.
Протонная теория Брёнстеда-Лаури
Основная статья: Протолитическая теория кислот и оснований
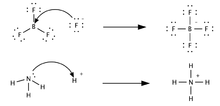 Сравнение моделей
Сравнение моделейкислотно-основного взаимодействия
по Льюису и Брёнстеду
Протолитическая (протонная) теория кислот и оснований была предложена в 1923 году независимо друг от друга датским учёным Й. Брёнстедом и английским учёным Т. Лаури. В ней понятие о кислотах и основаниях было объединено в единое целое, проявляющееся в кислотно-основном взаимодействии: А  В + Н+ (А — кислота, В — основание). Согласно этой теории кислотами являются молекулы или ионы, способные быть в данной реакции донорами протонов, а основаниями являются молекулы или ионы, присоединяющие протоны (акцепторы). Кислоты и основания получили общее название протолитов.
В + Н+ (А — кислота, В — основание). Согласно этой теории кислотами являются молекулы или ионы, способные быть в данной реакции донорами протонов, а основаниями являются молекулы или ионы, присоединяющие протоны (акцепторы). Кислоты и основания получили общее название протолитов.
Сущностью кислотно-основного взаимодействия является передача протона от кислоты к основанию. При этом кислота, передав протон основанию, сама становится основанием, так как может снова присоединять протон, а основание, образуя протонированную частицу, становится кислотой. Таким образом, в любом кислотно-основном взаимодействии участвуют две пары кислот и оснований, названные Бренстедом сопряженными: А1 + В2  А2 + В1.
А2 + В1.
Одно и то же вещество в зависимости от условий взаимодействия может быть как кислотой, так и основанием (амфотерность). Например, вода при взаимодействии с сильными кислотами является основанием: H2O + H+ H3О+, а реагируя с аммиаком, становится кислотой: NH3 + H2O
H3О+, а реагируя с аммиаком, становится кислотой: NH3 + H2O  NH4+ + OH−.
NH4+ + OH−.
Теория сольвосистем
Основная статья: Теория сольвосистем
Теория сольвосистем — расширение теории Аррениуса-Оствальда на другие ионные (в частности, протонные растворители). Предложена американскими химиками Г. Кэди, Э. Франклин и Ч. Краусом
Определения. Ионный растворитель — растворитель, самодиссоциирующий на катион и анион. Катион при этом называется ионом лиония, а анион — ионом лиата. Протонный растворитель — растворитель, способный к автопротолизу, то есть передаче иона H+ от одной молекулы к другой:
- 2HL ↔ H2L+ + L—
Это растворители, содержащие достаточно полярную связь с участием водорода и неподеленную электронную пару на каком-либо другом неметалле (чаще всего, азоте, кислороде или фторе).
Примечание: в данном определении «зашита» протонная теория, ибо автопротолиз есть кислотно-основная реакция по Брестеду-Лоури. В нём также «зашита» теория Льюиса, поскольку именно она объясняет причины образования ионов лиония.
Ион H2L+ при этом называется ионом лиония, а L— — ионом лиата.
Кислоты — это вещества, образующие в данном растворителе ион лиония.
Основания — вещества, образующие в данном растворителе ион лиата.
Соли — вещества, диссоциирующие в данном растворителе с образованием катиона и аниона, не являющихся лионием и лиатом.
Продукты реакции. В реакции кислоты с основанием (реакция нейтрализации образуется соль и растворитель.
Примеры.
| Растворитель | Самодиссоциация | Лионий | Лиат | Константа самодиссоциации | Кислота | Основание | Реакция нейтрализации |
|---|---|---|---|---|---|---|---|
| H2O | 2H2O ↔ H3O+ + OH— | H3O+ | OH— | 2·10-16 (25°С) | HCl | NaOH | NaOH + HCl = NaCl + H2O |
| NH3 | 2NH3 ↔ NH4+ + NH2— | NH4+ | NH2— | ~10-34(-33°C) | HCl NH4Cl | KNH2 | KNH2 + HCl = NaCl + NH3 KNH2 + NH4Cl = NaCl + 2NH3 |
| HF | 2HF ↔ H2F+ + F— | H2F+ | F— | ~10-12 | HCl | NaF NaOH (даёт NaF) | HCl + NaF = NaCl + HF |
| KCl | KCl↔K+ + Cl— | K+ | Cl— | Велика | KOH | HCl | KOH (кислота) + HCl (основание) = KCl (растворитель) + H2O (соль) |
Количественные характеристики и критерии протекания реакции Силы кислот и оснований характеризуются их константой диссоциации.
Константы диссоциации зависят от растворителя. Протонные растворители с высоким константами автодиссоциации («кислотные растворители», например HF) дифференцируют кислоты (в них кислоты становятся слабыми и различающимися по силе) но нивелируют основания (все основания становятся сильными, правращаясь в ион лиата). Протонные растворители с низкими константами автодиссоциации («основные растворители, например NH3) дифференцируют основания, но нивелируют кислоты (которые становятся сильными, превращаясь в лионий).
Реакция идёт от сильных кислот к слабым.
Область применимости. Позволяет предсказывать кислотно-основные реакции в любых растворителях. Управление кислотно-основными процессами при помощи растворителя. Расширяет на неводные растворы понятие водородного показателя (pH) как концентрацию ионов лиония. Описывает основные свойства веществ, не содержащих групп ОН.
Однако для многих задач теория слишком громоздкая.
Специфические черты Некоторые кислотно-основные реакции в этой теории могут встать «с ног на голову», например
- KOH (кислота) + HCl (основание) = KCl (растворитель) + H2O (соль)
Электронная теория Льюиса
Основная статья: Теория Льюиса
В теории Льюиса (1923 г.) на основе электронных представлений было ещё более расширено понятие кислоты и основания. Кислота Льюиса — молекула или ион, имеющие вакантные электронные орбитали, вследствие чего они способны принимать электронные пары. Это, например, ионы водорода – протоны, ионы металлов (Ag+, Fe3+), оксиды некоторых неметаллов (например, SO3, SiO2), ряд солей (AlCl3), а также такие вещества как BF3, Al2O3. Кислоты Льюиса, не содержащие ионов водорода, называются апротонными. Протонные кислоты рассматриваются как частный случай класса кислот. Основание Льюиса — это молекула или ион, способные быть донором электронных пар: все анионы, аммиак и амины, вода, спирты, галогены. Примеры химических реакций между кислотами и основаниями Льюиса:
- AlCl3 + Cl− → AlCl4−
- BF3 + F− → BF4−
- PCl5 + Cl− → PCl6−.
Общая теория Усановича
Наиболее общая теория кислот и оснований была сформулирована М. Усановичем в 1939 году. В основе теории лежит представление о том, что всякое кислотно-основное взаимодействие — это реакция солеобразования. Согласно этой теории «кислота — это частица, которая может отщеплять катионы, включая протон, или присоединять анионы, включая электрон. Основание — частица, которая может присоединять протон и другие катионы или отдавать электрон и другие анионы» (формулировка 1964 г.). В отличие от Льюиса Усанович в основе понятий «кислота» и «основание» использует знак заряда частицы, а не строение электронной оболочки.
По Усановичу, в реакции гидролиза SO3 + 2H2O  H3O+ + HSO4— — вода, отдавая анион OH—, является основанием, а триоксид серы, присоединяя этот анион — кислотой, аналогично в реакции: SnCl4 + 2KCl
H3O+ + HSO4— — вода, отдавая анион OH—, является основанием, а триоксид серы, присоединяя этот анион — кислотой, аналогично в реакции: SnCl4 + 2KCl  K2SnCl6 — тетрахлорид олова, присоединяющий анионы хлора, выступает в роли кислоты. Таким образом, данная формулировка кислот и оснований позволяет отнести к кислотно-основным взаимодействиям и все окислительно-восстановительные реакции.
K2SnCl6 — тетрахлорид олова, присоединяющий анионы хлора, выступает в роли кислоты. Таким образом, данная формулировка кислот и оснований позволяет отнести к кислотно-основным взаимодействиям и все окислительно-восстановительные реакции.
Теория Усановича фактически отменяет один из основополагающих принципов классической химии — представления о классах кислот и оснований: «кислоты и основания — это не классы соединений; кислотность и основность — это функции вещества. Будет ли вещество кислотой или основанием, зависит от партнера»[4].
К недостаткам теории Усановича относят её слишком общий характер и недостаточно чёткую определённость формулировки понятий «кислота» и «основание». К недостаткам относят также то обстоятельство, что она не описывает неионогенные кислотно-основные превращения. Наконец, она не позволяет делать количественные предсказания[5].
Литература
- Современные теории кислот и оснований: Учеб. пособие. — Новочеркасск: УПЦ Набла. — 2003. — 52 с.
- Геворкян А. А. Обобщенная теория кислот и оснований. Новое воззрение на реакционную способность атомов и молекул. — Гитутюн, 2006 г. — 158 стр.
- Москва В.В. Понятие кислоты и основания в органической химии // Соросовский образовательный журнал, 1996, №12, с. 33-40.
- Фиалков А.Я. Не только в воде. Л., Химия, 1989.
Примечания
Сопряженные кислоты — Conjugate acid
Сопряженная кислота , в теории кислотно-щелочного Бренстеда-Лоури , представляет собой вид , образованный приема протона ( Н + ) с помощью основания , другими словами, это основание с водородом иона , добавленной к нему. С другой стороны, сопр женное основание является то , что остается после того, как кислотное пожертвовал протона во время химической реакции. Следовательно, сопряженное основание представляет собой вид , образованный удалением протона от кислоты. Поскольку некоторые кислоты , способны высвобождать несколько протонов, сопряженное основание кислоты сам по себе может быть кислым.
Таким образом, это может быть представлено в виде следующей химической реакции:
- Кислота + база ⇌ Конъюгат база + Конъюгат кислоты

Брёнстед и Мартин Lowry представил теорию Бренстеда-Лоури, который предложил , чтобы любое соединение , которое может передавать протон любое другое соединение представляет собой кислоту, и соединение , которое принимает протон является базой. Протон является ядерной частицы с блоком положительный электрический заряд; она представлена символ H + , потому что он представляет собой ядро из водорода атома , то есть катион водорода .
Катион может быть конъюгат кислоты, и анион может быть сопр женным основанием, в зависимости от которой вещество участвует и который кислотно-щелочной теории является точка зрения. Самый простой анион , который может быть сопром женного основанием представляет собой сольватированные электроны , чьи сопряженной кислота является атомарным водородом.
Кислотно-основные реакции
В кислотно-щелочной реакции , кислота плюс основание реагирует с образованием конъюгата основание плюс сопряженная кислота:
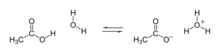
Конъюгаты образуются, когда кислота теряет протон водорода или основание получает протон водорода. Обратитесь к следующему рисунку:
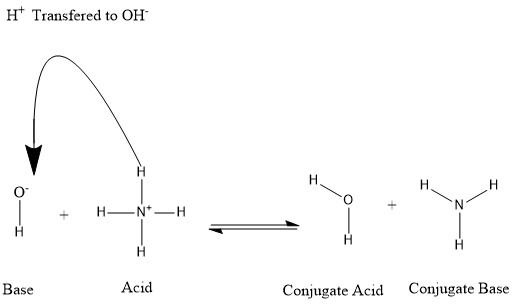
Говорят , что молекула воды является сопряженной кислотой гидроксида — иона после того, как последний получила протон водорода пожертвованного аммония . С другой стороны, аммиак является сопряженным основанием для кислотного аммония после того, как аммоний пожертвовал ион водорода к производству молекулы воды. Мы можем также обратиться к OH- в качестве сопряженного основания H
2 O, так как молекула воды отдает протоннаправлении производстваNH +
4 в обратной реакции, которая является процесс преобладающим в природе за счет силы основанияNH
3 над гидроксидиона. Основываясь на этой информации, очевидночто термины «кислота», «Base», «конъюгат кислота», и «конъюгат база» не являются фиксированными для определенных видов химических веществ; но являются взаимозаменяемымизависимости от реакцииимеющей место.
Прочность конъюгатов
Силы сопряженной кислоты прямо пропорциональны его константа диссоциации . Если конъюгат кислота является сильной, его диссоциация будет иметь более высокую константу равновесия и продукты реакции будут отдавать предпочтение. Силы сопряженного основания можно рассматривать как склонность вида «тянуть» протоны водорода к себе. Если сопряженное основание классифицируется как сильный, он будет «удерживать» на протон водорода , когда в растворе и его кислота не диссоциирует.
С другой стороны, если разновидность классифицируется как сильная кислота, ее сопряженное основание будет слабым в природе. Пример такого случая будет диссоциация соляной кислоты HCl в воде. Так как HCl , является сильной кислотой (она диссоциирует в значительной степени), сопряженного с ней основания ( Cl —
) Будет слабым сопряженное основание. Таким образом, в этой системе, большинство Н +
будет в виде гидроксонии ионов Н
3 O +
вместо того, присоединены к аниону Cl и конъюгат баз будет слабее, чем молекулы воды.
Аналогичным образом, если кислота является слабым, его сопряженное основание будет сильным. При рассмотрении вопроса о том, что КВт равно произведению концентраций Н + и ОН. Слабая кислота будет иметь низкую концентрацию H +. КВт (1,0 * 10 ^ -14), деленное на низкой концентрации H + приводит к низкой концентрации OH-, а также. Таким образом, слабые кислоты будут иметь слабые сопряженные основания, в отличии от неправильного представления, что они имеют сильные сопряженные основания.
Определение сопряженных кислотно-пар оснований
Кислота и сопряженное основание, а также основание и конъюгат кислоты, известны как сопряженные пары. При нахождении сопряженной кислоты или основания, важно , чтобы посмотреть на реагентах в химическом уравнении . В этом случае реагенты являются кислоты и основания, а кислота соответствует сопряженного основания на стороне продукта химического уравнения; как это делает основание к сопряженной кислоты на стороне продукта уравнения.
Для того, чтобы идентифицировать сопряженную кислоту, искать пары соединений, которые связаны между собой . Кислотно-щелочная реакцию можно рассматривать в до и после смысла. Прежде , чем это Реагент сторона уравнения, то после того, как это побочный продукт из уравнения. Сопряженная кислота в стороне после уравнения получает ион водорода, так что в перед стороной уравнения соединения , которое имеет один меньше водорода иона сопряженной кислоты является базовым. Сопряженное основание в после части уравнения потерял ион водорода, так что в перед стороне уравнения, соединение , которое имеет еще один ион водорода сопряженной базы является кислотой.
Рассмотрим следующую кислотно-щелочной реакции:
- HNO
3 +Н
2 O→H
3 O +
+ NO —
3
Азотная кислота ( HNO
3 ) представляет собойкислотупоскольку она жертвует протон молекулы воды и еесопряженное основаниеявляетсянитрат(NO —
3 ). Молекула воды действует как основаниетакон получает водорода протон и сопряженная кислота являетсягидроксонияион (H
3 O +
).
Приложения
Одно из применений сопряженных кислот и оснований лежат в буферных системах, которые включают в себя буферный раствор . В буфере, слабая кислота и ее сопряженное основание (в форме соли), или слабое основание и его конъюгат кислота, используются для того , чтобы ограничить изменение рНа во время процесса титрования. Буферы имеют как органические , так и неорганические химические приложения. Например, кроме буферов, используемых в лабораторных процессах, нашей крови действует как буфер для поддержания рН. Самый важный буфер в нашей крови является угольная кислота-бикарбонатный буфер , который предотвращает резкие изменения рН , когда СО
2 вводится. Эти функциикакнапример:
- Колорадо2+ЧАС2О↽—⇀ЧАС2Колорадо3↽—⇀HCO3-+ЧАС+{\ Displaystyle {\ се {CO2 + h3O <=> Н2СО3 <=> НСО3 ^ — + Н +}}}
Кроме того, здесь приведена таблица общих буферов.
Буферизация агент рК Полезный диапазон рН Лимонная кислота 3,13, 4,76, 6,40 2.1 — 7.4 Уксусная кислота 4,8 3,8 — 5,8 КН 2 РО 4 , 7,2 6,2 — 8,2 CHES 9,3 8.3-10.3 Борат 9,24 8,25 — 10,25
Второе общее применение с органическим соединением , будет производством буфера с помощью уксусной кислоты. Если уксусная кислота, слабая кислота с формулой CH
3 СООН, было сделано в буферный раствор, он долженбы быть объединен с его конъюгат базовойCH
3 COO —
в форме соли. Полученная смесь называется ацетатный буфер, состоящей из водных CH
3 СООНи водный растворСН
3 COONa. Уксусная кислота, наряду со многими другими слабыми кислотами, служаткачестве полезных компонентов буферов в различных условиях лаборатории, каждый полезнопределах их собственного диапазона рН.
Пример с неорганическим соединением будет лекарственное использование сопряженного основания молочной кислоты, известной как лактата в растворе лактата Рингера и раствор Гартмана . Молочная кислота имеет формулу C
3 Н
6 вывода
6 и сопряженное основание используют в внутривенные жидкостикоторые состоят из катионов натрия и калияа также лактата и хлориданионов в растворе с дистиллированной водой. Эти жидкости обычно изотонические по отношению к крови человека икак правилоиспользуются для пики до уровня жидкости в системе после тяжелой потери крови изза травмы, хирургическое вмешательство или ожоги.
Таблица кислот и их сопряженных оснований
Табличные ниже приведены несколько примеров кислот и их сопряженных оснований; обратите внимание , как они отличаются только один протон (H + ионов). Кислота сила уменьшается , и сопр женное основание увеличивает прочность вниз на стол.
Таблица оснований и их сопряженных кислот
В отличие от этого, здесь таблица оснований и их сопряженных кислот. Аналогичным образом, базовая сила уменьшается и сила сопряженной кислоты повышает вниз таблицу.
Смотрите также
Рекомендации
внешняя ссылка
Теории кислот и оснований — это… Что такое Теории кислот и оснований?
Теории кислот и оснований — совокупность фундаментальных физико-химических представлений, описывающих природу и свойства кислот и оснований. Все они вводят определения кислот и оснований — двух классов веществ, реагирующих между собой. Задача теории — предсказание продуктов реакции между кислотой и основанием и возможности её протекания, для чего используются количественные характеристики силы кислоты и основания. Различия между теориями лежат в определениями кислот и оснований, характеристики их силы и, как следствие — в правилах предсказания продуктов реакции между ними. Все они имеют свою область применимости, каковые области частично пересекаются.
Кислотно-основные взаимодействия чрезвычайно распространенены в природе и находят широкое применение в научной и производственной практике. Теоретические представления о кислотах и основаниях имеют важное значение в формировании всех концептуальных систем химии и оказывают разностороннее влияние на развитие многих теоретических концепций во всех основных химических дисциплинах.
На основе современной теории кислот и оснований разработаны такие разделы химических наук, как химия водных и неводных растворов электролитов, рН-метрия в неводных средах, гомо- и гетерогенный кислотно-основный катализ, теория функций кислотности и многие другие.
Эволюция представлений о кислотно-основных взаимодействиях

Представления о кислотно-основных взаимодействиях относятся к числу фундаментальных химических положений. Понятия «кислота» и «основание» сформировались еще в XVII веке, однако их содержание неоднократно пересматривалось и уточнялось.
Образная теория кислот и оснований была предложена Н. Лемери. В своем «Курсе химии» (1675) он попытался объяснить физические и химические свойства веществ на языке их формы и структуры. Согласно представлениям Лемери кислоты на своей поверхности имеют острые шипы, вызывающие на коже колющие ощущения. Основания, названные им щелочами, состоят из пористых тел. «Шипы» кислот проникают в «поры», при этом они ломаются или притупляются, и кислоты превращаются в нейтральные соли[1].
Научные представления о природе кислот и оснований начали формироваться в конце XVIII в. В работах А. Лавуазье кислотные свойства связывались с наличием в составе вещества атомов кислорода. Известные тогда минеральные и органические кислоты, действительно, содержали кислород. Эта гипотеза быстро показала свою несостоятельность, когда благодаря работам Г. Дэви и Ж. Гей-Люссака стал известен целый ряд кислот, не содержащих кислорода (например, галогеноводороды, синильные кислоты), в то время, как многие кислородсодержащие соединения не проявляют кислотных свойств.
С начала XIX века кислотами стали считать вещества, способные к взаимодействию с металлам с выделением водорода (Ю. Либих, 1839). Примерно в это же время Й. Берцелиус выдвинул идею, объясняющую кислотно-основные свойства веществ их электрической «дуалистической» природой. Так, к кислотам он относил электроотрицательные оксиды неметаллов и некоторых металлов (например, хрома, марганца и др.), а электроположительные оксиды металлов считал основаниями. Таким образом, кислотность или основность Берцелиусом рассматривается как функциональное, а не абсолютное свойство соединения. Берцелиус впервые сделал попытку количественной оценки и предсказания силы кислот и оснований[2].
C появлением теории электролитической диссоциации С. Аррениуса (1887) возникла возможность описания кислотно-основных свойств исходя из продуктов ионизации электролита. Благодаря работам В. Оствальда теория получила развитие для слабых электролитов.
В начале XX в. американские химики Г. Кэди, Э. Франклин и Ч. Краус создали теорию сольвосистем, распространившую положения теории Аррениуса-Освальда на все растворители, способные к самодиссоциации.
В основу современных теорий кислот и оснований положены представления Й. Брёнстеда и Г. Льюиса. Имеются вполне успешные попытки создать обобщенные теории (М. Усанович, 1939), но они не находят широкого применения[3].
Водородная теория Либиха
Определения. Кислота — вещество, способное реагировать с металлом с выделением водорода. Понятие «основание» в этой теории отсутствует.
Продукты реакции. При реакции кислоты с металлом образуется соль и водород.
Примеры. Кислота — HCl.
Реакция 2HCl + Zn = ZnCl2 + H2↑
Критерии протекания реакции. С сильными кислотами реагируют металлы, стоящие в ряду активностей левее водорода. Чем слабее кислота, тем более активный металл нужен для реакции между ними. Количественные характеристики. Поскольку теория используется редко, количественные характеристики силы кислоты (а значит, и предсказания направления реакции) в рамках данной теории не разработаны.
Область применимости. Предсказание взаимодействия водородсодержащих веществ с металлами в любых растворителях.
Специфические черты. В соответствии с этой теорией этиловый спирт и аммиак являются слабыми кислотами, так как способны реагировать со щелочными металлами:
- 2C2H5OH + 2Na = 2C2H5ONa + H2↑
- 2NH3 + 2Na = 2NaNH2 + H2↑
Теория электролитической диссоциации Аррениуса-Оствальда
Основная статья: Теория электролитической диссоциации
Определения. Кислоты — это вещества, образующие в водном растворе ионы гидратированные катионы водорода Н+ (ионы гидроксония) и анионы кислотного остатка.
Основания — вещества, диссоциирующие в водном растворе с образованием катионов металла и гидроксид-анионов ОН−.
Соли — вещества, диссоциирующие с образованием катиона металла и аниона кислотного остатка.
Продукты реакции. В реакции кислоты с основанием (реакция нейтрализации образуется соль и соли и воды.
Примеры. Кислота — HCl (кислотный остаток Cl—):
- HCl + H2O ↔ H3O+ + Cl—
Основание — NaOH:
- NaOH ↔ Na+ + OH—
Реакция нейтрализации (соль — NaCl):
- HCl + NaOH = NaCl + H2O
Критерии протекания реакции. Сильные кислоты реагируют с сильными основаниями. Чем слабее кислота, тем более сильное основание нужно для реакции.
Количественные характеристики Сила кислоты и основания характеризуются их константами диссоциации K.
- Для кислоты HA K = [H+]·[A—]/[HA]
- Для основания MOH K = [M+]·[OH—]/[MOH]
Чтобы прошла реакция между кислотой и основанием, произведение их констант диссоциации должно быть больше, чем 10-14 (ионное произведение воды).
Область применимости. Она вполне удовлетворительно описывает реакции достаточно сильных кислот и оснований друг с другом и свойства их водных растворов. На основе представлений о степени и константе диссоциации было закреплено деление электролитов на сильные и слабые, введено понятие водородного показателя, распространение которого на щелочные среды требует, однако, дополнительных допущений (введения ионного произведения воды).
Теорию можно применять для описания гидролиза солей и реакции кислот и оснований с солями, однако при этом требуется весьма громоздкий аппарат — протонная теория (см. ниже) гораздо удобнее.
Применимость теории Аррениуса-Оствальда ограничивается водными растворами. кроме того, она не позволяет объяснить наличие основных свойств аммиака, фосфина и других соединений, не содержащих гидроксогрупп.
Протонная теория Брёнстеда-Лаури
Основная статья: Протолитическая теория кислот и оснований
 Сравнение моделей
Сравнение моделейкислотно-основного взаимодействия
по Льюису и Брёнстеду
Протолитическая (протонная) теория кислот и оснований была предложена в 1923 году независимо друг от друга датским учёным Й. Брёнстедом и английским учёным Т. Лаури. В ней понятие о кислотах и основаниях было объединено в единое целое, проявляющееся в кислотно-основном взаимодействии: А  В + Н+ (А — кислота, В — основание). Согласно этой теории кислотами являются молекулы или ионы, способные быть в данной реакции донорами протонов, а основаниями являются молекулы или ионы, присоединяющие протоны (акцепторы). Кислоты и основания получили общее название протолитов.
В + Н+ (А — кислота, В — основание). Согласно этой теории кислотами являются молекулы или ионы, способные быть в данной реакции донорами протонов, а основаниями являются молекулы или ионы, присоединяющие протоны (акцепторы). Кислоты и основания получили общее название протолитов.
Сущностью кислотно-основного взаимодействия является передача протона от кислоты к основанию. При этом кислота, передав протон основанию, сама становится основанием, так как может снова присоединять протон, а основание, образуя протонированную частицу, становится кислотой. Таким образом, в любом кислотно-основном взаимодействии участвуют две пары кислот и оснований, названные Бренстедом сопряженными: А1 + В2  А2 + В1.
А2 + В1.
Одно и то же вещество в зависимости от условий взаимодействия может быть как кислотой, так и основанием (амфотерность). Например, вода при взаимодействии с сильными кислотами является основанием: H2O + H+ H3О+, а реагируя с аммиаком, становится кислотой: NH3 + H2O
H3О+, а реагируя с аммиаком, становится кислотой: NH3 + H2O  NH4+ + OH−.
NH4+ + OH−.
Теория сольвосистем
Основная статья: Теория сольвосистем
Теория сольвосистем — расширение теории Аррениуса-Оствальда на другие ионные (в частности, протонные растворители). Предложена американскими химиками Г. Кэди, Э. Франклин и Ч. Краусом
Определения. Ионный растворитель — растворитель, самодиссоциирующий на катион и анион. Катион при этом называется ионом лиония, а анион — ионом лиата. Протонный растворитель — растворитель, способный к автопротолизу, то есть передаче иона H+ от одной молекулы к другой:
- 2HL ↔ H2L+ + L—
Это растворители, содержащие достаточно полярную связь с участием водорода и неподеленную электронную пару на каком-либо другом неметалле (чаще всего, азоте, кислороде или фторе).
Примечание: в данном определении «зашита» протонная теория, ибо автопротолиз есть кислотно-основная реакция по Брестеду-Лоури. В нём также «зашита» теория Льюиса, поскольку именно она объясняет причины образования ионов лиония.
Ион H2L+ при этом называется ионом лиония, а L— — ионом лиата.
Кислоты — это вещества, образующие в данном растворителе ион лиония.
Основания — вещества, образующие в данном растворителе ион лиата.
Соли — вещества, диссоциирующие в данном растворителе с образованием катиона и аниона, не являющихся лионием и лиатом.
Продукты реакции. В реакции кислоты с основанием (реакция нейтрализации образуется соль и растворитель.
Примеры.
| Растворитель | Самодиссоциация | Лионий | Лиат | Константа самодиссоциации | Кислота | Основание | Реакция нейтрализации |
|---|---|---|---|---|---|---|---|
| H2O | 2H2O ↔ H3O+ + OH— | H3O+ | OH— | 2·10-16 (25°С) | HCl | NaOH | NaOH + HCl = NaCl + H2O |
| NH3 | 2NH3 ↔ NH4+ + NH2— | NH4+ | NH2— | ~10-34(-33°C) | HCl NH4Cl | KNH2 | KNH2 + HCl = NaCl + NH3 KNH2 + NH4Cl = NaCl + 2NH3 |
| HF | 2HF ↔ H2F+ + F— | H2F+ | F— | ~10-12 | HCl | NaF NaOH (даёт NaF) | HCl + NaF = NaCl + HF |
| KCl | KCl↔K+ + Cl— | K+ | Cl— | Велика | KOH | HCl | KOH (кислота) + HCl (основание) = KCl (растворитель) + H2O (соль) |
Количественные характеристики и критерии протекания реакции Силы кислот и оснований характеризуются их константой диссоциации.
Константы диссоциации зависят от растворителя. Протонные растворители с высоким константами автодиссоциации («кислотные растворители», например HF) дифференцируют кислоты (в них кислоты становятся слабыми и различающимися по силе) но нивелируют основания (все основания становятся сильными, правращаясь в ион лиата). Протонные растворители с низкими константами автодиссоциации («основные растворители, например NH3) дифференцируют основания, но нивелируют кислоты (которые становятся сильными, превращаясь в лионий).
Реакция идёт от сильных кислот к слабым.
Область применимости. Позволяет предсказывать кислотно-основные реакции в любых растворителях. Управление кислотно-основными процессами при помощи растворителя. Расширяет на неводные растворы понятие водородного показателя (pH) как концентрацию ионов лиония. Описывает основные свойства веществ, не содержащих групп ОН.
Однако для многих задач теория слишком громоздкая.
Специфические черты Некоторые кислотно-основные реакции в этой теории могут встать «с ног на голову», например
- KOH (кислота) + HCl (основание) = KCl (растворитель) + H2O (соль)
Электронная теория Льюиса
Основная статья: Теория Льюиса
В теории Льюиса (1923 г.) на основе электронных представлений было ещё более расширено понятие кислоты и основания. Кислота Льюиса — молекула или ион, имеющие вакантные электронные орбитали, вследствие чего они способны принимать электронные пары. Это, например, ионы водорода – протоны, ионы металлов (Ag+, Fe3+), оксиды некоторых неметаллов (например, SO3, SiO2), ряд солей (AlCl3), а также такие вещества как BF3, Al2O3. Кислоты Льюиса, не содержащие ионов водорода, называются апротонными. Протонные кислоты рассматриваются как частный случай класса кислот. Основание Льюиса — это молекула или ион, способные быть донором электронных пар: все анионы, аммиак и амины, вода, спирты, галогены. Примеры химических реакций между кислотами и основаниями Льюиса:
- AlCl3 + Cl− → AlCl4−
- BF3 + F− → BF4−
- PCl5 + Cl− → PCl6−.
Общая теория Усановича
Наиболее общая теория кислот и оснований была сформулирована М. Усановичем в 1939 году. В основе теории лежит представление о том, что всякое кислотно-основное взаимодействие — это реакция солеобразования. Согласно этой теории «кислота — это частица, которая может отщеплять катионы, включая протон, или присоединять анионы, включая электрон. Основание — частица, которая может присоединять протон и другие катионы или отдавать электрон и другие анионы» (формулировка 1964 г.). В отличие от Льюиса Усанович в основе понятий «кислота» и «основание» использует знак заряда частицы, а не строение электронной оболочки.
По Усановичу, в реакции гидролиза SO3 + 2H2O  H3O+ + HSO4— — вода, отдавая анион OH—, является основанием, а триоксид серы, присоединяя этот анион — кислотой, аналогично в реакции: SnCl4 + 2KCl
H3O+ + HSO4— — вода, отдавая анион OH—, является основанием, а триоксид серы, присоединяя этот анион — кислотой, аналогично в реакции: SnCl4 + 2KCl  K2SnCl6 — тетрахлорид олова, присоединяющий анионы хлора, выступает в роли кислоты. Таким образом, данная формулировка кислот и оснований позволяет отнести к кислотно-основным взаимодействиям и все окислительно-восстановительные реакции.
K2SnCl6 — тетрахлорид олова, присоединяющий анионы хлора, выступает в роли кислоты. Таким образом, данная формулировка кислот и оснований позволяет отнести к кислотно-основным взаимодействиям и все окислительно-восстановительные реакции.
Теория Усановича фактически отменяет один из основополагающих принципов классической химии — представления о классах кислот и оснований: «кислоты и основания — это не классы соединений; кислотность и основность — это функции вещества. Будет ли вещество кислотой или основанием, зависит от партнера»[4].
К недостаткам теории Усановича относят её слишком общий характер и недостаточно чёткую определённость формулировки понятий «кислота» и «основание». К недостаткам относят также то обстоятельство, что она не описывает неионогенные кислотно-основные превращения. Наконец, она не позволяет делать количественные предсказания[5].
Литература
- Современные теории кислот и оснований: Учеб. пособие. — Новочеркасск: УПЦ Набла. — 2003. — 52 с.
- Геворкян А. А. Обобщенная теория кислот и оснований. Новое воззрение на реакционную способность атомов и молекул. — Гитутюн, 2006 г. — 158 стр.
- Москва В.В. Понятие кислоты и основания в органической химии // Соросовский образовательный журнал, 1996, №12, с. 33-40.
- Фиалков А.Я. Не только в воде. Л., Химия, 1989.