Способы получения.
⇐ ПредыдущаяСтр 2 из 3Следующая ⇒Хром обычно получают в виде сплава с железом (феррохром). Для этого хромит восстанавливают углем:
FeCr2O4 + 4C = Fe + 2Cr + 4CO
Относительно чистый хром получают методом алюмотермии:
2Al + Cr2O3 = 2Cr + Al2O3
Необходимый для получения металлического хрома оксид выделяют из хромита. Вначале проводят обжиг исходного хромсодержащего сырья в смеси с карбонатом натрия и доломитом при 1100–1200 °С:
4 FeCr2O4 + 8Na2CO3 + 7O2 = 8Na2CrO4 + 2Fe2O3 + 8CO2;
образующийся при этом хромат натрия выщелачивают водой и после дополнительной обработки выделяют в щелочной раствор. Затем восстанавливают серой в процессе кипячения до оксида хрома (III).
Более чистый хром получают электролизом оксида хрома (VI) или хромкалиевых квасцов. Особо чистый хром образуется при термическом разложении органических хромсодержащих комплексных соединений.
Сегодня общий объем потребления чистого хрома (не менее 99% Cr) составляет около 15 тысяч тонн, из них около трети приходится на электролитический хром. Мировым лидером в производстве высокочистого хрома является английская фирма Bell Metals. Первое место по объемам потребления занимают США (50%), второе – страны Европы (25%), третье – Япония. Рынок металлического хрома довольно нестабилен, и цены на металл колеблются в широком диапазоне.
Соединения хрома.Хром образует множество химических соединений, в которых он может находиться во всех степенях окисления от 0 до +6. Соединения хрома очень разнообразны по цвету: белые, синие, зеленые, коричневые, красные, желтые, оранжевые, фиолетовые и черные.
У хрома степень окисления +3. +6 является наиболее устойчивой.
Оксид хрома (III) Cr 2O3 – темно-зеленый порошок, в кристаллическом состоянии – черное с металлическим блеском вещество. Температура плавления 1990°С, плотность 5,21 г/см3. Химически инертен. В воде, кислотах и щелочах не растворяется. С трудом растворяется в сильных кислотах при длительном нагревании.
Проявляет амфотерные свойства. При сплавлении с оксидами, гидроксидами и карбонатами щелочных металлов образует хромиты, проявляя кислотные свойства:
Cr2O3 + 2KOH = 2KCrO2 + H2O;
Cr2O3 + Na2CO3 = 2NaCrO2 + CO2.
При сплавлении с кислотным реагентом – дисульфатом калия – образует сульфат хрома (III), проявляя основные свойства:
3K2S2O7 = 3K2SO4 + 3SO3;
Cr2O3 + 3SO3 = Cr
Cr2O3 + 3K2S2O7 = Cr2(SO4)3 + 3K2SO4
Оксид хрома (III) получается при термическом разложении дихромата аммония:
(NH4)2Cr2O7 = Cr2O3 + N2 + 4H2O
или при восстановлении дихромата калия коксом или серой:
2K2Cr2O7 + 3C = 2Cr2O3 + 2K2CO3 + CO2;
K2Cr2O7 + S = Cr2O3 + K2SO4
Гидроксид хрома (III) Cr(OH)3– аморфное или кристаллическое вещество, цвет зависит от условий осаждения и изменяется от голубого и зеленого до черно-фиолетового, разлагается при температуре около 150°С:
2Cr(OH)3 = Cr2O3 + 3H2O
Проявляет амфотерные свойства, легко растворяется в кислотах и щелочах:
2Cr(OH)3 + 6HCl = 2CrCl3 + 3H2O;
Cr(OH)3 + 3NaOH = Na3[Cr(OH)6].
Образуется при действии щелочей или водного раствора аммиака на растворы солей хрома:
CrCl3 + 3NH3 + 3H2O = Cr(OH)3 + 3NH4Cl
или при пропускании углекислого газа через щелочной раствор гексагидроксохромата (III) натрия:
Na3[Cr(OH)6] + 3СО2 = Cr(OH)3 + 3NaHCO3.
 Соли хрома (III). Хром в степени окисления +3 образует два типа солей, в которые входит в состав катиона и аниона.
Соли хрома (III). Хром в степени окисления +3 образует два типа солей, в которые входит в состав катиона и аниона.
NaCrO2 + HCl + H2O = Cr(OH)3 + NaCl;
в избытке кислоты:
NaCrO2 + 4HCl = CrCl3 + NaCl + 2H2O.
Соли Cr3+ проявляют все свойства солей, большинство из них хорошо растворимы в воде и гидролизуют.
Соединения хрома (III) проявляют окислительные и восстановительные свойства:
2CrCl3 + 3H2O2 + 10 KOH = 2K2CrO4 + 6KCl + 8H2O (Cr3+ – восстановитель)
2CrCl3 + 3Zn + 4HCl = 2CrCl2 + 3ZnCl2 + 2H2 (Cr3+ – окислитель)
Оксид хрома (VI) CrO3 – темно-красное кристаллическое вещество, имеет цепочечную структуру. Гигроскопичен, расплывается на воздухе, малоустойчив, разлагается при нормальных условиях. Очень сильный окислитель. Проявляет кислотные свойства.
Растворяется в воде, образуя хромовые кислоты:
CrO3 + H2O = H2CrO4,
2CrO3 + H2O = H2Cr2O7.
В растворе хромовых кислот существует равновесие:
2H2CrO4 = H2Cr2O7 + H2O.
При разбавлении раствора равновесие смещается в сторону образования хромовой кислоты.
Реагирует с основными оксидами и основаниями:
CrO3 + BaO = BaCrO4,
CrO3 + 2NaOH = Na2CrO4 + H2O
Оксид хрома (VI) – очень сильный окислитель, окисляет фосфор, углерод и серу, многие органические вещества, например:
4CrO3 + 3C = 2Cr2O3 + 3CO2;
Образуется при разложении хромата натрия серной кислотой при температуре около 200°С:
Na2CrO4 + 2H2SO4 = CrO3 + 2NaHSO4 + H2O
Хромовые кислоты в свободном состоянии не выделены, в растворе проявляют свойства сильных кислот.

Хроматы – соли хромовых кислот. Хроматы – соли хромовой кислоты – имеют в своем составе анион CrO42- и обладают желтой окраской, дихроматы – соли дихромовой кислоты – содержат анион Cr2O72- оранжевого цвета. Хроматы устойчивы в щелочной среде, дихроматы – в кислой, в растворе существует равновесие :
2CrO42- + 2H+ = Cr2O72- + H2O.
При нагревании дихроматы разлагаются:
4K2Cr2O7 = 4K2CrO4 + 2Cr2O3 + 3O2.
Соли хрома (VI) – сильные окислители, восстанавливаются до соединений хрома (III). В нейтральной среде образуется гидроксид хрома (III):
K2Cr2O7 + 3(NH4)2S + H2O = 2Cr(OH)3 + 3S + 6NH3 + 2KOH
в кислой соли хрома (III):
K2Cr2O7 + 3K2SO3 + 4H2SO4 = Cr2(SO4)3 + 4K2SO4 + 4H2O;
в щелочной – производные анионного комплекса [Cr(OH)6]3-:
2K2
Наибольшее значение имеют соли натрия и калия, получить их можно при сплавлении хромистого железняка с соответствующими карбонатами при температуре выше 1000°С на воздухе:
4FeCr2O4 + 8Na2CO3 + 7O2 = 8Na2CrO4 + 2Fe2O3 + 8CO2.
mykonspekts.ru
формула, характеристика и химические свойства :: SYL.ru
Среди многообразия химических элементов и их соединений сложно выделить наиболее полезное для человечества вещество. Каждое уникально по своим свойствам и возможностям применения. Технический прогресс значительно облегчает исследовательский процесс, но и ставит перед ним новые задачи. Химические элементы, открытые несколько сотен лет назад и изученные во всех проявлениях, получают в современном мире более технологичные направления использования. Данная тенденция распространяется на соединения, существующие в природе и созданные людьми.
Оксид
В земной коре и на просторах Вселенной существует множество химических соединений, которые отличаются по классам, типам, характеристикам. Одним из самых распространенных видов соединений является оксид (окись, окисел). К нему относят песок, воду, углекислый газ, т. е. основополагающие вещества для существования человечества и всей биосферы Земли. Оксидами называют вещества, которые имеют в составе атомы кислорода со степенью окисления -2, при этом связь между элементами является бинарной. Их образование происходит в результате химической реакции, условия которой разнятся в зависимости от состава оксида.
Характерными признаками данного вещества являются три позиции: вещество сложное, состоит из двух атомов, один из них – кислород. Большое количество существующих оксидов объясняется тем, что многие химические элементы образуют несколько веществ. Они идентичны по составу, но атом, вступающий в реакцию с кислородом, проявляет несколько степеней валентности. Например, оксид хрома (2, 3, 4, 6), азота (1, 2, 3, 4 ,5) и т. д. При этом их свойства зависят от степени валентности элемента, вступающего в окислительную реакцию.
По принятой классификации оксиды бывают основными и кислотными. Также выделяется амфотерный вид, который проявляет свойства основного окисла. Кислотные оксиды – это соединения неметаллов или элементов с высокой валентностью, их гидратами являются кислоты. К основным окислам относят все вещества, имеющие связь кислород + металл, их гидратами являются основания.

Хром
В 18 веке химик И. Г. Леман обнаружил неизвестный минерал, который был назван красным сибирским свинцом. Профессор Парижской минералогической школы Вокелен провел ряд химических реакций с полученным образцом, в результате которых был выделен неизвестный металл. Основными свойствами, обозначенными ученым, стали его устойчивость к кислотным средам и тугоплавкость (жаропрочность). Название «хром» (Chromium) возникло из-за широкой цветовой гаммы, которая характеризуется соединениям элемента. Металл достаточно инертен, в чистом виде не встречается в природных условиях.
Основными минералами, содержащими хром, являются: хромит (FeCr2O4), меланохроит, вокеленит, дитцеит, тарапакаит. Химический элемент Cr располагается в 6 группе периодической системы Д. И. Менделеева, имеет атомный номер 24. Электронная конфигурация атома хрома позволяет элементу иметь валентность +2, +3, +6, при этом наиболее устойчивыми являются соединения трехвалентного металла. Возможны реакции, при которых степень окисления равна +1, +5, +4. Хром химически не активен, поверхность металла покрывается пленкой (эффект пассивирования), предотвращающей реакции с кислородом и водой при нормальных условиях. Оксид хрома, образующийся на поверхности, предохраняет металл от взаимодействия с кислотами и галогенами при отсутствии катализаторов. Соединения с простыми веществами (не металлами) возможны при температуре от 300 оС (хлор, бром, сера).
При взаимодействии со сложными веществами требуются дополнительные условия, например, с раствором щелочи реакция не происходит, с ее расплавами процесс происходит очень медленно. С кислотами хром вступает в реакцию при наличии в качестве катализатора высокой температуры. Оксид хрома можно получить из различных минералов путем воздействия температуры. В зависимости от будущей степени окисления элемента применяются концентрированные кислоты. При этом валентность хрома в соединении варьируется от +2 до +6 (высший оксид хрома).

Применение
За счет уникальных антикоррозийных свойств и жаропрочности большое практическое значение имеют сплавы на основе хрома. При этом в процентном соотношении его доля не должна превышать половины общего объема. Большим недостатком хрома является его хрупкость, что уменьшает возможности обработки сплавов. Наиболее распространенным способом применения металла является изготовление покрытий (хромирование). Защитная пленка может составлять слой в 0,005 мм, но она будет надежно предохранять металлическое изделие от коррозии и внешних воздействий. Соединения хрома используются для изготовления жаропрочных конструкций в металлургической промышленности (плавильные печи). Антикоррозийные покрытия декоративного направления (металлокерамика), специальная легированная сталь, электроды для сварочных аппаратов, сплавы на основе кремния, алюминия являются востребованными на мировых рынках. Оксид хрома за счет низкой возможности окисления и высокой жаропрочности служит катализатором многих химических реакций, протекающих при высоких температурах (1000 оС).

Двухвалентные соединения
Оксид хрома (2) CrO (закись) является порошком ярко-красного или черного цвета. В воде нерастворим, при нормальных условиях не окисляется, проявляет ярко выраженные основные свойства. Вещество твердое, тугоплавкое (1550 оС), не является токсичным. В процессе нагревания до 100 оС окисляется до Cr2O3. В слабых растворах азотной и серной кислот не растворяется, реакция происходит с хлороводородной кислотой.

Получение, применение
Данное вещество считается низшим оксидом. Имеет достаточно узкую сферу применения. В химической промышленности оксид хрома 2 используется для очистки углеводородов от кислорода, который он притягивает в процессе окисления при температуре свыше 100 оС. Получить закись двухвалентного хрома можно тремя способами:
- Разложением карбонила Cr(CO)6 при наличии в качестве катализатора высокой температуры.
- Восстанавливая при помощи фосфорной кислоты оксид хрома 3.
- Амальгама хрома окисляется кислородом или азотной кислотой.
Трехвалентные соединения

Для оксидов хрома степень окисления +3 является самой устойчивой формой вещества. Cr2O3 (хромовая зелень, сесквиоксид, эсколаид) в химическом отношении инертен, нерастворим в воде, имеет высокую температуру плавления (более 2000 оС). Оксид хрома 3 – зеленый тугоплавкий порошок, очень твердый, имеет амфотерные свойства. Вещество растворимо в концентрированных кислотах, реакция со щелочами происходит в результате сплавления. Может восстанавливаться до чистого металла при взаимодействии с сильным восстановителем.
Получение и применение
За счет высокой твердости (сопоставимой с корундом) наиболее распространено использование вещества в абразивных и полирующих материалах. Оксид хрома (формула Cr2O3) имеет зеленый цвет, поэтому его применяют в качестве пигмента при изготовлении стекол, красок, керамики. Для химической промышленности данное вещество используется как катализатор для протекания реакций с органическими соединениями (синтез аммиака). Трехвалентный оксид хрома применяется для создания искусственных драгоценных камней и шпинелей. Для получения используется несколько видов химических реакций:
- Окисление закиси хрома.
- Нагревание (прокаливанием) бихромата или хромата аммония.
- Разложение гидроксида трехвалентного хрома или шестивалентного оксида.
- Прокаливание хромата или бихромата ртути.
Шестивалентные соединения
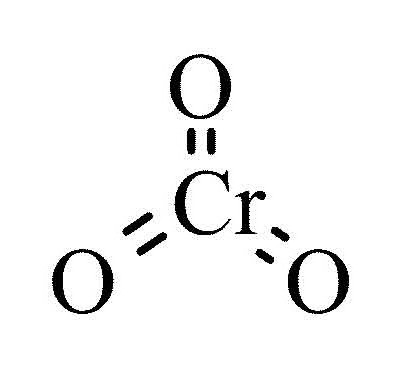
Формула высшего оксида хрома – CrO3. Вещество фиолетового или темно-красного цвета, может существовать в виде кристаллов, игл, пластин. Химически активен, токсичен, при взаимодействии с органическими соединениями существует опасность самовозгорания и взрыва. Оксид хрома 6 — хромовый ангидрид, трёхокись хрома — хорошо растворим в воде, при нормальных условиях взаимодействует с воздухом (расплывается), температура плавления – 196 оС. Вещество имеет ярко выраженные кислотные характеристики. При химической реакции с водой образуется дихромовая или хромовая кислота, без дополнительных катализаторов взаимодействует со щелочами (хроматы желтого цвета). Для галогенов (йод, сера, фосфор) является сильным окислителем. В результате нагревания свыше 250 оС образуется свободный кислород и трехвалентный оксид хрома.

Как получают и где применяют
Оксид хрома 6 получают обработкой хроматов (бихроматов) натрия или калия концентрированной серной кислотой либо при реакции хромата серебра с хлороводородной кислотой. Высокая химическая активность вещества обуславливает основные направления его применения:
- Получение чистого металла — хрома.
- В процессе хромирования поверхностей, в том числе электролитическим способом.
- Окисление спиртов (органических соединений) в химической промышленности.
- В ракетной технике используется в качестве воспламенителя топлива.
- В химических лабораториях очищает посуду от органических соединений.
- Используется в пиротехнической отрасли.
www.syl.ru
Соединения хрома
Оксид хрома(II) и гидроксид хрома(II) имеют основной характер
Cr(OH) +2HCl→CrCl
+2HCl→CrCl
 O
OСоединение хрома(II)-сильные восстановители; переходят в соединение хрома(III) под действием кислорода воздуха.
2CrCl +
2HCl
→ 2CrCl
+
2HCl
→ 2CrCl +
H
+
H
4Cr(OH) +O
+O +
2H
+
2H O→4Cr(OH)
O→4Cr(OH)
Оксид
хрома(III) Cr O
O —
зеленый, нерастворимый в воде порошок.
Может быть получен при прокаливании
гидроксида хрома(III)
или дихроматов калия и аммония:
—
зеленый, нерастворимый в воде порошок.
Может быть получен при прокаливании
гидроксида хрома(III)
или дихроматов калия и аммония:
2Cr(OH) —
—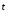 →Cr
→Cr O
O +
3H
+
3H O
O
4K Cr
Cr O
O —
—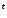 →
2Cr
→
2Cr O
O + 4K
+ 4K CrO
CrO + 3O
+ 3O
(NH )
) Cr
Cr O
O —
—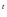 →
Cr
→
Cr O
O + N
+ N + H
+ H O
O
С концентрированными растворами кислот и щелочей взаимодействует с трудом:
Сr2О3 + 6 КОН + 3Н2О = 2К3[Сr(ОН)6]
Сr2О3 + 6НСl = 2СrСl3 + 3Н2О
Гидроксид хрома (III) Сr(ОН)3 получают при действии щелочей на на растворы солей хрома (III):
СrСl3 +3КОН = Сr(ОН)3↓ + 3КСl
Гидроксид хрома (III) представляет собой осадок серо – зеленого цвета, при получении которого, щелочь надо брать в недостатке. Полученный таким образом гидроксид хрома (III), в отличие от соответствующего оксида легко взаимодействует с кислотами и щелочами, т.е. проявляет амфотерные свойства:
Сr(ОН)3 + 3НNО3 = Сr(NО3)3 + 3Н2О
Сr(ОН)3 + 3КОН = К3[Сr(ОН)6](гексагидроксохромит К)
При сплавлении Сr(ОН)3 со щелочами получаются метахромиты и ортохромиты:
Cr(OH)3 + KOH = KCrO2(метахромит К) + 2H2O
Cr(OH)3 + KOH = K3CrO3(ортохромит К)+ 3H2O
Соединения хрома(VI).
Оксид хрома (VI) — СrО3 – темно – красное кристаллическое вещество, хорошо растворимо в воде – типичный кислотный оксид. Этому оксиду соответствует две кислоты:
СrО3 + Н2О = Н2СrО4 (хромовая кислота – образуется при избытке воды)
СrО3 + Н2О =Н2Сr2О7 (дихромовая кислота – образуется при большой концентрации оксида хрома (3)).
Оксид хрома (6) – очень сильный окислитель, поэтому энергично взаимодействует с органическими веществами:
Окисляет также иод, серу, фосфор, уголь:
При нагревании до 2500С оксид хрома (6) разлагается:
Оксид хрома (6) можно получить при действии концентрированной серной кислоты на твердые хроматы и дихроматы:
Хромовая и дихромовая кислоты.
Хромовая и дихромовая кислоты существуют только в водных растворах, образуют устойчивые соли, соответственно хроматы и дихроматы. Хроматы и их растворы имеют желтую окраску, дихроматы – оранжевую.
Хромат — ионы СrО42- и дихромат – ионы Сr2О72- легко переходят друг в друга при изменении среды растворов
В кислой среде раствора хроматы переходят в дихроматы:
В щелочной среде дихроматы переходят в хроматы:
При разбавлении дихромовая кислота переходит в хромовую кислоту:
Зависимость свойств соединений хрома от степени окисления.
Степень окисления | +2 | +3 | +6 |
Оксид | СrО | Сr2О3 | СrО3 |
Характер оксида | основной | амфотерный | кислотный |
Гидроксид | Сr(ОН)2 | Сr(ОН)3 – Н3СrО3 | Н2СrО4 Н2Сr2О7 |
Характер гидроксида | основной | амфотерный | кислотный |
→ ослабление основных свойств и усиление кислотных→ | |||
Окислительно – восстановительные свойства соединений хрома.
Реакции в кислотной среде.
В кислотной среде соединения Сr+6 переходят в соединения Сr+3 под действием восстановителей: H2S, SO2, FeSO4
Реакции в щелочной среде.
В щелочной среде соединения хрома Сr+3 переходят в соединения Сr+6 под действием окислителей: J2, Br2, Cl2, Ag2O, KClO3, h3O2, KMnO4:
studfile.net
Cr2O3 + Al = ? уравнение реакции
В результате сплавления оксида хрома (III) с алюминием (Cr2O3 + Al = ?), протекающем при температуре , происходит образование оксида алюминия и свободного хрома. Молекулярное уравнение реакции имеет вид:
Данная реакция относится к окислительно-восстановительным, поскольку химические элементы алюминий и хром изменяют свои степени окисления. Схемы электронного баланса выглядят следующим образом:
Оксид алюминия представляет собой кристаллы белого цвета, отличающиеся тугоплавкостью и термической устойчивостью. В прокаленном виде он химически пассивен; не реагирует с водой, разбавленными кислотами и щелочами. Проявляет амфотерные свойства; реагирует с концентрированными кислотами, щелочами в концентрированном растворе и при спекании.
Оксид алюминия в промышленности получают из природных минералов, которые его содержат, например, бокситов, нефелинов, каолина, алунитов и т.д. В лаборатории эту процедуру осуществляют по следующему уравнению:
ru.solverbook.com
Cr2O3 + K2CO3 = ? уравнение реакции
Оксид хрома , или хромовая охра, представляет собой твердый грязно-зеленый тугоплавкий порошок со структурой корунда. При комнатной температуре он обладает полупроводниковыми свойствами, а ниже — становится антиферромагнетиком. Цвет этого вещества зависит от размера частиц: крупные кристаллы, полученные из расплава, практически черные, а мельчайший порошок, образующийся при конденсации из газовой фазы, имеет красный цвет. При нагревании становится коричневым, но при охлаждении зеленая окраска восстанавливается.
Мелкий порошок оксида хрома (III) образуется при сжигании тонко раздробленного металла, дегидратации гидроксида, нагревании хромового ангидрида или хлористого хромилла, сплавлении дихроматов с серой или углем:
Оксид хрома (III) – это самое устойчивое соединение хрома. Он амфотерен, но благодаря высокой энергии кристаллической решетки не реагирует не только с водой, но и растворами кислот и щелочей. Для перевода его в растворимое состояние без изменения степени окисления используют хлорирование в смеси с углем:
сплавление с пиросульфатами, карбонатами (Cr2O3 + K2CO3 = ?) или гидроксидами щелочных металлов
Мелкодисперсный порошок применяют в качестве абразивного материала (пасты ГОИ), зеленого пигмента, катализатора в органическом синтезе. Оксид хрома (III) служит основной добавкой к корунду при выращивании из расплава кристаллов рубина, которые используют в ювелирной и часовой промышленности, а также в качестве лазерного материала в оптоэлектронике.
ru.solverbook.com