Чистые вещества и смеси ~ С химией по жизни
Дорогие мои восьмиклассники!Чистое вещество имеет определенный постоянный состав или структуру (соль, сахар).
В жизни редко встречаются чистые вещества, чаще — смеси веществ. Воздух – это смесь азота, кислорода и других газов, морская вода – смесь воды и растворенных солей.
Смеси — это физические сочетания чистых веществ, не имеющие определенного или чистого состава.Примером смеси может служить обыкновенный чай (напиток), который многие самостоятельно готовят и пьют по утрам. Кто-то любит крепкий чай (большое кол-во заварки), кто-то любит сладкий чай (большое кол-во сахара)… Как видим, смесь под названием «чай» всегда получается немного разной, хотя и состоит из одних и тех же компонентов. Однако, следует отметить, что каждый компонент смеси сохраняет набор своих характеристик, поэтому, разные вещества можно выделить из смеси.
| Роберт Бойль |
 Только чистая дистиллированная вода имеет tпл = 0 °С, tкип= 100 °С, не имеет вкуса. Морская вода замерзает при более низкой, а закипает при более высокой температуре, вкус у нее горько-соленый. Вода Черного моря замерзает при более низкой, а закипает при более высокой температуре, чем вода Балтийского моря. Почему? Дело в том, что в морской воде содержатся другие вещества, например растворенные соли, т.е. она представляет собой смесь различных веществ, состав которой меняется в широких пределах, свойства же смеси не являются постоянными. Определение понятия «смесь» было дано в XVII в. английским ученым Робертом Бойлем: «Смесь – целостная система, состоящая из разнородных компонентов».
В результате изучения темы «Чистые вещества и смеси», необходимо:
Только чистая дистиллированная вода имеет tпл = 0 °С, tкип= 100 °С, не имеет вкуса. Морская вода замерзает при более низкой, а закипает при более высокой температуре, вкус у нее горько-соленый. Вода Черного моря замерзает при более низкой, а закипает при более высокой температуре, чем вода Балтийского моря. Почему? Дело в том, что в морской воде содержатся другие вещества, например растворенные соли, т.е. она представляет собой смесь различных веществ, состав которой меняется в широких пределах, свойства же смеси не являются постоянными. Определение понятия «смесь» было дано в XVII в. английским ученым Робертом Бойлем: «Смесь – целостная система, состоящая из разнородных компонентов».
В результате изучения темы «Чистые вещества и смеси», необходимо:— иметь представление о чистых веществах и смесях: однородных и неоднородных; свойствах чистых веществ и смесей, их составе;
Для лучшего усвоения материала, рекомендую:
1. Посмотреть видеоурок;Другие видеоуроки по школьной программе смотрите на InternetUrok.
 ru 2. познакомиться с данными таблицы;
ru 2. познакомиться с данными таблицы;3. изучить классификацию смесей;
4. выполнить интерактивное задание «Смеси»;
5. выполнить интерактивное задание «Смеси в природе»;
6. выполнить интерактивное задание «Смеси в сельском хозяйстве»;
7. повторить п. 23, выполнить № 1-3, с.124
Желаю удачи!
Похожие материалы:Урок №4. Чистые вещества и смеси. Способы разделения смесей
I. Новый материал
При подготовке урока использованы материалы автора: Н.К.Черемисиной,
учителя химии средней школы № 43
(г. Калининград), Источник
Мы живем среди химических веществ. Мы вдыхает воздух,
а это смесь газов (азота, кислорода и других), выдыхаем углекислый
газ. Умываемся водой — это еще одно вещество, самое распространенное
на Земле. Пьём молоко — смесь воды с мельчайшими капельками
молочного жира, и не только: здесь еще есть молочный белок казеин,
минеральные соли, витамины и даже сахар, но не тот, с которым
пьют чай, а особый, молочный — лактоза. Едим яблоки, которые состоят из
целого набора химических веществ — здесь и сахар, и яблочная кислота,
и витамины… Когда прожеванные кусочки яблока попадают в желудок, на
них начинают действовать пищеварительные соки человека, которые помогают
усваивать все вкусные и полезные вещества не только яблока, но и любой другой
пищи. Мы не только живем среди химических веществ, но и сами из
них состоим. Каждый человек — его кожа, мышцы, кровь, зубы, кости, волосы
построены из химических веществ, как дом из кирпичей. Азот, кислород, сахар,
витамины – вещества природного, естественного происхождения.
Едим яблоки, которые состоят из
целого набора химических веществ — здесь и сахар, и яблочная кислота,
и витамины… Когда прожеванные кусочки яблока попадают в желудок, на
них начинают действовать пищеварительные соки человека, которые помогают
усваивать все вкусные и полезные вещества не только яблока, но и любой другой
пищи. Мы не только живем среди химических веществ, но и сами из
них состоим. Каждый человек — его кожа, мышцы, кровь, зубы, кости, волосы
построены из химических веществ, как дом из кирпичей. Азот, кислород, сахар,
витамины – вещества природного, естественного происхождения.
Чем же отличаются чистые вещества от смесей веществ?
Индивидуальное чистое вещество обладает определённым
набором характеристических свойств (постоянными физическими свойствами). Только
чистая дистиллированная вода имеет tпл = 0 °С, tкип= 100 °С, не имеет вкуса.
Морская вода замерзает при более низкой, а закипает при более высокой
температуре, вкус у нее горько-соленый. Вода Черного моря замерзает при более
низкой, а закипает при более высокой температуре, чем вода Балтийского моря.
Почему? Дело в том, что в морской воде содержатся другие вещества, например
растворенные соли, т.е. она представляет собой смесь различных веществ, состав
которой меняется в широких пределах, свойства же смеси не являются постоянными.
Определение понятия «смесь» было дано в XVII в. английским
ученым Робертом Бойлем:
Только
чистая дистиллированная вода имеет tпл = 0 °С, tкип= 100 °С, не имеет вкуса.
Морская вода замерзает при более низкой, а закипает при более высокой
температуре, вкус у нее горько-соленый. Вода Черного моря замерзает при более
низкой, а закипает при более высокой температуре, чем вода Балтийского моря.
Почему? Дело в том, что в морской воде содержатся другие вещества, например
растворенные соли, т.е. она представляет собой смесь различных веществ, состав
которой меняется в широких пределах, свойства же смеси не являются постоянными.
Определение понятия «смесь» было дано в XVII в. английским
ученым Робертом Бойлем:
Сравнительная характеристика смеси и чистого вещества
Признаки сравнения | Чистое вещество | Смесь |
Состав | Постоянный | Непостоянный |
Вещества | Одно и то же | Различные |
Физические свойства | Постоянные | Непостоянные |
Изменение энергии при образовании | Происходит | Не происходит |
Разделение | С помощью химических реакций | Физическими методами |
Смеси отличаются друг от друга по внешнему виду.
Классификация смесей показана в таблице:
Приведём примеры суспензий (речной песок + вода), эмульсий (растительное масло + вода) и растворов (воздух в колбе, поваренная соль + вода, разменная монета: алюминий + медь или никель + медь).
В суспензиях видны частицы твердого вещества, в эмульсиях – капельки жидкости, такие смеси называются неоднородными (гетерогенными), а в растворах компоненты не различимы, они являются однородными (гомогенными) смесями.
Способы разделения смесей
В природе вещества существуют в виде смесей. Для лабораторных исследований, промышленных производств, для нужд фармакологии и медицины нужны чистые вещества.
Для очистки
веществ применяются различные способы разделения смесей
Эти способы основаны на различиях в физических свойствах компонентов смеси.
Рассмотрим способы разделения гетерогенных и гомогенных смесей.
Пример смеси | Способ разделения |
Суспензия – смесь речного песка с водой | Отстаивание Разделение отстаиванием основано на различных плотностях веществ. Более тяжелый песок оседает на дно. Так же можно разделить и эмульсию: отделить нефть или растительное масло от воды. В лаборатории это можно сделать с помощью делительной воронки. Нефть или растительное масло образует верхний, более легкий слой. В результате отстаивания выпадает роса из тумана, осаждается сажа из дыма, отстаиваются сливки в молоке. Разделение смеси воды и растительного масла отстаиванием |
Смесь песка и поваренной соли в воде | Фильтрование На чем основано разделение гетерогенных смесей с
помощью фильтрования?На различной растворимости веществ в воде и на
различных размерах частиц. Разделение смеси крахмала и воды фильтрованием |
Смесь порошка железа и серы | Действие магнитом или водой Порошок железа притягивался магнитом, а порошок серы
– нет. Несмачивающийся порошок серы всплывал на поверхность воды, а тяжелый смачивающийся порошок железа оседал на дно. Разделение смеси серы и железа с помощью магнита и воды |
Раствор соли в воде – гомогенная смесь | Выпаривание или кристаллизация Вода испаряется, а в фарфоровой чашке остаются кристаллы соли. При выпаривании воды из озер Эльтон и Баскунчак получают поваренную соль. Этот способ разделения основан на различии в температурах кипения растворителя и растворенного вещества.Если вещество, например сахар, разлагается при нагревании, то воду испаряют неполностью – упаривают раствор, а затем из насыщенного раствора осаждают кристаллы сахара.Иногда требуется очистить от примесей растворители с меньшей температурой кипения, например воду от соли. В этом случае пары вещества необходимо собрать и затем сконденсировать при охлаждении. Такой способ разделения гомогенной смеси называется  В специальных приборах – дистилляторах получают дистиллированную воду, которую используют для нужд фармакологии, лабораторий, систем охлаждения
автомобилей. В
домашних условиях можно сконструировать такой дистиллятор: В специальных приборах – дистилляторах получают дистиллированную воду, которую используют для нужд фармакологии, лабораторий, систем охлаждения
автомобилей. В
домашних условиях можно сконструировать такой дистиллятор:Если же разделять смесь спирта и воды, то первым будет отгоняться (собираться в пробирке-приемнике) спирт с tкип = 78 °С, а в пробирке останется вода. Перегонка используется для получения бензина, керосина, газойля из нефти. Разделение однородных смесей |
Особым методом разделения компонентов, основанным на различной поглощаемости их определенным веществом, является хроматография.
Дома вы можете проделать следующий опыт. Подвесьте
полоску из фильтровальной бумаги над сосудом с красными чернилами, погружая в
них лишь конец полоски. Раствор впитывается бумагой и поднимается по ней. Но
граница подъема краски отстает от границы подъема воды. Так происходит
разделение двух веществ: воды и красящего вещества в чернилах.
С помощью хроматографии русский ботаник М. С. Цвет впервые выделил хлорофилл из зеленых частей растений. В промышленности и лабораториях вместо фильтровальной бумаги для хроматографии используют крахмал, уголь, известняк, оксид алюминия. А всегда ли требуются вещества с одинаковой степенью очистки?
Для различных целей необходимы вещества с различной степенью очистки. Воду для приготовления пищи достаточно отстоять для удаления примесей и хлора, используемого для ее обеззараживания. Воду для питья нужно предварительно прокипятить. А в химических лабораториях для приготовления растворов и проведения опытов, в медицине необходима дистиллированная вода, максимально очищенная от растворенных в ней веществ. Особо чистые вещества, содержание примесей в которых не превышает одной миллионной процента, применяются в электронике, в полупроводниковой, ядерной технике и других точных отраслях промышленности.
Прочитайте стихотворение Л. Мартынова «Дистиллированная вода»:
Вода
Благоволила
Литься!
Она
Блистала
Столь чиста,
Что ни напиться,
Ни умыться.
И это было неспроста.
Ей не хватало
Ивы, тала
И горечи цветущих лоз,
Ей водорослей не хватало
И рыбы, жирной от стрекоз.
Ей не хватало быть волнистой,
Ей не хватало течь везде.
Ей жизни не хватало
Чистой –
Дистиллированной воде!
Применение дистиллированной воды
II. Задания для закрепления
1) Поработайте с тренажёрами №1-4 (необходимо загрузить тренажёр)
Тренажёр №1. Чистые вещества и смеси
Тренажёр №2. Смеси
Тренажёр №3. Смеси в природе
Тренажёр №4. Смеси в сельском хозяйстве
2) Решите задачу:
Дана смесь сахара, речного песка и железных опилок. Предложите способ разделения этой смеси.3) Творческое задание:
Подготовьте электронную презентацию на тему «Чистые вещества и смеси, которые нас окружают»
Чистые вещества и смеси веществ. — Techemy
Индивидуальное чистое вещество обладает определенным набором характеристических свойств. От чистых веществ следует отличать смеси веществ, которые могут состоять из двух или большего числа чистых веществ, сохраняющих присущие им свойства.
От чистых веществ следует отличать смеси веществ, которые могут состоять из двух или большего числа чистых веществ, сохраняющих присущие им свойства.
Смеси веществ делятся на гомогенные (однородные) и гетерогенные (неоднородные). В таблице приведены различные примеры возможных смесей веществ в разных агрегатных состояниях.
Агрегатное состояние составных частей (до образования смеси)
Гомогенная смесь (система)
Гетерогенная смесь (система)
Твердое-твердое
Твердые растворы, сплавы, например латунь, бронза
Горные породы, например гранит, минералосодержащие руды
Твердое-жидкое
Жидкие растворы, например водные растворы солей
А. Твердое в жидком: суспензии или взвеси, например частицы глины в воде, коллоидные растворы
Б. Жидкое в твердом: жидкость в пористых телах, например почвы грунты
Твердое-газообразное
Хемосорбированный водород в платине, палладии, сталях
А. Твердое в газообразном: порошки, аэрозоли, дым, пыль, смог
Твердое в газообразном: порошки, аэрозоли, дым, пыль, смог
Б. Газообразное в твердом: пористые материалы, например пемза, пенопласт
Жидкое-жидкое
Жидкие растворы, например раствор уксусной кислоты в воде
Двух- и многослойные жидкие системы, эмульсии, например молоко — капли жидкого жира в воде
Жидкое-газообразное
Жидкие растворы, например раствор диоксида углерода в воде
А. Жидкое в газообразном: аэрозоли жидкости в газе, туманы
Б. Газообразное в жидком: пены, например мыльная пена
Газообразное-газообразное
Газовые растворы (смеси любых количеств и любого числа газов)
Гетерогенная система невозможна
В гомогенных смесях составные части нельзя обнаружить ни визуально, ни с помощью оптических приборов, поскольку вещества находятся в раздробленном состоянии на микроуровне. Гомогенными смесями являются смеси любых газов и истинные растворы, а также смеси некоторых жидкостей и твердых веществ, например сплавы.
В гетерогенных смесях либо визуально, либо с помощью оптических приборов можно различить области (агрегаты) разных веществ, разграниченные поверхностью раздела; каждая из этих областей внутри себя гомогенна. Такие области называются фазой.
Гомогенная смесь состоит из одной фазы, гетерогенная смесь состоит из двух или большего числа фаз.
Гетерогенные смеси, в которых одна фаза в виде отдельных частиц распределена в другой, называются дисперсными системами. В таких системах различают дисперсионную среду (распределяющую среду) и дисперсную фазу (раздробленное в дисперсионной среде вещество). Гетерогенные системы делят по размеру частиц дисперсной фазы на истинные растворы, высокодистперстные, среднедисперстные и грубодисперстные системы.
Класс дисперстности
Размер частиц дисперстной фазы (d), м
Дисперсность (1/d), шт./м
Примеры
Истинные растворы
… < 10-9
… > 109
Растворы хлорида натрия, сахарозы, уксусной кислоты, медного купороса, сплавы, газовые смеси и др.
Высокодисперстные (коллоидные растворы)
10-9 — 10-7
109 — 107
Коллоидные растворы золота, серебра, туман, аэрозоли, лиозоли, ксерозоли.
Среднедисперстные
10-7 — 10-5
107 — 105
Растворимый кофе, сахарная пудра, мука, соусы, цемент и др.
Грубодисперстные
10-5 < …
… < 105
Крупы, сахарный песок, щебень, и др.
Чистыми веществами называются вещества, которые при проведении физических методов не разделяются на два или более других веществ и не изменяют своих физических свойств.
В природе не существует абсолютно чистых веществ. Например, так называемый особо чистый алюминий все еще содержит 0,001 % примесей других веществ. Таким образом, абсолютно чистое вещество — это абстракция. Правда, когда речь идет о каком-либо веществе, то химия пользуется этой абстракцией, т. е. считает, что вещество истинно чистое, хотя практически берется вещество с некоторым содержанием примесей. Конечно, химик должен стремиться использовать в своей практике по возможности чистые вещества, содержащие минимальное количество примесей, следует учитывать, что даже незначительное содержание примесей может существенно изменить химические свойства вещества.
Конечно, химик должен стремиться использовать в своей практике по возможности чистые вещества, содержащие минимальное количество примесей, следует учитывать, что даже незначительное содержание примесей может существенно изменить химические свойства вещества.
Химическая промышленность выпускает реактивы различной степени чистоты, так что у химика всегда имеется выбор, в зависимости от цели использования реактива. Так, для приготовления охлаждающих смесей целесообразно применять технический (невысокой степени очистки) хлорид натрия, тогда как для изучения химических свойств NaCl следует взять химически чистый реактив.
С помощью физических методов разделения можно провести разделение смесей на их составные части, т. е. на относительно чистые вещества.
Агрегатное состояние составных частей (до образования смеси)
Физическое свойство используемое для разделения
Метод разделения
Твердое-твердое
Плотность
Смачиваемость
Размер частиц
Растворимость
Магнетизм
Отстаивание, седиментация
Флотация, пенная флотация
Просеивание
Экстракция, выщелачивание
Магнитная сепарация
Твердое-жидкое
Температура кипения жидкости
Плотность
Размер частиц
Растворимость твердого вещества
Выпаривание, дистилляция, осушка
Седиментация, декантация (сливание жидкости с осадка)
Фильтрование
Кристаллизация
Твердое-газообразное
Плотность
Размер частиц
Электрический заряд твердых частиц
Седиментация, центробежная сепарация
Фильтрование
Электрофильтрование
Жидкое-жидкое
Плотность
Температура кипения
Растворимость
Отстаивание (в делительной воронке, в маслоотделителе), центрифугирование
Дистилляция
Экстракция
Жидкое-газообразное
Плотность
Растворимость газа
Седиментация, центробежная сепарация
Отгонка газа (путем повышения температуры), промывание с помощью другой жидкости
Газообразное-газообразное
Температура конценсации
Абсорбируемость
Адсорбируемость
Размер частиц
Масса
Конденсация
Абсорбция (поглощение объемом сорбента)
Адсорбция (поглощение поверхностью сорбента)
Диффузия
Центрифугирование
Различия между смесями веществ и сложными веществами
Купить неорганические реактивы, inorganic chemicals в Санкт-Петербурге
В каталоге товаров/продукции представлены неорганические реактивы — категории: ;
Купить органические соединения, реактивы, organic chemicals в Санкт-Петербурге
В каталоге товаров/продукции представлены органические соединения, реактивы — реактивы Карла Фишера для волюметрии, реактивы HYDRANAL, органические растворители, органические кислоты, органические соли и соединения, категории: reagents for Karl Fischer volumetry, other reagents HYDRANAL, organic solvents, organic acids, organic salts and compounds, ; , , , , органические соединения, органические соли,реактивы Карла Фишера для волюметрии
Подробнее. ..
Купить реактивы карла фишера для волюметрии — reagents for Karl Fischer volumetry в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Использование реактивов Гидранал позволяет определить воду в составе химических реактивов, пищевых продуктов, фармацевтическихпрепаратов. Содержание воды влияет на множество химических и физических параметров выпускаемой продукции. Реактивы Карла Фишера произв…
..
Купить реактивы карла фишера для волюметрии — reagents for Karl Fischer volumetry в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Использование реактивов Гидранал позволяет определить воду в составе химических реактивов, пищевых продуктов, фармацевтическихпрепаратов. Содержание воды влияет на множество химических и физических параметров выпускаемой продукции. Реактивы Карла Фишера произв…органические растворители
Подробнее… Купить органические растворители (organic solvents) в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Купить органический растворитель в Санкт-Петербурге по выгодной цене. Компания ХИМСНАБ-СПБ предлагает следующую фасовку растворителей: п/э или стеклянная бутылка 1 литр; п/э канистра 10 литров; п/э канистра 5 литров; стеклянный флакон 1 литр, бочка, и бочка, 250 кг. Реактивы и растворители. ..
..органические кислоты
Подробнее… Купить органические кислоты — organic acids в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Органические вещества, проявляющие кислотные свойства (кислоты их кислые соли и средние соли содержатся во многих товарах. Благодаря наличию свободных кислот и кислых солей многие продукты и их водные вытяжки обладают кислой реакцией. К ним относятся карбоновые кислоты, содержа…Купить химические реактивы, chemicals в Санкт-Петербурге
В каталоге товаров/продукции представлены химические реактивы — вода, неорганические реактивы, органические соединения, реактивы, растворы, особо чистые вещества, категории: water, inorganic chemicals, organic chemicals, solutions, highly purified substances, ; дистиллированная вода, вода (УФ-ВЭЖХ) для аналитики, бидистиллированная вода, вода для молекулярной биологии, , , , ,неорганические реактивы
Подробнее. ..
Купить неорганические реактивы — inorganic chemicals в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93.
Неорганическое соединение, как правило, представляет собой химическое соединение, которое не имеет связей СН , то есть соединение, которое не является органическим соединением
Химические соединения, реагенты и реактивы находят свое применение в различных областях: научные-исследов…
..
Купить неорганические реактивы — inorganic chemicals в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93.
Неорганическое соединение, как правило, представляет собой химическое соединение, которое не имеет связей СН , то есть соединение, которое не является органическим соединением
Химические соединения, реагенты и реактивы находят свое применение в различных областях: научные-исследов…органические соединения, реактивы
Подробнее… Купить органические реактивы — organic chemicals в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Купить органический реактив в Санкт-Петербурге по выгодной цене. химические реактивы химические реактивы химические реактивы хим. реактивы продукцию chemicals химические реактивы, chemicals вода, неорганические реактивы, органические реактивы, растворы, особо чистые вещества особо чистые веще. ..
..растворы
Подробнее… Купить растворы — solutions в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. В каталоге ХИМСНАБ-СПБ представлен большой выбор готовых специальных растворов различного назначения: буферные растворы, растворы для заполнения, очистки и хранения электродов, стандартные растворы для кондуктометров, реактивы карла фишера для кулонометрии. Купить раствор в Санкт-Петербурге по выгодной цене: …особо чистые вещества
Подробнее… Купить особо чистые вещества (ультрачистые вещества) в Санкт-Петербурге, в компании Химснаб-СПБ, телефон +7-812-337-18-93. В высокочистых веществах содержатся примесей в незначительном количестве, что они не влияют на основные специфические свойства веществ. Свойства особо чистых веществ используют для создания новых приборов, устройств и технологических процессов. Они находят применени… Оставьте заявку ON-LINE или позвоните. Менеджер компании ответит на ваши вопросы.
Свойства особо чистых веществ используют для создания новых приборов, устройств и технологических процессов. Они находят применени… Оставьте заявку ON-LINE или позвоните. Менеджер компании ответит на ваши вопросы.
Широкий ассортимент
В каталоге компании более 4000 наименований продукции в 200 товарных категориях: химические реактивы, лаб. оборудование и посуда, аксессуары и принадлежности для лабораторий, различные виды удобрений, химическое сырьеи многе другое. Можно подобрать продукцию воспользовавшись фильтром характеристик.
Проверенные поставщики
Компания реализует товары и продукцию только от проверенных поставщиков гарантирующих качестно продукции.
Консультация по продукции
Менеджеры компании проконсультируют вас по ассортименту реализуемой продукции, звоните в рабочее время
Доставка
География потребителей выходит за пределы России, компания «Химснаб-СПБ» осуществляет доставку приобретаемых товаров и продукции по Санкт-Петербургу, Ленинрадской обл, России и странам СНГ.
Индивидуальный подход
Строим свое сотрудничество с клиентом с учетом всех пожеланий клиента.
Гибкий и индивидуальный подход к каждому клиенту, ориентированность на долгосрочные партнерские отношения, строгое соблюдение оговоренных сроков и предоставления документов заказчику являются неоспоримыми преимуществами компании «Химснаб-СПБ». Мы заботимся о том, чтобы каждый наш клиент остался доволен приобретаемой продукцией и полученным результатом, который является нашим общим успехом!
Мы заботимся о том, чтобы каждый наш клиент остался доволен приобретаемой продукцией и полученным результатом, который является нашим общим успехом!
Малотоннажная химия
Реализация продукции малотоннажной химии: продукция химической и нефтехимической промышленности. Малотоннажная химия дает возможность на скромном оборудовании и в небольших объемах производить дорогостоящие модификаторы, пластификаторы, ингибиторы и другие микродобавки, способные наделять конечный продукт новыми свойствами
Комплексное снабжение, оснащение
Компания Химснаб-СПБ имеет многолетний опыт работы на рынке химической продукции и лабораторного оборудования. Компания тесно сотрудничает со многими промышленными и производственными организациями и имеет возможность осуществлять комплексное снабжение и оснащение предприятии различных отраслений промышленности необходимым оборудованием и расходными материалами.
Предствленная информация на страницах данного интернет-сайта и в каталоге продукции носит исключительно информационный характер и ни при каких условиях не является публичной офертой, определяемой положениями Статьи 437 (2) Гражданского кодекса РФ. Для получения подробной информации о наличии и стоимости указанных товаров и (или) услуг,обращайтесь к менеджерам отдела продаж: форма обратной связи, e-mail, телефон.
Реализация продукции для сельского хозяйства, химической, строительной, нефтегазовой, металлургической, текстильной, кожевенной, и других отраслей промышленности.
Чистые вещества и смеси. Разделение смесей. 5 Класс «введение в химию»
Слайды и текст этой презентации
Слайд 1
Чистые вещества и смеси. разделение смесей
5 класс
«Введение в химию»
учитель химии МАОУ «СОШ №2»
Волкова О.В.
Слайд 2
Эпиграф занятия
Нет на карте белых пятен,
Вся Земля давно открыта,
Очень трудно жить на свете,
В наше время без открытий.
Слайд 3
Цель занятия :
познакомиться с понятиями «чистые вещества» и «смеси»;
виды смесей;
способами разделения смесей.
Слайд 4
Задание1. Используя текст, закончить определения понятий: чистое вещество, смесь.
Мы живем среди химических веществ. Мы вдыхает воздух, а это смесь газов (азота, кислорода и других), выдыхаем углекислый газ. Умываемся водой — это еще одно вещество, самое распространенное на Земле. Пьём молоко — смесь воды с мельчайшими капельками молочного жира, и не только: здесь еще есть молочный белок казеин, минеральные соли, витамины и даже сахар, но не тот, с которым пьют чай, а особый, молочный — лактоза. Едим яблоки, которые состоят из целого набора химических веществ — здесь и сахар, и яблочная кислота, и витамины… Мы не только живем среди химических веществ, но и сами из них состоим. Каждый человек — его кожа, мышцы, кровь, зубы, кости, волосы построены из химических веществ, как дом из кирпичей. И всё это – это тоже вещества, точнее, смеси веществ. Совершенно чистые вещества в природе не встречаются.
Совершенно чистые вещества в природе не встречаются.
Слайд 5
Работа с терминами
Вещества, образованные только одинаковыми частицами (например, атомы, молекулы) называются чистыми веществами.
В природе чистые вещества никогда не встречаются. Любое, даже самое чистое вещество обязательно содержит в себе примеси других веществ. Это смеси.
или
Смесь — это материал, состоящий из двух или нескольких веществ.
Слайд 6
определите, где на рисунке изображена смесь и чистое вещество?
Слайд 7
Задание 2. Внимательно рассмотрите предложенные вам смеси
Отличаются ли смеси по внешнему виду друг от друга? Если отличаются, то чем?
Какие бывают смеси?
Слайд 8
Работа с терминами
Смеси, в которых невооружённым глазом или при помощи микроскопа можно заметить частицы веществ, называют неоднородными.
Смеси, в которых даже с помощью микроскопа нельзя обнаружить частицы веществ, входящих в смесь, называют однородными.
Слайд 9
Классификация смесей :
Слайд 10
разделение смесей
Слайд 11
разделение неоднородных смесей Отстаивание
ФИЛЬТРОВАНИЕ
Слайд 12
разделение однородных смесей
Слайд 13
Перегонка Дистилляция
Слайд 14
Результаты эксперимента:
Название опыта.Что делали?.Способ?.Что наблюдали?
вода + масло
смесь неоднородная.вода + масло
отстаивание.отстаивание.Расслоение жидкостей: масло образует верхний, более легкий слой; нижний слой — вода.
вода + ил
смесь неоднородная.вода + ил перемешивание,
фильтрование.фильтрование.После перемешивания — вода мутная;
после фильтрования — прозрачная.
вода + соль
смесь однородная
вода + песок
смесь неоднородная.вода + соль
вода + песок
перемешивание,
фильтрование.?
фильтрование.?
После перемешивания — вода мутная;
после фильтрования — прозрачная.
Слайд 15
Сделайте вывод о способах разделения смесей
Слайд 16
Рефлексия
«Покажи своё лицо» Выберите нужную букву:
А) Узнал много интересной информации, усвоил материал.
Б) Узнал много интересной информации, усвоил материал частично.
В) Узнал много интересной информации, но ничего не понял.
Г) Мне было скучно.
Выберите смайлик:
А)Хорошо
Б)Усвоил материал частично
В)Ничего не понял
Г) скучно
Слайд 17
Домашнее задание:
1.Принести скрепки, чистую банку 0,5л, карандаш, прочную хлопчатобумажную или шерстяную нить.
2.Выполнить презентацию (по желанию)
«Процесс фильтрования в быту, в технике и
в природе».
Слайд 18
Чистые вещества и смеси. Разделение смесей | Природоведение. Реферат, доклад, сообщение, краткое содержание, конспект, сочинение, ГДЗ, тест, книга
Каждое вещество состоит из определённых частиц. Например, вода состоит из молекул воды, в которой два атома водорода соединены с одним атомом кислорода. Молекулы воды отличаются по составу, форме, размерам, свойствам от молекул других веществ. Если в посудине содержатся только молекулы воды и отсутствуют частицы других веществ, то такая вода является чистым веществом.
Молекулы воды отличаются по составу, форме, размерам, свойствам от молекул других веществ. Если в посудине содержатся только молекулы воды и отсутствуют частицы других веществ, то такая вода является чистым веществом.
Чистые вещества. Чистые вещества характеризуются постоянными физическими свойствами. Например, только чистая вода кипит при температуре 100 °С и замерзает при 0 °С. Если в ней растворить соль, то температура кипения превысит 100 °С, а температура замерзания снизится. Поэтому во время гололедицы тротуары посыпают поваренной солью.
Состав чистого вещества постоянный, независимо от того, как его добывали и где вещество находится в природе.
Чистыми веществами называют вещества, которые состоят из частиц одного вещества и характеризуются постоянными физическими свойствами.
Ознакомьтесь с примерами чистых веществ на рис. 22.
Рис. 22. Чистые вещества: а — самородное золото; б — газообразное вещество хлор в запаянной стеклянной ампуле; в — очищенная вода в стакане 22. Чистые вещества: а — самородное золото; б — газообразное вещество хлор в запаянной стеклянной ампуле; в — очищенная вода в стакане |
Покупая в магазине соль, сахар, крахмал, мы считаем, что это чистые вещества. Однако и в этих продуктах питания имеются незначительные примеси других веществ. Следовательно, в природе и повседневной жизни вещества в чистом виде практически не встречаются.
| Йогурт — пример смеси, изготовленной человеком |
Смеси. В природе, технике, быту преобладают смеси двух или нескольких веществ. Природными смесями являются воздух, природный газ, нефть, молоко, морская вода, гранит, горные породы, фруктовые соки. По рис. 23 выясните, в каких агрегатных состояниях могут находиться смеси.
К известным вам смесям, которые созданы и используются человеком, относятся: строительные смеси, бензин, краски, стиральные порошки, зубные пасты, кетчупы, майонезы, разнообразные блюда и т. д.
д.
| Рис. 23. Природные смеси: а — нефть; б — молоко; в — морская вода; г — гранит; д — горные породы; е — фруктовые соки |
Смесь — это два и больше веществ, смешанных между собой. Различают твёрдые, жидкие, газообразные смеси.
| Рис. 24. Образование смеси лимонной кислоты и воды |
На рис. 24 показано, как из лимонной кислоты и воды приготовили смесь. Молекулы этих веществ смешаны между собой.
Вы также можете приготовить разные смеси, например чай, мыльный раствор, компот, тесто — смесь из муки, соды и воды.
Отдельные вещества в составе смеси принято называть компонентами. Компоненты природной смеси гранита увидеть просто. В другой природной смеси — молоке — компоненты не видны, хотя в её составе много веществ и среди них — вода, жиры, белки. Эти компоненты можно определить с помощью микроскопа. А вот рассмотреть компоненты такой природной смеси, как морская вода, не удаётся даже под микроскопом.
Эти компоненты можно определить с помощью микроскопа. А вот рассмотреть компоненты такой природной смеси, как морская вода, не удаётся даже под микроскопом.
Смеси бывают природные и приготовленные человеком. Для приготовления одной смеси необходимо иметь два или несколько веществ. Материал с сайта //iEssay.ru
| Разделение смеси во время изготовления творога |
Смесь воды и сахара может долго оставаться без изменений. Природная смесь — молоко через несколько дней пребывания в тёплом месте начинает разделяться на компоненты. В верхнем слое накапливается жир, под ним становятся видимыми сгущение белковых молекул и жидкость. Чтобы получить отдельно сметану, масло и творог, смесь надо разделить.
Разделить смесь — означает отделить каждый её компонент.
Для проведения отдельных опытов необходимы чистые вещества. Поэтому используют разные способы извлечения из одного вещества частиц другого вещества. О способах разделения смесей вы узнаете в следующем параграфе.
Поэтому используют разные способы извлечения из одного вещества частиц другого вещества. О способах разделения смесей вы узнаете в следующем параграфе.
Уроки 3-4. Чистые вещества и смеси. Способы разделения смесей.
1. Что такое чистые вещества?
Чистые вещества – вещества, которые имеют постоянный качественный и количественный состав.
Смеси – это многокомпонентные системы, в которых свойства веществ сохраняются.
Неоднородные смеси – это гетерогенные системы, в которых обнаруживается поверхность раздела фаз.
Однородные смеси – это гомогенные системы, в которых невооружённым глазом поверхность раздела фаз не обнаруживается.
2. Чем смеси отличаются от чистых веществ?
В смеси свойства компонентов сохраняются, состав смеси непостоянен.
3. Подчеркните названия чистых веществ: сталь, алюминий, кока-кола, кислород, спиртовой раствор иода, поваренная соль, морская вода, воздух, железо, почва, дистиллированная вода.
4. Чтобы выявить свойства вещества, нужно брать для исследования чистые вещества, потому что смеси, т.е. компоненты смесей, будут мешать исследованию.
5. Зачем нужно разделение смесей?
Для того, чтобы получить чистые вещества.
6. На чем основано разделение смесей?
На различных химических свойствах их компонентов.
7. Метод фильтрования основан на выделении веществ из неоднородной смеси, образованной растворимыми и нерастворимыми в воде веществами.
8. Метод отстаивания основан на различии в плотностях веществ, смешанных с водой.
9. Метод выпаривания основан на разных температурах кипения компонентов смеси, выделяют таким образом вещества из гомогенной смеси.
10. Метод дистилляции (перегонки) основан на разделении однородных смесей путём испарения летучих жидкостей с последующей конденсацией их паров.
11. Метод кристаллизации основан на частичном упаривании воды, при охлаждении растворённое вещество выделяется в виде кристаллов.
Метод кристаллизации основан на частичном упаривании воды, при охлаждении растворённое вещество выделяется в виде кристаллов.
12. Метод хроматографии основан на различном поглощении разделяемых веществ поверхностью другого вещества.
13. В сахарный песок случайно попали древесные опилки. Опишите способ, которым можно очистить сахар от примесей.
1) растворить в воде;
2) отфильтровать – отделить опилки;
3)выпарить – на дне чашки останется сахар.
14. Опишите способ, которым можно разделить смесь, состоящую из речного песка, древесных опилок и поваренной соли.
1) растворить в воде – соль растворится, а песок, как более тяжёлый осядет на дне;
2) отфильтровать опилки;
3) выпарить воду – на дне чашки останется поваренная соль.
15. При исследовании образца воды было выявлено, что в воде содержатся нерастворимые частички твердого вещества (предположительно древесные стружки), несмешивающаяся с водой жидкость (возможно масло). Образец имеет неприятный запах и неестественный цвет, кроме того, содержит растворенную соль. Как очистить такую воду? Опишите последовательность операций.
Образец имеет неприятный запах и неестественный цвет, кроме того, содержит растворенную соль. Как очистить такую воду? Опишите последовательность операций.
1) отделить воду от масла делительной воронкой – отделится масло;
2) отфильтровать – отделятся древесные стружки;
3) выпарить – на дне чашки останется соль, которая была растворена в воде.
Веществ и смесей | Введение в химию
Цель обучения
- Отличить химические вещества от смесей
Ключевые моменты
- Вещество можно разделить на две категории: чистые вещества и смеси. Чистые вещества далее разбиваются на элементы и соединения. Смеси — это физически комбинированные структуры, которые можно разделить на исходные компоненты.
- Химическое вещество состоит из одного типа атомов или молекул.
- Смесь состоит из различных типов атомов или молекул, которые не связаны химически.
- Гетерогенная смесь — это смесь двух или более химических веществ, в которой можно визуально различить различные компоненты.

- Гомогенная смесь — это смесь, состав которой однороден, и каждая часть раствора имеет одинаковые свойства.
- Существуют различные методы разделения для разделения веществ, включая дистилляцию, фильтрацию, выпаривание и хроматографию.Для этого разделения вещество может находиться в одной или двух разных фазах.
Условия
- веществоФорма вещества, имеющая постоянный химический состав и характерные свойства. Он состоит из одного типа атомов или молекул.
- элемент: Химическое вещество, состоящее из определенного типа атома, которое не может быть расщеплено или преобразовано с помощью химической реакции.
- смесь: Что-то, что состоит из различных, несвязанных элементов или молекул.
Химические вещества
В химии химическое вещество — это форма вещества, имеющая постоянный химический состав и характерные свойства. Его нельзя разделить на компоненты без разрыва химических связей. Химические вещества могут быть твердыми, жидкостями, газами или плазмой. Изменения температуры или давления могут вызывать переход веществ между различными фазами вещества.
Химические вещества могут быть твердыми, жидкостями, газами или плазмой. Изменения температуры или давления могут вызывать переход веществ между различными фазами вещества.
Элемент — это химическое вещество, состоящее из определенного вида атома и, следовательно, не может быть расщеплено или преобразовано в результате химической реакции в другой элемент.Все атомы элемента имеют одинаковое количество протонов, хотя они могут иметь разное количество нейтронов и электронов.
Чистое химическое соединение — это химическое вещество, которое состоит из определенного набора молекул или ионов, которые химически связаны. Два или более элемента, объединенных в одно вещество в результате химической реакции, например вода, образуют химическое соединение. Все соединения являются веществами, но не все вещества являются соединениями. Химическое соединение может быть либо атомами, связанными вместе в молекулы, либо кристаллами, в которых атомы, молекулы или ионы образуют кристаллическую решетку. Соединения, состоящие в основном из атомов углерода и водорода, называются органическими соединениями, а все остальные — неорганическими соединениями. Соединения, содержащие связи между углеродом и металлом, называются металлоорганическими соединениями.
Соединения, состоящие в основном из атомов углерода и водорода, называются органическими соединениями, а все остальные — неорганическими соединениями. Соединения, содержащие связи между углеродом и металлом, называются металлоорганическими соединениями.
Химические вещества часто называют «чистыми», чтобы отличить их от смесей. Типичный пример химического вещества — чистая вода; он всегда имеет одни и те же свойства и одинаковое отношение водорода к кислороду, независимо от того, выделен ли он из реки или изготовлен в лаборатории.Другие химические вещества, обычно встречающиеся в чистом виде, — это алмаз (углерод), золото, поваренная соль (хлорид натрия) и рафинированный сахар (сахароза). Простые или кажущиеся чистыми вещества, встречающиеся в природе, на самом деле могут быть смесями химических веществ. Например, водопроводная вода может содержать небольшие количества растворенного хлорида натрия и соединений, содержащих железо, кальций и многие другие химические вещества. Чистая дистиллированная вода — это вещество, а морская вода, поскольку она содержит ионы и сложные молекулы, представляет собой смесь.
Химические смеси
Смесь — это система материалов, состоящая из двух или более различных веществ, которые смешаны, но не соединены химически. Под смесью понимается физическая комбинация двух или более веществ, в которой сохранены идентичности отдельных веществ. Смеси имеют форму сплавов, растворов, суспензий и коллоидов.
Встречающиеся в природе кристаллы серы Сера встречается в природе в виде элементарной серы, сульфида и сульфатных минералов, а также в виде сероводорода.Это месторождение полезных ископаемых состоит из смеси веществ.Гетерогенные смеси
Гетерогенная смесь — это смесь двух или более химических веществ (элементов или соединений), в которой различные компоненты можно визуально различить и легко разделить физическими средствами. Примеры включают:
- смеси песка и воды
- смеси песка и опилок
- каменный конгломерат
- вода и масло
- салат
- трейл микс
- смеси золотого порошка и серебряного порошка

Гомогенные смеси
Гомогенная смесь — это смесь двух или более химических веществ (элементов или соединений), различные компоненты которой невозможно различить визуально. Состав гомогенных смесей постоянный. Часто разделение компонентов гомогенной смеси является более сложной задачей, чем разделение компонентов гетерогенной смеси.
Различие между гомогенными и гетерогенными смесями зависит от масштаба отбора проб.В достаточно малом масштабе любую смесь можно назвать гетерогенной, потому что образец может быть размером с одну молекулу. На практике, если интересующие свойства одинаковы, независимо от того, сколько смеси взято, смесь является однородной.
Физические свойства смеси, такие как температура плавления, могут отличаться от свойств ее отдельных компонентов. Некоторые смеси можно разделить на компоненты физическими (механическими или термическими) способами.
Химия 1.2 Classification Matter (Part 1 of 3) — YouTube Введение в классификацию вещества как вещества или смеси веществ. Смеси описываются как гетерогенные или гомогенные. Описываются три распространенных метода разделения. Часть 2 из 3: http://www.youtube.com/watch?v=SoFywULNF3s (Вещества) Часть 3 из 3: http://www.youtube.com/watch?v= LXMyN9kco7E (диаграммы частиц)
Показать источники
Смеси описываются как гетерогенные или гомогенные. Описываются три распространенных метода разделения. Часть 2 из 3: http://www.youtube.com/watch?v=SoFywULNF3s (Вещества) Часть 3 из 3: http://www.youtube.com/watch?v= LXMyN9kco7E (диаграммы частиц)
Показать источникиBoundless проверяет и курирует высококачественный контент с открытой лицензией из Интернета. Этот конкретный ресурс использовал следующие источники:
3.05: Чистые вещества и смеси
Учебная цель
- Различают чистые вещества и смеси
- Определять смеси как однородные или неоднородные
Чистые вещества
Когда мы говорим о чистом веществе , мы говорим о чем-то, что содержит только один вид материи. Это может быть либо один элемент, либо одно соединение, но каждый образец этого вещества, который вы исследуете, должен содержать одно и то же с фиксированным, определенным набором свойств.
| Чистое вещество | Элемент или соединение? | Состоит из: |
|---|---|---|
| Свинец (Pb) | элемент | атома свинца |
| Кислород (O 2 ) | элемент | молекулы кислорода * |
| Вода (H 2 O) | соединение | молекулы воды |
| Аммиак (NH 3 ) | соединение | молекулы аммиака |
* Примечание: чистый газообразный кислород состоит из молекул, но по-прежнему считается элементом, а не соединением, поскольку молекулы состоят из элементов одного типа. Соединения состоят из одного или нескольких элементов.
Соединения состоят из одного или нескольких элементов.
Смеси
Если мы берем два или более чистых вещества и смешиваем их вместе, мы называем это смесью . Смеси всегда можно снова разделить на составляющие чистые вещества, потому что связывание между атомами составляющих веществ не происходит в смеси. В то время как соединение может иметь свойства, сильно отличные от входящих в его состав элементов, в смесях вещества сохраняют свои индивидуальные свойства.Например, натрий — мягкий блестящий металл, а хлор — едкий зеленый газ. Эти два элемента могут объединяться с образованием соединения, хлорида натрия (поваренная соль), которое представляет собой белое кристаллическое твердое вещество, имеющее — ни свойств натрия или хлора. Если, однако, вы смешали поваренную соль с молотым перцем, вы все равно могли бы видеть отдельные зерна каждого из них, и, если бы вы были терпеливы, вы могли бы взять пинцет и осторожно разделить их обратно на чистую соль и чистый перец. .
.
Гетерогенная смесь
Гетерогенная смесь представляет собой смесь, состав которой неоднороден по всей смеси. Овощной суп — это неоднородная смесь. Любая данная ложка супа будет содержать различное количество различных овощей и других компонентов супа.
Гомогенная смесь / Раствор
Гомогенная смесь представляет собой комбинацию двух или более веществ, которые так тщательно перемешаны, что смесь ведет себя как единое вещество.Еще одно слово для обозначения однородной смеси — раствор. Таким образом, комбинация соли и стальной ваты представляет собой неоднородную смесь, поскольку легко увидеть, какие частицы вещества представляют собой кристаллы соли, а какие — стальную вату. С другой стороны, если вы возьмете кристаллы соли и растворите их в воде, очень трудно определить наличие более чем одного вещества, просто взглянув, даже если вы используете мощный микроскоп. Соль, растворенная в воде, представляет собой гомогенную смесь или раствор (Рисунок \ (\ PageIndex {3} \)).
Рисунок \ (\ PageIndex {3} \): Типы смесей © Thinkstock Слева комбинация двух веществ представляет собой гетерогенную смесь, поскольку частицы двух компонентов выглядят по-разному. Справа кристаллы соли растворились в воде настолько тонко, что вы не можете сказать, присутствует ли соль. Гомогенная смесь выглядит как единое вещество.
Пример \ (\ PageIndex {3} \)
Определите следующие комбинации как гетерогенные смеси или гомогенные смеси.
- газированная вода (двуокись углерода растворяется в воде.)
- смесь металлической стружки железа и порошка серы (и железо, и сера являются элементами.)
Рисунок \ (\ PageIndex {4} \): Смесь железной стружки и порошка серы ( Asoult, смесь Fe-S 03, CC BY 4.0)
Решение
- Поскольку диоксид углерода растворен в воде, мы можем сделать вывод из поведения кристаллов соли, растворенных в воде, что диоксид углерода, растворенный в воде, является (также) гомогенной смесью.

- Если предположить, что железо и сера просто смешаны вместе, должно быть легко увидеть, что такое железо, а что такое сера, так что это гетерогенная смесь.
Упражнение \ (\ PageIndex {3} \)
Являются ли следующие комбинации гомогенными смесями или гетерогенными смесями?
- человеческое тело
- амальгама, комбинация некоторых других металлов, растворенных в небольшом количестве ртути
Ответы
- гетерогенная смесь
- однородная смесь
Классификация материалов
Рисунок \ (\ PageIndex {1} \): Взаимосвязь между типами веществ и методами, используемыми для разделения смесей Обычная поваренная соль называется хлоридом натрия.Считается веществом , потому что оно имеет однородный и определенный состав. Все образцы хлорида натрия химически идентичны. Вода — тоже чистое вещество.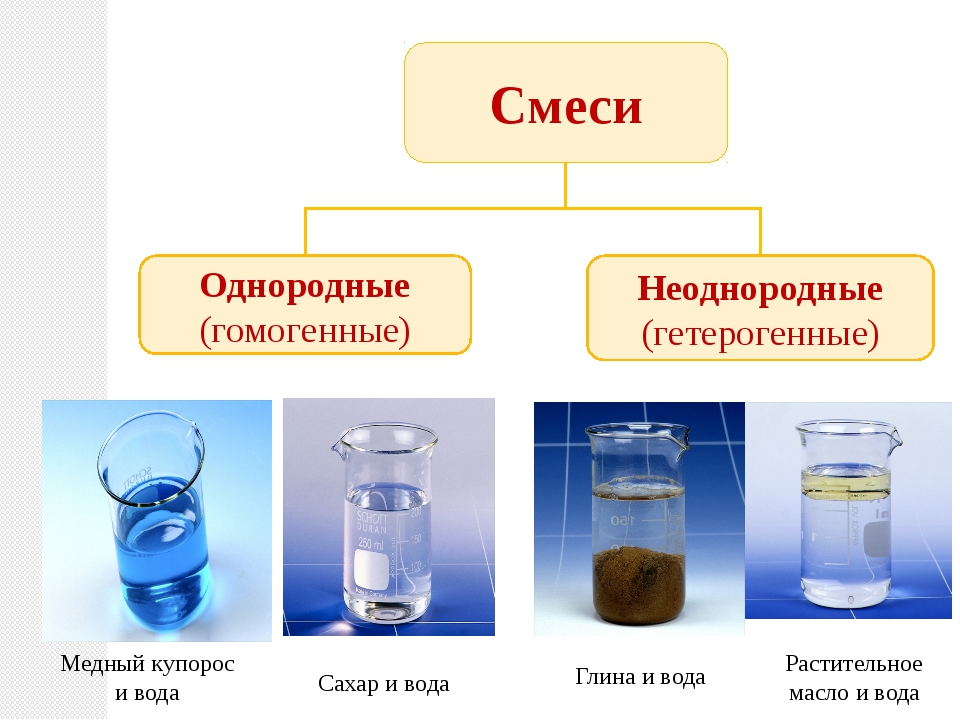 Соль легко растворяется в воде, но соленую воду нельзя классифицировать как вещество, поскольку ее состав может варьироваться. Вы можете растворить небольшое или большое количество соли в определенном количестве воды. Смесь представляет собой физическую смесь двух или более компонентов, каждый из которых сохраняет свою индивидуальность и свойства в смеси .Только форма соли изменяется, когда она растворяется в воде. Он сохраняет свой состав и свойства.
Соль легко растворяется в воде, но соленую воду нельзя классифицировать как вещество, поскольку ее состав может варьироваться. Вы можете растворить небольшое или большое количество соли в определенном количестве воды. Смесь представляет собой физическую смесь двух или более компонентов, каждый из которых сохраняет свою индивидуальность и свойства в смеси .Только форма соли изменяется, когда она растворяется в воде. Он сохраняет свой состав и свойства.
Этап
Фаза — это любая часть образца, имеющая однородный состав и свойства. По определению, чистое вещество или гомогенная смесь состоит из одной фазы. Гетерогенная смесь состоит из двух или более фаз. Когда масло и вода смешиваются, они не смешиваются равномерно, а образуют два отдельных слоя. Каждый из слоев называется фазой.
Пример \ (\ PageIndex {1} \)
Определите каждое вещество как соединение, элемент, гетерогенную смесь или гомогенную смесь (раствор).
- чай фильтрованный
- свежевыжатый апельсиновый сок
- компакт-диск
- оксид алюминия, белый порошок с соотношением атомов алюминия и кислорода 2: 3
- селен
Дано : химическое вещество
Запрошено : его классификация
Стратегия:
- Определите, является ли вещество химически чистым.
 Если оно чистое, это либо элемент, либо соединение. Если вещество можно разделить на элементы, это соединение.
Если оно чистое, это либо элемент, либо соединение. Если вещество можно разделить на элементы, это соединение. - Если вещество не является химически чистым, это либо гетерогенная смесь, либо гомогенная смесь. Если его состав однороден во всем, это однородная смесь.
Решение:
- A) Чай представляет собой раствор соединений в воде, поэтому он не является химически чистым. Обычно его отделяют от чайных листьев фильтрацией.
B) Поскольку состав раствора однороден повсюду, это однородная смесь . - A) Апельсиновый сок содержит твердые частицы (мякоть), а также жидкость; он не является химически чистым.
B) Апельсиновый сок представляет собой неоднородную смесь , поскольку его состав неоднороден. - A) Компакт-диск — это твердый материал, содержащий более одного элемента, с видимыми по краям участками разного состава.
 Следовательно, компакт-диск не является химически чистым.
Следовательно, компакт-диск не является химически чистым.
B) Области разного состава указывают на то, что компакт-диск представляет собой гетерогенную смесь. - A) Оксид алюминия представляет собой отдельное химически чистое соединение .
- A) Селен — один из известных элементов .
Упражнение \ (\ PageIndex {1} \)
Определите каждое вещество как соединение, элемент, гетерогенную смесь или гомогенную смесь (раствор).
- белое вино
- ртуть
- заправка для салата в стиле ранчо
- сахар столовый (сахароза)
- Ответ:
- гомогенная смесь (раствор)
- Ответ б:
- элемент
- Ответ c:
- гетерогенная смесь
- Ответ d:
- соединение
Пример \ (\ PageIndex {2} \)
Как бы химик классифицировал каждый образец вещества?
- соленая вода
- почва
- вода
- кислород
РЕШЕНИЕ
- Соленая вода действует как единое целое, даже если содержит два вещества — соль и воду.
 Морская вода — это однородная смесь или раствор.
Морская вода — это однородная смесь или раствор. - Почва состоит из маленьких кусочков различных материалов, поэтому представляет собой неоднородную смесь.
- Вода — это вещество; более конкретно, поскольку вода состоит из водорода и кислорода, она представляет собой соединение.
- Кислород, вещество, это элемент.
Упражнение \ (\ PageIndex {2} \)
Как бы химик классифицировал каждый образец вещества?
- кофе
- водород
- яйцо
- Ответ:
- однородная смесь (раствор), предположим, это фильтрованный кофе
- Ответ б:
- элемент
- Ответ c:
- смесь гетерогенная.
- Чистые вещества состоят из одного элемента или соединений.
- Комбинации разных веществ называются смесями.
- Гомогенные смеси — это смеси двух или более соединений (или элементов), которые не отличаются друг от друга визуально.
- Гетерогенные смеси — это смеси двух или более соединений (или элементов), которые визуально отличимы друг от друга.
- Вещество можно разделить на две категории: чистые вещества и смеси.Чистые вещества далее разбиваются на элементы и соединения. Смеси — это физически комбинированные структуры, которые можно разделить на исходные компоненты.
- Химическое вещество состоит из одного типа атомов или молекул.
- Смесь состоит из различных типов атомов или молекул, которые не связаны химически.
- Гетерогенная смесь — это смесь двух или более химических веществ, в которой можно визуально различить различные компоненты.
- Гомогенная смесь — это смесь, состав которой однороден, и каждая часть раствора имеет одинаковые свойства.
- Существуют различные методы разделения для разделения веществ, включая дистилляцию, фильтрацию, выпаривание и хроматографию. Для этого разделения вещество может находиться в одной или двух разных фазах.

- смесь : Что-то, что состоит из различных, несвязанных элементов или молекул.
- элемент : химическое вещество, которое состоит из определенного типа атома и не может быть разрушено или преобразовано с помощью химической реакции.
- вещество : форма вещества, имеющая постоянный химический состав и характерные свойства. Он состоит из одного типа атомов или молекул.
- смеси песка и воды
- смеси песка и опилок
- каменный конгломерат
- вода и масло
- салат
- трейл микс
- смеси золотого порошка и серебряного порошка
- Элементы — это простейшие законченные химические вещества.Каждому элементу соответствует отдельная запись в периодической таблице. Элемент — это материал, состоящий из одного типа атомов. Каждый тип атома содержит одинаковое количество протонов.
- Химические связи соединяют элементы вместе, образуя более сложные молекулы, называемые соединениями.
 Соединение состоит из двух или более типов элементов, удерживаемых вместе ковалентными или ионными связями.
Соединение состоит из двух или более типов элементов, удерживаемых вместе ковалентными или ионными связями. - Элементы не могут быть разделены на более мелкие части без большого количества энергии. Соединения, с другой стороны, могут быть разорваны с помощью практического количества энергии, например тепла от огня.
- Вещество можно разделить на две категории: чистые вещества и смеси. Чистые вещества далее разбиваются на элементы и соединения. Смеси представляют собой физически комбинированные структуры, которые можно разделить на исходные компоненты.
- элемент : Любое из простейших химических веществ, которое нельзя изменить в результате химической реакции или каких-либо химических средств. Состоит из атомов, имеющих одинаковое количество протонов.
- химическая связь : Любая из нескольких сил притяжения, которые служат для связывания атомов вместе с образованием молекул.
- соединение : Вещество, состоящее из двух или более элементов.
 Состоит из фиксированного соотношения химически связанных атомов. Обладает уникальными свойствами, которые отличаются от свойств отдельных его элементов.
Состоит из фиксированного соотношения химически связанных атомов. Обладает уникальными свойствами, которые отличаются от свойств отдельных его элементов. - часто проводит электричество
- податливый
- блестящий
- иногда магнитный.
- обычно непроводящий
- не податливый
- тусклый (не блестящий)
- немагнитный.

- молекулярные соединения, удерживаемые вместе ковалентными связями
- солей, удерживаемых ионными связями
- интерметаллические соединения, удерживаемые металлическими связями
- комплексов, скрепленных координатными ковалентными связями.

- Различайте и описывайте три типа материи: элементы, соединения, смеси.
- Определите чистые и нечистые материалы.
- Приведите несколько примеров элементов, смесей и соединений.
- Объясните различные свойства каждой группы материалов.
- Объясните, как инженеры-химики используют эти термины при решении задач, связанных с очисткой воды и перегонкой сырой нефти.
- Объясните, как инженеры-материаловеды и инженеры-механики используют эти термины при создании новых композитных материалов.
- Объясните, что такое металлические сплавы, и объясните значение металлических сплавов в материаловедении и материаловедении.
- Приведите примеры применения неметаллических сплавов.
- Химические технологии предоставляют людям средства изменять или модифицировать материалы и производить химические продукты.
(Оценки
9 —
12) Подробнее
Посмотреть согласованную учебную программу
Вы согласны с таким раскладом? Спасибо за ваш отзыв!
- Материалы имеют разное качество и могут быть классифицированы как натуральные, синтетические или смешанные.
 (Оценки
9 —
12) Подробнее
(Оценки
9 —
12) ПодробнееПосмотреть согласованную учебную программу
Вы согласны с таким раскладом? Спасибо за ваш отзыв!
- 20 комплектов болтов, гаек и шайб
- 9 пластиковых тарелок
- лента и маркер для нумерации посуды
- четыре примера элементов:
- алюминий (один небольшой лист фольги)
- медь (небольшой кусок проволоки или трубки)
- утюг (стружка или магнит)
- уголь (в виде чистого угольного карандаша или графита)
- четыре примера соединений:
- вода, или H 2 0 (~ 100 мл)
- поваренная соль, или NaCl (~ 10 г)
- пищевая сода или NaHCO 3 (~ 10 г)
- яичная скорлупа или морская ракушка, или CaCO 3
- четыре примера смесей, как однородных, так и гетерогенных:
- надутый мешок Ziploc (на примере воздуха)
- бутылка кока-колы или другой газированной воды
- заправка для салата (например, уксус из масла и воды)
- соленая вода
- Таблица данных, по одной на учащегося
- Блюдо 1: 4 шайбы
- Тарелка 2: 4 болта
- Блюдо 3: 4 ореха
- Тарелка 4: соедините 1 гайку с 1 болтом (4 комплекта)
- Тарелка 5: соедините 2 гайки с 1 болтом (4 комплекта)
- Тарелка 6: соедините 1 гайку и 1 шайбу с 1 болтом (4 комплекта)
- Блюдо 7: 1 шайба, 1 гайка, 1 состав, как в тарелке 5, и 1 состав, как в тарелке 6
- Тарелка 8: 2 шайбы, 1 гайка и 2 болта
- Блюдо Состав 9: 1, как в чашке 4, и состав 2, как в чашке 5.

- Разделите класс на группы по четыре ученика в каждой. Раздайте пустые таблицы данных.
- Обратите внимание каждого учащегося на Таблицу A. Наборы шайб, болтов и гаек можно использовать для передачи концепции элементов, смесей и соединений.Объясните учащимся: если они воспринимают каждую шайбу, болт и гайку как отдельный атом, то содержимое тарелок 1, 2 и 3 является элементами, потому что все они являются одним и тем же атомом и не могут быть далее сведены к более простым веществам. Содержимое тарелок 4, 5 и 6 является составным, потому что они показывают одно вещество, состоящее из двух или более различных атомов, химически связанных друг с другом, а содержимое тарелок 7, 8 и 9 является смесями, поскольку они представляют собой материалы, содержащие два или более элементов или соединений и смешиваются в любых пропорциях.

- После обсуждения таблицы A предложите каждой группе пройтись по таблице B, сравнить и сопоставить различные элементы в таблице и составить список их обсуждения. Попросите их классифицировать материалы в каждой посуде как элемент, однородную смесь, гетерогенную смесь или соединение, записав это в свои таблицы данных. Попросите учащихся обсудить свои списки. (Ожидается, что некоторые классифицируют материалы как элементы, смеси и соединения.)
- На этом этапе объясните различные типы вопросов, используя классную доску по мере необходимости.Затем снова обсудите все материалы в Таблице B и разделите их на классы элементов, смесей (гомогенные и гетерогенные) и соединения.
- Опишите три типа материи: элементы, соединения и смеси.
- Определите чистые и нечистые материалы.
- Приведите несколько примеров элементов, смесей и соединений.
- Объясните различные свойства каждой группы материалов.

- Объясните, как инженеры-химики используют эти термины при решении задач, связанных с очисткой воды и перегонкой сырой нефти.
- Объясните, как инженеры-материаловеды и инженеры-механики используют эти термины при создании новых композитных материалов.
- Объясните, что такое металлические сплавы, и объясните значение металлических сплавов в материаловедении и материаловедении.
- Приведите некоторые применения неметаллических сплавов.
- Учитель ставит по одной четырехугольной «подставке» на каждый второй стол.

- Разделите учащихся на группы по 4 человека и разместите их за столом с подставкой. (ОБЪЯВЛЕНИЕ).
- Студенты берут Chromebook и открывают форму Google «Смеси и чистые вещества».Студенты пока не отвечают.
- Учащиеся читают вопросы в Google Form и записывают выбранные ответы в своем разделе подставки, закрывая свои ответы, пока все в их группе не заполнят их.
- Каждый член группы делится своими ответами на первый вопрос и своими рассуждениями. (Обращайтесь к каждой букве по одному вопросу за раз) Группа должна прийти к консенсусу (не обязательно быть единодушным) по вопросу №1, прежде чем перейти к №2. Сделайте это для всех 5 вопросов.
- После того, как все вопросы были обсуждены и групповой консенсус достигнут и записан в центре, студенты возвращаются к своим партам и индивидуально отвечают на форму; их ответы будут основаны на групповом обсуждении, но могут не совпадать с групповым консенсусом.
- Раздайте рабочие листы: «Раздаточный материал о смесях и чистых веществах».

- Видят ли они признаки химического изменения?
- Если нет, то что это говорит вам о том, что происходит на уровне частиц мрамора и воды?
- Заполните раздел «Демо №1» в раздаточном материале, отрисовывая модели частиц до и после смешивания частиц.
- Видят ли учащиеся признаки химического изменения?
- Если нет, то что это говорит вам о том, что происходит на уровне частиц мрамора и воды?
- Завершите демонстрационный раздел № 2 раздаточного материала, отрисовывая модели частиц до и после смешивания частиц.

- Видят ли ученики признаки химического изменения?
- Если нет, то что это говорит вам о том, что происходит на уровне частиц с железом и серой?
- Заполните раздел «Демо № 3» в раздаточном материале, нарисовав модели частиц до и после смешивания частиц.
Резюме
Вещество можно разделить на две большие категории: чистые вещества и смеси. Чистое вещество — это форма вещества, имеющая постоянный состав и постоянные свойства во всем образце. Смеси представляют собой физические комбинации двух или более элементов и / или соединений. Смеси можно разделить на однородные и гетерогенные. Элементы и соединения являются примерами чистых веществ. Соединения — это вещества, состоящие из более чем одного типа атомов.Элементы — это простейшие вещества, состоящие только из одного типа атомов.
Смеси представляют собой физические комбинации двух или более элементов и / или соединений. Смеси можно разделить на однородные и гетерогенные. Элементы и соединения являются примерами чистых веществ. Соединения — это вещества, состоящие из более чем одного типа атомов.Элементы — это простейшие вещества, состоящие только из одного типа атомов.
Основные выводы
Классификация веществ (элементы, соединения, смеси) — Введение в химию
Вещества и смеси
Вещества состоят из чистых элементов или химически связанных элементов, тогда как смеси состоят из несвязанных веществ.
ЦЕЛИ ОБУЧЕНИЯ
Отличить химические вещества от смесей
КЛЮЧЕВЫЕ ВХОДЫ
Ключевые моменты
Ключевые термины
Вещества химические
В химии химическое вещество — это форма вещества, имеющая постоянный химический состав и характерные свойства.Его нельзя разделить на компоненты без разрыва химических связей. Химические вещества могут быть твердыми, жидкостями, газами или плазмой. Изменения температуры или давления могут вызывать переход веществ между различными фазами вещества.
Элемент — это химическое вещество, состоящее из определенного вида атома и, следовательно, не может быть расщеплено или преобразовано в результате химической реакции в другой элемент. Все атомы элемента имеют одинаковое количество протонов, хотя они могут иметь разное количество нейтронов и электронов.
Все атомы элемента имеют одинаковое количество протонов, хотя они могут иметь разное количество нейтронов и электронов.
Чистое химическое соединение — это химическое вещество, которое состоит из определенного набора молекул или ионов, которые химически связаны. Два или более элемента, объединенных в одно вещество в результате химической реакции, например вода, образуют химическое соединение. Все соединения являются веществами, но не все вещества являются соединениями. Химическое соединение может быть либо атомами, связанными вместе в молекулы, либо кристаллами, в которых атомы, молекулы или ионы образуют кристаллическую решетку. Соединения, состоящие в основном из атомов углерода и водорода, называются органическими соединениями, а все остальные — неорганическими соединениями.Соединения, содержащие связи между углеродом и металлом, называются металлоорганическими соединениями.
Химические вещества часто называют «чистыми», чтобы отличить их от смесей. Типичный пример химического вещества — чистая вода; он всегда имеет одни и те же свойства и одинаковое отношение водорода к кислороду, независимо от того, выделен ли он из реки или изготовлен в лаборатории. Другие химические вещества, обычно встречающиеся в чистом виде, — это алмаз (углерод), золото, поваренная соль (хлорид натрия) и рафинированный сахар (сахароза).Простые или кажущиеся чистыми вещества, встречающиеся в природе, на самом деле могут быть смесями химических веществ. Например, водопроводная вода может содержать небольшие количества растворенного хлорида натрия и соединений, содержащих железо, кальций и многие другие химические вещества. Чистая дистиллированная вода — это вещество, а морская вода, поскольку она содержит ионы и сложные молекулы, представляет собой смесь.
Другие химические вещества, обычно встречающиеся в чистом виде, — это алмаз (углерод), золото, поваренная соль (хлорид натрия) и рафинированный сахар (сахароза).Простые или кажущиеся чистыми вещества, встречающиеся в природе, на самом деле могут быть смесями химических веществ. Например, водопроводная вода может содержать небольшие количества растворенного хлорида натрия и соединений, содержащих железо, кальций и многие другие химические вещества. Чистая дистиллированная вода — это вещество, а морская вода, поскольку она содержит ионы и сложные молекулы, представляет собой смесь.
Химические смеси
Смесь — это система материалов, состоящая из двух или более различных веществ, которые смешаны, но не соединены химически.Под смесью понимается физическая комбинация двух или более веществ, в которой сохранены идентичности отдельных веществ. Смеси имеют форму сплавов, растворов, суспензий и коллоидов.
Кристаллы серы природного происхождения: Сера встречается в природе в виде элементарной серы, сульфидов и сульфатных минералов, а также в виде сероводорода. Это месторождение полезных ископаемых состоит из смеси веществ.
Это месторождение полезных ископаемых состоит из смеси веществ.Гетерогенные смеси
Гетерогенная смесь — это смесь двух или более химических веществ (элементов или соединений), в которой различные компоненты можно визуально различить и легко разделить физическими средствами.Примеры включают:
Interactive: Oil and Water : исследуйте взаимодействия, вызывающие воду и масло отделить от смеси.
Гомогенные смеси
Гомогенная смесь — это смесь двух или более химических веществ (элементов или соединений), различные компоненты которой невозможно различить визуально. Часто разделение компонентов гомогенной смеси является более сложной задачей, чем разделение компонентов гетерогенной смеси.
Различие между гомогенными и гетерогенными смесями зависит от масштаба отбора проб. В достаточно малом масштабе любую смесь можно назвать гетерогенной, потому что образец может быть размером с одну молекулу.На практике, если интересующие свойства одинаковы, независимо от того, сколько смеси взято, смесь является однородной.
Физические свойства смеси, такие как температура плавления, могут отличаться от свойств ее отдельных компонентов. Некоторые смеси можно разделить на компоненты физическими (механическими или термическими) способами.
Классифицирующее вещество (3 части): Введение в классификацию вещества как вещества или смеси веществ.Смеси описываются как гетерогенные или гомогенные. Описаны три распространенных метода разделения.
Элементы и соединения
Элемент — это материал, который состоит из одного типа атомов, а соединение состоит из двух или более типов атомов.
ЦЕЛИ ОБУЧЕНИЯ
Различать элементы и соединения и изучать методы разделения
КЛЮЧЕВЫЕ ВХОДЫ
Ключевые моменты
Ключевые термины
Элементы
Химический элемент — это чистое вещество, состоящее из одного типа атомов. У каждого атома есть атомный номер, который представляет количество протонов, которые находятся в ядре одного атома этого элемента.Периодическая таблица элементов упорядочена по возрастанию атомного номера.
Химические элементы делятся на металлы, металлоиды и неметаллы. Металлы, обычно находящиеся в левой части таблицы Менделеева:
Алюминий, железо, медь, золото, ртуть и свинец являются металлами.
В отличие от неметаллов, которые можно найти в правой части таблицы Менделеева (справа от лестницы):
Примеры элементарных неметаллов включают углерод и кислород.
Металлоиды обладают некоторыми характеристиками металлов и некоторыми характеристиками неметаллов. Кремний и мышьяк — металлоиды.
По состоянию на ноябрь 2011 г. было идентифицировано 118 элементов (последним из них был идентифицирован ununseptium в 2010 г.). Из этих 118 известных элементов только первые 98 встречаются на Земле в природе. Элементы, которые не встречаются на Земле в природе, являются синтетическими продуктами ядерных реакций, созданных человеком.80 из 98 встречающихся в природе элементов стабильны; остальные радиоактивны, что означает, что они распадаются на более легкие элементы в течение времени от долей секунды до миллиардов лет.
Периодическая таблица Менделеева: Периодическая таблица Менделеева содержит 118 элементов, включая металлы (розовый), неметаллы (синий) и металлоиды (зеленый). Водород и гелий — безусловно, самые распространенные элементы во Вселенной. Однако железо является наиболее распространенным элементом (по массе) в составе Земли, а кислород — наиболее распространенным элементом в слое, которым является земная кора.
Однако железо является наиболее распространенным элементом (по массе) в составе Земли, а кислород — наиболее распространенным элементом в слое, которым является земная кора.
Хотя вся известная химическая материя состоит из этих элементов, сама химическая материя составляет лишь около 15% вещества во Вселенной. Остальное — темная материя, загадочная субстанция, не состоящая из химических элементов. В темной материи отсутствуют протоны, нейтроны или электроны.
Соединения
Чистые образцы изолированных элементов редко встречаются в природе. В то время как 98 природных элементов были идентифицированы в образцах минералов из земной коры, лишь небольшая часть из них может быть обнаружена как узнаваемые относительно чистые минералы.Среди наиболее распространенных таких «самородных элементов» — медь, серебро, золото и сера. Углерод также обычно встречается в форме угля, графита и алмазов. Благородные газы (например, неон) и благородные металлы (например, ртуть) также можно найти в их чистых, несвязанных формах в природе. Тем не менее, большинство этих элементов находится в смесях.
Тем не менее, большинство этих элементов находится в смесях.
Когда два отдельных элемента химически объединены, т. Е. Между их атомами образуются химические связи, результат называется химическим соединением. Большинство элементов на Земле связываются с другими элементами, образуя химические соединения, такие как натрий (Na) и хлорид (Cl), которые вместе образуют поваренную соль (NaCl).Вода — еще один пример химического соединения. Два или более составляющих элемента соединения можно разделить с помощью химических реакций.
Химические соединения имеют уникальную и определенную структуру, которая состоит из фиксированного соотношения атомов, удерживаемых вместе в определенном пространственном расположении химическими связями. Химические соединения могут быть:
Чистые химические элементы не считаются химическими соединениями, даже если они состоят из двухатомных или многоатомных молекул (молекул, которые содержат только несколько атомов одного элемента, например H 2 или S 8 ).
ЛИЦЕНЗИИ И АТРИБУЦИИ
CC ЛИЦЕНЗИОННЫЙ КОНТЕНТ, ПРЕДЫДУЩИЙ РАЗДЕЛ
CC ЛИЦЕНЗИОННОЕ СОДЕРЖАНИЕ, СПЕЦИАЛЬНЫЙ АТРИБУЦИЯ
Как смеси и чистые вещества похожи
Смеси и чистые вещества похожи, потому что смеси состоят из двух или более чистых веществ.Это означает, что там, где чистые вещества обладают одним набором свойств, смеси могут иметь два или более набора одинаковых свойств на основе чистых веществ, составляющих смесь. В то же время чистое вещество также может быть смесью двух разных состояний.
Смеси могут быть однородными, что означает, что все части смеси имеют одинаковые свойства, или гетерогенными, что означает, что разные части имеют разные свойства. В обоих случаях смеси отличаются от чистых веществ, потому что компоненты смеси могут быть разделены и потому что процентное содержание каждого компонента в смеси может варьироваться.
TL; DR (слишком долго; не читал)
Смеси похожи на чистые вещества, потому что они либо гомогенные, либо гетерогенные комбинации двух или более чистых веществ. Подобно чистым веществам, смеси имеют четко определенные свойства, такие как температура кипения, вес и цвет, но, в отличие от чистых веществ, они могут быть разделены на компоненты, и их процентный состав может варьироваться.
Общие свойства
Как смеси, так и чистые вещества имеют вес, объем и цвет, а твердые вещества также имеют форму, твердость или текстуру.У чистых веществ и смесей есть точки, в которых они закипают и затвердевают, хотя смеси могут иметь несколько точек, отражающих смешанные вместе чистые вещества.
Особые случаи смесей, которые также являются чистыми веществами, представляют собой гетерогенные смеси чистого вещества, существующие в двух различных состояниях. Например, смесь колотого льда и воды является гетерогенной смесью, потому что она имеет разные свойства в зависимости от того, измеряются ли свойства куска льда или жидкой воды. Это также чистое вещество, потому что и лед, и вода представляют собой единое чистое соединение.
Это также чистое вещество, потому что и лед, и вода представляют собой единое чистое соединение.
И смеси, и чистые вещества обладают химическими свойствами, такими как воспламеняемость, токсичность, теплота сгорания и реакционная способность с другими веществами. Чистые вещества и гомогенные смеси обладают одинаковыми химическими свойствами во всем веществе или смеси, в то время как химические свойства гетерогенных смесей могут различаться в разных частях смеси.
Разные свойства
Смеси и чистые вещества различаются в том, что касается их разделения.Чистые вещества нельзя разделить на какие-либо другие вещества, в то время как смеси всегда можно разделить на два или более чистых вещества физическими средствами. Такие физические методы включают дистилляцию для отделения двух жидкостей или жидкости от твердого вещества, фильтрацию для удаления твердых веществ из жидкостей, центрифугирование для разделения материалов разного веса и декантирование для отделения жидкости от тяжелого твердого вещества.
Еще одно различие между смесями и чистыми веществами состоит в том, что химический состав чистого вещества всегда одинаков. Это может быть элемент, состоящий из отдельных атомов, или соединение, состоящее из молекул, которые объединяют несколько разных атомов.В любом случае процентное содержание каждого элемента в соединении фиксировано.
Смеси не имеют фиксированного состава. Являются ли они однородными или гетерогенными смесями, их состав может произвольно изменяться. Например, соленая вода — это раствор, представляющий собой однородную смесь соли и воды. Количество соли в воде может очень существенно. Масло и уксус образуют гетерогенную смесь, и любое количество масла можно смешать с любым количеством уксуса.
Хотя это возможное изменение является ключевым признаком смесей и отличает их от чистых веществ, тот факт, что смеси состоят из чистых веществ, остается главной основой их сходства.
Элемент, смесь, соединение — активность
Быстрый просмотр
Уровень оценки: 11 (10-12)
Требуемое время: 30 минут
Расходные материалы на группу: 2,00 доллара США
Размер группы: 4
Зависимость действий:
Тематические области: Химия
Подпишитесь на нашу рассылку новостей
Резюме
Студенты лучше понимают различные типы материалов, такие как чистые вещества и смеси, и учатся различать гомогенные и гетерогенные смеси, обсуждая набор примеров материалов, которые они используют и с которыми сталкиваются в своей повседневной жизни.Инженерное соединение
Материаловеды и инженеры-механики сосредотачиваются на понимании природы и свойств различных материалов, чтобы они могли повторять их и создавать более надежные продукты. Они используют преимущества различной прочности и способности различных материалов для создания композитов с существенно разными физическими или химическими свойствами. Понимание свойств данного материала, элемента, компонента или композита является важной частью процесса инженерного проектирования.
Цели обучения
После этого занятия студенты должны уметь:
Образовательные стандарты Каждый урок или задание TeachEngineering соотносится с одним или несколькими научными предметами K-12,
образовательные стандарты в области технологий, инженерии или математики (STEM).
Все 100000+ стандартов K-12 STEM, охватываемых TeachEngineering , собираются, обслуживаются и упаковываются сетью стандартов достижений (ASN) ,
проект D2L (www.achievementstandards.org).
В ASN стандарты имеют иерархическую структуру: сначала по источникам; например , по штатам; внутри источника по типу; например , естественные науки или математика;
внутри типа по подтипу, затем по классу, и т. д. .

Международная ассоциация преподавателей технологий и инженерии — Технология
ГОСТ
Предложите выравнивание, не указанное вышеКакое альтернативное выравнивание вы предлагаете для этого контента?
Список материалов
Поделиться со всем классом:
Рабочие листы и приложения
Посетите [www. teachengineering.org/activities/view/uoh_sep_mixtures_activity1] для печати или загрузки.
teachengineering.org/activities/view/uoh_sep_mixtures_activity1] для печати или загрузки.Больше подобной программы
Разделительные смесиСтуденты узнают, как классифицировать материалы как смеси, элементы или соединения и определять свойства каждого типа. Также вводится концепция разделения смесей, поскольку почти каждый элемент или соединение в природе находится в нечистом состоянии, таком как смесь двух или более веществ, и…
Есть железо? !! Чтобы получить представление о смесях и концепции разделения смесей, учащиеся используют сильные магниты, чтобы найти элемент железа в хлопьях хлопьев для завтрака, обогащенных железом.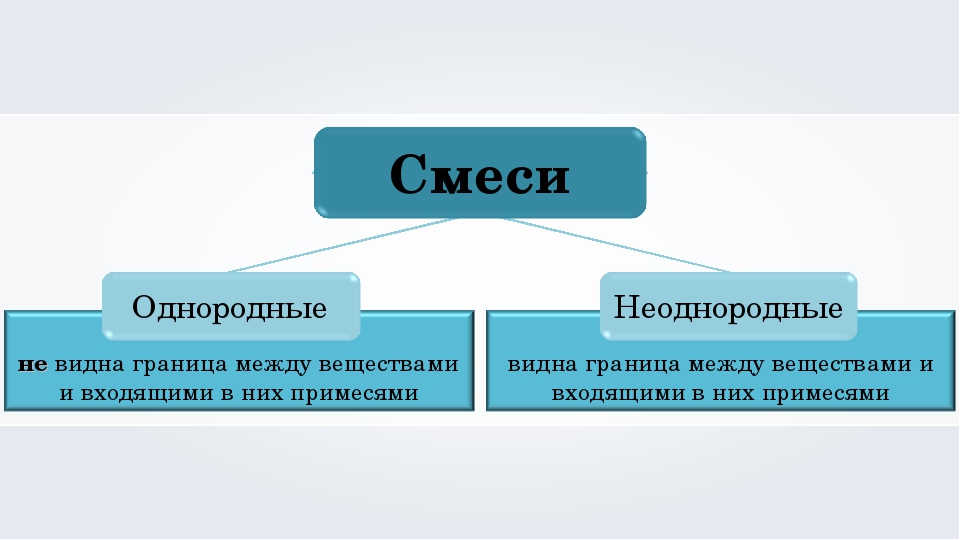 Благодаря этой деятельности они видят, как железный компонент этой гетерогенной смеси (злака) сохраняет свои свойства и…
Благодаря этой деятельности они видят, как железный компонент этой гетерогенной смеси (злака) сохраняет свои свойства и…
Введение / Мотивация
Мы все полностью окружены материей. Чтобы лучше понять этот вопрос — как он влияет на вас, как вы влияете на него и как этим можно манипулировать в наших интересах, — нам необходимо получить базовое понимание типов и свойств материи.Разнообразие материи в мире и во Вселенной поражает. Если мы хотим понять это разнообразие, мы должны начать со способа организации и описания материи.
Вся материя состоит из элементов, которые являются основными веществами, которые не могут быть расщеплены химическими средствами. Элемент представляет собой вещество, которое не может быть далее восстановлено до более простых веществ обычными способами. По сути, элемент — это вещество, состоящее из одного типа атомов.
По сути, элемент — это вещество, состоящее из одного типа атомов.
Соединение представляет собой чистое вещество, состоящее из двух или более различных атомов, химически связанных друг с другом.Это означает, что он не может быть разделен на составляющие механическими или физическими средствами, а может быть разрушен только химическим путем.
Смесь — это материал, содержащий два или более элементов или соединений, которые находятся в тесном контакте и смешиваются в любой пропорции. Например, воздух, морская вода, сырая нефть и т. Д. Составляющие смеси можно разделить физическими средствами, такими как фильтрация, испарение, сублимация и магнитная сепарация. Составляющие смеси сохраняют свой первоначальный набор свойств.Кроме того, смеси можно разделить на гомогенные и гетерогенные смеси. Гомогенная смесь имеет одинаковый однородный вид и состав по всей массе. Например, сахар или соль, растворенные в воде, спирт в воде и т. Д. Гетерогенная смесь состоит из явно разных веществ или фаз. Три фазы или состояния вещества — это газ, жидкость и твердое тело. Гетерогенная смесь не имеет однородного состава по своей массе.
Три фазы или состояния вещества — это газ, жидкость и твердое тело. Гетерогенная смесь не имеет однородного состава по своей массе.
Новые материалы относятся к числу величайших достижений всех времен и с самого начала истории играли ключевую роль в росте, процветании, безопасности и качестве жизни людей.Новые материалы открывают двери новым технологиям, будь то гражданская, химическая, строительная, ядерная, авиационная, сельскохозяйственная, механическая, биомедицинская или электротехническая инженерия.
Изучение металлических сплавов, которые представляют собой смесь различных металлов, составляет важную часть материаловедения и материаловедения. Из всех металлических сплавов, используемых сегодня, сплавы железа (сталь, нержавеющая сталь, чугун, инструментальная сталь, легированные стали) составляют самую большую долю как по количеству, так и по коммерческой стоимости.Железо, легированное углеродом в различных пропорциях, дает стали с низким, средним и высоким содержанием углерода. Что касается сталей, твердость и предел прочности стали напрямую связаны с количеством присутствующего углерода, причем повышение уровня углерода также приводит к снижению пластичности и вязкости. Добавление кремния и графитизация производят чугун. Добавление хрома, никеля и молибдена к углеродистой стали (более 10%) дает нам нержавеющую сталь.
Что касается сталей, твердость и предел прочности стали напрямую связаны с количеством присутствующего углерода, причем повышение уровня углерода также приводит к снижению пластичности и вязкости. Добавление кремния и графитизация производят чугун. Добавление хрома, никеля и молибдена к углеродистой стали (более 10%) дает нам нержавеющую сталь.
Другими важными металлическими сплавами являются сплавы алюминия, титана, меди и магния.Медные сплавы известны давно (с бронзового века), тогда как сплавы трех других металлов были разработаны относительно недавно. Сплавы алюминия, титана и магния также известны и ценятся за их высокое отношение прочности к весу и, в случае магния, за их способность обеспечивать электромагнитное экранирование. Эти материалы идеальны для ситуаций, в которых высокое отношение прочности к весу более важно, чем общая стоимость, например, в аэрокосмической промышленности и некоторых областях автомобильной техники.
Помимо металлов, полимеры и керамика также являются важной частью материаловедения.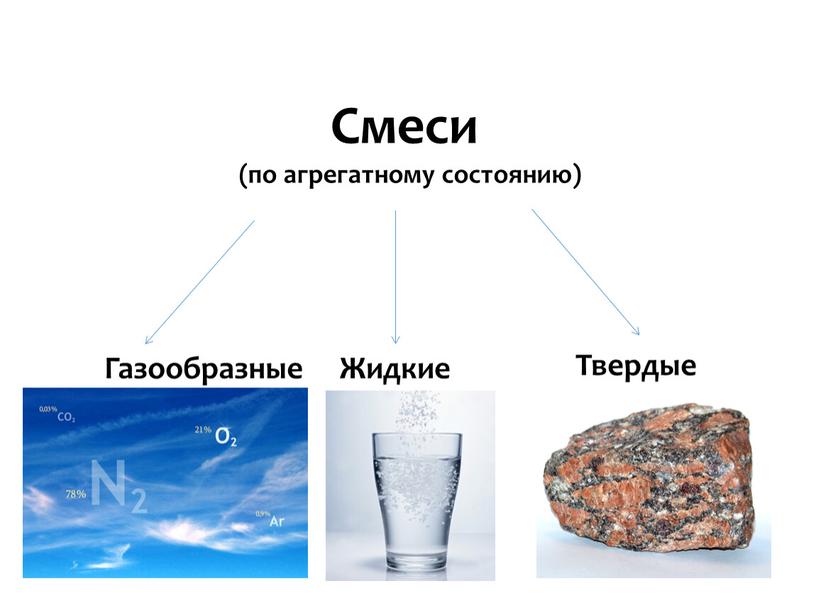 Полимеры — это сырье (смолы), используемое для производства того, что мы обычно называем пластиком. Пластмассы — это действительно конечный продукт, созданный после того, как один или несколько полимеров или добавок были добавлены в смолу во время обработки, которой затем придается окончательная форма.
Полимеры — это сырье (смолы), используемое для производства того, что мы обычно называем пластиком. Пластмассы — это действительно конечный продукт, созданный после того, как один или несколько полимеров или добавок были добавлены в смолу во время обработки, которой затем придается окончательная форма.
Еще одно промышленное применение — производство композитных материалов. Композиционные материалы — это структурированные материалы, состоящие из двух или более макроскопических фаз.Области применения варьируются от конструктивных элементов, таких как железобетон, до теплоизоляционных плиток, которые играют ключевую и неотъемлемую роль в системе тепловой защиты космического шаттла НАСА, которая защищает поверхность шаттла от тепла, возникающего при повторном входе в атмосферу Земли. . Одним из примеров является армированный углерод-углерод (RCC). Светло-серый материал выдерживает температуру входа до 1510 ° C (2750 ° F) и защищает передние кромки крыла и носовую часть космического челнока. RCC — это ламинированный композитный материал, изготовленный из графитовой вискозной ткани и пропитанный фенольной смолой.
RCC — это ламинированный композитный материал, изготовленный из графитовой вискозной ткани и пропитанный фенольной смолой.
Другие примеры можно увидеть в «пластиковых» корпусах телевизоров, сотовых телефонов и других современных устройств. Эти пластиковые корпуса обычно представляют собой композитный материал.
Процедура
Перед мероприятием
Соберите материалы и сделайте копии таблицы данных, по одной на каждого учащегося.
Приготовьте девять пластиковых тарелок с болтами, гайками и шайбами, как описано ниже. Поместите их на стол (называемый таблицей A).Обозначьте номера блюд как-нибудь, например, скотчем или маркером.
Поместите примеры элементов, соединений и смесей в другую таблицу (называемую таблицей B) и пометьте их. Вы также можете маркировать соединения их конкретной химической формулой (например, поваренная соль будет NaCl).
Со студентами
Словарь / Определения
соединение: чистое химическое вещество, состоящее из двух или более различных химических элементов.
элемент: вещество, состоящее из одного типа атома.
гетерогенная смесь: смесь, состоящая из явно разных веществ или фаз.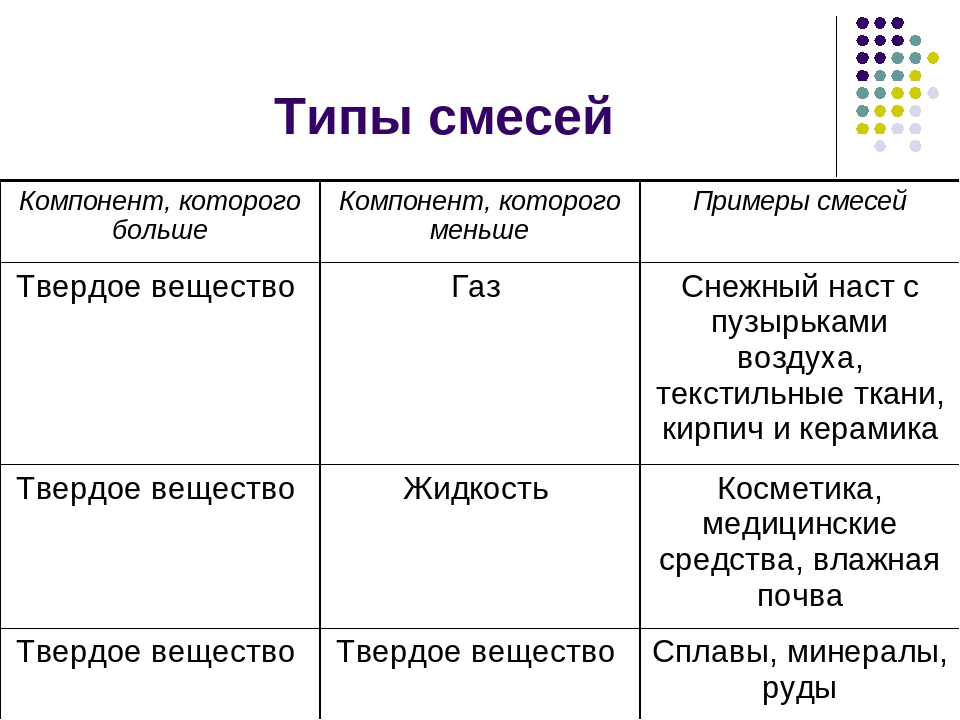
однородная смесь: смесь, имеющая одинаковый однородный внешний вид и состав по всей своей массе.
смесь: вещество, состоящее из двух или более материалов, которые химически не соединены.
раствор: однородная смесь, состоящая из двух или более веществ.
Оценка
Вопросы : задайте учащимся исследовательские вопросы в ходе заключительного обсуждения в классе.Ответы учащихся и их вклад в обсуждение раскрывают их понимание концепций деятельности. Как вариант, попросите учащихся индивидуально ответить на вопросы в форме заключительного письменного теста.
Вопросы для расследования
Авторские права
© 2013 Регенты Университета Колорадо; оригинал © 2010 Хьюстонский университетАвторы
Парния Мохаммади; Роберто ДималиватПрограмма поддержки
Национальный научный фонд GK-12 и программы исследований для учителей (RET), Университет ХьюстонаБлагодарности
Это содержимое цифровой библиотеки было разработано Инженерным колледжем Хьюстонского университета в рамках гранта Национального научного фонда GK-12 номер DGE 0840889. Однако это содержание не обязательно отражает политику NSF, и вы не должны рассчитывать на одобрение со стороны федерального правительства.
Однако это содержание не обязательно отражает политику NSF, и вы не должны рассчитывать на одобрение со стороны федерального правительства.
Последнее изменение: 23 января 2021 г.
Смеси и чистые вещества | Научно-образовательный проект — Chantier 7
План урока: смеси и чистые вещества
План урока разработан и реализован Амандой Саннити и Мелани Слип (члены команды проекта Chantier7)
Часть: Химия — смеси и чистые вещества
Предварительная проверка:
Вопрос: Обратите внимание на следующие изображения.Какое изображение лучше всего иллюстрирует раствор соленой воды на молекулярном уровне?
(Разработано членами команды проекта Chantier 7)
Инструкция:
Демо №1: Шарики в воде
Покажите ученикам, что у вас есть шарики и вода, и попросите их заполнить модели частиц для каждого из них в раздаточном материале.Добавьте шарики в стакан с водой. Попросите их рассказать о смеси после того, как вы перемешали.
Устная беседа:
Демо № 2: соль и вода
Покажите студентам, что вы собираетесь смешать соль в стакане с водой.Попросите учащихся отдельно нарисовать модели частиц для соли и воды. Добавьте соль в стакан с водой. После перемешивания спросите их, что вы думаете об этой смеси.
Устная беседа:
Демо № 3: сера и железо
Попросите учащихся наблюдать за серу и железом по отдельности, нарисовав модели частиц для каждого и описав их цвет и текстуру. Проверьте оба вещества с помощью магнита. Смешайте железо и серу до однородной массы.
Устная беседа:
Пост-тест
Вопрос: Обратите внимание на следующие изображения. Обведите стакан со смесью.
(Разработано членами команды проекта Chantier 7)
Chem4Kids.com: Содержание: Смеси
Смеси везде, куда ни глянь.
 Большинство вещей в природе представляют собой смеси. Посмотрите на скалы, океан или даже на атмосферу.Все они являются смесями, и у смесей около физических свойств, , а не химических. Это утверждение означает, что отдельные молекулы любят находиться рядом друг с другом, но их основная химическая структура не меняется, когда они входят в смесь. Если бы химическая структура изменилась, это называлось бы реакцией.
Большинство вещей в природе представляют собой смеси. Посмотрите на скалы, океан или даже на атмосферу.Все они являются смесями, и у смесей около физических свойств, , а не химических. Это утверждение означает, что отдельные молекулы любят находиться рядом друг с другом, но их основная химическая структура не меняется, когда они входят в смесь. Если бы химическая структура изменилась, это называлось бы реакцией. Когда вы видите дистиллированную воду (H 2 O), это чистое вещество. Это означает, что в жидкости есть только молекулы воды. Смесь представляет собой стакан воды с растворенными в ней другими веществами, возможно, одним из тех порошков, которые вы принимаете, если заболеете.Каждое из веществ в этом стекле сохраняет свои химические свойства. Итак, если у вас есть растворенных веществ в воде, вы можете вскипятить воду и все еще оставить растворенные вещества. Если вы добавили немного соли (NaCl) в воду, а затем вскипятили воду, соль останется в кастрюле. Соль остается, потому что для ее плавления требуется очень высокая температура (даже больше, чтобы ее вскипятить).
Соль остается, потому что для ее плавления требуется очень высокая температура (даже больше, чтобы ее вскипятить).
Если положить песок в стакан с водой, он считается смесью.Всегда можно отличить смесь, потому что каждое из веществ может быть выделено из группы разными физическими способами. Вы всегда можете вытащить песок из воды, отфильтровав воду. Если вы были заняты, вы можете просто оставить смесь песка и воды в покое на несколько минут. Иногда смеси расслаиваются сами по себе.




 Если оно чистое, это либо элемент, либо соединение. Если вещество можно разделить на элементы, это соединение.
Если оно чистое, это либо элемент, либо соединение. Если вещество можно разделить на элементы, это соединение. Следовательно, компакт-диск не является химически чистым.
Следовательно, компакт-диск не является химически чистым.  Морская вода — это однородная смесь или раствор.
Морская вода — это однородная смесь или раствор.
 Соединение состоит из двух или более типов элементов, удерживаемых вместе ковалентными или ионными связями.
Соединение состоит из двух или более типов элементов, удерживаемых вместе ковалентными или ионными связями. Состоит из фиксированного соотношения химически связанных атомов. Обладает уникальными свойствами, которые отличаются от свойств отдельных его элементов.
Состоит из фиксированного соотношения химически связанных атомов. Обладает уникальными свойствами, которые отличаются от свойств отдельных его элементов.

 (Оценки
9 —
12) Подробнее
(Оценки
9 —
12) Подробнее




