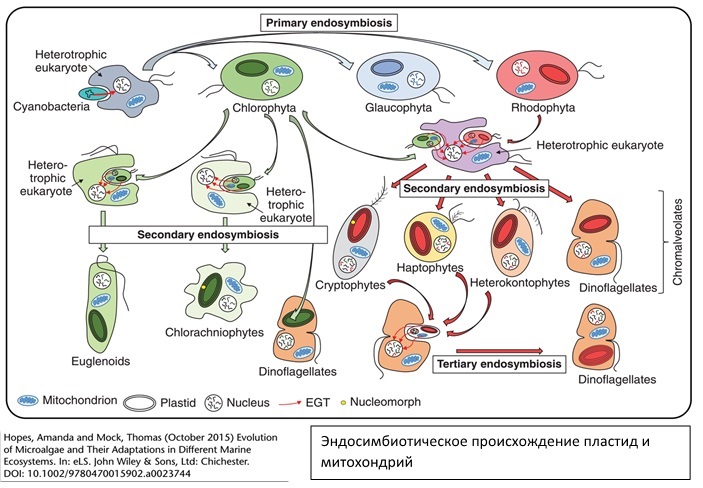
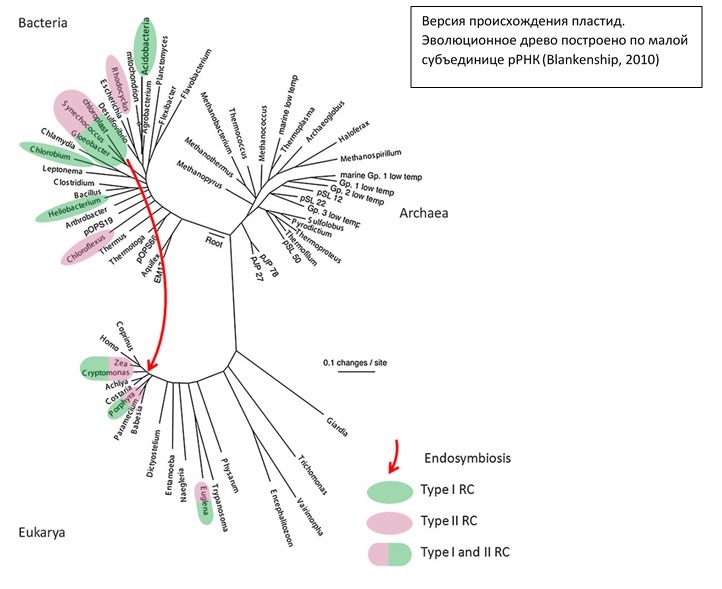
Прежде чем перейти непосредственно к рассмотрению фотосинтеза, на всякий случай напомним немного про органеллы, в которых происходит большинство реакций, связанных с этим процессом – про хлоропласты. Пластиды были приобретены предком Архепластид как минимум 1,2 млрд лет назад путем эндосимбиоза с цианобактерией (см приложения в конце статьи). Архепластиды — супергруппа в современной систематике, включающая красных, зеленых, глаукофитовых, криптофитовых (Adl et al., 2018) водорослей, группу Streptophyta (харовые в широком смысле и наземные растения) и прочие группы.
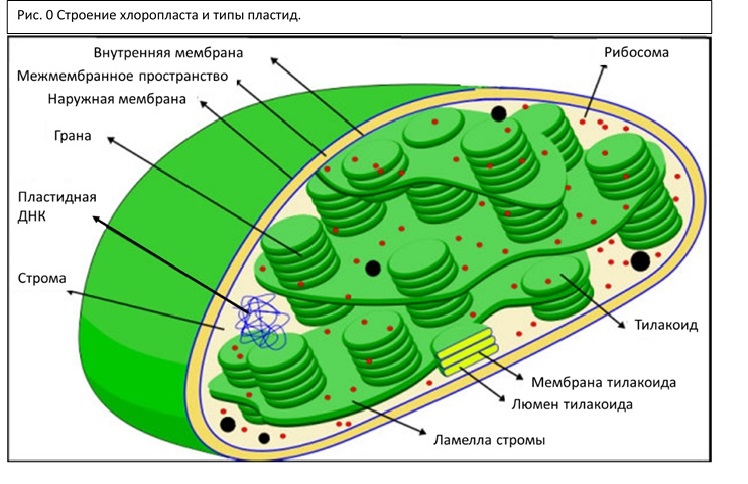 Хлоропласт, как и все пластиды – двумембранная органелла клетки. Наружная мембрана – исходно эукариотическая, по составу похожа на мембраны эндоплазматического ретикулума, она высоко проницаема для многих органических соединений и низкомолекулярных пептидов. В наружной мембране содержится большое количество рецепторов и транслокаторов, за счет которых осуществляется обмен с внешней средой.
Хлоропласт, как и все пластиды – двумембранная органелла клетки. Наружная мембрана – исходно эукариотическая, по составу похожа на мембраны эндоплазматического ретикулума, она высоко проницаема для многих органических соединений и низкомолекулярных пептидов. В наружной мембране содержится большое количество рецепторов и транслокаторов, за счет которых осуществляется обмен с внешней средой.
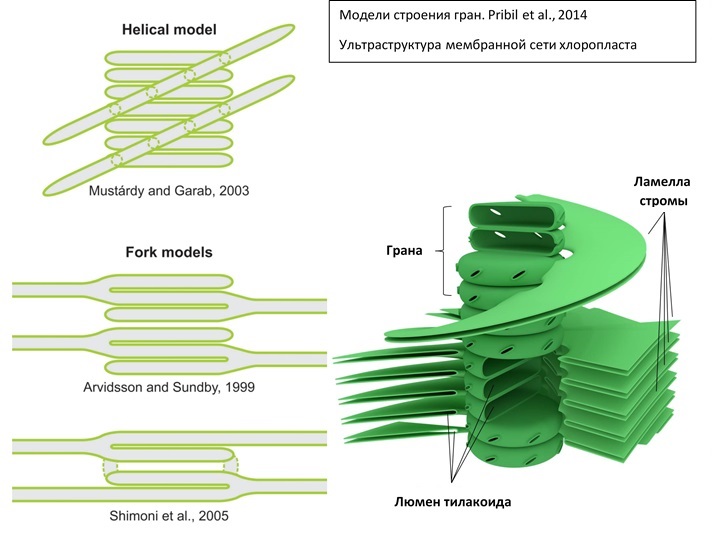
Внутренняя мембрана, о которой речь будет идти и далее, обладает высокой избирательностью проницаемости, контролирует транспорт, является основным барьером, разделяющим внутреннее содержимое пластиды от цитоплазмы и разграничивающим различные компартменты самого хлоропласта. Внутренняя мембрана образует обширную мембранную сеть внутри хлоропласта, образуя тилакоиды (небольшие мембранные пузырьки), часто собранные в стопки или граны и крупные свободные ламеллы стромы. Внутреннее пространство тилакоида и ламеллы называется люменом.
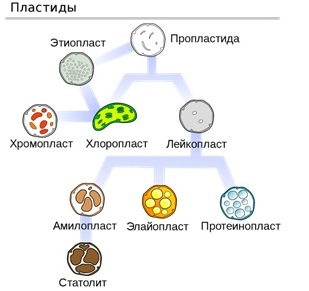
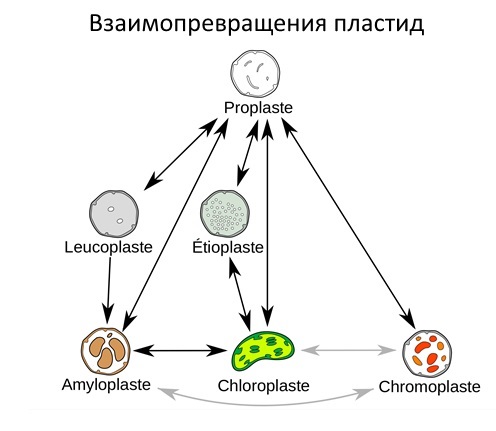
В высших растениях может быть большое разнообразие различных пластид, но в одной клетке только один тип. При этом многие типы пластид могут обратимо друг в друга превращаться.
Фотосинтез – один из основополагающих процессов биосферы, это наиболее мощный механизм преобразования солнечной энергии в энергию химических связей, что делает его роль ключевой в биоэнергетике как растений, так и животных.
Световая фаза фотосинтеза включает в себя разнообразные процессы, основная цель которых – преобразование солнечной энергии в энергию химических связей. Эти процессы локализованы на мембране тилакоида. По сути люмен тилакоида аналогичен межмембранному пространству митохондрии. Как и внутренняя мембрана митохондрии оболочка тилакоида представляет собой сопрягающую мембрану. Сопрягаются и в том и другом случае процессы перекачки протонов и перенос электронов по электрон-транспортной цепи. Далее за счет градиента протонов синтезируется АТФ, а электроны восстанавливают NADP+ до NAPDH+H+.
 Вообще, в клетках есть две основные формы энергии – энергия химических связей (АТФ, например) и энергия градиентов (градиент протонов у растений, натрия – у животных), с которой неразрывно связана разность потенциалов и для создания которой необходима мембрана с жестко контролируемой проницаемостью. Не очень корректно, но использование энергии градиента можно сравнить с принципом работы гидроэлектростанций, где за счет разницы давления воды раскручиваются турбины и вырабатывается электричество. Эти две формы энергии обязательно присутствуют в любой живой клетке, а также могут быть конвертированны одна в другую. На этом факте основаны многие задания на олимпиадах, которые могут звучать как-то так:
Вообще, в клетках есть две основные формы энергии – энергия химических связей (АТФ, например) и энергия градиентов (градиент протонов у растений, натрия – у животных), с которой неразрывно связана разность потенциалов и для создания которой необходима мембрана с жестко контролируемой проницаемостью. Не очень корректно, но использование энергии градиента можно сравнить с принципом работы гидроэлектростанций, где за счет разницы давления воды раскручиваются турбины и вырабатывается электричество. Эти две формы энергии обязательно присутствуют в любой живой клетке, а также могут быть конвертированны одна в другую. На этом факте основаны многие задания на олимпиадах, которые могут звучать как-то так:
Рассчитайте сколько молекул АТФ может синтезироваться в митохондрии в аэробных условиях при полном окислении сахарозы?
Электронно транспортная цепь со сложным механизмом сопряжения возникла не сразу. Но рассмотрим все по порядку и начнем с предыстории.
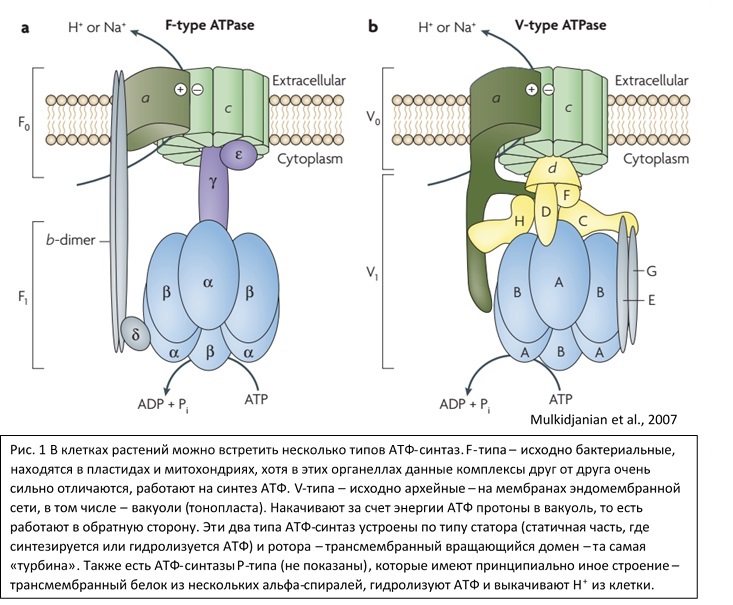
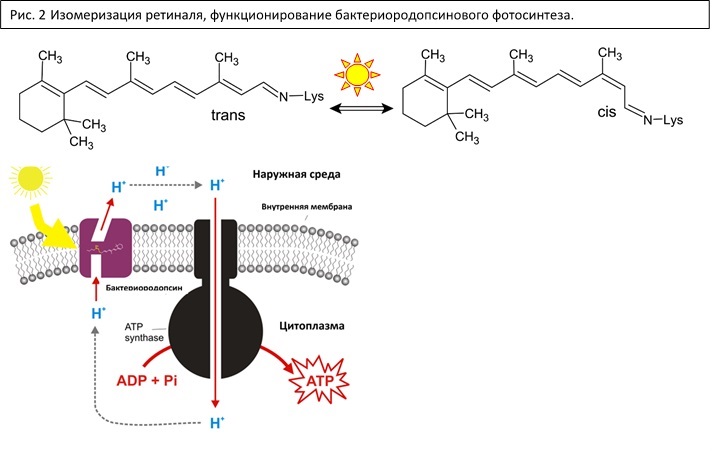
Основными пигментами, участвующими в реакциях световой фазы являются хлорофиллы у эукариотических фотосинтезирующих организмов или бактериохлорофиллы у прокариотических, но самый первый механизм преобразования энергии света не задействовал эти пигменты. Речь про родопсиновый фотосинтез, встречаемый у группы архей Euryarchaeota (Halobacteria). Этот тип примечателен своим потрясающе простым устройством. Ключевым ферментом является собственно пигмент-белковый комплекс – бактериородопсин, в котором содержится ретиналь. Да, именно тот самый, что и в наших зрительных рецепторах. Под действием света ретиналь претерпевает цис-транс переход, что приводит к конформационным изменениям бактериородопсина и переносу протона из цитоплазмы наружу. Таким образом создается протонный градиент, который далее используется для синтеза АТФ на АТФ-синтазе (в данном случае не обычная, а архейного типа, похожая на вакуолярную АТФ-синтазу V-типа у растений). Прекрасный механизм, ничего лишнего!
Хлорофилльный фотосинтез появился позднее. Несмотря на все разнообразие хлорофиллов, только хлорофилл а и бактериохлорофилл а, располагаясь в димерах, могут непосредственно преобразовывать энергию света.
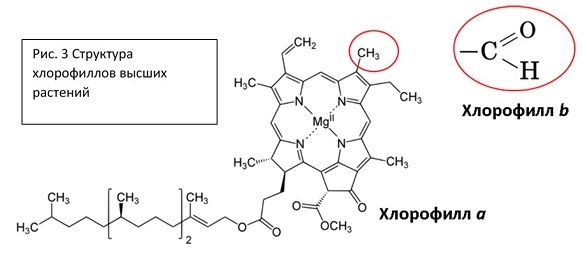 Все хлорофиллы имеют тетрапиррольную структуру порфирина, которая преимущественно и определяет свойства молекулы. Молекула плоская, несет систему сопряженных двойных связей, формирующих π-электронное облако, благодаря чему может довольно легко вступать в процессы фотоокисления (отдавать электрон) или фотовосстановления (принимать электрон). В центре хелатирован магний, который сильно влияет на свойства молекулы – выравнивает и перераспределяет электронную плотность по кольцам порфирина, образует координационные связи с молекулами воды, аминокислотными остатками, участвует в формировании димерных структур реакционных центров фотосистем. Также имеются полярные периферические группы, которые определяют взаимодействия хлорофиллов с различными компонентами хлоропласта. У многих хлорофиллов помимо тетрапиррольного кольца есть еще фитольный хвост. Фитол – дитерпеноид, содержащий 20 атомов углерода. Фитол практически не влияет на спектральные свойства хлорофилла, но определяет его взаимодействие с гидрофобной фракцией мембран и белков.
Все хлорофиллы имеют тетрапиррольную структуру порфирина, которая преимущественно и определяет свойства молекулы. Молекула плоская, несет систему сопряженных двойных связей, формирующих π-электронное облако, благодаря чему может довольно легко вступать в процессы фотоокисления (отдавать электрон) или фотовосстановления (принимать электрон). В центре хелатирован магний, который сильно влияет на свойства молекулы – выравнивает и перераспределяет электронную плотность по кольцам порфирина, образует координационные связи с молекулами воды, аминокислотными остатками, участвует в формировании димерных структур реакционных центров фотосистем. Также имеются полярные периферические группы, которые определяют взаимодействия хлорофиллов с различными компонентами хлоропласта. У многих хлорофиллов помимо тетрапиррольного кольца есть еще фитольный хвост. Фитол – дитерпеноид, содержащий 20 атомов углерода. Фитол практически не влияет на спектральные свойства хлорофилла, но определяет его взаимодействие с гидрофобной фракцией мембран и белков.
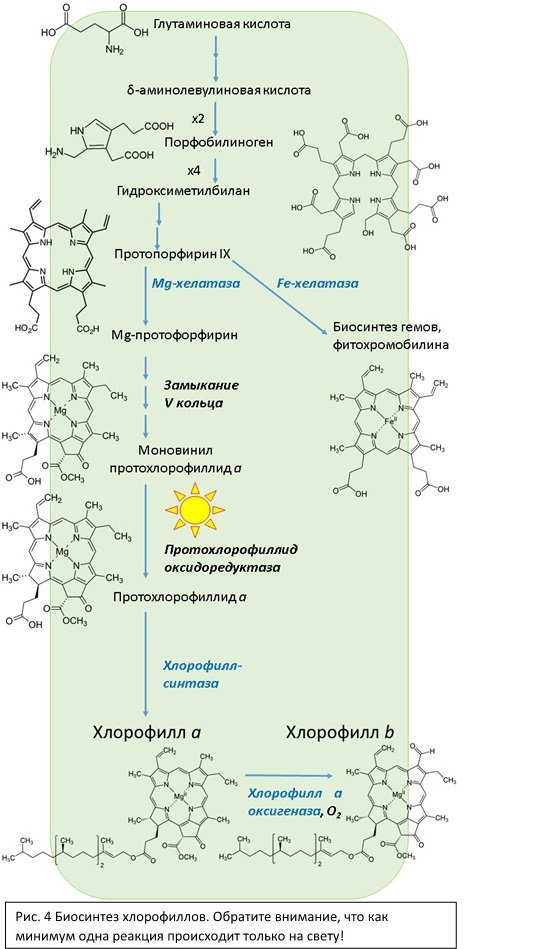
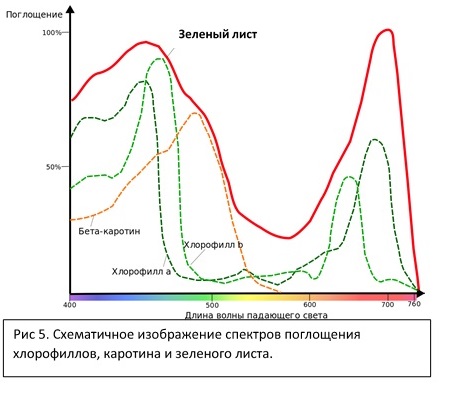
Хлорофилл а является основным фотосинтетическим пигментом эукариотических фотосинтезирующих организмов, цианобактерий (у которых это единственная форма хлорофилла). Максимумы поглощения приблизительно 430 и 670 нм, то есть в синей и красной области. Между этими максимумами «зеленый провал», в котором хлорофиллы практически не поглощают.
Хлорофилл b – дополнительный пигмент, характерный для высших растений, выполняет в основном светособирающую роль. Красноволновый максимум поглощения несколько сдвинут в коротковолновую область, благодаря чему «зеленый провал» несколько сужается.
Хлорофилл d, f – цианобактериальные. В некоторой литературе можно найти, что хлорофилл d есть у красных водорослей, но это ошибка.
Хлорофилл e – по некоторым довольно старым источникам, имеется у одного лишь представителя Xanthophyceae.
Бактериохлорофиллов тоже много (a, b, c, d, e, f, g), основной – бактериохлорофилл a. Для бактериохлорофиллов характерны длинноволновые максимумы поглощения.
Тетрапиррольные пигменты могут быть не только циклические, но и линейные, называемые фикобилинами. Различают фикоэритрин, фикоцианин и аллофикоцианин (по увеличению длины волны максимумов поглощения). Фикобилины есть, например, у цианобактерий, красных и криптофитовых водорослей, где они выполняют роль светособирающих антенн. У цианобактерий и красных водорослей — фикобилипротеины.
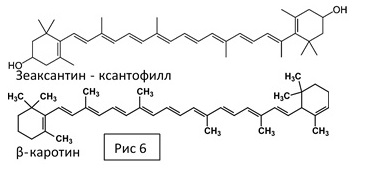 Помимо хлорофиллов в пигментных системах в обязательном порядке присутствуют каротиноиды – кислород-содержащие (ксантофиллы) и бескислородные (каротины). Это изопреноидные соединения с 40 атомами углерода, биосинтез которых происходит в пластидах. Благодаря длинной цепи сопряженных связей каротиноиды способны поглощать свет, передавать энергию возбуждения хлорофиллам, а также диссипировать ее в тепло. Этим частично объясняются фотопротекторные функции этих пигментов. Каротиноиды также могут забирать от хлорофиллов избыток энергии, тушить триплетный хлорофилл, защищать от активных форм кислорода (синглетный кислород, супероксидрадикал) и органических радикалов. Помимо этого, каротиноиды участвуют в структуризации мембран, определяют конформацию пигмент-белковых комплексов, придают окраску различным частям растений.
Помимо хлорофиллов в пигментных системах в обязательном порядке присутствуют каротиноиды – кислород-содержащие (ксантофиллы) и бескислородные (каротины). Это изопреноидные соединения с 40 атомами углерода, биосинтез которых происходит в пластидах. Благодаря длинной цепи сопряженных связей каротиноиды способны поглощать свет, передавать энергию возбуждения хлорофиллам, а также диссипировать ее в тепло. Этим частично объясняются фотопротекторные функции этих пигментов. Каротиноиды также могут забирать от хлорофиллов избыток энергии, тушить триплетный хлорофилл, защищать от активных форм кислорода (синглетный кислород, супероксидрадикал) и органических радикалов. Помимо этого, каротиноиды участвуют в структуризации мембран, определяют конформацию пигмент-белковых комплексов, придают окраску различным частям растений.
Что же все-таки такое антенна? Антенна – совокупность пигмент-белковых комплексов, способная улавливать свет и передавать энергию к реакционному центру.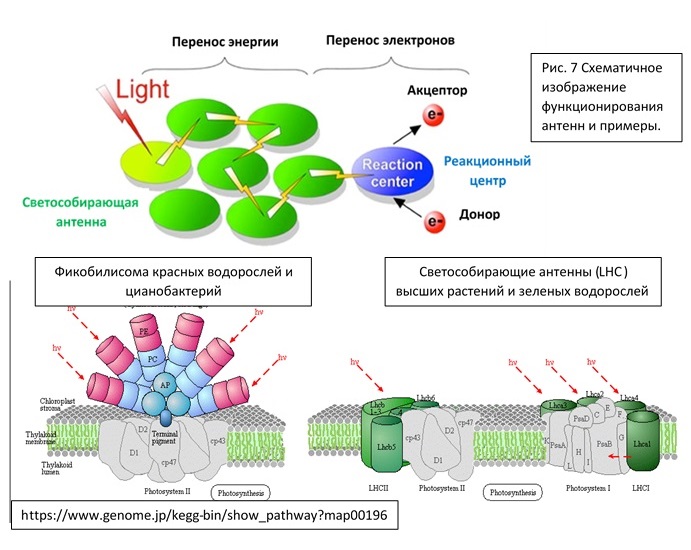
Основная функция – увеличить площадь сбора световой энергии. В антеннах пигменты (хлорофиллы и каротиноиды) очень тесно друг с другом взаимодействуют, что позволяет им обмениваться энергией. Говоря очень упрощенно, по антеннам перемещается экситон – некоторое возбужденное состояние, которое передается от пигмента с большей энергией возбуждения к пигменту с меньшей, попадая в конечном счете на реакционный центр, который таким образом выступает в качестве энергетической ловушки. Все процессы происходят очень быстро – за пикосекунды. Если говорить чуть подробнее, то в антеннах между хлорофиллами энергия передается путем образования переменного электрического поля между двумя пигментами, предлагается механизм осциллирующего диполя. Можно это представить на некотором механическом аналоге – в виде связанных колебаний.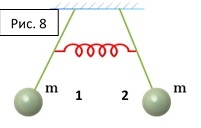
Представьте два шарика на упругих нерастяжимых подвесах, соединенных неким передаточным механизмом. Если начать периодически колебать один шарик, то со временем колебания передадутся на другой. На рисунке 9 схематично изображены процессы происходящие при этом на электронных орбиталях молекул.
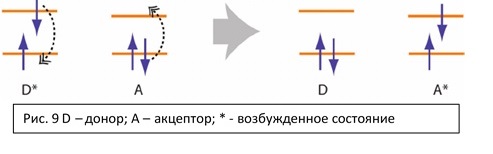 Миграция энергии от каротиноида к хлорофиллу может идти и иным механизмом, что связано с особенностями возбуждения каротинов и стабильностью их возбужденных состояний.
Миграция энергии от каротиноида к хлорофиллу может идти и иным механизмом, что связано с особенностями возбуждения каротинов и стабильностью их возбужденных состояний.
Таким образом, в антеннах передается именно энергия, а все электроны остаются связанными со своими молекулами. В реакционном центре же под действием этой энергии происходит разделение зарядов в димере хлорофилла а и выбитый электрон поступает в электрон-транспортную цепь, на акцептор (см рисунок 7). А образовавшаяся «дырка» на пигменте реакционного центра восполняется за счет притока электронов от донора.
Существует несколько механизмов, каким образом восполнить ушедший электрон, в качестве доноров могут выступать различные соединения. Например, сероводород у анаэробных фотосинтезирующих зеленых серных бактерий, вода у эукариот и цианобактерий или пул хинолов, который в свою очередь принял электроны от фотосистемы. Но обо всем по порядку.
Электрон-транспортная цепь (ЭТЦ) хлоропласт высших растений состоит из двух фотосистем (ФС I и ФС II), цитохромного комплекса (цитохром b6/f), пула хинонов, пластоцианина, светособирающих антенн и некоторых стромальных белков.
В ЭТЦ есть несколько типов переносчиков.
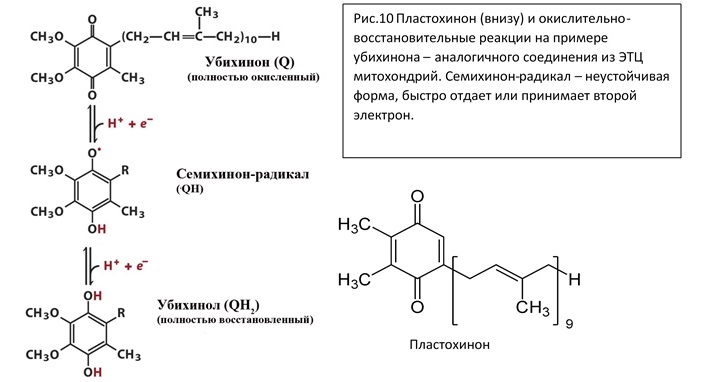
Хиноны (окисленная форма, восстановленная – хинол) – гидрофобные двуэлектронные, располагаются внутри мембраны. Могут находиться в трех состояниях окисленности-восстановленности (редокс статус). Переносят электроны со второй фотосистемы на цитохромный комплекс. Помимо электронов переносят также и протоны, благодаря чему формируется протонный градиент.
Пластоцианин – медь-содержащий одноэлектронный белковый переносчик, располагающийся в люмене тилакоида.
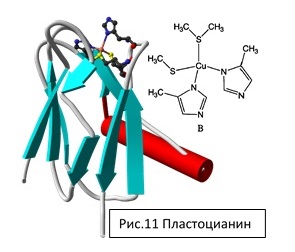
Гемы – одноэлектронные переносчики, кофакторы цитохромов.
Железосерные кластеры – комплексы, состоящие из элементов железа и серы. Различаются по геометрии, числу и соотношению железа и серы. Непосредственно связаны с аминокислотами белков – цистеином и гистидином чаще всего. Переносят один (Fe-S, 2Fe-2S) или 2 электрона (4Fe-4S) за счет изменения степени окисленности железа. Железосерные кластеры имеются в цитохромном комплексе (белок Риске), в первой фотосистеме и в ферредоксине. Ферредоксин – стромальный белок, принимающий электроны от первой фотосистемы и передающий их на NADP+.
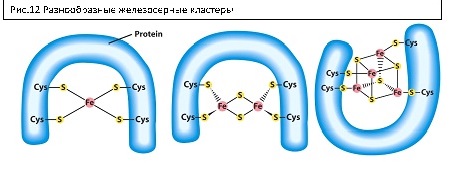 Прежде чем поговорить об ЭТЦ высших растений, необходимо сперва упомянуть прототипы ее компонентов.
Прежде чем поговорить об ЭТЦ высших растений, необходимо сперва упомянуть прототипы ее компонентов.
Вторая фотосистема берет свое начало от фотосистемы пурпурных бактерий.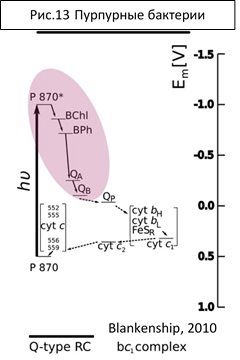
Система димерная (на рисунке 13 не показано), состоит из двух очень похожих белков (L и M), которые несут в себе одинаковые по переносчикам транспортные цепи (бактериохлорофилл-бактериофеофитин-хинон), но работает только цепь на L белке. Еще существует крупная субъединица H, которая защищает ЭТЦ внутри фотосистемы от внешних акцепторов. Пигментом в реакционном центре здесь является P870. Первичный акцептор электронов – бактериофеофитин (хлорофилл без магния, но с двумя протонами вместо него). Здесь же участвует бактериохлорофилл (BChl800). С бактериофеофитина электрон поступает на хиноны. QA (QLMQ) – связанный хинон, QB (QMPQ) – свободный, выходит в мембрану и несет два электрона к цитохромному комплексу, где окисляется, отдавая электроны и выносит два протона в люмен. Тут не b6/f цитохром, а bc1, как в митохондриях. С цитохрмного комплекса электроны поступают на подвижный люменальный цитохром с, который возвращает их на реакционный центр.
Этот тип фотосинтеза позволяет накачать протоны и синтезировать АТФ но не дает восстановительного эквивалента (NADPH), который пурпурным бактериям приходится образовывать, используя обратный транспорт электронов по ЭТЦ. Но это уже совсем другая история.
Фотосистема зеленых серных бактерий является прообразом первой фотосистемы эукариот и цианобактерий.
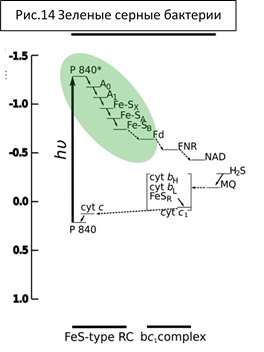 Пигмент в данном случае – Р840. Первичный акцептор – бактериохлорофилл A0, далее электрон идет на филлохинон А1 (витамин К1) и на железосерные кластеры Fx, FA, FB, с них на ферредоксин (ФД). Ферредоксин взаимодействует с фд-NADPH-оксидоредуктазой которая восстанавливает NADPH электронами с ФД. В данном случае электрон израсходован на образование восстановительного эквивалента, но надо также, как и в предыдущем случае, заполнить образовавшуюся «дырку» на пигменте реакционного центра. У зеленых серных фотосинтезирующих бактерий донором является сероводород, который, отдавая электроны, окисляется до серы или сульфатов. Отобранные от h3S электроны поступают через хинолы на цитохромный комплекс (снова bc1), а затем переносятся цитохромом с на реакционный центр. В данном случае, в противоположность тому, что имеется у пурпурных, идет образование NADPH, но не АТФ. Позволить себе получать сразу и NADPH и АТФ могут только эукариоты и цианобактерии, которые, вообще говоря, и дали начало пластидам.
Пигмент в данном случае – Р840. Первичный акцептор – бактериохлорофилл A0, далее электрон идет на филлохинон А1 (витамин К1) и на железосерные кластеры Fx, FA, FB, с них на ферредоксин (ФД). Ферредоксин взаимодействует с фд-NADPH-оксидоредуктазой которая восстанавливает NADPH электронами с ФД. В данном случае электрон израсходован на образование восстановительного эквивалента, но надо также, как и в предыдущем случае, заполнить образовавшуюся «дырку» на пигменте реакционного центра. У зеленых серных фотосинтезирующих бактерий донором является сероводород, который, отдавая электроны, окисляется до серы или сульфатов. Отобранные от h3S электроны поступают через хинолы на цитохромный комплекс (снова bc1), а затем переносятся цитохромом с на реакционный центр. В данном случае, в противоположность тому, что имеется у пурпурных, идет образование NADPH, но не АТФ. Позволить себе получать сразу и NADPH и АТФ могут только эукариоты и цианобактерии, которые, вообще говоря, и дали начало пластидам.
В хлоропластах и цианобактериях ЭТЦ представляет собой комбинирование двух описанных бактериальных систем (рисунок 15). 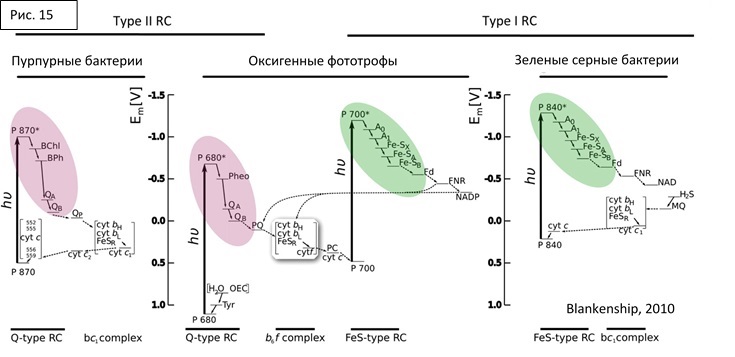
Окислительно-восстановительный (редокс) потенциал – способность химического вещества присоединять электроны. Выражается в милливольтах. Чем более отрицательные значения принимает редокс потенциал, тем лучшим донором электронов является вещество, чем более положительный – более сильным акцептором. Обратите внимание, что на схемах (рисунки 13-16) ось ординат отображает восстановительную способность, поэтому отрицательные значения сверху.
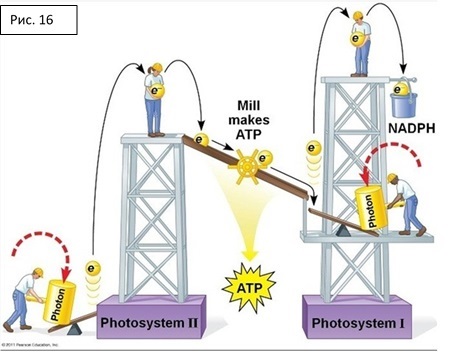
На рисунках 16 и 17 схематично показана общая логика процессов, происходящих в ЭТЦ. Пигмент ФСII, Р680 – очень сильный окислитель, но его восстановительная сила в возбужденном состоянии Р680* относительно невысока, ее не хватит для восстановления NADPH. Пигмент второй фотосистемы, Р700 – не очень сильный окислитель, но Р700* имеет очень высокую восстановительную способность. Таким образом, роль первой фотосистемы при функционировании полной ЭТЦ – восстановление NADPH. Происходит это после возбуждения P700 вспышкой света («Photon» на рисунке) и ухода электрона по ЭТЦ первой фотосистемы на ферредоксин. Ушедший электрон восполняется электроном, выбитым из второй фотосистемы. По пути переноса электронов от ФСII к ФСI совершается работа – перекачивание протонов, создание градиента, за счет которого далее синтезируется АТФ. 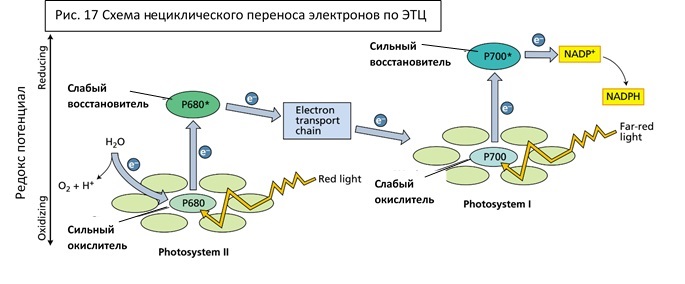
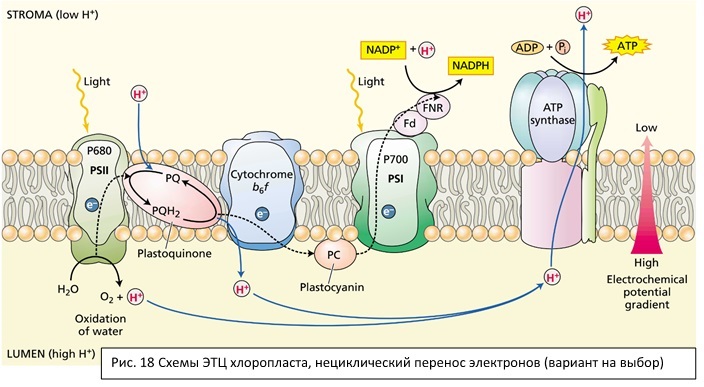
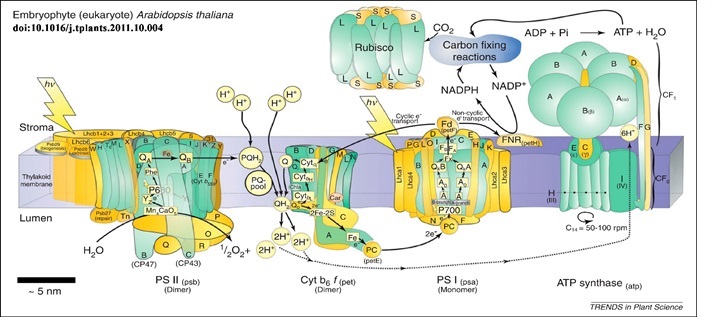
Таким образом, электроны от ФСII восстанавливают Р700+ ФСI, и снова возникает проблема донора электронов, уже для второй фотосистемы. Чисто теоретически донором может быть все тот же сероводород, как у зеленых серных бактерий. Сероводород довольно легко окислить и продукт окисления довольно инертен и неопасен. Но сероводорода мало на Земле. А вот воды много. При этом вода – очень плохой восстановитель, очень трудно отобрать у нее электроны. Более того, продукты окисления высокоактивны и могут вызывать повреждения. Но фактор распространения оказался решающим, вода используется в качестве донора электронов: 2h3O 4e-+4H++O2. Именно очень сильный окислительный потенциал P680 позволяет существовать оксигенному фотосинтезу, который появился где-то 2,1-2,5 млрд лет назад у цианобактерий. Помимо огромного преимущества, для самих фотосинтетиков — это событие сыграло одну из ключевых ролей в формировании атмосферы, что называется кислородной катастрофой, именно оксигеный фотосинтез определил создание условий, пригодных для развития сложных форм жизни на Земле.
Сам процесс окисления воды происходит в марганцевом кластере – сложноустроенном белковом комплексе, в реакционном центре которого содержится, помимо прочего, 4 марганца, хлор и кальций (см рис 19), связанных с аминокислотными остатками. Кластер может постепенно отдавать по одному электрону на реакционный центр ФСII, восстанавливая пигмент Р680+, отдавший электрон в ЭТЦ. Посредником между Р680 и марганцевым кластером является Tyr Z (тирозин-161 белка D1 второй фотосистемы). Марганцевый кластер, изменяя поочередно степень окисления, может отдавать последовательно 4 электрона, которые далее восполняются за счет окисления двух молекул воды.
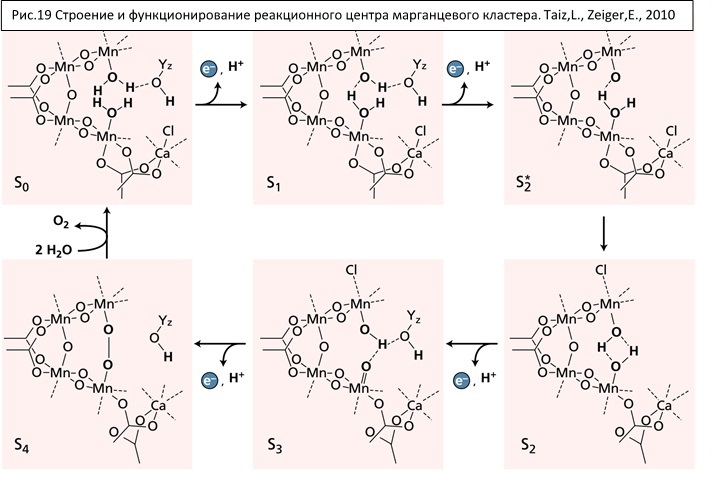
Марганцевый кластер располагается с люменальной стороны тилакоида, соединен с донорной частью ФСII. Обратите внимание, что в результате работы Mn-кластера в люмене также накапливаются протоны.
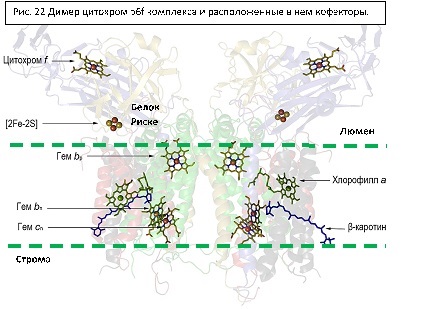
Вторая фотосистема (рис 20) состоит из множества белков – более 20, среди них есть белки, в которых непосредственно происходят фотохимические процессы (D1 и D2), комплексы внутренних и внешних антенн и большое количество других, необходимых для сборки, стабилизации, регулирования. Главный белок – D1, на нем происходят практически все основные события – разделение зарядов, формирование донорно-акцепторных пар. Структурно на него очень похож D2, с которым они находятся в димере. Р680 расположен на стыке между двумя этими белками, образуя связь с аминокислотами одного и второго. Всего реакционный центр ФС II несет 2 β-каротина, 2 феофитина, 6 хлорофиллов а.
На D1 и D2 есть похожие цепи электронных переносчиков, но функционирует только та, что на D1. С Р680* электрон передается на первичный акцептор – феофитин, с него на связанный хинон QA, с него на QB, который выходит в мембрану, в пул пластохинонов и далее может идти к цитохромному комплексу.
Забегая вперед, скажем про еще один (альтернативный) путь восстановления P680+. Он реализуется в том случае, если по каким-либо причинам перекрывается перенос электронов по ЭТЦ или нарушается работа водоокисляющего комплекса. В данном случае электрон с феофитина и/или с хинола поступает на цитохром b559, откуда далее идет к хлорофиллу ChlD и/или ChlZ и затем через каротин на P680+.
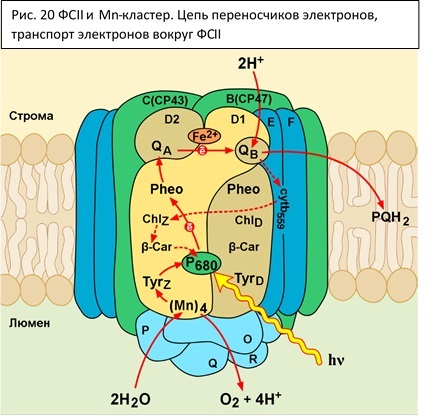
CP43 (=psbC) и CP47(=psbB) – внутренние светособирающие антенны фотосистемы. В них содержится несколько хлорофиллов а и β-каротины. CP29,26,24 (=Lhcb4,5,6) – внешние антенны, в них содержатся хлорофиллы а и b, лютеины, неоксантины и виолаксантины (которые превращаются в зеаксантин в виолаксантиновом цикле) . Также существует подвижный светособирающий комплекс (ССК II). Состоит из трех субъединиц (Lhcb1,2,3). При тусклой и нормальной освещенности ССК II находится рядом с ФСII, при избыточном освещении ССК II отходит и может присоединяться к ФС I. 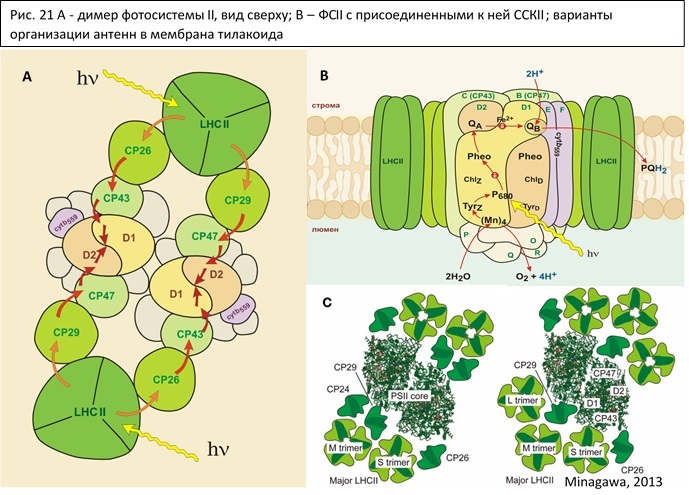
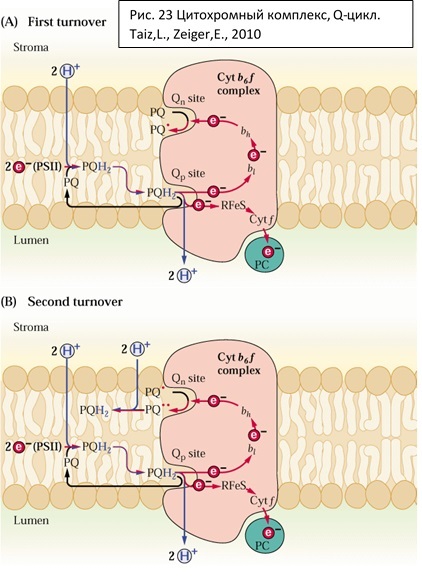
 Цитохром b6f в общем похож на митохондриальные и бактериальные bc1. Это димерный комплекс, в котором есть два сайта связывания пластохинонов (Qp – со стороноы люмена, здесь окисляется пластохинол; Qn – со стороны стромы, в нем восстанавливается пластохинон). Также имеются цитохромы – низкопотенциальный bL и высокопотенциальный bH, цитохром f – связь с пластоцианином. Подробно прочитать про функционирование можно в Википедии, статья очень хорошо написана (https://ru.wikipedia.org/?oldid=94460479). Если коротко, то основные происходящие в комплексе процессы следующие. Пластохинол связывается в Qp сайте, окисляется, превращаясь в семихинон, при этом первый протон выходит в люмен. Первый электрон идет по так называемой высокопотенциальной ветви на белок Риске – 2Fe2S – содержащий белок, который, претерпевая конформационные изменения после акцептирования электрона, передает его на цитохром f. После передачи электрона на белок Риске этот путь временно перекрывается и следующий электрон уходит от семихинона, окисляя его до пластохинона (второй протон уходит в люмен), идет по цепи цитохромов – низкопотенциального и высокопотенциального, откуда сбрасывается на пластохинон, связанный в Qn сайте, восстанавливая его до семихинона (протон берется из стромы). Из Qp пластохинон уходит обратно в мембрану и в Qp связывается следующий пластохинол. Снова повторяются описанные процессы окисления и переноса электронов, и уже в Qn – сайте семихинон восстанавливается до пластохинола, который может уйти в мембранный пул, а затем связаться в Qp сайте. Описанные процессы называются Q-циклом (рис. 23). Можно представить все в виде уравнения:
Цитохром b6f в общем похож на митохондриальные и бактериальные bc1. Это димерный комплекс, в котором есть два сайта связывания пластохинонов (Qp – со стороноы люмена, здесь окисляется пластохинол; Qn – со стороны стромы, в нем восстанавливается пластохинон). Также имеются цитохромы – низкопотенциальный bL и высокопотенциальный bH, цитохром f – связь с пластоцианином. Подробно прочитать про функционирование можно в Википедии, статья очень хорошо написана (https://ru.wikipedia.org/?oldid=94460479). Если коротко, то основные происходящие в комплексе процессы следующие. Пластохинол связывается в Qp сайте, окисляется, превращаясь в семихинон, при этом первый протон выходит в люмен. Первый электрон идет по так называемой высокопотенциальной ветви на белок Риске – 2Fe2S – содержащий белок, который, претерпевая конформационные изменения после акцептирования электрона, передает его на цитохром f. После передачи электрона на белок Риске этот путь временно перекрывается и следующий электрон уходит от семихинона, окисляя его до пластохинона (второй протон уходит в люмен), идет по цепи цитохромов – низкопотенциального и высокопотенциального, откуда сбрасывается на пластохинон, связанный в Qn сайте, восстанавливая его до семихинона (протон берется из стромы). Из Qp пластохинон уходит обратно в мембрану и в Qp связывается следующий пластохинол. Снова повторяются описанные процессы окисления и переноса электронов, и уже в Qn – сайте семихинон восстанавливается до пластохинола, который может уйти в мембранный пул, а затем связаться в Qp сайте. Описанные процессы называются Q-циклом (рис. 23). Можно представить все в виде уравнения:
2Cytf3++2H++2PQh3+PQ +2e-2PQ+PQh3+4H++2Cytf2+
Сократив хиноны и хинолы, но не сокращая протоны, так как они по разные стороны от мембраны, получим:
2Cytf3++2H++PQh3 +2e-PQ+4H++2Cytf2+
Таким образом, если рассматривать процесс в динамике, получается, что на каждый пластохинол, окисленный в Qp сайте через мембрану переносится 4 протона и восстанавливается 2 цитохрома f. А цитохром f передает электрон на пластоцианин. Значит, на каждый окисленный пластохинол к первой фотосистеме приходит два электрона.
 Пластоцианин, приняв электрон от цитохрома f, (Cu2+Pc + e− → Cu+Pc), перемещается в люменальном пространстве и передает e− на I фотосистему: Cu+Pc → Cu2+Pc + e−.
Пластоцианин, приняв электрон от цитохрома f, (Cu2+Pc + e− → Cu+Pc), перемещается в люменальном пространстве и передает e− на I фотосистему: Cu+Pc → Cu2+Pc + e−.
Первая фотосистема также является сложным белковым комплексом. Белки A (PsaA) и В (PsaB) образуют гетеродимер, содержащий реакционный центр и первичные акцепторы: Р700, А0, А1, Fx. Белок С содержит железо-серные кластеры (4Fe4S) FA, FB. Белки D, E образуют сайт связывания ферредоксина (Fd), F обуславливает связь с пластоцианином (PC). С ферредоксином связывается FNR – Fd:NADP+-редуктаза (содержит FAD – кофактор флавиновой природы), восстанавливается NADP+ до NADPH.
В первой фотосистеме, в отличие от второй, функционируют обе ветви транспорта, но, возможно, при разных условиях. Также есть вариант переноса на уровне железосерных кластеров.
Пигмент P700* — очень мощный восстановитель, его потенциала хватает, чтобы восстановить NADP+.
Первичным акцептором электрона является хлорофилл а695 (А0), далее электрон переходит на акцептор хинольной природы (филлохинон, витамин К1) и FeS кластеры.
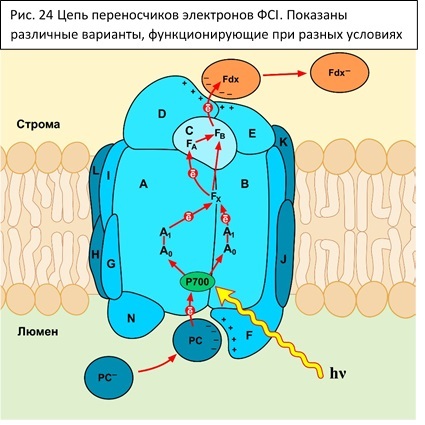
У первой фотосистемы также есть свои антенны. Внутренние антенны располагаются непосредственно на белках А и B, содержат β-каротины и хлорофилл а. Внешние – Lhca1-4, несут хророфиллы а и b, каротин и ксантофиллы.
Ферредоксин растений содержит 2Fe2S кластер, относительно устойчив к кислороду.
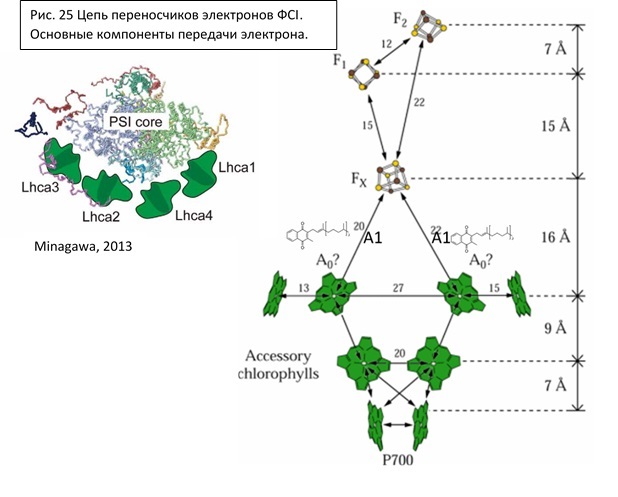
Теперь немного поговорим о том, как может изменяться транспорт электронов, в зависимости от условий. На ЭТЦ влияет множество различных факторов, основные из которых: интенсивность освещения, доступность NADP+, величина протонного градиента, pH стромы и люмена.
На избыточном свету могут начинать происходить фотодеструктивные процессы. Прежде всего это связано с Р680. Если по каким-либо причинам транспорт электронов по ЭТЦ перекрывается, невозможность релаксировать возбужденное состояние P680* приведет к многочисленным, уже вкратце упоминавшимся негативным последствиям, в нейтрализации которых каротиноиды играют существенную роль. Еще вариант восстановления – замена D1 белка, который на ярком свету очень быстро разрушается.
Чтобы снизить риск возникновения фотодеструкции, существует ряд превентивных мер. Мы уже говорили об альтернативном транспорте вокруг ФС II – это одна из таких мер.
Также существует транспорт вокруг первой фотосистемы. ФС I более устойчива на ярком свету, чем ФСII, поэтому при избыточной интенсивности света происходит изменение антенных систем: ССКII отсоединяется от ФСII и присоединяется к ФСI. Это, с одной стороны, приводит к уменьшению притока энергии к Р860, а значит и уменьшает разрушение ФСII. С другой стороны, интенсифицирует приток энергии к Р700. В циклическом транспорте вокруг ФСI участвует новый фермент – ферредоксин-пластохинон оксидоредуктаза, таким образом, электроны с ферредоксина идут не на восстановление NADPH, а на восстановление пластохинонов. NADPH нет, но градиент протонов нагнетается, АТФ синтезируется (работает Q-цикл). Этот транспорт помогает как раз в том случае, когда из-за перевосстановленности пула NADP (нехватки NADP+) происходит торможение потока электронов по ЭТЦ, что может усилить их сброс на кислород с образованием активных форм кислорода. Как уже упоминали, переход ССК II связан с изменением мембранной структуры хлоропласт – разбираются граны. Дело в том, ч в хлоропластах каждый компонент ЭТЦ расположен в определенном месте тилакоидых мембран и мембран ламелл стромы. Из-за сильно выпирающей стромальной части первая фотосистема может располагаться только на ламеллах стромы и на внешних частях гран. ССК II участвуют в сборке гран, взаимодействуя с ССК II других тилакоидов, то есть располагаются на смежных мембранах внутри граны. Там же находится и вторая фотосистема. Именно из-за этого при перераспределении ССК II между тилакоидами граны и ламеллами происходит распад гран. Этот процесс обратим: при изменении интенсивности освещения или других условий граны вновь собираются. 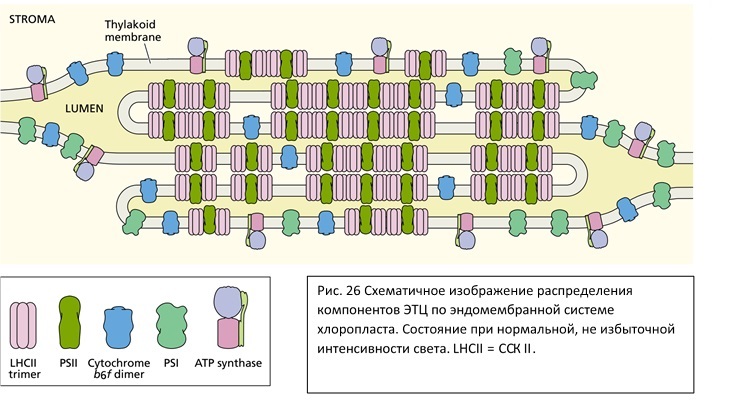
Другой альтернативный вариант, как можно разгрузить ЭТЦ – перенести электроны с ферредоксина на кислород с образованием суперокидрадикала. Это активная форма кислорода, но она может быстро нейтрализоваться до перекиси водорода (другая форма АФК) супероксиддисмутазой. А перекись водорода пероксидазой за счет окисления аскорбата (анион аскорбиновой кислоты) восстанавливается до кислорода и воды. Другое название этого процесса – реакция Мелера.

Существует еще один альтернативный путь – хлородыхание. В тилакоидной мембране присутствует NADPH-дегидрогеназа – фермент, окисляющий NADPH и передающий электроны на пластохиноны. Пластохиноны дальше могут окисляться на пластидной альтернативной оксидазе, в результате работы которой кислород восстанавливается до воды. Таким образом, в ходе фотосинтеза кислород не только выделяется, но и расходуется, при определенных условиях.
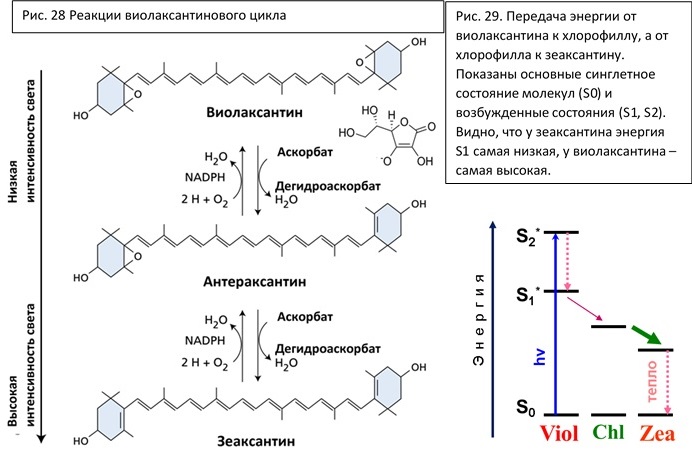
Вкратце рассмотрим еще один интересный механизм защиты СФ II от деструкции – виолаксантиновый цикл. Он проходит в антенных комплнксах, содержащих соответствующие ксантофиллы, при избыточной освещенности. Реакции и превращения изображены на рисунке 28. На пути виолаксантин-зеаксантин действует расположенная с люменальной стороны мембраны де-эпоксидаза, в обратном направлении – эпоксидаза, располагающаяся со стромальной стороны мембраны тилакоида. Ферменты регулируются состоянием pH. Де-эпоксидаза активируется при сильном закислении люмена (=стресс, избыточное освещение), то есть при создании довольно высокого протонного градиента, который, в свою очередь, тоже может тормозить ЭТЦ. Конечным результатом реакции является изменение числа сопряженных двойных связей в ксантофилле, что влияет на его фотохимические свойства. На рисунке 29 показаны энергетические уровни (основные и возбужденные) виолаксантина, хлорофилла и зеаксантина, из соотношения которых видно, как может между ними переходить возбужденное состояние. Таким образом, виолаксантин работает как антенна и передает энергию на хлорофилл (при низкой освещенности), а зеаксантин выполняет защитную роль, забирая избыток энергии.
Приложения (Происхождение пластид, строение хлоропласта).
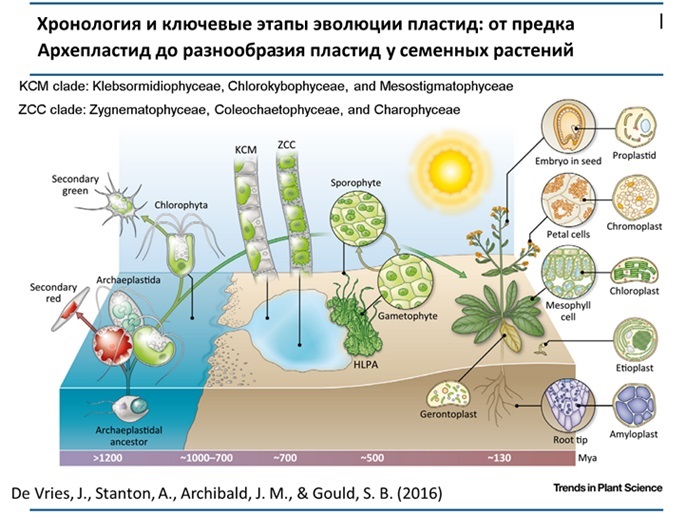
«Что такое фотосинтез, и как он работает?» – Яндекс.Кью
Фотосинтез – это биологический процесс синтеза углеводов из неорганических веществ за счёт энергии солнца. В природе существует несколько вариантов фотосинтеза. У растений фотосинтез происходит в хлоропластах – специальных клеточных органеллах, являющихся потомками цианобактерий. Хлоропласты имеют две мембраны – наружную и внутреннюю. Внутренняя мембрана образует микроскопические «мешочки» — тилакоиды, которые складываются в «стопки» — граны (в каждом хлоропласте множество гран). На мембранах тилакоидов находятся сложные белковые комплексы, образующие элегантно функционирующую систему переноса электронов. С некоторыми белками ассоциированы молекулы хлорофилла. Когда луч света (определённой длины электромагнитная волна) падает на молекулу хлорофилла, происходит её активация, то есть переход в возбуждённое состояние, и он отдаёт свой электрон дальше по цепочке. Чтобы восполнить отданный электрон, необходима какая-то молекула-донор, которая поделится с хлорофиллом своим электроном. У растений (но не у всех фотосинтетиков!) таким донором является вода. Таким образом, под действием световой энергии происходит не только возбуждение хлорофилла, но и окисление воды, которое логично называется фотоокислением. При этом, конечно, в молекулах воды остаются невостребованными атомы кислорода. Они образуют двухатомные молекулы O2. Это тот самый кислород, которым мы дышим, а фотосинтез – основной процесс, образующий его в таком виде.
Далее за счёт запущенного процесса передачи электрона по цепи переносчиков происходит накопление протонов в люмене тилакоида, то есть его внутреннем пространстве. Протоны выходят изнутри тилакоидов в жижу хлоропластов, называемую стромой (термин «строма» применяется и в других биологических контекстах). Но переходят они не просто через мембрану тилакоида, это физически невозможно, но есть специальный белковый комплекс, встроенный в мембрану, – АТФ-синтаза. Проходящие через отверстие в нём протоны заставляют вращаться одну часть этого комплекса относительно другой, благодаря чему происходит фосфорилирование АДФ (аденозиндифосфата) с образованием АТФ (аденозинтрифосфата), богатой энергией молекулы. Кроме того, в определённый момент передачи электронов по цепочке происходит генерация НАДФ∙H.
Всё что было до этого момента называется световой фазой фотосинтеза. Дальнейшие процессы составляют темновую фазу, для которой свет не нужен. В ней происходит сам синтез углеводов (это уже органические вещества), причём источником атомов углерода являются молекулы углекислого газа CO2 (неорганическое вещество). Молекулы АТФ и НАДФ∙H необходимы для протекания определённых реакций на пути синтеза углеводов.
Таким образом, общее уравнение фотосинтеза растений с учётом световой и темновой фаз имеет следующую форму:
6CO2 + 6h3O = C6h22O6 + 6O2.
CO2 – источник углерода; h3O – источник электронов; C6h22O6 – глюкоза, вступающая в дальнейшие метаболические процессы; O2 – побочный продукт фотоокисления воды.
Световая фаза фотосинтеза у растений:
Темновая фаза фотосинтеза (обратите внимание на молекулы АТФ и НАДФ∙H, приходящие из световой фазы, и молекулу глюкозы, являющуюся целью фотосинтеза):
Важно, что данная схема фотосинтеза присуща не всем фотосинтетикам. Например, есть бактерии, у которых донором электронов является не вода, а сероводород, следовательно, побочным продуктом будет не кислород, а сера.
В любом случае, все фотосинтетики являются автотрофными организмами, то есть способны синтезировать органические вещества из неорганических.
Фотосинтез имеет огромное значение для экосистем, поскольку от него зависит баланс кислорода и углекислого газа.
Фотохимический этап фотосинтеза — Студопедия.Нет
(циклическое и нециклическое фосфорилирование)
Фотохимические реакции фотосинтеза — это реакции, в которых энергия света преобразуется в энергию химических связей АТФ и НАДФН2.
Энергия поглощенных квантов света стекается от сотен молекул-антенн к реакционному центру. Хлорофилл реакционного центра, отдает электрон, который поступает в электронно-транспортную цепь. Перенос электрона по цепи переносчиков включает ряд окислительно-восстановительных реакций, в ходе которых выделяется энергия. Эта энергия может быть использована для синтеза АТФ. Процесс преобразования энергии квантов света в АТФ получил название фотосинтетического фосфорилирования (Д.Арнон).
Различают два основных типа фотосинтетического фосфорилирования: нециклическое и циклическое (Рис. 21). При циклическом потоке электроны, переданные от молекулы хлорофилла первичному акцептору, возвращаются к ней обратно. При нециклическом потоке происходит фотоокисление воды и передача электрона от воды к НАДФ.
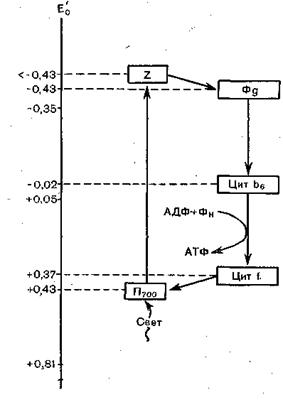
Рисунок 21. – Схема циклического фосфорилирования
В этом процессе принимает участие только фотосистема I. В результате поглощения кванта света молекула П700 отдает возбужденный электрон сначала неидентифицированному переносчику Z, а затем от ферредоксина через ряд переносчиков возвращается к П700. На участке электронно-транспортной цепи между цитохромом b6 и цитохромом f энергия электрона аккумулируется в энергию АТФ. Таким образом, в этом случае П700 является и донором и акцептором электрона. Суммарное уравнение циклического фотосинтетического фосфорилирования:
АДФ + Н3РО4 + hv → АТФ + Н2О
Нециклическое фосфорилирование
При нециклическом потоке электронов принимают участие две фотосистемы. Энергия квантов света стекается к молекуле пигмента П700, которая переходит в возбужденное состоянии и легко отдает электрон (фотохимическая реакция). При этом молекула П700 окисляется и остается в виде положительно заряженной молекулы (Рис. 22).
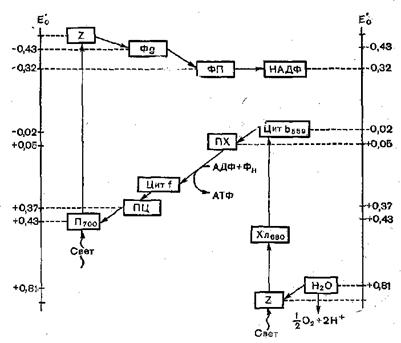
Рисунок 22. – Схема нециклического фосфорилирования
Электрон передвигается по направлению к НАДФ через ряд переносчиков, расположенных в порядке возрастания О/В потенциала. Электроны передвигаются в сторону более высоких окислительно-восстановительных потенциалов. Переносчик, воспринимающий электрон от П700 — неидентифицированный акцептор Z имеет Е0— -0,55. Следующим переносчиком является железосодержащий белок ферредоксин (Е0 — -0,43). От ферредоксина электрон переносится на НАДФ (Е0— —0,32). Этот перенос осуществляется с помощью специфического фермента (ферредоксин-НАДФ-редуктазы), коферментом которого является флавинадениндинуклеотид (ФАД).
Отдав электрон, П700 остается в виде ионизированной молекулы, благодаря чему она является хоршим акцептором электронов. Источником электрона, заполняющего электронную «дырку» П700, является фотосистема II. Под влиянием поглощенного кванта света возбужденный электрон молекулы П680 воспринимается акцептором и передается дальше по цепи переносчиков. Чтобы фотосистема II все время находилась в рабочем состоянии, «электронная дырка» в П680 должна непрерывно пополняться новыми электронами. Их источником являются молекулы воды, находящиеся во внутритилакоидном пространстве. Окислителем ее служит хлорофилл, действующий вместе с ионами Мn2+ и С1_. Данный процесс называется фотоокислением, так как он индуцируется хлорофиллом, окисленным под влиянием света. Т.о. донорами электронов являются две молекулы воды, которые окисляются хлорофиллом последовательно:
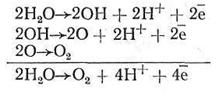
Полученный от П680 неизвестным акцептором Z электрон передается далее на пластохинон (Е0 + 0,11). Считается, что в переносе электронов участвует 65 молекул пластохинона. От пластохинонов электрон воспринимается молекулой цитохрома f (Е0 + 0,36), при этом происходит выброс энергии, которая идет на синтез АТФ. Следующий переносчик — пластоцианин (Е0 + 0,37) — это медьсодержащий белок, в котором на каждую молекулу белка приходится два атома меди. От пластоцианина электрон заполняет электронную «дырку» в П700.
Суммарное уравнение нециклического фотосинтетического фосфорилирования:
2НАДФ +2Н2О + 2 АДФ + 2 Н3РО 4 + 8hv → 2 НАДФН2 + 2 АТФ +2 Н2О + О2
Синтез АТФ в ЭТЦ
Механизм фотофосфорилирования АДФ объясняет хемиосмотическая теория, разработанная английским биохимиком П. Митчеллом (1961-1966).
Цепь переносчиков электронов и протонов, действующая в соответствии с окислительно-восстановительным градиентом, перешнуровывает мембрану таким образом, что трансмембранный перенос ē и Н+ в одну сторону чередуется с переносом в обратную сторону только ē. В результате функционирования такого механизма (Н+-помпы) по одну сторону мембраны накапливается избыток Н+ и возникает электрохимический потенциал ионов Н+, который служит формой запасания энергии. Обратный пассивный ток ионов Н+ через протонный канал Н+-АТРазы, получивший название фактора сопряжения сопровождается образованием макроэргической фосфатной связи АТР. Этот фермент выглядит как грибовидная частица на поверхности мембраны тилакоидов. Его молекула состоит из двух частей: головки, выступающей с наружной стороны мембраны и содержащей активный центр фермента, и ножки, погруженной в мембрану и представляющей канал, через который передвигаются протоны.
Темновая фаза фотосинтеза
В темновой фазе фотосинтеза в строме хлоропластов при помощи АТФ и НАДФН2 световой стадии восстанавливается поглощенный СО2 с образованием углеводов и других органических соединений.
Этот путь ассимиляции СО2 обнаружен у всех фотосинтезирующих растений. Он был назван циклом Кальвина в честь американского биохимика М. Кальвина, который с сотрудниками открыл и изучил его в 1946-1956 годах с помощью метода меченых атомов и хроматографии. За это в 1961г. он был удостоен Нобелевской премии.
Цикл состоит из трех этапов: карбоксилирования, восстановления, регенерации первичного акцептора СО2 и синтеза конечного продукта фотосинтеза.
1. Карбоксилирование.
Происходит в результате присоединения молекулы углекислого газа к органическому акцептору — пятиуглеродному фосфорилированному сахару — рибулезодифосфату (РДФ). Реакция идет с участием ключевого фермента фотосинтеза — рибулезодифосфаткарбоксилазы (РДФ-карбоксилаза). В итоге образуется нестойкое шестиуглеродное соединение, которое легко гидролизуется на две молекулы фосфоглицериновой кислоты (ФГК) (Рис. 23).
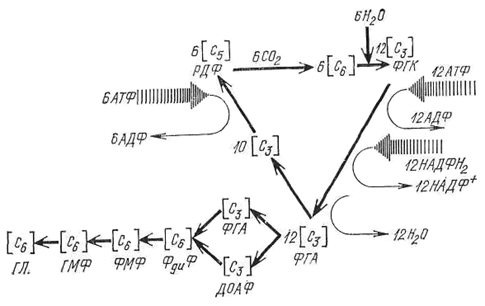
Рисунок 23. – Схема темновой стадии фотосинтеза
2. Восстановление.
При этом каждая молекула ФГК фосфорилируется еще раз с участием АТФ и фермента фосфоглицерокиназы и превращается в более реакционноспособное соединение — диФГК. Последняя с помощью фермента триозофосфат-дегидрогеназы восстанавливается водородом НАДФН2 до фосфоглицеринового альдегида (ФГА).
Часть молекул ФГА идет на регенерацию РДФ, а остальные выводятся из цикла Кальвина и используются в синтезе гексоз.
3. Регенерация и синтез конечного продукта фотосинтеза.
Регенерация рибулезодифосфата происходит из ФГА вследствие семи последовательных ферментативных реакций. Продуктом их служит рибулозо-5-фосфат. Он повторно фосфорилируется и превращается в РДФ. На этом цикл Кальвина замыкается.
Молекулы ФГА, выведенные из цикла, используются в синтезе гексоз. Для этого необходимо, чтобы одна из двух молекул ФГА изомеризовалась в диоксиацетонфосфат (ДОАФ), что осуществляется с помощью фермента триозофосфатизомеразы. После этого ДОАФ вступает в реакцию конденсации с ФГА. В результате синтезируется молекула фруктозодифосфата (ФдиФ). При отщеплении от нее остатка фосфорной кислоты образуется фруктозомонофосфат (ФМФ), который затем изомеризуется в глюкозомонофосфат (ГМФ). Последний, отдав остаток фосфорной кислоты, превращается в глюкозу.
Т.о., для синтеза одной молекулы глюкозы в цикле Кальвина необходимо 18 АТФ и 12 НАДФН2, которые образуются в световой фазе при воздействии 8 квантов света.
Реакции темновой стадии фотосинтеза протекают в строме хлоропластов, вблизи поверхности тилакоидов, поставляющих продукты световых реакций. В промежутках между тилакоидами откладываются зерна ассимиляционного крахмала.
Среди продуктов фотосинтеза обнаружены аминокислоты. При недостатке НАДФН2 ФГК превращается не в ФГА, а в пировиноградную кислоту. Она, присоединяя аммиак, образует аланин. Из пировиноградной кислоты в цикле Кребса образуются органические кислоты, которые в ходе реакций аминирования и переаминирования дают аминокислоты.
Отклонения от С3-пути фотосинтеза
С4-путь фотосинтеза (цикл Хетча-Слэка-Карпилова)
Советским ученым Карпиловым Ю.С. (1960), а затем австралийскими учеными М. Хетчем и К. Слэком (1966) был описан путь фотосинтеза, характерный для тропических и субтропических растений (сахарный тростник, кукуруза, сорго, амарант и др.). При этом пути фотосинтеза первым продуктом карбоксилирования является соединение, содержащее 4 атома углерода. Поэтому этот путь получил название С4-пути.
Листья этих растений содержат хлоропласты двух типов:
1) мелкие гранальные в клетках мезофилла листа;
2) крупные, лишенные гран и фотосистемы II, в клетках обкладки, окружающих сосудистые пучки. Клетки обкладки имеют утолщенные клеточные стенки, расположены вокруг сосудистых пучков в 1 или 2 слоя.
Хлоропласты разных типов клеток характеризуются не только особенностями строения, но и разным типам фосфорилирования. В клетках мезофилла по преимуществу происходит нециклическое фосфорилирование и образуется АТФ и НАДФН2, необходимые для цикла Кальвина, идущего в клетках обкладки. В хло-ропластах клеток обкладки идет только циклическое фосфорилирование. Такое разделение типов фосфорилирования, возможно, связано с тем, что к хлоро-пластам клеток обкладки, расположенным в глубине листа, проникает по преимуществу более длинноволновый свет, который не поглощается фотосистемой II.
На первом этапе С4-пути углекислый газ, диффундирующий в лист через устьица, попадает в цитоплазму клеток мезофилла с мелкими хлоропластами, где при помощи фосфоэнолпируваткарбоксилазы присоединяется к фосфоэнолпировиноградной (ФЭП) кислоте, образуя щавелевоуксусную кислоту (оксалоацетат). Она транспортируется в хлоропласты, где восстанавливается до яблочной кислоты (малат) при участии НАДФН2. В присутствии ионов аммония щавелевоуксусная кислота может превращатся в аспарагиновую кислоту (аспартат). Яблочная или аспарагиновая кислоты переходят в хлоропласты клеток обкладки, декарбоксилируются и окисляются до пировиноградной кислоты. Образующийся при этом СО2 включается в цикл Кальвина, а пировиноградная кислота переносится в клетки мезофилла, где превращается в фосфоэнолпировиноградную кислоту. Такой механизм позволяет растениям фотосинтезировать при закрытых из-за высокой температуры устьицах. Кроме того, продукты цикла Кальвина образуются в хлоропластах клеток обкладки, окружающих проводящие пучки, что способствует быстрому оттоку фотоассимилятов и тем самым повышает интенсивность фотосинтеза.
Таким образом, при С4-пути реакция карбоксилирования происходит дважды. Это позволяет растению создавать запасы углерода в клетках. Акцепторы С02 (ФЕП и РДФ) регенерируют, что и создает возможность непрерывного функционирования циклов. Фиксация С02 с участием ФЕП и образованием малата или аспартата служит своеобразным насосом для поставки СО2 в хлоропласты обкладки, функционирующих по С3-пути. Поскольку при таком механизме фотосинтеза принимают участие два типа клеток и два типа хлоропластов, этот путь называют еще кооперативным.
CAM-путь фотосинтеза
У суккулентов (кактусов и растений сем. толстянковых (Crassulaceae) тип фотосинтеза получил название CAM (Crassulaceae acid metabolism)-путь. Химизм фиксации С02 при САМ-пути сходен с С4-путем, однако если у С4— растений фотосинтез разделен в пространстве, то при САМ-пути — во времени. Устьица у суккулентов днем обычно закрыты, что предотвращает потерю воды в ходе транспирации, а ночью открыты. В темноте СО2 поступает в листья, где фосфоэнолпируваткарбоксилаза присоединяет его к фосфоэнолпировиноградной кислоте, образуя щавелевоуксусную кислоту. Она восстанавливается НАДФН2-зависимой малатдегидрогеназой до яблочной кислоты, которая накапливается в вакуолях. Днем яблочная кислота переходит из вакуоли в цитоплазму, где декарбоксилируется и окисляется до пировиноградной кислоты. СО2 диффундирует в хлоропласты и включается в цикл Кальвина.
Осуществление фотосинтеза по такому пути позволяет растениям максимально экономить воду и поддерживать процесс фотосинтеза в условиях острого водного дефицита. Однако САМ-путь не может обеспечить высокой продуктивности растений, поэтому данные растения медленно растут и не могут конкурировать с С3— и С4-растениями при менее экстремальных условиях. Возможна смена путей фиксации С02. При достаточном количестве воды растения с САМ-метаболизмом могут переходить на С3-путь.
Фотодыхание
Фотодыхание – это активируемый светом процесс выделения СО2 и поглощения О2. Так как первичным продуктом фотодыхания является гликолевая кислота, оно еще называется гликолатным путем. Фотодыхание усиливается при низком содержании СО2 и высокой концентрации О2 в воздухе. Протекает только на свету. Осуществляется при взаимодействии трех органелл – хлоропластов, пероксисом и митохондрий.
В этих условиях рибулозодисфаткарбоксилаза хлоропластов катализирует не карбоксилирование рибулозодифосфата, а его расщепление на 3-фосфоглицериновую и 2-фосфогликолевую кислоты. Последняя дефосфорилируется с образованием гликолевой кислоты (Рис. 24).
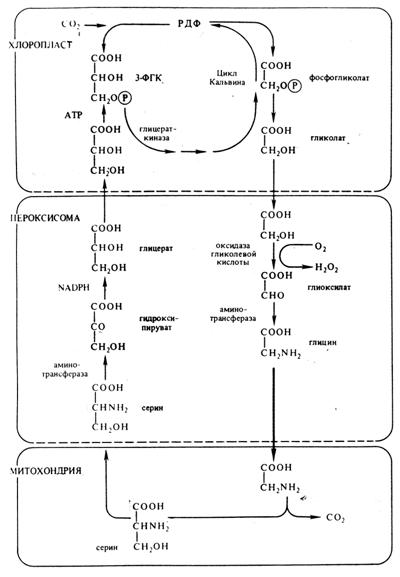
Рис. 24. – Схема фотодыхания.
Гликолевая кислота из хлоропласта переходит в пероксисому, где окисляется гликолатоксидазой до глиоксиловой кислоты. Образующаяся при этом перекись водорода разлагается каталазой, присутствующей в пероксисоме. Глиоксиловая кислота аминируется, превращаясь в глицин. Глицин транспортируется в митохондрию, где из двух молекул глицина синтезируется серин и освобождается СО2.
Серин может поступать в пероксисому и под действием аминотрансферазы передает аминогруппу на пировиноградную кислоту с образованием аланина, а сам превращается в гидроксипировиноградную кислоту. Последняя при участии НАДФН2 восстанавливается в глицериновую кислоту. Она переходит в хлоропласты, где включается в цикл Кальвина.
Таким образом, термин фотодыхание имеет лишь формальный смысл: О2 потребляется, СО2 выделяется, однако в функциональном плане к дыханию этот процесс прямого отношения не имеет.
Экология фотосинтеза
Влияние внутренних и внешних факторов на фотосинтез
Фотосинтез осуществляется в полуавтономных органеллах – хлоропластах. Однако на него в значительной мере оказывают влияние факторы внутренней и внешней среды.
Влияние внутренних факторов на фотосинтез.
1. Содержание хлорофилла. С увеличением содержания в клетке хлорофилла увеличивается интенсивность фотосинтеза. Однако прямой зависимости между этими показателями нет. Так, за время позеленения этиолированных листьев количество хлорофилла может увеличиться в 20 раз, а интенсивность фотосинтеза — только в 2 раза.
2. Степень открытости устьиц. В том случае, если содержание воды поддерживается в листе на достаточно высоком уровне, увеличение ширины устьичных щелей, как правило, сопровождается увеличением интенсивности фотосинтеза. При полном закрытии устьиц фотосинтез протекает, но в очень слабой степени.
3. Отток ассимилятов. Накопление фотоассимилятов в хлоропластах и в околопластидном пространстве приводит к ингибированию ферментов, участвующих в фотосинтезе.
4. Возраст листа и растения.В ходе роста листа интенсивность фотосинтеза увеличивается. Наибольшая интенсивность характерна для сформировавшихся листьев. По мере дальнейшего увеличения возраста листьев (процесс старения) интенсивность фотосинтеза падает. На интенсивность фотосинтеза оказывает влияние возраст всего растения. У большинства однолетних растений интенсивность фотосинтеза возрастает в процессе онтогенеза и достигает максимума в фазу бутонизации, цветения. После цветения интенсивность фотосинтеза в листьях снижается и возрастает снова при созревании плодов.
Влияние внешних факторов на фотосинтез.
1 Свет. Имеется нижний порог освещенности, при котором растения начинают фотосинтезировать. Затем зависимость интенсивности фотосинтеза от освещенности имеет логарифмический характер с последующим выходом на плато. Уровень освещения, при котором поглощение СО2 в ходе фотосинтеза равно выделению СО2 в процессе дыхания, называется световым компенсационным пунктом. Значение светового компенсационного пункта неодинаково не только у теневыносливых (составляет примерно 1 % от полного света) и светолюбивых растений (около 3 — 5 % от полного солнечного света), но и у листьев разных ярусов одного и того же растения, оно зависит также от концентрации СО2 в воздухе. Важен и спектральный состав света. При освещении красным светом образуются преимущественно углеводы, синим – амино- и органические кислоты.
При очень высокой интенсивности света может наблюдаться депрессия фотосинтеза. На начальных этапах депрессии хлоропласты передвигаются к боковым стенкам клетки (фототаксис) и поворачиваются ребром к свету. При этом интенсивность фотосинтеза может резко сокращаться. Причиной депрессии фотосинтеза являются также перегрев и нарушение водного баланса. На ярком свету возможно необратимое фотоокисление хлорофилла.
2. Температура. При низкой освещенности фотосинтез идет с одинаковой скоростью при 15 и 25оС. Это объясняется тем, что при низкой освещенности интенсивность фотосинтеза зависит от скорости световых реакций. При высокой освещенности интенсивность фотосинтеза лимитируется скоростью темновых реакций и Q10 примерно равен 2. Для большинства растения С3-типа оптимальная температура 20-25оС, для растений С4-типа она равна 25-40оС. При температуре выше оптимальной интенсивность фотосинтеза снижается из-за инактивации ферментов и закрытия устьиц. Нижняя температурная граница фотосинтеза у растений северных широт находится в пределах —15 °С (сосна, ель) —0,5 °С, а у тропических растений — в зоне низких положительных температур 4 — 8 °С.
3. Содержание СО2 в воздухе. Повышение содержания СО2 с 0,03% до 0,3% вызывает увеличение интенсивности фотосинтеза. Дальнейшее возрастание концентрации СО2 до 1% не сказывается на фотосинтезе, но более высокий уровень СО2 в воздухе приводит к депрессии фотосинтеза. Высокие концентрации СО2 особенно неблагоприятны при высокой освещенности, так как происходит ингибирование темновых реакций.
4. Снабжение водой. При полном насыщении листа водой устьица закрываются, что снижает интенсивность фотосинтеза. В условиях засухи чрезмерная потеря воды листом также вызывает закрывание устьиц под влиянием увеличения содержания в листьях абсцизовой кислоты, что уменьшает поступление СО2, снижает транспирацию и приводит к повышению температуры листа. Обезвоживание также снижает активность ферментов. Максимальный интенсивность фотосинтеза наблюдается при небольшом водном дефиците листа (порядка 5 — 20% от полного насыщения) при открытых устьицах.
5. Содержание О2 в воздухе. Процесс фотосинтеза обычно осуществляется в аэробных условиях при концентрации кислорода 21%. Увеличение содержания или отсутствие кислорода для фотосинтеза неблагоприятны.
Высокие концентрации О2 (25 — 30%) снижают фотосинтез («эффект Варбурга»). Повышение парциального давления О2 и уменьшение концентрации СО2 активируют фотодыхание. Кислород непосредственно снижает активность РДФ-карбоксилазы, а также может окислять первичные восстановленные продукты фотосинтеза.
6. Минеральное питание. Исключение любого элемента минерального питания отрицательно сказывается на фотосинтезе. Особенно важны такие элементы как фосфор, магний, железо, марганец, хлор, медь, калий и азот.
В условиях недостатка фосфора нарушаются фотохимические и темновые реакции фотосинтеза. Особенно резко дефицит фосфора проявляется при высокой интенсивности света, при этом более чувствительными оказываются темновые реакции.
Магний входит в состав хлорофиллов, участвует в деятельности сопрягающих белков при синтезе АТФ, влияет на активность реакций карбоксилирования и восстановления НАДФ.
Железо в восстановленной форме необходимо для процессов биосинтеза хлорофилла и железосодержащих соединений хлоропластов (цитохромов, ферредоксина).
Необходимость марганца и хлора для зеленых растений связана с их участием в фотоокислении воды.
Медь входит в состав пластоцианина, поэтому у растений дефицит меди вызывает снижение интенсивности фотосинтеза.
Уменьшение содержания калия сопровождается разрушаением структуры гран в хлоропластах, устьица слабо открываются на свету и недостаточно закрываются в темноте, ухудшается водный режим листа, нарушаются все процессы фотосинтеза.
Недостаток азота сильно сказывается на формировании пигментных систем, структур хлоропласта и его общей активности. Концентрация азота определяет количество и активность РДФ-карбоксилазы.
7. Загрязнение окружающей среды. Фотосинтетический аппарат растений, очень чувствителен к вредным газам: окись углерода, окислы азота, хлор, фтор и др. Особенно часто встречаются повреждения, связанные с действием сернистого газа (SО2), который ингибирует транспорт электронов в хлоропластах и фотолиз воды, нарушает цикл Кальвина, замедляет транспорт ассимилятов. Больше всего газа проникает, когда устьица открыты полностью. Концентрация сернистого газа, равная 0,00004 %, является токсичной для многих видов хвойных растений. Наряду со снижением интенсивности фотосинтеза сернистый газ изменяет и качественный состав продуктов фотосинтеза. Пыль, сажа, плотным слоем покрывают листья растений, почти полностью закупоривают устьица, резко снижают (до двух раз) доступ света к мезофиллу листа.
8. Заболевания растений (ржавчина, мучнистая роса и др). Ингибирование процесса фотосинтеза под влиянием патогена может происходить вследствие действия выделяемых грибом токсинов, вызывающих деструктивные изменения фотосистем, ультраструктуры хлоропластов и отмиранием отдельных участков листа, снижения содержания хлорофилла и каротиноидов, затемнения листа мицелием гриба и т. д.
Суточная и сезонная динамика фотосинтеза
Исследования фотосинтеза растений естественных наземных экосистем были начаты в первой четверти XX в. работами В. Н. Любименко, С. П. Костычева и др. Факторы внешней среды, рассмотренные ранее, действуют совместно и в различных сочетаниях. Однако ведущую роль играют свет, температура и водный режим.
Суточная динамика фотосинтеза
С восходом солнца интенсивность фотосинтеза возрастает вместе с освещенностью, достигая максимальных значений в 9 — 12 ч. Дальнейший характер процесса определяется степенью обводненности листьев, температурой воздуха и интенсивностью солнечного света.
В умеренную погоду при достаточной влажности почвы и воздуха фотосинтез возрастает постепенно, достигая максимальных значений в полдень. Дневной ход фотосинтезаописывается одновершинной кривой, следуя за изменениями освещенности и температуры.
Переменная погода ведет к полной зависимости этого хода от освещенности с образованием многовершинной кривой.
В большинстве же случаев по мере повышения освещенности и температуры интенсивность фотосинтеза достигает максимальных значений перед полуднем, затем наблюдается ее спад с последующим вторым максимумом к 16—17 ч, образуя двухвершинную кривую.
При очень жаркой и сухой погоде кривая становится одновершинной с максимумом в утренние часы.
Наблюдающийся спад фотосинтеза получил название полуденной депрессии. Среди условий, вызывающих эту депрессию, следует назвать водный дефицит листьев, закрывание устьиц, перегрев листьев, слабый отток ассимилятов из хлоропластов, фотоокисление хлорофилла и инактивацию ферментов, в том числе карбоксилаз, на сильном свету, резкое повышение дыхания, понижение содержания СО2 около листьев в связи с ее усиленным потреблением зелеными листьями.
Сезонная динамика фотосинтеза
Для листопадных древесных растений умеренной зоны характерно постепенное увеличение скорости ассимиляции от ранней весны до конца лета. При недостатке воды в почве снижение интенсивности фотосинтеза происходит быстрее. У длительно вегетирующих деревьев и кустарников сезонный максимум регистрируется в самом начале жаркого и сухого периода. К осени интенсивность фотосинтеза постепенно снижается. Неопадающая листва хвойных, за исключением лиственниц, позволяет им фотосинтезировать в течение более длительного времени, включая раннюю весну и позднюю осень. Этим можно отчасти объяснить примерно одинаковую продуктивность лиственных и хвойных лесов в одних и тех же условиях.
У травянистых растений интенсивность фотосинтеза также возрастает до фазы бутонизации и цветения, а затем снижается. Резкий подъем фотосинтетической активности в период заложения репродуктивных органов связан с усиленным потреблением ассимилятов на формирование цветков и плодов.
Скороспелые сорта сельскохозяйственных растений раньше снижают и прекращают фотосинтез, чем позднеспелые с более продолжительным вегетационным периодом. Первые поэтому рекомендуют для северных, а вторые — для более южных районов.
ЛАБОРАТОРНЫЙ ПРАКТИКУМ
Световая фаза — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 24 декабря 2018; проверки требует 1 правка. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 24 декабря 2018; проверки требует 1 правка.Световая фаза — этап фотосинтеза, в течение которого за счёт энергии солнца образуются богатые энергией соединения АТФ и молекулы — носители энергии.
Осуществляется на внутренних мембранах хлоропластов, на которых располагаются молекулы хлорофилла. Хлорофилл поглощает энергию солнечного света, которая затем используется при синтезе молекул АТФ из АДФ и фосфорной кислоты, а также способствуют расщеплению молекул воды: 2H2O = 4H+ + 4e— + O2. Кислород, образующийся при расщеплении выделяется в окружающую среду в свободной форме.
Под влиянием энергии солнечного света молекула хлорофилла возбуждается, в результате чего один из её электронов переходит на более высокий энергетический уровень. Этот электрон, проходя по цепи переносчиков (белков мембраны хлоропласта), отдаёт избыточную энергию на окислительно-восстановительные реакции (синтез молекул АТФ).
Молекулы хлорофилла, потерявшие электроны, присоединяют электроны, образующиеся при расщеплении молекулы воды.
Под действием света электрон в реакционном центре переходит в возбуждённое состояние «перескакивая» на высокий энергетический уровень молекулы хлорофилла. Часть электронов, захваченных ферментами способствует образованию АТФ путём присоединения остатка фосфорной кислоты и АДФ. Другая часть электронов принимает участие в разложении воды на молекулярный кислород, ионы водорода и электроны. Образовавшийся водород с помощью электронов присоединяется к веществу, способному транспортировать водород в пределах хлоропласта.