Оксиды. Химические свойства и способы получения » HimEge.ru
Оксиды — сложные вещества, состоящие из двух элементов, один из которых — атом кислорода в степени окисления -2.
По способности образовывать соли оксиды делят на солеобразующие и несолеобразующие (СО,SiO,NO,N2О). Солеобразующие оксиды, в свою очередь, классифицируют на основные, кислотные и амфотерные.
Основными называются оксиды, которым соответствуют основания, кислотными — оксиды, которым отвечают кислоты. К амфотерным относятся оксиды, проявляющие химические свойства как основных, так и кислотных оксидов.
Основные оксиды образуют только элементы-металлы: щелочные (Li2О, Na2О, К2О, Cs2О, Rb2О), щелочноземельные (CaO, SrO, BaO, RaO) и магний (MgO), а также металлы d-семейства в степени окисления +1, +2, реже +3(Cu2O, CuO, Ag2O, СrO, FeO, MnO, СоO, NiO).
Кислотные оксиды образуют как элементы-неметаллы (СО2, SO2, NO2,Р2O5, Cl2O7), так и элементы-металлы, степень окисления атома металла должна быть +5 и выше(V2O5, СrO3, Mn2O7, MnO3). Амфотерные оксиды образуют только элементы металлы (ZnO, AI2O3, Fe2O3, BeO, Cr2O3, PbO, SnO, MnO2).
В обычных условиях оксиды могут находиться в трех агрегатных состояниях: все основные и амфотерные оксиды твердые вещества, кислотные оксиды могут быть жидкими (SO3,Сl2O7,Mn2O7), газообразными (CO2, SO2, NO2) и твердыми (P2O5, SiO2). Некоторые имеют запах (NO2, SO2), однако большинство оксидов запаха не имеют. Одни оксиды окрашены: бурый газ NO 2, вишнево-красный CrO3, черные CuO и Ag2O, красные Cu2O и HgO, коричневый Fe2O3, белые SiO2, Аl2O3 и ZnO, другие — бесцветные (H2O, CO2, SO2).
Большинство оксидов устойчивы при нагревании; легко разлагаются при нагревании оксиды ртути и серебра. Основные и амфотерные оксиды имеют немолекулярное строение, для них характерна кристаллическая решетка ионного типа. Большинство кислотных оксидов вещества молекулярного строения (одно из немногих исключений — оксид кремния (IV), имеющий атомную кристаллическую решетку).
Химические свойства оксидов
Al2O3+6KOH+3H2O=2K3[Al(OH)6] — гексагидроксоалюминат калия;
ZnO+2NaOH+H2O=Na2[Zn(OH)4] — тетрагидроксоцинкат натрия;
Смотрите также:
Основные оксиды — получение и химические свойства
Кислотные оксиды — получение и химические свойства
Химические свойства амфотерных оксидов
Задания 8 ЕГЭ по химии тест онлайн
Часть IV. ЭКОЛОГИЧЕСКАЯ ОБСТАНОВКА В ПРОМЫШЛЕННЫХ ЦЕНТРАХ КЕМЕРОВСКОЙ ОБЛАСТИ
Часть IV. ЭКОЛОГИЧЕСКАЯ
ОБСТАНОВКА В ПРОМЫШЛЕННЫХ
ЦЕНТРАХ КЕМЕРОВСКОЙ ОБЛАСТИ
ЭКОЛОГИЧЕСКАЯ
ОБСТАНОВКА В ПРОМЫШЛЕННЫХ
ЦЕНТРАХ КЕМЕРОВСКОЙ ОБЛАСТИ
Раздел 3. ГОРОД НОВОКУЗНЕЦК
3.1. Выбросы загрязняющих веществ в атмосферный воздух
3.1.1 .Стационарные источники
В 2006 году в городе Новокузнецке зарегистрировано 4069 стационарных источников выбросов загрязняющих веществ в атмосферный воздух, в том числе организованных – 2817.
По данным Управления по технологическому и экологическому надзору Ростехнадзора по Кемеровской области, в 2006 году в городе Новокузнецк общая масса загрязняющих веществ, поступивших в атмосферу, составила 435,548 тыс. т.
Обобщенные данные об изменении массы выбросов загрязняющих веществ в атмосферу от стационарных источников представлены в табл. 3.1.
Таблица 3.1
Динамика массы выбросов загрязняющих веществ в атмосферный воздух от стационарных источников, тыс. т
Наименование загрязняющего вещества | 2002 | 2003 | 2004 | 2005 | 2006 |
Всего, в том числе: | 487,7 | 476,5 | 451,5 | 435,548 | |
Твердые | 66,7 | 60,9 | 60,4 | 56,3 | 51,127 |
Газообразные и жидкие, всего, из них: |
|
|
|
| 384,421 |
оксид углерода | 276,5 | 284,9 | 283,3 | 284,1 | 277,429 |
углеводороды (без ЛОС) | 58,132 | 56,135 | 44,92 | 39,33 | 41,702 |
диоксид серы | 52,7 | 40,9 | 40,6 | 42,06 | 38,327 |
оксиды азота (в пересчете на диоксид азота) | 25,8 | 26,1 | 22,3 | 21,37 | 19,389 |
летучие органические соединения (ЛОС) |
|
|
|
| 1,712 |
прочие газообразные и жидкие | 3,03 | 3,22 | 0,22 | 3,91 | 5,862 |
В сравнении с 2005 годом общая масса выбросов
загрязняющих веществ в атмосферу уменьшилась на 15,952 тыс. т в результате модернизации и реконструкции газоочистного
оборудования на крупных предприятиях города, внедрения современных
энергосберегающих технологий, использования сырья высокого качества, выполнения
запланированных природоохранных мероприятий.
т в результате модернизации и реконструкции газоочистного
оборудования на крупных предприятиях города, внедрения современных
энергосберегающих технологий, использования сырья высокого качества, выполнения
запланированных природоохранных мероприятий.
Основная доля в выбросах загрязняющих веществ в атмосферу приходится на оксид углерода – 63,7 %; твердые вещества – 11,7 %; углеводороды (без ЛОС) – 9,6 %; диоксид серы – 8,8 %, диоксид азота – 4,4 %.
Город Новокузнецк является крупным промышленным центром и имеет выраженную специализацию – металлургическое производство, химическая промышленность, добыча угля, промышленное и гражданское строительство и другие.
В 2006 году на предприятиях города
уловлено 2426,468 т загрязняющих веществ, что составляет 84,8 %
к отходящим. Наиболее высокая
степень улавливания загрязняющих веществ отмечена на предприятиях по
производству прочих неметаллических минеральных продуктов (стекла и изделий из
стекла; керамических изделий; цемента, извести и гипса; резка, обработка,
отделка камня и другие) – 90,8 %, по добыче топливно-энергетические
полезных ископаемых – 90,2 %, на предприятиях металлургического
производства – 85,3 %; низкая
– на предприятиях транспорта и связи – 27,5 % (табл. 3.2).
3.2).
Таблица 3.2
Сведения о выбросах загрязняющих веществ в атмосферный воздух, их очистке и утилизации по видам экономической деятельности, тыс. т
Наименование вида экономической деятельности | К-во предприятий | Масса загрязняющих веществ | Выброшенных в атмосферу | Фактически уловлено в % к отходящим | ||
Отходящих | Уловленных и обезвреженных | |||||
всего | из них утилизировано | |||||
Всего по городу | 232 | 2862,020 | 2426,468 | 1103,704 | 435,548 | 84,8 |
Металлургическое производство | 15 | 1815,281 | 1548,242 | 897,033 | 85,3 | |
Производство и распределение электроэнергии, газа и воды | 11 | 557,615 | 440,158 | 44,970 | 117,457 | 78,9 |
Добыча топливно-энергетических полезных ископаемых | 7 | 450,159 | 405,840 | 130,432 | 44,319 | 90,2 |
Производство прочих неметаллических минеральных продуктов | 8 | 33,847 | 30,724 | 30,682 | 3,123 | 90,8 |
Транспорт и связь | 47 | 1,187 | 0,327 | 0,100 | 0,860 | 27,5 |
Строительство | 33 | 1,083 | 0,687 | 0,410 | 0,396 | 63,4 |
Производство машин и оборудования | 17 | 0,403 | 0,127 | 0,019 | 0,276 | 31,5 |
Химическая промышленность | 2 | 0,061 | 0,030 | 0 | 0,031 | 49,1 |
Другие | 92 | 2,380 | 0,330 | 0,028 | 2,056 | 13,9 |
Увеличилась масса выбросов загрязняющих веществ в атмосферный воздух:
– в связи с увеличением объемов производства на ОАО «ЗСМК», ООО «Производственная компания “Кузнецкий цементный завод”», ОАО «Кузнецкие ферросплавы», ОАО «Завод Универсал», ОАО «Органика»;
– в связи с увеличением производительности дегазационного оборудования и вводом в эксплуатацию вентиляционных установок на ОАО «ОУК “Южкузбассуголь”» – филиал «Шахта “Абашевская”»;
– в результате использования углей низкого качества и изменением
сырьевой базы топлива на МКП «Теплоэнергия»,
ОАО ЦОФ «Абашевская».
Таблица 3.3
Динамика массы выбросов загрязняющих веществ в атмосферный воздух от крупных промышленных предприятий, т
Наименование предприятия | 2002 | 2003 | 2004 | 2005 | 2006 |
Всего |
|
| 421 308 | 408 557 | 406 186 |
ОАО «ЗСМК» | 214 667 | 211 241 | 210 346 | 208 048 | 208 344 |
Абагурский филиал ОАО «Евразруда» | 79 918 | 78 307 | 79 781 | 74 128 | 73 690 |
Филиал «Шахта “Абашевская”» ОАО «ОУК “Южкузбассуголь”» | 56 188 | 51 246 | 43 875 | 38 856 | 40 809 |
ОАО «РУСАЛ Новокузнецк» | 31 419 | 28 097 | 27 156 | 25 667 | 25 460 |
Западно-Сибирская
ТЭЦ | 31 280 | 28 241 | 24 724 | 27 507 | 24 531 |
ОАО «Кузнецкие ферросплавы» | 8288 | 8340 | 10 761 | 10 420 | 10 846 |
МКП «Теплоэнергия» | 9351 | 10 066 | 10 974 | 8633 | 9095 |
Филиал
«Кузнецкая ТЭЦ» | 10 520 | 9688 | 9489 | 10 729 | 8476 |
ООО «ПК “Кузнецкий» цементный завод”» | 2100 | 2000 | 1815 | 2436 | 2889 |
ОАО ЦОФ «Кузнецкая» | 843 | 1024 | 1285 | 1210 | 853 |
ОАО ЦОФ «Абашевская» | 854 | 825 | 913 | 841 | 845 |
ОАО «Завод Универсал» | 330 | 400 | 170 | 65 | 328 |
ОАО «Органика» | 27 | 19 | 19 | 17 | 20 |
Снизилась масса выбросов загрязняющих веществ в атмосферный воздух:
– за счет уменьшения количества сожженного твердого топлива, улучшения его качества и увеличения доли потребления газа на ОАО «Кузбассэнерго», филиал «Кузнецкая ТЭЦ»;
– за счет повышения эффективности пылеулавливающего оборудования на ОАО ЦОФ «Кузнецкая», ОАО «РУСАЛ Новокузнецк»;
– в связи с сокращением объемов производства
агломерата на ОАО «Евразруда», Абагурский филиал.
Город Новокузнецк состоит из шести территориальных районов. Основная нагрузка по выбросам загрязняющих веществ в атмосферный воздух приходится на Заводской район (54,2 %).
Таблица 3.4
Масса выбросов загрязняющих веществ в атмосферный воздух по районам
Район | Масса загрязняющих веществ, тыс. т | Доля вклада, % |
Всего по городу | 435,548 | 100 |
Заводской | 236,218 | 54,2 |
Центральный | 100,768 | 23,1 |
Орджоникидзевский | 51,258 | 11,8 |
Кузнецкий | 45,728 | 10,5 |
Куйбышевский | 1,548 | 0,4 |
Ильинский | 0,028 | — |
Рис. 3.2. Выбросы загрязняющих веществ в атмосферу по
районам города Новокузнецка, тыс. т
3.2. Выбросы загрязняющих веществ в атмосферу по
районам города Новокузнецка, тыс. т
Заводский район. На территории района размещены: ОАО «Западно-Сибирский металлургический комбинат», ОАО «Западно-Сибирская ТЭЦ», ОАО ЦОФ «Кузнецкая», ОАО «Завод Гидромаш», ОАО «Шахта “Большевик”» и другие.
Основные загрязняющие вещества: оксид углерода, диоксид серы, пыль, окислы азота.
Центральный район. На территории района размещены: предприятия бывшего Кузнецкого металлургического комбината – ОАО «Новокузнецкий металлургический комбинат», ООО «Сталь НК», ООО «Евроазиатская энергетическая компания», ООО «Завод ремонта металлургического оборудования», ООО «Независимая сервисная компания “Новокузнецк”», ООО «Сибирские товары», ООО «АТП КМК», Абагурский филиал ОАО «Евразруда», ООО «Производственная компания “Кузнецкий цементный завод”», ООО «Кузнецкие металлоконструкции» и другие.
Основные загрязняющие
вещества: оксид углерода, сернистый ангидрид (диоксид серы), оксиды азота, выбросы
коксохимического производства, твердые вещества.
Кузнецкий район. На территории района размещены: ОАО «РУСАЛ Новокузнецк», ОАО «Кузнецкие ферросплавы», ОАО «Завод Универсал», филиал «Кузнецкая ТЭЦ» ОАО «Кузбассэнерго», ОАО «Органика» и другие.
Основные загрязняющие вещества: оксид углерода, диоксид серы, оксиды азота, газообразные фтористые соединения, твердые вещества, бенз(а)пирен.
Орджоникидзевский район. На территории района размещены: филиал «Шахта “Абашевская”» ОАО «ОУК “Южкузбассуголь”», ОАО ЦОФ «Абашевская», МКП «Теплоэнергия», ООО «АТП “Южкузбассуголь”», ОАО «Орджоникидзевское АТП» и другие.
Основные загрязняющие вещества: метан, оксид углерода, диоксид серы, оксиды азота, углерод (сажа), зола углей, пыль.
Куйбышевский район. На территории района размещены:
ООО «Авангард-Бетон», Кемеровская дистанция гражданских сооружений,
водоснабжения и водоотведения, ОАО «Новокузнецкий хладокомбинат»,
предприятия транспорта (в том числе железнодорожного) и связи, районные
котельные и другие.
Основные загрязняющие вещества: оксид углерода, диоксид серы, зола углей.
Air pollution and health | UNECE
Загрязнение воздуха в настоящее время считается самой большой угрозой здоровью из-за окружающей среды в мире, ежегодно приводя к 7 миллионам случаев смерти во всем мире. Загрязнение воздуха вызывает и усугубляет ряд заболеваний — от астмы до рака, болезней легких и болезней сердца. Международное агентство по изучению рака классифицирует канцерогенное для человека загрязнение наружного воздуха и твердые частицы, как один из его основных компонентов.Таким образом, в соответствии с последними оценками Всемирной организации здравоохранения, подверженность влиянию загрязненного воздуха, является более важным фактором риска для основных неинфекционных заболеваний, чем считалось ранее. Загрязнение воздуха является крупнейшим источником бремени болезней из окружающей среды.
Основными веществами, влияющими на здоровье, являются: оксиды азота (NOx), оксиды серы (SOx), озон и твердые частицы, причем последние — особенно твердые частицы размером менее 2,5 микрон (PM 2,5) — вызывают наибольшее беспокойство, поскольку эти крошечные частицы проникают глубоко в легкие, влияя как на дыхательную, так и на сосудистую системы. Как степень, так и продолжительность воздействия загрязненного воздуха влияют на состояние здоровья.
Как степень, так и продолжительность воздействия загрязненного воздуха влияют на состояние здоровья.
В Европейском регионе загрязнение воздуха затрагивает почти каждого отдельного человека, причем более 90% граждан подвергаются воздействию ежегодных уровней содержания мелких твердых частиц, превышающих руководящие принципы ВОЗ по качеству воздуха.
Воздействие загрязнения воздуха на здоровье человека вызывает растущую обеспокоенность, поскольку исследования раскрывают все больше связей между рядом серьезных заболеваний среди различных возрастных групп и загрязнением воздуха (например, диабет, неврологическое развитие, преждевременные роды, рождение с малым весом и т. д.).
Что мы делаем
Сокращая загрязнение воздуха, Конвенция устраняет самый большой в мире риск для здоровья окружающей среды в отношении неинфекционных заболеваний и, таким образом, помогает странам в предотвращении заболеваемости и преждевременной смертности, одной из целей в рамках Цели 3 в области устойчивого развития, касающейся хорошего здоровья и благополучия.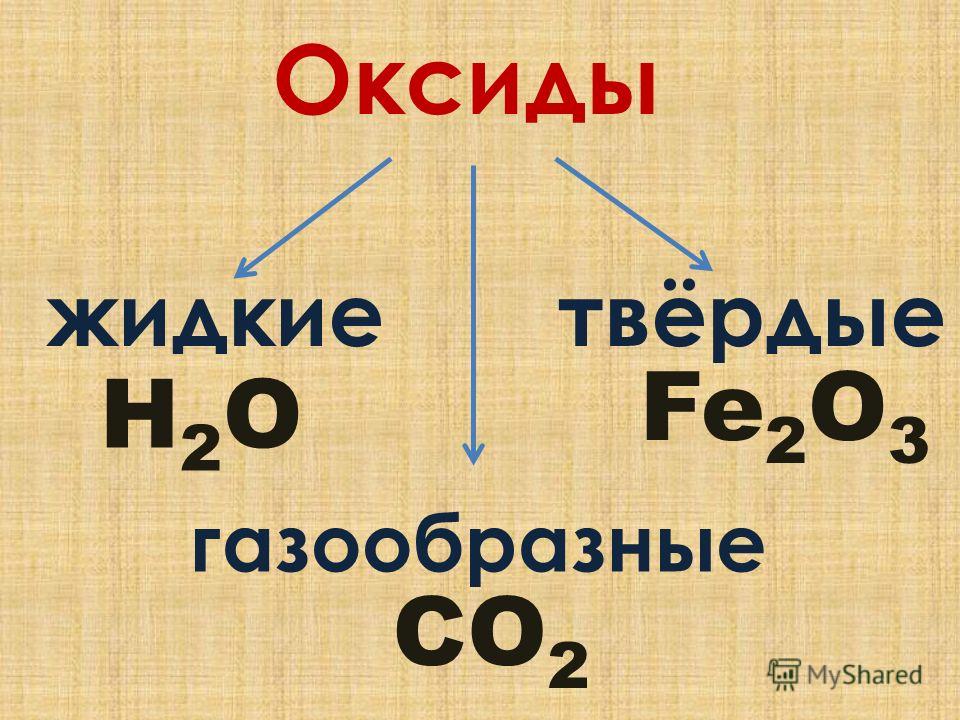 В дополнение к профилактике, Совместная целевая группа по аспектам воздействия загрязнения воздуха на здоровье человека оценивает как трансграничное загрязнение воздуха на большие расстояния влияет на здоровье человека, и помогает определить приоритеты для руководства будущими стратегиями мониторинга и борьбы с загрязнением. Группа также консультирует по вопросам мониторинга и моделирования деятельности, чтобы улучшить качество оценок. Работа группы основана на оценках концентраций загрязнения воздуха (особенно на основе Совместной программы мониторинга и оценки распространения загрязнителей воздуха на большие расстояния в Европе — ЕМЕП), а также на результатах оценки опасности, проведенной ВОЗ.
В дополнение к профилактике, Совместная целевая группа по аспектам воздействия загрязнения воздуха на здоровье человека оценивает как трансграничное загрязнение воздуха на большие расстояния влияет на здоровье человека, и помогает определить приоритеты для руководства будущими стратегиями мониторинга и борьбы с загрязнением. Группа также консультирует по вопросам мониторинга и моделирования деятельности, чтобы улучшить качество оценок. Работа группы основана на оценках концентраций загрязнения воздуха (особенно на основе Совместной программы мониторинга и оценки распространения загрязнителей воздуха на большие расстояния в Европе — ЕМЕП), а также на результатах оценки опасности, проведенной ВОЗ.
Что такое Твердое и жидкое шлакоудаление?
как показала практика жидкое шлакоудаление приводит к значительным потеря тепла и большому выбросу токсичных оксидов азота, поэтому ныне
В настоящее время существует 2 вида топок по способу удаления шлаковых остатков из котлов — топки с жидким и твердым шлакоудалением.
Твердое шлакоудаление подразумевает выпадение твердых спекшихся шлаковых масс в шлаковый бункер, а жидкое — стекание шлака в расплавленном виде при температуре около 1700 °С в шлаковые ванны, где он также гранулируется.
После разработки в 1950х гг конструкции топок с жидким шлакоудалением, в СССР начался активный переход на эту систему.
Как показала практика, жидкое шлакоудаление приводит к значительным потеря тепла и большому выбросу токсичных оксидов азота, поэтому ныне практикуется обратный переход на котлы с твердым шлакоудалением
Твердое шлакоудаление применяют для сжигания бурых, каменных углей, сланцев и фрезерного торфа.
Целесообразно в таких топках использовать топливо с тугоплавкой золой, с температурой начала жидкоплавного состояния более 1400°С, а также топлива с умеренными значениями этих температур.
Преимущества топок с твердым шлакоудалением:
— более низкие тепловые напряжения и более низкую температуру газов в зоне ядра горения;
— оксиды азота образуются только из азотосодержащей массы топлива, тогда как в топках с жидким шлакоудалением при температуре до 1700 °С образуются еще и термические оксиды азота.
— концентрация NOx в газах топок с твердым шлакоудалением в 2-3 раза ниже, чем с жидким.
Недостатком котлов, имеющих твердое шлакоудаление:
— недожог топлива и большой вынос золы через дымовые трубы;
— количество уловленной золы составляет лишь до 10% золосодержания топлива, что приводит к быстрому изнашиванию конвективных поверхностей котлов и дополнительным затратам на золоулавливание.
Топочные камеры, использующие твердое шлакоудаление, конструктивно изготавливают без изменения сечения топки по высоте.
В нижней части камеры выполняют холодную воронку, образованную сближением заднего и фронтового экранов с большим уклоном (50-60°).
Благодаря этому температура газов в нижней части топки снижается, расплавленные частицы шлака, выпадающие из ядра факела, быстро отвердевают и скатываются по экранированным поверхностям воронки в шлакоприемник.
Твердое шлакоудаление делает топки очень чувствительными к шлакованию, то есть появлению наростов шлака на стенах.
При недостаточном охлаждения стен холодной воронки, или малом их наклоне жидкие капли шлака не гранулируются, а твердый шлак, накапливающийся на скатах, размягчается, а затем прилипает к холодным скатам.
Значительные отложения, периодически отрываются и падают в горловину воронки, вызывая затруднения в работе шлакоудаляющих устройств.
Поэтому большое значение для этого типа топок имеет организация горения и компоновка горелочных устройств.
Из шлакоприемника шлак в остывшем виде механически удаляется в канал шлакозолоудаления.
Далее твердое шлакоудаление может быть организовано тремя способами: механическим, гидравлическим, пневматическим.
Самый простой способ удаления шлака — с помощью механических средств — грейферов, скреперов, а также ленточных, шнековых, скребковых транспортеров.
Последние особенно широко применяются для удаления шлака.
На топливных электростанциях (ТЭС) шлак чаще всего удаляется гидравлическим способом, где движущей силой является вода.
Также для перемещения шлаковых остатков используют воздух — сжатый или вакуум.
Во многих случаях применяют раздельное удаление: золы — пневматическим способом, шлака — гидравлическим. На небольших котельных используется вакуумное удаление золы и шлака.
Техпроцесс твердого шлакуоудаления.
Распределение температуры в топочной камере при удалении шлака в твердом состоянии характеризуется изотермами, показанными на рис 1.
Наивысшая температура устанавливается в ядре факела в центральной части топки, располагающемся примерно на уровне горелок.
В результате отдачи теплоты топочным экранам около них располагается изотерма с относительно низкой температурой.
Рис. 1. Топка с твердым шлакоудалением:
1 — холодная воронка; 2 — шлаковая ванна с водой;
3 — канал гидрозолоудаления; 4 — горелка; 5 — настенные экраны;
6 — ядро факела; 7 — шнековый шлакоудаляющий механизм; в — электродвигатель.
По мере перемещения расплавленной в ядре факела золы к периферии и попадания в область сравнительно низкой температуры золовые частицы охлаждаются и затвердевают.
Частицы золы при нагреве в ядре факела и охлаждении затем около топочных экранов дважды проходят все стадии изменения физического состояния от твердого до жидкого (или размягченного) и обратно.
На пути движения вверх частицы золы также охлаждаются вместе с газами и должны выноситься из топки в гранулированном (отвердевшем) состоянии. Топочные камеры, работающие с твердым шлакоудалением, по конструкции выполняются открытыми, т.е. без изменения сечения топки по высоте.
Отличительная особенность этих топок — наличие в нижней части топки холодной воронки, образованной путем сближения фронтового и заднего экранов с большим уклоном (50…60°) до расстояния b’ = 1,0…1,2 м.
За счет этого быстро снижается температура газов в нижней части топки, и выпадающие из ядра факела расплавленные шлаковые частицы, попадая в эту зону, отвердевают (гранулируются) снаружи и по крутым скатам воронки ссыпаются в шлакоприемную ванну.
Количество шлака, уловленного таким способом через холодную воронку, невелико и составляет 5…10% общего золосодержания топлива, т.е. аШЛ = 0,05…0,10.
Гранулированные шлаковые частицы непрерывно удаляются из ванны специальным механизмом.
Водяная ванна выполняет одновременно роль гидрозатвора, препятствующего проникновению снизу в топку холодного воздуха.
Аэродинамика топочного объема должна быть так организована, чтобы вблизи настенных экранов температура газов была не выше характерной температуры золы tA (см. § 3.3), начиная с которой золовые частицы становятся липкими и создают опасность шлакования стен.
На рис. 2 показано, как влияет тепловое напряжение сечения топки qf на распределение температур по сечению.
При высоких тепловых напряжениях увеличивается температура газов вблизи стен, что создает опасность их шлакования.
Поэтому средние тепловые напряжения сечения топочной камеры при твердом шлакоудалении, как правило, должны иметь невысокие значения (qf = 3…4 МВт/м2).
Это неизбежно приводит к увеличению размеров сечения топочных камер.
Для прочного удержания футеровки вначале на трубы экранов со стороны топочного объема обычно приваривают шипы (диаметром 10 мм и длиной 15…18 мм) и затем наносят слой изоляции (рис.2).
Рис. 2. Топочная камера с жидким шлакоудалением: а — общий вид топки; б — вид футерованного экрана;
1 — камера сгорания; 2 — под топки; 3 — шлаковая летка;
4 — камера охлаждения; 5 — труба; 6 — шипы до их покрытия обмазкой;
7 — огнеупорная обмазка труб (футеровка) по шипам.
Подовая часть топки выполняется горизонтальной или слабонаклонной к центру топки.
Здесь на трубы пода накладывают 2…3 слоя огнеупорного кирпича на огнеупорной связке.
В центре пода оставляется 1 или 2 футерованных отверстия для слива шлака (летка) размером около 500…800 мм.
Расплавленный шлак переливается через край и тонкими струями стекает в шлаковую ванну, где при контакте с водой отвердевает.
Повышению уровня температуры в этой зоне способствует 2-сторонний пережим топки, который уменьшает теплоотдачу радиацией в верхнюю часть топки, где открытые экраны имеют более низкую температуру.
При жидком шлакоудалении через шлаковую летку удаляется до 20…30% минеральной массы топлива в виде расплавленного шлака.
Камера охлаждения полностью экранирована открытыми трубами.
Здесь завершается сжигание недогоревшей части топлива и охлаждение продуктов сгорания до необходимой температуры на выходе, при которой должна гранулироваться вся зола в объеме уходящих из топки газов.
По конструкции топочные камеры с жидким шлакоудалением выполняются 1-камерными открытыми и полуоткрытыми (с пережимом) , а также 2-камерными.
В топочных устройствах с пережимом за счет покрытия футеровкой настенных экранов в зоне горения достигается высокая температура газов 1600…1800°С, которая на 150…200°С выше температуры tН. Ж.
Ж.
Объемное тепловое напряжение в камере горения выше среднего по топке в целом в 4…5 раз и составляет qК.Гv = 500…800 кВт/м3.
В циклонных камерах горения за счет тангенциального ввода горячего воздуха (горизонтальные циклоны) или угловой установки горелок с тангенциальным направлением струй (вертикальные предтопки) создается интенсивное вихревое движение горящего факела.
В циклоне уровень температур более высокий — 1700…1900°С, а тепловые напряжения объема достигают 2…4 МВт/м3.
Однако за счет более низких тепловых напряжений значительной по размерам камеры (зоны) охлаждения газов среднее значение qv для топочного устройства только на 20…30% выше, чем в топках с твердым удалением шлаков.
Доля удаления шлаков в жидком виде составляет аШЛ = 0,6…0,7.
Более высокий процент улавливания золы позволяет по условиям износа металла поверхностей повысить скорость продуктов сгорания в конвективных газоходах, что интенсифицирует теплообмен и уменьшает габариты и затрату металла поверхностей нагрева.
Основной недостаток топок с жидким шлакоудалением — опасность застывания шлака при пониженной нагрузке котла, отсюда известные ограничения DМИН.
Топки с жидким шлакоудалением применяются в основном при сжигании слабореакционных топлив (при VгЛ < 15%) с умеренными значениями температуры плавления золы (tС ≈ 1300…1350°С).
ТУГОПЛАВКИЕ ОКСИДЫ — это… Что такое ТУГОПЛАВКИЕ ОКСИДЫ?
- ТУГОПЛАВКИЕ ОКСИДЫ
соединения металлов с кислородом, имеющие высокую tпл. Кроме простых Т. о. (образов, одним металлом), в технике применяют сложные оксиды, состоящие из двух и более разл. оксидов металлов в виде твёрдых р-ров или хим. соединений. Примеры Т. о.: Al2O3. UO32, BeO, HfO2, ThO2. ZrO2. Т. о. наиболее широко используются в радиотехнич.
 , металлургич., хим. отраслях пром-сти, в ядерной энергетике, а также в ракетной и космич. технике.
, металлургич., хим. отраслях пром-сти, в ядерной энергетике, а также в ракетной и космич. технике.
Большой энциклопедический политехнический словарь. 2004.
- ТУГОПЛАВКИЕ МЕТАЛЛЫ
- ТУГОПЛАВКИЕ СОЕДИНЕНИЯ
Смотреть что такое «ТУГОПЛАВКИЕ ОКСИДЫ» в других словарях:
ТУГОПЛАВКИЕ ОКСИДЫ — соединения металлов с кислородом, имеющие высокую температуру плавления. Кроме простых Т. о. (образованных одним металлом), в технике применяют сложные оксиды, состоящие из двух и более различных оксидов металлов в виде твёрдых растворов или хим … Большая политехническая энциклопедия
Тугоплавкие оксиды — соединения металлов с кислородом, имеющие высокую tпл. Кроме простых тугоплавких оксидов (образованных одним металлом), в технике применяют сложные оксиды, состоящие из двух и более различных оксидов металлов в виде твердых растворов или… … Энциклопедический словарь по металлургии
ТУГОПЛАВКИЕ ОКСИДЫ — соединения металлов с кислородом, имеющие высокую tпл.
 Кроме простых тугоплавких оксидов (образованным одним металлом), в технике применяют сложные оксиды, состоящие из двух и более различных оксидов металлов в виде твердых растворов или… … Металлургический словарь
Кроме простых тугоплавких оксидов (образованным одним металлом), в технике применяют сложные оксиды, состоящие из двух и более различных оксидов металлов в виде твердых растворов или… … Металлургический словарьТУГОПЛАВКИЕ ВЫСОКОТЕМПЕРАТУРНЫЕ СОЕДИНЕНИЯ — хим. соединения металлов, обладающих высокими температурами разложения в твёрдом состоянии без участия жидкой фазы, с бором (бориды), углеродом (карбиды), азотом (нитриды), кремнием (силициды), кислородом (см. ). Высокотемпературные и тугоплавкие … Большая политехническая энциклопедия
ТУГОПЛАВКИЕ СОЕДИНЕНИЯ — соединения металлов с В (смотри Бориды), С (смотри Карбиды), N2 (смотри Нитриды), Si (смотри Силициды), O2 (смотри Тугоплавкие оксиды), обладающие высокой tпл. Тугоплавкие соединения разделяют на металлоподобные и неметаллические. К тугоплавким… … Металлургический словарь
ТУГОПЛАВКИЕ СОЕДИНЕНИЯ — соединения металлов, обладающих высокими темп рамп плавления, с бором (см.
 Бориды), углеродом (см. Карбиды), азотом (см. Нитриды), кремнием (см. Силициды), кислородом (см. Тугоплавкие оксиды). Т. с. делятся на 2 группы: металлоподобные и… … Большой энциклопедический политехнический словарь
Бориды), углеродом (см. Карбиды), азотом (см. Нитриды), кремнием (см. Силициды), кислородом (см. Тугоплавкие оксиды). Т. с. делятся на 2 группы: металлоподобные и… … Большой энциклопедический политехнический словарьОксиды — Оксид (окисел, окись) бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй… … Википедия
КЕРМЕТЫ — искусств. материалы, получаемые прессованием и спеканием (см. Порошковая металлургия) керамич. и металлич. порошков. К. обладают рядом ценных св в, присущих как керамике, так и металлу. В К. в качестве керамич. составляющей используют тугоплавкие … Большой энциклопедический политехнический словарь
неметаллические включения — Инородные образования в жидких и тв. металлах и сплавах — хим. соединения металлов с неметаллами.
 Н. в. классифицируют по хим., минералогам, составу, происхождению. По хим. составу н. в. подразделяют на: алюминатные (осн. составляющая… … Справочник технического переводчика
Н. в. классифицируют по хим., минералогам, составу, происхождению. По хим. составу н. в. подразделяют на: алюминатные (осн. составляющая… … Справочник технического переводчиканеметаллические включения — [nonmetalic inclusions] инородные образования в жидких и твёрдых металлах и сплавах химические соединения металлов с неметаллами. Неметаллические включения классифицируют по химическому, минералогическому составу, происхождению. По химическому… … Энциклопедический словарь по металлургии
Оксиды, их классификация. Cвойства оксидов в свете ТЭД
Оксиды – это сложные вещества, состоящие из двух элементов, одним из которых является кислород в степени окисления -2. Следовательно, оксиды – это бинарные соединения.
По
агрегатному состоянию они бывают жидкими, примером такого оксида
является вода, или оксид водорода, примером твердого оксида
является уже известный вам оксид кремния (IV),
или песок, а также различные разновидности кварца;
примером газообразных оксидов являются углекислый газ, или оксид
углерода (IV), а также угарный газ,
или оксид углерода (II).
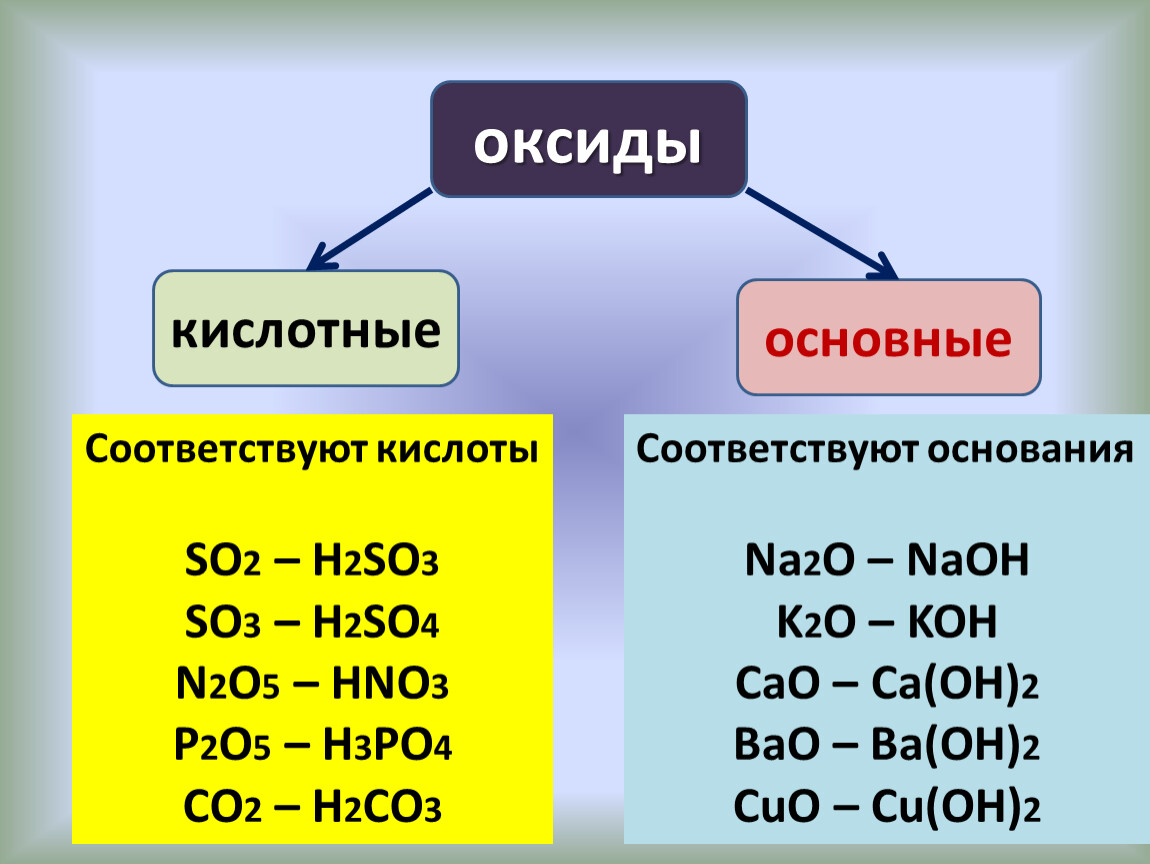
По химическим свойствам оксиды делятся на солеобразующие и несолеобразующие. Несолеобразующие оксиды не реагируют с кислотами и основаниями, а также не образуют солей. К несолеобразующим оксидам относятся такие оксиды, как оксид углерода (II) – CO, оксид азота (I) – N2O и оксид азота (II) – NO. К солеобразующим оксидам относятся основные, амфотерные и кислотные.
Основные
оксиды – это оксиды, которым соответствуют основания. К
основным оксидам относятся оксиды металлов I
и II A
группы, а также оксиды металлов с небольшими степенями
окисления (+1, +2). Кроме того, все основные оксиды являются твёрдыми
веществами. Например, оксид магния (MgO) –
это основный оксид, потому что магний – металл II
A группы,
ему соответствует основание Mg(OH)2. CrO – тоже основный оксид,
т.к. у хрома степень окисления в данном случае +2, этому оксиду соответствует
основание – Cr(OH)2.
Na2O
– основный оксид, т.к. натрий – металл I
A группы,
ему соответствует основание NaOH.
CrO – тоже основный оксид,
т.к. у хрома степень окисления в данном случае +2, этому оксиду соответствует
основание – Cr(OH)2.
Na2O
– основный оксид, т.к. натрий – металл I
A группы,
ему соответствует основание NaOH.
Основные оксиды вступают в реакции обмена с кислотами. При этом образуется соль и вода. Для того чтобы в этом убедиться, проведём эксперимент: поместим в пробирку немного порошка оксида меди (II), как видите, он чёрного цвета, в эту пробирку нальём раствора серной кислоты и слегка нагреем. Постепенно проходит реакция, т.к. порошок начинает растворяться. Чтобы убедиться в том, что в результате реакции образуется соль, несколько капель содержимого пробирки поместим на предметное стекло и выпарим, после чего на стекле появляются кристаллы соли.
CuO + H2SO4 = CuSO4 + H2O
CuO + 2H+ = Cu2+ + H2O
Основные
оксиды вступают в реакции соединения с кислотными оксидами, при этом образуются
соли. Например, при взаимодействии оксида натрия с оксидом
фосфора (V) образуется соль –
фосфат натрия, в результате взаимодействия оксида магния с оксидом серы (VI)
образуется соль – сульфат магния, а при взаимодействии оксида кальция с оксидом
углерода (IV) образуется соль –
карбонат кальция.
Например, при взаимодействии оксида натрия с оксидом
фосфора (V) образуется соль –
фосфат натрия, в результате взаимодействия оксида магния с оксидом серы (VI)
образуется соль – сульфат магния, а при взаимодействии оксида кальция с оксидом
углерода (IV) образуется соль –
карбонат кальция.
3Na2O + P2O5 = 2Na3PO4
MgO + SO3 = MgSO4
CaO + CO2 = CaCO3
Основные
оксиды вступают в реакции соединения с водой с образованием щелочей. Если
образуется нерастворимое основание, то такая реакция не идёт. Например,
если мы нальём в две пробирки воды и капнем туда несколько капель лакмуса, а
затем поместим в первую пробирку оксид кальция, а в другую оксид меди (II),
то реакция у нас идёт только в первой пробирке, т.к. образовалась щёлочь и
лакмус изменил свою окраску на синюю, во второй пробирке изменений нет, т.к.
оксид меди (II) не реагирует с водой,
ведь Cu(OH)2
– нерастворимое в воде основание.
образовалась щёлочь и
лакмус изменил свою окраску на синюю, во второй пробирке изменений нет, т.к.
оксид меди (II) не реагирует с водой,
ведь Cu(OH)2
– нерастворимое в воде основание.
CaO + H2O = Ca(OH)2
CaO + H2O = Ca2+ + 2OH—
CuO + H2O ≠
Кислотные
оксиды – это оксиды, которым соответствуют кислоты. К
кислотным оксидам относятся оксиды неметаллов и оксиды металлов с большими
степенями окисления. Например, оксиду азота (V)
соответствует азотная кислота, оксиду фосфора (V)
– фосфорная кислота, оксиду серы (IV)
– сернистая кислота, оксиду серы (VI)
– серная кислота, оксиду кремния (IV)
– кремниевая кислота, оксиду углерода (IV)
– угольная кислота, оксиду хрома (VI)
– хромовая кислота, оксиду марганца (VII)
– марганцевая кислота.
N2O5 → HNO3
P2O5 → H3PO4
SO2 → H2SO3
SO3 → H2SO4
SiO2 → H2SiO3
CO2 → H2CO3
CrO3 → H2CrO4
Mn2O7 → HMnO4
Кислотные оксиды вступают в реакции обмена с основаниями, при этом образуется соль и вода. Если через пробирку с известковой водой пропустить углекислый газ, то известковая вода мутнеет, следствие образования соли – карбоната кальция.
CO2 + Ca(OH)2 = CaCO3↓ + H2O
CO2 + Ca2+ + 2OH— = CaCO3↓ + H2O
Кислотные
оксиды вступают в реакции соединения с основными оксидами,
при этом образуются соли. Например, в результате взаимодействия оксида
серы (IV) и оксида калия
образуется соль – сульфит калия, в результате взаимодействия оксида
кремния (IV) с оксидом натрия при
нагревании, образуется соль – силикат натрия, при взаимодействии оксида
азота (V) с оксидом бария,
образуется соль – нитрат бария.
Например, в результате взаимодействия оксида
серы (IV) и оксида калия
образуется соль – сульфит калия, в результате взаимодействия оксида
кремния (IV) с оксидом натрия при
нагревании, образуется соль – силикат натрия, при взаимодействии оксида
азота (V) с оксидом бария,
образуется соль – нитрат бария.
SO2 + K2O = K2SO3
SiO2 + Na2O = Na2SiO3
N2O5 + BaO = Ba(NO3)2
Кроме
этого, кислотные оксиды вступают в реакции соединения с водой, при этом образуются
кислоты, однако эти реакции возможные, если оксид растворим в воде.
Для этого подтверждения, нальём в одну пробирку дистиллированной воды, а в
другую – раствор углекислого газа (газированной воды). В первую пробирку
добавим оксида кремния (IV).
А затем в каждую из пробирок добавим несколько капель лакмуса. В первой
пробирке изменений нет, а во второй лакмус окрасился в красный цвет, значит, во
второй пробирке кислота. В первой пробирке кислоты не образовалось, потому что
оксид кремния (IV) не растворим в воде.
В первую пробирку
добавим оксида кремния (IV).
А затем в каждую из пробирок добавим несколько капель лакмуса. В первой
пробирке изменений нет, а во второй лакмус окрасился в красный цвет, значит, во
второй пробирке кислота. В первой пробирке кислоты не образовалось, потому что
оксид кремния (IV) не растворим в воде.
SiO2 + H2O ≠
CO2 + H2O ↔ H2CO3
твердооксидных топливных элементов
твердооксидных топливных элементовТвердооксидные топливные элементы
от
Эрнест Гарнизон
Это вводный курс к углубленному уроку по твердооксидным топливным элементам. Я решил, что Solid Oxide — лучший вариант, так как не было дорогих электродов и электролит был твердым.
Цель этой веб-страницы — познакомить с альтернативными источниками энергии, которые теперь доступно.Топливный элемент в настоящее время Используется на небольших строительных площадках по всему миру.
Основные реакции
2H 2 + O 2 ® 2H 2 O + 2e —
Основные сведения о топливных элементах
Что такое топливный элемент?
Топливо Ячейка — это устройство, которое генерирует электричество с помощью химическая реакция.Каждый топливный элемент имеет два электрода, один положительный и один отрицательный, называемые, соответственно, катод и анод. Реакции, которые производят электричество проходит на электродах.
Каждый топливный элемент также имеет электролит, который несет электрически заряженные частицы от одного электрода к другой, и катализатор, который ускоряет реакции на электроды.
Водород является основным топливом, но для топливных элементов также требуется кислород. Топливные элементы очень привлекательны тем, что они генерируют электричество с очень небольшим загрязнением водород и кислород, используемые для производства электроэнергии в конечном итоге объединяются с образованием безвредного побочного продукта, а именно вода.
Один деталь терминологии: один топливный элемент генерирует крошечное количество электричества постоянного тока (DC).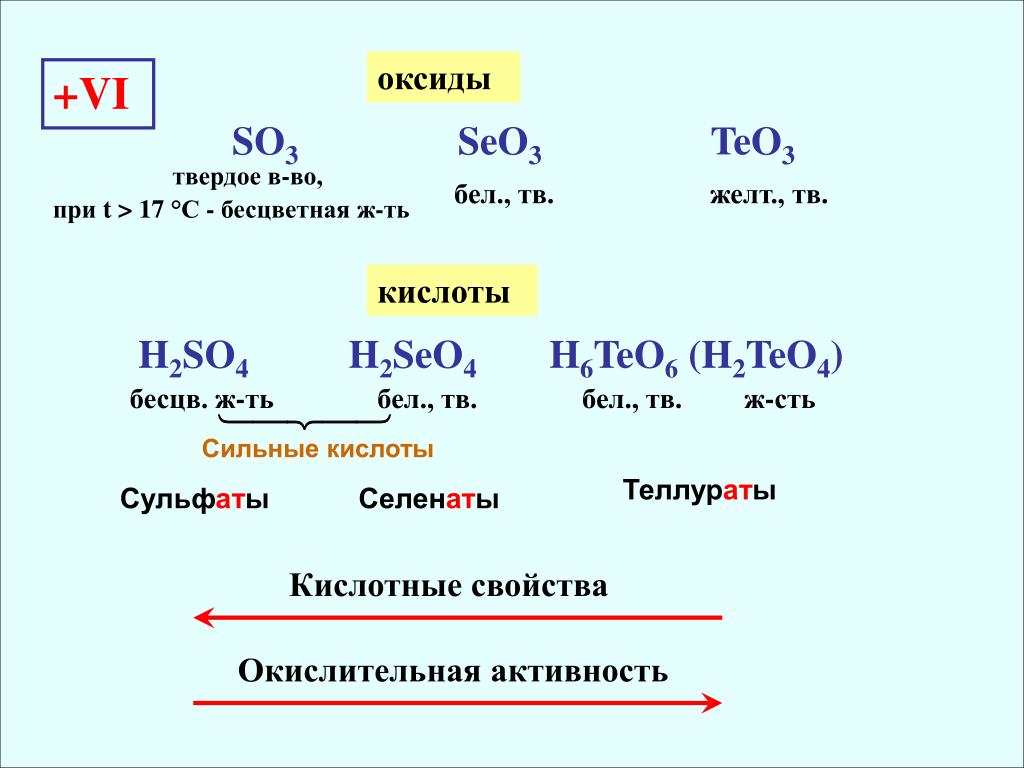 В На практике многие топливные элементы обычно собираются в куча. Ячейка или стопка, принципы одинаковы.
В На практике многие топливные элементы обычно собираются в куча. Ячейка или стопка, принципы одинаковы.
Как работают топливные элементы?
Топливный элемент предназначен для производства электрического ток, который может быть направлен за пределы клетки, чтобы делать работа, например, питание электродвигателя или освещение лампочка или город.Из-за электричества ведет себя, этот ток возвращается в топливный элемент, завершая электрическую схему.
Есть несколько видов топливных элементов, и каждый работает немного иначе. Но в общих чертах атомы водорода входят в топливный элемент на аноде, где происходит химическая реакция лишает их электронов. Атомы водорода теперь ионизированы и несут положительный электрический обвинение. Отрицательно заряженные электроны обеспечивают ток через провода для работы. Если переменный ток (AC), выход постоянного тока топливного элемента должен быть проходит через преобразователь, называемый инвертором.
Атомы водорода теперь ионизированы и несут положительный электрический обвинение. Отрицательно заряженные электроны обеспечивают ток через провода для работы. Если переменный ток (AC), выход постоянного тока топливного элемента должен быть проходит через преобразователь, называемый инвертором.
Кислород попадает в топливный элемент на катоде, а в некоторых элементах типы (например, проиллюстрированный выше), он там сочетается с электронами, возвращающимися из электрического цепи и ионы водорода, которые прошли через электролит с анода.В других типах клеток кислород собирает электроны, а затем проходит через электролит к аноду, где он соединяется с ионы водорода.
электролит играет ключевую роль. Он должен разрешать только соответствующие ионы проходят между анодом и катодом.Если бы свободные электроны или другие вещества могли путешествовать через электролит они нарушили бы химический реакция.
Ли они объединяются на аноде или катоде, вместе водород и кислород образует воду, которая стекает из клетки. Пока поскольку топливный элемент снабжен водородом и кислородом, он будет производить электричество.
Даже лучше, поскольку топливные элементы создают электричество химически, а не путем сжигания, они не подлежат термодинамические законы, ограничивающие обычную электростанцию. Следовательно, топливные элементы более эффективны в извлечении энергии из топливо.Отработанное тепло некоторых ячеек также может быть еще больше повышая эффективность системы.
Следовательно, топливные элементы более эффективны в извлечении энергии из топливо.Отработанное тепло некоторых ячеек также может быть еще больше повышая эффективность системы.
Так почему я не могу пойти и купить горючее? клетка?
Базовый работу топливного элемента может быть несложно проиллюстрировать.Но строить недорого, экономно, надежные топливные элементы — дело гораздо более сложное.
Ученые изобретатели разработали множество различных типов и размеры топливных элементов в поисках большего эффективность, и технические детали каждого типа различаются. Многие из вариантов, которые стоят перед разработчиками топливных элементов: сдерживается выбором электролита. Дизайн электроды, например, и материалы, используемые для изготовления они зависят от электролита. Сегодня основная Типы электролитов: щелочь, расплавленный карбонат, фосфорная кислота, протонообменная мембрана (PEM) и твердый оксид.Первые три — жидкие электролиты; последние два — твердые тела.
Многие из вариантов, которые стоят перед разработчиками топливных элементов: сдерживается выбором электролита. Дизайн электроды, например, и материалы, используемые для изготовления они зависят от электролита. Сегодня основная Типы электролитов: щелочь, расплавленный карбонат, фосфорная кислота, протонообменная мембрана (PEM) и твердый оксид.Первые три — жидкие электролиты; последние два — твердые тела.
Тип топлива также зависит от электролита. Некоторым клеткам нужно чистый водород, поэтому требуется дополнительное оборудование, такое как риформер для очистки топлива. Другие клетки могут терпят некоторые примеси, но может потребоваться более высокая температуры, чтобы работать эффективно. Жидкие электролиты циркулировать в некоторых ячейках, что требует насосов. Тип электролита также диктует, что клетки работают температура расплавленных карбонатных элементов нагревается, просто как следует из названия.
Жидкие электролиты циркулировать в некоторых ячейках, что требует насосов. Тип электролита также диктует, что клетки работают температура расплавленных карбонатных элементов нагревается, просто как следует из названия.
Каждый тип топливного элемента имеет преимущества и недостатки по сравнению с другие, и ни один еще не является достаточно дешевым и эффективным широко заменить традиционные способы производства электроэнергии, такая угольная, гидроэлектрическая или даже атомная энергия растения.
В следующем списке описаны пять основных видов топлива. клетки. Более подробную информацию можно найти в тех конкретные области этого сайта.
Различные типы топливных элементов.
Рисунок щелочной ячейки.
Щелочь топливные элементы работают на сжатом водороде и кислороде. Обычно они используют раствор гидроксида калия. (химически КОН) в воде в качестве электролита. КПД составляет около 70 процентов, а рабочий температура составляет от 150 до 200 C (примерно от 300 до 400 F).Мощность ячейки колеблется от 300 Вт (Вт) до 5 Вт. киловатт (кВт). Щелочные клетки использовались в Apollo космический корабль, чтобы обеспечить электричеством и питьем вода. Однако они требуют чистого водородного топлива, и их катализаторы на платиновых электродах дороги. И как и любая емкость, наполненная жидкостью, они могут протекать.
И как и любая емкость, наполненная жидкостью, они могут протекать.
Чертеж ячейки расплавленного карбоната
Расплавленный Карбонат топливные элементы (MCFC) используют высокотемпературные соединения соли (например, натрия или магния) карбонаты (химически, CO 3 как электролит.КПД колеблется от 60 до 80 процентов, а рабочая температура составляет около 650 C (1200 F). Установки мощностью до 2 МВт (МВт) были построены, и существуют проекты для блоков до 100 МВт. Высокая температура ограничивает ущерб от «отравление» клетки угарным газом и отходящее тепло может быть переработано для получения дополнительных электричество. Их никелевые электроды-катализаторы недорогой по сравнению с платиной, используемой в других клетки. Но высокая температура также ограничивает материалы и безопасное использование M C F C они могли бы вероятно, будет слишком жарко для домашнего использования. Также карбонат-ионы из электролита расходуются в реакциях, заставляя вводить углекислый газ в компенсировать.
Их никелевые электроды-катализаторы недорогой по сравнению с платиной, используемой в других клетки. Но высокая температура также ограничивает материалы и безопасное использование M C F C они могли бы вероятно, будет слишком жарко для домашнего использования. Также карбонат-ионы из электролита расходуются в реакциях, заставляя вводить углекислый газ в компенсировать.
фосфорная Кислота топливные элементы (PAFC) используют фосфорную кислоту в качестве электролит. КПД колеблется от 40 до 80 процентов, и рабочая температура составляет от 150 до 200 ° C (от 300 до 400 ° C). F). Существующая фосфорная кислота ячейки имеют мощность до 200 кВт, а блоки 11 МВт имеют был протестирован. P A F C s терпят окись углерода концентрация около 1,5 процента, что расширяет выбор топлива, которое они могут использовать. Если используется бензин, серу необходимо удалить. Платиновые электроды-катализаторы необходимы, а внутренние части должны выдерживать коррозионная кислота.
P A F C s терпят окись углерода концентрация около 1,5 процента, что расширяет выбор топлива, которое они могут использовать. Если используется бензин, серу необходимо удалить. Платиновые электроды-катализаторы необходимы, а внутренние части должны выдерживать коррозионная кислота.
Рисунок того, как работают топливные элементы на основе фосфорной кислоты и PEM.
Протонообменная мембрана (PEM) топливные элементы работают с полимерным электролитом в форма тонкого проницаемого листа. КПД около 40 до 50 процентов, а рабочая температура составляет около 80 C (около 175 F). Выходы ячеек в целом диапазон от 50 до 250 кВт. Твердый гибкий электролит не протекают и не трескаются, и эти элементы работают при низкой достаточная температура, чтобы сделать их подходящими для дома и машины. Но их топливо должно быть очищено, а платина катализатор используется с обеих сторон мембраны, поднимая расходы.
Но их топливо должно быть очищено, а платина катализатор используется с обеих сторон мембраны, поднимая расходы.
Чертеж твердооксидной ячейки
твердый Оксид топливные элементы (ТОТЭ) используют твердый керамический состав металла (например, кальция или циркония) оксиды (химически, O 2 ) как электролит.КПД составляет около 60 процентов, а рабочие температуры около 1000 C (около 1800 F). Мощность ячеек до 100 кВт. При таком высокие температуры, для извлечения риформинга не требуется водород из топлива, а отходящее тепло может быть переработано сделать дополнительное электричество. Однако высокий температурные ограничения применения блоков ТОТЭ, и они имеют тенденцию быть довольно большими. Пока твердые электролиты не могут течь, они могут треснуть.
Пока твердые электролиты не могут течь, они могут треснуть.
Давайте посмотрим, что вы узнали.
Чтобы перейти на страницу тестирования, щелкните здесь.
Это результаты исследования, проведенного в этом году в Северо-Западном университете на твердооксидный электролит. Электролит обычно CaO или ZrO и работает при температуре около 1000 C. Эффективность работы составляет около 60% и мощность около 100 кВтч.
- Одновременная оптимизация электрические характеристики и механическая прочность
- Минимизация электрических потерь
- Герметичные газовые уплотнения для предотвращения смешивания топлива и окислителя
- Технологичность
- Масштабируемость
- Сложность формирования отложений с помощью e.
 г. шламовое покрытие и ЭВД
г. шламовое покрытие и ЭВД - Узор по всей ширине трубки проще с плоскими поверхностями
- Большая ширина ячейки (1 см) может привести к резистивным потерям
Хорошие механические свойства
- Использует пористые опоры
- Высокое сопротивление
- Устраняет контакты высокого давления под давлением между ТОТЭ и ИС. тарелки
- Плоская геометрия трубы легко обрабатывается
- Маленькие элементы более устойчивы к дефектам тонкого электролита
- Маленькие (1-2 мм) ячейки минимизируют токи электрода, потери сопротивления
- Текущий поток вдоль поверхности, а не между отдельные части
- Поскольку пластины не соприкасаются, производственные допуски уменьшились
- Устраняет межсоединения и уменьшает количество полей потока на 2 (относительно планарного ТОТЭ
- Сплющенные трубки обеспечивают высокую объемную плотность и сводят к минимуму проблемы с герметизацией
Сравните потери ISOFC с плоской стопкой 10 см ´ 10 см SOFC
(Предположения: 0. 5 Вт / см 2 при 0,7 В, 0,2 Связаться с сопротивлением)
5 Вт / см 2 при 0,7 В, 0,2 Связаться с сопротивлением)
PSZ: TCE близко к YSZ
- относительно низкая ионная проводимость
- высокий перелом прочность
- проводимость, TCE (13,5 ´ 10 xx )
Возможные методы нанесения рисунка
- Теневые маски легко выравниваются на плоских подложках
- Легко сделать 0.Особенности 1 мм. В соответствии с 1 2 мм широкие ячейки
- Выравнивание маски необходимо, если куски удаляются между напылением (например, для спекания
Назад на страницу индекса SMART.
Energy IQ: Что такое твердооксидный топливный элемент и как работают топливные элементы
У инженерных сетей и микросетей много общего. Оба выполняют одну и ту же функцию — обеспечивать потребителей электроэнергией. Оба подвержены одним и тем же ограничениям — гарантируя, что выработка электроэнергии и электрическая нагрузка всегда равны. Однако их компоненты разные.
Оба подвержены одним и тем же ограничениям — гарантируя, что выработка электроэнергии и электрическая нагрузка всегда равны. Однако их компоненты разные.
имеют гораздо меньший масштаб, чем инженерные сети, и в результате включают компоненты, которые соответственно уменьшены в масштабе.
Вот основные компоненты микросети:
Ресурсы выработки электроэнергии в микросетях
Бьющееся сердце микросети состоит из набора ресурсов, генерирующих электроэнергию.Типичные ресурсы генерации в микросетях включают дизельные генераторы и / или генераторы природного газа, солнечные батареи и ветряные турбины.
Самые простые микросети обычно строятся вокруг одного или нескольких дизель-генераторов. Когда доступен природный газ, в число доступных опций также входят газовые генераторы. Например, более старые островные микросети основаны на небольшой электростанции, состоящей из нескольких дизельных двигателей, соединенных с генераторами переменного тока. Генераторы являются выбором по умолчанию для питания микросети, поскольку они могут покрывать широкий диапазон нагрузок и могут использоваться в качестве резервного источника питания.Они быстро запускаются, реагируют на изменения нагрузки и могут работать на различных видах топлива.
Генераторы являются выбором по умолчанию для питания микросети, поскольку они могут покрывать широкий диапазон нагрузок и могут использоваться в качестве резервного источника питания.Они быстро запускаются, реагируют на изменения нагрузки и могут работать на различных видах топлива.
Технология топливных элементов становится действенным вариантом для обеспечения электропитания микросетей по требованию. Топливные элементы могут работать на природном газе, водороде и других менее распространенных видах топлива. Хотя их стоимость остается слишком высокой для широкого использования, водородные топливные элементы рассматриваются как потенциальный источник маломасштабной электроэнергии без выбросов CO2.
Щелкните изображение, чтобы поближе познакомиться с компонентами микросетейПрерывистые источники энергии в микросетях
Стоимость солнечных панелей стала настолько низкой, что в некоторых регионах их установка в домах и на предприятиях является простой задачей. Университетские городки, промышленные предприятия и другие объекты, оснащенные микросетями, могут устанавливать солнечные батареи в большом количестве, что позволяет значительно сэкономить на счетах за электроэнергию. Фактически, многие строят микросети специально, чтобы иметь возможность лучше интегрировать и использовать свои солнечные ресурсы.
Университетские городки, промышленные предприятия и другие объекты, оснащенные микросетями, могут устанавливать солнечные батареи в большом количестве, что позволяет значительно сэкономить на счетах за электроэнергию. Фактически, многие строят микросети специально, чтобы иметь возможность лучше интегрировать и использовать свои солнечные ресурсы.
Накопитель энергии в микросетях
Многие домовладельцы иногда предпочитают дополнить свою домашнюю фотоэлектрическую установку аккумуляторной батареей. Точно так же многие владельцы микросетей включают в свои системы аккумуляторы энергии.При рекордно низкой цене на литий-ионные батареи, преимущества добавления ресурса хранения энергии часто оправдывают дополнительные затраты.
Например, аккумуляторные системы хранения энергии предоставляют услугу, известную как «сдвиг во времени». Батареи с синхронизацией по времени собирают дополнительную электроэнергию от негабаритной солнечной системы в течение дня, а затем разряжают батарею после захода солнца, чтобы удовлетворить потребности в ночной нагрузке. Точно так же батареи могут разряжаться, когда выходная мощность солнечной батареи не соответствует требованиям нагрузки, например, в короткие периоды пиковой нагрузки.Это позволяет владельцу максимально использовать прерывистые ресурсы.
Точно так же батареи могут разряжаться, когда выходная мощность солнечной батареи не соответствует требованиям нагрузки, например, в короткие периоды пиковой нагрузки.Это позволяет владельцу максимально использовать прерывистые ресурсы.
Еще одним преимуществом аккумуляторных систем является их способность мгновенно реагировать на изменения спроса на электроэнергию в микросети. Наличие батареи в качестве резервной емкости часто намного более рентабельно, чем использование дополнительного генератора на холостом ходу 24 часа в сутки, 7 дней в неделю на случай, если спрос неожиданно возрастет. Думайте о накоплении энергии как о жире в микросети, где хранится энергия.
Управление нагрузкой в микросетях
Некоторые владельцы микросетей имеют возможность активно управлять спросом на электроэнергию так же, как они управляют производством электроэнергии.
По умолчанию, когда большая электрическая машина запускается где-то в микросети, генераторы, питающие микросеть, должны быстро наращивать мощность, чтобы удовлетворить дополнительный спрос. У микросетей, которые активно управляют спросом, есть другой вариант. Они могут снизить спрос в другом месте микросети, например, временно отключив кондиционер в здании. В результате спрос и генерация снова уравновешиваются без увеличения генерации.
У микросетей, которые активно управляют спросом, есть другой вариант. Они могут снизить спрос в другом месте микросети, например, временно отключив кондиционер в здании. В результате спрос и генерация снова уравновешиваются без увеличения генерации.
Управление и связь в микросетях
Microgrids нуждается в мозге и нервной системе для безопасной и эффективной работы, поэтому необходимо обладать сложными системами управления микросетями.
Коммунальные сети большой площади обслуживают миллионы потребителей и обладают значительной инерцией, что ограничивает возможность быстрых неконтролируемых изменений. Микросети, напротив, включают меньше нагрузок и ресурсов и более чувствительны к изменениям нагрузки и генерации. Запуск нескольких больших электрических машин без гарантии того, что эквивалентное количество выработки доступно, — верный способ вывести из строя микросеть.
Система управления микросетью обычно включает в себя несколько контроллеров и датчиков, распределенных по ее территории. Система диспетчерского управления и сбора данных (SCADA) также необходима для сбора данных и распространения инструкций.
Система диспетчерского управления и сбора данных (SCADA) также необходима для сбора данных и распространения инструкций.
Если система SCADA — это нервная система микросети, то программное обеспечение для управления энергопотреблением — это мозг; это программное обеспечение может быть очень сложным. Функции искусственного интеллекта (ИИ) и машинного обучения позволяют современному программному обеспечению для управления энергопотреблением научиться лучше прогнозировать нагрузку со стороны потребителей на микросети и генерацию из возобновляемых источников, чтобы оптимизировать работу системы для наиболее рентабельной работы.Программное обеспечение для управления энергопотреблением обеспечивает максимальное использование возобновляемых ресурсов, минимизацию затрат на ископаемое топливо и поддержание надежности оборудования и микросети при распределении нагрузки в рамках параметров, указанных владельцем микросети.
Распределительные устройства, инверторы и другое оборудование
Наконец, микросети включают другие важные компоненты, такие как электрические кабели, автоматические выключатели, трансформаторы и многое другое. Эти компоненты представляют собой кости, мышцы и кровеносные сосуды микросети.Они подключают генерирующие ресурсы к потребителям и позволяют системе управления микросетью вносить изменения в состояние микросети.
Эти компоненты представляют собой кости, мышцы и кровеносные сосуды микросети.Они подключают генерирующие ресурсы к потребителям и позволяют системе управления микросетью вносить изменения в состояние микросети.
Автоматические переключатели, например, изолируют различные генерирующие активы, чтобы гарантировать, что, например, инвертор переменного тока, связанный с солнечной батареей, не подает электричество на дизельный генератор. Инверторы преобразуют мощность постоянного тока, подаваемую батареями или солнечными панелями, в мощность переменного тока, которая адекватно синхронизируется с другими ресурсами переменного тока в микросети.
Хотите узнать больше о микросетях? Возможно вам понравится:
Произошла ошибка при установке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie.Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie.Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.
Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.

Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт
не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к
остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Министерство энергетики инвестирует 34 миллиона долларов в разработку маломасштабных систем твердооксидных топливных элементов (SOFC)
ВАШИНГТОН, округ Колумбия — Сегодня Министерство энергетики США (DOE) объявило отбор из 12 проектов, которые получат около 34 миллионов долларов федерального финансирования в соответствии с объявлением о возможности финансирования (FOA), Small-Scale Solid Oxide Fuel Cell Systems и Разработка технологии гибридных электролизеров.
Настоящая FOA направлена на разработку передовых технологий, которые могут улучшить нынешнее состояние гибридных систем малых твердооксидных топливных элементов (SOFC), использующих технологии твердооксидных электролизеров, до точки коммерческой готовности для производства водорода и выработки электроэнергии.Он также добивается валидации ТОТЭ с использованием синтез-газа от объектов газификации.
«Администрация Трампа стремится сделать системы SOFC коммерчески доступными для производства водорода и электроэнергии. Выбор этих проектов для финансирования — огромный шаг к достижению этой цели », — сказал министр энергетики Дэн Бруйетт. «Работая с национальными лабораториями, академическими учреждениями и частным сектором, мы объединяем огромный объем знаний и опыта для развития — и, в конечном итоге, коммерциализации — этих технологий.
Выбор этих проектов для финансирования — огромный шаг к достижению этой цели », — сказал министр энергетики Дэн Бруйетт. «Работая с национальными лабораториями, академическими учреждениями и частным сектором, мы объединяем огромный объем знаний и опыта для развития — и, в конечном итоге, коммерциализации — этих технологий.
Это исследование является частью программы SOFC Управления ископаемой энергии (FE) Министерства энергетики США, которая направлена на создание высокоэффективной и рентабельной электроэнергии из угля и природного газа с практически нулевыми выбросами в атмосферу. Отобранные проекты направлены на достижение общей цели обеспечения эффективной и надежной электросети, а также защиты окружающей среды.
«ТОТЭ - это электрохимические устройства, которые преобразуют химическую энергию топлива и окислителя непосредственно в электрическую энергию.Они уникальны тем, что вырабатывают электричество в результате электрохимической реакции, а не в процессе горения », — сказал помощник министра по ископаемым источникам энергии Стивен Винберг. «Это означает, что ТОТЭ намного более эффективны и экологически безопасны, чем традиционные процессы производства электроэнергии».
«Это означает, что ТОТЭ намного более эффективны и экологически безопасны, чем традиционные процессы производства электроэнергии».
Отобранные для отбора кандидаты получили наивысшие технические баллы в своей области интересов в соответствии с DOE FOA, выпущенным в мае этого года. Чтобы узнать больше о 12 выбранных проектах, посетите веб-сайт FE.
###
Контакты для СМИ: (202) 586-4940
границ | Перовскитовый хромит с собранными на месте Ni-Co наносплавами: потенциальный бифункциональный электродный катализатор для твердооксидных ячеек
Введение
Быстрый рост мирового потребления ископаемого топлива в последние годы привел к некоторым серьезным экологическим проблемам, таким как парниковый эффект эффект (Pérez-Lombard et al., 2008). Поэтому исследователи разработали множество передовых технологий для решения этих проблем.Топливный элемент (FC) — это устройство, которое напрямую преобразует химическую энергию в электричество за пределами цикла Карно (O’hayre et al. , 2016). Этот процесс также осуществляется экологически безопасным способом со значительными экологическими преимуществами с точки зрения низкого уровня выбросов загрязняющих веществ.
, 2016). Этот процесс также осуществляется экологически безопасным способом со значительными экологическими преимуществами с точки зрения низкого уровня выбросов загрязняющих веществ.
Работающий в диапазоне температур от 500 до 800 ° C, твердооксидный топливный элемент (ТОТЭ) считается наиболее эффективным топливным элементом с гибким выбором топлива, включая углеводородное топливо (Stambouli and Traversa, 2002).Кроме того, высокая рабочая температура ускоряет кинетику окисления топлива, что позволяет избежать использования катализаторов из благородных металлов и значительно снизить общую стоимость системы. К сожалению, нынешнюю технологию для ТОТЭ по-прежнему сложно реализовать в крупных масштабах, в основном из-за неудовлетворительных характеристик и стабильности топливного электрода (анода) (Da Silva and de Souza, 2017). Топливные электроды обычно требуют высокой каталитической активности, хорошей проводимости, высокой пористости и совместимости с электролитами, а также соединителями. Ранее композит из кермета Ni-YSZ широко исследовался в качестве анода для ТОТЭ, который обеспечивает отличную ионную и электронную проводимость. Однако его низкая окислительно-восстановительная стабильность и быстрая дезактивация из-за осаждения углерода по-прежнему препятствуют его применению (Prakash et al., 2014).
Ранее композит из кермета Ni-YSZ широко исследовался в качестве анода для ТОТЭ, который обеспечивает отличную ионную и электронную проводимость. Однако его низкая окислительно-восстановительная стабильность и быстрая дезактивация из-за осаждения углерода по-прежнему препятствуют его применению (Prakash et al., 2014).
Альтернативным кандидатом на замену Ni-YSZ является семейство оксидов перовскита, которые обладают превосходной стабильностью при высоких температурах, широкими возможностями структурной перестройки, а также хорошей совместимостью с коммерческим материалом электролита (Sunarso et al., 2017). Оксид перовскита хромита лантана LaCrO 3-δ обладает превосходной химической, механической и термодинамической стабильностью. Легирование двухвалентного элемента, включая Sr или Ca, в позиции A приводит к переходу Cr 3+ в Cr 4+ , который создает больше электронных дырок в валентной зоне и, таким образом, улучшает электронную проводимость. Между тем, образовавшиеся кислородные вакансии вызывают ионную проводимость за счет компенсации заряда (то есть поддерживают электрическую нейтральность системы) (Setz et al. , 2015; Сарно и др., 2018).
, 2015; Сарно и др., 2018).
Однако применение хромита лантана в ТОТЭ все еще сдерживается его низкой каталитической активностью, в основном из-за отсутствия реактивных центров. Чтобы решить эту проблему, каталитически активные наночастицы металлов были внедрены на поверхность перовскита путем влажной пропитки (инфильтрации) или химического осаждения (Sfeir et al., 2001). Однако агломерация наночастиц неизбежно произойдет после длительной эксплуатации из-за слабой адгезии оксидов металлов, что приведет к необратимой деградации клеток (Jiang, 2006).
В качестве альтернативы был предложен способ выделения in-situ для преодоления этого барьера при изготовлении катализатора. Основная концепция распада in-situ заключается в растворении каталитических переходных металлов в структуре перовскита (в узлах B) в процессе подготовки воздуха (окислительная атмосфера) и их частичном выделении из решетки в восстановительной атмосфере. . Такой процесс представляет собой массив высокодисперсных наночастиц на перовскитовой подложке. По сравнению с методом инфильтрации, наночастицы, полученные с помощью растворения in-situ , были помещены в перовскитную матрицу, что свидетельствует о стабильной границе раздела металлических частиц и оксидов-носителей (Kwon et al., 2020). Кроме того, согласно исследованию Neagu et al., Ожидается, что растворенных частиц in-situ сохранят более высокую окислительно-восстановительную стабильность и лучшее сопротивление отложению углерода при работе с углеводородным топливом (Neagu et al., 2015).
По сравнению с методом инфильтрации, наночастицы, полученные с помощью растворения in-situ , были помещены в перовскитную матрицу, что свидетельствует о стабильной границе раздела металлических частиц и оксидов-носителей (Kwon et al., 2020). Кроме того, согласно исследованию Neagu et al., Ожидается, что растворенных частиц in-situ сохранят более высокую окислительно-восстановительную стабильность и лучшее сопротивление отложению углерода при работе с углеводородным топливом (Neagu et al., 2015).
Помимо методологии изготовления, введение второго металла (гостевой металл) для создания активного центра наносплава, как ожидается, позволит эффективно управлять свойствами катализатора металл / оксид.Например, было подтверждено, что сплавы на основе Ni лучше подавляют образование углеродных волокон, чем чистый Ni (An et al., 2011). Takanabe et al. продемонстрировали, что каталитическая активность катализатора из сплава Ni-Co постепенно увеличивается с увеличением содержания Ni, в то время как стойкость к коксу возрастает пропорционально количеству содержания Co (Takanabe et al. , 2005). Grgicak et al. изучили сплав Ni-Co по сравнению с одним металлическим Ni и отметили, что сплав Ni-Co проявляет очень стабильную активность, а также способствует электрохимической активности в углеродсодержащей среде в широком диапазоне температур (500–900 ° C) ( Grgicak et al., 2008). Следовательно, необходимо учитывать правильное соотношение Ni и Co для компромисса между реакционной активностью и стойкостью к закоксовыванию.
, 2005). Grgicak et al. изучили сплав Ni-Co по сравнению с одним металлическим Ni и отметили, что сплав Ni-Co проявляет очень стабильную активность, а также способствует электрохимической активности в углеродсодержащей среде в широком диапазоне температур (500–900 ° C) ( Grgicak et al., 2008). Следовательно, необходимо учитывать правильное соотношение Ni и Co для компромисса между реакционной активностью и стойкостью к закоксовыванию.
На основании вышеизложенного в данной работе был приготовлен перовскит из хромита лантана из сплава Ni-Co (LSC-NiCo) и систематически изучено влияние содержания Ni / Co и дефицита катионов на структурные и химические свойства. Электрохимические характеристики электрода с расплавленным сплавом Ni-Co оценивались как в режиме ТОТЭ, так и в режиме SOEC.Результаты показывают, что LSC-NiCo может быть многообещающим кандидатом для обратимых твердооксидных ячеек.
Методология эксперимента
Синтез материалов ячейки
Экспериментальная процедура изготовления электрода
Метод сжигания комплексообразования лимонной кислоты и этилендиаминтетрауксусной кислоты (ЭДТА) был применен для приготовления электродных материалов. Раствор прекурсора получают растворением стехиометрических количеств нитратов металлов в деионизированной воде с добавкой лимонной кислоты (C 6 H 8 O 7 ) и EDTA (C 10 H 16 N 2 O 8 ) в качестве кохелатирующих агентов.Нитраты металлов включают гексагидрат нитрата лантана (III) (La (NO 3 ) 3 · 6H 2 O), безводный нитрат стронция (Sr (NO 3 ) 2 ), нитрат хрома (III) нона гидрат (Cr (NO 3 ) 3 · 9H 2 O), гексагидрат нитрата никеля (II) (Ni (NO 3 ) 2 · 6H 2 O) и кобальт (II) гексагидрат нитрата (Co (NO 3 ) 2 · 6H 2 O). Молярное соотношение нитрата металла, ЭДТА и лимонной кислоты составляет 1: 1: 1.5. Затем pH раствора доводят до ~ 8 с помощью гидроксида аммония (NH 4 OH) для лучшего результата хелатирования. Затем раствор перемешивают и нагревают при 80 ° C до образования геля.
Раствор прекурсора получают растворением стехиометрических количеств нитратов металлов в деионизированной воде с добавкой лимонной кислоты (C 6 H 8 O 7 ) и EDTA (C 10 H 16 N 2 O 8 ) в качестве кохелатирующих агентов.Нитраты металлов включают гексагидрат нитрата лантана (III) (La (NO 3 ) 3 · 6H 2 O), безводный нитрат стронция (Sr (NO 3 ) 2 ), нитрат хрома (III) нона гидрат (Cr (NO 3 ) 3 · 9H 2 O), гексагидрат нитрата никеля (II) (Ni (NO 3 ) 2 · 6H 2 O) и кобальт (II) гексагидрат нитрата (Co (NO 3 ) 2 · 6H 2 O). Молярное соотношение нитрата металла, ЭДТА и лимонной кислоты составляет 1: 1: 1.5. Затем pH раствора доводят до ~ 8 с помощью гидроксида аммония (NH 4 OH) для лучшего результата хелатирования. Затем раствор перемешивают и нагревают при 80 ° C до образования геля. Гель быстро нагревают до 300 ° C и выдерживают при 300 ° C в течение 0,5–1 ч, чтобы произошел процесс самовозгорания геля с образованием порошка-прекурсора (порошка как такового). Затем порошки прекурсора измельчаются и спекаются при 1200 ° C в течение 5 часов с образованием единой фазы целевого оксида перовскита.Обозначение материалов приведено в таблице 1.
Гель быстро нагревают до 300 ° C и выдерживают при 300 ° C в течение 0,5–1 ч, чтобы произошел процесс самовозгорания геля с образованием порошка-прекурсора (порошка как такового). Затем порошки прекурсора измельчаются и спекаются при 1200 ° C в течение 5 часов с образованием единой фазы целевого оксида перовскита.Обозначение материалов приведено в таблице 1.
ТАБЛИЦА 1 . обозначение биметаллического эксперимента по легированию.
Катод из LSCF ((La 0,60 Sr 0,40 ) 0,95 Co 0,20 Fe 0,80 O 3-δ ) был приобретен из материалов топливных элементов, используемых в качестве воздушного электрода в этой работе.
Изготовление твердооксидных ячеек
Электродные чернила были изготовлены путем тщательного смешивания электродного порошка, GDC10 power (10% оксида церия, легированного гадолинием, материалы топливных элементов) и электродного клея в массовом соотношении 1.5: 1,5: 1,7 в фрезерном станке в течение 2 ч. Буферные слои GDC, введенные на границе раздела электродов и электролита, были получены путем смешивания порошка GDC10 с электродным клеем при весовом соотношении 1,7: 3. Буферные слои были нанесены с двух сторон электролита (диаметр 25 мм, толщина 0,3 мм, оксид циркония, легированный иттрием, 8 мол.%, Материалы топливных элементов). Буферные слои сушили в сушильном шкафу (при 90 ° C в течение 15 мин) и спекали с электролитом при 1300 ° C в течение 5 часов. Затем краской топливного электрода наносили краску на одну сторону буферного слоя с площадью закрашивания 0.965 см 2 . После сушки чернил на воздухе топливный электрод LSC спекали при 1200 ° C в течение 5 часов. Воздушный электрод LSCF окрашивали с другой стороны ячейки, затем спекали при 950 ° C в течение 4 часов в печи для получения хорошей адгезии между электродом и электролитом. Золотая паста была нанесена с обеих сторон электрода в качестве токоприемника.
Буферные слои GDC, введенные на границе раздела электродов и электролита, были получены путем смешивания порошка GDC10 с электродным клеем при весовом соотношении 1,7: 3. Буферные слои были нанесены с двух сторон электролита (диаметр 25 мм, толщина 0,3 мм, оксид циркония, легированный иттрием, 8 мол.%, Материалы топливных элементов). Буферные слои сушили в сушильном шкафу (при 90 ° C в течение 15 мин) и спекали с электролитом при 1300 ° C в течение 5 часов. Затем краской топливного электрода наносили краску на одну сторону буферного слоя с площадью закрашивания 0.965 см 2 . После сушки чернил на воздухе топливный электрод LSC спекали при 1200 ° C в течение 5 часов. Воздушный электрод LSCF окрашивали с другой стороны ячейки, затем спекали при 950 ° C в течение 4 часов в печи для получения хорошей адгезии между электродом и электролитом. Золотая паста была нанесена с обеих сторон электрода в качестве токоприемника.
Установка для электрохимических испытаний SOFC
Хорошо изготовленные элементы были помещены в установку для электрохимических испытаний, показанную на дополнительном рисунке S1. Изготовленная ячейка герметизировалась на самодельной установке из коаксиального оксида алюминия с двумя трубками с помощью керамического герметика (Ceramabond 552, Aremco Products) для разделения воздуха и топливного газа, вводимых в разные камеры. Токосъемники для двух электродов были подключены к электрохимической рабочей станции (потенциостату) серебряными проволоками диаметром 0,5 мм. Объемные расходомеры использовались для контроля расхода входящего газа, а выходящие газы, протекающие на катоде и аноде, удалялись из системы, чтобы уносить образующиеся продукты и, таким образом, позволять реакции продолжаться.После отверждения керамического герметика при комнатной температуре на воздухе эту установку следует поместить в трубчатую печь Thermolyne и затем нагреть до 70 и 260 ° C в течение 1 часа со скоростью линейного изменения 1 ° C мин. -1 . Наконец, он был нагрет до рабочей температуры со скоростью нарастания 2 ° C мин. -1 для тестирования. Электрохимические характеристики оценивались с использованием электрохимической рабочей станции с потенциостатом Solartron 1,287 и анализатором частотной характеристики Solartron 1,255 для сбора данных и измерения выработанной мощности при работе ТОТЭ (дополнительный рисунок S1).
Изготовленная ячейка герметизировалась на самодельной установке из коаксиального оксида алюминия с двумя трубками с помощью керамического герметика (Ceramabond 552, Aremco Products) для разделения воздуха и топливного газа, вводимых в разные камеры. Токосъемники для двух электродов были подключены к электрохимической рабочей станции (потенциостату) серебряными проволоками диаметром 0,5 мм. Объемные расходомеры использовались для контроля расхода входящего газа, а выходящие газы, протекающие на катоде и аноде, удалялись из системы, чтобы уносить образующиеся продукты и, таким образом, позволять реакции продолжаться.После отверждения керамического герметика при комнатной температуре на воздухе эту установку следует поместить в трубчатую печь Thermolyne и затем нагреть до 70 и 260 ° C в течение 1 часа со скоростью линейного изменения 1 ° C мин. -1 . Наконец, он был нагрет до рабочей температуры со скоростью нарастания 2 ° C мин. -1 для тестирования. Электрохимические характеристики оценивались с использованием электрохимической рабочей станции с потенциостатом Solartron 1,287 и анализатором частотной характеристики Solartron 1,255 для сбора данных и измерения выработанной мощности при работе ТОТЭ (дополнительный рисунок S1).
Характеристики материалов
Фазу катализатора анализировали методом порошковой рентгеновской дифракции (XRD) с использованием рентгеновского дифрактометра Rigaka D / max-2500 с излучением Cu Kα при комнатной температуре, и данные анализировали с помощью Jade и Программное обеспечение Xpert Highscore Plus. Микроструктура и морфология катализаторов, изображения поперечного сечения и поверхности клеток, а также состав материала с помощью анализа SEM-EDS были получены при комнатной температуре с помощью оборудования Zeiss Sigma 300VP-FESEM.Термогравиметрический (ТГА) анализ материалов выполняли с использованием прибора Q600 (инструмент TA) в различных атмосферах. Температурную программу окисления (TPO) проводили с использованием приборов TG-Mass Spectrometry (термостат QMS 200) (TG-MS). Анализ программы восстановления температуры водорода (H 2 -TPR) выполняли с использованием самодельной установки температурной программы, оснащенной газовым хроматографом Hewlett Packard 5,890 Series. Рентгеновские фотоэлектронные спектры получены на приборе Thermo fisher Scientific K-Alpha + .Пик C1s XPS был откалиброван до 284,6 эВ, как показано на дополнительном рисунке S2.
Рентгеновские фотоэлектронные спектры получены на приборе Thermo fisher Scientific K-Alpha + .Пик C1s XPS был откалиброван до 284,6 эВ, как показано на дополнительном рисунке S2.
Результаты
Порошковая дифракция рентгеновских лучей (XRD) была использована для подтверждения кристаллических структур изготовленных материалов. Согласно исследованию материалов с различным процентным содержанием Co / Ni, оптимальная концентрация легирующей примеси в B-позиции была подтверждена как 9 мол.% (Дополнительный рисунок S3), а более высокое содержание легирования приведет к сосуществованию примеси NiO. Кроме того, мы изменили состав материала, варьируя дефицит A-участка и соотношение Ni / Co.На рисунках 1A, B показаны соответствующие рентгенограммы. Все три материала, LSC-6309NiCo, LSC-6309Ni и LSC-7309NiCo, успешно образовали одну фазу оксида перовскита LSC, как отмечено звездочкой (*) (Pudmich et al., 2000). Более того, некоторый незначительный сдвиг пика может быть идентифицирован путем детального анализа положения пика (Рисунок 1B). Пики дифракции (104) для LSC-6309NiCo, LSC-6309Ni и LSC-7309NiCo находятся при 32,75 °, 32,85 ° и 32,65 ° (2θ) соответственно. Согласно закону Брэгга (nλ = 2dsinθ), LSC-6309Ni должен иметь наименьшее расстояние d и параметр ячейки, в то время как LSC-7309NiCo имеет самую большую элементарную ячейку.Предварительно изменение объема ячейки можно объяснить разным ионным радиусом примесей. Ионные радиусы для 6-кратной координации B-позиции Cr 3+ , Ni 2+ и Co 2+ составляют 0,615, 0,69 и 0,745 Å соответственно (Sebastian, 2010). Таким образом, можно ожидать, что биметаллическое легирование Ni-Co имеет увеличенный объем элементарной ячейки. Кроме того, уменьшение объема элементарной ячейки LSC-6309NiCo по сравнению с LSC-7309NiCo в основном вызвано нестехиометрией катиона A-сайта, что согласуется с литературными результатами A.В. Ковалевский и др. (Ковалевский и др., 2014).
Пики дифракции (104) для LSC-6309NiCo, LSC-6309Ni и LSC-7309NiCo находятся при 32,75 °, 32,85 ° и 32,65 ° (2θ) соответственно. Согласно закону Брэгга (nλ = 2dsinθ), LSC-6309Ni должен иметь наименьшее расстояние d и параметр ячейки, в то время как LSC-7309NiCo имеет самую большую элементарную ячейку.Предварительно изменение объема ячейки можно объяснить разным ионным радиусом примесей. Ионные радиусы для 6-кратной координации B-позиции Cr 3+ , Ni 2+ и Co 2+ составляют 0,615, 0,69 и 0,745 Å соответственно (Sebastian, 2010). Таким образом, можно ожидать, что биметаллическое легирование Ni-Co имеет увеличенный объем элементарной ячейки. Кроме того, уменьшение объема элементарной ячейки LSC-6309NiCo по сравнению с LSC-7309NiCo в основном вызвано нестехиометрией катиона A-сайта, что согласуется с литературными результатами A.В. Ковалевский и др. (Ковалевский и др., 2014).
РИСУНОК 1 . A) картины XRD и B) частичное увеличенное изображение оксида перовскита LSC-6309NiCo, LSC-6309Ni и LSC-7309NiCo, C) картины XRD восстановленных образцов R-LSC-6309NiCo, R-LSC- 6309Ni и R-LSC-7309NiCo, D) H 2 -Кривые TPR свежего LSC, LSC-6309NiCo, LSC-6309Ni и LSC-7309NiCo и E) TGA-диаграмма в 5% H 2 / N 2 для LSC-6309NiCo, LSC-6309Ni и LSC-7309NiCo.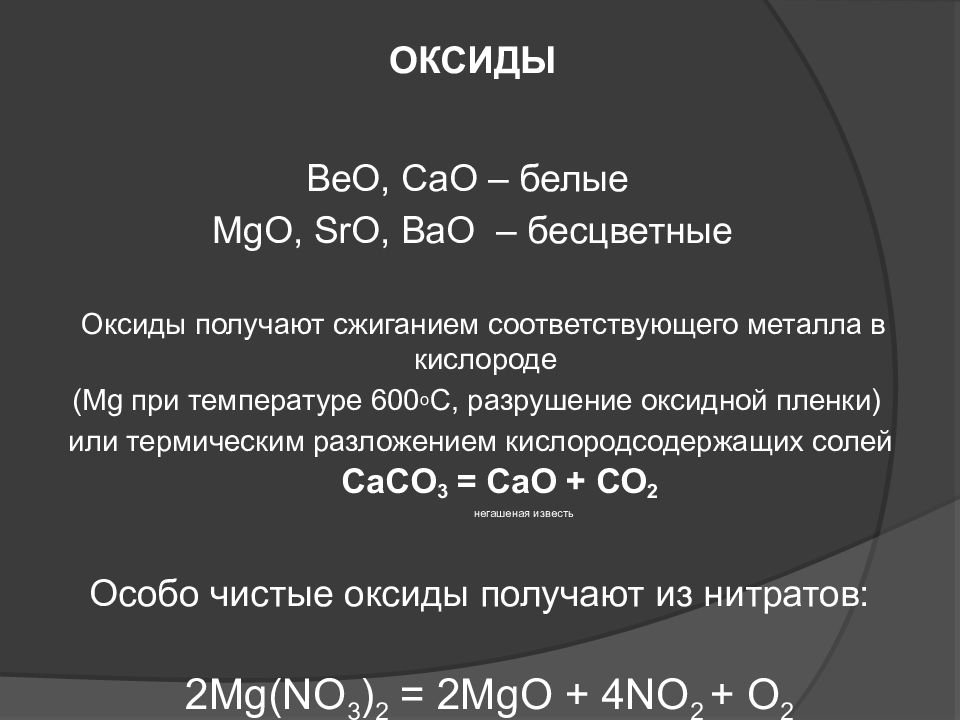
При обработке распылением на месте на различных образцах ожидается, что металлические частицы будут небольшого размера (наноразмеры) и будут равномерно декорированы на поверхности исходного LSC. Тенденцию к распаду металлических частиц можно частично предсказать с помощью свободной энергии Гиббса. Значения свободной энергии Гиббса реакции восстановления каждого катиона были рассчитаны с использованием программного обеспечения HSC 6.0 и показаны на дополнительном рисунке S4. Только Co и Ni термодинамически благоприятны для выделения при высокой температуре от 600 до 900 ° C, поскольку только восстановления Co 3 O 4 и NiO имеют отрицательную свободную энергию Гиббса.Например, при 800 ° C восстановление Co 3 O 4 до Co имеет свободную энергию Гиббса -256,91 кДж / моль, а для NiO до Ni -46,646 кДж / моль, в то время как все остальные элементы все еще показать положительные значения. Кроме того, ожидается, что расплавленные металлические частицы Ni и Co образуют фазу сплава Ni-Co во время высокотемпературной обработки распадом in situ на поверхности перовскита. Теоретически известно, что Co и Ni соседствуют друг с другом в периодической таблице и удовлетворяют правилу Юма-Розери, что указывает на то, что они могут легко образовывать фазу твердого раствора (сплав) с различными соотношениями (Janghorban et al., 2001). Таким образом, предварительно предполагается, что образование сплава Ni-Co во время процесса распада в этом эксперименте является благоприятным.
Теоретически известно, что Co и Ni соседствуют друг с другом в периодической таблице и удовлетворяют правилу Юма-Розери, что указывает на то, что они могут легко образовывать фазу твердого раствора (сплав) с различными соотношениями (Janghorban et al., 2001). Таким образом, предварительно предполагается, что образование сплава Ni-Co во время процесса распада в этом эксперименте является благоприятным.
На основе этих теоретических оценок все образцы восстанавливали при 800 ° C в течение 3 часов в атмосфере 5% H 2 / N 2 , в течение которой легирующие примеси (Ni, Co) должны были растворяться на месте выходят из объемного LSC и равномерно распределяются по поверхности. Диаграммы XRD для восстановленных образцов R-LSC-6309NiCo, R-LSC-6309Ni и R-LSC-7309NiCo, а также их подробные положения пиков распада показаны на рисунке 1C.Все восстановленные образцы успешно сохранили основную структуру LSC после процесса высокотемпературного восстановления, на что указывают пики, отмеченные звездочкой.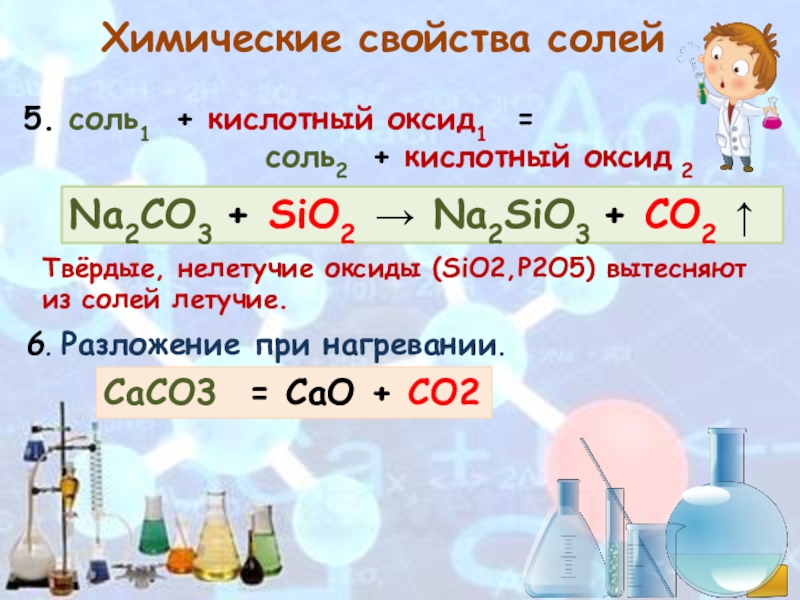 Дифракционный пик, обозначенный полым кружком, был обнаружен для LSC-6309Ni, что указывает на образование металлического Ni. Кроме того, как для R-LSC-6309NiCo, так и для R-LSC-7309NiCo был обнаружен четкий дифракционный пик, обозначенный сплошным кружком, который может быть отнесен к сплаву Ni-Co (Kwon et al., 2018).
Дифракционный пик, обозначенный полым кружком, был обнаружен для LSC-6309Ni, что указывает на образование металлического Ni. Кроме того, как для R-LSC-6309NiCo, так и для R-LSC-7309NiCo был обнаружен четкий дифракционный пик, обозначенный сплошным кружком, который может быть отнесен к сплаву Ni-Co (Kwon et al., 2018).
Чтобы исследовать восстанавливаемость материалов этой серии и синергетический эффект между Co и Ni, были проведены испытания на восстановление с программированием температуры водорода (H 2 -TPR).Как показано на рисунке 1D, нет очевидного пика потребления H 2 , встречающегося в структуре перовскита LSC, что указывает на то, что LSC, возможно, не распадается на наночастицы в восстановительной атмосфере с повышением температуры. Этот результат согласуется с диаграммой свободной энергии Гиббса, как упоминалось ранее. Легирование активных металлов Ni и Co значительно улучшило восстанавливаемость материала. Прозрачные пики потребления H 2 наблюдаются как для LSC-6309NiCo, так и для LSC-6309Ni. Кривая LSC-6309Ni имеет два четких пика потребления H 2 при ∼470 ° C и 530 ° C. Основываясь на предыдущих исследованиях (Rida et al., 2012; Jahangiri et al., 2013), первый пик (α-пик) LSC-6309Ni соответствует восстановлению Ni 3+ до Ni 2+ (около 500 ° C), а второй пик (β-пик) представляет собой восстановление от Ni 2+ до металлического Ni 0 (до 600 ° C). Преобразование Ni 2+ в Ni 0 потребляет большое количество водорода, что может быть подтверждено по площади пика β, поскольку использование образцов для измерения H 2 -TPR такое же.Материал LSC-6309NiCo имеет аналогичную форму пика α при ∼470 ° C, но с гораздо более низким пиком β при 510 ° C. Материал с различной концентрацией B-сайтов показывает аналогичную форму графиков TPR (дополнительный рисунок S5). Это явление указывает на то, что образование растворов Ni-Co значительно изменяет восстановительные свойства материала. Предыдущее исследование показало, что основной пик H 2 -TPR для Co 3 O 4 происходит при 433 ° C, который просто перекрывается с пиком α Ni.
Кривая LSC-6309Ni имеет два четких пика потребления H 2 при ∼470 ° C и 530 ° C. Основываясь на предыдущих исследованиях (Rida et al., 2012; Jahangiri et al., 2013), первый пик (α-пик) LSC-6309Ni соответствует восстановлению Ni 3+ до Ni 2+ (около 500 ° C), а второй пик (β-пик) представляет собой восстановление от Ni 2+ до металлического Ni 0 (до 600 ° C). Преобразование Ni 2+ в Ni 0 потребляет большое количество водорода, что может быть подтверждено по площади пика β, поскольку использование образцов для измерения H 2 -TPR такое же.Материал LSC-6309NiCo имеет аналогичную форму пика α при ∼470 ° C, но с гораздо более низким пиком β при 510 ° C. Материал с различной концентрацией B-сайтов показывает аналогичную форму графиков TPR (дополнительный рисунок S5). Это явление указывает на то, что образование растворов Ni-Co значительно изменяет восстановительные свойства материала. Предыдущее исследование показало, что основной пик H 2 -TPR для Co 3 O 4 происходит при 433 ° C, который просто перекрывается с пиком α Ni.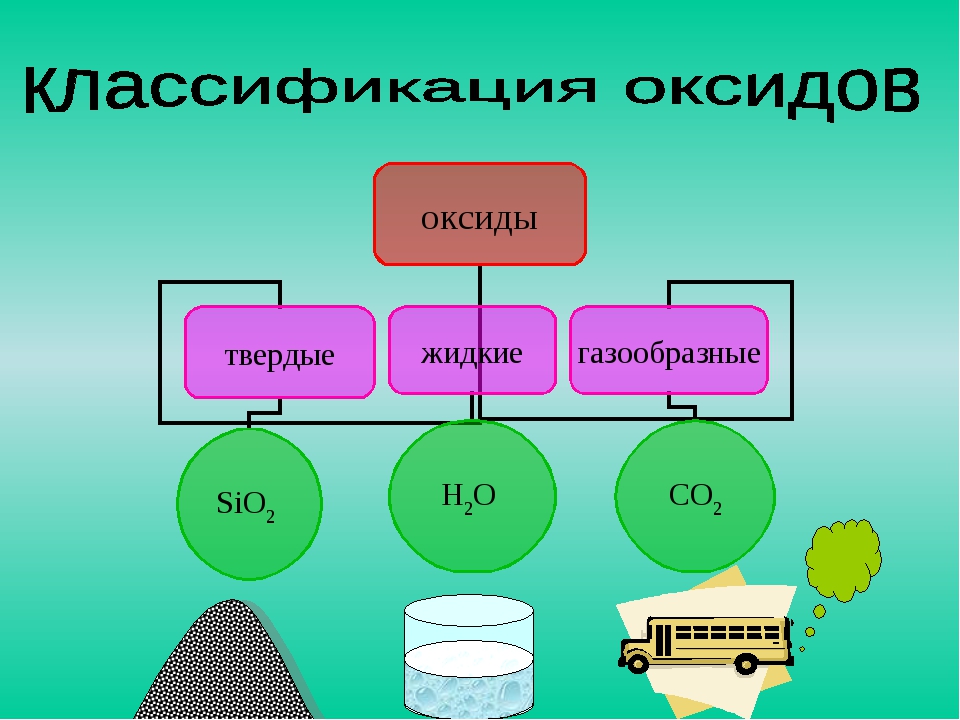 21 Этим также можно объяснить более широкий диапазон пика α в LSC-6309NiCo, чем в LSC-6309Ni. Пик β для LSC-7309NiCo переместился к более низкой температуре и частично слился с пиком α. Этот результат означает, что процесс распада LSC-7309NiCo требует более высокой энергии, чем LSC-6309NiCo, для превращений Ni 3+ в Ni 2+ и Ni 2+ в Ni 0 . Результат TPR ясно доказывает, что добавление второго металла Co может значительно облегчить восстановление материалов.Наличие дефицита A-сайта также может ускорить восстановление для образования большего количества наночастиц Ni-Co.
21 Этим также можно объяснить более широкий диапазон пика α в LSC-6309NiCo, чем в LSC-6309Ni. Пик β для LSC-7309NiCo переместился к более низкой температуре и частично слился с пиком α. Этот результат означает, что процесс распада LSC-7309NiCo требует более высокой энергии, чем LSC-6309NiCo, для превращений Ni 3+ в Ni 2+ и Ni 2+ в Ni 0 . Результат TPR ясно доказывает, что добавление второго металла Co может значительно облегчить восстановление материалов.Наличие дефицита A-сайта также может ускорить восстановление для образования большего количества наночастиц Ni-Co.
По мере того, как происходит распад in-situ , ионы кислорода скоординированной решетки, окружающие катионы, также покидают оксид перовскита LSC. Нестехиометрические ионы кислорода внесли в структуру изрядное количество кислородных вакансий (δ). Количество кислородных вакансий играет важную роль в ионной проводимости и электрохимической каталитической активности перовскитного материала. В этом эксперименте ТГА была проведена для измерения потери веса материалов при повышении температуры в восстановительной атмосфере. Как утверждали предыдущие исследования, первичная потеря веса на кривой связана с образованием кислородных вакансий (He et al., 2014; Konsolakis et al., 2015). ТГА эксплуатировали для различных материалов от 100 до 850 ° C при скорости нагрева 20 ° C в минуту в 5% H 2 / N 2 . На рисунке 1E показано сравнение кривых ТГА для LSC-6309NiCo, LSC-6309Ni и LSC-7309NiCo, потери веса для них составляют ~ 2.2%, ∼2,3% и ∼1,8% соответственно. LSC-6309NiCo имел такую же потерю веса, что и LSC-6309Ni, но имел очевидную более низкую начальную температуру и большую потерю веса на второй стадии и в первой половине третьей стадии (аналогично LSC-6303NiCo и LSC-6306NiCo, показанным в Дополнительных материалах). Рисунок S6). Второй и третий этапы являются основными этапами введения кислородных вакансий в структуру, при этом LSC-6309NiCo начинается при 380 и 510 ° C, а LSC-6309Ni — при 420 и 580 ° C.
В этом эксперименте ТГА была проведена для измерения потери веса материалов при повышении температуры в восстановительной атмосфере. Как утверждали предыдущие исследования, первичная потеря веса на кривой связана с образованием кислородных вакансий (He et al., 2014; Konsolakis et al., 2015). ТГА эксплуатировали для различных материалов от 100 до 850 ° C при скорости нагрева 20 ° C в минуту в 5% H 2 / N 2 . На рисунке 1E показано сравнение кривых ТГА для LSC-6309NiCo, LSC-6309Ni и LSC-7309NiCo, потери веса для них составляют ~ 2.2%, ∼2,3% и ∼1,8% соответственно. LSC-6309NiCo имел такую же потерю веса, что и LSC-6309Ni, но имел очевидную более низкую начальную температуру и большую потерю веса на второй стадии и в первой половине третьей стадии (аналогично LSC-6303NiCo и LSC-6306NiCo, показанным в Дополнительных материалах). Рисунок S6). Второй и третий этапы являются основными этапами введения кислородных вакансий в структуру, при этом LSC-6309NiCo начинается при 380 и 510 ° C, а LSC-6309Ni — при 420 и 580 ° C. В последней части третьего этапа, примерно при 600 ° C, потеря веса LSC-6309Ni увеличилась, что привело к аналогичному увеличению количества LSC-6309NiCo.Этот результат указывает на то, что материал с дефицитом A-узла, как в результате монометаллического легирования, так и биметаллического легирования, должен вводить аналогичное количество кислородных вакансий в структуру, но биметаллический легированный перовскит демонстрирует облегченный процесс распада. Для сравнения, LSC-7309NiCo имеет меньшую потерю веса, чем LSC-6309NiCo и LSC-6309Ni, а начальные температуры для второго и третьего этапов составляют около 420 и 580 ° C, что выше, чем у LSC-6309NiCo. Сравнивая результат этих кривых ТГА, можно сделать вывод, что введение дефицита A-сайта и биметаллическое легирование Ni и Co может способствовать образованию кислородных вакансий в структуре, тем самым улучшая ионную проводимость и каталитическую активность.
В последней части третьего этапа, примерно при 600 ° C, потеря веса LSC-6309Ni увеличилась, что привело к аналогичному увеличению количества LSC-6309NiCo.Этот результат указывает на то, что материал с дефицитом A-узла, как в результате монометаллического легирования, так и биметаллического легирования, должен вводить аналогичное количество кислородных вакансий в структуру, но биметаллический легированный перовскит демонстрирует облегченный процесс распада. Для сравнения, LSC-7309NiCo имеет меньшую потерю веса, чем LSC-6309NiCo и LSC-6309Ni, а начальные температуры для второго и третьего этапов составляют около 420 и 580 ° C, что выше, чем у LSC-6309NiCo. Сравнивая результат этих кривых ТГА, можно сделать вывод, что введение дефицита A-сайта и биметаллическое легирование Ni и Co может способствовать образованию кислородных вакансий в структуре, тем самым улучшая ионную проводимость и каталитическую активность.
Идентификация распада дополнительно анализируется с помощью изображений микроструктуры SEM. На рис. 2А показано изображение свежего порошка LSC-6309NiCo, полученное с помощью СЭМ. Очевидно, что на поверхности свежего образца с размером частиц около 500 нм не удалось обнаружить растворения металлических наночастиц. Для сравнения, многочисленные количества распущенных наночастиц наблюдаются на восстановленном образце R-LSC-6309NiCo, который был предварительно обработан 5% -ным раствором H 2 -N 2 при 800 ° C в течение 4 часов, как показано на рисунке 2B. .Распавшиеся частицы равномерно диспергированы на поверхности массы. На рисунках 2C, D показаны результаты точечного сканирования для R-LSC-6309NiCo. Объемная фаза на Фигуре 2C отмечена точкой 1), а выделившаяся частица отмечена точкой (2). На Рисунке 2D показано, что La обнаруживается при 0,5, 4,7, 5,1 и 5,9 кэВ, Sr при 1,8 кэВ и Cr при 0,25 и 5,4 кэВ как для основной, так и для разложившейся частицы. Кроме того, отчетливые пики Co и Ni обнаруживаются в точке 2) при 7 и 7,5 кэВ соответственно, тогда как пики для точки 1) в этих положениях слабы.
На рис. 2А показано изображение свежего порошка LSC-6309NiCo, полученное с помощью СЭМ. Очевидно, что на поверхности свежего образца с размером частиц около 500 нм не удалось обнаружить растворения металлических наночастиц. Для сравнения, многочисленные количества распущенных наночастиц наблюдаются на восстановленном образце R-LSC-6309NiCo, который был предварительно обработан 5% -ным раствором H 2 -N 2 при 800 ° C в течение 4 часов, как показано на рисунке 2B. .Распавшиеся частицы равномерно диспергированы на поверхности массы. На рисунках 2C, D показаны результаты точечного сканирования для R-LSC-6309NiCo. Объемная фаза на Фигуре 2C отмечена точкой 1), а выделившаяся частица отмечена точкой (2). На Рисунке 2D показано, что La обнаруживается при 0,5, 4,7, 5,1 и 5,9 кэВ, Sr при 1,8 кэВ и Cr при 0,25 и 5,4 кэВ как для основной, так и для разложившейся частицы. Кроме того, отчетливые пики Co и Ni обнаруживаются в точке 2) при 7 и 7,5 кэВ соответственно, тогда как пики для точки 1) в этих положениях слабы. Аналогичный метод был также применен для подтверждения образования наночастиц Ni в R-LSC-6309Ni (см. Дополнительный рисунок S7). Сделан вывод, что частицы распада на основе R-LSC-6309NiCo действительно являются сплавом Ni-Co. Изображения ПЭМ на рис. 3 дополнительно подтверждают структуру сплава Ni-Co из разложившихся частиц на поверхности R-LSC-6309NiCo. Здесь выпавшая частица отмечена точкой (3).
Аналогичный метод был также применен для подтверждения образования наночастиц Ni в R-LSC-6309Ni (см. Дополнительный рисунок S7). Сделан вывод, что частицы распада на основе R-LSC-6309NiCo действительно являются сплавом Ni-Co. Изображения ПЭМ на рис. 3 дополнительно подтверждают структуру сплава Ni-Co из разложившихся частиц на поверхности R-LSC-6309NiCo. Здесь выпавшая частица отмечена точкой (3).
РИСУНОК 2 . СЭМ-изображения (A), свежей микроструктуры LSC-6309NiCo, (B), восстановленного образца R-LSC-6309NiCo и (C – D) , коррелированные результаты точечного сканирования EDS.
РИСУНОК 3 . (A) TEM и (B) STEM-HAADF изображения уменьшенного образца R-LSC-6309NiCo и (C) коррелированное элементное отображение La, Sr, Cr, O, Ni и Co для точки (1) в (B) , который представлен голубым, салатовым, зеленым, оранжевым, красным и синим соответственно.
Чтобы понять эволюцию элементного состава и валентного состояния образцов до и после распада, дополнительно использовались спектры рентгеновской фотоэлектронной спектроскопии (XPS).Как показано на рисунке 4A, XPS-спектры Ni2p аналогичны спектрам NiO, что свидетельствует о его основном составе Ni 2+ (Du et al., 2015). После обработки распылением положения пиков Ni2p1 / 2 и Ni2p3 / 2 смещаются в режим более низкой энергии связи на 0,61 эВ, что предполагает значительное уменьшение валентности Ni после восстановления и образование металлического состояния Ni (Liu et al., 2016 ). XPS-спектры O1s различных образцов показаны на рисунке 4B. Процентное содержание кислорода, полученное с помощью аппроксимации пика XPS, показано в дополнительной таблице S1.Есть огромные различия в спектрах O1s XPS образцов до и после распада. Спектр O1s высокого разрешения может быть деконволюционирован на четыре пика при 532,8, 530,1, 530,3 и 528,8 эВ, которые могут быть отнесены к поверхностно-поглощенным формам молекулярного кислорода, поверхностно адсорбированным кислородом / гидроксильной группой, поверхностно адсорбированным кислородом / гидроксильной группой и кристаллическим кислородом. соответственно. После распада R-LSC-6309NiCo представляет собой повышенную концентрацию O 2 / OH (38,58%) и O 2 2- / O — (21.50%), что свидетельствует о более высоком содержании кислородных вакансий (Zhu et al., 2016). Большее количество кислородных вакансий на образцах также может способствовать диффузии ионов и способствовать каталитической реакции. Подобно Ni2p XPS-спектрам, XPS-спектры Co2p3 / 2 и Co2p1 / 2 образцов после восстановления имеют синий сдвиг на 0,55 эВ. Данные, собранные с помощью XPS, согласуются с характеристиками XRD и SEM, подтверждая образование сплава Ni-Co.
соответственно. После распада R-LSC-6309NiCo представляет собой повышенную концентрацию O 2 / OH (38,58%) и O 2 2- / O — (21.50%), что свидетельствует о более высоком содержании кислородных вакансий (Zhu et al., 2016). Большее количество кислородных вакансий на образцах также может способствовать диффузии ионов и способствовать каталитической реакции. Подобно Ni2p XPS-спектрам, XPS-спектры Co2p3 / 2 и Co2p1 / 2 образцов после восстановления имеют синий сдвиг на 0,55 эВ. Данные, собранные с помощью XPS, согласуются с характеристиками XRD и SEM, подтверждая образование сплава Ni-Co.
РИСУНОК 4 . XPS-спектры образцов LSC-6309NiCo и R-LSC-6309NiCo: (A) Ni2p, (B) O1s и (C) Co2p.
СЭМ-изображение микроструктуры поперечного сечения испытанной ячейки показано на рисунке 5A. Можно наблюдать плотный электролит YSZ толщиной 300 мкм, и между электродом и электролитом были введены два буферных слоя GDC по 15 мкм. Слои топливного и воздушного электродов толщиной примерно 30 мкм наносились поверх слоев GDC. На рисунке 5B показана кривая j-V для ячеек LSC-6309NiCo и LSC-6309Ni (анод) при 850 ° C в чистом газе H 2 . Тестируемые клетки восстанавливали с помощью 5% газа H 2 / N 2 в течение 2 часов перед испытанием, чтобы вызвать выделение сплава Ni-Co на месте.В газе H 2 значения OCV для ячеек LSC-6309NiCo и LSC-6309Ni составляли 1,15 и 1,13 В соответственно. Наблюдаемые высокие значения OCV указывают на незначительную утечку газа в ячейке. Ячейка LSC-6309NiCo может генерировать максимальную плотность мощности 329 мВт / см 2 с плотностью тока 599 мА / см 2 , в то время как ячейка LSC-6309Ni имела максимальную выходную мощность только 237 мВт / см 2 с плотностью тока 441 мА / см 2 . На рисунке 5C показаны электрохимические характеристики клеток LSC-6309NiCo и LSC-6309Ni в синтез-газе при 850 ° C.Значения OCV 1,11 и 1,14 В были определены, как и ожидалось, для LSC-6309NiCo и LSC-6309Ni, соответственно, в синтез-газе.
Слои топливного и воздушного электродов толщиной примерно 30 мкм наносились поверх слоев GDC. На рисунке 5B показана кривая j-V для ячеек LSC-6309NiCo и LSC-6309Ni (анод) при 850 ° C в чистом газе H 2 . Тестируемые клетки восстанавливали с помощью 5% газа H 2 / N 2 в течение 2 часов перед испытанием, чтобы вызвать выделение сплава Ni-Co на месте.В газе H 2 значения OCV для ячеек LSC-6309NiCo и LSC-6309Ni составляли 1,15 и 1,13 В соответственно. Наблюдаемые высокие значения OCV указывают на незначительную утечку газа в ячейке. Ячейка LSC-6309NiCo может генерировать максимальную плотность мощности 329 мВт / см 2 с плотностью тока 599 мА / см 2 , в то время как ячейка LSC-6309Ni имела максимальную выходную мощность только 237 мВт / см 2 с плотностью тока 441 мА / см 2 . На рисунке 5C показаны электрохимические характеристики клеток LSC-6309NiCo и LSC-6309Ni в синтез-газе при 850 ° C.Значения OCV 1,11 и 1,14 В были определены, как и ожидалось, для LSC-6309NiCo и LSC-6309Ni, соответственно, в синтез-газе. Ячейка LSC-6309NiCo вырабатывала максимальную плотность мощности 258 мВт / см 2 с плотностью тока 455 мА / см 2 по сравнению с ячейкой LSC-6309Ni, имеющей максимальную плотность мощности 170 мВт / см 2 и с плотностью тока 307 мА / см 2 . Эти результаты демонстрируют, что элемент LSC, легированный сплавом Ni-Co, может поддерживать повышенную каталитическую активность как для H 2 , так и для окисления синтез-газа.
Ячейка LSC-6309NiCo вырабатывала максимальную плотность мощности 258 мВт / см 2 с плотностью тока 455 мА / см 2 по сравнению с ячейкой LSC-6309Ni, имеющей максимальную плотность мощности 170 мВт / см 2 и с плотностью тока 307 мА / см 2 . Эти результаты демонстрируют, что элемент LSC, легированный сплавом Ni-Co, может поддерживать повышенную каталитическую активность как для H 2 , так и для окисления синтез-газа.
РИСУНОК 5 . (A) SEM изображение площади поперечного сечения ячейки, (B) кривые LSC-6309NiCo и LSC-6309Ni при 850 ° C в чистом газе H 2 и (C) дюйм syngas, (D) jV кривые LSC-6309NiCo и LSC-6309Ni при 850 ° C в 70% CO 2 /30% CO, (E) Кратковременная стабильность электролизеров с LSC-6309NiCo и Катоды LSC-6309Ni при 850 ° C при различных приложенных напряжениях и кривые TPO (F) для обработанных CH 4 LSC-6309NiCo и LSC-6309Ni.
Дополнительный рисунок S8A иллюстрирует характеристики EIS для ячеек LSC-6309NiCo и LSC-6309Ni от 10 6 до 0,1 Гц в условиях напряжения холостого хода с газом H 2 при температуре 850 ° C. Пересечения кривых с действительной осью (ось x ) на высоких частотах представляют их омическое сопротивление, которое в основном вызвано материалом электролита (Fabbri et al., 2008). Ячейки LSC-6309NiCo и LSC-6309Ni показали схожие омические сопротивления 0,54 и 0.56 Ом, что является разумным при толщине электролита YSZ 300 мкм. Разница между двумя пересечениями на высокой и низкой частоте с осью x представляет собой активационное сопротивление поляризации, которое является суммой реакционных сопротивлений электрода (анода и катода) (Zuo et al., 2006). Реальные части импеданса на низкой частоте для LSC-6309NiCo и LSC-6309Ni частично сравниваются на частотах 10, 1 и 0,1 Гц, что отмечено пунктирными линиями на рисунке. Ячейка LSC-6309NiCo показала явное снижение реального импеданса по сравнению с LSC-6309Ni на тех же частотах. Этот результат продемонстрировал более низкое сопротивление поляризации ячейки LSC-6309NiCo по сравнению с ячейкой LSC-6309Ni. Более низкое значение поляризационного сопротивления LSC-6309NiCo также указывает на его лучшие электрохимические характеристики. Дополнительный рисунок S8B представляет собой диаграмму EIS для ячеек LSC-6309NiCo и LSC-6309Ni для окисления синтез-газа при 850 ° C в условиях OCV. По сравнению с диаграммой EIS окисления H 2 , значительного увеличения омического сопротивления в атмосфере синтез-газа не обнаружено.Кроме того, реальные значения импеданса каждой ячейки сравниваются при 10, 1 и 0,1 Гц. По-видимому, LSC-6309Ni имеет явно большее значение реального импеданса, чем LSC-6309NiCo на каждой частоте.
Этот результат продемонстрировал более низкое сопротивление поляризации ячейки LSC-6309NiCo по сравнению с ячейкой LSC-6309Ni. Более низкое значение поляризационного сопротивления LSC-6309NiCo также указывает на его лучшие электрохимические характеристики. Дополнительный рисунок S8B представляет собой диаграмму EIS для ячеек LSC-6309NiCo и LSC-6309Ni для окисления синтез-газа при 850 ° C в условиях OCV. По сравнению с диаграммой EIS окисления H 2 , значительного увеличения омического сопротивления в атмосфере синтез-газа не обнаружено.Кроме того, реальные значения импеданса каждой ячейки сравниваются при 10, 1 и 0,1 Гц. По-видимому, LSC-6309Ni имеет явно большее значение реального импеданса, чем LSC-6309NiCo на каждой частоте.
Кроме того, электрохимические характеристики SOEC с использованием катодов LSC-6309NiCo и LSC-6309Ni были оценены при 850 ° C в атмосфере CO 2 / CO в соотношении 70: 30. Газ CO был добавлен в топливный газ CO 2 во время электрохимического испытания, чтобы предотвратить окисление растворенных частиц. Ячейки испытывали в основном в режиме электролиза (отрицательная плотность тока) с приложенными напряжениями от 0 до 0,9 В (по сравнению с OCV). На рисунке 5D показана кривая j-V для SOEC, оборудованного катодами LSC-6309Ni и LSC-6309NiCo. Значения OCV для обеих ячеек составляют 0,84–0,82 В, что близко к теоретическим значениям в атмосфере 70% CO 2 /30% CO. Как показано, элемент LSC-6309NiCo имеет плотности тока 0,039, 0,136 и 0,245 мА / см 2 при приложенных напряжениях 0,1, 0,3 и 0.5 В соответственно, в то время как LSC-6309Ni имеет соответствующие плотности тока 0,027, 0,089 и 0,179 мА / см 2 . Элемент LSC-6309NiCo показал лучшие характеристики, чем элемент LSC-6309Ni, в атмосфере CO 2 / CO при всех приложенных напряжениях, что демонстрирует, что элемент LSC с биметаллическими присадками имеет лучшие каталитические свойства в процессе восстановления CO 2 .
Ячейки испытывали в основном в режиме электролиза (отрицательная плотность тока) с приложенными напряжениями от 0 до 0,9 В (по сравнению с OCV). На рисунке 5D показана кривая j-V для SOEC, оборудованного катодами LSC-6309Ni и LSC-6309NiCo. Значения OCV для обеих ячеек составляют 0,84–0,82 В, что близко к теоретическим значениям в атмосфере 70% CO 2 /30% CO. Как показано, элемент LSC-6309NiCo имеет плотности тока 0,039, 0,136 и 0,245 мА / см 2 при приложенных напряжениях 0,1, 0,3 и 0.5 В соответственно, в то время как LSC-6309Ni имеет соответствующие плотности тока 0,027, 0,089 и 0,179 мА / см 2 . Элемент LSC-6309NiCo показал лучшие характеристики, чем элемент LSC-6309Ni, в атмосфере CO 2 / CO при всех приложенных напряжениях, что демонстрирует, что элемент LSC с биметаллическими присадками имеет лучшие каталитические свойства в процессе восстановления CO 2 .
Кратковременная стабильность работы электролизеров LSC-6309NiCo и LSC-6309Ni была протестирована в 70% CO. 2 /30% CO при 850 ° C с различными приложенными напряжениями и показана на рисунке 5E.Обе ячейки работали в режиме SOEC в течение 30 минут при постоянных напряжениях 0,1, 0,3 и 0,5 В (по сравнению с OCV). Электролизная ячейка LSC-6309NiCo показывает хорошую стабильность при всех напряжениях и плотностях тока ячейки с увеличением приложенного напряжения. Напротив, электролизная ячейка LSC-6309Ni демонстрирует хорошую стабильность при приложенных напряжениях 0,1 и 0,3 В. Существенная деградация ячейки LSC-6309Ni была обнаружена при приложенном напряжении 0,5 В. Возможной причиной такой деградации может быть влияние отложения углерода на частицах Ni из-за чрезмерного восстановления атмосферы CO 2 / CO (Li et al., 2015). В результате стабильный рабочий потенциал LSC-6309Ni может быть определен как 0,3 В относительно OCV. Морфология объемных материалов LSC сохраняется после краткосрочных испытаний, как показано на дополнительном рисунке S9. В целом, биметаллический легированный LSC перовскит показал лучшую стабильность, чем LSC, легированный никелем, в атмосфере SOEC при различных приложенных потенциалах.
2 /30% CO при 850 ° C с различными приложенными напряжениями и показана на рисунке 5E.Обе ячейки работали в режиме SOEC в течение 30 минут при постоянных напряжениях 0,1, 0,3 и 0,5 В (по сравнению с OCV). Электролизная ячейка LSC-6309NiCo показывает хорошую стабильность при всех напряжениях и плотностях тока ячейки с увеличением приложенного напряжения. Напротив, электролизная ячейка LSC-6309Ni демонстрирует хорошую стабильность при приложенных напряжениях 0,1 и 0,3 В. Существенная деградация ячейки LSC-6309Ni была обнаружена при приложенном напряжении 0,5 В. Возможной причиной такой деградации может быть влияние отложения углерода на частицах Ni из-за чрезмерного восстановления атмосферы CO 2 / CO (Li et al., 2015). В результате стабильный рабочий потенциал LSC-6309Ni может быть определен как 0,3 В относительно OCV. Морфология объемных материалов LSC сохраняется после краткосрочных испытаний, как показано на дополнительном рисунке S9. В целом, биметаллический легированный LSC перовскит показал лучшую стабильность, чем LSC, легированный никелем, в атмосфере SOEC при различных приложенных потенциалах.
Предыдущие исследования показали низкую стойкость к осаждению углерода топливных электродов, легированных частицами никеля, работающих в угольных газах.Полученный из угля топливный газ, применяемый к твердым оксидным элементам, таким как углеводороды, синтез-газ и даже газ CO 2 , может вызвать отложение углерода и привести к ухудшению характеристик элемента (Chen et al., 2011). Следовательно, сопротивление осаждению углерода является еще одним важным параметром для анализа каталитической активности электрода. Стойкость к осаждению углерода Ni и Ni-Co оксида перовскита LSC исследовалась в этой работе с помощью анализа O 2 -TPO. Образцы спекали в газе CH 4 при 850 ° C в течение 24 ч.После обработки газом CH 4 образцы вставляли для испытания ТГА при температуре от 0 до 850 ° C на воздухе. Выход газа ТГА был соединен с МС, поэтому можно было измерить удельное количество произведенного CO 2 при различных температурах. Профиль O 2 -TPO, измеренный с помощью МС, показан на рисунке 5F. Площади пиков CO 2 для LSC-6309NiCo и LSC-6309Ni составляли 4,21 × 10 –9 и 5,30 × 10 –9 соответственно. Из этого результата можно сделать вывод, что по сравнению с каталитическим материалом, легированным никелем, добавление Co в катализатор может эффективно подавлять образование отложений углерода на материале электрода, как исследовал К.Takanabe et al. (Таканабе и др., 2005). Более того, положение пика CO 2 электродного материала LSC-6309Ni составляет около 620 ° C, в то время как положение пика для LSC-6309NiCo составляет около 470 ° C. Более низкая рабочая температура электродного материала LSC-6309NiCo указывает на меньшую энергию, необходимую для окислительно-восстановительной обработки. По сравнению с LSC-6309Ni, LSC-6309NiCo показывает более высокое сопротивление отложению углерода и более низкую требуемую температуру восстановления. Это связано с тем, что образование поверхностного сплава Ni-Co может эффективно подавлять связывание нежелательного углерода и предпочтительно окислять атом углерода до газовой фазы.
Площади пиков CO 2 для LSC-6309NiCo и LSC-6309Ni составляли 4,21 × 10 –9 и 5,30 × 10 –9 соответственно. Из этого результата можно сделать вывод, что по сравнению с каталитическим материалом, легированным никелем, добавление Co в катализатор может эффективно подавлять образование отложений углерода на материале электрода, как исследовал К.Takanabe et al. (Таканабе и др., 2005). Более того, положение пика CO 2 электродного материала LSC-6309Ni составляет около 620 ° C, в то время как положение пика для LSC-6309NiCo составляет около 470 ° C. Более низкая рабочая температура электродного материала LSC-6309NiCo указывает на меньшую энергию, необходимую для окислительно-восстановительной обработки. По сравнению с LSC-6309Ni, LSC-6309NiCo показывает более высокое сопротивление отложению углерода и более низкую требуемую температуру восстановления. Это связано с тем, что образование поверхностного сплава Ni-Co может эффективно подавлять связывание нежелательного углерода и предпочтительно окислять атом углерода до газовой фазы. Монометаллический Ni с большей вероятностью способствует образованию углерод-углеродных связей (Nikolla et al., 2009), что приводит к плохой устойчивости LSC-6309Ni к осаждению углерода.
Монометаллический Ni с большей вероятностью способствует образованию углерод-углеродных связей (Nikolla et al., 2009), что приводит к плохой устойчивости LSC-6309Ni к осаждению углерода.
Заключение
Оксиды перовскита на основе LSC были приготовлены в данной работе в качестве потенциального электродного материала для ТОТЭ и SOEC. Роль стехиометрии в A-сайте и концентрации легирующей примеси в B-сайте на свойства материала изучалась с помощью XRD, TPR, TPO, TGA, XPS и SEM. LSC-6309NiCo и LSC-6309Ni были выбраны для испытаний электрохимических характеристик в SOFC и SOEC.На основании результатов экспериментов можно сделать следующие выводы:
Оксид перовскита LSC, легированный Ni и Co, был получен методом горения с уровнем легирования насыщения до 9 мол.%.
Появление дефицита A-узла является ключевой движущей силой, запускающей распад частиц сплава Nano Ni-Co. Было обнаружено, что инкорпорация Co способствовала процессу распада.
Материалы, декорированные из сплава Ni-Co, обладают лучшими электрохимическими характеристиками как в режимах ТОТЭ, так и в режимах SOEC. Между тем, образование сплава Ni-Co эффективно уменьшило отложение углерода в элементе при работе в режиме SOEC.
Между тем, образование сплава Ni-Co эффективно уменьшило отложение углерода в элементе при работе в режиме SOEC.
Заявление о доступности данных
Исходные материалы, представленные в исследовании, включены в статью / дополнительные материалы, дальнейшие запросы можно направить соответствующему автору.
Вклад авторов
YS, JL и JL разработали эту работу. LC и ZL провели эксперименты. Все авторы обсудили рукопись.
Финансирование
Эта работа поддержана Национальным фондом естественных наук Китая (№ 21773195). Это исследование финансируется Канадским советом по естественным наукам и инженерным исследованиям, грантом Discovery (GRPIN – 2016–05494) и грантом Alberta Innovates Technology Futures Research Grant.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Выражение признательности
YS выражает признательность за поддержку со стороны Nanqiang Young Top-Notch Talent Fellowship из Университета Сямэнь. Это исследование стало возможным в рамках исследовательской инициативы Университета Альберты по энергетическим системам будущего, отчасти благодаря финансированию из Первого фонда передовых исследований Канады.
Это исследование стало возможным в рамках исследовательской инициативы Университета Альберты по энергетическим системам будущего, отчасти благодаря финансированию из Первого фонда передовых исследований Канады.
Дополнительные материалы
Дополнительные материалы к этой статье можно найти в Интернете по адресу: https://www.frontiersin.org/articles/10.3389/fchem.2020.595608 / полный # дополнительный-материал.
Ссылки
An, W., Gatewood, D., Dunlap, B., and Turner, C.H. (2011). Каталитическая активность биметаллических никелевых сплавов для анодных реакций твердооксидных топливных элементов из теории функционала плотности. J. Источники энергии 196, 4724–4728. doi: 10.1016 / j.jpowsour.2011.01.007
CrossRef Полный текст | Google Scholar
Chen, T., Wang, W. G., Miao, H., Li, T., and Xu, C. (2011). Оценка поведения осаждения углерода на топливном элементе с анодной опорой из стабилизированного никелем / иттрием диоксида циркония, работающего на моделированном синтез-газе. J. Источники энергии 196, 2461–2468. doi: 10.1016 / j.jpowsour.2010.11.095
J. Источники энергии 196, 2461–2468. doi: 10.1016 / j.jpowsour.2010.11.095
CrossRef Полный текст | Google Scholar
Да Силва, Ф. С. и де Соуза, Т. М. (2017). Новые материалы для технологий твердооксидных топливных элементов: обзор литературы. Внутр. J. Водородная энергия. 42, 26020–26036. doi: 10.1016 / j.ijhydene.2017.08.105
CrossRef Полный текст | Google Scholar
Du, X., Ding, Y., and Li, C. (2015). Самосборка с контролируемой морфологией и наноструктурированный NiO: эффективный и надежный фотокаталитический катализатор окисления воды, древний и надежный катализатор фотокаталитического окисления воды. ChemCatChem 7, 2370–2376. doi: 10.1002 / cctc.201500308
CrossRef Полный текст | Google Scholar
Fabbri, E., Pergolesi, D., D’Epifanio, A., Di Bartolomeo, E., Balestrino, G., Licoccia, S., et al. (2008). Разработка и изготовление химически устойчивого двухслойного электролита с протонным проводником для твердооксидных топливных элементов с промежуточной температурой (ИТ-ТОТЭ). Energy Environ. Sci. 1, 355–359. doi: 10.1039 / b806655h
Energy Environ. Sci. 1, 355–359. doi: 10.1039 / b806655h
CrossRef Полный текст | Google Scholar
Grgicak, C.М., Пакульска, М. М., О’Брайен, Дж. С., и Джорджи, Дж. Б. (2008). Синергетические эффекты анодов ТОТЭ из кермета, легированных Ni1-xCox-YSZ и Ni1-xCux-YSZ, для окисления водородного и метанового топлива, содержащего h3S. J. Источники энергии 183, 26–33. doi: 10.1016 / j.jpowsour.2008.05.002
CrossRef Полный текст | Google Scholar
He, W., Huang, H., Chen, M., Gao, J.-F., and Chen, C.-S. (2014). Стабильность и свойство переноса кислорода La0.8Sr0.2Cr0.5Fe0.5O3-δ. Ионика твердого тела 260, 86–89.doi: 10.1016 / j.ssi.2014.03.018
CrossRef Полный текст | Google Scholar
Джахангири, А., Агабозорг, Х., и Пахлаванзаде, Х. (2013). Эффекты замещения Fe на Ni в оксидах типа La-Ni-O перовскита при риформинге метана с CO2 и O2. Внутр. J. Hydrogen Energy 38, 10407–10416. doi: 10.1016 / j.ijhydene.2013. 05.080
05.080
CrossRef Полный текст | Google Scholar
Janghorban, K., Kirkaldy, J. S., and Weatherly, G. C. (2001). Правило размера Юма-Розери и двухлуночные микроструктуры в золоте-никеле. J. Phys. Конденс. Matter 13, 8661. doi: 10.1088 / 0953-8984 / 13/38/309
CrossRef Полный текст | Google Scholar
Jiang, S. P. (2006). Обзор мокрой пропитки — альтернативного метода изготовления высокопроизводительных наноструктурированных электродов твердооксидных топливных элементов. Mater. Sci. Eng., A. 418, 199–210. doi: 10.1016 / j.msea.2005.11.052
CrossRef Полный текст | Google Scholar
Konsolakis, M., Sgourakis, M., and Carabineiro, S.А. С. (2015). Поверхностные и окислительно-восстановительные свойства бинарных оксидов кобальта-церия: влияние содержания Co и условий предварительной обработки. Прил. Прибой. Sci. 341, 48–54. doi: 10.1016 / j.apsusc.2015.02.188
CrossRef Полный текст | Google Scholar
Ковалевский, А. В., Яремченко, А. А., Популо, С., Вайденкафф, А., Фраде, Дж. Р. (2014). Влияние дефицита катиона в A-позиции на термоэлектрические характеристики донорно-замещенного титаната стронция. J. Phys. Chem. С .118, 4596–4606. doi: 10.1021 / jp409872e
В., Яремченко, А. А., Популо, С., Вайденкафф, А., Фраде, Дж. Р. (2014). Влияние дефицита катиона в A-позиции на термоэлектрические характеристики донорно-замещенного титаната стронция. J. Phys. Chem. С .118, 4596–4606. doi: 10.1021 / jp409872e
CrossRef Полный текст | Google Scholar
Квон, О., Джу, С., Чой, С., Сенгодан, С., и Ким, Г. (2020). Обзор распада и его движущих сил в перовскитах. J. Phys. Energy 2, 032001. doi: 10.1088 / 2515-7655 / ab8c1f
CrossRef Полный текст | Google Scholar
Kwon, O., Kim, K., Joo, S., Jeong, H.Y., Shin, J., Han, J. W., et al. (2018). Самособирающиеся наночастицы сплава в слоистом двойном перовските в качестве катализатора окисления топлива для твердооксидных топливных элементов. J. Mater. Chem. 6, 15947–15953. doi: 10.1039 / c8ta05105d
CrossRef Полный текст | Google Scholar
Li, W., Shi, Y., Luo, Y., Wang, Y., and Cai, N. (2015). Осаждение углерода на узорчатых электродах из диоксида циркония, стабилизированного никелем / оксидом иттрия, для режимов твердооксидного топливного элемента / твердооксидного электролизного элемента. J. Источники энергии 276, 26–31. doi: 10.1016 / j.jpowsour.2014.11.106
J. Источники энергии 276, 26–31. doi: 10.1016 / j.jpowsour.2014.11.106
CrossRef Полный текст | Google Scholar
Лю, Ю., Фу, Н., Чжан, Г., Лу, В., Чжоу, Л., и Хуанг, Х. (2016). Дендриты ядра / оболочки Ni @ NiO для электрохимического накопления энергии со сверхдлительным сроком службы. J. Mater. Chem. 4, 15049–15056. doi: 10.1039 / c6ta05508g
CrossRef Полный текст | Google Scholar
Neagu, D., Oh, T. S., Miller, D. N., Ménard, H., Bukhari, S. M., Gamble, S. R., et al. (2015). Частицы никеля с наноразъемами с повышенной устойчивостью к коксованию, выращенные in situ путем окислительно-восстановительного распада. Нат. Commun. 6, 8120–8128. DOI: 10.1038 / ncomms9120
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Nikolla, E., Schwank, J., and Linic, S. (2009). Прямое электрохимическое окисление углеводородных топлив на ТОТЭ: повышенная углеродостойкость анодов из никелевых сплавов. J. Electrochem. Soc. 156, B1312 – B1316. doi: 10.1149 / 1.3208060
Electrochem. Soc. 156, B1312 – B1316. doi: 10.1149 / 1.3208060
CrossRef Полный текст | Google Scholar
О’Хейр, Р., Ча, С. В., Колелла, В., и Принц, Ф. Б. (2016). Основы топливных элементов . Нью-Джерси, штат Нью-Джерси, США: Джон Вили и сыновья.
Google Scholar
Перес-Ломбард, Л., Ортис, Дж. И Поут, К. (2008). Обзор информации о потреблении энергии в зданиях. Energy Build. 40, 394–398. doi: 10.1016 / j.enbuild.2007.03.007
CrossRef Полный текст | Google Scholar
Prakash, B. S., Kumar, S. S., and Aruna, S. (2014). Свойства и развитие Ni / YSZ в качестве анодного материала в твердооксидных топливных элементах: обзор. Обновить. Поддерживать. Energy Rev. 36, 149–179. DOI: 10.1016 / j.rser.2014.04.043
CrossRef Полный текст | Google Scholar
Pudmich, G., Boukamp, B.A., Gonzalez-Cuenca, M., Jungen, W., Zipprich, W., and Tietz, F. (2000). Перовскиты на основе хромита / титаната для применения в качестве анодов в твердооксидных топливных элементах. Ионика твердого тела 135, 433–438. doi: 10.1016 / S0167-2738 (00) 00391-X
Ионика твердого тела 135, 433–438. doi: 10.1016 / S0167-2738 (00) 00391-X
CrossRef Полный текст | Google Scholar
Рида, К., Пенья, М.А., Састре, Э., и Мартинес-Ариас, А. (2012). Влияние температуры прокаливания на структурные свойства и каталитическую активность в реакциях окисления перовскита LaNiO3, полученного методом Печини. J. Rare Earths 30, 210–216. doi: 10.1016 / S1002-0721 (12) 60025-8
CrossRef Полный текст | Google Scholar
Sarno, C., Luisetto, I., Zurlo, F., Licoccia, S., and Di Bartolomeo, E. (2018). Композитные аноды на основе хромита лантана для сухого риформинга метана. Внутр. J. Hydrogen Energy 43, 14742–14750. doi: 10.1016 / j.ijhydene.2018.06.021
CrossRef Полный текст | Google Scholar
Себастьян, М. Т. (2010). Диэлектрические материалы для беспроводной связи .Амстердам, Нидерланды: Эльзевир.
Google Scholar
Сетц, Л. Ф. Г., Сантакрус, И., Леон-Рейна, Л., Де ла Торре, А. Г., Аранда, М. А. Г., Мелло-Кастаньо, С. Р. Х. и др. (2015). Хромит лантана, легированный стронцием и кобальтом: характеристика синтезированных порошков и спеченных материалов. Ceram. Int. 41, 1177–1187. doi: 10.1016 / j.ceramint.2014.09.046
Г., Аранда, М. А. Г., Мелло-Кастаньо, С. Р. Х. и др. (2015). Хромит лантана, легированный стронцием и кобальтом: характеристика синтезированных порошков и спеченных материалов. Ceram. Int. 41, 1177–1187. doi: 10.1016 / j.ceramint.2014.09.046
CrossRef Полный текст | Google Scholar
Sfeir, J., Buffat, P. A., Möckli, P., Xanthopoulos, N., Vasquez, R., Joerg Mathieu, H., et al. (2001). Катализаторы на основе хромита лантана для окисления метана непосредственно на анодах ТОТЭ. J. Catal. 202, 229–244. doi: 10.1006 / jcat.2001.3286
CrossRef Полный текст | Google Scholar
Stambouli, A. B., and Traversa, E. (2002). Твердооксидные топливные элементы (ТОТЭ): обзор экологически чистого и эффективного источника энергии. Обновить. Поддерживать. Energy Rev. 6, 433–455. doi: 10.1016 / S1364-0321 (02) 00014-X
CrossRef Полный текст | Google Scholar
Сунарсо, Дж., Хашим, С.С., Чжу, Н., Чжоу, В. (2017). Применение оксидов перовскита в высокотемпературном отделении кислорода, твердооксидных топливных элементах и мембранных реакторах: обзор. Прог. Энергия сгорания. Sci. 61, 57–77. doi: 10.1016 / j.pecs.2017.03.003
Прог. Энергия сгорания. Sci. 61, 57–77. doi: 10.1016 / j.pecs.2017.03.003
CrossRef Полный текст | Google Scholar
Takanabe, K., Nagaoka, K., and Aika, K.-I. (2005). Повышенная стойкость к отложению кокса диоксида титана, нанесенная на биметаллические кобальтовые и никелевые катализаторы для риформинга метана с диоксидом углерода. Catal. Lett. 102, 153–157. doi: 10.1007 / s10562-005-5848-4
CrossRef Полный текст | Google Scholar
Zhu, Y., Zhou, W., Yu, J., Chen, Y., Liu, M., and Shao, Z. (2016). Повышение электрокаталитической активности оксидов перовскита путем настройки дефицита катионов для реакций восстановления и выделения кислорода. Chem. Матер. 28, 1691–1697. doi: 10.1021 / acs.chemmater.5b04457
CrossRef Полный текст | Google Scholar
Zuo, C., Zha, S., Liu, M., Hatano, M., и Uchiyama, M. (2006). Ba (Zr0.1Ce0.7Y0.2) O3-δ в качестве электролита для низкотемпературных твердооксидных топливных элементов. Adv. Матер. 18, 3318–3320. doi: 10.1002 / adma.200601366
Adv. Матер. 18, 3318–3320. doi: 10.1002 / adma.200601366
CrossRef Полный текст | Google Scholar
Изучение новых материалов для снижения рабочей температуры твердооксидных топливных элементов
Плазменный шлейф во время измерения PLD на месте. Предоставлено: Венский технологический университет.Исследователи из TU Wien исследуют новые материалы, которые можно использовать для снижения рабочей температуры твердооксидных топливных элементов.Для этого они применяют инновационный метод.
Твердооксидные топливные элементы состоят из трех важных частей: анода, катода и электролита. В то время как кислород входит в состав катода, кислород затем транспортируется через электролит к аноду, где кислород вступает в реакцию с водородом с образованием воды. Топливный элемент способен преобразовывать энергию, выделяемую в процессе, в электричество. По этой причине топливные элементы все чаще используются в стационарных системах энергоснабжения и в автомобильной промышленности.
По этой причине топливные элементы все чаще используются в стационарных системах энергоснабжения и в автомобильной промышленности.
Чтобы снизить рабочую температуру твердооксидных топливных элементов с нынешних 800 ° C до 450 ° C до 600 ° C, ученые из TU Wien исследуют альтернативные материалы, которые подходят для использования в качестве катодов при таких более низких температурах. Маркус Кубичек и его команда недавно опубликовали результаты анализа материалов в журнале Journal of Materials Chemistry A .
Пониженная рабочая температура
Твердооксидные топливные элементы производятся с 1980-х годов.Теперь исследователи пытаются разработать новые топливные элементы, которые обладают высокой долговременной стабильностью и дешевле в производстве. Для этого необходимо снизить рабочую температуру примерно до 450-600 ° C. Для работы твердооксидного топливного элемента при более низких температурах, особенно довольно медленный кислородный обмен на катоде, представляет собой узкое место. Поэтому исследователи во всем мире ищут способы разработки новых электродных материалов, которые могут достаточно быстро включать кислород даже при более низких температурах.
Поэтому исследователи во всем мире ищут способы разработки новых электродных материалов, которые могут достаточно быстро включать кислород даже при более низких температурах.
Пути кислородного обмена
Ученые из исследовательского подразделения «Техническая электрохимия» уже много лет работают над так называемыми смешанными проводящими материалами (MIEC). Оксиды этого класса материалов особенно хорошо подходят для катодов топливных элементов, поскольку они могут проводить как ионы кислорода, так и электроны при более высоких температурах.Это работает в первую очередь за счет дефектов, то есть минимальных отклонений от идеальной кристаллической решетки, которые намеренно вводятся в материал.
«Самыми важными дефектами внутри этих материалов являются кислородные вакансии, электроны и дырки. Чтобы иметь возможность целенаправленно оптимизировать эти материалы, очень важно лучше понять роль этих дефектов в реакции внедрения кислорода, — объясняет Маркус Кубичек, руководитель проекта FWF «Определение характеристик оксидных тонких пленок в процессе роста на месте».»Исследователям это удалось.
Чтобы иметь возможность целенаправленно оптимизировать эти материалы, очень важно лучше понять роль этих дефектов в реакции внедрения кислорода, — объясняет Маркус Кубичек, руководитель проекта FWF «Определение характеристик оксидных тонких пленок в процессе роста на месте».»Исследователям это удалось.
Уникальная измерительная техника во всем мире
Чтобы измерить кинетику реакции включения кислорода, исследователи используют измерения «in situ PLD», которые являются уникальными во всем мире. Материалы электродов осаждаются в вакуумной камере с помощью лазера и измеряются непосредственно после осаждения с помощью импедансной спектроскопии. «Поскольку даже самые мелкие примеси могут иметь сильное влияние на результаты измерения, нам нужен был метод измерения, который позволил бы нам исследовать нетронутые поверхности электродов.«Нам удалось сделать это здесь впервые», — объясняет Кристоф Ридл, исследовательская группа твердотельной ионики. «Только с помощью разработанного здесь метода in-situ мы смогли идеально совместить теоретическое моделирование и реальные результаты измерений», — добавляет он.
Разные материалы, одинаковые кислородные пути
Исследователи использовали свой метод измерения, чтобы исследовать реакцию кислородного обмена на поверхности пяти многообещающих материалов. «Изюминкой наших измерений является то, что мы впервые смогли наблюдать, что реакция кислородного обмена, похоже, протекает по одному и тому же механизму на очень разных материалах», — описывает Маттеус Зибенхофер.«Решающим фактором здесь является наличие кислородных вакансий на поверхности».
Юрген Флейг, глава рабочей группы «Ионика твердого тела», заключает: «В этом исследовании мы смогли объединить различные результаты исследований и экспериментальные разработки последних нескольких лет и, таким образом, описать и понять наиболее важные реакции в этой области. твердых оксидных топливных элементов намного лучше ».
Новый аспект химии топливных элементов
Дополнительная информация: Маттеус Зибенхофер и др.
 , Исследование путей восстановления кислорода на чистых катодных поверхностях ТОТЭ с помощью импедансной спектроскопии in situ PLD, Journal of Materials Chemistry A (2021).DOI: 10.1039 / D1TA07128A Предоставлено
Венский технологический университет
, Исследование путей восстановления кислорода на чистых катодных поверхностях ТОТЭ с помощью импедансной спектроскопии in situ PLD, Journal of Materials Chemistry A (2021).DOI: 10.1039 / D1TA07128A Предоставлено
Венский технологический университет Ссылка :
Исследование новых материалов для снижения рабочей температуры твердооксидных топливных элементов (2021 г., 30 ноября)
получено 26 декабря 2021 г.
с https: // физ.org / news / 2021-11-materials-temperature-solid -xide-fuel. html
html
Этот документ защищен авторским правом. За исключением честных сделок с целью частного изучения или исследования, никакие часть может быть воспроизведена без письменного разрешения. Контент предоставляется только в информационных целях.
Оксид перовскита для твердооксидных топливных элементов
‘) var cartStepActive = true var buybox = document.querySelector («[id-данных = id _» + отметка времени + «]»). parentNode ; []. slice.call (buybox.querySelectorAll («. покупка-опция»)). forEach (initCollapsibles) функция initCollapsibles (подписка, индекс) {
var toggle = subscription.querySelector («. цена-опции-покупки»)
subscription.classList.remove («расширенный»)
var form = subscription.querySelector («. Purchase-option-form»)
if (form && cartStepActive) {
var formAction = form.getAttribute («действие»)
form.setAttribute («действие», formAction.replace («/ checkout», «/ cart»))
document.querySelector («# сценариев электронной торговли»). addEventListener («загрузка», bindModal (форма, formAction, отметка времени, индекс), false)
}
var priceInfo = subscription.querySelector («. price-info»)
var buyOption = toggle.parentElement if (переключить && форму && priceInfo) {
переключать.
forEach (initCollapsibles) функция initCollapsibles (подписка, индекс) {
var toggle = subscription.querySelector («. цена-опции-покупки»)
subscription.classList.remove («расширенный»)
var form = subscription.querySelector («. Purchase-option-form»)
if (form && cartStepActive) {
var formAction = form.getAttribute («действие»)
form.setAttribute («действие», formAction.replace («/ checkout», «/ cart»))
document.querySelector («# сценариев электронной торговли»). addEventListener («загрузка», bindModal (форма, formAction, отметка времени, индекс), false)
}
var priceInfo = subscription.querySelector («. price-info»)
var buyOption = toggle.parentElement if (переключить && форму && priceInfo) {
переключать. setAttribute («роль», «кнопка»)
toggle.setAttribute («tabindex», «0») toggle.addEventListener («клик», функция (событие) {
var extended = toggle.getAttribute («aria-extended») === «true» || ложный
toggle.setAttribute («расширенный ария»,! расширенный)
form.hidden = расширенный
если (! расширено) {
покупка вариант.classList.add («расширенный»)
} еще {
buyOption.classList.remove («расширенный»)
}
priceInfo.hidden = расширенный
}, ложный)
}
} function bindModal (form, formAction, timestamp, index) {
var weHasBrowserSupport = window.
setAttribute («роль», «кнопка»)
toggle.setAttribute («tabindex», «0») toggle.addEventListener («клик», функция (событие) {
var extended = toggle.getAttribute («aria-extended») === «true» || ложный
toggle.setAttribute («расширенный ария»,! расширенный)
form.hidden = расширенный
если (! расширено) {
покупка вариант.classList.add («расширенный»)
} еще {
buyOption.classList.remove («расширенный»)
}
priceInfo.hidden = расширенный
}, ложный)
}
} function bindModal (form, formAction, timestamp, index) {
var weHasBrowserSupport = window.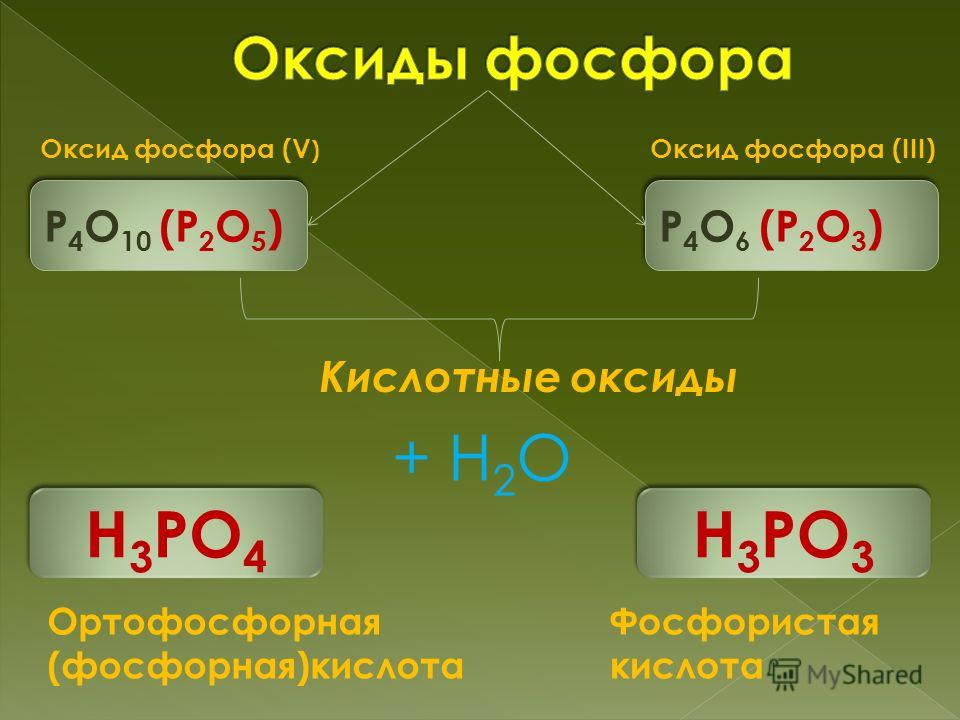 fetch && Array.from return function () {
var Buybox = EcommScripts? EcommScripts.Ящик для покупок: null
var Modal = EcommScripts? EcommScripts.Modal: null
if (weHasBrowserSupport && Buybox && Modal) {
var modalID = «ecomm-modal_» + отметка времени + «_» + индекс
var modal = новый модальный (modalID)
modal.domEl.addEventListener («закрыть», закрыть)
function close () {
форма.querySelector («кнопка [тип = отправить]»). focus ()
} form.setAttribute (
«действие»,
formAction.replace («/ checkout», «/ cart? messageOnly = 1»)
)
form.
fetch && Array.from return function () {
var Buybox = EcommScripts? EcommScripts.Ящик для покупок: null
var Modal = EcommScripts? EcommScripts.Modal: null
if (weHasBrowserSupport && Buybox && Modal) {
var modalID = «ecomm-modal_» + отметка времени + «_» + индекс
var modal = новый модальный (modalID)
modal.domEl.addEventListener («закрыть», закрыть)
function close () {
форма.querySelector («кнопка [тип = отправить]»). focus ()
} form.setAttribute (
«действие»,
formAction.replace («/ checkout», «/ cart? messageOnly = 1»)
)
form. addEventListener (
«Отправить»,
Buybox.interceptFormSubmit (
Buybox.fetchFormAction (window.fetch),
Buybox.triggerModalAfterAddToCartSuccess (модальный),
console.log,
),
ложный
)
document.body.appendChild (modal.domEl)
}
}
} function initKeyControls () {
документ.addEventListener («нажатие клавиши», функция (событие) {
if (document.activeElement.classList.contains («покупка-опция-цена») && (event.code === «Space» || event.code === «Enter»)) {
if (document.activeElement) {
event.
addEventListener (
«Отправить»,
Buybox.interceptFormSubmit (
Buybox.fetchFormAction (window.fetch),
Buybox.triggerModalAfterAddToCartSuccess (модальный),
console.log,
),
ложный
)
document.body.appendChild (modal.domEl)
}
}
} function initKeyControls () {
документ.addEventListener («нажатие клавиши», функция (событие) {
if (document.activeElement.classList.contains («покупка-опция-цена») && (event.code === «Space» || event.code === «Enter»)) {
if (document.activeElement) {
event. preventDefault ()
document.activeElement.click ()
}
}
}, ложный)
} function initialStateOpen () {
var buyboxWidth = buybox.offsetWidth
; []. slice.call (buybox.querySelectorAll («. покупка-опция»)). forEach (function (option, index) {
var toggle = option.querySelector («. покупка-вариант-цена»)
var form = option.querySelector («. Purchase-option-form»)
var priceInfo = option.querySelector («. цена-информация»)
if (buyboxWidth> 480) {
toggle.click ()
} еще {
if (index === 0) {
переключать.нажмите ()
} еще {
toggle.
preventDefault ()
document.activeElement.click ()
}
}
}, ложный)
} function initialStateOpen () {
var buyboxWidth = buybox.offsetWidth
; []. slice.call (buybox.querySelectorAll («. покупка-опция»)). forEach (function (option, index) {
var toggle = option.querySelector («. покупка-вариант-цена»)
var form = option.querySelector («. Purchase-option-form»)
var priceInfo = option.querySelector («. цена-информация»)
if (buyboxWidth> 480) {
toggle.click ()
} еще {
if (index === 0) {
переключать.нажмите ()
} еще {
toggle. setAttribute («расширенная ария», «ложь»)
form.hidden = «скрытый»
priceInfo.hidden = «скрыто»
}
}
})
} initialStateOpen () если (window.buyboxInitialised) вернуть
window.buyboxInitialised = true initKeyControls ()
}) () .
setAttribute («расширенная ария», «ложь»)
form.hidden = «скрытый»
priceInfo.hidden = «скрыто»
}
}
})
} initialStateOpen () если (window.buyboxInitialised) вернуть
window.buyboxInitialised = true initKeyControls ()
}) () .
 , металлургич., хим. отраслях пром-сти, в ядерной энергетике, а также в ракетной и космич. технике.
, металлургич., хим. отраслях пром-сти, в ядерной энергетике, а также в ракетной и космич. технике. Кроме простых тугоплавких оксидов (образованным одним металлом), в технике применяют сложные оксиды, состоящие из двух и более различных оксидов металлов в виде твердых растворов или… … Металлургический словарь
Кроме простых тугоплавких оксидов (образованным одним металлом), в технике применяют сложные оксиды, состоящие из двух и более различных оксидов металлов в виде твердых растворов или… … Металлургический словарь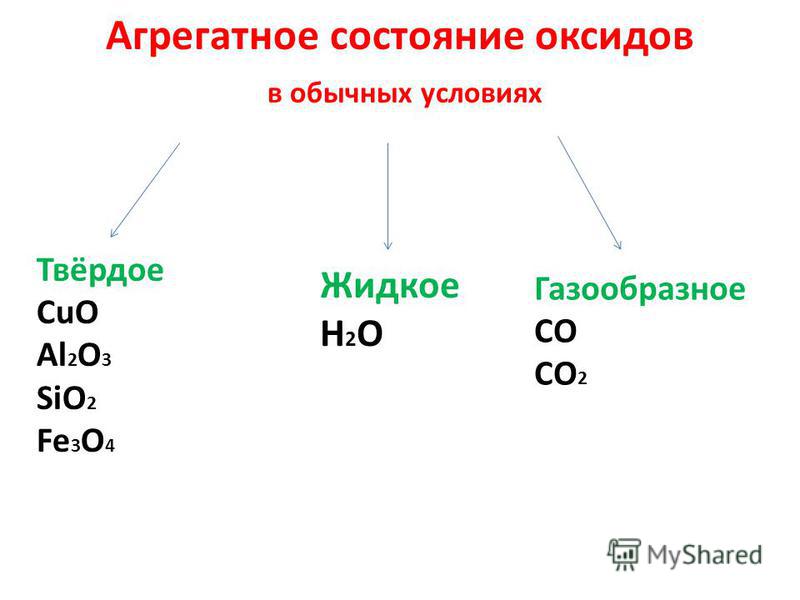 Бориды), углеродом (см. Карбиды), азотом (см. Нитриды), кремнием (см. Силициды), кислородом (см. Тугоплавкие оксиды). Т. с. делятся на 2 группы: металлоподобные и… … Большой энциклопедический политехнический словарь
Бориды), углеродом (см. Карбиды), азотом (см. Нитриды), кремнием (см. Силициды), кислородом (см. Тугоплавкие оксиды). Т. с. делятся на 2 группы: металлоподобные и… … Большой энциклопедический политехнический словарь Н. в. классифицируют по хим., минералогам, составу, происхождению. По хим. составу н. в. подразделяют на: алюминатные (осн. составляющая… … Справочник технического переводчика
Н. в. классифицируют по хим., минералогам, составу, происхождению. По хим. составу н. в. подразделяют на: алюминатные (осн. составляющая… … Справочник технического переводчика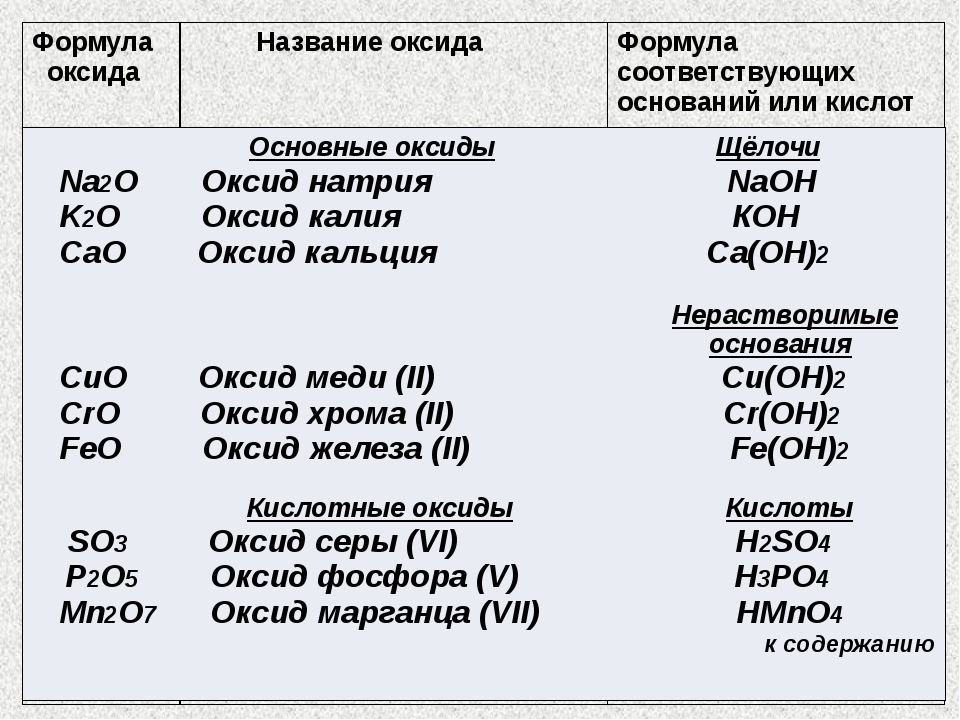 г. шламовое покрытие и ЭВД
г. шламовое покрытие и ЭВД 