Про сахара с точки зрения химика. Химия на кухне 2 / Хабр
Старинная форма фасовки сахара — «сахарная голова»
Выкладываю продолжение, как обещал. Первый пост был про соль.
Про сахар. Какие бывают сахара. Про кленовый сахар и сахар ли он? Сосульки из кленового сока — ценный дар природы. Моно- и много- сахариды. Что общего у омара, тарантула, ёлки, гриба, мёда и ракеты «Кассам». Ставим химический опыт по превращению крахмала… Как блеснуть эрудицией. Фруктоза — польза и вред, две стороны вопроса. Кто виноват в том, что от молока болит живот. Как получается, что кислое варенье меньше засахаривается. Из чего делают мёд. Из чего делают сахар. Про тростниковый сахар — едим ради его вкуса.
Всем привет! Что-то после рассказов про «белую смерть», захотелось поговорить про «сладкую». Это такой каламбур, шутка юмора. Вопрос вреда, и в данном случае, как Вы уже догадываетесь, заключается в основном, в неумеренном потреблении. Ну вот, значит, встречаются на полке много разных сортов сахара, и из местных и приезжие, и начинают выяснять, кто из них лучше… Стоп! Не допустим мордобоя, и разберемся сами.

Сироп из кленового сока
Вот и начнем разбор полётов с него, потому что, его мало и штука это интересная. Это традиционный продукт, который получали в США и Канаде, в то время, когда сахара свекловичного еще не было, а тростниковый был дорог. Получают его упариванием весеннего кленового сока. Кстати, наверное Вы знаете, что так же как из берёзы, весной, можно добывать сок и из клёна, и не обязательно в Америке. Во время моего проживания в подмосковном Троицке, случилась такая весна, что морозец еще держался, а в деревьях сок уже двинулся. В результате из всех трещинок и поломов на веточках начали расти сосульки.
Реально вкусные сосульки
Вычислив природу образования этих странно высоко висящих сосулек — попробовал их на вкус… в общем первый сок с любого дерева сладенький, отдает древесиной, некоторые породы деревьев давали совсем вкусный, некоторые — с неприятным привкусом, но сладкий. Так что в кленовом сахаре нет ничего удивительного, зато есть довольно много минеральных веществ, и сладость его определяется… Оп!
Да ведь получается, что это и не сахар вовсе, а лишь его близкий химический родственник — глюкоза.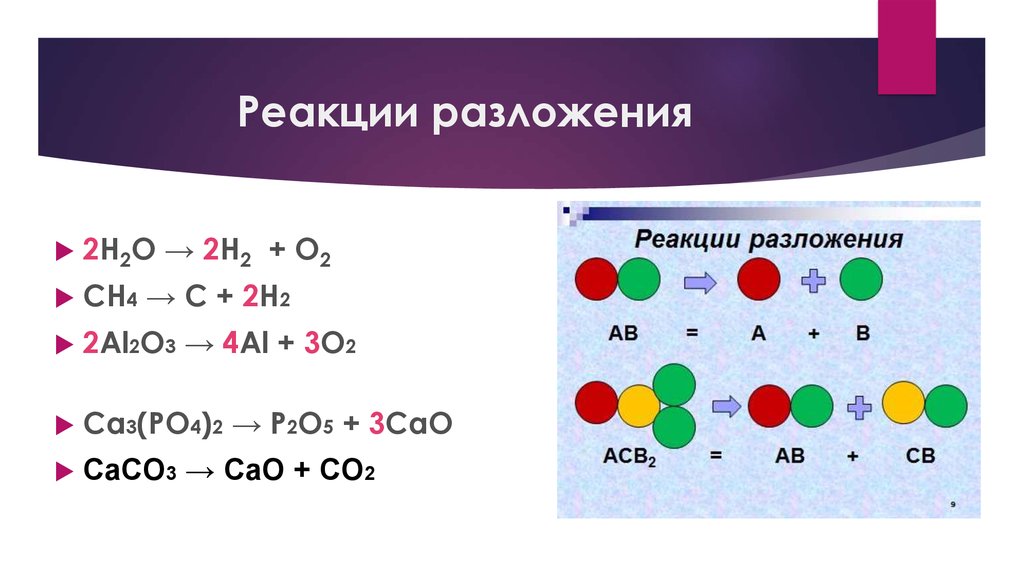 Она получается в дереве при расщеплении накопленного осенью крахмала. Вот так, легко и естественно, мы пришли к теме моно-, ди-, и полисахаридов. Постараюсь внести ясность. Сахара — это целый класс соединений, их еще зовут — углеводы. На самом деле какая-то смысловая разница между ними есть, расплывчатая, но нас сильно стыдить за её незнание вряд ли будут. Вообще, растительное царство, оказывается, в основном, состоит из разнообразнейших углеводов или по-другому поли-, олиго-, три-, ди- и моносахаридов. При этом некоторые из них бывают сладкими… Удивил?
Она получается в дереве при расщеплении накопленного осенью крахмала. Вот так, легко и естественно, мы пришли к теме моно-, ди-, и полисахаридов. Постараюсь внести ясность. Сахара — это целый класс соединений, их еще зовут — углеводы. На самом деле какая-то смысловая разница между ними есть, расплывчатая, но нас сильно стыдить за её незнание вряд ли будут. Вообще, растительное царство, оказывается, в основном, состоит из разнообразнейших углеводов или по-другому поли-, олиго-, три-, ди- и моносахаридов. При этом некоторые из них бывают сладкими… Удивил?
Итак: что вообще, в химии, значит сахара или углеводы? Ну их так назвали потому что, в начале развития химии, их анализ показывал, что они как бы состоят из смеси молекул воды и углерода. Тогда еще не вникали в тонкости структуры молекулы — то есть, как атомы соединены между собой. А это важно. Анализ, чаще всего, выполнялся самым простым способом — сжиганием и взвешиванием. После сжигания становилось известно количество углерода, водорода и кислорода, содержавшегося в навеске вещества. А сахарами — понятно — под рукой был сахар, и вещи химически похожие на него, стали называть (моно, ди… поли-) — сахаридами или углеводами. Самые простые молекулы сахаров, которые уже не удавалось расщепить кипячением в воде с кислотой, назвали моносахаридами, — сахара, одна молекула которых расщеплялась на две молекулы моносахаридов — назвали дисахаридами. Олигосахариды, это сахара состоящие из небольшого количества моносахаридов. В этом месте каждый сам придумывает ему приятную шутку про олигархов и олигосахариды. Напрашивается. Полисахариды — это разнообразнейшие природные полимеры из моносахаридов.
А сахарами — понятно — под рукой был сахар, и вещи химически похожие на него, стали называть (моно, ди… поли-) — сахаридами или углеводами. Самые простые молекулы сахаров, которые уже не удавалось расщепить кипячением в воде с кислотой, назвали моносахаридами, — сахара, одна молекула которых расщеплялась на две молекулы моносахаридов — назвали дисахаридами. Олигосахариды, это сахара состоящие из небольшого количества моносахаридов. В этом месте каждый сам придумывает ему приятную шутку про олигархов и олигосахариды. Напрашивается. Полисахариды — это разнообразнейшие природные полимеры из моносахаридов.
Вы удивитесь, но панцирь краба, шкурка тарантула и основное вещество грибов, состоят из полисахарида — хитина. Ах, какой соблазн — начать производство — «крабового сахара». Или «скорпионового», да хоть «грибного». Или даже водки. Нет! Не получается. Моносахарид из хитина хоть и не сладкий, а очень интересный. Это глюкозамин — популярное средство при болях в суставах. Хотя официальная медицина и эксперименты показывают, что плацебо почти так же хорошо действует. Только вот, если уж очень болит, тогда был замечен положительный эффект. Хотя, многие люди клянутся, что им реально помогает. Это вещество можно делать из шкурок от креветок. А вот если из этого хитина сделать трисахарид — хитозан, получится средство для похудения и перспективное средство для заживления ран. Мощный полисахарид — целлюлоза (она состоит из глюкозы, кстати), из неё гм… делают деревья, бумагу, хлопок и бездымный порох. Первый искусственный пластик был из нитроцеллюлозы и делали из него шары для бильярда и клавиши для роялей. До этого приходилось использовать слоновую кость.
Только вот, если уж очень болит, тогда был замечен положительный эффект. Хотя, многие люди клянутся, что им реально помогает. Это вещество можно делать из шкурок от креветок. А вот если из этого хитина сделать трисахарид — хитозан, получится средство для похудения и перспективное средство для заживления ран. Мощный полисахарид — целлюлоза (она состоит из глюкозы, кстати), из неё гм… делают деревья, бумагу, хлопок и бездымный порох. Первый искусственный пластик был из нитроцеллюлозы и делали из него шары для бильярда и клавиши для роялей. До этого приходилось использовать слоновую кость.
Пектин — тоже полисахарид, природный, его много в яблоках и цитрусовых( и не только). Моносахарид, из которого он состоит, штука нам не слишком знакомая и сказать про неё что-либо интересное не могу, а грузить Вас ненужным не буду. Прелесть пектина, в том, что его легко и приятно извлекать из жмыха от выжимок сока. В общем, сырья навалом. Причем это не какая-то синтетика, вполне себе натуральный продукт. Старинный мармелад и зефир — обязаны были своему происхождению именно яблокам, вернее их пектину. В старинный зефир, видимо, добавляли просто разваренный яблочный жмых — ну или не сильно очищенный, даже вроде опилки от яблочных семянок попадались, поэтому он был сероватый и имел интересный такой, натуральный вкус. Там, в составе, яблоки фигурируют или яблочный пектин. Не помню.
Старинный мармелад и зефир — обязаны были своему происхождению именно яблокам, вернее их пектину. В старинный зефир, видимо, добавляли просто разваренный яблочный жмых — ну или не сильно очищенный, даже вроде опилки от яблочных семянок попадались, поэтому он был сероватый и имел интересный такой, натуральный вкус. Там, в составе, яблоки фигурируют или яблочный пектин. Не помню.
Похоже на яблочный мармелад времён моей юности
А яблочный мармелад обходился естественным пектином, получавшимся из яблок при варке. Пектин — почти не усваивается организмом, зато хорошо соединяется с ионами тяжёлых металлов и радионуклидов(что то же самое, он радиацию не чувствует, он чувствует тяжелый металл. Химия) — это используют в медицине. Неплохое свойство для пищевой добавки, блокировать ядовитые тяжёлые металлы(многие из тяжелых металлов — ядовиты).
Поперечное сечение гликогена. В середине — белок. Вокруг — шуба из глюкозных частиц.
А вот еще полисахарид — гликоген, — основной запасной углевод человека и животных.
Ну и распространённый углевод — крахмал. Из углеводов, до сих пор, именно его, мы съедаем больше всего. Моносахарид из которого построен крахмал — глюкоза. Потому и едим.
Вот так химики рисуют молекулы гликогена и крахмала
Внимание, опыт! Предлагаю химический опыт для домашней работы. Делать натощак. Чем голоднее будете, тем выше активность фермента амилаза в Вашей слюне. Берёте кусочек хлеба, чёрного, несладкого и жуёте. Долго. По мере жевания, Вы увидите, что хлеб становится слаще и слаще. Крахмал в хлебе, под действием фермента амилаза, превращается в сладкую мальтозу(глюкозу). Вот так лаборатория!
А ещё, если нагреть крахмал(до соответствующей температуры), то он станет «модифицированным» или по-старинному «декстрином».
Просто станет лучше растворяться, даже в холодной воде. Не путать с ГМ! Потому повара часто прожаривают муку для приготовления соуса — она разойдётся в тёплой воде, и не будет комочков при приготовлении соуса. Можете сделать соус бешамель, и считать это домашней работой — рецепт взять из Интернета.
Не путать с ГМ! Потому повара часто прожаривают муку для приготовления соуса — она разойдётся в тёплой воде, и не будет комочков при приготовлении соуса. Можете сделать соус бешамель, и считать это домашней работой — рецепт взять из Интернета.
Мука, превращается, превращается в элегантный соус
В заголовке обещал упомянуть арабскую народную ракету «Кассам», к сахару она имеет то отношение, что её топливо состоит из смеси сахара и удобрения — селитры. Очень бюджетный вариант. Любители домашнего малобюджетного ракетостроения тоже очень уважают смесь из расплавленного сахара с селитрой, по причине сравнительной безопасности, удобства работы с ней и доступности.
Так что родственников у нашего сахара много — как у китайца с фамилией Ванг. Мы пробежались по всему этому богатству. Просто чтоб было интересно.
А сейчас, внимание! Штука, которую надо знать, чтобы прослыть тонким знатоком химии: — углеводы, это всё состоящее из сахаров и крахмала (обычно так говорят о том что едят, но как мы видели, это не совсем так — панцирь омара сожрать трудно, а усвоить ещё труднее). Углеводороды — это всё воняющее бензином и горючее, даже газ. Это едят в единственном случае — детский вазелин при запорах. Да и то, потому что, он как вошел, так и вышел, ну никак не усваивается. Запомнить просто — (угле-)водород — газ, его не съешь, (угле-)вод — вода, её можно выпить, а значит, съедобно. Теперь Вы можете блеснуть эрудицией на любой тусовке. И при переводах.
Углеводороды — это всё воняющее бензином и горючее, даже газ. Это едят в единственном случае — детский вазелин при запорах. Да и то, потому что, он как вошел, так и вышел, ну никак не усваивается. Запомнить просто — (угле-)водород — газ, его не съешь, (угле-)вод — вода, её можно выпить, а значит, съедобно. Теперь Вы можете блеснуть эрудицией на любой тусовке. И при переводах.
Так. Мы выяснили, что сахаров этих и моно и других, очень много. Не драматизируем. В реальной жизни нас волнует совсем немногие из них. О них поговорим. Моносахариды глюкоза и фруктоза употребляются нами в чистом виде и даже легко усваиваются.
Глюкоза усваивается моментально. Собственно она разносится кровью по нашему организму, для получения энергии, как топливо.
Фруктоза — в чистом виде этот моносахарид начали производить относительно недавно, лет 30-50 назад. До этого, его добывали в чистом виде, кажется, из клубней гладиолуса. Отделять фруктозу от глюкозы, например из мёда — не умели. А потому была она лекарством. Фруктоза считалась хорошим заменителем сахара — она в полтора раза слаще его, значит принесёт меньше калорий, она не повышает уровень сахара в крови, она не так быстро всасывается, как глюкоза, значит не будет сразу откладываться в жир. Она меньше вредит зубам, чем сахар, потому что хуже усваивается микробами. Теперь, когда фруктозу научились делать дёшево и много из сахара, стали выясняться и другие факторы. Выяснилось, что хоть она и слаще, люди используют не меньше фруктозы, а пьют более сладкое. Ещё — глюкоза моментально попадает в кровь и в нас начинает работать один из механизмов насыщения — уровень глюкозы растёт и есть перестаёт хотеться. Второй механизм — по срабатыванию датчика набитости желудка 8)). Ещё — фруктоза усваивается только печенью, так что при избытке калорий, там же в жир и откладывается. И какой вывод можно сделать? Если есть сколько надо, и регулировать калорийность своей пищи и количество движения, продукты с фруктозой вреда не принесут.
А потому была она лекарством. Фруктоза считалась хорошим заменителем сахара — она в полтора раза слаще его, значит принесёт меньше калорий, она не повышает уровень сахара в крови, она не так быстро всасывается, как глюкоза, значит не будет сразу откладываться в жир. Она меньше вредит зубам, чем сахар, потому что хуже усваивается микробами. Теперь, когда фруктозу научились делать дёшево и много из сахара, стали выясняться и другие факторы. Выяснилось, что хоть она и слаще, люди используют не меньше фруктозы, а пьют более сладкое. Ещё — глюкоза моментально попадает в кровь и в нас начинает работать один из механизмов насыщения — уровень глюкозы растёт и есть перестаёт хотеться. Второй механизм — по срабатыванию датчика набитости желудка 8)). Ещё — фруктоза усваивается только печенью, так что при избытке калорий, там же в жир и откладывается. И какой вывод можно сделать? Если есть сколько надо, и регулировать калорийность своей пищи и количество движения, продукты с фруктозой вреда не принесут.
Так что, однозначно — если Вы голодны и выпьете немного фруктозосодержащего напитка, это будет полезно. Избыток — нет. Немного добавлю фактов, что бы Вы могли более философски глянуть на публикации по фруктозе. Наш любимый сахар (химики его зовут- сахароза), это дисахарид, его молекула слеплена из одной молекулы глюкозы и одной фруктозы. В организме он обязательно расщепляется на фруктозу и глюкозу. И было это испокон веков. Пчелиный мед — как было где-то красиво определено — «отрыжка насекомых, из полупереваренных выделений половых органов растений». Хе-хе. Так вот, в мёде, фруктоза и глюкоза пополам. Фруктоза во фруктах — вообще, однозначно, полезна — яблоки, груши, инжир — содержат довольно много фруктозы. Так что, мне видится причина вреда — переедание, вызванное неестественно вкусными продуктами. И вот еще штрих. Мы об этом забыли, но это было, и было хорошо. Инвертный сахар. А что это такое? Раствор сахара кипятили с небольшим количеством серной кислоты. Да, при этом молекула сахарозы разваливалась на исходную фруктозу и глюкозу. Кислоту осаждали мелом. Избыток мела и получившийся гипс отфильтровывали. Как видите, ничего криминального. Гипс, мел — источники кальция. А в чём же смысл реакции? Получавшийся раствор был в полтора раза слаще исходного сахара. За счет сладости фруктозы и глюкозы.
Мы об этом забыли, но это было, и было хорошо. Инвертный сахар. А что это такое? Раствор сахара кипятили с небольшим количеством серной кислоты. Да, при этом молекула сахарозы разваливалась на исходную фруктозу и глюкозу. Кислоту осаждали мелом. Избыток мела и получившийся гипс отфильтровывали. Как видите, ничего криминального. Гипс, мел — источники кальция. А в чём же смысл реакции? Получавшийся раствор был в полтора раза слаще исходного сахара. За счет сладости фруктозы и глюкозы.
Так же происходит и у пчёл, только они используют специальный фермент. Такой раствор имеет ещё один неочевидный плюс. Он засахаривается гораздо медленнее, чем исходный сахарный сироп. Пчёлы это тоже знают, им работать с засахарившимся мёдом трудно — ложек и зубов нету. Почему засахаривается труднее? Вы только не обижайтесь( голосом Мкртчана — из Мимино), я Вам сейчас скажу одну очевидную для химика вещь: — Когда растёт кристалл -любого вещества — на его поверхность нарастают только молекулы того типа, из которых сложен этот кристалл. Во всяком случае они к этому стремятся. И сильно. Поэтому перекристаллизация, издревле, любимый способ очистки множества веществ. Растворили грязное, вырастили кристаллы, остатки отделили, кристаллы будут сильно чище. Так вот, когда у нас в растворе два разных сахара, возможные центры роста кристалла видят только свои молекулы и получается, что возможностей для роста кристаллов (засахаривания) в два раза меньше.
Во всяком случае они к этому стремятся. И сильно. Поэтому перекристаллизация, издревле, любимый способ очистки множества веществ. Растворили грязное, вырастили кристаллы, остатки отделили, кристаллы будут сильно чище. Так вот, когда у нас в растворе два разных сахара, возможные центры роста кристалла видят только свои молекулы и получается, что возможностей для роста кристаллов (засахаривания) в два раза меньше.
Немного про мёд. Мёд продукт исторически популярный и освящённый традицией. Ещё древние римляне лакомились напитком из мёда пополам с виноградным соком. И ничего у них не склеивалось. Нам трудно проникнуться теми ощущениями. Да, не было в те времена ничего столь же концентрированно сладкого и питательного, как мёд. Пища была достаточно грубой, с малым содержанием жиров и с очень малым количеством сладостей, поэтому съедение мёда вызывало необычно быстрый прилив сил и сытости. Даже от малого количества. В фильме «Легенда о Нараяме», люди чрезвычайно бедны, питаются почти одними трудноусвояемыми бобами. Одна из старушек собралась помирать. Плохо ей стало. Перед смертью ей сварили риса — гораздо более легко усвояемый продукт. Старушка поела и — ей стало хорошо, она выздоровела. Благодаря чудодейственной силе риса.
Одна из старушек собралась помирать. Плохо ей стало. Перед смертью ей сварили риса — гораздо более легко усвояемый продукт. Старушка поела и — ей стало хорошо, она выздоровела. Благодаря чудодейственной силе риса.
Процесс сбора и приготовления мёда пчелами тоже впечатляющ. Ручная работа, да какая мелкая! Сначала пчела облетает тысячу цветков и собирает 70 миллиграмм нектара, отвозит его в улей, где специальные работники долго его жуют для ферментирования, потом раскладывают по сотам и упаривают до нужных кондиций, обмахивая крыльями. Запечатывают воском. И только тогда мёд готов. С химической же точки зрения мёд состоит в основном, из смеси фруктозы, глюкозы и совсем чуть других сахаров. Остальные вещества составляют около 3%. Боюсь навлечь гнев читателей, но не забудьте — я ведь химик: рекламные публикации о составе мёда невнятны и нелогичны, так же как и про гималайскую соль. Там есть немного ферментов, в основном, амилазы — мёд с горячим чаем, приводит к разрушению ферментов, которые там были (амилаза и другие, если дожили — их разрушить не трудно, даже небольшим нагревом). Опять же, фермент — это природный катализатор, ускоритель какой-то химической реакции. Ну есть в мёде фермент, расщепляющий крахмал до мальтозы и сахарозу на глюкозу и фруктозу, а нам от этого какая польза? Чуть лучше булка усвоится. Не за то любим. Бывает у людей и детей аллергия на мёд, бывает что им мёд не нравится. Не надо переживать, на свете есть много других полезных продуктов. Но! Давайте вспомним метафору о том, что человек есть сумма «харда» и «софта». Софт — это наши эмоции, чувства, убеждения и вера. Если Вам приятно и хорошо попить чаю с мёдом — пейте на здоровье, будет полезно. Как выбрать хороший мёд — не скажу, не знаю. Я его вообще не покупаю, у жены дядька — пасечник. Дарит.
Опять же, фермент — это природный катализатор, ускоритель какой-то химической реакции. Ну есть в мёде фермент, расщепляющий крахмал до мальтозы и сахарозу на глюкозу и фруктозу, а нам от этого какая польза? Чуть лучше булка усвоится. Не за то любим. Бывает у людей и детей аллергия на мёд, бывает что им мёд не нравится. Не надо переживать, на свете есть много других полезных продуктов. Но! Давайте вспомним метафору о том, что человек есть сумма «харда» и «софта». Софт — это наши эмоции, чувства, убеждения и вера. Если Вам приятно и хорошо попить чаю с мёдом — пейте на здоровье, будет полезно. Как выбрать хороший мёд — не скажу, не знаю. Я его вообще не покупаю, у жены дядька — пасечник. Дарит.
Немного скажу о других сахаридах, различных ди- и трисахаридах. Например в горохе есть некий трисахарид, который, нами в большинстве, не усваивается. А вот микробы кишечника начинают его жадно лопать. Результат — бурчание в животе, и не побоюсь этого выражения: — «испускание ветров». В молоке другой сахар — лактоза, который усваивается далеко не всеми людьми. То есть, маленькие дети имеют фермент для его расщепления, а у взрослых его активность может падать совсем. Вообще, мутация, позволяющая усваивать молочный сахар появилось в Европе 5000 лет назад, и связана с одомашниванием молочного скота. Так что, если у вас от молока болит живот — Вы не европеец. А если Вы можете пить молоко литрами — то Вы мутант-европеец. Это шутка такая.
То есть, маленькие дети имеют фермент для его расщепления, а у взрослых его активность может падать совсем. Вообще, мутация, позволяющая усваивать молочный сахар появилось в Европе 5000 лет назад, и связана с одомашниванием молочного скота. Так что, если у вас от молока болит живот — Вы не европеец. А если Вы можете пить молоко литрами — то Вы мутант-европеец. Это шутка такая.
Уйдём теперь от этих ужасных проблем к нашей простой, доброй милой сахарозе. Итак добывают её двумя способами: — первый нам наиболее привычный и известный — из сахарной свёклы(она -белая). Кстати, Вы её пробовали?
Сахарная свёкла — на вкус не очень
Но сладкая. Так вот, из свекольной стружки вымывают сахар. Получившийся коричневый раствор, очищают от примесей известью, углекислым и сернистым газом — сернистый газ, это вонючий газ получающийся при сгорании серы, им чистят подвалы и теплицы от всяких грибков и вредителей, придают дивный светлый цвет кураге и изюму. Вреда от него особого нет, он благополучно нейтрализуется и переходит в безвредные сульфаты. Так вот, раствор упаривают, и для получения рафинированного сахара, обрабатывают активированным углем. Он связывает на своей поверхности все красящие и вонючие вещества и получается совсем прозрачный раствор. Кстати, свекловичный сахар, традиционно очищают углём из твёрдых пород дерева, а вот рафинированный тростниковый(который становится совсем белым), по- традиции очищают костным углем. Углем, полученным при пережигании костей животных(по большей части коров, вероятно- не бойтесь, там ничего органического не остается, уголь, фосфаты кальция, всё нерастворимое). Так что свекловичный сахар можно считать вполне себе постным(вегетарианским?). Ну и нерафинированный тростниковый, потому что в процессе их приготовления животные не были задействованы. На самом деле вопрос постности сахара решается сугубо директивно, я думаю. Вернёмся к очищенному сахарному сиропу — его упаривают, вносят затравку кристаллов сахара, выпадающие кристаллы отделяют и сушат. Вот и получился рафинированный сахар-песок.
Так вот, раствор упаривают, и для получения рафинированного сахара, обрабатывают активированным углем. Он связывает на своей поверхности все красящие и вонючие вещества и получается совсем прозрачный раствор. Кстати, свекловичный сахар, традиционно очищают углём из твёрдых пород дерева, а вот рафинированный тростниковый(который становится совсем белым), по- традиции очищают костным углем. Углем, полученным при пережигании костей животных(по большей части коров, вероятно- не бойтесь, там ничего органического не остается, уголь, фосфаты кальция, всё нерастворимое). Так что свекловичный сахар можно считать вполне себе постным(вегетарианским?). Ну и нерафинированный тростниковый, потому что в процессе их приготовления животные не были задействованы. На самом деле вопрос постности сахара решается сугубо директивно, я думаю. Вернёмся к очищенному сахарному сиропу — его упаривают, вносят затравку кристаллов сахара, выпадающие кристаллы отделяют и сушат. Вот и получился рафинированный сахар-песок. Раньше из него делали твёрдый сахар-рафинад. Смешивали сахар-песок с сахарным сиропом. Вещь получалась по твёрдости — ядрёная и экономичная. Пока растворишь или сгрызёшь кусок, выпьешь три стакана чая. Теперь кусковой, быстрорастворимый сахар делают обработкой сахара -песка паром и прессованием. Получается гораздо более удобосъедаемый продукт.
Раньше из него делали твёрдый сахар-рафинад. Смешивали сахар-песок с сахарным сиропом. Вещь получалась по твёрдости — ядрёная и экономичная. Пока растворишь или сгрызёшь кусок, выпьешь три стакана чая. Теперь кусковой, быстрорастворимый сахар делают обработкой сахара -песка паром и прессованием. Получается гораздо более удобосъедаемый продукт.
Сахарный тростник
С тростниковым сахаром всё похоже и всё по-другому. Это был первый вид сахара, который люди начали делать. Получают его из сока сахарного тростника. Получается, густой коричневый сироп. Но вкус у него приятный, хотя цвет очень тёмный. Такой сироп бывает в магазине, но перед покупкой приглядитесь — должно быть написано, что он сделан конкретно из сахарного тростника. Ещё продают нерафинированный тростниковый сахар. А так же продается тёмный кусковой тростниковый сахар, его кажется делают из смеси рафинированного и тростникового сиропа, приятный на вкус.
Тёмный тростниковый кусковой сахар
С ценой интересная зависимость получается — чем продукт ближе к высушенному тростниковому соку, тем он дороже… Хотя не логично до крайности. Чем больше мы возимся на заводе с тростниковым сахаром, тем дешевле он становится… Парадоксы маркетинга. А вот ещё более тёмный продукт — фариновый сахар. Мягкая сахарная паста тёмного цвета. Тоже из тростника.
Чем больше мы возимся на заводе с тростниковым сахаром, тем дешевле он становится… Парадоксы маркетинга. А вот ещё более тёмный продукт — фариновый сахар. Мягкая сахарная паста тёмного цвета. Тоже из тростника.
Фариновый сахар
Бывает ещё — Крупный карамельный сахар. Крупные, красивые кристаллы золотисто-тёмного цвета. Увы цвет в этом случае получается из-за добавки карамелизованного (нагреванием) сахара и не связан с веществами из тростниковой травки, а значит и вкус у него — сахарный.
Крупный карамельный сахар
На этом тему закончим — хотя есть ведь ещё и несахарные подсластители… может когда-нибудь поговорим и об этом. А вывод у нас будет такой: все сахара, вещь в некотором роде, искусственная, яблоко всяко полезнее, а уж если хотите съесть сахара выбирайте тот, который нравится. Вкус или цвет — тоже могут нести положительные эмоции, а это, согласитесь — хорошо.
Cпасибо за внимание. Теперь буду думать о следующем посте. Больше готовых у меня нет, так что когда будет — не знаю, это как Музы распорядятся. Предыдущий пост смотрите
Предыдущий пост смотрите
Названия химических элементов
Названия химических элементовНазвания химических элементов
| Z | Символ | Name | Название |
| 1 | H | Hydrogen | Водород |
| 2 | He | Helium | Гелий |
| 3 | Li | Lithium | Литий |
| 4 | Be | Beryllium | Бериллий |
| 5 | B | Boron | Бор |
| 6 | C | Carbon | Углерод |
| 7 | N | Nitrogen | Азот |
| 8 | O | Oxygen | Кислород |
| 9 | F | Fluorine | Фтор |
| 10 | Ne | Neon | Неон |
| 11 | Na | Sodium | Натрий |
| 12 | Mg | Magnesium | Магний |
| 13 | Al | Aluminium | Алюминий |
| 14 | Si | Silicon | Кремний |
| 15 | P | Phosphorus | Фосфор |
| 16 | S | Sulfur | Сера |
| 17 | Cl | Chlorine | Хлор |
| 18 | Ar | Argon | Аргон |
| 19 | K | Potassium | Калий |
| 20 | Ca | Calcium | Кальций |
| 21 | Sc | Scandium | Скандий |
| 22 | Ti | Titanium | Титан |
| 23 | V | Vanadium | Ванадий |
| 24 | Cr | Chromium | Хром |
| 25 | Mn | Manganese | Марганец |
| 26 | Fe | Iron | Железо |
| 27 | Co | Cobalt | Кобальт |
| 28 | Ni | Nickel | Никель |
| 29 | Cu | Copper | Медь |
| 30 | Zn | Zinc | Цинк |
| 31 | Ga | Gallium | Галлий |
| 32 | Ge | Germanium | Германий |
| 33 | As | Arsenic | Мышьяк |
| 34 | Se | Selenium | Селен |
| 35 | Br | Bromine | Бром |
| 36 | Kr | Krypton | Криптон |
| 37 | Rb | Rubidium | Рубидий |
| 38 | Sr | Strontium | Стронций |
| 39 | Y | Yttrium | Иттрий |
| 40 | Zr | Zirconium | Цирконий |
| 41 | Nb | Niobium | Ниобий |
| 42 | Mo | Molybdenum | Молибден |
| 43 | Tc | Technetium | Технеций |
| 44 | Ru | Ruthenium | Рутений |
| 45 | Rh | Rhodium | Родий |
| 46 | Pd | Palladium | Палладий |
| 47 | Ag | Silver | Серебро |
| 48 | Cd | Cadmium | Кадмий |
| 49 | In | Indium | Индий |
| 50 | Sn | Tin | Олово |
| 51 | Sb | Antimony | Сурьма |
| 52 | Te | Tellurium | Теллур |
| 53 | I | Iodine | Иод |
| 54 | Xe | Xenon | Ксенон |
| 55 | Cs | Caesium | Цезий |
| 56 | Ba | Barium | Барий |
| 57 | La | Lanthanum | Лантан |
| 58 | Ce | Cerium | Церий |
| 59 | Pr | Praseodymium | Празеодим |
| 60 | Nd | Neodymium | Неодим |
| 61 | Pm | Promethium | Прометий |
| 62 | Sm | Samarium | Самарий |
| 63 | Eu | Europium | Европий |
| 64 | Gd | Gadolinium | Гадолиний |
| 65 | Tb | Terbium | Тербий |
| 66 | Dy | Dysprosium | Диспрозий |
| 67 | Ho | Holmium | Гольмий |
| 68 | Er | Erbium | Эрбий |
| 69 | Tm | Thulium | Тулий |
| 70 | Yb | Ytterbium | Иттербий |
| 71 | Lu | Lutetium | Лютеций |
| 72 | Hf | Hafnium | Гафний |
| 73 | Ta | Tantalum | Тантал |
| 74 | W | Tungsten | Вольфрам |
| 75 | Re | Rhenium | Рений |
| 76 | Os | Osmium | Осмий |
| 77 | Ir | Iridium | Иридий |
| 78 | Pt | Platinum | Платина |
| 79 | Au | Gold | Золото |
| 80 | Hg | Mercury | Ртуть |
| 81 | Tl | Thallium | Таллий |
| 82 | Pb | Lead | Свинец |
| 83 | Bi | Bismuth | Висмут |
| 84 | Po | Polonium | Полоний |
| 85 | At | Astatine | Астат |
| 86 | Rn | Radon | Радон |
| 87 | Fr | Francium | Франций |
| 88 | Ra | Radium | Радий |
| 89 | Ac | Actinium | Актиний |
| 90 | Th | Thorium | Торий |
| 91 | Pa | Protactinium | Протактиний |
| 92 | U | Uranium | Уран |
| 93 | Np | Neptunium | Нептуний |
| 94 | Pu | Plutonium | Плутоний |
| 95 | Am | Americium | Америций |
| 96 | Cm | Curium | Кюрий |
| 97 | Bk | Berkelium | Берклий |
| 98 | Cf | Californium | Калифорний |
| 99 | Es | Einsteinium | Эйнштейний |
| 100 | Fm | Fermium | Фермий |
| 101 | Md | Mendelevium | Менделевий |
| 102 | No | Nobelium | Нобелий |
| 103 | Lr | Lawrencium | Лоуренсий |
| 104 | Rf | Rutherfordium | Резерфордий |
| 105 | Db | Dubnium | Дубний |
| 106 | Sg | Seaborgium | Сиборгий |
| 107 | Bh | Bohrium | Борий |
| 108 | Hs | Hassium | Хассий |
| 109 | Mt | Meitnerium | Мейтнерий |
| 110 | Ds | Darmstadtium | Дармштадтий |
| 111 | Rg | Roentgenium | Рентгений |
| 112 | Cn | Copernicium | Коперниций |
| 113* | Nh | Nihonium | Нихоний |
| 114 | Fl | Flerovium | Флеровий |
| 115* | Mc | Moscovium | Московий |
| 116 | Lv | Livermorium | Ливерморий |
| 117* | Ts | Tennessine | Тенессин |
| 118* | Og | Oganesson | Оганессон |
Символы и названия элементов даны по материалам 2009
г. IUPAC (International Union of Pure and Applied Chemistry) (см. Pure Appl. Chem., 2011, 83,
359-396).
IUPAC (International Union of Pure and Applied Chemistry) (см. Pure Appl. Chem., 2011, 83,
359-396).
ATOMIC WEIGHTS OF THE
ELEMENTS 2009
Имена flerovium (Fl) для 114-го элемента и livermorium (Lv) для 116-го элемента
были одобрены (см. Pure Appl. Chem., 2012, 84,
1669-1672)
* После утверждения открытия этих элементов, первооткрывателям было предложено дать им имена. Отдел неорганической химии IUPAC рассмотрел эти предложения и рекомендует их для принятия. До официального утверждения имен советом IUPAC, проходит пятимесячного публичное обсуждение, которое закончится 8 ноября 2016 года.(см. http://iupac.org/elements.html)
В учебнике по химии советуют пить раствор соды для лечения рака и отбеливания зубов. Почему не стоит этого делать? | Громадское телевидение
В учебнике по химии для учащихся 9 классов, который Минобразования рекомендовало в 2017 году, указано, что пищевая сода помогает в профилактике и лечении онкозаболеваний, а также в отбеливании зубов. Мы узнали у экспертов, почему не стоит следовать этим советам.
Мы узнали у экспертов, почему не стоит следовать этим советам.
Автор учебника Савчин М.М. пишет, что пищевая сода создает щелочную среду, в которой не могут размножаться раковые клетки, вирусы и бактерии. Поэтому раствор пищевой соды советуют пить «для профилактики и лечения онкологических заболеваний, смягчения кашля при простуде, отбеливание зубов, лечение грибковых заболеваний и болезней желудочно-кишечного тракта». А еще указывается, что рекомендации предоставили по материалам сайта «Всеукраинской ассоциации пенсионеров».
Мы обратились в Минобразования с запросом разъяснить, почему учебник с советами недоказуемой медицины рекомендовало министерство.
fullscreenФото:Скриншот страницы учебника
Коротко о кислотности организма и соде
Преподавательница химии и аспирантка специальности «Биология» Нежинского университета имени Гоголя Ольга Пихова рассказала нам, что в разных частях нашего организма разный рН (уровень кислотности). Например, для мышц кислотность меняется вследствие тренировок, есть нагрузки — производится молочная кислота.
Для крови даже небольшие изменения рН могут быть смертельными, говорит преподавательница. Изменение кислотности крови может наступать при определенных болезнях. Например, из-за диареи, рвоты и даже постоянного употребления мочегонных средств, а также при переливании больших объемов крови.
«Питье раствора соды не меняет кислотность во всем организме, — объясняет чванливое. — Попадание соды в желудок приводит к реакции нейтрализации желудочной кислоты и выделения воды и углекислого газа».
Кроме того, бикарбонат (сода) входит в состав буферной системы крови, поэтому это соединение регулирует кислотность крови, но это происходит внутри, а не с помощью внешнего попадания соды.
Онкологические заболевания
Врач-онколог Андрей Гардашников нам в комментарии рассказал, что нет никаких официальных рекомендаций применять пищевую соду для профилактики и лечения онкологических заболеваний, а также нет данных доказательной медицины относительно оправданности таких советов. По его словам, питье соды или ее введение не уменьшают возможности развития рака:
По его словам, питье соды или ее введение не уменьшают возможности развития рака:
«Онкологические болезни развиваются в живом организме. Для их развития нужен живой человек, с совместимыми для жизни кислотно-щелочным балансом, уровнем глюкозы и многими другими факторами. Если существенно сдвинуть кислотно-щелочной баланс в состояние алкалоза (увеличение кислотности — ред.) и вызвать этим смерть человека — тогда и онкологический процесс развиваться точно не будет. Кстати, клетки злокачественных опухолей неплохо приспосабливаются к различным изменениям в метаболизме человека. Они живучи».
Врач также отметил, что вопрос профилактики и лечения онкологических болезней не такой примитивный, как кажется, то есть правила «не ешь мяса» (хотя есть определенные виды рака, которые действительно бывают у любителей мяса) или «пей соду и не будет рака» — не работают.
Существует множество факторов, которые приводят к онкозаболеваниям, в частности генетическая предрасположенность, радиоактивное излучение, гормональные нарушения, но не кислотность, пишут в Минздраве.
слушайте также
Отбеливание зубов
Если просто пить раствор соды, то отбеливание не произойдет, поскольку он попадет прямо в желудок. С помощью соды можно снять пигментированный зубной налет из-за вещества, рассказала стоматолог Елена Мовчан. Но это не очень полезно.
«Эмаль зуба царапается и дальше ее очень сложно отполировать. Как следствие, поврежденная эмаль будет более уязвима к внешним раздражителям. Может появиться чувствительность, дефекты эмали, быстрое появление зубного налета. Потому эмаль после соды поврежденная, а к шероховатой поверхности зубной налет прикрепляется быстрее, чем к гладкой, заполированной», — рассказала врач.
Если же вы хотите отбелить зубы, то стоит обратиться к стоматологу. Он должен осмотреть вас и сказать, нет ли противопоказаний к процедурам профессионального или домашнего отбеливания, для использования отбеливающих паст.
9 занимательных фактов о Нобелевской премии | Политика и общество: анализ событий в Европе, России, мире | DW
Нобелевская премия существует уже 112 лет. Кто он, нобелевский лауреат? Сколько ему лет и откуда он? Как часто премию присуждают женщинам, и какие ученые дважды удостаивались почетной награды? DW собрала 9 наиболее интересных фактов о Нобелевской премии.
1. США по нобелевке впереди всех
Больше всего Нобелевских премий по научным дисциплинам — физике, химии и медицине — доставалось американцам. Их доля — 43 процента. На втором месте по физике и химии — немцы, на третьем — англичане. Что касается медицины, то тут порядок обратный. На четвертом месте — французы.
2. Нобелевские лауреаты рождаются чаще весной или зимой
Чаще всего лауреатами Нобелевской премии становились люди, родившиеся 21 мая и 28 февраля.
3. Лауреату премии, как правило, больше 50 лет
Средний возраст удостоенных Нобелевской премии во всех шести номинациях — 59 лет. Чуть моложе лауреаты премий по дисциплинам естествознания. Среди химиков и физиков это 57 лет, по медицине — 55.
4. Нобелевской награды достойны и стар и млад
Самым молодым ученым, получившим премию, стал в 1915 году 25-летний физик Уильям Лоренс Брэгг. А самыми преклонными ее обладателями — Леонид Гурвиц (2007) и Ллойд Стауэлл Шепли (2012). Когда их удостоили Нобелевских премий по экономике, ученым было соответственно 90 и 89 лет.
5. Премия присуждалась и посмертно
На церемонии вручения Нобелевской премии в Стокгольме, 2012 год
Дважды в истории Нобелевскую премию присудили посмертно: Нобелевскую премию мира за 1961 год — Дагу Хаммершельду, а премию по литературе за 1931 год — Эрику Акселю Карлфельдту.
Официальные правила позволяют выдвигать кандидата на премию только при его жизни. Хаммершельд и Карлфельдт были номинированы при жизни, но к моменту оглашения имен лауреатов отошли в мир иной.
В 1974 году награду решили больше умершим не выдавать. Тем не менее в 2011 году Нобелевской премии снова удостоили покойника. Когда Нобелевский комитет оглашал имя Ральфа Стайнмана, номинированного на премию по медицине, еще не было известно, что за три дня до церемонии он скончался. Позже премию Стайнмана получили его наследники.
6. Дважды лауреаты Нобелевской премии
Четверо ученых оказались лауреатами премии дважды. Американский физик Джон Бардин получил ее в первый раз в 1956 году за изобретение транзистора, а во второй раз — в 1972 году за разработку теории сверхпроводимости (способности некоторых материалов обладать строго нулевым электрическим сопротивлением).
Англичанину Фредерику Сенгеру два раза присуждали Нобелевскую премию по химии — в 1958 году за установление структуры инсулина и в 1980 году — за фундаментальные исследования биохимических свойств нуклеиновых кислот, в особенности рекомбинантных ДНК.
Две разные премии получал американский химик Лайнус Карл Полинг — в 1954 году по химии, а в 1962-м — премию мира. Полинг был активным противником испытаний ядерного оружия.
7. Нобелевская премия — не женское дело
Среди лауреатов мало женщин. Самая известная женщина, дважды удостоенная премии, — Мария Кюри. В 1903 году она получила награду по физике за исследования явлений радиации, а в 1911-м — по химии за открытие элементов радия и полония.
В общей сложности женщин награждали Нобелевской премией 44 раза, причем за достижения в области одной из трех дисциплин естествознания — только 16 раз. Это всего 3 процента от общего числа лауреатов премии в этих областях. Две женщины получали премии по физике, четыре — по химии и 10 — по медицине.
8. От нобелевки отказывались, и не раз
Лауреаты Нобелевской премии мира Ле Дых Тхо и премии в области литературы Жан-Поль Сартр отказались принять награды. Сартр вообще не хотел никаких официальных чествований, а Ле Дых Тхо мотивировал в 1973 году свой отказ продолжающейся гражданской войной во Вьетнаме.
9. Немцам запрещали получать Нобелевскую премию
Во времена пребывания у власти в Германии национал-социалистов немецким ученым было запрещено принимать эти награды. В результате без премий остались в 1938 и 1939 годах химики Рихард Кун (Richard Kuhn) и Адольф Бутенандт (Adolf Butenandt), а также Герхард Домагк (Gerhard Domagk) — лауреат Нобелевской премии 1939 года по медицине. После окончания Второй мировой войны они все-таки получили дипломы и медали, но не финансовую часть премии.
Урок 8. количество вещества. молярная масса. молярный объём газазакон авогадро — Химия — 8 класс
Количество вещества. Молярная масса. Молярный объем газа. Закон Авогадро
Из курса физики мы знаем о таких физических величинах, как масса, объём и плотность. При помощи этих величин легко характеризовать вещества. Например, мы идём в магазин и покупаем 1 кг сахара или литровую бутылку минеральной воды. Но оказывается, что этих величин недостаточно, если необходимо рассмотреть вещество с точки зрения числа частиц. Сколько молекул сахара содержится в 1 кг сахара? А сколько молекул воды в литровой бутылке? А в одной капле? Ответ на этот вопрос можно получить, если знать ещё об одной физической величине, которая называется количество вещества. Точное число молекул посчитать сложно, но если считать не штуками, а порциями, то задача упрощается. Например, мы никогда не покупаем в магазине спички поштучно, но купив одну порцию спичек – коробок, знаем, что там 100 штук. И салфетки мы тоже поштучно не покупаем, но купив пачку салфеток, то есть порцию, мы точно будем знать, сколько штук салфеток мы купили.
Количество вещества – это порция вещества с определённым числом структурных частиц. Количество вещества принято обозначать греческой буквой ν [ню]. В системе СИ единица измерения количества вещества называется моль. Один моль вещества содержит столько же структурных частиц, сколько атомов содержится в 12 г углерода, а именно 6*1023 частиц. Это количество является постоянной величиной и называется «постоянная Авогадро». Количество вещества можно определить как отношение числа структурных частиц к числу частиц в одном моле вещества.
Например, количество вещества, которое соответствует 3*1023 атомов железа можно легко рассчитать по этой формуле.
Преобразовав исходную формулу легко определить число структурных частиц по известному количеству вещества: N = v * NA
Своё имя эта постоянная получила в честь Амедео Авогадро, который в 1811 году сделал предположение, которое затем подтвердилось экспериментально и теперь носит имя Закона Авогадро. Закон Авогадро: «в равных объёмах различных газов при одинаковых условиях (температура и давление) содержится одинаковое количество молекул».
Из закона Авогадро следует, что при одинаковых условиях массы газов, содержащие одинаковое число структурных частиц, будут занимать одинаковый объём. При давлении 1 атмосфера и температуре 0 градусов Цельсия 1 моль любого газа занимает объём равный 22, 4 л. Этот объём называется молярный объём. А условия – нормальные условия. Молярный объём обозначается Vm, показывает объём газа количеством 1 моль. При нормальных условиях является постоянной величиной.
При нормальных условиях количество вещества это отношение объёма к молярному объему.
По этой формуле можно определить объём вещества, если известно его количество: V = ν * Vm
Массу вещества количеством 1 моль называют молярной массой, обозначают буквой M. Молярная масса численно равна относительной молекулярной массе. Единица измерения молярной массы г/моль.
Зная массу вещества, легко определить количество вещества.
Найдём количество вещества 5,6 г железа.
Чтобы найти массу вещества по известному количеству преобразуем формулу: m = ν * M
Справочный материал
• Количество вещества ν [ню] – это физическая величина, характеризующая количество однотипных структурных единиц (любые частицы, из которых состоит вещество – атомы, молекулы, ионы и т.д), содержащихся в веществе. Единица измерения количества вещества в Международной системе единиц (СИ) – моль.
• Моль – это единица измерения количества вещества. Один моль вещества содержит столько же структурных частиц, сколько атомов содержится в 12 г углерода.
• Молярная масса (M) – масса вещества количеством один моль. Единица измерения г/моль.
• Нормальные условия (н.у.) – физические условия, определяемые давлением 101325 Па (нормальная атмосфера) и температурой 273,15 К (0 °С).
• Молярный объём (Vm) – объём вещества количеством один моль. Единица измерения л/моль; при н.у. Vm = 22,4 л/моль
• Закон Авогадро – в равных объёмах различных газов при одинаковых условиях (температура и давление) содержится одинаковое количество молекул.
• Постоянная Авогадро (NA) показывает число структурных частиц в веществе количеством один моль.
Предраковые состояния: что это и как не пропустить — Профилактика — Информация
Когда нужно начать беспокоиться и что делать, чтобы не спровоцировать онкологическое заболевание?
Многие онкологические заболевания не возникают беспочвенно, довольно часто организм человека сигнализирует о неполадках определенными состояниями, которые в медицине объединены под общим термином «предраковые».
Предопухолевым состоянием, или предраком, считают изменение тканей, которое с высокой вероятностью может превратиться в злокачественную опухоль. Стоит понимать, что предрак — это все же не рак и даже не начальная его стадия.
Как правило, к этой категории относят доброкачественные новообразования или длительные хронические воспаления.
Хотя это еще не онкологическая патология, необходимо внимательно следить за своим здоровьем, чтобы вовремя начать лечение, если малигнизация (процесс ракового перерождения) все-таки начнется. Какие заболевания относят к предраку и как не допустить развития онкологических процессов?
Классификация предраковых состояний
Понятие «предрак» возникло в 1896 году на Международном конгрессе дерматологов и применялось только к наиболее доступному для клинического наблюдения раку кожи. В дальнейшем удалось установить, какие еще органы человека подвержены развитию злокачественных опухолей. Таким образом, стало возможно выявить и предраковые заболевания, зная их локализацию. Отсюда появился и термин «профилактика рака», и довольно быстро диагностика опасных очагов стала достаточно популярной.
Многочисленные проявления предрака подразделяют на облигатные (обязательные) и факультативные (необязательные).
Первая группа включает врожденные дефекты и генетически предопределенные процессы, при которых неизбежно рано или поздно развиваются злокачественные опухоли. К числу облигатных заболеваний относят, например:
- пигментную ксеродерму — хроническое наследственное заболевание, обусловленное повышенной чувствительностью кожи к солнечной радиации и УФ-лучам;
- болезнь Боуэна — редкое заболевание кожных покровов, характеризующееся одним или несколькими пятнисто-узелковыми образованиями на теле;
- эритроплазию Кейра — состояние, представляющее собой поражение эпителиальных клеток слизистых оболочек и кожи.
Эти патологии встречаются не так уж и часто, но при обнаружении хотя бы одного похожего симптома необходимо обратиться к онкологу.
Заболевания группы факультативных предраков характеризуются относительно невысокой степенью вероятности перерождения в рак.
Среди них встречается язва желудка, кожный рог — доброкачественное образование, представленное в виде кожного нароста на теле; кератоакантома — опухоль кожи, внешне напоминающая купол с небольшой лункой в центре и характеризующаяся быстрым ростом и циклическим течением.
Провоцирующие факторы
На развитие предраковых состояний влияют экзогенные (внешние) и эндогенные (внутренние) факторы. Экзогенные факторы могут быть условно сгруппированы следующим образом:
- физические факторы. Например, ультрафиолетовое повреждение кожи от воздействия солнечных лучей может спровоцировать развитие меланомы.
- механические факторы. Это травмы, которые сопровождаются длительным раздражением. Например, родинки, которые регулярно травмируются одеждой, обувью, в процессе эпиляции или бритья. Из-за такого воздействия может начаться процесс озлокачествления.
- химические раздражители. Они делятся на две группы: бытовые и производственные. В первом случае речь идет о вредных привычках. Например, употребление табака оказывает грубое раздражающее действие на слизистую оболочку полости рта, дыхательных путей; кроме того, продукты сгорания табака содержат множество канцерогенов — веществ, напрямую провоцирующих развитие онкологических процессов. Производственные раздражители (аэрозоли или пары кислот) в зависимости от продолжительности воздействия могут приводить к острой или хронической химической травме, а при регулярном контакте способствуют развитию предраковых заболеваний.
- биологические факторы. Например, наличие инфекции Хеликобактер пилори (бактерия, которая живет на слизистой оболочке желудка), приводит к хроническому повреждению слизистой продуктами жизнедеятельности этой бактерии, что может стать благоприятной почвой для предраковых состояний желудочно-кишечного тракта и дальнейшего развития рака.
К эндогенным факторам относят особенности иммунитета.
Именно состояние иммунной системы является определяющим условием развития предраковых состояний. От уровня защиты зависит, смогут ли внешние или внутренние факторы нанести организму вред и запустить развитие заболевания.
К эндогенным факторам также можно отнести различные возрастные изменения и генетическую предрасположенность к определенным патологиям.
По данным исследования, опубликованного American Cancer Society, более 90% онкологических процессов обусловлены факторами внешней среды и образом жизни. Остальные 10% опухолей развиваются из-за генетических мутаций.
Диагностика и профилактика предрака
Переход предрака в рак может занимать годы, большинство из предраковых образований никогда не пройдут через злокачественное перерождение, но некоторые прогрессируют очень быстро. Как правило, именно это пытаются предотвратить специалисты. Определяющим фактором здесь является ранняя диагностика.
Проведение скрининга, детального обследования, позволяет выявить предраковые болезни, установить, возможен ли переход в рак, при необходимости определить подходящие методы лечения. Для верной постановки диагноза важны такие критерии, как привычки пациента, семейная история болезней, перенесенные заболевания и условия работы, которые могут подразумевать вредные воздействия.
Диагностика предрака зависит от его локализации.
При наличии жалоб необходимые обследования назначит врач, если жалоб нет — в качестве профилактики достаточно будет регулярной диспансеризации.
В нее входят стандартные анализы, инструментальная диагностика, а также консультации профильных специалистов. Для каждой возрастной группы подобран такой набор обследований, который с наибольшей вероятностью поможет обнаружить серьезные заболевания.
Так, каждому в рамках диспансеризации необходимо сдавать анализ крови и мочи, проходить флюорографию или делать рентген грудной клетки, а также ультразвуковое исследование органов брюшной полости. Женщинам показано УЗИ органов малого таза, консультации гинеколога и маммолога, а мужчинам — уролога. Колоно- и гастроскопия рекомендованы людям в возрасте старше сорока лет.
В качестве альтернативы диспансеризации можно пройти «чекап», индивидуально подобранный набор обследований с учетом особенностей здоровья и образа жизни пациента (например, для индивидуальной диагностики онкологических или сердечно-сосудистых заболеваний).
Кроме того, в целях профилактики развития рака и предрака следует пересмотреть свой образ жизни: сбалансированно питаться, минимизировать в рационе потенциально опасные продукты, добавить в ежедневные приемы пищи больше овощей и фруктов. Необходимо уделять время физическим нагрузкам, отказаться от вредных привычек и чаще проводить время на свежем воздухе.
Лечение опасных состояний
Лечение предраковых заболеваний бывает двух типов: удаление или разрушение очага болезни и предотвращение роста опухолевой ткани. При факультативном проявлении и низкой степени вероятности перехода в рак достаточно наблюдения в динамике. Очаг не удаляется, а лечение нацелено на регресс патологии. Облигатные проявления предрака подвергаются удалению, так как с высокой вероятностью могут переродиться в онкологическую опухоль. Однако даже после их радикального удаления важно продолжать регулярно следить за состоянием здоровья, так как всегда остается патогенный фон и существует вероятность рецидива (возврата) предракового состояния в том или ином виде.
По материалам сайта health.mail.ru
Стало известно, как изменится ОГЭ в 2021 году — Российская газета
Федеральный институт педагогических измерений (ФИПИ) опубликовал демоверсии и другие проекты документов для ОГЭ в 2021 году. Всего — материалы по 14 школьным предметам.
При этом изменений нет только в трех из них: по русскому языку, географии и информатике.
Напомним, последнее серьезное изменение в ОГЭ (экзамен для девятиклассников) произошло еще в прошлом году, когда во все предметы добавились задания, ориентированные на практику. Они были нацелены на то, чтобы проверить, как школьник может искать информацию, анализировать ее, применять знания, аргументировать свое мнение.
— Из-за эпидемиологической ситуации ОГЭ в 2020 году проведен не был. Тем не менее в проекты 2021 года внесен ряд изменений, — рассказали в Рособрнадзоре.
Так, количество заданий в ОГЭ по математике уменьшилось на одно за счет объединения заданий на преобразование алгебраических (№13 — в старой версии) и числовых выражений (№8 — в старой версии) в одно — №8. Задание на работу с последовательностями и прогрессиями (№ 12 в ОГЭ-2020) заменено на задание с практическим содержанием, направленное на проверку умения применять знания о последовательностях и прогрессиях в прикладных ситуациях — теперь оно под номером 14. Также скорректирован порядок заданий в соответствии с их тематикой и сложностью.
В ОГЭ по литературе изменена нумерация заданий. Суммарное число заданий экзаменационной работы увеличилось с 4 до 5 за счет нового задания базового уровня сложности, требующего анализа фрагмента предложенного произведения в заданном направлении. Фрагмент можно выбрать самостоятельно.
В ОГЭ по истории общее число заданий увеличено с 21 до 24. В работу включены три задания с кратким ответом (15, 16 и 17), нацеленные на проверку знаний по всеобщей истории (истории зарубежных стран).
По обществознанию количество заданий в КИМ с кратким ответом в виде одной цифры сокращено с 14 до 13. Но зато добавлено задание 5 с развернутым ответом на анализ визуальной информации.
В ОГЭ по иностранным языкам тоже внесены изменения. Раздел «Задания по аудированию» теперь состоит из 11 заданий с кратким ответом. В разделе «Задание по письменной речи» в задании 35 необходимо написать личное (электронное) письмо в ответ на электронное письмо друга по переписке.
В ОГЭ по биологии сократилось общее количество заданий с 30 до 29. В первой части работы количество заданий уменьшилось на два, но во второй части добавлено одно задание.
В ОГЭ по физике к тексту физического содержания вместо двух заданий с выбором одного верного ответа предлагается одно задание на множественный выбор. Увеличилось число заданий с развернутым ответом: добавлена еще одна качественная задача. В 2021 году задания 21 будут построены преимущественно на прогнозировании результатов опытов или интерпретации их результатов, а задания 22 — на практико-ориентированном контексте. Расширилось содержание заданий 17 (это экспериментальное задание на реальном оборудовании). К проведению косвенных измерений добавлено исследование зависимости одной физической величины от другой, включающее не менее трех прямых измерений с записью абсолютной погрешности.
Работа по химии в 2021 году тоже изменилась. В заданиях 2 (определение строения атома химического элемента и характеристика его положения в Периодической системе) и 3 (построение последовательности элементов с учетом закономерностей изменения свойств элементов по группам и периодам) требуется вписать в поле ответа цифровые значения, соответствующие условию задания. В заданиях 5 (виды химической связи), 8 (химические свойства простых веществ и оксидов) и 16 (чистые вещества, смеси, правила работы с веществами в лаборатории и в быту) требуется осуществить выбор двух ответов из предложенных в перечне 5 вариантов (множественный выбор ответа). В заданиях 4 (валентность, степень окисления) и 12 (признаки химических реакций) требуется установить соответствия между позициями двух множеств.
Все это сейчас — на общественном обсуждении. Все замечания и предложения принимаются на адрес: [email protected] до 30 сентября 2020 года.
Что такое обратный осмос и как он работает
Обратный осмос или RO — это метод фильтрации, который используется для удаления ионов и молекул из раствора путем приложения давления к раствору на одной стороне полупроницаемой или селективной мембраны. Большие молекулы (растворенные вещества) не могут пересечь мембрану, поэтому они остаются на одной стороне. Вода (растворитель) может проникать через мембрану. В результате молекулы растворенных веществ становятся более концентрированными на одной стороне мембраны, в то время как противоположная сторона становится более разбавленной.
Как работает обратный осмос
Чтобы понять обратный осмос, он помогает сначала понять, как масса переносится посредством диффузии и регулярного осмоса. Диффузия — это движение молекул из области с более высокой концентрацией в область с более низкой концентрацией. Осмос — это особый случай диффузии, в которой молекулы представляют собой воду, а градиент концентрации возникает через полупроницаемую мембрану. Полупроницаемая мембрана пропускает воду, но понятия (например.g., Na + , Ca 2+ , Cl — ) или более крупные молекулы (например, глюкоза, мочевина, бактерии). Диффузия и осмос являются термодинамически благоприятными и будут продолжаться до тех пор, пока не будет достигнуто равновесие. Осмос можно замедлить, остановить или даже обратить, если к мембране приложить достаточное давление со «концентрированной» стороны мембраны.
Обратный осмос происходит, когда вода перемещается через мембрану против градиента концентрации , от более низкой концентрации к более высокой.Для иллюстрации представьте себе полупроницаемую мембрану с пресной водой с одной стороны и концентрированным водным раствором с другой. Если имеет место нормальный осмос, пресная вода будет проходить через мембрану, разбавляя концентрированный раствор. При обратном осмосе на сторону с концентрированным раствором оказывается давление, заставляющее молекулы воды проходить через мембрану на сторону пресной воды.
Для обратного осмоса используются мембраны разного размера. Хотя поры небольшого размера лучше справляются с фильтрацией, для перемещения воды требуется больше времени.Это похоже на попытку вылить воду через фильтр (большие отверстия или поры) по сравнению с попыткой вылить ее через бумажное полотенце (отверстия меньшего размера). Однако обратный осмос отличается от простой мембранной фильтрации, поскольку он включает диффузию и зависит от скорости потока и давления.
Использование обратного осмоса
Обратный осмос часто используется для фильтрации воды в коммерческих и жилых помещениях. Это также один из методов опреснения морской воды. Обратный осмос не только снижает содержание соли, но также может отфильтровывать металлы, органические загрязнения и патогены.Иногда обратный осмос используется для очистки жидкостей, в которых вода является нежелательной примесью. Например, обратный осмос можно использовать для очистки этанола или зернового спирта, чтобы повысить его стойкость.
История обратного осмоса
Обратный осмос — это не новый метод очистки. Первые примеры осмоса через полупроницаемые мембраны были описаны Жаном-Антуаном Нолле в 1748 году. Хотя этот процесс был известен в лабораториях, он не использовался для опреснения морской воды до 1950 года в Калифорнийском университете в Лос-Анджелесе.Многие исследователи усовершенствовали методы использования обратного осмоса для очистки воды, но этот процесс был настолько медленным, что его невозможно было использовать в промышленных масштабах. Новые полимеры позволили производить более эффективные мембраны. К началу 21 века опреснительные установки стали способны опреснять воду со скоростью 15 миллионов галлонов в день, при этом около 15 000 заводов уже работают или планируются.
8.6: Обратный осмос — Chemistry LibreTexts
Цели обучения
- Что такое обратный осмос и каково его основное применение?
- Объясните роль осмотического давления в сохранении пищевых продуктов и приведите пример.
- Опишите роль осмоса в подъеме воды в растениях (где полупроницаемая мембрана?) И почему он не может быть единственной причиной для очень высоких деревьев.
Если для достижения осмотического равновесия требуется давление в \ (Π \) атм, то из этого следует, что приложение более высокого гидростатического давления к стороне осмотической ячейки с высоким содержанием растворенных веществ заставит воду течь обратно в пресную среду. водная сторона. Этот процесс, известный как обратный осмос , в настоящее время является основной технологией, применяемой для опреснения океанской воды и восстановления «использованной» воды электростанций, сточных вод и даже сточных вод.Он также широко используется для деионизации обычной воды и ее очистки в промышленных целях (особенно в производстве напитков и продуктов питания) и питьевых целях.
Для предварительной обработки обычно используется фильтрация с активированным углем для удаления органических веществ и хлора (который имеет тенденцию к повреждению мембран обратного осмоса). Хотя бактерии не могут проходить через полупроницаемые мембраны, в последних могут образовываться точечные утечки, поэтому часто рекомендуется какая-либо форма дезинфекции. Эффективность и стоимость или RO критически зависят от свойств полупроницаемой мембраны.
(слева) Крупные установки обратного осмоса используют картриджи с несколькими мембранами. Этот в Тампа-Бэй, Флорида, поставляет опресненную питьевую воду для 2,4 миллиона жителей. (справа) Многие устройства обратного осмоса меньшего размера, подходящие для домашнего использования, могут поместиться под кухонной раковиной.Осмотическое производство электроэнергии
Осмотическое давление морской воды почти 26 атм. Поскольку давление в 1 атм будет поддерживать столб воды высотой 10,6 м, это означает, что осмотический поток пресной воды через полупроницаемую мембрану в морскую воду в принципе может поддерживать столб последней размером 26 x 10.3 = 276 м (904 фута)!
Итак, представьте осмотическую ячейку, в одну сторону которой поступает пресная вода из реки, а с другой стороны — морская вода. Осмотический поток пресной воды в сторону забортной воды заставляет последнюю подниматься по стояку, содержащему турбину, соединенную с генератором, обеспечивая, таким образом, постоянный и бестопливный источник электроэнергии. Ключевым компонентом такой схемы, впервые предложенной израильским ученым в 1973 году и известной как осмос с замедленным давлением (PRO), является, конечно, полупроницаемая мембрана, способная пропускать воду с достаточно высокой скоростью.
Первый в мире экспериментальный завод PRO был открыт в 2009 году в Норвегии. Его мощность составляет всего 4 кВт, но он служит доказательством схемы, которая, по оценкам, способна обеспечить до 2000 тераватт-часов энергии по всему миру. Полупроницаемая мембрана работает при давлении около 10 атм и пропускает 10 л воды в секунду, генерируя около 1 ватт на 2 м мембраны. PRO — это всего лишь одна из форм мощности градиента солености , которая зависит от разницы между концентрациями соли в разных водоемах.
1 атм эквивалентен 1034 г см –2 , поэтому из плотности воды получаем (1034 г см –2 ) ÷ (1 г см –3 ) = 1034 см = 10,3 м.
Осмос в биологии и физиологии
Поскольку многие мембраны и ткани клеток растений и животных имеют тенденцию быть проницаемыми для воды и других малых молекул, осмотический поток играет важную роль во многих физиологических процессах.
Физиологический раствор
Внутри клетки содержатся соли и другие растворенные вещества, которые разбавляют внутриклеточную воду.Если клеточная мембрана проницаема для воды, при контакте клетки с чистой водой вода будет втягиваться в клетку, что приведет к ее разрыву. Это легко и наглядно увидеть, если поместить эритроциты в каплю воды и наблюдать в микроскоп, как они лопаются. Это причина того, что для поддержания объема крови или для введения терапевтических агентов во время медицинских процедур вводят «нормальный физиологический раствор», а не чистую воду.
Чтобы предотвратить раздражение чувствительных мембран, всегда следует добавлять немного соли в воду, используемую для промывания глаз, носа, горла или кишечника.Нормальный физиологический раствор содержит 0,91% (мас. / Об.) Хлорида натрия, что соответствует 0,154 M, что делает его осмотическое давление близким к давлению крови.
Консервирование
Сушка фруктов, использование сахара для консервирования джема и желе, а также использование соли для консервирования некоторых видов мяса — старые методы консервирования продуктов. Идея состоит в том, чтобы снизить концентрацию воды до уровня ниже, чем у живых организмов. Из любой бактериальной клетки, попавшей в такую среду, будет вытягиваться осмотически вода, и она погибнет от обезвоживания.Подобный эффект замечает любой, кто подолгу прижимает леденец к внутренней стенке рта; пораженная поверхность становится обезвоженной и становится заметно шероховатой при прикосновении к языку.
В пищевой промышленности то, что известно как вода активность измеряется по шкале от 0 до 1, где 0 означает отсутствие воды, а 1 означает всю воду. Микроорганизмы, вызывающие порчу пищевых продуктов, как правило, подавляются в пищевых продуктах, где активность воды ниже 0.6. Однако, если pH пищи ниже 4,6, микроорганизмы подавляются (но не уничтожаются немедленно), когда активность воды ниже 0,85.
Диарея
При наличии чрезмерного количества растворенных веществ в кишечнике вода вытягивается из стенок кишечника, вызывая диарею. Это может произойти при употреблении в пищу пищи, которая не может быть переварена должным образом (например, молоко у людей с непереносимостью лактозы). Непереваренный материал способствует концентрации растворенного вещества, повышая его осмотическое давление.Ситуация усугубляется, если материал подвергается бактериальной ферментации, которая приводит к образованию метана и углекислого газа, вызывая пенистые выделения.
Водный транспорт в растениях
Осмотический поток играет важную роль в транспортировке воды от ее источника в почве к ее высвобождению путем транспирации из листьев, ему помогают силы водородной связи между молекулами воды. Подъем капилляров не считается существенным фактором.
Вода поступает в корни через осмос, что обусловлено низкой концентрацией воды внутри корней, которая поддерживается как активным [неосмотическим] переносом ионных питательных веществ из почвы, так и поступлением сахаров, которые фотосинтезируются в листьях. Это создает определенное количество корневого давления , которое направляет молекулы воды вверх по сосудистым каналам стебля или ствола. Но максимальное давление корней, которое было измерено, может подтолкнуть воду только примерно на 20 метров, в то время как самые высокие деревья превышают 100 метров.Давление на корни может быть единственной движущей силой переноса воды у невысоких растений или даже у высоких, таких как деревья без листьев. Любой, кто видел кажущиеся нежными и хрупкие растения, пробивающиеся сквозь асфальтовое покрытие, не может не быть впечатлен!
Но когда более высокие растения активно дышат (теряют воду в атмосферу), осмос усиливается за счет того, что физиологи растений называют напряжением сцепления или тяговым усилием . Когда каждая молекула H 2 O выходит из отверстия в листе он тянет за собой цепочку молекул под собой.Таким образом, водородные связи не менее важны, чем осмос в общем процессе транспортировки воды. Если почва становится сухой или засоленной, осмотическое давление снаружи корня становится больше, чем внутри растения, и растение страдает от «напряжения воды», то есть увядания.
Пьют ли рыбу воду? Они мочатся?
Следующий раздел довольно длинный, но для тех, кто интересуется биологией, он предлагает прекрасный пример того, как ограничения, наложенные осмосом, привели к эволюции существ, живущих в океане, в пресноводные виды.Это касается аммиака NH 3 , продукта метаболизма белков, который вырабатывается у всех животных, но очень токсичен и должен быть устранен.
Морские беспозвоночные (те, что живут в морской воде) покрыты мембранами, достаточно проницаемыми для воды и небольших молекул, таких как аммиак. Таким образом, вода может диффундировать в любом направлении по мере необходимости, а аммиак может распространяться так же быстро, как и образуется. Здесь ничего особенного.
У беспозвоночных, обитающих в пресной воде, действительно есть проблема: концентрация соли в их телах составляет около 1%, что намного больше, чем в пресной воде.По этой причине они развили окружающие мембраны, которые в значительной степени непроницаемы для солей (для предотвращения их диффузии из организма) и для воды (для предотвращения осмотического притока внутрь). Но эти организмы также должны иметь возможность обмениваться кислородом и углекислым газом со своими среда. Специальные органы дыхания (жабры), которые опосредуют этот процесс, поскольку они проницаемы для этих двух газов, также будут пропускать молекулы воды (размеры которых сопоставимы с размерами дыхательных газов).Чтобы защитить пресноводных беспозвоночных от разрушительных последствий неограниченного притока воды через жаберные мембраны, эти животные обладают специальными выделительными органами, которые выводят избыток воды обратно в окружающую среду. Таким образом, у таких животных через тело проходит постоянный поток воды. Аммиак и другие вещества, которые необходимо вывести, поглощаются этим потоком, который представляет собой непрерывный поток разбавленной мочи.
Рыбы делятся на два основных класса: у большинства рыб костлявые скелеты, известные как костистые.Акулы и скаты имеют хрящ вместо костей, и их называют пластиножаберными. С костистыми насекомыми, обитающими в пресной воде, ситуация во многом такая же, как и с пресноводными беспозвоночными; они постоянно впитывают и выводят воду. Тот факт, что животное живет в воде, не означает, что у него неограниченный запас воды. У морских костистых насекомых есть более сложная проблема. Их жабры водопроницаемы, как и у морских беспозвоночных. Но содержание соли в морской воде (около 3%), превышающее примерно 1% в крови рыбы, вытягивает воду из рыбы.Таким образом, эти животные постоянно теряют воду и были бы подвержены высыханию, если бы вода могла свободно выходить из их жабр. У некоторых, конечно, есть, и вместе с ними уходит большая часть азота в форме NH 3 .
Физиология лосося реагирует на пресную и морскую воду, чтобы поддерживать осмотический баланс. Рыбы являются осморегуляторами, но должны использовать разные механизмы, чтобы выжить в (а) пресноводной или (б) морской среде. Изображение используется с разрешением (CC BY 3.0; OpenStax).Таким образом, большая часть отработанного азота выходит не через обычные органы выделения, как у большинства позвоночных, а через жабры.Но чтобы предотвратить чрезмерную потерю воды, жабры уменьшили проницаемость для этой воды, а вместе с ней и для NH 3 сопоставимых размеров. Таким образом, чтобы предотвратить отравление аммиаком, его остаток превращается в нетоксичное вещество (оксид триметиламина (CH 3 ) 3 NO), которое выводится через почки.
Морские гибкие ответвления решают проблему потери воды другим способом: они преобразуют отработанный аммиак в мочевину (NH 3 ) 2 CO, который хорошо растворим и не токсичен.Их почки способны контролировать количество выделяемой мочевины, так что их кровь удерживает около 2-2,5% этого вещества. В сочетании с 1 процентом солей и других веществ в их крови это повышает осмотическое давление внутри животного до уровня немного выше, чем у морской воды. Таким образом, тот же механизм, который защищает их от отравления аммиаком, также обеспечивает им достаточное водоснабжение.
Авторы и авторство
RO и химия воды
Ограничения производительности
Химия воды
Связанные с мембраной
Проектирование системы
Конструктивные ограничения
— Сульфат
— Бикарбонат
TDS
Качество продукции
Восстановление
Рабочее давление
НЕОРГАНИЧЕСКИЕ ФУЛАНТЫ
ДЕПОЗИТ | ОБЩИЙ | МЕНЬШЕ ОБЩЕГО |
ФОСФАТЫ | CA, MG | AL, FE, SR, BA, F, ПБ |
КАРБОНАТЫ | CA, MG | SR, BA, PB, CU |
СУЛЬФАТЫ | CA | SR, BA |
СИЛИКАТЫ | AL, TI, K, NA | FE, MN, MG, CA |
ГИДРОКСИДЫ | FE, MG, MN | AL |
СУЛЬФИДЫ | FE, Миннесота |
ЖЕСТКОСТЬ ВОДЫ
1.Всего кальция и содержание магния.
2. Выражается в Мг / л карбонат кальция.
1 зерно = 17,1 мг / л
3. Когда твердость больше, чем общая щелочность, то превышение
называется постоянной твердостью.
Когда жгут меньше всего щелочность, вся газированная
или временная твердость.
4. Умягчение воды обменивает ионы кальция и магния (жесткость)
с ионами натрия (из соли)
СРОК ЖЕСТКОСТИ / ЗЕРНА
Мягкий Вода 0 — 1
Слегка жесткий 1 — 3
Умеренно сложно 3-7
Жесткий 7–10
Очень тяжело Более 10
НОМОГРАММА ОПРЕДЕЛЕНИЯ ЗНАЧЕНИЯ pH ПО ИЗВЕСТНОМУ СО2 И ЩЕЛОЧНОСТИ
ИНДЕКС НАСЫЩЕННОСТИ ЛАНЖЕЛЬЕРА (ИНДЕКС НАСЫЩЕННОСТИ CACO3)
— Критерии, используемые для определения необходимость контроля отложений карбоната кальция.
LSI = pH — pH
pHs = EPCA + p ALK + C — От график
pHs = (9,30 + A + B) — (C + D) — Из справочника
Для расчета pH вам необходимо знать:
* Концентрация кальция брака (CACO3)
* Щелочность брака (CACO3)
* TDS отклонения
* pH отбраковки
Если LSI положительный = масштаб формирование
Если LSI равен 0 = нейтраль
Если LSI отрицательный = коррозионный Тенденции
СРАВНЕНИЕ РАСТВОРИМОСТИ
CaSO 4
| PPM Ca
PPM SO 4 | MG / L AS CaSO 4 |
Чистый Вода | 1.9 м | 1874 |
@ I R = 0,1133 | 2,8 млн | 2275 |
10 мг / л HMP | 10 млн | 4298 |
SRSO 4
| PPM SR
PPM SO 4 | MG / L AS СРСО 4 |
Чистый Вода | 3.1 К | 102 |
@ I R = 0,1133 | 12 К | 201 |
10 мг / л HMP | 24 К | 402 |
БАСО 4 | PPM BA
PPM SO 4 | MG / L AS БАСО 4 |
Чистый Вода | 0.9 | 2,2 |
@ I R = 0,1133 | 2,9 | 6,8 |
10 мг / л HMP | 5,8 | 13,6 |
CAF 2 | MG / L AS CAF 2 |
Чистый Вода | 16.8 |
Кремнезем
Воздействие кремнезема при обратном осмосе
Кремнезем присутствует в воде в диапазоне 1-100 мг / л. При 25 ° C (или 77 ° F) и pH растворимости кремнезема в воде составляет около 100 мг / л. При 30 ° C (или 86 ° F) растворимость составляет 120 мг / л, тогда как при pH 7 и 150. мг / л при pH 5. Эта информация представлена на графике снизу:
Другие нерастворимые соединения
утюг : Воздействие на воздух, хлорирование
АЛЮМИНИЙ ГИДРОКСИД : Наименее растворим при A pH из 5.7 Эффективность очистки при pH от 3 до 4.
HUMIC ACID : High Mol. Вес. органический кислоты. Растворимость низкая при pH от 5 до 6. Рекомендуется фильтровать после корректировки pH.
СЕРЫ : pH менее 6, сульфид в воде преобразован в сероводород. Плохой отказ.
Удалить дегазатором. Некоторый образующаяся сера превращается в сульфат при хлорировании. Обрастание серой необратимый.
Производительность мембраны со временем
1.Взвешенные твердые частицы осаждаются медленно.
2. Микроорганизмы медленно растут и размножаются.
3. Может иметь место масштабирование.
4. Окислитель (хлор) атакует мембрану.
Увеличение падения давления
Потеря пермеата
Повышение TDS
пермеатаPuretec Промышленная вода | Что такое обратный осмос?
Обратный осмос — это технология, которая используется для удаления большого количества загрязняющих веществ из воды путем проталкивания воды под давлением через полупроницаемую мембрану.
Эта статья нацелена на аудиторию, которая практически не имеет опыта работы с водой обратного осмоса и попытается объяснить основы простыми словами, которые должны дать читателю лучшее общее представление о технологии воды обратного осмоса и ее применениях. .
В этой статье рассматриваются следующие темы:
- Общие сведения об осмосе и воде обратного осмоса
- Как работает обратный осмос (RO)?
- Какие загрязнения удаляет обратный осмос (RO)?
- Расчет производительности и конструкции систем обратного осмоса (RO)
- Отказ от соли%
- Солевой проход%
- Восстановление %
- Фактор концентрации
- Скорость потока
- Баланс массы
- Понимание разницы между проходами и ступенями в системе обратного осмоса (RO)
- 1 этап против двухступенчатой системы обратного осмоса (RO)
- Множество
- Система обратного осмоса (RO) с рециркуляцией концентрата
- Однопроходные и двухходовые системы обратного осмоса (RO)
- Предварительная обработка обратного осмоса (RO)
- Обрастание
- Масштабирование
- Химическая атака
- Механическое повреждение
- Решения для предварительной обработки обратного осмоса (RO)
- Мультимедийная фильтрация
- Микрофильтрация
- Антискаланты и ингибиторы образования накипи
- Умягчение ионным обменом
- Бисульфит натрия (SBS) для инъекций
- Гранулированный активированный уголь (GAC)
- Тенденции производительности обратного осмоса (RO) и нормализация данных
- Очистка мембран обратным осмосом (RO)
- Резюме
Что такое обратный осмос
Обратный осмос , обычно называемый RO , представляет собой процесс, в котором вы деминерализуете или деионизируете воду, проталкивая ее под давлением через полупроницаемую мембрану обратного осмоса.
Осмос
Чтобы понять цель и процесс обратного осмоса, вы должны сначала понять естественный процесс осмоса .
Осмос — это естественное явление и один из важнейших процессов в природе. Это процесс, при котором более слабый солевой раствор имеет тенденцию переходить в крепкий солевой раствор. Примеры осмоса — это когда корни растений поглощают воду из почвы, а наши почки поглощают воду из нашей крови.
Ниже представлена диаграмма, показывающая, как работает осмос. Раствор с меньшей концентрацией будет иметь естественную тенденцию переходить в раствор с более высокой концентрацией. Например, если у вас есть контейнер, полный воды с низкой концентрацией соли, и другой контейнер, полный воды с высокой концентрацией соли, и они разделены полупроницаемой мембраной, тогда вода с более низкой концентрацией соли начнет мигрировать. в сторону емкости с водой с более высокой концентрацией соли.
Полупроницаемая мембрана — это мембрана, которая пропускает одни атомы или молекулы, но не другие. Простой пример — дверь-ширма. Он позволяет молекулам воздуха проходить сквозь него, но не вредителям или чему-либо большему, чем отверстия в дверце экрана. Другой пример — ткань для одежды Gore-tex, содержащая чрезвычайно тонкую пластиковую пленку, в которой вырезаны миллиарды мелких пор. Поры достаточно велики, чтобы пропускать водяной пар, но достаточно малы, чтобы препятствовать прохождению жидкой воды.
Обратный осмос — это процесс обратного осмоса . В то время как осмос происходит естественным образом без потребности в энергии, чтобы обратить процесс осмоса вспять, вам необходимо приложить энергию к более солевому раствору. Мембрана обратного осмоса — это полупроницаемая мембрана, которая позволяет проходить молекулам воды, но не большинству растворенных солей, органических веществ, бактерий и пирогенов. Однако вам необходимо «протолкнуть» воду через мембрану обратного осмоса, применяя давление, превышающее естественное осмотическое давление, чтобы опреснить (деминерализовать или деионизировать) воду в процессе, пропуская чистую воду, удерживая при этом большую часть. загрязняющих веществ.
Ниже представлена диаграмма, описывающая процесс обратного осмоса. Когда к концентрированному раствору прикладывается давление, молекулы воды выталкиваются через полупроницаемую мембрану, и загрязнения не пропускаются.
Как работает обратный осмос?
Обратный осмос работает с использованием насоса высокого давления для увеличения давления на солевой стороне обратного осмоса и проталкивания воды через полупроницаемую обратную мембрану, оставляя почти все (от 95% до 99%) растворенных солей в воде. отклонить поток.Необходимое давление зависит от концентрации соли в исходной воде. Чем более концентрирована исходная вода, тем большее давление требуется для преодоления осмотического давления.
Опресненная вода, которая является деминерализованной или деионизированной, называется пермеатной (или продуктивной) водой. Водный поток, который несет концентрированные загрязнители, которые не прошли через мембрану обратного осмоса, называется потоком отбракованных (или концентрированных).
Когда исходная вода входит в мембрану обратного осмоса под давлением (давление, достаточное для преодоления осмотического давления), молекулы воды проходят через полупроницаемую мембрану, а соли и другие загрязнители не могут проходить и выводятся через сбросной поток (также известный в виде потока концентрата или рассола), который идет в канализацию или может быть возвращен в систему подачи питательной воды в некоторых случаях для повторного использования через систему обратного осмоса для экономии воды.Вода, которая проходит через мембрану обратного осмоса, называется пермеатом или водой-продуктом, и обычно из нее удаляется от 95% до 99% растворенных солей.
Важно понимать, что система обратного осмоса использует перекрестную фильтрацию, а не стандартную фильтрацию, при которой загрязнения собираются внутри фильтрующего материала. При перекрестной фильтрации раствор проходит через фильтр или пересекает фильтр с двумя выходами: фильтрованная вода идет в одну сторону, а загрязненная вода идет в другую сторону.Чтобы избежать накопления загрязняющих веществ, фильтрация с поперечным потоком позволяет воде сметать накопившиеся загрязнения, а также обеспечивает достаточную турбулентность для поддержания чистоты поверхности мембраны.
Какие загрязняющие вещества обратный осмос удалит из воды?
Обратный осмос способен удалять до 99% + растворенных солей (ионов), частиц, коллоидов, органических веществ, бактерий и пирогенов из питательной воды (хотя нельзя полагаться на систему обратного осмоса для удаления 100% бактерий и вирусы).Мембрана обратного осмоса отфильтровывает загрязнения в зависимости от их размера и заряда. Любое загрязняющее вещество с молекулярной массой более 200, вероятно, отторгается правильно работающей системой обратного осмоса (для сравнения молекулярная масса молекулы воды составляет 18). Точно так же, чем больше ионный заряд загрязнителя, тем больше вероятность, что он не сможет пройти через мембрану обратного осмоса. Например, ион натрия имеет только один заряд (одновалентный) и не отторгается RO мембраной, как, например, кальций, который имеет два заряда.Аналогичным образом, именно поэтому система обратного осмоса не очень хорошо удаляет газы, такие как CO2, потому что они не сильно ионизируются (заряжаются) в растворе и имеют очень низкий молекулярный вес. Поскольку система обратного осмоса не удаляет газы, пермеатная вода может иметь уровень pH немного ниже, чем обычно, в зависимости от уровней CO2 в исходной воде, поскольку CO2 преобразуется в угольную кислоту.
Обратный осмос очень эффективен при очистке солоноватых, поверхностных и грунтовых вод как для больших, так и для малых потоков.Некоторые примеры отраслей, в которых используется вода обратного осмоса, включают фармацевтическую промышленность, питательную воду для котлов, продукты питания и напитки, отделку металлов и производство полупроводников и многие другие.
Расчетные характеристики и расчетные характеристики обратного осмоса
Есть несколько расчетов, которые используются для оценки производительности системы обратного осмоса, а также для конструктивных соображений. В системе обратного осмоса есть приборы, которые отображают качество, расход, давление, а иногда и другие данные, такие как температура или часы работы.Чтобы точно измерить производительность системы обратного осмоса, вам потребуются как минимум следующие рабочие параметры:
- Давление подачи
- Давление пермеата
- Давление концентрата
- Проводимость корма
- Проводимость пермеата
- Расход сырья
- Поток пермеата
- Температура
Отказ от соли%
Это уравнение показывает, насколько эффективно мембраны обратного осмоса удаляют загрязнения.Он не говорит вам, как работает каждая отдельная мембрана, а скорее как система в целом работает. Хорошо спроектированная система обратного осмоса с правильно функционирующими мембранами обратного осмоса будет отбрасывать от 95% до 99% большинства загрязнителей питательной воды (которые имеют определенный размер и заряд). Вы можете определить, насколько эффективно мембраны обратного осмоса удаляют загрязнения, используя следующее уравнение:
| Отклонение соли% = | Электропроводность питательной воды — Электропроводность пермеатной воды | × 100 |
| Электропроводность сырья |
Чем выше отвод соли, тем лучше работает система.Низкое отторжение соли может означать, что мембраны требуют очистки или замены.
Солевой проход%
Это просто обратное отторжение соли, описанное в предыдущем уравнении. Это количество солей, выраженное в процентах, которые проходят через систему обратного осмоса. Чем ниже солевой канал, тем лучше работает система. Высокий уровень прохождения соли может означать, что мембраны требуют очистки или замены.
| Прохождение соли% = (1 -% отклонения соли) |
Восстановление %
Процент извлечения — это количество воды, которое «извлекается» как хорошая пермеатная вода.Другой способ думать о процентном извлечении — это количество воды, которое не отправляется в дренаж в виде концентрата, а собирается в виде пермеата или воды в виде продукта. Более высокий процент извлечения означает, что вы отправляете меньше воды в дренаж в виде концентрата и экономите больше пермеата. Однако, если процент извлечения слишком высок для конструкции обратного осмоса, это может привести к более серьезным проблемам из-за образования накипи и засорения. % Извлечения для системы обратного осмоса устанавливается с помощью программного обеспечения для проектирования с учетом множества факторов, таких как химический состав питательной воды и предварительная обработка обратным осмосом перед системой обратного осмоса.Следовательно, правильный процент извлечения, при котором должен работать RO, зависит от того, для чего он был разработан. Рассчитав процент извлечения, вы можете быстро определить, работает ли система не по назначению. Расчет% извлечения ниже:
| % Извлечение = | Скорость потока пермеата (галлонов в минуту) | × 100 |
| Скорость подачи (галлонов в минуту) |
Например, если степень извлечения составляет 75%, это означает, что на каждые 100 галлонов питательной воды, попадающей в систему обратного осмоса, вы получаете 75 галлонов пригодной для использования пермеатной воды и 25 галлонов сточных вод в виде концентрата.Промышленные системы обратного осмоса обычно имеют степень извлечения от 50% до 85% в зависимости от характеристик питательной воды и других проектных соображений.
Фактор концентрации
Коэффициент концентрации связан с восстановлением системы обратного осмоса и является важным уравнением при проектировании системы обратного осмоса. Чем больше воды вы извлекаете в виде пермеата (чем выше процент извлечения), тем больше концентрированных солей и загрязняющих веществ вы собираете в потоке концентрата. Это может привести к более высокому потенциалу образования накипи на поверхности мембраны обратного осмоса, когда коэффициент концентрации слишком высок для конструкции системы и состава питательной воды.
| Коэффициент концентрации = | 1 |
| 1 — Извлечение% |
Концепция не отличается от котла или градирни. В обоих случаях из системы выходит очищенная вода (пар), в результате чего остается концентрированный раствор. По мере увеличения степени концентрации могут быть превышены пределы растворимости и осаждение на поверхности оборудования в виде накипи.
Например, если ваш поток подачи составляет 100 галлонов в минуту, а поток пермеата составляет 75 галлонов в минуту, то извлечение будет (75/100) x 100 = 75%. Чтобы найти коэффициент концентрации, формула должна быть 1 ÷ (1-75%) = 4.
Коэффициент концентрации 4 означает, что вода, поступающая в поток концентрата, будет в 4 раза более концентрированной, чем исходная вода. Если исходная вода в этом примере составляла 500 частей на миллион, тогда поток концентрата был бы 500 x 4 = 2000 частей на миллион.
Поток
| Gfd = | галлонов в минуту пермеата × 1440 мин / день |
| Количество элементов RO в системе × площадь каждого элемента RO |
Например, у вас есть следующее:
Система обратного осмоса производит 75 галлонов пермеата в минуту.У вас есть 3 сосуда обратного осмоса, и каждый сосуд содержит 6 мембран обратного осмоса. Таким образом, у вас всего 3 x 6 = 18 мембран. В системе обратного осмоса используется мембрана Dow Filmtec BW30-365. Этот тип мембраны (или элемента) обратного осмоса имеет площадь поверхности 365 квадратных футов.
Чтобы найти поток (Gfd):
| Gfd = | 75 галлонов в минуту × 1440 мин / день | = | 108 000 |
| 18 элементов × 365 кв. Футов | 6 570 |
Поток 16 Гсф.
Это означает, что 16 галлонов воды проходит через каждый квадратный фут каждой мембраны обратного осмоса в день. Это число может быть хорошим или плохим в зависимости от типа химического состава питательной воды и конструкции системы. Ниже приводится общее практическое правило для диапазонов потоков для различных источников воды, которые можно лучше определить с помощью программного обеспечения для проектирования обратного осмоса. Если бы вы использовали мембраны обратного осмоса Dow Filmtec LE-440i в приведенном выше примере, то поток был бы 14. Поэтому важно учитывать, какой тип мембраны используется, и стараться поддерживать тип мембраны одинаковым во всей системе. .
| Источник питательной воды | Gfd |
|---|---|
| Сточные воды | 5-10 |
| Морская вода | 8-12 |
| Солоноватоводные поверхностные воды | 10-14 |
| Солоноватая колодезная вода | 14–18 |
| Пермеат обратного осмоса | 20-30 |
Баланс массы
Уравнение массового баланса используется для определения того, правильно ли показывает ваш расходомер и приборы контроля качества или требует калибровки.Если ваши приборы не считывают правильно, то собираемые вами данные о производительности бесполезны. Для выполнения расчета массового баланса вам потребуется собрать следующие данные из системы обратного осмоса:
- Расход сырья (галлонов в минуту)
- Расход пермеата (галлонов в минуту)
- Расход концентрата (галлонов в минуту)
- Проводимость питания (мкСм)
- Проводимость пермеата (мкСм)
- Концентрат Проводимость (мкСм)
Уравнение баланса массы:
(Поток исходного материала 1 x проводимость исходного материала) = (расход пермеата x проводимость пермеата)
+ (расход концентрата x проводимость концентрата)
1 Поток исходного материала равен потоку пермеата + потоку концентрата
Например, если вы собрали следующие данные из системы обратного осмотра:
| Поток пермеата | 5 галлонов в минуту |
| Проводимость сырья | 500 мкСм |
| Проводимость пермеата | 10 мкСм |
| Поток концентрата | 2 галлона в минуту |
| Концентрат Проводимость | 1200 мкСм |
Тогда уравнение баланса масс будет:
(7 x 500) = (5 x 10) + (2 x 1200)
3,500 ≠ 2,450
Тогда найдите разницу
(разница / сумма) x 100
((3500 — 2450) / (3500 + 2450)) x 100
= 18%
Разница в +/- 5% — это нормально.Обычно достаточно разницы от +/- 5% до 10%. Разница в> +/- 10% недопустима, и требуется калибровка оборудования обратного осмоса, чтобы гарантировать, что вы собираете полезные данные. В приведенном выше примере уравнение баланса массы обратного осмоса выходит за пределы допустимого диапазона и требует внимания.
Система обратного осмоса (RO): понимание разницы между проходами и стадиями в системе обратного осмоса (RO)
Термины этап и этап часто ошибочно принимают за одно и то же в системе обратного осмотра и могут сбивать с толку терминологию оператора обратного осмотра.Важно понимать разницу между 1 и 2 этапами RO и 1 и 2 проходами RO.
Разница между одно- и двухступенчатой системой обратного осмоса
В одноступенчатой системе обратного осмоса питательная вода входит в систему обратного осмоса одним потоком и выходит из системы обратного осмоса в виде концентрата или пермеата.
В двухступенчатой системе концентрат (или отходы) с первой ступени затем становится питательной водой для второй ступени. Пермеатная вода, собираемая с первой ступени, объединяется с пермеатной водой со второй ступени.Дополнительные этапы увеличивают выход из системы.
Множество
В системе обратного осмоса массив описывает физическое расположение сосудов под давлением в двухступенчатой системе. Сосуды высокого давления содержат мембраны обратного осмоса (обычно в сосуде высокого давления находится от 1 до 6 мембран обратного осмоса). На каждой ступени может быть определенное количество сосудов высокого давления с мембранами обратного осмоса. Затем отбраковка каждой ступени становится потоком сырья для следующей последующей ступени.Двухступенчатая система обратного осмоса, показанная на предыдущей странице, представляет собой массив 2: 1, что означает, что концентрат (или отбраковка) из первых 2 сосудов обратного осмоса подается в следующий 1 сосуд.
Система обратного осмоса с рециркуляцией концентрата
С системой обратного осмоса, которая не может быть правильно организована, и химический состав питательной воды позволяет это, можно использовать установку рециркуляции концентрата, в которой часть потока концентрата возвращается в питательную воду на первую ступень, чтобы помочь увеличить восстановление системы.
Однопроходный обратный осмос против двухходового обратного осмоса
Подумайте о проходе как об отдельной системе обратного осмоса. Имея это в виду, разница между однопроходной системой обратного осмоса и двухпроходной системой обратного осмоса заключается в том, что при двухпроходной системе обратного осмоса пермеат из первого прохода становится питательной водой для второго прохода (или второго обратного осмоса), что в конечном итоге дает пермеат гораздо более высокого качества, потому что он прошел через две системы обратного осмоса.
Помимо получения пермеата гораздо более высокого качества, система двойного прохода также позволяет удалять газообразный диоксид углерода из пермеата путем нагнетания щелочи между первым и вторым проходами.Использование CO 2 нежелательно, если после обратного осмоса используются слои ионообменной смолы со смешанным слоем. Добавляя каустик после первого прохода, вы увеличиваете pH пермеата первого прохода и превращаете C02 в бикарбонат (HCO3-) и карбонат (CO3-2) для лучшего отвода мембранами обратного осмоса во втором проходе. Это невозможно сделать с помощью однопроходного обратного осмоса, потому что введение каустика и образующегося карбоната (CO3-2) в присутствии катионов, таких как кальций, вызовет отложение на мембранах обратного осмоса.
Предварительная обработка обратного осмоса
Надлежащая предварительная обработка с использованием как механической, так и химической обработки имеет решающее значение для системы обратного осмоса, чтобы предотвратить загрязнение, образование накипи и дорогостоящий преждевременный выход из строя мембраны обратного осмоса, а также необходимость частой очистки.Ниже приводится краткое изложение общих проблем, с которыми сталкивается система обратного осмоса из-за отсутствия надлежащей предварительной обработки.
Обрастание
Загрязнение происходит, когда на поверхности мембраны накапливаются загрязнения, которые эффективно закупоривают мембрану. В муниципальной питательной воде содержится много загрязнителей, которые не видны человеческому глазу и безвредны для потребления человеком, но достаточно велики, чтобы быстро загрязнить (или закупорить) систему обратного осмоса. Загрязнение обычно происходит в передней части системы обратного осмоса и приводит к более высокому перепаду давления в системе обратного осмоса и более низкому потоку пермеата.Это приводит к более высоким эксплуатационным расходам и, в конечном итоге, к необходимости очистки или замены мембран обратного осмоса. В конечном итоге засорение в некоторой степени произойдет, учитывая очень мелкие поры в мембране обратного осмоса, независимо от того, насколько эффективен ваш график предварительной обработки и очистки. Однако, имея надлежащую предварительную обработку, вы минимизируете потребность в решении проблем, связанных с обрастанием на регулярной основе.
Загрязнение может быть вызвано следующими причинами:
- Твердые или коллоидные вещества (грязь, ил, глина и т. Д.))
- Органические вещества (гуминовые / фульвокислоты и т. Д.)
- Микроорганизмы (бактерии и др.). Бактерии представляют собой одну из наиболее распространенных проблем загрязнения, так как мембраны обратного осмоса, используемые сегодня, не переносят дезинфицирующих средств, таких как хлор, и поэтому микроорганизмы часто могут процветать и размножаться на поверхности мембраны. Они могут образовывать биопленки, которые покрывают поверхность мембраны и приводят к сильному загрязнению.
- Прорыв фильтрующего материала перед установкой обратного осмоса.В угольных слоях GAC и в слоях умягчителя может образоваться утечка из-под дренажа, и если на месте не будет надлежащей постфильтрации, среда может засорить систему обратного осмоса.
Выполняя аналитические тесты, вы можете определить, имеет ли питающая вода для вашего обратного осмоса высокий потенциал загрязнения. Для предотвращения загрязнения системы обратного осмоса используются методы механической фильтрации. Самыми популярными методами предотвращения загрязнения являются использование мультимедийных фильтров (MMF) или микрофильтрация (MF). В некоторых случаях картриджной фильтрации будет достаточно.
Масштабирование
По мере того, как некоторые растворенные (неорганические) соединения становятся более концентрированными (помните обсуждение коэффициента концентрации), может происходить образование накипи, если эти соединения превышают свои пределы растворимости и осаждаются на поверхности мембраны в виде отложений. Результатами масштабирования являются более высокий перепад давления в системе, более высокий проход соли (меньшее отталкивание соли), низкий поток пермеата и более низкое качество пермеатной воды. Примером обычной накипи, которая имеет тенденцию образовываться на мембране обратного осмоса, является карбонат кальция (CaCO3).
Химическая атака
Современные тонкопленочные композитные мембраны не устойчивы к хлору и хлораминам. Окислители, такие как хлор, «прожигают» дыры в порах мембраны и могут нанести непоправимый ущерб. Результатом химического воздействия на мембрану обратного осмоса является более высокий поток пермеата и более высокий проход соли (пермеат более низкого качества). Вот почему рост микроорганизмов на мембранах обратного осмоса имеет тенденцию так легко загрязнять мембраны обратного осмоса, поскольку нет биоцида, препятствующего их росту.
Механическое повреждение
Частью схемы предварительной обработки должны быть водопровод и контроль системы обратного осмоса до и после. Если произойдет «жесткий запуск», возможно механическое повреждение мембран. Аналогичным образом, если в системе обратного осмоса слишком большое противодавление, то также может произойти механическое повреждение мембран обратного осмоса. Эти проблемы могут быть решены путем использования двигателей с частотно-регулируемым приводом для запуска насосов высокого давления для систем обратного осмоса и путем установки обратного (ых) клапана (ов) и / или предохранительных клапанов для предотвращения чрезмерного обратного давления на установку обратного осмоса, которое может вызвать необратимое повреждение мембраны.
Растворы для предварительной обработки
Ниже приведены некоторые решения для предварительной обработки систем обратного осмоса, которые могут помочь минимизировать загрязнение, образование накипи и химическое воздействие.
Мультимедийная фильтрация (MMF)
Мультимедийный фильтр используется для предотвращения загрязнения системы обратного осмоса. Мультимедийный фильтр обычно содержит три слоя материала, состоящего из антрацитового угля, песка и граната, с поддерживающим слоем гравия на дне.Эти носители лучше всего подходят из-за различий в размере и плотности. Более крупный (но более легкий) антрацитовый уголь будет наверху, а более тяжелый (но меньший) гранат останется внизу. Расположение фильтрующего материала позволяет удалять самые крупные частицы грязи в верхней части слоя материала, при этом более мелкие частицы грязи задерживаются все глубже и глубже в среде. Это позволяет всему слою действовать как фильтр, что позволяет значительно увеличить время работы фильтра между обратной промывкой и более эффективным удалением твердых частиц.
Хорошо управляемый мультимедийный фильтр может удалять частицы размером до 15-20 микрон. Мультимедийный фильтр, в котором используется добавка коагулянта (который заставляет крошечные частицы соединяться вместе с образованием частиц, достаточно крупных для фильтрации), может удалять частицы размером до 5-10 микрон. Для сравнения: ширина человеческого волоса составляет около 50 микрон.
Мультимедийный фильтр рекомендуется, когда значение индекса плотности ила (SDI) больше 3 или когда мутность больше 0.2 NTU. Точного правила нет, но следует соблюдать приведенные выше рекомендации, чтобы предотвратить преждевременное загрязнение мембран обратного осмоса.
Важно установить картриджный фильтр 5 микрон непосредственно после блока MMF на тот случай, если нижний дренаж MMF выйдет из строя. Это предотвратит повреждение насосов, находящихся ниже по потоку, и засорение системы обратного осмоса MMF.
Микрофильтрация (MF)
Микрофильтрация (MF) эффективна при удалении коллоидных и бактериальных веществ и имеет размер пор всего 0.1-10 мкм. Микрофильтрация помогает снизить вероятность загрязнения установки обратного осмоса. Конфигурация мембраны может быть разной у разных производителей, но чаще всего используется тип «полое волокно». Обычно вода перекачивается с внешней стороны волокон, а чистая вода собирается с внутренней стороны волокон. Мембраны для микрофильтрации, используемые в системах питьевой воды, обычно работают в «тупиковом» потоке. В тупиковом потоке вся вода, подаваемая на мембрану, фильтруется через мембрану.Образуется осадок на фильтре, который необходимо периодически отмывать от поверхности мембраны. Степень извлечения обычно превышает 90 процентов для источников питательной воды, которые имеют довольно высокое качество и низкую мутность.
Антискаланты и ингибиторы образования накипи
Антискаланты и ингибиторы образования накипи, как следует из их названия, представляют собой химические вещества, которые можно добавлять в питательную воду перед установкой обратного осмоса, чтобы помочь снизить потенциал образования накипи в питательной воде. Антискаланты и ингибиторы образования накипи увеличивают пределы растворимости проблемных неорганических соединений.Увеличивая пределы растворимости, вы можете концентрировать соли дальше, чем это было бы возможно в противном случае, и, следовательно, достичь более высокой скорости извлечения и работать с более высоким коэффициентом концентрации. Антискаланты и ингибиторы образования накипи препятствуют образованию накипи и росту кристаллов. Выбор антискаланта или ингибитора образования накипи и правильная дозировка зависят от химического состава питательной воды и конструкции системы обратного осмоса.
Умягчение ионным обменом
Смягчитель воды может использоваться для предотвращения образования накипи в системе обратного осмоса путем обмена ионов, образующих накипь, на ионы, не образующие накипи.Как и в случае с блоком MMF, важно установить картриджный фильтр 5 микрон непосредственно после устройства для смягчения воды на тот случай, если нижний дренаж смягчителя выйдет из строя.
Бисульфит натрия (SBS) для инъекций
Добавляя бисульфит натрия (SBS или SMBS), который является восстановителем, в поток воды перед обратным обратным осмосом в соответствующей дозе, вы можете удалить остаточный хлор.
Гранулированный активированный уголь (GAC)
GAC используется как для удаления органических компонентов, так и остаточных дезинфицирующих средств (таких как хлор и хлорамины) из воды.Носители GAC изготавливаются из угля, ореховой скорлупы или дерева. Активированный уголь удаляет остаточный хлор и хлорамины с помощью химической реакции, которая включает перенос электронов с поверхности ГАУ на остаточный хлор или хлорамины. Хлор или хлорамины превращаются в хлорид-ион, который больше не является окислителем.
Недостатком использования GAC перед установкой обратного осмоса является то, что GAC быстро удаляет хлор в самом верху слоя GAC. Это оставит остаток слоя GAC без какого-либо биоцида для уничтожения микроорганизмов.Слой GAC будет поглощать органические вещества по всему слою, которые являются потенциальной пищей для бактерий, поэтому в конечном итоге слой GAC может стать питательной средой для роста бактерий, которые могут легко перейти к мембранам обратного осмоса. Аналогичным образом, слой GAC может производить очень маленькие углеродные частицы при некоторых обстоятельствах, которые потенциально могут загрязнить RO.
Анализ тенденций и нормализация данных RO
Мембраны обратного осмоса являются сердцем системы обратного осмоса, и необходимо собрать определенные данные, чтобы определить состояние мембран обратного осмоса.Эти точки данных включают давление в системе, потоки, качество и температуру. Температура воды прямо пропорциональна давлению. По мере снижения температуры воды она становится более вязкой, и поток пермеата обратного осмоса будет падать, поскольку для проталкивания воды через мембрану требуется большее давление. Аналогичным образом, когда температура воды увеличивается, поток пермеата обратного осмоса увеличивается. В результате данные о рабочих характеристиках системы обратного осмоса должны быть нормализованы, чтобы изменения потока не интерпретировались как ненормальные при отсутствии проблем.Нормализованные потоки, давления и задержка солей должны быть рассчитаны, нанесены на график и сопоставлены с исходными данными (когда RO был введен в эксплуатацию или после того, как мембраны были очищены или заменены), чтобы помочь устранить любые проблемы, а также определить, когда чистить или проверять мембраны на предмет обнаружения повреждать. Нормализация данных помогает отобразить истинную производительность мембран обратного осмоса. Как правило, когда нормализованное изменение составляет +/- 15% от исходных данных, вам необходимо принять меры. Если вы не следуете этому правилу, то очистка мембран обратного осмоса может оказаться не очень эффективной для приведения мембран к почти новым характеристикам.
Очистка мембраны обратного осмоса
Мембраны обратного осмосанеизбежно потребуют периодической очистки от 1 до 4 раз в год в зависимости от качества питательной воды. Как правило, если нормализованное падение давления или нормализованное прохождение соли увеличилось на 15%, то пора очистить мембраны обратного осмоса. Если нормализованный поток пермеата снизился на 15%, то также пора очистить мембраны обратного осмоса. Вы можете очистить мембраны обратного осмоса на месте или попросить их удалить из системы обратного осмоса и очистить за пределами объекта в сервисной компании, которая специализируется на этой услуге.Было доказано, что очистка мембран за пределами площадки более эффективна для обеспечения лучшей очистки, чем очистка салазок на месте.
Очистка мембраныRO включает очистители с низким и высоким pH для удаления загрязнений с мембраны. Накипь устраняется с помощью очистителей с низким pH и органических веществ, коллоидные и биообрастающие вещества обрабатываются очистителем с высоким pH. Очистка мембран обратного осмоса — это не только использование соответствующих химикатов. Есть много других факторов, таких как потоки, температура и качество воды, правильно спроектированные и рассчитанные на уборочные устройства и многие другие факторы, которые должна учитывать опытная сервисная группа, чтобы правильно очистить мембраны обратного осмоса.
Обратный осмос: резюме
Обратный осмос — это эффективная и проверенная технология производства воды, которая подходит для многих промышленных применений, требующих деминерализованной или деионизированной воды. Дальнейшая постобработка после системы обратного осмоса, такая как деионизация смешанного слоя, может повысить качество пермеата обратного осмоса и сделать его пригодным для самых требовательных применений. Правильная предварительная обработка и мониторинг системы обратного осмоса имеют решающее значение для предотвращения дорогостоящего ремонта и внепланового обслуживания.При правильной конструкции системы, программе технического обслуживания и квалифицированной сервисной поддержке ваша система обратного осмоса должна обеспечивать долгие годы воды высокой чистоты.
A Праймер по технологии обратного осмоса — Химическая инженерия
Нехватка воды — одна из самых серьезных глобальных проблем современности. Опреснение и повторное использование воды — эффективные и надежные средства обеспечения новых водных ресурсов. Среди множества доступных методов очистки воды обратный осмос (RO) широко продемонстрировал превосходную надежность и экономическую эффективность при удалении растворенных веществ, таких как соли и следовые примеси.В этой статье рассматривается развитие и состояние технологии обратного осмоса для промышленной очистки воды, очистки сточных вод и производства питьевой воды. В нем также рассматриваются технологические достижения, которые позволили повысить производительность процесса, надежность и снизить стоимость, а также описаны доступные в настоящее время компоненты и методы. Наконец, рассматриваются перспективы будущих достижений в этой области.
Нехватка воды и опреснение
Мировые ресурсы пресной воды находятся под огромным давлением.Более одной трети населения мира проживает в стране, испытывающей нехватку воды, а к 2025 году эта цифра, по прогнозам, вырастет до почти двух третей мирового населения [ 1 ]. Промышленные предприятия потребляют около 60% всего забора пресной воды в развитых странах, таких как США. Вместе промышленность и сельское хозяйство обеспечивают около 90% мирового потребления пресной воды [ 2 ]. Совершенно необходимы эффективные и устойчивые методы очистки воды для промышленного и сельскохозяйственного водоснабжения.
Воду следует сохранять, перерабатывать и повторно использовать, чтобы снизить нагрузку на водоснабжение, но это не удовлетворит возросший спрос, вызванный ростом населения и экономическим ростом. Очистка ресурсов соленой воды и повторное использование сточных вод предлагает новые и надежные источники пресной воды без ущерба для существующих ресурсов пресной воды. Сегодня около 300 миллионов человек в 150 странах уже полагаются на опресненную воду. В 2016 году глобальное производство воды путем опреснения, по прогнозам, превысит 10 триллионов галлонов в год (38 миллиардов кубометров 3 в год), что вдвое превышает уровень производства воды в мире путем опреснения в 2008 году [ 3 ].
Ранние методы опреснения и очистки воды включали дистилляцию, которая использует большое количество энергии для испарения пресной воды из соленой [ 4 ]. Дистилляционные установки для опреснения все еще работают в некоторых регионах мира, где имеется много энергии и она недорога. Однако в подавляющем большинстве недавно построенных или планируемых опреснительных и водоочистных установок используется технология обратного осмоса.
Благодаря технологическим усовершенствованиям за последние 20 лет стоимость производства пресной воды с обратным осмосом была снижена в четыре или более раз, и этот процесс стал надежным компонентом муниципальной и промышленной инфраструктуры (рис. 1).В настоящее время RO является наиболее энергоэффективной и универсальной технологией опреснения и очистки воды и эталоном для сравнения любой новой технологии очистки воды [ 5,6 ].
РИСУНОК 1. Обратный осмос стал наиболее эффективной и универсальной технологией опреснения и очистки воды
RO наиболее широко известен своим использованием для очистки питьевой воды от морской, солоноватой или загрязненной воды, где RO удаляет соли и другие растворенные или взвешенные вещества из питательной воды.Многие удивляются, узнав, что его использование в других приложениях широко распространено и хорошо зарекомендовало себя. Например, RO используется для удаления минералов из котловой воды на электростанциях, для очистки сточных вод и солоноватых грунтовых вод, а также для концентрирования пищевых жидкостей, таких как молоко.
Принципы обратного осмоса
Осмос — это естественное движение воды из зоны с высокой концентрацией воды (с низкой концентрацией соли) через солевой барьер в зону с низкой концентрацией воды (с высокой концентрацией соли).Поток определяется разницей в осмотическом потенциале двух растворов, количественно определяемой как осмотическое давление. Применение внешнего давления для изменения естественного потока воды через барьер — это обратный осмос.
Процесс осмоса через полупроницаемую мембрану впервые наблюдал в 1748 году Жан-Антуан Нолле. RO был известен в 1950-х годах, но практически не демонстрировался до начала 1960-х годов, когда в Калифорнийском университете в Лос-Анджелесе были открыты асимметричные мембраны (www.ucla.edu) Сиднея Лоеба и Шринивасы Сурираджан [ 7 ]. Эти мембраны характеризовались тонким «поверхностным» слоем, поддерживаемым поверх высокопористой и гораздо более толстой подложки. Эта базовая структура остается основой современных мембран обратного осмоса.
Когда солевой раствор подвергается воздействию давления на мембрану обратного осмоса, примеси остаются на стороне мембраны, находящейся под давлением, поскольку рассол и очищенная вода протекает через мембраны в виде пермеата. Обратный осмос требует потока через мембраны, известного как поперечный поток, чтобы не допускать попадания концентрата на поверхности мембраны и обеспечивать непрерывный и почти постоянный поток пермеата.Это отличается от обычных процессов фильтрации, в которых примеси попадают в фильтр или накапливаются в виде корки, которую необходимо периодически промывать или удалять для восстановления производительности.
Минимальное давление, необходимое для отделения чистой воды от нечистой, можно рассматривать как барьер. Высота этого барьера зависит от осмотического давления или осмотического потенциала воды, который, в свою очередь, зависит от ее солености и состава. Более соленая вода имеет более высокий осмотический потенциал и требует большего давления для опреснения.Чтобы пропускать пермеат через мембраны с разумными потоками, осмотический потенциал должен не только соблюдаться, но и преодолеваться. Это избыточное давление частично зависит от проницаемости мембран. Кроме того, концентрация соли в непосредственной близости от поверхности мембраны повышается, что увеличивает осмотический барьер выше, чем в основной части соленой воды — явление, известное как поляризация концентрации. Концентрационная поляризация уменьшается с поперечным потоком.
Другие недостатки в системах обратного осмоса, которые повышают требования к энергии, включают сопротивление потоку через мембраны, механические и объемные потери КПД в насосах и потери на вязкое трение в проточной воде.Кроме того, поверхности мембраны могут быть заблокированы загрязняющими веществами, включая органические и неорганические загрязнения или соли, которые выпадают в осадок из раствора.
Для RO-обработки солоноватых, промышленных и сточных вод (в совокупности именуемых промышленным RO) уровни солености и соответствующие требования к давлению подачи обычно ниже, чем для RO морской воды. Следовательно, потребность в энергии обычно не является основным фактором затрат. Однако стоимость и практичность утилизации рассола, а также необходимость в процессе обработки изменений состава сырья более значительны в промышленных применениях обратного осмоса.Чтобы ограничить производство рассола и достичь высокого выхода очищенной воды, промышленные системы обратного осмоса работают с высокой степенью извлечения, где извлечение определяется как отношение потока пермеата к потоку исходной воды. Однако высокая степень извлечения увеличивает риск загрязнения мембраны, создает проблемы для поддержания поперечного потока, снижает качество пермеата и может снизить гибкость процесса при изменении параметров питательной воды.
Многие из этих проблем были решены с помощью новых технологий, повышающих полезность RO.
Системы обратного осмоса
МембраныRO включены в системы, которые доставляют исходную воду к мембранам, применяют поперечный поток, который уносит концентрат с поверхности мембраны, и обеспечивают путь для транспортировки воды, которая проникает через мембраны. Основными компонентами системы обратного осмоса являются мембранные элементы, насосы и устройства, используемые для управления потоком и давлением. Обычно насос высокого давления обеспечивает как движущую силу для разделения, так и поперечный поток, но в некоторых современных технологических схемах для управления поперечным потоком используется циркуляционный насос, так что роль насоса высокого давления сводится к созданию давления в системе и приведения в движение. поток пермеата.
Конфигурации процесса обратного осмоса
Типичная система промышленного обратного осмоса показана на рисунке 2. Насос высокого давления (ВД) питает систему. Сосуды под давлением, содержащие несколько мембранных элементов, расположены параллельно. Каждый сосуд высокого давления содержит шесть или семь последовательно соединенных мембранных элементов, причем концентрат каждого элемента подается в следующий элемент. На одной стадии обычно достигается 50% извлечения, а более высокие скорости извлечения требуют нескольких стадий. Производительность нескольких ступеней уравновешивается за счет дросселирования потока пермеата от передних ступеней и повышения давления подачи на более поздние ступени с помощью подкачивающего насоса (ВР).Количество сосудов высокого давления, установленных параллельно на каждой последующей ступени, сокращается для поддержания достаточного перетока на более поздних ступенях. Наконец, рассол дросселируется из системы через клапан или устройство, регулирующее давление в системе.
РИСУНОК 2. В типичной системе обратного осмоса насос высокого давления (ВД) нагнетает питательную воду через мембранные элементы, расположенные параллельно.При 50% извлечении на каждую стадию требуется четыре стадии для достижения более 90% общего извлечения. Несколько этапов усложняют конструкцию и эксплуатацию и снижают гибкость процесса.В качестве альтернативы извлечение можно увеличить, непрерывно возвращая часть рассола в подачу через мембрану. Однако увеличение солености корма, рассола и пермеата, вызванное рециркуляцией рассола, обычно подрывает преимущества, которые он дает.
Новые процессы обратного осмоса с замкнутым циклом (полупериодические), в которых рециркуляция рассола используется в периодическом режиме, обеспечивают новые средства для достижения высокой степени извлечения без использования нескольких стадий или снижения качества пермеата [ 8,9 ]. Такой процесс показан на рисунке 3.Насос высокого давления питает замкнутый контур, состоящий из одноступенчатых мембранных элементов и циркуляционного насоса (ЦП). Пермеат производится со скоростью, равной расходу насоса высокого давления. Рассол рециркулирует без сброса давления. Когда достигается желаемый процент извлечения, рассол вымывается из системы и вытесняется питательной водой из насоса высокого давления. Замена рассола и питательной воды выполняется без остановки насоса высокого давления, без образования пермеата и без сброса давления в системе. Затем процесс возвращается в режим замкнутого цикла, во время которого нет потока отбракованного рассола.
РИСУНОК 3. В процессах обратного осмоса с замкнутым контуром используется рециркуляция рассола для достижения высокой степени извлечения без использования нескольких стадий.В процессах обратного осмоса с замкнутым контуром достигнуто извлечение более 97%. Потребность в энергии снижается, поскольку среднее давление подачи мембраны, необходимое для достижения заданной скорости извлечения, ниже. Возможность изменить восстановление на панели управления обеспечивает значительную гибкость. Частая промывка системы путем обмена рассола и питательной воды также помогает подавить засорение и накипь, так что можно поддерживать более высокие скорости извлечения.
При обратном осмотре морской воды обычно требуется более высокое давление, чем при промышленном обратном осмотре. Это делает потребление энергии более важным и ограничивает скорость восстановления. Типичный процесс обратного осмоса морской воды проиллюстрирован на рисунке 4. Как и в промышленной системе обратного осмоса с замкнутым контуром, в процессе обработки морской воды для питания мембранного массива используются как насос высокого давления, так и циркуляционный насос. Кроме того, устройство рекуперации энергии (ERD) используется для удаления рассола и замены его питательной водой при поддержании давления в системе.Эти устройства экономят энергию за счет рекуперации гидравлической энергии из отбракованного рассола и возврата ее в процесс подачи низкого давления, тем самым снижая нагрузку на насос высокого давления.
РИСУНОК 4 . Процессы обратного осмоса морской воды требуют более высокого давления, чем в промышленных процессах обратного осмоса, что делает потребление энергии более важнымДля применений с низким извлечением и повышенным давлением, таких как концентрирование рассола и опреснение морской воды, используется альтернативный процесс с замкнутым циклом для минимизации потребности в энергии [ 10,11 ].В этой технологической конфигурации рассол вытесняется из мембран питательной водой под давлением из боковой камеры. Замена, опорожнение и наполнение боковой камеры осуществляется в гидростатических условиях практически без потери энергии давления.
Мембраны
Процессы обратного осмосапостроены вокруг полупроницаемых мембран, способных отфильтровывать соли. Первые мембраны были изготовлены из ацетата целлюлозы и служили наилучшей доступной технологией до 1980-х годов, когда были разработаны надежные тонкопленочные композитные мембраны (TFC) [ 12 ].Мембраны TFC демонстрируют гораздо более высокую внутреннюю проницаемость для воды, чем мембраны из ацетата целлюлозы, из-за их чрезвычайно тонких селективных слоев. Сегодня почти во всех операциях обратного осмоса используются мембраны TFC [ 13 ]. Несмотря на значительное улучшение характеристик и стоимости мембран TFC, все еще существуют недостатки, препятствующие их применению. Эти ограничения включают склонность к загрязнению и восприимчивость к воздействию окислителей, таких как хлор.
Насосы
Насос высокого давления обеспечивает давление, необходимое для проталкивания воды через мембраны, и в процессе, показанном на Рисунке 1, подает поперечный поток, который контролирует поляризацию концентрации.Типичное давление для промышленной очистки воды составляет от 150 до 450 фунтов на квадратный дюйм (от 10 до 31 бара). Давление обратного осмоса морской воды составляет от 750 до 1200 фунтов на квадратный дюйм (от 52 до 83 бар). Обычно используются насосы центробежного типа с достаточным количеством ступеней и характеристик для удовлетворения требований к давлению. В некоторых приложениях с высоким давлением предпочтительны поршневые насосы из-за их более высокой эффективности.
Межступенчатый подкачивающий насос, показанный на Рисунке 1, увеличивает давление в потоке концентрата, чтобы преодолеть его повышенное осмотическое давление на более поздних стадиях.Как и насос высокого давления, подкачивающий насос управляет как потоком пермеата, так и поперечным потоком. Он рассчитан и работает так, чтобы «уравновесить» поток и поток между ступенями, чтобы все отдельные мембранные элементы работали в пределах своих проектных границ и не использовались ни чрезмерно, ни недостаточно. Типичное давление наддува для промышленной очистки воды составляет от 40 до 200 фунтов на квадратный дюйм (от 3 до 14 бар). В некоторых технологических конфигурациях в качестве межступенчатого подкачивающего насоса используется гидравлический турбонагнетатель, приводимый в действие потоком и давлением рассола с последующих ступеней.
Циркуляционный насос, показанный на рисунках 2 и 3, предназначен для обеспечения перетока. Эти насосы обеспечивают только давление, достаточное для преодоления потерь на трение в проточных каналах и достижения желаемой скорости поперечного потока. Типичное применяемое давление составляет от 10 до 50 фунтов на квадратный дюйм (от 0,7 до 3,4 бара). Циркуляционный насос должен быть оснащен уплотнением вала и подшипниками, рассчитанными на давление поступающего рассола.
Устройства рекуперации энергии
Устройства рекуперации энергии (ERD) устанавливаются в потоке рассола в процессах обратного осмоса морской воды для рекуперации потраченной впустую гидравлической энергии.Первоначально эти устройства представляли собой реверсивные насосы или турбины, механически соединенные с насосом высокого давления. Чистый КПД передачи энергии — произведение КПД турбины и КПД насоса — может достигать 80% для очень больших устройств. В начале 2000-х годов были введены изобарические ERD, позволяющие напрямую передавать давление от потока отбракованных материалов к потоку исходных материалов мембран. Эти устройства обеспечивают чистую эффективность передачи 90% или более и уменьшают размер насоса высокого давления [ 14 ].Турбинные ERD в настоящее время используются в некоторых системах обратного осмоса морской воды из-за их относительно низкой стоимости. ERD обычно не применяются в промышленных установках обратного осмоса, потому что поток рассола не содержит достаточно энергии, чтобы оправдать их стоимость.
Стоимость
Стоимость воды, произведенной на установке обратного осмоса, включает капитальные затраты (CAPEX) и эксплуатационные расходы (OPEX). Капитальные затраты на объем произведенной воды зависят от стоимости строительства и нормы амортизации станции, процентной ставки (желаемый доход от капитальных вложений) и загрузки станции (коэффициент загрузки).OPEX состоит из постоянных затрат на персонал, страхование и т. Д., А также переменных затрат на эксплуатацию, техническое обслуживание и ремонт (включая расходные материалы). Затраты на электроэнергию прямо пропорциональны цене на электроэнергию и включают в себя энергию перекачки, непосредственно потребляемую для обратного осмоса, и энергию, используемую для предварительной обработки, последующей обработки и всех операций завода. Дополнительные затраты могут быть понесены на получение питательной воды и утилизацию солевого концентрата.
Промышленный RO
Исходя из типичных финансовых факторов и факторов использования, капитальные затраты промышленной установки обратного осмоса зависят в первую очередь от состава обрабатываемой воды и стоимости предварительной и последующей очистки.Однако многие промышленные установки обратного осмоса могут быть установлены на существующих объектах или размещены в контейнерах, что снижает или устраняет стоимость строительных работ. Приблизительные затраты на типичную промышленную установку обратного осмоса с производительностью по пермеату 367 галлонов / мин (2 000 м 3 / сутки) при степени извлечения 75%, исходя из предположения, что срок службы установки составляет 10 лет, сведены в Таблицу 1. Около 70% указанных капитальных затрат идет на оборудование, а остальная часть — на установку. Затраты на эксплуатацию и техническое обслуживание оцениваются в 0 долларов.57 за 1000 галлонов. Затраты на утилизацию рассола основаны на средней плате за сточные воды в США в размере 7,60 долларов за 1000 галлонов [17].
| Таблица 1. Приблизительная стоимость промышленной установки обратного осмоса 367 галлонов в минуту (2 000 м 3 / день) (срок службы 10 лет) | ||||||||
| Промышленный RO | 75% восстановление | 90% восстановление | ||||||
| Текущая стоимость, 10 лет | Стоимость, галлон / сут | Стоимость 1000 галлонов | % от общего количества | Текущая стоимость, 10 лет | Стоимость, галлон / сут | % от общего количества | Стоимость 1000 галлонов | |
| Капитальные затраты | $ 521 195 | $ 0.99 | $ 0,28 | 6% | $ 521 195 | $ 0,99 | 12% | $ 0,28 |
| Энергетика | $ 480 727 | $ 0,91 | $ 0,26 | 6% | $ 600 909 | $ 1,14 | 14% | $ 0,32 |
| O&M | $ 1 148 252 | 2,17 $ | $ 0,62 | 13% | $ 1 148 252 | 2,17 долл. США | 26% | $ 0.62 |
| рассол | $ 6 436 578 | $ 12,18 | $ 3,48 | 75% | 2 145 526 долл. США | $ 4,06 | 49% | $ 1,16 |
| Всего | $ 8 586 752 | $ 16,25 | $ 4,64 | 100% | $ 4 415 882 | $ 8,36 | 100% | $ 2,39 |
Значения в таблице 1 ясно показывают, что утилизация рассола является самой большой статьей расходов для промышленного RO.В этом примере увеличение извлечения с 75% до 90% лишь незначительно увеличивает потребление энергии, но снижает затраты на утилизацию рассола в три раза и снижает общую стоимость владения почти вдвое.
Морская вода RO
Установки обратного осмоса с морской водой обычно больше промышленных установок обратного осмоса, и предполагаемый срок их службы составляет до 25 лет. Типичная потребность в капитальных затратах для установки обратного осмоса морской воды среднего масштаба в 2008 г. составляла примерно 6 долларов за галлон в день (1 585 долларов за м 3 / день) установленного пермеата.Таким образом, строительство завода производительностью 10 миллионов галлонов в день (38000 м 3 в день) стоит около 60 миллионов долларов. OPEX составляет примерно 0,57 доллара на 1000 галлонов (около 2,8 миллиона долларов в год для завода с производительностью 10 миллионов галлонов в день [ 15 ]. При типичной потребности в энергии 3,2 кВтч / м 3 , включая предварительную и последующую обработку и При тарифе на электроэнергию или цене на электроэнергию в размере 0,10 долл. США / кВтч стоимость энергии для станции мощностью 10 млн галлонов в сутки составляет 4,4 млн долл. США в год. Итоговые затраты на приведенную стоимость за 25 лет эксплуатации представлены в таблице 2.
| Таблица 2. Приведенные затраты на установку обратного осмоса с морской водой 38 000 м 3 / день (10 миллионов галлонов в день) за 25 лет | ||||||||
| Морская вода RO | Типичное потребление энергии | 5% Снижение энергопотребления | ||||||
| Текущая стоимость, 25 лет | Стоимость, галлон / сут | Стоимость 1000 галлонов | % от общего количества | Текущая стоимость, 25 лет | Стоимость, галлон / сут | Стоимость 1000 галлонов | % от общего количества | |
| Капитальные затраты | $ 60 004 542 | $ 6.00 | $ 0,66 | 14% | $ 60 004 542 | 6,00 $ | $ 0,66 | 15% |
| Энергетика | $ 216 953 081 | $ 21,69 | $ 2,38 | 52% | $ 209 569 720 | $ 20.96 | $ 2,30 | 51% |
| O&M | $ 138 571 724 | $ 13,86 | $ 1,52 | 33% | $ 138 571 724 | $ 13,86 | $ 1.52 | 34% |
| Всего | $ 415 529 347 | $ 41,55 | $ 4,55 | 100% | $ 408 145 986 | $ 40,81 | $ 4,47 | 100% |
Данные в таблице 1 показывают, что энергия составляет более половины общих затрат на 25-летнюю операцию обратного осмоса с морской водой и более чем в три раза превышает капитальные затраты на строительство завода. Энергосберегающие методы и технологии легко оправдываются с точки зрения затрат.Например, сокращение потребления энергии обратным осмотром морской воды на 5% на рассмотренной выше установке площадью 38 000 м 3 3 / сут (10 млн галлонов в сутки) позволит сэкономить более 7 млн долл. США в текущей стоимости. Эта стоимость эквивалентна 12% стоимости владения заводом. Если для экономии энергии 5% потребуется увеличение общей стоимости установки на 1%, инвестиции окупятся примерно через три года.
Для контекста следует отметить, что большинство методов доставки большого количества воды являются дорогостоящими.Традиционное распределение и очистка воды требует строительства заводов и инфраструктуры. В развитом мире цена производства 1000 галлонов воды из традиционных источников воды колеблется от 6 до 15 долларов (1,52–3,88 доллара за м 3 ) [ 17 ]. Сравнение этих цифр с перечисленными выше затратами показывает, что обратное водоснабжение может быть экономически выгодным средством водоснабжения.
Возможный технологический прогресс
Технология обратного опреснения продолжает совершенствоваться. Вот некоторые возможные будущие достижения в отношении ключевых компонентов операций RO и их потенциальная ценность.
Мембраны. Мембраны со сверхвысокой проницаемостью, включая графеновые мембраны или мембраны TFC, изготовленные из углеродных нанотрубок или аквапоринов, в последнее время привлекли большое внимание из-за их способности снижать давление, необходимое для обеспечения проницаемости, тем самым снижая потребность в энергии RO [ 18 ]. Однако высокая проницаемость обычно снижает отторжение соли. Если предположить, что удаление солей может быть улучшено, количество энергии, которое можно сэкономить за счет использования мембран со сверхвысокой проницаемостью, вероятно, будет очень небольшим.Существующие установки обратного осмоса уже работают на пределе термодинамики, при этом прикладываемое давление всего на 10-20% выше осмотического давления концентрата. Некоторая часть этого избыточного давления необходима, чтобы направить поперечный поток мимо любого используемого материала мембраны. Хотя эти мембраны могут позволить использовать меньшую площадь мембраны и, следовательно, сэкономить на капитальных затратах, это потребует изменения конструкции мембранных элементов, поскольку концентрационная поляризация, вызванная высокими потоками воды, уже препятствует работе современных тонкопленочных композитных мембранных элементов.Кроме того, загрязнение мембран усугубляется при более высоких потоках воды, что еще больше снижает ценность мембран со сверхвысокой проницаемостью для обратного осмоса.
Уменьшение или отказ от предварительной обработки может снизить стоимость обратного осмоса, но это потребует разработки устойчивых к загрязнению мембран или мембранных покрытий. Достижения в мембранной технологии могут также снизить потребность в дополнительной обработке, которая в настоящее время требуется для снижения концентраций бора и хлоридов в пермеате до уровней, подходящих для использования в сельском хозяйстве.Однако мембраны с лучшим селективным отводом ионов обычно менее проницаемы для воды, что увеличивает требования к давлению подачи и потребление энергии.
Насосы и ERD. Несмотря на то, что не было значительных улучшений в эффективности насосов или электродвигателей специально для применений обратного осмоса, проектировщики насосов и установок могут снизить потребление энергии с помощью интеллектуальных технологических схем. К ним относятся использование более крупных центробежных насосов с изначально более высоким КПД и частотно-регулируемых приводов (ЧРП) вместо дроссельных клапанов для регулирования расхода и давления.Хотя частотно-регулируемые приводы для очень больших двигателей могут быть дорогостоящими, в насос высокого давления можно подавать питание с помощью подкачивающего насоса, оснащенного частотно-регулируемым приводом. Правильно управляемый подкачивающий насос может позволить обоим насосам работать с максимальной эффективностью, несмотря на меняющиеся условия технологического процесса и питательной воды. Кроме того, использование подкачивающего насоса позволяет использовать насос высокого давления с более высокой чистой положительной высотой всасывания, что может повысить эффективность насоса.
Несмотря на явно продвинутый уровень изобарических ERD, инновации продолжают расширять область применения этих устройств, улучшать их производительность и надежность и, в конечном итоге, снижать капитальные и эксплуатационные расходы на RO морской воды.Эффективность ERD может быть увеличена за счет установки дополнительных блоков ERD, тем самым уменьшая расход на каждый блок и уменьшая потери дифференциального давления, за счет затяжки уплотнений клапана и снижения скорости выхода рассола [19].
Расширенные технологические разработки. Использование нескольких ступеней может снизить требования к давлению подачи почти до теоретических требований к минимальному давлению [20] и потенциально обеспечить более сбалансированную работу мембраны. Однако давление концентрата на последней ступени намного выше, чем давление подачи на первой ступени, что делает невозможным использование изобарных устройств рекуперации энергии в многоступенчатых конфигурациях, что подрывает некоторый потенциал энергосбережения этих конструкций для морской воды. РО.Кроме того, требуемые дополнительные насосы увеличивают капитальные затраты.
Операции обратного осмоса с замкнутым контуром обеспечивают преимущества энергосбережения за счет многоступенчатости без необходимости использования устройств рекуперации энергии или дополнительных насосов. Они облегчают работу с высокой степенью извлечения, снижая производство рассола, утилизация которого является самым большим компонентом затрат в большинстве промышленных применений обратного осмоса.
Прямой осмос. В прямом осмосе используется водопроницаемая и отталкивающая соль мембрана между двумя растворами с разным осмотическим давлением.Этими решениями могут быть природные ресурсы, потоки отходов или растворы высокой чистоты. Естественный осмос заставляет воду проникать через мембрану из менее соленого «исходного раствора» в более соленый «вытяжной раствор». В технических решениях для вытяжки используются специально подобранные растворенные вещества для вытяжки, которые отделяются от извлеченной воды и рециркулируются для облегчения непрерывной операции прямого осмоса. Однако регенерация вытяжного раствора является дорогостоящим этапом [21]. Недавно предложенная конструкция представляет собой гибридную систему, в которой используется прямой осмотический контактор для разбавления морской воды сточными водами перед обработкой обратным осмосом [22].Однако для этой системы требуется двухмембранная работа, что увеличивает затраты, а для производства питьевой воды необходимо преодолеть негативное общественное мнение об использовании сточных вод в качестве источника питьевой воды.
Заключительные замечания
Обратный осмос — надежное, экономичное и хорошо зарекомендовавшее себя средство очистки воды для бытового и промышленного использования. Компоненты обратного осмоса и технологические разработки улучшились в последние годы, что снизило затраты на очистку воды. Для большинства промышленных применений обратного осмоса повышение извлечения, тем самым уменьшая образование рассола, представляет собой величайшую возможность экономии.Для обратного осмоса морской воды сокращение потребления энергии имеет наибольшие перспективы для снижения общих затрат. Ожидаемые будущие технологические достижения могут обеспечить увеличение извлечения и дополнительную экономию энергии, особенно при проектировании процессов обратного осмоса с замкнутым циклом.
Под редакцией Скотта Дженкинса
Список литературы
1. Сервис, Р.Ф., Science , vol. 313, стр. 1088, 2006.
2. ЮНЕСКО, Вода для людей, Вода для жизни, Доклад ООН о мировом развитии водных ресурсов, Организация Объединенных Наций по вопросам образования, науки и культуры, 2003 г.
3. Schiermeier, Q., Nature, vol. 452, стр. 260 2008.
4. Национальный исследовательский совет (США), Комитет по развитию технологий опреснения, «Опреснение: национальная перспектива», National Academies Press, 2008.
5. Фрицманн, К., Ловенберг, Дж., Винтгенс, Т. и Мелин, Т., Desalination , vol. 216, стр. 1, 2007.
6. Semiat, R., Environ. Sci. Технол ., т. 42, стр. 8,193, 2008 г.
7. Лоеб, С. и Сурираджан, С., «Деминерализация морской воды с помощью осмотической мембраны», Серия «Успехи в химии», том. 38, стр. 117, 1962.
8. Efraty, A., Патент США № 7,695,614, 2010b.
9. Эфрати, А., Серия опреснения замкнутого цикла №4: опреснение солоноватой воды с высокой степенью извлечения, низкое потребление энергии новым одноступенчатым методом без потери энергии рассола, опреснение и водоподготовка, т.42, стр. 262–268, 2012.
10. Efraty, A., Патент США № 7,628,921, 2010a.
11. Эфрати, А., Барак, Р., Гал, З., Опреснение в замкнутом цикле — новая технология с низким энергопотреблением и высокой степенью извлечения без рекуперации энергии, опреснения и очистки воды, т. 31. С. 95–101, 2011.
.
12. Ларсон Р.Э., Кадотт Дж. Э. и Петерсон Р.Дж., Desalination , vol. 38, стр. 473, 1981.
13. Ли, К.П., Арнот Т.К., Маттиа Д., J. Membr. Sci. , т. 370, стр. 1, 2011.
14. Стовер Р.Л., Desalination vol. 203, стр. 168, 2007.
15. Соммарива, К., «Экономика и финансирование опреснения и очистки воды», Balaban Desalination Publications, 2010.
16. Отчет об опреснении воды, Media Analytics, 15 сентября, [Отрывок], 2008 г.
17. Global Water Intelligence, vol.14 (2), сентябрь 2013 г.
18. Элимелех М. и Филип У.А., Science , vol. 333, стр. 712, 2011.
19. Стовер Р.Л. и Эндрюс В., IDA Journal vol. 4 (1), с. 38, 2012.
20. Чжу А.З., Христофидес П.Д. and Cohen, Y., Ind. Eng. Chem. Res ., Vol. 48, стр. 6010, 2009.
21. McGinnis, R.L., Elimelech, M., Desalination , vol. 207, стр.370, 2007.
22. Cath, T.Y., Hancock, N.T., Lundin, C.D. Hoppe-Jones, C. и Drewes, J.E., J. Membr. Sci ., Т. 362, стр. 417, 2010.
Автор
Ричард Стовер — исполнительный вице-президент Desalitech, Inc. (One Gateway Center, Suite 250, Newton, MA 02458; телефон: 1-510-333-2767; электронная почта: [email protected]). Стовер имеет более чем 27-летний профессиональный опыт в области водных технологий. Он занимал должность главного технического директора и вице-президента Energy Recovery, Inc., ведущий поставщик устройств рекуперации энергии для опреснения морской воды. Он руководил техническими и коммерческими усилиями, которые вывели компанию из стартапа через IPO. Затем Стовер занимал должность вице-президента компании Oasys Water, разрабатывая метод прямого осмоса для концентрирования рассола. Текущая работа Stover с Desalitech увеличивает эффективность очистки промышленных, солоноватых вод и сточных вод с помощью продуктов обратного осмоса с высокой степенью извлечения. Компания Stover получила множество патентов на опреснение. Он был одним из лауреатов премии Сидни Лёба Европейского общества опреснения воды за выдающиеся инновации.Имеет докторскую степень. из Калифорнийского университета в Беркли и степень бакалавра наук из Техасского университета в Остине, оба в области химического машиностроения.
RO (Обратный осмос) Антискаланты | AWC
Нанофильтрация и обратный осмос: мембранный антискалант обратного осмоса В системах обратного осмоса используется поперечная мембранная фильтрация, при которой неочищенная вода выходит из системы в виде концентрированного рассола. Когда вода переходит на сторону пермеата, неочищенная фракция воды остается со всеми солями, органическими веществами и коллоидными частицами, которые задерживаются мембраной.Чем выше эксплуатационный выход, тем более концентрированным будет рассол. Когда растворенные соли в рассоле превышают насыщение, они начинают выпадать в осадок в виде чешуек. Точно так же органические и коллоидные частицы имеют более высокий потенциал загрязнения, поскольку они становятся более концентрированными по длине мембранной системы.AWC разработала высокоэффективные ингибиторы, которые устраняют наиболее сложные накипи и значительно снижают коллоидное и органическое загрязнение в мембранных системах обратного осмоса (RO) и нанофильтрации (NF).Все антискаланты AWC одобрены NSF для использования в питьевых мембранных системах. Наши антискаланты очень эффективны для всех источников питательной воды, включая грунтовые воды, сточные воды, пресные поверхностные воды, морскую воду и городскую воду.
Наши высокоэффективные антискаланты обратного осмоса (RO) эффективны при исключительно низких дозировках и могут препятствовать образованию накипи даже при очень высокой степени насыщения. Использование антискалантов AWC может устранить необходимость в дозировании кислоты, позволить предприятиям работать с более высоким извлечением и снизить частоту очистки.
AWC RO антискаланты контролируют отложения, такие как карбонат кальция, фосфат кальция, сульфат кальция, сульфат бария, сульфат стронция, фторид кальция, гидроксид железа, фосфат железа, диоксид кремния и коллоидные загрязнения. Наши противообрастающие средства обратного осмоса диспергируют коллоидный диоксид кремния и природные органические вещества.
В системах обратного осмосаиспользуется поперечная мембранная фильтрация, при которой неочищенная вода выходит из системы в виде концентрированного рассола.Когда вода переходит на сторону пермеата, неочищенная фракция воды остается со всеми солями, органическими веществами и коллоидными частицами, которые задерживаются мембраной. Чем выше эксплуатационный выход, тем более концентрированным будет рассол. Когда растворенные соли в рассоле превышают насыщение, они начинают выпадать в осадок в виде чешуек. Точно так же органические и коллоидные частицы имеют более высокий потенциал загрязнения, поскольку они становятся более концентрированными по длине мембранной системы.
Что такое антискаланты обратного осмоса?
Антискаланты обратного осмоса — это специальные химические вещества, которые добавляются перед системой обратного осмоса мембран.Эти химические ингибиторы образования накипи предназначены для предотвращения или замедления образования минеральных отложений на поверхности мембраны. По этой причине правильный антискалант имеет решающее значение для стабильной работы системы обратного осмоса.
химикаты обратного осмоса и антискалант
Минеральные отложения образуются, когда растворенным минералам в воде дают возможность сконцентрироваться до предела насыщения, где они начнут выходить из раствора. Подобно водяным пятнам на окне, вода, распыляемая на окно, кажется прозрачной, но в каждой капле есть растворенные минералы.Когда эта вода испаряется, растворенные минералы остаются и проявляют себя как пятно с жесткой водой.
В мембранной системе обратного осмоса вода проталкивается через мембрану, но растворенные минералы не могут пройти, поэтому они остаются. Представьте, если бы каждое из этих «пятен» осталось и к ним присоединились бы другие пятна, чтобы сформировать большую область минеральной чешуи. Накипь на поверхности мембраны будет препятствовать проникновению воды, поэтому важно предотвратить образование накипи, чтобы системы обратного осмоса работали непрерывно.
Использование неподходящего химического средства против накипи может привести к быстрому образованию накипи и последующей потере производительности. Однако, вводя правильный антискалант обратного осмоса с правильной мощностью дозы, можно полностью устранить проблемы образования накипи. Современные компьютерные модели прогнозирования масштаба, такие как Proton®, могут определять серьезность потенциала масштабирования и рекомендовать оптимальный антискалант и дозировку.
RO Антискаланты обычно требуют очень низких дозировок и могут работать вместе с другими химическими веществами, подаваемыми выше по потоку.Антискаланты обратного осмоса также в целом безопасны в обращении и соответствуют всем экологическим требованиям, предъявляемым к химикатам обратного осмоса, подаваемым на водоочистные сооружения.
AWC предоставляет мембранному сообществу химические решения для оптимизации работы системы обратного осмоса. Не забудьте связаться с нами сегодня по телефону (813) — 246-5448, чтобы узнать больше.
Произошла ошибка при настройке вашего пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки вашего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.