Типы кристаллических решёток — урок. Химия, 8–9 класс.
Большинство твёрдых веществ имеет кристаллическое строение, которое характеризуется строго определённым расположением частиц.
Если соединить частицы условными линиями, то получится пространственный каркас, называемый кристаллической решёткой.
Точки, в которых размещены частицы кристалла, называют узлами решётки. В узлах воображаемой решётки могут находиться атомы, ионы или молекулы.
В зависимости от природы частиц, расположенных в узлах, и характера связи между ними различают четыре типа кристаллических решёток: ионную, металлическую, атомную и молекулярную.
Ионными называют решётки, в узлах которых находятся ионы.
Их образуют вещества с ионной связью. В узлах такой решётки располагаются положительные и отрицательные ионы, связанные между собой электростатическим взаимодействием.
Ионные кристаллические решётки имеют соли, щёлочи, оксиды активных металлов.
Ионы могут быть простые или сложные. Например, в узлах кристаллической решётки хлорида натрия находятся простые ионы натрия Na+ и хлора Cl−, а в узлах решётки сульфата калия чередуются простые ионы калия K+ и сложные сульфат-ионы SO42−.
Связи между ионами в таких кристаллах прочные. Поэтому ионные вещества твёрдые, тугоплавкие, нелетучие. Такие вещества хорошо растворяются в воде.
Рис. \(1\). Кристаллическая решётка хлорида натрия
Рис. \(2\). Кристаллы хлорида натрия
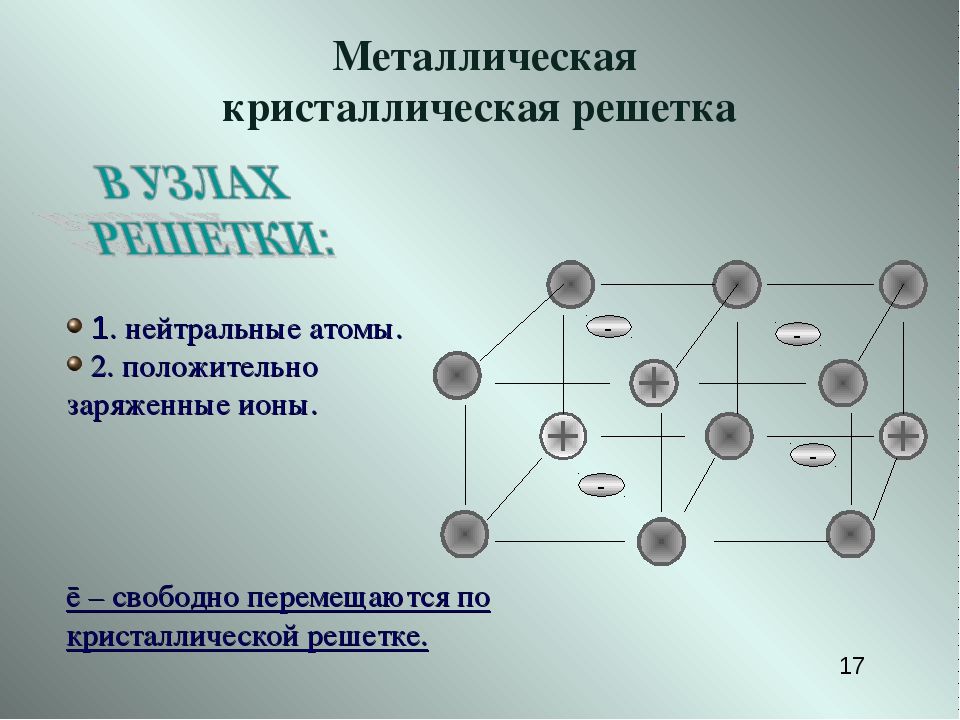
Металлическими называют решётки, которые состоят из положительных ионов и атомов металла и свободных электронов.
Их образуют вещества с металлической связью. В узлах металлической решётки находятся атомы и ионы (то атомы, то ионы, в которые легко превращаются атомы, отдавая свои внешние электроны в общее пользование).
Такие кристаллические решётки характерны для простых веществ металлов и сплавов.
Температуры плавления металлов могут быть разными (от \(–37\) °С у ртути до двух-трёх тысяч градусов). Но все металлы имеют характерный металлический блеск, ковкость, пластичность, хорошо проводят электрический ток и тепло.
Рис. \(3\). Металлическая кристаллическая решётка
Рис. \(4\). Изделие из металла
Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы, соединённые ковалентными связями.
Такой тип решётки имеет алмаз — одно из аллотропных видоизменений углерода. К веществам с атомной кристаллической решёткой относятся графит, кремний, бор и германий, а также сложные вещества, например, карборунд SiC и кремнезём, кварц, горный хрусталь, песок, в состав которых входит оксид кремния(\(IV\)) SiO2.
Таким веществам характерны высокая прочность и твёрдость. Так, алмаз является самым твёрдым природным веществом.
У веществ с атомной кристаллической решёткой очень высокие температуры плавления и кипения.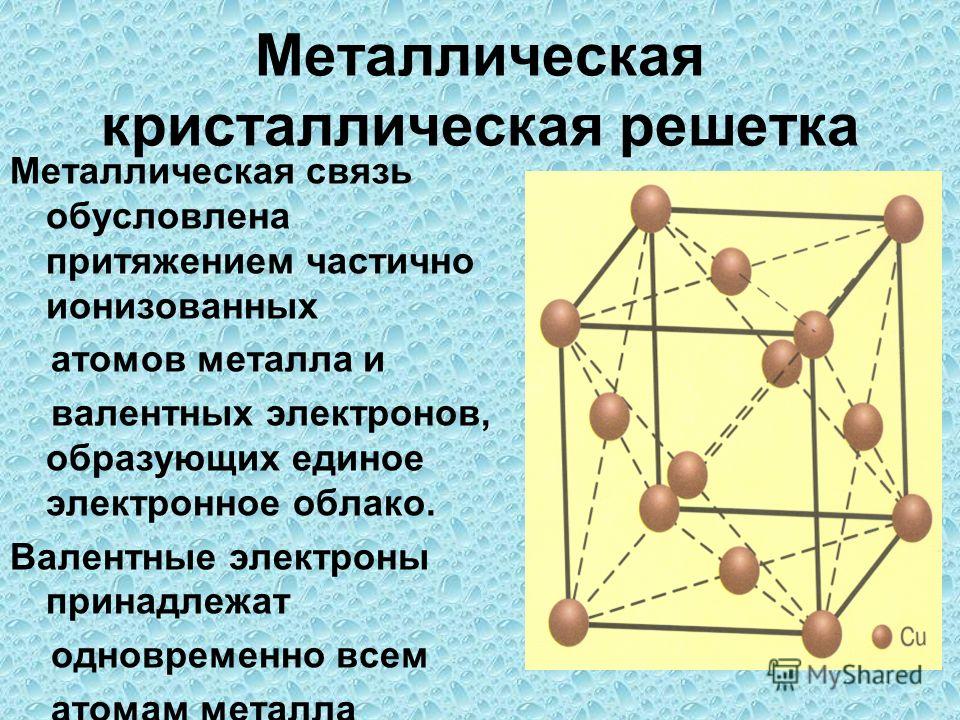 Например, температура плавления кремнезёма — \(1728\) °С, а у графита она выше — \(4000\) °С.
Например, температура плавления кремнезёма — \(1728\) °С, а у графита она выше — \(4000\) °С.
Атомные кристаллы практически нерастворимы.
Рис. \(5\). Кристаллическая решётка алмаза
Рис. \(6\). Алмаз
Молекулярными называют решётки, в узлах которых находятся молекулы, связанные слабым межмолекулярным взаимодействием.
Несмотря на то, что внутри молекул атомы соединены очень прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного притяжения. Поэтому молекулярные кристаллы имеют небольшую прочность и твёрдость, низкие температуры плавления и кипения.
Многие молекулярные вещества при комнатной температуре представляют собой жидкости и газы.
Такие вещества летучи. Например, кристаллические иод и твёрдый оксид углерода(\(IV\)) («сухой лёд») испаряются, не переходя в жидкое состояние.
Некоторые молекулярные вещества имеют запах.
Такой тип решётки имеют простые вещества в твёрдом агрегатном состоянии: благородные газы с одноатомными молекулами (He,Ne,Ar,Kr,Xe,Rn), а также неметаллы с двух- и многоатомными молекулами (h3,O2,N2,Cl2,I2,O3,P4,S8).
Молекулярную кристаллическую решётку имеют также вещества с ковалентными полярными связями: вода — лёд, иод, твёрдые аммиак, кислоты, оксиды большинства неметаллов. Большинство органических соединений тоже представляют собой молекулярные кристаллы (нафталин, сахар, глюкоза).
Рис. \(7\). Кристаллическая решётка иода
Рис. \(8\). Иод
Если известно строение вещества, то можно предсказать его свойства.
Попробуем определить, каковы примерно температуры плавления у фторида натрия, фтороводорода и фтора.
У фторида натрия — ионная кристаллическая решётка. Значит, его температура плавления будет высокой. Фтороводород и фтор имеют молекулярные кристаллические решётки. Поэтому их температуры плавления будут невысокими. Молекулы фтороводорода полярные, а фтора — неполярные. Значит, межмолекулярное взаимодействие у фтороводорода будет сильнее, и его температура плавления будет выше по сравнению со фтором.
Фтороводород и фтор имеют молекулярные кристаллические решётки. Поэтому их температуры плавления будут невысокими. Молекулы фтороводорода полярные, а фтора — неполярные. Значит, межмолекулярное взаимодействие у фтороводорода будет сильнее, и его температура плавления будет выше по сравнению со фтором.
Экспериментальные данные подтверждают эти предположения: температуры плавления NaF, HF и F2 составляют соответственно \(995\) °С, \(–83\) °С, \(–220\) °С.
Источники:
Рис. 1.Кристаллическая решётка хлорида натрия https://upload.wikimedia.org/wikipedia/commons/e/e9/Sodium-chloride-3D-ionic.png
Рис. 2. Кристаллы хлорида натрия https://cdn.pixabay.com/photo/2015/09/24/17/08/crystal-955935_960_720.jpg
Рис. 3. Металлическая кристаллическая решётка © ЯКласс
Рис. 4. Изделие из металла https://cdn.pixabay.com/photo/2013/07/12/17/22/database-152091_960_720.png
Рис. 5. Кристаллическая решётка алмаза https://image.shutterstock.com/image-vector/illustration-chemical-carbon-has-several-600w-1717122967. jpg
jpg
Рис. 6. Алмаз https://cdn.pixabay.com/photo/2014/10/24/08/09/diamond-500872_960_720.jpg
Рис. 7. Кристаллическая решётка иода © ЯКласс
Рис. 8. Иод https://upload.wikimedia.org/wikipedia/commons/7/7c/Iod_kristall.jpg
Строение вещества
Тренировочные тесты ЕГЭ по химии
Вещества молекулярного и немолекулярного строения. Типы кристаллических решёток. Зависимость свойств веществ от их состава и строения.
1. Молекулярное строение имеет
1) С12 2) СаО 3) ZnCl2 4) NaBr
2. Кристаллическая решетка хлорида кальция
1) металлическая
2) молекулярная
3) ионная
4) атомная
3. Кристаллическая решетка твердого оксида углерода (IV)
1) ионная
2) молекулярная
3) металлическая
4) атомная
4. Молекулярную кристаллическую решетку имеет
1) CaF2 2) СО2 3) SiO2 4) A1F3
5.
1) Н2О 2) H2SO4 3) SiО2 4) СО2
6. Молекулярное строение имеет
1) алмаз
2) азот
3) кремний
4) поваренная соль
7. Немолекулярное строение имеет
1) азот 2) графит 3) аммиак 4) кислород
8. Наибольшую температуру плавления имеет
1) водород
2) кислород
3) оксид углерода (IV)
4) оксид кремния (IV)
9. Ионное строение имеет
1) оксид бора
2) оксид углерода (IV)
3) оксид серы (VI)
4) оксид магния
10. Вещества с металлической кристаллической решеткой
1) хрупкие, легкоплавкие
2) проводят электрический ток, пластичные
3) обладают низкой тепло- и электропроводностью
4) обладают хорошими оптическими свойствами
11. Немолекулярное строение имеет каждое из двух веществ:
Немолекулярное строение имеет каждое из двух веществ:
1) СО2иСl2 2) Fe и NaCl 3) СО и Mg 4) Na2CO3 и I2 (тв)
12. Вещества твердые, прочные, с высокой температурой плавления, расплавы которых проводят электрический ток, имеют кристаллическую решетку
1) металлическую
2) молекулярную
3) атомную
4) ионную
13. Молекулярную кристаллическую решетку имеет
1) кремний
2) оксид углерода (IV)
3) оксид кремния
4) нитрат аммония
14. Молекулярная кристаллическая решетка характерна для каждого из веществ, расположенных в ряду:
1) хлорид калия, азот, метан
2) иод, диоксид углерода, гелий
3) алюминий, бром, алмаз
4) водород, сульфат магния, оксид железа (Ш)
15. Ионную кристаллическую решетку имеет каждое из веществ, расположенных в ряду:
1) натрий, хлорид натрия, гидрид натрия
2) кальций, оксид кальция, карбонат кальция
3) бромид натрия, сульфат калия, хлорид железа (II)
4) фосфат магния, хлорид калия, оксид фосфора (V)
16. Молекулярное строение имеет
Молекулярное строение имеет
1) СO2 2) КВг 3) MgSО4 4) SiO2
17. Ионы являются структурными частицами
1) кислорода
2) воды
3) оксида углерода (IV)
4) хлорида натрия
18. Металлическую кристаллическую решетку имеет
1) малахит
2) бронза
3) кремнезем
4) графит
19. Кристаллическая решетка брома
1) молекулярная
2) металлическая
3) ионная
4) атомная
20. Верны ли следующие суждения о зависимости свойств веществ от особенностей их кристаллической решетки?
А. Расплавы веществ с ионной кристаллической решеткой проводят электрический ток.
Б. Алмаз и кварц имеют атомную кристаллическую решетку.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
21. Немолекулярное строение имеет
Немолекулярное строение имеет
1) | H2O | 2) | NH3 | 3) | SiO2 | 4) | CO2 |
22. Ионы являются структурной единицей для каждого из двух веществ:
1) СН4 и I2 2) SO, и Н2О 3) Сl2 и NH3 4) LiF и KCl
23. Молекулярное строение имеет каждое из двух веществ:
1) NН4С1 и CH3NH3
2) Na2CO3 и HNO3
3) C2H5OH и СН4
4} H2S и CH3COONa
24. Молекулярную кристаллическую решетку имеет
Молекулярную кристаллическую решетку имеет
1) фторид кальция
2) бромид алюминия
3) сероводород
4) хлорид меди (П)
25. Молекулярное строение имеет
1) С2Н5ОН 2) А1 3) Fe2(SO4)3 4) КСЮ3
26. Вещества только немолекулярного строения приведены в ряду
1) S8, O2(г), лед
2) Fe, NaCl (тв), алмаз
3) СО2 (г), N2 (г), А1
4) графит, Na2CO3 (тв), I2
27. Утверждение о том, что структурной частицей данного вещества является молекула, справедливо только для
1) | алмаза |
2) | поваренной соли |
3) | кремния |
4) | азота |
28. Кристаллическая решетка хлорида кальция
Кристаллическая решетка хлорида кальция
1) | ионная |
2) | молекулярная |
3) | металлическая |
4) | атомная |
29. Кристаллическая решетка льда
1) | ионная |
2) | молекулярная |
3) | металлическая |
4) | атомная |
30. Молекулярную кристаллическую решетку имеет
Молекулярную кристаллическую решетку имеет
1) | CaF2 | 2) | SO2 | 3) | SiO2 | 4) | AlF3 |
31. Простые вещества, имеющие одинаковый тип кристаллической решетки, образованы элементами
1) | малых периодов |
2) | побочных подгрупп |
3) | главных подгрупп |
4) | больших периодов |
Ответы: 1-1, 2-3, 3-2, 4-2, 5-3, 6-2, 7-2, 8-4, 9-4, 10-2, 11-2, 12-4, 13-2, 14-2, 15-3, 16-1, 17-4, 18-2, 19-1, 20-3, 21-3, 22-4, 23-3, 24-3, 25-1, 26-2, 27-4, 28-1, 29-2, 30-2, 31-3
Вещества молекулярного и немолекулярного строения.
 Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения — Химическая связь и строение вещества
Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения — Химическая связь и строение веществаТесты с кратким ответом с решениями
1. Атом является структурной единицей в кристаллической решетке
1) фосфорной кислоты
2) белого фосфора
3) кремнезема
4) хлорида аммония
2. Вещества с атомной кристаллической решеткой
1) очень твердые и тугоплавкие
2) хрупкие и легкоплавкие
3) проводят электрический ток в растворах
4) проводят электрический ток в расплавах
3. Молекулярную кристаллическую решетку имеют
1) Н2O и СuO
2) СO2и K2S
3) NaCl и H2SO4
4) НСl и O3
4. Вещество, имеющее низкую температуру плавления, возгоняющееся при нагревании, неэлектропроводное, имеет кристаллическую решетку
1) ионную
2) молекулярную
3) металлическую
4) атомную
5.
1) фторид кальция
2) медь
3) алмаз
4) оксид кремния(IV)
6. Твердое, хрупкое вещество, расплав которого проводит электрический ток, имеет кристаллическую решетку
1) атомную
2) металлическую
3) молекулярную
4) ионную
7. Вещество, имеющее высокую электропроводность, ковкое, пластичное, имеет кристаллическую решетку
1) ионную
2) металлическую
3) молекулярную
4) атомную
8. В кристалле вольфрама частицы связаны металлической связью, поэтому вольфрам
1) тугоплавок
2) химически стоек
3) электропроводен
4) имеет высокую плотность
9. Какие из приведенных утверждений верны? А. Вещества с молекулярной решеткой имеют низкие температуры плавления и низкую электропроводность. Б. Вещества с атомной решеткой пластичны и обладают высокой электрической проводимостью.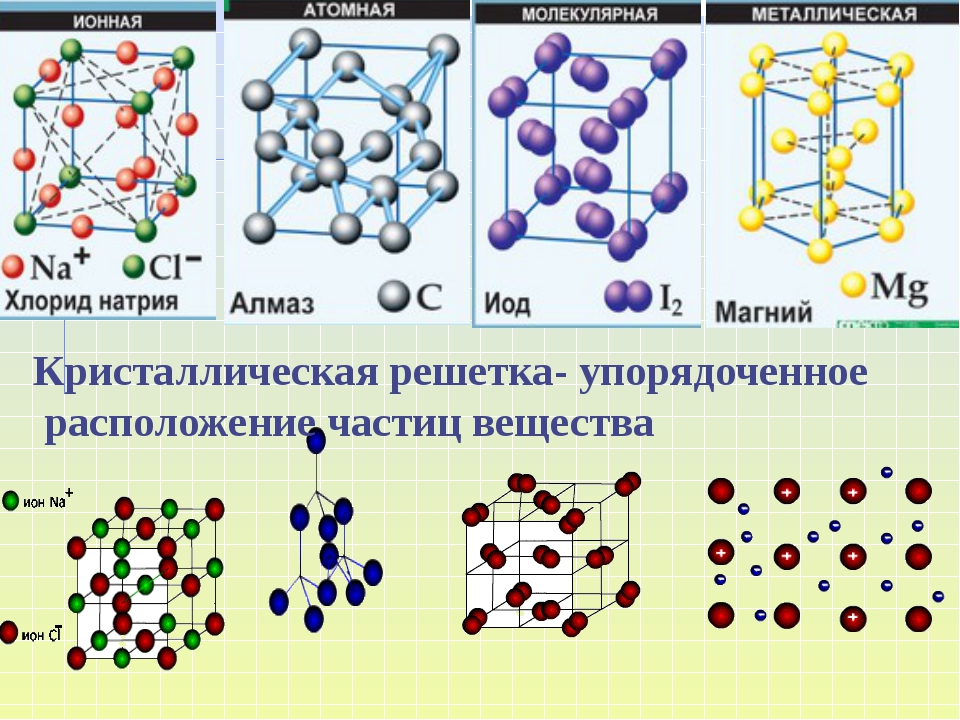
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
10. Немолекулярное строение имеет
1) водород
2) железо
3) кислород
4) угарный газ
Тесты с выбором ответа для самостоятельного решения
11. Атомную кристаллическую решетку имеет
1) железо
2) графит
3) карбонат кальция
4) азотная кислота
12. Кристаллическую структуру, подобную структуре алмаза, имеет
1) кремнезем SiO2
2) оксид натрия Na2O
3) оксид углерода(II) СО
4) белый фосфор Р4
13. Вещества, обладающие твердостью, тугоплавкостью, хорошей растворимостью в воде, как правило, имеют кристаллическую решетку
1) молекулярную
2) атомную
3) ионную
4) металлическую
14. Кристаллическая решетка хлорида кальция
1) атомная
2) молекулярная
3) металлическая
4) ионная
15. Кристаллическая решетка оксида углерода(IV)
Кристаллическая решетка оксида углерода(IV)
1) ионная
2) атомная
3) металлическая
4) молекулярная
16. Немолекулярное строение имеет
1) фуллерен
2) алмаз
3) вода
4) углекислый газ
17. Ионную кристаллическую решетку имеет
1) хлорид натрия
2) хлор
3) натрий
4) бромоводород
18. Ионную кристаллическую решетку имеет
1) фтор
2) фтороводород
3) гидрид натрия
4) хлорид титана(IV)
19. Молекулярную кристаллическую решетку имеет
1) фторид серы(VI)
2) сульфид натрия
3) графит
4) натрий
20. Молекулярную кристаллическую решетку имеет
1) литий
2) оксид натрия
3) красный фосфор
4) белый фосфор
Ответы на тесты раздела 1.3.3
1. 3 2. 1 3. 4 4. 2 5. 1 6. 4 7. 2 8. 3 9. 1 10. 2 11. 2 12. 1 13. 3 14. 4 15. 4 16. 2 17. 1 18. 3 19. 1 20. 4
3 14. 4 15. 4 16. 2 17. 1 18. 3 19. 1 20. 4
Решения тестов раздела 1.3.3
Решение 1. Атомные кристаллические решетки — это решетки, в узлах которых располагаются атомы, связанные ковалентными связями. К соединениям с атомной кристаллической решеткой относятся алмаз, германий, бор, красный фосфор Р, кремнезем SiO2 и др. Из соединений, приведенных в задании, фосфорная кислота Н3РО4 и белый фосфор Р4 имеют молекулярную кристаллическую решетку, кремнезем SiO2 — атомную, а хлорид аммония NH4Cl — ионную кристаллическую решетку.
Ответ: 3.
Решение 2. Вещества с атомной кристаллической решеткой, как правило, являются очень твердыми и тугоплавкими. Это обусловлено наличием прочных ковалентных связей между атомами, находящимися в узлах решетки. Так, оксид кремния(IV) SiO2 (атомная решетка) — это твердое вещество с высокой температурой плавления, а оксид углерода(IV) СО2 (молекулярная решетка) — газ при обычных условиях. Вещества с атомной кристаллической решеткой, как правило, не проводят электрический ток (нет ионов) и могут быть достаточно хрупкими. Так, алмаз раскалывается при ударе.
Вещества с атомной кристаллической решеткой, как правило, не проводят электрический ток (нет ионов) и могут быть достаточно хрупкими. Так, алмаз раскалывается при ударе.
Ответ: 1.
Решение 3. Молекулярная кристаллическая решетка — это решетка, в узлах которой находятся молекулы, между которыми действуют силы межмолекулярного взаимодействия. Молекулярные решетки характерны для неметаллов (Н2, О3, N2, Сl2, белый фосфор Р4, S8 и др.), для многих неорганических веществ (НСl, HNO3, H2SO4, Н2O, СO2 и др.), для большинства органических веществ (СН4, С6Н6, С2Н5ОН, СН3СООН и др.). Среди веществ, перечисленных в задании, молекулярную решетку имеют: Н2O, СO2, H2SO4, НСl и O3. Вещества CuO, K2S, NaCl имеют ионные кристаллические решетки.
Ответ: 4.
Решение 4. Силы межмолекулярного взаимодействия существенно слабее химических связей, поэтому вещества с молекулярной кристаллической решеткой имеют низкие температуры плавления. Эти силы увеличиваются с увеличением объема молекул, поэтому они возрастают, например, в ряду F2 — Cl2 – Вr2 – I2. Это приводит к увеличению температур кипения и плавления веществ в этом ряду и обуславливает то, что при обычных условиях фтор и хлор — газы, бром — жидкость, а иод — твердое вещество, легко возгоняющееся при нагревании. Вещество, охарактеризованное в задании, имеет молекулярную кристаллическую решетку.
Ответ: 2.
Решение 5. Ионная кристаллическая решетка — это решетка, в узлах которой находятся положительные и отрицательные ионы, между которыми существует ионная связь. Ионные кристаллические решетки характерны для большинства солей (K2SO4, CH3COONa и др.), для щелочей (NaOH, Ва(ОН)2 и др. ), для оксидов активных металлов (К2O, СаО и др.). Из перечисленных в задании веществ фторид кальция CaF2 имеет ионную кристаллическую решетку, медь — металлическую, а алмаз и оксид кремния(IV) — атомную кристаллическую решетку.
), для оксидов активных металлов (К2O, СаО и др.). Из перечисленных в задании веществ фторид кальция CaF2 имеет ионную кристаллическую решетку, медь — металлическую, а алмаз и оксид кремния(IV) — атомную кристаллическую решетку.
Ответ: 1.
Решение 6. Вещества с ионной кристаллической решеткой имеют высокие температуры плавления. Эти вещества (оксиды, соли, основания) являются твердыми при обычных условиях. При нагревании или растворении в воде эти вещества распадаются на ионы, и их расплавы и растворы проводят электрический ток. Вещества с ионной связью являются хрупкими веществами. В этой связи можно заключить, что вещество, описанное в задании, имеет ионную кристаллическую решетку.
Ответ: 4.
Решение 7. Металлическая кристаллическая решетка — это решетка, в узлах которой находятся атомы и положительные ионы металлов, связанные с помощью свободных электронов. Металлическая кристаллическая решетка характерна для металлов. Наличие свободных электронов обуславливает такие свойства металлов, как металлический блеск, электро- и теплопроводность, ковкость, пластичность. Металлы имеют сравнительно высокие температуры плавления. Наиболее тугоплавкий металл — вольфрам, наиболее легкоплавкий — ртуть. Описанные в задании свойства соответствуют металлической кристаллической решетке.
Наличие свободных электронов обуславливает такие свойства металлов, как металлический блеск, электро- и теплопроводность, ковкость, пластичность. Металлы имеют сравнительно высокие температуры плавления. Наиболее тугоплавкий металл — вольфрам, наиболее легкоплавкий — ртуть. Описанные в задании свойства соответствуют металлической кристаллической решетке.
Ответ: 2.
Решение 8. Высокие температуры плавления и химическая стойкость характерны и для веществ, например, с атомной кристаллической решеткой. Наличие металлической связи обуславливает такие свойства металлов, как металлический блеск, электро- и теплопроводность, ковкость, пластичность. Полезно запомнить, что в кристаллических решетках d-металлов помимо металлической связи возможны и ковалентные связи между атомами металлов, что приводит к увеличению твердости металлов, например хрома.
Ответ: 3.
Решение 9. Первое суждение справедливо: в соединениях с молекулярной кристаллической решеткой между молекулами существуют слабые силы межмолекулярного взаимодействия. Поэтому эти соединения имеют низкие температуры плавления. Отсутствие в этих соединениях свободных электронов обуславливает крайне низкую их электропроводность.
Поэтому эти соединения имеют низкие температуры плавления. Отсутствие в этих соединениях свободных электронов обуславливает крайне низкую их электропроводность.
Второе суждение неверно. Для соединений с атомной решеткой не характерны пластичность и высокая электропроводность. Алмаз, например, хрупок и может быть расколот при ударе. Алмаз в отличие от графита не проводит электрический ток. Справедливо только суждение А.
Ответ: 1.
Решение 10. Из перечисленных соединений молекулярные кристаллические решетки имеют водород Н2, кислород О2, угарный газ СО. Немолекулярное строение имеет металл железо, у которого металлическая кристаллическая решетка.
Ответ: 2.
Кристаллические атомная — Справочник химика 21
Твердые растворы замещения образуются в том случае, если кристаллические решетки компонентов однотипны и размеры частиц компонентов близки. Необходимым условием образования твердых растворов является также и известная близость химических свойств веществ (одинаковый тип химической связи). Так, в кристалле КС1 ионы хлора могут быть постепенно замещены ионами брома, т. е. можно осуществить практически непрерывный переход вещества от состава КС1 к составу КВг без заметного изменения устойчивости кристаллической решетки. Свойства образующихся твердых растворов непрерывно меняются от КС1 к КВг. Ниже приведены примеры ионных, атомных, молекулярных и металлических твердых растворов замещения. [c.134]
Так, в кристалле КС1 ионы хлора могут быть постепенно замещены ионами брома, т. е. можно осуществить практически непрерывный переход вещества от состава КС1 к составу КВг без заметного изменения устойчивости кристаллической решетки. Свойства образующихся твердых растворов непрерывно меняются от КС1 к КВг. Ниже приведены примеры ионных, атомных, молекулярных и металлических твердых растворов замещения. [c.134]
По строению вещества Молекула, молекулярная или атомная решетка Ионный кристалл (ионная кристаллическая решетка) Кристалл металла (металлическая решетка) [c.57]
В узлах атомных кристаллических решеток находятся нейтральные атомы, соединенные друг с другом ковалентными связями. Веществ, обладающих атомной решеткой, сравнительно немного. К ним относятся алмаз, кремний, некоторые соединения элементов с углеродом и кремнием — карбиды и силициды. [c.144]
Все твердые атомные соединения, как кристаллические, так и аморфные, имеют единую электронную структуру. Однако между электронными структурами этих двух типов атомных соединений имеется существенное различие. Так, энергетические состояния валентных электронов в кристаллических атомных соединениях группируются в квазинепрерывные зоны, тогда как для структур аморфного типа характерно локализованное состояние валентных электронов /68/. [c.109]
Однако между электронными структурами этих двух типов атомных соединений имеется существенное различие. Так, энергетические состояния валентных электронов в кристаллических атомных соединениях группируются в квазинепрерывные зоны, тогда как для структур аморфного типа характерно локализованное состояние валентных электронов /68/. [c.109]
Неметаллы, как правило, являются диэлектриками. При смычных условиях они находятся либо в виде двухатомных (галогены, водород, азот, кислород) и одноатомных молекул (благородные газы), либо в виде атомных кристаллов (сера, фосфор, углерод, селен). Промежуточное положение между металлами и неметаллами занимают полуметаллы (бор, кремний, германий, мышьяк, сурьма, теллур). Для них характерны свойства металлов и неметаллов. Как правило, они имеют кристаллические атомные решетки с ковалентной связью. Многие из них являются проводниками. [c.246]
Полупроводниковыми свойствами могут обладать как кристаллические вещества, так и некоторые стекла.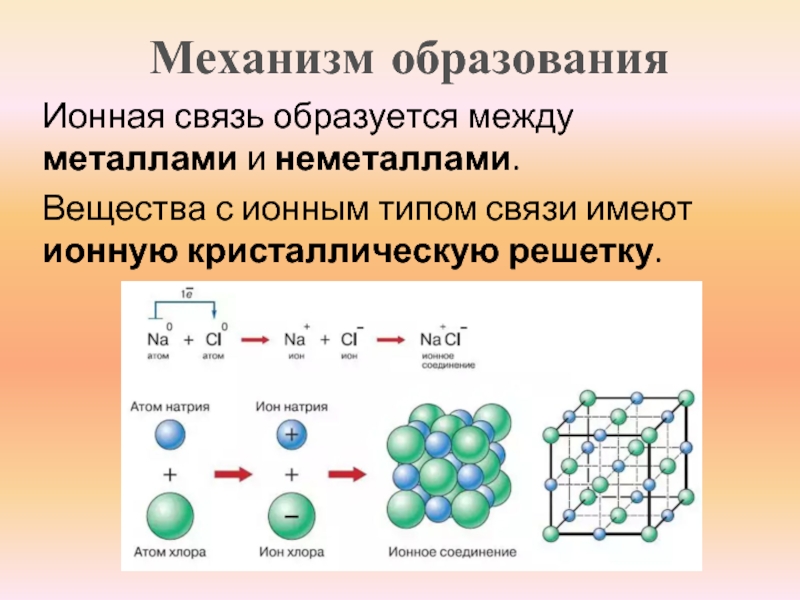 Полупроводниковые кристаллы могут состоять из частиц, связанных ковалентной связью (германий, кремний, карборунд и др.), т. е, обладать атомной кристаллической решеткой, В настоящее время эта группа полупроводниковых материалов привлекает наибольшее внимание. Однако полупроводниковыми свойствами могут обладать в определенных условиях также и многие кристаллы с ионной или молекулярной решеткой (неорганические и органические). [c.145]
Полупроводниковые кристаллы могут состоять из частиц, связанных ковалентной связью (германий, кремний, карборунд и др.), т. е, обладать атомной кристаллической решеткой, В настоящее время эта группа полупроводниковых материалов привлекает наибольшее внимание. Однако полупроводниковыми свойствами могут обладать в определенных условиях также и многие кристаллы с ионной или молекулярной решеткой (неорганические и органические). [c.145]
Исследования Н. И. Кобозева и др. [333, стр. 86] показали, что кристаллическая фаза железных катализаторов является каталитически недеятельной. Активные центры представляют собой до-кристаллические атомные образования, причем на 2000 атомов же леза приходится один каталитически активный центр. Поскольку плотность (вернее, насыпная плотность) карбонильного железа почти в 2 раза выше плотности обычного железного катализатора (4,5 вместо 2,5), число активных центров в 1 см катализатора у него больше. Так, если для железа это число равно 1,35 10 , то для карбонильного железа оно возрастает до 2,43 10 . [c.157]
[c.157]
Развитие стереохимии на протяжении последнего столетия может быть отмечено тремя особенно важными этапами 1874 г. можно считать годом основания стереохимии органических соединений Ле Белем и Вант-Гоффом, между 1891 и 1905 гг. Альфред Вернер разработал вопросы строения неорганических комплексных соединений, с 1916 по 1941 г. координационное учение было распространено на кристаллические соединения и разработана общая геометрия молекулярных и кристаллических атомных конфигураций. [c.11]
Оксид ВеО имеет структуру типа вюрцита (см. рис. 194), отличается высокой энергией кристаллической решетки и высокой энергией Гиббса образования (АО/ = —582 кДимоль). Он тугоплавок (т. пл. 2530″С), теплопроводен предварительно прокаленный (при 400°С) химически неактивен. Применяют ВеО в качестве химически стойкого и огнеупорного материала для изготовления тиглей и специальной керамики, а в атомной энергетике — как замедлитель и отражатель нейтронов. ВеО входит в состав некоторых стеклообразующих смесей. [c.472]
ВеО входит в состав некоторых стеклообразующих смесей. [c.472]
В соответствии с природой составляющих частиц кристаллические решетки могут быть ионными, атомными (ковалентными или металлическими) и молекулярными. [c.101]
Таким образом, в периодической системе при переходе от р-элементов Vin группы к s-элементам 1 группы уменьшение числа валентных электронов обусловливает закономерный переход от неметаллов с молекулярными кристаллическими решетками (Аг, lj, Р4) к неметаллам с атомно-цепной (S ), атомно-слоистой (Р ос) и атомно-коорди-национной структурами и далее к металлическим координа- [c.233]
Как уже указывалось, образованию твердых растворов благоприятствуют близость химических свойств, атомных радиусов и типов кристаллической структуры исходных веществ (с. 134). Несоблюдение одного из этих условий приводит к тому, что твердые растворы между компонентами образуются лишь в ограниченных пределах концентраций или же не образуются вообще. Например, предельная растворимость ряда металлов в никеле г =0,124 нм) выражается в виде следующего ряда [c.254]
Например, предельная растворимость ряда металлов в никеле г =0,124 нм) выражается в виде следующего ряда [c.254]
Преимущества определения положения атомных плоскостей при помощи индексов (/г, к, /), а не осевых отрезков, отсекаемых плоскостями на осях координат, будут очевидны, если учесть, что они всегда являются простыми целыми числами и величина их не зависит от внешних влияний (температура, растяжение, сжатие и т. п.), чего не наблюдается у осевых отрезков. Кроме того, индексы (й, к, I) наиболее просто определяют положение атомных плоскостей в кристаллической решетке. [c.111]
Большое число веществ с атомной кристаллической решеткой, в частности некоторые нитриды, фосфиды, карбиды, силициды и бориды, приобрели большое значение в разных областях повой техники благодаря присущей им термостойкости, тугоплавкости, высокой твердости (и при высоких температурах) или другим ценным свойствам. [c.133]
Энергия кристаллической решетки Е для атомных и молекулярных кристаллов может быть определена по уравнению [c. 142]
142]
Уравнение Вульфа—Брегга. Русский физик Г. В. Вульф дал наглядное объяснение отклонению рентгеновских лучей при прохождении их через кристаллическое вещество. Он показал, что рассеивание рентгеновских лучей атомами можно рассматривать как отражение рентгеновских лучей от параллельных атомных плоскостей кристалла. [c.112]
Совокупность атомов, удерживаемых вместе химическими связями, называется молекулой. Обычно (хотя далеко не всегда) образование связей в молекуле можно объяснить существованием электронных пар, каждая из которых связывает между собой два атома. Такая связь, образуемая электронной парой, называется ковалентной связью. Сумма атомных масс всех атомов в молекуле дает ее молекулярную массу. Хотя атомы, относящиеся к различным молекулам, непосредственно не связываются друг с другом, все молекулы обладают некоторой липкостью и притягиваются к другим молекулам. Эти вандерваальсовы силы притяжения заставляют молекулы газа слипаться друг с другом, образуя жидкость, если температура становится достаточно низкой под действием тех же сил молекулы жидкости выстраиваются в правильную кристаллическую решетку, когда температура вещества понижается еще больше. Температуры, при которых происходят два указанных перехода, называются соответственно температурой кипения (7 п) и температурой плавления (7 ,). [c.52]
Температуры, при которых происходят два указанных перехода, называются соответственно температурой кипения (7 п) и температурой плавления (7 ,). [c.52]
Наиболее высокими температурами плавления обладают некоторые группы кристаллов с атомной решеткой. Сюда относятся многие карбиды, силициды, нитриды и бориды метал юв. Плавление кристаллов происходит при той температуре, при которой тепловое движение частиц, усиливающееся при нагревании, становится способным в той или другой степени преодолевать взаимное притяжение частиц. Здесь речь идет о колебательном движении частиц, образующих кристаллическую решетку, и о взаимном притяжении между этими частицами. [c.151]
Во избежание существенного уменьщения точности результатов при расчете теплового эффекта реакции по теплотам образования компонентов необходимо, чтобы все эти данные относились к одинаковому состоянию веществ (одинаковое агрегатное состояние, кристаллическая форма, температура), и чтобы при расчете всех этих данных были использованы одинаковые значения различных вспомогательных величин, одинаковые значения физических постоянных, атомных весов и т. д. Таким образом, для получения более точных результатов все значения теплот образования, применяемые для расчета теплового эффекта какой-нибудь данной реакции, должны быть приведены в одну систему значений и обладать необходимой внутренней согласованностью. [c.55]
д. Таким образом, для получения более точных результатов все значения теплот образования, применяемые для расчета теплового эффекта какой-нибудь данной реакции, должны быть приведены в одну систему значений и обладать необходимой внутренней согласованностью. [c.55]
Реакционная способность углеродистых материалов зависит прежде всего от их молекулярной и кристаллической структуры, а затем от степени их пористости и содержания минеральных веществ [1, 2, 106, 212, 266]. По современным научным воззрениям, процесс сгорания углеводородов, углеродистых материалов и даже алмаза проходит в две стадии вначале разрываются все атомные связи, а затем каждый атом сгорает в отдельности. Это означает, что чем меньше требуется энергии на разрыв межатомных связей в молекуле данного соединения, тем больше его реакционная способность. [c.219]
По характеру частиц, находящихся в узлах кристаллической решетки, и ио характеру связи между ними кристаллические решетки подразделяются на следующие типы ионный, молекулярный, атомный и металлический. [c.69]
[c.69]
По современным воззрениям, электронная струюура кристаллического атомного вещества представляет собой квантовую систему периодической структуры, электроны которой неразличимы и каждый из них взаимодействует сразу со всей системой в целом. Трехмерная непрерывная сеть межатомных связей в твердом теле периодического строения является системой волноводов для волн электронного газа, состоящего из валентных электронов, уровни энергии которых тесно сгруппированы в квазинепрерывные зоны. Наличие свободных, не связанных с определенными атомами, электронов, способных перемещаться по всему объему тела, определяет металлическое состояние этих веществ. Наиболее характерными представите- ями этого типа твердых веществ являются металлы. Обобществленные электроны, обеспечивающие металлическую связь в кристаллических твердых веществах, в отличие от электронов обычной ковалентной связи, существенно слабее связаны с определенным атомом. Поэтому работа выхода электрона, характеризующая прочность связи электронов со всей системой, для кристаллических атомных веществ имеет обычно малые значения. Так, для металлов значение ее лежит в пределах от 1,9 э6 для цезия, до 5,3 эб-для платины, тогда как потенциал ионизации для соединений с обычной кова- [c.109]
Так, для металлов значение ее лежит в пределах от 1,9 э6 для цезия, до 5,3 эб-для платины, тогда как потенциал ионизации для соединений с обычной кова- [c.109]
Адсорбционная теория не может объяснить процесс запарафинирования, когда материалом подложки являются кристаллические атомные вещества, в частности, металлы, в которых благодаря металлическим связям имеются обобществленные, не связанные с конкретными атомами и способные перемещаться по всему объему тела наружные электроны. [c.111]
В этом случае более соответствует экспериментальным фактам электрическая теория адгезии /58/, которая позволяет следующим образом объяснять механизм процесса. Согласно этой теории, при тесном соприкосновений диэлектрика, каковым являются парафиновые дисперсные частицы, и кристаллического атомного тела, благодаря разности давлений электронного газа, часть электронов подложки переходит в парафиновую частицу, обра (уя двойной электрический слой между поверхностями. В результате парафиновые частицы заряжаются отрицательно, а металлическая поверхность подложки приобретает положительный заряд. По этой теории работа разрушения адгезионной связи, т.е. преодоления возникающих между поверхностями электрических сил, будет определяться формулой /56/ [c.111]
В результате парафиновые частицы заряжаются отрицательно, а металлическая поверхность подложки приобретает положительный заряд. По этой теории работа разрушения адгезионной связи, т.е. преодоления возникающих между поверхностями электрических сил, будет определяться формулой /56/ [c.111]
Во-вторых, нанесение полимерного защитного покрытия резко меняет природу материала подложки место кристаллического атомного соединения — металла — занимает аморфное атомное соединение — полимер, т.е. происходит замена типа электронной структуры материала подложки. Замена кристаллического атомного соединения, у которого каждый электрон взаимодействует сразу со всей системой в целом, на аморфное атомное соединение, электронная структура которого представляет собой набор дискретных уровней, разделенных высокими потенциальными барьерами, препятствующими распределению электронных волн за границу каждой данной межатомной связи, меняет механизм взаимодействия подложки с такими типичными молекулярными твердыми соединениями, какими являются кристаллические парафиновые частицы.
 В результате такой замены более интенсивная адгезионная связь, основанная на образовании двойного электрического слоя, возникающего в результате контактной электризации поверхностей металла и парафиновой частицы, с энергией более 65 кДж/моль /56/, сменяется адгезионной связью, определяемой ван-дер-ваальсовыми силами, энергия которых не превышает 50 кДж/моль. Поэтому смена металлической поверхности на полимерную уже сама по себе должна привести к ослаблению адгезионной связи. Действительно, как бьшо показано экспериментально /30/, сила прилипания парафина к поверхности такого наиболее интенсивно парафинирующегося полимера, как полиэтилен, в 2,3 раза ниже, чем у стали. [c.143]
В результате такой замены более интенсивная адгезионная связь, основанная на образовании двойного электрического слоя, возникающего в результате контактной электризации поверхностей металла и парафиновой частицы, с энергией более 65 кДж/моль /56/, сменяется адгезионной связью, определяемой ван-дер-ваальсовыми силами, энергия которых не превышает 50 кДж/моль. Поэтому смена металлической поверхности на полимерную уже сама по себе должна привести к ослаблению адгезионной связи. Действительно, как бьшо показано экспериментально /30/, сила прилипания парафина к поверхности такого наиболее интенсивно парафинирующегося полимера, как полиэтилен, в 2,3 раза ниже, чем у стали. [c.143] На основе всесторонних исследований оптического муара с помощью растров (сеток) А. В. Шубников предсказал возможность получения муара при наложении кристаллических атомных решеток (1926 г.). Его идея была реализована в 1957 г. с помощью электронного микроскопа, а затем в 1965—1968 гг.— с помощью рентгеновской дифракции. Рентгенодифракционный муар кристаллических атомных решеток в 10 раза более чувствительный, чем электронно-микроскопический, и соответственно и его возможности намного шире, особенно при исследованиях реальной структуры высокосовершенных кристаллов. По геометрии легко определяется характер искажения решетки (сжатие — растяжение решеток) — дилатацистшый муар или (поворот решетки) — ротационный муар. С помощью рентгеновского муара можно измерить искажения решетки Аё/с1 К)- и повороты решетки в 10- рад. Еще более расширяются возможности измереш я рентгенодифракционного муара при использовании трехкристального интерферометра. Здесь появляются новые возможности измерения абсолютных величин периодов решетки, длин рентгеновских волн, перемещений в 10- сл и углов поворота 10 рай и т. д. [c.403]
Рентгенодифракционный муар кристаллических атомных решеток в 10 раза более чувствительный, чем электронно-микроскопический, и соответственно и его возможности намного шире, особенно при исследованиях реальной структуры высокосовершенных кристаллов. По геометрии легко определяется характер искажения решетки (сжатие — растяжение решеток) — дилатацистшый муар или (поворот решетки) — ротационный муар. С помощью рентгеновского муара можно измерить искажения решетки Аё/с1 К)- и повороты решетки в 10- рад. Еще более расширяются возможности измереш я рентгенодифракционного муара при использовании трехкристального интерферометра. Здесь появляются новые возможности измерения абсолютных величин периодов решетки, длин рентгеновских волн, перемещений в 10- сл и углов поворота 10 рай и т. д. [c.403]
Атомно — металлические кристаллы вследствие не-локализованностн металлической связи хара1 теризуются высокими координационными числами. Для них наиболее характерны три типа кристаллических решеток (рис. 65) кубическая гранецентрирован-ная (к. ч. 12), гексагональная (к. ч. 12) и кубическая объемноцентри-рованная (к. ч. 8). Кубическую гранецентрированную решетку имеет, например, медь, кубическую объемноцентрированную — железо, гексагональную — магний. [c.101]
65) кубическая гранецентрирован-ная (к. ч. 12), гексагональная (к. ч. 12) и кубическая объемноцентри-рованная (к. ч. 8). Кубическую гранецентрированную решетку имеет, например, медь, кубическую объемноцентрированную — железо, гексагональную — магний. [c.101]
Если газ, образующийся в результате возгонки, состоит из тех же частиц, что и сам кристалл, то энергия кристаллической решетки совпадает со значением энергии возгонки (сублима 1,ии). Это относится к молекулярным, атомно-ковалентным и атомно-металлическим кристаллам. Таким образом, в этом случае энергию кристаллической решетки можно определить экспериментально. [c.166]
Алмаз — кристаллическое вещество с атомной координационной кубической решеткой (рис. 166). Вследствие5/7 -гибридизации каждый атом в алмазе образует равноценные прочные о-связи с четырьмя [c.392]
Эта задача была решена Н. И. Кобозевым в 1939 г. в созданной им теории активных ансамблей, основное исходное положение которой заключается в следующем носителем каталитической активности является находящаяся на поверхности атомная (докристаллическая) фаза катализатора относитель-. но которой поверхность носителя (или кристаллическая фаза самого катализатора) выполняет функцию инертной подкладки., Для каждого же данного процесса активным центром является ансамбль из определенного числа п атомов катализатора. [c.355]
но которой поверхность носителя (или кристаллическая фаза самого катализатора) выполняет функцию инертной подкладки., Для каждого же данного процесса активным центром является ансамбль из определенного числа п атомов катализатора. [c.355]
Пластичность металлов также объясняется специфическими свойствами металлической связи. При мехаиическом воздействии на твердое тело отдельные слои его кристаллической решетки смещаются отиосительнс друг друга. В кристаллах с атомной структурой это приводит к разрыву ковалентных связей между атомами, принадлежащими различным слоям, и кристалл разрущается. В кристаллах с ионной структурой при взаимном смещении слоев неизбежно создается такое положение, при котором рядом оказы-вйются одноименно заряженные ионы при этом возникают силы Е ле.- лростатнческого отталкивания и кристалл также разрушается. В случае же металла при смещении отдельных с. юев его кристаллической решетки происходит лишь некоторое перераспределение электронного газа, связывающего друг с другом атомы металла, но разрыва химических сг,язей не происходит—металл деформируется, пе разрушаясь. [c.534]
[c.534]
Естественно, что теория кристаллического поля, исходящая из ионной модели, требует видоизменения при рассмотрении комплексов, в которых имеется заметная доля ковалентной связи. Когда эта доля сравнительно невелика, используется теория прля лигандов, по которой наличие ковалентной связи учитывается введением определенных поправок в расчеты, проводимые методами теории кристаллического поля. При рассмотрении комплексных соединений со значительной долей ковалентной связи применяется метод молекулярных орбиталей, учитывающий, так же как и теория кристаллического поля, особенности симметрии атомных орби талей (такой метод часто также называют теорией поля-лигандов) [c.121]
Уникальная, среди металлов кристаллическая решетка Ga, состоящая из атомных пар Ga >, обусловливает необычные свойства металлического галлия — мииимал-ьную температуру плавления в ряду металлов подгруппы IIIA, меньшую плотность кристаллов по сравнению с жидкостью, соответственно 5,9037 и 6,0947 г/см [c. 344]
344]
При действии на уран избытка Рг образуется гексафторид иРб—бесцветное, легко возгоняющееся кристаллическое вещество (давление его пара достигает 101 кПа при 56,5 °С). Это единственное соединение урана, существующее в газообразном состоянии при низкой температуре, что имеет большое практическое значение, поскольку необходимое для получения атомной энергии разделение изотопов и осуществляют с помощью различных процессов, протекающих в газовой фазе. При растворении в воде ирб гидролизуется, образуя иОгр2 и НР. Тетрафторид ир4 получают действием НР на иОз- С хлором уран образует [c.609]
Большой интерес представляют насыщенные пары при высоких температурах, Процесс испарения жидкости или сублимации твердого тела при любых температурах происходит в результате того, что тепловое движение преодолевает связи между частицами. Однако при обычных или более низких температурах тепловое движение может преодолевать лишь сравнительно слабые силы межмолекулярного взаимодействия, а при высоких — оно способно разрывать и достаточно прочные связи, в частности химические связи между атомами в кристаллах с атомной решеткой. Поэтому в парах при высоких температурах могут содержаться свободные атомы или группы атомов с ненасыщенной валентностью (свободные радикалы). Так, кристаллические полуторные окислы некоторых металлов (АЬОз, ЬааОз, РгаОа и др.) при образовании паров в области 2000° К претерпевают химическое разложение по реакциям [c.239]
Поэтому в парах при высоких температурах могут содержаться свободные атомы или группы атомов с ненасыщенной валентностью (свободные радикалы). Так, кристаллические полуторные окислы некоторых металлов (АЬОз, ЬааОз, РгаОа и др.) при образовании паров в области 2000° К претерпевают химическое разложение по реакциям [c.239]
Особый интерес представляют условия образования твердых растворов замещения, в которых железо играет роль растворителя. И. И. Корнилов установил связь между растворимостью элементов в железе и их ионными диаметрами атомный диаметр растворимого элемента должен отличаться от атомного диамет)ра железа не более чем на 8—15%. Только при этих условиях не происходит значительной деформации кристаллической решетки растворителя и изменения характера связи. Если это ра.зличие не превышает 8%, то образуются непрерывные твердые растворы если различие составляет 8—15%, то образуются ограниченные твердые растворы. Так, например, хром, с атомным диаметром, отличающимся от железа не более чем на 1,5%, дает с ним непрерывный ряд твердых растворов молибден, отличающийся от железа по атомному диаметру на 10%, ограниченно растворяется в железе еще меньше растворяется вольфрам и т. д. Отмеченные закономерности в отношении растворимости элементов в железе распространяются и на некоторые другие элементы. [c.123]
д. Отмеченные закономерности в отношении растворимости элементов в железе распространяются и на некоторые другие элементы. [c.123]
Твердые растворы внедрения. Б кристаллической решетке твердых растворов внедрения атомы растворенного элемента не замещают атомы растворителя, а располагаются между атомами в узлах решетки. Чаще всего твердые растворы внедрения образуются при растворенин в металлах переходных групп неметаллов с малыми атомными диаметрами, таких, например, как водород, азот, углерод, бор. В частности, твердый раствор углерода в у-железе (аустенит) является твердым раствором внедрения. Твердые растворы внедрения чаще всего образуют металлы, имеющие гранецентрированную кубическую решетку. [c.123]
В. И. Клименкова и Ю. Н. Алексеенко [104] опубликовали работу по изменению свойств искусственного графита под действием быстрых нейтронов в условиях атомного реактора, где графит является замедлителем. При этом происходит значиг тельное нарушение (разупорядочение) кристаллической решетки графита с одновременным изменением ряда свойств. Увеличивается почти в 2 раза модуль Юнга, повышается твердость, удельное электросопротивление возрастает примерно в 3 раза, удельный объем увеличивается на несколько процентов и теплопроводность графита уменьшается в 20 раз. Графит теряет свои обычные свойства и приобретает качества, характерные для кокса, прокаленного при 1300—1400°С. [c.205]
Увеличивается почти в 2 раза модуль Юнга, повышается твердость, удельное электросопротивление возрастает примерно в 3 раза, удельный объем увеличивается на несколько процентов и теплопроводность графита уменьшается в 20 раз. Графит теряет свои обычные свойства и приобретает качества, характерные для кокса, прокаленного при 1300—1400°С. [c.205]
Физика — 10
Виды кристаллической решетки. В зависимости от вида химической связи и взаимодействия между частицами, расположенными в узлах кристаллической решетки, существуют четыре вида кристаллических решеток. Это металлическая, атомная, ионная и молекулярная кристаллическая решетка.
Металлическая решетка. В узлах металлической решетки находятся положительные ионы металла. Такие кристаллы возникают в результате взаимодействия между атомами одного вида металла с очень маленькой энергией ионизации. Внешние валентные электроны в атомах металлов очень слабо связаны с ядром. При переходе в твердое состояние атомы располагаются настолько близко друг к другу, что валентные электроны покидают свой атом и становятся свободными внутри кристалла.
Внешние валентные электроны в атомах металлов очень слабо связаны с ядром. При переходе в твердое состояние атомы располагаются настолько близко друг к другу, что валентные электроны покидают свой атом и становятся свободными внутри кристалла.
Освобожденные валентные электроны в виде электронного газа беспорядочно движутся между положительными ионами кристаллической решетки и, связывая их, образуют металлическую связь (c). Концентрация свободных электронов в металле равна концентрации ионов.
Атомная решетка. В узлах атомной решетки находятся нейтральные атомы. Ковалентная связь между атомами возникает за счет электронной пары их валентных электронов. Ковалентная связь характерна для кристаллов sp элементов. Как пример таких кристаллов можно привести кремний, германий и другие. Атомы этих элементов на внешнем электронном уровне имеют четыре валентных электрона. Каждый электрон такого атома образует ковалентную связь с одним из электронов соседнего атома, в результате образуются четыре ковалентные связи. Таким образом, атом, присоединив к себе четыре электрона, приобретает устойчивую электронную конфигурацию восьмиэлектронного инертного газа s2p6. В ковалентной связи движение электронов имеет направленный характер, то есть каждый электрон движется вокруг ядер четырех атомов (d).
Каждый электрон такого атома образует ковалентную связь с одним из электронов соседнего атома, в результате образуются четыре ковалентные связи. Таким образом, атом, присоединив к себе четыре электрона, приобретает устойчивую электронную конфигурацию восьмиэлектронного инертного газа s2p6. В ковалентной связи движение электронов имеет направленный характер, то есть каждый электрон движется вокруг ядер четырех атомов (d).
Ионная решетка. В узлах ионной решетки находятся положительные и отрицательные ионы. Ионная связь возникает из-за обмена электронами в результате взаимодействия двух разных атомов с малой и большой энергией ионизации. Кулоновская сила притяжения между ионами противоположных знаков удерживает их в узлах кристаллической решетки. Как образец такого вида вещества можно привести кристаллическую решетку соединения водорода с щелочным металлом, например, NaCl(e).
Молекулярная решетка. В узлах молекулярной кристаллической решетки находятся молекулы. Молекулы, располагаясь в определенном порядке, создают друг с другом межмолекулярную связь. Находящиеся в газообразном состоянии водород, хлор, четырехоксидный углерод в твердом состоянии образуют молекулярную решетку. У кристаллов такого типа связь между молекулами очень слабая, поэтому она разрушается при низких температурах, то есть вещество плавится. Это можно ясно видеть на модели кристалла льда (f). Из модели видно, что каждый атом кислорода окружен четырьмя атомами водорода. Атомы водорода играют связывающую роль между атомами кислорода. При нагревании льда его кристаллическая решетка быстро разрушается.
Аморфные тела. Аморфные тела характеризуются отсутствием дальнего порядка в расположении частиц. Так как этот порядок выполняется только для соседних частиц, то говорят, что аморфные тела — это твердые тела, частицы которых обладают ближним порядком расположения.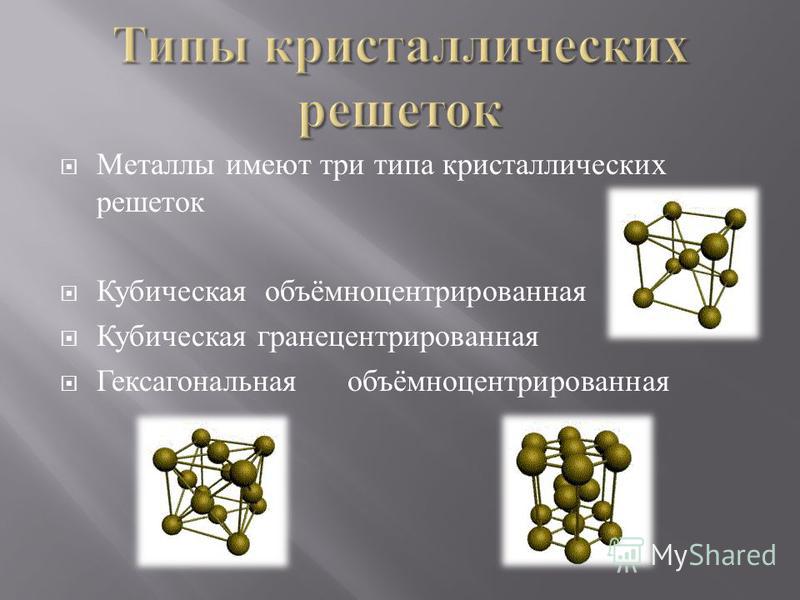
Строение веществ » HimEge.ru
В химические взаимодействия вступают не отдельные атомы или молекулы, а вещества. По типу связи различают вещества молекулярного и немолекулярного строения.
Это вещества, состоящие из молекул. Связи между молекулами в таких веществах очень слабые, намного слабее, чем между атомами внутри молекулы, и уже при сравнительно низких температурах они разрываются — вещество превращается в жидкость и далее в газ (возгонка йода). Температуры плавления и кипения веществ, состоящих из молекул, повышаются с увеличением молекулярной массы. К молекулярным веществам относятся вещества с атомной структурой (С, Si, Li, Na, К, Си, Fe, W), среди них есть металлы и неметаллы.
Немолекулярное строение веществК веществам немолекулярного строения относятся ионные соединения. Таким строением обладает большинство соединений металлов с неметаллами: все соли (NaCl, K2S04), некоторые гидриды (LiH) и оксиды (CaO, MgO, FeO), основания (NaOH, КОН).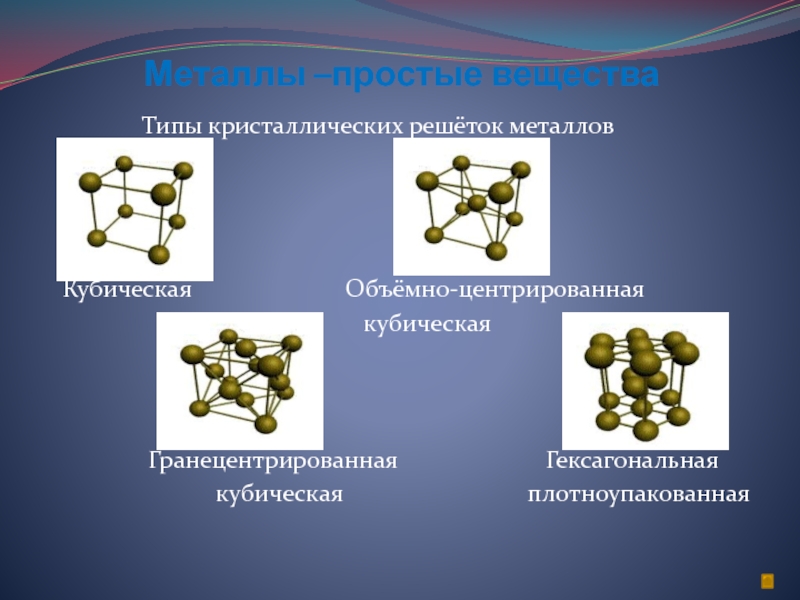 Ионные (немолекулярные) вещества имеют высокие температуры плавления и кипения.
Ионные (немолекулярные) вещества имеют высокие температуры плавления и кипения.
Аморфные вещества не имеют четкой температуры плавления — при нагревании они постепенно размягчаются и переходят в текучее состояние. В аморфном состоянии, например, находятся пластилин и различные смолы.
Кристаллические вещества характеризуются правильным расположением тех частиц, из которых они состоят: атомов, молекул и ионов — в строго определенных точках пространства. При соединении этих точек прямыми линиями образуется пространственный каркас, называемый кристаллической решеткой. Точки, в которых размещены частицы кристалла, называют узлами решетки.
В зависимости от типа частиц, расположенных в узлах кристаллической решетки, и характера связи между ними, различают четыре типа кристаллических решеток: ионные, атомные, молекулярные и металлические.
Ионные кристаллические решеткиИонными называют кристаллические решетки, в узлах которых находятся ионы. Их образуют вещества с ионной связью, которой могут быть связаны как простые ионы Na+, Сl—, так и сложные S042-, ОН—. Следовательно, ионными кристаллическими решетками обладают соли, некоторые оксиды и гидроксиды металлов. Например, кристалл хлорида натрия построен из чередующихся положительных ионов Na+ и отрицательных Сl—, образующих решетку в форме куба.
Их образуют вещества с ионной связью, которой могут быть связаны как простые ионы Na+, Сl—, так и сложные S042-, ОН—. Следовательно, ионными кристаллическими решетками обладают соли, некоторые оксиды и гидроксиды металлов. Например, кристалл хлорида натрия построен из чередующихся положительных ионов Na+ и отрицательных Сl—, образующих решетку в форме куба.
Ионная кристаллическая решетка поваренной соли
Связи между ионами в таком кристалле очень устойчивы. Поэтому вещества с ионной решеткой отличаются сравнительно высокой твердостью и прочностью, они тугоплавки и нелетучи.
Атомные кристаллические решеткиАтомными называют кристаллические решетки, в узлах которых находятся отдельные атомы. В таких решетках атомы соединены между собой очень прочными ковалентными связями. Примером веществ с таким типом кристаллических решеток может служить алмаз — одно из аллотропных видоизменений углерода.
Атомная кристаллическая решетка алмаза
Большинство веществ с атомной кристаллической решеткой имеют очень высокие температуры плавления (например, у алмаза она свыше 3500 °С), они прочны и тверды, практически нерастворимы.
Молекулярные кристаллические решеткиМолекулярными называют кристаллические решетки, в узлах которых располагаются молекулы.
Молекулярная кристаллическая решетка йода
Химические связи в этих молекулах могут быть и полярными (НСl, Н2O), и неполярными (N2, О2). Несмотря на то, что атомы внутри молекул связаны очень прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного притяжения. Поэтому вещества с молекулярными кристаллическими решетками имеют малую твердость, низкие температуры плавления, летучи. Большинство твердых органических соединений имеют молекулярные кристаллические решетки (нафталин, глюкоза, сахар).
Металлические кристаллические решеткиВещества с металлической связью имеют металлические кристаллические решетки.
Металлическая кристаллическая решетка
В узлах таких решеток находятся атомы и ионы (то атомы, то ионы, в которые легко превращаются атомы металла, отдавая свои внешние электроны «в общее пользование»). Такое внутреннее строение металлов определяет их характерные физические свойства: ковкость, пластичность, электро- и теплопроводность, характерный металлический блеск.
6.4: Кристаллические структуры металлов
Кристаллическая природа металлов
Все металлические элементы (кроме Cs, Ga и Hg) представляют собой твердые кристаллические вещества при комнатной температуре. Подобно ионным твердым веществам, металлы и сплавы имеют очень сильную тенденцию к кристаллизации, независимо от того, получены ли они термической обработкой или другими методами, такими как восстановление раствора или гальваника. Металлы легко кристаллизуются, и даже при очень быстром охлаждении трудно образовать стеклообразный металл. Расплавленные металлы имеют низкую вязкость, и идентичные (по существу сферические) атомы могут очень легко упаковываться в кристалл. Однако стеклообразные металлы могут быть получены путем быстрого охлаждения сплавов, особенно если составляющие атомы имеют разные размеры. Различные атомы не могут упаковываться в простую элементарную ячейку, что иногда делает кристаллизацию достаточно медленной, чтобы сформировать стекло.
Однако стеклообразные металлы могут быть получены путем быстрого охлаждения сплавов, особенно если составляющие атомы имеют разные размеры. Различные атомы не могут упаковываться в простую элементарную ячейку, что иногда делает кристаллизацию достаточно медленной, чтобы сформировать стекло.
Объемно-центрированная кубическая |
ГПУ (слева) и ГЦК (справа) плотная упаковка сфер |
Кристаллические структуры
Большинство металлов и сплавов кристаллизуются в одной из трех очень распространенных структур: объемно-центрированной кубической (ОЦК), гексагональной плотноупакованной (ГПУ) или кубической плотноупакованной (ГЦК, также называемой гранецентрированной кубической, ГЦК).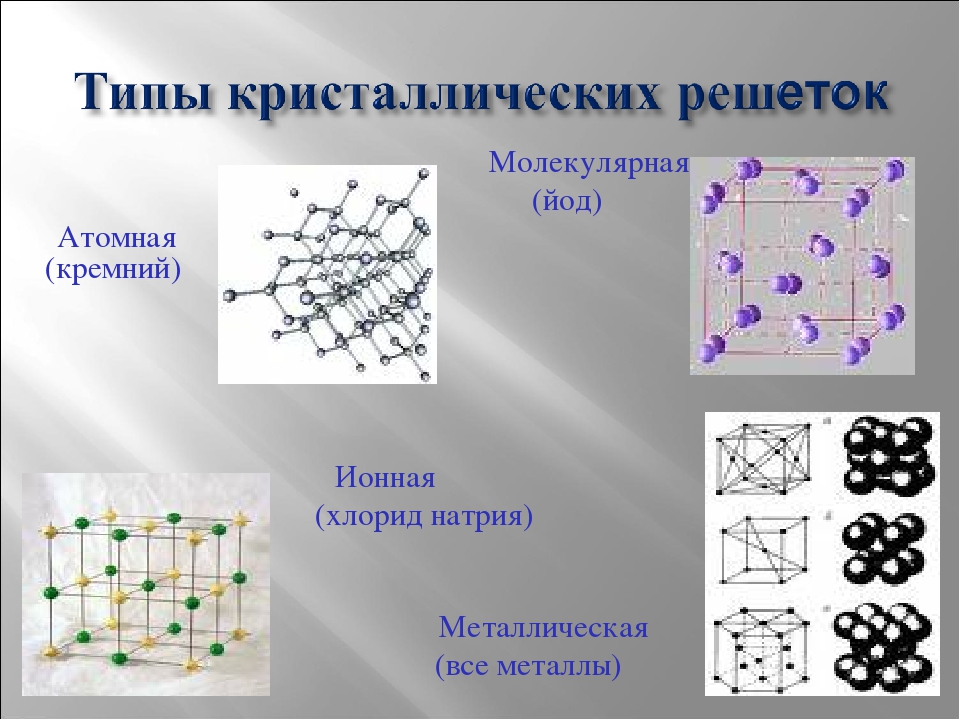 Во всех трех структурах координационное число атомов металла (т. Е. Число равноудаленных ближайших соседей) достаточно велико: 8 для ОЦК и 12 для ГПУ и ГПУ. Мы можем сопоставить это с низкими координационными числами (то есть с низкой валентностью — например, 2 для O, 3 для N или 4 для C), обнаруженными в неметаллах. В структуре ОЦК ближайшие соседи находятся в углах куба, окружающего атом металла в центре. В структурах ГПУ и ЦПУ атомы упаковываются, как штабелированные пушечные ядра или бильярдные шары, слоями с шестикоординатным расположением.У каждого атома также есть еще шесть ближайших соседей из слоев выше и ниже. Последовательность укладки — это ABCABC … в решетке ccp и ABAB … в hcp. В обоих случаях можно показать, что сферы заполняют 74% объема решетки. Это наибольшая объемная доля, которую можно заполнить решеткой из равных сфер.
Во всех трех структурах координационное число атомов металла (т. Е. Число равноудаленных ближайших соседей) достаточно велико: 8 для ОЦК и 12 для ГПУ и ГПУ. Мы можем сопоставить это с низкими координационными числами (то есть с низкой валентностью — например, 2 для O, 3 для N или 4 для C), обнаруженными в неметаллах. В структуре ОЦК ближайшие соседи находятся в углах куба, окружающего атом металла в центре. В структурах ГПУ и ЦПУ атомы упаковываются, как штабелированные пушечные ядра или бильярдные шары, слоями с шестикоординатным расположением.У каждого атома также есть еще шесть ближайших соседей из слоев выше и ниже. Последовательность укладки — это ABCABC … в решетке ccp и ABAB … в hcp. В обоих случаях можно показать, что сферы заполняют 74% объема решетки. Это наибольшая объемная доля, которую можно заполнить решеткой из равных сфер.
Атомы в металлических кристаллах имеют тенденцию собираться в плотные структуры, которые эффективно заполняют пространство. Простая квадратная упаковка (см. Выше), на которой основана простая кубическая структура, неэффективна и поэтому редко встречается среди металлических кристаллических структур.Структуры, ориентированные на тело или лицо, заполняют пространство более эффективно и чаще.
Выше), на которой основана простая кубическая структура, неэффективна и поэтому редко встречается среди металлических кристаллических структур.Структуры, ориентированные на тело или лицо, заполняют пространство более эффективно и чаще.
Периодические тенденции в структуре и поведении металлов
Помните, где мы находим металлические элементы в периодической таблице — везде, кроме правого верхнего угла. Это означает, что по мере того, как мы спускаемся по группе в p-блоке (скажем, группа IVA, углеродная группа или группа VA, азотная группа), свойства элементов постепенно изменяются от неметаллов к металлоидам и к металлам. Группа углерода хорошо иллюстрирует переход.Начиная сверху, элемент углерод имеет две устойчивые аллотропы — графит и алмаз. В каждом из них валентность атомов углерода точно удовлетворяется за счет создания четырех электронных парных связей с соседними атомами. В графите у каждого углерода есть три ближайших соседа, поэтому есть две одинарные связи и одна двойная связь. В алмазе есть четыре ближайших соседа, расположенные в вершинах тетраэдра, поэтому с каждым из них существует одинарная связь.
В алмазе есть четыре ближайших соседа, расположенные в вершинах тетраэдра, поэтому с каждым из них существует одинарная связь.
Два элемента прямо под углеродом (кремний и германий) в периодической таблице также имеют структуру алмаза (напомним, что эти элементы не могут легко образовывать двойные связи между собой, поэтому нет графитового аллотропа для Si или Ge).Хотя алмаз является хорошим изолятором, и кремний, и германий являются полупроводниками (то есть металлоидами). Механически они твердые, как алмаз. Как и углерод, каждый атом Si и Ge удовлетворяет своей валентности четыре, создавая одинарные связи с четырьмя ближайшими соседями.
Следующим элементом после германия является олово (Sn). Олово имеет два аллотропа, один с алмазной структурой, а другой со слегка искаженной ОЦК-структурой. Последний имеет металлические свойства (металлический блеск, пластичность) и проводимость примерно в 10 9 раз выше, чем Si.Наконец, свинец (Pb), элемент под Sn, имеет структуру ccp, а также является металлическим.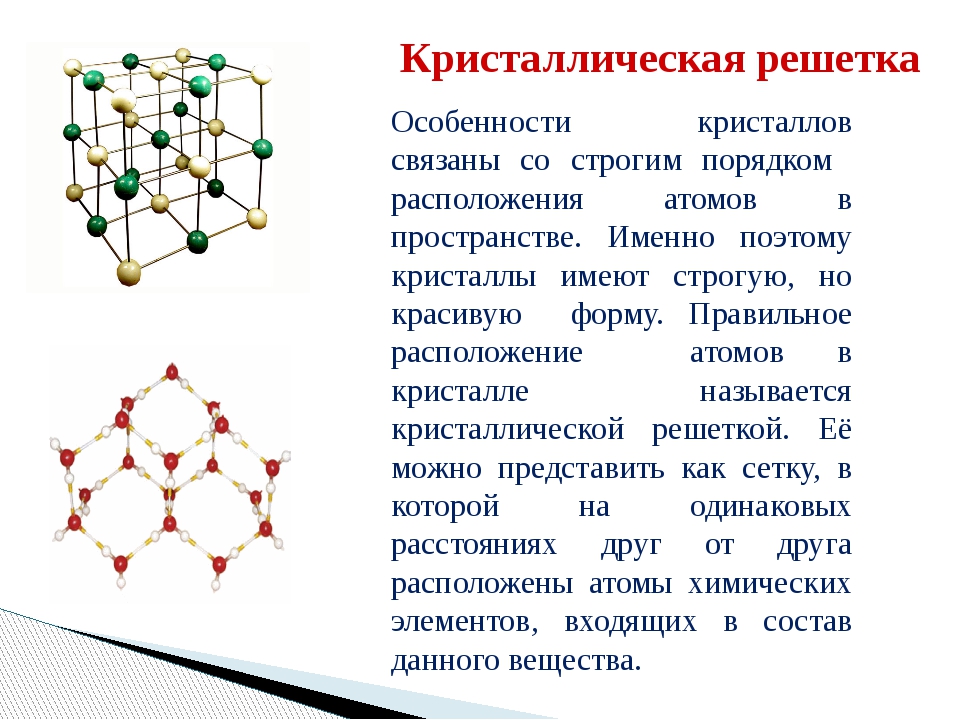 Обратите внимание на тенденции изменения координационного числа и проводящих свойств:
Обратите внимание на тенденции изменения координационного числа и проводящих свойств:
| Элемент | Строение | Coord. нет. | Электропроводность |
|---|---|---|---|
| К | графит, алмаз | 3, 4 | полуметалл, изолятор |
| Si | алмаз | 4 | полупроводник |
| Ge | алмаз | 4 | полупроводник |
| Sn | бриллиант, искаженный bcc | no.»> 4, 8 | полупроводник, металл |
| Пб | куб.см | 12 | металл |
Элементы C, Si и Ge подчиняются правилу октетов, и мы можем легко идентифицировать электронные парные связи в их структурах.Sn и Pb, с другой стороны, принимают структуры с высокими координационными числами. У них недостаточно валентных электронов для создания электронных парных связей с каждым соседом (это общая черта металлов). В этом случае происходит то, что валентные электроны «размазываются» или делокализованы по всем атомам в кристалле. Лучше всего думать о связи в металлах как о кристаллическом расположении положительно заряженных ядер с «морем» общих валентных электронов, склеивающих структуру.Поскольку электроны не локализованы в какой-либо конкретной связи между атомами, они могут перемещаться в электрическом поле, поэтому металлы хорошо проводят электричество.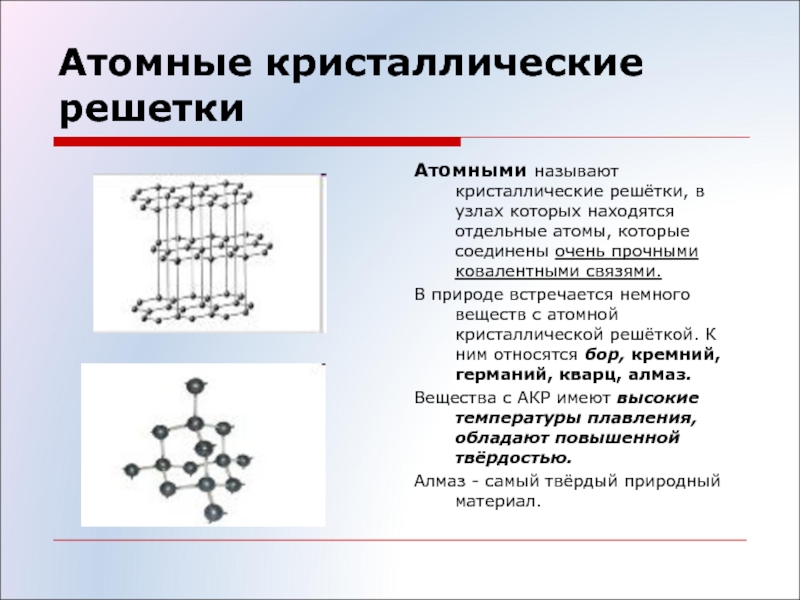 Другой способ описать связь в металлах — ненаправленный. То есть ближайшие соседи атома окружают его во всех направлениях, а не в нескольких конкретных направлениях (например, в углах тетраэдра, как мы обнаружили для алмаза). С другой стороны, неметаллы (изоляторы и полупроводники) имеют направленную связь. Поскольку соединение является ненаправленным, а координационные числа высокие, деформировать координационную сферу (т.е.е., разрыв или растяжение связей), чем в случае неметалла. Вот почему такие элементы, как Pb, намного более пластичны, чем C, Si или Ge.
Другой способ описать связь в металлах — ненаправленный. То есть ближайшие соседи атома окружают его во всех направлениях, а не в нескольких конкретных направлениях (например, в углах тетраэдра, как мы обнаружили для алмаза). С другой стороны, неметаллы (изоляторы и полупроводники) имеют направленную связь. Поскольку соединение является ненаправленным, а координационные числа высокие, деформировать координационную сферу (т.е.е., разрыв или растяжение связей), чем в случае неметалла. Вот почему такие элементы, как Pb, намного более пластичны, чем C, Si или Ge.
решетчатых структур в кристаллических твердых телах — химия: первые атомы 2e
Цели обучения
К концу этого раздела вы сможете:
- Опишите расположение атомов и ионов в кристаллических структурах
- Вычислить ионные радиусы, используя размеры элементарной ячейки
- Объяснить использование измерений дифракции рентгеновских лучей для определения кристаллических структур
Более 90% твердых веществ природного и антропогенного происхождения являются кристаллическими. Большинство твердых веществ образуются с регулярным расположением своих частиц, потому что общее притягивающее взаимодействие между частицами максимизируется, а общая межмолекулярная энергия сводится к минимуму, когда частицы упаковываются наиболее эффективным образом. Регулярное расположение на атомном уровне часто отражается на макроскопическом уровне. В этом модуле мы исследуем некоторые детали структур металлических и ионных кристаллических твердых тел и узнаем, как эти структуры определяются экспериментально.
Большинство твердых веществ образуются с регулярным расположением своих частиц, потому что общее притягивающее взаимодействие между частицами максимизируется, а общая межмолекулярная энергия сводится к минимуму, когда частицы упаковываются наиболее эффективным образом. Регулярное расположение на атомном уровне часто отражается на макроскопическом уровне. В этом модуле мы исследуем некоторые детали структур металлических и ионных кристаллических твердых тел и узнаем, как эти структуры определяются экспериментально.
Структуры металлов
Мы начнем обсуждение кристаллических твердых тел с рассмотрения элементарных металлов, которые относительно просты, поскольку каждый содержит только один тип атомов. Чистый металл — это кристаллическое твердое тело, атомы которого плотно упакованы в повторяющийся узор. Некоторые свойства металлов в целом, такие как их пластичность и пластичность, во многом обусловлены наличием одинаковых атомов, расположенных в правильном порядке. Различные свойства одного металла по сравнению с другим частично зависят от размеров их атомов и особенностей их пространственного расположения.В следующих разделах мы исследуем сходства и различия четырех наиболее распространенных геометрических форм металлических кристаллов.
Различные свойства одного металла по сравнению с другим частично зависят от размеров их атомов и особенностей их пространственного расположения.В следующих разделах мы исследуем сходства и различия четырех наиболее распространенных геометрических форм металлических кристаллов.
Элементарные ячейки металлов
Структуру кристаллического твердого вещества, будь то металл или нет, лучше всего описать, рассматривая его простейшую повторяющуюся единицу, которая называется его элементарной ячейкой. Элементарная ячейка состоит из узлов решетки, которые представляют расположение атомов или ионов. Вся структура состоит из этой элементарной ячейки, повторяющейся в трех измерениях, как показано на (Рисунок).
Элементарная ячейка показывает расположение точек решетки, повторяющихся во всех направлениях.
Давайте начнем наше исследование структуры кристаллической решетки и элементарных ячеек с наиболее простой структуры и самой простой элементарной ячейки. Чтобы визуализировать это, представьте, что вы берете большое количество одинаковых сфер, таких как теннисные мячи, и равномерно размещаете их в контейнере. Самый простой способ сделать это — создать слои, в которых сферы в одном слое находятся прямо над сферами в слое ниже, как показано на (Рисунок).Такое расположение называется простой кубической структурой, а элементарная ячейка называется простой кубической элементарной ячейкой или примитивной кубической элементарной ячейкой.
Чтобы визуализировать это, представьте, что вы берете большое количество одинаковых сфер, таких как теннисные мячи, и равномерно размещаете их в контейнере. Самый простой способ сделать это — создать слои, в которых сферы в одном слое находятся прямо над сферами в слое ниже, как показано на (Рисунок).Такое расположение называется простой кубической структурой, а элементарная ячейка называется простой кубической элементарной ячейкой или примитивной кубической элементарной ячейкой.
Когда атомы металла расположены сферами в одном слое непосредственно над или под сферами в другом слое, структура решетки называется простой кубической. Обратите внимание, что сферы соприкасаются.
В простой кубической структуре сферы не упакованы так плотно, как могли бы, и они «заполняют» только около 52% объема контейнера.Это относительно неэффективное устройство, и только один металл (полоний, Po) кристаллизуется в простой кубической структуре. Как показано на (Рисунок), твердое тело с таким расположением состоит из плоскостей (или слоев), в которых каждый атом контактирует только с четырьмя ближайшими соседями в своем слое; один атом прямо над ним в верхнем слое; и один атом прямо под ним в слое ниже. Число других частиц, с которыми контактирует каждая частица в кристаллическом твердом теле, известно как ее координационное число.Следовательно, для атома полония в простом кубическом массиве координационное число равно шести.
Число других частиц, с которыми контактирует каждая частица в кристаллическом твердом теле, известно как ее координационное число.Следовательно, для атома полония в простом кубическом массиве координационное число равно шести.
Атом в структуре простой кубической решетки контактирует с шестью другими атомами, поэтому его координационное число равно шести.
В простой кубической решетке элементарная ячейка, повторяющаяся во всех направлениях, представляет собой куб, определяемый центрами восьми атомов, как показано на (Рисунок). Атомы в соседних углах этой элементарной ячейки контактируют друг с другом, поэтому длина края этой ячейки равна двум атомным радиусам или одному атомному диаметру.Кубическая элементарная ячейка содержит только те части этих атомов, которые находятся в ней. Поскольку атом в углу простой кубической элементарной ячейки состоит в общей сложности из восьми элементарных ячеек, только одна восьмая этого атома находится в конкретной элементарной ячейке.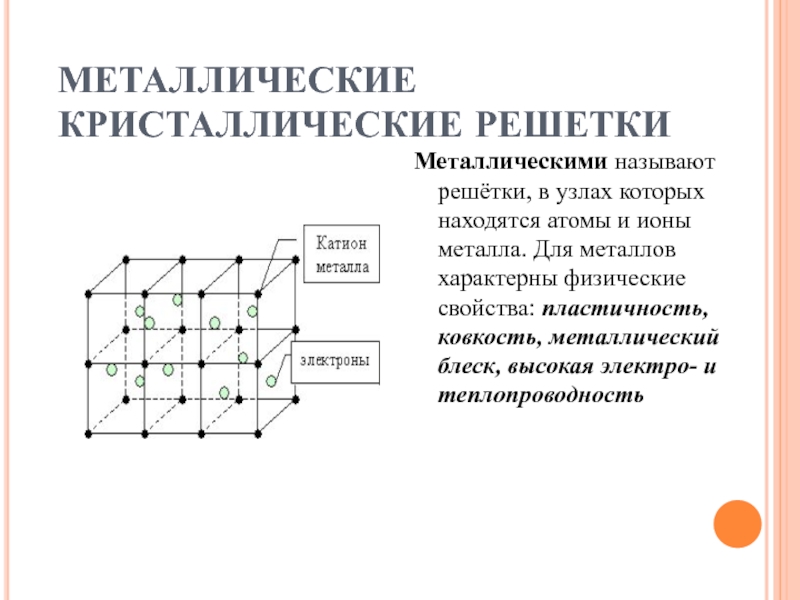 А поскольку каждая простая кубическая элементарная ячейка имеет по одному атому в каждом из восьми «углов», в одной простой кубической элементарной ячейке находится атом.
А поскольку каждая простая кубическая элементарная ячейка имеет по одному атому в каждом из восьми «углов», в одной простой кубической элементарной ячейке находится атом.
Простая элементарная ячейка кубической решетки содержит одну восьмую атома в каждом из восьми углов, так что всего она содержит один атом.
Расчет атомного радиуса и плотности металлов, часть 1 Длина ребра элементарной ячейки альфа-полония составляет 336 мкм.
(а) Определите радиус атома полония.
(b) Определите плотность альфа-полония.
Раствор Альфа-полоний кристаллизуется в простой кубической элементарной ячейке:
(a) Два соседних атома По контактируют друг с другом, поэтому длина края этой ячейки равна двум атомным радиусам По: l = 2 r .Следовательно, радиус Po равен
. (b) Плотность определяется по формуле. Плотность полония может быть определена путем определения плотности его элементарной ячейки (масса, содержащаяся в элементарной ячейке, деленная на объем элементарной ячейки). Поскольку элементарная ячейка По содержит одну восьмую атома По в каждом из восьми углов, элементарная ячейка содержит один атом По.
Поскольку элементарная ячейка По содержит одну восьмую атома По в каждом из восьми углов, элементарная ячейка содержит один атом По.
Массу элементарной ячейки По можно найти по формуле:
Объем элементарной ячейки По можно определить по:
(Обратите внимание, что длина края была преобразована из pm в см, чтобы получить обычные единицы объема для плотности.)
Следовательно, плотность
Проверьте свои знания Длина края элементарной ячейки для никеля составляет 0,3524 нм. Плотность Ni 8,90 г / см 3 . Кристаллизуется ли никель в виде простой кубической структуры? Объяснять.
Ответ:
Нет. Если бы Ni был простым кубическим, его плотность была бы выражена как:
Тогда плотность Ni была бы
. Поскольку фактическая плотность Ni не близка к этой, Ni не образует простую кубическую структуру.
Большинство металлических кристаллов являются одним из четырех основных типов элементарных ячеек.А пока мы сосредоточимся на трех кубических элементарных ячейках: простой кубической (которую мы уже видели), объемно-центрированной кубической элементарной ячейке и кубической элементарной ячейке с гранецентрированной структурой — все они проиллюстрированы на (Рисунок). (Обратите внимание, что на самом деле существует семь различных систем решеток, некоторые из которых имеют более одного типа решеток, всего 14 различных типов элементарных ячеек. Мы оставляем более сложные геометрии на потом в этом модуле.)
(Обратите внимание, что на самом деле существует семь различных систем решеток, некоторые из которых имеют более одного типа решеток, всего 14 различных типов элементарных ячеек. Мы оставляем более сложные геометрии на потом в этом модуле.)
Кубические элементарные ячейки металлов показывают (на верхних рисунках) расположение узлов решетки и (на нижних рисунках) атомов металлов, расположенных в элементарной ячейке.
Некоторые металлы кристаллизуются в виде кубической элементарной ячейки с атомами во всех углах и атомом в центре, как показано на (Рисунок). Это называется объемно-центрированным кубическим (ОЦК) твердым телом. Атомы в углах элементарной ячейки ОЦК не контактируют друг с другом, а контактируют с атомом в центре. Элементарная ячейка BCC содержит два атома: одна восьмая атома в каждом из восьми угловых атомов (атом от углов) плюс один атом от центра. Любой атом в этой структуре касается четырех атомов в слое над ним и четырех атомов в слое под ним.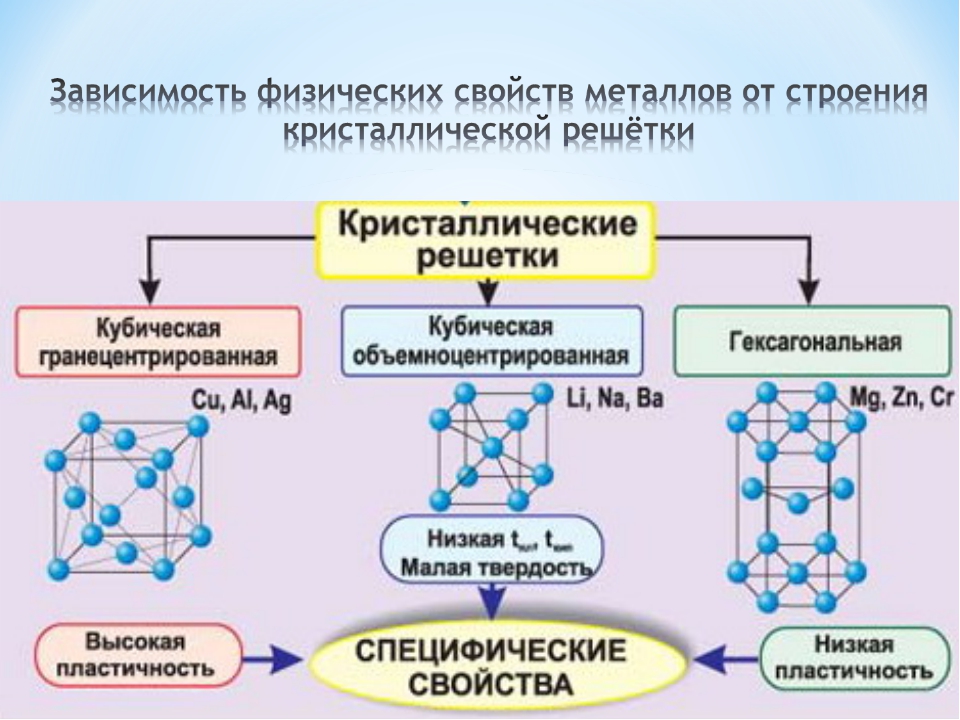 Таким образом, атом в структуре ОЦК имеет координационное число восемь.
Таким образом, атом в структуре ОЦК имеет координационное число восемь.
В объемно-центрированной кубической структуре атомы в определенном слое не касаются друг друга. Каждый атом касается четырех атомов в слое выше и четырех атомов в слое ниже.
Атомы в структурах BCC упакованы намного эффективнее, чем в простой кубической структуре, занимая около 68% от общего объема. Изоморфные металлы со структурой BCC включают K, Ba, Cr, Mo, W и Fe при комнатной температуре.(Элементы или соединения, которые кристаллизуются с одинаковой структурой, считаются изоморфными.)
Многие другие металлы, такие как алюминий, медь и свинец, кристаллизуются в структуре, которая имеет кубическую элементарную ячейку с атомами во всех углах и в центре каждой грани, как показано на (Рисунок). Такое расположение называется гранецентрированным кубическим (ГЦК) твердым телом. Элементарная ячейка FCC содержит четыре атома: одну восьмую атома в каждом из восьми угловых атомов (атом от углов) и половину атома на каждой из шести граней атомов от граней).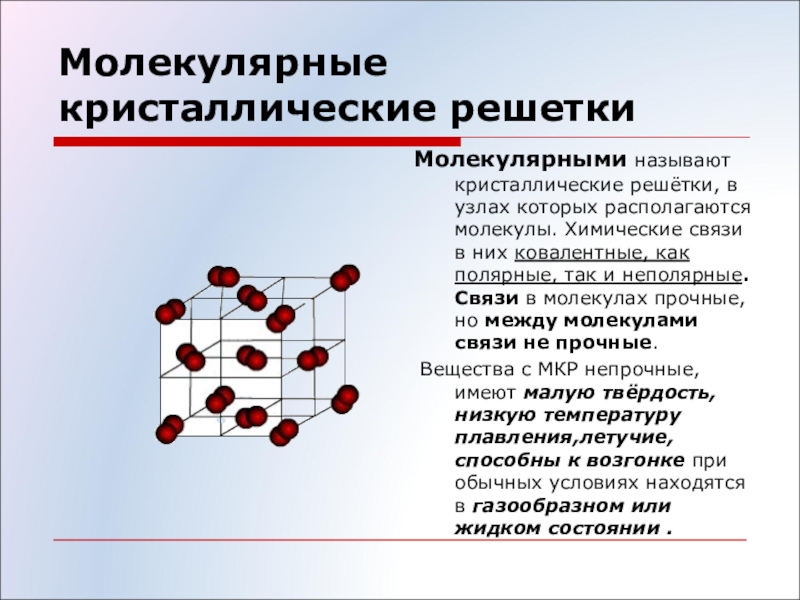 Атомы в углах касаются атомов в центрах соседних граней по диагоналям граней куба. Поскольку атомы находятся в идентичных узлах решетки, они имеют идентичное окружение.
Атомы в углах касаются атомов в центрах соседних граней по диагоналям граней куба. Поскольку атомы находятся в идентичных узлах решетки, они имеют идентичное окружение.
Гранецентрированное кубическое твердое тело имеет атомы по углам и, как следует из названия, в центрах граней его элементарных ячеек.
Атомы в конфигурации ГЦК упакованы как можно ближе друг к другу, причем атомы занимают 74% объема. Эта структура также называется кубической плотнейшей упаковкой (CCP).В CCP есть три повторяющихся слоя гексагонально расположенных атомов. Каждый атом контактирует с шестью атомами в своем собственном слое, с тремя в слое выше и с тремя в слое ниже. В этом расположении каждый атом касается 12 ближайших соседей и, следовательно, имеет координационное число 12. Тот факт, что устройства FCC и CCP эквивалентны, может быть не сразу очевиден, но почему они на самом деле имеют одинаковую структуру, показано на (Рисунок).
Компоновка CCP состоит из трех повторяющихся слоев (ABCABC…) гексагонально расположенных атомов. Атомы в структуре CCP имеют координационное число 12, потому что они контактируют с шестью атомами в своем слое, плюс три атома в слое выше и три атома в слое ниже. Поворачивая перспективу, мы видим, что структура CCP имеет элементарную ячейку с гранью, содержащей атом из слоя A в одном углу, атомы из слоя B по диагонали (в двух углах и в середине лица) и атом из слоя C в оставшемся углу. Это то же самое, что и гранецентрированное кубическое расположение.
Атомы в структуре CCP имеют координационное число 12, потому что они контактируют с шестью атомами в своем слое, плюс три атома в слое выше и три атома в слое ниже. Поворачивая перспективу, мы видим, что структура CCP имеет элементарную ячейку с гранью, содержащей атом из слоя A в одном углу, атомы из слоя B по диагонали (в двух углах и в середине лица) и атом из слоя C в оставшемся углу. Это то же самое, что и гранецентрированное кубическое расположение.
Поскольку более тесная упаковка максимизирует общее притяжение между атомами и минимизирует общую межмолекулярную энергию, атомы в большинстве металлов упаковываются таким образом. Мы находим два типа плотнейшей упаковки в простых металлических кристаллических структурах: CCP, с которой мы уже сталкивались, и гексагональная плотнейшая упаковка (HCP), показанная на (Рисунок). Оба состоят из повторяющихся слоев гексагонально расположенных атомов. В обоих типах второй слой (B) размещается на первом слое (A), так что каждый атом во втором слое контактирует с тремя атомами в первом слое. Третий слой размещается одним из двух способов. В HCP атомы в третьем слое находятся непосредственно над атомами в первом слое (т.е. третий слой также относится к типу A), а наложение состоит из чередующихся плотноупакованных слоев типа A и типа B (то есть ABABAB). В CCP атомы в третьем слое не находятся над атомами в любом из первых двух слоев (т. Е. Третий слой относится к типу C), а наложение состоит из чередующихся плотноупакованных слоев типа A, типа B и типа C ( т.е. ABCABCABC ⋯). Около двух третей всех металлов кристаллизуются в виде плотноупакованных массивов с координационным числом 12.Металлы, которые кристаллизуются в структуре HCP, включают Cd, Co, Li, Mg, Na и Zn, а металлы, которые кристаллизуются в структуре CCP, включают Ag, Al, Ca, Cu, Ni, Pb и Pt.
Третий слой размещается одним из двух способов. В HCP атомы в третьем слое находятся непосредственно над атомами в первом слое (т.е. третий слой также относится к типу A), а наложение состоит из чередующихся плотноупакованных слоев типа A и типа B (то есть ABABAB). В CCP атомы в третьем слое не находятся над атомами в любом из первых двух слоев (т. Е. Третий слой относится к типу C), а наложение состоит из чередующихся плотноупакованных слоев типа A, типа B и типа C ( т.е. ABCABCABC ⋯). Около двух третей всех металлов кристаллизуются в виде плотноупакованных массивов с координационным числом 12.Металлы, которые кристаллизуются в структуре HCP, включают Cd, Co, Li, Mg, Na и Zn, а металлы, которые кристаллизуются в структуре CCP, включают Ag, Al, Ca, Cu, Ni, Pb и Pt.
В обоих типах плотнейшей упаковки атомы упакованы максимально компактно. Гексагональная плотнейшая упаковка состоит из двух чередующихся слоев (ABABAB…). Плотнейшая кубическая упаковка состоит из трех чередующихся слоев (ABCABCABC…).
Расчет атомного радиуса и плотности металлов, часть 2 Кальций кристаллизуется в гранецентрированной кубической структуре.Длина ребра его элементарной ячейки составляет 558,8 пм.
(а) Каков атомный радиус Са в этой структуре?
(b) Рассчитайте плотность Ca.
Решение
(a) В структуре ГЦК атомы Са контактируют друг с другом по диагонали грани, поэтому длина диагонали равна четырем атомным радиусам Са (d = 4 r ). Два смежных ребра и диагональ лица образуют прямоугольный треугольник, длина каждой стороны которого равна 558.8 пм и длина гипотенузы, равная четырем атомным радиусам Ca:
Решение дает
(b) Плотность дается как Плотность кальция может быть найдена путем определения плотности его элементарной ячейки: например, масса, содержащаяся в элементарной ячейке, деленная на объем элементарной ячейки. Гранецентрированная элементарная ячейка Са имеет одну восьмую атома на каждом из восьми угловых атомов и половину атома на каждом из шести граней атомов), всего четыре атома в элементарной ячейке.
Массу элементарной ячейки можно найти по:
Объем элементарной ячейки Са можно определить по:
(Обратите внимание, что длина края была преобразована из pm в см, чтобы получить обычные единицы объема для плотности.)
Тогда плотность
Проверьте свое обучение Серебро кристаллизуется в структуре FCC. Длина ребра его элементарной ячейки 409 мкм.
(а) Каков атомный радиус Ag в этой структуре?
(b) Рассчитайте плотность Ag.
Ответ:
(а) 144 пм; (б) 10,5 г / см 3
В общем случае элементарная ячейка определяется длиной трех осей ( a , b и c ) и углами ( α , β и γ ) между ними, как проиллюстрировано на (Рисунок). Оси определяются как длины между точками пространственной решетки. Следовательно, оси элементарной ячейки соединяют точки с идентичной средой.
Элементарная ячейка определяется длиной трех ее осей ( a , b и c ) и углами ( α , β и γ ) между осями.
Существует семь различных систем решеток, некоторые из которых имеют более одного типа решетки, всего четырнадцать различных элементарных ячеек, которые имеют форму, показанную на (Рисунок).
Существует семь различных систем решеток и 14 различных элементарных ячеек.
Структуры ионных кристаллов
Ионные кристаллы состоят из двух или более различных типов ионов, которые обычно имеют разные размеры. Упаковка этих ионов в кристаллическую структуру более сложна, чем упаковка атомов металла того же размера.
Большинство одноатомных ионов ведут себя как заряженные сферы, и их притяжение для ионов противоположного заряда одинаково во всех направлениях. Следовательно, стабильные структуры для ионных соединений возникают (1), когда ионы одного заряда окружены как можно большим количеством ионов противоположного заряда, и (2) когда катионы и анионы контактируют друг с другом. Структуры определяются двумя основными факторами: относительными размерами ионов и соотношением количества положительных и отрицательных ионов в соединении.
Следовательно, стабильные структуры для ионных соединений возникают (1), когда ионы одного заряда окружены как можно большим количеством ионов противоположного заряда, и (2) когда катионы и анионы контактируют друг с другом. Структуры определяются двумя основными факторами: относительными размерами ионов и соотношением количества положительных и отрицательных ионов в соединении.
В простых ионных структурах мы обычно находим анионы, которые обычно больше, чем катионы, расположенные в виде плотноупакованного массива. (Как было замечено ранее, дополнительные электроны, притянутые к одному и тому же ядру, делают анионы крупнее, а меньшее количество электронов, притягиваемых к тому же ядру, делает катионы меньше по сравнению с атомами, из которых они образованы.) Более мелкие катионы обычно занимают один из двух типов дырок ( или пустоты), оставшиеся между анионами. Меньшее из отверстий находится между тремя анионами в одной плоскости и одним анионом в соседней плоскости.Четыре аниона, окружающие это отверстие, расположены по углам тетраэдра, поэтому отверстие называется тетраэдрическим отверстием. Дыра большего размера находится в центре шести анионов (три в одном слое и три в соседнем слое), расположенных в углах октаэдра; это называется октаэдрическим отверстием. (Рисунок) иллюстрирует оба этих типа отверстий.
Дыра большего размера находится в центре шести анионов (три в одном слое и три в соседнем слое), расположенных в углах октаэдра; это называется октаэдрическим отверстием. (Рисунок) иллюстрирует оба этих типа отверстий.
Катионы могут занимать два типа дырок между анионами: октаэдрические дырки и тетраэдрические дырки.
В зависимости от относительных размеров катионов и анионов, катионы ионного соединения могут занимать тетраэдрические или октаэдрические отверстия, как показано на (Рисунок).Относительно небольшие катионы занимают тетраэдрические отверстия, а более крупные — октаэдрические. Если катионы слишком велики, чтобы поместиться в октаэдрические отверстия, анионы могут принять более открытую структуру, такую как простой кубический массив. Тогда более крупные катионы могут занять большие кубические отверстия, что стало возможным благодаря более открытому пространству.
Размер катиона и форма отверстия, занимаемого соединением, напрямую связаны.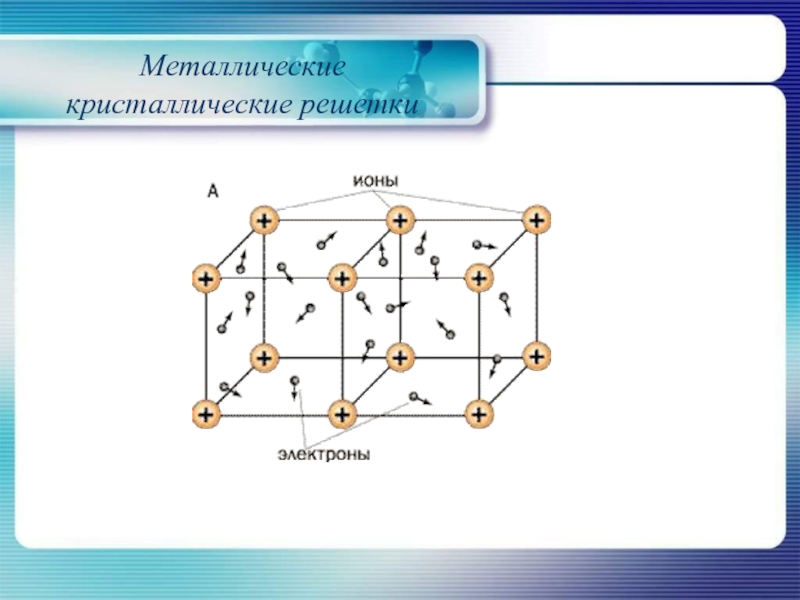
Есть две тетраэдрические дырки для каждого аниона в массиве анионов HCP или CCP.Соединение, которое кристаллизуется в виде плотноупакованного массива анионов с катионами в тетраэдрических отверстиях, может иметь максимальное соотношение катион: анион 2: 1; все тетраэдрические отверстия заполнены при этом соотношении. Примеры включают Li 2 O, Na 2 O, Li 2 S и Na 2 S. Соединения с соотношением менее 2: 1 также могут кристаллизоваться в виде плотноупакованного массива анионов с катионами. в тетраэдрических дырках, если подходят ионные размеры. Однако в этих соединениях часть тетраэдрических дырок остается вакантной.
Заполнение четырехгранных отверстий Сульфид цинка является важным промышленным источником цинка, а также используется в качестве белого пигмента в красках. Сульфид цинка кристаллизуется с ионами цинка, занимающими половину тетраэдрических дырок в плотноупакованном массиве сульфид-ионов. Какая формула сульфида цинка?
Решение Поскольку на каждый анион (сульфид-ион) приходится две тетраэдрических дырки и половина этих дырок занята ионами цинка, на каждый сульфид-ион должно приходиться или 1 ион цинка. Таким образом, формула ZnS.
Таким образом, формула ZnS.
Проверьте свои знания Селенид лития можно описать как плотнейшую упаковку ионов селенида с ионами лития во всех тетраэдрических отверстиях. Какая у него формула селенида лития?
Отношение октаэдрических дырок к анионам в структуре HCP или CCP составляет 1: 1. Таким образом, соединения с катионами в октаэдрических дырках в плотноупакованном массиве анионов могут иметь максимальное соотношение катион: анион 1: 1. Например, в NiO, MnS, NaCl и KH все октаэдрические отверстия заполнены.Отношения менее 1: 1 наблюдаются, когда некоторые из октаэдрических отверстий остаются пустыми.
Стехиометрия ионных соединений Сапфир — это оксид алюминия. Оксид алюминия кристаллизуется с ионами алюминия в двух третях октаэдрических отверстий в плотноупакованном массиве оксидных ионов. Какая формула у оксида алюминия?
Решение Поскольку на каждый анион (оксидный ион) приходится одна октаэдрическая дырка и только две трети этих дырок заняты, отношение алюминия к кислороду должно быть: 1, что дало бы простейшее целочисленное отношение 2: 3, поэтому формула Al 2 O 3 .
Проверьте свои знания Белый пигмент оксида титана кристаллизуется с ионами титана в половине октаэдрических отверстий в плотноупакованном массиве оксидных ионов. Какая формула оксида титана?
В простом кубическом массиве анионов есть одно кубическое отверстие, которое может быть занято катионом для каждого аниона в массиве. В CsCl и других соединениях с такой же структурой все кубические дырки заняты. Половина кубических дырок занята в SrH 2 , UO 2 , SrCl 2 и CaF 2 .
Различные типы ионных соединений часто кристаллизуются в одной и той же структуре, если относительные размеры их ионов и их стехиометрия (две основные характеристики, определяющие структуру) схожи.
Элементарные ячейки ионных соединений
Многие ионные соединения кристаллизуются с кубическими элементарными ячейками, и мы будем использовать эти соединения, чтобы описать общие особенности ионных структур.
Когда ионное соединение состоит из катионов и анионов одинакового размера в соотношении 1: 1, оно обычно образует простую кубическую структуру.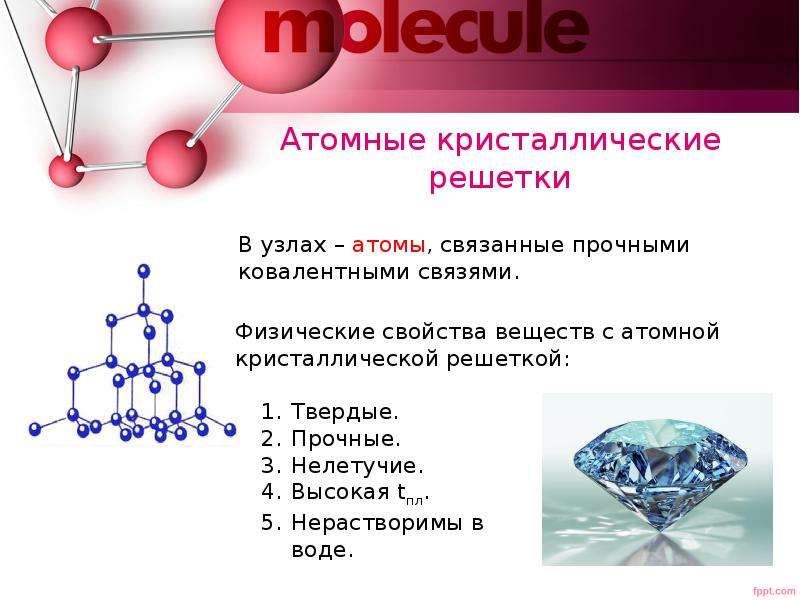 Примером этого является хлорид цезия, CsCl (проиллюстрирован на (Рисунок)), причем Cs + и Cl — имеют радиусы 174 и 181 мкм соответственно. Мы можем представить это как ионы хлорида, образующие простую кубическую элементарную ячейку с ионом цезия в центре; или в виде ионов цезия, образующих элементарную ячейку с ионом хлорида в центре; или как простые кубические элементарные ячейки, образованные ионами Cs + , перекрывающими элементарные ячейки, образованные ионами Cl — . Ионы цезия и ионы хлора соприкасаются по диагоналям тела элементарных ячеек.Один ион цезия и один ион хлорида присутствуют в элементарной ячейке, что дает стехиометрию 1: 1, требуемую формулой для хлорида цезия. Обратите внимание, что в центре ячейки нет точки решетки, и CsCl не является структурой BCC, потому что ион цезия не идентичен иону хлорида.
Примером этого является хлорид цезия, CsCl (проиллюстрирован на (Рисунок)), причем Cs + и Cl — имеют радиусы 174 и 181 мкм соответственно. Мы можем представить это как ионы хлорида, образующие простую кубическую элементарную ячейку с ионом цезия в центре; или в виде ионов цезия, образующих элементарную ячейку с ионом хлорида в центре; или как простые кубические элементарные ячейки, образованные ионами Cs + , перекрывающими элементарные ячейки, образованные ионами Cl — . Ионы цезия и ионы хлора соприкасаются по диагоналям тела элементарных ячеек.Один ион цезия и один ион хлорида присутствуют в элементарной ячейке, что дает стехиометрию 1: 1, требуемую формулой для хлорида цезия. Обратите внимание, что в центре ячейки нет точки решетки, и CsCl не является структурой BCC, потому что ион цезия не идентичен иону хлорида.
Ионные соединения с катионами и анионами аналогичного размера, такие как CsCl, обычно образуют простую кубическую структуру. Их можно описать элементарными ячейками с катионами по углам или анионами по углам.
Их можно описать элементарными ячейками с катионами по углам или анионами по углам.
Мы сказали, что расположение точек решетки произвольно. Это иллюстрируется альтернативным описанием структуры CsCl, в которой узлы решетки расположены в центрах ионов цезия. В этом описании ионы цезия расположены в точках решетки в углах ячейки, а ион хлорида расположен в центре ячейки. Две элементарные ячейки разные, но они описывают идентичные структуры.
Когда ионное соединение состоит из катионов и анионов в соотношении 1: 1, которые значительно различаются по размеру, оно обычно кристаллизуется с помощью элементарной ячейки FCC, как показано на (Рисунок).Примером этого является хлорид натрия, NaCl, причем Na + и Cl — имеют радиусы 102 и 181 мкм соответственно. Мы можем представить это как ионы хлора, образующие ячейку FCC, причем ионы натрия расположены в октаэдрических отверстиях в середине краев ячейки и в центре ячейки. Ионы натрия и хлора соприкасаются друг с другом по краям ячейки. Элементарная ячейка содержит четыре иона натрия и четыре иона хлорида, что дает стехиометрию 1: 1, требуемую формулой NaCl.
Элементарная ячейка содержит четыре иона натрия и четыре иона хлорида, что дает стехиометрию 1: 1, требуемую формулой NaCl.
Ионные соединения с анионами, размер которых намного превышает размер катионов, например NaCl, обычно образуют структуру ГЦК. Их можно описать элементарными ячейками ГЦК с катионами в октаэдрических дырках.
Кубическая форма сульфида цинка, цинковая обманка, также кристаллизуется в элементарной ячейке FCC, как показано на (Рисунок). Эта структура содержит сульфид-ионы в узлах решетки ГЦК-решетки. (Расположение сульфид-ионов идентично расположению хлорид-ионов в хлориде натрия.) Радиус иона цинка составляет всего около 40% от радиуса сульфид-иона, поэтому эти маленькие ионы Zn 2+ расположены в чередующихся тетраэдрических дырках, то есть в одной половине тетраэдрических дырок. В элементарной ячейке четыре иона цинка и четыре иона сульфида, что дает эмпирическую формулу ZnS.
ZnS, сульфид цинка (или цинковая обманка) образует элементарную ячейку FCC с ионами сульфида в узлах решетки и гораздо меньшими ионами цинка, занимающими половину тетраэдрических отверстий в структуре.
Элементарная ячейка с фторидом кальция, подобная той, что показана на (Рисунок), также является элементарной ячейкой FCC, но в этом случае катионы расположены в точках решетки; эквивалентные ионы кальция расположены в узлах решетки ГЦК-решетки. Все тетраэдрические позиции в массиве ГЦК ионов кальция заняты ионами фтора. В элементарной ячейке четыре иона кальция и восемь ионов фтора, что дает соотношение кальций: фтор 1: 2 в соответствии с химической формулой CaF 2 .Внимательное изучение (Рисунок) покажет простой кубический массив ионов фтора с ионами кальция в одной половине кубических дырок. Структуру нельзя описать в терминах пространственной решетки точек на фторид-ионах, потому что не все фторид-ионы имеют одинаковое окружение. Ориентация четырех ионов кальция относительно ионов фтора различается.
Фторид кальция, CaF 2 , образует элементарную ячейку ГЦК с ионами кальция (зеленый) в узлах решетки и ионами фтора (красный), занимающими все тетраэдрические узлы между ними.
Расчет ионных радиусов
Если мы знаем длину края элементарной ячейки ионного соединения и положение ионов в ячейке, мы можем вычислить ионные радиусы для ионов в соединении, если мы сделаем предположения об индивидуальных ионных формах и контактах.
Расчет ионных радиусов Длина края элементарной ячейки LiCl (NaCl-подобная структура, FCC) составляет 0,514 нм или 5,14 Å. Предполагая, что ион лития достаточно мал, чтобы ионы хлора контактировали, как показано на (Рисунок), рассчитайте ионный радиус для иона хлорида.
Примечание. Единица измерения длины, ангстрема, Å, часто используется для представления размеров в атомном масштабе и эквивалентна 10 −10 м.
Решение На лицевой стороне элементарной ячейки LiCl ионы хлора контактируют друг с другом по диагонали грани:
Рисуя прямоугольный треугольник на лицевой стороне элементарной ячейки, мы видим, что длина диагонали равна четырем радиусам хлорида (один радиус от каждого углового хлорида и один диаметр, равный двум радиусам, от иона хлорида в центре). грани), поэтому d = 4 r .Из теоремы Пифагора имеем:
грани), поэтому d = 4 r .Из теоремы Пифагора имеем:
, что дает:
Решение этого дает:
Проверьте свои знания Длина края элементарной ячейки KCl (NaCl-подобная структура, FCC) составляет 6,28 Å. Предполагая, что анион-катионный контакт проходит по краю ячейки, рассчитайте радиус иона калия. Радиус иона хлорида составляет 1,82 Å.
Ответ:
Радиус иона калия 1,33 Å.
Важно понимать, что значения ионных радиусов, рассчитанные на основе длин краев элементарных ячеек, зависят от множества допущений, таких как идеальная сферическая форма для ионов, которые в лучшем случае являются приблизительными.Следовательно, такие расчетные значения сами по себе являются приблизительными, и сравнения нельзя зайти слишком далеко. Тем не менее, этот метод оказался полезным для расчета ионных радиусов на основе экспериментальных измерений, таких как рентгеновские кристаллографические определения.
Рентгеновская кристаллография
Размер элементарной ячейки и расположение атомов в кристалле могут быть определены из измерений дифракции рентгеновских лучей на кристалле, называемых рентгеновской кристаллографией. Дифракция — это изменение направления движения электромагнитной волны, когда она встречает физический барьер, размеры которого сопоставимы с размерами длины волны света.Рентгеновские лучи — это электромагнитное излучение с длиной волны, равной расстоянию между соседними атомами в кристаллах (порядка нескольких Å).
Когда пучок монохроматических рентгеновских лучей попадает на кристалл, его лучи рассеиваются во всех направлениях атомами внутри кристалла. Когда рассеянные волны, распространяющиеся в одном направлении, сталкиваются друг с другом, они претерпевают интерференцию , процесс, посредством которого волны объединяются, приводя к увеличению или уменьшению амплитуды (интенсивности) в зависимости от степени, в которой максимумы объединяющихся волн находятся разделены (см.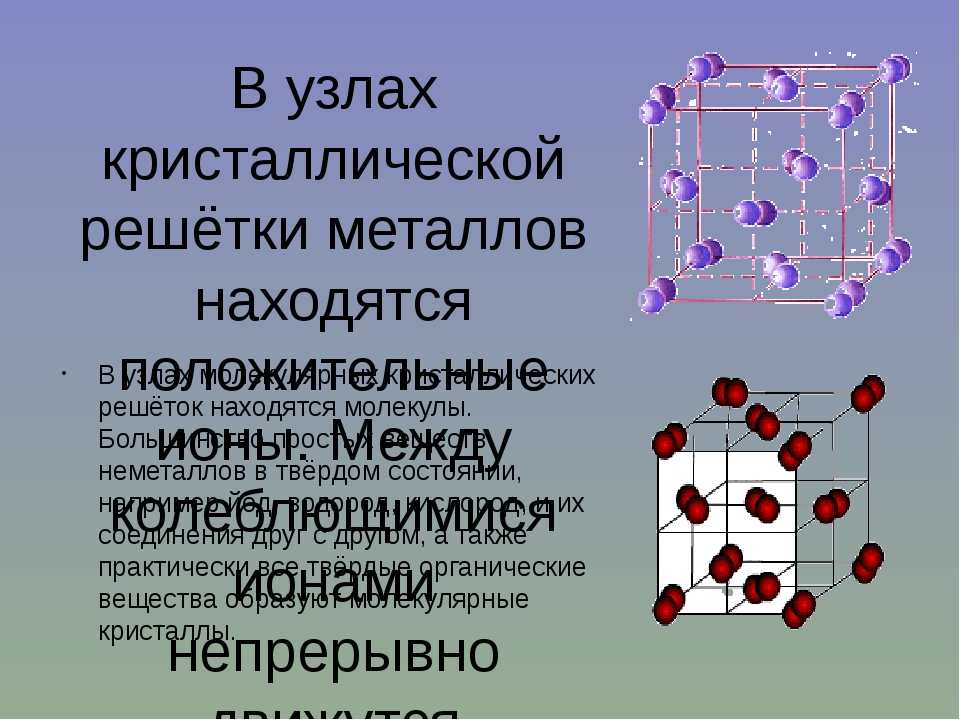 (рисунок)).
(рисунок)).
Световые волны, занимающие одно и то же пространство, испытывают интерференцию, объединяясь, давая волны большей (а) или меньшей (б) интенсивности, в зависимости от разделения их максимумов и минимумов.
Когда рентгеновские лучи определенной длины волны, λ , рассеиваются атомами в соседних плоскостях кристалла, разделенных расстоянием, d , они могут претерпевать конструктивную интерференцию, когда разница между расстояниями, пройденными двумя волнами до их комбинация представляет собой целочисленный множитель длины волны n .Это условие выполняется, когда угол дифрагированного луча, θ , связан с длиной волны и межатомным расстоянием уравнением:
Это соотношение известно как уравнение Брэгга в честь У. Х. Брэгга, английского физика, который первым объяснил это явление. (Рисунок) иллюстрирует два примера дифрагированных волн от одних и тех же двух кристаллических плоскостей.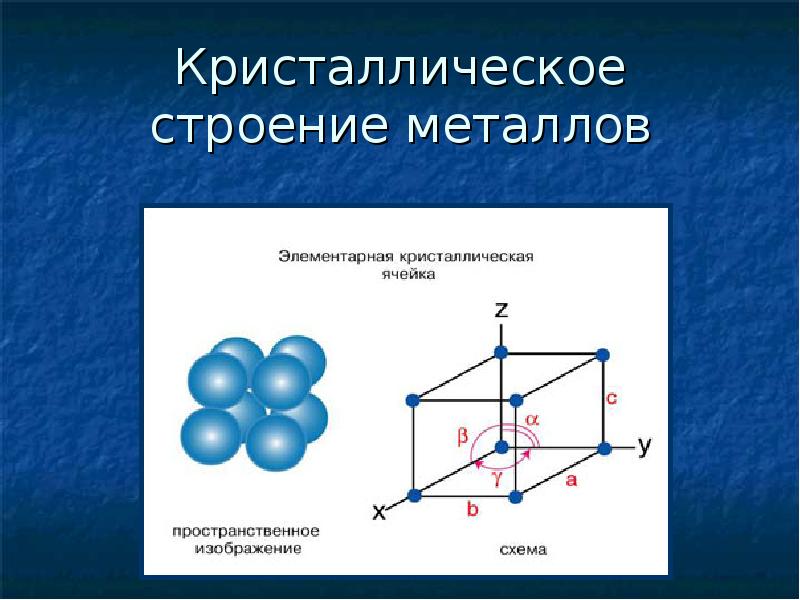 На рисунке слева изображены волны, дифрагированные под углом Брэгга, приводящие к конструктивной интерференции, а на рисунке справа показаны дифракция и другой угол, который не удовлетворяет условию Брэгга, что приводит к деструктивной интерференции.
На рисунке слева изображены волны, дифрагированные под углом Брэгга, приводящие к конструктивной интерференции, а на рисунке справа показаны дифракция и другой угол, который не удовлетворяет условию Брэгга, что приводит к деструктивной интерференции.
Дифракция рентгеновских лучей, рассеянных атомами внутри кристалла, позволяет определить расстояние между атомами. Верхнее изображение показывает конструктивную интерференцию между двумя рассеянными волнами и результирующей дифрагированной волной высокой интенсивности. На нижнем изображении показаны деструктивная интерференция и дифрагированная волна низкой интенсивности.
Посетите этот сайт для получения дополнительных сведений об уравнении Брэгга и симуляторе, который позволяет исследовать влияние каждой переменной на интенсивность дифрагированной волны.
Рентгеновский дифрактометр, такой как изображенный на (Рисунок), можно использовать для измерения углов, под которыми рентгеновские лучи дифрагируют при взаимодействии с кристаллом, как описано ранее. Из таких измерений можно использовать уравнение Брэгга для вычисления расстояний между атомами, как показано в следующем примере упражнения.
Из таких измерений можно использовать уравнение Брэгга для вычисления расстояний между атомами, как показано в следующем примере упражнения.
(a) В дифрактометре луч рентгеновских лучей попадает на кристаллический материал, создавая (b) картину дифракции рентгеновских лучей, которая может быть проанализирована для определения кристаллической структуры.
Использование уравнения Брэгга В дифрактометре рентгеновские лучи с длиной волны 0,1315 нм использовались для создания дифракционной картины для меди. Дифракция первого порядка ( n = 1) произошла под углом θ = 25,25 °. Определите расстояние между дифрагирующими плоскостями в меди.
Решение Расстояние между плоскостями находится путем решения уравнения Брэгга, nλ = 2 d sin θ для d .
Это дает:
Проверьте свои знания Кристалл с расстоянием между плоскостями, равным 0,394 нм, дифрагирует рентгеновские лучи с длиной волны 0,147 нм. Каков угол дифракции первого порядка?
Каков угол дифракции первого порядка?
Рентгеновский кристаллограф Розалинд Франклин
Открытие структуры ДНК в 1953 году Фрэнсисом Криком и Джеймсом Уотсоном — одно из величайших достижений в истории науки. Они были удостоены Нобелевской премии по физиологии и медицине 1962 года вместе с Морисом Уилкинсом, предоставившим экспериментальное доказательство структуры ДНК.Британский химик Розалинд Франклин внесла неоценимый вклад в это грандиозное достижение своей работой по измерению рентгеновских дифракционных изображений ДНК. В начале своей карьеры исследования Франклин структуры углей оказались полезными для британских военных действий. Сосредоточив свое внимание на биологических системах в начале 1950-х годов, Франклин и докторант Раймонд Гослинг обнаружили, что ДНК состоит из двух форм: длинного тонкого волокна, образующегося при намокании (тип «B»), и короткого широкого волокна, образующегося при сушке ( наберите «А»).Ее рентгеновские дифракционные изображения ДНК ((Рисунок)) предоставили важную информацию, которая позволила Уотсону и Крику подтвердить, что ДНК образует двойную спираль, и определить детали ее размера и структуры. Франклин также провел новаторское исследование вирусов и РНК, содержащей их генетическую информацию, обнаружив новую информацию, которая радикально изменила совокупность знаний в этой области. После развития рака яичников Франклин продолжала работать до своей смерти в 1958 году в возрасте 37 лет. Среди множества посмертных признаний ее работы, Чикагская медицинская школа Финчского университета медицинских наук изменила свое название на Университет медицины и науки Розалинды Франклин в 2004 году. и приняла изображение ее знаменитого рентгеновского дифракционного изображения ДНК в качестве официального логотипа университета.
Франклин также провел новаторское исследование вирусов и РНК, содержащей их генетическую информацию, обнаружив новую информацию, которая радикально изменила совокупность знаний в этой области. После развития рака яичников Франклин продолжала работать до своей смерти в 1958 году в возрасте 37 лет. Среди множества посмертных признаний ее работы, Чикагская медицинская школа Финчского университета медицинских наук изменила свое название на Университет медицины и науки Розалинды Франклин в 2004 году. и приняла изображение ее знаменитого рентгеновского дифракционного изображения ДНК в качестве официального логотипа университета.
На этой иллюстрации показано изображение дифракции рентгеновских лучей, подобное тому, которое Франклин нашла в своем исследовании. (кредит: Национальный институт здоровья)
Ключевые концепции и резюме
Структуры кристаллических металлов и простых ионных соединений можно описать в терминах упаковки сфер. Атомы металла могут упаковываться в гексагональные структуры с плотнейшей упаковкой, кубические структуры с плотнейшей упаковкой, объемно-центрированные структуры и простые кубические структуры. Анионы в простых ионных структурах обычно принимают одну из этих структур, а катионы занимают пространства, оставшиеся между анионами.Маленькие катионы обычно занимают тетраэдрические дырки в плотноупакованном массиве анионов. Катионы большего размера обычно занимают октаэдрические отверстия. Катионы еще большего размера могут занимать кубические дырки в простом кубическом массиве анионов. Структуру твердого тела можно описать, указав размер и форму элементарной ячейки и ее содержимое. Тип структуры и размеры элементарной ячейки могут быть определены путем измерения дифракции рентгеновских лучей.
Анионы в простых ионных структурах обычно принимают одну из этих структур, а катионы занимают пространства, оставшиеся между анионами.Маленькие катионы обычно занимают тетраэдрические дырки в плотноупакованном массиве анионов. Катионы большего размера обычно занимают октаэдрические отверстия. Катионы еще большего размера могут занимать кубические дырки в простом кубическом массиве анионов. Структуру твердого тела можно описать, указав размер и форму элементарной ячейки и ее содержимое. Тип структуры и размеры элементарной ячейки могут быть определены путем измерения дифракции рентгеновских лучей.
Ключевые уравнения
Химия: упражнения в конце главы
Опишите кристаллическую структуру железа, которое кристаллизуется с двумя эквивалентными атомами металла в кубической элементарной ячейке.
Структура этой низкотемпературной формы железа (ниже 910 ° C) является объемно-центрированной кубической.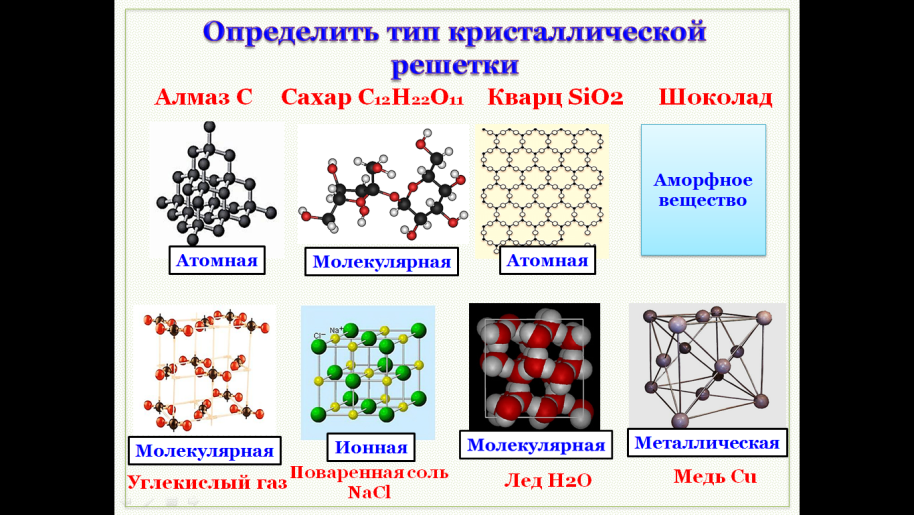 В каждом из восьми углов куба находится по одной восьмой атома, а в центре куба — по одному атому.
В каждом из восьми углов куба находится по одной восьмой атома, а в центре куба — по одному атому.
Опишите кристаллическую структуру Pt, которая кристаллизуется с четырьмя эквивалентными атомами металла в кубической элементарной ячейке.
Какое координационное число атома хрома в объемноцентрированной кубической структуре хрома?
Каково координационное число атома алюминия в гранецентрированной кубической структуре алюминия?
Металлический кобальт кристаллизуется в гексагональной плотноупакованной структуре.Какое координационное число атома кобальта?
Металлический никель кристаллизуется в кубической плотноупакованной структуре. Какое координационное число атома никеля?
Вольфрам кристаллизуется в объемно-центрированной кубической элементарной ячейке с длиной ребра 3,165 Å.
(а) Каков атомный радиус вольфрама в этой структуре?
(б) Рассчитайте плотность вольфрама.
(а) 1,370 Å; (б) 19,26 г / см
Платина (атомный радиус = 1. 38 Å) кристаллизуется в кубическую плотноупакованную структуру. Рассчитайте длину кромки гранецентрированной кубической элементарной ячейки и плотность платины.
38 Å) кристаллизуется в кубическую плотноупакованную структуру. Рассчитайте длину кромки гранецентрированной кубической элементарной ячейки и плотность платины.
Барий кристаллизуется в объемноцентрированной кубической элементарной ячейке с длиной ребра 5,025 Å
(а) Каков атомный радиус бария в этой структуре?
(б) Рассчитайте плотность бария.
(а) 2,176 Å; (б) 3,595 г / см 3
Алюминий (атомный радиус 1,43 Å) кристаллизуется в кубической плотноупакованной структуре.Рассчитайте длину ребра гранецентрированной кубической элементарной ячейки и плотность алюминия.
Плотность алюминия 2,7 г / см 3 ; кремния 2,3 г / см 3 . Объясните, почему Si имеет более низкую плотность, хотя в нем более тяжелые атомы.
Кристаллическая структура Si показывает, что он менее плотно упакован (координационное число 4) в твердом теле, чем Al (координационное число 12).
Свободное пространство в металле может быть найдено путем вычитания объема атомов в элементарной ячейке из объема ячейки. Вычислите процент свободного пространства в каждой из трех кубических решеток, если все атомы в каждой имеют одинаковый размер и касаются своих ближайших соседей. Какая из этих структур представляет собой наиболее эффективную упаковку? То есть в каких упаковках меньше всего неиспользуемого места?
Вычислите процент свободного пространства в каждой из трех кубических решеток, если все атомы в каждой имеют одинаковый размер и касаются своих ближайших соседей. Какая из этих структур представляет собой наиболее эффективную упаковку? То есть в каких упаковках меньше всего неиспользуемого места?
Сульфид кадмия, иногда используемый художниками в качестве желтого пигмента, кристаллизуется с кадмием, занимая половину тетраэдрических отверстий в плотно упакованном массиве сульфид-ионов. Какая формула сульфида кадмия? Поясните свой ответ.
В массиве с плотнейшей упаковкой для каждого аниона существуют две тетраэдрические дырки. Если занята только половина тетраэдрических дырок, количество анионов и катионов равно. Формула сульфида кадмия — CdS.
Соединение кадмия, олова и фосфора используется в производстве некоторых полупроводников. Он кристаллизуется с кадмием, занимающим одну четверть тетраэдрических дырок, и оловом, занимающим одну четверть тетраэдрических дырок в плотно упакованном массиве фосфид-ионов. Какая формула соединения? Поясните свой ответ.
Какая формула соединения? Поясните свой ответ.
Какова формула магнитного оксида кобальта, используемого в записывающих лентах, который кристаллизуется с атомами кобальта, занимающими одну восьмую тетраэдрических дырок и половину октаэдрических дырок в плотно упакованном массиве оксидных ионов?
Соединение, содержащее цинк, алюминий и серу, кристаллизуется с плотнейшей упаковкой сульфид-ионов. Ионы цинка находятся в одной восьмой тетраэдрических дырок, а ионы алюминия — в половине октаэдрических дырок.Какова эмпирическая формула соединения?
Соединение таллия и йода кристаллизуется в виде простого кубического массива иодид-ионов с ионами таллия во всех кубических дырках. Какая формула этого йодида? Поясните свой ответ.
В простом кубическом массиве только одно кубическое отверстие может быть занято катионом для каждого аниона в массиве. Соотношение таллия и йодида должно быть 1: 1; следовательно, формула таллия — TlI.
Какой из следующих элементов реагирует с серой с образованием твердого тела, в котором атомы серы образуют плотноупакованный массив со всеми занятыми октаэдрическими отверстиями: Li, Na, Be, Ca или Al?
Каков массовый процент титана в рутиле, минерале, который содержит титан и кислород, если структуру можно описать как плотнейшую упаковку оксидных ионов с ионами титана в половине октаэдрических отверстий? Какова степень окисления титана?
59. 95%; Степень окисления титана +4.
95%; Степень окисления титана +4.
Объясните, почему химически похожие хлориды щелочных металлов NaCl и CsCl имеют разную структуру, тогда как химически разные NaCl и MnS имеют одинаковую структуру.
Поскольку минералы образовались из расплавленной магмы, разные ионы занимали одни и те же участки в кристаллах. Литий часто встречается вместе с магнием в минералах, несмотря на разницу в заряде их ионов. Предложите объяснение.
Оба иона близки по размеру: Mg, 0.65; Ли 0,60. Это сходство позволяет им довольно легко обмениваться друг с другом. Разница в заряде обычно компенсируется переключателем Si 4+ на Al 3+ .
Иодид рубидия кристаллизуется с кубической элементарной ячейкой, содержащей иодид-ионы по углам и ион рубидия в центре. Какая формула соединения?
Один из различных оксидов марганца кристаллизуется с кубической элементарной ячейкой, содержащей ионы марганца по углам и в центре.Ионы оксида расположены в центре каждого края элементарной ячейки. Какая формула соединения?
Какая формула соединения?
NaH кристаллизуется с той же кристаллической структурой, что и NaCl. Длина ребра кубической элементарной ячейки NaH составляет 4,880 Å.
(a) Рассчитайте ионный радиус H — . (Ионный радиус Li + составляет 0,0,95 Å.)
(б) Рассчитайте плотность NaH.
Иодид таллия (I) кристаллизуется с той же структурой, что и CsCl. Длина ребра элементарной ячейки TlI равна 4.20 Å. Вычислите ионный радиус TI + . (Ионный радиус I — составляет 2,16 Å.)
Кубическая элементарная ячейка содержит ионы марганца по углам и ионы фтора в центре каждого края.
(а) Какова эмпирическая формула этого соединения? Поясните свой ответ.
(б) Каково координационное число иона Mn 3+ ?
(c) Рассчитайте длину края элементарной ячейки, если радиус иона Mn 3+ равен 0.65 А.
(d) Рассчитайте плотность соединения.
Каково расстояние между плоскостями кристалла, которые дифрагируют рентгеновские лучи с длиной волны 1,541 нм под углом θ 15,55 ° (отражение первого порядка)?
Дифрактометр, использующий рентгеновские лучи с длиной волны 0,2287 нм, дает пик дифракции первого порядка для угла кристалла θ = 16,21 °. Определите расстояние между дифрагирующими плоскостями в этом кристалле.
Определите расстояние между дифрагирующими плоскостями в этом кристалле.
Металл с расстоянием между плоскостями 0.4164 нм дифрагирует рентгеновские лучи с длиной волны 0,2879 нм. Каков угол дифракции для дифракционного пика первого порядка?
Золото кристаллизуется в кубической гранецентрированной элементарной ячейке. Отражение второго порядка (n = 2) рентгеновских лучей для плоскостей, составляющих вершину и основание элементарных ячеек, находится при θ = 22,20 °. Длина волны рентгеновского излучения составляет 1,54 Å. Какова плотность металлического золота?
Когда электрон в возбужденном атоме молибдена падает с L на K-оболочку, испускается рентгеновское излучение.Эти рентгеновские лучи дифрагируют под углом 7,75 ° на плоскостях с разделением 2,64 Å. Какова разница в энергии между оболочкой K и оболочкой L в молибдене в предположении дифракции первого порядка?
1,74 10 4 эВ
Глоссарий
- объемно-центрированная кубическая (ОЦК) твердое тело
- кристаллическая структура, которая имеет кубическую элементарную ячейку с точками решетки по углам и в центре ячейки
- объемно-центрированная кубическая элементарная ячейка
- простейший повторяющийся элемент объемно-центрированного кубического кристалла; это куб, содержащий точки решетки в каждом углу и в центре куба
- Уравнение Брэгга
- Уравнение, связывающее углы, под которыми рентгеновские лучи дифрагируют атомами внутри кристалла
- координационный номер
- Число атомов, ближайших к любому данному атому в кристалле или к центральному атому металла в комплексе
- плотнейшая кубическая упаковка (ПГУ)
- кристаллическая структура, в которой плоскости плотно упакованных атомов или ионов уложены в виде серии из трех чередующихся слоев с различной относительной ориентацией (ABC)
- дифракция
- Перенаправление электромагнитного излучения, возникающее при встрече с физическим барьером соответствующих размеров
- гранецентрированная кубическая (FCC) сплошная
- Кристаллическая структура, состоящая из кубической элементарной ячейки с точками решетки по углам и в центре каждой грани
- гранецентрированная кубическая элементарная ячейка
- простейший повторяющийся элемент гранецентрированного кубического кристалла; это куб, содержащий точки решетки в каждом углу и в центре каждой грани
- Гексагональная плотная упаковка (HCP)
- Кристаллическая структура, в которой плотно упакованные слои атомов или ионов уложены в виде серии из двух чередующихся слоев с разной относительной ориентацией (AB)
- отверстие
- (также междоузлия) пространство между атомами внутри кристалла
- изоморфный
- с такой же кристаллической структурой
- октаэдрическое отверстие
- открытое пространство в кристалле в центре из шести частиц, расположенных по углам октаэдра
- простая кубическая элементарная ячейка
- (также примитивная кубическая элементарная ячейка) элементарная ячейка в простой кубической структуре
- простая кубическая структура
- Кристаллическая структура с кубической элементарной ячейкой с узлами решетки только по углам
- пространственная решетка
- все точки в кристалле, которые имеют идентичное окружение
- четырехгранное отверстие
- тетраэдрическое пространство, образованное четырьмя атомами или ионами в кристалле
- элементарная ячейка
- Наименьшая часть пространственной решетки, которая повторяется в трех измерениях, образуя всю решетку
- Рентгеновская кристаллография
- Экспериментальный метод определения расстояний между атомами в кристалле путем измерения углов, под которыми рентгеновские лучи дифрагируют при прохождении через кристалл
Кристаллические структуры и элементарная ячейка — Видео и стенограмма урока
Типы кристаллов
Кристаллы часто делятся на четыре категории в зависимости от типов частиц и связи между частицами.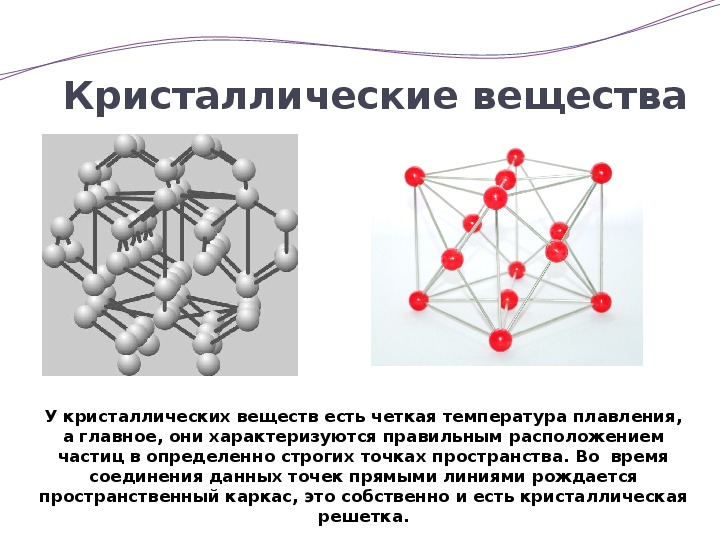 К четырем типам относятся ионные кристаллы, кристаллы ковалентной сетки, металлические кристаллы и ковалентные молекулярные кристаллы.
К четырем типам относятся ионные кристаллы, кристаллы ковалентной сетки, металлические кристаллы и ковалентные молекулярные кристаллы.
Ионные кристаллы состоят как из положительных, так и из отрицательных ионов, которые расположены в регулярном повторяющемся узоре. Сильная ионная связь между ионами в кристалле делает его очень твердым и хрупким. Ионные кристаллы имеют высокие температуры плавления и являются хорошими проводниками электричества.Соль представляет собой твердое ионное кристаллическое вещество.
Кристаллы с ковалентной сеткой , иногда называемые твердыми атомами, имеют атомы, которые ковалентно связаны с атомом рядом с ними, что означает, что два атома имеют общие электроны. Алмаз представляет собой кристалл с ковалентной сеткой, потому что атомы углерода в алмазе ковалентно связаны с другими атомами углерода. Эти типы кристаллов твердые и хрупкие, имеют высокие температуры плавления и обычно не проводят электричество.
Эти типы кристаллов твердые и хрупкие, имеют высокие температуры плавления и обычно не проводят электричество.
Металлические кристаллы состоят из катионов металлов, окруженных свободно движущимися валентными электронами.Электроны исходят от атомов металлов и принадлежат кристаллу в целом. Эти кристаллы являются хорошими проводниками электричества, потому что электроны в кристаллической структуре очень подвижны.
Ковалентный молекулярный кристалл , также иногда называемый молекулярным твердым телом, состоит из ковалентно связанных молекул, которые удерживаются вместе межмолекулярными силами, такими как силы дисперсии Лондона, диполь-дипольные силы и водородная связь.Этот тип кристаллов мягкий, имеет низкую температуру плавления и является хорошим изолятором. Кристаллы льда — это ковалентные молекулярные кристаллы.
Краткое содержание урока
Кристаллические вещества состоят из повторяющейся трехмерной структуры, образованной меньшими идентичными единицами. Общее трехмерное расположение частиц кристалла называется кристаллической структурой . Фактическое расположение частиц в кристалле представляет собой решетку . Самая маленькая часть кристалла, которая имеет трехмерный узор всей решетки, называется элементарной ячейкой .Существует четыре различных типа кристаллов, включая ионные кристаллы, кристаллы с ковалентной сеткой, металлические кристаллы и ковалентные молекулярные кристаллы.
Результаты обучения
По завершении этого урока вы, возможно, сможете:
- Подробно рассказать о структурном составе кристаллических веществ: кристаллическая структура, решетка и элементарная ячейка
- Обсудите, из чего состоят твердые кристаллические тела и как определяется их форма
- Опишите характеристики и приведите примеры четырех типов кристаллов: ионные, ковалентные сетчатые, металлические и ковалентные молекулярные кристаллы
Решетчатые структуры в кристаллических твердых телах — химия
Более 90% природных и искусственных твердых тел являются кристаллическими. Большинство твердых веществ образуются с регулярным расположением своих частиц, потому что общее притягивающее взаимодействие между частицами максимизируется, а общая межмолекулярная энергия сводится к минимуму, когда частицы упаковываются наиболее эффективным образом. Регулярное расположение на атомном уровне часто отражается на макроскопическом уровне. В этом модуле мы исследуем некоторые детали структур металлических и ионных кристаллических твердых тел и узнаем, как эти структуры определяются экспериментально.
Большинство твердых веществ образуются с регулярным расположением своих частиц, потому что общее притягивающее взаимодействие между частицами максимизируется, а общая межмолекулярная энергия сводится к минимуму, когда частицы упаковываются наиболее эффективным образом. Регулярное расположение на атомном уровне часто отражается на макроскопическом уровне. В этом модуле мы исследуем некоторые детали структур металлических и ионных кристаллических твердых тел и узнаем, как эти структуры определяются экспериментально.
Мы начнем обсуждение кристаллических твердых тел с рассмотрения элементарных металлов, которые относительно просты, поскольку каждый содержит только один тип атомов. Чистый металл — это кристаллическое твердое тело, атомы которого плотно упакованы в повторяющийся узор. Некоторые свойства металлов в целом, такие как их пластичность и пластичность, во многом обусловлены наличием одинаковых атомов, расположенных в правильном порядке. Различные свойства одного металла по сравнению с другим частично зависят от размеров их атомов и особенностей их пространственного расположения. В следующих разделах мы исследуем сходства и различия четырех наиболее распространенных геометрических форм металлических кристаллов.
В следующих разделах мы исследуем сходства и различия четырех наиболее распространенных геометрических форм металлических кристаллов.
Структуру кристаллического твердого вещества, будь то металл или нет, лучше всего описать, рассматривая его простейшую повторяющуюся единицу, которая называется его элементарной ячейкой. Элементарная ячейка состоит из узлов решетки, которые представляют расположение атомов или ионов. Вся структура состоит из этой элементарной ячейки, повторяющейся в трех измерениях, как показано в [ссылка].
Элементарная ячейка показывает расположение точек решетки, повторяющихся во всех направлениях.
Давайте начнем наше исследование структуры кристаллической решетки и элементарных ячеек с наиболее простой структуры и самой простой элементарной ячейки. Чтобы визуализировать это, представьте, что вы берете большое количество одинаковых сфер, таких как теннисные мячи, и равномерно размещаете их в контейнере. Самый простой способ сделать это — создать слои, в которых сферы в одном слое находятся прямо над сферами в слое ниже, как показано в [ссылка]. Такое расположение называется простой кубической структурой, а элементарная ячейка называется простой кубической элементарной ячейкой или примитивной кубической элементарной ячейкой.
Такое расположение называется простой кубической структурой, а элементарная ячейка называется простой кубической элементарной ячейкой или примитивной кубической элементарной ячейкой.
Когда атомы металла расположены сферами в одном слое непосредственно над или под сферами в другом слое, структура решетки называется простой кубической. Обратите внимание, что сферы соприкасаются.
В простой кубической структуре сферы не упакованы так плотно, как могли бы, и они «заполняют» только около 52% объема контейнера.Это относительно неэффективное устройство, и только один металл (полоний, Po) кристаллизуется в простой кубической структуре. Как показано в [ссылка], твердое тело с таким расположением состоит из плоскостей (или слоев), в которых каждый атом контактирует только с четырьмя ближайшими соседями в своем слое; один атом прямо над ним в верхнем слое; и один атом прямо под ним в слое ниже. Число других частиц, с которыми контактирует каждая частица в кристаллическом твердом теле, известно как ее координационное число. Следовательно, для атома полония в простом кубическом массиве координационное число равно шести.
Следовательно, для атома полония в простом кубическом массиве координационное число равно шести.
Атом в структуре простой кубической решетки контактирует с шестью другими атомами, поэтому его координационное число равно шести.
В простой кубической решетке элементарная ячейка, повторяющаяся во всех направлениях, представляет собой куб, определяемый центрами восьми атомов, как показано в [ссылка]. Атомы в соседних углах этой элементарной ячейки контактируют друг с другом, поэтому длина края этой ячейки равна двум атомным радиусам или одному атомному диаметру.Кубическая элементарная ячейка содержит только те части этих атомов, которые находятся в ней. Поскольку атом в углу простой кубической элементарной ячейки состоит в общей сложности из восьми элементарных ячеек, только одна восьмая этого атома находится в конкретной элементарной ячейке. А поскольку каждая простая кубическая элементарная ячейка имеет по одному атому в каждом из восьми «углов», существует \ (8 \ phantom {\ rule {0. 2em} {0ex}} × \ phantom {\ rule {0.2em} {0ex} } \ frac {1} {8} \ phantom {\ rule {0.2em} {0ex}} = 1 \) атом внутри одной простой кубической элементарной ячейки.
2em} {0ex}} × \ phantom {\ rule {0.2em} {0ex} } \ frac {1} {8} \ phantom {\ rule {0.2em} {0ex}} = 1 \) атом внутри одной простой кубической элементарной ячейки.
Простая элементарная ячейка кубической решетки содержит одну восьмую атома в каждом из восьми углов, так что всего она содержит один атом.
Расчет атомного радиуса и плотности металлов, часть 1
Длина ребра элементарной ячейки альфа-полония составляет 336 мкм.
(а) Определите радиус атома полония.
(b) Определите плотность альфа-полония.
Раствор
Альфа-полоний кристаллизуется в простой кубической элементарной ячейке:
(a) Два соседних атома По контактируют друг с другом, поэтому длина края этой ячейки равна двум атомным радиусам По: l = 2 r .Следовательно, радиус Po равен \ (r \ phantom {\ rule {0.2em} {0ex}} = \ phantom {\ rule {0.2em} {0ex}} \ frac {\ text {l}} {2} \ фантом {\ rule {0.2em} {0ex}} = \ phantom {\ rule {0. 2em} {0ex}} \ frac {\ text {336 pm}} {2} \ phantom {\ rule {0.2em} {0ex }} = \ text {168 pm}. \)
2em} {0ex}} \ frac {\ text {336 pm}} {2} \ phantom {\ rule {0.2em} {0ex }} = \ text {168 pm}. \)
(b) Плотность задается как \ (\ text {density} \ phantom {\ rule {0.2em} {0ex}} = \ phantom {\ rule {0.2em} {0ex}} \ frac {\ text {mass} } {\ text {volume}}. \) Плотность полония можно определить, определив плотность его элементарной ячейки (масса, содержащаяся в элементарной ячейке, деленная на объем элементарной ячейки).{3} \)
Поскольку фактическая плотность Ni не близка к этой, Ni не образует простой кубической структуры.
Большинство металлических кристаллов являются одним из четырех основных типов элементарных ячеек. А пока мы сосредоточимся на трех кубических элементарных ячейках: простой кубической (которую мы уже видели), объемно-центрированной кубической элементарной ячейке и кубической элементарной ячейке с гранецентрированной структурой — все они проиллюстрированы в [ссылка]. (Обратите внимание, что на самом деле существует семь различных систем решеток, некоторые из которых имеют более одного типа решетки, всего 14 различных типов элементарных ячеек. Мы оставляем более сложные геометрические формы на потом в этом модуле.)
Мы оставляем более сложные геометрические формы на потом в этом модуле.)
Кубические элементарные ячейки металлов показывают (на верхних рисунках) расположение узлов решетки и (на нижних рисунках) атомов металлов, расположенных в элементарной ячейке.
Некоторые металлы кристаллизуются в структуре, которая имеет кубическую элементарную ячейку с атомами во всех углах и атомом в центре, как показано в [ссылка]. Это называется объемно-центрированным кубическим (ОЦК) твердым телом. Атомы в углах элементарной ячейки ОЦК не контактируют друг с другом, а контактируют с атомом в центре.Элементарная ячейка BCC содержит два атома: по одной восьмой атома в каждом из восьми углов \ (\ left (8 \ phantom {\ rule {0.2em} {0ex}} × \ phantom {\ rule {0.2em} { 0ex}} \ frac {1} {8} \ phantom {\ rule {0.2em} {0ex}} = \ phantom {\ rule {0.2em} {0ex}} 1 \) атом из углов) плюс один атом из центр. Любой атом в этой структуре касается четырех атомов в слое над ним и четырех атомов в слое под ним. Таким образом, атом в структуре ОЦК имеет координационное число восемь.
Таким образом, атом в структуре ОЦК имеет координационное число восемь.
В объемно-центрированной кубической структуре атомы в определенном слое не касаются друг друга.Каждый атом касается четырех атомов в слое выше и четырех атомов в слое ниже.
Атомы в структурах BCC упакованы намного эффективнее, чем в простой кубической структуре, занимая около 68% от общего объема. Изоморфные металлы со структурой BCC включают K, Ba, Cr, Mo, W и Fe при комнатной температуре. (Элементы или соединения, которые кристаллизуются с одинаковой структурой, считаются изоморфными.)
Многие другие металлы, такие как алюминий, медь и свинец, кристаллизуются в структуре, которая имеет кубическую элементарную ячейку с атомами во всех углах и в центре каждой грани, как показано в [ссылка].Такое расположение называется гранецентрированным кубическим (ГЦК) твердым телом. Элементарная ячейка FCC содержит четыре атома: по одной восьмой атома в каждом из восьми углов \ (\ left (8 \ phantom {\ rule {0. 2em} {0ex}} × \ phantom {\ rule {0.2em} { 0ex}} \ frac {1} {8} \ phantom {\ rule {0.2em} {0ex}} = 1 \) атом из углов) и по половине атома на каждой из шести граней \ (\ left (6 \ phantom {\ rule {0.2em} {0ex}} × \ phantom {\ rule {0.2em} {0ex}} \ frac {1} {2} \ phantom {\ rule {0.2em} {0ex}} = 3 \) атомов с граней). Атомы в углах касаются атомов в центрах соседних граней по диагоналям граней куба.Поскольку атомы находятся в идентичных узлах решетки, они имеют идентичное окружение.
2em} {0ex}} × \ phantom {\ rule {0.2em} { 0ex}} \ frac {1} {8} \ phantom {\ rule {0.2em} {0ex}} = 1 \) атом из углов) и по половине атома на каждой из шести граней \ (\ left (6 \ phantom {\ rule {0.2em} {0ex}} × \ phantom {\ rule {0.2em} {0ex}} \ frac {1} {2} \ phantom {\ rule {0.2em} {0ex}} = 3 \) атомов с граней). Атомы в углах касаются атомов в центрах соседних граней по диагоналям граней куба.Поскольку атомы находятся в идентичных узлах решетки, они имеют идентичное окружение.
Гранецентрированное кубическое твердое тело имеет атомы по углам и, как следует из названия, в центрах граней его элементарных ячеек.
Атомы в конфигурации ГЦК упакованы как можно ближе друг к другу, причем атомы занимают 74% объема. Эта структура также называется кубической плотнейшей упаковкой (CCP). В CCP есть три повторяющихся слоя гексагонально расположенных атомов. Каждый атом контактирует с шестью атомами в своем собственном слое, с тремя в слое выше и с тремя в слое ниже.В этом расположении каждый атом касается 12 ближайших соседей и, следовательно, имеет координационное число 12. Тот факт, что устройства FCC и CCP эквивалентны, может быть не сразу очевиден, но почему они на самом деле являются одной и той же структурой, проиллюстрировано в [ссылка].
Тот факт, что устройства FCC и CCP эквивалентны, может быть не сразу очевиден, но почему они на самом деле являются одной и той же структурой, проиллюстрировано в [ссылка].
Компоновка CCP состоит из трех повторяющихся слоев (ABCABC…) гексагонально расположенных атомов. Атомы в структуре CCP имеют координационное число 12, потому что они контактируют с шестью атомами в своем слое, плюс три атома в слое выше и три атома в слое ниже.Поворачивая перспективу, мы видим, что структура CCP имеет элементарную ячейку с гранью, содержащей атом из слоя A в одном углу, атомы из слоя B по диагонали (в двух углах и в середине лица) и атом из слоя C в оставшемся углу. Это то же самое, что и гранецентрированное кубическое расположение.
Поскольку более тесная упаковка максимизирует общее притяжение между атомами и минимизирует общую межмолекулярную энергию, атомы в большинстве металлов упаковываются таким образом.Мы находим два типа плотнейшей упаковки в простых металлических кристаллических структурах: CCP, с которой мы уже сталкивались, и гексагональная плотнейшая упаковка (HCP), показанная в [link]. Оба состоят из повторяющихся слоев гексагонально расположенных атомов. В обоих типах второй слой (B) размещается на первом слое (A), так что каждый атом во втором слое контактирует с тремя атомами в первом слое. Третий слой размещается одним из двух способов. В HCP атомы в третьем слое находятся непосредственно над атомами в первом слое (т.е.е., третий слой также относится к типу A), и стопка состоит из чередующихся плотноупакованных слоев типа A и типа B (то есть ABABAB). В CCP атомы в третьем слое не находятся над атомами в любом из первых двух слоев (т. Е. Третий слой относится к типу C), а наложение состоит из чередующихся плотноупакованных слоев типа A, типа B и типа C ( т.е. ABCABCABC ⋯). Около двух третей всех металлов кристаллизуются в плотноупакованных массивах с координационным числом 12. Металлы, которые кристаллизуются в структуре HCP, включают Cd, Co, Li, Mg, Na и Zn, а металлы, которые кристаллизуются в структуре CCP, включают Ag , Al, Ca, Cu, Ni, Pb и Pt.
Оба состоят из повторяющихся слоев гексагонально расположенных атомов. В обоих типах второй слой (B) размещается на первом слое (A), так что каждый атом во втором слое контактирует с тремя атомами в первом слое. Третий слой размещается одним из двух способов. В HCP атомы в третьем слое находятся непосредственно над атомами в первом слое (т.е.е., третий слой также относится к типу A), и стопка состоит из чередующихся плотноупакованных слоев типа A и типа B (то есть ABABAB). В CCP атомы в третьем слое не находятся над атомами в любом из первых двух слоев (т. Е. Третий слой относится к типу C), а наложение состоит из чередующихся плотноупакованных слоев типа A, типа B и типа C ( т.е. ABCABCABC ⋯). Около двух третей всех металлов кристаллизуются в плотноупакованных массивах с координационным числом 12. Металлы, которые кристаллизуются в структуре HCP, включают Cd, Co, Li, Mg, Na и Zn, а металлы, которые кристаллизуются в структуре CCP, включают Ag , Al, Ca, Cu, Ni, Pb и Pt.
В обоих типах плотнейшей упаковки атомы упакованы максимально компактно. Гексагональная плотнейшая упаковка состоит из двух чередующихся слоев (ABABAB…). Плотнейшая кубическая упаковка состоит из трех чередующихся слоев (ABCABCABC…).
Гексагональная плотнейшая упаковка состоит из двух чередующихся слоев (ABABAB…). Плотнейшая кубическая упаковка состоит из трех чередующихся слоев (ABCABCABC…).
Расчет атомного радиуса и плотности металлов, часть 2
Кальций кристаллизуется в гранецентрированной кубической структуре. Длина ребра его элементарной ячейки составляет 558,8 пм.
(а) Каков атомный радиус Са в этой структуре?
(b) Рассчитайте плотность Ca.{2}} {16}} \ phantom {\ rule {0.2em} {0ex}} = \ text {197,6 pmg для радиуса Ca}. \)
(b) Плотность определяется как \ (\ text {density} \ phantom {\ rule {0.2em} {0ex}} = \ phantom {\ rule {0.2em} {0ex}} \ frac {\ text {mass} } {\ text {volume}}. \) Плотность кальция можно найти, определив плотность его элементарной ячейки: например, массу, содержащуюся в элементарной ячейке, деленную на объем элементарной ячейки. Гранецентрированная элементарная ячейка Са содержит по одной восьмой атома в каждом из восьми углов \ (\ left (8 \ phantom {\ rule {0. 2em} {0ex}} × \ phantom {\ rule {0.2em} {0ex}} \ frac {1} {8} \ phantom {\ rule {0.2em} {0ex}} = 1 \) атом) и одно- половина атома на каждой из шести граней \ (6 \ phantom {\ rule {0.2em} {0ex}} × \ phantom {\ rule {0.2em} {0ex}} \ frac {1} {2} \ phantom {\ rule {0.2em} {0ex}} = 3 \) атомы), всего четыре атома в элементарной ячейке.
2em} {0ex}} × \ phantom {\ rule {0.2em} {0ex}} \ frac {1} {8} \ phantom {\ rule {0.2em} {0ex}} = 1 \) атом) и одно- половина атома на каждой из шести граней \ (6 \ phantom {\ rule {0.2em} {0ex}} × \ phantom {\ rule {0.2em} {0ex}} \ frac {1} {2} \ phantom {\ rule {0.2em} {0ex}} = 3 \) атомы), всего четыре атома в элементарной ячейке.
Массу элементарной ячейки можно найти по:
\ (\ text {элементарная ячейка 1 Ca} \ phantom {\ rule {0.2em} {0ex}} × \ phantom {\ rule {0.2em} {0ex}} \ frac {\ text {4 атома Ca}} { \ text {Элементарная ячейка 1 Ca}} \ phantom {\ rule {0.{3} \)
Проверьте свои знания
Серебро кристаллизуется в структуре FCC. Длина ребра его элементарной ячейки 409 мкм.
(а) Каков атомный радиус Ag в этой структуре?
(b) Рассчитайте плотность Ag.
Ответ:
(а) 144 пм; (б) 10,5 г / см 3
В общем случае элементарная ячейка определяется длиной трех осей ( a , b и c ) и углами ( α , β и γ ) между ними, как проиллюстрировано в [ссылка].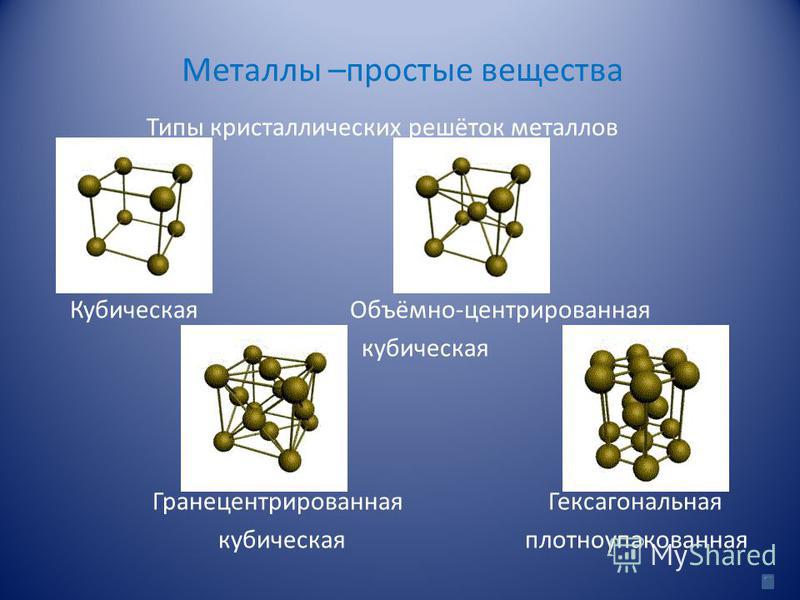 Оси определяются как длины между точками пространственной решетки. Следовательно, оси элементарной ячейки соединяют точки с идентичной средой.
Оси определяются как длины между точками пространственной решетки. Следовательно, оси элементарной ячейки соединяют точки с идентичной средой.
Элементарная ячейка определяется длиной трех ее осей ( a , b и c ) и углами ( α , β и γ ) между осями.
Существует семь различных систем решеток, некоторые из которых имеют более одного типа решетки, всего четырнадцать различных элементарных ячеек, формы которых показаны в [ссылка].
Существует семь различных систем решеток и 14 различных элементарных ячеек.
Ионные кристаллы состоят из двух или более различных типов ионов, которые обычно имеют разные размеры. Упаковка этих ионов в кристаллическую структуру более сложна, чем упаковка атомов металла того же размера.
Большинство одноатомных ионов ведут себя как заряженные сферы, и их притяжение для ионов противоположного заряда одинаково во всех направлениях. Следовательно, стабильные структуры для ионных соединений возникают (1), когда ионы одного заряда окружены как можно большим количеством ионов противоположного заряда, и (2) когда катионы и анионы контактируют друг с другом.Структуры определяются двумя основными факторами: относительными размерами ионов и соотношением количества положительных и отрицательных ионов в соединении.
Следовательно, стабильные структуры для ионных соединений возникают (1), когда ионы одного заряда окружены как можно большим количеством ионов противоположного заряда, и (2) когда катионы и анионы контактируют друг с другом.Структуры определяются двумя основными факторами: относительными размерами ионов и соотношением количества положительных и отрицательных ионов в соединении.
В простых ионных структурах мы обычно находим анионы, которые обычно больше, чем катионы, расположенные в виде плотноупакованного массива. (Как было замечено ранее, дополнительные электроны, притянутые к одному и тому же ядру, делают анионы больше, а меньшее количество электронов, притягиваемых к тому же ядру, делает катионы меньше по сравнению с атомами, из которых они образованы.Катионы меньшего размера обычно занимают дырки (или пустоты) одного из двух типов, оставшиеся между анионами. Меньшее из отверстий находится между тремя анионами в одной плоскости и одним анионом в соседней плоскости. Четыре аниона, окружающие это отверстие, расположены по углам тетраэдра, поэтому отверстие называется тетраэдрическим отверстием.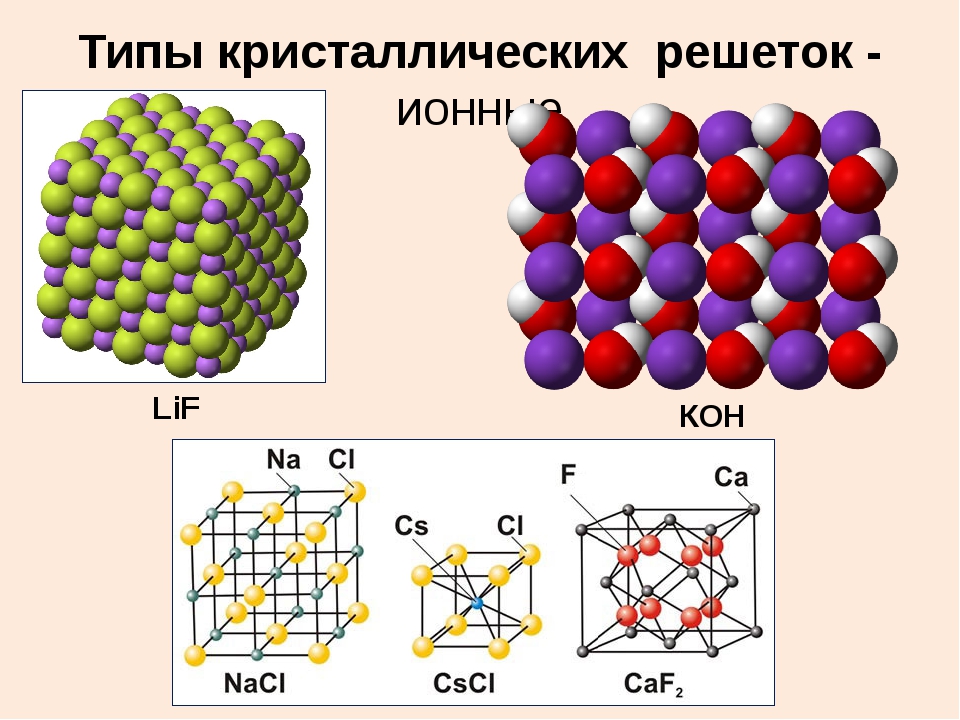 Дыра большего размера находится в центре шести анионов (три в одном слое и три в соседнем слое), расположенных в углах октаэдра; это называется октаэдрическим отверстием.[ссылка] иллюстрирует оба этих типа отверстий.
Дыра большего размера находится в центре шести анионов (три в одном слое и три в соседнем слое), расположенных в углах октаэдра; это называется октаэдрическим отверстием.[ссылка] иллюстрирует оба этих типа отверстий.
Катионы могут занимать два типа дырок между анионами: октаэдрические дырки и тетраэдрические дырки.
В зависимости от относительных размеров катионов и анионов, катионы ионного соединения могут занимать тетраэдрические или октаэдрические отверстия, как показано в [ссылка]. Относительно небольшие катионы занимают тетраэдрические отверстия, а более крупные — октаэдрические. Если катионы слишком велики, чтобы поместиться в октаэдрические отверстия, анионы могут принять более открытую структуру, такую как простой кубический массив.Тогда более крупные катионы могут занять большие кубические отверстия, что стало возможным благодаря более открытому пространству.
Размер катиона и форма отверстия, занимаемого соединением, напрямую связаны.
Есть две тетраэдрические дырки для каждого аниона в массиве анионов HCP или CCP. Соединение, которое кристаллизуется в виде плотноупакованного массива анионов с катионами в тетраэдрических отверстиях, может иметь максимальное соотношение катион: анион 2: 1; все тетраэдрические отверстия заполнены при этом соотношении.Примеры включают Li 2 O, Na 2 O, Li 2 S и Na 2 S. Соединения с соотношением менее 2: 1 также могут кристаллизоваться в виде плотноупакованного массива анионов с катионами. в тетраэдрических дырках, если подходят ионные размеры. Однако в этих соединениях часть тетраэдрических дырок остается вакантной.
Заполнение четырехгранных отверстий
Сульфид цинка является важным промышленным источником цинка, а также используется в качестве белого пигмента в красках. Сульфид цинка кристаллизуется с ионами цинка, занимающими половину тетраэдрических дырок в плотноупакованном массиве сульфид-ионов.Какая формула сульфида цинка?
Решение
Поскольку на каждый анион (сульфид-ион) приходится две тетраэдрических дырки, и половина этих дырок занята ионами цинка, должно быть \ (\ frac {1} {2} \ phantom {\ rule {0. 4em} {0ex}} × \ phantom {\ rule {0.2em} {0ex}} 2, \) или 1, ион цинка на ион сульфида. Таким образом, формула ZnS.
4em} {0ex}} × \ phantom {\ rule {0.2em} {0ex}} 2, \) или 1, ион цинка на ион сульфида. Таким образом, формула ZnS.
Проверьте свои знания
Селенид лития можно описать как плотнейшую упаковку ионов селенида с ионами лития во всех тетраэдрических отверстиях. Какая у него формула селенида лития?
Отношение октаэдрических дырок к анионам в структуре HCP или CCP составляет 1: 1.Таким образом, соединения с катионами в октаэдрических дырках в плотноупакованном массиве анионов могут иметь максимальное соотношение катион: анион 1: 1. Например, в NiO, MnS, NaCl и KH все октаэдрические отверстия заполнены. Отношения менее 1: 1 наблюдаются, когда некоторые из октаэдрических отверстий остаются пустыми.
Стехиометрия ионных соединений
Сапфир — оксид алюминия. Оксид алюминия кристаллизуется с ионами алюминия в двух третях октаэдрических отверстий в плотноупакованном массиве оксидных ионов.Какая формула у оксида алюминия?
Решение
Поскольку на каждый анион (оксидный ион) приходится одна октаэдрическая дырка и только две трети этих дырок заняты, отношение алюминия к кислороду должно быть \ (\ frac {2} {3} \): 1, что даст \ ({\ text {Al}} _ {2 \ text {/} 3} \ text {O}. \) Простейшее целочисленное отношение равно 2: 3, поэтому формула будет Al 2 O 3 .
\) Простейшее целочисленное отношение равно 2: 3, поэтому формула будет Al 2 O 3 .
Проверьте свои знания
Белый пигмент оксида титана кристаллизуется с ионами титана в половине октаэдрических отверстий в плотноупакованном массиве оксидных ионов.Какая формула оксида титана?
В простом кубическом массиве анионов есть одно кубическое отверстие, которое может быть занято катионом для каждого аниона в массиве. В CsCl и других соединениях с такой же структурой все кубические дырки заняты. Половина кубических дырок занята в SrH 2 , UO 2 , SrCl 2 и CaF 2 .
Различные типы ионных соединений часто кристаллизуются в одной и той же структуре, если относительные размеры их ионов и их стехиометрия (две основные характеристики, определяющие структуру) схожи.
Многие ионные соединения кристаллизуются с кубическими элементарными ячейками, и мы будем использовать эти соединения, чтобы описать общие особенности ионных структур.
Когда ионное соединение состоит из катионов и анионов одинакового размера в соотношении 1: 1, оно обычно образует простую кубическую структуру. Примером этого является хлорид цезия, CsCl (проиллюстрирован в [ссылка]), при этом Cs + и Cl — имеют радиусы 174 и 181 мкм соответственно. Мы можем представить это как ионы хлорида, образующие простую кубическую элементарную ячейку с ионом цезия в центре; или в виде ионов цезия, образующих элементарную ячейку с ионом хлорида в центре; или как простые кубические элементарные ячейки, образованные ионами Cs + , перекрывающими элементарные ячейки, образованные ионами Cl — .Ионы цезия и ионы хлора соприкасаются по диагоналям тела элементарных ячеек. Один ион цезия и один ион хлорида присутствуют в элементарной ячейке, что дает стехиометрию 1: 1, требуемую формулой для хлорида цезия. Обратите внимание, что в центре ячейки нет точки решетки, и CsCl не является структурой BCC, потому что ион цезия не идентичен иону хлорида.
Ионные соединения с катионами и анионами аналогичного размера, такие как CsCl, обычно образуют простую кубическую структуру. Их можно описать элементарными ячейками с катионами по углам или анионами по углам.
Мы сказали, что расположение точек решетки произвольно. Это иллюстрируется альтернативным описанием структуры CsCl, в которой узлы решетки расположены в центрах ионов цезия. В этом описании ионы цезия расположены в точках решетки в углах ячейки, а ион хлорида расположен в центре ячейки. Две элементарные ячейки разные, но они описывают идентичные структуры.
Когда ионное соединение состоит из катионов и анионов в соотношении 1: 1, которые значительно различаются по размеру, оно обычно кристаллизуется с помощью элементарной ячейки FCC, как показано в [ссылка].Примером этого является хлорид натрия, NaCl, причем Na + и Cl — имеют радиусы 102 и 181 мкм соответственно. Мы можем представить это как ионы хлора, образующие ячейку FCC, причем ионы натрия расположены в октаэдрических отверстиях в середине краев ячейки и в центре ячейки. Ионы натрия и хлора соприкасаются друг с другом по краям ячейки. Элементарная ячейка содержит четыре иона натрия и четыре иона хлорида, что дает стехиометрию 1: 1, требуемую формулой NaCl.
Ионы натрия и хлора соприкасаются друг с другом по краям ячейки. Элементарная ячейка содержит четыре иона натрия и четыре иона хлорида, что дает стехиометрию 1: 1, требуемую формулой NaCl.
Ионные соединения с анионами, размер которых намного превышает размер катионов, например NaCl, обычно образуют структуру ГЦК. Их можно описать элементарными ячейками ГЦК с катионами в октаэдрических дырках.
Кубическая форма сульфида цинка, цинковая обманка, также кристаллизуется в элементарной ячейке FCC, как показано в [ссылка]. Эта структура содержит сульфид-ионы в узлах решетки ГЦК-решетки. (Расположение сульфид-ионов идентично расположению хлорид-ионов в хлориде натрия.) Радиус иона цинка составляет всего около 40% от радиуса сульфид-иона, поэтому эти маленькие ионы Zn 2+ расположены в чередующихся тетраэдрических дырках, то есть в одной половине тетраэдрических дырок. В элементарной ячейке четыре иона цинка и четыре иона сульфида, что дает эмпирическую формулу ZnS.
ZnS, сульфид цинка (или цинковая обманка) образует элементарную ячейку FCC с ионами сульфида в узлах решетки и гораздо меньшими ионами цинка, занимающими половину тетраэдрических отверстий в структуре.
Элементарная ячейка с фторидом кальция, подобная той, что показана на [ссылка], также является элементарной ячейкой FCC, но в этом случае катионы расположены в точках решетки; эквивалентные ионы кальция расположены в узлах решетки ГЦК-решетки. Все тетраэдрические позиции в массиве ГЦК ионов кальция заняты ионами фтора. В элементарной ячейке четыре иона кальция и восемь ионов фтора, что дает соотношение кальций: фтор 1: 2 в соответствии с химической формулой CaF 2 .Внимательное изучение [ссылка] покажет простой кубический массив ионов фтора с ионами кальция в одной половине кубических дырок. Структуру нельзя описать в терминах пространственной решетки точек на фторид-ионах, потому что не все фторид-ионы имеют одинаковое окружение. Ориентация четырех ионов кальция относительно ионов фтора различается.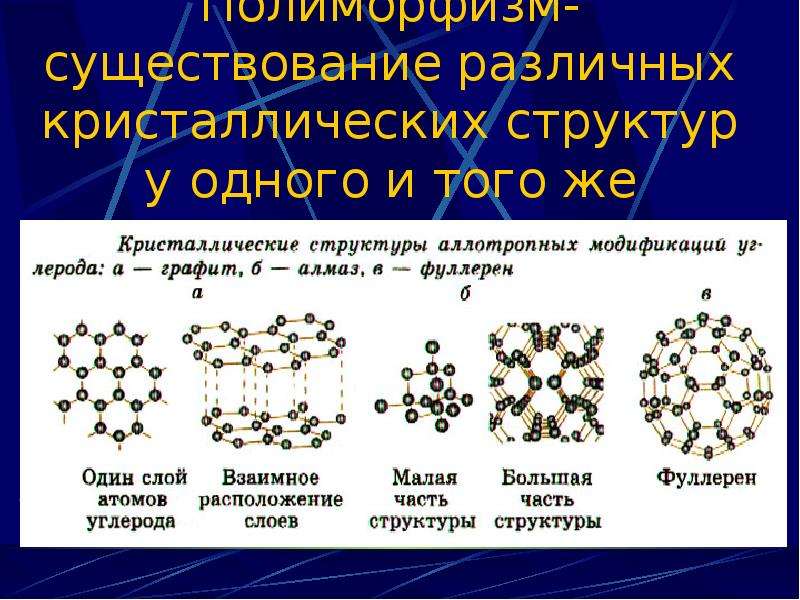
Фторид кальция, CaF 2 , образует элементарную ячейку ГЦК с ионами кальция (зеленый) в узлах решетки и ионами фтора (красный), занимающими все тетраэдрические узлы между ними.
Размер элементарной ячейки и расположение атомов в кристалле могут быть определены из измерений дифракции рентгеновских лучей на кристалле, называемых рентгеновской кристаллографией. Дифракция — это изменение направления движения электромагнитной волны, когда она встречает физический барьер, размеры которого сопоставимы с размерами длины волны света. Рентгеновские лучи — это электромагнитное излучение с длиной волны, равной расстоянию между соседними атомами в кристаллах (порядка нескольких Å).
Когда пучок монохроматических рентгеновских лучей попадает на кристалл, его лучи рассеиваются во всех направлениях атомами внутри кристалла. Когда рассеянные волны, распространяющиеся в одном направлении, сталкиваются друг с другом, они претерпевают интерференцию , процесс, посредством которого волны объединяются, приводя к увеличению или уменьшению амплитуды (интенсивности) в зависимости от степени, в которой максимумы объединяющихся волн находятся разделенные (см. [ссылка]).
[ссылка]).
Световые волны, занимающие одно и то же пространство, испытывают интерференцию, объединяясь, давая волны большей (а) или меньшей (б) интенсивности, в зависимости от разделения их максимумов и минимумов.
Когда рентгеновские лучи определенной длины волны, λ , рассеиваются атомами в соседних плоскостях кристалла, разделенных расстоянием, d , они могут претерпевать конструктивную интерференцию, когда разница между расстояниями, пройденными двумя волнами до их комбинация представляет собой целочисленный множитель длины волны n . Это условие выполняется, когда угол дифрагированного луча, θ , связан с длиной волны и межатомным расстоянием уравнением:
\ (п \ lambda = 2d \ phantom {\ rule {0.2em} {0ex}} \ text {sin} \ phantom {\ rule {0.2em} {0ex}} \ theta \)
Это соотношение известно как уравнение Брэгга в честь У.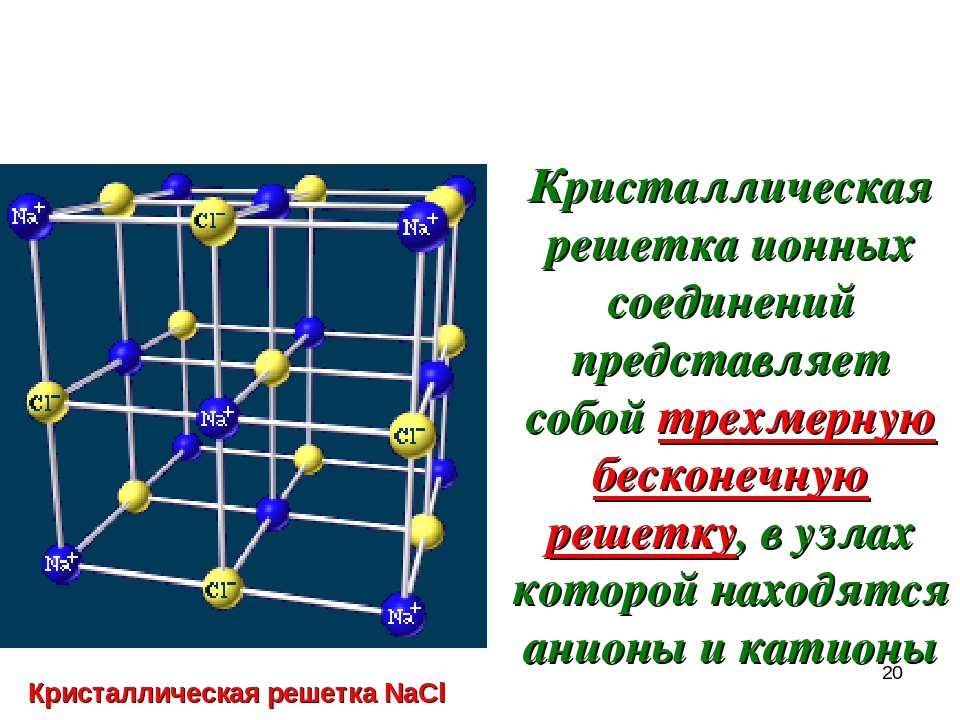 Х. Брэгга, английского физика, который первым объяснил это явление. [ссылка] иллюстрирует два примера дифрагированных волн от одних и тех же двух плоскостей кристалла. На рисунке слева изображены волны, дифрагированные под углом Брэгга, приводящие к конструктивной интерференции, а на рисунке справа показаны дифракция и другой угол, который не удовлетворяет условию Брэгга, что приводит к деструктивной интерференции.
Х. Брэгга, английского физика, который первым объяснил это явление. [ссылка] иллюстрирует два примера дифрагированных волн от одних и тех же двух плоскостей кристалла. На рисунке слева изображены волны, дифрагированные под углом Брэгга, приводящие к конструктивной интерференции, а на рисунке справа показаны дифракция и другой угол, который не удовлетворяет условию Брэгга, что приводит к деструктивной интерференции.
Дифракция рентгеновских лучей, рассеянных атомами внутри кристалла, позволяет определить расстояние между атомами. Верхнее изображение показывает конструктивную интерференцию между двумя рассеянными волнами и результирующей дифрагированной волной высокой интенсивности. На нижнем изображении показаны деструктивная интерференция и дифрагированная волна низкой интенсивности.
Посетите этот сайт для получения дополнительных сведений об уравнении Брэгга и симуляторе, который позволяет исследовать влияние каждой переменной на интенсивность дифрагированной волны.
Рентгеновский дифрактометр, такой как проиллюстрированный в [ссылка], может использоваться для измерения углов, под которыми рентгеновские лучи дифрагируют при взаимодействии с кристаллом, как описано ранее. Из таких измерений можно использовать уравнение Брэгга для вычисления расстояний между атомами, как показано в следующем примере упражнения.
(a) В дифрактометре луч рентгеновских лучей попадает на кристаллический материал, создавая (b) картину дифракции рентгеновских лучей, которая может быть проанализирована для определения кристаллической структуры.
Использование уравнения Брэгга
В дифрактометре рентгеновские лучи с длиной волны 0,1315 нм использовались для создания дифракционной картины для меди. Дифракция первого порядка ( n = 1) произошла под углом θ = 25,25 °. Определите расстояние между дифрагирующими плоскостями в меди.
Решение
Расстояние между плоскостями находится путем решения уравнения Брэгга, nλ = 2 d sin θ , для d .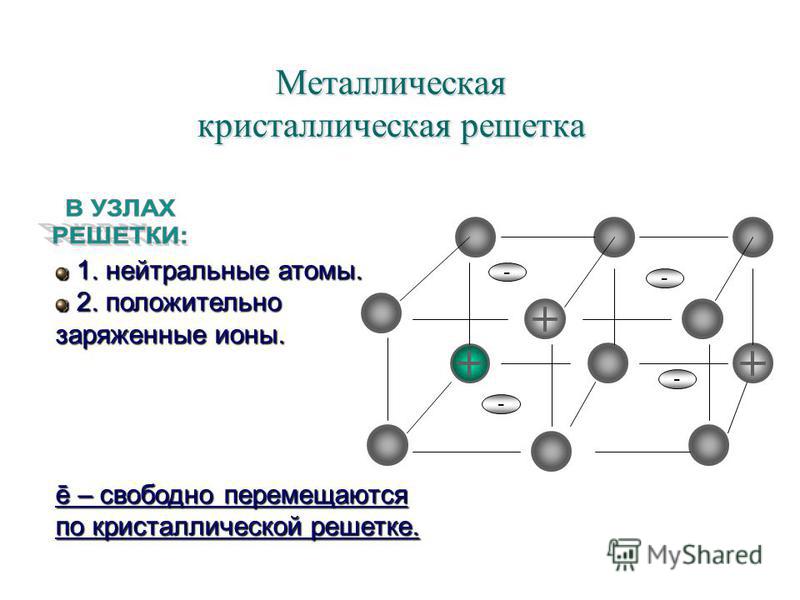
Это дает: \ (d \ phantom {\ rule {0.2em} {0ex}} = \ phantom {\ rule {0.2em} {0ex}} \ frac {n \ lambda} {2 \ phantom {\ rule {0.2 em} {0ex}} \ text {sin} \ phantom {\ rule {0.2em} {0ex}} \ theta} \ phantom {\ rule {0.2em} {0ex}} = \ phantom {\ rule {0.2em} {0ex}} \ frac {1 \ left (0,1315 \ phantom {\ rule {0.2em} {0ex}} \ text {nm} \ right)} {2 \ phantom {\ rule {0.2em} {0ex}} \ текст {sin} \ phantom {\ rule {0.2em} {0ex}} \ left (25.25 \ text {°} \ right)} \ phantom {\ rule {0.2em} {0ex}} = \ text {0,154 нм} \)
Check Your Learning
Кристалл с расстоянием между плоскостями, равным 0.394 нм дифрагирует рентгеновские лучи с длиной волны 0,147 нм. Каков угол дифракции первого порядка?
Рентгеновский кристаллограф Розалинд Франклин
Открытие структуры ДНК в 1953 году Фрэнсисом Криком и Джеймсом Уотсоном — одно из величайших достижений в истории науки. Они были удостоены Нобелевской премии по физиологии и медицине 1962 года вместе с Морисом Уилкинсом, предоставившим экспериментальное доказательство структуры ДНК. Британский химик Розалинд Франклин внесла неоценимый вклад в это грандиозное достижение своей работой по измерению рентгеновских дифракционных изображений ДНК.В начале своей карьеры исследования Франклин структуры углей оказались полезными для британских военных действий. Сосредоточив свое внимание на биологических системах в начале 1950-х годов, Франклин и докторант Раймонд Гослинг обнаружили, что ДНК состоит из двух форм: длинного тонкого волокна, образующегося при намокании (тип «B»), и короткого широкого волокна, образующегося при сушке ( наберите «А»). Ее рентгеновские дифракционные изображения ДНК ([ссылка]) предоставили важную информацию, которая позволила Уотсону и Крику подтвердить, что ДНК образует двойную спираль, и определить детали ее размера и структуры.Франклин также провел новаторское исследование вирусов и РНК, содержащей их генетическую информацию, обнаружив новую информацию, которая радикально изменила совокупность знаний в этой области. После развития рака яичников Франклин продолжала работать до своей смерти в 1958 году в возрасте 37 лет.
Британский химик Розалинд Франклин внесла неоценимый вклад в это грандиозное достижение своей работой по измерению рентгеновских дифракционных изображений ДНК.В начале своей карьеры исследования Франклин структуры углей оказались полезными для британских военных действий. Сосредоточив свое внимание на биологических системах в начале 1950-х годов, Франклин и докторант Раймонд Гослинг обнаружили, что ДНК состоит из двух форм: длинного тонкого волокна, образующегося при намокании (тип «B»), и короткого широкого волокна, образующегося при сушке ( наберите «А»). Ее рентгеновские дифракционные изображения ДНК ([ссылка]) предоставили важную информацию, которая позволила Уотсону и Крику подтвердить, что ДНК образует двойную спираль, и определить детали ее размера и структуры.Франклин также провел новаторское исследование вирусов и РНК, содержащей их генетическую информацию, обнаружив новую информацию, которая радикально изменила совокупность знаний в этой области. После развития рака яичников Франклин продолжала работать до своей смерти в 1958 году в возрасте 37 лет.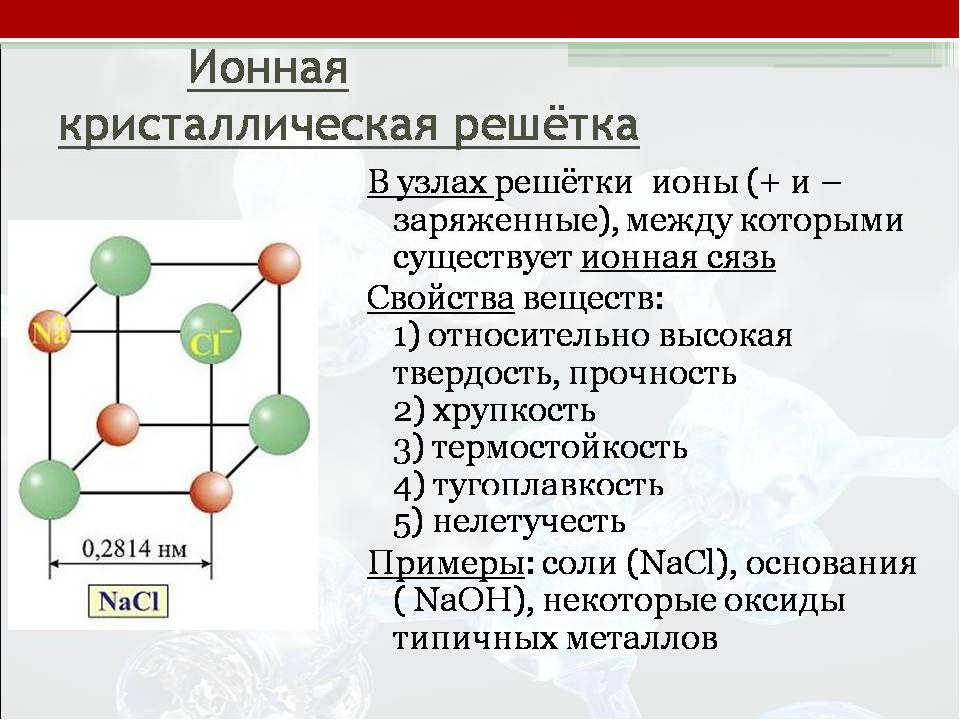 Среди множества посмертных признаний ее работы, Чикагская медицинская школа Финчского университета медицинских наук изменила свое название на Университет медицины и науки Розалинды Франклин в 2004 году. и приняла изображение ее знаменитого рентгеновского дифракционного изображения ДНК в качестве официального логотипа университета.
Среди множества посмертных признаний ее работы, Чикагская медицинская школа Финчского университета медицинских наук изменила свое название на Университет медицины и науки Розалинды Франклин в 2004 году. и приняла изображение ее знаменитого рентгеновского дифракционного изображения ДНК в качестве официального логотипа университета.
На этой иллюстрации показано изображение дифракции рентгеновских лучей, подобное тому, которое Франклин нашла в своем исследовании. (кредит: Национальный институт здоровья)
Структура металлов
Структура металлов
Структура Металлы и другие одноатомные твердые вещества
Структуры чистых металлов легко описать, потому что
атомы, образующие эти металлы, можно рассматривать как идентичные
идеальные сферы.То же можно сказать и о структуре
инертные газы (He, Ne, Ar и др.) при очень низких температурах.
Все эти вещества кристаллизуются в одну из четырех основных структур:
простая кубическая ( SC ), объемно-центрированная кубическая ( BCC ),
гексагональный с максимальной плотностью упаковки ( HCP ) и кубической с максимальной плотностью упаковки ( CCP ).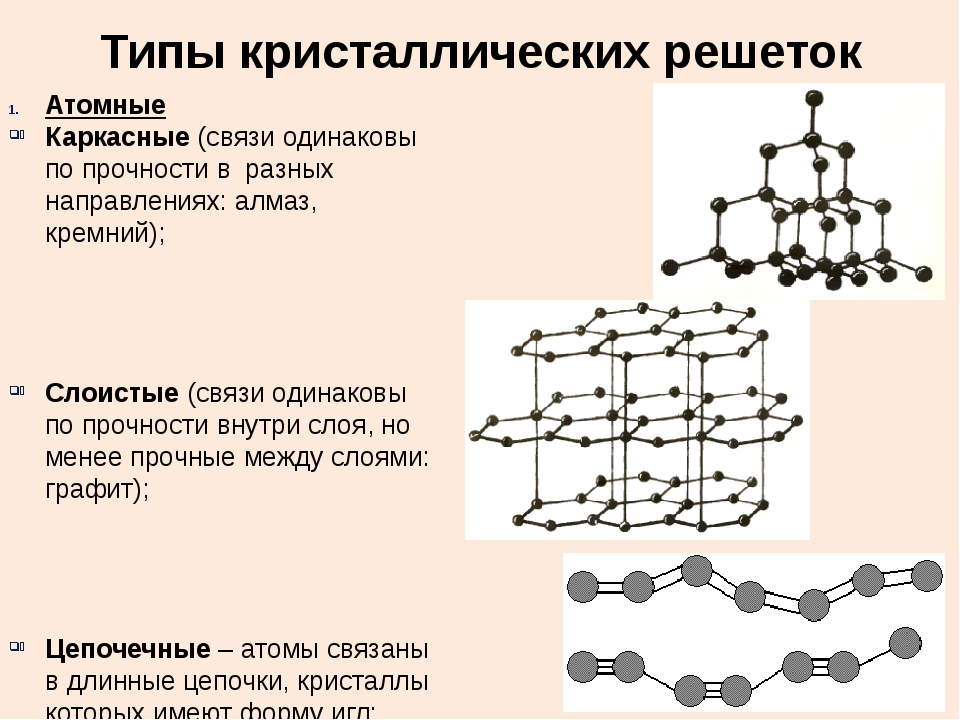
Простая кубическая упаковка
Когда твердое вещество кристаллизуется, частицы, образующие твердое тело упаковать как можно плотнее.Чтобы проиллюстрировать этот принцип, давайте попробуйте представить, как лучше всего укладывать шары, например, пинг-понг шары в пустую коробку.
Один из подходов включает в себя осторожную упаковку мячей для пинг-понга в образуют квадратную упакованную плоскость сфер, как показано на рисунке ниже.
Наклонив коробку в одну сторону, мы можем сложить вторую плоскость из сферы прямо поверх первой. Результат — регулярный структура, в которой простейшая повторяющаяся единица — куб из восьми сферы, как показано на рисунке ниже.
Эта структура называется простой кубической упаковкой . Каждый сфера в этой структуре касается четырех одинаковых сфер в тот же самолет. Он также касается одной сферы в плоскости выше и одной в самолете внизу. Каждый атом в этой структуре может образовывать связи с его шесть ближайших соседей. Поэтому говорят, что каждая сфера имеет координационный номер из 6.
Простая кубическая структура не является эффективным способом использования космос.Только 52% доступного пространства фактически занято сферы в простой кубической структуре. Остальное пустое место. Поскольку такая структура неэффективна, кристаллизуется только один элемент — полоний. в простой кубической структуре.
Телоцентрированный кубический Упаковка
Другой подход начинается с разделения сфер для образования плоскость квадратной формы, в которой они не совсем касаются друг друга, как показано на рисунке ниже.
Сферы во второй плоскости упаковываются над отверстиями в первая плоскость, как показано на рисунке ниже.
Сферы в третьей плоскости упаковываются над отверстиями во второй. самолет. Сферы в четвертой плоскости упаковываются над отверстиями в третьей. самолет и так далее. В результате получается структура, в которой Плоскости атомов с нечетными номерами идентичны, а плоскости атомов с четными номерами самолеты идентичны.Это ABABABAB . . . повторение структура известна как объемно-центрированная кубическая упаковка .
Эта структура называется объемно-центрированной кубической , потому что каждая сфера касается четырех сфер в плоскости выше и еще четырех в плоскости ниже, расположенной по углам куба. Таким образом, повторяющаяся единица в этой структуре — куб из восьми сфер с девятой одинаковой сферой в центре тела в другими словами, куб с центром тела, как показано на рисунке ниже.Координационный номер в данной структуре — 8.
Изучите кубический кристалл с центром в теле внизу:
Нажмите левую кнопку мыши и перетащите конструкцию. Нажмите вправо кнопку мыши, чтобы просмотреть параметры.
Для этой страницы требуется MDL Chime плагин. Загрузите его здесь.
Объемно-центрированная кубическая набивка — более эффективная способ использования пространства по сравнению с простой кубической упаковкой68% пространства в этой конструкции заполнено.Все металлы в Группа IA (Li, Na, K и т. Д.), Более тяжелые металлы в группе IIA. (Ca, Sr и Ba), а также ряд ранних переходных металлов (например, Ti, V, Cr, Mo, W и Fe) упаковываются в объемно-центрированные кубические структура.
Ближайшая упаковка Конструкции
Две конструкции так эффективно упаковывают сферы, что называются структурами плотнейшей упаковки .
Оба начинают с упаковки сфер в плоскости в каждая сфера касается шести других сфер, ориентированных по углам шестиугольника, как показано на рисунке ниже.
Затем вторая плоскость образована упаковочными сферами. над треугольными отверстиями в первой плоскости, как показано на рисунок ниже.
Сферы в третьем самолете могли упаковываться непосредственно над сферами в первой плоскости, чтобы сформировать ABABABAB . . . повторяющаяся структура. Поскольку эта структура состоит из чередующиеся плоскости гексагональных плотноупакованных сфер, это называется гексагональной плотноупакованной структурой .Каждая сфера касается трех сфер в плоскости выше, трех сфер в плоскости ниже, и шесть сфер в той же плоскости, как показано на рисунок ниже. Таким образом, координационное число в гексагональной структура с плотной упаковкой — 12.
74% пространства в гексагональной плотноупакованной структура заполнена. Более эффективного способа упаковки сфер не существует. известно, и важна гексагональная структура с плотнейшей упаковкой. для металлов, таких как Be, Co, Mg и Zn, а также инертного газа He при низких температурах.
Есть еще один способ укладки гексагональной плотнейшие плоскости сфер. Атомы в третьей плоскости могут быть упакованы над отверстиями в первой плоскости, которые были не используется для формирования второй плоскости. Четвертый шестиугольник плотно упакованная плоскость атомов тогда упаковывается непосредственно над первый. В результате получается ABCABCABC . . . структура, который называется куб. плотнейшей упаковки . Каждая сфера в этом структура касается шести других в той же плоскости, трех в плоскости вверху, и три в плоскости внизу, как показано на рисунке ниже.Таким образом, координационный номер по-прежнему 12.
Разница между гексагональной и кубической структуры с наиболее плотной упаковкой можно понять, отметив, что атомы в первой и третьей плоскостях лежат непосредственно друг над другом в гексагональной плотноупакованной структуре. В кубической плотноупакованной структуры, атомы в этих плоскостях ориентированы в разные стороны.
Кубическая структура плотнейшей упаковки такая же, как эффективна как гексагональная плотноупакованная структура.(Оба используют 74% доступного пространства.) Многие металлы, включая Ag, Al, Au, Ca, Co, Cu, Ni, Pb и Pt кристаллизуются в кубических плотноупакованных структура. То же самое и со всеми инертными газами, кроме гелия, когда они газы охлаждаются до достаточно низких температур, чтобы они затвердевали.
Гранецентрированная кубическая элементарная ячейка — простейшая повторяющееся звено в кубической плотноупакованной структуре. Фактически, наличие гранецентрированных кубических элементарных ячеек в этой структуре объясняет, почему структура известна как кубическая самая плотная упаковка.
Координационные номера и Конструкции из металлов
Координационные числа четырех структур металлов приведены в таблице ниже. Это легко понять, почему металлы упаковываются в гексагональную или кубическую упаковку с максимальной плотностью конструкции. Эти конструкции не только эффективно используют пространство. по возможности, у них также есть максимально возможная координация числа, что позволяет каждому атому металла образовывать связи с наибольшее количество соседних атомов металла.
Координационные числа для общего кристалла Конструкции
| Структура | Координация Номер | Укладка Шаблон | ||
| простая кубическая | 6 | AAAAAAAA .. . | ||
| объемно-центрированная кубическая | 8 | АБАБАБАБ . . . | ||
| Гексагональный плотноупакованный | 12 | АБАБАБАБ . . . | ||
| куб. Плотнейшая | 12 | ABCABCABC .. . |
Менее очевидно, почему треть металлов упаковывать в кубическую структуру с центром в теле, в которой Координационный номер всего 8. Популярность данной конструкции можно понять, обратившись к рисунку ниже.
Координационное число для объемно-центрированной кубической структуры, приведенные в таблице выше, учитываются только атомы, которые фактически касаться данного атома в этой структуре.Рисунок выше показывает, что каждый атом также почти касается четырех соседей в тот же самолет, пятый сосед двумя самолетами выше, а шестой два самолета внизу. Расстояние от каждого атома до ядер эти соседние атомы всего на 15% больше, чем расстояние до ядра атомов, которых он действительно касается. Каждый атом в объемно-центрированная кубическая структура, таким образом, может образовывать в общей сложности 14 облигации восемь сильных связей с атомами, которых он касается, и шесть более слабых связывается с атомами, которых почти касается.
Это помогает понять, почему металл может предпочесть объемно-центрированную кубическую структуру гексагональной или кубическая плотноупакованная структура. Каждый атом металла в плотноупакованные структуры могут образовывать прочные связи с 12 соседними атомы. В объемно-центрированной кубической структуре каждый атом образует всего 14 связей с соседними атомами, хотя шесть из них облигации несколько слабее остальных восьми.
Физические свойства что результат из структуры металлов
Структуры металлов могут быть использованы для объяснения многие из характерных физических свойств металлов.
На просьбу объяснить, почему металлы имеют характерный металлический блеск или блеск, многие скажут что металлы отражают (буквально отбрасывают) свет, который сияет на их поверхности. По сути, они могут возразить, что свет отражается от металлической поверхности, как ракетка отскакивает от стен площадки для ракетбола. Что-то не так с этим аналогия, однако. Металлы фактически поглощают значительную долю света, падающего на их поверхность.
Часть энергии, улавливаемой, когда металл поглощает свет, превращается в тепловую энергию. (Вы можете легко Продемонстрируйте это, положив руку на поверхность автомобиля. который провел несколько часов на солнце.) Остальная энергия переизлучается металлом как «отраженный» свет. Серебряный лучше любого другого металла по отражению света, и все же только 88% света, попадающего на поверхность серебряного зеркала, составляет переизлучен. Это поднимает важный вопрос: почему металлы поглощают свет, когда другие вещества, такие как стекло в окна машины, не так ли? Свет поглощается, когда энергия этого излучение равно энергии, необходимой для возбуждения электрона до возбужденное состояние с более высокой энергией или когда энергия может быть использована для перемещать электрон через твердое тело.Поскольку электроны делокализован в металлах и поэтому свободно перемещаться по твердым металлам легко впитывают свет. Другие твердые тела, такие как стекло, не имеют электроны, которые могут двигаться через твердое тело, поэтому они не могут поглощать свет, как металлы. Эти твердые вещества бесцветны и могут только быть окрашенным путем добавления примеси, в которой энергия, связанная с при возбуждении электрона с одной орбитали на другую попадает в видимая часть спектра. Стекло обычно окрашивают добавление небольшого количества одного из переходных металлов.Кобальт дает синий цвет, хром делает стекло зеленым, а следы золота придают темно-красный цвет.
Почему металлы твердые? Неметаллы, такие как водород и кислород являются газами при комнатной температуре, потому что эти элементы можно получить заполненную оболочку валентных электронов, поделившись парами электронов с образованием относительно небольших молекул, таких как H 2 и O 2 , которые движутся достаточно быстро в комнате температура для перехода из жидкости в газовую фазу.Металлы этого не могут. На металле недостаточно электронов атом, чтобы позволить ему заполнить свою валентную оболочку, разделяя пары электроны с одним или двумя ближайшими соседями. Единственный способ металл может получить эквивалент заполненной оболочки валентных электронов заключается в том, что эти электроны могут быть разделены между несколькими соседние атомы металла. Это возможно только при большом количестве атомы металлов держатся близко друг к другу, и поэтому металлы твердые вещества при комнатной температуре.
Почему металлы податливы и пластичны? Большинство металлов упаковывать в объемно-центрированные кубические, гексагональные плотноупакованные или кубические структуры с плотнейшей упаковкой. Теоретически изменение формы металл — это просто вопрос приложения силы, которая заставляет атомы в одной из плоскостей скользят мимо атомов в соседней плоскости, как показано на рисунке ниже. На практике легче сделайте это, когда металл горячий.
Почему металлы являются хорошими проводниками тепла и электричество? Как мы уже видели, делокализация валентные электроны в металле позволяют твердому телу проводить электрический ток.Чтобы понять, почему металлы проводят тепло, вспомните эта температура является макроскопическим свойством, которое отражает кинетическая энергия отдельных атомов или молекул. Плотный упаковка атомов в металле означает, что кинетическая энергия может быть переносится от одного атома к другому как быстро, так и эффективно.
Твердые растворы и Интерметаллические соединения
Большинство растворов, с которыми работают химики, включают газ (например, HCl) или твердое вещество (например, NaCl), растворенное в жидкость (например, вода).Также возможно приготовление растворов в котором газ, жидкость или твердое вещество растворяются в твердом теле. В наиболее важным классом твердых растворов являются те, в которых один твердое вещество растворяется в другом. Два примера твердых растворов медь, растворенная в алюминии, и углерод, растворенный в железе.
Растворимость одного твердого вещества в другом обычно зависит от температуры. При комнатной температуре, например, медь не растворяется в алюминии. Однако при 550C алюминий может формируют решения, содержащие до 5.6% меди по весу. Алюминий металл, пропитанный медью при 550C, будет пытаться отвергать атомы меди, когда она остывает до комнатной температуры. В теории, раствор может отклонять атомы меди, образуя поликристаллическая структура, состоящая из мелких кристаллов более или менее чистый алюминий с вкраплениями мелких кристаллов меди металл. Вместо этого атомы меди соединяются с алюминием. атомов по мере охлаждения раствора с образованием интерметаллида с формулой CuAl 2 .
CuAl 2 — прекрасный пример разница между смесью (например, раствор меди растворенный в алюминии) и соединение. Решение может содержать различное количество меди и алюминия. Например, при 550 ° C раствор может содержать от 0 до 5,6% металлической меди по масса. Интерметаллид имеет фиксированный состав CuAl 2 всегда 49,5% алюминия по весу.
Интерметаллические соединения, такие как CuAl 2 являются ключом к процессу, известному как дисперсионное твердение .Алюминиевые металлические пакеты в кубической структуре плотнейшей упаковки, в которой одна плоскость атомов может проскользнуть мимо другой. В результате чистый металлический алюминий слишком слаб, чтобы его можно было использовать в качестве конструкционного металла в автомобили или самолеты. Дисперсионное упрочнение дает сплавы, которые в пять-шесть раз прочнее алюминия и отличный конструкционный металл.
Первый этап дисперсионного твердения алюминий предполагает нагрев металла до 550С. Медь тогда добавляется до образования раствора, который гасят холодной водой.В раствор остывает так быстро, что атомы меди не могут собраться вместе для образования микрокристаллов металлической меди.
Сравнение монолитной стены с кирпичной имеет одно важное недостаток. Это наводит на мысль, что атомы не могут двигаться через металл. Это не совсем так. Распространение через металл может появиться, хотя происходит это медленно. За период со временем атомы меди могут перемещаться через закаленный раствор с образованием микрокристаллы интерметаллида CuAl 2 , которые настолько малы, что их трудно увидеть в микроскоп.
Эти частицы CuAl 2 обе твердые и сильный. Так сильно они препятствуют потоку металлического алюминия что их окружает. Эти микрокристаллы CuAl 2 укрепить алюминиевый металл, мешая плоскости пути атомы скользят мимо друг друга. В результате получается металл, который одновременно тверже и прочнее чистого алюминия.
Медь растворяется в алюминии при высокой температуре является примером раствора замещения , в котором медь атомы упаковываются в позиции, обычно занимаемые атомами алюминия.Есть еще один способ приготовления твердого раствора. Атомы одного элемента можно упаковать в отверстия, или пустот, , между атомами основного элемента, потому что даже самые эффективные кристаллические структуры используют только 74% доступного пространства в кристалл. В результате получается межстраничное решение .
Сталь, работающая при высоких температурах, является хорошим примером межстраничный раствор. Сталь образуется путем растворения углерода в железо. При очень высоких температурах железо упаковывается в кубический плотно упакованная структура, которая оставляет достаточно места, чтобы позволить атомы углерода помещаются в отверстия между атомами железа.Ниже 910C, железо-металлические пакеты в объемно-центрированной кубической структуре, в отверстия слишком малы, чтобы удерживать атомы углерода.
Это имеет важные последствия для свойства стали. При температуре выше 910 ° С углерод легко растворяется в железе с образованием твердого раствора, содержащего столько же как 1% углерода по весу. Этот материал одновременно податлив и пластичный, и его можно раскатывать в тонкие листы или забивать различные формы. Когда этот раствор остынет ниже 910 ° C, утюг превращается в объемно-центрированную кубическую структуру, а атомы углерода отбраковываются из металла.Если раствору дать остыть постепенно атомы углерода мигрируют через металл, образуя соединение формулы Fe 3 C, которое осаждает из раствора. Эти кристаллы Fe 3 C служат тому же роль в стали, которую кристаллы CuAl 2 играют в алюминии, они препятствуют потоку плоскостей атомов металлов и тем самым делают металл прочнее.
Отверстия в наиболее плотно упакованных и простые кубические структуры
Металлы — не единственные твердые частицы, которые упаковываются в простые кубический, объемно-центрированный кубический, гексагональный плотнейшей упаковки и кубический плотноупакованные структуры.Использование большого количества ионных твердых веществ эти конструкции тоже.
хлорид натрия (NaCl) и сульфид цинка (ZnS), например, формировать кристаллы, которые можно представить себе как кубические плотно упакованные массивы отрицательных ионов (Cl — или S 2 — ), с положительными ионами (Na + или Zn 2+ ), упакованные в дырки между наиболее плотноупакованными плоскостями отрицательных ионов. Там это тонкое различие между этими структурами, однако, потому что ионы Na + в пакете NaCl в разных отверстиях от тех, которые используются ионами Zn 2+ в ZnS.
Есть два вида отверстий в плотно упакованном структура. Так называемые четырехгранные отверстия показаны на рисунок ниже. Сплошные линии на этом рисунке представляют одну плоскость. наиболее плотно упакованных атомов. Пунктирные линии обозначают вторую плоскость атомов, которые упаковываются над дырками в первой плоскости. Каждое из отверстий, отмеченных цифрой t , касается трех атомов в первая плоскость и один атом во второй плоскости. Они называются тетраэдрические отверстия, потому что положительные ионы, которые упаковываются в эти отверстия окружены четырьмя отрицательными ионами, расположенными по углам тетраэдра.
октаэдрических отверстий в плотнейшей упаковке структура показана на рисунке ниже. Еще раз твердый линии представляют одну плоскость наиболее плотно упакованных атомов, а штриховые линии соответствуют второй плоскости, которая набивается над отверстиями. в первом самолете. Каждое отверстие отмечено знаком o касается трех атомов в первой плоскости и трех атомов в второй самолет. Их называют октаэдрическими отверстиями, потому что положительные ионы, которые занимают эти дырки, окружены шестью отрицательными ионами расположены к углам октаэдра.
Тетраэдрические отверстия очень маленькие. Самый большой атом, который может поместиться в тетраэдрическое отверстие, не искажая тетраэдр имеет радиус всего 0,225 радиуса атомов которые образуют отверстие. Октаэдрические отверстия почти вдвое больше, чем четырехгранные отверстия. Самый большой атом, который может поместиться в октаэдрическая дыра имеет радиус 0,414 радиуса атомов которые образуют отверстие. Относительный размер атомов или ионов, которые образуют кристалл, поэтому определяет, будет ли тетраэдрический или используются октаэдрические отверстия.
Иногда положительные ионы слишком велики для упаковки тетраэдрические или октаэдрические отверстия в плотноупакованном структура отрицательных ионов. Когда это происходит, отрицательные ионы упакованы в простую кубическую структуру, а положительные ионы — в кубических отверстия между плоскостями отрицательных ионов.
Правила радиуса
Обсуждение тетраэдра, октаэдра и кубических отверстий в предыдущем разделе предполагает, что структура ионного твердого тела зависит от относительного размера ионов, которые сформировать твердое тело.Относительный размер этих ионов определяется радиусом отношение , которое представляет собой радиус положительного иона, деленный на радиус отрицательного иона.
Связь между координационным числом положительных ионов в ионных твердых телах и отношение радиусов ионы приведены в таблице ниже. По мере увеличения отношения радиусов количество отрицательных ионов, которые могут упаковываться вокруг каждого положительного ион увеличивается. Когда коэффициент радиуса находится между 0.225 и 0,414, положительные ионы стремятся упаковываться в тетраэдрические отверстия между плоскостями отрицательные ионы в кубической или гексагональной плотноупакованной структуре. Когда отношение радиусов составляет от 0,414 до 0,732, положительное значение ионы стремятся упаковываться в октаэдрические дырки между плоскостями отрицательных ионы в плотноупакованной структуре.
Правила соотношения радиусов
| Радиус Передаточное отношение | Координация Номер | Отверстия, в которых Пакет положительных ионов | ||
| 0.225 — 0,414 | 4 | четырехгранных отверстий | ||
| 0,414 — 0,732 | 6 | октаэдрических отверстий | ||
| 0,732 — 1 | 8 | кубических отверстий | ||
| 1 | 12 | Плотноупакованная структура |
Из приведенной выше таблицы следует, что четырехгранные отверстия не используются, пока положительный ион не станет достаточно большим, чтобы коснуться всех четыре отрицательных иона, образующих это отверстие.Поскольку радиус увеличивается с 0,225 до 0,414, положительный ион искажает структура отрицательных ионов в сторону структуры, которая пуристы могут описать как плотно упакованный .
Как только положительный ион станет достаточно большим, чтобы прикоснуться ко всем шести отрицательным ионам в октаэдрическом отверстии, положительный ионы начинают упаковываться в октаэдрические дырки. Эти отверстия используются пока положительный ион не станет настолько большим, что он не сможет поместиться даже в искаженное восьмигранное отверстие.
В конце концов точка достигнута при котором положительный ион больше не может вписываться ни в тетраэдрические или октаэдрические дырки в кристалле с плотнейшей упаковкой. Когда отношение радиусов составляет от 0,732 до 1, ионные твердые частицы имеют тенденцию кристаллизоваться в простой кубический массив отрицательных ионов с положительные ионы, занимающие некоторые или все кубические дырки между эти самолеты. Когда отношение радиусов составляет около 1, положительные ионы могут быть включены непосредственно в позиции плотноупакованная структура.
| Практическая задача 1: следующие соединения имеют аналогичные эмпирические формулы. Использовать правила отношения радиусов и таблица ионных радиусов в приложение, чтобы объяснить, почему у них разные конструкции. (а) NaCl (б) ZnS (в) CsCl Нажмите здесь, чтобы проверить свой ответ на практическую задачу 1 |
На структуру ионных твердых тел также влияют: различия в количестве тетраэдрических и октаэдрических дырок в плотноупакованной структуре.Столько же восьмигранных дыр, так как есть сферы, которые образуют наиболее плотно упакованные структура. Таким образом, если NaCl представляет собой соль 1: 1, в которой Na + ионы занимают октаэдрические дырки в плотноупакованном массиве Cl — . ионов, все октаэдрические дырки в этой структуре должны быть заполненный.
Тетраэдрических отверстий в два раза больше. плотноупакованная структура. Ионы Zn 2+ в ZnS поэтому занимают только половину тетраэдрических отверстий в плотноупакованный массив ионов S 2-.
Справка по викторине: основы металлов
Используйте поиск, чтобы быстро найти ответы на вопросы — откройте окно поиска (ctrl + f), затем введите ключевое слово из вопроса, чтобы перейти к этим терминам в материале курса
Атомное соединение
Материя, как мы ее знаем, существует в трех общих состояниях. Эти три состояния — твердое, жидкое и газообразное. Атомные или молекулярные взаимодействия, происходящие внутри вещества, определяют его состояние. В этой главе мы будем иметь дело в первую очередь с твердыми телами, потому что твердые тела имеют наибольшее значение при инженерных приложениях материалов.Жидкости и газы будут упомянуты только для сравнения.
Твердое вещество удерживается вместе силами, возникающими между соседними атомами или молекулами. Эти силы возникают из-за различий в электронных облаках атомов. Другими словами, валентные электроны или электроны на внешней оболочке атомов определяют их притяжение для своих соседей. Когда физическое притяжение между молекулами или атомами материала велико, материал удерживается вместе. Молекулы в твердых телах тесно связаны между собой.Когда притяжение слабее, вещество может быть в жидкой форме и свободно течь. В газах практически отсутствуют силы притяжения между атомами или молекулами, а их частицы могут свободно перемещаться независимо друг от друга.
Типы связей в материале определяются тем, как силы удерживают материю вместе. На Рисунке 1 показано несколько типов облигаций, их характеристики перечислены ниже
a. Ионная связь — в этом типе связи один или несколько электронов полностью передаются от атома одного элемента к атому другого, и элементы удерживаются вместе силой притяжения из-за противоположной полярности заряда.
г. Ковалентная связь — связь, образованная общими электронами. Электроны разделяются, когда атому нужны электроны для завершения своей внешней оболочки, и он может делиться этими электронами со своим соседом. Тогда электроны являются частью обоих атомов, и обе оболочки заполнены.
г. Металлическая связь — в этом типе связи атомы не разделяют и не обмениваются электронами, чтобы соединиться вместе. Вместо этого многие электроны (примерно по одному на каждый атом) более или менее свободно перемещаются по металлу, так что каждый электрон может взаимодействовать со многими неподвижными атомами.
г. Молекулярная связь — когда электроны нейтральных атомов проводят больше времени в одной области своей орбиты, временный слабый заряд будет существовать. Молекула будет слабо притягивать другие молекулы. Иногда это называют ван-дер-ваальсовыми или молекулярными связями.
эл. Водородная связь — эта связь аналогична молекулярной связи и возникает из-за легкости, с которой атомы водорода готовы отдать электрон атомам кислорода, фтора или азота.
Таблица 1: Пример материалов и их связейТип связи не только определяет, насколько хорошо материал удерживается вместе, но также определяет, какими микроскопическими свойствами обладает материал.Такие свойства, как способность проводить тепло или электрический ток, определяются свободой движения электронов. Это зависит от типа склеивания. Знание микроскопической структуры материала позволяет нам предсказать, как этот материал будет вести себя в определенных условиях. И наоборот, материал может быть изготовлен синтетически с заданной микроскопической структурой, чтобы получить свойства, желательные для определенных технических приложений.
Рисунок 1: Типы связыванияПорядок в микроструктурах
Твердые тела обладают большей межатомной притяженностью, чем жидкости и газы.Однако существуют большие различия в свойствах твердых материалов, используемых в инженерных целях. Свойства материалов зависят от их межатомных связей. Эти же связи также определяют пространство между конфигурациями атомов в твердых телах. Все твердые вещества можно разделить на аморфные или кристаллические.
Аморфный
Аморфные материалы не имеют регулярного расположения своих молекул. Такие материалы, как стекло и парафин, считаются аморфными. Аморфные материалы обладают свойствами твердых тел.Они имеют определенную форму и объем и медленно диффундируют. У этих материалов также отсутствуют четко определенные точки плавления. Во многих отношениях они напоминают жидкости, которые очень медленно текут при комнатной температуре.
Кристаллический
В кристаллической структуре атомы расположены в трехмерном массиве, называемом решеткой. Решетка имеет правильную повторяющуюся конфигурацию во всех направлениях. Группа частиц из одной части кристалла имеет точно такое же геометрическое соотношение, что и группа из любой другой части того же кристалла.
Общие кристаллические структуры
В металлах и во многих других твердых телах атомы расположены в регулярные массивы, называемые кристаллами. Кристаллическая структура состоит из атомов, расположенных по схеме, которая периодически повторяется в трехмерной геометрической решетке. Это повторение вызывают силы химической связи. Именно этот повторяющийся паттерн определяет такие свойства, как прочность, пластичность, плотность (описанная в следующих главах), проводимость (свойство проводить или передавать тепло, электричество и т. Д.).) и форма.
В общем, три наиболее распространенных основных кристаллических структуры, связанные с металлами: (а) объемно-центрированная кубическая, (б) гранецентрированная кубическая и (в) гексагональная плотноупакованная. На рисунке 2 показаны эти три шаблона.
Объемно-центрированный кубический
В объемно-центрированном кубическом (ОЦК) расположении атомов элементарная ячейка состоит из восьми атомов в углах куба и одного атома в центре тела куба.
Гранецентрированный кубический
В гранецентрированном кубическом (FCC) расположении атомов элементарная ячейка состоит из восьми атомов в углах куба и одного атома в центре каждой из граней куба. .
Гексагональная плотноупакованная
В гексагональной плотноупакованной структуре (HCP) элементарная ячейка состоит из трех слоев атомов. Верхний и нижний слои содержат шесть атомов в углах шестиугольника и по одному атому в центре каждого шестиугольника. Средний слой содержит три атома, расположенных между атомами верхнего и нижнего слоев, отсюда и название — плотно упакованные.
Рисунок 2: Общие типы решетокБольшинство диаграмм структурных ячеек для форм железа BCC и FCC нарисованы так, как если бы они были одного размера, как показано на рисунке 2, но это не так.В устройстве BCC структурная ячейка, которая использует только девять атомов, намного меньше.
Металлы, такие как α-железо (Fe) (феррит), хром (Cr), ванадий (V), молибден (Mo) и вольфрам (W), обладают ОЦК-структурой. Эти ОЦК-металлы обладают двумя общими свойствами: высокой прочностью и низкой пластичностью (что допускает остаточную деформацию). Металлы FCC, такие как γ-железо (Fe) (аустенит), алюминий (Al), медь (Cu), свинец (Pb), серебро (Ag), золото (Au), никель (Ni), платина (Pt) и торий (Th), как правило, имеет более низкую прочность и более высокую пластичность, чем металлы с ОЦК.Структуры HCP обнаружены в бериллии (Be), магнии (Mg), цинке (Zn), кадмие (Cd), кобальте (Co), таллии (Tl) и цирконии (Zr).
Если бы вы взяли небольшой кусок обычного металла и исследовали его под микроскопом, вы бы увидели структуру, аналогичную изображенной на рисунке 3 (а). Каждая из световых областей называется зерном или кристаллом, то есть областью пространства, занимаемой непрерывной кристаллической решеткой. Темные линии, окружающие зерна, — это границы зерен. Зернистая структура относится к расположению зерен в металле, причем зерно имеет определенную кристаллическую структуру.Граница зерна относится к внешней области зерна, которая отделяет его от других зерен.
Граница зерен представляет собой область несоответствия между зернами и обычно имеет ширину от одного до трех атомных диаметров. Границы зерен разделяют кристаллические области с различной ориентацией (поликристаллические), в которых кристаллические структуры идентичны. Рисунок 3 (b) представляет четыре зерна разной ориентации и границы зерен, которые возникают на границах раздела между зернами.
Рисунок 3: Зерна и границы (а) Микроскопический (б) АтомныйОчень важной характеристикой металла является средний размер зерна.Размер зерна определяет свойства металла. Например, меньший размер зерна увеличивает прочность на разрыв и имеет тенденцию к увеличению пластичности. Для улучшения свойств ползучести при высоких температурах предпочтительно использовать зерна большего размера. Ползучесть — это остаточная деформация, которая увеличивается со временем при постоянной нагрузке или напряжении. С повышением температуры ползучесть становится все легче.
Еще одним важным свойством зерен является их ориентация. На рис. 4 (а) представлено случайное расположение зерен, при котором ни одно направление внутри зерен не совпадает с внешними границами металлического образца.Эта случайная ориентация может быть получена путем поперечной прокатки материала. Если бы такой образец был достаточно прокатан в одном направлении, он мог бы развить структуру с ориентированными зернами в направлении прокатки, как показано на рисунке 4 (b). Это называется предпочтительной ориентацией. Во многих случаях предпочтительная ориентация очень желательна, но в других случаях она может быть очень вредной. Например, предпочтительная ориентация урановых тепловыделяющих элементов может привести к катастрофическим изменениям размеров во время использования в ядерном реакторе.
Рисунок 4: Ориентация зерен(a) Случайно (b) Предпочтительно
Важная информация в этой главе резюмируется ниже.
Типы связей и их характеристики
- Ионная связь — Атом с одним или несколькими электронами полностью передается от одного элемента к другому, и элементы удерживаются вместе силой притяжения из-за противоположной полярности обвинение.
- Ковалентная связь — Атом, которому нужны электроны для завершения своей внешней оболочки, делит эти электроны со своим соседом.
- Металлическая связь — Атомы не разделяют и не обмениваются электронами для связи друг с другом. Вместо этого многие электроны (примерно по одному на каждый атом) более или менее свободно перемещаются по металлу, так что каждый электрон может взаимодействовать со многими неподвижными атомами.
- Молекулярная связь — Когда нейтральные атомы претерпевают смещение центров своего заряда, они могут слабо притягивать другие атомы со смещенными зарядами. Иногда это называют облигацией Ван-дер-Ваальса.
- Водородная связь — Эта связь аналогична молекулярной связи и возникает из-за легкости, с которой атомы водорода замещают свой заряд.
Порядок в микроструктурах
- Аморфные микроструктуры не имеют четко определенных точек плавления и упорядоченного расположения частиц.
- Кристаллические микроструктуры организованы в трехмерные массивы, называемые решетками.
Типы решеток
- Кристаллическая структура состоит из атомов, расположенных по схеме, которая периодически повторяется в трехмерной геометрической решетке.
- Объемно-центрированная кубическая структура — это структура атомов, в которой элементарная ячейка состоит из восьми атомов в углах куба и одного атома в центре тела куба.
- Гранецентрированная кубическая структура — это расположение атомов, в котором элементарная ячейка состоит из восьми атомов в углах куба и одного атома в центре каждой из шести граней куба.
- Гексагональная плотноупакованная структура — это структура атомов, в которой элементарная ячейка состоит из трех слоев атомов. Верхний и нижний слои содержат шесть атомов в углах шестиугольника и по одному атому в центре каждого шестиугольника. Средний слой состоит из трех атомов, расположенных между атомами верхнего и нижнего слоев.
- Металлы, содержащие структуры BCC, включают феррит, хром, ванадий, молибден и вольфрам. Эти металлы обладают высокой прочностью и низкой пластичностью. Металлы, содержащие структуры FCC, включают аустенит, алюминий, медь, свинец, серебро, золото, никель, платину и торий. Эти металлы обладают низкой прочностью и высокой пластичностью.
- Металлы, содержащие структуры HCP, включают бериллий, магний, цинк, кадмий, кобальт, таллий и цирконий. Металлы HCP не так пластичны, как металлы FCC.
Зернистая структура и граница
- Зерно — это область пространства, занятая сплошной кристаллической решеткой.
- Зернистая структура — это расположение зерен в металле с зерном, имеющим определенную кристаллическую структуру.
- Граница зерна — это внешняя область зерна, которая отделяет его от других зерен.
- Ползучесть — это остаточная деформация, которая увеличивается со временем при постоянной нагрузке или напряжении.
- Малый размер зерна увеличивает прочность на разрыв и пластичность.
Полиморфизм — это свойство или способность металла существовать в двух или более кристаллических формах в зависимости от температуры и состава. Этим свойством обладает большинство металлов и металлических сплавов. Уран — хороший пример металла, проявляющего полиморфизм. Металлический уран может существовать в трех различных кристаллических структурах. Каждая структура существует в определенной фазе, как показано на рисунке 5.
Рисунок 5: Кривая охлаждения для нелегированного урана1. Альфа-фаза, от комнатной температуры до 663 ° C
2.Бета-фаза от 663 ° C до 764 ° C
3. Гамма-фаза от 764 ° C до точки плавления 1133 ° C
Альфа-фаза
Альфа (α) фаза стабильна при комнатной температуре и имеет кристаллическую систему, характеризующуюся тремя неравными осями под прямым углом.
В альфа-фазе свойства решетки различаются по осям X, Y и Z. Это потому, что регулярное повторяющееся состояние атомов отличается. Из-за этого условия при нагревании фаза расширяется в направлениях X и Z и сжимается в направлении Y.На рисунке 6 показано, что происходит с размерами (Å = ангстрем, одна стомиллионная часть сантиметра) элементарной ячейки альфа-урана при нагревании.
Как показано, нагревание и охлаждение альфа-фазы урана может привести к резким изменениям размеров и большим деформациям металла. Таким образом, чистый уран используется не в качестве топлива, а только в сплавах или соединениях.
Рис. 6 Изменение альфа-урнана при нагревании от 0 до 300 ° CБета-фаза
Бета (β) -фаза урана возникает при повышенных температурах.Эта фаза имеет тетрагональную (имеющую четыре угла и четыре стороны) структуру решетки и является довольно сложной.
Гамма-фаза
Гамма (γ) фаза урана образуется при температурах, превышающих температуры, необходимые для стабильности бета-фазы. В гамма-фазе структура решетки является ОЦК и при нагревании расширяется одинаково во всех направлениях.
Дополнительные примеры
Два дополнительных примера полиморфизма перечислены ниже.1. Нагревание чугуна до 907 ° C вызывает переход железа с BCC (альфа, феррит) в форму FCC (гамма, аустенит).
2. Цирконий является HCP (альфа) до 863 ° C, где он переходит в форму BCC (бета, цирконий).
Свойства одной полиморфной формы одного и того же металла будут отличаться от свойств другой полиморфной формы. Например, гамма-железо может растворять до 1,7% углерода, тогда как альфа-железо может растворять только 0,03%.
Сплавы
Сплав представляет собой смесь двух или более материалов, по крайней мере, один из которых является металлом. Сплавы могут иметь микроструктуру, состоящую из твердых растворов, где вторичные атомы вводятся в качестве замещающих или межузельных атомов в кристаллическую решетку.Сплав также может быть кристаллом с металлическим соединением в каждой точке решетки. Кроме того, сплавы могут состоять из вторичных кристаллов, встроенных в первичную поликристаллическую матрицу. Этот тип сплава называется композитным (хотя термин «композит» не обязательно означает, что материалы компонентов являются металлами).
Общие характеристики сплавов
Сплавы обычно прочнее чистых металлов, хотя обычно они обладают пониженной электрической и теплопроводностью.Прочность — важнейший критерий, по которому судят о многих конструкционных материалах. Поэтому сплавы используются для инженерного строительства. Сталь, вероятно, самый распространенный конструкционный металл, является хорошим примером сплава. Это сплав железа и углерода с другими элементами, которые придают ему определенные желаемые свойства.
Как упоминалось в предыдущей главе, иногда материал может состоять из нескольких твердых фаз. Прочность этих материалов повышается за счет превращения твердой структуры в форму, состоящую из двух вкрапленных фаз.Когда рассматриваемый материал представляет собой сплав, можно закалить металл из расплавленного состояния с образованием вкрапленных фаз. Тип и скорость закалки определяют окончательную структуру твердого тела и, следовательно, его свойства.
Нержавеющая сталь типа 304
Нержавеющая сталь типа 304 (содержащая 18-20% хрома и 8-10,5% никеля) используется в баках реакторов для производства трития, трубопроводах технологической воды и исходных технологических теплообменниках. Этот сплав устойчив к большинству видов коррозии.
Состав общих технических материалов
Широкий спектр конструкций, систем и компонентов, используемых в общей промышленности, изготовлен из самых разных материалов. Многие из материалов представляют собой сплавы с основным металлом — железом, никелем или цирконием. Выбор материала для конкретного применения основан на многих факторах, включая температуру и давление, которым будет подвергаться материал, устойчивость материалов к определенным типам коррозии, ударную вязкость и твердость материалов, а также другие свойства материала.
Нержавеющая сталь широко используется в различных системах. Существует около 40 стандартных типов нержавеющей стали и множество других специализированных типов под различными торговыми наименованиями. Изменяя виды и количество легирующих элементов, сталь можно адаптировать к конкретным применениям. Нержавеющие стали классифицируются как аустенитные и ферритные в зависимости от структуры их решетки. Аустенитные нержавеющие стали, включая 304 и 316, имеют гранецентрированную кубическую структуру атомов железа с углеродом в твердом растворе внедрения.Ферритные нержавеющие стали, включая тип 405, имеют объемно-центрированную кубическую решетку железа и не содержат никель. Ферритные стали легче сваривать и изготавливать, и они менее подвержены коррозионному растрескиванию под напряжением, чем аустенитные нержавеющие стали. Они обладают умеренной устойчивостью к другим видам химического воздействия.
Другими металлами, имеющими особые применения в некоторых критических областях, являются инконель и циркалой. Состав этих металлов и различных типов нержавеющей стали приведен в Таблице 2 ниже.
Таблица 2: Типичный состав стандартных технических материалов[HR] Микроскопические дефекты
Микроскопические дефекты обычно классифицируются как точечные, линейные или межфазные дефекты.
1. Точечные дефекты имеют атомные размеры.
2. Линейные дефекты или дислокации обычно имеют длину в несколько атомов.
3. Межфазные дефекты больше линейных дефектов и возникают на двумерной площади.
Точечные дефекты
Точечные дефекты кристаллов можно разделить на три основные категории дефектов.Они проиллюстрированы на рисунке 7.
1. Вакансионные дефекты возникают из-за отсутствия атома в позиции решетки. Дефект вакансионного типа может возникать из-за несовершенной упаковки во время процесса кристаллизации или из-за повышенных тепловых колебаний атомов, вызванных повышенной температурой.
2. Дефекты замещения возникают из-за примеси, присутствующей в позиции решетки.
3. Межузельные дефекты возникают из-за того, что примесь находится в межузельном узле или один из атомов решетки находится в межузельном положении, а не в его решеточной позиции.Межузельное пространство относится к местоположениям между атомами в решетчатой структуре.
Примеси внедрения, называемые модификаторами сетки, действуют как точечные дефекты в аморфных твердых телах. Наличие точечных дефектов может повысить или снизить ценность материала для инженерного строительства в зависимости от предполагаемого использования.
Рисунок 7: Точечные дефектыЛинейные дефекты
Рисунок 8: Линейные дефекты (дислокации)Линейные дефекты называются дислокациями и возникают только в кристаллических материалах.Дислокации могут быть краевыми, винтовыми или смешанными, в зависимости от того, как они искажают решетку, как показано на рисунке 8. Важно отметить, что дислокации не могут заканчиваться внутри кристалла. Они должны заканчиваться краем кристалла или другой дислокацией, или они должны замыкаться сами на себя.
Краевые дислокации представляют собой дополнительный ряд или плоскость атомов в кристаллической структуре. Дефект может проходить по прямой линии на всем протяжении кристалла или по неправильной траектории.Он также может быть коротким, простираясь лишь на небольшое расстояние в кристалл, вызывая скольжение на одно атомное расстояние вдоль плоскости скольжения (направление движения краевого дефекта).
Скольжение происходит, когда кристалл подвергается напряжению, и дислокация движется через кристалл, пока не достигнет края или не будет остановлена другой дислокацией, как показано на рисунке 9. Позиция 1 показывает нормальную кристаллическую структуру. Положение 2 показывает силу, приложенную с левой стороны, и противодействующую силу, приложенную с правой стороны.Позиции с 3 по 5 показывают, как конструкция скользит. Позиция 6 показывает окончательно деформированную кристаллическую структуру. Скольжение одной активной плоскости обычно составляет порядка 1000 атомных расстояний, и для получения податливости требуется проскальзывание во многих плоскостях.
Винтовые дислокации могут быть образованы разрывом кристалла параллельно направлению скольжения. Если винтовая дислокация прослеживается на всем протяжении всей цепи, это покажет картину проскальзывания, аналогичную картине винтовой резьбы. Рисунок может быть как левым, так и правым.Для этого необходимо, чтобы некоторые из атомных связей постоянно переформировывались, так что кристалл после получения имеет почти такую же форму, что и раньше.
Ориентация дислокаций может варьироваться от чистого края до чистого винта. В какой-то промежуточный момент они могут обладать характеристиками как кромки, так и винта. Важность дислокаций основана на легкости, с которой они могут перемещаться через кристаллы.
Дефекты интерфейса
Дефекты интерфейса существуют под углом между любыми двумя гранями кристалла или кристаллической формы.Эти дефекты обнаруживаются на свободных поверхностях, границах доменов, границах зерен или межфазных границах. Свободные поверхности — это границы раздела между газами и твердыми телами. Границы домена относятся к интерфейсам, где электронные структуры различны с обеих сторон, заставляя каждую сторону действовать по-разному, хотя с обеих сторон существует одинаковое атомное расположение. Границы зерен существуют между кристаллами с одинаковой структурой решетки, которые имеют разную пространственную ориентацию. Поликристаллические материалы состоят из множества зерен, разделенных расстоянием, обычно равным нескольким атомным диаметрам.Наконец, межфазные границы существуют между областями, где материалы существуют в разных фазах (то есть, ОЦК рядом со структурами ГЦК).
Макроскопические дефекты
Трехмерные макроскопические дефекты называются объемными дефектами. Обычно они возникают в гораздо большем масштабе, чем микроскопические дефекты. Эти макроскопические дефекты обычно появляются в материале во время очистки от его необработанного состояния или в процессе изготовления.
Самый распространенный дефект в объеме возникает из-за попадания посторонних частиц в основной материал.Эти частицы второй фазы, называемые включениями, редко используются, поскольку они значительно изменяют структурные свойства. Примером включения могут быть частицы оксида в чистом металле или кусочек глины в структуре стекла.
К другим объемным дефектам относятся газовые карманы или усадочные полости, обычно встречающиеся в отливках. Эти промежутки ослабляют материал и, следовательно, защищены от повреждений во время изготовления. Обработка и ковка металлов могут вызвать трещины, которые действуют как концентраторы напряжений и ослабляют материал.Любые дефекты сварки или соединения также могут быть классифицированы как объемные дефекты.
Важная информация в этой главе кратко изложена ниже.
Полиморфизм
- Полиморфизм — это свойство или способность металла существовать в двух или более кристаллических формах в зависимости от температуры и состава.
- Металл может существовать в трех фазах или кристаллических структурах.
- Металлические фазы урана:
- Альфа — от комнатной температуры до 663 ° C
- Бета — от 663 ° C до 764 ° C
- Гамма — от 764 ° C до 1133 ° C
- Альфа-фаза предотвращает образование чистого урана используется в качестве топлива из-за свойств расширения.
Сплавы
- Сплав представляет собой смесь двух или более материалов, по крайней мере, один из которых является металлом.
- Микроструктуры сплавов
- Твердые растворы, в которых вторичные атомы введены в качестве замещающих или межузельных атомов в кристаллическую решетку.
- Кристалл с металлическими связями
- Композиты, в которых вторичные кристаллы заключены в первичную поликристаллическую матрицу.
- Сплавы обычно прочнее чистых металлов, хотя сплавы обычно имеют меньшую электрическую и теплопроводность, чем чистые металлы.
- Двумя желательными свойствами нержавеющей стали типа 304 являются коррозионная стойкость и высокая прочность.
Микроскопические дефекты
- Точечные дефекты находятся в диапазоне размеров отдельных атомов.
- Линейные (дислокационные) дефекты обычно имеют длину в несколько атомов. Неровности линий могут быть краевыми, винтовыми или смешанными, в зависимости от искажения решетки. Недостатки линий не могут заканчиваться внутри кристалла; они должны заканчиваться на краю кристалла или другой дислокации или закрываться сами собой.
- Межфазные дефекты больше, чем дефекты линий, и возникают на двумерной области. Межфазные дефекты существуют на свободных поверхностях, границах доменов, границах зерен или межфазных границах.
- Скольжение возникает, когда кристалл подвергается напряжению, и дислокации проходят через кристалл, пока не достигнут края или не будут остановлены другой дислокацией.
Макроскопические дефекты
- Объемные дефекты — это трехмерные дефекты.
- Инородные частицы, входящие в состав основного материала (включения), являются наиболее распространенным дефектом объема
- Газовые карманы
- Усадочные полости
- Дефекты сварки или соединения
Определение напряжения
Когда металл подвергается нагрузке ( сила), он искажается или деформируется, независимо от того, насколько прочен металл или легкая нагрузка. Если нагрузка небольшая, искажение, вероятно, исчезнет при снятии нагрузки
. Интенсивность или степень искажения называется напряжением.Если деформация исчезает и металл возвращается к своим первоначальным размерам после снятия нагрузки, деформация
называется упругой деформацией. Если деформация исчезает, а металл остается деформированным, тип деформации называется пластической деформацией. Подробнее о штамме мы поговорим в следующей главе.
Когда к металлу прилагается нагрузка, сама атомная структура деформируется, сжимается, деформируется или растягивается в процессе. Атомы, составляющие металл, расположены в определенном геометрическом узоре
, характерном для этого конкретного металла или сплава, и поддерживаются в этом узоре за счет межатомных сил.При таком расположении атомы находятся в состоянии с минимальной энергией, и
стремится оставаться в этом состоянии. Над металлом нужно работать (то есть нужно добавлять энергию), чтобы исказить атомный узор. (Работа равна силе, умноженной на расстояние, на которое перемещается сила
.)
Напряжение — это внутреннее сопротивление или противодействие материала искажающим эффектам внешней силы или нагрузки. Эти противодействующие силы стремятся вернуть атомы в их нормальное положение.
Полное развиваемое сопротивление равно внешней нагрузке.Это сопротивление известно как стресс.
Хотя невозможно измерить интенсивность этого напряжения, можно измерить внешнюю нагрузку и площадь
, к которой она приложена. Напряжение (и) можно приравнять к нагрузке на единицу площади или силе (F), приложенной к площади поперечного сечения (A) перпендикулярно силе, как показано в уравнении
(2-1).
Напряжение = σ = F / A (2-1)
где:
s = напряжение (фунты на кв. Дюйм или фунты силы на дюйм 2)
F = приложенная сила (фунты силы на дюйм 2)2)
A = площадь поперечного сечения (дюйм 2)
Типы напряжений
Напряжения возникают в любом материале, который подвергается нагрузке или приложенной силе. Существует много типов напряжений, но все они могут быть классифицированы по одной из шести категорий: остаточные напряжения
, структурные напряжения, напряжения давления, напряжения течения, термические напряжения и усталостные напряжения.
Остаточное напряжение
Остаточное напряжение возникает из-за производственных процессов, которые создают напряжения в материале.Сварка оставляет в свариваемых металлах остаточные напряжения. Напряжения, связанные со сваркой, обсуждаются далее в этом модуле.
Структурное напряжение
Структурные напряжения — это напряжения, возникающие в элементах конструкции из-за веса, который они поддерживают. Вес обеспечивает нагрузки. Эти напряжения обнаруживаются в фундаментах и каркасах зданий, а также в деталях машин.
Напряжения давления
Напряжения давления — это напряжения, возникающие в сосудах, содержащих материалы под давлением.Нагрузка обеспечивается той же силой, что и давление.
Напряжения потока
Напряжения потока возникают, когда масса текущей жидкости создает динамическое давление на стенку трубы. Сила удара жидкости о стену действует как нагрузка. Этот тип напряжения может проявляться неустойчиво при колебаниях расхода. Гидравлический удар является примером кратковременного напряжения течения.
Термические напряжения
Термические напряжения существуют всякий раз, когда в материале присутствуют градиенты температуры.Разные температуры вызывают разное расширение и подвергают материалы внутреннему напряжению. Этот тип напряжения особенно заметен в механизмах, работающих при высоких температурах и охлаждаемых холодной жидкостью.
Усталостные напряжения
Усталостные напряжения возникают из-за циклического приложения напряжения. Напряжения могут быть вызваны вибрацией или термоциклированием.
Важность всех напряжений возрастает, когда поддерживающие их материалы имеют дефекты. Дефекты обычно добавляют материалу дополнительную нагрузку.Кроме того, когда нагрузки циклические или нестационарные, напряжения могут сильнее влиять на материал. Дополнительные напряжения, связанные с дефектами и циклическими нагрузками, могут превышать напряжение, необходимое для разрушения материала.Типы приложенного напряжения
Интенсивность напряжения в теле компонента выражается как один из трех основных типов внутренней нагрузки. Они известны как растяжение, сжатие и сдвиг. На рисунке 1 показаны различные типы стресса. Математически существует только два типа внутренней нагрузки, поскольку растягивающее и сжимающее напряжение можно рассматривать как положительную и отрицательную версии одного и того же типа нормальной нагрузки.
Однако в механической конструкции реакция компонентов на два условия может быть настолько различной, что лучше и безопаснее рассматривать их как отдельные типы.
Как показано на рисунке 1, плоскость растягивающего или сжимающего напряжения лежит перпендикулярно оси действия силы, от которой оно возникает. Плоскость касательного напряжения лежит в плоскости силовой системы, из которой оно исходит. Важно, чтобы эти различия
были достаточно ясными как в уме, так и в способах выражения.
Растягивающее напряжение
Растягивающее напряжение — это тип напряжения, при котором два участка материала по обе стороны от плоскости напряжения имеют тенденцию разъединяться или удлиняться, как показано на Рисунке 1 (а) .
Напряжение сжатия
Напряжение сжатия противоположно растягивающему напряжению. Соседние части материала имеют тенденцию давить друг на друга через типичную плоскость напряжения, как показано на рисунке 1 (b).
Напряжение сдвига
Напряжение сдвига существует, когда две части материала имеют тенденцию скользить друг по другу в любой типичной плоскости сдвига при приложении силы, параллельной этой плоскости, как показано на Рисунке 1 (c).
Оценка механических свойств производится по трем основным типам напряжений. Поскольку растягивающие и сжимающие нагрузки создают напряжения, действующие поперек плоскости, в направлении, перпендикулярном (нормальном) к плоскости, растягивающие и сжимающие напряжения называются нормальными напряжениями. Сокращенные обозначения следующие.Для растягивающих напряжений: «+ S N » (или «S N ») или «σ» (сигма)
Для сжимающих напряжений: «-S N » или «-σ» (минус сигма)
Способность материала реагировать на сжимающее напряжение или давление называется сжимаемостью .Например, металлы и жидкости несжимаемы, а газы и пары сжимаемы. Напряжение сдвига равно силе, деленной на площадь поверхности, параллельную направлению, в котором действует сила, как показано на рисунке 1 (c).
Два типа напряжения могут присутствовать одновременно в одной плоскости, при условии, что одно из напряжений является напряжением сдвига. При определенных условиях в материале могут одновременно присутствовать различные комбинации основных типов напряжений. Примером может служить корпус реактора во время работы.Стена испытывает растягивающее напряжение в различных местах из-за температуры и давления жидкости, действующей на стену. Напряжение сжатия прикладывается снаружи к другим участкам стены из-за внешнего давления, температуры и сжатия опор, связанных с резервуаром. В этой ситуации растягивающие и сжимающие напряжения считаются главными напряжениями. Если присутствует, напряжение сдвига будет действовать под углом 90 ° к главному напряжению.
Деформация
Определение деформации
При использовании металла в машиностроении определенное напряженное состояние обычно существует в значительном объеме материала.Реакция атомной структуры проявится в макроскопическом масштабе. Следовательно, всякий раз, когда к металлу прикладывается напряжение (независимо от того, насколько оно маленькое), должно происходить пропорциональное изменение размеров или искажение.
Такое пропорциональное изменение размеров (интенсивность или степень деформации) называется деформацией и измеряется как общее удлинение на единицу длины материала из-за некоторого приложенного напряжения. Уравнение 2-2 иллюстрирует эту пропорцию или искажение.
Деформация = ε = δ / л (2-2)
где:
ε = деформация (дюйм./ дюйм)
δ = общее удлинение (дюйм)
L = исходная длина (дюйм)
Типы деформации
Деформация может иметь две формы; упругая деформация и пластическая деформация.
Упругая деформация
Упругая деформация — это временное изменение размеров, которое существует только при приложении исходного напряжения и исчезает сразу после снятия напряжения. Упругая деформация также называется упругой деформацией. Приложенные напряжения заставляют атомы в кристалле перемещаться из положения равновесия.Все атомы смещаются на одинаковую величину и при этом сохраняют свою относительную геометрию. Когда напряжения снимаются, все атомы возвращаются в исходное положение, и остаточная деформация не происходит.
Пластическая деформация
Пластическая деформация (или пластическая деформация) — это изменение размеров, которое не исчезает при снятии инициирующего напряжения. Обычно это сопровождается некоторой упругой деформацией.
Явления упругой деформации и пластической деформации в материале называются соответственно упругостью и пластичностью.При комнатной температуре большинство металлов обладают некоторой эластичностью, которая проявляется при малейшем напряжении. Обычно они также обладают некоторой пластичностью, но это может не проявиться до тех пор, пока напряжение не будет заметно увеличено. Величина пластической деформации, когда она действительно возникает, вероятно, будет намного больше, чем величина упругой деформации для данного приращения напряжения. Металлы, вероятно, будут демонстрировать меньшую эластичность и большую пластичность при повышенных температурах. Некоторые чистые нелегированные металлы (особенно алюминий, медь и золото) демонстрируют небольшую эластичность, если она вообще есть, при напряжении в отожженном (нагретом и затем медленно охлаждаемом для предотвращения хрупкости) состоянии при комнатной температуре, но действительно демонстрируют заметную пластичность.Некоторые нелегированные металлы и многие сплавы обладают заметной эластичностью при комнатной температуре, но не обладают пластичностью.
Напряженное состояние непосредственно перед тем, как начинает проявляться пластическая деформация, называется пределом пропорциональности или пределом упругости и определяется уровнем напряжения и соответствующим значением упругой деформации. Предел пропорциональности выражается в фунтах на квадратный дюйм. Для интенсивностей нагрузки, превышающей предел пропорциональности, деформация состоит как из упругих, так и из пластических деформаций.
Как упоминалось ранее в этой главе, деформация измеряет пропорциональное изменение размеров без приложения нагрузки.Такие значения деформации легко определяются и перестают быть достаточно точными только тогда, когда пластическая деформация становится доминирующей.
Когда металл подвергается деформации, его объем остается постоянным. Следовательно, если объем остается постоянным при изменении размера на одной оси, то размеры по крайней мере еще одной оси должны измениться. Если одно измерение увеличивается, другое должно уменьшаться. Есть несколько исключений. Например, деформационное упрочнение включает поглощение энергии деформации в структуре материала, что приводит к увеличению в одном измерении без смещения уменьшения в других измерениях.Это приводит к уменьшению плотности материала и увеличению объема.
Если к материалу приложена растягивающая нагрузка, материал будет вытягиваться по оси нагрузки (перпендикулярно плоскости растягивающего напряжения), как показано на Рисунке 2 (а). И наоборот, если нагрузка сжимающая, осевой размер уменьшится, как показано на рисунке 2 (b). Если объем постоянный, должно произойти соответствующее поперечное сжатие или расширение. Это поперечное изменение будет иметь постоянную связь с осевой деформацией.Отношение или отношение поперечной деформации к осевой называется коэффициентом Пуассона по имени его первооткрывателя. Обычно обозначается буквой ν.
Деформация кубических структур
Может ли материал пластически деформироваться при низких приложенных напряжениях, зависит от его структуры решетки. Плоскостям атомов легче скользить друг по другу, если эти плоскости плотно упакованы. Поэтому решетчатые структуры с плотноупакованными плоскостями допускают большую пластическую деформацию, чем неупакованные.Кроме того, структуры кубической решетки позволяют легче проскальзывать, чем некубические решетки. Это происходит из-за их симметрии, которая обеспечивает плотную упаковку плоскостей в нескольких направлениях. Большинство металлов состоит из объемно-центрированных кубических (ОЦК), гранецентрированных кубических (ГЦК) или гексагональных плотноупакованных (ГПУ) кристаллов, которые более подробно обсуждаются в Модуле 1, Структура металлов. Кубическая гранецентрированная кристаллическая структура будет легче деформироваться под нагрузкой перед разрушением, чем объемно-центрированная кубическая структура.
ОЦК-решетка хоть и кубическая, но не плотно упакована и образует прочные металлы. α-железо и вольфрам имеют форму ОЦК. Решетка FCC имеет кубическую форму, плотно упакована и образует более пластичные материалы. γ-железо, серебро, золото и свинец имеют структуру FCC. Наконец, решетки HCP имеют плотную упаковку, но не кубическую. Металлы HCP, такие как кобальт и цинк, не так пластичны, как металлы FCC.
Рис. 11: Изменение формы цилиндра под действием напряженияВажная информация в этой главе кратко изложена ниже.
- Напряжение — это внутреннее сопротивление материала искажающим воздействиям внешней силы или нагрузки.
Напряжение = σ = F / A
- Три типа напряжения
- Растягивающее напряжение — это тип напряжения, при котором два участка материала по обе стороны от плоскости напряжения имеют тенденцию разъединяться или удлиняться.
- Напряжение сжатия противоположно растягивающему. Соседние части материала имеют тенденцию прижиматься друг к другу.
- Напряжение сдвига возникает, когда две части материала имеют тенденцию скользить друг по другу при приложении силы, параллельной этой плоскости.
- Сжимаемость — это способность материала реагировать на сжимающее напряжение или давление.
- Деформация — это пропорциональное изменение размеров, или интенсивность, или степень деформации материала, находящегося под напряжением.
Деформация = ε = δ / L
- Пластическая деформация — это изменение размеров, которое не исчезает при снятии инициирующего напряжения.
- Предел пропорциональности — это величина напряжения непосредственно перед точкой (порогом), в которой начинает появляться пластическая деформация, или уровень напряжения и соответствующее значение упругой деформации.
- Два типа деформации:
- Упругая деформация — это временное изменение размеров, которое существует только при приложении исходного напряжения и исчезает сразу после снятия напряжения.
- Пластическая деформация (пластическая деформация) — это изменение размеров, которое не исчезает при снятии инициирующего напряжения.
- Кубические гранецентрированные кристаллические структуры γ-железа легче деформируются под нагрузкой перед разрушением, чем объемноцентрированные кубические структуры α-железа.
Закон Хука
Если металл находится под небольшим напряжением, имеет место временная деформация, предположительно разрешенная упругим смещением атомов в пространственной решетке. Снятие напряжения приводит к постепенному возвращению металлу первоначальной формы и размеров. В 1678 году английский ученый Роберт Гук провел эксперименты, в ходе которых были получены данные, которые показали, что в диапазоне упругости материала деформация пропорциональна напряжению. Удлинение стержня прямо пропорционально растягивающей силе и длине стержня и обратно пропорционально площади поперечного сечения и модулю упругости.
Экспериментальный закон Гука может быть задан уравнением (2-3).
δ = P l / A E (2-3)
Эта простая линейная зависимость между силой (напряжением) и удлинением (деформацией) была сформулирована с использованием следующих обозначений.
P = усилие, создаваемое удлинением стержня (фунт-сила)
l = длина стержня (дюймы)
A = площадь поперечного сечения стержня (дюймы 2)
δ = общее удлинение стержня (дюймы)
E = постоянная упругости материала, называемая модулем упругости или модулем Юнга (фунт-сила / дюйм. 2 )
Величина E, отношение единичного напряжения к единичной деформации, является модулем упругости материала при растяжении или сжатии и часто называется модулем Юнга.
Ранее мы узнали, что растягивающее напряжение или просто напряжение приравнивается к нагрузке на единицу площади или силе, приложенной к площади поперечного сечения, перпендикулярной силе, измеренной в фунтах силы на квадратный дюйм.
σ = P / A (2-4)
Мы также узнали, что деформация при растяжении или удлинение стержня на единицу длины определяется следующим образом:
ε = δ / l (2-5)
Таким образом , условия описанного выше эксперимента адекватно выражаются законом Гука для упругих материалов.Для материалов при растяжении деформация (ε) пропорциональна приложенному напряжению σ.
ε = σ / E (2-6)
, где
E = модуль Юнга (фунт-сила / дюйм 2 )
σ = напряжение (фунт / кв. Дюйм)
ε = деформация (дюйм / дюйм)
Модуль Юнга (модуль упругости)
Модуль Юнга (иногда называемый модулем упругости, что означает «мера» упругости) является чрезвычайно важной характеристикой материала. Это численная оценка закона Гука, а именно отношения напряжения к деформации (мера сопротивления упругой деформации).Для расчета модуля Юнга напряжение (в любой точке) ниже пропорционального предела делится на соответствующую деформацию. Его также можно рассчитать как наклон прямолинейного участка кривой напряжения-деформации. (Расположение на кривой напряжение-деформация будет обсуждено позже.)
E = Модуль упругости = напряжение / деформация = фунт / кв. Дюйм. Дюйм = фунт / кв. Дюйм
или
E = σ / ε (2-7)
Теперь мы видим, что модуль Юнга можно легко вычислить при условии, что напряжение и соответствующее удлинение или деформация единицы были определены с помощью испытания на растяжение, как описано ранее.Деформация (ε) — это число, представляющее отношение двух длин; следовательно, мы можем сделать вывод, что модуль Юнга измеряется в тех же единицах, что и напряжение (σ), то есть в фунтах на квадратный дюйм. В таблице 1 приведены средние значения модуля упругости E для нескольких металлов, используемых в промышленности. Предел текучести и предел прочности будут более подробно обсуждены в следующем разделе ниже.
Таблица 1: Свойства обычных конструкционных материалов Пример:Каково удлинение 200 дюймов алюминиевой проволоки с 0.01 квадратный дюйм, если он выдерживает вес 100 фунтов?
Решение:
δ = Pl / AE (2-8)
= (100 фунтов) (200 дюймов) / (0,01 дюйма) 2 (1,0 x 10 7 фунт / дюйм 2 )
δ = 0,2 дюйма
Модули упругости
Модули упругости , относящиеся к поликристаллическому материалу, — это модуль упругости Юнга, модуль упругости при сдвиге и модуль упругости в объеме.
Модуль упругости
Модуль упругости Юнга — это модуль упругости для напряжения при растяжении и сжатии, который обычно оценивается с помощью испытаний на растяжение.Модуль упругости Юнга подробно обсуждается выше.
Модуль упругости
Модуль упругости при сдвиге определяется при кручении цилиндрического испытательного образца. Его символ — G.
Объемный модуль
Объемный модуль упругости — это упругая реакция на гидростатическое давление и равностороннее растяжение или объемная реакция на гидростатическое давление и равностороннее растяжение. Это также свойство материала, которое определяет упругую реакцию на приложение напряжения.
Испытания на растяжение (нагрузку) и кривые растяжения
Для определения несущей способности и величины деформации перед разрушением образец материала обычно испытывают с помощью Испытания на растяжение . Это испытание заключается в приложении постепенно увеличивающейся силы натяжения на одном конце отрезка материала. Другой конец закрепляется на жесткой опоре, так что образец медленно разрывается. Испытательная машина оснащена устройством для индикации и, возможно, записи величины силы на протяжении всего испытания.Одновременно производятся измерения увеличивающейся длины выбранного участка в середине образца, называемого измерительной длиной. Измерения нагрузки и удлинения обычно прекращают вскоре после начала пластической деформации; однако всегда записывается достигнутая максимальная нагрузка. Точка разрушения — это точка разрушения материала из-за пластической деформации. После того, как образец был разорван и извлечен из машины, сломанные концы соединяют вместе и проводят измерения увеличенной теперь измерительной длины и среднего диаметра минимального поперечного сечения.Средний диаметр минимального поперечного сечения измеряется только в том случае, если используемый образец является цилиндрическим.
Табличные результаты в конце теста состоят из следующего.
а. обозначение испытуемого материала
б. исходные размеры поперечного сечения образца в пределах измерительной длины
c. исходная длина колеи
д. серия частых считываний, определяющих нагрузку и соответствующий размер измерительной длины
e. конечный средний диаметр минимального сечения
ф.конечная длина колеи
г. описание внешнего вида поверхностей излома (например, чашка-конус, волчье ухо, диагональ, начало)
График результатов строится на основе табличных данных. Некоторые испытательные машины оснащены автографом, который рисует график во время теста. (Оператору не нужно записывать какие-либо показания нагрузки или удлинения, кроме максимума для каждого из них.) Оси координат на графике представляют собой деформацию для оси x или шкалу абсцисс и напряжение для оси y или шкалу ординат.Ордината для каждой точки, нанесенной на график, находится путем деления каждой из табличных нагрузок на исходную площадь поперечного сечения образца; соответствующая абсцисса каждой точки находится путем деления увеличения измерительной длины на исходную измерительную длину. Эти два расчета производятся следующим образом.
Напряжение = нагрузка / площадь исходного поперечного сечения = P / A
o = фунт / кв. Дюйм или фунт / дюйм 2 (2-9)Деформация = (мгновенная расчетная длина — исходная) / исходная расчетная длина = удлинение / исходная расчетная длина (2-10)
= (L — L
o) / L o = дюймы на дюйм x 100 = удлинение в процентах (2-11)Рассчитанные здесь напряжения и деформации иногда являются называется «инженерное напряжение и деформация».Это не истинные напряжения и деформации, которые можно вычислить на основе площади и расчетной длины, которые существуют
для каждого приращения нагрузки и деформации. Например, истинная деформация — это натуральный логарифм удлинения (ln (L / Lo)), а истинное напряжение — это P / A, где A — площадь. Последние значения обычно используются для научных исследований, но инженерные значения полезны для определения значений несущей способности материала. Ниже предела упругости инженерное напряжение и истинное напряжение практически идентичны.
Графические результаты или диаграмма напряжения-деформации типичного испытания на растяжение конструкционной стали показаны на рисунке 3. Отношение напряжения к деформации, или градиент графика напряжения-деформации, называется модулем упругости или Модуль упругости. Наклон части кривой, где напряжение пропорционально деформации (между точками 1 и 2), называется модулем Юнга, и применяется закон Гука.
Следующие наблюдения проиллюстрированы на рисунке 3: Рисунок 3: Типичная кривая напряжения-деформации пластичного материалаЗакон Гука применяется между точками 1 и 2.
Закон Гука становится спорным между пунктами 2 и 3, и напряжение увеличивается быстрее.
Область между точками 1 и 2 называется эластичной областью. Если снять напряжение, материал вернется к своей исходной длине.
Точка 2 — это предел пропорциональности (PL) или предел упругости, а точка 3 — это предел текучести (YS) или предел текучести.
Область между точками 2 и 5 известна как пластиковая область, потому что материал не вернется к своей исходной длине.
Точка 4 — это точка предела прочности, а точка 5 — точка разрушения, в которой происходит разрушение материала.
Рисунок 3 представляет собой кривую зависимости напряжения от деформации, типичную для пластичного материала, где прочность мала, а область пластичности велика. Материал будет выдерживать большее напряжение (деформацию) перед разрушением.
На рис. 4 представлена кривая напряжения-деформации, типичная для хрупкого материала, где пластическая область мала, а прочность материала высока.
Рис. 4: Типичная кривая напряжения-деформации хрупкого материалаИспытание на растяжение позволяет получить три описательных факта о материале.Это напряжение, при котором начинается наблюдаемая пластическая деформация или «податливость»; предел прочности при растяжении или максимальная интенсивность нагрузки, которую можно нести при растяжении; и относительное удлинение или деформация (величина, на которую материал будет растягиваться) и соответствующее процентное уменьшение площади поперечного сечения, вызванное растяжением. Также можно определить точку разрыва или перелома.
Важная информация в этой главе кратко изложена ниже.
- Закон Гука гласит, что в диапазоне упругости материала деформация пропорциональна напряжению.Он измеряется с помощью следующего уравнения:
δ = Pl / AE
- Модуль Юнга (модуль упругости) — это отношение напряжения к деформации или градиент графика «напряжение-деформация». Он измеряется с использованием следующего уравнения:
E = σ / ε
Объемный модуль упругости
- Объемный модуль упругости — это упругая реакция на гидростатическое давление и равностороннее растяжение или объемная реакция на гидростатическое давление и равностороннее растяжение.Это также свойство материала, которое определяет упругую реакцию на приложение напряжения.
- Точка разрушения — это точка разрушения материала из-за пластической деформации.
- Пластичный материал деформируется (удлиняется) больше, чем хрупкий, как показано на рисунках в тексте. Кривые напряжения-деформации, обсуждаемые в этой главе для пластичных и хрупких материалов, демонстрируют, как каждый материал будет реагировать на напряжение и деформацию.
- На рисунках 3 и 4 показаны особенности пластичного и хрупкого материала соответственно.Закон Гука применяется между точками 1 и 2. Упругая область находится между точками 1 и 2. Пластическая область находится между точками 2 и 5.
Прочность
Прочность — это способность материала сопротивляться деформации. Прочность компонента обычно определяется исходя из максимальной нагрузки, которую можно выдержать до того, как разрушение станет очевидным. Если при простом растяжении остаточная деформация (пластическая деформация), которая имеет место в компоненте до разрушения, несущая способность в момент окончательного разрыва, вероятно, будет меньше максимальной нагрузки, поддерживаемой при более низкой деформации, поскольку нагрузка наносится на значительно меньшую площадь поперечного сечения.При простом сжатии нагрузка при разрыве будет максимальной, применимой на значительно увеличенной площади по сравнению с площадью поперечного сечения без нагрузки.
Эту неясность можно преодолеть, используя номинальное значение напряжения для растяжения и сдвига. Это определяется делением соответствующей максимальной нагрузки на исходную площадь поперечного сечения компонента. Таким образом, прочность материала — это максимальное номинальное напряжение, которое он может выдержать. Номинальное напряжение упоминается при цитировании «прочности» материала и всегда определяется типом напряжения, например пределом прочности на растяжение, пределом прочности на сжатие или пределом прочности на сдвиг.
Для большинства конструкционных материалов трудность определения прочности на сжатие может быть преодолена путем замены значения прочности на сжатие значением прочности на растяжение. Эта замена является безопасным предположением, поскольку номинальная прочность на сжатие всегда больше номинальной прочности на разрыв, поскольку эффективное поперечное сечение увеличивается при сжатии и уменьшается при растяжении.
Когда к металлу прикладывается сила, слои атомов внутри кристаллической структуры перемещаются по отношению к соседним слоям атомов.Этот процесс называется скольжением. Границы зерен имеют тенденцию предотвращать скольжение. Чем меньше размер зерна, тем больше площадь границы зерна. Уменьшение размера зерна в результате холодной или горячей обработки металла имеет тенденцию замедлять скольжение и, таким образом, увеличивает прочность металла. Холодная и горячая обработка обсуждаются в следующей главе.
Предел прочности на разрыв
Рис. 3. Кривая деформации-деформации для типичного пластичного материалаПредел прочности на разрыв (UTS) — это максимальное сопротивление разрушению.Это эквивалентно максимальной нагрузке, которую может выдержать один квадратный дюйм площади поперечного сечения, когда нагрузка прилагается как простое натяжение. Он выражается в фунтах на квадратный дюйм.
UTS = максимальная нагрузка / площадь исходного поперечного сечения = P
max / A o = psiЕсли доступна полная инженерная кривая напряжения-деформации, как показано на Рисунке 3, предел прочности при растяжении отображается как значение координаты напряжения в самой высокой точке кривой. Материалы, которые сильно удлиняются перед разрушением, подвергаются такому значительному уменьшению площади поперечного сечения, что материал будет нести меньшую нагрузку на заключительных этапах испытания (это было отмечено на рисунках 3 и 4 уменьшением напряжения непосредственно перед разрывом). .Заметное уменьшение поперечного сечения называется «сужением». Предел прочности на разрыв часто сокращают до «прочности на разрыв» или даже до «предела». Иногда используется термин «максимальная сила», но он может вводить в заблуждение и поэтому не используется в некоторых дисциплинах.
Предел текучести
Рис. 5: Кривая напряжения-деформации типичного хрупкого материалаРяд терминов был определен с целью определения напряжения, при котором начинается пластическая деформация. Чаще всего для этой цели используется предел текучести.Предел текучести определяется как напряжение, при котором возникает заданная величина остаточной деформации. Графическая часть ранних стадий испытания на растяжение используется для оценки предела текучести. Для определения предела текучести заданная величина остаточной деформации устанавливается вдоль оси деформации графика справа от начала координат (ноль). Это обозначено на Рисунке 5 как Точка (D). Rev. 0
Прямая линия проведена через точку (D) Рис. 5 Типичная кривая напряжения-деформации хрупкого материала с тем же наклоном, что и начальный участок кривой напряжения-деформации.Точка пересечения новой линии и кривой деформации проецируется на ось напряжений. Значение напряжения в фунтах на квадратный дюйм — это предел текучести. Это обозначено на рисунке 5 как точка 3. Этот метод построения графика выполняется с целью вычитания упругой деформации из общей деформации, оставляя предварительно определенное «постоянное смещение» в качестве остатка. Когда указывается предел текучести, следует указывать величину смещения, использованную при определении. Например, «Предел текучести (при 0.2% смещения) = 51 200 фунтов на кв. Дюйм ».
Примеры предела текучести
Ниже приведены некоторые примеры предела текучести металлов.
Алюминий от 3,5 x 104 до 4,5 x 104 фунтов на кв. Дюйм
Нержавеющая сталь от 4,0 x 104 до 5,0 x 104 фунтов на кв. Дюйм
Углеродистая сталь от 3,0 x 104 до 4,0 x 104 фунтов на кв. Дюйм
Альтернативные значения
Иногда вместо предела текучести используются альтернативные значения . Некоторые из них кратко описаны ниже.
• Предел текучести , определяемый методом делителя, предполагает наличие наблюдателя с парой разделителей, наблюдающего за видимым удлинением между двумя контрольными отметками на образце.Когда происходит видимое растяжение, нагрузка в этот момент записывается, и рассчитывается напряжение, соответствующее этой нагрузке.
• Мягкая сталь при испытании на растяжение часто проявляет особую характеристику, известную как предел текучести. Если построена кривая напряжения-деформации, наблюдается падение нагрузки (или иногда постоянная нагрузка), хотя деформация продолжает увеличиваться. В итоге за счет деформации металл упрочняется, и при дальнейшем деформировании нагрузка возрастает. Верхняя точка на S-образной части кривой, где начинается текучесть, известна как верхний предел текучести, а точка минимума — это нижний предел текучести.Это явление очень неприятно при некоторых операциях глубокой вытяжки листовой стали. Сталь продолжает удлиняться и становиться тоньше в тех местах, где начинается пластическая деформация, оставляя неприглядные углубления, называемые растяжными деформациями или «червями».
• Предел пропорциональности определяется как напряжение, при котором кривая напряжения-деформации сначала отклоняется от прямой линии. Ниже этого предельного значения напряжения отношение напряжения к деформации является постоянным, и говорят, что материал подчиняется закону Гука (напряжение пропорционально деформации).Пропорциональный предел обычно не используется в спецификациях, потому что отклонение начинается настолько постепенно, что наверняка возникнут разногласия относительно точного напряжения, при котором линия начинает изгибаться.
• Предел упругости ранее был определен как напряжение, при котором начинается пластическая деформация. Этот предел не может быть определен из кривой напряжения-деформации. Метод определения предела должен включать последовательность слегка увеличивающихся нагрузок с промежуточной полной разгрузкой для обнаружения первой пластической деформации или «остаточного схватывания».«Как и пропорциональный предел, его определение вызвало бы споры. Однако предел упругости используется как описательный, качественный термин.
Во многих ситуациях предел текучести используется для определения допустимого напряжения, которому может подвергаться материал. Для компонентов, которые должны выдерживать высокое давление, таких как те, которые используются в реакторах с водой под давлением (PWR), этот критерий неадекватен. Чтобы охватить эти ситуации, теория отказа максимального напряжения сдвига была включена в Кодекс ASME (Американское общество инженеров-механиков) по котлам и сосудам под давлением, раздел III, Правила строительства сосудов под давлением.
Пластичность
Относительное удлинение, указанное при испытании на растяжение, определяется как максимальное удлинение измерительной длины, деленное на исходную расчетную длину. Измерение определяется, как показано на Рисунке 6.
Рисунок 6: Измерение Elogation после разрушенияПроцентное удлинение = конечная расчетная длина — начальная расчетная длина / начальная расчетная длина (2-13)
= (L
x — L o / L o ) = дюймов на дюйм x 100 (2-14)Уменьшение площади — это пропорциональное уменьшение площади поперечного сечения образца для испытания на растяжение в плоскости разрушения, измеренной после разрушения.
Процент уменьшения площади (RA) =
площадь исходного поперечного сечения — минимальная конечная площадь / площадь исходного поперечного сечения (2-15)
= (A
0 — A min ) / A o = уменьшение площади / исходная площадь = кв. Дюйм / кв. Дюйм x 100 (2-16) Уменьшение площади указывается как дополнительная информация (в процентах удлинения) о деформационных характеристиках материала. Эти два показателя используются как индикаторы пластичности, способности материала растягиваться при растяжении.Поскольку удлинение не является равномерным по всей длине измерительного прибора и наибольшее в центре шейки, относительное удлинение не является абсолютной мерой пластичности. (Из-за этого при измерении удлинения в процентах всегда следует указывать измерительную длину.) Уменьшение площади, измеряемое при минимальном диаметре шейки, является лучшим индикатором пластичности.Пластичность чаще определяется как способность материала легко деформироваться при приложении растягивающего усилия или как способность материала противостоять пластической деформации без разрыва.Пластичность также можно рассматривать с точки зрения изгибаемости и разрушаемости. Пластичные материалы перед разрушением деформируются. Отсутствие пластичности часто называют хрупкостью. Обычно, если два материала имеют одинаковую прочность и твердость, более желателен тот, который имеет более высокую пластичность. Пластичность многих металлов может измениться при изменении условий. Повышение температуры увеличивает пластичность. Снижение температуры вызовет снижение пластичности и переход от пластичного к хрупкому поведению.Облучение также снизит пластичность.
Холодная обработка также снижает пластичность металлов. Холодная деформация выполняется в температурном диапазоне и в течение определенного промежутка времени для получения пластической деформации, но не для снятия деформационного упрочнения. Незначительное добавление примесей к металлам, намеренное или непреднамеренное, может оказать заметное влияние на переход от пластичного к хрупкому поведению. Нагревание металла после холодной обработки до температуры, при которой атомы металла возвращаются в свое равновесное положение, или выше, увеличит пластичность этого металла.Этот процесс называется отжиг .
Пластичность желательна при высоких температурах и давлении в реакторных установках из-за дополнительных напряжений на металлах. Высокая пластичность в этих применениях помогает предотвратить хрупкое разрушение.
Ковкость
Рис. 7: Податливая деформация цилиндра при равномерном осевом сжатииЕсли пластичность — это способность материала легко деформироваться при приложении растягивающего усилия, пластичность — это способность металла проявлять большую деформацию или пластическая реакция при воздействии сжимающей силы.Равномерная сжимающая сила вызывает деформацию, как показано на рисунке 7. Материал сжимается в осевом направлении под действием силы и расширяется в боковом направлении. Сдерживание из-за трения на контактных поверхностях вызывает осевое напряжение снаружи. Силы растяжения действуют по окружности с боковым расширением или увеличением обхвата. Пластический поток в центре материала также вызывает напряжение.
Следовательно, критерий разрушения (то есть предел пластической деформации) для пластического материала, скорее всего, будет зависеть от растягивающего, а не сжимающего напряжения.Изменение температуры может изменить как режим пластического течения, так и режим разрушения.
Прочность
Рисунок 8: Испытательное оборудование по ШарпиКачество, известное как вязкость , описывает реакцию материала на внезапные удары. Он определяется как работа, необходимая для деформации одного кубического дюйма металла до его разрушения. Вязкость измеряется тестом Шарпи или тестом Изода.
В обоих этих тестах используется образец с надрезом. Расположение и форма насечки стандартные.Точки опоры образца, а также удар молотка должны постоянно зависеть от места надреза.
Испытания проводятся путем установки образцов, как показано на Рисунке 8, и позволяя маятнику известного веса упасть с заданной высоты. Максимальная энергия, развиваемая молотком, составляет 120 фут-фунтов в тесте Изода и 240 фут-фунт в тесте Шарпи. При правильной калибровке машины энергия, поглощенная образцом, может быть измерена по восходящему колебанию маятника после того, как он разрушил образец материала, как показано на рисунке 9.Чем больше энергии поглощается образцом, тем меньше будет качание маятника вверх и тем прочнее будет материал.
Рис. 9: Испытание на вязкость материалаПоказатели вязкости являются относительными и применимы только для случаев, когда используются именно этот тип образца и метод нагружения. Образец другой формы даст совершенно другой результат. Насечки ограничивают деформацию небольшим объемом металла, что снижает ударную вязкость. Фактически, именно форма металла в дополнение к составу материала определяет ударную вязкость материала.
Твердость
Твердость — это свойство материала, которое позволяет ему противостоять пластической деформации, проникновению, вдавливанию и царапинам. Следовательно, твердость важна с инженерной точки зрения, поскольку сопротивление износу из-за трения или эрозии паром, маслом и водой обычно увеличивается с увеличением твердости.
Испытания на твердость служат важной потребности в промышленности, даже если они не измеряют уникальное качество, которое можно назвать твердостью. Тесты носят эмпирический характер, основаны на экспериментах и наблюдениях, а не на фундаментальной теории.Его главная ценность — это устройство для проверки, способное обнаруживать определенные различия в материалах, когда они возникают, даже если эти различия могут быть неопределенными. Например, две партии материала с одинаковой твердостью могут быть, а могут и не быть одинаковыми, но если их твердость различна, материалы определенно не похожи.
Было разработано несколько методов испытания на твердость. Чаще всего используются программы Brinell, Rockwell, Vickers, Tukon, Sclerscope и файлы test. Первые четыре основаны на испытаниях на вдавливание, а пятое — на высоте отскока металлического молотка с алмазным наконечником.Тест файла устанавливает характеристики того, насколько хорошо файл прикусывает материал.
В результате множества испытаний были подготовлены сравнения с использованием формул, таблиц и графиков, которые показывают взаимосвязь между результатами различных испытаний на твердость конкретных сплавов. Однако между любыми двумя методами нет точной математической связи. По этой причине результат одного типа испытания на твердость, преобразованный в показания другого типа, должен иметь обозначение «преобразовано из» (например, «352 Бринелля преобразовано из Rockwell C-38»).
Еще одно удобное преобразование — это преобразование твердости по Бринеллю в предел прочности на разрыв. Для закаленной и отпущенной стали предел прочности (psi) примерно в 500 раз превышает число твердости по Бринеллю (при условии, что прочность не превышает 200000 psi).
Как сплавы влияют на физические свойства
Никель — важный легирующий элемент. В концентрациях менее 5% никель повысит ударную вязкость и пластичность стали без повышения твердости. При добавлении в таких небольших количествах твердость не повышается, поскольку не образует карбидов, твердых соединений с углеродом.
Хром в стали образует карбид, упрочняющий металл. Атомы хрома также могут занимать определенные места в кристаллической решетке, что будет иметь эффект увеличения твердости, не влияя на пластичность. Добавление никеля усиливает действие хрома, давая сталь повышенной твердости и пластичности.
Медь очень похожа на никель по своему воздействию на сталь. Медь не образует карбид, но увеличивает твердость, замедляя движение дислокаций.
Молибден образует сложный карбид при добавлении в сталь. Благодаря структуре карбида он значительно упрочняет сталь, но также сводит к минимуму увеличение зерна. Молибден усиливает желаемые свойства никеля и хрома.
Нержавеющие стали — это легированные стали, содержащие не менее 12% хрома. Важной характеристикой этих сталей является их устойчивость ко многим коррозионным условиям.
Важная информация в этой главе кратко изложена ниже.
• Прочность — это способность материала сопротивляться деформации. Увеличение скольжения снизит прочность материала.
• Предел прочности на разрыв (UTS) — это максимальное сопротивление разрушению.
• Предел текучести — это напряжение, при котором возникает заданная величина остаточной деформации.
• Пластичность — это способность материала легко деформироваться при приложении растягивающего усилия или способность материала выдерживать пластическую деформацию без разрыва.Повышение температуры увеличивает пластичность. Пластичность снижается при более низких температурах, холодной обработке и облучении. Пластичность желательна при высоких температурах и давлении.
• Ковкость — это способность металла проявлять большую деформацию или пластическую реакцию при воздействии сжимающей силы.
• Вязкость описывает реакцию материала на внезапные удары. Он определяется как работа, необходимая для деформации одного кубического дюйма металла до его разрушения.
• Твердость — это свойство материала, которое позволяет ему противостоять пластической деформации, проникновению, вдавливанию и царапинам.
Термическая обработка
Термическая обработка крупных компонентов из углеродистой стали проводится с целью использования кристаллических дефектов и их эффектов и, таким образом, получения определенных желаемых свойств или условий.
Во время производства, изменяя скорость охлаждения ( закалка ) металла, размер зерна и структура зерна контролируются.Характеристики зерна контролируются для получения различных уровней твердости и прочности на разрыв. Как правило, чем быстрее охлаждается металл, тем меньше размер зерна. Это сделает металл более твердым. По мере увеличения твердости и предела прочности термообработанной стали ударная вязкость и пластичность снижаются.
Скорость охлаждения, используемая при закалке, зависит от метода охлаждения и размера металла. Равномерное охлаждение важно для предотвращения деформации. Обычно стальные детали закаливают в масле или воде.
Из-за кристаллического рисунка нержавеющей стали типа 304 в баке реактора (установка по производству трития) термообработка не подходит для повышения твердости и прочности.
Сварка может вызвать внутренние напряжения, которые останутся в материале после завершения сварки. В нержавеющих сталях типа 304 кристаллическая решетка гранецентрированная кубическая (аустенит). Во время высокотемпературной сварки температура окружающего металла может составлять от 500 ° F до 1000 ° F. В этой области температур аустенит превращается в объемноцентрированную кубическую решетчатую структуру (бейнит).Когда металл остынет, области, окружающие сварной шов, содержат некоторое количество исходного аустенита и некоторое количество вновь образованного бейнита. Проблема возникает из-за того, что «коэффициент упаковки» (PF = объем атомов / объем элементарной ячейки) не такой же для кристаллов FCC и для кристаллов BCC.Образовавшийся бейнит занимает больше места, чем исходная решетка аустенита. Это удлинение материала вызывает в нем остаточные сжимающие и растягивающие напряжения. Напряжения при сварке можно свести к минимуму, используя сварку радиатора, которая приводит к более низким температурам металла, и отжиг.
Отжиг — еще один распространенный процесс термообработки компонентов из углеродистой стали. Во время отжига компонент медленно нагревается до повышенной температуры и выдерживается там в течение длительного периода времени, а затем охлаждается. Процесс отжига проводится для получения следующих эффектов.а. для смягчения стали и повышения пластичности
b. для снятия внутренних напряжений, вызванных предыдущими процессами, такими как термообработка, сварка или механическая обработка
c. для улучшения зеренной структуры
Холодная и горячая обработка
Пластическая деформация, которая выполняется в температурном диапазоне и в течение такого интервала времени, что деформационное упрочнение не снимается, называется холодной обработкой.Получены обширные знания о структуре холоднодеформированного состояния. На ранних стадиях пластической деформации скольжение происходит в основном по первичным плоскостям скольжения, и дислокации образуют компланарные массивы. По мере деформации происходит поперечное скольжение. Холоднодеформированная структура формирует области с высокой плотностью дислокаций, которые вскоре превращаются в сетки. Размер зерна уменьшается с деформацией при низкой деформации, но вскоре достигает фиксированного размера. Холодная обработка снижает пластичность.
Горячая обработка относится к процессу, при котором металлы деформируются выше их температуры рекристаллизации, и деформационное упрочнение не происходит.Горячая обработка обычно проводится при повышенных температурах. Однако свинец подвергается горячей деформации при комнатной температуре из-за его низкой температуры плавления. С другой стороны, молибден подвергается холодной деформации при деформации даже при красном нагреве из-за его высокой температуры рекристаллизации.
Сопротивление металлов пластической деформации обычно падает с температурой. По этой причине большие массивные секции всегда подвергаются горячей ковке, прокатке или экструзии. Металлы демонстрируют отчетливо вязкие характеристики при достаточно высоких температурах, а их сопротивление течению увеличивается при высоких скоростях формования.Это происходит не только потому, что это характерно для вязких веществ, но и потому, что скорость рекристаллизации может быть недостаточно высокой.
Коррозия
Коррозия — это износ материала из-за взаимодействия с окружающей средой. Это процесс, при котором атомы металла покидают металл или образуют соединения в присутствии воды и газов. Атомы металла удаляются из структурного элемента до тех пор, пока он не выйдет из строя, или оксиды накапливаются внутри трубы, пока она не закупорится.Все металлы и сплавы подвержены коррозии. Даже благородные металлы, такие как золото, в некоторых средах подвержены коррозионному воздействию.
Коррозия металлов — естественный процесс. Большинство металлов не являются термодинамически стабильными в металлической форме; они хотят подвергнуться коррозии и вернуться к более стабильным формам, которые обычно встречаются в рудах, например к оксидам. Коррозия является основной проблемой для ядерных реакторных установок. Коррозия происходит постоянно по всей реакторной установке, и ей подвержен каждый металл.Хотя эту коррозию невозможно устранить, ее можно контролировать.
Общая коррозия
Общая коррозия с участием воды и стали обычно возникает в результате химического воздействия, при котором поверхность стали окисляется с образованием оксида железа (ржавчины). Многие системы и компоненты завода изготовлены из железа.
Некоторые стандартные методы, связанные с выбором материала для защиты от общей коррозии, включают:
- Использование коррозионно-стойких материалов, таких как нержавеющая сталь и сплавы никеля, хрома и молибдена.(Имейте в виду, что коррозия является электрохимической по своей природе, а коррозионная стойкость нержавеющих сталей является результатом поверхностных оксидных пленок, которые мешают электрохимическому процессу.)
- Использование защитных покрытий, таких как краски и эпоксидные смолы.
- Нанесение металлических и неметаллических покрытий или футеровки на поверхность, которая защищает от коррозии, но позволяет материалу сохранять свою структурную прочность (например, сосуд высокого давления из углеродистой стали с облицовкой из нержавеющей стали в качестве футеровки).
Гальваническая коррозия
Гальваническая коррозия возникает, когда два разнородных металла с разными потенциалами находятся в электрическом контакте в электролите. Это также может иметь место с одним металлом с неоднородностями (несходствами) (например, включениями примесей, зернами разного размера, различием в составе зерен или различиями в механическом напряжении). Между разными металлами существует разница в электрическом потенциале, которая служит движущей силой для электрического тока, протекающего через корродирующий агент или электролит.Этот ток приводит к коррозии одного из металлов. Чем больше разность потенциалов, тем больше вероятность гальванической коррозии. Гальваническая коррозия вызывает ухудшение только одного из металлов. Менее стойкий, более активный становится участком анодной (отрицательной) коррозии. Более сильный, благородный — катодный (положительный) и защищенный. Если бы не было электрического контакта, оба металла равномерно подверглись бы воздействию коррозионной среды. Тогда это будет называться общей коррозией.
Для любого конкретного носителя можно составить список, располагая металлы последовательно от наиболее активных или наименее благородных до пассивных или наиболее благородных. Гальванический ряд для морской воды обсуждается в Справочнике по основам химии.
Гальваническая коррозия имеет особое значение при проектировании и выборе материалов. Выбор материала важен, потому что разные металлы контактируют друг с другом и могут образовывать гальванические элементы. Дизайн важен для сведения к минимуму различных условий потока и возникающих в результате областей накопления коррозии.Незакрепленные продукты коррозии важны, потому что они могут быть доставлены в активную зону реактора и облучены.
В некоторых случаях электрохимическая коррозия может быть полезной на предприятии. Например, если к дну стального резервуара для воды прикрепить кусочки цинка, цинк станет анодом, и он подвергнется коррозии. Сталь в резервуаре становится катодом, и на нее не влияет коррозия. Этот метод известен как катодная защита. Защищаемый металл вынужден стать катодом, и он будет корродировать гораздо медленнее, чем другой металл, который используется в качестве расходуемого анода.
Локальная коррозия
Локальная коррозия определяется как избирательное удаление металла путем коррозии на небольших участках или участках поверхности металла, контактирующих с коррозионной средой, обычно с жидкостью. Обычно это происходит, когда небольшие локальные сайты атакуются с гораздо большей скоростью, чем остальная часть исходной поверхности. Локальная коррозия возникает, когда коррозия сочетается с другими деструктивными процессами, такими как напряжение, усталость, эрозия и другие формы химического воздействия.Локальные механизмы коррозии могут причинить больше повреждений, чем любой из этих деструктивных процессов по отдельности. Существует много различных типов локальной коррозии. Точечная коррозия, коррозионное растрескивание под напряжением, коррозия под напряжением хлорида, коррозия под действием едкого напряжения, коррозия под напряжением на первичной стороне, вмятин на трубке теплообменника, отходы и межкристаллитная агрессивная коррозия подробно обсуждаются в Справочнике по основам химии.
Коррозионное растрескивание под напряжением
Одной из наиболее серьезных металлургических проблем и одной из основных проблем ядерной промышленности является коррозионное растрескивание под напряжением (SCC).SCC — это тип межкристаллитной коррозии, которая возникает на границах зерен под действием растягивающего напряжения. Он имеет тенденцию распространяться, когда напряжение открывает трещины, которые подвержены коррозии, которые затем подвергаются дальнейшей коррозии, ослабляя металл за счет дальнейшего растрескивания. Трещины могут следовать межзерновым или трансгранулярным путям, и часто существует тенденция к ветвлению трещин.
Трещины образуются и распространяются примерно под прямым углом к направлению растягивающих напряжений при уровнях напряжений, намного более низких, чем те, которые требуются для разрушения материала в отсутствие агрессивной среды.По мере того, как растрескивание проникает дальше в материал, оно в конечном итоге уменьшает поддерживающее поперечное сечение материала до точки разрушения конструкции из-за перегрузки.
Напряжения, вызывающие растрескивание, возникают в результате остаточной холодной обработки, сварки, шлифования, термической обработки или могут применяться извне во время эксплуатации и, чтобы быть эффективными, должны быть растягивающими (в отличие от сжатия).
SCC возникает в металлах, подвергающихся воздействию окружающей среды, где, если бы напряжение не присутствовало или было на гораздо более низком уровне, не было бы никакого повреждения.Если бы конструкция, подверженная тем же напряжениям, находилась в другой среде (не вызывающей коррозии для этого материала), разрушения не было бы. Примерами SCC в атомной промышленности являются трещины в системах трубопроводов из нержавеющей стали и стержнях клапанов из нержавеющей стали.
Наиболее эффективные средства предотвращения SCC: 1) правильное проектирование; 2) снижение стресса; 3) удаление критически важных веществ в окружающей среде, таких как гидроксиды, хлориды и кислород; 4) и избегание застойных участков и щелей в теплообменниках, где может концентрироваться хлорид и гидроксид.Низколегированные стали менее восприимчивы, чем высоколегированные, но они подвержены SCC в воде, содержащей ионы хлора. Однако на сплавы на основе никеля не действуют хлорид- или гидроксид-ионы.
Примером сплава на основе никеля, устойчивого к коррозионному растрескиванию под напряжением, является инконель. Инконель состоит из 72% никеля, 14-17% хрома, 6-10% железа и небольшого количества марганца, углерода и меди.
Хлоридная коррозия под напряжением
Одной из наиболее важных форм коррозии под напряжением, которая беспокоит ядерную промышленность, является хлоридная коррозия под напряжением .Хлоридная коррозия под напряжением — это тип межкристаллитной коррозии, которая возникает в аустенитной нержавеющей стали при растягивающем напряжении в присутствии кислорода, хлорид-ионов и высокой температуры.
Считается, что это начинается с отложений карбида хрома по границам зерен, которые оставляют металл открытым для коррозии. Эта форма коррозии контролируется за счет поддержания низкого содержания хлорид-иона и кислорода в окружающей среде и использования низкоуглеродистых сталей.
Едкая коррозия под напряжением
Несмотря на обширную квалификацию инконеля для конкретных применений, с трубами из инконеля возник ряд проблем с коррозией.Повышенная стойкость инконелю к коррозионному растрескиванию под воздействием каустика может быть достигнута путем его термообработки при температуре от 620 ° C до 705 ° C, в зависимости от температуры предшествующей обработки раствором. Другие проблемы, которые наблюдались при использовании инконеля, включают в себя излишки, вмятины на трубках, точечную коррозию и межкристаллитную атаку.
Важная информация в этой главе кратко изложена ниже.
Закалка
- Изменение скорости охлаждения (закалки) металла контролирует размер зерна и структуру зерен.
- Характеристики зерна контролируются для получения различных уровней твердости и прочности на разрыв.
- Повышение твердости и прочности на разрыв термически обработанной стали; снижается вязкость и пластичность.
Сварка
- Создает сжимающие и растягивающие напряжения
- Напряжения сводятся к минимуму за счет использования сварки с радиатором и отжига
Отжиг
- Смягчает сталь и повышает пластичность
- Снимает внутренние напряжения
- Коррозия — это естественное разрушение металла, при котором атомы металла покидают металл или образуют соединения в присутствии воды или газов.Общая коррозия может быть сведена к минимуму за счет использования коррозионно-стойких материалов и добавления защитных покрытий и футеровки.
- Гальваническая коррозия возникает, когда разнородные металлы существуют при разных электрических потенциалах в присутствии электролита. Гальваническую коррозию можно уменьшить за счет тщательного проектирования и выбора материалов с учетом разнородных металлов и использования расходуемых анодов.
- Локальная коррозия может быть особенно разрушительной в присутствии других разрушающих сил, таких как напряжение, усталость и другие формы химического воздействия.
Концерн
Другой формой коррозионного растрескивания является водородное охрупчивание . Хотя охрупчивание материалов принимает различные формы, водородное охрупчивание высокопрочных сталей имеет наиболее разрушительный эффект из-за катастрофического характера трещин, когда они возникают. Водородное охрупчивание — это процесс, при котором сталь теряет пластичность и прочность из-за крошечных трещин, возникающих в результате внутреннего давления водорода (H 2 ) или газообразного метана (CH 4 ), образующихся на границах зерен.В циркониевых сплавах водородная хрупкость вызывается гидрированием циркония. На ядерных реакторных установках термин «водородная хрупкость» обычно относится к охрупчиванию циркониевых сплавов, вызванному гидрированием циркония.
Источники водорода
Источники водорода, вызывающие охрупчивание, были обнаружены при производстве стали, при обработке деталей, при сварке, хранении или локализации газообразного водорода и связаны с водородом в качестве загрязнителя в окружающей среде, который часто является побочный продукт общей коррозии.Последнее касается атомной отрасли. Водород может образовываться в результате коррозионных реакций, таких как ржавление, катодная защита и гальваника. К охлаждающей жидкости реактора также может быть добавлен водород для удаления кислорода из систем охлаждающей жидкости реактора.
Водородное охрупчивание нержавеющей стали
Рис. 10: Водородное охрупчиваниеКак показано на Рис. 10, водород диффундирует по границам зерен и соединяется с углеродом (C), который легирован железом, с образованием газообразного метана.Метан не подвижен и собирается в небольших пустотах по границам зерен, где создает огромное давление, которое вызывает трещины. Водородная хрупкость является основной причиной того, что теплоноситель реактора поддерживается на нейтральном или основном pH на установках без алюминиевых компонентов.
Если металл находится под высоким растягивающим напряжением, может произойти хрупкое разрушение. При обычных комнатных температурах атомы водорода поглощаются металлической решеткой и диффундируют через зерна, стремясь собираться во включениях или других дефектах решетки.Если напряжение вызывает растрескивание в этих условиях, путь является межкристаллитным. При высоких температурах абсорбированный водород имеет тенденцию собираться на границах зерен, и в этом случае растрескивание под напряжением становится межкристаллитным. Считается, что растрескивание мартенситных и дисперсионно-упрочненных стальных сплавов является формой водородного коррозионного растрескивания под напряжением, которое возникает в результате попадания в металл части атомарного водорода, который образуется в следующей реакции коррозии.
3 Fe + 4 H 2 O → Fe 3 O 4 + 4 H 2
Водородное охрупчивание не является постоянным условием.Если растрескивания не происходит и условия окружающей среды изменяются таким образом, что водород не образуется на поверхности металла, водород может повторно диффундировать из стали, так что пластичность восстанавливается.
Для решения проблемы водородного охрупчивания особое внимание уделяется контролю количества остаточного водорода в стали, контролю количества поглощения водорода при обработке, разработке сплавов с улучшенной стойкостью к водородному охрупчиванию, разработке покрытий или покрытий с низким или нулевым охрупчиванием. и ограничение количества водорода, вводимого на месте (на месте) в течение срока службы детали.
Водородное охрупчивание циркониевых сплавов
Водородное охрупчивание — проблема циркония и циркониевых сплавов, которые часто используются в качестве материалов оболочки для ядерных реакторов. Цирконий реагирует с водой следующим образом.
Zr + 2 H 2 O → ZrO 2 + 2H 2 ↑
Часть водорода, образующегося при коррозии циркония в воде, соединяется с цирконием с образованием отдельной фазы гидрида циркония (ZrH 1,5 ) тромбоциты.Затем металл становится хрупким (снижается пластичность) и легко ломается. В пластинках гидрида циркония начинают образовываться трещины, которые распространяются по металлу. Циркалой-2 (сплав циркония), который использовался в качестве оболочки твэла, может поглощать до 50% образующегося при коррозии водорода и подвержен водородному охрупчиванию, особенно вблизи поверхности. Исследования, проведенные в Westinghouse, Batelle и других местах, показали, что никель в циркалое-2 отвечает за улавливание водорода.Это привело к разработке циркалоя-4, который содержит значительно меньше никеля, чем циркалой-2, и менее подвержен охрупчиванию. Кроме того, введение ниобия в циркалой-4 дополнительно снижает степень абсорбции водорода.
Важная информация в этой главе кратко изложена ниже.
Водородное охрупчивание
Условиями, необходимыми для водородного охрупчивания стали, являются присутствие водорода, растворенного в воде, и углерода в стали.Водород, растворенный в воде, поступает из:
- Производство стали
- Обработка деталей
- Сварка
- Хранение или локализация газообразного водорода
- Относится к водороду как загрязнителю в окружающей среде, который часто является побочным продуктом общего коррозия
Водородное охрупчивание является результатом водород, который диффундирует по границам зерен и соединяется с углеродом с образованием газообразного метана. Газообразный метан собирается в небольших пустотах вдоль границ зерен, где он создает огромное давление, которое вызывает трещины и снижает пластичность стали.Если металл находится под высоким растягивающим напряжением, может произойти хрупкое разрушение.
Циркалой-4 менее подвержен водородной хрупкости, чем циркалой-2, потому что:
- Циркалой-4 содержит меньше никеля
- Введение ниобия в циркалой-4 снижает степень поглощения водорода металлом.
структура кристаллической решетки металлов
структура кристаллической решетки металлов ПРОСТЫЙ КУБИЧЕСКИЙ МЕТАЛЛ В металле все атомы идентичны, и большинство из них имеют сферическую форму (
склеивание не зависит от направления).Таким образом, металлы имеют тенденцию принимать относительно
простые конструкции. Самый простой:
Нажмите на левую элементарную ячейку выше, чтобы исследовать ее в VRML. Здесь мы видим две элементарные ячейки, уложенные стопкой, чтобы сформировать решетку. Обратите внимание, что в каждом случае обнаруживается одна и та же общая структура.
Хотя мы показали пространство между сферами, это только для «открыть» структуру для просмотра. В настоящем кристалле сферы соприкасаются как показано в элементарной ячейке и решетке ниже.
Таким образом, длина края ячейки в 2 раза больше радиуса сферы.
Щелкните элементарную ячейку и решетку, чтобы исследовать их в VRML. В 3-D эффективность упаковки определяется по формуле:
Это низкое значение неудивительно. Помните, что двумерная квадратная решетка неэффективно использует пространство. Простая кубическая решетка является ее трехмерным аналогом, а также содержит много пустого места.
Обратим внимание на пустые места в решетке. Каждый В центре элементарной ячейки находится одно крупное междоузлие (47,65% громкость). 8 атомов касаются этого пространства, поэтому межузельное координационное число равно 8, а его геометрия является кубическим (у куба 8 углов).
Поскольку каждая элементарная ячейка содержит (8 x 1/8 =) 1 атом и 1 междоузлие сайта, количество атомов и междоузлий одинаковое. Изучите структуру ниже, которая показывает расположение любого
одиночный атом в простой кубической решетке; обратите внимание, что каждый атом имеет
6 соседей, поэтому атомная координация число равно 6. Координационная геометрия
октаэдр (у октаэдра 6 углов).
Октаэдрическая координация атома. An
октаэдр.
Поскольку и координационное число, и эффективность упаковки низкие, простая кубическая решетка неэффективно использует пространство. Очень мало примеров простых кубические решетки известны (альфа-полоний — один из немногих известных простых кубические решетки).
Ниже мы снова видим сечение простой кубической решетки в виде
«на самом деле» — с атомами, соприкасающимися друг с другом. Обратите внимание на каналы формируется путем совмещения межстраничных объявлений.Эти пустые места могут позволить
другие маленькие атомы входят в кристалл.