Химические знаки и формулы — параграф 4 ГДЗ химия 7 (Габриелян)
1. Знаки каких химических элементов содержат заглавную букву С? Запишите их и произнесите.
Ответ, согласно учебнику: C (углерод), Ca (кальций), Cu (медь), Cl (хлор), Cr (хром).
Полный ответ: C (углерод), Ca (кальций), Cu (медь), Cl (хлор), Cr (хром), Co (кобальт), Cd (кадмий), Cs (цезий), Ce (церий), Cm (кюрий), Cf (калифорний).
2. Из табл. 2 выпишите отдельно знаки элементов-металлов и элементов-неметаллов. Произнесите их названия.
Металлы: Al (алюминий), Fe (железо), Au (золото), K (калий), Ca (кальций), Mg (магний), Cu (медь), Na (натрий), Hg (ртуть), Pb (свинец), Ag (серебро), Cr (хром), Zn (цинк).
Неметаллы: N (азот), H (водород), O (кислород), S (сера), C (углерод), P (фосфор), Cl (хлор).
3. Что такое химическая формула? Запишите формулы следующих веществ:
а) серной кислоты, если известно, что в состав ее молекулы входят два атома водорода, один атом серы и четыре атома кислорода;
б) сероводорода, молекула которого состоит из двух атомов водорода и одного атома серы;
Что объединяет все эти вещества?
Химическая формула — это формула, выражающая качественный и количественный состав вещества при помощи символов химических элементов и индексов.
а) H2SO4)
б) H2S
в) SO2)
Все эти вещества содержат один и тот же химический элемент — серу (S).
4. Изготовьте из пластилина объемные модели молекул следующих веществ:
а) аммиака, молекула которого содержит один атом азота и три атома водорода;
б) хлороводорода, молекула которого состоит из одного атома водорода и одного атома хлора;
в) хлора, молекула которого состоит из двух атомов хлора.
Напишите формулы этих веществ и прочитайте их.
NH3 — читается как «эн аш три»
HCl — читается как «аш хлор»
C 2 — читается как «хлор два»
5. На рис. 40 изображены модели молекул четырех химических веществ. Сколько химических элементов образуют эти вещества? Назовите их, запишите символы этих элементов и произнесите их.
Эти вещества образованы 4-мя химическими элементами:
H (аш) — водород
O — кислород
C (цэ) — углерод
S — сера
Урок химии 7 класс Химическая формула. Относительная молекулярная масса /конспект+презентация/
Описание слайда:Исследовательское моделирование H O h3 O2 h3O 3h3O 2. Введение новых знаний. Создание и решение проблемной ситуации. Исследовательское моделирование. Учитель: Что означают знаки (символы) химических элементов? Учащиеся: Символы химических элементов используют для обозначения атомов определённого вида; удобное международное сокращение греческих или латинских названий элементов. Учитель: Знаки химических элементов — это знаковые модели. Давайте попробуем создать предметные модели частиц, из которых состоят вещества. Начнем с атомов. Чем отличаются друг от друга атомы разных видов, т.е. разных химических элементов? Учащиеся: Атомы разных видов отличаются массой, размерами, строением. Учитель: Вам выданы шаростержневые модели. Для того, чтобы показать отличие атомов друг от друга, шарики разного цвета. Это – цвет моделей, шариков, но не атомов. Атомы не окрашены. Учитель: Положите на лоток три шарика, обозначающие атомы элемента водорода. Учитель: Как учесть их количество? Учащиеся: Записать цифру три перед знаком элемента водорода. Учитель: Вы за партой работаете в парах. Сколько атомов водорода в ваших моделях приходится на двоих? Как это обозначим в записи? Учащиеся: Записать цифру шесть перед знаком элемента водорода. Учитель: Выложите в лотке модели двух атомов кислорода. Сколько атомов кислорода в ваших моделях приходится на двоих? Как это обозначим в записи? Учащиеся: Записать цифру четыре перед химическим знаком элемента кислорода. Учитель: Но во многих веществах атомы объединяются друг с другом. Например, самый лёгкий газ водород, состоит из молекул. Каждая состоит из двух атомов элемента водорода. Создайте модель молекулы газа водорода, используя металлический стержень для соединения атомов. 1 молекула газа водорода, состоит из двух атомов (Н2). Выложите на лоток две молекулы газа водорода. Две молекулы газа водорода, каждая состоит из двух атомов. Как это записать, используя знаки? (2 Н2) Цифры в данной записи называются: индекс, коэффициент. Попробуйте объяснить, что означает индекс? Коэффициент? Где записывается индекс? Коэффициент? Работа по заполнению таблицы в опорной схеме. Учащиеся: Индекс указывает на число атомов в молекуле, коэффициент – на число отдельных частиц. Учитель: Молекула воды состоит из одного атома кислорода и двух атомов водорода, расположенных под углом. Соберите модель на столах (на доске – магнитная модель, рисунок в тетради, запись) (Н2О) Сколько молекул воды в ваших моделях приходится на двоих? Как это обозначим в записи? Учитель: Дайте определение простым, сложным веществам. Учащиеся: Сложные вещества состоят из атомов разного вида. Учитель: Итак, состав веществ записывается знаковыми моделями, т.е. химическими формулами. О чем говорит нам химическая формула? Учащиеся: О том, из каких атомов состоит вещество, в каком количестве атомы входят в состав вещества. Качественный состав вещества показывает, из атомов каких химических элементов оно состоит. Количественный состав показывает число атомов каждого химического элемента в составе вещества. Учитель: так о чём пойдет речь на уроке? Ученик: о химической формуле, КАЧЕСТВЕНном И КОЛИЧЕСТВЕННом СОСТАВе вещества.
Восстановительная часть
Основные понятия химии
Атом– частица вещества, состоящая из положительного заряженного ядра и отрицательно заряженных электронов.
Молекула– наименьшая частица вещества, обладающая его химическими свойствами. Химические свойства молекул определяются их составом и химическим строением.
Химический элемент– определенный вид атомов с одинаковым зарядом ядра.
Простые вещества– вещества, образованные из атомов одного элемента. Например:N2,O2,Cl2,P4,S8и т.п.
Сложные вещества, или химические соединения – вещества, образованные атомами разных элементов. Например:NH3;Ca(H2PO4)2;MgCl2;KNO3 и т.п.
Относительная атомная масса химического
элемента– отношение средней массы
атома естественного изотопического
состава элемента к 1/12 массы атома изотопа
углерода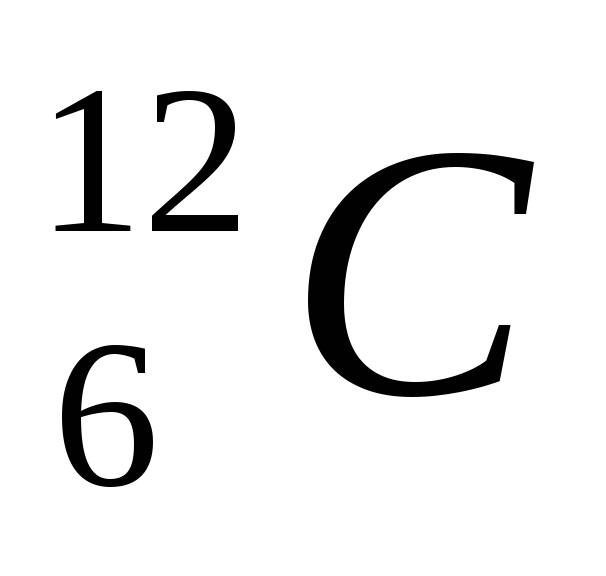 .
Относительные атомные массы элементов
обозначаютAr,
где индекс «r» –
начальная буква английского словаrelative(относительный).
.
Относительные атомные массы элементов
обозначаютAr,
где индекс «r» –
начальная буква английского словаrelative(относительный).
Записи Ar(H),Ar(O),Ar(C) означают относительные массы водорода, кислорода и углерода соответственно.
Вместо термина «относительная атомная масса» можно использовать исторически сложившийся термин «атомная масса».
Относительная молекулярная масса(Мr) равна отношению
средней массы молекулы естественного
изотопического состава к 1/12 массы
изотопа углерода .
.
Относительная молекулярная масса равна сумме относительных атомных масс всех атомов, входящих в состав молекулы вещества. Она легко высчитывается по формуле вещества.
Относительная молекулярная масса
вещества показывает, во сколько раз
масса молекулы данного вещества больше
1/12 массы атома 
Моль– это единица количества вещества, принятая в международной системе единиц (СИ).
Один моль содержит, столько структурных
единиц (молекул, атомов, ионов или других
частиц), сколько атомов содержит 12 г изотопа углерода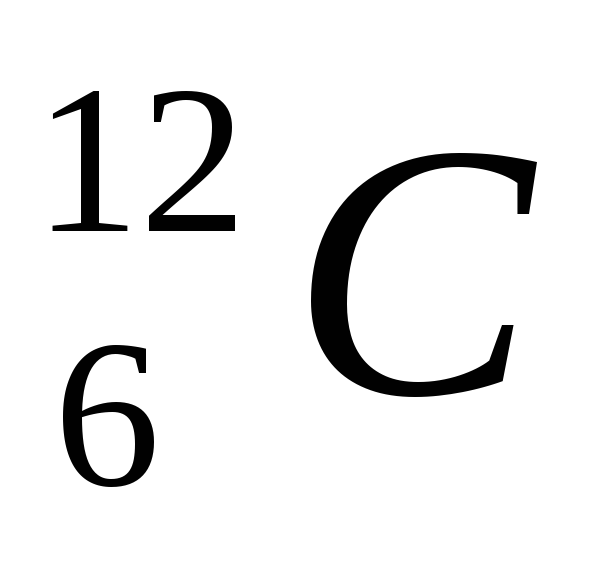 .
.
Зная массу одного атома углерода (1,999∙10-23г), можно легко вычислить число атомов (NA) в 12 г углерода.
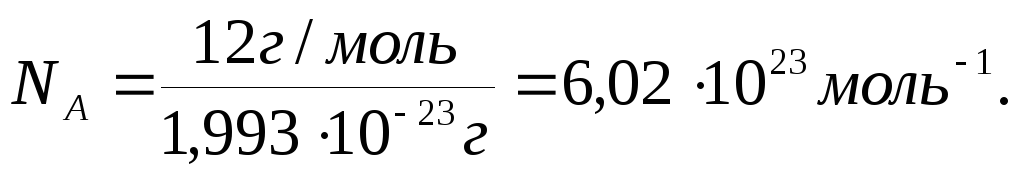
Это число называется постоянной Авогадро.
Единица количества (моль) обозначается «n».
Молярная масса вещества– это величина, равная отношению массы вещества (

Химические знаки, формулы и уравнения
Элементы принято обозначать химическими знаками (символами). Символ элемента состоит из первой буквы (или первой и одной из последующих букв) латинского названия элемента; первая буква всегда прописная, вторая – строчная. Например: Aluminium(алюминий) обозначаютAl,Ferrum(железо) –Fe,Zincum(цинк) –Zn.
Состав сложных веществ изображают при помощи химических формул: H2SO4;FeCl3и т.п. Подстрочными индексами обозначают число атомов данного типа в молекуле. Формулами обозначают и состав простых веществ:Cl2,F2,O2,P4.
Химические уравнения записывают при помощи химических формул и знаков:
FeCl 3 + 3NaOH = Fe(OH)3+3NaCl.
Коэффициенты перед формулами веществ показывают общее количество молекул данного вещества, необходимых для проведения реакции.
Химические реакции– явления, при которых одни вещества превращаются в другие, отличающиеся от исходных составом и свойствами. При этом не происходит изменение состава ядер атомов.
Различают реакции:
Экзо- и эндотермические (по признаку выделения или поглощения теплоты).
Разложения, соединения, замещения и обмена (по признаку числа исходных и конечных веществ).
Обратимые и необратимые (по признаку обратимости).
Протекающие без изменения степеней окисления атомов и с изменением степеней окисления (по признаку изменения степеней окисления атомов).
Конспект урока по теме » Химические формулы»
Цели урока: 1) Дать первые представления о химических формулах, научить школьников их читать. 2) Сформировать понятия о коэффициентах и индексах. 3) Дать понятие относительной атомной и молекулярной массы.4) Научить ребят рассчитывать относительную молекулярную массу.
Оборудование: ПСХЭ Д.И. Менделеева.
Ход урока.
1. Оргмомент. Проверка Д.З.
Контрольный диктант по таблице № 1.
Фронтальный опрос.
—Кто такой Д.И. Менделеев. Рассказать о его научном подвиге.
Работа у таблицы.
Рассказать и показать устройство ПСХЭ. Сколько периодов, сколько групп, сколько элементов в ней.
«Цепочка»
По цепочке весь класс; Задание : определить «домашний адрес» элементов которые я буду указывать.
Работа по группам.
Разбить класс на несколько групп по 4 человека, раздать карточки , работа дается на 10 минут, в карточки 4-ре задания, с группы отвечают 2 человека, выставить оценки.
2. Изучение нового материала.
Химические формулы – это аналоги слов. Как слова записываются с помощью букв так и химические формулы записываются с помощью хим. символов.
Химические формулы отображают состав вещества.
Задание : выразите состав глюкозы если известно что в ее состав входя 6 атомов углерода, 12 атомов водорода, 6 атомов кислорода. .
Индекс – число атомов элемента. Ставится внизу справо от химического знака. Индекс 1 не пишется. . Итак:
Химическая формула- условная запись состав вещества с помощью знаков хим. элементов и индексов.
Знаки отражают качественный а индексы количественный состав.
Коэффициент.
Если надо отобразить несколько одинаковых молекул то надо поставить перед формулой цифру – это цифра называется коэффициент.
Работа в тетради.
Индекс показывает число атомов а коэффициент число молекул.
Примеры: 4H2O – 4 аш два о. 3NaCl – 3 натрий хлор, 7О – 7 кислорода, 4Fe- 4 железа.
Относительная атомная масса.
Атомы имеют микроскопические ничтожно малые размеры. Естественно что малым размерам соответствуют малые массы. Например масса атома кислорода в кг. Равна = 26.667*10-27 кг. Выписываю значение массы атома кислорода на доске в развернутом виде.
0.000000000000000000000000026667 кг.
Сделать вывод: с такими числами работать неудобно.
Вопрос классу: Какую единицу массы следует выбрать чтобы легко работалось с таким малыми массами?
Относительная атомная масса показывает во сколько раз масса атома данного элемента больше массы атома водорода. Ar – Не имеет едениц измерения.
Относительные атомные массы элементов находятся в таблице Д.И. Менделеева. Например: Ar(Fe)=56 Это означает что масса атома железа больше массы атома водорода в 56 раз.
Работа с ПСХЭ.
Ребята сами находят в таблице атомные массы , несколько переписывают в тетрадь.
Относительная молекулярная масса.
Относительная молекулярная масса – это масса одной молекулы, и показывает во сколько раз масса молекулы данного вещества больше массы молекулы водорода. Обозначается – Mr. Mr= Ar + Ar + Ar +…Ar то есть : относительная молекулярная масса равняется сумме относительных атомных масс элементов из которых состоит молекула.
Например: найдем массу молекулы воды Mr( H2O)= 1*2+16=18
Найдем Mr(NaCl)=23+ 35=58
Таким образом : относительная атомная масса – это масса одного атома, а относительная молекулярная масса – это масса одной молекулы.
3. Закрепление.
Работа в тетрадях.
Задание № 1. Записать 3 молекулы серной кислоты, если известно, что в состав молекулы входят 2 атома водорода, 1 атом серы и 4 атома кислорода. H2SO4.
Записать 2 молекулы углекислого газа , если известно что в состав молекулы входят 1 атом углерода и 2 атома кислорода. CO2.
Задание № 2. Найти молекулярную массу соляной киcлоты HCl Mr(HCl)=1+35=36
Найти молекулярную массу азотной кислоты HNO3Mr(HNO3)=1+14+4*16=79
Найти молекулярную массу хлорида кальция CaCl2Mr(CaCl2)=40+35*2=110
После выполнения заданий несколько тетрадей на проверку.
«Да-нет».
Химическая формула показывает хим. состав вещества. Да
Индекс показывает число атомов элемента в молекуле. Да.
Коэффициент показывает так же число атомов элемента в молекуле. Нет.
Относительная атомная масса – это масса нескольких атомов. Нет.
Относительная молекулярная масса – это масса одной молекулы. Да.
Опрос.
—Что такое атомная масса? Масса одного атома.
—Что означает атомная масса? Во сколько раз масса данного элемента больше атомной массы водорода.
—Как найти атомную массу? Все атомные массы записаны в таблице.
—Что такое молекулярная масса? Как ее найти? По формуле( смотреть выше).
4. Рефлексия.
Ребята должны расслабится отложить все в сторону . Нужно спросить у ребят понравился ли им урок , что по их мнению сложно и непонятно ,а что наоборот запомнилось легко и хорошо.
5. Д.З. параграф № 5 , упр. 1-2 устно, 4-5 письменно Объявить ребятам, что на следующем уроке будет самостоятельная работа по ранее изученным темам; поэтому повторить параграф № 1-4.
Презентация к уроку по химии (8 класс) по теме: Химические знаки и формулы
По теме: методические разработки, презентации и конспекты
 Модульный урок «Состав вещества. Химические знаки иформулы»
Модульный урок «Состав вещества. Химические знаки иформулы»Обобщающий урок по теме «Состав вещества. Химические знаки и формулы» в 7 классе с использованием технологии модульного обучения. Учебник О.С. Габриэлян, И.Г. Остроумов «Введение в химию. Вещест…
 Проверочная работа по теме «Периодическая система химических элементов Д.И.Менделеева. Знаки химических элементов. Химические формулы. Относительная атомная и молекулярная массы»
Проверочная работа по теме «Периодическая система химических элементов Д.И.Менделеева. Знаки химических элементов. Химические формулы. Относительная атомная и молекулярная массы»Проверочная работа по теме «Периодическая система химических элементов Д.И.Менделеева. Знаки химических элементов. Химические формулы. Относительная атомная и молекулярная массы» предназначена дл…
 Проверочная работа по теме»«Периодическая система химических элементов Д.И.Менделеева. Знаки химических элементов. Химические формулы. Аr и Mr»
Проверочная работа по теме»«Периодическая система химических элементов Д.И.Менделеева. Знаки химических элементов. Химические формулы. Аr и Mr»Проверочная работа по теме «Периодическая система химических элементов Д.И.Менделеева. Знаки химических элементов. Химические формулы. Аr и Mr» предназначена для учащихся 8 классов. Она включает…
 Презентация к уроку химии в 8 классе «Химические знаки» (учебник Химия-8, авторы Рудзитис Г.Е., Фельдман Ф.Г.)
Презентация к уроку химии в 8 классе «Химические знаки» (учебник Химия-8, авторы Рудзитис Г.Е., Фельдман Ф.Г.)Презентация позволит провести урок по данной теме с высокой плотностью, с развитием интереса к химии. Используется элемент проблемно-диалогической технологии….
 Видеоурок в 8 классе на тему «Валентность химических элементов. Определение валентности химических элементов по формуле бинарных соединений. Составление химических формул бинарных соединения по валентности».
Видеоурок в 8 классе на тему «Валентность химических элементов. Определение валентности химических элементов по формуле бинарных соединений. Составление химических формул бинарных соединения по валентности».https://youtu.be/ukzxfFKKAxc…
 Химические элементы и химические знаки
Химические элементы и химические знакиХимические элементы. Химические знаки…
 Домашний эксперимент по теме » Химические знаки»
Домашний эксперимент по теме » Химические знаки»Данные химические эксперименты позволяют обучающимся находить в составе различных объектов химические знаки изучаемых химических элементов….
I.Организационный момент | 2 мин | Приветствие. Проверка готовности учащихся к УЗ. Организация внимания. Обеспечить мотивацию учения школьников, принятие ими целей УЗ. | Приветствует учащихся, контролирует готовность учащихся к работе на уроке. | Готовит принадлежности, необходимые для учебной деятельности | Готовность к учебной деятельности | Л.: Умение сосредоточиваться на выполнение учебных задач Р. Умение ставить цель деятельности, намечать пути ее достижения | II. Проверка выполнения домашнего задания | 5мин | Установить правильность полноту и осознанность выполнения ДЗ. Выявить пробелы в знаниях и способах действий, устранить выявленные пробелы. | Объясняет условия выполнения заданий на карточках. (Смотри Приложение )контролирует оценивание | Выполняют задания, индивидуально, взаимопроверка в парах по образцу ,выставяют оценки | Знать понятия «модель», «моделирование» и значение моделирования | Р: Взаимоконтроль выполнения Л:Умение применять полученные знания при выполнении заданий | III. Актуализация знаний | 3 мин | Обеспечить мотивацию учащихся к активной работе на уроке. Создать проблемный вопрос. | Озвучивает тему урока ( прил 2 — стихотворение), помогает поставить цели и задачи урока, наметить пути их достижения.Обосновывает значимость изучаемого материала. Задает учащимся наводящие вопросы. | Формулирует цели урока. Отвечают на вопросы учителя Записывают в тетради тему урока | Актуализация опорных знаний и способов действий | Л.: Умение осознавать необходимость получения новых знаний для решения учебной задачи | IY.Усвоение новых знаний и способов действий 1. беседа о значениизнаний о химических знаках 2.работа у доски (провести сравнение химического языка и русского) 3. Основатель химической символики — Берцелиус Работа с таблицей в учебнике 4.этимология химических элементов 5.химическая формула и ее характеристика | 13 мин | Обеспечить восприятие, осмысление и первичное запоминание изучаемого материала; | 1.Организует беседу с проблемным вопросом по теме. – для чего нужно изучить химические знаки? 2.Организует работу у доски — сравнить химический язык с русским языком 3.Организует работу с табл 2 в учебнике по выяснению причин обозначения химических элементов 4.обьясняет условия работы в парах по заданию: раскрасить ПС в разные цвета в зависимости от этимологии(прил.3.–ПС) 5.объяснение у доскиЧто такое химическая формула? Качественный и количественный состав вещества на примере молекулы хлорида натрия и углекислого газа (индекс и химическая формула, простое и сложное вещество– новые определения) | 1.отвечают на вопросы 2.Работают у доски с карточками 3.табл №2 в учебнике ,стр29,делают вывод 4.работают в парах, с карточками, раскрашивая ПС в разные цвета Делают вывод 5. дают определение – молекула и химический элемент – записывают в тетрадь | Причины обозначения химических элементов1 буквой и двумя. Разные группы химических элементов, в зависимости от причин их названия | П: Поиск и выделение необходимой информации. Структурирование знаний. Анализ объектов. Построение логической цепи рассуждений. К:инициативное сотрудничество в поиске и выборе информации, умение планировать и согласованно выполнять совместную деятельность, распределять роли, взаимно контролировать друг друга. Р: умение работать по алгоритму, навыки самоконтроля. |
Технологическая карта урока по химии в 7 классе » Химические знаки и формулы»
Карточки для проверки ДЗ по теме «Моделирование»
Фамилия и имя учащегося и класс: | |
Что это за предмет? а) муляж, б) модель, в) схема, г) копия По каким признакам вы это определили? а) по размерам б) по цвету в) сходство с оригиналом г) по материалу, из которого изготовлено Для чего изготавливают подобные предметы? а) для игр б) для подробного изучения основных признаков и структуры в) для сохранения копии оригинала для потомков г) для коллекций Основные признаки предмета, сходные с оригиналом? а)размер б) главные элементы, признаки, части в)материал, из которого изготовлен предмет Выберите подобные предметы из списка: а) электрофорная машина, б) модель головного мозга человека, в) резиновый мяч, г) кукла | |
Карточки для проверки ДЗ по теме «Моделирование»
Фамилия и имя учащегося и класс: | |
Что это за предмет? а) муляж, б) модель, в) схема, г) копия По каким признакам вы это определили? а) по размерам б) по цвету в) сходство с оригиналом г) по материалу, из которого изготовлено Для чего изготавливают подобные предметы? а) для игр б) для подробного изучения основных признаков и структуры в) для сохранения копии оригинала для потомков г) для коллекций Основные признаки предмета, сходные с оригиналом? а)размер б) главные элементы, признаки, части в)материал, из которого изготовлен предмет Выберите подобные предметы из списка: а) электрофорная машина, б) модель головного мозга человека, в) резиновый мяч, г) кукла | |
Выберите из списка элементы и раскрасьте таблицу в цвета, соответственно причинам их названия:
№35 (Br) – зловонный
№ 53 (I) – фиолетовый
№ 52 (Te)
№ 32 (Ge)
№1 (H) – рождающий воду
№ 92 (U)
№8 (O) – рождающий кислоты
№ 96 (Cm)
№ 94 (Pu)
№ 22 (Ti)
№ 73(Ta)
№ 84 (Po)
№ 87 (Fr)
№ 44 (Ru)
№ 95 (Am)
Названия, указывающие на свойства простых веществ – красный цвет
Географические названия ХЭ – синий цвет
ХЭ, названныев честь планет – желтый цвет
ХЭ, названные в честь ученых –зеленый цвет
Имена мифических героев – коричневый цвет
Пример: Химический элемент, названный в честь планет – желтый цвет № 94 Плутоний (Pu) – Плутон
Выберите из списка элементы и раскрасьте таблицу в цвета, соответственно причинам их названия:
№35 (Br) – зловонный
№ 53 (I) – фиолетовый
№ 52 (Te)
№ 32 (Ge)
№1 (H) – рождающий воду
№ 92 (U)
№8 (O) – рождающий кислоты
№ 96 (Cm)
№ 94 (Pu)
№ 22 (Ti)
№ 73(Ta)
№ 84 (Po)
№ 87 (Fr)
№ 44 (Ru)
№ 95 (Am)
Названия, указывающие на свойства простых веществ – красный цвет
Географические названия ХЭ – синий цвет
ХЭ, названныев честь планет – желтый цвет
ХЭ, названные в честь ученых –зеленый цвет
Имена мифических героев – коричневый цвет