Конспект «Валентность химических элементов» — УчительPRO
Валентность химических элементов
В образовании новых химических связей участвуют неспаренные электроны внешнего энергетического уровня. Именно они, как правило, определяют валентностъ элемента.
■ Валентность — это способность атомов химических элементов образовывать химические связи с другими атомами.

Валентность выражается числом атомов одновалентных элементов, которое атом данного элемента может замещать или присоединять во время образования определенного химического соединения. Валентность — свойство элемента, проявляемое в соединениях. Валентность обозначают римскими цифрами, она может составлять от I до VIII.
Существуют одновалентные (Н, Li, Na, K, F, Br), двухвалентные (Mg, Ca, Ba, O, S), трехвалентные (Al, N, P), четырехвалентные (C, Si) и т. п. элементы. Понятно, что один атом двухвалентного элемента соединяется с двумя атомами одновалентного элемента (CaCl
Существуют атомы, имеющие постоянную (Na, K, Ca, Al, О) и переменную валентности. Например, валентность серы бывает II, IV и VI:
Рассмотрев электронно-графические формулы элементов, можно определить, что валeнтность атома водорода равна I (имеет один неспаренный электрон). По одному неспаренному электрону у лития, фтора, натрия, калия. Эти атомы тоже одновалентны. Магний двухвалентен, т. к. у него два неспаренных электрона. У атомов гелия, неона и аргона все электроны спарены и отсутствуют свободные орбитали. Эти элементы химически инертны, то есть обладают нулевой валентностью.
Однако химические элементы в соединениях далеко не всегда проявляют валентность, соответствующую количеству неспаренных электронов в основном состоянии атома. Например, углерод может проявлять валентность IV (CO2).
Возможность проявлять ту или иную валентность зависит также и от количества свободных орбиталей на внешнем электронном слое атома: при наличии незанятых электронами р-орбиталей один из спаренных s-электронов может переходить на свободную р-орбиталь (при условии получения определенной порции дополнительной энергии извне).
Состояние атома, при котором электроны переходят с одной орбитали на другую в пределах одного энергетического уровня, называется возбужденным.
Пример. Рассмотрим атом углерода в основном и возбужденном состояниях (значком * обозначается возбужденное состояние атома):
В основном состоянии атом углерода имеет два неспаренных электрона на р-подуровне; при переходе атома в возбужденное состояние один из двух электронов s-подуровня может переходить на свободную р-орбиталь. Количество неспаренных электронов в возбужденном состоянии увеличится до четырех. Валентность углерода при этом также изменится с двух до четырех.
Если в атомах нет свободных орбиталей (например, у кислорода или фтора), то разъединить электронные пары в этом случае невозможно. Поэтому вaлентность этих элементов будет совпадать с количеством неспаренных электронов: кислород двухвалентен, фтор одновалентен.

Конспект урока «Валентность химических элементов».
Следующая тема: «Определение валентности + Примеры»
uchitel.pro
Валентность (химия) — это… Что такое Валентность (химия)?
- Валентность (химия)
Валентность (от лат. valens — имеющий силу) — способность атомов химических элементов образовывать химические связи с атомами других элементов. В свете строения атома валентность — это способность атомов отдавать или присоединять определенное число электронов. В соединениях, образованных при помощи ионных связей, валентность атомов определяется числом присоединенных или отданных электронов. В соединениях с ковалентными связями валентность атомов определяется числом образовавшихся «общих» электронных пар. Однако в настоящее время весьма затруднительно найти меру для характеристики способности атома к образованию химической связи. Существуют количественные характеристики способности атомов соединяться друг с другом: понятие валентности (ковалентности), понятие степени (состояния) окисления и понятие координационного числа.
Мнемонические правила
- Калий, натрий, серебро — одновалентное добро.
- Калий, натрий, серебро с водородом заодно.
- Железо, алюминий, хром — их валентность равна трем.
Литература
- Коулсон Ч. Валентность. М.: Мир, 1965.
- Маррел Дж., Кеттл С., Теддер Дж. Теория валентности. Пер. с англ. М.: Мир. 1968.
Wikimedia Foundation. 2010.
- Валентность (грамматика)
- Валенты Бадыляк
Смотреть что такое «Валентность (химия)» в других словарях:
Валентность (в лингвистике) — Валентность в синтаксисе способность слов сочетаться с другими элементами. Термин заимствован из химии (ср. валентность (химия)). Валентность слова определяется его лексическим значением, частью речи, к которой оно относится, а также… … Википедия
Валентность (грамматика) — Валентность в синтаксисе способность слов сочетаться с другими элементами. Термин заимствован из химии (ср. валентность (химия)). Валентность слова определяется его лексическим значением, частью речи, к которой оно относится, а также… … Википедия
Валентность (лингвистика) — У этого термина существуют и другие значения, см. Валентность (значения). Валентность (от лат. valentia сила) в синтаксисе способность слова вступать в синтаксические связи с другими элементами[1]. Термин заимствован из химии (ср. валентность… … Википедия
Валентность (химич.) — Валентность (от лат. valentia ≈ сила), способность атома к образованию химических связей. Количественной мерой В. обычно принято считать число других атомов в молекуле, с которыми данный атом образует связи. В. ≈ одно из фундаментальных понятий… … Большая советская энциклопедия
Валентность (в химии) — Валентность (от лат. valens имеющий силу) способность атомов химических элементов образовывать химические связи с атомами других элементов. В свете строения атома валентность это способность атомов отдавать или присоединять определенное число… … Википедия
ВАЛЕНТНОСТЬ — (от лат. valere иметь значение), или атомность, число атомов водорода или эквивалентных ему атомов или радикалов, к рое может присоединить данный атом или радикал. В. является одной из основ распределения элементов в периодической системе Д. И.… … Большая медицинская энциклопедия
валентность — – способность атома химического элемента образовывать химические связи с другими атомами. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
Валентность — У этого термина существуют и другие значения, см. Валентность (значения). Валентность (от лат. valēns «имеющий силу») способность атомов химических элементов образовывать определённое число химических связей с атомами других… … Википедия
Валентность — I Валентность (от лат. valentia сила) способность атома к образованию химических связей. Количественной мерой В. обычно принято считать число других атомов в молекуле, с которыми данный атом образует связи. В. одно из фундаментальных… … Большая советская энциклопедия
Химия — I Химия I. Предмет и структура химии Химия одна из отраслей естествознания, предметом изучения которой являются химические элементы (Атомы), образуемые ими простые и сложные вещества (молекулы (См. Молекула)), их превращения и… … Большая советская энциклопедия
Валентность (химия) — это… Что такое Валентность (химия)?
- Валентность (химия)
Валентность (от лат. valens — имеющий силу) — способность атомов химических элементов образовывать химические связи с атомами других элементов. В свете строения атома валентность — это способность атомов отдавать или присоединять определенное число электронов. В соединениях, образованных при помощи ионных связей, валентность атомов определяется числом присоединенных или отданных электронов. В соединениях с ковалентными связями валентность атомов определяется числом образовавшихся «общих» электронных пар. Однако в настоящее время весьма затруднительно найти меру для характеристики способности атома к образованию химической связи. Существуют количественные характеристики способности атомов соединяться друг с другом: понятие валентности (ковалентности), понятие степени (состояния) окисления и понятие координационного числа.
Мнемонические правила
- Калий, натрий, серебро — одновалентное добро.
- Калий, натрий, серебро с водородом заодно.
- Железо, алюминий, хром — их валентность равна трем.
Литература
- Коулсон Ч. Валентность. М.: Мир, 1965.
- Маррел Дж., Кеттл С., Теддер Дж. Теория валентности. Пер. с англ. М.: Мир. 1968.
Wikimedia Foundation. 2010.
- Валентность (грамматика)
- Валенты Бадыляк
Смотреть что такое «Валентность (химия)» в других словарях:
Валентность (в лингвистике) — Валентность в синтаксисе способность слов сочетаться с другими элементами. Термин заимствован из химии (ср. валентность (химия)). Валентность слова определяется его лексическим значением, частью речи, к которой оно относится, а также… … Википедия
Валентность (грамматика) — Валентность в синтаксисе способность слов сочетаться с другими элементами. Термин заимствован из химии (ср. валентность (химия)). Валентность слова определяется его лексическим значением, частью речи, к которой оно относится, а также… … Википедия
Валентность (лингвистика) — У этого термина существуют и другие значения, см. Валентность (значения). Валентность (от лат. valentia сила) в синтаксисе способность слова вступать в синтаксические связи с другими элементами[1]. Термин заимствован из химии (ср. валентность… … Википедия
Валентность (химич.) — Валентность (от лат. valentia ≈ сила), способность атома к образованию химических связей. Количественной мерой В. обычно принято считать число других атомов в молекуле, с которыми данный атом образует связи. В. ≈ одно из фундаментальных понятий… … Большая советская энциклопедия
Валентность (в химии) — Валентность (от лат. valens имеющий силу) способность атомов химических элементов образовывать химические связи с атомами других элементов. В свете строения атома валентность это способность атомов отдавать или присоединять определенное число… … Википедия
ВАЛЕНТНОСТЬ — (от лат. valere иметь значение), или атомность, число атомов водорода или эквивалентных ему атомов или радикалов, к рое может присоединить данный атом или радикал. В. является одной из основ распределения элементов в периодической системе Д. И.… … Большая медицинская энциклопедия
валентность — – способность атома химического элемента образовывать химические связи с другими атомами. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
Валентность — У этого термина существуют и другие значения, см. Валентность (значения). Валентность (от лат. valēns «имеющий силу») способность атомов химических элементов образовывать определённое число химических связей с атомами других… … Википедия
Валентность — I Валентность (от лат. valentia сила) способность атома к образованию химических связей. Количественной мерой В. обычно принято считать число других атомов в молекуле, с которыми данный атом образует связи. В. одно из фундаментальных… … Большая советская энциклопедия
Химия — I Химия I. Предмет и структура химии Химия одна из отраслей естествознания, предметом изучения которой являются химические элементы (Атомы), образуемые ими простые и сложные вещества (молекулы (См. Молекула)), их превращения и… … Большая советская энциклопедия
biograf.academic.ru
Валентность (химия) — это… Что такое Валентность (химия)?
- Валентность (химия)
Валентность (от лат. valens — имеющий силу) — способность атомов химических элементов образовывать химические связи с атомами других элементов. В свете строения атома валентность — это способность атомов отдавать или присоединять определенное число электронов. В соединениях, образованных при помощи ионных связей, валентность атомов определяется числом присоединенных или отданных электронов. В соединениях с ковалентными связями валентность атомов определяется числом образовавшихся «общих» электронных пар. Однако в настоящее время весьма затруднительно найти меру для характеристики способности атома к образованию химической связи. Существуют количественные характеристики способности атомов соединяться друг с другом: понятие валентности (ковалентности), понятие степени (состояния) окисления и понятие координационного числа.
Мнемонические правила
- Калий, натрий, серебро — одновалентное добро.
- Калий, натрий, серебро с водородом заодно.
- Железо, алюминий, хром — их валентность равна трем.
Литература
- Коулсон Ч. Валентность. М.: Мир, 1965.
- Маррел Дж., Кеттл С., Теддер Дж. Теория валентности. Пер. с англ. М.: Мир. 1968.
Wikimedia Foundation. 2010.
- Валентность (грамматика)
- Валенты Бадыляк
Смотреть что такое «Валентность (химия)» в других словарях:
Валентность (в лингвистике) — Валентность в синтаксисе способность слов сочетаться с другими элементами. Термин заимствован из химии (ср. валентность (химия)). Валентность слова определяется его лексическим значением, частью речи, к которой оно относится, а также… … Википедия
Валентность (грамматика) — Валентность в синтаксисе способность слов сочетаться с другими элементами. Термин заимствован из химии (ср. валентность (химия)). Валентность слова определяется его лексическим значением, частью речи, к которой оно относится, а также… … Википедия
Валентность (лингвистика) — У этого термина существуют и другие значения, см. Валентность (значения). Валентность (от лат. valentia сила) в синтаксисе способность слова вступать в синтаксические связи с другими элементами[1]. Термин заимствован из химии (ср. валентность… … Википедия
Валентность (химич.) — Валентность (от лат. valentia ≈ сила), способность атома к образованию химических связей. Количественной мерой В. обычно принято считать число других атомов в молекуле, с которыми данный атом образует связи. В. ≈ одно из фундаментальных понятий… … Большая советская энциклопедия
Валентность (в химии) — Валентность (от лат. valens имеющий силу) способность атомов химических элементов образовывать химические связи с атомами других элементов. В свете строения атома валентность это способность атомов отдавать или присоединять определенное число… … Википедия
ВАЛЕНТНОСТЬ — (от лат. valere иметь значение), или атомность, число атомов водорода или эквивалентных ему атомов или радикалов, к рое может присоединить данный атом или радикал. В. является одной из основ распределения элементов в периодической системе Д. И.… … Большая медицинская энциклопедия
валентность — – способность атома химического элемента образовывать химические связи с другими атомами. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
Валентность — У этого термина существуют и другие значения, см. Валентность (значения). Валентность (от лат. valēns «имеющий силу») способность атомов химических элементов образовывать определённое число химических связей с атомами других… … Википедия
Валентность — I Валентность (от лат. valentia сила) способность атома к образованию химических связей. Количественной мерой В. обычно принято считать число других атомов в молекуле, с которыми данный атом образует связи. В. одно из фундаментальных… … Большая советская энциклопедия
Химия — I Химия I. Предмет и структура химии Химия одна из отраслей естествознания, предметом изучения которой являются химические элементы (Атомы), образуемые ими простые и сложные вещества (молекулы (См. Молекула)), их превращения и… … Большая советская энциклопедия
dvc.academic.ru
Валентность — это… Что такое Валентность?
Вале́нтность (от лат. valēns «имеющий силу») — способность атомов химических элементов образовывать определённое число химических связей с атомами других элементов.
История возникновения понятия «валентность»
Этимологию термина валентность возможно отследить начиная с 1425 года, когда его начали использовать в научных текстах в значении «экстракт», «препарат». Использование в рамках современного определения зафиксировано в 1884 году (нем. Valenz).[1] В 1789 году Уильям Хиггинс опубликовал работу, в которой высказал предположение о существовании связей между мельчайшими частицами вещества.[2]
Однако точное и позже полностью подтверждённое понимание феномена валентности было предложено в 1852 году химиком Эдуардом Франклендом в работе, в которой он собрал и переосмыслил все существовавшие на тот момент теории и предположения на этот счёт.[3]. Наблюдая способность к насыщению разных металлов и сравнивая состав органических производных металлов с составом неорганических соединений, Франкленд ввёл понятие о «соединительной силе», положив этим основание учению о валентности. Хотя Франкленд и установил некоторые частные закономерности, его идеи не получили развития.
Решающую роль в создании теории валентности сыграл Фридрих Август Кекуле. В 1857 г. он показал, что углерод является четырёхосновным (четырёхатомным) элементом, и его простейшим соединением является метан СН4. Уверенный в истинности своих представлений о валентности атомов, Кекуле ввёл их в свой учебник органической химии: основность, по мнению автора — фундаментальное свойство атома, свойство такое же постоянное и неизменяемое, как и атомный вес. В 1858 г. взгляды, почти совпадающие с идеями Кекуле, высказал в статье «О новой химической теории» Арчибальд Скотт Купер.
Уже три года спустя, в сентябре 1861 г. А. М. Бутлеров внёс в теорию валентности важнейшие дополнения. Он провёл чёткое различие между свободным атомом и атомом, вступившим в соединение с другим, когда его сродство «связывается и переходит в новую форму». Бутлеров ввёл представление о полноте использования сил сродства и о «напряжении сродства», то есть энергетической неэквивалентности связей, которая обусловлена взаимным влиянием атомов в молекуле. В результате этого взаимного влияния атомы в зависимости от их структурного окружения приобретают различное «химическое значение». Теория Бутлерова позволила дать объяснение многим экспериментальным фактам, касавшимся изомерии органических соединений и их реакционной способности.
Огромным достоинством теории валентности явилась возможность наглядного изображения молекулы. В 1860-х гг. появились первые молекулярные модели. Уже в 1864 г. А. Браун предложил использовать структурные формулы в виде окружностей с помещёнными в них символами элементов, соединённых линиями, обозначающими химическую связь между атомами; количество линий соответствовало валентности атома. В 1865 г. А. фон Гофман продемонстрировал первые шаростержневые модели, в которых роль атомов играли крокетные шары. В 1866 г. в учебнике Кекуле появились рисунки стереохимических моделей, в которых атом углерода имел тетраэдрическую конфигурацию.
Современные представления о валентности
С момента возникновения теории химической связи понятие «валентность» претерпело существенную эволюцию. В настоящее время оно не имеет строгого научного толкования, поэтому практически полностью вытеснено из научной лексики и используется, преимущественно, в методических целях.
Резонансная модель образования ковалентных связей в молекуле HNO3В основном, под валентностью химических элементов понимается способность свободных его атомов к образованию определённого числа ковалентных связей. В соединениях с ковалентными связями валентность атомов определяется числом образовавшихся двухэлектронных двухцентровых связей. Именно такой подход принят в теории локализованных валентных связей, предложенной в 1927 году В. Гайтлером и Ф. Лондоном в 1927 г. Очевидно, что если в атоме имеется n неспаренных электронов и m неподелённых электронных пар, то этот атом может образовывать n + m ковалентных связей с другими атомами[4]. При оценке максимальной валентности следует исходить из электронной конфигурации гипотетического, т. н. «возбуждённого» (валентного) состояния. Например, максимальная валентность атома бериллия, бора и азота равна 4 (например, в Be(OH)42-, BF4— и NH4+), фосфора — 5 (PCl5), серы — 6 (H2SO4), хлора — 7 (Cl2O7).
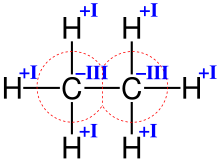 Структурная формула молекулы этана
Структурная формула молекулы этанаВ ряде случаев, с валентностью отождествляются такие характеристики молекулярной системы как степень окисления элемента, эффективный заряд на атоме, координационное число атома и т. д. Эти характеристики могут быть близки и даже совпадать количественно, но ни коим образом не тождественны друг другу[5]. Например, в изоэлектронных молекулах азота N2, монооксида углерода CO и цианид-ионе CN— реализуется тройная связь (то есть валентность каждого атома равна 3), однако степень окисления элементов равна, соответственно, 0, +2, −2, +2 и −3. В молекуле этана (см. рис.) углерод четырёхвалентен, как и в большинстве органических соединений, тогда как степень окисления формально равна −3.
Особенно это справедливо для молекул с делокализованными химическими связями, например в азотной кислоте степень окисления азота равна +5, тогда как азот не может иметь валентность выше 4. Известное из многих школьных учебников правило — «Максимальная валентность элемента численно равна номеру группы в Периодической таблице» — относится исключительно к степени окисления. Понятия «постоянной валентности» и «переменной валентности» также преимущественно относятся к степени окисления.
Семиполярные и донорно-акцепторные (дативные) связи по своей сути являются «двойными» связями, поскольку при их образовании происходят оба процесса: перенос электрона (образование ионной связи) и обобществление электронов (образование ковалентной связи).
Понятие валентности нельзя использовать и в очень многих случаях, когда невозможно применить модель двухэлектронных двухцентровых связей[6]. Представления о валентности не применимы к описанию кластерным соединениям, бороводородам, карборанам, π-комплексам, соединениям благородных газов и многим другим. Например, катионы щелочных металлов в комплексах с краун-эфирами проявляют валентность, намного превышающую их степень окисления.
Некорректным будет использование валентности для описания соединений ионной, кристаллической природы. Так в кристалле хлорида натрия NaCl у каждого иона Na+ или Cl— — центра элементарной ячейки — реальное число соседних ионов координационное число равно 6, а степень окисления — +1 и −1 соответственно. Локализованных же электронных пар вовсе нет.
В современной химии активно используется метод молекулярных орбиталей, в котором отсутствуют какие-либо аналоги понятия валентности атома. Между тем, понятие кратности химической связи наиболее близко к характеристике числа образуемых связей. Отождествление единичной связи с двухэлектронной молекулярной орбиталью возможно лишь в предельном, локализованном случае[5]. В квантовой химии аналога понятия валентности как характеристики атома в молекуле не существует, а используемое понятие спин-валентности относится к изолированному атому[7].
См. также
Примечания
- ↑ Valence — Online Etymology Dictionary.
- ↑ Partington J.R. A Short History of Chemistry. — Dover Publications, Inc, 1989. — ISBN 0-486-65977-1
- ↑ Frankland E. On a New Series of Organic Bodies Containing Metals. // Phil. Trans. 1852. Vol. 142. P. 417—444.
- ↑ Неорганическая химия / Б. Д. Степин, А. А. Цветков ; Под ред. Б. Д. Степина. — М.: Высш. шк., 1994. — С. 71—72
- ↑ 1 2 Валентность атомов в молекулах / Корольков Д. В. Основы неорганической химии. — М.: Просвещение, 1982. — С. 126
- ↑ Развитие учения о валентности. Под ред. Кузнецова В. И. М.: Химия, 1977. стр.19.
- ↑ Татевский В. М. Квантовая механика и теория строения молекул. М.: Изд-во МГУ, 1965. Глава 3.
Ссылки
Литература
- Л. Паулинг Природа химической связи. М., Л.: Гос. НТИ хим. литературы, 1947.
- Картмелл, Фоулс. Валентность и строение молекул. М.: Химия, 1979. 360 с.]
- Коулсон Ч. Валентность. М.: Мир, 1965.
- Маррел Дж., Кеттл С., Теддер Дж. Теория валентности. Пер. с англ. М.: Мир. 1968.
- Развитие учения о валентности. Под ред. Кузнецова В. И. М.: Химия, 1977. 248с.
- Валентность атомов в молекулах / Корольков Д. В. Основы неорганической химии. — М.: Просвещение, 1982. — С. 126.
biograf.academic.ru
Валентность (химия) — это… Что такое Валентность (химия)?
- Валентность (химия)
Валентность (от лат. valens — имеющий силу) — способность атомов химических элементов образовывать химические связи с атомами других элементов. В свете строения атома валентность — это способность атомов отдавать или присоединять определенное число электронов. В соединениях, образованных при помощи ионных связей, валентность атомов определяется числом присоединенных или отданных электронов. В соединениях с ковалентными связями валентность атомов определяется числом образовавшихся «общих» электронных пар. Однако в настоящее время весьма затруднительно найти меру для характеристики способности атома к образованию химической связи. Существуют количественные характеристики способности атомов соединяться друг с другом: понятие валентности (ковалентности), понятие степени (состояния) окисления и понятие координационного числа.
Мнемонические правила
- Калий, натрий, серебро — одновалентное добро.
- Калий, натрий, серебро с водородом заодно.
- Железо, алюминий, хром — их валентность равна трем.
Литература
- Коулсон Ч. Валентность. М.: Мир, 1965.
- Маррел Дж., Кеттл С., Теддер Дж. Теория валентности. Пер. с англ. М.: Мир. 1968.
Wikimedia Foundation. 2010.
- Валентность (грамматика)
- Валенты Бадыляк
Смотреть что такое «Валентность (химия)» в других словарях:
Валентность (в лингвистике) — Валентность в синтаксисе способность слов сочетаться с другими элементами. Термин заимствован из химии (ср. валентность (химия)). Валентность слова определяется его лексическим значением, частью речи, к которой оно относится, а также… … Википедия
Валентность (грамматика) — Валентность в синтаксисе способность слов сочетаться с другими элементами. Термин заимствован из химии (ср. валентность (химия)). Валентность слова определяется его лексическим значением, частью речи, к которой оно относится, а также… … Википедия
Валентность (лингвистика) — У этого термина существуют и другие значения, см. Валентность (значения). Валентность (от лат. valentia сила) в синтаксисе способность слова вступать в синтаксические связи с другими элементами[1]. Термин заимствован из химии (ср. валентность… … Википедия
Валентность (химич.) — Валентность (от лат. valentia ≈ сила), способность атома к образованию химических связей. Количественной мерой В. обычно принято считать число других атомов в молекуле, с которыми данный атом образует связи. В. ≈ одно из фундаментальных понятий… … Большая советская энциклопедия
Валентность (в химии) — Валентность (от лат. valens имеющий силу) способность атомов химических элементов образовывать химические связи с атомами других элементов. В свете строения атома валентность это способность атомов отдавать или присоединять определенное число… … Википедия
ВАЛЕНТНОСТЬ — (от лат. valere иметь значение), или атомность, число атомов водорода или эквивалентных ему атомов или радикалов, к рое может присоединить данный атом или радикал. В. является одной из основ распределения элементов в периодической системе Д. И.… … Большая медицинская энциклопедия
валентность — – способность атома химического элемента образовывать химические связи с другими атомами. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
Валентность — У этого термина существуют и другие значения, см. Валентность (значения). Валентность (от лат. valēns «имеющий силу») способность атомов химических элементов образовывать определённое число химических связей с атомами других… … Википедия
Валентность — I Валентность (от лат. valentia сила) способность атома к образованию химических связей. Количественной мерой В. обычно принято считать число других атомов в молекуле, с которыми данный атом образует связи. В. одно из фундаментальных… … Большая советская энциклопедия
Химия — I Химия I. Предмет и структура химии Химия одна из отраслей естествознания, предметом изучения которой являются химические элементы (Атомы), образуемые ими простые и сложные вещества (молекулы (См. Молекула)), их превращения и… … Большая советская энциклопедия
dal.academic.ru
Валентность (химия) — это… Что такое Валентность (химия)?
- Валентность (химия)
Валентность (от лат. valens — имеющий силу) — способность атомов химических элементов образовывать химические связи с атомами других элементов. В свете строения атома валентность — это способность атомов отдавать или присоединять определенное число электронов. В соединениях, образованных при помощи ионных связей, валентность атомов определяется числом присоединенных или отданных электронов. В соединениях с ковалентными связями валентность атомов определяется числом образовавшихся «общих» электронных пар. Однако в настоящее время весьма затруднительно найти меру для характеристики способности атома к образованию химической связи. Существуют количественные характеристики способности атомов соединяться друг с другом: понятие валентности (ковалентности), понятие степени (состояния) окисления и понятие координационного числа.
Мнемонические правила
- Калий, натрий, серебро — одновалентное добро.
- Калий, натрий, серебро с водородом заодно.
- Железо, алюминий, хром — их валентность равна трем.
Литература
- Коулсон Ч. Валентность. М.: Мир, 1965.
- Маррел Дж., Кеттл С., Теддер Дж. Теория валентности. Пер. с англ. М.: Мир. 1968.
Wikimedia Foundation. 2010.
- Валентность (грамматика)
- Валенты Бадыляк
Смотреть что такое «Валентность (химия)» в других словарях:
Валентность (в лингвистике) — Валентность в синтаксисе способность слов сочетаться с другими элементами. Термин заимствован из химии (ср. валентность (химия)). Валентность слова определяется его лексическим значением, частью речи, к которой оно относится, а также… … Википедия
Валентность (грамматика) — Валентность в синтаксисе способность слов сочетаться с другими элементами. Термин заимствован из химии (ср. валентность (химия)). Валентность слова определяется его лексическим значением, частью речи, к которой оно относится, а также… … Википедия
Валентность (лингвистика) — У этого термина существуют и другие значения, см. Валентность (значения). Валентность (от лат. valentia сила) в синтаксисе способность слова вступать в синтаксические связи с другими элементами[1]. Термин заимствован из химии (ср. валентность… … Википедия
Валентность (химич.) — Валентность (от лат. valentia ≈ сила), способность атома к образованию химических связей. Количественной мерой В. обычно принято считать число других атомов в молекуле, с которыми данный атом образует связи. В. ≈ одно из фундаментальных понятий… … Большая советская энциклопедия
Валентность (в химии) — Валентность (от лат. valens имеющий силу) способность атомов химических элементов образовывать химические связи с атомами других элементов. В свете строения атома валентность это способность атомов отдавать или присоединять определенное число… … Википедия
ВАЛЕНТНОСТЬ — (от лат. valere иметь значение), или атомность, число атомов водорода или эквивалентных ему атомов или радикалов, к рое может присоединить данный атом или радикал. В. является одной из основ распределения элементов в периодической системе Д. И.… … Большая медицинская энциклопедия
валентность — – способность атома химического элемента образовывать химические связи с другими атомами. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
Валентность — У этого термина существуют и другие значения, см. Валентность (значения). Валентность (от лат. valēns «имеющий силу») способность атомов химических элементов образовывать определённое число химических связей с атомами других… … Википедия
Валентность — I Валентность (от лат. valentia сила) способность атома к образованию химических связей. Количественной мерой В. обычно принято считать число других атомов в молекуле, с которыми данный атом образует связи. В. одно из фундаментальных… … Большая советская энциклопедия
Химия — I Химия I. Предмет и структура химии Химия одна из отраслей естествознания, предметом изучения которой являются химические элементы (Атомы), образуемые ими простые и сложные вещества (молекулы (См. Молекула)), их превращения и… … Большая советская энциклопедия
partners.academic.ru