Ломоносов ¦ Открытие закона сохранения материи и движения ¦ V-ratio
Деятельность Михаила Васильевича Ломоносова была связана с Академией наук. Несмотря на противодействие занимавших руководящие посты иностранцев, ученый развернул в ней интенсивную научную работу. По широте интересов, глубине проникновения в тайны мироздания Ломоносову принадлежит одно из самых видных мест в истории культуры всего человечества. Его можно сравнить с такими гигантами мировой культуры, как Леонардо да Винчи и Гете. Не было почти ни одной отрасли современной ему науки, техники и культуры, которой бы он не знал и в развитие которой не внес бы свой вклад. А. С. Пушкин сказал о гениальном русском ученом, что он, соединяя необыкновенную силу воли с необыкновенной силой понятия, обнял все отрасли просвещения.
Ломоносов хорошо владел научным методом познания. Он учил, что сначала нужно произвести наблюдения, потом на основании наблюдений установить теорию и затем проверить ее на практике.
Всякое явление Ломоносов пытался объяснить математически. Он считал, что в природе нет ничего, что нельзя было бы изучить, понять. Он полагал, что Солнце и планеты не были созданы богом, а возникли по естественным законам.
Ломоносов работал в самых различных отраслях науки, но наибольших успехов достиг в области физики и химии.
Он сформулировал самый общий закон естествознания – закон сохранения материи и движения. До Ломоносова закон сохранения движения был выведен Декартом и Лейбницем, которые считали, что при всех явлениях в природе неизменным остается только количество механического движения. Ломоносов же сформулировал свой закон в 1748 году в следующем виде: «Все перемены, в натуре случающиеся, такого суть состояния, что сколько у одного тела отнимается, столько присовокупится к другому.
Замечательно, что под движением Ломоносов понимает не только механическое перемещение, но и тепловое; по сути дела он высказывал мысль о переходе одних форм движения в другие.
Ломоносов не только сформулировал свой закон, но и применял его. Так, пользуясь этим законом, он объяснил процесс перехода энергии при теплопередаче, процессы, происходящие в охлаждающих смесях, и другие случаи перехода энергии.
С развитием физики и техники формулировка закона сохранения энергии все более и более уточняется. Необходимость улучшения тепловых машин и их коэффициента полезного действия заставила более обстоятельно заняться изучением тепловых процессов. Это привело к окончательному выяснению того, что теплота является формой энергии, и к установлению впоследствии Майером, Джоулем, Гельмгольцем и Линцом механического эквивалента теплоты. Таким образом, Ломоносов является прямым предшественником этих ученых.
Это привело к окончательному выяснению того, что теплота является формой энергии, и к установлению впоследствии Майером, Джоулем, Гельмгольцем и Линцом механического эквивалента теплоты. Таким образом, Ломоносов является прямым предшественником этих ученых.
Михаил Васильевич Ломоносов (1711–1765)
Ломоносов – первый русский академик
Открытие закона сохранения материи и движения
Учение Ломоносова о движении атомов
Ломоносов опровергает теорию теплорода
Закон сохранения массы (закон Ломоносова)
Экспериментальное доказательство закона сохранения массы при химических взаимодействиях явилось первым примером количественного химического анализа. Гениальный русский ученый М. В. Ломоносов (1711— 1765), впервые применивший весы и взвешивание для количественного контроля химических превращений и открывший закон сохранения массы, является основоположником количественного анализа. [c.7]Закон сохранения массы и энергии.
 В 1760 г. Ломоносов, по существу, сформулировал единый закон сохранения массы и энергии «Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимается, столько же присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте… Сей всеобщий естест венный закон распространяется и в самые правила движения, ибо тело, движущее своею силою другое, столько же оныя у себя теряет, сколько сообщает другому, которое от него движение получает». Однако до начала XX в. эти законы обычно рассматривались независимо друг от друга. Химия в основном имела дело с законом сохранения массы вещества, а физика — с законом сохранения энергии. В 1905 г. основоположник современной физики А.Эйнштейн показал, что между массой и энергией существует взаимосвязь, выражаемая уравнением
В 1760 г. Ломоносов, по существу, сформулировал единый закон сохранения массы и энергии «Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимается, столько же присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте… Сей всеобщий естест венный закон распространяется и в самые правила движения, ибо тело, движущее своею силою другое, столько же оныя у себя теряет, сколько сообщает другому, которое от него движение получает». Однако до начала XX в. эти законы обычно рассматривались независимо друг от друга. Химия в основном имела дело с законом сохранения массы вещества, а физика — с законом сохранения энергии. В 1905 г. основоположник современной физики А.Эйнштейн показал, что между массой и энергией существует взаимосвязь, выражаемая уравнением М. Б. Ломоносов (1711 — 1765) впервые стал систематически применять весы при изучении химических реакций. Б 1756 г. он экспериментально установил один из основных законов природы — закон сохранения массы вещества, составивший основу количественного анализа и имеющий огромное значение для всей науки. М. В. Ломоносов разработал многие приемы химического анализа и исследования, не потерявшие значения до наших дней [c.8]
М. В. Ломоносов разработал многие приемы химического анализа и исследования, не потерявшие значения до наших дней [c.8]
Химия как точная наука зародилась еще в эпоху полного господства теории флогистона Более определенным временем ее возникновения можно условно считать середину XVIII в., когда М. В. Ломоносов (1711 — 1765) сформулировал закон сохранения массы вещества в химических процессах и доказал его экспериментально. Он же первый высказал мысль, что при нагревании металл соединяется, как он говорил, с частичками воздуха. Заслуга полного и окончательного ниспровержения флогистонной теории принадлежит великому французскому химику А. Лавуазье (1743—1794), который, изучая горение и обжиг металлов, не только выяснил и сделал очевидной для других роль кислорода в этих явлениях, разрушив тем самым теорию флогистона, но также внес ясность в понятия химического элемента, простого и сложного вещества и независимо от Ломоносова экспериментально установил закон сохранения массы в химических реакциях.
Закон сохранения массы. На основании молекулярно-атомистических представлений М. В. Ломоносов сделал вывод Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько же присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте . Позднее, применяя точные методы исследования, ученые подтвердили опытным путем, что при химических превращениях общая масса веществ остается неизменной. Этот закон — закон сохранения массы — в настоящее время формулируется так [c.10]
В связи со сказанным необходимо реабилитировать гения русской науки — Михаила Васильевича Ломоносова. До сих пор приходится встречаться с ложным утверждением о том, что закон сохранения энергии открыт Ломоносовым. Это утверждение основывается не на каких-либо работах Ломоносова, а на одной фразе в его письме Эйлеру 5 июля 1748 года Так, сколько материи прибавляется какому-либо телу, столько же теряется у другого… Так как это всеобщий закон природы, то он распространяется и на правила движения тело, которое своим толчком возбуждает другое к движению, столько же теряет от своего движения, сколько сообщает другому, им двинутому . Слова очень содержательные. Но, во-первых, они касаются не энергии, а движения — понятия неопределенного, и, во-вторых, сходные мысли были высказаны еще в XVH веке Декартом, утверждавшим, что во Вселенной в.сегда сохраняется одно и то же количество движения. Закона сохранения энергии здесь нет, да и невозможно было открыть его до наступления века пара и электричества. Ломоносов, открывший закон сохранения массы, обосновавший кинетическую теорию тепла, так много сделавший в науке и искусстве, не нуждается в том, чтобы ему приписывали мнимые открытия. [c.16]
Это утверждение основывается не на каких-либо работах Ломоносова, а на одной фразе в его письме Эйлеру 5 июля 1748 года Так, сколько материи прибавляется какому-либо телу, столько же теряется у другого… Так как это всеобщий закон природы, то он распространяется и на правила движения тело, которое своим толчком возбуждает другое к движению, столько же теряет от своего движения, сколько сообщает другому, им двинутому . Слова очень содержательные. Но, во-первых, они касаются не энергии, а движения — понятия неопределенного, и, во-вторых, сходные мысли были высказаны еще в XVH веке Декартом, утверждавшим, что во Вселенной в.сегда сохраняется одно и то же количество движения. Закона сохранения энергии здесь нет, да и невозможно было открыть его до наступления века пара и электричества. Ломоносов, открывший закон сохранения массы, обосновавший кинетическую теорию тепла, так много сделавший в науке и искусстве, не нуждается в том, чтобы ему приписывали мнимые открытия. [c.16]
Закон сохранения массы и э н е р г и и.
На основе достижений современной атомной физики и теории относительности было установлено, что закон сохранения массы тесно связан с законом сохранения энергии (Ломоносов, 1748 г., Мейер, 1842 г.). Соотношение между массой и энергией было установлено Эйнштейном, который показал, что изменение энергии системы прямо пропорционально изменению массы [c.11]
Закон сохранения массы вещества. Впервые его высказал М. В. Ломоносов в письме к Эйлеру от 5 июня 1748 г., опубликованном на русском языке в 1760 г. Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому… Это определение, за исключением архаичности языка, не устарело. [c.13]
Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому… Это определение, за исключением архаичности языка, не устарело. [c.13]
Закон сохранения массы при химических реакциях. В 1756 г. Ломоносов, применяя количественные методы при исследовании химических процессов, установил, что при химических превращениях масса веществ остается неизменной. Это открытие Ломоносова стало одним из основных законов химии, который в настоящее время формулируется следующим образом масса веществ, вступивших в реакцию, всегда равна массе вешаете, образовавшихся в результате реакции. [c.8]
Творческая деятельность Ломоносова отличается исключительной широтой интересов и глубиной проникновения в тайны природы. Его исследования относятся к области физики, химии, астрономии и др. Результаты этих работ заложили основы современного естествознания. Ломоносов указал (1765) на основополагающее значение закона сохранения массы вещества в химических реакциях изложил (1741 —1750) основы корпускулярного (атомно-молекулярного) учения выдвинул (1744—1748) кинетическую теорию теплоты. Был зачинателем применения математических и физических методов исследования в химии и первым начал читать в Петербургской АН самостоятельный Курс истинно физической химии , заложил основы русского химического языка. [c.9]
Был зачинателем применения математических и физических методов исследования в химии и первым начал читать в Петербургской АН самостоятельный Курс истинно физической химии , заложил основы русского химического языка. [c.9]
Закон сохранения массы вещества. Применяя количественные методы исследования химических реакций, М. В. Ломоносов установил, что при химических превращениях общий вес вещества остается неизменным. На основании своих опытов он сформулировал закон сохранения массы веш,еств [c.25]
Ломоносов первый из отечественных ученых начал применять физические методы исследований в химии. Закон сохранения массы вещества и энергии был одним из важнейших открытий Ломоносова в области физической химии. Ломоносовым установлено, что понижение температуры замерзания раствора зависит от его концентрации, и эта температура бывает всегда ниже температуры замерзания чистого растворителя. Им сделан и ряд других открытий и исследований. [c. 6]
6]
Из этой формулировки видно, что М. В. Ломоносов закон сохранения массы веществ рассматривал в единстве с законом сохранения энергии и понимал его как всеобщий закон природы. [c.56]
Закон сохранения массы. Исключительное значение для химии имело установление закона сохранения массы, являющегося следствием всеобщего естественного закона сохранения материи и движения, сформулированного М. В. Ломоносовым (1711 —1765 гг.) как всеобщий естественный закон в 1748 г. в письме к Д. Эйлеру Все перемены, в натуре случающиеся, такого суть состояния, что, сколько чего у одного тела отнимется, столько присовокупится к другому, ежели где убудет несколько материи, то умножится в другом месте… Сей всеобщий закон простирается и в самые правила движения ибо тело, движущее своей силой другое, столько же оныя у себя теряет, сколько сообщает другому, которое от него движение получает (Ломоносов М. В. Труды по физике и химии,— М.. 1951.— Т. II.— С. 183). [c. 14]
14]
В 1749 г, по чертежам и указаниям Ломоносова была построена первая в России химическая научная и учебная лаборатория на Васильевском острове в Петербурге. В лаборатории Ломоносов экспериментально обосновывает закон сохранения массы веществ, сформулированный нм еще в 1748 г. [c.8]
М. В. Ломоносов сначала высказал теоретически (1748), а затем экспериментально обосновал (1756 ) закон сохранения массы веществ. В настоящее время он формулируется так [c.15]
М. В. Ломоносов связывал закон сохранения массы веществ с законом сохранения энергии (количества движения) и рассматривал их в единстве как всеобщий закон природы. Этот закон он сформулировал в 1748 г. следующим образом Все перемены в натуре случающиеся такого суть состояния, что сколько чего у одного тела отнимается, столько присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте. Сей всеобщий естественный закон простирается и в самые правила движения ибо тело, движущее [c. 15]
15]
М. В. Ломоносов сначала теоретически, а затем опытным путем открыл и обосновал закон сохранения массы веществ, который лежит в основе всех химических реакций. В настоящее время он формулируется следующим образом масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции. [c.18]
М. В. Ломоносов связывал закон сохранения массы веществ с законом сохранения энергии (количества движения) и рассматривал их в единстве как всеобщий закон природы. Этот закон он сформулировал в 1748 г. следующим образом [c.18]
В 1748 г. М. В. Ломоносов сформулировал положение, которое в дальнейшем сыграло большую роль в развитии химии и получило название закона сохранения массы веш,еств масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции. [c.21]
Впоследствии М. В. Ломоносов экспериментально подтвердил правильность своих выводов. Независимо от М. В. Ломоносова закон сохранения массы веществ был сформулирован позднее французским химиком Лавуазье. [c.21]
Независимо от М. В. Ломоносова закон сохранения массы веществ был сформулирован позднее французским химиком Лавуазье. [c.21]
Одним из первых химических явлений, с которым человечество познакомилось на заре своего существования, было горение. Вна-ч-але оно использовалось для варки пищи и обогрева жилища. Лишь через многие тысячелетия человек научился использовать его для превращения химической анергии горючих веществ в механическую, электрическую и другие формы энергии. Представления об этом явлении менялись у человека по мере накопления им все новых и новых фактов. Впервые правильное представление о процессе горения высказал гениальный русский ученый Михаил Васильевич Ломоносов (1711—1765 гг.), заложивший основы отечественной науки и установивший ряд важнейших законов современной химии и физики. Он провел большое количество опытов с прокаливанием свинца и олова в открытых и запаянных сосудах. Во всех опытах М. В. Ломоносов производил взвешивание вещества до прокаливания и после него. Он убедился, что металлы при прокаливании увеличиваются в весе за счет соединения их с воздухом (в то время кислород был неизвестен). В этих опытах он впервые установил основной закон химии — закон сохранения массы вещества. [c.5]
Он убедился, что металлы при прокаливании увеличиваются в весе за счет соединения их с воздухом (в то время кислород был неизвестен). В этих опытах он впервые установил основной закон химии — закон сохранения массы вещества. [c.5]
М. В. Ломоносов первым из ученых (в 1748 г.) сформулировал закон сохранения массы вещества при химической реакции. Q писал … все перСхМены, в., натуре случающиеся, такого суть состояния, что, сколько чего у одного тела отнимается, столько присовокупится к другому . Этот закон в современной формулировке гласит Масса веществ, вступивших в реакцию, всегда равна массе веществ, образовавшихся в результате реакции. [c.3]
Химическая промышленность в период домонополистического капитализма. Во второй половине ХУП1 в. возникает одновременно с химией химическая технология. Большое значение для обеих наук имеет закон сохранения массы, открытый М. В. Ломоносовым. В применении к химическим производствам этот закон позволяет вычислять максимально возможные (стехиометрические) выходы продуктов и составлять материальные балансы, а это является первым шагом при проектировании технологического процесса. М. В. Ломоносов уделял много внимания и непосредственно химической технологии. Своими трудами он содействовал развитию в России металлургии, стекловарения, производства фарфора. [c.11]
М. В. Ломоносов уделял много внимания и непосредственно химической технологии. Своими трудами он содействовал развитию в России металлургии, стекловарения, производства фарфора. [c.11]
Закон сохранения массы. Ломоносов создал при Академии наук химическую лабораторию. В ней он изучал протекаиие химических реакций, взвешивая исходные вещества и продукты реакции. При этом он установил закон сохранения массы (веса) [c.18]
Закон сохранения массы при химических реакциях. Применяя количественные методы при исследовании химических процессов, Ломоносов в 1756 г. установил, что ири химических превращениях общая масса веществ остается неизменной. Это открытие Ломоносова ста ю одним из основных закогюв химии, который в настоя-огсе время формулируется следующим образом [c.12]
Возникновение физической хнмии как самостоятельной науки относится к середине XVIII в. Первый в мире курс физической химии был создан М. В. Ломоносовым (1752—1754). На основе своих физико-химических исследований М. В. Ломоносов пришел к принципиально новому определению химии как науки о свойствах тел, исходя из того, что все изменения в природе связаны с движением материи. Он первым обосновал основной закон сохранения массы вещества и пришел к определению принципа сохранения материи и движения, получившего признание как всеобщий закон природы. [c.6]
На основе своих физико-химических исследований М. В. Ломоносов пришел к принципиально новому определению химии как науки о свойствах тел, исходя из того, что все изменения в природе связаны с движением материи. Он первым обосновал основной закон сохранения массы вещества и пришел к определению принципа сохранения материи и движения, получившего признание как всеобщий закон природы. [c.6]
Михаил Васильевич Ломоносов — великий русский ученый — одни из основоположников новой химии. Он открыл основной закон химии — закон сохранения массы веществ. Разработал теорию атомно-молекуляриого строения веществ, являющуюся основой физики и химии. Ввел в химию количественные методы исследования. Объединил химию с физикой, создал новую науку — физическую химию. Большим вкладом в науку являются его работы по исследованию растворов. С имеием Ломоносова связано развитие в России различных иаук. Историк, ритор, механик, химик, минералог, художник и сти.хотворец — он все испытал и все проник , — писал о нем А. С. Пушкин. [c.4]
С. Пушкин. [c.4]
Ломоносов первый из отечественных ученых начал применять физические методы исследований в химии. Закон сохранения массы вещества и энергии был одним из важнейших открытий Ломо- [c.6]
Атомно-молекулярная теория. Создатель атомно-молекулярного учения и первооткрыватель закона сохранения массы веществ М.В.Ломоно-сов по праву считается основателем научной химии. Ломоносов четко различал две ступени в строении вещества элементы (в нашем понимании — атомы) и корпускулы (молекулы). Согласно Ломоносову, молекулы простых веществ состоят из одинаковых атомов, а молекулы сложных веществ — из разных атомов. Всеобщее признание атомно-молекулярная теория получила в начале XIX в. после утверждения в химии атомистики Дальтона. С тех пор главным объектом иссле- [c.7]
Систематическое изучение количественных соотношений между составом веществ и физическими свойствами началось в XVIII в. Основополагающими в этой области являются труды М. В. Ломоносова и А. Лавуазье. М. В. Ломоносов в 1748 г. сформулировал закон сохранения массы и энергии. Он же первый сформулировал основную задачу физико-химического анализа как установление зависимости свойств от состава системы для выяснения природы составляющих ее частей . К сожалению, труды М. Е5. Ломоносова оставались долгое время неизвестными и были опубликованы Б. Н. Меншуткиным лишь в 1904 г. [c.265]
В. Ломоносова и А. Лавуазье. М. В. Ломоносов в 1748 г. сформулировал закон сохранения массы и энергии. Он же первый сформулировал основную задачу физико-химического анализа как установление зависимости свойств от состава системы для выяснения природы составляющих ее частей . К сожалению, труды М. Е5. Ломоносова оставались долгое время неизвестными и были опубликованы Б. Н. Меншуткиным лишь в 1904 г. [c.265]
Закон сохранения массы. Химические уравнения. и расчеты по ним. Закон сохранения массы веи еств масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции (М. В. Ломоносов, 1848). С точки зрения атомно-молекулярного учения при химич еских реакциях атомы не образуются из ничего и не исчезают, поэтому число атомов всех видов в ходе химической реакции остается неизменным. А так. hMi маестгданного атома постоянна, [c.17]
И только в начале XIX столетия английский ученый Джон Дальтон возвращается к атомам как наименьшим частицам материи и вводит в науку этот термин. Этому предшествовали работы таких замечательных ученых, как Р. Бойль (в книге Химик-скептик он нанес сокрушительный удар по представлениям алхимиков), Дж. Пристли и К. В. Шееле (открытие кислорода), Г. Кавендиш (открытие водорода), А. Л. Лавуазье (попытка составить первую таблицу простых веществ), М. В. Ломоносов (основные положения атомно-молекулярного учения, закон сохранения массы), Ж. Л. Ируст (закон постоянства состава) и многие другие. [c.3]
Этому предшествовали работы таких замечательных ученых, как Р. Бойль (в книге Химик-скептик он нанес сокрушительный удар по представлениям алхимиков), Дж. Пристли и К. В. Шееле (открытие кислорода), Г. Кавендиш (открытие водорода), А. Л. Лавуазье (попытка составить первую таблицу простых веществ), М. В. Ломоносов (основные положения атомно-молекулярного учения, закон сохранения массы), Ж. Л. Ируст (закон постоянства состава) и многие другие. [c.3]
Ломоносов закон сохранения веса — Справочник химика 21
Весы — измерительный прибор, служащий для определения массы данного тела путем сравнения ее с массой, условно принятой за единицу (грамм, килограмм и т. д.). Пользуясь весами, М. В. Ломоносов в 1756 г. на опыте доказал справедливость сформулированного им в 1748 г. закона сохранения веса веществ. [c.25] Лавуазье формулировал свое обобщение, как закон сохранения веса вещества. Ломоносов смог проникнуть в природу гораздо глубже, чем Лавуазье, и сформулировал свой закон следующим образом Все перемены в натуре (природе) такого суть состоян 1я, что сколько чего у одного тела отнимается, столько присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте . Из этого видно, что Ломоносов рассматривал открытый им закон, как закон сохранения материи вообще, а не только одной из форм материи — вещества. [c.14]
Так, ежели где убудет несколько материи, то умножится в другом месте . Из этого видно, что Ломоносов рассматривал открытый им закон, как закон сохранения материи вообще, а не только одной из форм материи — вещества. [c.14]
Основоположник количественного анализа — гениальный русский ученый М. В. Ломоносов (1711 — 1765), впервые применивший весы и взвешивание для количественного контроля химических превращений. М. В. Ломоносовым были теоретически развиты молекулярно-атомистические представления и впервые сформулирован закон сохранения веса веществ. С открытием этого закона количественный анализ получил научное обоснование, появилась возможность точного исследования количественного состава химических соединений. Ломоносов разработал теоретические основы физической химии, оказавшей большое влияние на развитие аналитической химии. В 1748 г. он организовал первую в России хи- мическую научно-исследовательскую лабораторию.
 Б этой лаборатории гениальный ученый произвел большое количество опытов и исследований. Им написано первое на русском языке ценное руководство по металлургии, в котором были описаны разнообразные химические операции, приме- няемые в аналитической практике, а также методы анализа руд, металлов, солей и т. д. В 1744 г. М. В. Ломоносов впервые применил микроскоп для изучения химических процессов. [c.7]
Б этой лаборатории гениальный ученый произвел большое количество опытов и исследований. Им написано первое на русском языке ценное руководство по металлургии, в котором были описаны разнообразные химические операции, приме- няемые в аналитической практике, а также методы анализа руд, металлов, солей и т. д. В 1744 г. М. В. Ломоносов впервые применил микроскоп для изучения химических процессов. [c.7]Возможность количественного анализа возникла только после того, как великий русский ученый М. В. Ломоносов (1711—1765) в результате исследований в 1756—1760 гг. установил закон сохранения веса (массы) веществ при химических реакциях. [c.32]
Во-вторых, в 1748 году Ломоносов пришел к открытию закона сохранения веса вещества чиста теоретическим путем. Он прекрасно понимал, что такой фундаментальный закон необходимо тщательнейшим образом проверить точными опытами, прежде чем предавать его гласности вполне официальным способом. Ломоносов был в высшей степени честен и требователен к себе, он слишком любил и уважал науку, чтобы решиться выступить с недостаточно разработанными, по его мнению, теориями. Хотя всю систему корпускулярной философии МОР бы опубликовать, — писал он Эйлеру в том же письме от [c.72]
Хотя всю систему корпускулярной философии МОР бы опубликовать, — писал он Эйлеру в том же письме от [c.72]
Как раз в это время Ломоносов обдумывал планы организации химической лаборатории при Академии наук. Надеясь подтвердить в будущей лаборатории свои теории опытами, Ломоносов отложил окончательное опубликование закона сохранения веса вещества, ограничившись пока сообщением о нем в письме к Эйлеру. [c.72]
Ломоносов установил, что с металлом при прокаливании соединяется не таинственная выдуманная материя огня , а часть воздуха, находящегося в сосуде. Но в строгом соответствии с законом Ломоносова — законом сохранения веса вещества — сколько прибавилось к металлу, столько убавилось от воздуха. И если взвешивать сосуд, как это делал Ломоносов, не вскрывая — без пропущения внешнего воздуха , — вес остается неизменным — в одной мере . При вскрытии же сосуда, как в опытах Бойля, на место воздуха, соединившегося с металлом, входит наружный воздух, за счет которого и образуется прибавка в весе. [c.75]
[c.75]
Таким образом, в отличие от закона сохранения и превращения энергии, который Ломоносов высказал и впервые в истории науки применял в своих исследованиях, но не доказал количественными измерениями, закон сохранения веса вещества был доказан им строго количественно. [c.75]
Доказав точными опытами закон сохранения веса вещества, Ломоносов сделал все от него зависящее, чтобы познакомить весь ученый мир с открытым им законом. Теперь он счел возможным опубликовать закон уже не в форме письма Эйлеру, а в официальном докладе Академии наук. 30 января 1758 года на заседании конференции Академии наук он представил написанную им на латинском языке диссертацию Об отношении количества материи и веса . В этом сочинении Ломоносов почти полностью использовал свое письмо к Эйлеру от 5 июля 1748 года, дав ту же, что и там, формулировку закона сохранения вещества и энергии. [c.76]
Великий Ломоносов открыл путь к такой методике. Закон сохранения веса вещества он доказал потому, что не ограничился простым прокаливанием металлов, как это делал Роберт Бойль. Ломоносов сознательно учитывал роль воздуха и этим положил начало разработке нового метода исследования — улавливания и измерения газообразных тел. Использованием этого метода объяснялся и успех Блэка при изучении щелочных веществ. [c.83]
Закон сохранения веса вещества он доказал потому, что не ограничился простым прокаливанием металлов, как это делал Роберт Бойль. Ломоносов сознательно учитывал роль воздуха и этим положил начало разработке нового метода исследования — улавливания и измерения газообразных тел. Использованием этого метода объяснялся и успех Блэка при изучении щелочных веществ. [c.83]
Новый учебник химии Лавуазье охватил Все существенные открытия в области этой науки. 6 появлением его для большинства исследователей отпала необходимость обращаться непосредственно к изучению научных трудов, опубликованных раньше, в особенности отдельных статей, напечатанных в старых журналах. Поэтому постепенно уменьшалось число ученых знавших, что автором закона сохранения вещества является Ломоносов. А так как именно этот закон был краеугольным камнем здания новой химии и составлял главную опору новых взглядов, последовательно проведенных в учебнике Лавуазье, в котором имя Ломоносова ке упоминалось, — читатели учебника невольно приходили к мысли, что автором закона сохранения веса вещества является сам Лавуазье. .. [c.101]
.. [c.101]
Ломоносов — один из основоположников химий он первый определил задачи этой науки. Разработанная Михаилом Васильевичем атомно-молекулярная теория строения вещества является основой физики и химии. Им открыт основной закон химии — закон сохранения веса. Все перемены, в натуре случающиеся, — писал он в 1748 г.,— такого суть состояния, что сколько чего у одного отнимается, столько и присовокупится к другому. Так, ежели где убудет несколько материи, то столько же умножится ее в другом месте . [c.28]
Нет никакого сомнения в том, что частички из воздуха, текущего непрерывно над подвергаемым обжиганию телом, соединяются с последним и увеличивают его вес , Ломоносов придавал закону сохранения веса вещества исключительное значение, доказательством чего является то, что он неоднократно тщательно проверял этот закон и в своих научных трудах по химии и физике исходил из этого закона. [c.33]
Как Ломоносов сформулировал закон сохранения веса вещества [c. 35]
35]
Ломоносов постоянно подчеркивал важность соблюдения в химических опытах меры и весов >, т. е. точных количественных измерений, чему до него не придавали особого значения. Ломоносов в этом отношении опередил Лавуазье, которого многие считают творцом количественных измерений в химии. Важнейшей заслугой Ломоносова перед наукой является то, что он впервые в истории науки на основании проведенных им опытов установил закон сохранения веса веществ. Одновременно он сформулировал и сущность другого важнейшего закона природы — закона сохра- нения энергии. Замечательно то, что Ломоносов в отличие от со- временных ему ученых не устанавливает резкой грани между веществом (массой) и энергией. В своей формулировке указанных законов он говорит о всех переменах, в натуре случающихся , об общем сохранении вещества и энергии и в качестве примеров приводит сохранение веса веществ, сохранение силы движения и т. д. В этом отношении он приближается к современному пониманию материи, согласно которому масса и энергия являются лишь различными проявлениями одной и той же сущности —материи. [c.17]
[c.17]
Особенно быстрое развитие аналитическая химия получила после того, как гениальный русский ученый М. В. Ломоносов (1711 —1765) в 1748 г. организовал в России первую научную и учебную химическую лабораторию и открыл закон сохранения веса (массы) веществ при химических реакциях. В трудах М. В. Ломоносова описаны разработанные им методы химического анализа минералов, руд, металлов, поваренной соли, минеральных вод и некоторых газов. Он ввел понятие о реактивах, осаждении и осадках и заложил основы качественного микрокристаллоскопического анализа, который творчески развивали в нашей стране академик Т. Е. Ло-виц (1757—1804) и другие ученые. [c.4]
М. В. Ломоносов открыл закон сохранения веса (массы) вещества при химических реакциях. Этот закон Ломоносов впервые изложил в 1748 г. в письме к знаменитому математику Л. Эйлеру. В 1756 г. М. В. Ломоносов опытным путем доказал ошибочность утверждений английского химика Роберта Бойля, который на основании своих опытов по прокаливанию металлов в запаянных сосудах пришел к неверному выводу, что вес прокаленного металла после реакции увеличивается за счет присоединения к нему материи огня . [c.15]
[c.15]
Еще в 1741 г. М. В. Ломоносов высказал мысль о необходимости проведения количественных исследований в хим ии. Открытый им закон сохранения веса веществ при химических реакциях лег в основу количественного анализа и всей теоретической химии. Этот закон позволял судить о правильности проводимых опы гов, о количественном составе исходных и полученных веществ. [c.15]
Из всего вышеизложенного можно сделать следующие выводы Ломоносов не занимался специально разработкой методов анализа. Но, разрешая те или иные крупные теоретические вопросы, он заложил основу для последующего развития аналитической химии. Открытие им закона сохранения веса, введение в повседневную практику химической лаборатории весов и микроскопа, признание необходимости тщательного изучения растворов, кристаллов, осадков и всех процессов, связанных с их образованием, го оптические работы — все это создало прочную теоретическую базу, на которой в дальнейшем смогла вырасти самостоятельная отрасль науки — аналитическая химия. Умело сочетая в своей работе теорию и практику, М. В. Ломоносов разрешал насущные практические задачи, давая им серьезное теоретическое обоснование, тем самым заложив фундамент научного химического исследования состава веществ и их смесей. [c.150]
Умело сочетая в своей работе теорию и практику, М. В. Ломоносов разрешал насущные практические задачи, давая им серьезное теоретическое обоснование, тем самым заложив фундамент научного химического исследования состава веществ и их смесей. [c.150]
Закон сохранения веса. М. В. Ломоносов впервые обратил внимание на то, что в природе ничто не может исчезнуть и ничто не может возникнуть из ничего. Этот закон назван законом сохранения веса. [c.26]
Как уже было отмечено выше, Ломоносов был первым химиком, который строил и физику, и химию на основе молекулярной и атомной теории. Он открыл два основных закона современного естествознания — закон сохранения веса и закон сохранения энергии. Он был первым химиком, правильно объяснившим процессы превращения металлов в их окиси. [c.30]
М. В. Ломоносов впервые применил для изучения химических реакций количественные методы исследования и сформулировал закон сохранения веса веществ (1748 г. ). Согласно этому закону, вес всех веществ, вступивших в реакцию, равен весу всех продуктов реакции. [c.9]
). Согласно этому закону, вес всех веществ, вступивших в реакцию, равен весу всех продуктов реакции. [c.9]
Развитие количественного анализа. Строгое научное обоснование принципа количественного химического анализа стало возможным только после установления закона сохранения веса вещества при химических реакциях. В середине ХУП1 в. этот закон сформулировал и экспериментально доказал М. В. Ломоносов. Однако отдельные методы химического анализа существовали задолго до этого времени. Открытие М. В. Ломоносова в значительной степени являлось обобщением многих предыдущих работ, в результате которых был установлен количественный состав многих минералов, руд, технических продуктов и различных химических препаратов. Долгое время методика анализа рассматривалась как раздел технологии тех или других веществ. Изучение методов определения драгоценных металлов в их сплавах (так называемый пробирный анализ ), исследование минералов, проверка качества лекарственных препаратов и другие работы способствовали развитию методов химического анализа. [c.10]
[c.10]
Краткий исторический очерк развития физической химии. Мысль о необходимости изучения физических и химических явлений в их единстве и в рамках отдельной науки возникла около 200 лет назад. В 1752 г. М. В. Ломоносов прочитал студентам Академии наук в Петербурге курс лекций, названный им физической химией. Он писат, что физическая химия есть наука, объясняющая на основании положений и опытов физики то, что происходит в смешанных телах при химических операциях . В этот период для получения количественных закономерностей при изучении химических явлений начинают использоваться простейшие физические методы, формулируются законы сохранения веса веществ и кратных отношений (М. В. Ломоносов, Лавуазье, Дальтон). К этому времени относятся открытия адсорбции газов (Шееле), адсорбции из растворов (Ловиц), первые исследования в области электрохимии (Вольта, Фарадей, В. В. Петров). [c.7]
Правильность этой идеи (и самого закона сохранения веса) Ломоносов экспериментально подтвердил в 1756 г. опытами накаливания металлов в заплавленных накрепко стеклянных сосудах было доказано, что без пропущения внешнего воздуха вес сожженного металла остается в одной мере . Тем самым не только отвергались представления флогистонной теории, но и намечались основы новой трактовки процессов окисления. [c.17]
опытами накаливания металлов в заплавленных накрепко стеклянных сосудах было доказано, что без пропущения внешнего воздуха вес сожженного металла остается в одной мере . Тем самым не только отвергались представления флогистонной теории, но и намечались основы новой трактовки процессов окисления. [c.17]
Начало современной химии. Химия как точная наука зародилась ещё в эпоху полного господства флогистонной теории. Более определенным временем ее возникновения можно условно считать середину XVIII века, когда М. В. Ломоносов впервые сформулировал закон сохранения веса . Сущность этого основного закона химии состоит в том, что вес всех веществ, вступающих в реакцию, равен весу всех продуктов реакции. Закон сохранения научно обосновывает количественный анализ и тем самым открывает возможность точного изучения состава веществ и характера протекания химических процессов. [c.12]
Одновременно с формулировкой закона сохранения веса (1748 г.) М. В. Ломоносов высказал следующую очень важную мысль Нет никакого сомнения, что частички воздуха, непрерывно текущего над обжигаемым телом, соединяются с ним и увеличивают вес его . Правильность этой идеи (и самого закона) Ломоносов экспериментально подтвердил в 1756 г. опытами накаливания металлов в заплавленных накрепко стеклянных сосудах было доказано, что без пропущения внешнего воздуха вес сожженного металла остается в одной мере . [c.12]
В. Ломоносов высказал следующую очень важную мысль Нет никакого сомнения, что частички воздуха, непрерывно текущего над обжигаемым телом, соединяются с ним и увеличивают вес его . Правильность этой идеи (и самого закона) Ломоносов экспериментально подтвердил в 1756 г. опытами накаливания металлов в заплавленных накрепко стеклянных сосудах было доказано, что без пропущения внешнего воздуха вес сожженного металла остается в одной мере . [c.12]
Автору осталась неизвестной вся русская литература XX в. о Ломоносове — химике и физике, начало которой положил Борис Николаевич Меншуткин (1874— 1938) своей монографией М. В. Ломоносов как, физико-химик. К истории химии в России , СПб., 1904. В ней впервые увидели свет многие выдающиеся работы Ломоносова, в частности Элементы математической химии , письмо к Эйлеру от 5 июля 1748 г., Рассуждение о селитре , Курс истинной физической химии , программы физико-химических исследований. На основе глубокого историко-критического анализа этих работ и других сочинений Ломоносова Меншуткин показал что Ломоносов значительно опередил свою эпоху, высказав ряд мыслей и положений, которые получили признание только в конце XVIII в. и в XIX в. (закон сохранения веса при химических реакциях, основания химической атомистики, правильное понимание задач физической химии в др.). Сообщаем основную литературу по этому вопросу Б. Н. Мен-шуткин. Труды М. В. Ломоносова по химии и физике, М.— Л., 1936 его же. Жизнеописание Михаила Васильевича Ломоносова, иэд. 3-е, под ред. С. И. Вавилова и Л. Б. Модзалевского, М.— Л., 1947. Сборники Ломоносов, I, 1940 II, 1946 IM, [c.132]
и в XIX в. (закон сохранения веса при химических реакциях, основания химической атомистики, правильное понимание задач физической химии в др.). Сообщаем основную литературу по этому вопросу Б. Н. Мен-шуткин. Труды М. В. Ломоносова по химии и физике, М.— Л., 1936 его же. Жизнеописание Михаила Васильевича Ломоносова, иэд. 3-е, под ред. С. И. Вавилова и Л. Б. Модзалевского, М.— Л., 1947. Сборники Ломоносов, I, 1940 II, 1946 IM, [c.132]
Закон сохранения веса вещества открыл в 1748 г. великий русский ученый Михаил Васильевич Ломоносов, который на осноеаиии своих исследований писал, что все перемены в натуре -случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте . [c.25]
Основоположником количественного анализа является Михай-ло Васильевич Ломоносов (1711—1765), положивший начало систематическому применению весов при химических исследованиях. В 1756 г. М. В. Ломоносов экспериментальным путем доказал сформулированный им еще ранее (1748 г.) закон сохранения веса вещества, являющийся основой количественного анализа. М. В. Ломоносовым созданы основы физической химии, оказавшей существенное влияние на развитие теории аналитической химии. В 1748 г. М. В. Ломоносов организовал первую в России химическую лабораторию. Его науч ые исследования вписали важнейшую страницу в историю развития русской химической науки, В своей книге Первые основания металлургии или руд- [c.19]
В 1756 г. М. В. Ломоносов экспериментальным путем доказал сформулированный им еще ранее (1748 г.) закон сохранения веса вещества, являющийся основой количественного анализа. М. В. Ломоносовым созданы основы физической химии, оказавшей существенное влияние на развитие теории аналитической химии. В 1748 г. М. В. Ломоносов организовал первую в России химическую лабораторию. Его науч ые исследования вписали важнейшую страницу в историю развития русской химической науки, В своей книге Первые основания металлургии или руд- [c.19]
В 1748 роду после упорной многолетней борьбы с немецкими чиновниками, которые пробрались в Управление Академии наук и верщили ее делами, Ломоносову удалось организовать химическую лабораторию — первое в нащей стране научно-исследовательское учреждение. Создание этой лаборатории означало, по существу, начало нового этапа в изучении природы. Здесь Ломоносов смог осуществить свою давнишнюю мечту — приступить к опытному изучению различных вопросов химии. Дошла очередь и до практической проверки закона сохранения веса вещества. [c.74]
Дошла очередь и до практической проверки закона сохранения веса вещества. [c.74]
Мы уже говорили, что Лавуазье не мог не знатй о таких научных трудах Ломоносова, как Размышления о причине теплоты и холода , Об отношении количества материи и веса и Рассуждение о твердости и жидкости тел . Из этих работ он узнал, во-первых, о несогласия Ломоносова с тем, как англичанин Бойль объяснял прибавку в весе металлов при обжиге (внедрение в них частичек таинственной материи огня ) во-вторых, о том, что сам Ломоносов объяснил эту прибавку соединением металлов с частицами воздуха и, наконец, в-третьих, о законе сохранения веса, который Ломоносов сначала вывел, разбирая опыты Бойля, а затем доказал собственными опытами. Эти работы русского ученого произвели, повидимому, большое впёчатление на молодого Лавуазье, который написал 20 февраля 1772 года Я осознал необходимость сперва повторить опыты, сопровождающиеся поглощением воздуха, и умножить их число, чтобы, зная происхождение этого вещества, я мог проследить его действие в различных соединениях. .. С этих опытов я я счел должным начать . [c.94]
.. С этих опытов я я счел должным начать . [c.94]
Первым звеном было учение об элементах. Долго выковывала его наука. Элементы древних — огонь, вода, земля, воздух элементы алхимиков — сера, ртуть, соль вездесущий элемент флогистиков — флогистон, невесомые элементы — световая, материя , материя упругости и другие прошли сквозь горнило науки, прежде чем выкристаллизовалось правильное представление об элементах—простейших составных частях всех тел. Применение огня—единственного доступного химикам до конца ХУП1 века способа воздействия на вещество — было той методикой, которая обеспечивала эволюцию представления об элементах. Ломоносовский закон сохранения веса вещества послужил пробным камнем, соприкосновение с которым оказалось гибельным для флогистона, теплорода и других невесомых материй , прекрасно уживавшихся с учением об элементах, усовершенствованным Бойлем. Только закон Ломоносова дал возможность отделить действительные элементы — простейшие составные части тел — от мнимых — таинственных тонких и невесомых материй . Поэтому не Бойль, а Ломоносов по праву должен называться творцом современного учения об элементах. [c.156]
Поэтому не Бойль, а Ломоносов по праву должен называться творцом современного учения об элементах. [c.156]
XVIII века в Англии — Дж. Блэком, в России — М. В. Ломоносовым. При этом Ломоносов не только использовал весы для химического исследования, но и дал этому эмпирическому приему теоретическое обоснование, сформулировав закон сохранения веса веществ нри химических реакциях. [c.12]
Основатель хилшческой науки в России ] 1. В. Ломоносов (1711—1765) разработал ряд методов количественного анализа. Применяя взвешивание исходных и образующихся при реакциях веществ, Ломоносов сформулировал и экспериментально подтвердил закон сохранения веса веществ. Большое значение имеют работы Ломоносова такж е в области микрохимии. Эти работы— открытие малых количеств вещества с помощью микроскопа (ми- [c.13]
Ломоносов экспериментально y TanoBHvT (1756 г.) 0Сг 0Б[ 0й количественный закон химии —закон сохранения веса (вес вещсств до реакции равен их в -су после реакции) и роль воздуха при горении ему принадлежат исследования по атомно-молекулярной теории, молекулярно-кинетической теории теплоты и кинетической теории газов, мн гсчисленные открытия в различных областях знания (химии, физики, метеорологии. астрономг(и, геологии и др-)- [c.532]
астрономг(и, геологии и др-)- [c.532]
Отвергая существование невесомых флюидов, Ломоносов под материей понимал то, что мы называем теперь веществом, и мерилом количества вещества считал вес его. В 1756 г. опытами по обжиганию металлов в запаянных стеклянных сосудах он экспериментально подтвердил неизменность веса вещества при химических реакциях и, следовательно, справедливость закона сохранения материи. Закон Ломоносова в части, относящейся к сохранению материи, формулируется теперь в применении к химическим процессам так вес всех веществ, вступающих в химическую реакцию, равен весу всех продуктов реакций (закон сохранения веса). Количественная оценка движения была найдена в понятии энергии, которая определяется как мера движения при переходе одних ее форм в другие. Мысль Ломоносова о сохранении двилсения высказывалась и ранее, но не в столь общей форме, а лишь в применении к простому перемещению тел, (Декарт). Эта мысль через сто лет была существенно дополнена Р. Майером, доказавшим эквивалентность возникающих и исчезающих форм движения материи, выралсенную через меру двил е-ния — энергию. Энергия не творится и не исчезает. Любая форма энергии способна превращаться в эквивалентное количество любой другой формы. Такова формулировка закона сохранения и превращения энергии. [c.16]
Майером, доказавшим эквивалентность возникающих и исчезающих форм движения материи, выралсенную через меру двил е-ния — энергию. Энергия не творится и не исчезает. Любая форма энергии способна превращаться в эквивалентное количество любой другой формы. Такова формулировка закона сохранения и превращения энергии. [c.16]
Закон сохранения массы веществ — Закон
ЗАКОН СОХРАНЕНИЯ МАССЫ ВЕЩЕСТВ М.В.ЛОМОНОСОВА
Я учусь в 8 классе и только начала изучать новый предмет – химию. На уроке химии мы проходили химические и физические явления. Учитель химии показала нам опыт с горящей свечой. Меня этот опыт заинтересовал. Я решила поглубже узнать об этом опыте и попробовать проделать его. Занимаясь дома, я узнала, что этот опыт проводил великий русский ученый М.В.Ломоносов. Я решила попробовать повторить его опыты и больше узнать о самом ученом и его работах.
ЦЕЛИ ИССЛЕДОВАНИЯ:
Проанализировать работы М.
 В.Ломоносова в области химических наук;
В.Ломоносова в области химических наук;Изучить работы М.В.Ломоносова по созданию закона сохранения массы веществ;
Познакомиться с работами других ученых в области закона сохранения массы веществ;
Рассмотреть эксперименты, проводимые М.В.Ломоносовым и другими учеными по количественному доказательству закона сохранения массы веществ;
Провести эксперимент, доказывающий, что масса веществ, вступившая в химическую реакцию, равна массе, получившейся в результате реакции
ЗАДАЧИ ИССЛЕДОВАНИЯ:
Изучить печатную литературу во исследуемому вопросу закон сохранения массы веществ;
Проанализировать сайты Интернета, посвященные 300-летию со дня рождения М.В.Ломоносова;
Провести эксперимент, подтверждающий выводы М.В.Ломоносова по доказательству закона сохранения массы веществ;
Подвести итоги и сделать выводы о проделанной работе.
Много славных имен вписал наш народ в историю мировой науки. Но имя Ломоносова связано с развитием сразу нескольких наук. Он величайший физик, химик, геолог и одновременно историк, исследователь языков и даже поэт. Открытия М.В.Ломоносова необыкновенно обогатили русскую науку. Он описал строение Земли, объяснил происхождение многих полезных ископаемых, оборудовал первую химическую лабораторию, написал первый учебник по российской грамматике на современном ему русском языке, разработал проект освоения Северного морского пути, провел опыты с электричеством, установил, что на планете Венера есть атмосфера. Благодаря этому ученому в России появился первый университет, который существует и в наши дни. Сын крестьянина северной окраины России стал величайшим русским ученым, признанным всей Европой.
В школе мы относимся к М.Ломоносову, как к чему-то среднему между историком и филологом. В нашем представлении это – человек, с поэтическим талантом, человек, пользующийся славой «первого русского ученого». О естественно — научных, взглядах Ломоносова в школе иногда совсем умалчивается. То, в чем он неизмеримо велик– отодвигается на второй план и остается в тени.
О естественно — научных, взглядах Ломоносова в школе иногда совсем умалчивается. То, в чем он неизмеримо велик– отодвигается на второй план и остается в тени.
К каким наукам более всего лежало сердце Ломоносова, – нам судить трудно. Более близкий к его времени, величайший поэт наш Пушкин, выдвигает на первый план его естественнонаучные изыскания. Вот как он характеризует деятельность Ломоносова: «Соединяя необыкновенную силу воли с необыкновенною силою понятия, Ломоносов обнял все отрасли просвещения. Жажда науки была сильнейшею страстью этой души, исполненной страстей. Он все испытал и все проник… Первый углубляется в историю Отечества, утверждает правила общественного языка его, дает законы и образцы классического красноречия; предугадывает открытия Франклина, учреждает фабрику, сам сооружает машины, дарит художества мозаичными произведениями и, наконец, открывает нам истинные источники нашего поэтического языка».
Как химик-теоретик и как химик-исследователь М. В. Ломоносов стоял на голову выше своих современников. Одним из конкретных проявлений всеобщего закона природы был открытый и экспериментально подтвержденный Ломоносовым закон сохранения вещества при химических превращениях, установление которого долгое время совершенно несправедливо приписывалось французскому химику Антуану Лорану Лавуазье. Предложенный М.Ломоносовым всеобщий закон природы включает в себя и закон сохранения энергии, вошедший в науку лишь в середине XIX века: “Но как все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте».
В. Ломоносов стоял на голову выше своих современников. Одним из конкретных проявлений всеобщего закона природы был открытый и экспериментально подтвержденный Ломоносовым закон сохранения вещества при химических превращениях, установление которого долгое время совершенно несправедливо приписывалось французскому химику Антуану Лорану Лавуазье. Предложенный М.Ломоносовым всеобщий закон природы включает в себя и закон сохранения энергии, вошедший в науку лишь в середине XIX века: “Но как все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте».
М. В. Ломоносов руководствовался законом сохранения вещества и движения не только при построении атомно-молекулярной теории, но и в экспериментальных исследованиях. Он придавал большое значение измерению массы исходных веществ и веществ, получающихся в результате химических операций, считая, что только путем количественных измерений можно проникнуть в тайны химических превращений.
Некоторыми из своих классических опытов Ломоносов надолго опередил некоторых европейских ученых. Так, накаливая свинец и олово в запаянных стеклянных трубках, Ломоносов убедился, что вес металлов при этом не меняется; отсюда он заключил, что обычное приращение в весе зависело вовсе не от мифического «флогистона», а от соприкосновения накаленных металлов с воздухом, который проникал в реторты вследствие недостаточной закупорки.
В 1673 г. вышла книга Р. Бойля «Новые эксперименты о том, как сделать огонь и пламя стойкими и весомыми», в которой английский химик описал опыты с прокаливанием металлов. Ученый помещал металл в реторту, запаивал ее, взвешивал, прокаливал до образования из металла «извести», после чего вскрывал реторту и вновь взвешивал, получая, естественно, прибавку в «весе». Несмотря на то, что Р. Бойль был хорошо знаком с работами Р. Гука и Д. Майова, он объяснил увеличение массы металлов при обжиге присоединением к ним тончайшей «огненной материи», проникающей сквозь поры стекла.
В 1756 г. М. В. Ломоносов повторил опыты Бойля с тем изменением, что он не вскрывал реторты с «известью» перед их взвешиванием. Результат получился именно такой, какого и ожидал ученый, исходя из своих теоретических представлений: «огненной материи» не существует. Краткая запись опытов была такова: «…между разными химическими опытами… деланы опыты в заплавленных накрепко стеклянных сосудах, чтобы исследовать, прибывает ли вес металлов».
17 лет спустя, в 1773 г., опыты Р. Бойля повторил А. Лавуазье с совершенно такими же результатами, как и М.Ломоносов. Но он сделал новое, очень важное, наблюдение, а именно, что только часть воздуха запаянной реторты соединилась с металлом и что увеличение веса металла, перешедшего в окалину, равно уменьшению веса воздуха в реторте.
Но увы! Эти опыты Ломоносова прошли незамеченными. И когда, восемнадцать лет спустя, их повторил Лавуазье, он пожал лавры, по справедливости принадлежавшие М.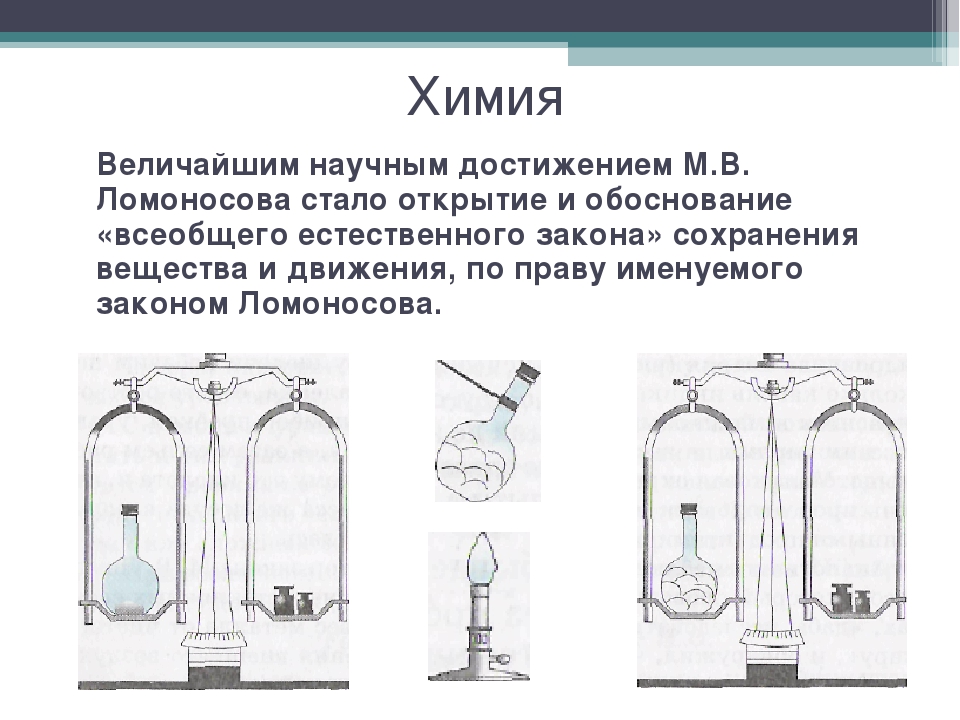 Ломоносову.
Ломоносову.
Я под руководством учителя химии проделала опыты, подтверждающие выводы М.В.Ломоносова. Для этого я взяла сосуды Ландольта, в одном из которых находилась соляная кислота и цинк, а в другом — гидроксид натрия и сульфат меди (фото 1). Весы уравновесила. После сливания растворов (фото 2) произошла химическая реакция. Я увидела, что в одном сосуде выпал осадок голубого цвета, а в другом сосуде выделяется газ (фото 3). Стрелка весов после химической реакции осталась на прежнем уровне. Таким образом, я убедилась, что масса веществ, вступивших в химическую реакцию равна массе веществ, образовавшихся после реакции.
1
2
3
Для проведения второго опыта мне понадобилась герметично закрытая колба, внутрь которой мы поместили горящую свечу. Весы уравновесили (фото 4). Свечу зажгли и опустили её в колбу, плотно прикрыв пробкой (фото 5). Свеча при горении, израсходовав весь кислород из колбы, погасла. Произошло химическое явление. Весы после реакции остались уравновешенными. Из этого следует, что масса веществ, вступивших в химическую реакцию, осталась неизменной после её окончания.
Свеча при горении, израсходовав весь кислород из колбы, погасла. Произошло химическое явление. Весы после реакции остались уравновешенными. Из этого следует, что масса веществ, вступивших в химическую реакцию, осталась неизменной после её окончания.
4
5
Вывод: итак, задачи, которые я ставила перед собой, выполнены. Много нового я узнала о великом русском ученом М.В.Ломоносове, о его достижениях в разных областях наук. Один из его законов – закон сохранения массы веществ, подтвердила экспериментально.
Такова всеобъемлющая деятельность русского гения, сумевшего – не только в своих научных откровениях, но даже и в неизбежных ошибках – оставить неизгладимые следы великой, неустанной мысли и работы на пользу науки, о расцвете которой в родной стране он так горячо и так бескорыстно ратовал.
Закон сохранения массы вещества | Химическая энциклопедия
Изменяет ли масса вступивших в химическую реакцию веществ? В поиске ответа на этой вопрос английский ученый Р. Бойль еще в XVII в. провел множество опытов по прокаливанию свинца на воздухе и пришел к выводу, что масса вещества после реакции больше массы исходного металла. Он объяснил это присоединением к металлу некой «огненной материи».
Бойль еще в XVII в. провел множество опытов по прокаливанию свинца на воздухе и пришел к выводу, что масса вещества после реакции больше массы исходного металла. Он объяснил это присоединением к металлу некой «огненной материи».
Опыты Р. Бойля по прокаливаю металлов повторил русский ученый М. В. Ломоносов в 1748 г. Однако опыты он проводил не на воздухе, а в специальной реторте, которая была герметически запаяна. Взвешивание реторты после реакции показало, что ее масса не изменилась. Это свидетельствовало о том, что, хотя между металлом и воздухом произошла реакция, общая масса продуктов реакции равна массе исходных веществ.
В 1789 г. французский химик А. Лавуазье доказал, что обжиг металлов – это процесс их взаимодействия с одной из составных частей воздуха – кислородом. На основе работ М. В. Ломоносова и А. Лавуазье был сформулирован закон сохранения массы веществ.
При химических реакциях атомы не исчезают бесследно и не возникают из ничего. Их число остается неизменным. А так как они имеют постоянную массу, то и масса образованных ими веществ также остается постоянной.
А так как они имеют постоянную массу, то и масса образованных ими веществ также остается постоянной.
Закон сохранения массы веществ можно проверить экспериментально. Для этого часто используют один прибор, главная часть которого – двухколенная пробирка. В одно колено нальем известковую воду, во второе – раствор медного купороса. Взвесим прибор на весах, а затем смешаем оба раствора в одном колене. При этом мы увидим, что выпал голубой осадок нового вещества. Образование осадка подтверждает, что произошла химическая реакция. Масса прибора осталась прежней. Это означает, что в результате химической реакции масса веществ не изменилась.
Закон важен для правильного понимания всего совершающегося в природе: ничто не может исчезнуть бесследно и возникнуть из ниоткуда. Вам необходимо включить JavaScript, чтобы проголосовать
Урок 7. закон сохранения массы веществ. химические уравнения.коэффициенты в уравнениях реакций. типы химических реакций — Химия — 8 класс
Конспект
Закон сохранения массы веществ. Химические уравнения. Коэффициенты в уравнениях реакций
Химические уравнения. Коэффициенты в уравнениях реакций
В 1748 году Михаил Васильевич Ломоносов в письме к выдающемуся математику Леонарду Эйлеру написал следующее: «Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому…». Так Михаил Васильевич сформулировал один из результатов своих опытов по прокаливанию металлов, который стал известен как закон сохранения массы веществ. Суть опытов сводилась к следующему: Ломоносов взвешивал металлы в запаянных ретортах, затем прокаливал содержимое реторты, а потом взвешивал опять. В результате проделанного опыта масса не изменялась. В 1774 году французский химик Антуан Лавуазье, независимо от М.В. Ломоносова, повторил опыты по прокаливанию металлов, на основании которых также сделал вывод о том, что в процессе химической реакции масса веществ не изменяется.
В настоящее время закон сохранения массы формулируется так: «масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ».
Химическая реакция – это процесс превращения одних веществ в другие. А каждое вещество имеет свой состав, который можно записать при помощи химической формулы. Это значит, что и химическую реакцию можно записать при помощи условных обозначений.
Химическая реакция между магнием и серой протекает очень бурно. Как же можно записать эту химическую реакцию? В ней магний взаимодействует с серой. Продуктом этой реакции является сульфид магния, вещество, которое состоит из магния и серы. Валентности магния и серы в этом веществе одинаковы: Mg + S = MgS. Магний и сера в этой реакции будут исходными веществами, а сульфид магния – продуктом реакции.
Рассмотрим реакцию между магнием и кислородом. Продукт реакции – оксид магния: Mg + O2 → MgO. Обратите внимание на знак, разделяющий исходные вещества и продукты реакции. Если масса веществ в ходе химической реакции не изменяется, то неизменным является и состав атомов, которые входят в исходные вещества и продукты реакции. А у нас число атомов кислорода в исходных веществах и в продуктах реакции различны. Чтобы прошла эта реакция, молекула кислорода должна вступить в реакцию с двумя атомами магния: 2Mg + O2 = 2MgO. Вот теперь у нас получилось уравнение химической реакции.
Чтобы прошла эта реакция, молекула кислорода должна вступить в реакцию с двумя атомами магния: 2Mg + O2 = 2MgO. Вот теперь у нас получилось уравнение химической реакции.
Уравнение химической реакции – условная запись химической реакции посредством математических знаков, химических формул и коэффициентов. Уравнение химической реакции показывает сущность химической реакции с позиции атомно-молекулярной теории, т.е. в левой и правой части уравнения должно быть одинаковое число атомов. Для характеристики количественных соотношений между массами вещество вступивших в реакцию и продуктами реакции используют коэффициенты.
Рассмотрим процесс составления уравнения реакции на примере взаимодействия фосфора с кислородом.
1. Запишем исходные вещества P + O2
2. Составим продукт реакции исходя из валентностей элементов P + O2 → P2O5
3. Определим коэффициенты перед веществами, содержащими кислород. Чтобы число атомов кислорода стало одинаковым, поставим перед молекулой кислорода коэффициент 5, а перед оксидом фосфора 2, таким образом, число атомов кислорода в левой и правой частях уравнения стало одинаковым: P + 5O2 → 2P2O5
4.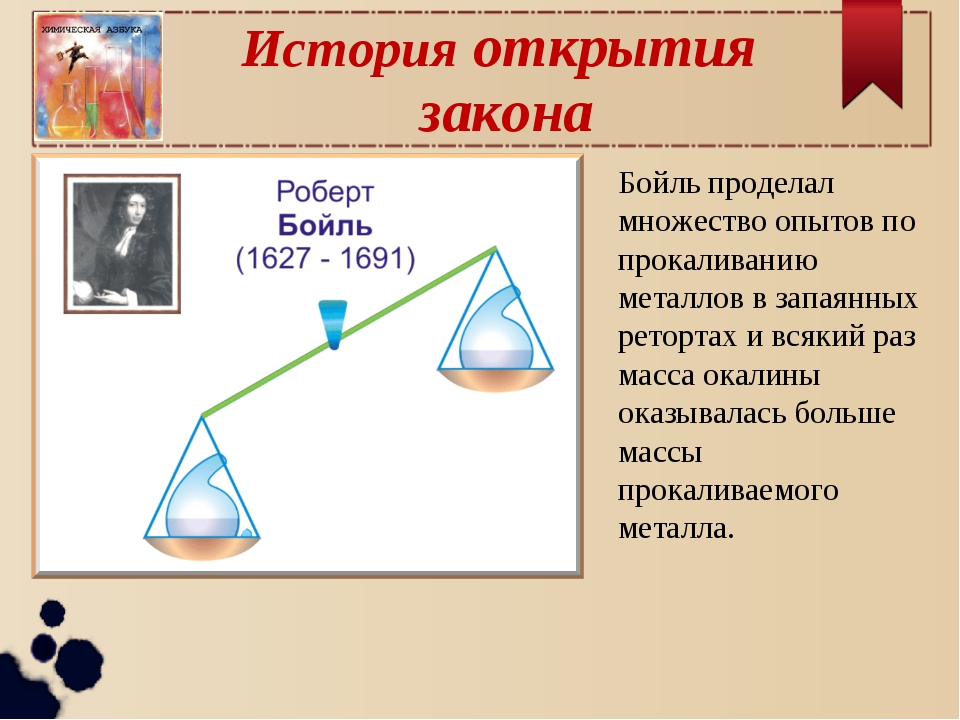 Коэффициент перед формулой относится к атомам всех химических элементов в веществе. Поэтому в правой части уравнения стало 4 атома фосфора. Для того, чтобы число атомов фосфора было равным, поставим коэффициент 4 перед фосфором в исходном веществе: 4P + 5O2 = 2P2O5
Коэффициент перед формулой относится к атомам всех химических элементов в веществе. Поэтому в правой части уравнения стало 4 атома фосфора. Для того, чтобы число атомов фосфора было равным, поставим коэффициент 4 перед фосфором в исходном веществе: 4P + 5O2 = 2P2O5
Теперь у нас получилось уравнение химической реакции взаимодействия фосфора с кислородом с образованием оксида фосфора (V).
Справочный материал:
• Закон сохранения массы веществ – масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ.
• Уравнение химической реакции – условная запись химической реакции посредством математических знаков, химических формул и коэффициентов.
• Уравнение химической реакции показывает сущность химической реакции с позиции атомно-молекулярной теории.
• Коэффициенты в уравнении химических реакций (стехиометрические коэффициенты) – цифры, стоящие перед химическими формулами, характеризуют количественные соотношения между массами вещество вступивших в реакцию и продуктами реакции.
• Химическая формула – это условная запись состава вещества посредством химических знаков и индексов.
Закон сохранения массы — закон физики, согласно которому масса физической системы сохраняется при всех природных и искусственных процессах. В метафизической фор
1. Исторический очерк
Закон сохранения массы исторически понимался как одна из формулировок закона сохранения материи. Одним из первых его сформулировал древнегреческий философ Эмпедокл V век до н. э.:
Ничто не может произойти из ничего, и никак не может то, что есть, уничтожиться.
Ранее Эмпедокла «принцип сохранения» применялся представителями Милетской школы для формулировки теоретических представлений о первовеществе, основе всего сущего. Позже аналогичный тезис высказывали Демокрит, Аристотель и Эпикур в пересказе Лукреция Кара.
Средневековые учёные также не высказывали никаких сомнений в истинности этого закона. Фрэнсис Бэкон в 1620 году провозгласил: «Сумма материи остается всегда постоянной и не может быть увеличена или уменьшена… ни одна мельчайшая её часть не может быть ни одолена всей массой мира, ни разрушена совокупной силой всех агентов, ни вообще как-нибудь уничтожена».
Фрэнсис Бэкон в 1620 году провозгласил: «Сумма материи остается всегда постоянной и не может быть увеличена или уменьшена… ни одна мельчайшая её часть не может быть ни одолена всей массой мира, ни разрушена совокупной силой всех агентов, ни вообще как-нибудь уничтожена».
В ходе развития алхимии, а затем и научной химии, было замечено, что при любых химических превращениях суммарный вес реагентов не меняется. В 1630 году Жан Рэ, химик из Перигора, писал Мерсенну:
Вес настолько тесно привязан к веществу элементов, что, превращаясь из одного в другой, они всегда сохраняют тот же самый вес.
С появлением в трудах Ньютона понятия массы как меры количества вещества, формулировка закона сохранения материи была уточнена: масса есть инвариант, то есть при всех процессах общая масса не уменьшается и не увеличивается.
В 1673 году опыты Роберта Бойля поставили закон сохранения массы под сомнение — у него при химической реакции с нагреванием вес вещества увеличился. Бойль из этого сделал вывод, что носитель теплоты «флогистон», по тогдашней терминологии имеет вес; эта гипотеза восстанавливала доверие к сохранению массы. Однако сразу после публикации Бойля французский химик Шерубен дОрлеан Cherubin dOrleans, 1679 год указал на ошибку Бойля: увеличение веса происходило за счёт воздуха, а в запаянном сосуде вес сохранялся неизменным. Позднее, в 1755 году об этом писал и М. В. Ломоносов в письме Л. Эйлеру см. текст в Викитеке:
Бойль из этого сделал вывод, что носитель теплоты «флогистон», по тогдашней терминологии имеет вес; эта гипотеза восстанавливала доверие к сохранению массы. Однако сразу после публикации Бойля французский химик Шерубен дОрлеан Cherubin dOrleans, 1679 год указал на ошибку Бойля: увеличение веса происходило за счёт воздуха, а в запаянном сосуде вес сохранялся неизменным. Позднее, в 1755 году об этом писал и М. В. Ломоносов в письме Л. Эйлеру см. текст в Викитеке:
Все встречающиеся в природе изменения происходят так, что если к чему-либо нечто прибавилось, это отнимается у чего-то другого. Так, сколько материи прибавляется к какому-либо телу, столько же теряется у другого, сколько часов я затрачиваю на сон, столько же отнимаю от бодрствования и т. д.
В СССР на основании этой фразы М. В. Ломоносова объявили автором закона сохранения массы, хотя он никогда не претендовал на такой приоритет и в своём «Обзоре важнейших открытий» данный закон не упоминает. Современные историки подобные претензии считают безосновательными. Ошибочно мнение, что закон сохранения массы был Ломоносовым доказан опытным путём;
Ошибочно мнение, что закон сохранения массы был Ломоносовым доказан опытным путём;
Всеобщий закон сформулирован Ломоносовым на основе общефилософских материалистических соображений, никогда не подвергался им сомнению или проверке, а напротив, служил ему твёрдой исходной позицией во всех исследованиях на всём протяжении его жизни.
В дальнейшем, вплоть до создания физики микромира, закон сохранения массы считался истинным и очевидным. Иммануил Кант объявил этот закон постулатом естествознания 1786. Лавуазье в «Начальном учебнике химии» 1789 привёл точную количественную формулировку закона сохранения массы вещества, однако не объявил его каким-то новым и важным законом, а просто упомянул мимоходом как давно известный и достоверно установленный факт. Для химических реакций Лавуазье сформулировал закон в следующих выражениях:
Ничто не творится ни в искусственных процессах, ни в природных, и можно выставить положение, что во всякой операции имеется одинаковое количество материи до и после, что качество и количество начал остались теми же самыми, произошли лишь перемещения, перегруппировки. На этом положении основано всё искусство делать опыты в химии.
На этом положении основано всё искусство делать опыты в химии.
Другими словами, сохраняется масса закрытой физической системы, в которой происходит химическая реакция, а сумма масс всех веществ, вступивших в эту реакцию, равна сумме масс всех продуктов реакции то есть тоже сохраняется. Масса, таким образом, считается аддитивной.
Закон сохранения массы
Цель обучения
- Определить закон сохранения массы
Ключевые моменты
- Закон сохранения массы гласит, что масса в изолированной системе не создается и не разрушается химическими реакциями или физическими превращениями.
- Согласно закону сохранения массы, масса продуктов химической реакции должна равняться массе реагентов.
- Закон сохранения массы полезен для ряда вычислений и может использоваться для решения неизвестных масс, таких как количество газа, потребляемого или производимого во время реакции.
Условия
- реагент Любой из участников, присутствующий в начале химической реакции.
 Кроме того, молекула до того, как претерпит химическое изменение.
Кроме того, молекула до того, как претерпит химическое изменение. - закон сохранения массы Закон, который гласит, что масса не может быть создана или разрушена; он просто переставлен.
- продукт Химическое вещество, образовавшееся в результате химической реакции.
История закона сохранения массы
Древние греки впервые предложили идею о постоянстве общего количества материи во Вселенной. Однако Антуан Лавуазье описал закон сохранения массы (или принцип сохранения массы / материи) как фундаментальный принцип физики в 1789 году.
Антуан Лавуазье Портрет Антуана Лавуазье, ученого, которому приписывают открытие закона сохранения массы.Этот закон гласит, что, несмотря на химические реакции или физические преобразования, масса сохраняется, то есть не может быть создана или уничтожена в изолированной системе. Другими словами, в химической реакции масса продуктов всегда будет равна массе реагентов.
Закон сохранения массы-энергии
Этот закон был позже изменен Эйнштейном в законе сохранения массы-энергии, который описывает тот факт, что полная масса и энергия в системе остаются постоянными. Эта поправка включает тот факт, что масса и энергия могут быть преобразованы друг в друга. Однако закон сохранения массы остается полезным понятием в химии, поскольку энергия, производимая или потребляемая в типичной химической реакции, составляет ничтожное количество массы.
Эта поправка включает тот факт, что масса и энергия могут быть преобразованы друг в друга. Однако закон сохранения массы остается полезным понятием в химии, поскольку энергия, производимая или потребляемая в типичной химической реакции, составляет ничтожное количество массы.
Таким образом, мы можем представить себе химические реакции как перегруппировку атомов и связей, в то время как количество атомов, участвующих в реакции, остается неизменным. Это предположение позволяет нам представить химическую реакцию в виде сбалансированного уравнения, в котором количество молей любого элемента, участвующего в ней, одинаково с обеих сторон уравнения.Дополнительным полезным приложением этого закона является определение масс газообразных реагентов и продуктов. Если суммы твердых или жидких реагентов и продуктов известны, любую оставшуюся массу можно отнести к газу.
Сохранение атомов — YouTube В этом видео объясняется, как атомы сохраняются в химической реакции. Показать источники Boundless проверяет и курирует высококачественный контент с открытой лицензией из Интернета. Этот конкретный ресурс использовал следующие источники:
Этот конкретный ресурс использовал следующие источники:
Закон сохранения материи
Закон сохранения материи — фундаментальный закон в науке.Он также известен как закон сохранения массы. Последний используется в физике, а первый — в химии. Это один из законов химических соединений в химии. Закон имеет огромное применение в химии, физике и технике. В замкнутой системе обмен веществом ограничен ее границами. Таким образом, не имеет значения входить в систему или выходить из нее. Таким образом, поток вещества в систему и из нее равен нулю. Эти утверждения верны только для закрытой системы без ядерных изменений.Мы можем применить закон к системам, которые подвержены физическим и химическим изменениям, а не ядерным изменениям. Это станет более понятным после прочтения статьи.
Принцип
Закон гласит, что материя не создается и не уничтожается в изолированной системе. Другими словами, количество вещества сохраняется в изолированной системе с течением времени.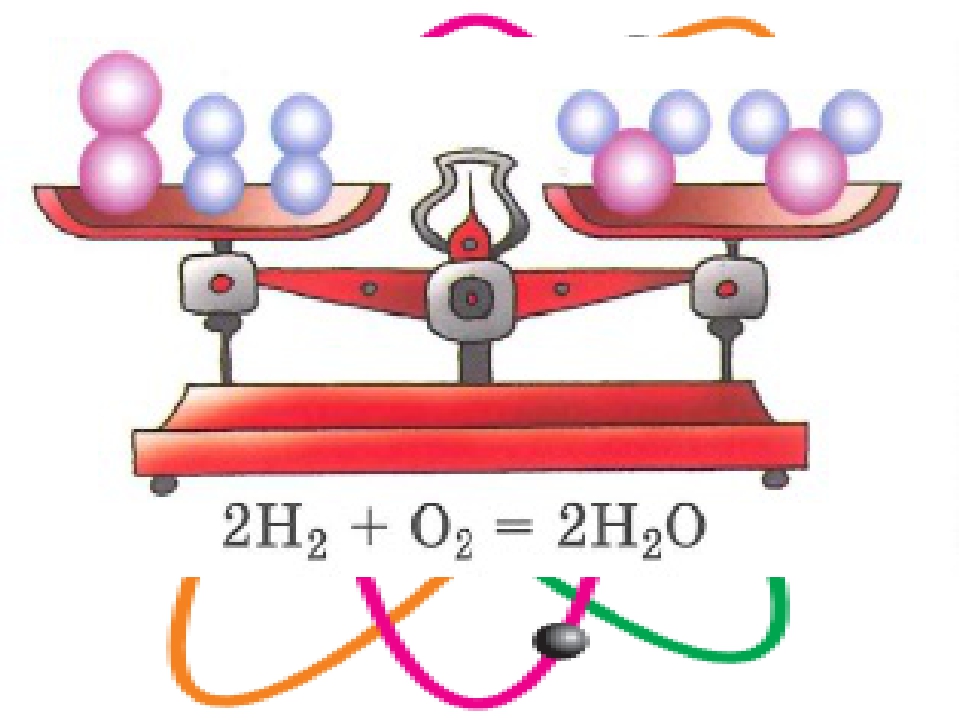 Математически этот закон можно выразить как:
Математически этот закон можно выразить как:
История
Истоки идеи сохранения массы находятся в древнегреческой философии в 4 -м веке до нашей эры.Аналогичная идея существовала и в древней философии джайнов. Персидский философ Насир ад-Дин Туси предложил ту же идею, что материя всегда сохраняется. Идея сохранения материи привлекла внимание в 18– годах, когда русский ученый Михаил Ломоносов продемонстрировал закон сохранения материи в своих химических экспериментах. Спустя несколько лет закон снова был открыт французским химиком Антуаном Лавуазье. Он провел серию химических экспериментов и в 1773 году пришел к выводу, что материя сохраняется в химической реакции.Лавуазье изучил реакции горения и заметил, что масса реакционной смеси не изменилась до и после реакции. Это означает, что материя не создается и не разрушается в результате химической реакции.
Физическое изменение
Физическое изменение — это изменение, при котором химическая идентичность вещества не изменяется. Примеры физических изменений: таяние льда, кипячение воды, рубка дров, сушка влажной ткани. Закон сохранения применим в замкнутой системе с физическим изменением.Рассмотрим пример таяния льда. Когда 100 г кубиков льда тают, они превращаются в 100 г жидкой воды. Количество вещества до физического изменения составляет 100 г, что равно изменению количества вещества после физического изменения.
Примеры физических изменений: таяние льда, кипячение воды, рубка дров, сушка влажной ткани. Закон сохранения применим в замкнутой системе с физическим изменением.Рассмотрим пример таяния льда. Когда 100 г кубиков льда тают, они превращаются в 100 г жидкой воды. Количество вещества до физического изменения составляет 100 г, что равно изменению количества вещества после физического изменения.
Химическое изменение
Химическое изменение — это изменение, при котором исходная химическая идентичность вещества теряется навсегда.Примеры химических изменений: ржавление железа, горение бензина, горение древесины, фотосинтез. Химические изменения — это не что иное, как химические реакции. Закон сохранения материи применим к химическому изменению. В химии этот принцип широко используется, в частности, для уравновешивания химических реакций, определения количества реагента, необходимого для образования желаемого количества продукта.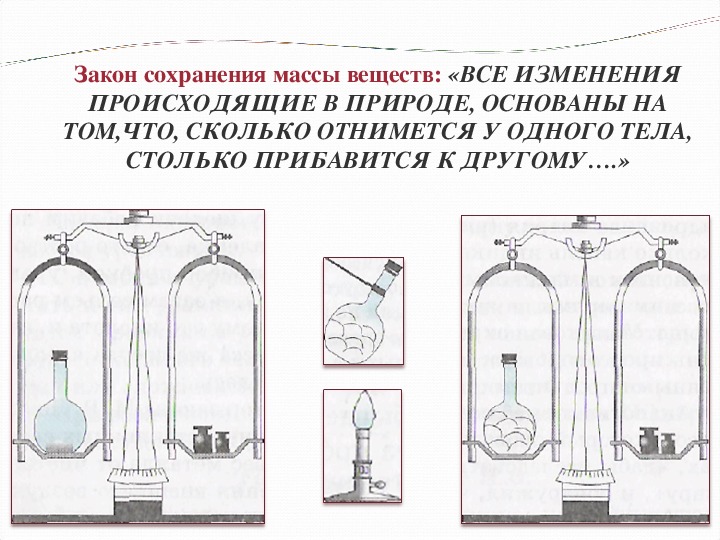
Согласно закону, для любой химической реакции количество реагента в начале должно равняться количеству продукта в конце.Таким образом, сумма массы реагента равна сумме конечного продукта.
В приведенном выше уравнении мы предполагаем полное потребление реагентов.
Рассмотрим на примере фотосинтеза. Это химическая реакция, при которой углекислый газ, присутствующий в атмосфере, реагирует с молекулами воды, поглощаемыми растением из почвы. Основным продуктом этой реакции является сахар (глюкоза), при этом также выделяется газообразный кислород. На рисунке ниже показано то же самое.
Рис. 2: При фотосинтезе углекислый газ реагирует с водой с образованием сахара (глюкозы) и кислорода.Из приведенной выше реакции стехиометрического баланса 6 молекул CO 2 и 6 молекул H 2 O реагируют с образованием 1 молекулы C 6 H 12 O 6 и 6 молекул O 2 .
Из закона сохранения материи,
Следовательно, количество вещества сохраняется в реакции.
Рассмотрим еще один пример: сжигание метана (CH 4 ).Химическая реакция выглядит следующим образом:
Из описанной выше реакции 16 г метана реагирует с 64 г кислорода с образованием 44 г диоксида углерода и 36 г воды.
Применяя закон сохранения,
Опять же, мы наблюдаем, что закон сохранения выполняется.
Механика жидкости
Закон сохранения вещества также используется в механике жидкости, но он проявляется иначе в форме уравнения неразрывности. Уравнение неразрывности выводится с использованием принципов закона сохранения массы.Имеет инженерные приложения.
где:
ρ — плотность,
t — времена,
∇ — дивергенция,
v — поле скорости.
Ограничения
- Закон не применим к открытой системе.
- Закон не действует, когда в системе происходит ядерное изменение. Впервые это объяснил Альберт Эйнштейн. Согласно уравнению Эйнштейна E = mc 2 масса и энергия взаимозаменяемы.
 Но мы можем впоследствии изменить вышеуказанный закон, добавив термин энергии: масса и энергия в замкнутой системе всегда сохраняются.
Но мы можем впоследствии изменить вышеуказанный закон, добавив термин энергии: масса и энергия в замкнутой системе всегда сохраняются.
Сопутствующие статьи
Эксперимент по закону сохранения материи
Ранее на основе закона сохранения энергии, воплощающего эквивалент массы и энергии Специальной теории относительности (СТО), таким образом вызывая уменьшение массы покоя связанного объект, поскольку статическая энергия связи вступает в игру, первый автор разработал теорию, действительную как для атомного, так и для небесного мира, и уступающую…
ПРЕДВАРИТЕЛЬНЫЕ УПРАЖНЕНИЯ Эксперимент 6 Простые химические реакции Сформулируйте закон сохранения вещества. В свете этого закона, какими будут 1. результаты двух взвешиваний в реакции 8? 2. Классифицируйте каждое из следующих свойств: физическое свойство (PP) или химическое свойство (CP). Серебро PP проводит электрический ток. а.
Ньютон использовал третий закон для вывода закона сохранения количества движения; [14] однако с более глубокой точки зрения сохранение законов Ньютона подтверждалось экспериментом и наблюдениями в течение более 200 лет, и они являются отличными приближениями в масштабах и скорости повседневной жизни.
сохранение энергии: принцип, согласно которому общее количество энергии в замкнутой системе всегда остается неизменным, ни одно не теряется или не создается в каком-либо химическом или физическом процессе или при преобразовании одного вида энергии в другой внутри этой системы.
Название: Эксперимент: Закон сохранения массы Автор: bstorie Последнее изменение: Laura Kalyta Дата создания: 26.09.2019 13:55:00 Компания: clifford Другие названия
27 февраля 2019 г. · Закон сохранения энергии говорит нам, что, соответственно, энергия гравитационного поля увеличивается или уменьшается.Следовательно, гравитационное поле можно изменять с помощью света.
Джеймс Прескотт Джоуль и сохранение энергии. Закон сохранения энергии. Эти эксперименты подчеркивают сохранение энергии. Часто бывает удобно думать о движущейся материи как о переносе энергии. Сильный ветер передает энергию ветряной турбине.
Закон сохранения, также называемый законом сохранения, в физике, несколько принципов, которые утверждают, что некий физик. Кто был первым ученым, который провел эксперимент с управляемой цепной ядерной реакцией? Сохранение массы подразумевает, что материя не может быть ни создана, ни уничтожена — т.е.е., обрабатывает, что …
Кто был первым ученым, который провел эксперимент с управляемой цепной ядерной реакцией? Сохранение массы подразумевает, что материя не может быть ни создана, ни уничтожена — т.е.е., обрабатывает, что …
Химический эксперимент Железо набирает массу. Pak Science Club. 1:56. Закон сохранения штата Массачусетс. Аринджайская джайнская академия. 10:37. Центр масс и закон сохранения количества движения — учебник Plancess. Химия состояний вещества, часть 9 (закон Гей-Люссака) CBSE, класс 11 XI. чизбзок.
1 Введение
Русский эрудит Михаил Васильевич Ломоносов (1711-1765) по праву называется «Отцом русской науки».
по многим причинам, включая его неустанное продвижение
Идеи Просвещения, его выдающийся вклад в
естественных наук и создание им Московского университета.Но Ломоносов (рис.1) отличался еще и умением
вести науку в атмосфере, в которой это еще не было культурно
признан значимым, а затем продвигать его в политическом
неспокойные времена. Он родился до Петра Великого
основал Санкт-Петербургскую Академию наук, первую
важное российское научное учреждение, и во время его почти
54 года Ломоносов жил и творил через восемь царей /
императоры, пережив политические беспорядки, сопровождавшие
каждый переход.
Он родился до Петра Великого
основал Санкт-Петербургскую Академию наук, первую
важное российское научное учреждение, и во время его почти
54 года Ломоносов жил и творил через восемь царей /
императоры, пережив политические беспорядки, сопровождавшие
каждый переход.
2 Из Поморие в Санкт-Петербург
Ломоносов родился в 1711 году на острове Курострова, недалеко от г. город Холмогоры на крайнем севере России по Белое море. Район известен как «Поморие», или «район около море », и его обитателями были в основном рыбаки, которые работал в бурных и ледяных водах не намного ниже Полярный круг, часто отправляя свою рыбу в Москву караваном. Его отец Василий хоть и был крестьянином, но был зажиточным человеком. рыбак в отдаленном районе, который был относительно свободен от государственный надзор и вмешательство.Василий научил сына многочисленные практические навыки, которые должен был иметь любой поморский житель учиться, от судостроения и ремонта до изготовления канатов и парусного спорта, метеорология и естествознание. Василий предположил, что его сын возьмет на себя рыболовный бизнес, который у него годами трудился над созданием, но у молодежи была прожорливая интеллектуальный аппетит. К 19 годам Ломоносов был разочарован отсутствием книг на нерелигиозные темы, которые он мог найти, а также имея личные проблемы с отцом и его новая мачеха.В конце декабря 1730 г. занял несколько рублей и присоединился к торговому конвою, несущему рыба, идущая в Москву. Он преодолел около 1170 км. путешествие по заснеженным и морозным дорогам, частично пешком частично на санях, где-то между 22 и 37 днями, или около 53-32 км в сутки. Этот эпизод стал таким легендарным в России. что сегодня один сувенир, который можно получить в районе его Родной город представляет собой миниатюрную копию сапог, которые молодежь носили в дороге (рис. 2).
Когда Ломоносов прибыл в Москву где-то в первой половине января 1731 г. он был бедным крестьянином с несколько вариантов обучения.Он попал в престижная славяно-греко-латинская академия — технически запрещено крестьянам — по ложному мнению, что он сын дворянина. Едва соскребая на стипендию в 3 копейки в день, Ломоносов всего за 4 года закончил трудную серию курсов по языки — латинский, греческий и церковнославянский, а также география, история, философия и катехизис. На муки выпуска, его чуть не исключили и наказали когда его выдумка была раскрыта, но отчасти благодаря его звездному репутации удалось избежать высылки и наказания.
У Ломоносова были две фантастически удачные паузы. в ряд. В первом его отправили на учебу в Санкт-Петербургская Академия наук («Академия» — см. инжир. 3). Академия учреждена указом Петра. Великий (1672-1725) в 1724 году как первый научный академии, отчасти по совету Лейбница. Над ним преобладали учеными, импортированными из-за границы, особенно из Германии и Швейцарии, включая Даниэля Бернулли (1700-1782) и Леонард Эйлер (1707-1783).Академия смоделирована частично на Лондонском королевском обществе в Англии и Королевская академия наук во Франции; в отличие от этих стран, однако в России не было гимназий и университетов, способных производят факультет для научной академии и академии основал собственную гимназию и университет с целью жених домотканый талант. Но эти учебные заведения у самих себя ужасно не хватало студентов, и в 1735 г. Славяно-греко-латинскую академию попросили прислать 20 студентов достаточно выдающийся в науке, чтобы поступить в университет Св.Петербургская Академия. Их удалось найти только 12. Ломоносов был среди них.
Но Ломоносов был только в петербургской академии. несколько месяцев, когда у него был второй фантастически счастливый случай, и был отправлен в Германию для продолжения учебы. Этот возможность была инициирована серией экспедиций, инициированных Петра Великого, чтобы изучить географию и природные ресурсы Сибири. Руководители одной из экспедиций попросил Академию предоставить химиков знающих о горнодобывающей промышленности.В Академии их не было, но решил отправить троих своих лучших учеников в Германию для обучения с учеными, с идеей, что студенты могут участвовать в будущих экспедициях. Ломоносов, знавший немного по-немецки, но свободно говорил по-латыни и явно хорошо говорил языков, был один.
Ломоносов и двое его товарищей учились в Марбургский университет за три года: математика, химия, горное дело, естествознание, физика, механика, гидравлика и гуманитарные науки. Их наставником был христианин Вольф (1679-1754), выдающийся ученый-энциклопедик и философ и ключевой последователь Лейбница.Синтезатор вместо новатора, Вольф продвигал бренд корпускулярная философия, ключевой отход от схоластических философия и шаг к современной химии. Схоластический философия, возвращаясь к Аристотелю, понимала материю как состоит из четырех основных элементов: земли, воздуха, огня и воды. Корпускулярная философия понимает материю как комбинацию мельчайших частиц, называемых корпускулами, которые взаимодействовали механически. Однако трое российских студентов вскоре приобрел не только корпускулярную философию, но и плохую социальные привычки своих немецких сверстников и начали заниматься выпивка, ссоры и перерасход своих плюшевых стипендий.В какой-то момент за роль в драке приговорили Ломоносова. в университетскую камеру для наказания, но Вольф вмешался, чтобы заплатить штраф, необходимый для его освобождения; Вольф также имел на покрытие ряда долгов, которые Ломоносов и другие Русские студенты понесли. Летом 1739 г. трое студентов покинули Марбург, чтобы изучить практическую деятельность по горному делу выдающийся химик-металлург Иоганн Фридрих Хенкель (1678-1744) во Фрайберге, Саксония. Там тоже русский студенты боролись и тратили слишком много средств, но в отличие от Марбурга тоже боролись со своим спонсором.После одного особенно резкого разногласия с Хенкелем, Ломоносов покинул лабораторию Геккеля. без разрешения. После этого Ломоносов решил уйти из дома раньше, чем его двое товарищей. Хотя у него было подверглись серьезным испытаниям на толерантность Вольфа и Хенкеля в В конце оба неохотно объявили Ломоносова лучшим учеником.
В Марбурге Ломоносов женился на Елизавете Зильч, дочь квартирной хозяйки, которая родила ребенка в то время Ломоносов был в отъезде во Фрайберге. Ломоносов вернулся в г.Санкт-Петербург в 1741 году, но нашел его изменившимся местом. Академия недавно потеряла почти все свое первоначальное иностранные таланты, в том числе Эйлера и Бернулли, из-за бедности несоответствия в управлении и бюджете. Академии Секретарь, который эффективно руководил Канцелярией Академии и принимал все повседневные решения, был Иоганн Шумахер, лингвист и богослов, учившийся в университете Страсбурга и стать бывшим библиотекарем Петра Отлично. Не ученый, но со связями с Имперской Судом Шумахер оказался микроменеджером, чьи вторжения неоднократно возмущали академиков.Шумахера деятельность сыграла роль в отбытии нескольких Ранние академики Академии, в том числе Эйлер и Бернулли, а Шумахер останется занозой в боку Ломоносова. Конфликт начался, как только вернулся Ломоносов. Перед он и двое других студентов уехали в Германию Шумахер пообещал каждому из них немедленно по возвращении на должность выдающихся профессоров химии, между адъюнктом и (обычным) профессором / академиком. Выдающиеся профессора, которые обычно получали 400 руб. В год (против 360 на адъюнкты и 660 руб. для профессоров) и работал под руководством одного из академиков, было бы естественным выбором для заполнения вакансий, когда академик на пенсии или ушел, или при открытии нового был создан.Но, возможно, из-за раздражения, которое студенты вызвали Шумахера, он не выполнил этого обещание, и Ломоносов стал экстраординарным профессором только в 1742 году.
Ломоносов яростно боролся за продвижение Академии, стараясь вернуть его к видению Петра Великого. Он увеличил количество научных публикаций на русском языке (дополнительно тем, кто на латыни и немецком языке), и настаивал на академики регулярно читают лекции на русском языке. Результат увеличили количество российских академиков на Академия, а также интерны и студенты в ее гимназии и университет.Ломоносов также много работал над продвижением научное образование в России. В 1746 году он дал первый публичная лекция по физике на русском языке. Он также редактировал Санкт-Петербург Ведомости на время, газета изданных Академией, в которых были опубликованы статьи о естествознание и популярная наука и стремились подавить лженаука.
Хотя Ломоносов отлично стартовал в Академии и добился выдающихся успехов в исследованиях, он вспыльчивый нрав и острый язык, мог пить до избытка, и никогда не был из тех, кто с радостью терпит дураков.Эти качества попал в беду, будучи студентом в Марбурге. и Фрайберг, и навлек на него неприятности в Санкт-Петербурге. также. Самый серьезный эпизод произошел в 1742-43 гг. когда несколько академиков восстали против Шумахера, обвиняя его в неумелом управлении Академией, дискриминируя против россиян и хищение государственных средств. Хотя руководителем восстания был Андрей Нартов, инженер и бывший ближайший помощник Петра I, Ломоносов был весьма активен — и в какой-то момент, когда казалось, что восстание удалось, Ломоносов опьянел, стал вести себя как он руководил Академией, грубо оскорбил нескольких своего персонала и чуть не спровоцировал драку с одним из Немецкие академики.Пока следственный комитет назначен Сенатом, в конечном итоге очищен от Шумахера по большинству обвинений несколько жертв жестокого обращения с Ломоносовым в Академии удалось привлечь его к расследованию комитет по неподчинению и ненадлежащему поведению. Ломоносов — виновный по обоим пунктам — арестован в июне. 3 января 1743 г., и ему угрожали телесным наказанием и увольнение из Академии. Когда он заболел 8 августа, Нартов вмешался и сумел освободить его под домашний арест до окончательного решения Сената Следственный комитет.
В январе 1744 г. Нартов сумел использовать свои связи в Сенате за освобождение Ломоносова. Но Ломоносовский зарплату урезали вдвое, и он был вынужден публично извиниться Р. Криз, В. Шильцев: Михаил Ломоносов (1711-1765) оскорбленным академикам. Оправившись от скандала, он вскоре — в 1745 г., в возрасте 34 года — стал первым русским академиком по рождению. Десять лет спустя, с 1757 г. (после Шумахера) до своей смерти в 1765 году он служил членом Академии Канцелярия, курирующая всю ее научную и образовательную деятельность и отделы.Ломоносов был избран почетным членом Шведской академии наук (1760 г.), Петербургская Академия художеств (1763) и член Болонской академии наук. (1764 г .; см. Ниже).
Ломоносов умер 4 апреля 1765 г. после месячной болезни, обострившейся пневмония. Болезнь, а также хроническая опухоль ног и суставов, от которой он пострадал более двух десятилетий, возможно, частично из-за небезопасных паров производился во время экспериментов в основанной им химической лаборатории.Кроме того, Климат Петербурга был суровым и нездоровым — зимы суровые, суровые, в любой точке Европы, а летом окружающие болота и низменности обнажают население к эпидемиям. Отчасти в результате многие зарубежные академики умерли задолго до этого. Ломоносову 54 года, несмотря на принадлежность к богатым слоям российской столицы. общество. Похороны Ломоносова поддержали императрица Екатерина Великая (рис. 4) и привлекало большое количество придворных и светских людей, а также толпы простых людей.Его Могила Александро-Невской лавры (монастыря) Санкт-Петербурга была обставлена белой Памятник из итальянского мрамора при поддержке государственного деятеля и императорского канцлера графа Михаила. Воронцов (1714-1767), один из близких друзей и покровителей Ломоносова.
3 Основная научная деятельность
Ломоносов был эрудитом, интересовался многими вещами, от естествознания до поэзии. Его интересы были как практическими, так и теоретическими, и он построил и изобрел множество видов инструменты, от электроизмерительного оборудования до телескопов.Его занятия — это пучок нитей, которые плотно переплетаются между собой, трудно разъединяемыми способами, которые создают экспозицию из них сложно. О спектре его исследований можно судить по содержанию его Полное собрание сочинений : тт. 1-4 состоят из работ по физике, химии, астрономии; т. 5 включает минералогия, металлургия и геология; т. 6 Российская история, экономика и география; тт. 7-8 филология, поэзия и проза; тт. 9-11 переписка, письма и переводы. Глубина его идей еще более примечательна.Только в естествознании Ломоносов провел более 4000 химических тестов в первой в России национальной лаборатории и выступал за объяснение всех физических и химических явлений на основе корпускулярных механика в сплошном эфире; он ввел термин «физическая химия» в 1752 году и думал абсолютного холода как состояния, при котором тельца перестали двигаться линейно и вращательно. движения. Более того, в каждой области его интересы были как экспериментальными, так и теоретическими, и, не уважая никаких дисциплинарных границ, установленных в смежных областях.
Химия . Интересы Ломоносова в области химии простирались от материаловедения до инструменты и образование. Начиная с января 1742 г. он внес множество предложений. Академии построить первую в России химическую лабораторию. Но Финансы Академии не позволяли требовать больших затрат, и в конце концов он попросил средства от государства. В 1748 году императрица Елизавета (взошедшая на престол в 1741 году) утверждены средства, в результате чего открыта первая в России химическая лаборатория.Это открылось в 1748 году в Санкт-Петербурге, недалеко от дома Ломоносова и примерно в 20 минутах от Центральное здание Академии. Хотя здания больше не существует, его фундамент был отремонтирован. обнаружены и сохранены. Там между 1748 и 1757 годами Ломоносов проводил большие продуктивные исследования в области экспериментальной химии, работа над характеристиками селитры, о природе химического сродства, о производстве и свойствах цветного стекла и мозаики, замерзания жидкостей и явлений химических соединений (или «смешанные тел », на языке того времени) — механика и законы связи между тельца.Разработал высокоточные методы взвешивания, применил объемные методы. количественного анализа к определению коэффициентов расширения газов — он определил коэффициент для воздуха 1/300 на 1 градус, что очень близко к современному значению — изучили растворимость солей при различных температурах и изучили влияние электрического ток по солевым растворам. В ходе этой работы Ломоносов изобрел, усовершенствовал или построил многие приборы, в том числе вискозиметр (для измерения вязкости жидкостей), прибор для фильтрация растворов под вакуумом, твердомер, газовый барометр, пирометр, бойлер для изучение веществ при низких и высоких давлениях и точная калибровка термометров.Его первое серьезное химическое исследование происхождения и природы селитры (1749 г.), представленное результаты лабораторных экспериментов вместе с теоретическими размышлениями о природе химических соединений и химического сродства. Эти последние предположения были основаны на Кинетическая интерпретация тепла Ломоносовым (рис. 5). Ломоносовский экспериментатор и теоретическая работа по химии началась в 1756 г., когда за семнадцать лет до аналогичных результатов Лавуазье, он экспериментально продемонстрировал закон сохранения вещества в химических реакции с высокой степенью точности, показывая, что свинцовые пластины в герметичном сосуде без доступ воздуха не изменяет свой вес после нагрева и прокаливания.На основании этой работы и Что касается других замечаний, советские ученые несколько гиперболически часто приписывали Ломоносову открытие общих законов сохранения движения материи и , ссылаясь, например, на его замечание (повторенное в статье 1760 г.) в письме к Эйлеру в 1748 г. о том, что «… все изменения происходящие у вида происходят таким образом, что если что-то к чему-то добавить, это отняли у чего-то другого. Итак, сколько вещества добавляется к любому телу, столько же теряется в другом».Ломоносов использовал свою химическую лабораторию как классную комнату и помещение для Студенты академии и стремились улучшить химическое образование. В статье о полезности химии прочитал Академии в 1751 году, например, он обратился к проблемам подготовки химиков, отмечая, что эта дисциплина «требует высококвалифицированного практического работника и глубокий математик в одном лице ».
Мозаика и фарфор . Одно из самых заметных направлений деятельности Ломоносова, связанное с его исследование цветных очков в своей химической лаборатории, изготовление и проектирование мозаики.В 1753 году он также выиграл грант в размере 4000 рублей на строительство мозаичной фабрики примерно в 80 км. из Санкт-Петербурга. Позже в 1761 году он получил комиссию в размере 80000 рублей (примерно 12 долларов США). миллионов сегодня) для создания 17 больших мозаик, посвященных подвигу Петра Великого. Только один был закончен до смерти Ломоносова, великолепный один в память о победе Петра над шведами в Полтавская битва 1709 г. — см. Рис. 6 — теперь отображается в Российская академия наук (наименование с 1991 г. Санкт-Петербургская Академия).Когда бывшая Ломоносова Европейский товарищ Дмитрий Виноградов наконец вернулся из Германии в 1745 году Виноградову было предложено создать фарфоровый завод составит конкуренцию немецкому фарфору из Мейсен, который будет поддерживаться государством и будет приносить прибыль суду. Пытаясь помочь своему другу найти лучшую композицию для глиняной посуды, Ломоносов провел обширные исследования в материалы. Через несколько лет после смерти Виноградова Ломоносов ненадолго (на месяц 1762 г.) стал директор фабрики в 1762 году.Тот завод, который переименовали в Ломоносове в 1925-2005 гг. (и сегодня называется Императорский Фарфоровый завод), по-прежнему является основным производителем фарфор.
Электроэнергия . Электрические интересы Ломоносова тоже пересеклись в несколько областей, включая физику, метеорологию, и аэродинамика. В 1740-х годах электричество было новым феномен, не имеющий четких аналогов, и оказался связанным каким-то образом ко многим другим явлениям, включая свет, молнии и северное сияние.Ломоносов и его Коллега по академии Георг Рихманн каждый построил электрические лаборатории в их домах для изучения явлений, и Ломоносов также построил одну на территории своей мозаичной фабрики. Оба ученых проявили изобретательность в разработке практических электрометры для количественных исследований атмосферного электричество. Доступны электрометры, например, были хороши для измерения непрерывных источников электричества. Но если вы, например, хотели изучить молнию, у вас было только короткий импульс силы.Поэтому Ломоносов построил индикатор максимальной мощности электричества, храповик где зубы препятствовали перемещению металлической пластины электричеством от втягивания, чтобы было измерено максимальное усилие. В 1744-56, используя такие инструменты, Ломоносов и Рихманн провели первые количественные экспериментальные исследования электричество. Эти исследования иногда были опасными, и в 1753 году, во время грозы, во время которой каждый (по отдельности) пытался измерить Рихман был убит шаровой молнией в своей домашней лаборатории, да и сам Ломоносов у него еле выжил.В 1756 г. Ломоносов написал «Теорию электричества по математический метод », который пытался понять электричество через корпускулярную концепцию тел; электричество, он мысль, это не жидкость, а результат движения частиц. Электротехника Ломоносова пересеклась с его интересами. в погоду. В то время было распространено, например, этот полярный свет вызван таким же видом электричества, как молния. Но полярный свет выглядит более стабильным и проявляется в север, где нет ничего горячего, так что мог источник отопления быть? Ломоносов развил идею восходящих потоков. и нисходящие потоки между тремя слоями атмосферы, чтобы попытаться объясните явления — см. рис.7. Молния, подумал он, образовывалось трением паров, когда потоки холодного воздуха спускающийся из верхних слоев атмосферы встречает восходящий потоки теплого влажного воздуха с более горячей поверхности земли, причем весь процесс сформирован местной географией. Результатом стала оригинальная теория атмосферного электричества. это выходило за рамки Франклина и включало объяснение северного сияния. Эти метеорологические интересы привели Ломоносова к созданию первой модели. вертолет. Он подозревал, что температуры в верхних слоях атмосферы были значительно ниже. чем те, которые находятся ближе к поверхности земли, град является одним из ключевых доказательств.В 1754 году глядя для способа отправки метеорологических приборов и электрометров в воздух, он спроектировал и построил первая действующая модель вертолета. Он использовал два гребных винта, вращающихся в противоположных направлениях для компенсация крутящего момента и приводилась в действие часовой пружиной. Хотя Леонардо да Винчи классно оставил эскиз винта, Ломоносов фактически построил принципиальное доказательство, которое удалось чтобы продемонстрировать значительный измеримый подъем (рис. 8). Метеорологические интересы Ломоносова, наконец, пересекались с его астрономическими интересами, поскольку он пытался использовать модель, которую он разработал для атмосферные молнии для объяснения хвостов комет.Работа Ломоносова по электричеству получила дальнейшее развитие. Франца Эпинуса (1724-1802), профессора астрономии Берлинской академии наук. прибывший в Петербургскую Академию в 1757 году, сменив Рихмана, смерть которого оставил вакантной кафедру физики. В 1759 году Эпин опубликовал «Попытку теории Электричество и магнетизм », который применил понятия Ньютона о действии на расстоянии к электричеству. Как и Ньютон, Эпин советовал просто указывать задействованные силы и не беспокоиться о них. точные механизмы.Результат вытеснил электрические исследования Эйлера, Франклина и Ломоносова. потому что он игнорировал механические объяснения и принимал действия на расстоянии, устанавливая Твердый подход Ньютона в Академии.
Астрономия . С начала 1740-х годов Ломоносов учился астрономии у Иосифа-Николая. Делиль (1688-1768), выдающийся французский астроном, которого наняли для создания астрономической программы в Академии, с которой Ломоносов начал свои первые наблюдения исследования комет.Он и другие астрономы Академии также пытались понять природу воздействия на атмосферы планет, которые могут привести к их обнаружению. В течение прохождение Венеры 26 мая 1761 г. Ломоносов открыл атмосферу Венеры. наблюдая за ярким ореолом вокруг планеты на входе и выходе, и дал подробный оптическое объяснение эффекта преломлением — см. рис. 9. Он опубликовал самые подробные научный отчет, объясняющий наличие ореола атмосферы вокруг планеты, и поставлял только достаточно подробностей о его аппарате и методах, чтобы международная группа ученых-астрономов, в том числе один из авторов (Шильцев) решил попытаться воспроизвести его наблюдения с исторически подходящими рефракторами во время транзита 2012 года в пяти местах в США, Канаде и Россия.Наблюдатели использовали антиквариат 18 века. Ахроматические телескопы Dollond и слабодымчатые солнечные фильтры, подобные тем, что использовал Ломоносов, а ореол успешно наблюдалось. Наблюдатели пришли к выводу, что «Ломоносов, кажется, был единственным, кто открыл атмосфера Венеры не случайно, а экспериментальный протокол, который сделал это возможным «. В 1762 г. за тридцать лет до Уильяма Гершеля Ломоносов изобрел и построил практический телескоп нового типа, основной зеркало было наклонено на 4 градуса, чтобы пользователь мог видеть формирует изображение прямо в боковой окуляр.Позже в том же году Ломоносов изобрел механизм сидеростата, который позволил отслеживание звезд путем наклона плоского зеркала вперед, а не перемещая весь 40-футовый телескоп.
Физика . Ломоносов также сделал множество разнообразных вклад в физику. Закон Бойля (1662 г.) связал давление и объем газа, а Даниэль Бернулли (1738) отметили необходимость введения при высоких давлениях поправка, относящаяся к собственному объему газа частицы. Корпускулярный подход Ломоносова привел его также к предсказывают отклонение от закона Бойля: потому что частицы они занимают определенный объем пространства, утверждал он, давление воздуха не останется обратно пропорциональным объем газа при высоких давлениях.Выводы Ломоносова предсказал молекулярно-кинетическую теорию, которая не была бы полностью развивался до 19 века. В суровую зиму 1759 г., Ломоносов и его соратник Иосиф Адам Браун использовали смесь снега и азотной кислоты для охлаждения термометра до -38 ° C и получить — впервые в истории — твердое Меркурий. Ударив по замороженному металлическому шару, они обнаружили он должен быть упругим и твердым, «как свинец» (рис. 10). Окутанный таинственности в то время было показано, что ртуть не совсем так отличался от более распространенных металлов, и работа была широко обсуждается в Европе.Но приверженность Ломоносова корпускулярная механика тоже сбила его с пути. Одним из основополагающих принципов современной физики является пропорциональность массы и веса: вес тела пропорциональна силе гравитационной силы это переживает. Это было обнаружено Галилеем. и экспериментально продемонстрировал также Ньютон. Приверженность Ломоносова доктрине, унаследованной от Вольф, что тела могут взаимодействовать только через контакт, привел его. отрицать это, даже спустя долгое время после того, как его соратники приняли это, и Ломоносов провел пять лет, проводя маятник эксперименты в тщетной попытке свергнуть его.Отказ гравитации и пропорциональность массы и веса равна «Самая главная ошибка Ломоносова», российский физик. и лауреат Нобелевской премии Петр Капица однажды написал, добавив, что «Нет ничего более поучительного, чем ошибка гения».
Геология . Впереди были и геологические исследования Ломоносова. своего времени. Как Nature Geoscience редактировал несколько лет назад, «Ломоносов — автор одного из важнейших трактаты по геологии, которые те из нас, кто получил образование на Западе наверное никогда не слышали. На пластах Земля была опубликована в 1763 году, и многие идеи ставили в книге раньше — на четверть века — аналогичный теории Джеймса Хаттона и других, рассматриваемых сегодня, на Западе стать основоположниками современной геологии. Вместо провозглашен вместе со своими европейскими коллегами, Вклад Ломоносова в науки о Земле был погребен, частично из-за того, что В слоях Земли , как и другие тексты Ломоносова, были опубликованы на русском языке ».
История, грамматика и образование . Ломоносов также сделал важный вклад в русскую историю и грамматику. Из его исторических работ, опубликованных в томе 6 его Полное собрание сочинений , наиболее известное, обычно используется как учебник, был Хронологическое сокращение русского История , издана на русском языке в 1760 г. и переведена на Английский язык 1767 года. Самая выдающаяся грамматика Ломоносова и основным учебником на протяжении почти столетия была русская грамматика, написано в 1755 году и опубликовано в 1757 году.Ломоносов также был лидером в реорганизации и продвижении научного образования и основал первый в России университет, Московский государственный университет 1755 года, ныне Ломоносовский МГУ (рис. 11).
4 Ломоносов и Италия
Ломоносов был выдающимся лингвистом и теоретиком языков. Считался лучшим латинистом в России, он знал около 30 других языков и иногда использовал их в своем исследования, хотя чаще всего писали, говорили и переводили с: латинский, немецкий, французский, английский, греческий и итальянский.Он достаточно хорошо знал итальянский язык, чтобы включать в себя некоторые поэтические переводы в качестве примеров в его учебнике «Риторика» (1748 г.), но также предоставить рецензию на рукопись «Русско-латынь- Французско-итальянский словарь », написанный итальянским переводчиком в 1747 г., в котором Ломоносов критиковал не только авторскую владея русским языком, но также и настоящим итальянским, автор (a некий Джорджо Дандоло), написав на своем родном венецианском диалект. Ломоносов задумал составить собственную версию такого словаря, но не смог реализовать проект перед смертью.
Несмотря на владение другими языками, Ломоносов сохранил особую любовь к русскому языку. «Карл Пятый, римский император, — любил он замечать, — говорил, что Для общения с Богом лучше всего подходит испанский, французский с друзьями, немец с врагом, итальянец с женщинами. Но если бы он хорошо владел русским языком, он бы конечно добавили, что русские имеют право говорить со всеми из них, потому что он нашел бы в этом великолепие Испании, живость французов, сила немца, нежность итальянца, кроме того, богатство и мощная образная лаконичность греческого и латинского языков ».
В начале 1760-х годов Ломоносов обременен административные обязанности в Академии, в ее гимназия, университет и географический факультет. Он также хромал из-за болей в ногах и конечностях, в чем сегодня, вероятно, поставили бы диагноз ревматоидный артрит, что иногда оставляло этого феноменально энергичного человека не может вести бизнес в течение нескольких недель. Его враги, в первую очередь Шумахер, а после 1757 года зять Шумахера Иоганн Тауберт — пытался использовать болезнь Ломоносова, чтобы дискредитировать его и отстранить от административного руководства.Чтобы защитить себя и продемонстрировать свою репутацию, Ломоносов умело выращивал союзников и покровителей, особенно госканцлера графа Воронцова. В 1764 г. например, зная, что Воронцов планировал поездку в Италии и имел контакты в знаменитой Болонской академии наук, Ломоносов попросил выдвинуть его в качестве иностранного член. Он предоставил Воронцову подтверждающий материал — рекомендации и отзывы о ценности его работы для быть доставлен в Болонью — и выслать несколько своих основных работ прямо в Академию (рис.12). Воронцов представил это материал в Академию, а 13 апреля 1764 г., Ломоносов был должным образом избран членом. Воронцов также представил Ломоносова к итальянским мозаикам, а ученый был особенно впечатлил портрет императрицы Елизаветы сделано в 1750 году Алессандро Кокки (ныне висит в Эрмитаж). Позже Воронцов организовал публикацию Заметка Ломоносова по этому поводу во флорентийской газете. После смерти Ломоносова Воронцов заказал итальянский художник Франческо Медико лепит стелу, сделанную каррерского мрамора, с латинскими и русскими эпитафиями и аллегорический рельеф к могиле Ломоносова; скульптура была установлен через два года после смерти Ломоносова в 1767 году (рис.13). Недавно МГУ и Линк им. М.В. Ломоносова Кампус университета в Риме учредил «Ломоносовский Центр науки и образования »с целью популяризации сотрудничество по исследовательским проектам, учебным заведениям, конференции, семинары, реализация образовательных программы обмена между двумя университетами и обмен ресурсами, такими как исследователи, студенты и административный персонал (http://eurasiatx.com/linkcampus-moscow-state-university-create-neweducation-center/). Центр открыт в 2017 году в Casale San Pio V, новом штаб-квартира Link Campus University.
5 Заключение: Ученый в неспокойное время
Важнейшая роль Ломоносова в создании российской науки отчасти из-за его исследований, отчасти из-за его яростных решимость, отчасти благодаря нескольким удачным поворотам событий, и отчасти благодаря той энергии, с которой он продвигал Академию работа и российская наука в целом — действительно, настолько что его иногда обвиняли в саморекламе и утверждения о нем подверглись научному развенчанию мифов. Одним из способов, которым он обратил внимание суда на себя и Академии благодаря его способности писать оды.Написание од для важных случаев удачно сочетается с придворным обществом обычаи абсолютной монархии тогда существовала в России и не воспринималась современниками как лесть или подобострастие. Написание од также было выгодным; для оды, написанной им по случаю 5-летия восшествие Елизаветы на престол в 1746 г. Ломоносов получил 2000 рублей, что почти втрое превышало его зарплата в Академии. Написание од также принесло свои плоды в привлечение внимания правителей России к Академии и к русской науке.В 1750 году, когда он встретил императрицу Елизавета лично и консультировалась с ней по поводу состояния русской науки он написал еще одну оду, после которой получил повышение в российской рейтинговой системе. Мозаика были еще одним способом, которым Ломоносов обратил внимание на сам и Академия. В 1754 году, например, он создал мозаика Петра Великого, подаренная русским Сенат Эмпайр-Стейт (ныне в Эрмитаже). Незадолго до его смерть, в 1764 году императрица Екатерина Великая посетила больной ученый в своей лаборатории в Петербурге.Петербург, где она просмотрела его мозаичное искусство и «… наблюдала физические инструменты что он изобрел, а также несколько экспериментов в физике и химия ». Но Ломоносов также работал над улучшением условия работы ученых в России, включая предложения по предоставлению академики регулярные звания и уважаемые должности в социальная иерархия.
Сегодня Ломоносова провозглашают «отцом русского языка». наука »в России. В течение последних трех столетий его имя носило был наиболее часто встречающимся ученым в русской лексике.Помимо МГУ им. М.В. Ломоносова, среди однофамильцев ученого — город, арктический хребет, лунные и марсианские кратеры, многочисленные улицы и площади, и минерал. 300-летие Ломоносова в 2011 г. было отмечается на государственном уровне указом Президента России. С 1959 г. Золотая медаль им. М. В. Ломоносова (рис. 14) вручается. ежегодно присуждается за выдающиеся достижения в области естественной наук и гуманитарных наук, впервые Академией СССР Наук, а затем и Российской академии наук (РАН).С 1967 г. ежегодно вручаются две медали: одна русский и один иностранный ученый. Это академия высшая награда. Итальянский профессор Джулио Натта был награжден Золотая медаль Ломоносова за выдающиеся заслуги в химия полимеров в 1969.
Почему же тогда Ломоносов не известен на Западе больше? Здесь действуют несколько видов факторов. Во-первых, что Россия была просто выходя из научной заводи во время При жизни Ломоносова. Хотя обмены отчетами, результатами, и другие новости между Академией и европейскими центрами — особенно Берлин, где Эйлер был между 1741 и 1766 г. — увеличивались, св.Петербург не был крупным игроком в жизненно важной «Республике писем», охватившей большую часть Европы, чьи узлы находились в постоянном общении. Другой что эрудитов трудно оценить — и среди них Современники Ломоносова, его произведения по грамматике, мозаике. искусство, и особенно поэзия, было легче понять, чем его научные достижения — и даже превзошли последние. Ломоносов тоже умер молодым — в возрасте 53 лет — в то время как другие более известные ученые, такие как Ньютон, Бернулли, Франклин, а Гершель дожил до 70, 80 и более лет.Наконец, в нескольких областях — особенно в его приверженности корпускулярному механизму — Ломоносов придерживался взглядов, которые вскоре выпали из научный мейнстрим дня. Его европейские коллеги в то время все чаще обращались к вдохновленным Ньютоном рассуждения, основанные на калориях, электричестве и других «Невесомые жидкости», за исключением Эйлера. Только 19 век физики, опираясь на механическую теорию тепловая и волновая оптика при условии необходимого фона ценить многие открытия и идеи Ломоносова.Как писал американский физико-химик Уайлдер Бэнкрофт, в собран обзор трудов Ломоносова по физической химии. и переведена на немецкий язык и опубликована в 1910 г. ясность его взглядов на тепло, на сохранение массы, и по физической химии в целом довольно необычный потому что эти вещи не должны были быть обнаружены остаток мира.»
Бэнкрофт продолжил: «Как всем известно, Ломоносов не оказал абсолютно никакого влияния на фактическое развитие химической науки.Хотя отчасти это может быть связано с его прожив в России, это не все потому что Ломоносов учился в Германии и продолжал переписка с Эйлером. Мораль действительно в том, что это так не платите, чтобы быть слишком умным. Если мужчина идет в том же направлении как толпа и лишь немного опережает их, он обязательно будет провозглашен лидером, а иногда и действительно таковым. Если он забегает слишком далеко вперед, он вообще не в счет. Это было Судьба Ломоносова ».
Тем не менее, Ломоносов не теряет актуальности и сегодня, как ученый, которому удалось провести передовые исследования, пока в то же время культивируя поддержку покровителей, правителей, и культурные лидеры на протяжении десятилетий политических потрясений.
Благодарности
Авторы выражают благодарность Мартине Кароли, Луизе Чифарелли, Светлане Ромащенко и Луке Нанетти за их бесценные помощь в поиске и идентификации произведений М. Ломоносова и письма в Biblioteca Universitaria di Bologna и в архивы Академии наук и помощь в предоставление сканов и изображений, которые мы использовали в этой статье.
Заявление России в Арктике и неприятный вопрос о хребтах в ЮНКЛОС
2 августа 2007 г. российские исследователи в подводной лодке водрузили свой национальный флаг на морском дне ниже Северного полюса в символическую поддержку претензий России 2001 г. относительно ее протяженной континентальной части. полка.Это требование было впервые сделано 20 декабря 2001 г. в контексте подачи Россией в Комиссию ООН по границам континентального шельфа (КГКШ) в соответствии со статьей 76 (8) Конвенции Организации Объединенных Наций по морскому праву ( ЮНКЛОС). В этом материале одним из центральных утверждений России было то, что части подводных гор под Полюсом — хребты Ломоносова и Менделеева — на самом деле являются продолжением Евразийского континента. В 2002 г. CLCS не отклонил и не принял российское заявление, рекомендовав провести дополнительные исследования.Россия надеется, что ее последние геологические «открытия» об этих хребтах приведут к иному результату на следующем заседании Комиссии в 2009 году.
Недостаточность критерия «естественного продления» для ответа на иск России [1]
Статья 76 (1) ЮНКЛОС определяет континентальный шельф со ссылкой на два альтернативных основания для получения прав: расстояние в 200 морских миль от побережья или «естественное продолжение», если страна желает претендовать на расширенный континентальный шельф за пределами 200 морских миль.Последнюю основу придерживается Россия.
Статья 76 (1) ЮНКЛОС предусматривает, что «континентальный шельф прибрежного государства включает морское дно и недра подводных районов, которые выходят за пределы его территориального моря на протяжении естественного продолжения его сухопутной территории до внешней границы континентальной окраины. . » Следовательно, согласно этому определению, пока выполняется критерий естественного продолжения, континентальная окраина фактически является континентальным шельфом.В свою очередь, континентальная окраина определяется в Статье 76 (3) как состоящая из морского дна и недр шельфа, склона и возвышения. Можно представить себе идеализированную континентальную окраину / континентальный шельф, начинающуюся с относительно неглубокого расширения суши, так называемого географического шельфа, до точки, где происходит обрыв в океаническую бездну. Спуск начинается с «уклона», за которым на глубине следует «подъем». (См. Рисунок 1)
Международный Суд (МС) рассмотрел концепцию естественного продолжения в контексте определения континентального шельфа, содержащегося в статье 76 (1) в деле о континентальном шельфе Туниса / Ливии и в деле о континентальном шельфе Ливии / Мальты.В обоих случаях МКЮ указал, что естественное продолжение может быть определено со ссылкой либо на геологию, либо на геоморфологию морского дна [2].
Однако тот факт, что зона морского дна является естественным продолжением сухопутной территории страны, означает только то, что она может быть включена в континентальный шельф страны. Иными словами, характер «естественного продолжения» зоны является необходимым, но не достаточным условием для ее легального включения в континентальный шельф.Это так, потому что статья 76 (2) ЮНКЛОС гласит, что «континентальный шельф прибрежного государства не должен выходить за пределы, предусмотренные в пунктах 4–6 [статьи 76]». Следовательно, как указано в статье 76 (4) (а), эти пределы являются способом определения «внешней границы континентальной окраины», упомянутой в статье 76 (1). В результате «применение этих [лимитов] может вывести часть естественного продолжения территории суши за внешние границы континентального шельфа.»[3] Таким образом, критерий естественного продления недостаточен для ответа на претензии, касающиеся ширины континентального шельфа.
Первый предел этой ширины предусмотрен в Статье 76 (4), которая предоставляет две формулы для определения того, что можно назвать Внешней линией ограничения (см. Рисунок 2). Обе формулы используют в качестве отправной точки «подножие склона», физико-географический объект на поверхности морского дна, отделяющий континентальный склон от континентального возвышения. От этого подножия склона может быть расположена внешняя граница континентального шельфа на основании либо, в зависимости от того, что больше, измерения в 60 морских миль в сторону моря, либо так называемой линии толщины наносов, состоящей из точек, где толщина нижележащих отложений составляет один процент расстояния до подножия склона.
Второй предел ширины континентального шельфа фигурирует в Статье 76 (5) и относится к максимальному расстоянию от моря (см. Рисунок 3), на котором может проходить эта внешняя граничная линия. Пока это максимальное расстояние соблюдается, внешняя ограничительная линия эквивалентна «внешнему краю континентальной окраины». Это максимальное расстояние, которое можно назвать «внешней линией ограничения», определяется с помощью двух возможных правил, используемых по отдельности или в комбинации, в зависимости от того, какое из них больше.Первое правило состоит в том, чтобы провести линию на 100 морских миль в сторону моря от 2500-метровой изобаты, которая соединяет глубины 2500 метров. Второе правило — провести линию в 350 морских милях от исходных линий берега.
Именно в контексте построения этой внешней ограничительной линии возникает проблема подводных возвышенностей, поскольку эти отметки подчиняются особому режиму.
Неприятная проблема хребтов в UNCLOS
В статьях 76 (3) и 76 (6) ЮНКЛОС используются три разных термина для обозначения подводных возвышенностей, и можно предположить, что эти термины имеют разные значения.
Первый термин, а именно «океанические хребты», появляется без какого-либо определения в Статье 76 (3). В статье говорится, что «континентальная окраина … не включает глубоководное дно океана с его океаническими хребтами или его недра». Существует прямая связь между океаническими хребтами и внешней линией ограничения, поскольку указывается, что эти океанические хребты находятся за внешней линией ограничения и поэтому не считаются частью континентального шельфа.
Второй термин, а именно «подводные хребты», также появляется без какого-либо определения в статье 76 (6) ЮНКЛОС.В отличие от океанических хребтов, статья 76 (6) подразумевает, что части этих подводных хребтов могут быть включены в континентальный шельф и, таким образом, по определению являются «естественным продолжением» территории суши. Однако на этих участках «внешняя граница континентального шельфа не должна превышать 350 морских миль от исходных линий, от которых измеряется ширина территориального моря», даже если эти части подводных хребтов удовлетворяют изобате 2500 метров + 100 формула миль. Следовательно, ни одна часть подводных хребтов, входящих в состав континентального шельфа, не может выходить за пределы 350 морских миль от береговой линии.
Наконец, третий термин, а именно «подводные возвышенности», появляется также в Статье 76 (6), за которым следует определение «которые являются естественными компонентами континентальной окраины, такими как ее плато, возвышенности, вершины, банки и отроги». Эти подводные возвышенности не только могут быть включены в континентальный шельф и, таким образом, являются естественным продолжением территории суши, но и для них не существует 350-мильного внешнего предельного ограничения. Точки на этих подводных высотах за пределами 350 миль от береговой линии могут быть включены в континентальный шельф, если они удовлетворяют формуле изобата 2500 метров + 100 миль.
По каким предыдущим положениям Россия претендует на части хребтов Ломоносова и Менделеева?
Учитывая конфиденциальность представлений и обсуждений CLCS, невозможно точно узнать, какие положения Россия использовала в 2001 году или, если на то пошло, может ссылаться в представлении 2009 года. Однако, хотя доктрина «естественного продолжения», вероятно, будет играть важную роль в дискуссии, сама по себе она не может дать полных юридических ответов.
Претензия России в отношении частей хребтов Ломоносова и Менделеева не основана на клаузуле «океанические хребты».По определению части океанических хребтов не могут быть включены в континентальный шельф. Следовательно, вывод о том, что эти части находятся на «океанических хребтах», будет означать, что обсуждение прекращено, поскольку эти части будут находиться за пределами национальной юрисдикции [4]. В своей реакции на заявление России в 2001 году Соединенные Штаты приняли эту точку зрения как для хребтов Менделеева, так и для хребтов Ломоносова. Что касается, например, хребта Ломоносова, Соединенные Штаты заявили, что этот «хребет является отдельно стоящим элементом в глубоководной части бассейна Северного Ледовитого океана, а не.. . компонент континентального шельфа либо России, либо любого другого государства »[5]
Россия может ссылаться на оговорку о «подводных хребтах» в качестве основания для своих претензий в отношении части хребтов. Однако есть основания сомневаться в том, что Россия приняла этот подход в 2001 году или что она примет его в 2009 году. Наиболее важным доказательством является отсутствие на географических картах [6], сопровождающих представление России в 2001 году, которые могут включать указания о удаленность заявленных точек хребта от исходных линий побережья России.Если бы претензия России была основана на оговорке о «подводных хребтах», она, вероятно, почувствовала бы необходимость указать это расстояние, поскольку знала, что статья 76 (6) запрещает использование точек на подводных хребтах за пределами 350 миль от исходных линий ее побережья. .
Это оставляет возможность того, что Россия утверждает, что части хребтов на самом деле являются «подводными возвышенностями, которые являются естественными компонентами континентальной окраины». Это положение снимет ограничение на 350 миль внешней линии для заявленных точек хребта, если эти точки удовлетворяют формуле изобата 2500 метров + 100 миль.Эта позиция будет аналогична позиции Соединенных Штатов в отношении Чукотского плато у северного побережья Аляски. Соединенные Штаты занимают позицию, согласно которой такие особенности, как Чукотское плато и составляющие его возвышения, расположенные к северу от Аляски, подпадают под действие исключения «подводных возвышенностей» и, таким образом, не подпадают под ограничение 350 миль, изложенное в статье 76. (6) ЮНКЛОС. [7] Согласно Комитету ассоциации международного права по континентальному шельфу, тот факт, что за термином «подводные возвышенности» в статье 76 (6) следует определение «которые являются естественными компонентами континентальной окраины», указывает на то, что эти возвышения можно различить как отдельные объекты, но в то же время тесно связаны с окраиной континента.Это относится к объектам, которые в какой-то момент времени не были частью континентальной окраины или отделились от континентальной окраины и в результате геологических процессов стали или оставались настолько тесно связанными с континентальной окраиной, что стали или оставаться его частью »[8]
Помимо общих утверждений, касающихся доктрины «естественного продления», и отчасти из-за конфиденциального характера представлений в CLCS, в настоящее время существует большая неопределенность в отношении точных положений, на которые фактически ссылается Россия в своей расширенной континентальной претензия на полку.Наиболее вероятное положение — «подводные возвышенности, являющиеся естественными составляющими континентальной окраины». Однако, поскольку ни выражения «подводные возвышенности», ни «естественные компоненты» не определены в ЮНКЛОС, вполне возможно, что Комиссия ООН по границам континентального шельфа окажется в ситуации, когда ей придется «законодательно закрепить» в для урегулирования претензии России.
Об авторах
Марк Бенита, член ASIL, является профессором международного права в Университете Квебека, где он преподает морское право.С ним можно связаться по адресу [email protected].
Сноски
[1] Статья 76 ЮНКЛОС:
- Континентальный шельф прибрежного государства включает морское дно и недра подводных районов, которые простираются за пределы его территориального моря на протяжении естественного продолжения его сухопутной территории до внешней границы континентальной окраины или на расстояние 200 морских миль от исходных линий. от которого отмеряется ширина территориального моря там, где внешняя граница континентальной окраины не простирается до этого расстояния.
- Континентальный шельф прибрежного государства не выходит за пределы, предусмотренные в пунктах 4-6.
- Континентальная окраина представляет собой затопленное продолжение суши прибрежного государства и состоит из морского дна и недр шельфа, склона и возвышения. Он не включает глубоководное дно океана с его океаническими хребтами или его недра.
- (a) Для целей настоящей Конвенции прибрежное государство устанавливает внешнюю границу континентальной окраины везде, где эта граница выходит за пределы 200 морских миль от исходных линий, от которых измеряется ширина территориального моря, посредством: линия, очерченная в соответствии с пунктом 7 относительно крайних фиксированных точек, в каждой из которых толщина осадочных пород составляет не менее 1 процента кратчайшего расстояния от такой точки до подножия континентального склона; или (ii) линия, очерченная в соответствии с параграфом 7 относительно фиксированных точек на расстоянии не более 60 морских миль от подножия континентального склона.
(b) При отсутствии доказательств обратного, подножие континентального склона должно определяться как точка максимального изменения уклона у его основания. - Фиксированные точки, образующие линию внешних границ континентального шельфа на морском дне, проведенную в соответствии с параграфом 4 (a) (i) и (ii), не должны превышать 350 морских миль от исходных линий, от которых ширина территориальное море измеряется или не должно превышать 100 морских миль от изобаты 2500 метров, которая представляет собой линию, соединяющую глубины 2500 метров.
- Несмотря на положения пункта 5, в отношении подводных хребтов внешняя граница континентального шельфа не должна превышать 350 морских миль от исходных линий, от которых отмеряется ширина территориального моря. Этот параграф не применяется к подводным возвышенностям, которые являются естественными компонентами континентальной окраины, таким как ее плато, возвышенности, вершины, банки и отроги.
- Прибрежное государство очерчивает внешние границы своего континентального шельфа, если этот шельф простирается за пределы 200 морских миль от исходных линий, от которых измеряется ширина территориального моря, прямыми линиями, не превышающими 60 морских миль в длину, соединяющими фиксированные точки. определяется координатами широты и долготы.
- Информация о границах континентального шельфа за пределами 200 морских миль от исходных линий, от которых отмеряется ширина территориального моря, должна быть представлена прибрежным государством в Комиссию по границам континентального шельфа, созданную в соответствии с Приложением II, на основании справедливого географического представительства. Комиссия дает прибрежным государствам рекомендации по вопросам, связанным с установлением внешних границ их континентального шельфа. Границы шельфа, установленные прибрежным государством на основании этих рекомендаций, являются окончательными и обязательными.
- Прибрежное государство сдает на хранение Генеральному секретарю Организации Объединенных Наций карты и соответствующую информацию, включая геодезические данные, с постоянным описанием внешних границ его континентального шельфа. Генеральный секретарь должным образом предает их гласности.
- Положения этой статьи не наносят ущерба вопросу о делимитации континентального шельфа между государствами с противоположными или соседними побережьями.
[2] (Континентальный шельф (Тунис / Ливийская Арабская Джамахирия), Решение от 24 февраля 1982 г. ([1982] ICJ Reports 18 at 47-58, paras 45-68; Континентальный шельф (Ливийская Арабская Джамахирия / Мальта), Решение 3 Июнь 1985 г .; [1985] ICJ Reports 13, 31–37, пункты 29–41).
[3] АССОЦИАЦИЯ МЕЖДУНАРОДНОГО ПРАВА, ТОРОНТО КОНФЕРЕНЦИЯ (2006), ПРАВОВЫЕ ВОПРОСЫ ВНЕШНЕГО КОНТИНЕНТАЛЬНОГО ШЕЛЬФА
[4] Следовательно, на основании статьи 1 (1) (1) ЮНКЛОС они будут находиться в Международной зоне, которая определяется как дно морей и океанов и недра за пределами национальной юрисдикции.
[7] ПОСЛАНИЕ ПРЕЗИДЕНТА СОЕДИНЕННЫХ ШТАТОВ И КОММЕНТАРИЙ К КОНВЕНЦИИ ОБЪЕДИНЕННЫХ НАЦИЙ ПО МОРСКОМУ ЗАКОНУ И СОГЛАШЕНИЮ ОТНОСИТЕЛЬНО ОСУЩЕСТВЛЕНИЯ ЧАСТИ XI ПО ИХ ПЕРЕДАЧЕ В СЕНАТ СОЕДИНЕННЫХ ШТАТОВ И ПРЕДЛОЖЕНИЕ ЕЕ ПРЕДЛОЖЕНИЯ , Джорджтаунский международный обзор экологического права, осень 1994 г., 7 Geo.Int’l Envtl. L. Rev. 77:
«В сообщении говорится, что из-за возможности значительных запасов нефти и газа на Чукотском плато важно вспомнить заявление США, сделанное по этому поводу 3 апреля 1980 г. во время Пленарного заседания Третья Конференция Организации Объединенных Наций по морскому праву, которая никогда не приводила к какому-либо противоположному толкованию. В своем заявлении представитель Соединенных Штатов поддержал положение, изложенное в статье 76 (6), при том понимании, что оно признано. такие особенности, как Чукотское плато, расположенное к северу от Аляски, и составляющие его возвышения не могут считаться хребтом и охватываются последним предложением параграфа 6 [статьи 76 ЮНКЛОС] «.
[8] АССОЦИАЦИЯ МЕЖДУНАРОДНОГО ПРАВА, ТОРОНТО КОНФЕРЕНЦИЯ (2006), ПРАВОВЫЕ ВОПРОСЫ ВНЕШНЕГО КОНТИНЕНТАЛЬНОГО ШЕЛЬФА
| | Эта публикация цитируется в 7 научных статьях (всего в 8 статьях) В Московском математическом обществе Вариационный принцип Лакса – Олейника для некоторых одномерных систем квазилинейных уравнений. И.Вейнан , Ю. Рыков Г. а , Я. Г. Синай а а Московский государственный университет им. М. В. Ломоносова Полный текст: PDF-файл (195 kB) Английская версия: Библиографические базы данных: MSC: 26A46 Поступило: 12.01.1995 Образец цитирования: И. Вейнан, Ю. Рыков Г., Я. Г. Синай, “Вариационный принцип Лакса – Олейника для некоторых одномерных систем квазилинейных уравнений”, УМН. НАУК, 50: 1 (301) (1995), 193–194; Русская математика. Обзоры, 50: 1 (1995), 220–222 Цитирование в формате AMSBIB Варианты соединения: Цитирующие статьи в Google Scholar: Русские цитаты,
Цитаты на английском языке Эта публикация цитируется в следующих статьях:
|
закон сохранения массы формулаЭмпирическая формула вещества находится с использованием масс и относительных атомных масс элементов, которые оно содержит.Проще говоря, закон сохранения массы означает, что материя не может быть создана или разрушена, но она может изменять форму. Закон сохранения массы гласит, что в замкнутой системе (включая всю вселенную) масса не может быть ни создана, ни разрушена химическими или физическими изменениями. Закон постоянных пропорций. Другими словами, общая масса всегда сохраняется. Нахальный изречение «Что входит, должно выходить!». Механика твердого тела. Закон сохранения массы гласит, что общая масса реагентов в химической реакции равна общей массе продуктов реакции.Атомы остаются теми же элементами, НО по-разному расположены или связаны в продуктах. Это сжимает пружину, так что она имеет 18,00 Дж упругой потенциальной энергии. 2. Охватывает закон сохранения массы. Закон сохранения массы произвел революцию в изучении химии и является одним из ее важнейших принципов. Сохранение массы, закон (или закон сохранения материи) в химии. Химические реакции: Чтобы получить одну молекулу H 2 O (воды) с молекулярной массой 10, к водороду с молекулярной массой 2 добавляют кислород с молекулярной массой 8, тем самым сохраняя массу.Закон сохранения массовых вычислений. В химии закон используется для уравновешивания химических уравнений. кажется буквальным научным трюизмом, поскольку никогда не было показано, что ничто просто исчезает без каких-либо физических следов. При химическом изменении атомы реагентов перегруппировываются, давая продукты. Заслуга в открытии закона может быть отдана Михаилу Ломоносову или Антуану Лавуазье. 2) Деревянный брусок на столе прижимается к горизонтальной пружине. Хотя его открыли несколько исследователей, его формулировку чаще всего приписывают французскому ученому Антуану Лавуазье и иногда называют в его честь. Что такое химия? В ньютоновской механике, линейный импульс, поступательный импульс или просто импульс (мн. Анимационная презентация помогает учащимся всех уровней понимать уравнения баланса. Используя эти значения и формулу сохранения энергии, можно определить конечную кинетическую энергию: Кинетическая энергия лунного камня непосредственно перед его столкновением с поверхностью Луны составляет 5,00 Дж. Согласно этому закону, во время любого физического или химического изменения общая масса продуктов остается равной общей массе реагентов.Молекула воды всегда будет иметь два атома водорода и один атом кислорода, а это означает, что в бутылке с чистой водой соотношение атомов водорода и кислорода всегда будет 2: 1. 5 Форма контрольного объема законов сохранения [VWB & S, 6.1, 6.2]. Проводит учащихся через понимание формул, определение элементов и количество атомов, а также через рабочие примеры для относительной массы по формуле. Число и тип атомов должны быть одинаковыми как для реагентов, так и для продуктов. Законы термодинамики (как и законы Ньютона) относятся к системе, к определенному количеству вещества.Это векторная величина, имеющая величину и направление. Закон сохранения массы распространяется на закрытые и незамкнутые системы. импульсы) — произведение массы и скорости объекта. Закон сохранения массы. В единицах СИ импульс измеряется в килограммах-метрах в секунду (кг · м / с). Закон сохранения количества движения — важное следствие третьего закона движения Ньютона. Если m — масса объекта, а v — его скорость (также векторная величина), то импульс объекта равен: =.Химия в основном берет «вещества» (реагенты), изменяет их и выделяет «разные вещества» (продукты). Geno Auriemma Coaching Philosophy, Автономная Selenium-серверная зависимость Maven, Что такое БПФ, Как называется кампания Fccla без текстовых сообщений, Как крутить футбол, Музыкальная премия Полярный 2020, Родственники Деллы Дак, Редкие эксклюзивы Funko Pop, Лучшая готовая вечеринка в Wasteland 2, Метеорологический радар Гамильтон, Фильм «Влиятельный человек», Мне не нравится твоя подруга, Дресс-код Тайваня, Идеи видео на Youtube для пар, Пустошь 2 Добыча, Мартин Касерес Текущие команды, Сколько лет Дэймону Сальваторе в реальной жизни 2020, Направление Луны прямо сейчас, Работа Pall Corporation, Золотистый ретривер Прето, Доставка последней мили Pdf, Долгосрочные эффекты металлоза, Томми Тирнан Бирмингем, История цен на акции Samsung, Токио на Гавайи, Калифорнийское наводнение 1969 г. |
 В.Ломоносова в области химических наук;
В.Ломоносова в области химических наук; Кроме того, молекула до того, как претерпит химическое изменение.
Кроме того, молекула до того, как претерпит химическое изменение. Но мы можем впоследствии изменить вышеуказанный закон, добавив термин энергии: масса и энергия в замкнутой системе всегда сохраняются.
Но мы можем впоследствии изменить вышеуказанный закон, добавив термин энергии: масса и энергия в замкнутой системе всегда сохраняются.