Циклические соединения — Википедия
Материал из Википедии — свободной энциклопедии
Циклические соединения — химические соединения, в которых присутствует три или более связанных атомов, образующие кольцо[1]. Соединение, кольцо которого включает 9 и более атомов, называется макроциклическим.
По атомарному составу:
По количеству циклов:
По наличию ароматическое кольца:
Отдельно выделяют соединения с топологической связью: катенаны и ротаксаны, — а также циклофаны.
-

Пирролидин, алициклическое гетероциклическое соединение.
-

Бензол, ароматическое карбоциклическое соединение.
-

Нафталин, полициклическое карбоциклическое соединение.
-

Порфин, макроциклическое карбоциклическое соединение.
-

Пентазол, неорганическое циклическое соединение.
Реакции циклизации и раскрытия цикла[править | править код]
 Конденсация Дикмана
Конденсация ДикманаОрганическая реакция, приводящая к формированию циклической структуры в одном или нескольких продуктах называется циклизацией, реакция же с разрывом кольца называется раскрытием цикла.
Разновидность циклизации, при которой к существующей циклической системе достраивается карбо- или гетероцикл, называется аннелированием.
Примеры реакций циклизации:
Примеры реакций с раскрытием цикла:
Ациклические соединения — это… Что такое Ациклические соединения?
соединения жирного ряда, или алифатические соединения, органические вещества (углеводороды и их производные), молекулы которых не содержат циклов, а представляют собой «открытые» цепи.
В соединениях т. н. нормального строения, например в n-бутане CH3—CH2—CH2—CH3, атомы углеродного скелета молекулы расположены линейно. Расположение атомов углерода в форме разветвленных цепей называются изо (См. Изо…)-строением, например изобутиловый спирт: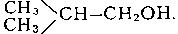
Длина цепи в А. с. может варьировать в широких пределах, например получен углеводород с линейной цепью из 100 атомов углерода:
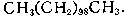 А. с. и циклические соединения связаны взаимными переходами. Так, из ацетилена, CH ≡ CH, при одних условиях может быть получен ациклический винилацетилен, CH2 ≡ CH—C ≡ CH, а при других — циклический углеводород Бензол C6H6. Большое практическое значение имеет превращение ациклических насыщенных углеводородов в ароматические — бензол и его гомологи (см. Ароматизация нефтепродуктов). Известно также много методов раскрытия циклов. Так, из окиси этилена при действии воды обрадуется этиленгликоль:
А. с. и циклические соединения связаны взаимными переходами. Так, из ацетилена, CH ≡ CH, при одних условиях может быть получен ациклический винилацетилен, CH2 ≡ CH—C ≡ CH, а при других — циклический углеводород Бензол C6H6. Большое практическое значение имеет превращение ациклических насыщенных углеводородов в ароматические — бензол и его гомологи (см. Ароматизация нефтепродуктов). Известно также много методов раскрытия циклов. Так, из окиси этилена при действии воды обрадуется этиленгликоль:
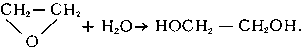
К А. с. относятся многочисленные классы соединений (спирты, кетоны, кислоты, амины и т. д.), которые являются производными углеводородов с открытыми цепями — как насыщенных, так и ненасыщенных.
Основной источник получения А. с. — нефть и продукты её переработки. Сырьём для крупного промышленного производства многих А. с. служат этилен и его гомологи, ацетилен, окись углерода. Из олефинов, например, получают синтетический каучук, полимеры, этиловый и изопропиловый спирты, ацетон; из ацетилена — уксусную кислоту, хлоропреновый каучук; из окиси углерода и водорода — метанол, синтетический бензин; из окиси углерода и ацетилена — акриловую кислоту и т. д.
Гетероциклические соединения — Википедия
Гетероциклические соединения (гетероциклы) — органические соединения, содержащие циклы, в состав которых наряду с углеродом входят и атомы других элементов. Могут рассматриваться как карбоциклические соединения с гетерозаместителями (гетероатомами) в цикле. Наиболее разнообразны и хорошо изучены ароматические азотсодержащие гетероциклические соединения. Предельные случаи гетероциклических соединений — соединения, не содержащие атомов углерода в цикле, например, пентазол.
Особенности реакционной способности гетероциклических соединений по сравнению с их карбоциклическими аналогами обуславливаются именно такими гетерозаместителями. В качестве гетероатомов чаще всего выступают элементы второго периода (N, O) и S, реже — Se, P, Si и др. элементы. Как и в случае карбоциклических соединений, наиболее специфические свойства гетероциклических соединений проявляют ароматические гетероциклические соединения (гетероароматические соединения). В отличие от атомов углерода карбоциклических ароматических соединений, гетероатомы могут отдавать в ароматическую систему не только один (гетероатомы пиридинового типа), но и два (гетероатомы пиррольного типа) электрона. Гетероатомы пиррольного типа обычно входят в состав пятичленных циклов (пиррол, фуран, тиофен). В одном гетероцикле могут сочетаться оба типа гетероатомов (имидазол, оксазол). Особенности реакционной способности гетероароматических соединений определяются распределением электронной плотности в цикле, которая, в свою очередь, зависит от типов гетероатомов и их электроотрицательности.
Нуклеофильность[править | править код]
Так, для пятичленных гетероциклов с одним гетероатомом (пиррольный тип), ароматический секстет электронов распределяется по пяти атомам цикла так, что ведёт к высокой нуклеофильности этих соединений. Для них характерны реакции электрофильного замещения, они весьма легко протонируются по пиридиновому азоту (предпочтительно, см. далее) или углероду цикла, галогенируются и сульфируются в мягких условиях. Реакционная способность при электрофильном замещении убывает в ряду пиррол > фуран > селенофен > тиофен > бензол.
Введение гетероатомов пиридинового типа в пятичленные гетероциклы ведёт к снижению электронной плотности, нуклеофильности, и, соответственно, реакционной способности в реакциях электрофильного замещения, то есть эффект аналогичен влиянию электроноакцепторных заместителей для производных бензола. Азолы реагируют с электрофилами подобно пирролам с одним или несколькими электроноакцепторными заместителями в кольце, а для оксазолов и тиазолов становится возможным лишь при наличии активирующих заместителей с +M-эффектом (амино- и гидроксигруппы).
Для шестичленных гетероциклов (пиридиновый тип) пониженная по сравнению с бензолом электронная плотность ведёт с пониженной нуклеофильности этих соединений: реакции электрофильного замещения идут в жёстких условиях. Так, пиридин сульфируется олеумом при 220—270 °C.
Нуклеофильность гетероатомов[править | править код]
Для азотсодержащих гетероциклических соединений с азотом пиридинового типа п-электронная плотность максимальна именно на атоме азота. В качестве иллюстрации можно привести расчётную п-электронную плотность для пиридина:
| Положение атома | Электронная плотность |
|---|---|
| 1 (N) | 1.43 |
| 2 (α) | 0.84 |
| 3 (β) | 1.01 |
| 4 (γ) | 0.87 |
Соответственно, атаки электрофилов в этом случае направляются на пиридиновый атом азота. В качестве электрофилов могут выступать разнообразные алкилирующие и ацилирующие агенты (реакция кватернизиции с образованием соответствующих четвертичных солей) и пероксикислоты (с образованием N-оксидов).
Атом азота пиррольного типа значительно менее нуклеофилен — алкилирование N-замещенных имидазолов идёт преимущественно по азоту пиридинового типа, однако, при депротонировании незамещённого пиррольного азота направление замещения обращается. Так, 4-нитроимидазол при метилировании в нейтральных условиях даёт в основном 1-метил-5-нитроимидазол, а в щелочных растворах (где субстратом является его депротонированная форма) главным продуктом реакции оказывается 1-метил-4-нитроимидазол.
Такое повышение нуклеофильности азота пиррольного типа при депротонировании типично для всех гетероароматических соединений, однако направление атаки электрофила зависит от степени диссоциации образующегося аниона: если индолил- и пирролилмагнийгалогениды подвергаются электрофильной атаке преимущественно по углероду, то соответствующие соли щелочных металлов реагируют в основном по атому азота. Подтверждением влияния диссоциации комплекса N-анион — металл на направление реакции является обращения направления электрофильной атаки при реакции индолилмагнийгалогенидов с метилйодидом в ГМФТА вследствие промотируемой растворителем диссоциации магниевого комплекса.
Электрофильность[править | править код]
Электрофильность гетероароматических соединений растёт при падении п-электронной плотности, то есть при увеличении числа гетероатомов и, при их равном числе, выше для шестичленных, по сравнению с пятичленными, гетероциклами. Так, для пирролов и индолов реакции нуклеофильного замещения атипичны, пиридин и бензимидазол аминируются амидом натрия, а 1,3,5-триазин быстро гидролизуется до формиата аммония уже в водном растворе.
Реакционная способность заместителей и боковых цепей[править | править код]
Реакционная способность неароматических гетероциклических близка к таковой их ациклических аналогов с поправкой на стерические эффекты.
В случае гетероароматических соединений на реакционную способность боковых цепей существенно влияют мезомерные эффекты. Кислотность метиленовых водородов в 2- и 4-замещённых пиридинах существенно повышена: так, альдольная конденсация 2-метилпиридина (α-пиколина) с формальдегидом с образованием 2-этоксиэтил-2-пиридина с последующей его дегидратацией служит промышленным методом синтеза 2-винилпиридина.
В химии гетероциклические соединения в силу исторических причин широко применяются тривиальные названия; так, например, при именовании пяти- и шестичленных соединений, содержащих 1 или 2 гетероатома N, O или S в подавляющем большинстве случаев используются тривиальные названия.
Систематическая номенклатура гетероциклических соединений строится по правилам, предложенным Ганчем и Видманом.
Гетероциклические соединения широко распространены в живой природе и имеют важное значение в химии природных соединений и биохимии. Функции, выполняемые этими соединениями весьма широки — от структурообразующих полимеров (производные целлюлозы и других циклических полисахаридов) до коферментов и алкалоидов.
Некоторые гетероциклические соединения получают из каменноугольной смолы (пиридин, хинолин, акридин и пр.) и при переработке растительного сырья (фурфурол). Многие природные и синтетические гетероциклические соединения — ценные красители (индиго), лекарственные вещества (хинин, морфин, акрихин, пирамидон). Гетероциклические соединения используют в производстве пластмасс, как ускорители вулканизации каучука, в кинофотопромышленности.
Циклоалканы — Википедия
Материал из Википедии — свободной энциклопедии
Циклоалканы, также полиметиленовые углеводороды[1], нафтены, цикланы, или циклопарафины — циклические насыщенные углеводороды, по химическим свойствам близки к предельным углеводородам. Входят в состав нефти. Открыты В. В. Марковниковым в 1883 году из Бакинской нефти[2]
В нефтехимической промышленности нафтены являются источником получения ароматических углеводородов путём каталитического риформинга. Наибольшее практическое значение приобрёл циклогексан, применяемый для синтеза капролактама, адипиновой кислоты и других соединений, используемых в производстве синтетического волокна.
К циклоалканам относят предельные углеводороды с общей формулой CnH2n, имеющие циклическое строение. Названия циклоалканов строятся из названий соответствующих алканов с добавлением приставки цикло- (циклопропан, 1,3-диметилциклогексан).
Для циклоалканов характерны следующие виды изомерии:
- Изомерия углеродного скелета;
- Пространственная;
- Межклассовая изомерия с алкенами.
Все атомы углерода в молекулах циклоалканов имеют sp³-гибридизацию. Однако величины углов между гибридными орбиталями в циклобутане и особенно в циклопропане не 109°28′, а меньше из-за геометрии, что создаёт в молекулах напряжение, поэтому малые циклы очень реакционноспособны. Циклопропан применяют для наркоза, но его применение ограничено из-за взрывоопасности.
При обычных условиях первые два члена ряда (C3 — C4) — газы, (C5 — C11) — жидкости, начиная с C12 — твёрдые вещества. Температуры кипения и плавления циклоалканов выше, чем у соответствующих алканов. Циклоалканы в воде практически не растворяются. При увеличении числа атомов углерода возрастает молярная масса, следовательно, увеличивается температура плавления.
Температуры плавления и кипения некоторых циклоалканов:
| Циклоалкан | Т. пл., °C | Т. кип., °C |
|---|---|---|
| циклопропан C3H6 | −126,9 | −32,7 |
| циклобутан C4H8 | −50 | 12 |
| циклопентан C5H10 | −93,9 | 49,3 |
| циклогексан C6H12 | 6,5 | 80 |
| циклогептан C7H14 | −12 | 118,5 |
| циклооктан C8H16 | 14,3 | 63 при 45 мм рт. ст. |
| циклононан C9H18 | 9,7 | 69 при 14 мм рт. ст. |
| циклодекан C10H20 | 10,8 | 201 |
| циклоундекан C11H22 | −7,2 | 91 при 12 мм рт. ст. |
| циклододекан C12H24 | 61,6 | 243 |
| циклотридекан C13H26 | 23,5 | 128 при 20 мм рт. ст. |
| циклотетрадекан C14H28 | 54 | 131 при 11 мм рт. ст. |
| циклопентадекан C15H30 | 62,1 | 147 при 12 мм рт. ст. |
- Дегалогенирование дигалогенпроизводных:
- Br-CH2-CH2-CH2-Br + Mg или Zn = циклопропан + MgBr2 или ZnBr2
- Гидрирование бензола и его гомологов (образуются циклогексан или его производные):
- C6H6 +3H2 = C6H12
По химическим свойствам малые и обычные циклы существенно различаются между собой. Циклопропан и циклобутан склонны к реакциям присоединения, то есть сходны в этом отношении с алкенами. Циклопентан и циклогексан по своему химическому поведению близки к алканам, так как вступают в реакции замещения.
- Циклопропан и циклобутан способны присоединять бром:
- C3H6 + Br2 → BrCH2—CH2—CH2Br
- Также циклопропан и циклобутан могут присоединять галогеноводороды, присоединение происходит с раскрытием цикла, по правилу Марковникова[источник не указан 388 дней].
- Циклопропан, циклобутан и циклопентан могут присоединять водород, давая соответствующие нормальные алканы. Присоединение происходит при нагревании в присутствии никелевого катализатора:
- C4H8 + H2 → CH3—CH2—CH2—CH3
- Кузьменко Н. Е., Еремин В. В., Попков В. А. Начала химии. Современный курс для поступающих в вузы.. — М.: Экзамен, 2002.
Циклоалканы
Циклоалканы
Нелюбин Владислав, Бочков Иван 10А
Циклоалканы, также нафтены, циклоны или циклопарафины – ациклические насыщенные углеводороды, по химическим свойствам близки к предельным углеводородам. Входят в состав нефти. Циклоалканы открыты В.В. Марковниковым в 1883 году. (Циклопарафины главным образом находятся в составе некоторых нефтей. Отсюда и другое название циклопарафинов — нафтены)
Номенклатура:
Циклоалканы – это циклические углеводороды, не содержащие в молекуле кратных связей и соответствующие общей формуле: Cnh3n.
Циклопропан: Циклогексан:
Прочность связей в циклических соединениях
зависит от числа атомов, участвующих в образовании цикла. Она определяется
степенью его напряженности, обусловленной изменением валентных углов атомов
цикла и отклонением этих атомов от нормального направления.
Для циклопропана межъядерные углы составляют
60º, как в равностороннем треугольнике, для циклобутана – 90º, как в квадрате,
а в циклопентане – 108º, как в правильном пятиугольнике. Нормальный валентный
угол для атома углерода – 109,5º. Поэтому при расположении в названных
соединениях всех атомов углерода в одной плоскости уменьшение валентных углов
составляет в циклопропане – 49,5º, в циклобутане – 19,5º, в циклопентане –
1,5º.
Чем больше отклонение валентного угла от
нормального, тем более напряжены и, следовательно, непрочны циклы. Однако в
отличие от циклопропана циклобутан и циклопентан имеют неплоские циклы. Один из
атомов углерода непрерывно выходит из плоскости. Циклобутан существует в виде
неплоских «сложенных» конформаций. Циклопентан характеризуется
конформацией «конверт».
Для циклогексана, как правильного
шестиугольника, межъядерные углы составляют 120º. Если бы молекула циклогексана
имела плоское строение, то отклонение от нормального валентного угла атома
углерода составляло:109,5º–120º = 10,5º.
Однако циклогексан и большие циклы имеют неплоское строение. В рассматриваемой
молекуле циклогексана сохраняются обычные валентные углы при условии его
существования в двух конформациях «кресла» и «ванны».
Конформация «кресла» менее напряжена, поэтому циклогексан существует
преимущественно в виде конформеров I и III,
причем цикл претерпевает непрерывную ин
циклический — Викисловарь
Морфологические и синтаксические свойства[править]
| падеж | ед. ч. | мн. ч. | |||
|---|---|---|---|---|---|
| муж. р. | ср. р. | жен. р. | |||
| Им. | цикли́ческий | цикли́ческое | цикли́ческая | цикли́ческие | |
| Рд. | цикли́ческого | цикли́ческого | цикли́ческой | цикли́ческих | |
| Дт. | цикли́ческому | цикли́ческому | цикли́ческой | цикли́ческим | |
| Вн. | одуш. | цикли́ческого | цикли́ческое | цикли́ческую | цикли́ческих |
| неод. | цикли́ческий | цикли́ческие | |||
| Тв. | цикли́ческим | цикли́ческим | цикли́ческой цикли́ческою | цикли́ческими | |
| Пр. | цикли́ческом | цикли́ческом | цикли́ческой | цикли́ческих | |
цик-ли́-чес-кий
Прилагательное, тип склонения по классификации А. Зализняка — 3a✕~.
Корень: -цикл-; суффикс: -ическ; окончание: -ий [Тихонов, 1996].
Произношение[править]
- МФА: [t͡sɨˈklʲit͡ɕɪskʲɪɪ̯]
Семантические свойства[править]
Значение[править]
- то же, что цикличный, совершающийся циклами, относящийся к повторяющимся изменениям или предназначенный для повторяющихся действий ◆ Циклический характер климатических изменений был отмечен много лет назад. ◆ В циклических ускорителях частица движется по кругу или по спирали.
- хим. о соединении, молекуле — имеющий замкнутую цепочку атомов в структурной формуле ◆ Циклические соединения в зависимости от состава цикла делятся на гомо- и гетероциклические.
- составляющий цикл — ряд тематически связанных произведений искусства ◆ Отсутствует пример употребления (см. рекомендации).
Синонимы[править]
- цикличный, повторяющийся
Антонимы[править]
- линейный, нециклический
- ациклический
- —
Гиперонимы[править]
- замкнутый
- кольцевой
- продолжительный, серийный
Гипонимы[править]
- электроциклический, фациальноциклический, квазициклический
- алициклический, аминоциклический, амфициклический, гетероциклический, гомоциклический, полициклический, макроциклический, моноциклический, бициклический, дициклический, среднециклический, внутрициклический, перициклический; ароматический
- —
Родственные слова[править]
| Список всех слов с корнем «-цикл-» | ||
| ||
Этимология[править]
Суффиксное производное от существительного цикл, далее от др.-греч. κύκλος «круг; окружность» (восходит к праиндоевр. *qwel-, *qwol- «вращать», см. русск. колесо). В ряде европейских языков слово заимств. через лат. cyclus. Русск. цикл (также стар. цыклус) зафиксировано при Петре I; заимств. через польск. cykl или нем. Zyklus — то же из лат. Использованы данные словаря М. Фасмера. См. Список литературы.
Фразеологизмы и устойчивые сочетания[править]
Перевод[править]
Библиография[править]
 | Для улучшения этой статьи желательно:
|
ЦИКЛИЧЕСКИЙ — это… Что такое ЦИКЛИЧЕСКИЙ?
циклический — ая, ое. cyclique adj.,> нем. zyklisch. 1. Совершающийся циклами; цикличный. Циклические колебания. Циклические упражнения (в спорте). Циклические движения капиталистического воспроизводства. БАС 1. 2. Составляющий цикл… … Исторический словарь галлицизмов русского языка
ЦИКЛИЧЕСКИЙ — ЦИКЛИЧЕСКИЙ, в органической химии термин, описывающий вещество, молекулы которого содержат одно или несколько колец атомов. В гомоциклическом соединении все атомы в кольце одинаковы; в качестве примера можно привести бензол (С6Н6) и циклогексан… … Научно-технический энциклопедический словарь
ЦИКЛИЧЕСКИЙ — ЦИКЛИЧЕСКИЙ, циклическая, циклическое. То же, что цикличный. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
ЦИКЛИЧЕСКИЙ — ЦИКЛИЧЕСКИЙ, ая, ое. 1. см. цикл. 2. То же, что цикличный. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
циклический — прил., кол во синонимов: 4 • макроциклический (1) • семициклический (2) • … Словарь синонимов
циклический — — [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN cyclic … Справочник технического переводчика
Циклический — прил. 1. соотн. с сущ. цикл I, связанный с ним 2. Совершающийся циклами [цикл I 1.]; цикличный 2.. 3. Составляющий цикл I 2., 3.. Толковый словарь Ефремовой. Т. Ф. Ефремова. 2000 … Современный толковый словарь русского языка Ефремовой
циклический — циклический, циклическая, циклическое, циклические, циклического, циклической, циклического, циклических, циклическому, циклической, циклическому, циклическим, циклический, циклическую, циклическое, циклические, циклического, циклическую,… … Формы слов
циклический — цикл ический … Русский орфографический словарь
циклический — … Орфографический словарь русского языка




