ФИЗИЧЕСКИЕ ЯВЛЕНИЯ, КОТОРЫЕ ПРОИСХОДЯТ С ФИЗИЧЕСКИМИ ТЕЛАМИ — Мегаобучалка
| 1.1. С ЧЕГО НАЧИНАЕТСЯ ИЗУЧЕНИЕ ЯВЛЕНИЙ, ПРОИСХОДЯЩИХ В ПРИРОДЕ? |
Человек живет в мире природы. Ты сам и все, что тебя окружает, — воздух, деревья, река, солнце — это различные объекты природы. С объектами природы постоянно происходят изменения, которые называются природными явлениями.
С древних времен люди пытались понять: как и почему происходят различные явления? Как летают птицы и почему они не падают? Как может дерево плыть по воде и почему оно не тонет? Некоторые природные явления — гром и молния, солнечное и лунное затмения — пугали людей, пока ученые не выяснили, как и почему они возникают.
Наблюдая и изучая явления, происходящие в природе, люди нашли им применение в своей жизни. Наблюдая за полетом птиц (рис. 1), люди сконструировали самолет (рис. 2).
| Рис. 1 | Рис. 2 |
Наблюдая за плавающим деревом, человек научился строить корабли, покорил моря и океаны. Изучив способ передвижения медузы (рис. 3), ученые придумали ракетный двигатель (рис. 4). Наблюдая за молнией, ученые открыли электричество, без которого сегодня люди не могут жить и работать. Всевозможные бытовые электрические устройства (осветительные лампы, телевизоры, пылесосы) окружают нас повсюду. Различные электрические инструменты (электродрель, электропила, швейная машинка) используются в школьных мастерских и на производстве.
| Рис. 3 | Рис. 4 |
Теперь ты знаешь, что одно из основных умений исследователя природы — это умение наблюдать. С наблюдения начинается изучение явлений, происходящих вокруг нас.
Выполни задание. Посмотри на рисунок 5 и скажи, какое явление природы на нем изображено?
| Рис. 5 |
| 1.2. ДЛЯ ЧЕГО НУЖНА ФИЗИКА? |
Посмотри, как с дерева падают листья. В этом простом природном явлении участвует множество объектов природы: дерево, лист, воздух, Земля. Объекты природы, которые участвуют в природном явлении и изучаются физикой, называются физическими телами, а природные явления, происходящие с ними, называются физическими явлениями.
| Наука, изучающая физические явления, которые происходят с физическими телами, называется физикой. |
Ученые разделили все физические явления на группы (рис. 6):
| Рис. 6 |
Механические явления — это явления, происходящие с физическими телами при их движении относительно друг друга (обращение Земли вокруг Солнца, движение автомобилей, качание маятника).
Магнитные явления — это явления, связанные с возникновением у физических тел магнитных свойств (притяжение магнитом железных предметов, поворот стрелки компаса на север).
Оптические явления — это явления, возникающие при распространении, преломлении и отражении света (отражение света от зеркала, миражи, появление тени).
Тепловые явления — это явления, связанные с нагреванием и охлаждением физических тел (кипение чайника, образование тумана, превращение воды в лед).
Атомные явления — это явления, возникающие при изменении внутреннего строения вещества физических тел (свечение Солнца и звезд, атомный взрыв).
Наблюдай и объясняй. 1. Приведи пример природного явления. 2. К какой группе физических явлений оно относится? Почему? 3. Назови физические тела, которые участвовали в физических явлениях.
megaobuchalka.ru
Строение атома. Атомные явления.
Испускание лучистых энергий раскаленными телами называются тепловым излучением.
Инфракрасное излучение излучается атомами и молекулами.
Инфракрасное излучение дают все тела при любой температуре.
Тела, нагретые до очень высоких температур, испускают невидимое ультрафиолетовое излучение.
Излучаются всеми твердыми телами, у которых t>1ООО0С, а также светящимися парами ртути.
Тела, которые полностью поглощают энергию излучений волн, любой длины, называются
Закон Стефана –
Больцмана: полная лучеиспускательная способность
абсолютно черного тела прямо пропорциональна
его абсолютной температуре в четвертой
степени: Ет =  ·T4 (Дж).
·T4 (Дж).
Ет — энергия электромагнитных излучений, испускающихся из единицы поверхности абсолютно черного тела за единицу времени при данной температуре по всем частотам (ν) или длинам волн (λ).
Т- температура тела по Кельвину.
 —
постоянная Стефана – Больцмана;
—
постоянная Стефана – Больцмана; =
5,672 . 10-8 Вт/м2 К4 .
=
5,672 . 10-8 Вт/м2 К4 .
Формула Макса
Планка 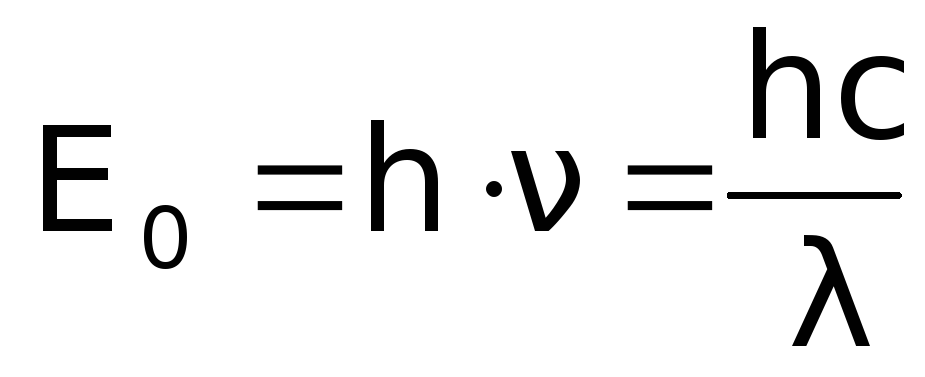
Е0 – самая малая доля энергии, т.е. энергия одного кванта (Дж).
ν – частота излучения (Гц)
h — постоянная Планка (h = 6,62х10-34 Дж · с)
Энергия фотона: Е = h · ν (Дж)
Импульс фотона: p=m · c= 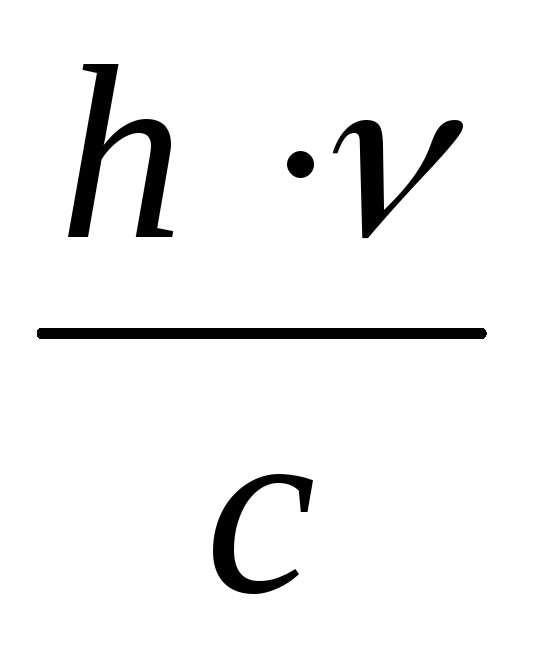 =
= =
=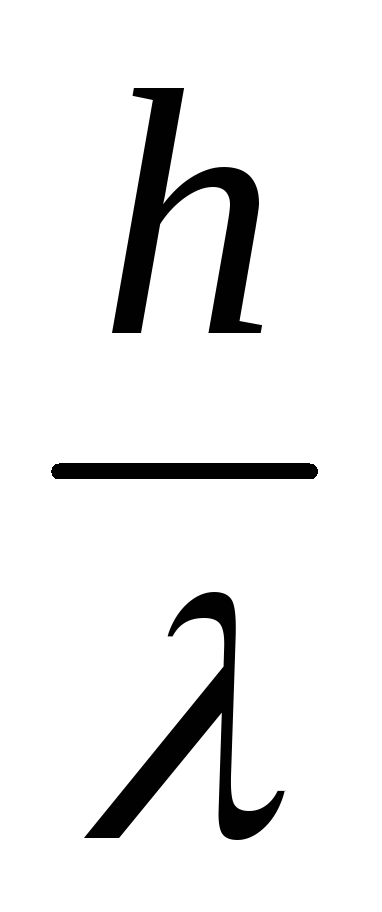
Формула Эйнштейна: h · ν =Aвых
 –Энергия
фотона расходуется на вырывание электрона
с поверхности вещества и сообщение ему
кинетической энергии.
–Энергия
фотона расходуется на вырывание электрона
с поверхности вещества и сообщение ему
кинетической энергии. Работу, совершаемую
для вырывания электрона с поверхности
металла, называют работой выхода
электрона. 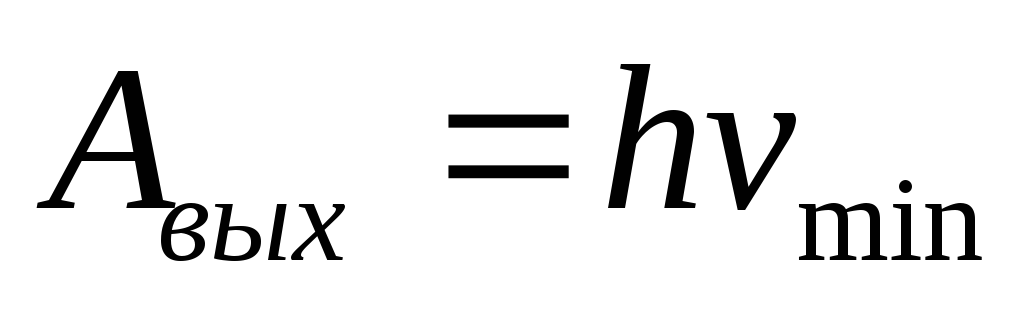 ,
гдеvmin–красная
граница фото эффекта или минимальная
частота,
,
гдеvmin–красная
граница фото эффекта или минимальная
частота, 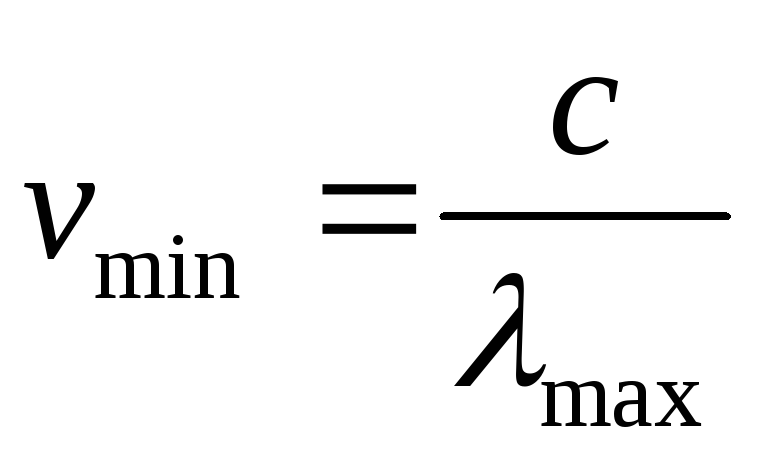 (
(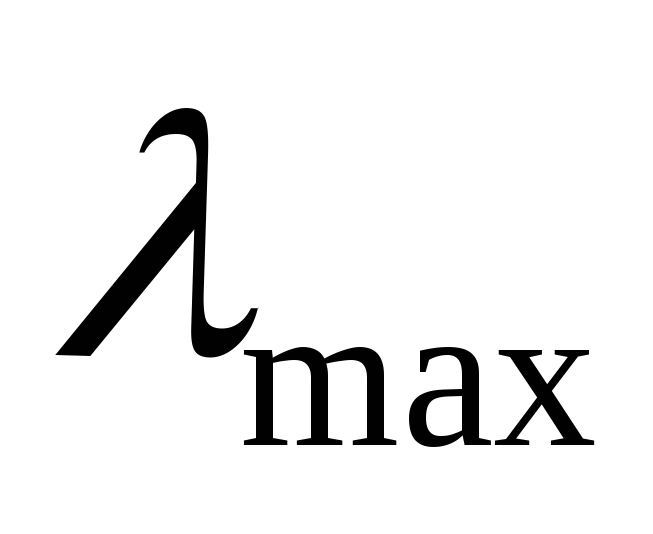 –
максимальная длина волны для фотоэффекта).
–
максимальная длина волны для фотоэффекта).
Фотон – элементарная частица с нулевой массой покоя. Скорость фотона равна 3.108 м/с.
Фотоэффектом называется явление вырывания электронов с поверхности твердых и жидких тел под действием излучений.
Пример решения задачи.
1. Определить максимальную кинетическую энергию фотоэлектрона калия при его освещении лучами длинной волны 4 * 10-7 м, если работа выхода электрона у калия 3,62 * 10-19 Дж.
Решение: h ν=Aвых + 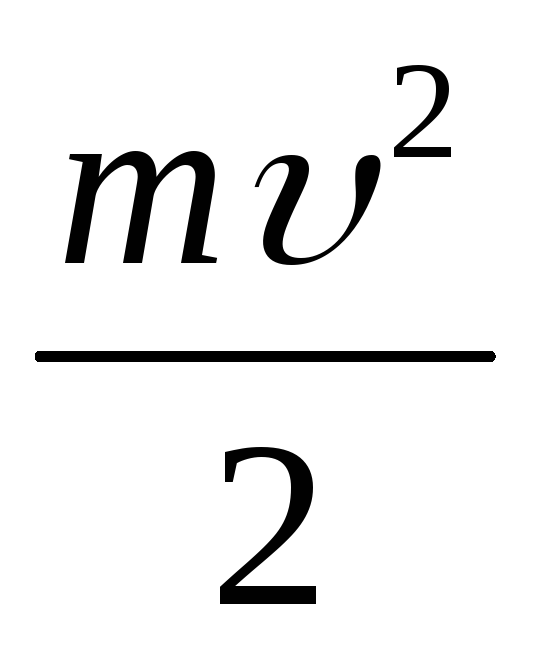 =
Авых +
Ек
=
Авых +
Ек  Ек = h ν — Авых.
Ек = h ν — Авых.
Так
как  ,то
Ек=
h
,то
Ек=
h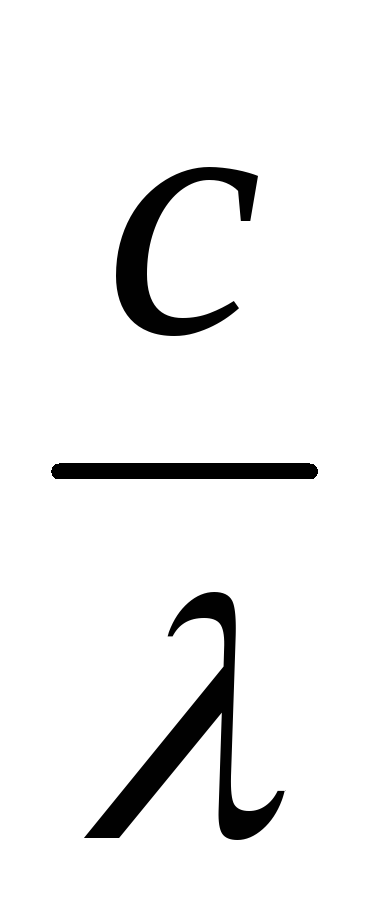 — Авых;
Ек =
6,62*10-34Дж*с
.
— Авых;
Ек =
6,62*10-34Дж*с
.  —
3,62*10-19 Дж
—
3,62*10-19 Дж
= 1,345*10
Лучи, возникающие при большом торможении быстрых электронов, называют рентгеновскими лучами. Они обладают большой проникающей способностью и используются в медицине, а также для исследования структуры кристаллов и сложных органических молекул.
В основе действия
ускорителей лежит работа электрического
поля А над заряженной частицей А=е U= 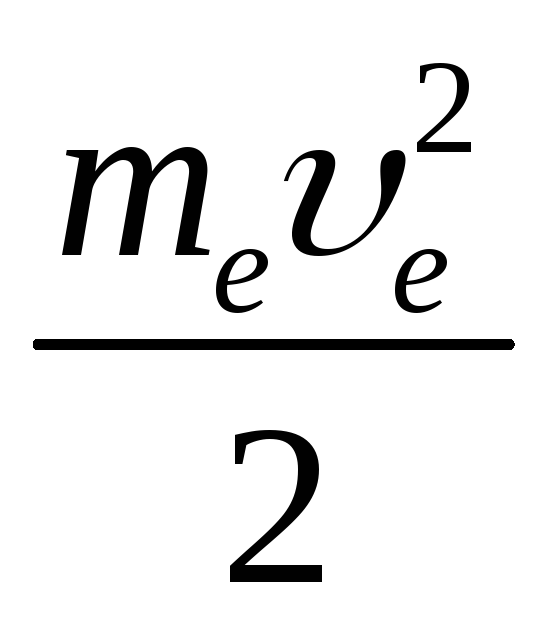
U – напряжение (В)
 е – скорость
электрона (м/с)
е – скорость
электрона (м/с)
mе – масса электрона (кг)
е – заряд электрона (Кл)
Радиоактивность – самопроизвольное превращение ядер одного химического элемента в ядра других химических элементов.
Излучение радиоактивных элементов в электрическом или магнитном полях распадаются на 3 вида:
а, β, γ – лучи.
γ-лучи–поток
коротковолновых электромагнитных
излучений (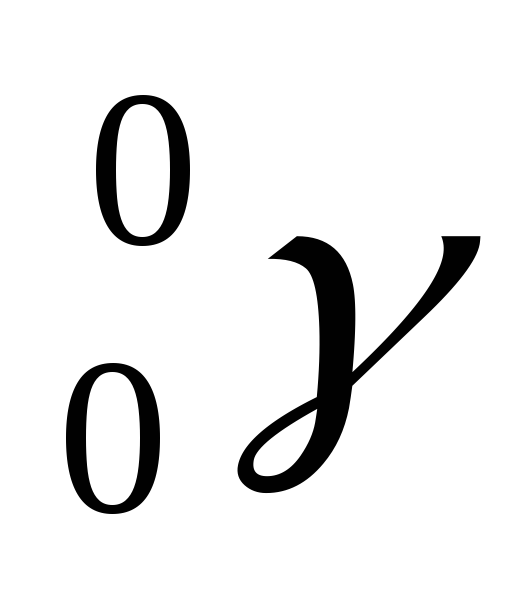 ).
В магнитном и электрическом полях не
меняет своего начального направления.
Проникающая способность самая большая.
Оказывает сильное биологическое
воздействие.
).
В магнитном и электрическом полях не
меняет своего начального направления.
Проникающая способность самая большая.
Оказывает сильное биологическое
воздействие.
β-лучи–поток
электронов
(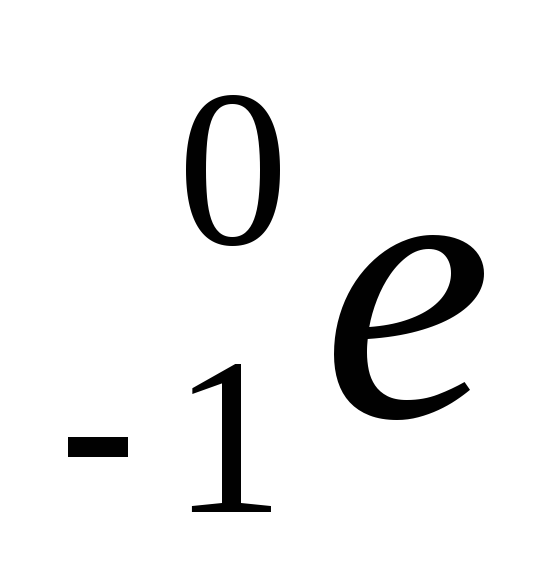 ),
движущихся со скоростями, близкими к
скорости света. В электрическом или
магнитном поле сильно отклоняется.
Заряжен отрицательно.
),
движущихся со скоростями, близкими к
скорости света. В электрическом или
магнитном поле сильно отклоняется.
Заряжен отрицательно.
α—лучи–поток
ядер атомов гелия (
Процесс самопроизвольного испускания α, β,γ–лучей ядрами радиоактивных элементов называется радиоактивностью, а сами лучи – радиоактивными излучениями.
Планетарную модель атома предложил Резерфорд. В центре атома расположено положительно заряженное ядро, вокруг вращаются отрицательно заряженные электроны. Атом – нейтральная система частиц. Количество положительных протонов в ядре и отрицательных электронов равно. Если атом теряет электрон, то образуется «+» ион, если атом приобретает электрон, то образуется «–» ион.
Атомное ядро состоит из положительно заряженных частиц – протонов, а также из нейтронов — заряд которого равен нулю. Количество протонов равно порядковому номеру элемента в таблице Менделеева. А = Ζ+N, А – массовое число (атомная масса), Z – число протонов, N – число нейтронов.
Спектр – разноцветные составляющие разложенного светового излучения, представленные в виде полос или отдельных линий. Существуют непрерывные, линейчатые и полосатые спектры излучения и столько же видов спектров поглощения.
Непрерывные или сплошные спектры дают тела, находящиеся в твёрдом или жидком состоянии, а также сильно сжатые газы.
Линейчатые спектры дают все вещества в газообразном атомарном состоянии. Линейчатый спектр частокол цветных линий различной яркости, разделённых широкими тёмными полосы.
Полосатые спектры создаются не атомами, а молекулами газа, не связанными или слабо связанными друг с другом. Полосатые спектры состоят из отдельных цветных полос, разделённых темными промежутками.
Газ поглощает наиболее интенсивно свет как раз тех длин волн, которые он испускает в сильно нагретом состоянии. Тёмные линии на фоне непрерывного спектра – это линии поглощения, образующие в совокупности спектр поглощения.
I постулат Бора. Атом может находиться в особых стационарных состояниях. Находясь в этих состояниях, он не излучает и не поглощает электромагнитные волны.
II постулат Бора. При переходе атома из одного стационарного состояния с энергией Еnв другое с энергией Ек испускается или поглощается один квант энергии. hν = Еп — Ек
ПРИМЕР: Каков
состав ядра Серебра (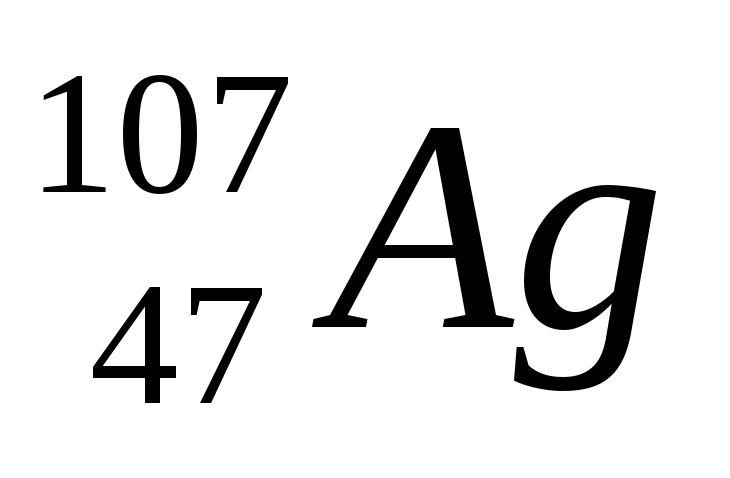 )
)
Решение:
А
= Z
+ N N
= А-Z.
Z=
47 протонов
N
= А-Z.
Z=
47 протонов N
= 107-47 = 60 нейтронов.
N
= 107-47 = 60 нейтронов.
Ответ: 47 протонов, 60 нейтронов.
studfile.net
ФИЗИКА АТОМА И АТОМНЫХ ЯВЛЕНИЙ 1 Введение
 ФИЗИКА АТОМА И АТОМНЫХ ЯВЛЕНИЙ
ФИЗИКА АТОМА И АТОМНЫХ ЯВЛЕНИЙ
 1. Введение 1. 1. Предмет атомной физики, её краткая история развития, цели и задачи 1. 2. Основные определения. Электрон, протон, нейтрон, атом, ион, молекула, нуклид, атомное ядро, химический элемент, изотопы 1. 3. Ядерные и оболочечные свойства атома 1. 4. Единицы измерения физических величин в атомной физике. Электрон-вольт. Моль, постоянная Авогадро, атомная единица массы, относительная атомная масса. Масштабы энергий, длин, частот, масс в атомной и ядерной физике 1. 5. Классическая, релятивистская и квантовая физика. Импульс и энергия 1. 6. Фотон. Шкала энергий фотонов (шкала электромагнитного излучения) 2
1. Введение 1. 1. Предмет атомной физики, её краткая история развития, цели и задачи 1. 2. Основные определения. Электрон, протон, нейтрон, атом, ион, молекула, нуклид, атомное ядро, химический элемент, изотопы 1. 3. Ядерные и оболочечные свойства атома 1. 4. Единицы измерения физических величин в атомной физике. Электрон-вольт. Моль, постоянная Авогадро, атомная единица массы, относительная атомная масса. Масштабы энергий, длин, частот, масс в атомной и ядерной физике 1. 5. Классическая, релятивистская и квантовая физика. Импульс и энергия 1. 6. Фотон. Шкала энергий фотонов (шкала электромагнитного излучения) 2
 Физика атома • Атомная физика (физика атома и атомных явлений) — это раздел физики, изучающий строение и свойства атомов, а также элементарные процессы, в которых атомы принимают участие • Объектами исследования атомной физики являются как атомы, так и молекулы, атомные и молекулярные ионы, экзотические атомы и другие микрочастицы • В явлениях, изучаемых в рамках атомной физики, основную роль играют электромагнитные взаимодействия • Результаты исследований в области атомной физики служат основой понимания химической связи, оптических и туннельных явлений, процессов в плазме, нейтральных жидкостях, твёрдых телах (в т. ч. полупроводниках и наноматериалах) • Теоретической основой самой атомной физики являются квантовая теория и квантовая электродинамика • Чёткой границы между атомной физикой и другими разделами физики не существует, и в соответствии с международной классификацией, атомная физика включена в область атомной, молекулярной физики и оптики 3
Физика атома • Атомная физика (физика атома и атомных явлений) — это раздел физики, изучающий строение и свойства атомов, а также элементарные процессы, в которых атомы принимают участие • Объектами исследования атомной физики являются как атомы, так и молекулы, атомные и молекулярные ионы, экзотические атомы и другие микрочастицы • В явлениях, изучаемых в рамках атомной физики, основную роль играют электромагнитные взаимодействия • Результаты исследований в области атомной физики служат основой понимания химической связи, оптических и туннельных явлений, процессов в плазме, нейтральных жидкостях, твёрдых телах (в т. ч. полупроводниках и наноматериалах) • Теоретической основой самой атомной физики являются квантовая теория и квантовая электродинамика • Чёткой границы между атомной физикой и другими разделами физики не существует, и в соответствии с международной классификацией, атомная физика включена в область атомной, молекулярной физики и оптики 3
 Краткая история развития атомной физики • Понятие «атом» употреблялось древнегреческими учеными (V – II веках до н. э. ) для обозначения наименьших, неделимых частиц, из которых состоит всё существующее в мире • Экспериментальные подтверждения атомистических представлений были получены в XIX века в химических и физических исследованиях • Представление о том, что атом состоит из положительно и отрицательно заряженных частей, было обосновано во второй половине XIX-го века • В 1897 г. Дж. Томсоном был открыт электрон, и вскоре доказано, что он является составной частью всех атомов • Представление об атоме как о системе, состоящей из ядра атомного и электронной оболочки, было обосновано Э. Резерфордом в 1911 году • После того, как это представление стало общепринятым, из атомной физики выделилась ядерная физика и, несколько позже, физика элементарных частиц 4
Краткая история развития атомной физики • Понятие «атом» употреблялось древнегреческими учеными (V – II веках до н. э. ) для обозначения наименьших, неделимых частиц, из которых состоит всё существующее в мире • Экспериментальные подтверждения атомистических представлений были получены в XIX века в химических и физических исследованиях • Представление о том, что атом состоит из положительно и отрицательно заряженных частей, было обосновано во второй половине XIX-го века • В 1897 г. Дж. Томсоном был открыт электрон, и вскоре доказано, что он является составной частью всех атомов • Представление об атоме как о системе, состоящей из ядра атомного и электронной оболочки, было обосновано Э. Резерфордом в 1911 году • После того, как это представление стало общепринятым, из атомной физики выделилась ядерная физика и, несколько позже, физика элементарных частиц 4
 Краткая история развития атомной физики • Основы современной атомной физики были заложены в начале XX-го века, когда на основе модели атома Э. Резерфорда и развития квантовых представлений М. Планка (1900) и А. Эйнштейна (1905) Н. Бором были даны объяснения ряда важнейших свойств атома (1913) и выдвинуты два «квантовых» постулата • Согласно первому из них, существуют особые (стационарные) состояния атома, в которых последний не излучает энергии, хотя входящие в его состав заряженные частицы (электроны) совершают ускоренное движение • Согласно второму постулату, излучение атома происходит при переходе из одного стационарного состояния в другое, а частота ν этого излучения определяется из условия h = E – E (правила частот Бора), где h — постоянная Планка, E и E — значения энергии атома в начальном и конечном состояниях • Первый постулат отражает факт устойчивости атома, второй — дискретность частот в атомных спектрах 5
Краткая история развития атомной физики • Основы современной атомной физики были заложены в начале XX-го века, когда на основе модели атома Э. Резерфорда и развития квантовых представлений М. Планка (1900) и А. Эйнштейна (1905) Н. Бором были даны объяснения ряда важнейших свойств атома (1913) и выдвинуты два «квантовых» постулата • Согласно первому из них, существуют особые (стационарные) состояния атома, в которых последний не излучает энергии, хотя входящие в его состав заряженные частицы (электроны) совершают ускоренное движение • Согласно второму постулату, излучение атома происходит при переходе из одного стационарного состояния в другое, а частота ν этого излучения определяется из условия h = E – E (правила частот Бора), где h — постоянная Планка, E и E — значения энергии атома в начальном и конечном состояниях • Первый постулат отражает факт устойчивости атома, второй — дискретность частот в атомных спектрах 5
 Краткая история развития атомной физики • На смену теории Бора, которая оказалась не в состоянии исчерпывающим образом объяснить свойства атомов и молекул, пришла последовательная квантовая теория, созданная в 20 -х – 30 -х годах XX-го века (В. Гейзенберг, Э. Шрёдингер, П. Дирак) • Тем не менее, постулаты Бора по-прежнему сохраняют свою значимость и неотъемлемым образом входят в основы физики микроскопических явлений • В рамках современной квантовой теории дано максимально полное объяснение свойств атома: принципы формирования оптических и рентгеновских спектров, поведение атомов в магнитных (эффект Зеемана) и электрических (эффект Штарка) полях, получили теоретическое обоснование периодическая система элементов и природа химической связи, были разработаны методы расчёта электронной структуры атомов, молекул и твёрдых тел (метод самосогласованного поля Хартри – Фока), созданы новые устройства для изучения структуры и свойств вещества (электронный микроскоп) • Развитие идей квантовой теории (гипотеза спина, принцип Паули и др. ), в свою очередь, опиралось на экспериментальные исследования в области атомной физики (линейчатые спектры атомов, фотоэффект, тонкая и сверхтонкая структура спектральных линий, опыты Франка и Герца, Дэвиссона и Джермера, Штерна и Герлаха, эффект Комптона, открытие дейтерия и других изотопов, эффект Оже и др. ) 6
Краткая история развития атомной физики • На смену теории Бора, которая оказалась не в состоянии исчерпывающим образом объяснить свойства атомов и молекул, пришла последовательная квантовая теория, созданная в 20 -х – 30 -х годах XX-го века (В. Гейзенберг, Э. Шрёдингер, П. Дирак) • Тем не менее, постулаты Бора по-прежнему сохраняют свою значимость и неотъемлемым образом входят в основы физики микроскопических явлений • В рамках современной квантовой теории дано максимально полное объяснение свойств атома: принципы формирования оптических и рентгеновских спектров, поведение атомов в магнитных (эффект Зеемана) и электрических (эффект Штарка) полях, получили теоретическое обоснование периодическая система элементов и природа химической связи, были разработаны методы расчёта электронной структуры атомов, молекул и твёрдых тел (метод самосогласованного поля Хартри – Фока), созданы новые устройства для изучения структуры и свойств вещества (электронный микроскоп) • Развитие идей квантовой теории (гипотеза спина, принцип Паули и др. ), в свою очередь, опиралось на экспериментальные исследования в области атомной физики (линейчатые спектры атомов, фотоэффект, тонкая и сверхтонкая структура спектральных линий, опыты Франка и Герца, Дэвиссона и Джермера, Штерна и Герлаха, эффект Комптона, открытие дейтерия и других изотопов, эффект Оже и др. ) 6
 Краткая история развития атомной физики • Во второй трети XX-го века в рамках атомной физики и на основе идей квантовой теории были разработаны новые экспериментальные методы физических исследований: электронный парамагнитный резонанс (ЭПР), фотоэлектронная спектроскопия (ФЭС), спектроскопия электронного удара (СЭУ), созданы устройства для их осуществления (мазер, лазер и др. ) • Непосредственное экспериментальное подтверждение получили фундаментальные принципы квантовой теории (интерференция квантовых состояний, лэмбовский сдвиг уровней и др. ), предложены новые методы расчёта электронной структуры вещества (теория функционала плотности), предсказаны новые физические явления (сверхизлучение) • Разработаны методы экспериментальных исследований процессов, происходящих с одиночными атомами, ионами и электронами, удерживаемыми электрическим и магнитным полями специальной конфигурации (атомными и ионными «ловушками» ) 7
Краткая история развития атомной физики • Во второй трети XX-го века в рамках атомной физики и на основе идей квантовой теории были разработаны новые экспериментальные методы физических исследований: электронный парамагнитный резонанс (ЭПР), фотоэлектронная спектроскопия (ФЭС), спектроскопия электронного удара (СЭУ), созданы устройства для их осуществления (мазер, лазер и др. ) • Непосредственное экспериментальное подтверждение получили фундаментальные принципы квантовой теории (интерференция квантовых состояний, лэмбовский сдвиг уровней и др. ), предложены новые методы расчёта электронной структуры вещества (теория функционала плотности), предсказаны новые физические явления (сверхизлучение) • Разработаны методы экспериментальных исследований процессов, происходящих с одиночными атомами, ионами и электронами, удерживаемыми электрическим и магнитным полями специальной конфигурации (атомными и ионными «ловушками» ) 7
 Краткая история развития атомной физики • Новые результаты в области атомной физики последней трети XX-го – начала XXI века в основном связаны с использованием лазеров • В научной практике широко применяются методы лазерной спектроскопии, в т. ч. нелинейной, на основе которых появилась возможность осуществлять спектроскопические измерения с одиночными атомами и молекулами, определять характеристики высоковозбуждённых состояний атомов, исследовать динамику внутриатомных и внутримолекулярных процессов длительностью до нескольких фемтосекунд (10– 15 с) • С помощью лазеров удалось осуществить и детально исследовать многофотонные процессы взаимодействия излучения с атомными системами (многофотонный фотоэффект, умножение частоты), а также охлаждение отдельных атомов до сверхнизких температур • Теоретические исследования последних десятилетий в области атомной физики связаны со стремительным прогрессом вычислительной техники и направлены на разработку эффективных методов и средств расчёта электронной структуры и свойств многоэлектронных атомных систем с учётом энергии электронной корреляции, релятивистских квантово-механических и квантовоэлектродинамических поправок 8
Краткая история развития атомной физики • Новые результаты в области атомной физики последней трети XX-го – начала XXI века в основном связаны с использованием лазеров • В научной практике широко применяются методы лазерной спектроскопии, в т. ч. нелинейной, на основе которых появилась возможность осуществлять спектроскопические измерения с одиночными атомами и молекулами, определять характеристики высоковозбуждённых состояний атомов, исследовать динамику внутриатомных и внутримолекулярных процессов длительностью до нескольких фемтосекунд (10– 15 с) • С помощью лазеров удалось осуществить и детально исследовать многофотонные процессы взаимодействия излучения с атомными системами (многофотонный фотоэффект, умножение частоты), а также охлаждение отдельных атомов до сверхнизких температур • Теоретические исследования последних десятилетий в области атомной физики связаны со стремительным прогрессом вычислительной техники и направлены на разработку эффективных методов и средств расчёта электронной структуры и свойств многоэлектронных атомных систем с учётом энергии электронной корреляции, релятивистских квантово-механических и квантовоэлектродинамических поправок 8
 Атомная физика • Исследования в области атомной физики нашли множество научных и практических применений • В промышленных целях для определения элементного состава вещества используются методы атомного спектрального анализа, включая ЭПР, ФЭС и СЭУ • Для решения геологических, биологических и медицинских задач используются методы дистанционного и локального лазерного спектрального атомного анализа, в промышленных и технических целях осуществляется лазерное разделение изотопов • Экспериментальные и теоретические методы атомной физики находят применение в астрофизике (определение состава и физических характеристик вещества звёзд и межзвёздной среды, исследование ридберговских атомов), метрологии (атомные часы) и других областях науки и техники 9
Атомная физика • Исследования в области атомной физики нашли множество научных и практических применений • В промышленных целях для определения элементного состава вещества используются методы атомного спектрального анализа, включая ЭПР, ФЭС и СЭУ • Для решения геологических, биологических и медицинских задач используются методы дистанционного и локального лазерного спектрального атомного анализа, в промышленных и технических целях осуществляется лазерное разделение изотопов • Экспериментальные и теоретические методы атомной физики находят применение в астрофизике (определение состава и физических характеристик вещества звёзд и межзвёздной среды, исследование ридберговских атомов), метрологии (атомные часы) и других областях науки и техники 9
 Цели и задачи курса атомной физики • Основная цель дисциплины «Физика атома и атомных явлений» , как части курса общей физики, заключается в формировании базовых знаний по физике микроскопических явлений на атомно-молекулярном уровне и умения применять их для решения прикладных проблем • Для достижения этой цели решаются следующие задачи: – анализ развития атомистических и становления квантовых представлений; – изучение важнейших экспериментальных фактов атомной физики и их взаимосвязи; – выявление специфики микроявлений и несостоятельности классической теории для их объяснения; – изучение основ квантовой механики и методов решения квантовомеханических задач; – систематическое изучение и объяснение на основе квантовой теории строения и свойств атомов и молекул, их поведения во внешних полях и во взаимодействии друг с другом 10
Цели и задачи курса атомной физики • Основная цель дисциплины «Физика атома и атомных явлений» , как части курса общей физики, заключается в формировании базовых знаний по физике микроскопических явлений на атомно-молекулярном уровне и умения применять их для решения прикладных проблем • Для достижения этой цели решаются следующие задачи: – анализ развития атомистических и становления квантовых представлений; – изучение важнейших экспериментальных фактов атомной физики и их взаимосвязи; – выявление специфики микроявлений и несостоятельности классической теории для их объяснения; – изучение основ квантовой механики и методов решения квантовомеханических задач; – систематическое изучение и объяснение на основе квантовой теории строения и свойств атомов и молекул, их поведения во внешних полях и во взаимодействии друг с другом 10
 ОСНОВНЫЕ ОПРЕДЕЛЕНИЯ: ЭЛЕКТРОН, ПРОТОН, НЕЙТРОН, АТОМ, ИОН, МОЛЕКУЛА, НУКЛИД, АТОМНОЕ ЯДРО, ХИМИЧЕСКИЙ ЭЛЕМЕНТ, ИЗОТОПЫ 11
ОСНОВНЫЕ ОПРЕДЕЛЕНИЯ: ЭЛЕКТРОН, ПРОТОН, НЕЙТРОН, АТОМ, ИОН, МОЛЕКУЛА, НУКЛИД, АТОМНОЕ ЯДРО, ХИМИЧЕСКИЙ ЭЛЕМЕНТ, ИЗОТОПЫ 11
 Электрон • Электрон — стабильная элементарная частица с отрицательным электрическим зарядом • Абсолютная величина заряда электрона равна элементарному заряду qe = –e ≈ – 1. 6∙ 10– 19 Кл • Масса электрона me = m ≈ 9. 11∙ 10– 31 кг • Спин электрона равен ½ • Магнитный момент электрона по модулю примерно равен магнетону Бора μe ≈ –μБ ≈ – 0. 579∙ 10– 4 э. В/Тл • Для обозначения электрона используются символ e или e– • Электроны образуют электронные оболочки всех атомов и ионов • Электрон имеет античастицу — позитрон (e+) 12
Электрон • Электрон — стабильная элементарная частица с отрицательным электрическим зарядом • Абсолютная величина заряда электрона равна элементарному заряду qe = –e ≈ – 1. 6∙ 10– 19 Кл • Масса электрона me = m ≈ 9. 11∙ 10– 31 кг • Спин электрона равен ½ • Магнитный момент электрона по модулю примерно равен магнетону Бора μe ≈ –μБ ≈ – 0. 579∙ 10– 4 э. В/Тл • Для обозначения электрона используются символ e или e– • Электроны образуют электронные оболочки всех атомов и ионов • Электрон имеет античастицу — позитрон (e+) 12
 Пучок электронов в магнитном поле 13
Пучок электронов в магнитном поле 13
 Электрон и позитрон • Спиральные треки электронов и позитронов в камере Вильсона • Электрон и позитрон рождаются в результате распада гамма-кванта • Треки электронов закручены по часовой стрелке, позитронов – против 14
Электрон и позитрон • Спиральные треки электронов и позитронов в камере Вильсона • Электрон и позитрон рождаются в результате распада гамма-кванта • Треки электронов закручены по часовой стрелке, позитронов – против 14
 Протон • Протон — стабильная элементарная частица с положительным электрическим зарядом • Заряд протона равен элементарному заряду qp = e ≈ 1. 6∙ 10– 19 Кл • Масса протона mp ≈ 1836 me ≈ 1. 67∙ 10– 27 кг • Спин протона равен ½ • Магнитный момент протона μp ≈ 8. 803∙ 10– 8 э. В/Тл • Протон обозначается символом p или p+ • Протон имеет античастицу — антипротон (p–) 15
Протон • Протон — стабильная элементарная частица с положительным электрическим зарядом • Заряд протона равен элементарному заряду qp = e ≈ 1. 6∙ 10– 19 Кл • Масса протона mp ≈ 1836 me ≈ 1. 67∙ 10– 27 кг • Спин протона равен ½ • Магнитный момент протона μp ≈ 8. 803∙ 10– 8 э. В/Тл • Протон обозначается символом p или p+ • Протон имеет античастицу — антипротон (p–) 15
 Аннигиляция антипротона • Антипротон (голубой трек) сталкивается с протоном в пузырьковой камере • В результате возникают четыре положительных пиона (красные треки) и четыре отрицательных (зелёные треки) • Жёлтый трек принадлежит мюону, который рождается в результате распада пиона 16
Аннигиляция антипротона • Антипротон (голубой трек) сталкивается с протоном в пузырьковой камере • В результате возникают четыре положительных пиона (красные треки) и четыре отрицательных (зелёные треки) • Жёлтый трек принадлежит мюону, который рождается в результате распада пиона 16
 Нейтрон • Нейтрон —элементарная частица с нулевым электрическим зарядом • Время жизни нейтрона в свободном состоянии составляет примерно 886 с • Масса нейтрона mn ≈ 1839 me ≈ 1. 67∙ 10– 27 кг • Спин нейтрона равен ½ • Несмотря на отсутствие электрического заряда, нейтрон обладает магнитным моментом μn ≈ – 6. 030∙ 10– 8 э. В/Тл • Нейтрон обозначается символом n или n 0 • Нейтрон имеет античастицу — антинейтрон • Протоны и нейтроны объединяют общим названием нуклоны • Атомные ядра состоят из протонов и нейтронов 17
Нейтрон • Нейтрон —элементарная частица с нулевым электрическим зарядом • Время жизни нейтрона в свободном состоянии составляет примерно 886 с • Масса нейтрона mn ≈ 1839 me ≈ 1. 67∙ 10– 27 кг • Спин нейтрона равен ½ • Несмотря на отсутствие электрического заряда, нейтрон обладает магнитным моментом μn ≈ – 6. 030∙ 10– 8 э. В/Тл • Нейтрон обозначается символом n или n 0 • Нейтрон имеет античастицу — антинейтрон • Протоны и нейтроны объединяют общим названием нуклоны • Атомные ядра состоят из протонов и нейтронов 17
 Нейтрон • Поскольку нейтроны не имеют электрического заряда, они не оставляют треков в камерах-детекторах частиц • Тем не менее нейтроны можно обнаружить по результатам их взаимодействия с другими, заряженными, частицами • Расцвеченное изображение показывает треки частиц в камере Вильсона, наполненной смесью газообразного водорода, этилового спирта и воды • Пучок нейтронов проникает в камеру снизу и вызывает трансмутации атомов кислорода и углерода, входящих в состав молекул этилового спирта 18
Нейтрон • Поскольку нейтроны не имеют электрического заряда, они не оставляют треков в камерах-детекторах частиц • Тем не менее нейтроны можно обнаружить по результатам их взаимодействия с другими, заряженными, частицами • Расцвеченное изображение показывает треки частиц в камере Вильсона, наполненной смесью газообразного водорода, этилового спирта и воды • Пучок нейтронов проникает в камеру снизу и вызывает трансмутации атомов кислорода и углерода, входящих в состав молекул этилового спирта 18
 Атом • Атом — микрочастица, состоящая из атомного ядра и окружающих его электронов (электронной оболочки) • Положительно заряженное ядро удерживает отрицательно заряженные электроны силами электрического притяжения • Поскольку ядро атома состоит из протонов и нейтронов, и при этом электрический заряд нейтрона равен нулю, протона — элементарному заряду e, заряд электрона равен −e, то при числе электронов в оболочке, равном числу протонов в ядре, суммарный электрический заряд атома равен нулю • Размеры ядра (~ 10– 15 – 10– 14 м) крайне малы по сравнению с размерами атома (~10– 10 м), однако из-за того, что масса протона (как и нейтрона) почти в 2 тысячи раз больше массы электрона, практически вся масса атома (≈ 99. 97 ℅) сосредоточена в ядре 19
Атом • Атом — микрочастица, состоящая из атомного ядра и окружающих его электронов (электронной оболочки) • Положительно заряженное ядро удерживает отрицательно заряженные электроны силами электрического притяжения • Поскольку ядро атома состоит из протонов и нейтронов, и при этом электрический заряд нейтрона равен нулю, протона — элементарному заряду e, заряд электрона равен −e, то при числе электронов в оболочке, равном числу протонов в ядре, суммарный электрический заряд атома равен нулю • Размеры ядра (~ 10– 15 – 10– 14 м) крайне малы по сравнению с размерами атома (~10– 10 м), однако из-за того, что масса протона (как и нейтрона) почти в 2 тысячи раз больше массы электрона, практически вся масса атома (≈ 99. 97 ℅) сосредоточена в ядре 19
 Атом золота Au • Изображение отдельного атома золота получено с помощью просвечивающего электронного микроскопа • Увеличение в 30 000 раз до размера в 35 мм 20
Атом золота Au • Изображение отдельного атома золота получено с помощью просвечивающего электронного микроскопа • Увеличение в 30 000 раз до размера в 35 мм 20
 Атомы золота Au Расцвеченное изображение атомов золота на графитовой подложке получено с помощью просвечивающего электронного микроскопа 21
Атомы золота Au Расцвеченное изображение атомов золота на графитовой подложке получено с помощью просвечивающего электронного микроскопа 21
 Атомы кремния Si • Расцвеченное изображение атомов кремния получено с помощью просвечивающего электронного микроскопа • Показана элементарная ячейка кристалла. Также видны связи между атомами • Увеличение в 45 000 раз до размера в 35 мм 22
Атомы кремния Si • Расцвеченное изображение атомов кремния получено с помощью просвечивающего электронного микроскопа • Показана элементарная ячейка кристалла. Также видны связи между атомами • Увеличение в 45 000 раз до размера в 35 мм 22
 Атомы марганца Mn • Расцвеченное изображение атомов марганца получено с помощью просвечивающего электронного микроскопа • Изображение демонстрирует отталкивание двух атомов марганца, внедрённых в полупроводниковый кристалл арсенида галлия Ga. As 23
Атомы марганца Mn • Расцвеченное изображение атомов марганца получено с помощью просвечивающего электронного микроскопа • Изображение демонстрирует отталкивание двух атомов марганца, внедрённых в полупроводниковый кристалл арсенида галлия Ga. As 23
 Атомы урана U • Расцвеченное изображение атомов урана получено с помощью просвечивающего электронного микроскопа • Маленькие точки правильной формы – отдельные атомы, более крупные образования – кластеры, состоящие из 2– 20 атомов • Размер поля зрения – примерно 100 Å. Увеличение в 3 500 000 раз до размера в 35 мм 24
Атомы урана U • Расцвеченное изображение атомов урана получено с помощью просвечивающего электронного микроскопа • Маленькие точки правильной формы – отдельные атомы, более крупные образования – кластеры, состоящие из 2– 20 атомов • Размер поля зрения – примерно 100 Å. Увеличение в 3 500 000 раз до размера в 35 мм 24
 Микрокристаллы уранила UO 22+ • Расцвеченное изображение микрокристаллов уранила получено с помощью просвечивающего электронного микроскопа • Каждое пятнышко представляет собой отдельный атом урана • Увеличение в 6 250 000 раз до размера в 35 мм 25
Микрокристаллы уранила UO 22+ • Расцвеченное изображение микрокристаллов уранила получено с помощью просвечивающего электронного микроскопа • Каждое пятнышко представляет собой отдельный атом урана • Увеличение в 6 250 000 раз до размера в 35 мм 25
 Атомы вольфрама W • Расцвеченное изображение острия вольфрамовой иглы получено с помощью ионного проектора • Видны отдельные атомы, а также следы атомов, удалённых с поверхности иглы за время экспозиции изображения (около 1 секунды) 26
Атомы вольфрама W • Расцвеченное изображение острия вольфрамовой иглы получено с помощью ионного проектора • Видны отдельные атомы, а также следы атомов, удалённых с поверхности иглы за время экспозиции изображения (около 1 секунды) 26
 Химический элемент, нуклид, изотопы • Атомы с определенным числом протонов Z в ядре принадлежат одному и тому же химическому элементу. Число Z называется атомным номером химического элемента. • Совокупность атомов с определенным числом протонов Z и нейтронов N в ядре называется нуклидом. Нуклиды обозначают, добавляя к названию элемента значение массового числа А, равного сумме Z + N (например, кислород-16, уран-235), или помещая число А возле символа элемента (16 О, 235 U). • Нуклиды одного и того же элемента называются изотопами. • Масса самого легкого атома — атома водорода, состоящего из одного протона и одного электрона, равна m. H ≈ 1. 67· 10– 27 кг. Массы остальных атомов приближенно в А раз больше, чем m. H. • В природе встречается 90 химических элементов и более 300 различных нуклидов; 270 из них стабильны, остальные — радиоактивны. Около 1 700 радиоактивных нуклидов получено искусственным путем. 27
Химический элемент, нуклид, изотопы • Атомы с определенным числом протонов Z в ядре принадлежат одному и тому же химическому элементу. Число Z называется атомным номером химического элемента. • Совокупность атомов с определенным числом протонов Z и нейтронов N в ядре называется нуклидом. Нуклиды обозначают, добавляя к названию элемента значение массового числа А, равного сумме Z + N (например, кислород-16, уран-235), или помещая число А возле символа элемента (16 О, 235 U). • Нуклиды одного и того же элемента называются изотопами. • Масса самого легкого атома — атома водорода, состоящего из одного протона и одного электрона, равна m. H ≈ 1. 67· 10– 27 кг. Массы остальных атомов приближенно в А раз больше, чем m. H. • В природе встречается 90 химических элементов и более 300 различных нуклидов; 270 из них стабильны, остальные — радиоактивны. Около 1 700 радиоактивных нуклидов получено искусственным путем. 27
 Периодическая система химических элементов 28
Периодическая система химических элементов 28
 Таблица изотопов 29
Таблица изотопов 29
 Изотопы гелия • Ядро гелия-4 содержит два нейтрона (голубые шарики) и два протона (красные шарики) • Ядро гелия-6 состоит из ядра гелия-4, окружённого двухнейтронным «гало» • В ядре гелия-8 таких пар нейтронов две 30
Изотопы гелия • Ядро гелия-4 содержит два нейтрона (голубые шарики) и два протона (красные шарики) • Ядро гелия-6 состоит из ядра гелия-4, окружённого двухнейтронным «гало» • В ядре гелия-8 таких пар нейтронов две 30
 Ионы • Процесс удаления или присоединения электронов к атому называют ионизацией • При числе электронов в оболочке, меньшем Z, получается положительный атомный ион, при большем, чем Z — отрицательный • Таким образом, ион — это электрически заряженный атом (или молекула), который образуется при отрыве или присоединении одного или нескольких электронов к нейтральному атому (или молекуле) 31
Ионы • Процесс удаления или присоединения электронов к атому называют ионизацией • При числе электронов в оболочке, меньшем Z, получается положительный атомный ион, при большем, чем Z — отрицательный • Таким образом, ион — это электрически заряженный атом (или молекула), который образуется при отрыве или присоединении одного или нескольких электронов к нейтральному атому (или молекуле) 31
 Ионы • Положительно заряженные ионы называются катионами, отрицательно заряженные — анионами. • Ионы обозначаются химическим символом с индексом, который указывает кратность (величину заряда в единицах элементарного заряда) и знак иона: H–, Na+, UO 22+ • Ионы могут представлять собой как устойчивые образования (как правило, в растворах или кристаллах), так и неустойчивые (в газах при обычных условиях) • Атомные катионы могут быть получены вплоть до заряда +(Z – 1). Так, на ускорителях ионов получены, например, U 90+ и U 91+ • Атомные анионы с зарядом 2 и более в свободном состоянии не существуют 32
Ионы • Положительно заряженные ионы называются катионами, отрицательно заряженные — анионами. • Ионы обозначаются химическим символом с индексом, который указывает кратность (величину заряда в единицах элементарного заряда) и знак иона: H–, Na+, UO 22+ • Ионы могут представлять собой как устойчивые образования (как правило, в растворах или кристаллах), так и неустойчивые (в газах при обычных условиях) • Атомные катионы могут быть получены вплоть до заряда +(Z – 1). Так, на ускорителях ионов получены, например, U 90+ и U 91+ • Атомные анионы с зарядом 2 и более в свободном состоянии не существуют 32
 Ионная ловушка (1959) • Ионная ловушка (ловушка Пеннинга), в которой созданы электрическое и магнитное поля специальной конфигурации, позволяет длительное время удерживать одиночные ионы и электроны 33
Ионная ловушка (1959) • Ионная ловушка (ловушка Пеннинга), в которой созданы электрическое и магнитное поля специальной конфигурации, позволяет длительное время удерживать одиночные ионы и электроны 33
 Молекула • Молекула — это наименьшая устойчивая частица вещества, состоящая более чем из одного атома • Молекула характеризуется определённым составом атомных ядер, числом электронов и пространственной структурой • Для обозначения количественного и качественного состава молекул используются химические формулы: O 2 (молекула кислорода), H 2 O (молекула воды), CH 4 (молекула метана), C 6 H 6 (молекула бензола), C 60 (молекула фуллерена) 34
Молекула • Молекула — это наименьшая устойчивая частица вещества, состоящая более чем из одного атома • Молекула характеризуется определённым составом атомных ядер, числом электронов и пространственной структурой • Для обозначения количественного и качественного состава молекул используются химические формулы: O 2 (молекула кислорода), H 2 O (молекула воды), CH 4 (молекула метана), C 6 H 6 (молекула бензола), C 60 (молекула фуллерена) 34
 Молекулы метана и бензола 35
Молекулы метана и бензола 35
 Молекула аспирина 36
Молекула аспирина 36
 Молекула фуллерена С 60 37
Молекула фуллерена С 60 37
 Молекула инсулина 38
Молекула инсулина 38
 Молекула ДНК • Расцвеченное изображение молекулы ДНК получено при помощи просвечивающего электронного микроскопа • В камере с высоким вакуумом образец ДНК покрывают тонким слоем платины • Металлическое покрытие даёт контрастное изображение в электронном микроскопе 39
Молекула ДНК • Расцвеченное изображение молекулы ДНК получено при помощи просвечивающего электронного микроскопа • В камере с высоким вакуумом образец ДНК покрывают тонким слоем платины • Металлическое покрытие даёт контрастное изображение в электронном микроскопе 39
 Ядерные и оболочечные свойства атома Ядерные свойства Оболочечные свойства Определяются составом ядра: радиоактивность, способность участвовать в ядерных реакциях и т. п. Определяются строением электронной оболочки: химические, физические (электрические, магнитные, оптические и т. д. ) 40
Ядерные и оболочечные свойства атома Ядерные свойства Оболочечные свойства Определяются составом ядра: радиоактивность, способность участвовать в ядерных реакциях и т. п. Определяются строением электронной оболочки: химические, физические (электрические, магнитные, оптические и т. д. ) 40
 ЕДИНИЦЫ ИЗМЕРЕНИЯ ФИЗИЧЕСКИХ ВЕЛИЧИН В АТОМНОЙ ФИЗИКЕ 41
ЕДИНИЦЫ ИЗМЕРЕНИЯ ФИЗИЧЕСКИХ ВЕЛИЧИН В АТОМНОЙ ФИЗИКЕ 41
 Энергия • Единицей энергии в СИ является джоуль (Дж), однако для величин энергии объектов и явлений атомной физики такая единица используется редко • Более употребительной является внесистемная единица энергии, называемая электрон-вольтом (э. В, e. V) • Электрон-вольт — это энергия, которую приобретает заряженная частица с элементарным зарядом, проходя ускоряющую разность потенциалов в 1 вольт: 1 э. В = 1. 602∙ 10− 19 Дж • Для измерения энергий в атомной и ядерной физике используются кратные (кэ. В, 1 кэ. В = 103 э. В, Мэ. В, 1 Мэ. В = 106 э. В) и дольные (мкэ. В, 1 мкэ. В = 10– 6 э. В) единицы электрон-вольта, а также некоторые другие: ридберг (Rydberg, Ry), хартри (hartree, Ha, или атомная единица, а. е. ) • Ридберг численно равен энергии ионизации атома водорода из основного состояния в приближении бесконечной массы ядра: 1 Ry ≈ 13. 606 э. В • Хартри равен абсолютной величине потенциальной энергии электрона в основном состоянии атома водорода в приближении бесконечной массы ядра: 1 Ha = 2 Ry ≈ 27. 211 э. В • Энергии состояний атомных систем, а также переходов между состояниями могут измеряться и в других единицах 42
Энергия • Единицей энергии в СИ является джоуль (Дж), однако для величин энергии объектов и явлений атомной физики такая единица используется редко • Более употребительной является внесистемная единица энергии, называемая электрон-вольтом (э. В, e. V) • Электрон-вольт — это энергия, которую приобретает заряженная частица с элементарным зарядом, проходя ускоряющую разность потенциалов в 1 вольт: 1 э. В = 1. 602∙ 10− 19 Дж • Для измерения энергий в атомной и ядерной физике используются кратные (кэ. В, 1 кэ. В = 103 э. В, Мэ. В, 1 Мэ. В = 106 э. В) и дольные (мкэ. В, 1 мкэ. В = 10– 6 э. В) единицы электрон-вольта, а также некоторые другие: ридберг (Rydberg, Ry), хартри (hartree, Ha, или атомная единица, а. е. ) • Ридберг численно равен энергии ионизации атома водорода из основного состояния в приближении бесконечной массы ядра: 1 Ry ≈ 13. 606 э. В • Хартри равен абсолютной величине потенциальной энергии электрона в основном состоянии атома водорода в приближении бесконечной массы ядра: 1 Ha = 2 Ry ≈ 27. 211 э. В • Энергии состояний атомных систем, а также переходов между состояниями могут измеряться и в других единицах 42
 Масса • Единицей массы в СИ является килограмм (кг), однако для измерения масс объектов атомной физики используется внесистемная единица измерения, называемая атомной единицей массы (а. е. м. ) • Атомная единица массы равна 1/12 массы несвязанного невозбуждённого атома углерода-12 (12 С): 1 а. е. м. ≈ 1. 66∙ 10− 27 кг • 1 а. е. м. приблизительно равна массе одного протона или нейтрона • Относительная атомная масса — масса атома, выраженная в а. е. м. • Постоянная Авогадро NA — физическая константа, численно равная количеству атомов в 12 г чистого изотопа углерода-12: NA ≈ 6. 022∙ 1023 моль– 1 • Моль (единица количества вещества в СИ) по определению содержит NA структурных элементов (атомов, молекул, ионов). 43
Масса • Единицей массы в СИ является килограмм (кг), однако для измерения масс объектов атомной физики используется внесистемная единица измерения, называемая атомной единицей массы (а. е. м. ) • Атомная единица массы равна 1/12 массы несвязанного невозбуждённого атома углерода-12 (12 С): 1 а. е. м. ≈ 1. 66∙ 10− 27 кг • 1 а. е. м. приблизительно равна массе одного протона или нейтрона • Относительная атомная масса — масса атома, выраженная в а. е. м. • Постоянная Авогадро NA — физическая константа, численно равная количеству атомов в 12 г чистого изотопа углерода-12: NA ≈ 6. 022∙ 1023 моль– 1 • Моль (единица количества вещества в СИ) по определению содержит NA структурных элементов (атомов, молекул, ионов). 43
 Длина • Единицей длины в СИ является метр (м). 1 метр равен расстоянию, которое проходит свет в вакууме за промежуток времени, равный 1/299792458 секунды. • За исключением измерений длин волн электромагнитного излучения радиодиапазона, такая единица длины редко применяется в атомной физике, а вместо неё для измерения линейных размеров, а также длин волн используются дольные единицы метра: сантиметр (см, 1 см = 10– 2 м), миллиметр (мм, 1 мм = 10– 3 м), микрометр (мкм, μм, 1 мкм = 10– 6 м), нанометр (нм, 1 нм = 10– 9 м), пикометр (пм, 1 пм = 10– 12 м) и другие, а также внесистемные единицы: ангстрем (Å, 1 Å = 0. 1 нм = 10– 10 м), бор (или боровский радиус) (1 бор ≈ 0. 529 Å) 44
Длина • Единицей длины в СИ является метр (м). 1 метр равен расстоянию, которое проходит свет в вакууме за промежуток времени, равный 1/299792458 секунды. • За исключением измерений длин волн электромагнитного излучения радиодиапазона, такая единица длины редко применяется в атомной физике, а вместо неё для измерения линейных размеров, а также длин волн используются дольные единицы метра: сантиметр (см, 1 см = 10– 2 м), миллиметр (мм, 1 мм = 10– 3 м), микрометр (мкм, μм, 1 мкм = 10– 6 м), нанометр (нм, 1 нм = 10– 9 м), пикометр (пм, 1 пм = 10– 12 м) и другие, а также внесистемные единицы: ангстрем (Å, 1 Å = 0. 1 нм = 10– 10 м), бор (или боровский радиус) (1 бор ≈ 0. 529 Å) 44
 Время • Единицей длительности промежутков времени в СИ является секунда (с) • В настоящее время секунда определяется на основе т. н. атомного эталона времени: одна секунда (или атомная секунда) равна 9 192 631 770 периодам электромагнитного излучения, соответствующего энергетическому переходу между двумя уровнями сверхтонкой структуры основного состояния изотопа 133 Cs (цезия-133) • Длительности быстропротекающих процессов в атомной физике принято измерять в дольных единицах секунды: нано-, пико- или фемтосекундах (нс, пс, фс, 1 фс = 10– 15 с) 45
Время • Единицей длительности промежутков времени в СИ является секунда (с) • В настоящее время секунда определяется на основе т. н. атомного эталона времени: одна секунда (или атомная секунда) равна 9 192 631 770 периодам электромагнитного излучения, соответствующего энергетическому переходу между двумя уровнями сверхтонкой структуры основного состояния изотопа 133 Cs (цезия-133) • Длительности быстропротекающих процессов в атомной физике принято измерять в дольных единицах секунды: нано-, пико- или фемтосекундах (нс, пс, фс, 1 фс = 10– 15 с) 45
 Масштабы физических величин в атомной и ядерной физике • Для явлений атомной физики характерны размеры от 10– 12 м (внутренние подоболочки тяжелых атомов) до десятых долей нанометра (размеры атомов и небольших молекул), энергии от 10– 6 э. В (сверхтонкая структура уровней) до 105 э. В (энергии связи электронов внутренних подоболочек), времена от десятков фемтосекунд (длительности сверхкоротких лазерных импульсов) до тысяч секунд (времена жизни метастабильных состояний атомов) • Типичные размеры молекул составляют 0. 1– 1 нм. Межъядерное расстояние у наименьшей молекулы (H 2) равно 0. 074 нм • Макромолекулы ДНК и многих полимеров могут иметь макроскопические размеры. Так, длина развёрнутой спирали ДНК может достигать нескольких сантиметров при ширине примерно 2 нм. 46
Масштабы физических величин в атомной и ядерной физике • Для явлений атомной физики характерны размеры от 10– 12 м (внутренние подоболочки тяжелых атомов) до десятых долей нанометра (размеры атомов и небольших молекул), энергии от 10– 6 э. В (сверхтонкая структура уровней) до 105 э. В (энергии связи электронов внутренних подоболочек), времена от десятков фемтосекунд (длительности сверхкоротких лазерных импульсов) до тысяч секунд (времена жизни метастабильных состояний атомов) • Типичные размеры молекул составляют 0. 1– 1 нм. Межъядерное расстояние у наименьшей молекулы (H 2) равно 0. 074 нм • Макромолекулы ДНК и многих полимеров могут иметь макроскопические размеры. Так, длина развёрнутой спирали ДНК может достигать нескольких сантиметров при ширине примерно 2 нм. 46
 Фотон • Фотон, или квант электромагнитного излучения (поля), — безмассовая элементарная частица, не имеющая электрического заряда • В вакууме фотон движется со скоростью c • Фотон имеет спин, равный 1 • Проекции спина на направления, перпендикулярные направлению распространению фотона, определяют состояние его поляризации • Фотон обозначается символом γ 47
Фотон • Фотон, или квант электромагнитного излучения (поля), — безмассовая элементарная частица, не имеющая электрического заряда • В вакууме фотон движется со скоростью c • Фотон имеет спин, равный 1 • Проекции спина на направления, перпендикулярные направлению распространению фотона, определяют состояние его поляризации • Фотон обозначается символом γ 47
 Излучение ионного аргонового лазера 48
Излучение ионного аргонового лазера 48
 Шкала энергий фотонов (шкала электромагнитного излучения) 49
Шкала энергий фотонов (шкала электромагнитного излучения) 49
present5.com