Взаимодействие азотной кислоты металлами и неметаллами
Взаимодействие азотной кислоты с металлами и неметаллами [c.115]Взаимодействие кислот окислителей с металлами и неметаллами. 1. В пробирку с газоотводной трубкой поместите медные стружки и прилейте 2—3 мл концентрированной азотной кислоты, слегка подогрейте. Выделяющийся бурый газ поглощается водой. Обнаружьте в образовав- [c.57]
И и к е л ь не окисляется на воздухе и легко растворяется только в разбавленной азотной кислоте. Химическая стойкость никеля обусловлена его склонностью к пассивированию, связанному с образованием на поверхности металла защитной оксидной пленки.С кислородом он начинает взаимодействовать только при 500°С. И лишь в измельченном состоянии при нагревании N1 реагирует с галогенами, серой и другими неметаллами. С большинством из них он, как и многие -элементы, образует соединения переменного состава (в том числе и металлоподобные).
По уравнению (1) процесс восстановления протекает при взаимодействии концентрированной азотной кислоты с металлами, электродные потенциалы которых положительны, например Си, Ag, Hg. При взаимодействии же с неметаллами или с металлами, электродные потенциалы которых отрицательны, но по абсолютной величине невелики, концентрированная азотная кислота восстанавливается по уравнению (2). [c.218]
Вследствие довольно высокой активности марганец легко окисляется при нагревании, в особенности в порошкообразном состоянии, кислородом, серой, галогенами. Компактный металл на воздухе устойчив. Так как покрывается оксидной пленкой, которая препятствует дальнейшему окислению металла.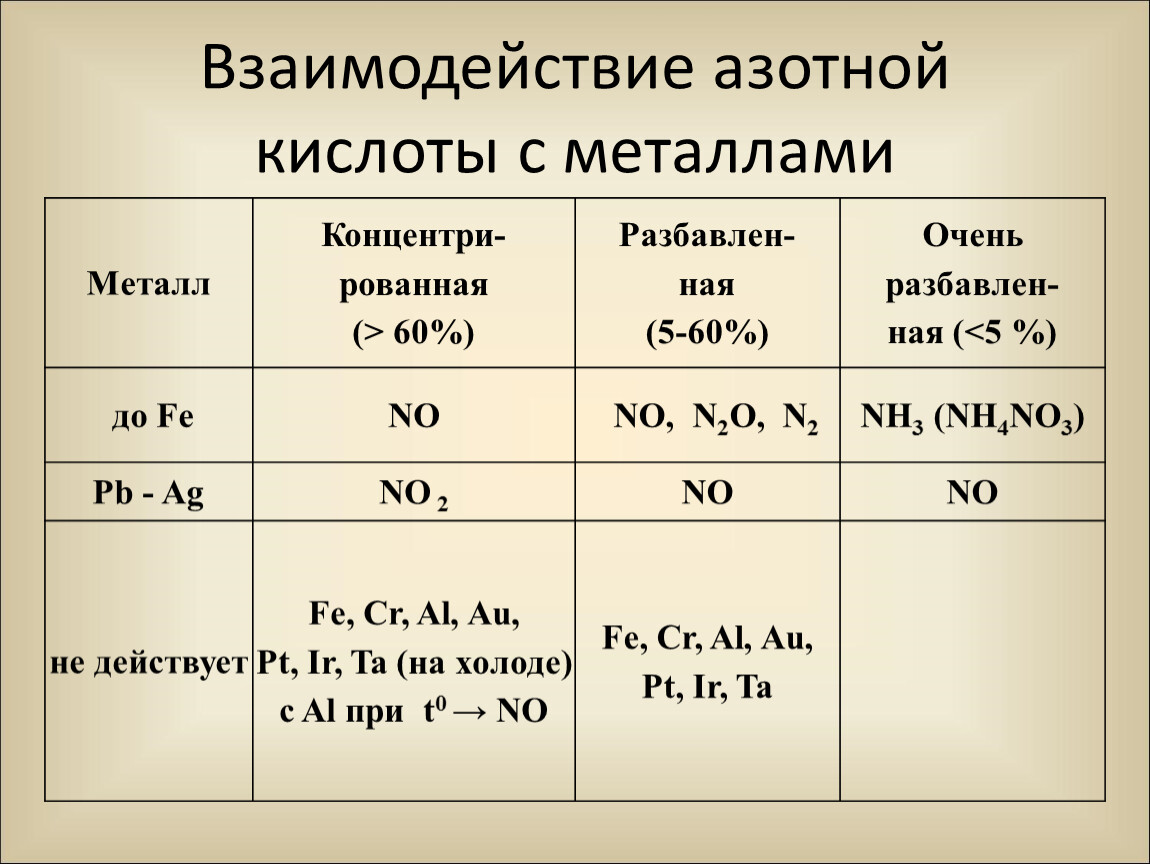
Общая характеристика элементов главной подгруппы V группы периодической системы. Азот. Строение атома, строение молекулы, степени окисления. Круговорот азота в природе. Получение, физические и химические свойства азота. Аммиак, строение молекулы, получение, физические и химические свойства. Восстановительные свойства аммиака. Аммиачная вода. Соли аммония, их получение. Термическое разложение солей аммония. Оксиды азота, их получение и основные химические свойства. Азотистая кислота. Окислительно-восстановительные свойства соединений азота со степенью окисления +3. Азотная кислота, ее получение и химические свойства. Окислительные свойства азотной кислоты в реакциях взаимодействия с металлами и неметаллами. Царская водка. Соли азотной кислоты, их термическое разложение. Азотные удобрения.
Концентрированная серная кислота растворяет марганец только при нагревании с выделением двуокиси серы. В азотной кислоте марганец растворяется, восстанавливая ее до окиси или закиси азота. Порошкообразный марганец взаимодействует при нагревании с многими неметаллами. С металлами образует сплавы.
[c.171]Азотная кислота — сильная и характеризуется ярко выраженными окислительными свойствами. В продажу обычно поступает 65%-ная ННОз плотностью 1400 кг/м . С водой азотная кислота смешивается в любых соотношениях. Животные и растительные ткани при действии на них азотной кислоты очень быстро разрушаются.
 Даже небольшое количество разбавленной азотной кислоты оставляет желтые пятна на коже. Концентрированная азотная кислота взаимодействует с многими неметаллами сера окисляется ею до серной кислоты при кипячении, уголь —до углекислого газа. Тлеющая лучинка, внесенная в пары азотной кислоты, воспламеняется скипидар, влитый в концентрированную азотную кислоту, загорается синий раствор индиго обесцвечивается. Концентрированная азотная кислота не действует на золото и платину. Железо, алюминий и некоторые другие металлы пассивируются концентрированной азотной кислотой, так как на их поверхности возникает плотная защитная пленка оксидов, нерастворимая в кислотах. Это свойство азотной кислоты позволяет хранить и транспортировать ее в стальных цистернах.
Даже небольшое количество разбавленной азотной кислоты оставляет желтые пятна на коже. Концентрированная азотная кислота взаимодействует с многими неметаллами сера окисляется ею до серной кислоты при кипячении, уголь —до углекислого газа. Тлеющая лучинка, внесенная в пары азотной кислоты, воспламеняется скипидар, влитый в концентрированную азотную кислоту, загорается синий раствор индиго обесцвечивается. Концентрированная азотная кислота не действует на золото и платину. Железо, алюминий и некоторые другие металлы пассивируются концентрированной азотной кислотой, так как на их поверхности возникает плотная защитная пленка оксидов, нерастворимая в кислотах. Это свойство азотной кислоты позволяет хранить и транспортировать ее в стальных цистернах. Некоторая соль А, полученная при взаимодействии металла с неметаллом, полностью окислилась при длительном кипячении с концентрированной азотной кислотой. При этом была получена кристаллическая соль В белого цвета, слабо растворимая только в концентрированной серной кислоте.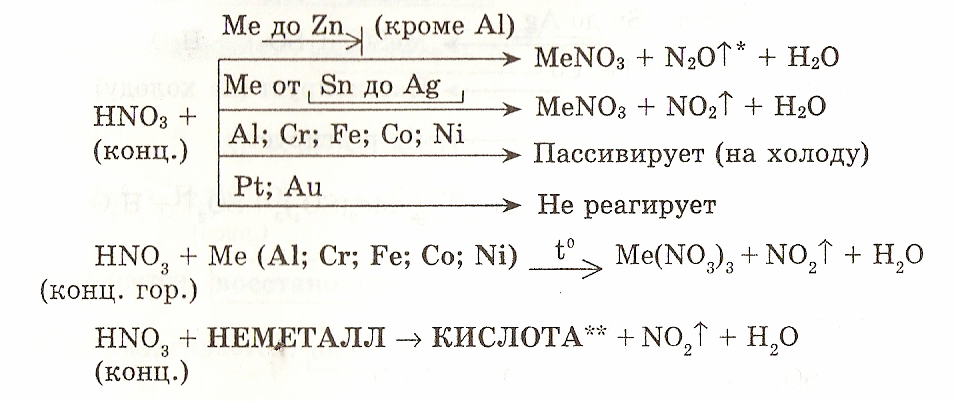 Продуктом реакции соли А с кипящей концентрированной соляной кислотой является вещество С, которое выпадает из охлажденного и достаточно разбавленного раствора в виде белых кристаллов. Каждое из трех соединений содержит металл в одной и той же степени окисления. [c.140]
Продуктом реакции соли А с кипящей концентрированной соляной кислотой является вещество С, которое выпадает из охлажденного и достаточно разбавленного раствора в виде белых кристаллов. Каждое из трех соединений содержит металл в одной и той же степени окисления. [c.140]
Азотная кислота является сильным окислителем, поэтому ее реакции с металлами значительно отличаются от реакций металлов с соляной и разбавленной серной кислотами практически никогда не наблюдается выделения водорода. Благодаря окислительным свойствам азотная кислота взаимодействует и с неметаллами.
[c.169]Приведенные схемы иллюстрируют наиболее типичные случаи взаимодействия азотной кислоты с металлами и неметаллами. Вообще же, окислительновосстановительные реакции, идуш 1е с участием HNO3, протекают сложно. [c.439]
Азотная кислота обладает сильно выраженными окислительными свойствами. Она разрушает животные и растительные ткани, окисляет почти все металлы и неметаллы.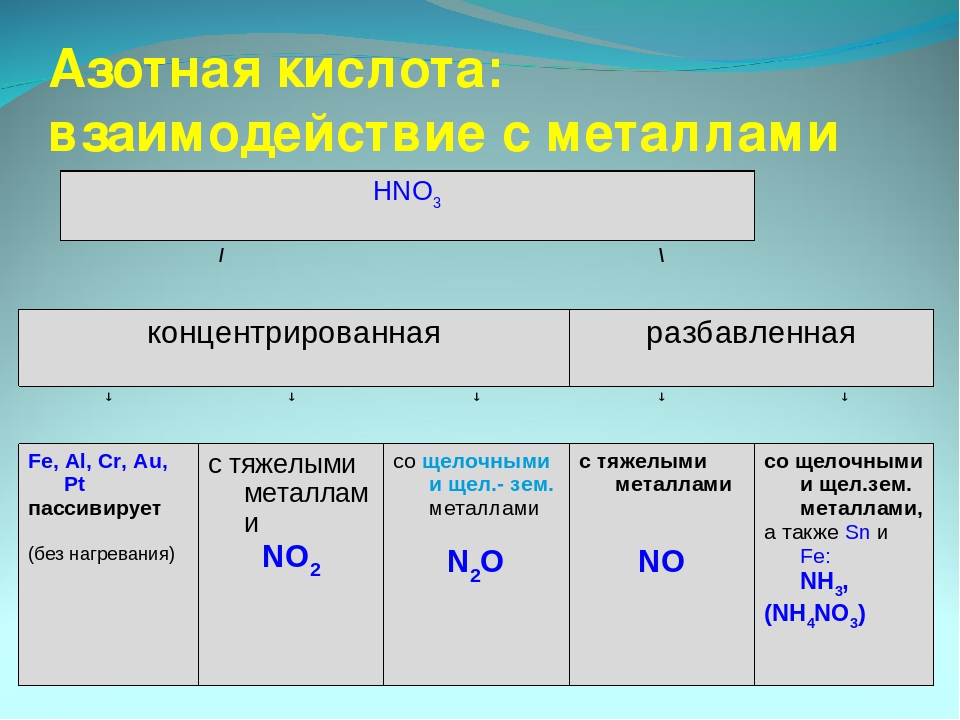 Образование тех или иных продуктов взаимодействия зависит от концентрации НЫОз, активности простого вещества и температуры (стр. 264). На рис. 183 показано влияние концентрации НЫОз на характер образующихся продуктов ее восстановления при взаимодействии с железом. Достаточно разбавленная кислота в основном восстанавливается до ЫН4ЫО3 с повышением ее концентрации становится более характерным образование ЫО концентрированная НЫОз восстанавливается до ЫОа-
Образование тех или иных продуктов взаимодействия зависит от концентрации НЫОз, активности простого вещества и температуры (стр. 264). На рис. 183 показано влияние концентрации НЫОз на характер образующихся продуктов ее восстановления при взаимодействии с железом. Достаточно разбавленная кислота в основном восстанавливается до ЫН4ЫО3 с повышением ее концентрации становится более характерным образование ЫО концентрированная НЫОз восстанавливается до ЫОа-
При обычных условиях простое вещество бор — твердое вещество ( = 2075 °С). Кристс1ллическое строение бора особенное. Оно не является характерным ни для Me uraTOB, ни для неметаллов. В нем реализуется большее число связей (>4), природа которых не является ни типично металлической, ни обычной ковалентно L Кристалл бора состоит из икосаэдров — правильных двадцати-вершинами. При обычных температурах бор весьма инертен, мпературах он становится аюгивным, взаимодействует с кисло-ми, серой, азотом, углеродом, водородом и многими металлами, нно реагирует с такими сильными окислителями, как фтор, го-фованная азотная кислота и царская водка.
Концентрированная азотная кислота взаимодействует со многими неметаллами сера окисляется ею до Н2504 при кипячении, уголь — до СО2. Тлеющая лучинка, внесенная в пары азотной кислоты, воспламеняется скипидар, влитый в концентрированную НЫОз, загорается синий раствор индиго обесцвечивается. Концентрированная НМОз не действует на золото и платину. Железо, алюминий и некоторые другие металлы пассивируются концентрированной азотной кислотой, так как на их поверхности возникает плотная защитная.пленка оксидов, нерастворимая в кислотах. Это свойство азотной,кислоты позволяет хранить и транспортировать ее в стальных цистернах. [c.322]
Азотная кислота HNO3— бесцветная жидкость с резким запахом, гигроскопична, кипит при 84 °С, хорошо растворима в воде. Разбавленная А. к. проявляет все свойства одноосновных кислот. Концентрированная (96—98 %) HNO3 красно-бурого цвета от присутствия в ней NOa-Ha свету и при нагревании HNO, разлагается на N0-2, О2 и HjO.
Алюминий получают в больших количествах из боксита АЬОз йНгО (л=1—3). Боксит очищают растворением в водном растворе NaOH и переосаждают в виде А1(0Н)з с помощью СОг. Дегидратированный продукт растворяют в расплаве криолита и проводят электролиз при 800—1000°С.
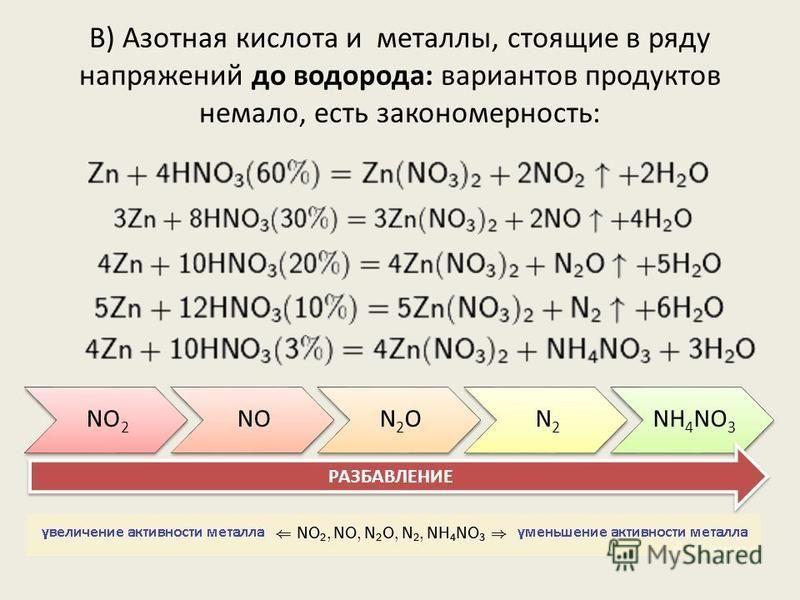 Алюминий — прочный твердый белый металл. Он очень электроположителен, но тем не менее устойчив по отношению к коррозии, так как на его поверхности образуется пр10чная плотная защитная оксидная пленка. Толстые оксидные пленки часто наносят на алюминий электролитически. Этот процесс называют анодированием. Свеженанесенные пленки можно окрасить пигментами. Алюминий растворим в разбавленных кислотах, но пассивируется концентрированной азотной кислотой. Если же разрушить защитную оксидную пленку механически или амальгамированием, то происходит энергичное взаимодействие даже с водой. Металлический алюминий легко взаимодействует с горячей водной натриевой щелочью, галогенами и различными неметаллами.
Алюминий — прочный твердый белый металл. Он очень электроположителен, но тем не менее устойчив по отношению к коррозии, так как на его поверхности образуется пр10чная плотная защитная оксидная пленка. Толстые оксидные пленки часто наносят на алюминий электролитически. Этот процесс называют анодированием. Свеженанесенные пленки можно окрасить пигментами. Алюминий растворим в разбавленных кислотах, но пассивируется концентрированной азотной кислотой. Если же разрушить защитную оксидную пленку механически или амальгамированием, то происходит энергичное взаимодействие даже с водой. Металлический алюминий легко взаимодействует с горячей водной натриевой щелочью, галогенами и различными неметаллами. Разбавленная же с металлами, стоящими в ряду напряжений после водорода, восстанавливается до N0, а расположенные до водорода превращают ее в N0, N2O, N2 или Nh5+. Чем более разбавлен раствор кислоты и активнее металл, тем глубже протекает процесс восстановления. Взаимодействуя с неметаллами (S, Р и др.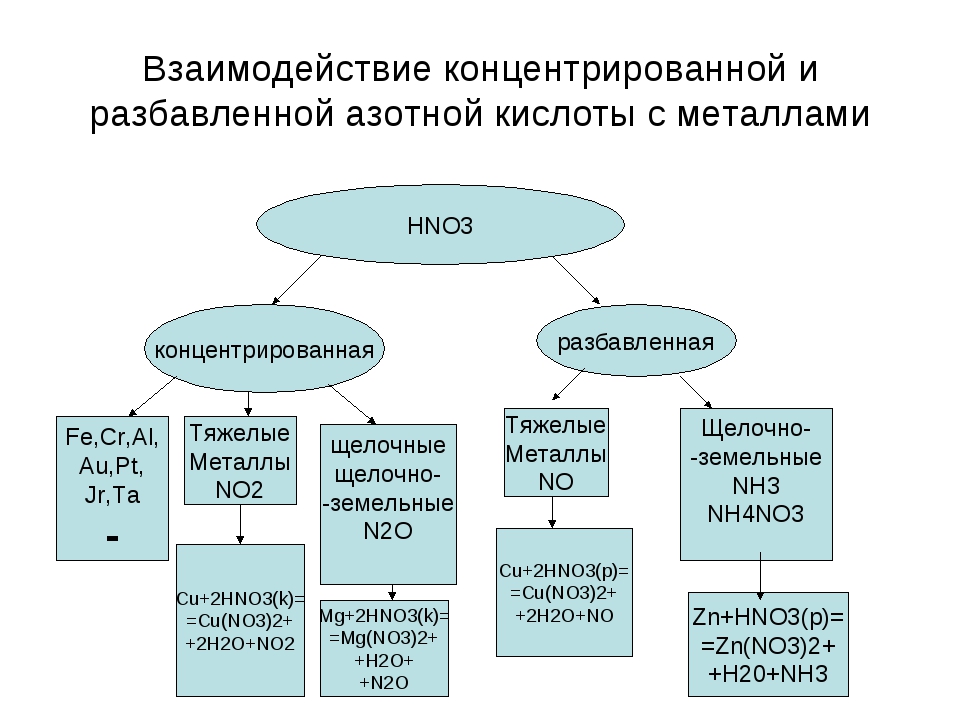 ) азотная кислота обычно восстанавливается до N0, а с переходными элементами до N0 и NO2 одновременно. С соляной кислотой HNO3 образует очень сильный окислитель — хлористый нитрозил [c.227]
) азотная кислота обычно восстанавливается до N0, а с переходными элементами до N0 и NO2 одновременно. С соляной кислотой HNO3 образует очень сильный окислитель — хлористый нитрозил [c.227]
Рассматриваемые металлы тугоплавки и высокостойки к химическим воздействиям лишь при высокой температуре, когда разрушается защитная оксидная пленка, они взаимодействуют с кислородом, углеродом, галогенами и другими неметаллами. Оксидная защитная пленка настолько устойчива, что металлы не поддаются действию кислот, ванадий окисляется лишь азотной кислотой. С водными растворами щелочей не реагируют. В расплавленных щелочах разрушается оксидная пленка, имеющая кислотный характер [c.246]
Азотная кислота обладает сильно выраженными окислительными свойствами. Она окисляет почти все металлы и неметаллы. Образование тех или иных продуктов взаимодействия зависит от концентрации HNO3 и активности простого вещества (стр. 218). HNO3 разрушает животные и растительные ткани. [c.371]
[c.371]
Висмут — типичный металл, сурьма, занимая промежуточное положение в подгруппе между Р, Аз и 81, проявляет свойства как металла, так и неметалла. Постепенная металлизация ог Р к В обусловлена ростом атомного радиуса и снижением энергии ионизации. В ряду Р— 5Ь—В1 восстановительная способность элементов увеличивается. В ряду напряжения рассматриваемые элементы стоят после водорода, поэтому они взаимодействуют только с кислотами — окислителями. Усиление металличности в ряду Р — 5Ь — Ш проявляется и в их реакциях вза-имодействия с азотной кислотой [c.172]
В чистом виде марганец — серебристо-белый, твердый, хрупкий металл, по внешности похожий на железо. На воздухе покрывается тонкой окисной пленкой, придающей металлу красноватый оттенок. Пленка предохраняет металл от окисления даже при нагревании его. Разведенные соляная и серная кислоты взаимодействуют с марганцем с выделением водорода и образованием солей двухвалентного марганца (МпС12, Мп504). Азотная и концентрированная серная кислоты, окисляя металл, дают соли, содержащие марганец различных степеней положительной валентности его. При нагревании марганец разлагает воду и реагирует со многими металлами и неметаллами. [c.530]
Азотная и концентрированная серная кислоты, окисляя металл, дают соли, содержащие марганец различных степеней положительной валентности его. При нагревании марганец разлагает воду и реагирует со многими металлами и неметаллами. [c.530]
Азотная кислота в заданиях ЕГЭ
Азотная кислота, как и серная, обладает особенными свойствами. При взаимодействии с металлами или сложными веществами в условиях реального эксперимента она может давать сложную смесь продуктов.
В рамках ЕГЭ превращения азотной кислоты в различных реакциях описываются таблицей:
При взаимодействии с неметаллами или сложными веществами концентрированной азотной кислоты в продуктах принято указывать NO2. Разбавленная азотная кислота обычно восстанавливается до NO:
S + 6HNO3 (конц.) = h3SO4 + 6NO2 + 2h3O
S + 2HNO3 (разб.) = h3SO4 + 2NO
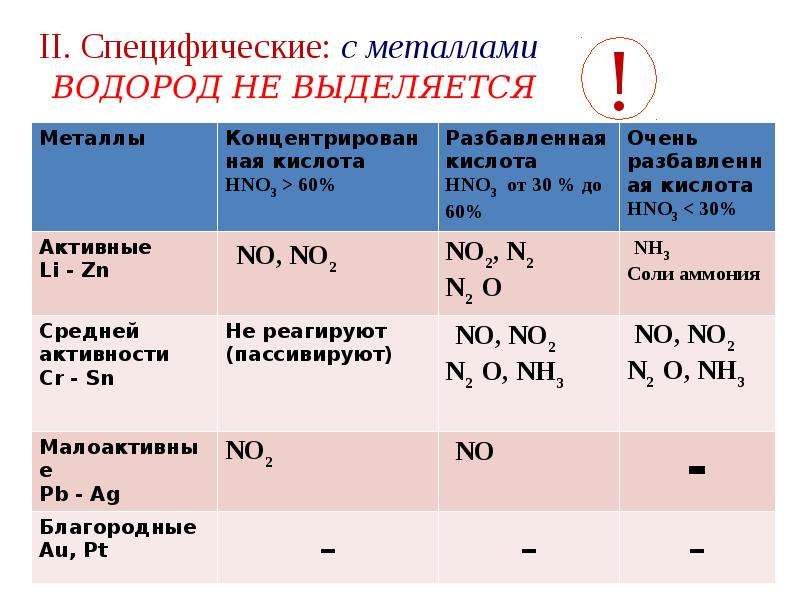
При взаимодействии азотной кислоты с металлами продукты реакции зависят от концентрации кислоты и от активности металла: чем разбавленнее кислота и активнее металл, тем ниже будет степень окисления у азота в продукте реакции.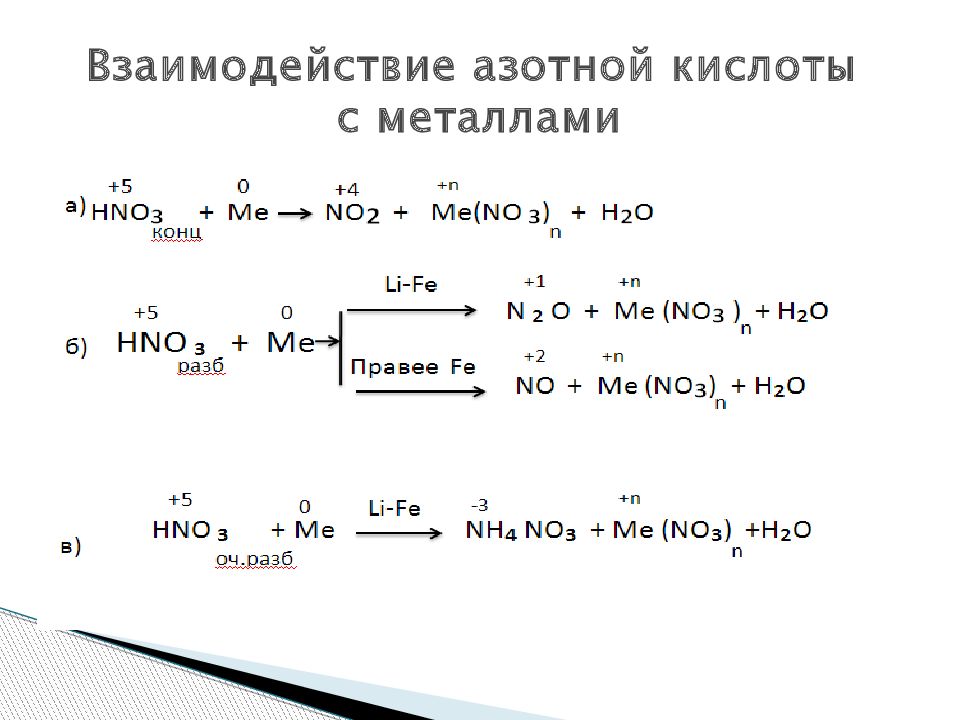 В рамках ЕГЭ условились для металлов правее железа указывать NO2 (концентрированная кислота) или NO (разбавленная кислота). Для остальных металлов выбираем любой из трех оставшихся продуктов исходя из контекста задания и общей логики. Это означает, что для, например, магния можно указать N2O, N2 или Nh5NO3, но нельзя брать NO2 или NO. При этом знать тонкости, что, допустим, 25%-ная кислота дает с кальцием азот, а 8%-ная – нитрат аммония, не нужно.
В рамках ЕГЭ условились для металлов правее железа указывать NO2 (концентрированная кислота) или NO (разбавленная кислота). Для остальных металлов выбираем любой из трех оставшихся продуктов исходя из контекста задания и общей логики. Это означает, что для, например, магния можно указать N2O, N2 или Nh5NO3, но нельзя брать NO2 или NO. При этом знать тонкости, что, допустим, 25%-ная кислота дает с кальцием азот, а 8%-ная – нитрат аммония, не нужно.
Попробуйте самостоятельно проанализировать приведенные ниже схемы реакций и объяснить выбор продуктов:
Cu + HNO3 (конц.) → Cu(NO3)2 + NO2 + h3O
Cu + HNO3 (разб.) → Cu(NO3)2 + NO + h3O
Zn + HNO3 (разб.) → Zn(NO3)2 + N2 + h3O
K + HNO3 (оч. разб.) → KNO3 + Nh5NO3 + h3O
Концентрированная азотная кислота, как и концентрированная серная, пассивирует железо, алюминий, хром и свинец. При комнатной температуре перечисленные металлы не растворяются в концентрированной азотной кислоте, но при нагревании реакция с ними возможна.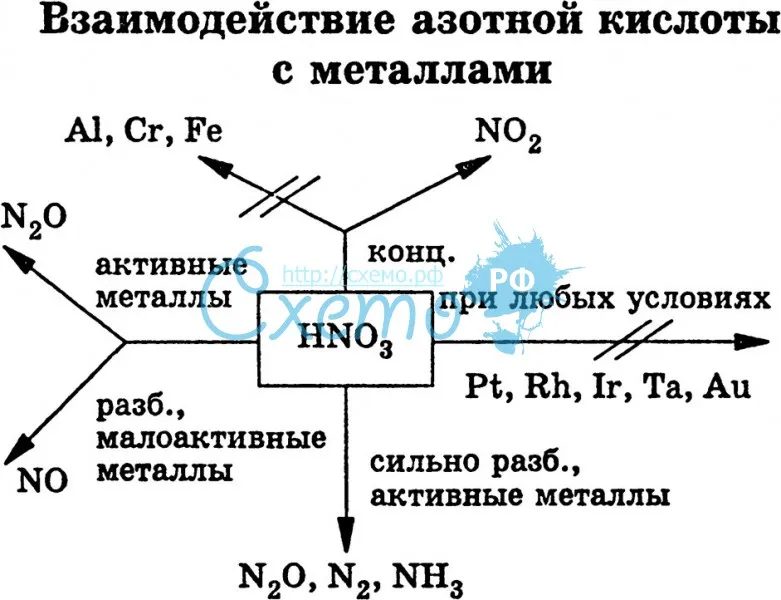
Давайте рассмотрим несколько заданий из ЕГЭ и определим, какие продукты нужно выбирать в каждом случае.
1. «Кальций растворили в азотной кислоте, при этом выделился газ, входящий в состав воздуха».
5Ca + 12HNO3 = 5Ca(NO3)2 + N2 + 6h3O
2. «…газ, полученный при действии на серебро концентрированной азотной кислоты».
Ag + 2HNO3 (конц.) = AgNO3 + NO2 + h3O
3. «К разбавленному раствору полученной кислоты (HNO3) добавили магний, в результате чего в растворе образовалось две соли, а выделения газообразных продуктов не происходило».
4Mg + 10HNO3 (разб.) = 4Mg(NO3)2 + Nh5NO3 + 3h3O
Медь стоит в ряду активности правее железа, поэтому в пункте А выбираем ответ 3, а в пункте Г – 2. Кальций относится к группе активных металлов, поэтому выбрать в пункте Б вариант 5 будет грубой ошибкой. Из азотной кислоты независимо от ее концентрации не выделяется водород, поэтому вариант 4 тоже не подходит. В пункте В протекает обычная реакция обмена, выбираем ответ 6.
Еще важно помнить, что азотная кислота «не дружит» с сульфидами, сульфитами и соединениями елеза (II). Если эти вещества встречаются в растворе, то протекает ОВР по схемам:
Это обстоятельство нужно учитывать при решении тестов и 31 заданий ЕГЭ.
В пунктах А и В вещества содержат двухзарядное железо, поэтому будет протекать окислительно-восстановительная реакция.
6. Из предложенного перечня веществ: сульфид натрия, углекислый газ, азотная кислота, хлорид железа (III), оксид кальция, выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения только одной из возможных реакций.
При выполнении этого задания может появиться желание записать реакцию вида:
Na2S + 2HNO3 = 2NaNO3 + h3S
Эта реакция имеет право на существование только при использовании очень разбавленной азотной кислоты. В противном случае между этой парой веществ будет протекать ОВР:
Na2S + 8HNO3 = Na2SO4 + 8NO2 + 4h3O
Не используйте спорные реакции, если есть альтернатива.
7. Из предложенного перечня веществ: азотная кислота, гидроксид железа (II), нитрат меди (II), карбонат кальция, хлорид лития, выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения только одной из возможных реакций.
При решении этого задания нельзя писать реакцию обмена между азотной кислотой и гидроксидом железа (II). Независимо от концентрации кислоты между ними будет протекать ОВР, например, такая:
3Fe(OH)2 + 10HNO3 = 3Fe(NO3)3 + NO + 8h3O
Учите химию, будьте бдительны и помните: на олимпиадах азотная кислота с металлами может давать водород.
Урок «Азотная кислота, состав, строение молекулы, физические и химические свойства, получение»
Тип урока: Урок передачи и приобретения новых знаний и умений.
Цели: Повторить и закрепить знания об общих химических свойствах кислот; изучить строение молекулы азотной кислоты, физические и специфические химические свойства азотной кислоты – взаимодействие ее с металлами; познакомить учащихся с промышленным и лабораторным способами получения чистой азотной кислоты.
В результате урока необходимо знать:
- Состав и строение молекулы азотной кислоты; число ковалентных связей, образуемых атомом азота и степень окисления азота в молекуле азотной кислоты.
- Общие химические свойства азотной кислоты: взаимодействие с индикаторами (лакмусом и метилоранжем), с основными и амфотерными оксидами, основаниями, с солями более слабых и более летучих кислот.
- Специфические химические свойства азотной кислоты: взаимодействие ее с металлами.
- Лабораторный и промышленный способы получения азотной кислоты.
Необходимо уметь:
- Составлять уравнения химических реакций с позиции теории электролитической диссоциации.
- Составлять уравнения реакций взаимодействия концентрированной и разбавленной кислоты с металлами с использованием метода электронного баланса.

Методы и методические приемы:
- Беседа.
- Самостоятельная работа учащихся по составлению уравнений химических реакций азотной кислоты с металлами.
- Лабораторная работа по изучению общих химических свойств азотной кислоты;
- Составление опорного конспекта.
- Творческая работа: сообщение учащегося о получении азотной кислоты.
- Демонстрация опытов: взаимодействие разбавленной и концентрированной азотной кислоты с медью.
- Демонстрация слайдов с помощью мультимедиа проектора.
- Взаимопроверка и взаимооценка результатов самостоятельной работы.
Оборудование и реактивы:
На столах учащихся: растворы азотной кислоты HNO3 (20 – 25 %), индикаторы лакмус и метилоранж, раствор гидроксида натрия NaOH, раствор сульфата меди (II) CuSO4, раствор сульфата железа (II) FeSO4, оксид меди (II) CuO, оксид алюминия Al2O3, раствор карбоната натрия Na2CO3, пробирки, пробиркодержатели.
На столе учителя: концентрированная азотная кислота HNO3 (60 – 65 %), разбавленная азотная кислота HNO3 (30 %), штатив с пробирками, медная проволока (кусочки), газоотводная трубка, кристаллизатор с водой, пробиркодержатель, мультимедийная установка (компьютер, проектор, экран).
План урока:
План урока написан на доске и отпечатан для составления опорного конспекта на столах учащихся (Приложение 1)
Ход урока:
I Повторение.
Учитель: На прошлых уроках мы изучили некоторые соединения азота. Давайте вспомним их.
Ученик: Это аммиак, соли аммония, оксиды азота.
Учитель: Какие оксиды азота являются кислотными?
Ученик: Оксид азота (III) N2O3 – азотистый ангидрид и оксид азота (V) N2O5 – азотный ангидрид, ему соответствует азотная кислота HNO3.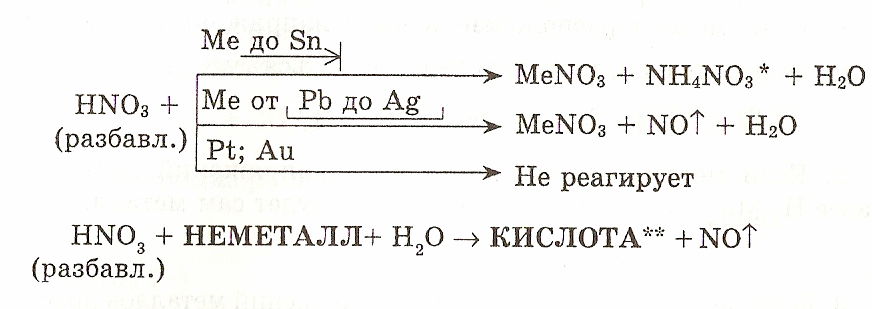
Учитель: Каков качественный и количественный состав азотной кислоты?
Учитель пишет на доске формулу азотной кислоты и просит ученика расставить степени окисления
Ученик: Молекула состоит из трех химических элементов: H, N, O – из одного атома водорода, одного атома азота и трех атомов кислорода.
II Состав и строение HNO3
Учитель: Как же образуется молекула азотной кислоты?
Учитель показывает презентацию об азотной кислоте (Приложение 2 – презентация, Приложение 3 – текст пояснения к презентации)
III Физические свойства:
Учитель: Теперь переходим к изучению физических свойств азотной кислоты.
Учащиеся составляют краткое описание физических свойств азотной кислоты.
Учитель на демонстрационном столе показывает, что представляет собой концентрированная азотная кислота HNO (60 – 65 %) — бесцветная жидкость, «дымящаяся на воздухе», с едким запахом. Концентрированная 100 % — ая HNO3 иногда окрашена в желтоватый цвет, т.к. она летучая и нестойкая, и при комнатной температуре разлагается с выделением оксида азота (IV) или «бурого» газа, именно поэтому ее хранят в бутылках из темного стекла.
Концентрированная 100 % — ая HNO3 иногда окрашена в желтоватый цвет, т.к. она летучая и нестойкая, и при комнатной температуре разлагается с выделением оксида азота (IV) или «бурого» газа, именно поэтому ее хранят в бутылках из темного стекла.
Учитель на доске пишет уравнение химической реакции разложения азотной кислоты:
Учитель: Азотная кислота гигроскопична, смешивается с водой в любых отношениях. В водных растворах – сильный электролит, при температуре – 41,6 0С затвердевает. На практике применяется 65 % азотная кислота, она не дымит, в отличие от 100 % — ой.
IV Химические свойства
Учитель: Переходим к следующему этапу урока. Азотная кислота – сильный электролит. Следовательно, ей будут присущи все общие свойства кислот. С какими веществами реагируют кислоты?
Ученик: С индикаторами, с основными и амфотерными оксидами, с основаниями, с солями более слабых и летучих кислот, с металлами.
Учитель: Перед вами общие свойства кислот.
Включается мультимедийная установка. Учитель показывает презентацию об общих химических свойствах кислот (Приложение 4).
Учитель: Проведем экспериментальный этап урока. Ваша задача – провести химические реакции, подтверждающие химические свойства кислот, на примере азотной кислоты. Работать будете группами по 4 человека. На партах лежат инструкции к лабораторным опытам (Приложение 5). В тетрадях надо составить уравнения химических реакций в молекулярном и ионном виде.
Далее учитель проверяет технику безопасности выполнения лабораторных опытов. Вызывает учеников к доске записывать уравнения реакций.
Учитель: Переходим к специфическим химическим свойствам азотной кислоты. Следует отметить, что азотная кислота, и разбавленная, и концентрированная, при взаимодействии с металлами не выделяет водород, а может выделять различные соединения азота – от аммиака до оксида азота (IV).
Включается мультимедийная установка. Учитель показывает презентацию о возможных продуктах восстановления азотной кислоты (Приложение 6).
Учитель: Посмотрим на схему. У каждого на столах лежат схемы восстановления азотной кислоты (разбавленной и концентрированной) металлами (Приложение 7).
Далее учитель демонстрирует опыты:
- Взаимодействие разбавленной азотной кислоты с медью. Собирание оксида азота (II) над водой.
- Взаимодействие концентрированной азотной кислоты с медью. Получение оксида азота (IV).
На доске записывает уравнения реакций:
Учитель: На основе опытов можно сделать выводы:
- Раствор азотной кислоты реагирует не только с металлами, стоящими в электрохимическом ряду напряжений металлов до водорода, но и с металлами, стоящими после водорода.
- В реакции с разбавленной HNO3 окислителем металлов является не ион водорода H+, а ион NO3-, у которого окислительные свойства сильнее.

- Концентрированная азотная кислота также реагирует с металлами, стоящими в электрохимическом ряду напряжений металлов правее водорода. Окислителем металлов в данном случае являются молекулы HNO3 за счет предельно окисленного атома азота .
- В окислительно-восстановительных реакциях с металлами азотная кислота выступает как сильный окислитель за счет атомов . Поэтому водород не выделяется, продуктами реакции являются соединения азота с более низкой степенью окисления, чем +5, а также соль и вода.
Учитель: Пользуясь схемами восстановления концентрированной и разбавленной азотной кислоты металлами, а также учебником на стр. 127, перейдем к самостоятельной работе по вариантам (Приложение 8). Каждый выполняет свой вариант. Вам предложены карточки – задания. Время работы 5-7 минут.
Включается мультимедийная установка. Учитель показывает правильные варианты ответов (Приложение 9). Учащиеся проверяют правильность выполнения задания.
Учащиеся проверяют правильность выполнения задания.
V Получение азотной кислоты HNO3
Ученик: (сообщение) В лаборатории азотную кислоту получают взаимодействием калийной или натриевой селитры с концентрированной серной кислотой при нагревании или без нагревания:
В промышленности азотную кислоту получают каталитическим окислением аммиака, синтезированного из азота воздуха:
Ученик показывает схему получения азотной кислоты (Приложение 10), а учащиеся записывают уравнения реакций в тетрадь.
VI Заключение
Учитель: На сегодняшнем уроке мы познакомились с составом и строением азотной кислоты. Повторили и закрепили общие свойства кислот на примере азотной кислоты, закрепили свои знания по теории ТЭД, теории строения атома и химической связи. Изучили специфические свойства азотной кислоты, а именно взаимодействие ее с металлами. Познакомились со способами получения азотной кислоты.
Познакомились со способами получения азотной кислоты.
Далее подводятся итоги, выставляются оценки. Учитель задает домашнее задание по учебнику, задачнику и конспекту.
Д/з: § 33, упр. 4 на стр. 128 учебника;
задачи: 4 – 35, 4 – 41 задачник;
выучить конспект.
Список литературы
- Кузнецова Н.Е., Титова И.М., Гара Н.Н., Жегин А.Ю. Химия: учебник для 9 класса общеобразовательных учреждений. – М.: Вентана – Граф, 2004.
- Энциклопедия для детей. Химия. – М.: Аванта, 2000.
- Максименко О.О. Химия. Пособие для поступающих в вузы. – М.: Эксмо, 2003.
- Полосин В.С., Прокопенко В.Г. Практикум по методике преподавания химии. Учебное пособие. – М.: Просвещение, 1989.
- Мартыненко Б.В. Химия: Кислоты и основания. – М.: Просвещение, 2000.
Взаимодействие азотной кислоты с металлами и неметаллами — ПОДГРУППА АЗОТА — НЕОРГАНИЧЕСКАЯ ХИМИЯ
Часть II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
НЕОРГАНИЧЕСКАЯ ХИМИЯ
Раздел 10. ПОДГРУППА АЗОТА
§ 10.8. Взаимодействие азотной кислоты с металлами и неметаллами
При взаимодействии азотной кислоты с металлами водород, как правило, не выделяется: он окисляется, образуя воду. Кислота же, в зависимости от концентрации и активности металла, может восстанавливаться до соединений:
+5 +4 +3 +2 +1 0 -С -С
HNO3-> NO2-> HNO2-> NO -> NO -> N2-> NH3 (NH4NO3).
Образуется также соль азотной кислоты. Ниже приведена схема взаимодействия азотной кислоты различной концентрации с металлами различной активности и продукты ее восстановления:
Рассмотрим, например, как будет
реагировать концентрированная и разбавленная азотная кислота с серебром.
Согласно схеме, концентрированная азотная кислота с тяжелыми металлами1 должна восстанавливаться до NO2; кроме того, будут образовываться Н2О и соль AgNO3. Запишем схему реакции:
+5 +1 +4
Ag + HNO3 (конц.) -> AgNO3 + NO2 + Н2О.
1 Определение тяжелых металлов см. § 12.2.
Коэффициенты в уравнении подбираем методом электронного баланса:
Разбавленная азотная кислота при взаимодействия с серебром (тяжелым металлом) восстанавливается до NO и образуются вода и соль АgNO3:
0 +5 +1 +2
3Аg + 4HNO3 (розв.) = 3АgNO3 + NO + 2Н2О;
Еще пример: довольно активный металл
цинк в зависимости от концентрации азотной кислоты может восстанавливать ее до оксида
азота(l)
N2O, свободного азота N2 и даже до аммиака NH3, который с избытком азотной кислоты
дает нитрат аммония Nh5NO3. В
последнем случае уравнения реакции следует записать так:
В
последнем случае уравнения реакции следует записать так:
0 +5 +2 -С
4Zn + 10HNO3 (очень розв.) = 4Zn (NO3)2+ NH4NO3+ ЗН2О;
Следует иметь в виду, что концентрированная азотная кислота при обычной температуре не взаимодействует с алюминием, хромом и железом. Она переводит их в пассивное состояние (см. § 12.7).
Азотная кислота не реагирует с Pt, Rh, lr, И, Au. Платина и золото растворяются в “царской водке» — смеси 3 объемов концентрированной соляной кислоты и 1 объема концентрированной азотной кислоты.
Азотная кислота взаимодействует с многими неметаллами, окисляя их до соответствующих кислот. Например:
0 +6
S + 2НNO3 = H2SO4 + 2NO;
0 +5
3Р + 5HNO3 + 2Н2О = 3 Н3РО4 + 5NO;
0 +3
В + 3НNО3 = Н3ВО3 + 3NO2;
0 +4
С
+ 4HNO3 =
СО2 + 2Н2О + 4NO2.
Она также взаимодействует с органическими соединениями. Нітруванням последних добывают взрывчатые вещества, органические красители, лекарства.
Химические свойства кислот
H2SO4 — серная (сульфаты)
HCl — соляная (Хлориды)
HNO3 — азотная (нитраты)
H3PO4 — фосфорная (Фосфаты)
H2SO3 -сернистая (сульфиты)
H2S -сероводород (сульфиды)
H2CO3 — угольная (карбонаты)
H2SiO3 — кремниевая (силикаты)
1. Кислоты реагируют
- с металлами, стоящими в ряду активностм левее водорода с выделением водорода (кроме азотной и концентрированной серной)
- с основными оксидами с образованием соли и воды
- с основаниями с образованием соли и воды
- с солями, образованными более слабыми кислотами с выпадением осадка или выделением газа
2. Азотная кислота реагирует со всеми металлами, кроме Au, Pt, Al, Fe, при этом водород не выделяется, а образуются различные соединения азота (NH4NO3, N2, N2O, NO, NO2) в зависимости от концентрации кислоты и активности металла.
Азотная кислота реагирует со всеми металлами, кроме Au, Pt, Al, Fe, при этом водород не выделяется, а образуются различные соединения азота (NH4NO3, N2, N2O, NO, NO2) в зависимости от концентрации кислоты и активности металла.
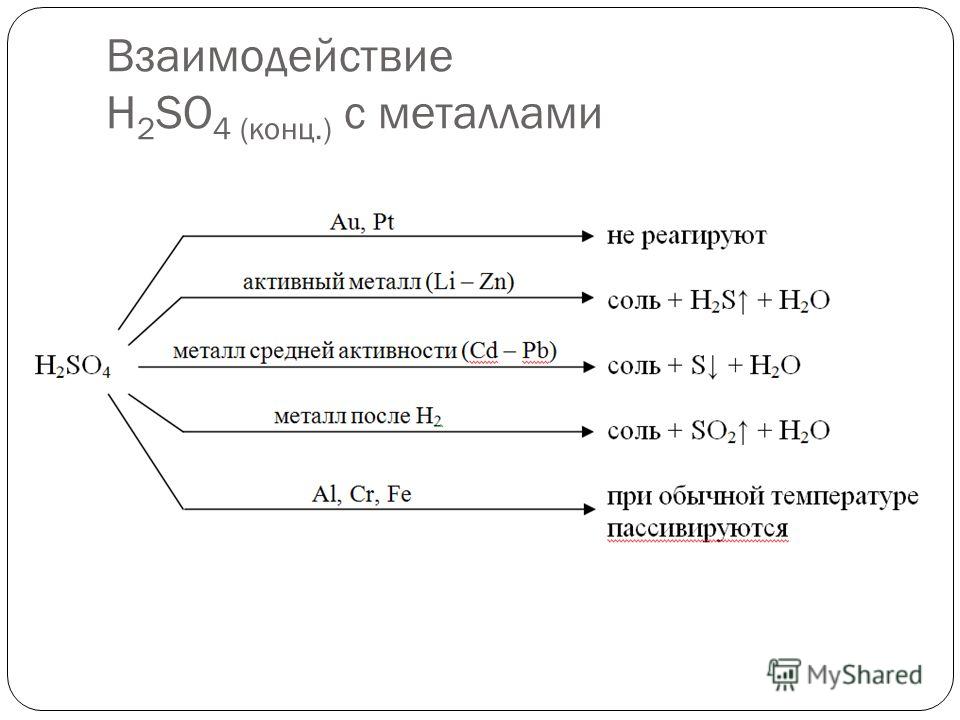
3. Концентрированная серная кислота реагирует со всеми металлами, кроме Au, Pt, Al, Fe, при этом водород не выделяется, а выделяются различные соединения серы (H2S, S, SO2) в зависимости от активности металла.
4. Вытеснительный ряд кислот (по убыванию):
H2SO4 —> HCl и HNO3 —> H3PO4 —> H2SO3 —> H2S —> H2CO3 —> H2SiO3
5. Кислоты (кроме нерастворимой в воде кремниевой кислоты) изменяют окраску индикаторов: фиолетовый лакмус в кислотах краснеет, оранжевый метилоранж становится розовым.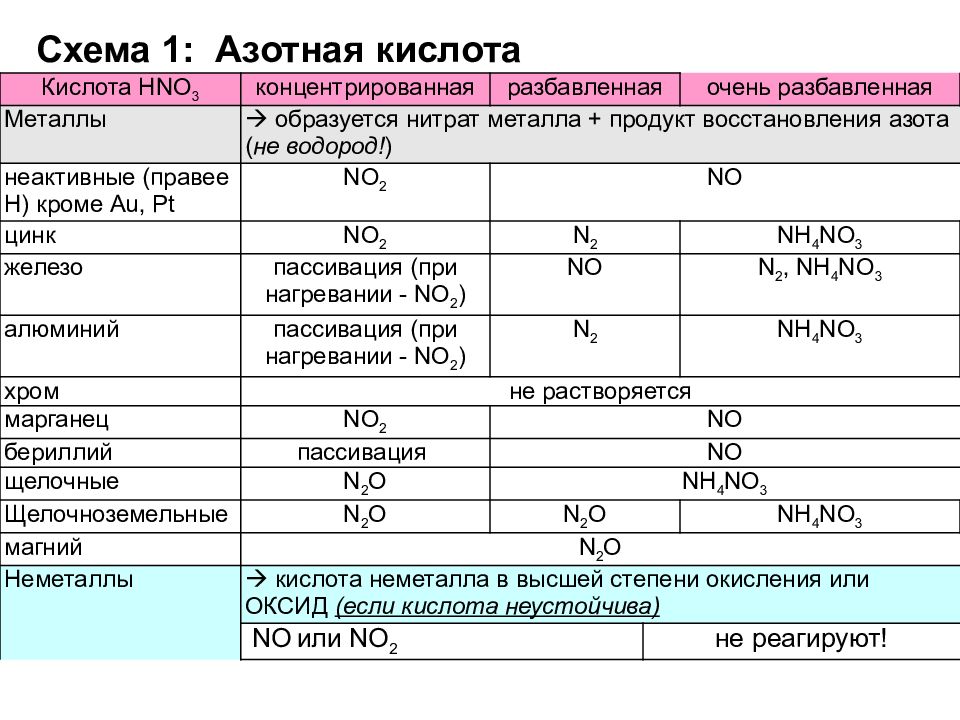
Давайте порассуждаем вместе
1. С разбавленным раствором серной кислоты реагирует
1) медь
2) оксид меди (II)
3) оксид серы (IV)
4) оксид кремния (IV)
Ответ: №2, т.к. кислоты реагируют с основными оксидами H2SO4 + CuO = CuSO4 + H2O
2. Какая из кислот реагирует и с гидроксидом бария и с хлоридом бария?
1) азотная
2) серная
3) соляная
4) угольная
Ответ: №2, т.к. выпадает нарастворимый в кислотах осадок сульфата бария
Ba(OH)2 + H2SO4 = BaSO4 + 2H2O
BaCl2 + H2SO4 = BaSO4 + 2HCl
3. Какая из перечисленных кислот реагирует с гидроксидом натрия, но не изменяет окраску лакмуса?
Какая из перечисленных кислот реагирует с гидроксидом натрия, но не изменяет окраску лакмуса?
1) серная
2) соляная
3) угольная
4) кремниевая
Ответ №4, т.к. кремниевая кислота не растворяется в воде и не изменяет окраску лакмуса
4. Какая из кислот реагирует с серебром даже в разбавленном растворе?
1) азотная
2) серная
3) фосфорная
4) соляная
Ответ: №1, т.к. азотная кислота сильный окислитель и реагирует даже с металлами, стоящими после водорода, выделяя NO
3Ag + 4HNO3 = 3AgNO3 + NO + 2H2O
5. Какое из веществ не реагирует с азотной кислотой, но реагирует с соляной кислотой с образованием белого осадка?
1) MgCO3
2) Zn
3) AgNO3
4) Cu
Ответ: №3, т.
к. AgNO3 + HCl = AgCl + HNO3 выпадает белый осадок хлорида серебра, нерастворимый в азотной кислоте.
6. Какое из веществ не реагирует с азотной кислотой, но реагирует с серной кислотой с образованием белого осадка?
1) CaCO3
2) BaCl2
3) Ag
4) Cu(NO3)2
Ответ: №2, т.к. BaCl2 + H2SO4 = BaSO4 + 2HCl выпадает белый осадок сульфата бария
7. Для серной кислоты справедливо высказывание:
1) плотность серной кислоты примерна равна 1 г/мл
2) серная кислота — легкоподвижная жидкость
3) растворение кислоты в воде — экзотермическая реакция
4) серная кислота не действует на цинк и медь
Ответ: №3, т.
к. при растворении концентрированной серной кислоты в воде выделяется большое количество тепла.
§ 27. Азотная кислота — гдз по химии для 9 класса Г.Е. Рудзитис, Ф.Г. Фельдман
Задание 1
Условие:
Решение:
Советы:
Азо́тная кислота́ — сильная одноосновная кислота. Твёрдая азотная кислота образует две кристаллические модификации с моноклинной и ромбической решётками.
Задание 2
Условие:
Решение:
Советы:
Окислители — это частицы (атомы, молекулы или ионы), которые принимают электроны в ходе химической реакции. При этом степень окисления окислителя понижается. Окислители при этом восстанавливаются. Восстановители — это частицы (атомы, молекулы или ионы), которые отдают электроны в ходе химической реакции. При этом степень окисления восстановителя повышается. Восстановители при этом окисляются.
Задание 3
Условие:
Решение:
Советы:
Основным из условий протекания ионных реакций является образование малодиссоциирующего вещества (слабого электролита), осадка или газа.Эти вещества записываются в молекулярном виде. Если выпадает осадок, то рядом с его формулой ставят стрелку, направленную вниз (↓), если образуется газ, то рядом с его формулой ставят стрелку, направленную вверх (↑).
Задание 4
Условие:
Решение:
Советы:
Азотная кислота по-разному реагирует с металлами. В этих реакциях в зависимости от концентрации кислоты и восстановительной способности металла выделяются различные оксиды азота, иногда азот и даже аммиак.
Задание 5
Условие:
Решение:
Советы:
В процессе окислительно-восстановительной реакции восстановитель отдаёт электроны, то есть окисляется; окислитель присоединяет электроны, то есть восстанавливается.
Задание 7
Условие:
Решение:
Советы:
Помни, что в неорганической химии модно найти неизвестное количество вещества по уравнение реакции.
Тест
Условие:
Решение:
Советы:
Попробуй подумать и ответить самостоятельно, основываясь на данное решение.
ICSC 0183 — АЗОТНАЯ КИСЛОТА
ICSC 0183 — АЗОТНАЯ КИСЛОТА| АЗОТНАЯ КИСЛОТА | ICSC: 0183 (Ноябрь 2016) |
| СЕЛИТРЯНОЙ СПИРТ | |
| CAS #: 7697-37-2 |
| UN #: 2031 |
| EINECS #: 231-714-2 |
| ОСОБЫЕ ОПАСНОСТИ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ТУШЕНИЕ ПОЖАРА | |
|---|---|---|---|
| ПОЖАР И ВЗРЫВ | Не горючее, но способствует возгоранию других веществ.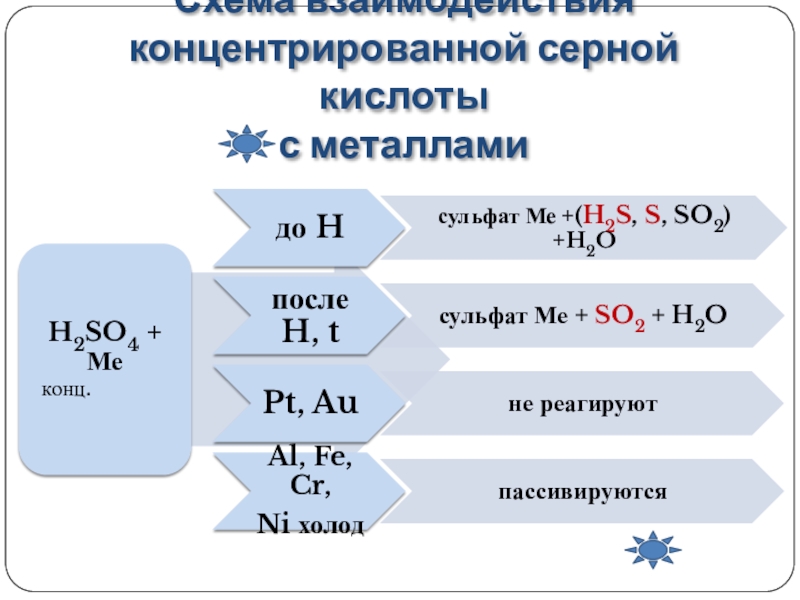 При пожаре выделяет раздражающие или токсичные пары (или газы). Риск взрыва при контакте с несовместимыми веществами. См. Химические Опасности. При пожаре выделяет раздражающие или токсичные пары (или газы). Риск взрыва при контакте с несовместимыми веществами. См. Химические Опасности. |
НЕ допускать контакта с несовместимыми материалами: См. Химические Опасности | Использовать большое количество воды, двуокись углерода. НЕ использовать порошок, пену. В случае пожара: охлаждать бочки и т.д. распыляя воду. Не допускать контакта вещества с водой. |
| ИЗБЕГАТЬ ЛЮБЫХ КОНТАКТОВ! ВО ВСЕХ СЛУЧАЯХ ОБРАТИТЬСЯ К ВРАЧУ! | |||
|---|---|---|---|
| СИМПТОМЫ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ПЕРВАЯ ПОМОЩЬ | |
| Вдыхание | Кашель. Боли в горле. Ощущения жжения. Сбивчивое дыхание. Затрудненное дыхание. | Применять вентиляцию, местную вытяжку или средства защиты органов дыхания. | Свежий воздух, покой. Полусидячее положение. Может потребоваться искусственное дыхание. Немедленно обратиться за медицинской помощью. Полусидячее положение. Может потребоваться искусственное дыхание. Немедленно обратиться за медицинской помощью. |
| Кожа | Боль. Окрашивание кожи в желтый цвет. Серьезные ожоги кожи. | Защитные перчатки. Защитная одежда. Фартук. | Надевать защитные перчатки при оказании первой помощи. Сначала промыть большим количеством воды в течение не менее 15 минут, затем удалить загрязненную одежду и снова промыть. Немедленно обратиться за медицинской помощью . |
| Глаза | Покраснение. Боль. Сильные ожоги. | Использовать маску для лица или средства защиты глаз в комбинации со средствами защиты органов дыхания.. | Промыть большим количеством воды в течение нескольких минут (снять контактные линзы, если это возможно сделать без затруднений). Немедленно обратиться за медицинской помощью. |
| Проглатывание | Ожоги в полости рта и горле. Ощущение жжения за грудиной. Боль в животе. Рвота. Шок или сильная слабость. Ощущение жжения за грудиной. Боль в животе. Рвота. Шок или сильная слабость. |
Не принимать пищу, напитки и не курить во время работы. | Прополоскать рот. Ничего не давать пить. НЕ вызывать рвоту. Обратиться за медицинской помощью. |
| ЛИКВИДАЦИЯ УТЕЧЕК | КЛАССИФИКАЦИЯ И МАРКИРОВКА |
|---|---|
| Покинуть опасную зону! Проконсультироваться со специалистом! Индивидуальная защита: костюм химической защиты, включая автономный дыхательный аппарат. НЕ засыпать древесными опилками или другими горючими абсорбентами. Вентилировать. Собрать подтекающую жидкость в герметичные контейнеры. Осторожно нейтрализовать остаток при помощи карбоната натрия. Затем смыть большим количеством воды. |
Согласно критериям СГС ООН ОПАСНО Может вызывать коррозию металловМожет усилить возгорание; окислитель Может вызвать раздражение дыхательных путей Вызывает серьезные ожоги кожи и повреждения глаз См Примечания Транспортировка |
| ХРАНЕНИЕ | |
| Отдельно от горючих веществ, восстановителей, оснований, органических химических веществ и пищевых продуктов и кормов. Прохладное место. Хранить сухим. Хранить в хорошо проветриваемом помещении. Хранить только в оригинальной упаковке. | |
| УПАКОВКА | |
| Небьющаяся упаковка. Поместить бьющуюся упаковку в небьющийся контейнер. Не перевозить с продуктами питания и кормами для животных. |
Исходная информация на английском языке подготовлена группой международных экспертов, работающих от имени МОТ и ВОЗ при финансовой поддержке Европейского Союза. |
| АЗОТНАЯ КИСЛОТА | ICSC: 0183 |
| ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА | |
|---|---|
|
Агрегатное Состояние; Внешний Вид
Физические опасности
Химические опасности
|
Формула: HNO3 |
| ВОЗДЕЙСТВИЕ НА ОРГАНИЗМ И ЭФФЕКТЫ ОТ ВОЗДЕЙСТВИЯ | |
|---|---|
|
Пути воздействия
Эффекты от кратковременного воздействия
|
Риск вдыхания
Эффекты от длительного или повторяющегося воздействия
|
| Предельно-допустимые концентрации |
|---|
|
TLV: 2 ppm как TWA; 4 ppm как STEL. EU-OEL: 2.6 mg/m3, 1 ppm как STEL |
| ОКРУЖАЮЩАЯ СРЕДА |
|---|
| ПРИМЕЧАНИЯ |
|---|
Симптомы отека легких часто не проявляются, пока не пройдет несколько часов, и они усугубляются физическими усилиями.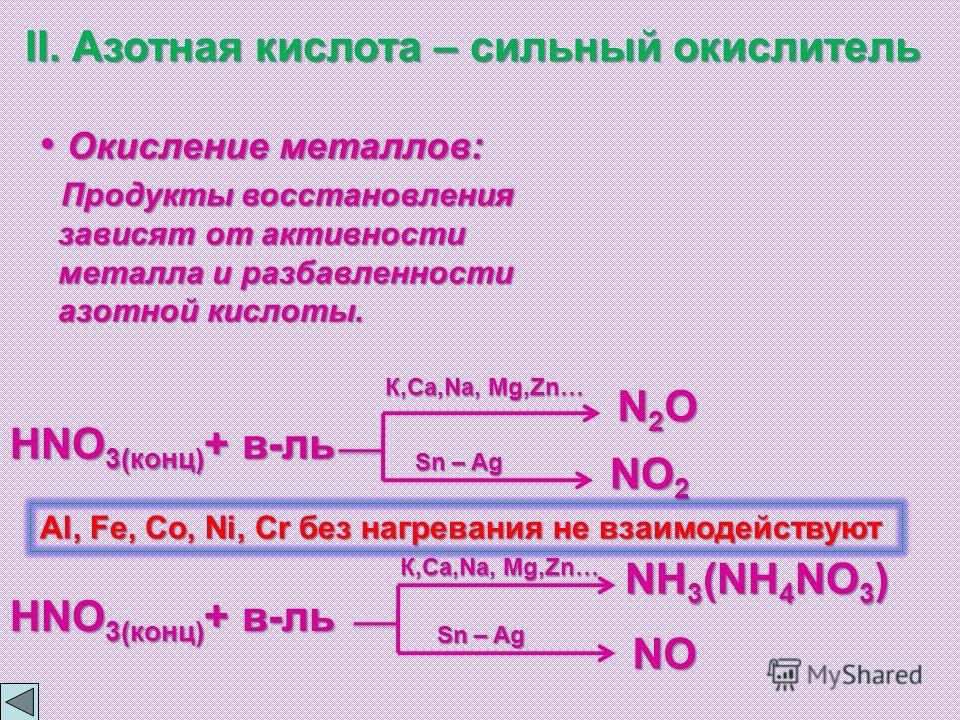 Поэтому крайне важны отдых и медицинское наблюдение. Поэтому крайне важны отдых и медицинское наблюдение.IARC considers mists of strong inorganic acid to be carcinogenic (group 1). However there is no information available on the carcinogenicity of other physical forms of this substance. Therefore no classification for carcinogenicity under GHS has been applied. NEVER pour water into this substance; when dissolving or diluting always add it slowly to the water. При превышении предельной допустимой концентрации запах не является достаточным предупреждающим признаком. Промойте загрязненную одежду большим количеством воды ввиду опасности возгорания |
| ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ |
|---|
|
Классификация ЕС Символ: O, C; R: 8-35; S: (1/2)-23-26-36-45; Примечание: B |
| (ru) | Ни МОТ, ни ВОЗ, ни Европейский Союз не несут ответственности за качество и точность перевода или за возможное использование данной информации. © Версия на русском языке, 2018 |
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.

- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только та информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.

- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только та информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.

- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только та информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.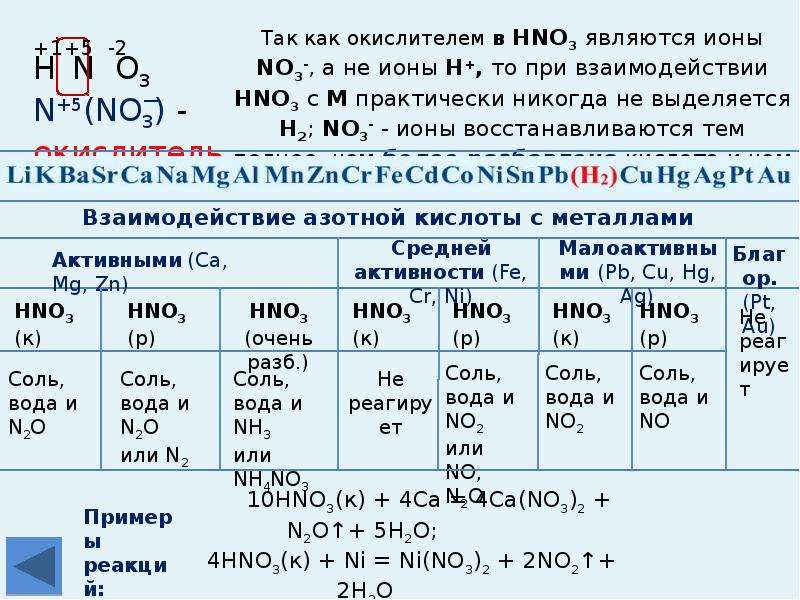 Например, сайт
не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к
остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Например, сайт
не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к
остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались.
 Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie. - Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только та информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.
Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.

Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только та информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт
не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к
остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом.
 Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере. - Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только та информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.

- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только та информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
.


 к. AgNO3 + HCl = AgCl + HNO3 выпадает белый осадок хлорида серебра, нерастворимый в азотной кислоте.
к. AgNO3 + HCl = AgCl + HNO3 выпадает белый осадок хлорида серебра, нерастворимый в азотной кислоте. к. при растворении концентрированной серной кислоты в воде выделяется большое количество тепла.
к. при растворении концентрированной серной кислоты в воде выделяется большое количество тепла.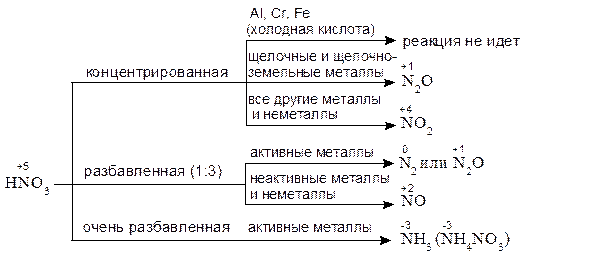 Эти вещества записываются в молекулярном виде. Если выпадает осадок, то рядом с его формулой ставят стрелку, направленную вниз (↓), если образуется газ, то рядом с его формулой ставят стрелку, направленную вверх (↑).
Эти вещества записываются в молекулярном виде. Если выпадает осадок, то рядом с его формулой ставят стрелку, направленную вниз (↓), если образуется газ, то рядом с его формулой ставят стрелку, направленную вверх (↑).
 1; Группа упаковки по ООН: I
1; Группа упаковки по ООН: I

 2
2 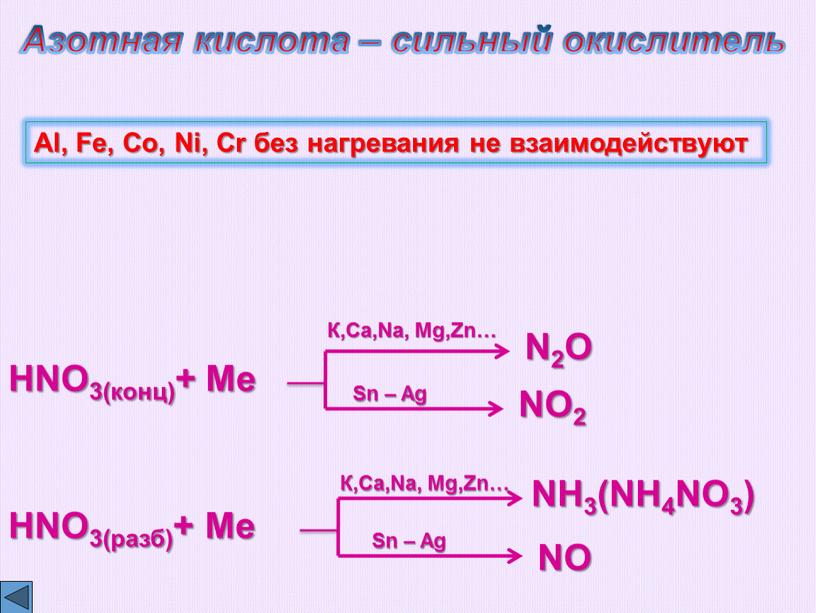


 Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
 Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.