Фторид калия — это… Что такое Фторид калия?
Фтори́д калия, фтористый калий — KF, калиевая соль плавиковой кислоты.
Распространение в природе
Фторид калия встречается в природе в виде редкого минерала кароббиитa.
Физико-химические свойства
Термодинамические параметры
| Свойство | Значение[1] |
|---|---|
| Энтальпия образования (298К, в твёрдой фазе) | -567,4 кДж/моль |
| Энтропия образования (298К, в твёрдой фазе) | 66,6 Дж/(моль·К) |
| Энтальпия плавления | 28,5 кДж/моль |
| Энтальпия кипения | 172,8 кДж/моль |
| Теплоёмкость (298К, в твёрдой фазе) | 49,32 Дж/(моль·К) |
Растворимость
- Дипольный момент молекулы фторида калия равен 7,33 Дб.
- Молярная электропроводность при бесконечном разведении при 25 °C равна 128,9 Cм·см2/моль.
- Проявляет диамагнитные свойства.

Методы получения
- Простым лабораторным методом получения фторида калия является растворение KOH или K2SO3 в плавиковой кислоте HF.
- В природе фторид калия встречается редко, и поэтому для промышленного получения KF часто используют природный минерал флюорит (CaF2), который спекают с поташом (K2CO3), затем выщелачивают, и после выпаривания воды получают достаточно чистый фторид калия.[3]
Химические свойства
- Типичная соль. В водном растворе подвергается диссоциации:
- KF ↔ K+ + F−.
Применение
- Применяется при изготовлении кислотоупорных замазок и специальных стёкол.
- В металлургии в качестве флюса.
- Как реагент при фторировании органических соединений.
- Для получения фторсдержацих соединений калия.
- Кислые соли — гидрофториды, легкоплавкие кристаллические вещества, используемые как электролиты при получении элементарного фтора.

Токсичность
Смертельная доза фторида калия для крыс (LD50), полученная орально составляет 245 мг/кг массы тела[4]
Примечания
- ↑ Рабинович В.А., Хавин З.Я. «Краткий химический справочник» Л.: Химия, 1977
- ↑ Фторид калия на Портале Естественных Наук
- ↑ Наука в Сибири (газета Сибирского отделения РАН)
- ↑ Свойства KF на ChemicalLand21 англ.
Фтористый калий — это… Что такое Фтористый калий?
- Фтористый калий
Фторид калия, фтористый калий — KF, калиевая соль плавиковой кислоты.
Распространение в природе
Фторид калия встречается в природе в виде редкого минерала кароббиитa.
Физико-химические свойства
Термодинамические параметры
Свойство Значение[1] Энтальпия образования (298К, в твёрдой фазе) -567,4 кДж/моль Энтропия образования (298К, в твёрдой фазе) 66,6 Дж/(моль·К) Энтальпия плавления 28,5 кДж/моль Энтальпия кипения 172,8 кДж/моль Теплоёмкость (298К, в твёрдой фазе) 49,32 Дж/(моль·К) Растворимость
Раствориетль Характеристика (г/100 мл) Вода (0°С) 44,7 Вода (10°С) 53,5 Вода (20°С) 94,9 Вода (30°С) 108 Вода (60°С) 142 Вода (90°С) 150 Этанол Мало растворим - Дипольный момент молекулы фторида калия равен 7,33 Дб.

- Молярная электропроводность при бесконечном разведении при 25°С равна 128,9 Cм·см2/моль.
- Проявляет диамагные свойства.[2]
Методы получения
- Простым лабораторным методом получения фторида калия является растворение KOH или K2SO3 в плавиковой кислоте HF.
- В природе фторид калия встречается редко, и поэтому для промышленного получения KF часто используют природный минерал флюорит (CaF2), который спекают с поташом (K2CO3), затем выщелачивают, и после выпаривания воды получают достаточно чистый фторид калия.[3]
Химичесекие свойства
- Типичная соль. В водном растворе подвергается диссоциации:
- KF ↔ K+ + F—.
Применение
- Применяется при изготовлении кислотоупорных замазок и специальных стёкол.
- В металлургии в качестве флюса.
- Как реагент при фторировании органических соединений.

- Для получения фторсдержацих соединений калия.
- Кислые соли — гидрофториды, легкоплавкие кристаллические вещества, используемые как электролиты при получении элементарного фтора.
Токсичность
фторида калия для крыс (LD50), полученная орально составляет 245 мг/кг массы тела[4]
Примечания
- ↑ Рабинович В.А., Хавин З.Я. «Краткий химический справочник» Л.: Химия, 1977
- ↑ Фторид калия на Портале Естественных Наук
- ↑ Наука в Сибири (газета Сибирского отделения РАН)
- ↑ Свойства KF на ChemicalLand21 англ.
- Дипольный момент молекулы фторида калия равен 7,33 Дб.
Wikimedia Foundation. 2010.
- Фтористый литий
- Фтороводородная кислота
Полезное
Смотреть что такое «Фтористый калий» в других словарях:
фтористый калий
— фторид калия … Cловарь химических синонимов Iкалий фтористый — kalio fluoridas statusas T sritis chemija formulė KF atitikmenys: angl.
 potassium fluoride rus. калий фтористый; калия фторид … Chemijos terminų aiškinamasis žodynas
potassium fluoride rus. калий фтористый; калия фторид … Chemijos terminų aiškinamasis žodynasКалий — (нем. Kalium, франц. и англ. Potassium) один из важнейших представителей группы щелочных металлов. Едкое кали есть типичная щелочь, подобная едкому натру, как кислоты серная, азотная, соляная суть типичные кислоты, почему соединения этого металла … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
фторид калия — фтористый калий … Cловарь химических синонимов I
Калия фторид — фтористый калий, KF, соль; бесцветные прозрачные кристаллы, расплывающиеся на воздухе, плотность 2,505 г/см3, tпл 857 °С. Растворимость 92,3 г в 100 г h3O при 18 °С. Получают растворением KOH или K2SO3 в плавиковой кислоте HF; применяется … Большая советская энциклопедия
Фтор — (хим. обозначение F, частица F2, атомный вес 19,05). Ф. химический элемент, составляющий вместе с хлором, бромом и йодом одну особую характерную группу тел, так называемую группу галоидов.
 Свое название Ф. получил от греческого слова φτοριος… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Свое название Ф. получил от греческого слова φτοριος… … Энциклопедический словарь Ф.А. Брокгауза и И.А. ЕфронаНиобий — (Niobium франц. и англ., Niob нем.; хим.), Nb = 94. В V группе периодической системы элементов имеются два редких металла, H. и тантал, которые относятся к ванадию подобно тому, как молибден и вольфрам к хрому; последние три металла члены… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Фторид калия — Общие … Википедия
Калия фторид — Фторид калия Общие Систематическое наименование Фторид калия Химическая формула KF Отн. молек. масса 58 а. е. м. Молярная … Википедия
Гидрофторид калия — Общие Систематическое наименование Гидрофторид калия Традиционные названия Фтористый калий, кислый Химическая формула KHF2 Физические свойства … Википедия
Задание 5
Задание 5.1
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит:
к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.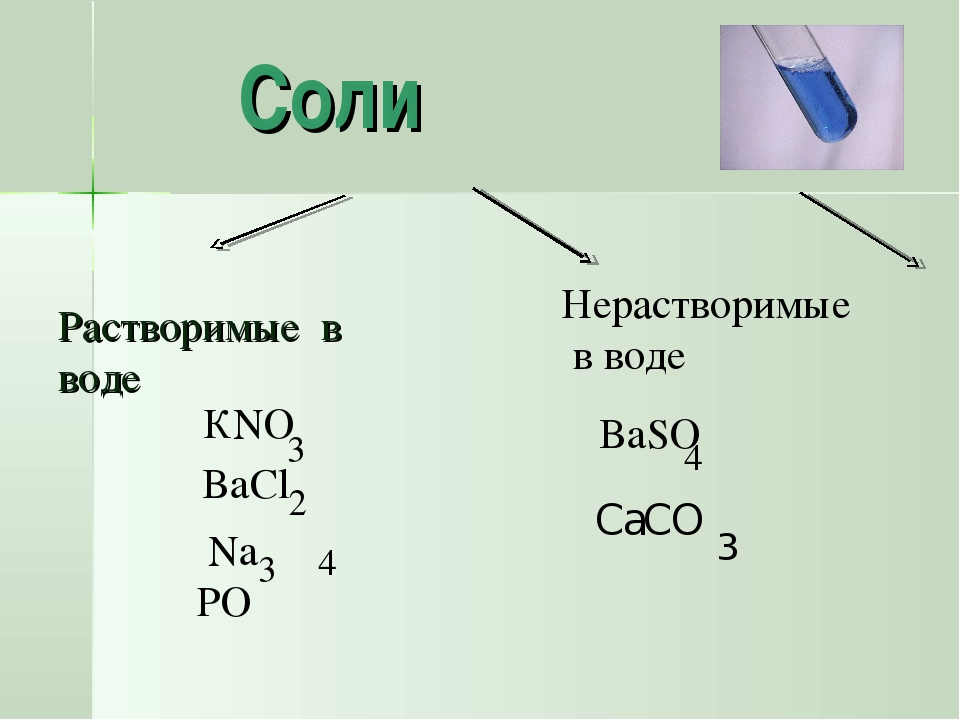
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) NH4HCO3 Б) KF В) NO |
1) соли средние 2) оксиды кислотные 3) оксиды несолеобразующие 4) соли кислые |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Источник — Демонстрационный вариант КИМ ЕГЭ по химии 2019 года
Решение
NH4HCO3 относится к кислым солям, для которых характерно содержание катионов водорода, способных в ходе обменных реакций замещаться другими катионами.
KF относится к средним солям, которые характеризуются отсутствием ионов водорода и гидроксид-ионов, способных к ионному обмену.
NO является несолеобразующим оксидом, который не проявляет кислотных или основных свойств.
Ответ: 413
Задание 5.2
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит:
к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) Fe(OH)NO3 Б) K2HPO4 В) HCOONH4 |
1) соли кислые 2) соли средние 3) соли основные 4) гидроксиды |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Fe(OH)NO3 относится к основным солям, для которых характерно присутствие гидроксильных групп, способных замещаться на анионы в ходе обменных реакций.
K2HPO4 относится к кислым солям, для которых характерно содержание катионов водорода, способных в ходе обменных реакций замещаться другими катионами.
HC(O)ONH4 (формиат аммония, аммонийная соль муравьиной кислоты) относится к средним солям, которые характеризуются отсутствием ионов водорода и гидроксид-ионов, способных к ионному обмену.
Ответ: 312
Задание 5.
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) P2O3 Б) SnO В) Mn2O7 |
1) оксиды основные 2) оксиды кислотные 3) оксиды несолеобразующие 4) оксиды амфотерные |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
P2O3 относится к кислотным оксидам (оксиды, гидраты которых являются кислотами).
SnO относится к амфотерным оксидам, которые проявляют как основные, так и кислотные свойства.
Mn2O7 относится к кислотным оксидам (оксиды, гидраты которых являются кислотами).
Ответ: 242
Задание 5. 4
4
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) Cr(OH)3 Б) KOH В) H2S |
1) сильная кислота 2) слабая кислота 3) амфотерный гидроксид 4) щелочь |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Cr(OH)3 является амфотерным гидроксидом, проявляющим как основные, так и кислотные свойства.
KOH является щелочью (растворимые основания).
H2S является слабой кислотой.
Ответ: 342
Задание 5.5
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит:
к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) HCN Б) H2SO4 В) CH3COONa |
1) сильная кислота 2) средняя соль 3) кислая соль 4) слабая кислота |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
HCN является слабой кислотой.
H2SO4 является сильной кислотой.
CH3COONa относится к средним солям, которые характеризуются отсутствием ионов водорода и гидроксид-ионов, способных к ионному обмену.
Ответ: 412
Задание 5.6
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) SO2 Б) BaO В) Cr2O3 |
1) оксиды основные 2) оксиды кислотные 3) оксиды несолеобразующие 4) оксиды амфотерные |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
SO2 относится к кислотным оксидам (оксиды, гидраты которых являются кислотами).
BaO относится к основным оксидам (оксиды, гидраты которых являются основаниями).
Cr2O3 относится к амфотерным оксидам, которые проявляют как основные, так и кислотные свойства.
Ответ: 214
Задание 5.7
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) N2O Б) BeO В) SiO2 |
1) оксиды несолеобразующие 2) оксиды кислотные 3) оксиды основные 4) оксиды амфотерные |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Источник — Открытый банк заданий ЕГЭ
Решение
N2O является несолеобразующим оксидом, который не проявляет кислотных или основных свойств.
BeO является амфотерным оксидом, который проявляет как основные, так и кислотные свойства.
SiO2 относится к кислотным оксидам (оксиды, гидраты которых являются кислотами).
Ответ: 142
Задание 5.8
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) гидроксид хрома (II) Б) гидроксид хрома (III) В) гидроксид хрома (VI) |
1) основания 2) основные оксиды 3) амфотерные гидроксиды 4) кислоты |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Источник — Открытый банк заданий ЕГЭ
Решение
Гидроксид хрома (II) Cr(OH)2 относится к основаниям.
Гидроксид хрома (III) Cr(OH)3 является амфотерным гидроксидом, проявляющим как основные, так и кислотные свойства.
Гидроксид хрома (VI) (хромовая кислота H2CrO4, дихромовая кислота H2Cr2O7) относится к кислотам.
Ответ: 134
Задание 5.9
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) NO Б) FeO В) ZnO |
1) оксиды несолеобразующие 2) оксиды кислотные 3) оксиды основные 4) оксиды амфотерные |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Источник — Открытый банк заданий ЕГЭ
Решение
NO является несолеобразующим оксидом, который не проявляет кислотных или основных свойств.
FeO относится к основным оксидам (оксиды, гидраты которых являются основаниями).
ZnO является амфотерным оксидом, который проявляет как основные, так и кислотные свойства.
Ответ: 134
Задание 5.10
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) NO2 Б) Na2O В) SiO2 |
1) оксиды амфотерные 2) оксиды кислотные 3) оксиды основные 4) оксиды несолеобразующие |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Источник — Открытый банк заданий ЕГЭ
Решение
NO2 относится к кислотным оксидам (оксиды, гидраты которых являются кислотами).
Na2O является основным оксидом (оксиды, гидраты которых являются основаниями).
SiO2 относится к кислотным оксидам (оксиды, гидраты которых являются кислотами).
Ответ: 232
Задание 5.11
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) Ca(OH)2 Б) Na2HPO4 В) Mg(OH)Cl |
1) соли средние 2) соли кислые 3) соли основные 4) гидроксиды |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ca(OH)2 является гидроксидом.
Na2HPO4 относится к кислым солям, для которых характерно содержание катионов водорода, способных в ходе обменных реакций замещаться другими катионами.
Mg(OH)Cl относится к основным солям, для которых характерно присутствие гидроксильных групп, способных замещаться
на анионы в ходе обменных реакций.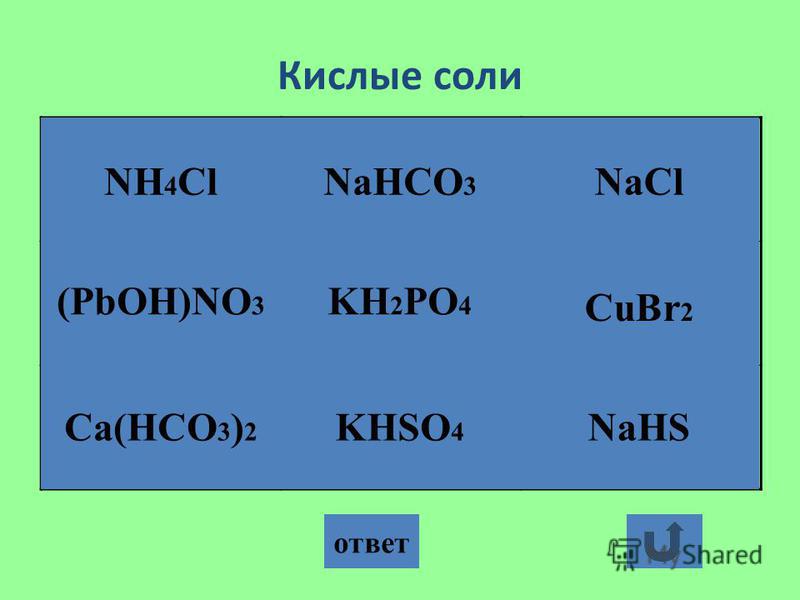
Ответ: 423
История: Наука и техника: Lenta.ru
Почти все знания современных людей о пиратах почерпнуты из фильмов с Джонни Деппом и «Острова сокровищ» — сабли, ром, деревянная нога, серьга в ухе. Реальная жизнь Карибского моря в золотом для пиратства XVII веке задокументирована крайне скупо и только сейчас начинает открываться историкам, в частности археологам. Именно они 15 лет копали остров Ла-Тортуга (не пиратский рай у побережья Гаити, а менее известный венесуэльский) и выяснили, как там жили, ели и пили, добывали соль, строили форты и сражались индейцы, испанцы и голландцы. О своих открытиях они рассказали на страницах журнала Post-Medieval Archaeology.
Карибская геополитика
Ла-Тортуга — это второй по величине венесуэльский остров (примерно 24 на 10 километров). Покрытый кустарником, лишенный пресной воды, он долгое время оставался пустынным (даже млекопитающим не удалось там зацепиться). Все изменила европейская политика: в 1597 году Испания закрыла восставшим против ее короля Нидерландам доступ к морской соли португальских портов — а без нее останавливалась приносившая огромные прибыли торговля соленой селедкой с балтийскими странами. Голландцы решили послать конвои (грузовые суда под эскортом военных) к солончакам Новой Андалусии, но уже в 1605 году португальский флот сжег и захватил все корабли северных «нарушителей».
Голландцы решили послать конвои (грузовые суда под эскортом военных) к солончакам Новой Андалусии, но уже в 1605 году португальский флот сжег и захватил все корабли северных «нарушителей».
На пустынный островок голландцы обратили внимание случайно. В XVII веке, отняв на несколько десятилетий у португальцев северо-восток Бразилии (с сахарными плантациями), они использовали соляные транспортники (zoutvaerders) для переброски в Новый Свет солдат и военных грузов. Чтобы суда не возвращались пустыми, их капитанам приказывали загрузиться солью на островах Бонэйр и Кюрасао — и на том же пути моряки обратили внимание на солончаки Тортуги. К счастью для них, испанский военный инженер Хуан Баутиста Антонелли, обследовавший остров, счел запасы там несущественными — и испанцы не стали посылать туда десант, как на другие острова у карибского берега континента. Это дало Нидерландам шанс закрепиться и начать тихо-мирно добывать соль.
Исследовавшие пространство Ла-Тортуги ученые описывают его как совокупность ландшафтов (scapes) — сложного единства повседневных практик, предметов и природных условий, составляющих исторически уникальную среду острова. Всего археологи выделили три таких «скейпа»: ландшафт бухты, солончака и битвы.
Всего археологи выделили три таких «скейпа»: ландшафт бухты, солончака и битвы.
Солнце, соль и песок
Встреча голландца XVII века с Ла-Тортугой начиналась на море, когда ему открывалась полоска берега — бурная растительность, белые песчаные пляжи и вода цвета бирюзы. Однако опытные моряки знали, что это мираж: росли на берегу лишь бесплодные мангровые заросли, обиталище комаров и гнуса, а прибрежные воды кишели скатами, муренами и жгучими кораллами. Бухта Пунта Салинас была крайне неудобной для кораблей — мало где моряки могли безопасно бросить якорь. В настоящее время о транспортах с солью свидетельствует балласт (камни, черепица, кирпичи) — их выбрасывали на дно, чтобы освободить место для груза.
Ла-Тортуга, вид с воздуха
Фото: José Miguel Pérez Gómez / academia.edu
Участники экспедиции делили свое время между кораблями, берегом и солончаком. Ялики сновали между флейтами и деревянной пристанью, перевозя людей, лопаты, тачки и пушки. Следы пристани из прочного дерева, укрепленной фашинами и песком, до сих пор видны на аэрофотоснимках бухты. Команды флейтов (за исключением капитанов и солдат) проводили весь день на солончаках, под палящим солнцем и атаками насекомых — и сами корабли, на которых они собирались, чтобы ужинать (голландской провизией) и курить трубки, напоминали им о доме.
Команды флейтов (за исключением капитанов и солдат) проводили весь день на солончаках, под палящим солнцем и атаками насекомых — и сами корабли, на которых они собирались, чтобы ужинать (голландской провизией) и курить трубки, напоминали им о доме.
Форт на Ла-Тортуге (реконструкция археологов)
Изображение: Julijan Vermeer & Konrad A. Antczak / academia.edu
А с утра моряки отправлялись вглубь острова. На них накидывались насекомые, белый песок слепил глаза. Скоро запах гнилых мангровых зарослей сигнализировал о близости соляных болот. Каждую весну, к концу сухого сезона, вода испарялась из лагун, и там кристаллизировались бело-розовые слои соли. Когда их снимали, пересыпали в мешки и грузили на корабли, лагуну приходилось «перезаряжать» вручную: голландцы несколько дней подряд носили туда морскую воду. Работать в таких условиях можно было только в ночные часы, но и тогда добыча соли загоняла десятки европейцев в могилу. Чтобы набить трюмы семи флейтов, потребовалось 28 344 тачки соли и два с половиной месяца, по свидетельству испанского моряка. За 1630-е годы, несмотря на периодические набеги кастильцев, голландцы установили между пристанью и лагуной мощный помост из сосновых досок, а на смену ведрам пришли ручные насосы. Наконец, они не поленились соорудить сложную систему каналов, дамб и площадок для высушивания соли, существенно расширив площадь промыслов.
За 1630-е годы, несмотря на периодические набеги кастильцев, голландцы установили между пристанью и лагуной мощный помост из сосновых досок, а на смену ведрам пришли ручные насосы. Наконец, они не поленились соорудить сложную систему каналов, дамб и площадок для высушивания соли, существенно расширив площадь промыслов.
Засады и диверсии
Но тут инженер Антонелли, прознавший о нидерландских промыслах под самым носом испанцев, решил действовать умнее. Пользуясь отсутствием голландцев зимой, он пригнал сто индейцев куманагото и 50 солдат с лопатами. Они прорыли два канала от соляного болота к морю, и в итоге лагуну заполнили бурные воды. Антонелли верно рассчитал, что силы прилива и отлива не дадут каналам закрыться. Даже если голландцы засыплют каналы, на откачку воды и уборку ила со дна лагуны потребуется как минимум несколько лет. Но даже в этом случае инженер приказал держать наготове шесть пирог с 50 индейцами и 20 испанцами — эта мобильная группа сможет снова открыть каналы за пару дней.
Трудолюбивые нидерландские торговцы не отчаялись и попытались обратить учиненные их врагами разрушения себе на пользу. Соединенную с морем лагуну они превратили в огромный резервуар соленой воды, которую наливали в ранее бесполезные окрестные пруды. Впрочем, последнее слово осталось за испанцами — разрушать всегда было легче, чем строить. Солдаты губернатора Новой Андалусии прокопали еще один канал и затопили все соляные болота.
Нападение испанцев и индейцев на голландский форт. Рисунок Хуана Баутиста Антонелли
Фото: academia.edu
Хотя основное время пребывания на острове занимала рутина (полив, выкапывание и перевозка соли), больше всего следов в археологической летописи Ла-Тортуги оставили битвы голландцев с испанцами, которые пытались заблокировать своим врагам доступ к промыслам. После первой, неудачной для них стычки в 1630 году, нидерландские моряки построили земляной бастион на берегу, и поставили туда три пушки: одна смотрела на корабли, другая — на соляное болото, третья — в сторону холма, откуда ранее атаковал испанский десант. Но в 1633 году новый губернатор Ариас Монтано вновь успешно атаковал, отбив у голландцев один флейт.
Но в 1633 году новый губернатор Ариас Монтано вновь успешно атаковал, отбив у голландцев один флейт.
После нескольких спокойных сезонов (моряки даже успели ликвидировать последствия разрушений), в 1638 году, испанцы подготовили новый десант. 13 пирог с испанскими мушкетерами и индейскими лучниками незаметно доплыли до западной части острова. Однако затем их увидели с разведывательного шлюпа голландцев. Увы, последние захотели узнать больше о врагах и выслали в их сторону еще три шлюпа. Испанцам удалось захватить один из них и выведать данные о численности и дислокации голландского гарнизона. На рассвете войска Монтано пошли в атаку и четыре часа штурмовали форт под огнем из пушек и мушкетов. К десяти утра им удалось прорубить топорами брешь в деревянной стене и ворваться внутрь, убив всех защитников.
Археологические улики
Именно форт стал главным урожаем археологов. Первый разведочный шурф дал ученым осколки трубок и мисок — судя по всему, они наткнулись на мусорную кучу. Дальнейшие раскопки открыли ученым массивную песчаную насыпь, окруженную со всех сторон рвом. При всей эфемерности этого сооружения с точки зрения обороны голландцы не поленились вырыть траншеи. Фрагменты 20 сосудов, собранные на территории форта, крайне разнообразны — это и столовая посуда, и изделия для хранения и приготовления пищи, американского, голландского, немецкого производства, из фарфора, керамики, стекла и металла.
Дальнейшие раскопки открыли ученым массивную песчаную насыпь, окруженную со всех сторон рвом. При всей эфемерности этого сооружения с точки зрения обороны голландцы не поленились вырыть траншеи. Фрагменты 20 сосудов, собранные на территории форта, крайне разнообразны — это и столовая посуда, и изделия для хранения и приготовления пищи, американского, голландского, немецкого производства, из фарфора, керамики, стекла и металла.
Помимо черепков, археологи обнаружили немало костей. Большинство (около 600) принадлежало кроликам — но неясно, привозили ли их на кораблях или ловили на месте, на дюнах Ла-Тортуги. Остальные — свиньям и коровам (28), птицам (43). Отсутствие ракушек местных моллюсков и рыбьих костей говорит о том, что голландцы опасались употреблять в пищу местную фауну и ели или привезенную провизию, или пойманных на острове знакомых им животных. Следов очагов на острове не обнаружено: видимо, моряки и мушкетеры опасались пожаров в форте (рядом с запасами пороха) и готовили на кораблях.
Наконец, на месте раскопок нашли сотни неиспользованных пуль для мушкетов разного калибра и несколько ядер. Примечательно, что у берега к востоку, югу и северо-востоку от форта снарядов не обнаружили. Пространственное распределение находок указывает на то, что огонь из мушкетов открывали с юга и юго-запада в сторону севера и северо-запада: эта линия огня в точности соответствует роковой атаке испанцев 1638 года (как ее показывали на рисунках современников).
Психологическая война
Однако даже эти скудные находки позволили ученым проникнуть в психику сторон, сражавшихся за остров. Так, ров, насыпь и частокол указывают на здравый смысл нидерландских капитанов: они рассудили, что их враги добираются до Ла-Тортуги только на пирогах, куда нельзя поставить тяжелую артиллерию. Значит, для обороны промыслов достаточно небольшого форта с четырьмя легкими пушками и парой десятков мушкетеров. Помимо расчетливости, ученые подчеркивают мастерство голландцев в контроле над природной средой острова: каналы, шлюзные ворота, мостки и насосы — эти сооружения навсегда изменили ландшафт Ла-Тортуги.
Материалы по теме:
Более того, голландцы были уверены, что их трудолюбие пересилит хаотические жесты деструктивного отчаяния со стороны кастильских хозяев Венесуэлы: рейд, другой рейд, но потом все равно все можно будет починить. Однако, как показала история, расчетливые голландцы недооценили упорство испанцев — и сопутствующую тем удачу.
Но нельзя сказать, что одна из сторон проиграла другой: голландцы включили тот же капиталистический расчет и прикинули, что дальнейшее противостояние набегам с материка обойдется слишком дорого — выгоднее будет искать соль в другом месте.
В Большом театре прошел пресс-брифинг гастролей Театра Ла Скала
С 10 по 16 сентября 2016 года на Исторической сцене Большого театра в рамках Открытого фестиваля искусств «Черешневый Лес», благодаря исключительной поддержке Торгового дома ГУМ, пройдут гастроли знаменитого миланского Театра Ла Скала.
Откроются гастроли 10 сентября оперой Джузеппе Верди «Симон Бокканегра» в постановке Федерико Тьецци под управлением выдающегося маэстро Мунг-Вун Чунга. 11 и 14 сентября будет исполнена опера Джузеппе Верди «Реквием», а 15 сентября состоится Концерт итальянской музыки, в программе которого музыкальные произведения Луиджи Керубини Концертная увертюра соль мажор и Симфония ре мажор, Джузеппе Верди – балет «Времена года» из оперы «Сицилийская вечерня», и Джоаккино Россини – увертюра к опере «Вильгельм Телль».
11 и 14 сентября будет исполнена опера Джузеппе Верди «Реквием», а 15 сентября состоится Концерт итальянской музыки, в программе которого музыкальные произведения Луиджи Керубини Концертная увертюра соль мажор и Симфония ре мажор, Джузеппе Верди – балет «Времена года» из оперы «Сицилийская вечерня», и Джоаккино Россини – увертюра к опере «Вильгельм Телль».
В преддверии спектаклей 8 сентября в Большом театре состоялся пресс-брифинг.
Александр Перейра, генеральный директор Театра Ла Скала:
– Для меня огромное счастье представлять нашу замечательную труппу московской публике. Это и музыкальный руководитель театра Риккардо Шайи, и маэстро Мунг-Вун Чунг, который был с нами на гастролях и в Корее, и в Шанхае, и наш главный герой Лео Нуччи – легенда итальянского оперного пения. А чтобы наглядно проиллюстрировать, как много общего у наших театров, мы пригласили солиста Большого театра Дмитрия Белосельского исполнить партию в «Реквиеме» Верди.
Риккардо Шайи, главный дирижер Театра Ла Скала:
– Находиться в Москве, в Большом театре – это большая честь. Ведь наши страны связывают давние дружеские и культурные связи. Наши сегодняшние гастроли – это продолжение сотрудничества, которое началось уже в 1970-е годы. Я сам очень много времени посвящаю работе с музыкой русских композиторов: Стравинского, Шостаковича, Чайковского, Рахманинова, Мусоргского, поэтому для меня быть здесь, в Большом, колыбели музыкального искусства России, – невероятное счастье. Я очень рад, что стал участником этого грандиозного межкультурного проекта. Гастроли – это серьезная, напряженная работа: мы отлаживаем звучание инструментов в новой обстановке, мы работаем со всемирно известными солистами из разных стран, каждый из которых обладает своими уникальными вокальными и художественными особенностями.
Ведь наши страны связывают давние дружеские и культурные связи. Наши сегодняшние гастроли – это продолжение сотрудничества, которое началось уже в 1970-е годы. Я сам очень много времени посвящаю работе с музыкой русских композиторов: Стравинского, Шостаковича, Чайковского, Рахманинова, Мусоргского, поэтому для меня быть здесь, в Большом, колыбели музыкального искусства России, – невероятное счастье. Я очень рад, что стал участником этого грандиозного межкультурного проекта. Гастроли – это серьезная, напряженная работа: мы отлаживаем звучание инструментов в новой обстановке, мы работаем со всемирно известными солистами из разных стран, каждый из которых обладает своими уникальными вокальными и художественными особенностями.
Маэстро Мунг-Вун Чунг, дирижер:
– Мое знакомство с Москвой началось в 1974 году, когда я приехал сюда участвовать в конкурсе им. П. И. Чайковского. Вернуться же в Москву спустя почти полвека вместе с Театром Ла Скала – это удивительное ощущение. Конкурс стал отправной точкой для моей карьеры, но, хоть я и посвятил музыке 40 лет, которые прошли с тех пор, я не считаю себя профессиональным музыкантом. Более того, иногда я просто ощущаю себя дилетантом: мне есть чему учиться. Самое главное для меня – играть то, что я люблю, с тем, кого люблю, а самое важное – для тех, кого люблю. Я надеюсь, нас всех – и музыкантов, и зрителей, объединит любовь к Джузеппе Верди.
Более того, иногда я просто ощущаю себя дилетантом: мне есть чему учиться. Самое главное для меня – играть то, что я люблю, с тем, кого люблю, а самое важное – для тех, кого люблю. Я надеюсь, нас всех – и музыкантов, и зрителей, объединит любовь к Джузеппе Верди.
Лео Нуччи, солист Театра Ла Скала:
– Впервые я посетил Москву, когда был здесь на гастролях Ла Скала в 1974 году. Тогда мы тоже привозили оперу «Симон Бокканегра», и я исполнял партию в хоре. Сейчас я снова пою на сцене Большого, но уже в главной роли самого Симона Бокканегры, и точно знаю, что мечты сбываются. Я хочу выразить огромную благодарность Большому театру: не случайно «большой» по-итальянски – это еще и «великий». Я благодарю ГУМ – спонсора гастролей, Театр Ла Скала и нашего музыкального руководителя Риккардо Шайи, благодаря которому в программе гастролей появилась опера «Симон Бокканегра». Я рад, что маэстро Мунг-Вун Чунг дал нам всем возможность насладиться этой музыкой.
Дмитрий Белосельский, солист Большого театра: – Мне выпала двойная честь: представлять Большой театр в Милане и Театр Ла Скала в Москве. Только что я с труппой Ла Скала был на гастролях в Сеуле и Шанхае, а сейчас буду выступать на родной сцене Большого театра со своими замечательными миланскими коллегами. Мы приехали в Москву сразу после гастролей по Азии. Я расспрашивал коллег по труппе Ла Скала – сотрудников театра, солистов – об их впечатлениях о Москве. В ответ слышал только восторженные отзывы. А от опытной труппы, которая объездила с гастролями полмира, услышать такие слова особенно приятно.
Только что я с труппой Ла Скала был на гастролях в Сеуле и Шанхае, а сейчас буду выступать на родной сцене Большого театра со своими замечательными миланскими коллегами. Мы приехали в Москву сразу после гастролей по Азии. Я расспрашивал коллег по труппе Ла Скала – сотрудников театра, солистов – об их впечатлениях о Москве. В ответ слышал только восторженные отзывы. А от опытной труппы, которая объездила с гастролями полмира, услышать такие слова особенно приятно.
Владимир Урин, генеральный директор Большого театра:
– Уникальные многолетние дружеские отношения связывают Большой театр и Театр Ла Скала. Мне очень хотелось, чтобы эти творческие контакты продолжались. В новых экономических условиях, когда так сложно найти финансирование, позволяющее такие обмены, я счастлив, что в лице компании ГУМ мы нашли верного партнера, который готов поддержать гастроли Театра Ла Скала в Москве и другие интересные проекты Большого. Чезаре Мария Рагальини, посол Италии в России: – Сентябрь стал для Москвы месяцем итальянской культуры. Только что в Музее изобразительных искусств им. А. С. Пушкина открылась выставка работ легендарного Рафаэля, а уже через день на сцене Большого театра зазвучат знаменитые арии в исполнении артистов Ла Скала.
Только что в Музее изобразительных искусств им. А. С. Пушкина открылась выставка работ легендарного Рафаэля, а уже через день на сцене Большого театра зазвучат знаменитые арии в исполнении артистов Ла Скала.
Михаил Куснирович, устроитель фестиваля «Черешневый Лес»:
– Фестиваль «Черешневый Лес» шел к этому событию 16 лет. В Москву приезжает Театр Ла Скала практически в полном составе, 346 человек, 12 огромных грузовиков с декорациями, целый филармонический оркестр, который дает отдельный концерт итальянской музыки. По рассказам папы я помню, что гастроли Ла Скала в Большом театре в 1974 году стали событием мирового масштаба. Лучший театр Италии дает спектакли в лучшем театре СССР. С тех пор Ла Скала всегда оставался идолом для нашей культурной общественности. Однако, когда появляется возможность соединить два великих театра – Большой и Ла Скала, серьезные институции со своими традициями и методами, требуется огромное усилие. Для нас гастроли Ла Скала – это культурологический рай: московская публика получает такой подарок.
Ла Пальма, Испания — туристический гид Planet of Hotels
Санта-Крус-де-ла-Пальма — столица острова и самый интересный с точки зрения достопримечательностей город. Он переполнен старинными домами с колониальной архитектурой, а в центре — на площади Испании, можно полюбоваться зданием ратуши, колокольней церкви Спасителя и оригинальным каменным фонтаном. Главный исторический памятник столицы — древняя крепость Кастильо-де-Санта-Каталина, не раз спасавшая местных жителей от пиратских атак. В городе есть очень необычный Морской музей — он располагается в точной копии корабля Христофора Колумба, выполненного в натуральную величину.Лос-Льянос-де-Аридане — самый большой город острова. Он представляет собой необычный сплав старинной архитектуры и современной, динамичной жизни. Прогулки по мощеным булыжником улицам среди изумительных домиков в стиле раннего барокко могут привести к сверкающему стеклом и металлом торговому центру, или наоборот — заставить надолго увлечься изучением необычно украшенных церквушек, построенных еще во времена конкистадоров. Самый красивый храм города — Иглесия-де-Нуэстра-Сеньора-де-лос-Ремедиос, расположен на центральной площади. Помимо него, на острове находится еще немало религиозных сооружений, достойных посещения. В них можно полюбоваться бесценными полотнами и скульптурами фламандских мастеров. В Лос-Льянос есть небольшой, но очень красивый пляж, покрытый черным вулканическим песком. Еще одна интересная туристическая достопримечательность, расположенная недалеко от города — равнина Аргуаль. Когда-то здесь располагались банановые плантации, а сейчас, по воскресеньям, открывается большой уличный рынок. На нем продаются всевозможные ремесленные товары, красивые украшения из застывшей лавы и смолы драконового дерева, антиквариат.
Самый красивый храм города — Иглесия-де-Нуэстра-Сеньора-де-лос-Ремедиос, расположен на центральной площади. Помимо него, на острове находится еще немало религиозных сооружений, достойных посещения. В них можно полюбоваться бесценными полотнами и скульптурами фламандских мастеров. В Лос-Льянос есть небольшой, но очень красивый пляж, покрытый черным вулканическим песком. Еще одна интересная туристическая достопримечательность, расположенная недалеко от города — равнина Аргуаль. Когда-то здесь располагались банановые плантации, а сейчас, по воскресеньям, открывается большой уличный рынок. На нем продаются всевозможные ремесленные товары, красивые украшения из застывшей лавы и смолы драконового дерева, антиквариат.
Пуэрто-де-Наос — небольшой поселок на побережье. Раньше о нем мало кто знал, но сейчас этот пляжный курорт стремительно набирает популярность среди туристов. Здесь расположены превосходные пляжи — сочетание черного песка и кокосовых пальм выглядит необыкновенно живописно, а развевающийся на ветру Голубой флаг свидетельствует об идеальной чистоте воды и побережья. Инфраструктура курорта отлично развита — в городе есть все необходимое для того, чтобы великолепно провести свой отпуск. В Пуэрто-де-Наос приезжают не только любители пляжного отдыха, но и экстремалы — парапланеристы, альпинисты, спелеологи и дайверы. Кроме того, здесь проложено немало маршрутов для захватывающих поездок на горных велосипедах и путешествий по каньонам.
Инфраструктура курорта отлично развита — в городе есть все необходимое для того, чтобы великолепно провести свой отпуск. В Пуэрто-де-Наос приезжают не только любители пляжного отдыха, но и экстремалы — парапланеристы, альпинисты, спелеологи и дайверы. Кроме того, здесь проложено немало маршрутов для захватывающих поездок на горных велосипедах и путешествий по каньонам.
Тасакорте — небольшой поселок с богатым историческим наследием. В квартале Чарко сохранились родовые дома испанской знати, построенные в XVI-XVII столетиях, и первая церковь острова с великолепными витражами. Рядом с ней расположена крытая аллея, заросшая бугенвиллеей и украшенная керамическими изразцами. В поселке находится единственный в Европе Музей бананов — на местных плантациях выращивали настолько качественные фрукты, что им присвоили категорию, дающую право называться «Тасакорте» — по месту происхождения. После того, как все интересные места будут изучены, можно прогуляться в сторону побережья. Недалеко от поселка есть небольшой и очень живописный пляж. Он не очень подходит для купания из-за близости скал, но на нем будет приятно отдохнуть среди камней и просто полюбоваться окрестностями.
Он не очень подходит для купания из-за близости скал, но на нем будет приятно отдохнуть среди камней и просто полюбоваться окрестностями.
Фуэнкальенте-де-ла-Пальма — муниципалитет с центром в деревне Лос-Канариос. Это небольшой пляжный курорт, ставший известным благодаря природным достопримечательностям. Практически вплотную к его побережью спускаются склоны вулканического хребта Кумбре-Вьеха, в южной части которого возвышается действующий вулкан Тенегия. Он является частью национального парка Лос-Волканес-де-Тенегия, часто посещаемого путешественниками. На побережье интерес для туристов представляет центр интерпретации при морском заповеднике, размещенный в бывшем доме смотрителя маяка. Его главный зал выполнен в виде огромной пещеры со стеклянным полом, через который можно наблюдать за океанскими обитателями. В 200 метрах от маяка, на морском дне, находится памятник «40 бразильским мученикам» — сорок крестов, установленных в память о португальском иезуите Игнасио де Асеведо и его спутниках — они были казнены на этом месте французскими корсарами. Мемориал очень популярен среди дайверов, а глубина в 20 метров позволяет погружаться сюда даже новичкам.
Мемориал очень популярен среди дайверов, а глубина в 20 метров позволяет погружаться сюда даже новичкам.
Города региона Коста-дель-Соль — Marbella & Co
План городов, деревень и важнейших областей региона Коста-дель-Соль
Málaga
Население: 570 000!
Малага, вид с Мавританского замка на горе Гибралфаро
Вполне справедливо назвать Малагу столицей региона Коста-дель-Соль. Как и в любом другом крупном городе Европы, здесь вы можете заняться шоппингом, развлечься и посетить важные культурные объекты. При этом город сохранил свое испанское обаяние благодаря чудесным улочкам и ресторанам, где вы можете насладиться традиционными андалусскими блюдами, такими как паэлья, попробовать хамон и местное вино.
Пабло Пикассо, который родился в этом городе, а также арабы и римляне, которые когда-то правили здесь, оставили заметный след в архитектуре, культуре и искусстве Малаги.
Прямо за главной улицей Аламеда-Принсипаль располагается здание, которое когда-то служило верфью. Теперь это популярный рынок, который обязательно рекомендуется посетить, чтобы закупиться продуктами.
Теперь это популярный рынок, который обязательно рекомендуется посетить, чтобы закупиться продуктами.
После восстановительных работ, завершенных несколько лет назад, порт сам по себе стал достопримечательностью. Теперь это спокойное и динамичное пространство с музеями, магазинами и ресторанами. Здесь регулярно проходят различные культурные события.
Из аэропорта до Малаги можно добраться на поезде, автобусе или машине.
Базарные дни с 8:00 до 14:00
- По понедельникам район Ла-Лус и район Кампанильяс
- По вторникам Пуэрто-де-ла-Торре
- По средам Уэлин и Ла-Пас
- По четвергам парк Хуан Хурадо
- По субботам Уэлин и Эль-Пало
- По воскресеньям открывается рынок искусства Галерее искусств на первом пирсе (11:00-16:00)
Фестивали / Ферии
- Карнавал — февраль
- Пасха, Страстная седмица – первое полнолуние весны (после 21/3)
- Летнее солнцестояние Костры святого Иоанна Крестителя — вечер 23 и день 24 июня
- Фестиваль малагеньяс — 3 августа
- Ферия в Малаге — вечером второй пятницы августа (но на самом деле она начинается в субботу и продолжается до следующей субботы.

- День святых невинных младенцев вифлеемских — 28 декабря
Torremolinos
Население: 67 000!
Торремолинос, набережная
Торремолинос — одно из старейших туристических направление региона Коста-дель-Соль. Его репутация не всегда была столь прекрасной, но за последние годы многое изменилось. Город последовательно модернизируется и усовершенствуется, и центр теперь полностью пешеходный. Здесь вы найдете большое разнообразие магазинов, ресторанов и баров. А на центральной площади часто проходят культурные события.
В городе есть аквапарк, парк крокодилов, и конечно же, море, песок и пляж, который тянется, насколько хватает глаз.
Город пользуется преимуществом расположения неподалеку от Малаги и аэропорта, до которых можно с легкостью добраться на поезде.
Базарные дни с 8:00 до 14:00
- По четвергам и воскресеньям Ярмарочная площадь
Фестивали / Ферии
- Карнавал — февраль
- Вердиалес — февраль
- Ретро танцы — февраль/март
- Фестиваль крестов — май
- Летнее солнцестояние Костры святого Иоанна Крестителя — вечер 23 и день 24 июня
- Ферия в честь Богоматери Кармельской — июль
- Фестиваль фламенко — июль/август
- День туриста — первый четверг сентября
- День жареной рыбы — первый четверг октября
- Ромерия в честь святого Михаила — воскресенье перед Ферией в честь святого Михаила
- Ферия в честь Святого Михаила — 25-29 сентября
Benalmádena
Население: 67 000!
Пуэрто-Марина, Бенальмадена
Бенальмадену можно разделить на три района:
Benalmádena Pueblo
Красивая традиционная андалусская деревушка с узкими улочками и старыми домами, 280 м над уровнем моря. Здесь расположено множество милых маленьких ресторанов, а из деревни открывается шикарный вид на побережье.
Здесь расположено множество милых маленьких ресторанов, а из деревни открывается шикарный вид на побережье.
Базарные дни с 8:00 до 14:00
- По пятницам площадь Альгуасиль
Arroyo de la Miel
Центральная часть Бенальмадены с множеством небольших ресторанчиков и магазинов. Посреди этой область располагается очень популярный парк развлечений Tivoli World, который был создан одним датчанином много лет назад. За парком Тиволи находится канатная дорога, по которой вы сможете добраться до вершины горы, откуда открывается чудесный вид на море и побережье. Там вы также сможете попасть на ежедневное кормление хищных птиц в орлином заповеднике.
Базарные дни с 8:00 до 14:00
- По пятницам Тиволи
Benalmádena Costa
Прибрежная зона растянулась на несколько километров. Здесь вы найдете казино, поле для гольфа и роскошные песчаные пляжи. Летом это место буквально оживает. Морской порт, который неоднократно выбирался самым красивым портом, является вишенкой на торте, ведь здесь вы сможете себя ощутить героем «Тысячи и одной ночи».
Базарные дни с 8:00 до 14:00
- По средам парк Палома
Фестивали / Ферии
- Карнавал — февраль
- Праздник Тела и Крови Христовых — через 2 недели после Пасхи
- Летнее солнцестояние Костры святого Иоанна Крестителя — вечер 23 и день 24 июня
- Веладилья-дель-Кармен — 16 июля
- Ферия в Бенальмадена-Пуэбло — 15 августа
- Ромерия в Бенальмадене — август
- День туриста 27 сентября
Fuengirola
Население: 77 000!
Набережная Фуэнхиролы — Рей-де-Испания
Фуэнхирола — конечный пункт назначения на популярном железнодорожном маршруте, который проходит по побережью от Малаги, и один из самых любимых городов у скандинавов. Здесь вы найдете все, о чем вы можете только мечтать, для ведения современного образа жизни. В центре Фуэнхиролы располагается главная площадь. Два раза в неделю она превращается в огромный рынок, а во время ежегодной Летней ярмарки весь город преобразуется на глазах. Возможно, основной достопримечательностью является набережная и пляж, который растянулся на 10 км. Здесь всегда можно встретить людей, которые гуляют, совершают пробежку или катаются на велосипеде. А на пляже можно поиграть в волейбол, заняться фитнесом и йогой. У вас всегда есть богатый выбор чирингито (пляжные бары), где вы сможете отведать копченую рыбу.
Два раза в неделю она превращается в огромный рынок, а во время ежегодной Летней ярмарки весь город преобразуется на глазах. Возможно, основной достопримечательностью является набережная и пляж, который растянулся на 10 км. Здесь всегда можно встретить людей, которые гуляют, совершают пробежку или катаются на велосипеде. А на пляже можно поиграть в волейбол, заняться фитнесом и йогой. У вас всегда есть богатый выбор чирингито (пляжные бары), где вы сможете отведать копченую рыбу.
Базарные дни с 8:00 до 14:00
- По вторникам Ярмарочная площадь
- По пятницам — Блошиный рынок на Ярмарочной площади
- По воскресеньям Мирамар, улица Мендес-Нуньес
Фестивали / Ферии
- Международная ярмарка Де-лос-Пуэблос — середина марта
- Летнее солнцестояние Костры святого Иоанна Крестителя — вечер 23 и день 24 июня
- Фиеста-дель-Кармен — 16 июля
- Ромерия — воскресенье перед 6 октября
- Фестиваль Росарио — 6-12 октября
Mijas
Население: 78 000!
Михас-Пуэбло. Традиционная живописная белая андалусская горная деревушка
Традиционная живописная белая андалусская горная деревушка
Mijas Pueblo
Михас-Пуэбло — красивая горная деревня на расстоянии 5 км от моря. Здесь перед вами предстанут белоснежно белые дома, арабские дворики и пышные цветы в горшках, висящих на стенах. Из Михаса открывается абсолютно невероятный вид на Коста-дель-Соль.
Базарные дни с 8:00 до 14:00
- По субботам Лас-Лагунас (улица Антонио Гарсия Буэно, улица Бенахарафе и улица Альфарнате)
Фестивали / Ферии
- Ферия (Лас-Лагунас) — первые две недели июня
- Ферия (Вирхен-де-ла-Пенья) — первые две недели сентября
- Фиеста-дель-Кармен — 16 июля
- Ромерия — конец октября
Mijas Costa
Михас Коста растянулся приблизительно на 11 км береговой линии и является излюбленным местом для игроков в гольф. Хотя он располагается не так далеко от самого Михаса, здесь ощущается современный, передовой стиль жизни.
Михас Коста включает две важные зоны: Ла-Кала-де-Михас и Калаонда.
La Cala de Mijas:
Ла-Кала-де-Михас, башня
Небольшой приятный городок Ла-Кала находится прямо у пляжа. Когда вы окончите свой обед в одном из ресторанов, вы можете совершить легкую прогулку по новой набережной, протяженность которой, как планируется, будет составлять 150 км. Уже достроен участок до Калаонды.
Базарные дни с 8:00 до 14:00
- По средам Ла-Кала-де-Михас
- По воскресеньям ипподром Коста-дель-Соль
Фестивали / Ферии
- Ферия (Ла-Кала) — последние две недели июля
Calahonda
Калаонда разраслась так сильно, что можно считать ее отдельным городом, хотя на самом деле она все еще является частью Михаса. Этот район особенно популярен среди любителей гольфа, поскольку в пределах 10 км располагаются 10 полей для гольфа. Если вам не нравится гольф, в вашем распоряжении также теннисные корты, фитнес клубы и песчаные пляжи с огромным выбором водных видов спорта. Кроме того, здесь вы найдете множество разнообразных ресторанов, кафе, баров и чирингито.
Кроме того, здесь вы найдете множество разнообразных ресторанов, кафе, баров и чирингито.
Базарные дни с 8:00 до 14:00
- По четвергам Калипсо
- Воскресный блошиный рынок в Калипсо
Marbella
Население: 140 000!
Виды над Марбельей и Пуэрто-Банус с горной грядой Сьерра-Бланка и пляжем Ла-Конча на заднем плане
Марбелья — это второй по величине город провинции Малага после самой Малаги.
Марбелья делится на следующие важные районы, а также включает деревню Сан-Педро-де-Алькантара.
Восточная часть Марбельи
От Калаонды до города Марбелья.
Популярный жилой район, растянувшийся приблизительно на 12 км.
Здесь вы найдете 5 гольф-клубов, бесчисленное количество пляжных баров (чирингито) и рестораны различной этнической принадлежности.
Эта область знаменита лучшими естественными песчаными пляжами и охраняемыми дюнами в Марбелье. Также известна своими сосновыми лесами.
Также известна своими сосновыми лесами.
Ниже представлены основные городские образования:
Cabopino / Puerto de Cabopino
В восточной части Марбельи находится Кабопино со своим собственным портом. Это место часто пропускают, потому оно незаметно с дороги. Порт выполнен в оригинальном средиземноморском стиле с отличными ресторанами и барами. На пляжах расположены дюны, которые теперь охраняются законом.
Elviria
Двигаясь в направлении Марбельи, вы попадете в Эльвирию. Это крайне популярная область благодаря песчаным пляжам в шаговой доступности от известных пятизвездочных отелей, пляжного клуба Nikki Beach и торгового центра.
Los Monteros
Известное прибрежное городское образование с роскошными виллами, отелем Los Monteros Hotel и клубом La Cabane Beach Club.
Las Dunas de Marbella
Построенное в 90-е муниципальное образование с отличным выбором вилл, таунхаусов и квартир.
(Golf) Rio Real
Все это является частью комплекса Лос-Монтерос, который включает знаменитый гольф-клуб Rio Real Golf Club. В северной части A7/N340 вы найдете несколько симпатичных жилых комплексов, расположенных всего в паре сотнях метрах от пляжа. Здесь располагается комплекс Рио-Реал-Плайя и ресторан El Trocadero.
В северной части A7/N340 вы найдете несколько симпатичных жилых комплексов, расположенных всего в паре сотнях метрах от пляжа. Здесь располагается комплекс Рио-Реал-Плайя и ресторан El Trocadero.
Marbella Town
Марбелья — густонаселенный международный город, а также излюбленное направление для богатых и знаменитых Здесь у вас есть доступ к морю, пляжам, набережной и большому разнообразию ресторанов — все, о чем можно только мечтать. Посетите старый город и вы увидите узкие, мощеные улочки, сувенирные магазины, бутики, галереи, бары и знаменитую Апельсиновую площадь. Заядлые шопоголики могут посетить торговый центр La Cañada, который включает множество модных бутиков, кинотеатров, ресторанов и большой супермаркет.
В городской черте и окрестностях находятся следующие городские образования и районы:
Золотая миля
Золотая миля — это отрезок от маяка Эль-Пирули в центре Марбельи до Пуэрто-Банус. Это богатый район с одними из самых древних городских образований в Марбелье. Немецкая аристократия начала застройку этой зоны в конце 60-х, соорудив пятизвездочные отели, Marbella Club Hotel и Puente Romano, и конечно же, изысканные виллы на берегу моря.
Немецкая аристократия начала застройку этой зоны в конце 60-х, соорудив пятизвездочные отели, Marbella Club Hotel и Puente Romano, и конечно же, изысканные виллы на берегу моря.
Nagüeles
Одно из старейших городских образований, где многие виллы были преобразованы или полностью перестроены в современном стиле.
Сьерра-Бланка и Каскада-де-Камохан
Две соседний роскошные зоны преимущественно с виллами и несколькими комплексами, состоящими из элитных квартир или таунхаусов.
Marbella Hill Club
Очень крупный комплекс с клиентами со всей планеты.
Базарные дни с 8:00 до 14:00
- По понедельникам Ярмарочная площадь
Фестивали / Ферии
- Карнавал — февраль
- Пасха Страстная седмица — первое полнолуние весны (после 21/3)
- Крус-де-Хуанар — 3 мая
- Ферия Сан-Бернабе — с субботы по субботу, включая 11 июня
- Летнее солнцестояние Костры святого Иоанна Крестителя — вечер 23 и день 24 июня
- Вирген-дель-Кармен — 16 июля
- Фиеста-дель-Тостон — 1 ноября
Западная часть Марбельи
От города Марбелья до реки Гуадальманса по дороге в Бенаавис.
Puerto Banús
Пуэрто-Банус — это место, где вы можете спокойно гулять, представлять себя владельцем одной из огромных яхт, причаливших в порту, и любоваться медленно проезжающими, роскошными автомобилями. Нередко может наткнуться на какую-нибудь знаменитость. Богатые и знамениты приезжают сюда ради пляжей, клубов и насыщенной ночной жизни.
Nueva Andalucía
На горной стороне дороги A7/N340 располагается одно из крупнейших городских образований в Марбелье. Это очень популярная область из-за близости к Пуэрто-Банус. Здесь вы найдете недвижимость на любой вкус: от небольших квартир до вилл на первой береговой линии за несколько миллионов долларов. В районе Нуэва Андалусия расположены одни из самых знаменитых полей для гольфа!
Базарные дни с 8:00 до 14:00
- По субботам неподалеку от торгового центра Centro Plaza
San Pedro de Alcántara
Этот чудесный маленький городок с узкими улочками, множеством магазинов, кафе и баров, а также потрясающей церковью на Пласа-де-ла-Иглесия находится у подножья гор Сьерра-де-Ронда. Город ощущается неиспорченным современной цивилизаций и располагается к западу от Марбельи и Пуэрто-Банус, в 10 минутах от Эстепоны.
Город ощущается неиспорченным современной цивилизаций и располагается к западу от Марбельи и Пуэрто-Банус, в 10 минутах от Эстепоны.
Базарные дни с 8:00 до 14:00
- По четвергам Ярмарочная площадь
Фестивали / Ферии
- Ферия 14-19 октября
Guadalmina Baja & Alta
Крайне популярной, престижной городское образование, особенно район Гуадальмина-Баха, рядом с пляжем, где общий вид формируют отдельно стоящие виллы, многие из которых принадлежат знаменитостям. В районе Гуадальмина-Альта, расположенный на горной части прибрежной дороги, построено множество вилл, квартир и таунхаусов, но что действительно привлекает внимание — три поля для гольфа. Все построено вокруг зеленой зоны, которая простирается по обе стороны от Гуадальмина-Баха — от пляжа до платной дороги и Валле-дель-Соль.
Estepona
Население: 67 000!
Пуэрто-де-Эстепона
Эстепона — довольно большой традиционный андалусский прибрежный город, который несет в себе атмосферу и обаяние старой рыбацкой деревни. Некоторые улочки настолько узкие, что они скорее подойдут для лошадей, а не для машин. В некоторых тапас-барах подают традиционные испанские блюда. Благодаря тому, что горы защищают город от холодного дыхания севера, здесь солнце светит примерно 325 дней в году, а средняя температура составляет около 18 градусов. В одно время здесь даже хотели построить Диснейленд, но в итоге был выбран Париж.
Некоторые улочки настолько узкие, что они скорее подойдут для лошадей, а не для машин. В некоторых тапас-барах подают традиционные испанские блюда. Благодаря тому, что горы защищают город от холодного дыхания севера, здесь солнце светит примерно 325 дней в году, а средняя температура составляет около 18 градусов. В одно время здесь даже хотели построить Диснейленд, но в итоге был выбран Париж.
Базарные дни с 8:00 до 14:00
- По средам проспект Хуан Карлос I
- По воскресеньям в гавани
Фестивали / Ферии
- Карнавал — февраль
- Сан-Исидро — 15 мая
- Летнее солнцестояние Костры святого Иоанна Крестителя — вечер 23 и день 24 июня
- Ферии и крупные фестивали — первая неделя июля
- Вирген-дель-Кармен — 16 июля
- День туриста 15 августа
Casares
Население: 5 700!
Касарес-Плайя
Касарес похож на открытку. Эта традиционная белая деревня прекрасна сама по себе. Однако отсюда также открываются виды на Средиземное море, Гибралтар и даже Африку. Здесь вы найдете два знаменитых поля для гольфа и первую в Европе искусственную Кристальную лагуну.
Эта традиционная белая деревня прекрасна сама по себе. Однако отсюда также открываются виды на Средиземное море, Гибралтар и даже Африку. Здесь вы найдете два знаменитых поля для гольфа и первую в Европе искусственную Кристальную лагуну.
Базарные дни с 8:00 до 14:00
- По пятницам улица Ла-Каррера
Фестивали / Ферии
- Фестиваль Росарио-дель-Кампо — последняя неделя мая
- Ферия Барриада-Секадеро — конец июня
- Ферия — начало августа
- Патрона — первая неделя сентября
- Ферия-дель-Кристо — сентябрь
Duquesa
Часть муниципалитета Манильва. Население: 14 000!
Порт Дукеса
Помимо 18-луночного поля для гольфа Дукеса славится своей чудесной пристанью. Здесь вы можете воспользоваться услугами порта или арендовать водный мотоцикл, вейкборд или падлборд, и даже заняться подводным плаванием. По обе стороны гавани расположены широкие песчаные пляжи.
По обе стороны гавани расположены широкие песчаные пляжи.
Базарные дни с 8:00 до 14:00
- По пятницам Сан-Луис-де-Сабинильяс, набережная
- Воскресенье — блошиный рынок в Сан-Луис-де-Сабинильяс, на набережной
Фестивали / Ферии
- Ферия — Манильва/Сабинильяс, 6-9 августа
Sotogrande
Часть муниципалитета Сан-Роке. Население: 29 000!
Пуэрто-де-Сотогранде
Сотогранде — один из самых престижных жилых районов на побережье. Здесь отдыхают одни из самых богатых и влиятельных европейских семей. Сотогранде знаменита пятью полями для гольфа. Гольф-клуб Valderrama принимал и Вольво Мастерс, и Кубок Райдера. Среди других спортивных объектов: гольф-академия, теннисные корты, поля для регби, ипподромы и 6 всемирно известных полей для поло. Советуем посетить пристань Сотогранде, где летом можно воспользоваться услугами водных такси, чтобы добраться до других городов Коста-дель-Соль.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.

- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
молекул | Бесплатный полнотекстовый | Происхождение солевых эффектов при фторировании SN2 с использованием KF, стимулированного ионными жидкостями: квантово-химический анализ
Во-первых, мы изучаем случай использования отношения субстрат: KF 1: 1, в котором соль металла действует только как фторирующий агент, т. Е. в качестве источника F — , поэтому солевые эффекты не могут быть приписаны этой ситуации. На рисунке 2 представлены состояния перехода (TS) и энергия для этого процесса (координаты и структуры до- и постреакционных комплексов см. В дополнительных материалах.За нуль свободной энергии принимаются «свободные» реагенты, для которых субстрат, CIPs KF, [bmim] PF 6 или [bmim] Cl все отделены друг от друга в фазе раствора). IL [bmim] PF 6 и KF используются в качестве промотора и фторирующего агента, соответственно, в том же количестве, что и субстрат (субстрат: KF: [bmim] PF 6 = 1: 1: 1). Мы нашли два пути реакции, случай 1 и случай 2 со свободной энергией активации Гиббса G ‡ , равной 22.8 и 21,4 ккал / моль соответственно. Энергетика реакции, изображенная на рисунке 2, предсказывает, что реакция будет протекать по механизму с более низким G ‡ (случай 2) в соответствии с принципом Кертина-Хендерсона (когда не возникает равновесия между свободными реагентами и предреакционным комплексом, реакция протекает предпочтительно по пути с наименьшей свободной энергией Гиббса TS, независимо от свободных энергий Гиббса предреакционных комплексов) [29]. Здесь соль металла KF реагирует как контактная ионная пара, а электроотрицательные атомы F в анионе ИЖ PF 6 — действуют как основание Льюиса, координируя противокатион K + , смягчая неблагоприятное кулоновское влияние последнего на нуклеофил F — .
В дополнительных материалах.За нуль свободной энергии принимаются «свободные» реагенты, для которых субстрат, CIPs KF, [bmim] PF 6 или [bmim] Cl все отделены друг от друга в фазе раствора). IL [bmim] PF 6 и KF используются в качестве промотора и фторирующего агента, соответственно, в том же количестве, что и субстрат (субстрат: KF: [bmim] PF 6 = 1: 1: 1). Мы нашли два пути реакции, случай 1 и случай 2 со свободной энергией активации Гиббса G ‡ , равной 22.8 и 21,4 ккал / моль соответственно. Энергетика реакции, изображенная на рисунке 2, предсказывает, что реакция будет протекать по механизму с более низким G ‡ (случай 2) в соответствии с принципом Кертина-Хендерсона (когда не возникает равновесия между свободными реагентами и предреакционным комплексом, реакция протекает предпочтительно по пути с наименьшей свободной энергией Гиббса TS, независимо от свободных энергий Гиббса предреакционных комплексов) [29]. Здесь соль металла KF реагирует как контактная ионная пара, а электроотрицательные атомы F в анионе ИЖ PF 6 — действуют как основание Льюиса, координируя противокатион K + , смягчая неблагоприятное кулоновское влияние последнего на нуклеофил F — . Основное различие между двумя механизмами — положение противокатиона K + . Похоже, что в (Случай 2) K + дополнительно стабилизируется за счет взаимодействия с электронным фенильным кольцом. На Рисунке 3 показаны TS и энергетика фторирования S N 2 под стимулирующими эффектами [bmim] Cl. Опять же, с соотношением субстрат: KF 1: 1. Мы получили два альтернативных пути, из которых (случай 2) более благоприятен с более низким G ‡ (23,9 ккал / моль).Более высокое значение G ‡ (21,4 ккал / моль) для фторирования S N 2 в [bmim] PF 6 , по-видимому, согласуется с экспериментально наблюдаемым более низким выходом реакции (~ 30%) по сравнению с что (~ 90%) в [bmim] PF 6 . Эта разница в стимулирующем влиянии двух ИЖ может быть результатом разницы в способности анионов ИЖ Cl — и PF 6 — : большее количество электроотрицательных и многочисленных атомов F в PF 6 — может отдавать частичные отрицательные заряды противокатиону K + намного лучше, чем Cl — .
Основное различие между двумя механизмами — положение противокатиона K + . Похоже, что в (Случай 2) K + дополнительно стабилизируется за счет взаимодействия с электронным фенильным кольцом. На Рисунке 3 показаны TS и энергетика фторирования S N 2 под стимулирующими эффектами [bmim] Cl. Опять же, с соотношением субстрат: KF 1: 1. Мы получили два альтернативных пути, из которых (случай 2) более благоприятен с более низким G ‡ (23,9 ккал / моль).Более высокое значение G ‡ (21,4 ккал / моль) для фторирования S N 2 в [bmim] PF 6 , по-видимому, согласуется с экспериментально наблюдаемым более низким выходом реакции (~ 30%) по сравнению с что (~ 90%) в [bmim] PF 6 . Эта разница в стимулирующем влиянии двух ИЖ может быть результатом разницы в способности анионов ИЖ Cl — и PF 6 — : большее количество электроотрицательных и многочисленных атомов F в PF 6 — может отдавать частичные отрицательные заряды противокатиону K + намного лучше, чем Cl — .
ВИЗУАЛИЗАЦИЯ ДВУХФАЗНЫХ ПОТОКОВ В РАСПЛАВЛЕННОЙ СОЛИ: ГЕЛИЕВОЕ КУРИЗИРОВАНИЕ ФТОРИДА ЛИТИЯ — ФТОРИДА НАТРИЯ — ФТОРИДА КАЛИЯ (LIF-NAF
Абстрактные
Испытательная установка для очень высоких температур была спроектирована и построена в Лаборатории теплогидравлических исследований Техасского университета A&M (TAMU) для проведения экспериментов по визуализации двухфазного потока в расплаве соли. Испытательный прибор из нержавеющей стали 316 (SST316), оснащенный прозрачной кварцевой секцией, был разработан для проведения экспериментов по визуализации одиночных пузырьков гелия, поднимающихся во фторидной соли в диапазоне температур 460-650 ° C.Фторид-соль, выбранная для этого исследования, представляла собой эвтектическую смесь LiF-NaF-KF (46,5-11,5-42%), также известную как FLiNaK. Был проведен ряд тестов с пузырьками гелия при температуре 550-600 ° C, и для оценки полей скорости был успешно применен метод измерения скорости изображения частиц (PIV). Проведенный анализ помог понять влияние размера и формы пузырька на конечную скорость пузырька гелия в FLiNaK. Каждый пузырек менял форму и траекторию на протяжении всего подъема в испытательной секции. Наблюдаемые формы пузырьков были эллипсоидными, качающимися и сферическими; наблюдаемые движения пузырьков были спиральными, зигзагообразными и прямолинейными.Пузырьки гелия были измерены и имели диапазон соотношения сторон 0,363 — 0,681 ± 10%, диапазон эквивалентного диаметра пузыря в пределах 2,96 — 6,47 ± 12% мм и экспериментальный диапазон конечной скорости 208,41 — 268,82 ± 3% мм / с. Безразмерные числа рассчитывались с теплофизическими свойствами жидкости и газа, оцененными в диапазоне 550-600 ° C и атмосферном давлении. Безразмерные диапазоны чисел в этом исследовании были определены как 243
Каждый пузырек менял форму и траекторию на протяжении всего подъема в испытательной секции. Наблюдаемые формы пузырьков были эллипсоидными, качающимися и сферическими; наблюдаемые движения пузырьков были спиральными, зигзагообразными и прямолинейными.Пузырьки гелия были измерены и имели диапазон соотношения сторон 0,363 — 0,681 ± 10%, диапазон эквивалентного диаметра пузыря в пределах 2,96 — 6,47 ± 12% мм и экспериментальный диапазон конечной скорости 208,41 — 268,82 ± 3% мм / с. Безразмерные числа рассчитывались с теплофизическими свойствами жидкости и газа, оцененными в диапазоне 550-600 ° C и атмосферном давлении. Безразмерные диапазоны чисел в этом исследовании были определены как 243
(PDF) Растворимость KF в воде методом молекулярной динамики с использованием метода интегрирования Кирквуда
tration. Поведение идеального члена показано на вставке
того же рисунка.На рис. 4 мы показываем кривую химического потенциала
в зависимости от концентрации раствора, подогнанную простым полиномом
порядка 3, вместе с горизонтальной линией
, соответствующей химическому потенциалу твердого
кристаллического兲 фаза.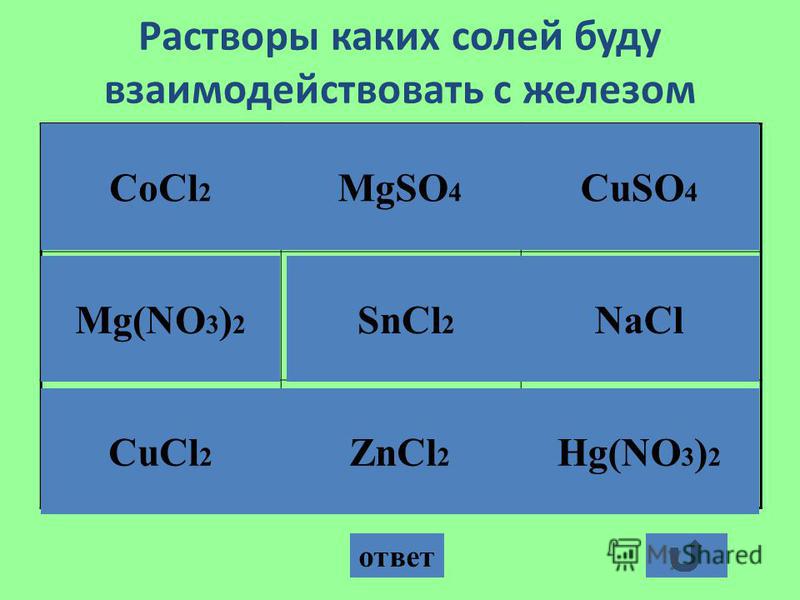 Пересечение находится при концентрации
Пересечение находится при концентрации
сÀ26 M, которая, следовательно, является значением насыщения
нашего водного раствора KF при TÀ320 К. Наше значение разумно сравнивает
с экспериментальной растворимостью, сÀ17. М.31 Соглашение
превосходит наши ожидания, поскольку модель, которую мы выбрали
, не может количественно воспроизвести плотность be-
havior концентрированных растворов; см. рис. 5.
V. ЗАКЛЮЧИТЕЛЬНЫЕ ЗАМЕЧАНИЯ
Эта статья представляет собой успешную попытку применить хорошо известные процедуры
для получения свободной энергии с помощью компьютерного моделирования, чтобы получить информацию о растворимости, одном из наиболее важных свойств
. концентрированных растворов электролитов.Воспользовавшись преимуществом моделирования при постоянной температуре и давлении
в сочетании с процедурой зарядки, впервые предложенной Кирквудом
, и другими более стандартными подходами к вычислению глобальной свободной энергии, мы продемонстрировали не только
.
выполнимость такого расчета, но также отсутствие серьезных вычислительных трудностей
в подходе. Однако надежность результатов сильно зависит от точности
моделей потенциала взаимодействия для представления реалистичной системы, имеющей физическое значение.Здесь прогресс будет исходить из
различных подходов, таких как моделирование ab initio. Важным моментом, который мы хотим подчеркнуть, является то, что статистическая механическая теория растворимости не представляет численных или концептуальных трудностей.
БЛАГОДАРНОСТИ
Авторы благодарят Рут Линден-Белл за разъяснения
дискуссий в CECAM. Эта работа была частично поддержана
проектом MIUR COFIN-2000. G.C.и Э. Выражаем благодарность за финансовую помощь
edge по соглашению об обмене
между Universita
t Ulm и Universita
´Roma I. M.F. и
T.C. благодарю за поддержку, соответственно, GDR-Practis
и проект Icarus в CINECA.
1Дж. Г. Кирквуд и И. Оппенгейм, Химическая термодинамика, McGraw-
Г. Кирквуд и И. Оппенгейм, Химическая термодинамика, McGraw-
Hill, New York, 1961, гл. 12.
2J. G. Kirkwood, J. Chem. Phys. 3, 300 1935 兲.
3С.T. Cui and J. G. Harris, J. Phys. Chem. 99, 2900 共1995兲.
4B. Guillot and Y. Guissani, Mol. Phys. 54,455共1985兲.
5M. Mezei, J. Comput. Chem. 13, 651 共1992兲.
6J. Perkyns and B. M. Pettitt, J. Phys. Chem. 98, 5147 共1994兲.
7G. Hummer, L. R. Pratt, and A. E. Garcia, J. Phys. Chem. 100, 1206
共1996兲.
8V. P. Sokhan, Mol. Simul. 19, 181 共1997兲.
9R. M. Lynden-Bell and J. C. Rasaiah, J. Phys. Chem. 107, 1981 共1997兲.
10T.Darden, D. Pearlman, and L. G. Pedersen, J. Phys. Chem. 109, 10921
共1998兲.
11 D. Frenkel and A. J. C. Ladd, J. Chem. Phys. 81, 3188 共1984兲.
12J. M. Polson, E. Trizac, S. Pronk, and D. Frenkel, J. Chem. Phys. 112,
5339 共2000兲.
13R. M. Lynden-Bell, J. C. Rasaiah, and J. P. Noworyta, Pure Appl. Chem.
Chem.
73, 1721 共2001兲.
14K. S. Shing and K. E. Gubbins, Mol. Phys. 43,717共1981兲.
15D. Frenkel and B. Smit, Understanding Molecular Simulation 共Academic,
New York, 1996兲, Chap.9.
16B. Widom, J. Chem. Phys. 39,2808共1963兲.
17H. J. C. Berendsen, J. P. M. Postma, W. F. van Gunsteren, and J. Hermans,
in Intermolecular Forces, edited by B. Pullman 共Reidel, Dordrecht, 1981兲,
p. 331.
18S. Chowdhuri and A. Chandra, J. Chem. Phys. 115, 3732 共2001兲.
19A. P. Lyubartsev and A. Laaksonen, J. Phys. Chem. 100, 16410 共1996兲.
20M. Tosi and F. G. Fumi, J. Phys. Chem. Solids 25,31共1964兲.
21H.J. C. Berendsen, J. R. Grigera, T. P. Straatsma, J. Phys. Chem. 91,
6269 共 1987 兲.
22л. X. Dang, D. Smith, J. Chem. Phys. 99,6950 共 1993 兲.
23л. Laudernet, T. Cartailler, P. Turq, M. Ferrario, J. Phys. Chem.共 быть
опубликовано 兲.
24Дж. P. Ryckaert, G. Ciccotti и H. J. C. Berendsen, J. Comp. Phys. 23 277
J. C. Berendsen, J. Comp. Phys. 23 277
共 1977 兲.
25С. Нос
´, мол. Phys. 81,511 1986 兲.
26М. Феррарио, Компьютерное моделирование в химической физике, под редакцией М.P.
Allen and D. J. Tildesley 共Kluwer Academic, Dordrecht, 1993兲,p.153.
27G. Ciccotti and J. P. Ryckaert, Comput. Phys. Rep. 4, 345 共1986兲.
28G. Kalibaeva, M. Ferrario, and G. Ciccotti, Mol. Phys. 共to be published兲.
29D. Frenkel and B. Smit, Understanding Molecular Simulation 共Academic,
New York, 2002兲, Chap. 12.
30P. H. Hunenberger and J. A. McCammon, J. Chem. Phys. 110, 1856
共1999兲.
31P. Pascal, Nouveau traite de chimie minerale, Vol.II, издание Masson,
Париж, 1963 г..
РИС. 5. Поведение плотности в зависимости от молярной концентрации для нашей модели dia-
monds по сравнению с экспериментальными значениями line.
4953J. Chem. Phys., Vol. 117, No. 10, 8 September 2002 Растворимость KF в воде
Загружено 21 декабря 2006 г. — 134.94.122.39. Распространение осуществляется с соблюдением лицензии AIP или авторских прав, см. Http://jcp.aip.org/jcp/copyright.jsp
— 134.94.122.39. Распространение осуществляется с соблюдением лицензии AIP или авторских прав, см. Http://jcp.aip.org/jcp/copyright.jsp
Коррозия материалов в эвтектической соли расплавленного фторида лития, фторида натрия и фторида калия
Абстрактные
Исследования статической коррозии были предприняты для определения совместимости нескольких возможных высокотемпературных материалов для контура теплопередачи в расплавленной эвтектической соли фторида щелочного металла, LiF-NaF-KF: 46.5-11,5-42 мол.% (Обычно называемый FLiNaK), а также расплав хлорида около эвтектической соли, KCl-MgCl2: 68-32 мол.%. Несколько жаропрочных сплавов: Hastelloy-N, Hastelloy-X, Haynes-230, Inconel-617 и Incoloy-800H, Nb-1Zr, почти чистый никелевый сплав Ni-201 и керамика C / SiSiC подвергались воздействию расплавленного FLiNaK. при 850 ° C в течение 500 ч в герметичных графитовых тиглях в атмосфере аргона. Коррозия происходила в основном из-за удаления легирования Cr из хромсодержащих сплавов, эффект, который был особенно заметен на границах зерен. Было отмечено, что коррозия происходит из-за избирательного воздействия Si-фазы в керамике C / SiSiC. Потеря веса сплава / площадь из-за воздействия расплавленной фторидной соли коррелировала с начальным содержанием Cr в сплавах и соответствовала содержанию Cr, измеренному в солях после испытаний на коррозию. Также было обнаружено, что потеря веса / площадь сплавов коррелирует с концентрацией углерода, присутствующего в сплавах с номинальным содержанием 20% Cr, из-за образования фаз карбида хрома на границах зерен.Было обнаружено, что механизмы коррозии хлоридной соли аналогичны механизмам, наблюдаемым в FLiNaK, но химическое воздействие оказалось менее агрессивным. Гальваническое покрытие сульфаматом Ni и плазменное напыление Mo купонов сплава Fe-Ni-Cr были исследованы для уменьшения растворения Cr. Химическое осаждение из паровой фазы пиролитического углерода и покрытия SiC также было исследовано для защиты композитов C / SiSiC. Результаты показывают, что никелирование потенциально может обеспечить защиту от коррозии сплавов в расплавленных фторидных солях.
Было отмечено, что коррозия происходит из-за избирательного воздействия Si-фазы в керамике C / SiSiC. Потеря веса сплава / площадь из-за воздействия расплавленной фторидной соли коррелировала с начальным содержанием Cr в сплавах и соответствовала содержанию Cr, измеренному в солях после испытаний на коррозию. Также было обнаружено, что потеря веса / площадь сплавов коррелирует с концентрацией углерода, присутствующего в сплавах с номинальным содержанием 20% Cr, из-за образования фаз карбида хрома на границах зерен.Было обнаружено, что механизмы коррозии хлоридной соли аналогичны механизмам, наблюдаемым в FLiNaK, но химическое воздействие оказалось менее агрессивным. Гальваническое покрытие сульфаматом Ni и плазменное напыление Mo купонов сплава Fe-Ni-Cr были исследованы для уменьшения растворения Cr. Химическое осаждение из паровой фазы пиролитического углерода и покрытия SiC также было исследовано для защиты композитов C / SiSiC. Результаты показывают, что никелирование потенциально может обеспечить защиту от коррозии сплавов в расплавленных фторидных солях. Кроме того, наличие промежуточного слоя оксида хрома на границе раздела между никелевым покрытием и подложкой из сплава может дополнительно повысить эффективность никелевого покрытия. Покрытие из пиролитического углерода и SiC на композитах C / SiSiC эффективно устраняет атаку фазы Si в композитах. Отслоение Mo-покрытия в FLiNaK помешало дальнейшему исследованию этого многообещающего подхода.
Кроме того, наличие промежуточного слоя оксида хрома на границе раздела между никелевым покрытием и подложкой из сплава может дополнительно повысить эффективность никелевого покрытия. Покрытие из пиролитического углерода и SiC на композитах C / SiSiC эффективно устраняет атаку фазы Si в композитах. Отслоение Mo-покрытия в FLiNaK помешало дальнейшему исследованию этого многообещающего подхода.
Факты о фториде калия, формула, свойства, применение, данные по безопасности
Фторид калия, представленный химической формулой KF, представляет собой неорганическое соединение, содержащее калий щелочного металла и фторид одноатомного аниона [1] .Он существует в твердом состоянии или в форме водного раствора, при этом минерал кароббиит представляет собой встречающийся в природе KF [1] . Он также присутствует в других соединениях, таких как дигидрат фторида калия (KFH 4 O 2 ) и тетрагидрат фторида калия (KFH 8 O 4 ) [1] .
Идентификация фторида калия | |
| Номер CAS | 7789-23-3 [1] |
| PubChem CID | 522689 [1] |
| ChemSpider ID | 23006 [2] |
| Номер ЕС | 232-151-5 [1, 3] |
| UNII | 9082WG1G3F [1] |
| Номер RTECS | TT0700000 |
| Ключ InChI | NROKBHXJSPEDAR-UHFFFAOYSA-M [1] |
Формула фторида калия
Как получают фторид калия
Его получают путем взаимодействия карбоната калия с избытком фтористоводородной кислоты и последующего испарения раствора с образованием кристаллов бифторида калия. [4] . Затем кристаллы нагревают для получения фторида калия, как показано следующими уравнениями [4] :
Затем кристаллы нагревают для получения фторида калия, как показано следующими уравнениями [4] :
K 2 CO 3 + 4HF → 2KHF 2 + H 2 O + CO 2 ↑
KHF 2 → KF + HF ↑
Реакции с другими соединениями
Нитрат серебра и фторид калия
Если водный раствор фторида калия смешать с раствором нитрата серебра, происходит реакция двойного замещения с образованием фторида серебра, как показано ниже. [5] :
2KF + 2AgNO 3 → 2KNO 3 + 2AgF
Фторид калия и бромистоводородная кислота
Когда фторид калия реагирует с бромистоводородной кислотой, он подвергается двойной реакции замещения с образованием бромида калия и фтористоводородной кислоты [6] :
КФ + HBr → KBr + HF
Фторид калия и вода
Взаимодействие фторида калия с водой приводит к его полной диссоциации, при этом ион фтора смешивается с водой с образованием плавиковой кислоты, а ионы калия остаются неактивными как ионы-наблюдатели. Ионное уравнение выглядит следующим образом: [7] :
Ионное уравнение выглядит следующим образом: [7] :
F — + H 2 O ↔ HF + OH —
Кристаллы фторида калия
Свойства и характеристики фторида калия
Общая недвижимость | |
| Молярная масса / молекулярный вес | 58,097 г / моль (безводный) [1, 3] |
Физические свойства | |
| Цвет и внешний вид | Белый / бесцветный расплывающийся кристаллический порошок [1] |
| Точка плавления | 858 ° C, 1576 ° F (безводный) [1, 3] |
| Точка кипения | 1502 ° C, 2741 ° F [1] |
| Плотность | 2.48 г см -3 [1, 3] |
| Состояние вещества при комнатной температуре | Цельный [1, 3] |
| pH | 8,5-10,3 при 25 ° C [9] |
| Растворимость | Не растворим в спирте, но растворим во фтористом водороде [1] |
| Растворимость в воде | 102 г / 100 мл при 25 ° C, 92 г / 100 мл при 18 ° C [1] |
| Магнитная восприимчивость ( χ ) | -23. 6 X 10 -6 см 3 моль -1 [8] 6 X 10 -6 см 3 моль -1 [8] |
Атомарные свойства | |
| Кристаллическая структура | Кубический |
Фторид калия, точечная структура Льюиса
Что используется для
- Фторирование соли как средство фторирования на уровне местных сообществ путем добавления KF к йодированной соли с концентрацией фторида менее 250 мг на кг [1] .
- Подготовка серебряного паяльного флюса, используемого мастерами-мастерами по металлу [1] .
- Повышение скорости химических реакций как катализатор в органическом синтезе [1] .
- Травление и матирование стекла из-за синтеза растворимых фторсиликатов [1] .
- Производство дезинфицирующих средств, инсектицидов и пестицидов [1] .
Это безопасно
Проглатывание или вдыхание чрезмерного количества KF может вызвать острую токсичность [1] . Поскольку он вызывает сильную коррозию, контакт с кожей может привести к сильным ожогам. [1] . Хотя он негорючий, при нагревании он разлагается с образованием токсичных паров [1] .
Поскольку он вызывает сильную коррозию, контакт с кожей может привести к сильным ожогам. [1] . Хотя он негорючий, при нагревании он разлагается с образованием токсичных паров [1] .
Артикул:
- Фторид калия — Pubchem.ncbi.nlm.nih.gov
- Фторид калия — Chemspider.com
- Фторид калия — Americanelements.com
- Карбонат калия взаимодействует с фтористым водородом — Chemiday.com
- Реакции осаждения — Chem.libretexts.org
- Балансир по химическим уравнениям — En.intl.chemicalaid.com
- Напишите чистое ионное уравнение для равновесия, которое устанавливается, когда фторид калия растворяется в воде — Chemistryfeedsolutions.wordpress.com
- Магнитная восприимчивость элементов и неорганических соединений — Gemstonemagnetism.com
- Фторид калия — Hamptonresearch.com
Взаимодействие металлического циркония и его сплавов Zry-2 и E110 с расплавом эвтектической соли LiF – NaF – KF, содержащей компоненты фторида циркония
Литература
Aomi, M. , Баба, Т., Мияшита, Т., Камимура, К., Ясуда, Т., Шинохара, Ю., и Такеда, Т. (2008). Оценка поведения гидридов при переориентации и механических свойств для оболочек твэлов с высоким выгоранием при промежуточном сухом хранении. Журнал Американского общества испытаний материалов International, 5 , 651–671. Поиск в Google Scholar
, Баба, Т., Мияшита, Т., Камимура, К., Ясуда, Т., Шинохара, Ю., и Такеда, Т. (2008). Оценка поведения гидридов при переориентации и механических свойств для оболочек твэлов с высоким выгоранием при промежуточном сухом хранении. Журнал Американского общества испытаний материалов International, 5 , 651–671. Поиск в Google Scholar
ASTM International (1999). Стандарт ASTM: Стандартная практика подготовки, очистки и оценки образцов для испытаний на коррозию. ASTM G1-03 (2011). Филадельфия, Пенсильвания, США.Искать в Google Scholar
Barborík, P., Vasková, Z., Boča, M., & Priščák, J. (2014). Физико-химические свойства системы (LiF + NaF + KF (eut.) + Na 7 Zr 6 F 31 ): фазовые равновесия, плотностные и объемные свойства, вязкость и поверхностное натяжение. Журнал химической термодинамики, 76 , 145–151. DOI: 10.1016 / j. jct.2014.03.024.10.1016 / j.jct.2014.03.024 Искать в Google Scholar
Бастл, З., Сенкевич, А.И. , Спировова, И., & Вртилкова, В. (2002). Спектроскопия остовного уровня с угловым разрешением окисления сплава Zr1Nb кислородом, водой и пероксидом водорода. Анализ поверхности и интерфейса, 34 , 477–480. DOI: 10.1002 / sia.1342.10.1002 / sia.1342 Искать в Google Scholar
, Спировова, И., & Вртилкова, В. (2002). Спектроскопия остовного уровня с угловым разрешением окисления сплава Zr1Nb кислородом, водой и пероксидом водорода. Анализ поверхности и интерфейса, 34 , 477–480. DOI: 10.1002 / sia.1342.10.1002 / sia.1342 Искать в Google Scholar
Бернарде, В., Гомес, С., Дельпё, С., Дюбуа, М., Герэн, К., Авиньан, Д., Реноден, Г., и Дюкло, Л. (2009). Защита ядерного графита от фторидных расплавов с помощью стеклоуглеродных отложений. Журнал ядерных материалов, 384 , 292–302.DOI: 10.1016 / j.jnucmat.2008.11.032.10.1016 / j.jnucmat.2008.11.032 Искать в Google Scholar
Boča, M., Danielik, V., Ivanová, Z., Mikšíková, E., & Kubíková, B . (2007). Фазовые диаграммы систем KF-K 2 TaF 7 и KF-Ta 2 O 5 . Журнал термического анализа и калориметрии, 90 , 159–165. DOI: 10.1007 / s10973-006-7700-5.10.1007 / s10973-006-7700-5 Искать в Google Scholar
Cox, B. (2005). Некоторые мысли о механизмах внутриреакторной коррозии циркониевых сплавов.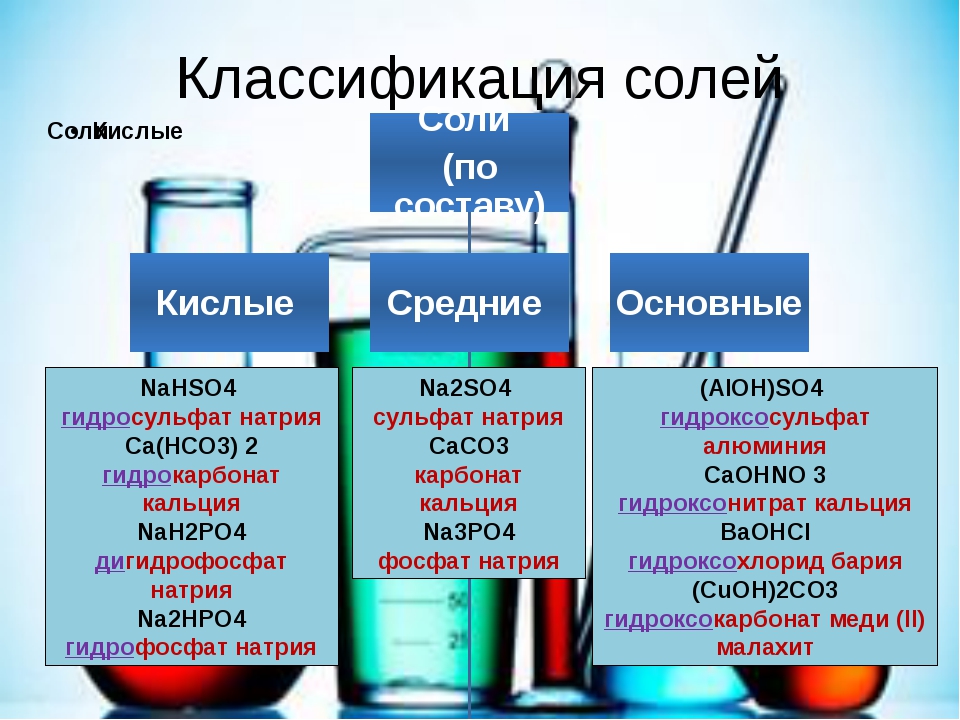 Журнал ядерных материалов, 336 , 331–368. DOI: 10.1016 / j.jnucmat.2004.09.029.10.1016 / j.jnucmat.2004.09.029 Искать в Google Scholar
Журнал ядерных материалов, 336 , 331–368. DOI: 10.1016 / j.jnucmat.2004.09.029.10.1016 / j.jnucmat.2004.09.029 Искать в Google Scholar
Danielik, V., Fellner, P., & Matal, O. (2009). Коррозия никеля в расплаве смеси LiF-NaF-ZrF 4 . Acta Chim Slovaca, 2 , 3–11. Поиск в Google Scholar
Эль-Рахман, Х.А.А., Барака, А.М., Морси, М.С., и Эль-Гвад, С.А.А. (1994). Роль концентрации оксид-иона в окислительном поведении циркония в расплаве NaNO 3 -KNO 3 эвтектика. Тонкие твердые пленки, 247 , 56–63. DOI: 10.1016 / 0040-6090 (94)-6.10.1016 / 0040-6090 (94)-6 Искать в Google Scholar
Ghosh, S., Vandarkuzhah, S., Venkatesh, P., Seenivasan, G., Субраманиан, Т., Редди, Б.П., и Нагараджан, К. (2009). Электрохимические исследования окислительно-восстановительного поведения циркония в расплаве эвтектики LiCl – KCl. Журнал электроаналитической химии, 627 , 15–27. DOI: 10.1016 / j.jelechem.2008. 12.011.10.1016 / j.jelechem.2008.12.011 Искать в Google Scholar
12.011.10.1016 / j.jelechem.2008.12.011 Искать в Google Scholar
Gil, A., Медрано, М., Марторелл, И., Ласаро, А., Доладо, П., Залба, Б., и Кабеза, Л. Ф. (2010). Современное состояние высокотемпературных аккумуляторов тепловой энергии для производства электроэнергии. Часть 1 — Концепции, материалы и моделирование. Обзоры возобновляемой и устойчивой энергетики, 14 , 31–55. DOI: 10.1016 / j.rser.2009.07.035.10.1016 / j.rser.2009.07.035 Искать в Google Scholar
Гийо, С., Фаик, А., Рахматуллин, А., Ламберт, Дж., Верон, Э. , Эчегут, П., Бессада, К., Кальве, Н., & Пи, X.(2012). Коррозионные эффекты между расплавленными солями и теплоаккумулирующим материалом для концентрированных солнечных электростанций. прикладная энергия, 94 , 174–181. DOI: 10.1016 / j.apenergy.2011.12.057.10.1016 / j.apenergy.2011.12.057 Искать в Google Scholar
Ким Ю. Э., Парк Дж. У. и Кливленд Дж. (2006). База данных теплофизических свойств материалов для легководных и тяжеловодных реакторов. Вена, Австрия: Международное агентство по атомной энергии, поиск в Google Scholar
Вена, Австрия: Международное агентство по атомной энергии, поиск в Google Scholar
Krýsa, J., Maixner, J., Matějka, P., & Vrtílková, V. (2000). Структура и состав пленок оксида циркония, сформированных в воде высокого давления с различной концентрацией Li + при 360 ° C. Химия и физика материалов, 63 , 1–8. DOI: 10.1016 / s0254-0584 (99) 00180-7.10.1016 / s0254-0584 (99) 00180-7 Искать в Google Scholar
Кубикова Б., Мацкова И. и Боча М. (2013). Фазовый анализ и объемные свойства системы (LiF – NaF – KF) eut -K 2 ZrF 6 . Monatshefte für Chemie – Chemical Monthly, 144 , 295–300. DOI: 10.1007 / s00706-012-0886-2.10.1007 / s00706-012-0886-2 Искать в Google Scholar
Кутти Т. Р., Рави К. и Гангули К. (1999). Исследования горячей твердости Zr и его сплавов для ядерных реакторов. Журнал ядерных материалов, 265 , 91–99. DOI: 10.1016 / s0022-3115 (98) 00610-2.10.1016 / s0022-3115 (98) 00610-2 Искать в Google Scholar
Квон, О. Х., Эом, К. Б., Ким, Дж. И., Сух, Дж.М. и Чон К. Л. (2011). Механические и лучевые свойства циркониевых сплавов, облученных в ханаро. Ядерная инженерия и технологии, 43 , 19–24. DOI: 10.5516 / net.2011.43.1.019.10.5516 / net.2011.43.1.019 Поиск в Google Scholar
Х., Эом, К. Б., Ким, Дж. И., Сух, Дж.М. и Чон К. Л. (2011). Механические и лучевые свойства циркониевых сплавов, облученных в ханаро. Ядерная инженерия и технологии, 43 , 19–24. DOI: 10.5516 / net.2011.43.1.019.10.5516 / net.2011.43.1.019 Поиск в Google Scholar
Marcus, P. (2002). Механизмы коррозии в теории и на практике (2-е изд.). Нью-Йорк, Нью-Йорк, США: Марсель — Деккер. Поиск в Google Scholar
МакДивитт, С. М., Абрахам, Д. П., Парк, Дж. Ю., и Кейзер, Д. Д., младший (1997). Отходы из нержавеющей стали и циркония образуются в результате обработки отработавшего ядерного топлива. Журнал Общества минералов, металлов и материалов (TMS), 49 , 29–32. DOI: 10.1007 / bf02914763.10.1007 / bf02914763 Поиск в Google Scholar
Медрано, М., Гил, А., Марторелл, И., Потау, X., и Кабеза, Л. Ф. (2010). Современное состояние высокотемпературных аккумуляторов тепловой энергии для производства электроэнергии. Часть 2 — Примеры из практики. Обзоры возобновляемой и устойчивой энергетики, 14 , 56–72. DOI: 10.1016 / j.rser.2009.07.036.10.1016 / j.rser.2009.07.036 Искать в Google Scholar
DOI: 10.1016 / j.rser.2009.07.036.10.1016 / j.rser.2009.07.036 Искать в Google Scholar
Netriová, Z., Боча, М., Даниелик, В., и Микшикова, Е. (2009). Фазовая диаграмма системы KF-K 2 TaF 7 -Ta 2 O 5 . Журнал термического анализа и калориметрии, 95 , 111–115. DOI: 10.1007 / s10973-008-9063-6.10.1007 / s10973-008-9063-6 Искать в Google Scholar
Northwood, D. O. (1985). Разработка и применение циркониевых сплавов. Материалы и дизайн, 6 , 58–70. DOI: 10.1016 / 0261-3069 (85)
-7.10.1016 / 0261-3069 (85)
-7 Искать в Google Scholar
Olson, L.К., Амбросек, Дж. У., Шридхаран, К., Андерсон, М. Х., и Аллен, Т. Р. (2009). Коррозия материалов в расплаве соли LiF – NaF – KF. Журнал химии фтора, 130 , 67–73. DOI: 10.1016 / j.jfluchem.2008.05.008.10.1016 / j.jfluchem.2008.05.008 Поиск в Google Scholar
Павлик В. и Боча М. (2012). Коррозия диборида титана в расплаве FLiNaK (eut) .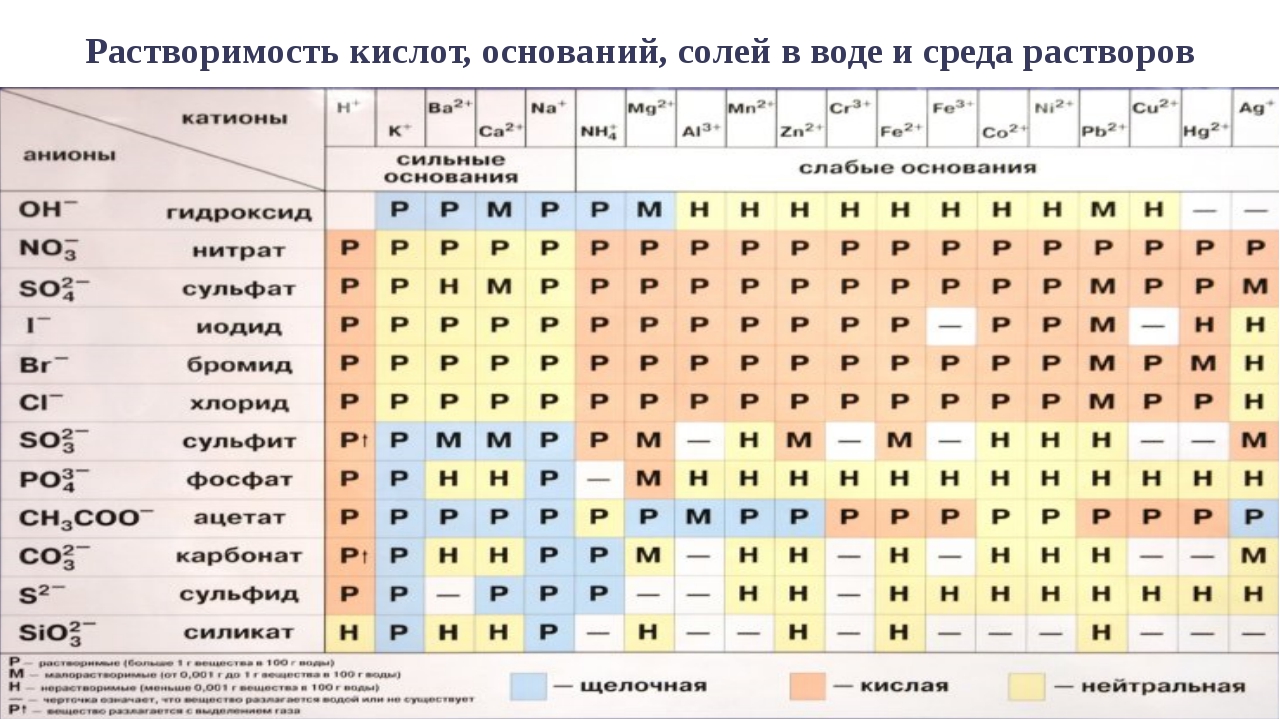 Химические документы, 66 , 1073–1077. DOI: 10.2478 / s11696-012-0202-y.10.2478 / s11696-012-0202-y Искать в Google Scholar
Химические документы, 66 , 1073–1077. DOI: 10.2478 / s11696-012-0202-y.10.2478 / s11696-012-0202-y Искать в Google Scholar
Podor, R., Дэвид, Н., Рапин, К., Виласи, М., и Бертод, П. (2007). Механизмы образования коррозионного слоя при погружении циркония в (Fe) -содержащий расплав стекла. Наука о коррозии, 49 , 3226–3240. DOI: 10.1016 / j.corsci.2007.03.005.10.1016 / j.corsci.2007.03.005 Искать в Google Scholar
Rudling, P., Strasser, A., & Garzarolli, F. (2007). Сварка циркониевых сплавов . Скултуна, Швеция: Advanced Nuclear Technology International, поиск в Google Scholar
Salanne, M., Саймон, К., Терк, П., и Мэдден, П. А. (2009). Теплопроводные свойства расплавов фторидов: определение из первых принципов. Journal of Fluorine Chemistry , 130, 38–44. DOI: 10.1016 / j.jfluchem.2008.07.013.10.1016 / j.jfluchem.2008.07.013 Искать в Google Scholar
Shankar, AR, Raju, VR, Rao, MN , Мудали, Великобритания, Хатак, Х.С., и Радж, Б.
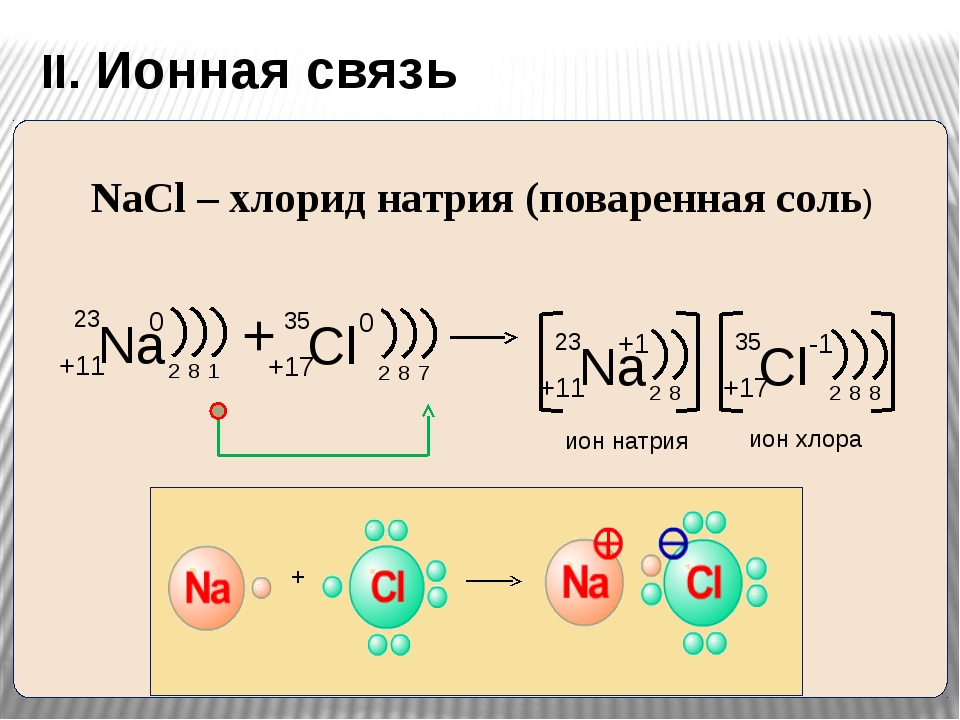

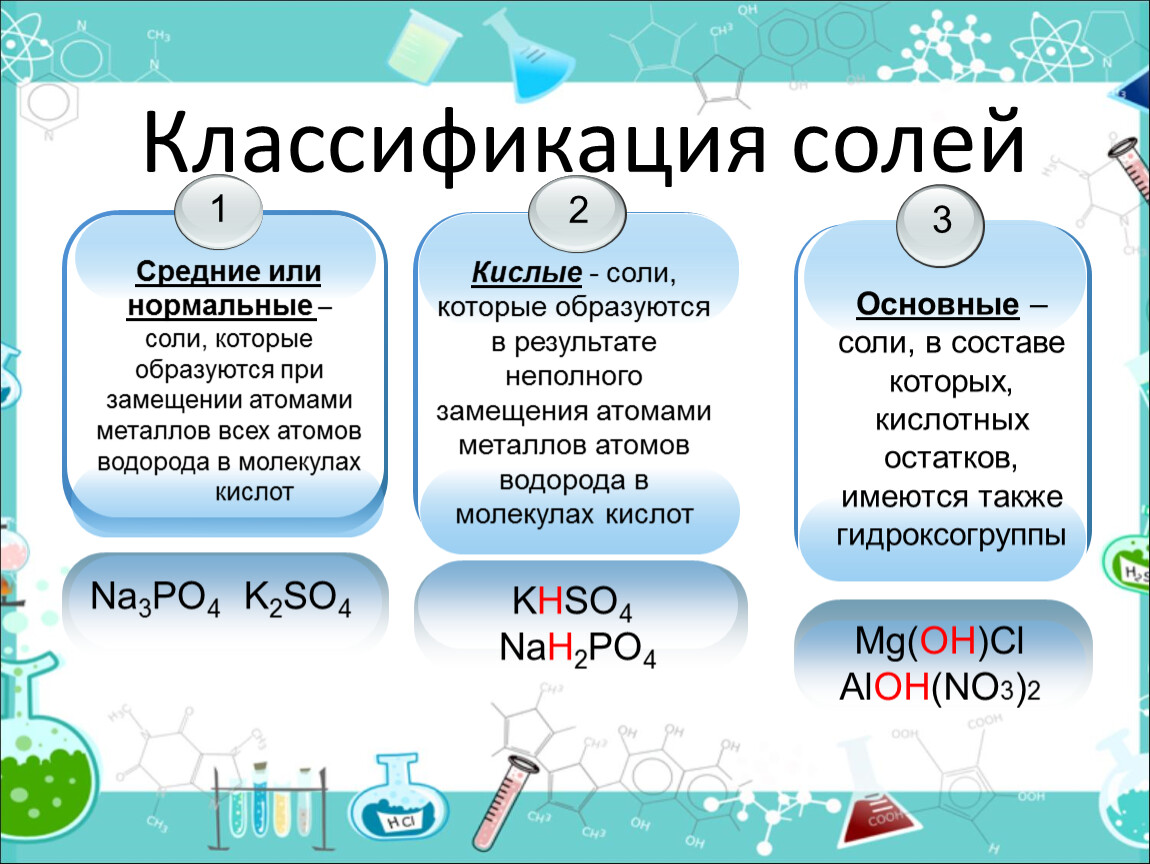

 potassium fluoride rus. калий фтористый; калия фторид … Chemijos terminų aiškinamasis žodynas
potassium fluoride rus. калий фтористый; калия фторид … Chemijos terminų aiškinamasis žodynas Свое название Ф. получил от греческого слова φτοριος… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Свое название Ф. получил от греческого слова φτοριος… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
