Кислородсодержащие органические соединения — это… Что такое Кислородсодержащие органические соединения?
- Кислородсодержащие органические соединения
Кислородсодержа́щие органи́ческие соедине́ния — соединения, содержащие в молекуле связи углерод — водород и углерод — кислород. К кислородсодержащим относится большая часть органических соединений.
Классификация
Важнейшие представители
См. также
CH He CLi CBe CB CC CN CO CF Ne CNa CMg CAl CSi CP CS CCl CAr CK CCa CSc CTi CV CCr CMn CFe CCo CNi CCu CZn CGa CGe CAs CSe CBr CKr CRb CSr CY CZr CNb CMo CTc CRu CRh CPd CAg CCd CIn CSn CSb CTe CI CXe CCs CBa CHf CTa CW CRe COs CIr CPt CAu CHg CTl CPb CBi CPo CAt Rn Fr Ra Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Fl Uup Lv Uus Uuo ↓ СLa CСе СPr СNd Pm СSm СEu СGd СTb СDy СHo СEr СTm СYb СLu Ac СTh СPa CU СNp СPu СAm СCm СBk Cf СEs Fm Md No Lr
Категория:Химическая связь с углеродом Основные соединения Большое применение в химии Академические исследования Соединение неизвестно/не получено - Кислородсодержащие органические соединения
Wikimedia Foundation. 2010.
- Кислородный редуктор
- Кислота нитрилотриметилфосфоновая
Смотреть что такое «Кислородсодержащие органические соединения» в других словарях:
Органические соединения — Органические вещества класс соединений, в состав которых входит углерод (за исключением карбидов, карбонатов, оксидов углерода и цианидов). Название «органические соединения» появилось на ранней стадии развития химии и говорит само за себя ученые … Википедия
Азотсодержащие органические соединения — один из важнейших типов органических соединений. В их состав входит азот. Они содержат в молекуле связь углерод водород и азот углерод. В нефти содержится азотсодержащий гетероцикл пиридин. Азот входит в состав белков,нуклеиновых кислот и… … Википедия
Германийсодержащие органические соединения — Германийорганические соединения металлоорганические соединения содержащие связь «германий углерод». Иногда ими называются любые органические соединения, содержащие германий. Первое германоорганическое соединение тетраэтилгерман, было… … Википедия
Кремний-органические соединения — Кремнийорганические соединения соединения, в молекулах которых имеется непосредственная связь кремний углерод. Кремнийорганические соединения иногда называют силиконами, от латинского названия кремния силициум . Кремнийорганические соединения… … Википедия
Органические вещества — Органические соединения, органические вещества класс химических соединений, в состав которых входит углерод (за исключением карбидов, угольной кислоты, карбонатов, оксидов углерода и цианидов).[1] Содержание 1 История 2 Класси … Википедия
Металлоорганические соединения — Металлорганические соединения (МОС) органические соединения, в молекулах которых существует связь атома металла с атомом/атомами углерода. Содержание 1 Типы металлоорганических соединений 2 … Википедия
Галогенорганические соединения — Галогенорганические соединения органические вещества, содержащие хотя бы одну связь C Hal углерод галоген. Галогенорганические соединения, в зависимости от природы галогена, подразделяют на: Фторорганические соединения;… … Википедия
Металлорганические соединения — Металлоорганические соединения(МОС) органические соединения, в молекулах которых существует связь атома металла с атомом/атомами углерода. Содержание 1 Типы металлоорганических соединений 2 Способы получения … Википедия
Оловоорганические соединения — органические соединения, в которых присутствует связь олово углерод , могут содержать как двухвалентное, итак и четырёхвалентное олово. Содержание 1 Методы синтеза 2 Типы 3 … Википедия
Гетероциклические соединения — (гетероциклы) органические соединения, содержащие циклы, в состав которых наряду с углеродом входят и атомы других элементов. Могут рассматриваться как карбоциклические соединения с гетерозаместителями (гетероатомами) в цикле. Наиболее… … Википедия
dic.academic.ru
Кислородсодержащие органические вещества. Видеоурок. Химия 9 Класс
Тема: Органические вещества
Урок: Кислородсодержащие органические вещества
Свойства кислородсодержащих органических веществ очень разнообразны, и они определяются тем, в состав какой группы атомов входит атом кислорода. Эта группа называется функциональной.
Группу атомов, которая существенным образом определяет свойства органического вещества, называют функциональной группой.
Существует несколько различных кислородсодержащих групп.
Производные углеводородов, в которых один или несколько атомов водорода замещены на функциональную группу, относят к определенному классу органических веществ (Таб. 1).
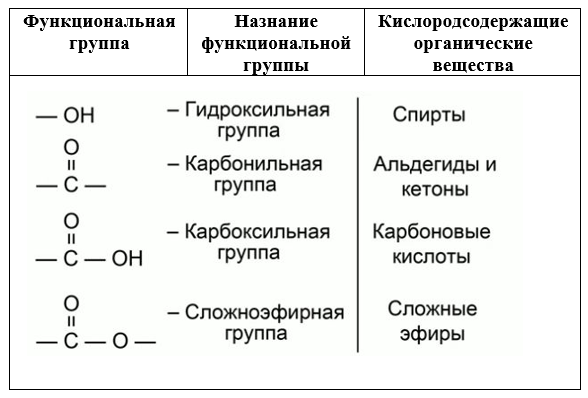
Таб. 1. Принадлежность вещества к определенному классу определяется функциональной группой
Одноатомные предельные спирты
Рассмотрим отдельных представителей и общие свойства спиртов.
Простейший представитель этого класса органических веществ – метанол, или метиловый спирт. Его формула – СН3ОН. Это бесцветная жидкость с характерным спиртовым запахом, хорошо растворимая в воде. Метанол – это очень ядовитое вещество. Несколько капель, принятых внутрь, приводят к слепоте человека, а немного большее его количество – к смерти! Раньше метанол выделяли из продуктов пиролиза древесины, поэтому сохранилось его старое название – древесный спирт. Метиловый спирт широко применяется в промышленности. Из него изготавливают лекарственные препараты, уксусную кислоту, формальдегид. Его применяют также в качестве растворителя лаков и красок.
Не менее распространенным является и второй представитель класса спиртов – этиловый спирт, или этанол.
Его формула – С2Н5ОН. По своим физическим свойствам этанол практически ничем не отличается от метанола. Этиловый спирт широко применяют в медицине, также он входит в состав спиртных напитков. Из этанола получают в органическом синтезе достаточное большое количество органических соединений.Получение этанола. Основным способом получения этанола является гидратация этилена. Реакция происходит при высокой температуре и давлении, в присутствии катализатора.
СН2=СН2 + Н2О → С2Н5ОН
Реакция взаимодействия веществ с водой называется гидратацией.
Многоатомные спирты
К многоатомным спиртам относятся органические соединения, в молекулах которых содержится несколько гидроксильных групп, соединенных с углеводородным радикалом.
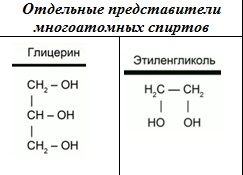
Рис. 1.
Одним из представителей многоатомных спиртов является глицерин (1,2,3-пропантриол). В состав молекулы глицерина входят три гидроксильных группы, каждая из которых находится у своего атома углерода. Глицерин – это очень гигроскопичное вещество. Он способен поглощать влагу из воздуха. Благодаря такому свойству, глицерин широко используется в косметологии и медицине. Глицерин обладает всеми свойствами спиртов. Представителем двух атомных спиртов является этиленгликоль. Его формулу можно рассматривать, как формулу этана, в которой атомы водорода у каждого атома замещены на гидроксильные группы. Этиленгликоль – это сиропообразная жидкость, сладковатая на вкус. Но она очень ядовита, и ни в коем случае ее нельзя пробовать на вкус! Этиленгликоль используется в качестве антифриза. Одним из общих свойств спиртов является их взаимодействие с активными металлами. В составе гидроксильной группы атом водорода способен замещаться на атом активного металла.
2С2Н5ОН + 2Na→ 2С2Н5ОNa+ H2↑
Получается этилат натрия, и выделяется водород. Этилат натрия – солеподобное соединение, которое относится к классу алкоголятов. В силу своих слабых кислотных свойств спирты не взаимодействуют с растворами щелочей.
Карбонильные соединения

Рис. 2. Отдельные представители карбонильных соединений
К карбонильным соединениям относятся альдегиды и кетоны. В составе карбонильных соединений находится карбонильная группа (см. Таб. 1). Простейшим альдегидом является формальдегид. Формальдегид – это газ с резким запахом,
Формальдегид широко используют в промышленности для изготовления пластмасс, которые не размягчаются при нагревании.
Простейшим представителем кетонов является ацетон. Это жидкость, которая хорошо растворяется в воде, и в основном его применяют в качестве растворителя. Ацетон обладает очень резким запахом.
Карбоновые кислоты
В составе карбоновых кислот находится карбоксильная группа (см. Рис. 1). Простейшим представителем этого класса является метановая, или муравьиная кислота. Муравьиная кислота содержится в муравьях, в крапиве и хвое ели. Ожог крапивой – это результат раздражающего действия муравьиной кислоты.

Таб. 2.
Наибольшее значение имеет уксусная кислота. Она необходима для синтеза красителей, медикаментов (например, аспирина), сложных эфиров, ацетатного волокна. 3-9%-ный водный раствор уксусной кислоты – уксус, вкусовое и консервирующее средство.
Кроме муравьиной и уксусной карбоновых кислот, существует целый ряд природных карбоновых кислот. К ним относятся лимонная и молочная, щавелевая кислоты. Лимонная кислота содержится в соке лимона, малины, крыжовника, в ягодах рябины и т.д. Широко применяется в пищевой промышленности и медицины. Лимонную и молочную кислоты используют в качестве консервантов. Молочную кислоту получают путем брожения глюкозы. Щавелевая кислота используется для удаления ржавчины и в качестве красителя. Формулы отдельных представителей карбоновых кислот приведены в Таб. 2.
В высших жирных карбоновых кислотах содержится, как правило, 15 и более атомов углерода. Например, стеариновая кислота содержит 18 атомов углерода. Соли высших карбонов кислот натрия и калия называются мылами.Стеарат натрия С17Н35СООNa входит в состав твердого мыла.
Между классами кислородсодержащих органических веществ существует генетическая связь.
Подведение итога урока
Вы узнали, что свойства кислородсодержащих органических веществ зависят от того, какая функциональная группа входит в состав их молекул. Функциональная группа определяет принадлежность вещества к определенному классу органических соединений. Между кислородсодержащими классами органических веществ существует генетическая связь.
Список рекомендованной литературы
1. Рудзитис Г.Е. Неорганическая и органическая химия. 9 класс: Учебник для общеобразовательных учреждений: базовый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М.: Просвещение, 2009.
2. Попель П.П. Химия. 9 класс: Учебник для общеобразовательных учебных заведений / П.П. Попель, Л.С. Кривля. – К.: ИЦ «Академия», 2009. – 248 с.: ил.
3. Габриелян О.С. Химия. 9 класс: Учебник. – М.: Дрофа, 2001. – 224с.
Рекомендованные ссылки на интернет-ресурсы
1. Interneturok.ru (Источник).
2. Hemi.nsu.ru (Источник).
3. ChemPort.Ru (Источник).
4. ХиМиК.ру (Источник).
Рекомендованное домашнее задание
1. Рудзитис Г.Е. Неорганическая и органическая химия. 9 класс: Учебник для общеобразовательных учреждений: базовый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М.: Просвещение, 2009. – №№ 2-4, 5 (с. 173).
2. Приведите формулы двух гомологов этанола и общую формулу гомологического ряда предельных одноатомных спиртов.
3. Что такое мыло?
interneturok.ru
Презентация к уроку по химии (10 класс) на тему: Презентация к уроку: Классификация кислородсодержащих органических веществ
Слайд 1
Кислородсодержащие органические соединения урок химии 10 класс Москвичева Ирина Анатольевна учитель химии МОУ « Сланцевская средняя общеобразовательная школа № 6»Слайд 2
Задачи урока: познакомиться с классификацией кислородсодержащих органических соединений; построение гомологических рядов веществ; выявление возможных видов изомерии; построение структурных формул изомеров веществ, номенклатура веществ.
Слайд 3
Классификация веществ С х Н у О z карбоновые кислоты альдегиды кетоны эфиры спирты фенолы одно- атомные -много R – OH R–( OH ) n простые сложные OH = R – C — O OH = R – C — O H — овая кислота -аль R – C – R || O -он R – O – R = R – C — O O – R — ол — n ол
Слайд 4
Гомологический ряд СН 3 – ОН С 2 Н 5 – ОН С 3 Н 7 – ОН С 4 Н 9 – ОН С 5 Н 11 – ОН метан ол этан ол пропан ол-1 бутан ол-1 пентан ол-1 Спирты С n H 2n+2 O
Слайд 5
Карбоновые кислоты = Н – C — O OH = СН 3 – C — O OH = СН 3 – СН 2 – C — O OH метан овая кислота (муравьиная) этан овая кислота (уксусная) пропан овая кислота ( пропионовая ) С n H 2n O 2
Слайд 6
Альдегиды = Н – C — O H = СН 3 – C — O H = СН 3 – СН 2 – C — O H метан аль муравьиный альдегид (формальдегид) этан аль уксусный альдегид (ацетальдегид) пропан аль пропионовый альдегид С n H 2n O
Слайд 7
Кетоны СН 3 – C – СН 3 || O СН 3 – СН 2 – C – СН 3 || O СН 3 – СН 2 – СН 2 – C – СН 3 || O пропан он (ацетон) бутан он пентан он-2 С n H 2n O
Слайд 8
Простые эфиры СН 3 – О –СН 3 С 2 Н 5 – О –СН 3 С 2 Н 5 – О –С 2 Н 5 С 3 Н 7 – О –С 2 Н 5 С 3 Н 7 – О –С 3 Н 7 диметил овый эфир метиэтил овый эфир диэтил овый эфир этилпропил овый эфир дипропил овый эфир С n H 2n+2 O Вывод: простые эфиры – производные предельных одноатомных спиртов.
Слайд 9
Сложные эфиры = Н – C — O O – СН 3 = СН 3 – C — O O – С Н 3 = СН 3 – СН 2 – C — O O – СН 3 метиловый эфир муравьиной кислоты ( метил формиат ) метиловый эфир уксусной кислоты ( метил ацетат ) метиловый эфир пропионовой кислоты С n H 2n O 2 Вывод: сложные эфиры – производные карбоновых кислот и спиртов.
Слайд 10
спирты эфиры кетоны альдегиды карбоновые кислоты Изомерия и номенклатура изомерия углеродного скелета межклассовая (сложные эфиры) углеродного скелета межклассовая (кетоны) углеродного скелета положения f- группы ( -С =О ) межклассовая (альдегиды) углеродного скелета положения f- группы ( -ОН ) межклассовая (простые эфиры) углеродного скелета межклассовая
Слайд 11
Составление формул изомеров. Номенклатура веществ. Задание: составьте структурные формулы возможных изомеров для веществ состава С 4 Н 10 О; С 4 Н 8 О 2 ; С 4 Н 8 О . К каким классам они принадлежат? Назовите все вещества по систематической номенклатуре. С 4 Н 10 О С 4 Н 8 О 2 С 4 Н 8 О С n H 2n+2 O С n H 2n O 2 С n H 2n O спирты и простые эфиры карбоновые кислоты и сложные эфиры альдегиды и кетоны
Слайд 12
СН 3 – СН 2 – СН – СН 3 | ОН СН 3 | СН 3 – С – СН 3 | ОН СН 3 – О – СН 2 – СН 2 – СН 3 СН 3 – СН 2 – О – СН 2 – СН 3 бутанол-1 2-метилпропанол-1 бутанол-2 2-метилпропанол-2 метилпропиловый эфир диэтиловый эфир I спирты II спирт III спирт
Слайд 13
= СН 3 – СН 2 – СН 2 – C — O OH = СН 3 – СН – C — O OH | СН3 = СН 3 – СН 2 – C — O O – СН 3 = СН 3 – C — O O – СН 2 – СН 3 бутановая кислота 2-метилпропановая кислота метиловый эфир пропионовой к-ты этиловый эфир уксусной кислоты
Слайд 14
= СН 3 – СН 2 – СН 2 – C — O H = СН 3 – СН – C — O H | СН3 СН 3 – СН 2 – C – СН 3 || O бутаналь 2-метилпропаналь бутанон-2
Слайд 15
Проверь себя! 1. Установите соответствие: общая формула класс вещество R – COOH R – O – R R – COH R – OH R – COOR 1 R – C – R || O сл. эфиры спирты карб . к-ты кетоны альдегиды пр. эфиры а) С 5 Н 11 –ОН б) С 6 Н 13 –СОН в) С 4 Н 9 –О–СН 3 г) С 5 Н 11 –СООН д) СН 3 –СО–СН 3 е) СН 3 –СООС 2 Н 5 2. Назовите вещества по систематической номенклатуре.
Слайд 16
Проверь себя! I II III IV V VI 3 6 5 2 1 4 Г В Б А Е Д
Слайд 17
Домашнее задание Параграф (17-21) – 1 и 2 части упр. 1,2,4,5 стр. 153-154 2 стр. 174 Урок окончен!
nsportal.ru
Урок обобщение » Кислородсодержащие органические соединения»
Тема урока: Кислородосодержащие органические соединения
Класс: 10 класс (базовый уровень)
Тип урока: урок обобщения и систематизации знаний
Цель урока:обобщить и систематизировать знания учащихся о кислородсодержащих
органических веществах.
Задачи урока:
Образовательные:
— создать условия для обобщения, систематизации знаний учащихся о кислородсодержащих соединениях, их составе, строении, свойствах, и применении.
Развивающие:
— содействовать развитию познавательной и творческой активности учащихся через выполнение эксперимента; развивать умение сравнивать, анализировать; быстро и чётко формулировать и высказывать свои мысли; умение осуществлять самоконтроль, взаимоконтроль, самооценку и самокоррекцию учебной деятельности; умение работать в паре.
Воспитательные:
— обеспечить формирование интереса к химической науке через эксперимент; убедить учащихся в практической значимости науки химии.
Форма работы: фронтальная,парная, индивидуальная
Оборудование:
Набор лабораторной посуды: пробирки, ступки,пестики
Набор реактивов:NaOH, CuSO4, FeCl3
Таблеткилевомицетин и парацетамол
Уксус столовый, лимон, растительное масло, йодная настойка,крем, ацетон, зарядка для телефона.
карта ученика Тест
Ход урока
I. Организационный этап, этап подготовки учащихся к учебно-познавательной деятельности
Учитель: мы с вами изучаем органические соединения. Какие органические соединения мы изучили
Ответы учащихся:
Учитель:Тема сегодняшнего урока: «Кислородсодержащие органические соединения». На уроке мы должны с вами систематизировать, обобщить знания об этих веществах, т.к. мы постоянно с ними встречаемся в повседневной жизни и не можем без них обойтись.
На столах у вас есть Карты оценки знаний. После выполнения задания вы будите оценивать свои знания . Критерии оценок записаны.
II. Этап обобщения и систематизации знаний и способов деятельности
II. 1. Классификация, номенклатура и изомерия кислородсодержащих органических соединений
Учитель:Давайте вспомним состав и строение этих веществ.
Дать определение : какие вещества называются спиртами, альдегидами, кимлотами.
Вспомнить обшие формулы этих соединений на магнитной . (С п Н2п+2 О; С п Н2п О С п Н2п О2)
Предлагаю вам выполнить задание №1 (слайд №2) назовите вещества, найдите изомеры .
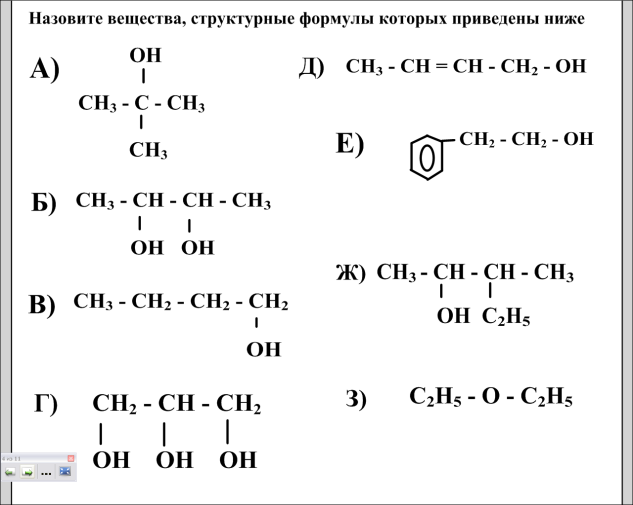
Задание №2
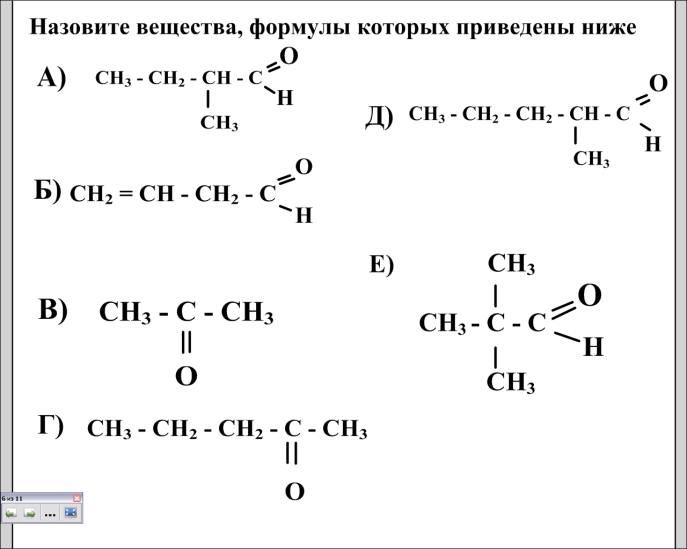
Задание № 3
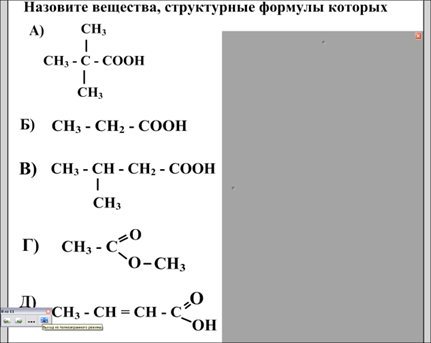
Учитель организует обсуждение выполненного задания и акцентирует внимание учащихся на взаимосвязи состава, строения и свойств веществ.
Оцените свои знания заполните 3 пункта по карте.
2. Химические свойства. Химические свойства кислородсодержащих соединений определяется функциональной группой и углеводородным радикалом. П еречислим основные свойства наших соединений. И условия их проводения.
А) Химические свойства спиртов: Окисление спиртов ( Сu О), с активными металлами, с галогеноводородам, Дегидротации ( Н2 SO4) С образованием непредельных соединений, и простых эфиров, с органическими кислотами.
Б) Альдегидов : Окисление альдегидов ( Cu(OH)2, Ag2O) восстановление до спиртов
В)Кислот: С металлами, основными оксидами, с солями, спиртами, с хлором.
3 Физкультурная пауза.
В классе развешаны карточки с формулами кислот , спиртов, альдегидов. Учитель читает предложение, учащиеся должны повернуть голову, в ту сторону, где находиться это вещество.
— в названии используется суффикс ол (аль), окончание овая
— возможна изомерия положения функциональной группы
— межклассовым изомером являются кетоны
— межклассовым изомером являются простые эфиры
— межклассовым изомером являются сложные эфиры
— между молекулами возможна водородная связь
— качественной реакцией является реакция «серебряного зеркала»
— образуются в результате реакции Кучерова.
— образуются окислением или дегидрированием первичных спиртов
— получают гидратацией алкенов
— относятся к кислородсодержащим органическим соединениям.
II. 2. Генетическая связь между классами органических соединений
Решить цепочку превращений:
Решить задачу: Соединение с молекулярной формулой С3 Н8 О подвергли реакции окисления в результате получили вещество состава С3 Н6 О. Э то вещество вступило в реакцию « серебряного зеркала», образуя вещество состава С3 Н6 О2.. При действия на него гидроксида кальция получили вещество , которой используется в качестве пищевой добавки по кодом Е 282. О но препятствует росту плесени в хлебобулочных и кондитерских изделиях. О пределите формулу довавки Е282. Напишите уравнения реакций. ( Пропионат кальция)
Оцените свои знания
II. 3. Качественные реакциина кислородсодержащие органические соединения(одноатомные и многоатомные спирты, карбоновые кислоты, альдегиды, фенол) (повторить, проговорить)
Учитель:Известно,что в лекарственных препаратах содержатся функциональные группы кислородсодержащих соединений. Используя, предложенные реактивы установите, какие функциональные группы содержатся в предложенных лекарственных препаратах: левомицетине и парацетамоле.(слайд № 5) слайд №6, слай № 7
Лабораторный опыт № 1Цель: установить функциональную группу, содержащуюся в лекарстве левомицетин.
Левомицетин – это высокотоксичный антибиотик, его используют при лечении дизентерии, брюшного тифа.
Разотрите 1/2 таблетки левомицетина, поместите порошок в пробирку, прилейте к нему 2 мл воды, перемешайте. Добавьте немного раствора NaOH и 1-2 капли раствора CuSO4, перемешайте. Что наблюдаете?Сделайте вывод.
Лабораторный опыт № 2
Цель:установить функциональную группу, содержащуюся в лекарстве парацетамол. Парацетамол – препарат, оказывающий обезболивающее и жаропонижающее действие. Его применяют при повышенной температуре, зубной и головной боли.
Разотрите 1/2 таблетки парацетамола, поместите порошок в пробирку, добавьте 2 мл воды,
Перемешайте, прилейте к нему немного раствора FeCl3, перемешайте. Что наблюдаете? Сделайте вывод.
Учащиеся выполняют лабораторные опыты, полученные результаты вносят в т е т р а ь формулируют выводы.Учитель организует обсуждение полученных результатов.(слайды №6,7)
Оцените свои знания
3. Решить задачу: Сколько граммов бромэтана образуется если для реакции взяли 92 граммов этилового спирта , если выход продукта составляет 90 %
II. 5. Взаимосвязь свойств и применения кислородсодержащих органических веществ
Учитель: Ребята, как вы считаете, для чего мы изучаем строение, свойства, способы получения веществ?(для того, чтобы уметь грамотно применять вещества)
Давайте вспомним области применениянаиболее важных кислородсодержащих органических соединений. С лайд № 8, 9 10.
Применение кислородсодержащих веществ
О каком веществе идет речь?
1. Бесцветная жидкость с резким кисловатым запахом.
2. Если это вещество не содержит воду, то при 16.60С она «замерзает» — образуя бесцветные кристаллы.
3. Она содержится в некоторых растениях, моче, поте, желчи.
4. Человеческий организм служит своеобразной «фабрикой» по выработке этого вещества, за сутки выделяется 0,5 кг
5. Служит для получения полимеров, красителей, ацетатного шелка, фото- и кинопленки.
6. Используется для домашнего консервирования.
( Уксусная кислота) 1. Вязкая, низкокипящая жидкость (tкип =2900С).
2.Смешивается с водой в любых отношениях.
3. Им обрабатывают некоторые материалы (кожу, ткани), которые после этого приобретают мягкость и эластичность
4. Идет на изготовление лаков и красок.
5.Используется для производства незамерзающих смесей – антифризов.
6. Его производное используется как взрывчатое вещество и в медицине.
7. Содержится в организме человека.
(Глицерин)
1. Это вещество использовал человек, имя которого известно во всем мире и связано с почетнейшими премиями.
2. Сырьем для его производства являются две жидкости. Одна из них используется в медицине, для отделки нож, в парфюмерии.
3. Другое сырье является качественным реактивом на белок. Белок желтеет.
4. Вещество используется в медицине уже больше 100 лет, как одно из эффективнейших сердечных средств.
5. «Я пью его в мельчайших дозах на сахар, капая раствор.
А он способен бросить в воздух любую из ближайших гор».
Ответ: нитроглицерин
III. Этап подведения итогов урока
Учительподводит итоги урока, комментирует выставленные отметки.
IV. Рефлексия
Учительпредлагает учащимся оценить свою работу на уроке и сформулировать затруднения, с которыми они столкнулись при выполнении заданий, подумать, над какими вопросами следует еще поработать. Рефлексия должна помочь учащимся определиться с выбором задания для домашней работы.
1 вариант
Предельным одноатомным спиртам соответствуют формулы:
А) CH2O Б) C4H10O В) C2H6O Г) CH4O
Д) C2H4O2
2. Функциональная группа кислот :
А) карбонильная Б) карбоксильная В) гидроксильная
Этанол реагирует с веществами:
А) NaOH Б) Na В) HCl Г) CH3COOH Д) FeCl3Качественная реакция на фенолы — это реакция с
А) NaOH
Б) Cu(OH)2
В) CuO
Г) FeCl3
Д) HNO3Этаналь реагирует с веществами
А) метанолом
Б) водородом
В) аммиачным раствором оксида серебра
Г) гидроксидом меди (II)
Д) хлороводородом
2.
3.
4.
5.
2 вариант
Этанол реагирует с веществами:
А) NaOH Б) Na В) HCl Г) Ch4COOH Д) FeCl3
Функциональной группой спиртов является
А) — COH Б) — OH В) — COOH Г)- NH2 Д) — NO2
2-метилбутанол-2
А) непредельный спирт
Б) предельный спирт
В) одноатомный спирт
Г) третичный спирт
Д) альдегид
Вы не наблюдали реакцию
А) на многоатомные спирты
Б) окисление спирта
В) взаимодействие фенола с хлоридом железа (III)
Г) «медного зеркала»
Д) «серебряного зеркала»
Уксусная кислота реагирует с веществами
А) водородом
Б) хлором
В) пропанолом
Г) гидроксидом натрия
Д) метаналем
Ответы учащиеся оформляют в таблице:
1.2.
3.
4.
5.
infourok.ru
Кислородосодержащие органические соединения. Спирты
Цель урока — создать условия для:
1. Осознания и осмысления блока новой информации по теме, способствовать осознанию основного фактического материала через работу с учебником, дополнительной литературой, применение ИКТ, организацию работы в парах, выполнение лабораторной работы.
2. Способствовать обучению школьников умению находить необходимые сведения в тексте учебника, умению работать с дополнительной учебной литературой, кратко и точно записывать информацию по теме.
3. Воспитания ответственного отношения к учебной деятельности через организацию работы фронтально, индивидуально.
Задачи урока.
1. В ходе урока повторить ранее изученный материал: понятия — гомологи, изомеры; умение писать формулы гомологов и изомеров, давать название спиртам.
2. Организовать работу по открытию новых знаний.
3. Обобщить полученные знания. Организовать первоначальное закрепление полученных знаний.
Оборудование: компьютер, экран, проектор, презентация, лабораторное оборудование.
Формы организации деятельности учащихся на уроке: фронтальная, в парах, индивидуальная.
Ход урока
1. Организационный момент.
2. Основная часть.
Целеполагание и мотивация.
Фронтальная беседа:
1. Какой изучаем предмет?
2. Дайте определение химии.
3. Какой раздел химии изучаем в 10 классе?
4. Какие вещества изучает органическая химия?
5. С какими веществами мы уже познакомились?
6. Почему они так называются?
Нам предстоит познакомиться с кислородсодержащими органическими веществами.
Почему они так называются?
Значит, отличие их от предыдущих веществ – наличие кислорода.
Тема урока: “Кислородсодержащие органические вещества”.
Какую группу веществ, содержащих кислород, будем изучать, вам предстоит угадать.
Вещества мы непростые
И известны, с древних пор
В медицине применимы:
Дать инфекции отпор.
По свойствам мы не так просты.
А называемся …. (Спирты)
Из большой группы кислородсодержащих органических веществ будем изучать – спирты.
Слайд № 1. Презентация
Что мы, можем узнать о спиртах, цель нашего урока? (На столах лежат листочки с планом характеристики веществ, используя которые ученики сформулируют цель). Приложение 1, Слайд № 2
Выяснили, о чем будем говорить на сегодняшнем уроке, поставили цель, приступаем к ее осуществлению.
На столах лежит все необходимое для работы: учебник О.С. Габриелян, химия 10 класс, учебник Г.Е. Рудзитис, химия 10 класс, план характеристики веществ, необходимое лабораторное оборудование. Приложение 2
Информация по пунктам плана берется из предложенных источников, фиксируется в тетради учащимися и затем озвучивается, дополняется, сравнивается с эталоном (слайды).
Первый пункт плана. Определение, общая формула, функциональная группа, классификация.
Приложение 3. Слайды № 3, 4, 5, 6, 7
Спирты – производные углеводородов, в молекуле которых один или несколько атомов водорода замещены на соответствующее число гидроксильных групп. Общая формула R – (OH)n -ОН функциональная группа.
Классификация спиртов:
— по типу углеводородного радикала – предельные, непредельные, ароматические спирты.
— по числу гидроксильных групп – одноатомные, двухатомные, трехатомные спирты.
— по типу атома углерода, связанного с гидроксильной группой – первичные, вторичные, третичные спирты.
Из большой группы спиртов будем более подробно изучать предельные одноатомные спирты – алканолы.
Общая формула алканолов CnH2n +1OH.
Второй пункт плана. Гомологический ряд, номенклатура. Слайд №8
CH3OH метанол в названии алканолов участвует числительное и суффикс — ол
C2H5OH этанол
C3H7OH пропанол
Если цепь атомов углерода разветвленная, чтобы назвать спирт нужно применить правило. Например:
Третий пункт плана. Изомерия. Слайд №9
Для алканолов характерны следующие виды структурной изомерии:
А) углеродного скелета,
Б) положения функциональной группы,
В) межклассовая (алканолам изомерны простые эфиры).
Формулы изомеров можно рассмотреть на примере бутанола.
Четвертый пункт плана. Способы получения. Слайд № 10
Спиртов нет в природе в свободном состоянии, поэтому их получают с помощью химических реакций.
1) Гидролиз галогенопроизводных алканов водными растворами щелочей:
C2H5CL + KOH = C2H5OH + KCL
2) Гидратация алкенов:
CH2 = CH2 + H2O = CH3 – CH2OH
У метанола и этанола есть персональные способы получения:
CO + H2O = CH3OH
Брожение:
C6H12O6 —> 2 C2H5OH + 2 CO2
Пятый пункт плана. Химические свойства. Слайд № 12, 13, 14
Информацию по данному пункту сообщает учитель. Во время изучения химических свойств ученики выполняют лабораторный опыт по изучению окислительных свойств.
1. Реакции окисления.
Окисление оксидом меди (2) первичных алканолов, образуется альдегид, вторичных алканолов, образуется кетон (лабораторная работа):
Горение:
С2Н5OH + 3O2 —> 2CO2 + 3H2O
2. Реакции, идущие с участием атома водорода гидроксильной группы.
Взаимодействие со щелочными металлами:
2C2H5OH + 2Na —>2C2H5ONa + H2
Взаимодействие с карбоновыми кислотами (реакция этерификации):
C2H5OH + CH3COOH = CH3COOC2H5 + H2O
3. Реакции, идущие с участием гидроксильной группы.
Взаимодействие с галогеноводородами:
CH3 – CH2OH + HCL—>CH3— CH2CL + H2O
Дегидратация внутримолекулярная (образуются алкены):
CH3 – CH2OH —>CH2 = CH2 + H2O
Дегидратация межмолекулярная (образуются простые эфиры):
C2H5OH + C2H5OH = C2H5- O- C2H5 + H2O
Обобщение по химическим свойствам спиртов: все реакции идут за счет гидроксильной группы. Ее еще называют — функциональная группа. Она обеспечивает и объясняет химические свойства алканолов.
Первичное закрепление.
На столах учащихся лежат листы с заданиями, выполняя их, они смогут проверить, насколько усвоили тему. Приложение 4
Рефлексия.
1. Достигли поставленной цели?
2. Какие имеющиеся знания, пригодились при изучении темы?
3. Что вызвало затруднение во время изучения темы?
Домашнее задание: пр. 9, записи в тетради.
urok.1sept.ru
Классификация органических веществ — урок. Химия, 8–9 класс.
Органических веществ известно более двадцати пяти миллионов. Для того чтобы разобраться во всём их многообразии, используют классификацию.
В основу современной классификации органических соединений положены два признака:
- строение углеродного скелета молекулы;
- наличие в молекуле функциональных групп.
По строению углеродной цепи все соединения делят на алифатические (с незамкнутой цепью атомов углерода) и циклические (с замкнутым в цикл углеродным скелетом).
Алифатические соединения могут иметь разное строение углеродной цепи.
Среди циклических веществ выделяют карбоциклические (в цикле только атомы углерода) и гетероциклические (кроме углерода содержат в цикле атомы кислорода или азота).
Атомы кислорода и азота в состав органических веществ входят в виде функциональных групп.
Функциональная группа — это группа атомов, которая определяет свойства вещества.
По наличию функциональной группы выделяют углеводороды (состоят из атомов углерода и водорода) и их производные.
С учётом связей между атомами углерода органические вещества делятся на насыщенные (с одинарными связями между атомами углерода) и ненасыщенные (с двойными и тройными связями).
Среди производных углеводородов можно выделить кислородсодержащие и азотсодержащие (содержат в молекулах третий элемент).
В зависимости от состава функциональной группы среди производных выделяют спирты R—OH, карбоновые кислоты R—COOH, амины R—Nh3 и другие классы веществ.
www.yaklass.ru
Кислородсодержащие органические соединения — это… Что такое Кислородсодержащие органические соединения?
- Кислородсодержащие органические соединения
Кислородсодержа́щие органи́ческие соедине́ния — соединения, содержащие в молекуле связи углерод — водород и углерод — кислород. К кислородсодержащим относится большая часть органических соединений.
Классификация
Важнейшие представители
См. также
CH He CLi CBe CB CC CN CO CF Ne CNa CMg CAl CSi CP CS CCl CAr CK CCa CSc CTi CV CCr CMn CFe CCo CNi CCu CZn CGa CGe CAs CSe CBr CKr CRb CSr CY CZr CNb CMo CTc CRu CRh CPd CAg CCd CIn CSn CSb CTe CI CXe CCs CBa CHf CTa CW CRe COs CIr CPt CAu CHg CTl CPb CBi CPo CAt Rn Fr Ra Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Fl Uup Lv Uus Uuo ↓ СLa CСе СPr СNd Pm СSm СEu СGd СTb СDy СHo СEr СTm СYb СLu Ac СTh СPa CU СNp СPu СAm СCm СBk Cf СEs Fm Md No Lr
Категория:Химическая связь с углеродом Основные соединения Большое применение в химии Академические исследования Соединение неизвестно/не получено - Кислородсодержащие органические соединения
Wikimedia Foundation. 2010.
- Кислородный редуктор
- Кислота нитрилотриметилфосфоновая
Смотреть что такое «Кислородсодержащие органические соединения» в других словарях:
Органические соединения — Органические вещества класс соединений, в состав которых входит углерод (за исключением карбидов, карбонатов, оксидов углерода и цианидов). Название «органические соединения» появилось на ранней стадии развития химии и говорит само за себя ученые … Википедия
Азотсодержащие органические соединения — один из важнейших типов органических соединений. В их состав входит азот. Они содержат в молекуле связь углерод водород и азот углерод. В нефти содержится азотсодержащий гетероцикл пиридин. Азот входит в состав белков,нуклеиновых кислот и… … Википедия
Германийсодержащие органические соединения — Германийорганические соединения металлоорганические соединения содержащие связь «германий углерод». Иногда ими называются любые органические соединения, содержащие германий. Первое германоорганическое соединение тетраэтилгерман, было… … Википедия
Кремний-органические соединения — Кремнийорганические соединения соединения, в молекулах которых имеется непосредственная связь кремний углерод. Кремнийорганические соединения иногда называют силиконами, от латинского названия кремния силициум . Кремнийорганические соединения… … Википедия
Органические вещества — Органические соединения, органические вещества класс химических соединений, в состав которых входит углерод (за исключением карбидов, угольной кислоты, карбонатов, оксидов углерода и цианидов).[1] Содержание 1 История 2 Класси … Википедия
Металлоорганические соединения — Металлорганические соединения (МОС) органические соединения, в молекулах которых существует связь атома металла с атомом/атомами углерода. Содержание 1 Типы металлоорганических соединений 2 … Википедия
Галогенорганические соединения — Галогенорганические соединения органические вещества, содержащие хотя бы одну связь C Hal углерод галоген. Галогенорганические соединения, в зависимости от природы галогена, подразделяют на: Фторорганические соединения;… … Википедия
Металлорганические соединения — Металлоорганические соединения(МОС) органические соединения, в молекулах которых существует связь атома металла с атомом/атомами углерода. Содержание 1 Типы металлоорганических соединений 2 Способы получения … Википедия
Оловоорганические соединения — органические соединения, в которых присутствует связь олово углерод , могут содержать как двухвалентное, итак и четырёхвалентное олово. Содержание 1 Методы синтеза 2 Типы 3 … Википедия
Гетероциклические соединения — (гетероциклы) органические соединения, содержащие циклы, в состав которых наряду с углеродом входят и атомы других элементов. Могут рассматриваться как карбоциклические соединения с гетерозаместителями (гетероатомами) в цикле. Наиболее… … Википедия
biograf.academic.ru