«Помогите, пожалуйста, с тестом, вот, собственно, и он:» – Яндекс.Кью
1.Укажите два вещества, с которыми взаимодействуют растворы серной и соляной кислот.
Укажите один или несколько правильных вариантов ответа:
хлорид бария
цинк
серебро
ацетилен
карбонат бария
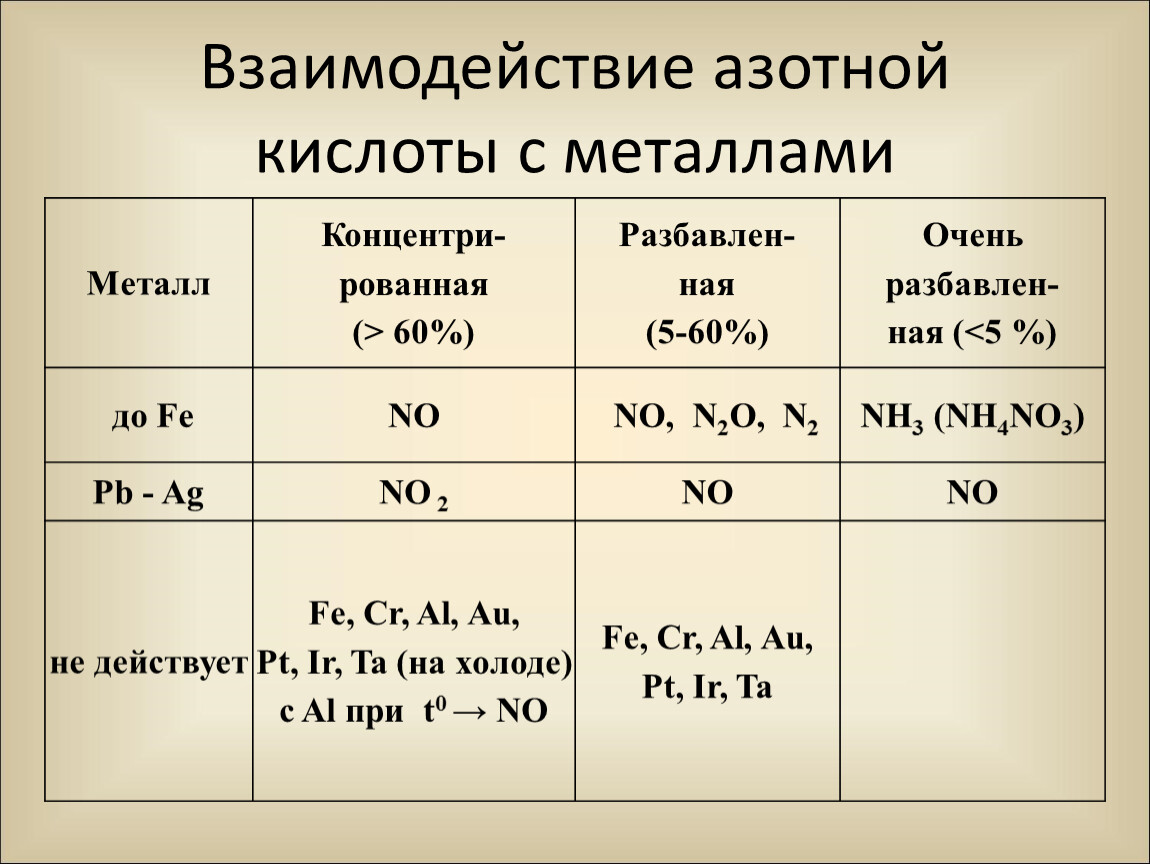
2.Концентрированная азотная кислота при обычных условиях не взаимодействует с
Укажите один или несколько правильных вариантов ответа:
оксидом натрия
золотом
алюминием
серой
гидроксидом цинка
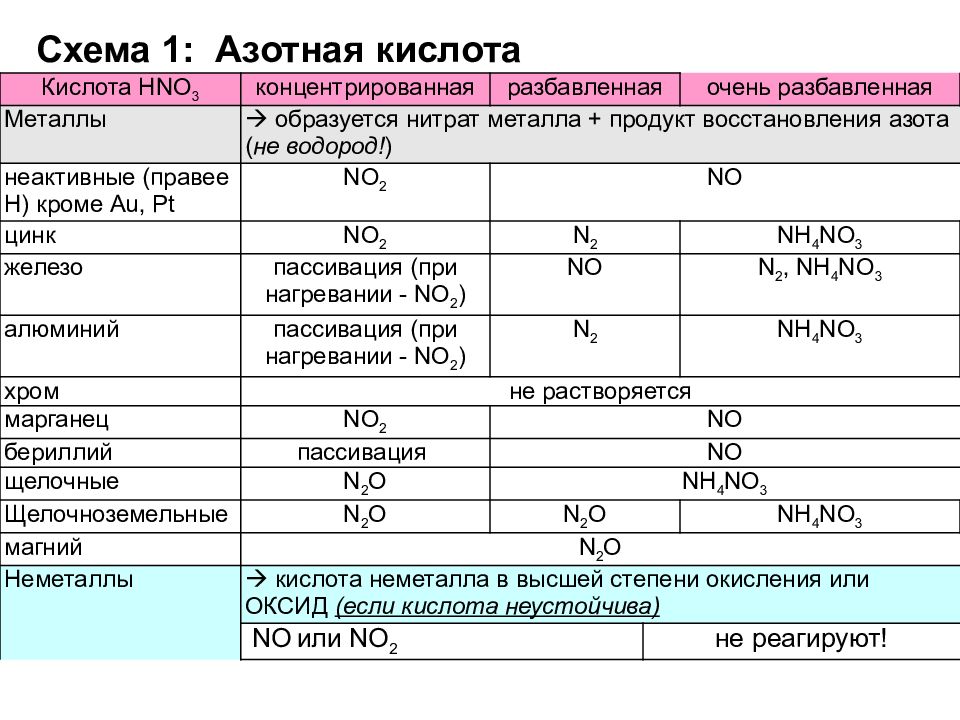
3.Укажите два вещества, с которыми при обычных условиях взаимодействуют раствор ортофосфорной кислоты и концентрированная серная кислота.
Укажите один или несколько правильных вариантов ответа:
оксид калия
железо
углерод
гидроксид лития
медь
4.Укажите две пары веществ, взаимодействие между которыми описывается уравнением в сокращенной ионной форме CO32– + 2H+ = CO2↑ + h3O.
Укажите один или несколько правильных вариантов ответа:
Na2CO3 и HCl
BaCO3 и h4PO4
CaCO3 и HNO3
K2CO3 и h3SO4
Li2CO3 и h3SiO3
5.Укажите два верных утверждения о правилах работы с кислотами в школьной химической лаборатории.
Укажите один или несколько правильных вариантов ответа:
в лаборатории можно пробовать на вкус известные в быту
кислоты, например, уксусную и лимонную
все опыты с кислотами можно проводить только под тягой
при разбавлении концентрированных кислот использовать
перчатки необязательно
при разбавлении концентрированных кислот необходимо вливать
кислоту в воду тонкой струйкой, а не наоборот
при попадании кислоты на кожу место ожога следует промыть
большим количеством воды и обработать раствором соды
6.Из предложенного перечня выберите два вещества, с которыми взаимодействуют уксусная и концентрированная серная кислота.
Укажите один или несколько правильных вариантов ответа:
этанол
гидроксид меди (II)
ртуть
оксид кремния
хлор
7. Установите соответствие между исходными вещества и продуктами реакции, протекающей при нагревании.
Установите соответствие между исходными вещества и продуктами реакции, протекающей при нагревании.
Cu и HNO3(р-р)
Cu и HNO3(конц)
Fe и h3SO4(конц)
Fe и h3SO4(р-р)
и
Fe2(SO4)3 + SO2 + h3O
Cu(NO3)2 + NO2 + h3O
Cu(NO3)2 + NO + h3O
FeSO4 + h3
8.Под действием концентрированной серной кислоты спирты подвергаются дегидратации. В зависимости от температуры протекает межмолекулярная или внутримолекулярная дегидратация спирта. Укажите продукты дегидратации этанола и пропанола-2 в разных температурных условиях.
Установите соответствие:
180℃
140℃
и
пропилен
диизопропиловый эфир
этилен
диэтиловый эфир
9.Какой коэффициент (наименьшее целое число) необходимо поставить перед формулой азотной кислоты в схеме реакции Zn + HNO3 → Zn(NO3)2 + N2O + h3O?
10.Установите соответствие между формулой вещества и реагентами, с каждым из которых оно может взаимодействовать.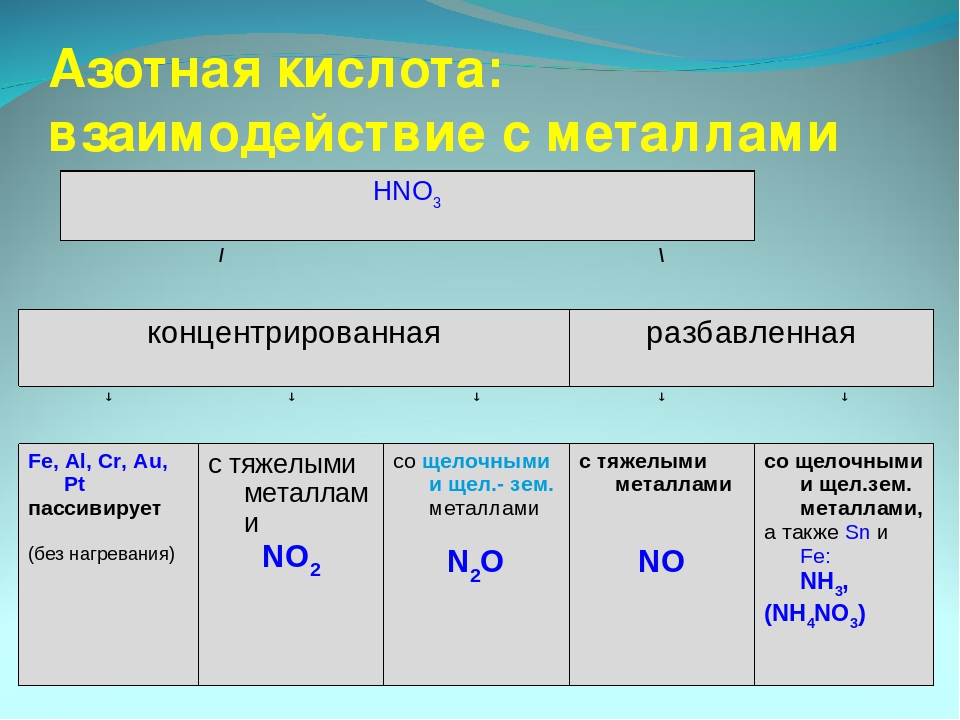
HCl
HNO2
и
MnO2, AgNO3
Kl, NaOH
Азотная кислота
Физические и химические свойства
Плотность безводной азотной кислоты ρ = 1522 кг/м3, температура плавления tпл— 41,15°С, температура кипения tкип 84° С.
С водой смешивается в любых отношениях с образованием азеотропной смеси с tкип = 121,8°C, содержащей 69,2% кислоты. Также существуют кристаллогидраты HNO3∙H2O с tпл -37,85°С и HNO3∙3H2O c tпл-18,5°С. В отсутствии воды азотная кислота неустойчива, разлагается на свету с выделением кислорода уже при обычных температурах (4HNO3 → 4NO2 + 2H2O + O2), причём выделяющейся двуокисью азота окрашивается в жёлтый цвет, а при высоких концентрациях NO2 — в красный.
Азотная кислота является сильным окислителем, окисляет серу до серной кислоты, фосфор — до фосфорной кислоты.
Некоторые металлы, например железо, хром, алюминий, легко растворяющиеся в разбавленной азотной кислоте, но устойчивы к воздействию концентрированной, что объясняется образованием на поверхности металла защитного слоя окисла. Такая особенность позволяет хранить и перевозить концентрированную азотную кислоту в стальных ёмкостях.
Смесь концентрированной азотной и соляной кислоты в отношении 1:3, называемая царской водкой, растворяет даже золото и платину. Органические соединения под действием азотной кислоты окисляются или нитруются, причём в последнем случае остаток (нитрогруппа NO2+) замещает в органических соединениях водород (происходит нитрование).
Соли азотной кислоты называютя нитратами, а соли с Na,K, Са, NO4+ — селитрами.
Получение
В 13 в. было описано получение азотной кислоты нагреванием калиевой селитры с квасцами, железным купоросом и глиной.
В середине 17 в. И. Р. Глаубер предложил получать азотную кислоту при умеренном (до 150°C) нагревании калиевой селитры с концентрированной серной кислотой: KNO3 + H2SO4 → HNO3 + KHSO4 До начала 20 в. этот способ применяли в промышленности, заменяя калиевую селитру более дешёвой природной чилийской селитрой NaNO3.
Современный способ производства азотной кислоты основан на каталитическом окислении аммиака кислородом воздуха. Основные стадии процесса:
- контактное окисление аммиака до окиси азота: 4NH3 + 5O2 → 4NO + 6H
- окисление окиси азота до двуокиси и поглощение смеси «нитрозных газов» водой:
2NO + O2 → 2NO2
3NO2 + H2O → 2HNO3 + NO - смесь аммиака (10 — 12% ) с воздухом пропускают через нагретую до 750 — 900°С сетку катализатора, которым служат сплавы платины — тройной (93% Pt, 3% Rh, 4% Pd) или двойной (90 — 95% Pt, 10 — 5% Rh)
- окисление NO до NO2 и растворение NO2 в воде — может быть проведенj при атмосферном давлении, под давлением до 1 Мн/м2 или комбинированным способом, при котором под давлением происходит только поглощение нитрозных газов водой
Получают азотную кислоту с концентрациями 45 — 49% или (при использовании давления) 55 — 58% .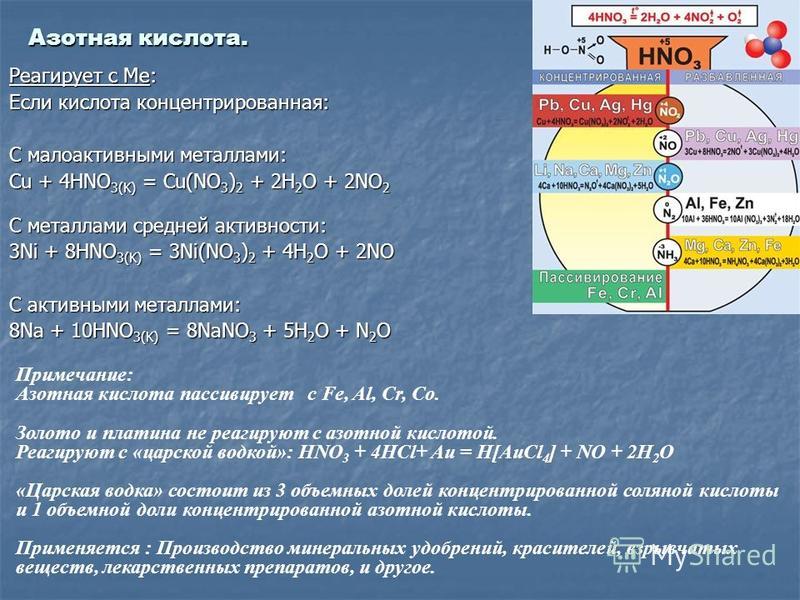 Дистилляцией таких растворов
может быть получена азотная кислота азеотропного состава. Более концентрированную кислоту (до 100% ) получают перегонкой растворов азотной кислоты с
концентрированной H 2SO4 или прямым синтезом — взаимодействием N2O4 с водой
(или разбавленной азотной кислотой) и кислородом: 2N2O4 + 2H2O + O2 → 4HNO3.
Дистилляцией таких растворов
может быть получена азотная кислота азеотропного состава. Более концентрированную кислоту (до 100% ) получают перегонкой растворов азотной кислоты с
концентрированной H 2SO4 или прямым синтезом — взаимодействием N2O4 с водой
(или разбавленной азотной кислотой) и кислородом: 2N2O4 + 2H2O + O2 → 4HNO3.
Применение азотной кислоты
Важнейшие области применения азотной кислоты — производство азотных и комбинированных удобрений, взрывчатых веществ (тринитротолуола и др.), органических красителей.
В органическом синтезе широко применяют смесь концентрированной азотной и серной кислоты — «нитрующую смесь».
Азотную кислоту используют в камерном способе производства серной кислоты, для получения фосфорной кислоты из фосфора, как окислитель ракетного топлива.
В металлургии азотую кислоту применяют для травления и растворения металлов, а также для разделения золота и серебра.
Токсичность
Вдыхание паров азотной кислоты приводит к отравлению, попадание кислоты (особенно концентрированной) на кожу вызывает ожоги. Предельно допустимое содержание азотной кислоты в воздухе промышленных помещений равно 50 мг/м3 в пересчёте на N2O5.
Концентрированная азотная кислота при соприкосновении с органическими веществами вызывает пожары и взрывы.
Химические свойства гидроксидов и кислот
Дидактический материал
Тренировочные тесты ЕГЭ по химии
Характерные химические свойства оснований, и амфотерных гидроксидов. Характерные химические
свойства кислот.
1. Гидроксид калия взаимодействует с каждым из двух веществ
1) NH3 и HCl 2) CO2 и CuCl2 3) H2SO4 и NaNO3 4) MgO и HNO3
2. Разбавленная хлороводородная кислота взаимодействует с каждым из двух веществ
1) медью и гидроксидом натрия
2) магнием и нитратом серебра
3) железом и оксидом кремния (IV)
4) свинцом и нитратом калия
3. С соляной кислотой взаимодействует
С соляной кислотой взаимодействует
1) NaHCO3 2)Hg 3) SiO2 4) S
4. Реакция нейтрализации происходит при взаимодействии
1) Fe2O3 и HCl
2) Fe(OH)3 и HCl
3) FeCl3 и NaNCS
4) Fe и HCl
5. Гидроксид железа (II) взаимодействует с
1) азотной кислотой
2) оксидом кальция
3) сульфатом меди
4) аммиаком
6. Разбавленная серная кислота не взаимодействует с
1) гидроксидом кальция
2) оксидом меди (II)
3) цинком
4) оксидом углерода (IV)
7. С гидроксидом калия реагирует каждое из двух веществ
1) AlCl3 и H2S
2) CuO и Ba(OH)2
3) CaCO3 и NH3
4) K2SO4 и AlCl3
8. Гидроксид кальция реагирует с каждым из двух веществ
1) HCl и СО2
2) HNO3 и MgO
3) HCl и KOH
4) BaCl2 и NaOH
9. Гидроксид калия реагирует с
Гидроксид калия реагирует с
1) водой
2) щелочью
3) кислотой
4) кислотой и щелочью
10. Гидроксид кальция не взаимодействует
1) HCl 2) ZnS 3) CO2 4) HNO3
11. Гидроксид хрома (III) реагирует с каждым из двух веществ
1) СО2 и HCl
2) SiO2 и Cu(OH)2
3) NO и NaNO3
4) H2
SO4 и NaOH
12. Реакция нейтрализации происходит между
1) | цинком и соляной кислотой |
2) | серной кислотой и хлоридом бария |
3) | гидроксидом кальция и азотной кислотой |
4) | гидроксидом натрия и сульфатом меди |
13 . С раствором серной кислоты взаимодействует каждое из двух веществ:
С раствором серной кислоты взаимодействует каждое из двух веществ:
1) | хлорид бария и оксид углерода (IV) |
2) | магний и хлорид бария |
3) | хлорид натрия и фосфорная кислота |
4) | медь и гидроксид калия |
14. Гидроксид кальция реагирует с
1) | Ba(NO3)2 | 2) | KCl | 3) | NH3·H2O | 4) | Na3PO4 |
15.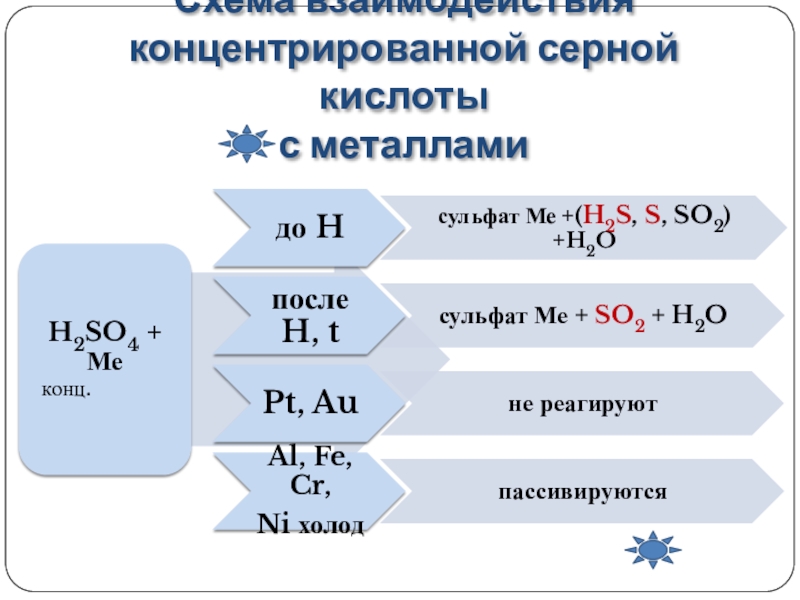 Концентрированная азотная кислота в обычных условиях не взаимодействует с
Концентрированная азотная кислота в обычных условиях не взаимодействует с
1) | магнием |
2) | гидроксидом натрия |
3) | железом |
4) | оксидом магния |
16. При сливании водных растворов уксусной кислоты и гидроксида калия образуется
1) | ацетат калия и водород |
2) | карбонат калия и вода |
3) | ацетат калия и вода |
4) | карбид калия и углекислый газ |
17. Гидроксид натрия не реагирует с
Гидроксид натрия не реагирует с
1) | Al(OH)3 | 2) | ZnO | 3) | H2SO4 | 4) | Ba(OH)2 |
18. Разбавленная серная кислота реагирует с каждым из двух веществ:
1) | Na2SiO3 и HNO3 |
2) | Fe2O3 и KNO3 |
3) | Ag и Cu(OH)2 |
4) | Fe и Al2O3 |
19. Как гидроксид алюминия, так и соляная кислота могут взаимодействовать с
Как гидроксид алюминия, так и соляная кислота могут взаимодействовать с
1) | CuO | 2) | H2SO4 | 3) | CO2 | 4) | NaOH |
20. Соляная кислота не взаимодействует ни с одним из двух веществ:
1) | цинком и гидроксидом натрия |
2) | медью и оксидом меди (II) |
3) | ртутью и оксидом углерода (IV) |
4) | магнием и аммиаком |
21. С каждым из перечисленных веществ: H2S, KOH, Zn
С каждым из перечисленных веществ: H2S, KOH, Zn
взаимодействует
1) | Pb(NO3)2 | 2) | ZnSO4 | 3) | Na2CO3 | 4) | HCl |
22. Разбавленная серная кислота может реагировать с каждым из двух веществ:
1) | серой и магнием |
2) | оксидом железа (II) и оксидом кремния (IV) |
3) | гидроксидом калия и хлоридом калия |
4) | нитратом бария и гидроксидом меди (II) |
23. С раствором серной кислоты взаимодействует каждое из двух веществ:
С раствором серной кислоты взаимодействует каждое из двух веществ:
1) | хлорид бария и оксид углерода (IV) |
2) | магний и хлорид бария |
3) | хлорид натрия и фосфорная кислота |
4) | медь и гидроксид калия |
24. Концентрированная азотная кислота в обычных условиях не взаимодействует с
1) | магнием |
2) | гидроксидом натрия |
3) | железом |
4) | оксидом магния |
25. Раствор гидроксида натрия реагирует с каждым из веществ, указанных попарно
Раствор гидроксида натрия реагирует с каждым из веществ, указанных попарно
1) | хлоридом железа (III) и углекислым газом |
2) | оксидом железа (II) и соляной кислотой |
3) | серной кислотой и карбонатом кальция |
4) | оксидом цинка и хлоридом калия |
26. Гидроксид натрия не реагирует с
1) | Al(OH)3 | 2) | ZnO | 3) | H2SO4 | 4) | Ba(OH)2 |
27. Разбавленная серная кислота реагирует с каждым из двух веществ:
Разбавленная серная кислота реагирует с каждым из двух веществ:
1) | Na2SiO3 и HNO3 |
2) | Fe2O3 и KNO3 |
3) | Ag и Cu(OH)2 |
4) | Fe и Al2O3 |
28. Как гидроксид алюминия, так и соляная кислота могут взаимодействовать с
1) | CuO | 2) | H2SO4 | 3) | CO2 | 4) | NaOH |
29. Соляная кислота не взаимодействует ни с одним из двух веществ:
Соляная кислота не взаимодействует ни с одним из двух веществ:
1) | цинком и гидроксидом натрия |
2) | медью и оксидом меди (II) |
3) | ртутью и оксидом углерода (IV) |
4) | магнием и аммиаком |
30. Раствор гидроксида натрия не взаимодействует с
1) | СО2 | 2) | HСl | 3) | SO2 | 4) | MgO |
ОТВЕТЫ: 1-2, 2-2, 3-1, 4-2, 5-1, 6-4, 7-1, 8-1, 9-3, 10-2, 11-4, 12-3, 13-2, 14-4, 15-1, 16-3, 17-4, 18-4, 19-4, 20-3, 21-1, 22-4, 23-2, 24-3, 25-3, 26-4, 27-4, 28-4, 29-3, 30-4, 31-1.
Основная информация о NO2 | Агентство по охране окружающей среды США
На этой странице:
Что такое NO
2 и как он попадает в воздух?Двуокись азота (NO 2 ) — это один из группы высокореактивных газов, известных как оксиды азота или оксиды азота (NO x ). Другие оксиды азота включают азотистую кислоту и азотную кислоту. NO 2 используется как индикатор для большей группы оксидов азота.
NO 2 попадает в воздух в первую очередь в результате сгорания топлива.NO 2 образуется в результате выбросов легковых, грузовых автомобилей и автобусов, электростанций и внедорожного оборудования.
Воздействие NO
2Воздействие на здоровье
Воздух для дыхания с высокой концентрацией NO 2 может вызывать раздражение дыхательных путей в дыхательной системе человека. Такое воздействие в течение коротких периодов времени может усугубить респираторные заболевания, особенно астму, приводя к респираторным симптомам (таким как кашель, хрипы или затрудненное дыхание), госпитализации и обращению в отделения неотложной помощи. Более длительное воздействие повышенных концентраций NO 2 может способствовать развитию астмы и потенциально повышать восприимчивость к респираторным инфекциям. Люди, страдающие астмой, а также дети и пожилые люди обычно подвергаются большему риску воздействия на здоровье NO 2 .
Более длительное воздействие повышенных концентраций NO 2 может способствовать развитию астмы и потенциально повышать восприимчивость к респираторным инфекциям. Люди, страдающие астмой, а также дети и пожилые люди обычно подвергаются большему риску воздействия на здоровье NO 2 .
NO 2 вместе с другими NO x вступает в реакцию с другими химическими веществами в воздухе с образованием твердых частиц и озона. Оба они также вредны при вдыхании из-за воздействия на дыхательную систему.
Воздействие на окружающую среду
NO 2 и другие NO x взаимодействуют с водой, кислородом и другими химическими веществами в атмосфере с образованием кислотных дождей. Кислотные дожди наносят вред уязвимым экосистемам, таким как озера и леса.
Нитратные частицы, образующиеся в результате NO x , делают воздух туманным и трудным для просмотра. Это влияет на многие национальные парки, которые мы посещаем ради просмотра.
NO x в атмосфере способствует загрязнению прибрежных вод биогенными веществами.
Что делается для уменьшения загрязнения NO
2 ?Национальные и региональные правила EPA по сокращению выбросов NO 2 и NO x помогут правительствам штатов и местным властям соответствовать Национальному стандарту качества окружающего воздуха (NAAQS).
EPA определяет районы, где качество воздуха не соответствует национальным стандартам NO 2 . Для этих территорий правительства штатов, местных властей и племен разрабатывают планы по сокращению количества NO 2 в воздухе.
Азотная кислота — обзор
28.4.2 Поспешная реакция при утечке на заводе
Азотная кислота просочилась через заглушку на кольцевой магистрали, которая обычно работала при манометрическом давлении 7 бар (100 фунтов на кв. Дюйм). Это вызвало коррозию оборудования, на которое попало. Заглушка была одной из нескольких, установленных подрядчиком по проектированию и сборке на случай, если возникнет необходимость в установке дополнительных инструментов, хотя это не является достоверным, поскольку никто, кто работал на заводе, не участвовал во время проектирования. Похоже, что с компанией никогда не консультировались о необходимости резьбовых заглушек. Ни один из них не откручивался за восемь лет, прошедших с момента постройки завода. Протекающая заглушка была сделана из мягкой стали, хотя трубопроводы были из нержавеющей стали, и заглушка была установлена неправильно. Обмотка резьбы политетрафторэтиленом (ПТФЭ) предотвратила более раннюю утечку.
Похоже, что с компанией никогда не консультировались о необходимости резьбовых заглушек. Ни один из них не откручивался за восемь лет, прошедших с момента постройки завода. Протекающая заглушка была сделана из мягкой стали, хотя трубопроводы были из нержавеющей стали, и заглушка была установлена неправильно. Обмотка резьбы политетрафторэтиленом (ПТФЭ) предотвратила более раннюю утечку.
Иногда необходимо установить временные заглушки для облегчения испытания под давлением, для облегчения слива или, как в этом случае, для упрощения установки дополнительных инструментов.Их позиции должны быть зарегистрированы, а если выяснится, что они не нужны, их следует заварить. Однако не выполняйте герметизацию сварного шва поверх обычной резьбовой заглушки, поскольку резьба вызывает коррозию, полное давление внутри оборудования прикладывается к уплотнению. Используйте специально разработанную пробку с сварным швом полной прочности. Кроме того, не используйте герметики в стыках, которые будут свариваться, так как сварка испарит герметик и сделает сварной шов пористым. Если использовался герметик, стык следует очистить перед сваркой.(Для других инцидентов см. Раздел 34.5 и Разделы с 7.1 по 7.5.)
Если использовался герметик, стык следует очистить перед сваркой.(Для других инцидентов см. Раздел 34.5 и Разделы с 7.1 по 7.5.)
Когда утечка была обнаружена, диспетчер технологического процесса немедленно решил слить кольцевую магистраль через несколько различных точек слива, чтобы она была опорожнена как можно скорее. Он не открывал вентиляционное отверстие в самой высокой точке кольцевой магистрали. Открытие нескольких точек слива привело к сложным скачкам давления и вакуума в кольцевой магистрали, а также к непредсказуемым движениям пробок жидкости. В результате из вентиляционного отверстия был выпущен столб жидкости высотой 3 м (10 футов).Пробку так и не нашли, поэтому она могла быть засосана в кольцевую магистраль из-за кратковременного вакуума. Всего было разлито 100 литров (25 галлонов) азотной кислоты.
Действия супервизора были понятны, но после того, как давление в кольцевой магистрали снизилось, небольшая задержка уже не имела бы значения. Двадцать минут, потраченные на обсуждение возможных методов, были бы потрачены не зря.
В кольцевой магистрали также могли быть воздушные карманы, и при повторной заправке кольцевой магистрали была принята пересмотренная процедура заполнения.Тем не менее, во время заправки произошел еще один сброс давления из открытого вентиляционного отверстия. Это показывает, насколько сложно оценить давление, возникающее при заполнении или опорожнении сложной системы трубопроводов — было много изменений отметки. Так же сложно избежать таких особенностей при проектировании. Постоянной инструкции, как слить кольцевую магистраль, не было. У сложных систем есть сложные проблемы, и их причины понять гораздо труднее, чем думают посторонние.
Расследование показало, что, хотя азотная кислота использовалась нечасто, тем не менее, давление в кольцевой магистрали постоянно поддерживалось.Этого не должно было быть. Действительно ли нужна была кольцевая магистраль?
Согласно отчету компании, самым важным уроком было не спешить с действиями, но я думаю, что более важным является необходимость заранее планировать работы, которые придется выполнить рано или поздно, и не оставлять людей в покое. работа, чтобы импровизировать, когда придет время.
работа, чтобы импровизировать, когда придет время.
Еще один урок заключается в том, что мы должны подвергать сомнению необходимость каждой вилки и обращать внимание на вилки, которые проектировщики или конструкторы вставляют для их собственного удобства.Те, которые добавлены строительным персоналом, обычно не показаны ни на одном чертеже.
КИСЛОТА АЗОТНАЯ, КРАСНАЯ ДЫМАЯ | CAMEO Chemicals
Химический лист данных
Химические идентификаторы | Опасности | Рекомендации по ответу | Физические свойства | Нормативная информация | Альтернативные химические названияХимические идентификаторы
В Поля химического идентификатора включать общие идентификационные номера, NFPA алмаз Знаки опасности Министерства транспорта США и общие описание химического вещества.Информация в CAMEO Chemicals поступает из множества источники данных.| Номер CAS | Номер ООН / NA | Знак опасности DOT | USCG CHRIS Код |
|---|---|---|---|
|
| никто | |
| Карманный справочник NIOSH | Международная карта химической безопасности | ||
| Азотная кислота | |||
NFPA 704
| Алмаз | Опасность | Значение | Описание |
|---|---|---|---|
| Здоровье | 4 | Может быть смертельным. | |
| Воспламеняемость | 0 | Не горит при типичных условиях пожара. | |
| Нестабильность | 1 | Обычно стабильный, но может стать нестабильным при повышенных температурах и давлениях. | |
| Специальный | OX | Обладает окислительными свойствами. |
(NFPA, 2010)
Общее описание
Жидкость от бледно-желтого до красновато-коричневого цвета, выделяющая красно-коричневые пары и имеющая удушающий запах. Очень токсично при вдыхании. Разъедает металлы или ткани. Продолжительное воздействие низких концентраций или кратковременное воздействие высоких концентраций может привести к неблагоприятным последствиям для здоровья.Скорость появления: Немедленно
Стойкость: Часы — дни
Порог запаха: ~ 1 ppm
Источник / использование / другая опасность: Используется во многих отраслях промышленности; Очень разъедает кожу / слизистые оболочки, а также металлы и другие материалы.
Опасности
Оповещения о реактивности
- Сильный окислитель
- Известная каталитическая активность
- Реагирует на воду
Реакции воздуха и воды
Пары в воздухе. Растворим во всех пропорциях с водой. При растворении в воде выделяется тепло, дым и разбрызгивание.
Пожарная опасность
Выдержка из руководства ERG 157 [Вещества — токсичные и / или коррозионные (негорючие / водочувствительные)]: Негорючее вещество, само по себе не горит, но может разлагаться при нагревании с образованием едких и / или токсичных паров.Для UN1796, UN1826, UN2031 при высоких концентрациях и для UN2032 они могут действовать как окислители, см. Также руководство ERG 140. Пары могут накапливаться в закрытых помещениях (подвал, цистерны, хопперы / цистерны и т. Д.). Вещество может реагировать с водой (в некоторых случаях бурно) с выделением коррозионных и / или токсичных газов и стоков. При контакте с металлами может выделяться горючий газообразный водород. Контейнеры могут взорваться при нагревании или при загрязнении водой. (ERG, 2016)
Контейнеры могут взорваться при нагревании или при загрязнении водой. (ERG, 2016)
Опасность для здоровья
Выдержка из руководства ERG 157 [Вещества — токсичные и / или коррозионные (негорючие / водочувствительные)]:TOXIC; Вдыхание, проглатывание или контакт (кожа, глаза) с парами, пылью или веществом может вызвать серьезные травмы, ожоги или смерть.Реакция с водой или влажным воздухом может привести к выделению токсичных, едких или легковоспламеняющихся газов. Реакция с водой может привести к выделению большого количества тепла, что приведет к увеличению концентрации паров в воздухе. При пожаре выделяются раздражающие, едкие и / или токсичные газы. Сток из воды для пожаротушения или разбавления воды может быть коррозионным и / или токсичным и вызывать загрязнение. (ERG, 2016)
Профиль реактивности
АЗОТНАЯ КИСЛОТА, КРАСНЫЙ ДЫМ — мощный окислитель и нитрующий агент. Ускоряет горение горючего материала и может вызвать обугливание, а затем воспламенение горючих материалов. Может воспламенить спирты, амины, аммиак, алкилы бериллия, бораны, дицианоген, гидразины, углеводороды, водород, нитроалканы, порошкообразные металлы, силаны или тиолы при контакте [Bretherick 1979. p.174]. Может бурно реагировать с мелкодисперсной сурьмой [Паскаль 10: 504. 1931-34]. Интенсивно Реагирует с пентафторидом брома [Mellor 2, Supp. 1: 172. 1956]. Реагирует с селенидом водорода и сероводородом с накалом [Berichte 3: 658]. Смеси с мелкодисперсным магнием взрывоопасны [Pieters 1957 p.28]. Окисляет фосфид магния при накале [Mellor 8: 842. 1946-47]. Смеси с уксусным ангидридом, содержащие более 50% азотной кислоты по массе, могут действовать как детонирующие взрывчатые вещества [BCISC 42: 2. 1971]. Травильный агент, приготовленный из равных долей ацетона, азотной кислоты и 75% водного раствора уксусной кислоты, взорвался через четыре часа после того, как был приготовлен и помещен в закрытую бутыль. Взрывчатым материалом мог быть тетранитрометан [Chem. Англ. News 38: 56. 1960]. Интенсивно Реагирует с фосфином [Един.
Может воспламенить спирты, амины, аммиак, алкилы бериллия, бораны, дицианоген, гидразины, углеводороды, водород, нитроалканы, порошкообразные металлы, силаны или тиолы при контакте [Bretherick 1979. p.174]. Может бурно реагировать с мелкодисперсной сурьмой [Паскаль 10: 504. 1931-34]. Интенсивно Реагирует с пентафторидом брома [Mellor 2, Supp. 1: 172. 1956]. Реагирует с селенидом водорода и сероводородом с накалом [Berichte 3: 658]. Смеси с мелкодисперсным магнием взрывоопасны [Pieters 1957 p.28]. Окисляет фосфид магния при накале [Mellor 8: 842. 1946-47]. Смеси с уксусным ангидридом, содержащие более 50% азотной кислоты по массе, могут действовать как детонирующие взрывчатые вещества [BCISC 42: 2. 1971]. Травильный агент, приготовленный из равных долей ацетона, азотной кислоты и 75% водного раствора уксусной кислоты, взорвался через четыре часа после того, как был приготовлен и помещен в закрытую бутыль. Взрывчатым материалом мог быть тетранитрометан [Chem. Англ. News 38: 56. 1960]. Интенсивно Реагирует с фосфином [Един. Рой. Soc. 13:88. 1835]. Взрывается при контакте с треххлористым фосфором [Comp. Ренд. 28:86]. Реагирует экзотермически с фталевой кислотой или фталевым ангидридом в присутствии серной кислоты с образованием потенциально взрывоопасных фталоилнитратов или нитритов или нитропроизводных этих соединений [Chem. & Инд 20: 790. 1972]. Реагирует энергично с азидом натрия [Mellor 8, Supp 2: 315. 1967]. Реагирует с ураном со взрывной силой [Katz and Rabinowitch 1951].
Рой. Soc. 13:88. 1835]. Взрывается при контакте с треххлористым фосфором [Comp. Ренд. 28:86]. Реагирует экзотермически с фталевой кислотой или фталевым ангидридом в присутствии серной кислоты с образованием потенциально взрывоопасных фталоилнитратов или нитритов или нитропроизводных этих соединений [Chem. & Инд 20: 790. 1972]. Реагирует энергично с азидом натрия [Mellor 8, Supp 2: 315. 1967]. Реагирует с ураном со взрывной силой [Katz and Rabinowitch 1951].
Принадлежит к следующей реактивной группе (группам)
Потенциально несовместимые абсорбенты
Будьте осторожны: жидкости с этой классификацией реактивной группы известно, что он реагирует с абсорбенты перечислено ниже.Дополнительная информация о абсорбентах, включая ситуации, на которые следует обращать внимание …
- Абсорбенты на основе целлюлозы
- Вспененные полимерные абсорбенты
Ответные рекомендации
В Поля рекомендаций ответа включать расстояния изоляции и эвакуации, а также рекомендации по пожаротушение, противопожарное реагирование, защитная одежда и первая помощь. В
информация в CAMEO Chemicals поступает из различных
источники данных.
В
информация в CAMEO Chemicals поступает из различных
источники данных.Изоляция и эвакуация
Выдержка из руководства ERG 157 [Вещества — токсичные и / или коррозионные (негорючие / водочувствительные)]:В качестве немедленной меры предосторожности изолировать место разлива или утечки во всех направлениях на расстоянии не менее 50 метров (150 футов) для жидкостей. и не менее 25 метров (75 футов) для твердых тел.
РАЗЛИВ: см. Таблицу 1 ERG — Начальные расстояния изоляции и защитных действий в спецификации UN / NA 2032.
ПОЖАР: Если цистерна, железнодорожный вагон или автоцистерна вовлечены в пожар, ИЗОЛИРУЙТЕСЬ на 800 метров (1/2 мили) во всех направлениях; также рассмотрите возможность начальной эвакуации на 800 метров (1/2 мили) во всех направлениях.(ERG, 2016)
Пожарная
Выдержка из руководства ERG 157 [Вещества — токсичные и / или коррозионные (негорючие / водочувствительные)]: Примечание: некоторые пены вступают в реакцию с материалом и выделяют коррозионные / токсичные газы.
МАЛЫЙ ПОЖАР: CO2 (кроме цианидов), сухой химикат, сухой песок, спиртоустойчивая пена.
БОЛЬШОЙ ПОЖАР: водяная струя, туман или спиртоустойчивая пена. Уберите контейнеры из зоны пожара, если это можно сделать без риска. Используйте водяную струю или туман; не используйте прямые потоки.Сделайте плотину противопожарной воды для последующей утилизации; не рассыпать материал.
ПОЖАР В ЦИСТЕРНАХ ИЛИ АВТОМОБИЛЬНЫХ / ПРИЦЕПНЫХ НАГРУЗКАХ: тушите пожар с максимального расстояния или используйте необслуживаемые держатели шлангов или контрольные насадки. Не допускайте попадания воды внутрь контейнеров. После того, как огонь потухнет, охладите емкости затопленным количеством воды. Немедленно удалите воду в случае появления шума из вентиляционных устройств безопасности или обесцвечивания бака. ВСЕГДА держитесь подальше от танков, охваченных огнем. (ERG, 2016)
Без огня
Выдержка из руководства ERG 157 [Вещества — токсичные и / или коррозионные (негорючие / водочувствительные)]: УСТРАНИТЬ все источники воспламенения (запретить курение, факелы, искры или пламя в непосредственной близости). Все оборудование, используемое при работе с продуктом, должно быть заземлено. Не прикасайтесь к поврежденным контейнерам или пролитому материалу, если не носите соответствующую защитную одежду. Остановите утечку, если вы можете сделать это без риска. Для уменьшения испарения можно использовать пену для улавливания паров. НЕ ПОЛУЧАЙТЕ ВОДУ В КОНТЕЙНЕРЫ. Используйте водяной спрей, чтобы уменьшить испарения или отвести облако пара. Избегайте попадания сточных вод на разлитый материал. Не допускайте попадания в водные пути, канализацию, подвалы или закрытые пространства.
Все оборудование, используемое при работе с продуктом, должно быть заземлено. Не прикасайтесь к поврежденным контейнерам или пролитому материалу, если не носите соответствующую защитную одежду. Остановите утечку, если вы можете сделать это без риска. Для уменьшения испарения можно использовать пену для улавливания паров. НЕ ПОЛУЧАЙТЕ ВОДУ В КОНТЕЙНЕРЫ. Используйте водяной спрей, чтобы уменьшить испарения или отвести облако пара. Избегайте попадания сточных вод на разлитый материал. Не допускайте попадания в водные пути, канализацию, подвалы или закрытые пространства.
НЕБОЛЬШОЙ РАЗЛИВ: Покройте СУХОЙ землей, СУХИМ песком или другим негорючим материалом, а затем накройте пластиковым листом, чтобы свести к минимуму распространение или контакт с дождем.Используйте чистые неискрящие инструменты, чтобы собрать материал и поместить его в неплотно закрытые пластиковые контейнеры для последующей утилизации. (ERG, 2016)
Защитная одежда
Кожа: Носите соответствующую личную защитную одежду для предотвращения контакта с кожей.
Глаза: Используйте соответствующие средства защиты глаз, чтобы избежать контакта с глазами.
Вымыть кожу: Рабочий должен немедленно промыть кожу, если она загрязнится.
Удаление: Намокшую или сильно загрязненную рабочую одежду следует снять и заменить.
Изменение: Нет рекомендаций относительно необходимости переодевания работника после рабочей смены.
Предоставить: Должны быть предусмотрены фонтаны для промывки глаз (при концентрации pH <2,5) в местах, где есть вероятность контакта рабочих с веществом; это независимо от рекомендаций, связанных с использованием средств защиты глаз. В непосредственной рабочей зоне должны быть предусмотрены средства для быстрого обмачивания тела (при концентрации pH <2,5) для экстренного использования, где существует вероятность воздействия.[Примечание: предполагается, что эти устройства обеспечивают достаточное количество или поток воды для быстрого удаления вещества из любых участков тела, которые могут подвергнуться воздействию.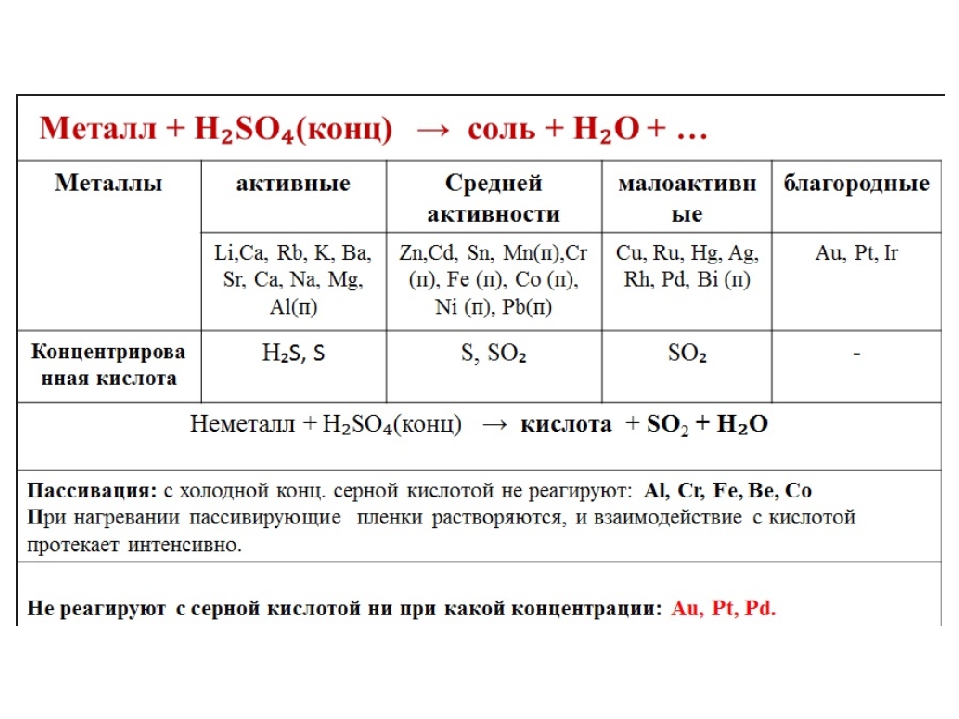 Фактическое определение того, что представляет собой адекватное устройство для быстрого слива, зависит от конкретных обстоятельств. В некоторых случаях должен быть легко доступен дренчерный душ, в то время как в других наличие воды из раковины или шланга можно считать достаточным.] (NIOSH, 2016)
Фактическое определение того, что представляет собой адекватное устройство для быстрого слива, зависит от конкретных обстоятельств. В некоторых случаях должен быть легко доступен дренчерный душ, в то время как в других наличие воды из раковины или шланга можно считать достаточным.] (NIOSH, 2016)
Ткани для костюмов DuPont Tychem®
Легенда ткани Tychem®
| QS = Tychem 2000 SFR |
| QC = Tychem 2000 |
| SL = Тихем 4000 |
| C3 = Тихем 5000 |
| TF = Тихем 6000 |
| TP = Tychem 6000 FR |
| BR = Тихем 9000 |
| RC = Tychem RESPONDER® CSM |
| TK = Тихем 10000 |
| RF = Тихем 10000 FR |
Детали тестирования
Данные о проницаемости ткани были получены для DuPont независимым
испытательные лаборатории с использованием ASTM F739, EN369, EN 374-3, EN ISO 6529
(методы A и B) или методы испытаний ASTM D6978. Нормализованное время прорыва
(время, при котором скорость проникновения равна 0,1 мкг / см2 / мин)
сообщается в минутах.
Все жидкие химикаты были протестированы при температуре примерно от 20 ° C до
27 ° C, если не указано иное.
Другая температура может существенно повлиять на
время прорыва; скорость проникновения обычно увеличивается с
температура.
Все химические вещества имеют
был протестирован при концентрации более 95%, если не указано иное
заявил.Если не указано иное, проницаемость измерялась для отдельных химикатов.
Характеристики проницаемости смесей могут значительно отличаться.
от проницаемости отдельных химических веществ.
Боевые отравляющие вещества (люизит, зарин, зоман, сера
Горчица, табун и нервно-паралитический агент VX) были протестированы при 22 ° C и 50%
относительная влажность в соответствии с военным стандартом MIL-STD-282.
Нормализованное время прорыва
(время, при котором скорость проникновения равна 0,1 мкг / см2 / мин)
сообщается в минутах.
Все жидкие химикаты были протестированы при температуре примерно от 20 ° C до
27 ° C, если не указано иное.
Другая температура может существенно повлиять на
время прорыва; скорость проникновения обычно увеличивается с
температура.
Все химические вещества имеют
был протестирован при концентрации более 95%, если не указано иное
заявил.Если не указано иное, проницаемость измерялась для отдельных химикатов.
Характеристики проницаемости смесей могут значительно отличаться.
от проницаемости отдельных химических веществ.
Боевые отравляющие вещества (люизит, зарин, зоман, сера
Горчица, табун и нервно-паралитический агент VX) были протестированы при 22 ° C и 50%
относительная влажность в соответствии с военным стандартом MIL-STD-282.
| Химическая промышленность | Номер CAS | Государство | QS | QC | SL | C3 | TF | TP | BR | RC | ТК | РФ |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Азотная кислота (50%) | 7697-37-2 | Жидкость | > 480 | |||||||||
| Азотная кислота (70%) | 7697-37-2 | Жидкость | 203 | > 480 | > 480 | > 480 | 140 | > 480 | > 480 | > 480 | > 480 | |
| Азотная кислота (90%) | 7697-37-2 | Жидкость | > 480 | > 480 | > 480 | > 480 | > 480 |
Специальные предупреждения от DuPont
- Зубчатые и переплетенные швы повреждены какой-либо опасной жидкостью
химические вещества, такие как сильные кислоты, и их не следует носить при
эти химические вещества присутствуют.

- ВНИМАНИЕ: эта информация основана на технических данных, которые
DuPont считает себя надежным. Подлежит пересмотру как
приобретаются дополнительные знания и опыт. DuPont не делает
гарантия результатов и не берет на себя никаких обязательств или ответственности …
… в связи с этой информацией. Ответственность за определить уровень токсичности и надлежащие средства индивидуальной защиты необходимое оборудование.Информация, изложенная здесь, отражает лабораторные эксплуатационные качества тканей, а не комплектных предметов одежды, в контролируемых условиях. Он предназначен для информационного использования лицами, имеющими технические навыки для оценка в соответствии с их конкретными условиями конечного использования, по их собственному усмотрению и риск. Любой, кто намеревается использовать эту информацию, должен сначала проверить что выбранная одежда подходит для предполагаемого использования.
 Во многих случаях,
швы и закрытия имеют более короткое время прорыва и более высокую проницаемость
ставки, чем ткань.Пожалуйста, свяжитесь с DuPont для получения конкретных данных. Если ткань
рвется, истирается или прокалывается, или если швы или затворы выходят из строя, или если
прикрепленные перчатки, козырьки и т. д. повреждены, конечный пользователь должен прекратить использование
одежды, чтобы избежать потенциального воздействия химикатов. Поскольку условия использования
находятся вне нашего контроля, мы не даем никаких гарантий, явных или подразумеваемых,
включая, помимо прочего, отсутствие гарантий товарной пригодности или пригодности
для конкретного использования и не несем ответственности в связи с любым использованием
эта информация.Эта информация не предназначена для использования в качестве лицензии на работу.
под или с рекомендацией нарушить какой-либо патент или техническую информацию
компании DuPont или других лиц, охватывающих любой материал или его использование.
Во многих случаях,
швы и закрытия имеют более короткое время прорыва и более высокую проницаемость
ставки, чем ткань.Пожалуйста, свяжитесь с DuPont для получения конкретных данных. Если ткань
рвется, истирается или прокалывается, или если швы или затворы выходят из строя, или если
прикрепленные перчатки, козырьки и т. д. повреждены, конечный пользователь должен прекратить использование
одежды, чтобы избежать потенциального воздействия химикатов. Поскольку условия использования
находятся вне нашего контроля, мы не даем никаких гарантий, явных или подразумеваемых,
включая, помимо прочего, отсутствие гарантий товарной пригодности или пригодности
для конкретного использования и не несем ответственности в связи с любым использованием
эта информация.Эта информация не предназначена для использования в качестве лицензии на работу.
под или с рекомендацией нарушить какой-либо патент или техническую информацию
компании DuPont или других лиц, охватывающих любой материал или его использование.
(DuPont, 2018)
Первая помощь
Глаза: При попадании этого химического вещества в глаза немедленно промойте глаза большим количеством воды, иногда приподнимая нижнее и верхнее веко. Немедленно обратитесь за медицинской помощью. Контактные линзы нельзя носить при работе с этим химическим веществом.Кожа: При попадании этого химического вещества на кожу немедленно промойте загрязненную кожу водой. Если это химическое вещество проникает в одежду, немедленно снимите одежду и промойте кожу водой. Немедленно обратитесь за медицинской помощью.
Дыхание: Если человек вдыхает большое количество этого химического вещества, немедленно выведите пострадавшего на свежий воздух. Если дыхание остановилось, выполните реанимацию «рот в рот». Держите пострадавшего в тепле и покое. Как можно скорее обратитесь за медицинской помощью.
Проглатывание: Если это химическое вещество было проглочено, немедленно обратитесь за медицинской помощью. (NIOSH, 2016)
(NIOSH, 2016)
Физические свойства
Точка воспламенения: данные недоступны
Нижний предел взрываемости (НПВ): данные недоступны
Верхний предел взрываемости (ВПВ): данные недоступны
Температура самовоспламенения: данные недоступны
Температура плавления: -44 ° F (NIOSH, 2016)
Давление газа: 48 мм рт. (NIOSH, 2016)
Плотность пара (относительно воздуха): данные отсутствуют
Удельный вес: данные недоступны
Точка кипения: 181 ° F при 760 мм рт. (NIOSH, 2016)
Молекулярная масса: 63 (NIOSH, 2016)
Растворимость воды: Смешиваемый (NIOSH, 2016)
Потенциал ионизации: 11.95 эВ (NIOSH, 2016)
IDLH: 25 частей на миллион (NIOSH, 2016)
AEGL (рекомендуемые уровни острого воздействия)
| Срок действия | AEGL-1 | AEGL-2 | AEGL-3 |
|---|---|---|---|
| 10 минут | 0,16 частей на миллион | 43 стр. / Мин. / Мин. | 170 частей на миллион |
| 30 минут | 0.16 страниц в минуту | 30 страниц в минуту | 120 страниц в минуту |
| 60 минут | 0,16 частей на миллион | 24 страниц в минуту | 92 страниц в минуту |
| 4 часа | 0,16 частей на миллион | 6 частей на миллион | 23 частей на миллион |
| 8 часов | 0,16 частей на миллион | 3 страницы на миллион | 11 страниц в минуту |
(NAC / NRC, 2017)
ERPG (Руководство по планированию действий в чрезвычайных ситуациях)
| Химическая промышленность | ЭРПГ-1 | ЭРПГ-2 | ЭРПГ-3 |
|---|---|---|---|
| Азотная кислота WFNA (7697-37-2) | 1 частей на миллион | 10 частей на миллион | 78 частей на миллион |
(АМСЗ, 2016)
PAC (Критерии защитного действия)
| Химическая промышленность | PAC-1 | ПАК-2 | PAC-3 |
|---|---|---|---|
| Азотная кислота (7697-37-2) | 0. 16 страниц в минуту 16 страниц в минуту | 24 страниц в минуту | 92 страниц в минуту |
(DOE, 2016)
Нормативная информация
В Поля нормативной информации включать информацию из Сводный список Раздела III Агентства по охране окружающей среды США Списки, химический объект Министерства внутренней безопасности США Стандарты борьбы с терроризмом, и Управления по охране труда и здоровья США Стандартный список управления производственной безопасностью особо опасных химических веществ (см. подробнее об этих источники данных).Сводный список списков Агентства по охране окружающей среды
| Нормативное название | Номер CAS / 313 Код категории | EPCRA 302 EHS TPQ | EPCRA 304 EHS RQ | CERCLA RQ | EPCRA 313 TRI | RCRA Код | CAA 112 (задний) RMP TQ |
|---|---|---|---|---|---|---|---|
| Азотная кислота | 7697-37-2 | 1000 фунтов | 1000 фунтов | 1000 фунтов | 313 | ||
Азотная кислота (конц. 80% или более) 80% или более) | 7697-37-2 | 1000 фунтов | 1000 фунтов | 1000 фунтов | Х | 15000 фунтов |
(Список списков EPA, 2015)
Стандарты по борьбе с терроризмом химического предприятия DHS (CFATS)
| ВЫПУСК | КРАЖА | САБОТАЖ | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Представляющее интерес химическое вещество | Номер CAS | Мин. Концентрация | STQ | Безопасность Выпуск | Мин. Концентрация Концентрация | STQ | Безопасность Выпуск | Мин. Концентрация | STQ | Безопасность Выпуск |
| Азотная кислота | 7697-37-2 | 80.00% | 15000 фунтов | токсичный | 68,00% | 400 фунтов | EXP / IEDP | |||
(DHS, 2007)
Список стандартов управления безопасностью процессов (PSM) OSHA
| Химическое название | Номер CAS | Пороговое количество (TQ) |
|---|---|---|
Азотная кислота (94. 5% по весу или более) 5% по весу или более) | 7697-37-2 | 500 фунтов |
(OSHA, 2011)
Альтернативные химические названия
В этом разделе представлен список альтернативных названий этого химического вещества, включая торговые наименования и синонимы.
- АКВА ФОРТИС
- АЗОТОВАЯ КИСЛОТА
- НИТРАТ ВОДОРОДА
- НИТАЛ
- АЗОТНАЯ КИСЛОТА
- АЗОТНАЯ КИСЛОТА (КОНЦЕНТРАЦИЯ 80% ИЛИ БОЛЕЕ)
- АЗОТНАЯ КИСЛОТА (HONO2)
- КИСЛОТА АЗОТНАЯ ДЫМАЯ
- КИСЛОТА АЗОТНАЯ КРАСНАЯ ДЫМАЯ
- КИСЛОТА АЗОТНАЯ, [ДЫМЯЩАЯ]
- НИТРИЛА ГИДРОКСИД
Произошла ошибка при установке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.
 Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт
не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к
остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Исследование азотной кислоты Иры Ремсена
Краткое описание:
Комическая реконструкция опыта Иры Ремсен с азотной кислотой.
Назначение / цель:
В этой классической демонстрации можно воспроизвести опыт Ира Ремсен с азотной кислотой. Ира Ремсен (1846-1927) была влиятельным химиком в Америке. Он основал химический факультет в Университете Джонса Хопкинса и основал первый центр химических исследований в этой стране. В этом эксперименте он описывает свой опыт с азотной кислотой.
Объяснение эксперимента:
Реакция — Азотная кислота реагирует с медью с образованием коричневого газообразного диоксида азота:
Cu (т.) + 4H + (водн.) + 2NO 3 — (водн.) → Cu 2+ (водн.) + 2NO 2 (г) + 2H 2 O (л)
Подготовка материалов:
Колба Эрленмейера 500 мл
5 мл концентрированной 16M азотной кислоты, HNO3
Несколько влажных сложенных бумажных полотенец
Большой кусок ткани, на который ранее была пролита пипетка с азотной кислотой
Медный пенни до 1982 года.
Представительство:
Предлагается прочитать свою учетную запись во время демонстрации:
«Читая учебник по химии, я наткнулся на утверждение, что азотная кислота действует на медь». Я устал читать такие абсурдные вещи и решил посмотреть, что это значит. Медь была мне более или менее знакома, поскольку в то время использовались медные центы. Я видел бутылку с надписью «азотная кислота» на столе в кабинете врача, где я тогда «сидел»! Я не знал его особенностей, но у меня все получалось, и я, вероятно, научился.Дух приключений был на мне. Имея азотную кислоту и медь, мне нужно было только узнать, что означают слова «действовать». Тогда утверждение «азотная кислота действует на медь» было бы чем-то большим, чем просто словами.
Все было по-прежнему. Ради познания я даже был готов пожертвовать одним из немногих медных центов, которыми тогда владел. Я положил одну из них на стол, открыл бутылку с надписью «азотная кислота», вылил немного жидкости на медь и приготовился к наблюдению. «
«
1. Поместите пенни в колбу на 500 мл.
2. Осторожно добавьте 5 мл концентрированной азотной кислоты.
3. Поместите несколько влажных сложенных бумажных полотенец поверх колбы для растворения выделяющегося газа.
«Но что это была за чудесная вещь, которую я увидел? Цент уже был изменен, и это тоже было немалое изменение. Зеленовато-голубая жидкость вспенилась и запылала над центом и над столом. Воздух в окрестностях представления стал темно-красный, поднялось большое цветное облако.Это было неприятно и душно — как мне это остановить? Я попытался избавиться от неприятного беспорядка, подняв его и выбросив из окна, которое я тем временем открыл. Я узнал еще один факт: азотная кислота действует не только на медь, но и на пальцы. Боль привела к еще одному непреднамеренному эксперименту. Я провел пальцами по брюкам, и был обнаружен еще один факт. Азотная кислота также действует на брюки.
4. Покажите аудитории большой кусок ткани, на который предварительно была пролита пипетка, если ранее была распылена азотная кислота.
5. Добавьте воду к азотной кислоте, чтобы остановить реакцию.
6. Промойте колбу и выньте пенни (теперь намного меньше!)
«Принимая все во внимание, это был самый впечатляющий эксперимент и, относительно, возможно, самый дорогостоящий эксперимент, который я когда-либо проводил. Я рассказываю о нем даже сейчас с интересом. Это было для меня откровением. Моя часть — узнать больше об этом замечательном виде действия. Ясно, что единственный способ узнать о нем — это увидеть его результаты, поэкспериментировать, поработать в лаборатории.«
Опасности:
Надевайте защитные очки. При использовании концентрированной азотной кислоты используйте защитную маску и перчатки. Эта демонстрация должна проводиться в хорошо проветриваемом помещении или в вытяжном шкафу. NO2 — токсичный газ.
Выбытие:
Нейтрализуйте кислоту бикарбонатом натрия и промойте полученный раствор в канализацию большим количеством воды.
Первичная ссылка:
Саммерлин, Л.Р., Боргфорд, К.Л., Или, Дж.Б., Химические демонстрации — Справочник для учителей, т. 2, 2-е изд. (1988) с.4.
Вторичные ссылки:
Гетман, Фредерик Х., J. Chem.Educ. (1940), 9-10.
1. Этот замечательный отрывок взят из книги Getman, Frederick H., J.Chem.Educ. (1940), 9-10.
2. Эта демонстрация — отличный способ начать курс химии — возможно, студенты узнают больше об Ире Ремсен.
3. Учитывая, когда Ира Ремсен проводил этот «эксперимент», попросите студентов прокомментировать его расследование.
4. Ира Ремсен является соавтором искусственного подсластителя сахарина.
Рекомендации по безопасности и опасности для здоровья при использовании азотной кислоты
Что такое азотная кислота? Обычно используется в удобрениях (а в редких случаях даже во взрывчатых веществах) Азотная кислота — это бесцветная или желтая жидкость с характерным едким, едким запахом и коррозионными свойствами. Эта минеральная кислота имеет множество применений и представляет несколько опасностей для здоровья при использовании без необходимых мер безопасности.Вот несколько важных советов по безопасному обращению и хранению азотной кислоты на рабочем месте от экспертов MSDSonline.
Эта минеральная кислота имеет множество применений и представляет несколько опасностей для здоровья при использовании без необходимых мер безопасности.Вот несколько важных советов по безопасному обращению и хранению азотной кислоты на рабочем месте от экспертов MSDSonline.
Также известная как aqua fortis или спирт селитры , азотная кислота используется для нитрования для создания нитросоединений в лабораторных или промышленных условиях. Полученные химические соединения различаются по стабильности, поэтому их можно использовать в производстве самых разных продуктов, в том числе:
- Взрывчатые вещества
- Боеприпасы
- Ракетное топливо
- Чернила и красители
- Древесина сосны и клена состаренная
- Коммерческие чистящие средства
Азотная кислота — это чрезвычайно коррозионная кислота, способная очень быстро вызвать серьезные химические ожоги. При вдыхании тумана азотной кислоты риски для здоровья включают коррозию слизистых оболочек, замедленный отек легких и даже смерть. Попадание в глаза может вызвать необратимое повреждение роговицы. Кроме того, при проглатывании азотная кислота может вызвать сильные, быстрые коррозионные ожоги рта, горла и желудочно-кишечного тракта.
При вдыхании тумана азотной кислоты риски для здоровья включают коррозию слизистых оболочек, замедленный отек легких и даже смерть. Попадание в глаза может вызвать необратимое повреждение роговицы. Кроме того, при проглатывании азотная кислота может вызвать сильные, быстрые коррозионные ожоги рта, горла и желудочно-кишечного тракта.
Это химическое вещество может также бурно реагировать с некоторыми соединениями, такими как металлические порошки и скипидар, и является сильным окислителем, способным вызвать пожар при контакте с органическими материалами.Из-за опасности, которую представляет азотная кислота, важно соблюдать строгие меры безопасности при обращении с ней.
Азотная кислота Безопасность, обращение и первая помощь При работе с азотной кислотой на рабочем месте мы настоятельно рекомендуем вам носить химические защитные очки, защитную маску для защиты от брызг, перчатки и одобренный паровой респиратор, если адекватная вентиляция отсутствует. В качестве дополнительной меры предосторожности станции для промывания глаз и помещения для мытья должны быть легко доступны.В случае контакта с азотной кислотой соблюдайте следующие инструкции по оказанию первой помощи:
В качестве дополнительной меры предосторожности станции для промывания глаз и помещения для мытья должны быть легко доступны.В случае контакта с азотной кислотой соблюдайте следующие инструкции по оказанию первой помощи:
- Вдыхание — Вызвать свежий воздух и немедленно обратиться за медицинской помощью.
- Контакт с глазами — Немедленно промойте глаза большим количеством воды в течение не менее 15 минут, чтобы предотвратить дальнейшее повреждение, а также немедленно обратитесь за медицинской помощью.
- Контакт с кожей — Немедленно промойте пораженный участок большим количеством воды в течение не менее 15 минут. Снимите загрязненную одежду и вымойте ее с мылом.Требуется немедленная медицинская помощь.
- Проглатывание — НЕ вызывайте рвоту. Прополоскать рот водой и дать стакан воды или молока. Никогда ничего не давайте человеку без сознания. Немедленно обратитесь за медицинской помощью.

Храните азотную кислоту в безопасном месте вдали от несовместимых материалов, таких как органические соединения, металлы, спирты или влага. Хранить контейнер плотно закрытым в прохладном, сухом, хорошо вентилируемом месте.Из-за высокого риска неблагоприятного воздействия на здоровье это химическое вещество необходимо утилизировать в соответствии с федеральными, государственными и местными нормативами по охране окружающей среды.
Узнать больше об азотной кислоте и других опасных химических веществах на рабочем месте
Если вы отвечаете за химическую безопасность своей организации, важно убедиться, что ваши сотрудники хорошо осведомлены обо всех рисках, связанных с азотной кислотой и другими потенциальными опасностями на рабочем месте . Просмотрите нашу обширную базу данных паспортов безопасности материалов, чтобы узнать больше.
Искусство безопасности
Керамическое искусство и гончарные изделия представляют собой множество опасностей. Конкретные опасности и меры предосторожности можно разделить на четыре области:
Конкретные опасности и меры предосторожности можно разделить на четыре области:
- работа с глиной
- остекление и окраска
- обжиг в печи
- возможность выщелачивания готовой продукции
Глина
Глины — это минералы, состоящие из гидратированных силикатов алюминия, часто содержащие большое количество кристаллического кремнезема. Другие примеси могут включать органические вещества или соединения серы.Иногда для изменения свойств глины добавляют грог (молотый огнеупорный кирпич), песок, тальк, вермикулит, перлит и небольшие количества минералов, таких как карбонат бария и оксиды металлов. Глину можно обрабатывать вручную или на гончарном круге, или отливать в глиняную суспензию в формы.
Глина изготавливается путем смешивания сухой глины с водой в смесителе для глины. Глиняный шликер изготавливается путем добавления тальков, которые сами по себе могут быть загрязнены волокнистым асбестом или асбестоподобными материалами. Важны географические источники тальков, например тальки штата Нью-Йорк, как известно, загрязнены асбестом, а тальки Вермонта — нет.У Pfizer есть тальки, не содержащие клетчатки.
Важны географические источники тальков, например тальки штата Нью-Йорк, как известно, загрязнены асбестом, а тальки Вермонта — нет.У Pfizer есть тальки, не содержащие клетчатки.
Опасности
- Известны случаи силикоза, или «гончарной гнили», в результате хронического вдыхания большого количества свободного кремнезема во время смешивания глины. Симптомы силикоза включают одышку, сухой кашель, эмфизему и высокую восприимчивость к легочным инфекциям, таким как туберкулез. На развитие болезни могут уйти годы. Воздействие кремнеземной пыли не опасно при контакте с кожей или проглатывании.
- Хроническое вдыхание каолина умеренно опасно и может привести к каолинозу — заболеванию, при котором легкие механически закупориваются.
- Асбест чрезвычайно токсичен при вдыхании и, возможно, при проглатывании. Вдыхание асбеста может вызвать асбестоз, рак легких, мезотелиому, рак желудка и рак кишечника.
- Песок, перлит, грог и вермикулит содержат свободный кремнезем и поэтому являются высокотоксичными при вдыхании.
 Вермикулит также часто бывает загрязнен асбестом.
Вермикулит также часто бывает загрязнен асбестом. - При добавлении глины или воды во время работы миксера существует опасность несчастного случая.
- Мешки с глиной и глазурью могут быть очень тяжелыми, и их поднятие может вызвать проблемы со спиной.
- Гиперчувствительность, пневмония, астма или другие респираторные проблемы могут возникнуть при контакте с плесенью, растущей во влажной глине, которая закисается или выдерживается во влажном месте, в стеках, которые стоят месяцами, или при вдыхании сухой состаренной глины. Формы могут вызвать или усугубить проблемы с кожей и изменить удобоукладываемость глины.
- Продолжительное использование гончарного круга может привести к синдрому плодолистного туннеля из-за неудобного положения запястий. Боль, онемение и / или иглы в большом и первых трех пальцах являются общими симптомами.Проблемы со спиной могут возникнуть из-за того, что вы долго наклоняетесь над гончарным кругом.
- Контакт рук с влажной глиной может привести к истиранию и сухости кончиков пальцев и рук.
 Движущиеся части колес могут вызвать порезы и ссадины.
Движущиеся части колес могут вызвать порезы и ссадины. - Обрывки глины на полу, скамейке и других поверхностях могут высохнуть и превратиться в порошок, создавая опасность при вдыхании из-за наличия свободного кремнезема. Точно так же восстановление глины путем измельчения и шлифовки готовой зеленой посуды может создавать очень высокие концентрации опасной кремнеземной пыли.
Меры предосторожности
- Используйте предварительно приготовленную глину, чтобы избежать воздействия большого количества глиняной пыли.
- Хранение и смешивание глины должно происходить в отдельном помещении. Мешки с глиной (и другими керамическими материалами) следует складывать на поддоны или решетки от пола для облегчения уборки.
- Все смесители для глины должны быть оборудованы местной вытяжной вентиляцией для удаления из воздуха мелких частиц кремнеземной пыли.
- Миксеры для глины должны быть оборудованы соответствующими ограждениями, чтобы их нельзя было открыть для добавления глины или воды во время вращения лопастей миксера.

- В студии носить отдельную рабочую одежду. Выбирайте одежду из материала и дизайна, не задерживающего пыль. Стирайте эту одежду еженедельно и отдельно от другой стирки.
- Избегайте контакта глины с поврежденной кожей. Используйте увлажняющий крем для кожи.
- Во избежание проблем со спиной всегда поднимайте ногу с согнутыми коленями. Кроме того, используйте стоячее колесо (педаль в стиле Крэнбрука) или поднимите электрические колеса на высоту, при которой не нужно наклоняться. Упражнения и массаж могут облегчить незначительную мышечную боль.
- Держите запястья в разогнутом положении, насколько это возможно, чтобы предотвратить синдром туннельного туннеля. Делайте частые перерывы в работе.
- Будьте осторожны с движущимися частями колес.
- Восстановите глину, разрезав еще влажную глину на мелкие кусочки, дав им высохнуть на воздухе и замочив в воде.
- Завершите обработку зеленой посуды, пока она еще влажная или влажная, с помощью тонкой губки вместо шлифовки, когда она высохнет.
 Не шлифуйте зелень, содержащую волокнистый тальк.
Не шлифуйте зелень, содержащую волокнистый тальк. - Ежедневно протирайте полы и рабочие поверхности влажной шваброй, чтобы минимизировать запыленность и предотвратить превращение сухих отходов в пыль.
Глазури
Глазури, используемые для окраски или отделки глиняных изделий, представляют собой смесь кремнезема, флюсов и красителей. Обычные флюсы включают свинец, барий, литий, кальций и натрий и используются для понижения точки плавления кремнезема. Фактические красители, которые представляют собой ассортимент оксидов металлов, обычно составляют менее 5% глазури по весу.
Первоначально растворимые соединения свинца-сырца, включая красный свинец, белый свинец, галенит и глет, использовались в качестве флюсов в глазури слабого горения.Фактически, в 1897 году у британских гончаров было зарегистрировано более 400 случаев отравления свинцом. Свинцовые фритты и хорошее ведение домашнего хозяйства значительно снизили количество гончаров, которые были отравлены этими высокотоксичными соединениями свинца. Фритты состоят из расплавленных минералов и соединений металлов, которые спекаются и измельчаются в порошок. Хотя иногда предполагается, что свинцовые фритты нерастворимы и нетоксичны, испытания на выщелачивание с кислотами показали, что многие фритты так же растворимы, как и сырые соединения свинца, и, фактически, были случаи отравления свинцом как в результате их вдыхания, так и проглатывания.
Фритты состоят из расплавленных минералов и соединений металлов, которые спекаются и измельчаются в порошок. Хотя иногда предполагается, что свинцовые фритты нерастворимы и нетоксичны, испытания на выщелачивание с кислотами показали, что многие фритты так же растворимы, как и сырые соединения свинца, и, фактически, были случаи отравления свинцом как в результате их вдыхания, так и проглатывания.
Техника изготовления керамогранита и керамики с сильным обжигом исключает необходимость использования свинца в качестве флюса. Кроме того, вместо свинца для условий слабого воспламенения можно использовать флюсы щелочноземельных или щелочноземельных металлов. Кремнезем также может быть удален из глазурей без свинца. Замещение может быть основано на оксиде бора в качестве стеклообразователя, а не на диоксиде кремния. Флюсы щелочноземельных металлов включают оксиды натрия, калия и лития; флюсы щелочноземельных металлов включают оксиды кальция, магния, бария и стронция. Минералы, содержащие эти флюсы, включают определенные полевые шпаты, нефелиновый сиенит, петалит, костную и растительную золу, путассу и доломит.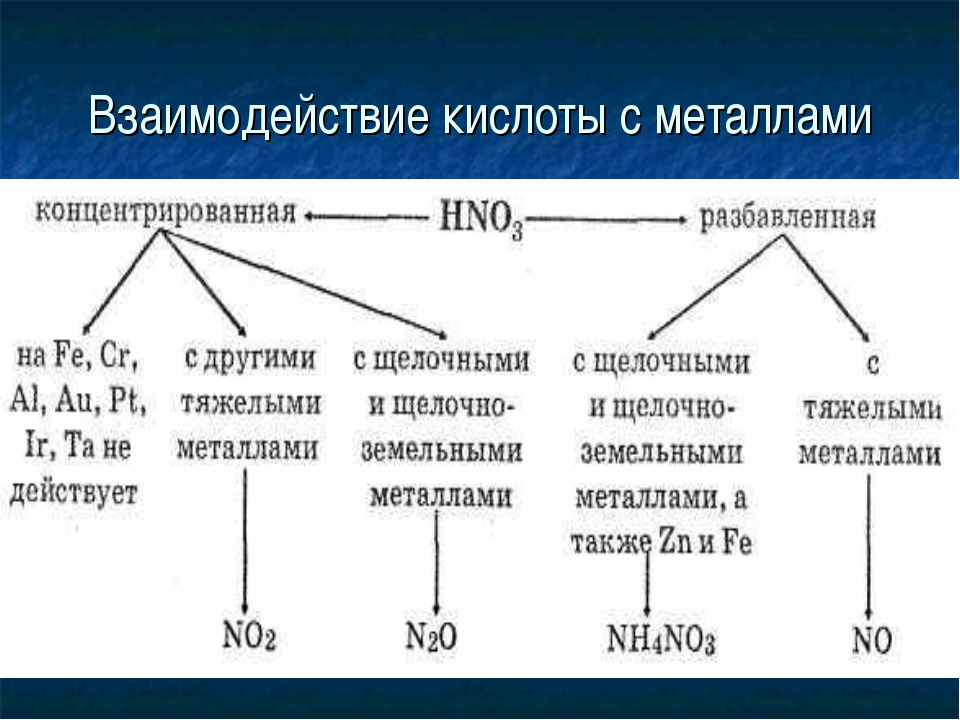
Ассортимент оксидов металлов или других соединений металлов при обжиге дает определенные цвета. Они добавляются в глазурь в таких небольших количествах, что обычно не представляют большой опасности. Глянцевые или металлические глазури обжигаются в восстановительной атмосфере. Эти глазури могут содержать ртуть, мышьяк, высокотоксичные растворители, такие как ароматические и хлорированные углеводороды, и масла, такие как масло лаванды. Обычные металлы часто представляют собой резинаты золота, платины, серебра и меди. Некоторые подглазурные и надглазурные покрытия используют в качестве носителя уайт-спирит вместо воды.
Компоненты глазури взвешиваются, сортируются и смешиваются с водой. Эти материалы часто находятся в виде мелкого порошка, что приводит к сильному запылению. Глазури можно окунать, нанести щеткой, налить или распылить на керамическое изделие.
Опасности
- Соединения свинца очень токсичны при вдыхании или проглатывании. Симптомы отравления свинцом включают: повреждение периферической нервной системы, головного мозга, почек или желудочно-кишечного тракта, а также анемию, хромосомные нарушения, врожденные дефекты и выкидыши.

- Пищевая посуда со свинцовой глазурью может выщелачивать свинец, если ее не обжечь должным образом или неправильно отрегулировать состав глазури. Например, добавление меди к свинцовым фриттам повышает растворимость свинца в изделиях, подвергнутых окончательному обжигу. Кислые напитки и продукты, такие как томатный сок, лимонный сок, газированные напитки, чай или кофе, могут увеличить этот риск.
- Этикетка глазури с пометкой «безопасна для свинца» означает, что готовая посуда при правильном обжиге не выделяет свинец в пищу или питье. Сама глазурь по-прежнему опасна при обращении и возгорании и может содержать свинец.В мастерской очень сложно контролировать условия стрельбы.
- Другие флюсы, такие как барий и литий, также очень токсичны при вдыхании, но в меньшей степени, чем свинец.
- Некоторые красящие соединения определенных металлов являются известными или вероятными канцерогенными веществами для человека, включая мышьяк, бериллий, кадмий, хром (VI), никель и уран.

- Красители сурьмы, бария, кобальта, свинца, лития, марганца и ванадия очень токсичны при вдыхании.
- Соединения сурьмы, мышьяка, хрома, ванадия и никеля умеренно токсичны при контакте с кожей.
- Свободный кремнезем содержится во многих глинах, растительной золе, кремне, кварцевых полевых шпатах, тальках и т. Д., Используемых в глазури. См. Обсуждение выше об опасностях кремнезема и болезни силикоза. Взвешивание и смешивание глазурей может привести к вдыханию этих токсичных материалов.
- Кальцинированная сода, карбонат калия, щелочной полевой шпат и плавиковый шпат, используемые в глазури, вызывают раздражение кожи.
- Нанесение глазури распылением очень опасно из-за возможного вдыхания тумана глазури.
- Погружение, заливка и чистка некоторых глазурей может вызвать раздражение кожи и случайное проглатывание из-за небрежных правил личной гигиены.
- Глазури, содержащие растворители, легковоспламеняемы и опасны.
Меры предосторожности
- Используйте бессвинцовые глазури.
 Если на этикетке глазури не указано «без свинца» или «без свинца», предполагайте, что она содержит свинец, пока не будет доказано обратное.
Если на этикетке глазури не указано «без свинца» или «без свинца», предполагайте, что она содержит свинец, пока не будет доказано обратное. - Свинцовую глазурь можно использовать только на непродовольственных товарах. Создавайте изделия, покрытые свинцовой глазурью, так, чтобы их нельзя было использовать в еде или питье. Глиняную посуду со свинцовым покрытием следует маркировать как содержащую свинец.
- По возможности не используйте красители, которые являются известными канцерогенными веществами для человека, и избегайте возможных канцерогенов для человека. Безопасный уровень воздействия канцерогенов неизвестен.
- Рассмотрите возможность использования респиратора при взвешивании и смешивании порошка. Мокрые глазури не опасны при вдыхании.Надлежащие процедуры по уборке и очистка от разливов снижают риск вдыхания или проглатывания токсичной пыли. Просыпанные порошки мокрой шваброй.
- При работе с влажной или сухой глазурью следует носить перчатки.
- При нанесении глазурей, содержащих растворители, должна быть обеспечена хорошая разбавляющая вентиляция или местная вытяжная вентиляция.

- Необходимо соблюдать основные правила личной гигиены, включая ограничение приема пищи, питья и курения в студии, а также использование средств индивидуальной защиты, таких как перчатки, и отдельную рабочую одежду или комбинезоны.Вымойте руки после работы. Остатки глазури и соскобы глазури можно гомогенизировать, комбинировать, тестировать и использовать в качестве глазури.
Обжиговые печи
Электрические печи и печи, работающие на топливе, используются для нагрева керамики до желаемой температуры обжига. Самый распространенный вид — электрические печи. Нагревательные элементы нагревают печь, поскольку электрический ток проходит через катушки. Температура повышается до тех пор, пока печь не отключится.
Топливные печи отапливаются за счет сжигания газа (природного или пропана), масла, древесины, кокса, древесного угля или других материалов.Чаще всего используется пропан или природный газ. Эти печи могут быть расположены как в помещении, так и на открытом воздухе. Топливо выделяет окись углерода и другие газы сгорания. Топливные печи обычно вентилируются сверху через дымоход.
Топливо выделяет окись углерода и другие газы сгорания. Топливные печи обычно вентилируются сверху через дымоход.
Температура обжига может варьироваться от 1382 ° F для раку и бисквитных изделий до 2372 ° F для керамических изделий и 2642 ° F для некоторых видов фарфора.
На ранних стадиях обжига бисквитного печенья органическое вещество глины окисляется до окиси углерода и других дымовых газов.Позднее сера распадается с образованием сильно раздражающих оксидов серы. Также нитраты и азотсодержащие органические вещества распадаются на оксиды азота.
Галенит, корнишпат, сырой полевой шпат, огнеупорные глины низкого качества, плавиковый шпат, гипс, лепидолит и криолит могут выделять токсичные газы и пары во время обжига глазури. Карбонаты, хлориды и фториды распадаются с выделением углекислого газа, хлора и фтора.
При температуре обжига керамогранита или выше, свинец, сурьма, кадмий, селен и драгоценные металлы испаряются, и пары металлов могут либо выходить из печи, либо оседать внутри печи или на керамической посуде в печи. Оксиды азота и озон могут образовываться из кислорода и азота в воздухе.
Оксиды азота и озон могут образовываться из кислорода и азота в воздухе.
Опасности
- Хлор, фтор, диоксид серы, диоксид азота и озон очень токсичны при вдыхании. Обжиг глины с высоким содержанием серы вызвал образование большого количества удушающего диоксида серы. Другое сильное острое воздействие газов не является обычным явлением. Вдыхание большого количества этих газов может привести к серьезным острым или хроническим проблемам с легкими. Длительное вдыхание низких уровней этих газов может вызвать хронический бронхит и эмфизему.Газообразный фтор также может вызывать проблемы с костями и зубами.
- Многие пары металлов, образующиеся при высоких температурах, очень токсичны при вдыхании. Поскольку свинец испаряется при относительно низкой температуре, он особенно опасен.
- Окись углерода от печей, работающих на топливе, или от сжигания органических веществ в глинах очень токсична при вдыхании и может вызвать кислородное голодание. Одним из симптомов отравления угарным газом является сильная лобная боль, которую невозможно снять с помощью анальгетиков.

- Горячие печи производят инфракрасное излучение, опасное для глаз.Были сообщения о катаракте после многих лет заглядывания внутрь горячих печей.
- Тепло, выделяемое печью, может вызвать термические ожоги. Фонд Edward Orton Jr. Ceramic Foundation сообщил, что когда печь работала при 2370 ° F, температура поверхности была на уровне 595 ° F и выше, а температура в одном футе от глазка составляла 156 ° F.
- Тепло, выделяемое даже небольшими электрическими печами, может вызвать пожар в присутствии горючих материалов или легковоспламеняющихся жидкостей.
- Если электрическая печь не отключится, нагревательные элементы плавятся, что может вызвать пожар.Газовые печи также выделяют много тепла, а температура в помещении часто превышает 100 ° F.
Меры предосторожности
- Инфракрасные очки, одобренные Американским национальным институтом стандартов (ANSI), или ручные сварочные щитки следует надевать, глядя в работающую печь. Рекомендуется оттенок от 1,7 до 3,0, но может потребоваться более темный оттенок, если пятна появляются перед глазами после того, как вы посмотрите от печи.

- Не используйте свинцовые составы при температуре керамогранита, так как свинец испаряется.
- Пиломатериалы, бумага, растворители или другие горючие и легковоспламеняющиеся материалы не должны храниться в печах.
- Всегда проверяйте, отключилась ли печь.
- При подозрении на утечку газа (например, запах газа): перекрыть газ в источнике; отключите питание камеры с помощью выключателя; и позвоните в газовую компанию. Проверьте на утечки обезжиренной мыльной водой или используйте одобренные растворы для обнаружения утечек.
СПЕЦИАЛЬНЫЕ ПРОЦЕССЫ
Хотя большинство обжигов глазури относится к обжигу покрытых глазурью горшка в печи, иногда используются специальные процессы. Соляная глазурь и раку для обжига являются двумя примерами.
Соляная глазурь Этот процесс включает бросание влажной соли (хлорида натрия) в нагретую печь во время обжига бисквитной посуды. Влажная соль при высоких температурах разлагается на натрий и хлор. Натрий вступает в реакцию с бисквитной посудой с образованием глазури. Также образуются большие количества газообразного хлористого водорода и, возможно, хлора.
Натрий вступает в реакцию с бисквитной посудой с образованием глазури. Также образуются большие количества газообразного хлористого водорода и, возможно, хлора.
Карбонат натрия (стиральная сода) также можно использовать.Вместо хлористого водорода образуется двуокись углерода.
Опасности
- Хлороводородный газ очень токсичен при вдыхании. Воздействие на здоровье схожее и более раздражающее по сравнению с большинством других печных газов. Часто местные законы об охране окружающей среды запрещают соляные печи.
- Хлористый водород и водяной пар образуют соляную кислоту, которая может вызвать коррозию металлической арматуры в этой области.
Меры предосторожности
- Замените хлорид натрия более безопасным карбонатом натрия.
- Остекление из хлоридно-натриевой соли следует выполнять только на открытом воздухе. Печи должны быть оборудованы вытяжными навесами и вытяжными трубами, достаточно высокими для безопасного рассеивания хлористого водорода.

- Все газовые трубопроводы и металлические приспособления следует регулярно проверять на предмет коррозии.
Raku включает в себя сначала обжиг посуды при низкой температуре в обычной газовой печи, а затем удаление еще горячих частей и помещение их в опилки, листья или другие органические материалы для фазы восстановления.
Опасности
- См. Выше информацию об опасностях и мерах предосторожности при использовании газовых печей.
- На этапе восстановления образуется большое количество дыма и окиси углерода.
- Обработанная древесина или другие материалы могут подвергаться воздействию высокотоксичных консервантов или пестицидов, таких как соединения мышьяка и хрома.
Меры предосторожности
- Раку следует делать только на открытом воздухе из-за дыма. Будьте осторожны, не размещайте раку возле воздухозаборников или открытых окон зданий.
- Не используйте материалы, обработанные консервантами или пестицидами на этапе восстановления.

ВЫЩИЩЕНИЕ ГОТОВЫХ КЕРАМИЧЕСКИХ ИЗДЕЛИЙ
Выщелачивание свинца
Существует реальная проблема выщелачивания свинца в продукты питания и напитки из гончарных изделий, обжигаемых свинцовой глазурью. Как Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), так и Управление по делам потребителей и корпораций Канады регулируют количество свинца, которое может вымываться из продуктов питания в продукты питания и напитки. Кислые жидкости вызывают особую озабоченность.Точно так же постоянный разогрев в микроволновой печи (например, кофейная кружка на работе) может привести к большему вымыванию свинцовой глазури. Многие случаи отравления свинцом и даже некоторые смертельные случаи произошли в результате выщелачивания свинца из глазурованной свинцом керамики.
В то время как коммерческие керамические компании регулярно проверяют свою посуду на выщелачивание свинца, ремесленные гончары не имеют такого же контроля качества, как керамическая промышленность, и выщелачивание свинца представляет собой большую проблему.
Согласно нормам США, керамическая посуда, не прошедшая испытания на выщелачивание свинца, должна иметь наклейку с надписью:
.«НЕ ДЛЯ ПИЩЕВОГО ИСПОЛЬЗОВАНИЯ — МОЖЕТ ОТРАВИТЬ ПИТАНИЕ. ТОЛЬКО ДЛЯ ДЕКОРАТИВНЫХ ЦЕЛЕЙ « |
Как упоминалось ранее, вы также можете просверлить отверстие в глиняной посуде, чтобы ее нельзя было использовать для жидкости или еды.
Не используйте свинцовые глазури, особенно для емкостей для еды и напитков. Любая посуда, покрытая свинцовой глазурью, должна регулярно проверяться в сертифицированных лабораториях.
Прочие вымываемые металлы
Другие металлы могут попадать в продукты питания и напитки.Кадмий — это единственный металл, помимо свинца, который в настоящее время регулируется в США и Канаде. Однако другие возможные токсичные металлы в глазури могут выщелачиваться. В некоторых тестах было замечено, что барий выщелачивается в опасных количествах из определенных составов глазури. Если бариевая или другая глазурь меняет цвет из-за контакта с пищевыми продуктами, не используйте сосуд для еды. Попробуйте использовать только глазури с флюсами из кальция, магния, калия и натрия и минимизируйте количество токсичных металлических красителей. Следует проводить плановые испытания на выщелачивание других металлов.В этой области необходимо провести дополнительные исследования.
В некоторых тестах было замечено, что барий выщелачивается в опасных количествах из определенных составов глазури. Если бариевая или другая глазурь меняет цвет из-за контакта с пищевыми продуктами, не используйте сосуд для еды. Попробуйте использовать только глазури с флюсами из кальция, магния, калия и натрия и минимизируйте количество токсичных металлических красителей. Следует проводить плановые испытания на выщелачивание других металлов.В этой области необходимо провести дополнительные исследования.


 Во многих случаях,
швы и закрытия имеют более короткое время прорыва и более высокую проницаемость
ставки, чем ткань.Пожалуйста, свяжитесь с DuPont для получения конкретных данных. Если ткань
рвется, истирается или прокалывается, или если швы или затворы выходят из строя, или если
прикрепленные перчатки, козырьки и т. д. повреждены, конечный пользователь должен прекратить использование
одежды, чтобы избежать потенциального воздействия химикатов. Поскольку условия использования
находятся вне нашего контроля, мы не даем никаких гарантий, явных или подразумеваемых,
включая, помимо прочего, отсутствие гарантий товарной пригодности или пригодности
для конкретного использования и не несем ответственности в связи с любым использованием
эта информация.Эта информация не предназначена для использования в качестве лицензии на работу.
под или с рекомендацией нарушить какой-либо патент или техническую информацию
компании DuPont или других лиц, охватывающих любой материал или его использование.
Во многих случаях,
швы и закрытия имеют более короткое время прорыва и более высокую проницаемость
ставки, чем ткань.Пожалуйста, свяжитесь с DuPont для получения конкретных данных. Если ткань
рвется, истирается или прокалывается, или если швы или затворы выходят из строя, или если
прикрепленные перчатки, козырьки и т. д. повреждены, конечный пользователь должен прекратить использование
одежды, чтобы избежать потенциального воздействия химикатов. Поскольку условия использования
находятся вне нашего контроля, мы не даем никаких гарантий, явных или подразумеваемых,
включая, помимо прочего, отсутствие гарантий товарной пригодности или пригодности
для конкретного использования и не несем ответственности в связи с любым использованием
эта информация.Эта информация не предназначена для использования в качестве лицензии на работу.
под или с рекомендацией нарушить какой-либо патент или техническую информацию
компании DuPont или других лиц, охватывающих любой материал или его использование.
 Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
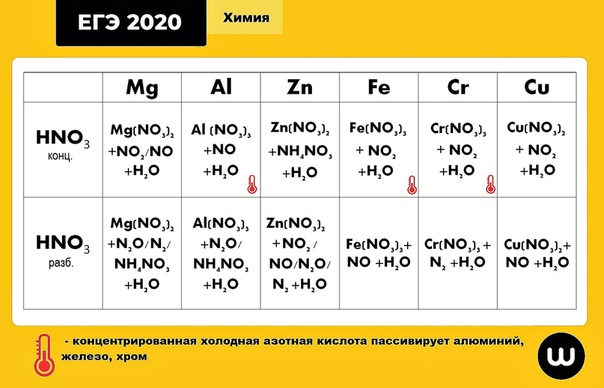 Вермикулит также часто бывает загрязнен асбестом.
Вермикулит также часто бывает загрязнен асбестом. Движущиеся части колес могут вызвать порезы и ссадины.
Движущиеся части колес могут вызвать порезы и ссадины.
 Не шлифуйте зелень, содержащую волокнистый тальк.
Не шлифуйте зелень, содержащую волокнистый тальк.

 Если на этикетке глазури не указано «без свинца» или «без свинца», предполагайте, что она содержит свинец, пока не будет доказано обратное.
Если на этикетке глазури не указано «без свинца» или «без свинца», предполагайте, что она содержит свинец, пока не будет доказано обратное.



