Что такое ковалентная связь определение. Ковалентная химическая связь
Каждый атом состоит из положительно заряженного ядра и отрицательно заряженной электронной оболочки. Благодаря зарядам ядра и электронов между соседними атомами возникают электростатические силы: притяжения и отталкивания. Если сближение атомов приводит к понижению энергии образующейся частицы (по сравнению с энергиями отдельных атомов), то образуется химическая связь.
Химическая связь — это силы взаимодействия, удерживающие частицы друг около друга.
Ученые доказали, что главную роль в образовании связи играют электроны, которые меньше всего связаны с ядром, т. е. расположенные на внешней электронной оболочке. Такие электроны называют валентными.
В атомах элементов главных подгрупп все валентные электроны расположены на последнем (внешнем) электронном слое и их число равно номеру группы.
В атомах элементов побочных подгрупп валентные электроны расположены, как правило, на двух последних электронных слоях,
Например, в атоме калия один валентный электрон, в атоме марганца — 7 валентных электронов (рис. 1).
Рис. 1. Электронные конфигурации атомов калия и марганца
Согласно теории химической связи наиболее устойчивыми являются внешние оболочки из восьми электронов — октет (если в атоме только 1 электронный слой, то для него наиболее устойчиво двухэлектронное состояние — дуплет).
Образование устойчивой электронной оболочки может происходить несколькими способами, поэтому различают разные виды химической связи.
Ковалентная связь — химическая связь, образованная перекрыванием электронных облаков атомов. Электронные облака (электроны), обеспечивающие связь, называются общей электронной парой.
Различают два механизма образования ковалентной связи: обменный и донорно-акцепторный.
При обменном механизме каждый атом предоставляет по одному электрону для образования общей пары:
А·+ В = А:В
При донорно-акцепторном механизме один атом предоставляет уже имеющуюся у него пару электронов (донор), а другой атом предоставляет свободную орбиталь для этой пары электронов (акцептор):
А: + □В = А:В
Связь, осуществляемая за счет образования общих электронных пар, в одинаковой мере принадлежащих обоим атомам, называется ковалентной неполярной .
Ковалентная неполярная связь образуется между атомами неметаллов с одинаковыми значениями относительной электроотрицательности, например в молекулах хлора, азота, между атомами углерода в этилене (табл. 1).
Молекулярные формулы | Электронные формулы | Графические формулы |
Табл. 1. Примеры соединений, в которых присутствуют ковалентные неполярные связи
Число общих электронных пар зависит от того, сколько электронов не хватает каждому атому для октета. Хлор — элемент VII-А подгруппы, следовательно, на его внешнем электронном слое 7 электронов. До октета не хватает одного электрона, значит, будет образована одна общая пара электронов в Cl 2 . Между атомами азота в молекуле N 2 образуются три общие электронные пары, т. е. тройная ковалентная связь. Между атомами углерода в этилене образуется двойная ковалентная связь.
Обратите внимание, что из каждого правила есть исключения и правило октета не всегда выполняется (пример — молекула сернистого газа SO 2).
Ковалентная полярная связь осуществляется за счет образования общих электронных пар, которые смещаются к атому более электроотрицательного элемента. При этом на атомах образуются частичные заряды: δ+ и δ- (рис. 2).
Рис. 2. Образование ковалентной связи в молекуле хлороводорода
Чем больше разность электроотрицательностей атомов элементов, тем больше полярность связи.
Ионная связь — предельный случай ковалентной полярной связи.
Ионная связь — это электростатическое притяжение между ионами, образованными путем практически полного смещения электронной пары к одному из атомов. Этот тип связи образуется, если разность значений относительной электроотрицательности атомов велика (как правило, больше 1,7 по шкале Полинга).
Ионная связь обычно образуется между типичным металлом и типичным неметаллом. Например, в хлориде натрия NaCl атом натрия свой 1 валентный электрон отдал атому хлора и превратил
Ковалентная химическая связь Википедия


Ковалентная связь (от лат. co — «совместно» и vales — «имеющий силу») — химическая связь, образованная перекрытием (обобществлением) пары валентных (находящихся на внешней оболочке атома) электронных облаков. Обеспечивающие связь электронные облака (электроны) называются общей электронной парой.
Ковалентная связь включает в себя многие виды взаимодействий, включая σ-связь, π-связь, металлическую связь, банановую связь и двухэлектронную трёхцентровую связь.[1][2]
С учётом статистической интерпретации волновой функции М. Борна плотность вероятности нахождения связывающих электронов концентрируется в пространстве между ядрами молекулы (рис.1). В теории отталкивания электронных пар рассматриваются геометрические размеры этих пар. Так, для элементов каждого периода существует некоторый средний радиус электронной пары (Å):
0,6 для элементов вплоть до неона; 0,75 для элементов вплоть до аргона; 0,75 для элементов вплоть до криптона и 0,8 для элементов вплоть до ксенона[3].
Характерные свойства ковалентной связи[ | ]
Характерные свойства ковалентной связи — направленность, насыщаемость, полярность, поляризуемость — определяют химические и физические свойства соединений.
- Направленность связи обусловлена молекулярным строением вещества и геометрической формы их молекулы.
Углы между двумя связями называют валентными.
- Насыщаемость — способность атомов образовывать ограниченное число ковалентных связей. Количество связей, образуемых атомом, ограничено числом его внешних атомных орбиталей.
- Полярность связи обусловлена неравномерным распределением электронной плотности вследствие различий в электроотрицательностях атомов.
По этому признаку ковалентные связи подразделяются на неполярные и полярные (неполярные — двухатомная молекула состоит из одинаковых атомов (H2, Cl2, N2) и электронные облака каждого атома распределяются симметрично относительно этих атомов; полярные — двухатомная молекула состоит из атомов разных химических элементов, и общее электронное облако смещается в сторону одного из атомов, образуя тем самым асимметрию распределения электрического заряда в молекуле, порождая дипольный момент молекулы).
- Поляризуемость связи выражается в смещении электронов связи под влиянием внешнего электрического поля, в том числе и другой реагирующей частицы. Поляризуемость определяется подвижностью электронов. Полярность и поляризуемость ковалентных связе
Химическая связь — это… Что такое Химическая связь?
 |
 |
Химическая связь — явление взаимодействия атомов, обусловленное перекрыванием электронных облаков связывающихся частиц, которое сопровождается уменьшением полной энергии системы.
При образовании ковалентной химической связи важную роль в уменьшении полной энергии играет обменное взаимодействие.
Теория химического строения Бутлерова
Термин «химическое строение» впервые ввёл А. М. Бутлеров в 1861 году. Также он заложил основы классической теории химического строения. Главные положения этой теории следующие:
- Атомы в молекулах соединены друг с другом в определённой последовательности. Изменение этой последовательности приводит к образованию нового вещества с новыми свойствами.
- Соединение атомов происходит в соответствии с их валентностью.
- Свойства веществ зависят не только от их состава, но и от «химического строения», то есть от порядка соединения атомов в молекулах и характера их взаимного влияния. Наиболее сильно влияют друг на друга атомы, непосредственно связанные между собой.
Типы связи
Простейшая одноэлектронная ковалентная химическая связь
Рис.1. Орбитальные радиусы элементов (ra) и длина одноэлектронной химической связи (d)Простейшая одноэлектронная химическая связь создаётся единственным валентным электроном. Оказывается, что один электрон способен удерживать в едином целом два положительно заряженных иона. В одноэлектронной связи кулоновские силы отталкивания положительно заряженных частиц компенсируются кулоновскими силами притяжения этих частиц к отрицательно заряженному электрону. Валентный электрон становится общим для двух ядер молекулы.
Примерами таких химических соединений являются молекулярные ионы: H2+, Li2+, Na2+, K2+, Rb2+, Cs2
+[1]:| Элемент | H | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|---|
| Электронная конфигурация | 1S1 | [He]2S1 | [Ne]3S1 | [Ar]4S1 | [Kr]5S1 | [Xe]6S1 |
| Межъядерное расстояние в молекулярном ионе xz+, Å | 1,06 | 3,14 | 3,43 | 4,18 | 4,44 | 4,70 |
| Орбитальный радиус атома, Å | 0,53 | 1,57 | 1,715 | 2,09 | 2,22 | 2,35 |
Существование молекулярных ионов водорода и щелочных металлов, в которых химическую связь создаёт единственный валентный электрон, расширяет и дополняет понятие химической связи. В перечисленных ионах ни о каком взаимодействии спинов электронов и перекрывания электронных облаков речи быть не может. Единственный связывающий электрон локализуется в пространстве между ядрами атомов и удерживает их в едином целом, образуя устойчивую химическую систему (рис.1).
Одинарная ковалентная связь
Рис.2.Неполярная ковалентная связь Рис.3.Полярная ковалентная связь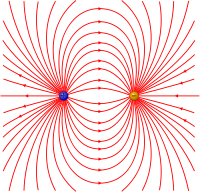 Рис.4.Силовые линии электрического диполя
Рис.4.Силовые линии электрического диполяОдинарная ковалентная химическая связь создаётся связывающей электронной парой. Во всех существующих теориях (теория валентных связей, теория молекулярных орбиталей, теория отталкивания валентных электронных пар, боровская модель химической связи) связывающая электронная пара располагается в пространстве между атомами молекулы. Различают полярную и неполярную ковалентную связи.
Неполярная ковалентная связь имеет место в гомоядерных двухатомных молекулах, в которых связывающая электронная пара равноудалена от обоих ядер молекулярной системы (рис.2). Расстояние d между атомными ядрами можно рассматривать как сумму ковалентных радиусов соответсвующих атомов.
Расстояние между атомными ядрами в одинарной двухэлектронной ковалентной связи короче аналогичного расстояния в простейшей одноэлектронной химической связи.
| Молекула | H2 | Li2 | Na2 | K2 | Rb2 | Cs2 |
|---|---|---|---|---|---|---|
| Межъядерное расстояние, Å [2] | 0,74 | 2,67 | 3,08 | 3,92 | 4,10 | 4,30 |
| Ковалентный радиус, Å | 0,37 | 1,335 | 1,54 | 1,96 | 2,05 | 2,15 |
| Орбитальный радиус, Å | 0,53 | 1,57 | 1,715 | 2,09 | 2,22 | 2,35 |
| Радиус связывающей электронной пары, Å | 0,379 | 0,826 | 0,755 | 0,726 | 0,852 | 0,949 |
| Энергия разрыва связи, кДж/моль [2] | 436 | 102 | 73 | 57 | 49 | 42 |
Разность между орбитальными и ковалентными радиусами характеризует степень перекрытия атомных орбиталей атомов, образующих химическую связь, и отражает деформацию электронной оболочки атомов.
Полярная ковалентная связь возникает в гетероядерных двухатомных молекулах (рис.3). Связывающая электронная пара в полярной химической связи приближена к атому с более высоким первым потенциалом ионизации.[3]
Характеризующее пространственную структуру полярных молекул расстояние d между атомными ядрами можно приближённо рассматривать как сумму ковалентных радиусов соответствующих атомов.[4]
Характеристика некоторых полярных веществ[2]| Молекула | LiH | NaH | KH | RbH | CsH |
|---|---|---|---|---|---|
| Межъядерное расстояние, Å | 1,60 | 1,89 | 2,24 | 2,37 | 2,49 |
| Энергия разрыва связи, кДж/моль | 236 | 200 | 182 | 165 | 176 |
Сдвиг связывающей электронной пары к одному из ядер полярной молекулы приводит к появлению электрического диполя (электродинамика) (рис.4).
Расстояние между центрами тяжести положительного и отрицательного зарядов называют длиной диполя. Полярность молекулы, как и полярность связи, оценивают величиной дипольного момента μ, представляющего собой произведение длины диполя l на величину электронного заряда:
μ = lq
Кратные ковалентные связи
Рис.5.sp2-гибридизация Рис.6.sp-гибридизацияКратные ковалентные связи представлены непредельными органическими соединениями, содержащими двойную и тройную химические связи. Для описания природы непредельных соединений Л.Полинг вводит понятия сигма- и π-связей, гибридизации атомных орбиталей.
Гибридизация Полинга для двух S- и двух p- электронов позволила объяснить направленность химических связей, в частности тетраэдрическую конфигурацию метана. Для объяснения структуры этилена из четырёх равноценных Sp3— электронов атома углерода приходится вычленять один p-электрон для образования дополнительной связи, получившей название π-связи. При этом три оставшиеся Sp2-гибридные орбитали располагаются в плоскости под углом 120° и образуют основные связи, например, плоскую молекулу этилена (рис.5).
В случае молекулы ацетилена в гибридизации принимают участие (по Полингу) всего лишь одна S- и одна p-орбитали, при этом образуются две Sp-орбитали, расположенные под углом в 180° и направленные в противоположные сороны. Две «чистые» p-орбитали атомов углерода попарно перекрываются во взаимоперпендикулярных плоскостях, образуя две π-связи линейной молекулы ацетилена (рис.6).
Взгляды Л.Полинга нашли отражение в его книге «Природа химической связи»[5], на долгие годы ставшей настольной книгой химика. В 1954 году Л.Полинг удостоен Нобелевской премии по химии с формулировкой «За исследование природы химической связи и его применение для опеделения структуры сложных соединений».
Однако физический смысл избирательной гибридизации атомных орбиталей оставался неясным, гибридизация представляла собой алгебраические преобразования, которым не могла быть приписана физическая реальность.
Лайнус Полинг предпринял попытку улучшения описания химической связи, исключив избритаельность гибридизации орбиталей в молекулах непредельных соединений и создав теорию изогнутой химической связи. В своём докладе на симпозиуме по теоретической органической химии, посвящённой памяти Кекуле (Лондон, сентябрь 1958 года), Л.Полинг предложил новый путь описания двойной связи как комбинации двух одинаковых изогнутых химических связей, а тройной связи — трёх изогнутых химических связей[6]. На этом симпозиуме Л.Полинг со всей категоричностью утверждал:
Могут найтись химики, полагающие что чрезвычайно важным новшеством… явилось описание σ,π- описания для двойной или тройной связи и сопряжённых систем вместо описания с помощью изогнутых связей. Я же утверждаю, что σ,π- описание менее удовлетворительно, чем описание с помощью изогнутых связей, что это нововведение является только переходящим и вскоре отомрёт.[6]
В новой теории Полинга все связывающие электроны становились равноценными и равноудалёнными от линии, соединяющей ядра молекулы. Теория изогнутой химической связи Полинга учитывала статистическую интерпретацию волновой функции М.Борна, кулоновскую электронную корреляцию электронов. Появился физический смысл — природа химической связи полностью определяется электрическим взаимодействием ядер и электронов. Чем больше связывающих электронов, тем меньше межъядерное расстояние и прочнее химическая связь между атомами углерода.
| Кратность связи | Структура связи | Межъядерное расстояние, Å | Энергия связи, кДж/моль |
|---|---|---|---|
| Одинарная (C-C) | Двухэлектронная двухцентровая | 1,54 | 348 |
| Двойная (C=C) | Четырёхэлектронная двухцентровая | 1,34 | 614 |
| Тройная (C=C) | Шестиэлектронная двухцентровая | 1,20 | 839 |
Трёхцентровая химическая связь
Дальнейшее развитие представлений о химической связи дал американской физикохимик У.Липскомб, разработавший теорию двухэлектронных трёхцентровых связей и топологическую теорию, позволяющую предсказывать строение ещё некоторых гидридов бора (бороводородов).
Электронная пара в трёхцентровой химической связи становится общей для трёх ядер атомов. В простейшем представителе трёхцентровой химической связи — молекулярном ионе водорода H3+ электронная пара удерживает в едином целом три протона (рис.6).
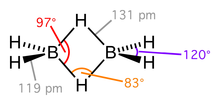 Рис.7.Диборан
Рис.7.ДиборанВ молекуле диборана функционируют четыре одинарные ковалентные связи B-H и две двухэлектронные трёхцентровые связи (рис.7). Межъядерное расстояние в одинарной ковалентной связи B-H составляет 1,19 Å, в то время как аналогичное расстояние в трёхцентровой связи B-H-B составляет 1,31 Å. Угол трёхцентровой связи B-H-B (φ) равен 830. Комбинация двух трёхцентровых связей в молекуле диборана позволяет удерживать ядра атомов бора на расстоянии dB-B = 2 · 1,31 · sin φ/2 = 1,736 Å. Ядра связывающих атомов водорода удалены от плоскости, в которой расположены четыре одинарные ковалентные связи B-H, на расстоянии h = 1,31 · cos φ/2 = 0,981 Å.
Трёхцентровые связи могут реализоваться не только в треугольнике из двух атомов бора и одного атома водорода, но и между тремя атомами бора, например в каркасных бороводородах (пентаборан — B5H9, декаборан — B10H4 и др.). В этих структурах есть обычные (концевые) и входящие в трёхцентровую связь (мостиковые) атома водорода и треугольники из атомов бора.[7]
Существование боранов с их двухэлектронными трёхцентровыми связями с «мостиковыми» атомами водорода нарушало каноническое учение о валентности. Атом водорода, считавшийся ранее стандартным одновалентным элементом, оказался связанным одинаковыми связями с двумя атомами бора и стал формально двухвалентным элементом. Работы У.Липскомба по расшифровке строения боранов расширяли представления о химической связи. Нобелевский комитет удостоил Уильяма Нанна Липскомба премии по химии за 1976 год с формулировкой «За исследования структуры боранов (боргидритов), проясняющие проблемы химических связей).
Многоцентровая химическая связь
Рис.8.Молекула ферроцена Рис.9.Дибензолхром Рис.10.УраноценВ 1951 году Т.Кили и П.Посон неожиданно при синтезе дициклопентадиенила получили совершенно новое железоорганическое соединение. Получение неизвестного ранее исключительно устойчивого жёлто-оранжевого кристаллического соединения железа сразу привлекло к себе внимание.
Э.Фишер и Д.Уилкинсон независимо друг от друга установили структуру нового соединения — два кольца циклопентадиенила расположены параллельно, слоями, или в виде «сэндвича» с атомом железа, расположенным между ними по центру (рис.8). Название «ферроцен» было предложено Р.Вудвордом (вернее, сотрудником его группы Д.Уайтингом). В нём отражено наличие в соединении атома железа и десяти углеродных атомов (zehn — десять).[7]
Все десять связей (C-Fe) в молекуле ферроцена равноценны, величина межъядерного расстояния Fe-c — 2,04 Å. Все атомы углерода в молекуле ферроцена структурно и химически эквивалентны, длина каждой связи C-C 1,40 — 1,41 Å (для сравнения, в бензоле длина связи C-C 1,39 Å). Вокруг атома железа возникает 36- электронная оболочка.[7]
В 1973 году Эрнст Отто Фишер и Джефри Уилкинсон были удостоены Нобелевской премии по химии с формулировкой «За новаторскую, проделанную независимо друг от друга работу, в области металлоорганических, так называемых сандвичевых соединений». Индвар Линдквист, член Шведской королевской академии наук, в своей речи при презентации лауреатов, заявил, что «открытие и доказательство новых принципов связей и структур, имеющихся в сандвичевых соединениях, являются значительным достижением, практическую значимость которых в настоящее время ещё невозможно предсказать».
В настоящее время получены дициклопентадиенильные производные многих металлов. Производные переходных металлов имеют ту же структуру и ту же природу связи, что и ферроцен. Лантаноиды образуют не сандвичеву структуру, а конструкцию, напоминающую трёхлучевую звезду[7]. Атомы La, Ce, Pr, Nd создают, следовательно, пятнадцати центровую химическую связь.
Вскоре вслед за ферроценом был получен дибензолхром (рис.9). По той же схеме получены дибензолмолибден и дибензолванадий[7]. Во всех соединениях этого класса атомы металла удерживают в едином целом два шестичленных кольца. Все 12 связей металл-углерод в этих соединениях идентичны.
Синтезирован также ураноцен [бис(циклооктатетраен)уран], в котором атом урана удерживает два восьмичленных кольца (рис.10). Все 16 связей уран-углерод в ураноцене идентичны. Ураноцен получают взаимодействием UCl4 со смесью циклооктатетраена и калия в тетрагидрофуране при минус 300 C.[8]
Динамика химической связи
Химическая связь достаточно динамична. Так, металлическая связь трансформируется в ковалентную в процессе фазового перехода при испарении металла. Переход металла из твёрдого в парообразное состояние требует затраты больших количеств энергии.[9]
| Металл | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|
| Теплота возгонки (ккал/г-атом) | 36 | 26 | 22 | 21 | 19 |
В парах указанные металлы состоят практически из гомоядерных двухатомных молекул и свободных атомов. При конденсации паров металла ковалентная связь превращается в металлическую.
Испарение солей с типичной ионной связью, например фторидов щелочных металлов, приводит к разрушению ионной связи и образованию гетероядерных двухатомных молекул с полярной ковалентной связью. При этом имеет место образование димерных молекул с мостиковыми связями.
Характеристика химической связи в молекулах фторидов щелочных металлов и их димерах.[2][10]
| ЭF | dЭF, Å | μ, D | Э2F2 | dЭF, Å | <F-Э-F |
|---|---|---|---|---|---|
| LiF | 1,56 | 6,60 | Li2F2 | 1,75 | 105° |
| NaF | 1,93 | — | Na2F2 | 2,08 | 95° |
| KF | 2,17 | 7,37 | K2F2 | 2,35 | 88° |
| RbF | 2,27 | — | Rb2F2 | 2,45 | 84° |
| CsF | 2,35 | 7,88 | Cs2F2 | 2,56 | 79° |
При конденсации паров фторидов щелочных металлов полярная ковалентная связь трансформируется в ионную с образованием соответствующей кристаллической решётки соли.
Механизм перехода ковалентной в металлическую связь
Рис.11. Соотношение между радиусом орбитали электронной пары re и длиной ковалентной химической связи d Рис.12.Ориентация диполей двухатомных молекул и образование искажённого октаэдрического фрагмента кластера при конденсации паров щелочных металлов Рис.13.Объёмноцентрированное кубическое расположение ядер в кристаллах щелочных металлов и связывающего звенаДисперсное притяжение (силы Лондона) обуславливает межатомное взаимодействие и образование гомоядерных двухатомных молекул из атомов щелочных металлов.
Образование ковалентной связи металл-металл сопряжено с деформацией электронных оболочек взаимодействующих атомов — валентные электроны создают связывающую электронную пару, электронная плотность которой концентрируется в пространстве между атомными ядрами возникшей молекулы. Характерной особенностью гомоядерных двухатомных молекул щелочных металлов является большая длина ковалентной связи (в 3,6-5,8 раза больше длины связи в молекуле водорода) и низкая энергия её разрыва.
В теории отталкивания электронных пар считается важным соотношение между радиусом орбитали электронной пары re и длиной ковалентной химической связи d (рис.11). Для элементов каждого периода таблицы Д. И. Менделеева существует некоторый радиус электронной пары (Å):
— 0,6 для элементов вплоть до неона;
— 0,75 для элементов вплоть до аргона;
— 0,75 для элементов вплоть до криптона;
— 0,8 для элементов вплоть до ксенона[11]
Указанное соотношение между re и d определяет неравномерность распределения электрических зарядов в молекуле — в средней части молекулы сосредоточен отрицательный электрический заряд связывающей электронной пары, а на концах молекулы — положительные электрические заряды двух атомных остовов.
Неравномерность распределения электрических зарядов создаёт условия взаимодействия молекул за счёт ориентационных сил (силы Ван-дер-Ваальса). Молекулы щелочных металлов стремятся ориентироваться таким образом, чтобы по сосоедству оказывались разноимённые электрические заряды. В результате между молекулами действуют силы притяжения. Благодаря наличию последних, молекулы щелочных металлов сближаются и более менее прочно стягиваются между собой. Одновременно происходит некоторая деформация каждой из них под действием ближе расположенных полюсов соседних молекул (рис.12).
Фактически, связывающие электроны исходной двухатомной молекулы, попадая в электрическое поле четырёх положительно заряженных атомных остовов молекул щелочных металлов отрываются с орбитального радиуса атома и становятся свободными.
При этом связывающая электронная пара становится общей уже для системы с шестью катионами. Начинается построение кристаллической решётки металла на этапе кластера. В кристаллической решётке щелочных металлов чётко выражена структура связывающего звена, имеющего форму искажённого сплющенного октаэдра — квадратной бипирамиды, высота которой и рёбра базиса равны величина постоянной трансляционной решётки aw (рис.13).
Величина постоянной трансляционной решётки aw кристалла щелочного металла значительно превышает длину ковалентной связи молекулы щелочного металла, поэтому принято считать, что электроны в металле находятся в свободном состоянии:
| Щёлочный металл | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|
| Постоянная решётка aw,Å [12] | 3,5021 | 4,2820 | 5,247 | 5,69 | 6,084 |
| Длина ковалентной связи, Me2, Å [13] | 2,67 | 3,08 | 3,92 | 4,10 | 4,30 |
Математическое построение, связанное со свойствами свободных электронов в металле, обычно отождествляют с «поверхностью Ферми», которую следует рассматривать как геометрическое место, где пребывают электроны, обеспечивая основное свойство металла — проводить электрический ток.[14]
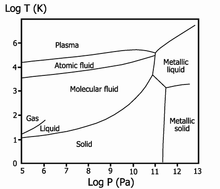
При сопоставлении процесса конденсации паров щелочных металлов с процессом конденсации газов, например, водорода, проявляется характерная особенность в свойствах металла. Так, если при конденсации водорода проявляются слабые межмолекулярные взаимодействия, то при конденсации паров металла протекают процессы, характерные для химических реакций. Сама конденсация паров металла идёт в несколько стадий и может быть описана следующей процессией: свободный атом → двухатомная молекула с ковалентной связью → металлический кластер → компактный металл с металлической связью.
Если рассматривать хронологию водородных технологий, то в 1935 году Юджин Вигнер и Хиллард Хантингтон предсказали возможность существования и металлического водорода. Действительно, ковалентная связь, свойственная молекулярному водороду, переходит в металлическую связь. Этот переход наблюдается для твёрдого водорода при высоком давлении (рис.14).
Механизм перехода ковалентной в ионную связь
Рис.15.Димеризация полярных молекулПереход ковалентной в ионную связь наблюдается для гетероядерных двухатомных молекул с полярной ковалентной связью, например, галогенидов щелочных металлов при переходе из газообразного в твёрдое состояние.
Атомы щелочных металлов при образовании соответствующего галогенида расходуют свой единственный внешний электрон и приобретают чётко выраженный положительный электрический заряд. Отрицательный электрический заряд фиксируется на атоме галогена. Молекулы галогенидов щелочных металлов фактически являются электрическими диполями.
Длина химической связи в молекулах галогенидов щелочных металлов (газовая фаза).[2]| ЭX | Длина химической связи, Å | |||
|---|---|---|---|---|
| ЭF | ЭCl | ЭBr | ЭI | |
| LiX | 1,56 | 2,02 | 2,17 | 2,39 |
| NaX | 1,93 | 2,36 | 2,50 | 2,71 |
| KX | 2,17 | 2,67 | 2,82 | 3,05 |
| Rbx | 2,27 | 2,79 | 2,95 | 3,18 |
| CsX | 2,35 | 2,91 | 3,07 | 3,32 |
Распределение силовых линий электрического диполя полярной ковалентной связи представлено на рис.4. При достаточно близких расстояниях силовые линии взаимно ориентируют полярные молекулы — одноимённо заряженные концы (полюса) их диполей взаимно отталкиваются, а разноимённо заряженные притягиваются. В результате между молекулами действуют силы притяжения, обусловленные взаимодействием их постоянных диполей и носящие название ориентационных сил.
Взаимодействие молекул галогенидов щелочных металлов сопровождается их димеризацией. Димерную молекулу можно рассматривать как электрический квадруполь (рис.15). В настоящее время известны основные характеристики димеров галогенидов щелочных металлов (длины химической связи и валентные углы между связями).[10]
Длина химической связи и валентные углы в димерах галогенидов щелочных металлов (Э2X2)(газовая фаза).[10]| Э2X2 | X=F | X=Cl | X=Br | X=I | ||||
|---|---|---|---|---|---|---|---|---|
| dЭF, Å | <F-Э-F,° | dЭCl, Å | <Cl-Э-Cl,° | dЭBr, Å | <Br-Э-Br, ° | dЭI, Å | <I-Э-I, ° | |
| Li2X2 | 1,75 | 105 | 2,23 | 108 | 2,35 | 110 | 2,54 | 116 |
| Na2X2 | 2,08 | 95 | 2,54 | 105 | 2,69 | 108 | 2,91 | 111 |
| K2X2 | 2,35 | 88 | 2,86 | 98 | 3,02 | 101 | 3,26 | 104 |
| Cs2X2 | 2,56 | 79 | 3,11 | 91 | 3,29 | 94 | 3,54 | 94 |
В процессе конденсации действие ориентационных сил усиливается, межмолекулярное взаимодействие сопровождается образованием кластеров, а затем и твёрдого вещества. Галогениды щелочных металлов образуют кристаллы с простой кубической и объёмно-центрированной кубической решёткой.
Тип кристаллической решётки и постоянная трансляционной решётки для галогенидов щелочных металлов.[12]
| Соединения и тип кристаллической решётки | Постоянная решётки, Å | ||||
|---|---|---|---|---|---|
| Li | Na | K | Rb | Cs | |
| фториды (куб) | 4,0279 | 4,628 | 5,344 | 5,64 | 6,020 |
| хлориды (куб) | 5,1399 | 5,639 | 6,21 | — | — |
| хлориды (ОЦК) | — | — | — | 3,749 | 4,10 |
| бромиды (куб) | 5,501 | 5,973 | 6,599 | 6,868 | 7,23 |
| бромиды (ОЦК) | — | — | — | — | 4,296 |
| иодиды (куб) | 6,012 | 6,475 | 7,066 | 7,340 | 7,66 |
| иодиды (ОЦК) | — | — | — | — | 4,567 |
В процессе кристаллизации происходит дальнейшее увеличение межатомного расстояния, приводящее к срыву электрона с орбитального радиуса атома щелочного металла и передаче электрона атому галогена с образованием соответствующих ионов. Силовые поля ионов равномерно распределяются во всех направлениях в пространстве. В связи с этим в кристаллах щелочных металлов силовое поле каждого иона координирует отнюдь не один ион с противоположным знаком, как принято качественно представлять ионную связь (Na+Cl—).
В кристаллах ионных соединений понятие простых двухионных молекул типа Na+Cl— и Cs+Cl— теряет смысл, поскольку ион щелочного металла связан с шестью ионами хлора (в кристалле хлористого натрия) и с восемью ионами хлора (в кристалле хлористого цезия. При этом все межионные расстояния в кристаллах равноудалены.
Примечания
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 124. — 320 с.
- ↑ 1 2 3 4 5 Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 132-136. — 320 с.
- ↑ Ганкин В.Ю., Ганкин Ю.В. Как образуется химическая связь и протекают химические реакции. — М.: издат.группа «Граница», 2007. — 320 с. — ISBN 978-5-94691296-9
- ↑ Некрасов Б. В. Курс общей химии. — М.: Госхимиздат, 1962. — С. 88. — 976 с.
- ↑ Паулинг Л. Природа химической связи / под редакцией Я.К.Сыркина. — пер. с англ. М.Е.Дяткиной. — М.-Л.: Госхимиздат, 1947. — 440 с.
- ↑ 1 2 Теоретическая органическая химия / под ред. Р.Х.Фрейдлиной. — пер. с англ. Ю.Г.Бунделя. — М.: Изд. иностранной литературы, 1963. — 365 с.
- ↑ 1 2 3 4 5 Леменовский Д.А., Левицкий М.М. Российский химический журнал (журнал Российского химического общества им. Д.И.Менделеева). — 2000. — Т. XLIV, вып.6. — С. 63-86.
- ↑ Химический энциклопедический словарь / гл. ред. И.Л.Кнунянц. — М.: Сов. энциклопедия, 1983. — С. 607. — 792 с.
- ↑ Некрасов Б. В. Курс общей химии. — М.: Госхимиздат, 1962. — С. 679. — 976 с.
- ↑ 1 2 3 Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 155-161. — 320 с.
- ↑ Гиллеспи Р. Геометрия молекул / пер. с англ. Е.З. Засорина и В.С. Мастрюкова, под ред. Ю.А Пентина. — М.: «Мир», 1975. — С. 49. — 278 с.
- ↑ 1 2 Справочник химика. — 2-е изд., перераб. и доп. — Л.-М.: ГНТИ Химической литературы, 1962. — Т. 1. — С. 402-513. — 1072 с.
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ.. — М.: «Химия», 1987. — С. 132-136. — 320 с.
- ↑ Зиман Дж. Электроны в металлах (введение в теорию поверхностей Ферми). Успехи физических наук.. — 1962. — Т. 78, вып.2. — 291 с.
См. также
Литература
- Маррел Дж., Кеттл С., Теддер Дж. Химическая связь. М.: Мир, 1980. 384 с.
- Пиментел Г., Спратли Р. Как квантовая механика объясняет химическую связь. Пер. с англ. М.: Мир, 1973. 332 с.
- Рюденберг К. Физическая природа химической связи. М.: Мир, 1964. 164 c.
- Бердетт Дж. Химическая связь. М.: Бином. Лаборатория знаний, 2008. 248 с. ISBN 978-5-94774-760-7, ISBN 978-5-03-003847-6, ISBN 0-471-97129-4
- Яцимирский К. Б., Яцимирский В. К. Химическая связь. Киев: Вища школа, 1975. 304 c.
- Краснов К. С. Молекулы и химическая связь. 2-ое изд. М: Высшая школа, 1984. 295 с.
- Татевский В. М. Строение молекул. М.: Химия, 1977. 512 с (Глава VIII. «Проблема химической связи в квантовой механике»)
- Татевский В. М. Квантовая механика и теория строения молекул. М.: Изд-во МГУ, 1965. 162 с. (§§ 30-31)
- Бейдер Р. Атомы в молекулах. Квантовая теория. М.: Мир, 2001. 532 c. ISBN 5-03-003363-7 Глава 7. Модели химической связи.
Ссылки
Классификация химических связей.
Крайне редко химические вещества состоят из отдельных, не связанных между собой атомов химических элементов. Таким строением в обычных условиях обладает лишь небольшой ряд газов называемых благородными: гелий, неон, аргон, криптон, ксенон и радон. Чаще же всего химические вещества состоят не из разрозненных атомов, а из их объединений в различные группировки. Такие объединения атомов могут насчитывать несколько единиц, сотен, тысяч или даже больше атомов. Сила, которая удерживает эти атомы в составе таких группировок, называется химическая связь.
Другими словами, можно сказать, что химической связью называют взаимодействие, которое обеспечивает связь отдельных атомов в более сложные структуры (молекулы, ионы, радикалы, кристаллы и др.).
Причиной образования химической связи является то, что энергия более сложных структур меньше суммарной энергии отдельных, образующих ее атомов.
Так, в частности, если при взаимодействии атомов X и Y образуется молекула XY, это означает, что внутренняя энергия молекул этого вещества ниже, чем внутренняя энергия отдельных атомов, из которых оно образовалось:
E(XY) < E(X) + E(Y)
По этой причине при образовании химических связей между отдельными атомами выделятся энергия.
Упрощенно можно считать, что в основе химических связей лежат электростатические силы, обусловленные взаимодействиями положительно заряженных ядер и отрицательно заряженных электронов.
В образовании химических связей принимают участие электроны внешнего электронного слоя с наименьшей энергией связи с ядром, называемые валентными. Например, у бора таковыми являются электроны 2 энергетического уровня – 2 электрона на 2s-орбитали и 1 на 2p-орбитали:

При образовании химической связи каждый атом стремится получить электронную конфигурацию атомов благородных газов, т.е. чтобы в его внешнем электронном слое было 8 электронов (2 для элементов первого периода). Это явление получило название правила октета.
Достижение атомами электронной конфигурации благородного газа возможно, если изначально одиночные атомы сделают часть своих валентных электронов общими для других атомов. При этом образуются общие электронные пары.
В зависимости от степени обобществления электронов можно выделить ковалентную, ионную и металлическую связи.
Ковалентная связь
Ковалентная связь возникает чаще всего между атомами элементов неметаллов. Если атомы неметаллов, образующие ковалентную связь, относятся к разным химическим элементам, такую связь называют ковалентной полярной. Причина такого названия кроется в том, что атомы разных элементов имеют и различную способность притягивать к себе общую электронную пару. Очевидно, что это приводит к смещению общей электронной пары в сторону одного из атомов, в результате чего на нем формируется частичный отрицательный заряд. В свою очередь, на другом атоме формируется частичный положительный заряд. Например, в молекуле хлороводорода электронная пара смещена от атома водорода к атому хлора:

Примеры веществ с ковалентной полярной связью:
СCl4, H2S, CO2, NH3, SiO2 и т.д.
Ковалентная неполярная связь образуется между атомами неметаллов одного химического элемента. Поскольку атомы идентичны, одинакова и их способность оттягивать на себя общие электроны. В связи с этим смещения электронной пары не наблюдается:

Вышеописанный механизм образования ковалентной связи, когда оба атома предоставляют электроны для образования общих электронных пар, называется обменным.
Также существует и донорно-акцепторный механизм.
При образовании ковалентной связи по донорно-акцепторному механизму общая электронная пара образуется за счет заполненной орбитали одного атома (с двумя электронами) и пустой орбитали другого атома. Атом, предоставляющий неподеленную электронную пару, называют донором, а атом со свободной орбиталью – акцептором. В качестве доноров электронных пар выступают атомы, имеющие спаренные электроны, например N, O, P, S.
Например, по донорно-акцепторному механизму происходит образование четвертой ковалентной связи N-H в катионе аммония NH4+:

Помимо полярности ковалентные связи также характеризуются энергией. Энергией связи называют минимальную энергию, необходимую для разрыва связи между атомами.
Энергия связи уменьшается с ростом радиусов связываемых атомов. Так, как мы знаем, атомные радиусы увеличиваются вниз по подгруппам, можно, например, сделать вывод о том, что прочность связи галоген-водород увеличивается в ряду:
HI < HBr < HCl < HF
Также энергия связи зависит от ее кратности – чем больше кратность связи, тем больше ее энергия. Под кратностью связи понимается количество общих электронных пар между двумя атомами.
Ионная связь
Ионную связь можно рассматривать как предельный случай ковалентной полярной связи. Если в ковалентной-полярной связи общая электронная пара смещена частично к одному из пары атомов, то в ионной она практически полностью «отдана» одному из атомов. Атом, отдавший электрон(ы), приобретает положительный заряд и становится катионом, а атом, забравший у него электроны, приобретает отрицательный заряд и становится анионом.
Таким образом, ионная связь — это связь, образованная за счет электростатического притяжения катионов к анионам.
Образование такого типа связи характерно при взаимодействии атомов типичных металлов и типичных неметаллов.
Например, фторид калия. Катион калия получается в результате отрыва от нейтрального атома одного электрона, а ион фтора образуется при присоединении к атому фтора одного электрона:
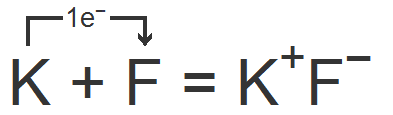
Между получившимися ионами возникает сила электростатического притяжения, в результате чего образуется ионное соединение.
При образовании химической связи электроны от атома натрия перешли к атому хлора и образовались противоположно заряженные ионы, которые имеют завершенный внешний энергетический уровень.
Установлено, что электроны от атома металла не отрываются полностью, а лишь смещаются в сторону атома хлора, как в ковалентной связи.
Большинство бинарных соединений, которые содержат атомы металлов, являются ионными. Например, оксиды, галогениды, сульфиды, нитриды.
Ионная связь возникает также между простыми катионами и простыми анионами (F−, Cl−, S2-), а также между простыми катионами и сложными анионами (NO3−, SO42-, PO43-, OH−). Поэтому к ионным соединениям относят соли и основания (Na2SO4, Cu(NO3)2, (NH4)2SO4), Ca(OH)2, NaOH).
Металлическая связь
Данный тип связи образуется в металлах.
У атомов всех металлов на внешнем электронном слое присутствуют электроны, имеющие низкую энергию связи с ядром атома. Для большинства металлов, энергетически выгодным является процесс потери внешних электронов.
Ввиду такого слабого взаимодействия с ядром эти электроны в металлах весьма подвижны и в каждом кристалле металла непрерывно происходит следующий процесс:
М0 — ne− = Mn+ , где М0 – нейтральный атом металла, а Mn+ катион этого же металла. На рисунке ниже представлена иллюстрация происходящих процессов.

То есть по кристаллу металла «носятся» электроны, отсоединяясь от одного атома металла, образуя из него катион, присоединяясь к другому катиону, образуя нейтральный атом. Такое явление получило название “электронный ветер”, а совокупность свободных электронов в кристалле атома неметалла назвали “электронный газ”. Подобный тип взаимодействия между атомами металлов назвали металлической связью.
Водородная связь
Если атом водорода в каком-либо веществе связан с элементом с высокой электроотрицательностью (азотом, кислородом или фтором), для такого вещества характерно такое явление, как водородная связь.
Поскольку атом водорода связан с электроотрицательным атомом, на атоме водорода образуется частичный положительный заряд, а на атоме электроотрицательного элемента — частичный отрицательный. В связи с этим становится возможным электростатическое притяжения между частично положительно заряженным атомом водорода одной молекулы и электроотрицательным атомом другой. Например водородная связь наблюдается для молекул воды:

Именно водородной связью объясняется аномально высокая температура плавления воды. Кроме воды, также прочные водородные связи образуются в таких веществах, как фтороводород, аммиак, кислородсодержащие кислоты, фенолы, спирты, амины.
Химическая связь — это… Что такое Химическая связь?
 |
 |
Химическая связь — явление взаимодействия атомов, обусловленное перекрыванием электронных облаков связывающихся частиц, которое сопровождается уменьшением полной энергии системы.
При образовании ковалентной химической связи важную роль в уменьшении полной энергии играет обменное взаимодействие.
Теория химического строения Бутлерова
Термин «химическое строение» впервые ввёл А. М. Бутлеров в 1861 году. Также он заложил основы классической теории химического строения. Главные положения этой теории следующие:
- Атомы в молекулах соединены друг с другом в определённой последовательности. Изменение этой последовательности приводит к образованию нового вещества с новыми свойствами.
- Соединение атомов происходит в соответствии с их валентностью.
- Свойства веществ зависят не только от их состава, но и от «химического строения», то есть от порядка соединения атомов в молекулах и характера их взаимного влияния. Наиболее сильно влияют друг на друга атомы, непосредственно связанные между собой.
Типы связи
Простейшая одноэлектронная ковалентная химическая связь
Рис.1. Орбитальные радиусы элементов (ra) и длина одноэлектронной химической связи (d)Простейшая одноэлектронная химическая связь создаётся единственным валентным электроном. Оказывается, что один электрон способен удерживать в едином целом два положительно заряженных иона. В одноэлектронной связи кулоновские силы отталкивания положительно заряженных частиц компенсируются кулоновскими силами притяжения этих частиц к отрицательно заряженному электрону. Валентный электрон становится общим для двух ядер молекулы.
Примерами таких химических соединений являются молекулярные ионы: H2+, Li2+, Na2+, K2+, Rb2+, Cs2+[1]:
| Элемент | H | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|---|
| Электронная конфигурация | 1S1 | [He]2S1 | [Ne]3S1 | [Ar]4S1 | [Kr]5S1 | [Xe]6S1 |
| Межъядерное расстояние в молекулярном ионе xz+, Å | 1,06 | 3,14 | 3,43 | 4,18 | 4,44 | 4,70 |
| Орбитальный радиус атома, Å | 0,53 | 1,57 | 1,715 | 2,09 | 2,22 | 2,35 |
Существование молекулярных ионов водорода и щелочных металлов, в которых химическую связь создаёт единственный валентный электрон, расширяет и дополняет понятие химической связи. В перечисленных ионах ни о каком взаимодействии спинов электронов и перекрывания электронных облаков речи быть не может. Единственный связывающий электрон локализуется в пространстве между ядрами атомов и удерживает их в едином целом, образуя устойчивую химическую систему (рис.1).
Одинарная ковалентная связь
Рис.2.Неполярная ковалентная связь Рис.3.Полярная ковалентная связь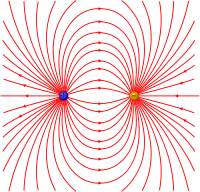 Рис.4.Силовые линии электрического диполя
Рис.4.Силовые линии электрического диполяОдинарная ковалентная химическая связь создаётся связывающей электронной парой. Во всех существующих теориях (теория валентных связей, теория молекулярных орбиталей, теория отталкивания валентных электронных пар, боровская модель химической связи) связывающая электронная пара располагается в пространстве между атомами молекулы. Различают полярную и неполярную ковалентную связи.
Неполярная ковалентная связь имеет место в гомоядерных двухатомных молекулах, в которых связывающая электронная пара равноудалена от обоих ядер молекулярной системы (рис.2). Расстояние d между атомными ядрами можно рассматривать как сумму ковалентных радиусов соответсвующих атомов.
Расстояние между атомными ядрами в одинарной двухэлектронной ковалентной связи короче аналогичного расстояния в простейшей одноэлектронной химической связи.
| Молекула | H2 | Li2 | Na2 | K2 | Rb2 | Cs2 |
|---|---|---|---|---|---|---|
| Межъядерное расстояние, Å [2] | 0,74 | 2,67 | 3,08 | 3,92 | 4,10 | 4,30 |
| Ковалентный радиус, Å | 0,37 | 1,335 | 1,54 | 1,96 | 2,05 | 2,15 |
| Орбитальный радиус, Å | 0,53 | 1,57 | 1,715 | 2,09 | 2,22 | 2,35 |
| Радиус связывающей электронной пары, Å | 0,379 | 0,826 | 0,755 | 0,726 | 0,852 | 0,949 |
| Энергия разрыва связи, кДж/моль [2] | 436 | 102 | 73 | 57 | 49 | 42 |
Разность между орбитальными и ковалентными радиусами характеризует степень перекрытия атомных орбиталей атомов, образующих химическую связь, и отражает деформацию электронной оболочки атомов.
Полярная ковалентная связь возникает в гетероядерных двухатомных молекулах (рис.3). Связывающая электронная пара в полярной химической связи приближена к атому с более высоким первым потенциалом ионизации.[3]
Характеризующее пространственную структуру полярных молекул расстояние d между атомными ядрами можно приближённо рассматривать как сумму ковалентных радиусов соответствующих атомов.[4]
Характеристика некоторых полярных веществ[2]| Молекула | LiH | NaH | KH | RbH | CsH |
|---|---|---|---|---|---|
| Межъядерное расстояние, Å | 1,60 | 1,89 | 2,24 | 2,37 | 2,49 |
| Энергия разрыва связи, кДж/моль | 236 | 200 | 182 | 165 | 176 |
Сдвиг связывающей электронной пары к одному из ядер полярной молекулы приводит к появлению электрического диполя (электродинамика) (рис.4).
Расстояние между центрами тяжести положительного и отрицательного зарядов называют длиной диполя. Полярность молекулы, как и полярность связи, оценивают величиной дипольного момента μ, представляющего собой произведение длины диполя l на величину электронного заряда:
μ = lq
Кратные ковалентные связи
Рис.5.sp2-гибридизация Рис.6.sp-гибридизацияКратные ковалентные связи представлены непредельными органическими соединениями, содержащими двойную и тройную химические связи. Для описания природы непредельных соединений Л.Полинг вводит понятия сигма- и π-связей, гибридизации атомных орбиталей.
Гибридизация Полинга для двух S- и двух p- электронов позволила объяснить направленность химических связей, в частности тетраэдрическую конфигурацию метана. Для объяснения структуры этилена из четырёх равноценных Sp3— электронов атома углерода приходится вычленять один p-электрон для образования дополнительной связи, получившей название π-связи. При этом три оставшиеся Sp2-гибридные орбитали располагаются в плоскости под углом 120° и образуют основные связи, например, плоскую молекулу этилена (рис.5).
В случае молекулы ацетилена в гибридизации принимают участие (по Полингу) всего лишь одна S- и одна p-орбитали, при этом образуются две Sp-орбитали, расположенные под углом в 180° и направленные в противоположные сороны. Две «чистые» p-орбитали атомов углерода попарно перекрываются во взаимоперпендикулярных плоскостях, образуя две π-связи линейной молекулы ацетилена (рис.6).
Взгляды Л.Полинга нашли отражение в его книге «Природа химической связи»[5], на долгие годы ставшей настольной книгой химика. В 1954 году Л.Полинг удостоен Нобелевской премии по химии с формулировкой «За исследование природы химической связи и его применение для опеделения структуры сложных соединений».
Однако физический смысл избирательной гибридизации атомных орбиталей оставался неясным, гибридизация представляла собой алгебраические преобразования, которым не могла быть приписана физическая реальность.
Лайнус Полинг предпринял попытку улучшения описания химической связи, исключив избритаельность гибридизации орбиталей в молекулах непредельных соединений и создав теорию изогнутой химической связи. В своём докладе на симпозиуме по теоретической органической химии, посвящённой памяти Кекуле (Лондон, сентябрь 1958 года), Л.Полинг предложил новый путь описания двойной связи как комбинации двух одинаковых изогнутых химических связей, а тройной связи — трёх изогнутых химических связей[6]. На этом симпозиуме Л.Полинг со всей категоричностью утверждал:
Могут найтись химики, полагающие что чрезвычайно важным новшеством… явилось описание σ,π- описания для двойной или тройной связи и сопряжённых систем вместо описания с помощью изогнутых связей. Я же утверждаю, что σ,π- описание менее удовлетворительно, чем описание с помощью изогнутых связей, что это нововведение является только переходящим и вскоре отомрёт.[6]
В новой теории Полинга все связывающие электроны становились равноценными и равноудалёнными от линии, соединяющей ядра молекулы. Теория изогнутой химической связи Полинга учитывала статистическую интерпретацию волновой функции М.Борна, кулоновскую электронную корреляцию электронов. Появился физический смысл — природа химической связи полностью определяется электрическим взаимодействием ядер и электронов. Чем больше связывающих электронов, тем меньше межъядерное расстояние и прочнее химическая связь между атомами углерода.
| Кратность связи | Структура связи | Межъядерное расстояние, Å | Энергия связи, кДж/моль |
|---|---|---|---|
| Одинарная (C-C) | Двухэлектронная двухцентровая | 1,54 | 348 |
| Двойная (C=C) | Четырёхэлектронная двухцентровая | 1,34 | 614 |
| Тройная (C=C) | Шестиэлектронная двухцентровая | 1,20 | 839 |
Трёхцентровая химическая связь
Дальнейшее развитие представлений о химической связи дал американской физикохимик У.Липскомб, разработавший теорию двухэлектронных трёхцентровых связей и топологическую теорию, позволяющую предсказывать строение ещё некоторых гидридов бора (бороводородов).
Электронная пара в трёхцентровой химической связи становится общей для трёх ядер атомов. В простейшем представителе трёхцентровой химической связи — молекулярном ионе водорода H3+ электронная пара удерживает в едином целом три протона (рис.6).
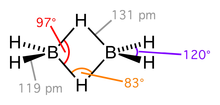 Рис.7.Диборан
Рис.7.ДиборанВ молекуле диборана функционируют четыре одинарные ковалентные связи B-H и две двухэлектронные трёхцентровые связи (рис.7). Межъядерное расстояние в одинарной ковалентной связи B-H составляет 1,19 Å, в то время как аналогичное расстояние в трёхцентровой связи B-H-B составляет 1,31 Å. Угол трёхцентровой связи B-H-B (φ) равен 830. Комбинация двух трёхцентровых связей в молекуле диборана позволяет удерживать ядра атомов бора на расстоянии dB-B = 2 · 1,31 · sin φ/2 = 1,736 Å. Ядра связывающих атомов водорода удалены от плоскости, в которой расположены четыре одинарные ковалентные связи B-H, на расстоянии h = 1,31 · cos φ/2 = 0,981 Å.
Трёхцентровые связи могут реализоваться не только в треугольнике из двух атомов бора и одного атома водорода, но и между тремя атомами бора, например в каркасных бороводородах (пентаборан — B5H9, декаборан — B10H4 и др.). В этих структурах есть обычные (концевые) и входящие в трёхцентровую связь (мостиковые) атома водорода и треугольники из атомов бора.[7]
Существование боранов с их двухэлектронными трёхцентровыми связями с «мостиковыми» атомами водорода нарушало каноническое учение о валентности. Атом водорода, считавшийся ранее стандартным одновалентным элементом, оказался связанным одинаковыми связями с двумя атомами бора и стал формально двухвалентным элементом. Работы У.Липскомба по расшифровке строения боранов расширяли представления о химической связи. Нобелевский комитет удостоил Уильяма Нанна Липскомба премии по химии за 1976 год с формулировкой «За исследования структуры боранов (боргидритов), проясняющие проблемы химических связей).
Многоцентровая химическая связь
Рис.8.Молекула ферроцена Рис.9.Дибензолхром Рис.10.УраноценВ 1951 году Т.Кили и П.Посон неожиданно при синтезе дициклопентадиенила получили совершенно новое железоорганическое соединение. Получение неизвестного ранее исключительно устойчивого жёлто-оранжевого кристаллического соединения железа сразу привлекло к себе внимание.
Э.Фишер и Д.Уилкинсон независимо друг от друга установили структуру нового соединения — два кольца циклопентадиенила расположены параллельно, слоями, или в виде «сэндвича» с атомом железа, расположенным между ними по центру (рис.8). Название «ферроцен» было предложено Р.Вудвордом (вернее, сотрудником его группы Д.Уайтингом). В нём отражено наличие в соединении атома железа и десяти углеродных атомов (zehn — десять).[7]
Все десять связей (C-Fe) в молекуле ферроцена равноценны, величина межъядерного расстояния Fe-c — 2,04 Å. Все атомы углерода в молекуле ферроцена структурно и химически эквивалентны, длина каждой связи C-C 1,40 — 1,41 Å (для сравнения, в бензоле длина связи C-C 1,39 Å). Вокруг атома железа возникает 36- электронная оболочка.[7]
В 1973 году Эрнст Отто Фишер и Джефри Уилкинсон были удостоены Нобелевской премии по химии с формулировкой «За новаторскую, проделанную независимо друг от друга работу, в области металлоорганических, так называемых сандвичевых соединений». Индвар Линдквист, член Шведской королевской академии наук, в своей речи при презентации лауреатов, заявил, что «открытие и доказательство новых принципов связей и структур, имеющихся в сандвичевых соединениях, являются значительным достижением, практическую значимость которых в настоящее время ещё невозможно предсказать».
В настоящее время получены дициклопентадиенильные производные многих металлов. Производные переходных металлов имеют ту же структуру и ту же природу связи, что и ферроцен. Лантаноиды образуют не сандвичеву структуру, а конструкцию, напоминающую трёхлучевую звезду[7]. Атомы La, Ce, Pr, Nd создают, следовательно, пятнадцати центровую химическую связь.
Вскоре вслед за ферроценом был получен дибензолхром (рис.9). По той же схеме получены дибензолмолибден и дибензолванадий[7]. Во всех соединениях этого класса атомы металла удерживают в едином целом два шестичленных кольца. Все 12 связей металл-углерод в этих соединениях идентичны.
Синтезирован также ураноцен [бис(циклооктатетраен)уран], в котором атом урана удерживает два восьмичленных кольца (рис.10). Все 16 связей уран-углерод в ураноцене идентичны. Ураноцен получают взаимодействием UCl4 со смесью циклооктатетраена и калия в тетрагидрофуране при минус 300 C.[8]
Динамика химической связи
Химическая связь достаточно динамична. Так, металлическая связь трансформируется в ковалентную в процессе фазового перехода при испарении металла. Переход металла из твёрдого в парообразное состояние требует затраты больших количеств энергии.[9]
| Металл | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|
| Теплота возгонки (ккал/г-атом) | 36 | 26 | 22 | 21 | 19 |
В парах указанные металлы состоят практически из гомоядерных двухатомных молекул и свободных атомов. При конденсации паров металла ковалентная связь превращается в металлическую.
Испарение солей с типичной ионной связью, например фторидов щелочных металлов, приводит к разрушению ионной связи и образованию гетероядерных двухатомных молекул с полярной ковалентной связью. При этом имеет место образование димерных молекул с мостиковыми связями.
Характеристика химической связи в молекулах фторидов щелочных металлов и их димерах.[2][10]
| ЭF | dЭF, Å | μ, D | Э2F2 | dЭF, Å | <F-Э-F |
|---|---|---|---|---|---|
| LiF | 1,56 | 6,60 | Li2F2 | 1,75 | 105° |
| NaF | 1,93 | — | Na2F2 | 2,08 | 95° |
| KF | 2,17 | 7,37 | K2F2 | 2,35 | 88° |
| RbF | 2,27 | — | Rb2F2 | 2,45 | 84° |
| CsF | 2,35 | 7,88 | Cs2F2 | 2,56 | 79° |
При конденсации паров фторидов щелочных металлов полярная ковалентная связь трансформируется в ионную с образованием соответствующей кристаллической решётки соли.
Механизм перехода ковалентной в металлическую связь
Рис.11. Соотношение между радиусом орбитали электронной пары re и длиной ковалентной химической связи d Рис.12.Ориентация диполей двухатомных молекул и образование искажённого октаэдрического фрагмента кластера при конденсации паров щелочных металлов Рис.13.Объёмноцентрированное кубическое расположение ядер в кристаллах щелочных металлов и связывающего звенаДисперсное притяжение (силы Лондона) обуславливает межатомное взаимодействие и образование гомоядерных двухатомных молекул из атомов щелочных металлов.
Образование ковалентной связи металл-металл сопряжено с деформацией электронных оболочек взаимодействующих атомов — валентные электроны создают связывающую электронную пару, электронная плотность которой концентрируется в пространстве между атомными ядрами возникшей молекулы. Характерной особенностью гомоядерных двухатомных молекул щелочных металлов является большая длина ковалентной связи (в 3,6-5,8 раза больше длины связи в молекуле водорода) и низкая энергия её разрыва.
В теории отталкивания электронных пар считается важным соотношение между радиусом орбитали электронной пары re и длиной ковалентной химической связи d (рис.11). Для элементов каждого периода таблицы Д. И. Менделеева существует некоторый радиус электронной пары (Å):
— 0,6 для элементов вплоть до неона;
— 0,75 для элементов вплоть до аргона;
— 0,75 для элементов вплоть до криптона;
— 0,8 для элементов вплоть до ксенона[11]
Указанное соотношение между re и d определяет неравномерность распределения электрических зарядов в молекуле — в средней части молекулы сосредоточен отрицательный электрический заряд связывающей электронной пары, а на концах молекулы — положительные электрические заряды двух атомных остовов.
Неравномерность распределения электрических зарядов создаёт условия взаимодействия молекул за счёт ориентационных сил (силы Ван-дер-Ваальса). Молекулы щелочных металлов стремятся ориентироваться таким образом, чтобы по сосоедству оказывались разноимённые электрические заряды. В результате между молекулами действуют силы притяжения. Благодаря наличию последних, молекулы щелочных металлов сближаются и более менее прочно стягиваются между собой. Одновременно происходит некоторая деформация каждой из них под действием ближе расположенных полюсов соседних молекул (рис.12).
Фактически, связывающие электроны исходной двухатомной молекулы, попадая в электрическое поле четырёх положительно заряженных атомных остовов молекул щелочных металлов отрываются с орбитального радиуса атома и становятся свободными.
При этом связывающая электронная пара становится общей уже для системы с шестью катионами. Начинается построение кристаллической решётки металла на этапе кластера. В кристаллической решётке щелочных металлов чётко выражена структура связывающего звена, имеющего форму искажённого сплющенного октаэдра — квадратной бипирамиды, высота которой и рёбра базиса равны величина постоянной трансляционной решётки aw (рис.13).
Величина постоянной трансляционной решётки aw кристалла щелочного металла значительно превышает длину ковалентной связи молекулы щелочного металла, поэтому принято считать, что электроны в металле находятся в свободном состоянии:
| Щёлочный металл | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|
| Постоянная решётка aw,Å [12] | 3,5021 | 4,2820 | 5,247 | 5,69 | 6,084 |
| Длина ковалентной связи, Me2, Å [13] | 2,67 | 3,08 | 3,92 | 4,10 | 4,30 |
Математическое построение, связанное со свойствами свободных электронов в металле, обычно отождествляют с «поверхностью Ферми», которую следует рассматривать как геометрическое место, где пребывают электроны, обеспечивая основное свойство металла — проводить электрический ток.[14]
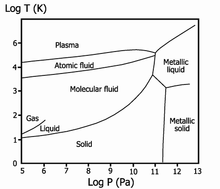
При сопоставлении процесса конденсации паров щелочных металлов с процессом конденсации газов, например, водорода, проявляется характерная особенность в свойствах металла. Так, если при конденсации водорода проявляются слабые межмолекулярные взаимодействия, то при конденсации паров металла протекают процессы, характерные для химических реакций. Сама конденсация паров металла идёт в несколько стадий и может быть описана следующей процессией: свободный атом → двухатомная молекула с ковалентной связью → металлический кластер → компактный металл с металлической связью.
Если рассматривать хронологию водородных технологий, то в 1935 году Юджин Вигнер и Хиллард Хантингтон предсказали возможность существования и металлического водорода. Действительно, ковалентная связь, свойственная молекулярному водороду, переходит в металлическую связь. Этот переход наблюдается для твёрдого водорода при высоком давлении (рис.14).
Механизм перехода ковалентной в ионную связь
Рис.15.Димеризация полярных молекулПереход ковалентной в ионную связь наблюдается для гетероядерных двухатомных молекул с полярной ковалентной связью, например, галогенидов щелочных металлов при переходе из газообразного в твёрдое состояние.
Атомы щелочных металлов при образовании соответствующего галогенида расходуют свой единственный внешний электрон и приобретают чётко выраженный положительный электрический заряд. Отрицательный электрический заряд фиксируется на атоме галогена. Молекулы галогенидов щелочных металлов фактически являются электрическими диполями.
Длина химической связи в молекулах галогенидов щелочных металлов (газовая фаза).[2]| ЭX | Длина химической связи, Å | |||
|---|---|---|---|---|
| ЭF | ЭCl | ЭBr | ЭI | |
| LiX | 1,56 | 2,02 | 2,17 | 2,39 |
| NaX | 1,93 | 2,36 | 2,50 | 2,71 |
| KX | 2,17 | 2,67 | 2,82 | 3,05 |
| Rbx | 2,27 | 2,79 | 2,95 | 3,18 |
| CsX | 2,35 | 2,91 | 3,07 | 3,32 |
Распределение силовых линий электрического диполя полярной ковалентной связи представлено на рис.4. При достаточно близких расстояниях силовые линии взаимно ориентируют полярные молекулы — одноимённо заряженные концы (полюса) их диполей взаимно отталкиваются, а разноимённо заряженные притягиваются. В результате между молекулами действуют силы притяжения, обусловленные взаимодействием их постоянных диполей и носящие название ориентационных сил.
Взаимодействие молекул галогенидов щелочных металлов сопровождается их димеризацией. Димерную молекулу можно рассматривать как электрический квадруполь (рис.15). В настоящее время известны основные характеристики димеров галогенидов щелочных металлов (длины химической связи и валентные углы между связями).[10]
Длина химической связи и валентные углы в димерах галогенидов щелочных металлов (Э2X2)(газовая фаза).[10]| Э2X2 | X=F | X=Cl | X=Br | X=I | ||||
|---|---|---|---|---|---|---|---|---|
| dЭF, Å | <F-Э-F,° | dЭCl, Å | <Cl-Э-Cl,° | dЭBr, Å | <Br-Э-Br, ° | dЭI, Å | <I-Э-I, ° | |
| Li2X2 | 1,75 | 105 | 2,23 | 108 | 2,35 | 110 | 2,54 | 116 |
| Na2X2 | 2,08 | 95 | 2,54 | 105 | 2,69 | 108 | 2,91 | 111 |
| K2X2 | 2,35 | 88 | 2,86 | 98 | 3,02 | 101 | 3,26 | 104 |
| Cs2X2 | 2,56 | 79 | 3,11 | 91 | 3,29 | 94 | 3,54 | 94 |
В процессе конденсации действие ориентационных сил усиливается, межмолекулярное взаимодействие сопровождается образованием кластеров, а затем и твёрдого вещества. Галогениды щелочных металлов образуют кристаллы с простой кубической и объёмно-центрированной кубической решёткой.
Тип кристаллической решётки и постоянная трансляционной решётки для галогенидов щелочных металлов.[12]
| Соединения и тип кристаллической решётки | Постоянная решётки, Å | ||||
|---|---|---|---|---|---|
| Li | Na | K | Rb | Cs | |
| фториды (куб) | 4,0279 | 4,628 | 5,344 | 5,64 | 6,020 |
| хлориды (куб) | 5,1399 | 5,639 | 6,21 | — | — |
| хлориды (ОЦК) | — | — | — | 3,749 | 4,10 |
| бромиды (куб) | 5,501 | 5,973 | 6,599 | 6,868 | 7,23 |
| бромиды (ОЦК) | — | — | — | — | 4,296 |
| иодиды (куб) | 6,012 | 6,475 | 7,066 | 7,340 | 7,66 |
| иодиды (ОЦК) | — | — | — | — | 4,567 |
В процессе кристаллизации происходит дальнейшее увеличение межатомного расстояния, приводящее к срыву электрона с орбитального радиуса атома щелочного металла и передаче электрона атому галогена с образованием соответствующих ионов. Силовые поля ионов равномерно распределяются во всех направлениях в пространстве. В связи с этим в кристаллах щелочных металлов силовое поле каждого иона координирует отнюдь не один ион с противоположным знаком, как принято качественно представлять ионную связь (Na+Cl—).
В кристаллах ионных соединений понятие простых двухионных молекул типа Na+Cl— и Cs+Cl— теряет смысл, поскольку ион щелочного металла связан с шестью ионами хлора (в кристалле хлористого натрия) и с восемью ионами хлора (в кристалле хлористого цезия. При этом все межионные расстояния в кристаллах равноудалены.
Примечания
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 124. — 320 с.
- ↑ 1 2 3 4 5 Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 132-136. — 320 с.
- ↑ Ганкин В.Ю., Ганкин Ю.В. Как образуется химическая связь и протекают химические реакции. — М.: издат.группа «Граница», 2007. — 320 с. — ISBN 978-5-94691296-9
- ↑ Некрасов Б. В. Курс общей химии. — М.: Госхимиздат, 1962. — С. 88. — 976 с.
- ↑ Паулинг Л. Природа химической связи / под редакцией Я.К.Сыркина. — пер. с англ. М.Е.Дяткиной. — М.-Л.: Госхимиздат, 1947. — 440 с.
- ↑ 1 2 Теоретическая органическая химия / под ред. Р.Х.Фрейдлиной. — пер. с англ. Ю.Г.Бунделя. — М.: Изд. иностранной литературы, 1963. — 365 с.
- ↑ 1 2 3 4 5 Леменовский Д.А., Левицкий М.М. Российский химический журнал (журнал Российского химического общества им. Д.И.Менделеева). — 2000. — Т. XLIV, вып.6. — С. 63-86.
- ↑ Химический энциклопедический словарь / гл. ред. И.Л.Кнунянц. — М.: Сов. энциклопедия, 1983. — С. 607. — 792 с.
- ↑ Некрасов Б. В. Курс общей химии. — М.: Госхимиздат, 1962. — С. 679. — 976 с.
- ↑ 1 2 3 Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 155-161. — 320 с.
- ↑ Гиллеспи Р. Геометрия молекул / пер. с англ. Е.З. Засорина и В.С. Мастрюкова, под ред. Ю.А Пентина. — М.: «Мир», 1975. — С. 49. — 278 с.
- ↑ 1 2 Справочник химика. — 2-е изд., перераб. и доп. — Л.-М.: ГНТИ Химической литературы, 1962. — Т. 1. — С. 402-513. — 1072 с.
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ.. — М.: «Химия», 1987. — С. 132-136. — 320 с.
- ↑ Зиман Дж. Электроны в металлах (введение в теорию поверхностей Ферми). Успехи физических наук.. — 1962. — Т. 78, вып.2. — 291 с.
См. также
Литература
- Маррел Дж., Кеттл С., Теддер Дж. Химическая связь. М.: Мир, 1980. 384 с.
- Пиментел Г., Спратли Р. Как квантовая механика объясняет химическую связь. Пер. с англ. М.: Мир, 1973. 332 с.
- Рюденберг К. Физическая природа химической связи. М.: Мир, 1964. 164 c.
- Бердетт Дж. Химическая связь. М.: Бином. Лаборатория знаний, 2008. 248 с. ISBN 978-5-94774-760-7, ISBN 978-5-03-003847-6, ISBN 0-471-97129-4
- Яцимирский К. Б., Яцимирский В. К. Химическая связь. Киев: Вища школа, 1975. 304 c.
- Краснов К. С. Молекулы и химическая связь. 2-ое изд. М: Высшая школа, 1984. 295 с.
- Татевский В. М. Строение молекул. М.: Химия, 1977. 512 с (Глава VIII. «Проблема химической связи в квантовой механике»)
- Татевский В. М. Квантовая механика и теория строения молекул. М.: Изд-во МГУ, 1965. 162 с. (§§ 30-31)
- Бейдер Р. Атомы в молекулах. Квантовая теория. М.: Мир, 2001. 532 c. ISBN 5-03-003363-7 Глава 7. Модели химической связи.
Ссылки
Химическая связь — это… Что такое Химическая связь?
 |
 |
Химическая связь — явление взаимодействия атомов, обусловленное перекрыванием электронных облаков связывающихся частиц, которое сопровождается уменьшением полной энергии системы.
При образовании ковалентной химической связи важную роль в уменьшении полной энергии играет обменное взаимодействие.
Теория химического строения Бутлерова
Термин «химическое строение» впервые ввёл А. М. Бутлеров в 1861 году. Также он заложил основы классической теории химического строения. Главные положения этой теории следующие:
- Атомы в молекулах соединены друг с другом в определённой последовательности. Изменение этой последовательности приводит к образованию нового вещества с новыми свойствами.
- Соединение атомов происходит в соответствии с их валентностью.
- Свойства веществ зависят не только от их состава, но и от «химического строения», то есть от порядка соединения атомов в молекулах и характера их взаимного влияния. Наиболее сильно влияют друг на друга атомы, непосредственно связанные между собой.
Типы связи
Простейшая одноэлектронная ковалентная химическая связь
Рис.1. Орбитальные радиусы элементов (ra) и длина одноэлектронной химической связи (d)Простейшая одноэлектронная химическая связь создаётся единственным валентным электроном. Оказывается, что один электрон способен удерживать в едином целом два положительно заряженных иона. В одноэлектронной связи кулоновские силы отталкивания положительно заряженных частиц компенсируются кулоновскими силами притяжения этих частиц к отрицательно заряженному электрону. Валентный электрон становится общим для двух ядер молекулы.
Примерами таких химических соединений являются молекулярные ионы: H2+, Li2+, Na2+, K2+, Rb2+, Cs2+[1]:
| Элемент | H | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|---|
| Электронная конфигурация | 1S1 | [He]2S1 | [Ne]3S1 | [Ar]4S1 | [Kr]5S1 | [Xe]6S1 |
| Межъядерное расстояние в молекулярном ионе xz+, Å | 1,06 | 3,14 | 3,43 | 4,18 | 4,44 | 4,70 |
| Орбитальный радиус атома, Å | 0,53 | 1,57 | 1,715 | 2,09 | 2,22 | 2,35 |
Существование молекулярных ионов водорода и щелочных металлов, в которых химическую связь создаёт единственный валентный электрон, расширяет и дополняет понятие химической связи. В перечисленных ионах ни о каком взаимодействии спинов электронов и перекрывания электронных облаков речи быть не может. Единственный связывающий электрон локализуется в пространстве между ядрами атомов и удерживает их в едином целом, образуя устойчивую химическую систему (рис.1).
Одинарная ковалентная связь
Рис.2.Неполярная ковалентная связь Рис.3.Полярная ковалентная связь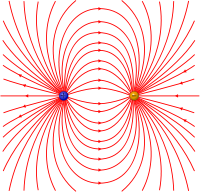 Рис.4.Силовые линии электрического диполя
Рис.4.Силовые линии электрического диполяОдинарная ковалентная химическая связь создаётся связывающей электронной парой. Во всех существующих теориях (теория валентных связей, теория молекулярных орбиталей, теория отталкивания валентных электронных пар, боровская модель химической связи) связывающая электронная пара располагается в пространстве между атомами молекулы. Различают полярную и неполярную ковалентную связи.
Неполярная ковалентная связь имеет место в гомоядерных двухатомных молекулах, в которых связывающая электронная пара равноудалена от обоих ядер молекулярной системы (рис.2). Расстояние d между атомными ядрами можно рассматривать как сумму ковалентных радиусов соответсвующих атомов.
Расстояние между атомными ядрами в одинарной двухэлектронной ковалентной связи короче аналогичного расстояния в простейшей одноэлектронной химической связи.
| Молекула | H2 | Li2 | Na2 | K2 | Rb2 | Cs2 |
|---|---|---|---|---|---|---|
| Межъядерное расстояние, Å [2] | 0,74 | 2,67 | 3,08 | 3,92 | 4,10 | 4,30 |
| Ковалентный радиус, Å | 0,37 | 1,335 | 1,54 | 1,96 | 2,05 | 2,15 |
| Орбитальный радиус, Å | 0,53 | 1,57 | 1,715 | 2,09 | 2,22 | 2,35 |
| Радиус связывающей электронной пары, Å | 0,379 | 0,826 | 0,755 | 0,726 | 0,852 | 0,949 |
| Энергия разрыва связи, кДж/моль [2] | 436 | 102 | 73 | 57 | 49 | 42 |
Разность между орбитальными и ковалентными радиусами характеризует степень перекрытия атомных орбиталей атомов, образующих химическую связь, и отражает деформацию электронной оболочки атомов.
Полярная ковалентная связь возникает в гетероядерных двухатомных молекулах (рис.3). Связывающая электронная пара в полярной химической связи приближена к атому с более высоким первым потенциалом ионизации.[3]
Характеризующее пространственную структуру полярных молекул расстояние d между атомными ядрами можно приближённо рассматривать как сумму ковалентных радиусов соответствующих атомов.[4]
Характеристика некоторых полярных веществ[2]| Молекула | LiH | NaH | KH | RbH | CsH |
|---|---|---|---|---|---|
| Межъядерное расстояние, Å | 1,60 | 1,89 | 2,24 | 2,37 | 2,49 |
| Энергия разрыва связи, кДж/моль | 236 | 200 | 182 | 165 | 176 |
Сдвиг связывающей электронной пары к одному из ядер полярной молекулы приводит к появлению электрического диполя (электродинамика) (рис.4).
Расстояние между центрами тяжести положительного и отрицательного зарядов называют длиной диполя. Полярность молекулы, как и полярность связи, оценивают величиной дипольного момента μ, представляющего собой произведение длины диполя l на величину электронного заряда:
μ = lq
Кратные ковалентные связи
Рис.5.sp2-гибридизация Рис.6.sp-гибридизацияКратные ковалентные связи представлены непредельными органическими соединениями, содержащими двойную и тройную химические связи. Для описания природы непредельных соединений Л.Полинг вводит понятия сигма- и π-связей, гибридизации атомных орбиталей.
Гибридизация Полинга для двух S- и двух p- электронов позволила объяснить направленность химических связей, в частности тетраэдрическую конфигурацию метана. Для объяснения структуры этилена из четырёх равноценных Sp3— электронов атома углерода приходится вычленять один p-электрон для образования дополнительной связи, получившей название π-связи. При этом три оставшиеся Sp2-гибридные орбитали располагаются в плоскости под углом 120° и образуют основные связи, например, плоскую молекулу этилена (рис.5).
В случае молекулы ацетилена в гибридизации принимают участие (по Полингу) всего лишь одна S- и одна p-орбитали, при этом образуются две Sp-орбитали, расположенные под углом в 180° и направленные в противоположные сороны. Две «чистые» p-орбитали атомов углерода попарно перекрываются во взаимоперпендикулярных плоскостях, образуя две π-связи линейной молекулы ацетилена (рис.6).
Взгляды Л.Полинга нашли отражение в его книге «Природа химической связи»[5], на долгие годы ставшей настольной книгой химика. В 1954 году Л.Полинг удостоен Нобелевской премии по химии с формулировкой «За исследование природы химической связи и его применение для опеделения структуры сложных соединений».
Однако физический смысл избирательной гибридизации атомных орбиталей оставался неясным, гибридизация представляла собой алгебраические преобразования, которым не могла быть приписана физическая реальность.
Лайнус Полинг предпринял попытку улучшения описания химической связи, исключив избритаельность гибридизации орбиталей в молекулах непредельных соединений и создав теорию изогнутой химической связи. В своём докладе на симпозиуме по теоретической органической химии, посвящённой памяти Кекуле (Лондон, сентябрь 1958 года), Л.Полинг предложил новый путь описания двойной связи как комбинации двух одинаковых изогнутых химических связей, а тройной связи — трёх изогнутых химических связей[6]. На этом симпозиуме Л.Полинг со всей категоричностью утверждал:
Могут найтись химики, полагающие что чрезвычайно важным новшеством… явилось описание σ,π- описания для двойной или тройной связи и сопряжённых систем вместо описания с помощью изогнутых связей. Я же утверждаю, что σ,π- описание менее удовлетворительно, чем описание с помощью изогнутых связей, что это нововведение является только переходящим и вскоре отомрёт.[6]
В новой теории Полинга все связывающие электроны становились равноценными и равноудалёнными от линии, соединяющей ядра молекулы. Теория изогнутой химической связи Полинга учитывала статистическую интерпретацию волновой функции М.Борна, кулоновскую электронную корреляцию электронов. Появился физический смысл — природа химической связи полностью определяется электрическим взаимодействием ядер и электронов. Чем больше связывающих электронов, тем меньше межъядерное расстояние и прочнее химическая связь между атомами углерода.
| Кратность связи | Структура связи | Межъядерное расстояние, Å | Энергия связи, кДж/моль |
|---|---|---|---|
| Одинарная (C-C) | Двухэлектронная двухцентровая | 1,54 | 348 |
| Двойная (C=C) | Четырёхэлектронная двухцентровая | 1,34 | 614 |
| Тройная (C=C) | Шестиэлектронная двухцентровая | 1,20 | 839 |
Трёхцентровая химическая связь
Дальнейшее развитие представлений о химической связи дал американской физикохимик У.Липскомб, разработавший теорию двухэлектронных трёхцентровых связей и топологическую теорию, позволяющую предсказывать строение ещё некоторых гидридов бора (бороводородов).
Электронная пара в трёхцентровой химической связи становится общей для трёх ядер атомов. В простейшем представителе трёхцентровой химической связи — молекулярном ионе водорода H3+ электронная пара удерживает в едином целом три протона (рис.6).
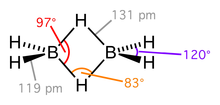 Рис.7.Диборан
Рис.7.ДиборанВ молекуле диборана функционируют четыре одинарные ковалентные связи B-H и две двухэлектронные трёхцентровые связи (рис.7). Межъядерное расстояние в одинарной ковалентной связи B-H составляет 1,19 Å, в то время как аналогичное расстояние в трёхцентровой связи B-H-B составляет 1,31 Å. Угол трёхцентровой связи B-H-B (φ) равен 830. Комбинация двух трёхцентровых связей в молекуле диборана позволяет удерживать ядра атомов бора на расстоянии dB-B = 2 · 1,31 · sin φ/2 = 1,736 Å. Ядра связывающих атомов водорода удалены от плоскости, в которой расположены четыре одинарные ковалентные связи B-H, на расстоянии h = 1,31 · cos φ/2 = 0,981 Å.
Трёхцентровые связи могут реализоваться не только в треугольнике из двух атомов бора и одного атома водорода, но и между тремя атомами бора, например в каркасных бороводородах (пентаборан — B5H9, декаборан — B10H4 и др.). В этих структурах есть обычные (концевые) и входящие в трёхцентровую связь (мостиковые) атома водорода и треугольники из атомов бора.[7]
Существование боранов с их двухэлектронными трёхцентровыми связями с «мостиковыми» атомами водорода нарушало каноническое учение о валентности. Атом водорода, считавшийся ранее стандартным одновалентным элементом, оказался связанным одинаковыми связями с двумя атомами бора и стал формально двухвалентным элементом. Работы У.Липскомба по расшифровке строения боранов расширяли представления о химической связи. Нобелевский комитет удостоил Уильяма Нанна Липскомба премии по химии за 1976 год с формулировкой «За исследования структуры боранов (боргидритов), проясняющие проблемы химических связей).
Многоцентровая химическая связь
Рис.8.Молекула ферроцена Рис.9.Дибензолхром Рис.10.УраноценВ 1951 году Т.Кили и П.Посон неожиданно при синтезе дициклопентадиенила получили совершенно новое железоорганическое соединение. Получение неизвестного ранее исключительно устойчивого жёлто-оранжевого кристаллического соединения железа сразу привлекло к себе внимание.
Э.Фишер и Д.Уилкинсон независимо друг от друга установили структуру нового соединения — два кольца циклопентадиенила расположены параллельно, слоями, или в виде «сэндвича» с атомом железа, расположенным между ними по центру (рис.8). Название «ферроцен» было предложено Р.Вудвордом (вернее, сотрудником его группы Д.Уайтингом). В нём отражено наличие в соединении атома железа и десяти углеродных атомов (zehn — десять).[7]
Все десять связей (C-Fe) в молекуле ферроцена равноценны, величина межъядерного расстояния Fe-c — 2,04 Å. Все атомы углерода в молекуле ферроцена структурно и химически эквивалентны, длина каждой связи C-C 1,40 — 1,41 Å (для сравнения, в бензоле длина связи C-C 1,39 Å). Вокруг атома железа возникает 36- электронная оболочка.[7]
В 1973 году Эрнст Отто Фишер и Джефри Уилкинсон были удостоены Нобелевской премии по химии с формулировкой «За новаторскую, проделанную независимо друг от друга работу, в области металлоорганических, так называемых сандвичевых соединений». Индвар Линдквист, член Шведской королевской академии наук, в своей речи при презентации лауреатов, заявил, что «открытие и доказательство новых принципов связей и структур, имеющихся в сандвичевых соединениях, являются значительным достижением, практическую значимость которых в настоящее время ещё невозможно предсказать».
В настоящее время получены дициклопентадиенильные производные многих металлов. Производные переходных металлов имеют ту же структуру и ту же природу связи, что и ферроцен. Лантаноиды образуют не сандвичеву структуру, а конструкцию, напоминающую трёхлучевую звезду[7]. Атомы La, Ce, Pr, Nd создают, следовательно, пятнадцати центровую химическую связь.
Вскоре вслед за ферроценом был получен дибензолхром (рис.9). По той же схеме получены дибензолмолибден и дибензолванадий[7]. Во всех соединениях этого класса атомы металла удерживают в едином целом два шестичленных кольца. Все 12 связей металл-углерод в этих соединениях идентичны.
Синтезирован также ураноцен [бис(циклооктатетраен)уран], в котором атом урана удерживает два восьмичленных кольца (рис.10). Все 16 связей уран-углерод в ураноцене идентичны. Ураноцен получают взаимодействием UCl4 со смесью циклооктатетраена и калия в тетрагидрофуране при минус 300 C.[8]
Динамика химической связи
Химическая связь достаточно динамична. Так, металлическая связь трансформируется в ковалентную в процессе фазового перехода при испарении металла. Переход металла из твёрдого в парообразное состояние требует затраты больших количеств энергии.[9]
| Металл | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|
| Теплота возгонки (ккал/г-атом) | 36 | 26 | 22 | 21 | 19 |
В парах указанные металлы состоят практически из гомоядерных двухатомных молекул и свободных атомов. При конденсации паров металла ковалентная связь превращается в металлическую.
Испарение солей с типичной ионной связью, например фторидов щелочных металлов, приводит к разрушению ионной связи и образованию гетероядерных двухатомных молекул с полярной ковалентной связью. При этом имеет место образование димерных молекул с мостиковыми связями.
Характеристика химической связи в молекулах фторидов щелочных металлов и их димерах.[2][10]
| ЭF | dЭF, Å | μ, D | Э2F2 | dЭF, Å | <F-Э-F |
|---|---|---|---|---|---|
| LiF | 1,56 | 6,60 | Li2F2 | 1,75 | 105° |
| NaF | 1,93 | — | Na2F2 | 2,08 | 95° |
| KF | 2,17 | 7,37 | K2F2 | 2,35 | 88° |
| RbF | 2,27 | — | Rb2F2 | 2,45 | 84° |
| CsF | 2,35 | 7,88 | Cs2F2 | 2,56 | 79° |
При конденсации паров фторидов щелочных металлов полярная ковалентная связь трансформируется в ионную с образованием соответствующей кристаллической решётки соли.
Механизм перехода ковалентной в металлическую связь
Рис.11. Соотношение между радиусом орбитали электронной пары re и длиной ковалентной химической связи d Рис.12.Ориентация диполей двухатомных молекул и образование искажённого октаэдрического фрагмента кластера при конденсации паров щелочных металлов Рис.13.Объёмноцентрированное кубическое расположение ядер в кристаллах щелочных металлов и связывающего звенаДисперсное притяжение (силы Лондона) обуславливает межатомное взаимодействие и образование гомоядерных двухатомных молекул из атомов щелочных металлов.
Образование ковалентной связи металл-металл сопряжено с деформацией электронных оболочек взаимодействующих атомов — валентные электроны создают связывающую электронную пару, электронная плотность которой концентрируется в пространстве между атомными ядрами возникшей молекулы. Характерной особенностью гомоядерных двухатомных молекул щелочных металлов является большая длина ковалентной связи (в 3,6-5,8 раза больше длины связи в молекуле водорода) и низкая энергия её разрыва.
В теории отталкивания электронных пар считается важным соотношение между радиусом орбитали электронной пары re и длиной ковалентной химической связи d (рис.11). Для элементов каждого периода таблицы Д. И. Менделеева существует некоторый радиус электронной пары (Å):
— 0,6 для элементов вплоть до неона;
— 0,75 для элементов вплоть до аргона;
— 0,75 для элементов вплоть до криптона;
— 0,8 для элементов вплоть до ксенона[11]
Указанное соотношение между re и d определяет неравномерность распределения электрических зарядов в молекуле — в средней части молекулы сосредоточен отрицательный электрический заряд связывающей электронной пары, а на концах молекулы — положительные электрические заряды двух атомных остовов.
Неравномерность распределения электрических зарядов создаёт условия взаимодействия молекул за счёт ориентационных сил (силы Ван-дер-Ваальса). Молекулы щелочных металлов стремятся ориентироваться таким образом, чтобы по сосоедству оказывались разноимённые электрические заряды. В результате между молекулами действуют силы притяжения. Благодаря наличию последних, молекулы щелочных металлов сближаются и более менее прочно стягиваются между собой. Одновременно происходит некоторая деформация каждой из них под действием ближе расположенных полюсов соседних молекул (рис.12).
Фактически, связывающие электроны исходной двухатомной молекулы, попадая в электрическое поле четырёх положительно заряженных атомных остовов молекул щелочных металлов отрываются с орбитального радиуса атома и становятся свободными.
При этом связывающая электронная пара становится общей уже для системы с шестью катионами. Начинается построение кристаллической решётки металла на этапе кластера. В кристаллической решётке щелочных металлов чётко выражена структура связывающего звена, имеющего форму искажённого сплющенного октаэдра — квадратной бипирамиды, высота которой и рёбра базиса равны величина постоянной трансляционной решётки aw (рис.13).
Величина постоянной трансляционной решётки aw кристалла щелочного металла значительно превышает длину ковалентной связи молекулы щелочного металла, поэтому принято считать, что электроны в металле находятся в свободном состоянии:
| Щёлочный металл | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|
| Постоянная решётка aw,Å [12] | 3,5021 | 4,2820 | 5,247 | 5,69 | 6,084 |
| Длина ковалентной связи, Me2, Å [13] | 2,67 | 3,08 | 3,92 | 4,10 | 4,30 |
Математическое построение, связанное со свойствами свободных электронов в металле, обычно отождествляют с «поверхностью Ферми», которую следует рассматривать как геометрическое место, где пребывают электроны, обеспечивая основное свойство металла — проводить электрический ток.[14]
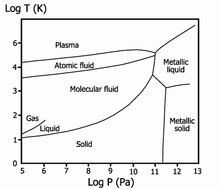
При сопоставлении процесса конденсации паров щелочных металлов с процессом конденсации газов, например, водорода, проявляется характерная особенность в свойствах металла. Так, если при конденсации водорода проявляются слабые межмолекулярные взаимодействия, то при конденсации паров металла протекают процессы, характерные для химических реакций. Сама конденсация паров металла идёт в несколько стадий и может быть описана следующей процессией: свободный атом → двухатомная молекула с ковалентной связью → металлический кластер → компактный металл с металлической связью.
Если рассматривать хронологию водородных технологий, то в 1935 году Юджин Вигнер и Хиллард Хантингтон предсказали возможность существования и металлического водорода. Действительно, ковалентная связь, свойственная молекулярному водороду, переходит в металлическую связь. Этот переход наблюдается для твёрдого водорода при высоком давлении (рис.14).
Механизм перехода ковалентной в ионную связь
Рис.15.Димеризация полярных молекулПереход ковалентной в ионную связь наблюдается для гетероядерных двухатомных молекул с полярной ковалентной связью, например, галогенидов щелочных металлов при переходе из газообразного в твёрдое состояние.
Атомы щелочных металлов при образовании соответствующего галогенида расходуют свой единственный внешний электрон и приобретают чётко выраженный положительный электрический заряд. Отрицательный электрический заряд фиксируется на атоме галогена. Молекулы галогенидов щелочных металлов фактически являются электрическими диполями.
Длина химической связи в молекулах галогенидов щелочных металлов (газовая фаза).[2]| ЭX | Длина химической связи, Å | |||
|---|---|---|---|---|
| ЭF | ЭCl | ЭBr | ЭI | |
| LiX | 1,56 | 2,02 | 2,17 | 2,39 |
| NaX | 1,93 | 2,36 | 2,50 | 2,71 |
| KX | 2,17 | 2,67 | 2,82 | 3,05 |
| Rbx | 2,27 | 2,79 | 2,95 | 3,18 |
| CsX | 2,35 | 2,91 | 3,07 | 3,32 |
Распределение силовых линий электрического диполя полярной ковалентной связи представлено на рис.4. При достаточно близких расстояниях силовые линии взаимно ориентируют полярные молекулы — одноимённо заряженные концы (полюса) их диполей взаимно отталкиваются, а разноимённо заряженные притягиваются. В результате между молекулами действуют силы притяжения, обусловленные взаимодействием их постоянных диполей и носящие название ориентационных сил.
Взаимодействие молекул галогенидов щелочных металлов сопровождается их димеризацией. Димерную молекулу можно рассматривать как электрический квадруполь (рис.15). В настоящее время известны основные характеристики димеров галогенидов щелочных металлов (длины химической связи и валентные углы между связями).[10]
Длина химической связи и валентные углы в димерах галогенидов щелочных металлов (Э2X2)(газовая фаза).[10]| Э2X2 | X=F | X=Cl | X=Br | X=I | ||||
|---|---|---|---|---|---|---|---|---|
| dЭF, Å | <F-Э-F,° | dЭCl, Å | <Cl-Э-Cl,° | dЭBr, Å | <Br-Э-Br, ° | dЭI, Å | <I-Э-I, ° | |
| Li2X2 | 1,75 | 105 | 2,23 | 108 | 2,35 | 110 | 2,54 | 116 |
| Na2X2 | 2,08 | 95 | 2,54 | 105 | 2,69 | 108 | 2,91 | 111 |
| K2X2 | 2,35 | 88 | 2,86 | 98 | 3,02 | 101 | 3,26 | 104 |
| Cs2X2 | 2,56 | 79 | 3,11 | 91 | 3,29 | 94 | 3,54 | 94 |
В процессе конденсации действие ориентационных сил усиливается, межмолекулярное взаимодействие сопровождается образованием кластеров, а затем и твёрдого вещества. Галогениды щелочных металлов образуют кристаллы с простой кубической и объёмно-центрированной кубической решёткой.
Тип кристаллической решётки и постоянная трансляционной решётки для галогенидов щелочных металлов.[12]
| Соединения и тип кристаллической решётки | Постоянная решётки, Å | ||||
|---|---|---|---|---|---|
| Li | Na | K | Rb | Cs | |
| фториды (куб) | 4,0279 | 4,628 | 5,344 | 5,64 | 6,020 |
| хлориды (куб) | 5,1399 | 5,639 | 6,21 | — | — |
| хлориды (ОЦК) | — | — | — | 3,749 | 4,10 |
| бромиды (куб) | 5,501 | 5,973 | 6,599 | 6,868 | 7,23 |
| бромиды (ОЦК) | — | — | — | — | 4,296 |
| иодиды (куб) | 6,012 | 6,475 | 7,066 | 7,340 | 7,66 |
| иодиды (ОЦК) | — | — | — | — | 4,567 |
В процессе кристаллизации происходит дальнейшее увеличение межатомного расстояния, приводящее к срыву электрона с орбитального радиуса атома щелочного металла и передаче электрона атому галогена с образованием соответствующих ионов. Силовые поля ионов равномерно распределяются во всех направлениях в пространстве. В связи с этим в кристаллах щелочных металлов силовое поле каждого иона координирует отнюдь не один ион с противоположным знаком, как принято качественно представлять ионную связь (Na+Cl—).
В кристаллах ионных соединений понятие простых двухионных молекул типа Na+Cl— и Cs+Cl— теряет смысл, поскольку ион щелочного металла связан с шестью ионами хлора (в кристалле хлористого натрия) и с восемью ионами хлора (в кристалле хлористого цезия. При этом все межионные расстояния в кристаллах равноудалены.
Примечания
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 124. — 320 с.
- ↑ 1 2 3 4 5 Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 132-136. — 320 с.
- ↑ Ганкин В.Ю., Ганкин Ю.В. Как образуется химическая связь и протекают химические реакции. — М.: издат.группа «Граница», 2007. — 320 с. — ISBN 978-5-94691296-9
- ↑ Некрасов Б. В. Курс общей химии. — М.: Госхимиздат, 1962. — С. 88. — 976 с.
- ↑ Паулинг Л. Природа химической связи / под редакцией Я.К.Сыркина. — пер. с англ. М.Е.Дяткиной. — М.-Л.: Госхимиздат, 1947. — 440 с.
- ↑ 1 2 Теоретическая органическая химия / под ред. Р.Х.Фрейдлиной. — пер. с англ. Ю.Г.Бунделя. — М.: Изд. иностранной литературы, 1963. — 365 с.
- ↑ 1 2 3 4 5 Леменовский Д.А., Левицкий М.М. Российский химический журнал (журнал Российского химического общества им. Д.И.Менделеева). — 2000. — Т. XLIV, вып.6. — С. 63-86.
- ↑ Химический энциклопедический словарь / гл. ред. И.Л.Кнунянц. — М.: Сов. энциклопедия, 1983. — С. 607. — 792 с.
- ↑ Некрасов Б. В. Курс общей химии. — М.: Госхимиздат, 1962. — С. 679. — 976 с.
- ↑ 1 2 3 Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 155-161. — 320 с.
- ↑ Гиллеспи Р. Геометрия молекул / пер. с англ. Е.З. Засорина и В.С. Мастрюкова, под ред. Ю.А Пентина. — М.: «Мир», 1975. — С. 49. — 278 с.
- ↑ 1 2 Справочник химика. — 2-е изд., перераб. и доп. — Л.-М.: ГНТИ Химической литературы, 1962. — Т. 1. — С. 402-513. — 1072 с.
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ.. — М.: «Химия», 1987. — С. 132-136. — 320 с.
- ↑ Зиман Дж. Электроны в металлах (введение в теорию поверхностей Ферми). Успехи физических наук.. — 1962. — Т. 78, вып.2. — 291 с.
См. также
Литература
- Маррел Дж., Кеттл С., Теддер Дж. Химическая связь. М.: Мир, 1980. 384 с.
- Пиментел Г., Спратли Р. Как квантовая механика объясняет химическую связь. Пер. с англ. М.: Мир, 1973. 332 с.
- Рюденберг К. Физическая природа химической связи. М.: Мир, 1964. 164 c.
- Бердетт Дж. Химическая связь. М.: Бином. Лаборатория знаний, 2008. 248 с. ISBN 978-5-94774-760-7, ISBN 978-5-03-003847-6, ISBN 0-471-97129-4
- Яцимирский К. Б., Яцимирский В. К. Химическая связь. Киев: Вища школа, 1975. 304 c.
- Краснов К. С. Молекулы и химическая связь. 2-ое изд. М: Высшая школа, 1984. 295 с.
- Татевский В. М. Строение молекул. М.: Химия, 1977. 512 с (Глава VIII. «Проблема химической связи в квантовой механике»)
- Татевский В. М. Квантовая механика и теория строения молекул. М.: Изд-во МГУ, 1965. 162 с. (§§ 30-31)
- Бейдер Р. Атомы в молекулах. Квантовая теория. М.: Мир, 2001. 532 c. ISBN 5-03-003363-7 Глава 7. Модели химической связи.
Ссылки
Химическая связь — это… Что такое Химическая связь?
 |
 |
Химическая связь — явление взаимодействия атомов, обусловленное перекрыванием электронных облаков связывающихся частиц, которое сопровождается уменьшением полной энергии системы.
При образовании ковалентной химической связи важную роль в уменьшении полной энергии играет обменное взаимодействие.
Теория химического строения Бутлерова
Термин «химическое строение» впервые ввёл А. М. Бутлеров в 1861 году. Также он заложил основы классической теории химического строения. Главные положения этой теории следующие:
- Атомы в молекулах соединены друг с другом в определённой последовательности. Изменение этой последовательности приводит к образованию нового вещества с новыми свойствами.
- Соединение атомов происходит в соответствии с их валентностью.
- Свойства веществ зависят не только от их состава, но и от «химического строения», то есть от порядка соединения атомов в молекулах и характера их взаимного влияния. Наиболее сильно влияют друг на друга атомы, непосредственно связанные между собой.
Типы связи
Простейшая одноэлектронная ковалентная химическая связь
Рис.1. Орбитальные радиусы элементов (ra) и длина одноэлектронной химической связи (d)Простейшая одноэлектронная химическая связь создаётся единственным валентным электроном. Оказывается, что один электрон способен удерживать в едином целом два положительно заряженных иона. В одноэлектронной связи кулоновские силы отталкивания положительно заряженных частиц компенсируются кулоновскими силами притяжения этих частиц к отрицательно заряженному электрону. Валентный электрон становится общим для двух ядер молекулы.
Примерами таких химических соединений являются молекулярные ионы: H2+, Li2+, Na2+, K2+, Rb2+, Cs2+[1]:
| Элемент | H | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|---|
| Электронная конфигурация | 1S1 | [He]2S1 | [Ne]3S1 | [Ar]4S1 | [Kr]5S1 | [Xe]6S1 |
| Межъядерное расстояние в молекулярном ионе xz+, Å | 1,06 | 3,14 | 3,43 | 4,18 | 4,44 | 4,70 |
| Орбитальный радиус атома, Å | 0,53 | 1,57 | 1,715 | 2,09 | 2,22 | 2,35 |
Существование молекулярных ионов водорода и щелочных металлов, в которых химическую связь создаёт единственный валентный электрон, расширяет и дополняет понятие химической связи. В перечисленных ионах ни о каком взаимодействии спинов электронов и перекрывания электронных облаков речи быть не может. Единственный связывающий электрон локализуется в пространстве между ядрами атомов и удерживает их в едином целом, образуя устойчивую химическую систему (рис.1).
Одинарная ковалентная связь
Рис.2.Неполярная ковалентная связь Рис.3.Полярная ковалентная связь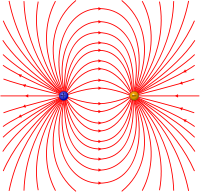 Рис.4.Силовые линии электрического диполя
Рис.4.Силовые линии электрического диполяОдинарная ковалентная химическая связь создаётся связывающей электронной парой. Во всех существующих теориях (теория валентных связей, теория молекулярных орбиталей, теория отталкивания валентных электронных пар, боровская модель химической связи) связывающая электронная пара располагается в пространстве между атомами молекулы. Различают полярную и неполярную ковалентную связи.
Неполярная ковалентная связь имеет место в гомоядерных двухатомных молекулах, в которых связывающая электронная пара равноудалена от обоих ядер молекулярной системы (рис.2). Расстояние d между атомными ядрами можно рассматривать как сумму ковалентных радиусов соответсвующих атомов.
Расстояние между атомными ядрами в одинарной двухэлектронной ковалентной связи короче аналогичного расстояния в простейшей одноэлектронной химической связи.
| Молекула | H2 | Li2 | Na2 | K2 | Rb2 | Cs2 |
|---|---|---|---|---|---|---|
| Межъядерное расстояние, Å [2] | 0,74 | 2,67 | 3,08 | 3,92 | 4,10 | 4,30 |
| Ковалентный радиус, Å | 0,37 | 1,335 | 1,54 | 1,96 | 2,05 | 2,15 |
| Орбитальный радиус, Å | 0,53 | 1,57 | 1,715 | 2,09 | 2,22 | 2,35 |
| Радиус связывающей электронной пары, Å | 0,379 | 0,826 | 0,755 | 0,726 | 0,852 | 0,949 |
| Энергия разрыва связи, кДж/моль [2] | 436 | 102 | 73 | 57 | 49 | 42 |
Разность между орбитальными и ковалентными радиусами характеризует степень перекрытия атомных орбиталей атомов, образующих химическую связь, и отражает деформацию электронной оболочки атомов.
Полярная ковалентная связь возникает в гетероядерных двухатомных молекулах (рис.3). Связывающая электронная пара в полярной химической связи приближена к атому с более высоким первым потенциалом ионизации.[3]
Характеризующее пространственную структуру полярных молекул расстояние d между атомными ядрами можно приближённо рассматривать как сумму ковалентных радиусов соответствующих атомов.[4]
Характеристика некоторых полярных веществ[2]| Молекула | LiH | NaH | KH | RbH | CsH |
|---|---|---|---|---|---|
| Межъядерное расстояние, Å | 1,60 | 1,89 | 2,24 | 2,37 | 2,49 |
| Энергия разрыва связи, кДж/моль | 236 | 200 | 182 | 165 | 176 |
Сдвиг связывающей электронной пары к одному из ядер полярной молекулы приводит к появлению электрического диполя (электродинамика) (рис.4).
Расстояние между центрами тяжести положительного и отрицательного зарядов называют длиной диполя. Полярность молекулы, как и полярность связи, оценивают величиной дипольного момента μ, представляющего собой произведение длины диполя l на величину электронного заряда:
μ = lq
Кратные ковалентные связи
Рис.5.sp2-гибридизация Рис.6.sp-гибридизацияКратные ковалентные связи представлены непредельными органическими соединениями, содержащими двойную и тройную химические связи. Для описания природы непредельных соединений Л.Полинг вводит понятия сигма- и π-связей, гибридизации атомных орбиталей.
Гибридизация Полинга для двух S- и двух p- электронов позволила объяснить направленность химических связей, в частности тетраэдрическую конфигурацию метана. Для объяснения структуры этилена из четырёх равноценных Sp3— электронов атома углерода приходится вычленять один p-электрон для образования дополнительной связи, получившей название π-связи. При этом три оставшиеся Sp2-гибридные орбитали располагаются в плоскости под углом 120° и образуют основные связи, например, плоскую молекулу этилена (рис.5).
В случае молекулы ацетилена в гибридизации принимают участие (по Полингу) всего лишь одна S- и одна p-орбитали, при этом образуются две Sp-орбитали, расположенные под углом в 180° и направленные в противоположные сороны. Две «чистые» p-орбитали атомов углерода попарно перекрываются во взаимоперпендикулярных плоскостях, образуя две π-связи линейной молекулы ацетилена (рис.6).
Взгляды Л.Полинга нашли отражение в его книге «Природа химической связи»[5], на долгие годы ставшей настольной книгой химика. В 1954 году Л.Полинг удостоен Нобелевской премии по химии с формулировкой «За исследование природы химической связи и его применение для опеделения структуры сложных соединений».
Однако физический смысл избирательной гибридизации атомных орбиталей оставался неясным, гибридизация представляла собой алгебраические преобразования, которым не могла быть приписана физическая реальность.
Лайнус Полинг предпринял попытку улучшения описания химической связи, исключив избритаельность гибридизации орбиталей в молекулах непредельных соединений и создав теорию изогнутой химической связи. В своём докладе на симпозиуме по теоретической органической химии, посвящённой памяти Кекуле (Лондон, сентябрь 1958 года), Л.Полинг предложил новый путь описания двойной связи как комбинации двух одинаковых изогнутых химических связей, а тройной связи — трёх изогнутых химических связей[6]. На этом симпозиуме Л.Полинг со всей категоричностью утверждал:
Могут найтись химики, полагающие что чрезвычайно важным новшеством… явилось описание σ,π- описания для двойной или тройной связи и сопряжённых систем вместо описания с помощью изогнутых связей. Я же утверждаю, что σ,π- описание менее удовлетворительно, чем описание с помощью изогнутых связей, что это нововведение является только переходящим и вскоре отомрёт.[6]
В новой теории Полинга все связывающие электроны становились равноценными и равноудалёнными от линии, соединяющей ядра молекулы. Теория изогнутой химической связи Полинга учитывала статистическую интерпретацию волновой функции М.Борна, кулоновскую электронную корреляцию электронов. Появился физический смысл — природа химической связи полностью определяется электрическим взаимодействием ядер и электронов. Чем больше связывающих электронов, тем меньше межъядерное расстояние и прочнее химическая связь между атомами углерода.
| Кратность связи | Структура связи | Межъядерное расстояние, Å | Энергия связи, кДж/моль |
|---|---|---|---|
| Одинарная (C-C) | Двухэлектронная двухцентровая | 1,54 | 348 |
| Двойная (C=C) | Четырёхэлектронная двухцентровая | 1,34 | 614 |
| Тройная (C=C) | Шестиэлектронная двухцентровая | 1,20 | 839 |
Трёхцентровая химическая связь
Дальнейшее развитие представлений о химической связи дал американской физикохимик У.Липскомб, разработавший теорию двухэлектронных трёхцентровых связей и топологическую теорию, позволяющую предсказывать строение ещё некоторых гидридов бора (бороводородов).
Электронная пара в трёхцентровой химической связи становится общей для трёх ядер атомов. В простейшем представителе трёхцентровой химической связи — молекулярном ионе водорода H3+ электронная пара удерживает в едином целом три протона (рис.6).
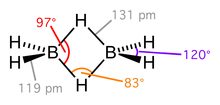 Рис.7.Диборан
Рис.7.ДиборанВ молекуле диборана функционируют четыре одинарные ковалентные связи B-H и две двухэлектронные трёхцентровые связи (рис.7). Межъядерное расстояние в одинарной ковалентной связи B-H составляет 1,19 Å, в то время как аналогичное расстояние в трёхцентровой связи B-H-B составляет 1,31 Å. Угол трёхцентровой связи B-H-B (φ) равен 830. Комбинация двух трёхцентровых связей в молекуле диборана позволяет удерживать ядра атомов бора на расстоянии dB-B = 2 · 1,31 · sin φ/2 = 1,736 Å. Ядра связывающих атомов водорода удалены от плоскости, в которой расположены четыре одинарные ковалентные связи B-H, на расстоянии h = 1,31 · cos φ/2 = 0,981 Å.
Трёхцентровые связи могут реализоваться не только в треугольнике из двух атомов бора и одного атома водорода, но и между тремя атомами бора, например в каркасных бороводородах (пентаборан — B5H9, декаборан — B10H4 и др.). В этих структурах есть обычные (концевые) и входящие в трёхцентровую связь (мостиковые) атома водорода и треугольники из атомов бора.[7]
Существование боранов с их двухэлектронными трёхцентровыми связями с «мостиковыми» атомами водорода нарушало каноническое учение о валентности. Атом водорода, считавшийся ранее стандартным одновалентным элементом, оказался связанным одинаковыми связями с двумя атомами бора и стал формально двухвалентным элементом. Работы У.Липскомба по расшифровке строения боранов расширяли представления о химической связи. Нобелевский комитет удостоил Уильяма Нанна Липскомба премии по химии за 1976 год с формулировкой «За исследования структуры боранов (боргидритов), проясняющие проблемы химических связей).
Многоцентровая химическая связь
Рис.8.Молекула ферроцена Рис.9.Дибензолхром Рис.10.УраноценВ 1951 году Т.Кили и П.Посон неожиданно при синтезе дициклопентадиенила получили совершенно новое железоорганическое соединение. Получение неизвестного ранее исключительно устойчивого жёлто-оранжевого кристаллического соединения железа сразу привлекло к себе внимание.
Э.Фишер и Д.Уилкинсон независимо друг от друга установили структуру нового соединения — два кольца циклопентадиенила расположены параллельно, слоями, или в виде «сэндвича» с атомом железа, расположенным между ними по центру (рис.8). Название «ферроцен» было предложено Р.Вудвордом (вернее, сотрудником его группы Д.Уайтингом). В нём отражено наличие в соединении атома железа и десяти углеродных атомов (zehn — десять).[7]
Все десять связей (C-Fe) в молекуле ферроцена равноценны, величина межъядерного расстояния Fe-c — 2,04 Å. Все атомы углерода в молекуле ферроцена структурно и химически эквивалентны, длина каждой связи C-C 1,40 — 1,41 Å (для сравнения, в бензоле длина связи C-C 1,39 Å). Вокруг атома железа возникает 36- электронная оболочка.[7]
В 1973 году Эрнст Отто Фишер и Джефри Уилкинсон были удостоены Нобелевской премии по химии с формулировкой «За новаторскую, проделанную независимо друг от друга работу, в области металлоорганических, так называемых сандвичевых соединений». Индвар Линдквист, член Шведской королевской академии наук, в своей речи при презентации лауреатов, заявил, что «открытие и доказательство новых принципов связей и структур, имеющихся в сандвичевых соединениях, являются значительным достижением, практическую значимость которых в настоящее время ещё невозможно предсказать».
В настоящее время получены дициклопентадиенильные производные многих металлов. Производные переходных металлов имеют ту же структуру и ту же природу связи, что и ферроцен. Лантаноиды образуют не сандвичеву структуру, а конструкцию, напоминающую трёхлучевую звезду[7]. Атомы La, Ce, Pr, Nd создают, следовательно, пятнадцати центровую химическую связь.
Вскоре вслед за ферроценом был получен дибензолхром (рис.9). По той же схеме получены дибензолмолибден и дибензолванадий[7]. Во всех соединениях этого класса атомы металла удерживают в едином целом два шестичленных кольца. Все 12 связей металл-углерод в этих соединениях идентичны.
Синтезирован также ураноцен [бис(циклооктатетраен)уран], в котором атом урана удерживает два восьмичленных кольца (рис.10). Все 16 связей уран-углерод в ураноцене идентичны. Ураноцен получают взаимодействием UCl4 со смесью циклооктатетраена и калия в тетрагидрофуране при минус 300 C.[8]
Динамика химической связи
Химическая связь достаточно динамична. Так, металлическая связь трансформируется в ковалентную в процессе фазового перехода при испарении металла. Переход металла из твёрдого в парообразное состояние требует затраты больших количеств энергии.[9]
| Металл | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|
| Теплота возгонки (ккал/г-атом) | 36 | 26 | 22 | 21 | 19 |
В парах указанные металлы состоят практически из гомоядерных двухатомных молекул и свободных атомов. При конденсации паров металла ковалентная связь превращается в металлическую.
Испарение солей с типичной ионной связью, например фторидов щелочных металлов, приводит к разрушению ионной связи и образованию гетероядерных двухатомных молекул с полярной ковалентной связью. При этом имеет место образование димерных молекул с мостиковыми связями.
Характеристика химической связи в молекулах фторидов щелочных металлов и их димерах.[2][10]
| ЭF | dЭF, Å | μ, D | Э2F2 | dЭF, Å | <F-Э-F |
|---|---|---|---|---|---|
| LiF | 1,56 | 6,60 | Li2F2 | 1,75 | 105° |
| NaF | 1,93 | — | Na2F2 | 2,08 | 95° |
| KF | 2,17 | 7,37 | K2F2 | 2,35 | 88° |
| RbF | 2,27 | — | Rb2F2 | 2,45 | 84° |
| CsF | 2,35 | 7,88 | Cs2F2 | 2,56 | 79° |
При конденсации паров фторидов щелочных металлов полярная ковалентная связь трансформируется в ионную с образованием соответствующей кристаллической решётки соли.
Механизм перехода ковалентной в металлическую связь
Рис.11. Соотношение между радиусом орбитали электронной пары re и длиной ковалентной химической связи d Рис.12.Ориентация диполей двухатомных молекул и образование искажённого октаэдрического фрагмента кластера при конденсации паров щелочных металлов Рис.13.Объёмноцентрированное кубическое расположение ядер в кристаллах щелочных металлов и связывающего звенаДисперсное притяжение (силы Лондона) обуславливает межатомное взаимодействие и образование гомоядерных двухатомных молекул из атомов щелочных металлов.
Образование ковалентной связи металл-металл сопряжено с деформацией электронных оболочек взаимодействующих атомов — валентные электроны создают связывающую электронную пару, электронная плотность которой концентрируется в пространстве между атомными ядрами возникшей молекулы. Характерной особенностью гомоядерных двухатомных молекул щелочных металлов является большая длина ковалентной связи (в 3,6-5,8 раза больше длины связи в молекуле водорода) и низкая энергия её разрыва.
В теории отталкивания электронных пар считается важным соотношение между радиусом орбитали электронной пары re и длиной ковалентной химической связи d (рис.11). Для элементов каждого периода таблицы Д. И. Менделеева существует некоторый радиус электронной пары (Å):
— 0,6 для элементов вплоть до неона;
— 0,75 для элементов вплоть до аргона;
— 0,75 для элементов вплоть до криптона;
— 0,8 для элементов вплоть до ксенона[11]
Указанное соотношение между re и d определяет неравномерность распределения электрических зарядов в молекуле — в средней части молекулы сосредоточен отрицательный электрический заряд связывающей электронной пары, а на концах молекулы — положительные электрические заряды двух атомных остовов.
Неравномерность распределения электрических зарядов создаёт условия взаимодействия молекул за счёт ориентационных сил (силы Ван-дер-Ваальса). Молекулы щелочных металлов стремятся ориентироваться таким образом, чтобы по сосоедству оказывались разноимённые электрические заряды. В результате между молекулами действуют силы притяжения. Благодаря наличию последних, молекулы щелочных металлов сближаются и более менее прочно стягиваются между собой. Одновременно происходит некоторая деформация каждой из них под действием ближе расположенных полюсов соседних молекул (рис.12).
Фактически, связывающие электроны исходной двухатомной молекулы, попадая в электрическое поле четырёх положительно заряженных атомных остовов молекул щелочных металлов отрываются с орбитального радиуса атома и становятся свободными.
При этом связывающая электронная пара становится общей уже для системы с шестью катионами. Начинается построение кристаллической решётки металла на этапе кластера. В кристаллической решётке щелочных металлов чётко выражена структура связывающего звена, имеющего форму искажённого сплющенного октаэдра — квадратной бипирамиды, высота которой и рёбра базиса равны величина постоянной трансляционной решётки aw (рис.13).
Величина постоянной трансляционной решётки aw кристалла щелочного металла значительно превышает длину ковалентной связи молекулы щелочного металла, поэтому принято считать, что электроны в металле находятся в свободном состоянии:
| Щёлочный металл | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|
| Постоянная решётка aw,Å [12] | 3,5021 | 4,2820 | 5,247 | 5,69 | 6,084 |
| Длина ковалентной связи, Me2, Å [13] | 2,67 | 3,08 | 3,92 | 4,10 | 4,30 |
Математическое построение, связанное со свойствами свободных электронов в металле, обычно отождествляют с «поверхностью Ферми», которую следует рассматривать как геометрическое место, где пребывают электроны, обеспечивая основное свойство металла — проводить электрический ток.[14]
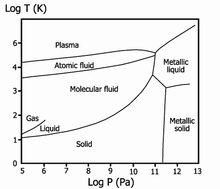
При сопоставлении процесса конденсации паров щелочных металлов с процессом конденсации газов, например, водорода, проявляется характерная особенность в свойствах металла. Так, если при конденсации водорода проявляются слабые межмолекулярные взаимодействия, то при конденсации паров металла протекают процессы, характерные для химических реакций. Сама конденсация паров металла идёт в несколько стадий и может быть описана следующей процессией: свободный атом → двухатомная молекула с ковалентной связью → металлический кластер → компактный металл с металлической связью.
Если рассматривать хронологию водородных технологий, то в 1935 году Юджин Вигнер и Хиллард Хантингтон предсказали возможность существования и металлического водорода. Действительно, ковалентная связь, свойственная молекулярному водороду, переходит в металлическую связь. Этот переход наблюдается для твёрдого водорода при высоком давлении (рис.14).
Механизм перехода ковалентной в ионную связь
Рис.15.Димеризация полярных молекулПереход ковалентной в ионную связь наблюдается для гетероядерных двухатомных молекул с полярной ковалентной связью, например, галогенидов щелочных металлов при переходе из газообразного в твёрдое состояние.
Атомы щелочных металлов при образовании соответствующего галогенида расходуют свой единственный внешний электрон и приобретают чётко выраженный положительный электрический заряд. Отрицательный электрический заряд фиксируется на атоме галогена. Молекулы галогенидов щелочных металлов фактически являются электрическими диполями.
Длина химической связи в молекулах галогенидов щелочных металлов (газовая фаза).[2]| ЭX | Длина химической связи, Å | |||
|---|---|---|---|---|
| ЭF | ЭCl | ЭBr | ЭI | |
| LiX | 1,56 | 2,02 | 2,17 | 2,39 |
| NaX | 1,93 | 2,36 | 2,50 | 2,71 |
| KX | 2,17 | 2,67 | 2,82 | 3,05 |
| Rbx | 2,27 | 2,79 | 2,95 | 3,18 |
| CsX | 2,35 | 2,91 | 3,07 | 3,32 |
Распределение силовых линий электрического диполя полярной ковалентной связи представлено на рис.4. При достаточно близких расстояниях силовые линии взаимно ориентируют полярные молекулы — одноимённо заряженные концы (полюса) их диполей взаимно отталкиваются, а разноимённо заряженные притягиваются. В результате между молекулами действуют силы притяжения, обусловленные взаимодействием их постоянных диполей и носящие название ориентационных сил.
Взаимодействие молекул галогенидов щелочных металлов сопровождается их димеризацией. Димерную молекулу можно рассматривать как электрический квадруполь (рис.15). В настоящее время известны основные характеристики димеров галогенидов щелочных металлов (длины химической связи и валентные углы между связями).[10]
Длина химической связи и валентные углы в димерах галогенидов щелочных металлов (Э2X2)(газовая фаза).[10]| Э2X2 | X=F | X=Cl | X=Br | X=I | ||||
|---|---|---|---|---|---|---|---|---|
| dЭF, Å | <F-Э-F,° | dЭCl, Å | <Cl-Э-Cl,° | dЭBr, Å | <Br-Э-Br, ° | dЭI, Å | <I-Э-I, ° | |
| Li2X2 | 1,75 | 105 | 2,23 | 108 | 2,35 | 110 | 2,54 | 116 |
| Na2X2 | 2,08 | 95 | 2,54 | 105 | 2,69 | 108 | 2,91 | 111 |
| K2X2 | 2,35 | 88 | 2,86 | 98 | 3,02 | 101 | 3,26 | 104 |
| Cs2X2 | 2,56 | 79 | 3,11 | 91 | 3,29 | 94 | 3,54 | 94 |
В процессе конденсации действие ориентационных сил усиливается, межмолекулярное взаимодействие сопровождается образованием кластеров, а затем и твёрдого вещества. Галогениды щелочных металлов образуют кристаллы с простой кубической и объёмно-центрированной кубической решёткой.
Тип кристаллической решётки и постоянная трансляционной решётки для галогенидов щелочных металлов.[12]
| Соединения и тип кристаллической решётки | Постоянная решётки, Å | ||||
|---|---|---|---|---|---|
| Li | Na | K | Rb | Cs | |
| фториды (куб) | 4,0279 | 4,628 | 5,344 | 5,64 | 6,020 |
| хлориды (куб) | 5,1399 | 5,639 | 6,21 | — | — |
| хлориды (ОЦК) | — | — | — | 3,749 | 4,10 |
| бромиды (куб) | 5,501 | 5,973 | 6,599 | 6,868 | 7,23 |
| бромиды (ОЦК) | — | — | — | — | 4,296 |
| иодиды (куб) | 6,012 | 6,475 | 7,066 | 7,340 | 7,66 |
| иодиды (ОЦК) | — | — | — | — | 4,567 |
В процессе кристаллизации происходит дальнейшее увеличение межатомного расстояния, приводящее к срыву электрона с орбитального радиуса атома щелочного металла и передаче электрона атому галогена с образованием соответствующих ионов. Силовые поля ионов равномерно распределяются во всех направлениях в пространстве. В связи с этим в кристаллах щелочных металлов силовое поле каждого иона координирует отнюдь не один ион с противоположным знаком, как принято качественно представлять ионную связь (Na+Cl—).
В кристаллах ионных соединений понятие простых двухионных молекул типа Na+Cl— и Cs+Cl— теряет смысл, поскольку ион щелочного металла связан с шестью ионами хлора (в кристалле хлористого натрия) и с восемью ионами хлора (в кристалле хлористого цезия. При этом все межионные расстояния в кристаллах равноудалены.
Примечания
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 124. — 320 с.
- ↑ 1 2 3 4 5 Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 132-136. — 320 с.
- ↑ Ганкин В.Ю., Ганкин Ю.В. Как образуется химическая связь и протекают химические реакции. — М.: издат.группа «Граница», 2007. — 320 с. — ISBN 978-5-94691296-9
- ↑ Некрасов Б. В. Курс общей химии. — М.: Госхимиздат, 1962. — С. 88. — 976 с.
- ↑ Паулинг Л. Природа химической связи / под редакцией Я.К.Сыркина. — пер. с англ. М.Е.Дяткиной. — М.-Л.: Госхимиздат, 1947. — 440 с.
- ↑ 1 2 Теоретическая органическая химия / под ред. Р.Х.Фрейдлиной. — пер. с англ. Ю.Г.Бунделя. — М.: Изд. иностранной литературы, 1963. — 365 с.
- ↑ 1 2 3 4 5 Леменовский Д.А., Левицкий М.М. Российский химический журнал (журнал Российского химического общества им. Д.И.Менделеева). — 2000. — Т. XLIV, вып.6. — С. 63-86.
- ↑ Химический энциклопедический словарь / гл. ред. И.Л.Кнунянц. — М.: Сов. энциклопедия, 1983. — С. 607. — 792 с.
- ↑ Некрасов Б. В. Курс общей химии. — М.: Госхимиздат, 1962. — С. 679. — 976 с.
- ↑ 1 2 3 Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. — М.: «Химия», 1987. — С. 155-161. — 320 с.
- ↑ Гиллеспи Р. Геометрия молекул / пер. с англ. Е.З. Засорина и В.С. Мастрюкова, под ред. Ю.А Пентина. — М.: «Мир», 1975. — С. 49. — 278 с.
- ↑ 1 2 Справочник химика. — 2-е изд., перераб. и доп. — Л.-М.: ГНТИ Химической литературы, 1962. — Т. 1. — С. 402-513. — 1072 с.
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ.. — М.: «Химия», 1987. — С. 132-136. — 320 с.
- ↑ Зиман Дж. Электроны в металлах (введение в теорию поверхностей Ферми). Успехи физических наук.. — 1962. — Т. 78, вып.2. — 291 с.
См. также
Литература
- Маррел Дж., Кеттл С., Теддер Дж. Химическая связь. М.: Мир, 1980. 384 с.
- Пиментел Г., Спратли Р. Как квантовая механика объясняет химическую связь. Пер. с англ. М.: Мир, 1973. 332 с.
- Рюденберг К. Физическая природа химической связи. М.: Мир, 1964. 164 c.
- Бердетт Дж. Химическая связь. М.: Бином. Лаборатория знаний, 2008. 248 с. ISBN 978-5-94774-760-7, ISBN 978-5-03-003847-6, ISBN 0-471-97129-4
- Яцимирский К. Б., Яцимирский В. К. Химическая связь. Киев: Вища школа, 1975. 304 c.
- Краснов К. С. Молекулы и химическая связь. 2-ое изд. М: Высшая школа, 1984. 295 с.
- Татевский В. М. Строение молекул. М.: Химия, 1977. 512 с (Глава VIII. «Проблема химической связи в квантовой механике»)
- Татевский В. М. Квантовая механика и теория строения молекул. М.: Изд-во МГУ, 1965. 162 с. (§§ 30-31)
- Бейдер Р. Атомы в молекулах. Квантовая теория. М.: Мир, 2001. 532 c. ISBN 5-03-003363-7 Глава 7. Модели химической связи.