Простые вещества — урок. Химия, 8–9 класс.
Все химические вещества делятся на простые и сложные.
Простыми называют вещества, образованные атомами одного химического элемента.
Некоторые простые вещества состоят из молекул.
Одноатомные молекулы образуют инертные газы гелий He, неон Ne, аргон Ar и другие.
Из двухатомных молекул состоят водород h3, кислород O2, азот N2, галогены F2, Cl2, Br2, I2.
Три атома — в молекулах озона O3, четыре — в молекулах белого фосфора P4, восемь — в молекулах серы S8.
Модели молекул водорода и азота
Модель молекулы белого фосфора
Другая группа простых веществ имеет немолекулярное строение. К таким веществам относятся все металлы, а также фосфор красный, алмаз, графит, кремний и другие.
Их химические формулы записывают химическим символом элемента без индекса: Fe, P, C, Si и т. д.
Модель кристалла железа
Химических элементов известно \(118\), а простых веществ — более \(400\). Один химический элемент может образовать несколько простых веществ.
Один химический элемент может образовать несколько простых веществ.
Явление существования нескольких простых веществ, образованных атомами одного химического элемента, называется аллотропией.
Простые вещества, состоящие из атомов одного химического элемента — аллотропные модификации (аллотропные видоизменения).
Пример:
химический элемент кислород образует простые вещества, отличающиеся составом молекул: кислород O2 и озон O3. Кислород — газ без запаха, необходим живым организмам для дыхания. Озон имеет запах, ядовит.
Химический элемент фосфор образует молекулярное вещество фосфор белый P4 и немолекулярное — фосфор красный P. Эти вещества отличаются не только строением, но и свойствами. Белый фосфор имеет запах, самовоспламеняется на воздухе. Красный фосфор без запаха, горит только при нагревании.
Химический элемент углерод образует немолекулярные вещества алмаз и графит. Они обозначаются одинаковой формулой — C, но имеют разное строение и отличаются свойствами. Алмаз представляет собой прозрачное, бесцветное, очень твёрдое вещество. Графит — непрозрачный, тёмно-серый, мягкий.
Алмаз представляет собой прозрачное, бесцветное, очень твёрдое вещество. Графит — непрозрачный, тёмно-серый, мягкий.
Алмаз и графит
Химический элемент и простое вещество
Названия химического элемента и простого вещества в большинстве случаев совпадают, поэтому следует различать эти два понятия.
Химический элемент — это определённый вид атомов. Атомы химического элемента могут входить в состав простых и сложных веществ. Можно охарактеризовать распространённость и формы нахождения химического элемента в природе, а также свойства его атомов (массу, размеры, строение).
Простое вещество образовано атомами одного химического элемента. Это одна из форм существования химического элемента в природе. Простое вещество характеризуется определённым составом, строением, физическими и химическими свойствами. Его применяют для получения других веществ.
Пример:
Химический элемент | Простое вещество |
| Относительная атомная масса кислорода равна \(16\) | Кислород плохо растворяется в воде |
| Азот входит в состав белков | Азот используют для получения аммиака |
| Атомы водорода входят в состав молекул воды | Водород легче воздуха |
Простые вещества определение — Справочник химика 21
V Стандартная энергия Гиббса образования. Под стандартной энергией Гиббса образования А0° понимают изменение энергии Гиббса при реакции образования 1 моля пещества, находящегося в стандартном состоянии, из простых веществ, каждое из которых также находится в стандартном состоянии. Это определение подразумевает, что стандартная энергия Гиббса образования простого вещества, устойчивого в стандартных условиях, равна нулю. [c.175]
Под стандартной энергией Гиббса образования А0° понимают изменение энергии Гиббса при реакции образования 1 моля пещества, находящегося в стандартном состоянии, из простых веществ, каждое из которых также находится в стандартном состоянии. Это определение подразумевает, что стандартная энергия Гиббса образования простого вещества, устойчивого в стандартных условиях, равна нулю. [c.175]ЭМПИРИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ СТАНДАРТНЫХ ТЕПЛОТ СГОРАНИЯ И ОБРАЗОВАНИЯ ИЗ ПРОСТЫХ ВЕЩЕСТВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ [c.23]
В органической химии определение теплот сгорания (ДЯс) и в настоящее время является важнейшей экспериментальной основой получения данных о теплотах образования из простых веществ (AЯf) и других параметров реакций образования и
Далее Блэк показал, что если оксид кальция оставить на воздухе, то он медленно превращается в карбонат кальция. Исходя из этого, Блэк заключил (правильно ), что в атмосфере присутствует небольшое количество углекислого газа. Это было первое четкое указание на то, что воздух не простое вещество и, следовательно, вопреки представлениям древних греков он не является элементом в определении Бойля, а представляет собой смесь по крайней мере двух различных веществ обычного воздуха и углекислого газа. Изучая влияние нагревания на примере карбоната кальция, Блэк установил, как меняется вес вещества при нагревании. Он также определил, какое количество карбоната кальция нейтрализует заданное количество кислоты. Таким образом, Блэк изучал химические реакции, используя метод количественного измерения. Этот метод был развит и усовершенствован Лавуазье.
Это было первое четкое указание на то, что воздух не простое вещество и, следовательно, вопреки представлениям древних греков он не является элементом в определении Бойля, а представляет собой смесь по крайней мере двух различных веществ обычного воздуха и углекислого газа. Изучая влияние нагревания на примере карбоната кальция, Блэк установил, как меняется вес вещества при нагревании. Он также определил, какое количество карбоната кальция нейтрализует заданное количество кислоты. Таким образом, Блэк изучал химические реакции, используя метод количественного измерения. Этот метод был развит и усовершенствован Лавуазье.
Для определения удельной поверхности з обычно применяются изотермы адсорбции паров простых веществ (N2, Аг, Кг) при низких температурах (большие значения величины С). При этом за стандарт принята величина для азота, адсорбированного при —195 °С (78 °К) на графитированной саже, равная 16,2 А . Определив с помощью низкотемпературной адсорбции стандартного пара удельную поверхность адсорбента з, легко далее решить и обратную задачу—найти величину (и для какого-либо другого адсорбата, определив на опыте изотерму адсорбции его пара и найдя величину емкости монослоя а из графика, аналогичного показанному на рис. XVI, 9. [c.454]
XVI, 9. [c.454]
НОВЫХ теориях и используя разработанную им номенклатуру, систематизировал накопленные к тому времени знания в области химии. Это был первый учебник по химии в современном понимании. В нем содержался, в частности, перечень всех известных в то время элементов или, вернее, всех веществ, которые Лавуазье, руководствуясь определением Бойля, считал элементами, т. е. веществами, которые нельзя разделить на более простые вещества (рис. 8). Лавуазье привел 33 элемента и, к его чести, только в двух случаях допустил несомненные ошибки. Это касалось света и теплорода (тепла), которые, как стало очевидно спустя несколько десятилетий, представляют собой вовсе не материальные субстанции, а формы энергии.
На этом этапе, наконец, стало возможным заменить определение элемента, данное Бойлем. Согласно Бойлю, элемент — это вещество, которое нельзя разложить на более простые вещества, новое определение элемента звучит так элемент — это совокупность атомов с одинаковым зарядом ядра.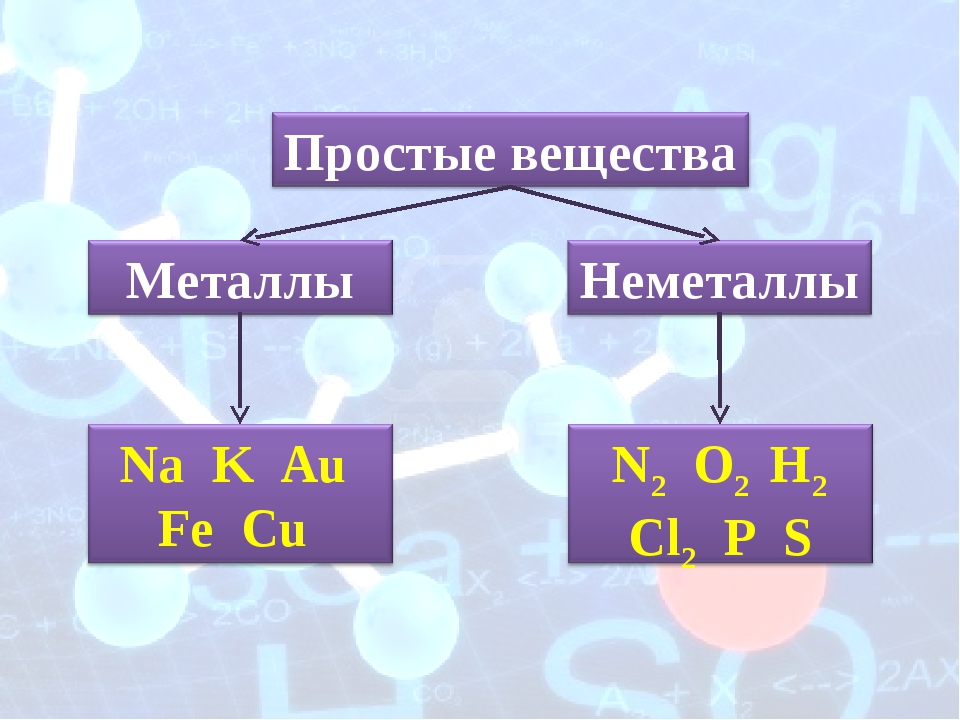 [c.156]
[c.156]
Как расчет термодинамических величин, отнесенных к молю раствора или компонента, так и развитие статистической теории требуют знания состава раствора, выраженного через мольные (л ,) или мольно-объемные (ср,) доли компонентов. Для расчета этих величин необходимо знать молекулярные веса компонентов, особенно полимера. Эта задача не проста. Для определения молекулярного веса Ма необходимо, как мы знаем, измерить кол-лигативное свойство предельно разбавленного раствора. Вследствие того что в растворах высокомолекулярных веществ имеют место большие отрицательные отклонения от закона Рауля, свойства предельно разбавленных растворов проявляются лишь при малых концентрациях растворенного вещества. Прн этих условиях такие коллигативные свойства, как понижение давления пара или понижение точки затвердевания, используемые для определения молекулярного веса, становятся настолько малыми, что их крайне трудно измерить. Только осмотическое давление таких растворов имеет достаточно точно измеримую величину (например, осмотическое давление 5%-ного раствора каучука в бензоле ( 2=4-19 ) равно 10 мм рт.
Для определения постоянных А и В уравнения (33) нужно АОт и АНт для данной группы соединений отнести к одному и тому же количеству простого вещества, общего для всех соединений, и построить график АО = / (АНт) [c.25]
Всякое изложение какого-либо материала строится на последовательности определений. Сначала формулируются определения наиболее общих понятий, затем с их помощью определяются менее общие понятия, далее — более частные и т. п. Таким способом строится иерархия (подчиненность) определений в изложении. Распределите нижеперечисленные термины в иерархическом порядке кислотный оксид, смесь, простое вещество, оксид, сложное вещество, основной оксид, элемент, молекула, атом, материя, вещество.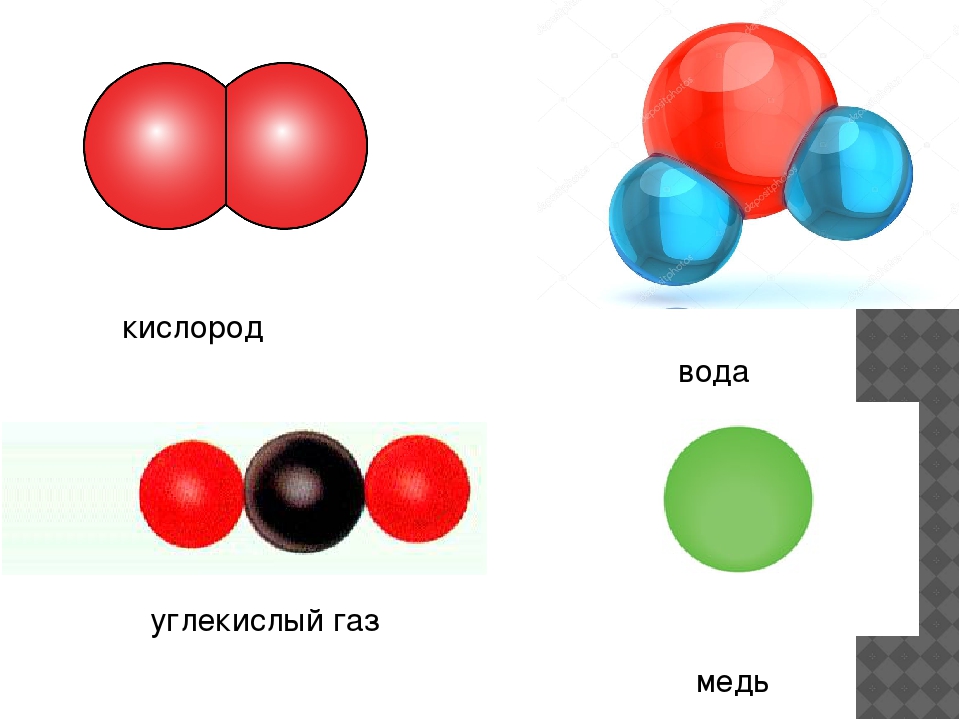
Рассмотрим задачу обработки экспериментальных данных при разработке математических моделей реакций, описываемых простейшими кинетическими схемами- Фактически под этим понимаются достаточно простые методы определения порядков единичной реакции и констант ее скорости, не требующие применения вычислительной техники. Такие методы могут оказаться полезными не только для простых, но и для сложных реакций, когда исследуется брутто-реакция превращения исходного вещества или интересным является формальная кинетика образования целевого продукта. Поэтому для целостности изложения напомним эти методы, хотя некоторые из них достаточно подробно описаны в ряде монографий, например 151. [c.424]
Определение параметров различных реакций. Кроме реакций образования компонентов из простых веществ для расчета параметров тех или других процессов могут быть использованы и параметры реакций некоторых других видов. [c.56]
К сожалению, для очень важной категории реакций — реакций образования из элементов (из простых веществ или свободных атомов) — применение описанных закономерностей при высоких температурах часто бывает существенно ограниченно. Расчет параметров реакций образования из простых веществ и определение их температурных зависимостей в широкой области температур большей частью сильно осложняются вследствие фазовых переходов, которые претерпевают простые вещества (полиморфные превращения, плавление, испарение), и частичной диссоциации их на атомы при высоких температурах. Поэтому целесообразнее рассматривать атомарные теплоты образования (или теплоты атомизации), атомарные энтропии образования (или энтропии атомизации) и другие параметры реакций образования вещества из свободных атомов. В настоящее время расчет этих величин не представляет затруднений, так как почти для всех элементов имеются дан-ные о значениях термодинамических функций их в состоянии одноатомного газа при разных температурах до 3000 К, и для некоторых элементов до 6000, 8000 и 20 ООО К-
Расчет параметров реакций образования из простых веществ и определение их температурных зависимостей в широкой области температур большей частью сильно осложняются вследствие фазовых переходов, которые претерпевают простые вещества (полиморфные превращения, плавление, испарение), и частичной диссоциации их на атомы при высоких температурах. Поэтому целесообразнее рассматривать атомарные теплоты образования (или теплоты атомизации), атомарные энтропии образования (или энтропии атомизации) и другие параметры реакций образования вещества из свободных атомов. В настоящее время расчет этих величин не представляет затруднений, так как почти для всех элементов имеются дан-ные о значениях термодинамических функций их в состоянии одноатомного газа при разных температурах до 3000 К, и для некоторых элементов до 6000, 8000 и 20 ООО К-
Соотношения (И, 8) служат также для определения атомарных теплот образования и атомарных энтропий образования по соответствующим обычным параметрам реакций образования из простых веществ. Раньше подобные определения были затруднены отсутствием необходимых данных о термодинамических параметрах процессов атомизации простых веществ. В настоящее же время такие данные имеются почти для всех элементов (как для 298,15 К, так и для более высоких температур). [c.57]
Раньше подобные определения были затруднены отсутствием необходимых данных о термодинамических параметрах процессов атомизации простых веществ. В настоящее же время такие данные имеются почти для всех элементов (как для 298,15 К, так и для более высоких температур). [c.57]
При определении изменения параметров реакции с изменением температуры достаточно знать изменения этих параметров для компонентов реакции, что и избавляет от усложнений, связанных с фазовыми переходами простых веществ. [c.64]
Расчет Кт по значениям К/, г компонентов реакции. Для определения 1 /С по значениям gKf,i проще всего использовать соотношение (11,3). В настоящее время при разных температурах определены для большого числа органических соединений (углеводородов, кислород- или серусодержащих соединений и других) и для некоторых неорганических соединений, главным образом простейших. Большей частью gKf определены для соединений, образующихся из простых веществ, не изменяющих своего агрегатного состояния и не имеющих полиморфных превращений в рассматриваемом интервале температур (например, из графита, Нг, О2, N2, СЬ, р2 или из веществ, которые могут быть приняты находящимися в таком состоянии [например, из 82 (г), Вгз (г) и др.
Определенные для веществ в стандартном состоянии стандартные энтальпии и другие стандартные термодинамические величины. обозначают верхним индексом (°), нижним индексом указывают температуру, при которой они определены например АЯ298 (определена при 298,15 К знаки, стоящие после запятой в индексе, обычно не указывают) или АЯюоо (определена при 1000 К). Такое единообразие делает расчеты строгими. Стандартная энтальпия образования вещества АЯ/ — это изменение энтальпии в процессе образования данного вещества в стандартном состоянии из термодинамически устойчивых фюрм простых веществ, также находящихся в стандартных состояниях. [c.166]
А5ь г-Последнее по существу не является необходимым для определения 1 /(т реакции, так как при расчете gK.T все величины, относящиеся к простым веществам, взаимно сокращаются, кроме
 68]
68]В Приложениях I—П1 приведены в табличной форме термодинамические свойства частиц, простых веществ и некоторых химических соединений при 298,15 К и при высоких температурах. Эти таблицы дают возможность самостоятельно проверить применение описанных соотношений и проследить закономерности, кроме того, они предоставляют основные данные для практических расчетов и для приближенного определения величин на основе методов сравнительного расчета. Таблицы дают, в частности, возможность, располагая данными о свойствах интересующего вещества при [c.312]
Второе следствие. Тепловой эффект реакции равен разности между суммой теплот образования продуктов реакции и суммой теплот образования исходных веществ. Под теплотой образования понимают то количество теплоты, которое выделяется или поглощается при образовании одного моля -го вещества из простых веществ, взятых в устойчивом состоянии при рассматриваемых условиях (Р, Т). Теплоту образования (энтальпию образования), так же как и теплоту сгорания, относят к строго определенному количеству вещества (моль, кг), указывая его агрегатное состояние. Только при этих условиях можно вычислять тепловые эффекты реакций на основании данного следствия, а также сравнивать тепловые эффекты различных реакций между собой. [c.211]
Только при этих условиях можно вычислять тепловые эффекты реакций на основании данного следствия, а также сравнивать тепловые эффекты различных реакций между собой. [c.211]
В справочнике [34] дана критическая оценка многих экспериментальных данных и приведены погрешности определения термодинамических величин для различных простых веществ и соединений. Выборочные данные о погрешностях для веществ, рассматриваемых в данной книге, приведены в табл. 3. [c.146]
Первый закон термохимии может быть использован для определения теплот образования соединений, полученных косвенным путем. Например, оксиды хлора СЬО, СЮа, СЬО не могут быть получены непосредственным взаимодействием хлора с кислородом, но они легко разлагаются на простые вещества, позволяя измерить тепловой эффект реакции разложения. Очевидно, что теплота образования этих оксидов равна тепловому эффекту реакций разложения, взятому с обратным знаком. [c.48]
Традиционное деление элементов на металлы и неметаллы исторически возникло из-за того, что простые вещества, образованные атомами элементов-металлов, как правило, находятся в металлическом состоянии и проявляют металлические свойства (высокую электро-и теплопроводность, блеск и т. д.), а простые вещества, образованные атомами элементов-неметаллов, при нормальных условиях этими свойствами не обладают. Однако в других условиях свойства простых веществ могут быть совершенно иными. Например, типичный металл натрий в газообразном состоянии образует молекулы Na2 с ковалентной связью, подобно Н2, а пары натрия не реагируют с парами воды. Почти так же любое вещество при определенном давлении может быть переведено в металлическое состояние, в том числе простые вещества, образованные атомами элементов-неметаллов. [c.95]
д.), а простые вещества, образованные атомами элементов-неметаллов, при нормальных условиях этими свойствами не обладают. Однако в других условиях свойства простых веществ могут быть совершенно иными. Например, типичный металл натрий в газообразном состоянии образует молекулы Na2 с ковалентной связью, подобно Н2, а пары натрия не реагируют с парами воды. Почти так же любое вещество при определенном давлении может быть переведено в металлическое состояние, в том числе простые вещества, образованные атомами элементов-неметаллов. [c.95]
Моделирование на АВМ более сложных схем по затратам времени мало отличается от моделирования простых схем, тогда как расчетные трудности возрастают с усложнением реакции исключительно быстро. Аналогично решаются задачи определения максимальной конверсии в проточном реакторе в зависимости от скорости подачи исходного вещества, определения оптимального соотношения исходных веществ для получения максимального выхода целевого вещества и т. п. Если в качестве независимой переменной подавать на горизонтальную развертку индикатора не время, [c.346]
п. Если в качестве независимой переменной подавать на горизонтальную развертку индикатора не время, [c.346]
Для органических соединений имеется возможность непосредственного определения теплоты сгорания. Любой углеводород, спирт, эфир и другие индивидуальные вещества легко сжечь до СО2 и жидкой Н2О. Получить же заданное индивидуальное соединение из простых веществ при прямом их взаимодействии в большинстве случаев нельзя, не говоря уже о трудностях измерения теплоты такого процесса. В связи с этим для органических реакций расчет теплот реакций по теплотам сгорания участвующих в реакции веществ получил широкое распространение. [c.15]
В ряде случаев представляет интерес определение теплоты образования химических соединений не из простых веществ, а из атомов, т. е. из гипотетических одноатомных газов (атомная теплота образования). Выделившееся при этом (мысленном) процессе теплота является мерой энергии всех связей и взаимодействия между атомами в молекуле и имеет большое значение для установления энергии каждой химической связи.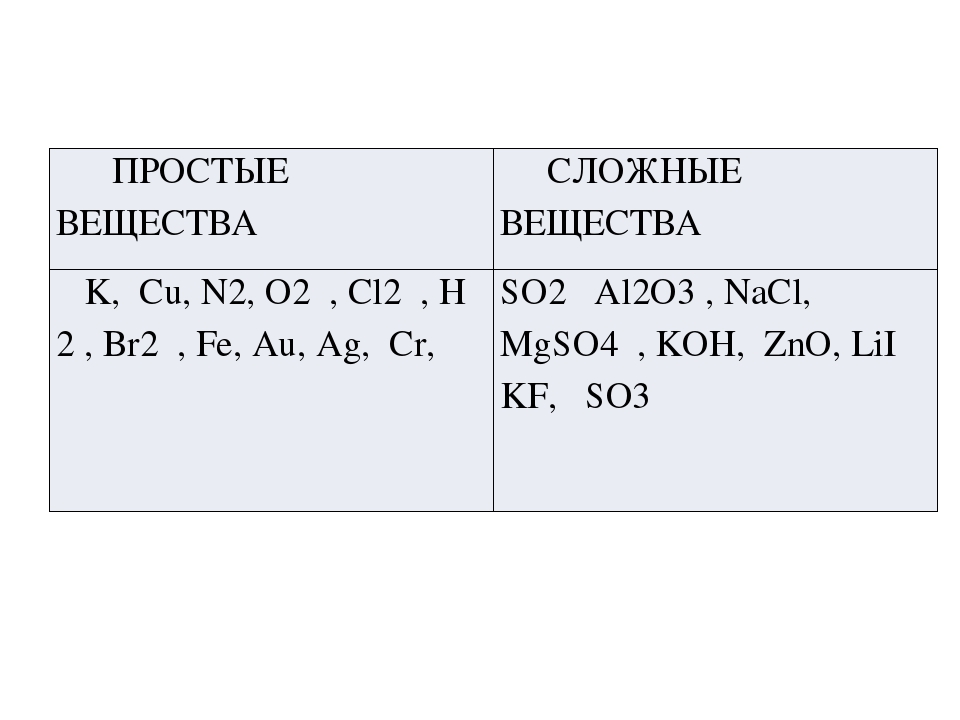 Теплоту образования соединений из простых веществ следует отличать от атомной теплоты образования. Для вычисления атомной теплоты образования необходимо учесть теп- лоту возгонки твердых веществ и теплоту диссоциации молекул газообразных веществ на атомы. [c.22]
Теплоту образования соединений из простых веществ следует отличать от атомной теплоты образования. Для вычисления атомной теплоты образования необходимо учесть теп- лоту возгонки твердых веществ и теплоту диссоциации молекул газообразных веществ на атомы. [c.22]
Сегодня химический элемент — это вид атомов Оказыва-егся, как все просто Один атом — просто материальная частица. Много одинаковых атомов (вид) — это уже химический элемент. Правда, надо помнить, что под атомом в данном случае понимается не гипотетический атом древних греков, а как уже упоминалось выше, конкретная частица материи (вещества) определенного состава и строения, по недоразумению унаследовавшая имя гипотетической частицы древних греков. [c.18]
Базируясь на своих представлениях о строении материи, Ломоносов разработал так называемую «корпускулярную теорию строения вещества», в которой впервые разграничил понятия атома, элемента, молекулы, простого вещества. С этого времени под «элементом» стали понимать элемент химический, а не абстрактный элемент материи.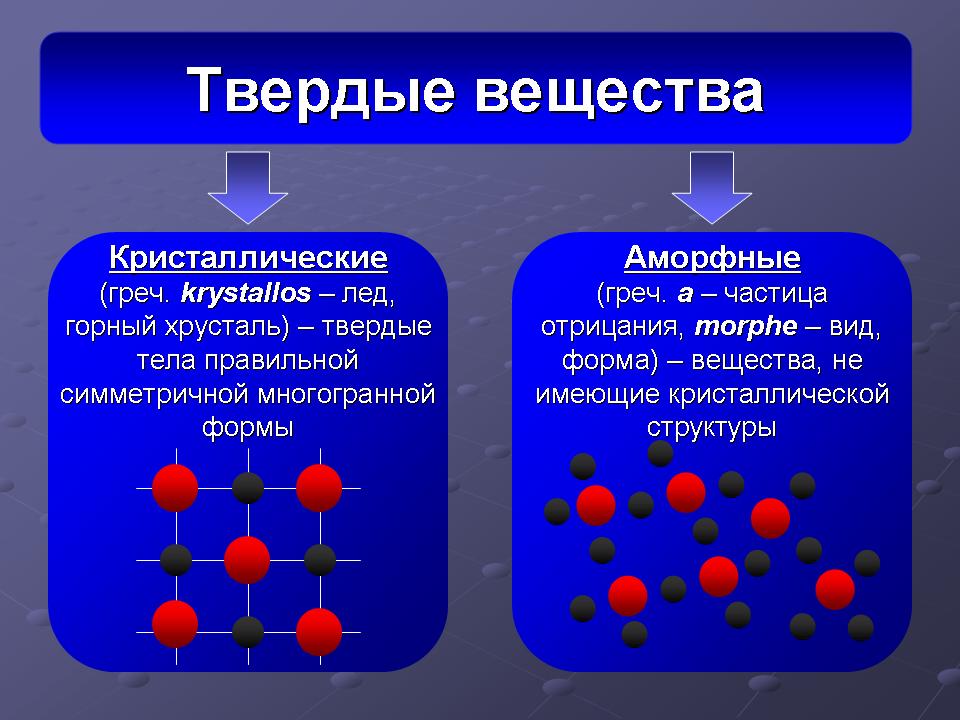 Правильнее было бы говорить «элемент химии», а не «химический элемент». Потому что термин элемент приобрел самое широкое использование в науке и технике элемент дома, моста, солнечной системы и т. д. К сожалению, в толковых и энциклопедических словарях нет современного определения элемента в широком смысле. Правда, в ФЭС [6, с. 793] довольно подробно описывается история возникновения и станов-.иения понятия «элемент». Первоначально — это буквы латинского алфавита Э(Ь)-Э(М)-Э(К)ты (иначе, члены ряда букв алфавита). Потом — простейшие начала физические элементы (Платон). У Аристотеля «элемент» становится философским термином, употребляющимся очень широко. В дальнейшем элементом стали называть составную часть сложного тела. Наиболее полно смысл термина «элемент» сегодня раскрывается в системно-структурном методе познания в сопоставлении (и противопоставлении) с другим коренным понятием метода «система». Здесь элемент — составная часть системы, органически связанная с другими ее частями (элементами), которые совокупно обеспечивают целостность последней.
Правильнее было бы говорить «элемент химии», а не «химический элемент». Потому что термин элемент приобрел самое широкое использование в науке и технике элемент дома, моста, солнечной системы и т. д. К сожалению, в толковых и энциклопедических словарях нет современного определения элемента в широком смысле. Правда, в ФЭС [6, с. 793] довольно подробно описывается история возникновения и станов-.иения понятия «элемент». Первоначально — это буквы латинского алфавита Э(Ь)-Э(М)-Э(К)ты (иначе, члены ряда букв алфавита). Потом — простейшие начала физические элементы (Платон). У Аристотеля «элемент» становится философским термином, употребляющимся очень широко. В дальнейшем элементом стали называть составную часть сложного тела. Наиболее полно смысл термина «элемент» сегодня раскрывается в системно-структурном методе познания в сопоставлении (и противопоставлении) с другим коренным понятием метода «система». Здесь элемент — составная часть системы, органически связанная с другими ее частями (элементами), которые совокупно обеспечивают целостность последней. [c.22]
[c.22]
Но его классы, в определенном смысле, стали и прообразом системы, так как все многообразие известных в то время химических элементов было приведено в относительный порядок — систему. Его классы металлов и неметаллов стали прообразами валентных групп элементов таблицы Менделеева. До сих пор первая валентная группа называется «группой металлов», при одном лишь уточнении — «щелочных», а седьмая — «металлоидов» (неметаллов). Здесь же от Лавуазье берет начало отождествление химического элемента и простого вещества. Металлы и неметаллы — это простые тела. Им (по Менделееву) отвечает понятие молекулы. Металлы и неметаллы — это форма организации атомов одного вида (химического элемента), а не сами химические элементы. Лавуазье, по существу, классифицировал не химические элементы, а простые вещества, так как в основе классификации лежали их физико-технические свойства. Его классификацию можно назвать качественно-описательной, потому что в ее основани- [c. 29]
29]
Для определенности теплоту образования любого вещества из простых веществ (не путать с теплотой образования нз атомов ) указывают, считая, что исходные простые вещества находятся в стандартном состоянии (см [c.56]
Энтальпия и внутренняя энергия образования простых веществ, согласно приведенному определению, равны нулю. Если элемент образует несколько простых веществ (гра(11ит и алмаз, белый и красный фосфор и т. п.), то стандартным считается состояние злег,1бнта в виде наиболее устойчивой при данных условиях модификации (например, при обычных условиях— графит в случае углерода, Оо в случае кислорода и т. д.) энтальпия и внутренняя энергия образования этой, наиболее устойчивой модификации принимаются равными нулю. [c.75]
Предсказание свойств веществ с помощью периодического закона. Периодический закон Д. И. Менделеева дает возможность определять свойства простых веществ и химических соединений. Впервые большое число таких определений было осуществлено самим Д. И. Менделеевым он рассчитал свойства и тех элементов, которые не были еще открыты. Как известно, предсказания Д. И. Менделеева полностью подтвердились. История естество-внания не знает других примеров столь многостороннего прогноза, который бы так блестяще оправдался. [c.38]
И. Менделеевым он рассчитал свойства и тех элементов, которые не были еще открыты. Как известно, предсказания Д. И. Менделеева полностью подтвердились. История естество-внания не знает других примеров столь многостороннего прогноза, который бы так блестяще оправдался. [c.38]
Теплота образования А12О3 из простых веществ, полученная по результатам определения в калорнметрнческой бомбе разными исследователями (приводится в основном по ) [c.34]
Справочник содержит выборочные значения различных термодинамических свойств металлов и сплавов при 298,15 К п высоких температурах и параметры фазовых переходов, в частности параметры процесса испарения (р ДС , ДЯ -) при разных температурах, В книге Ан. Н. Несмеянова сведены результаты определения давления насыщенного пара простых веществ различными методами, а также данные о молекулярнол составе пара. [c.78]
Все описанные соотношения справедливы не только для кислородсодержащих соединений.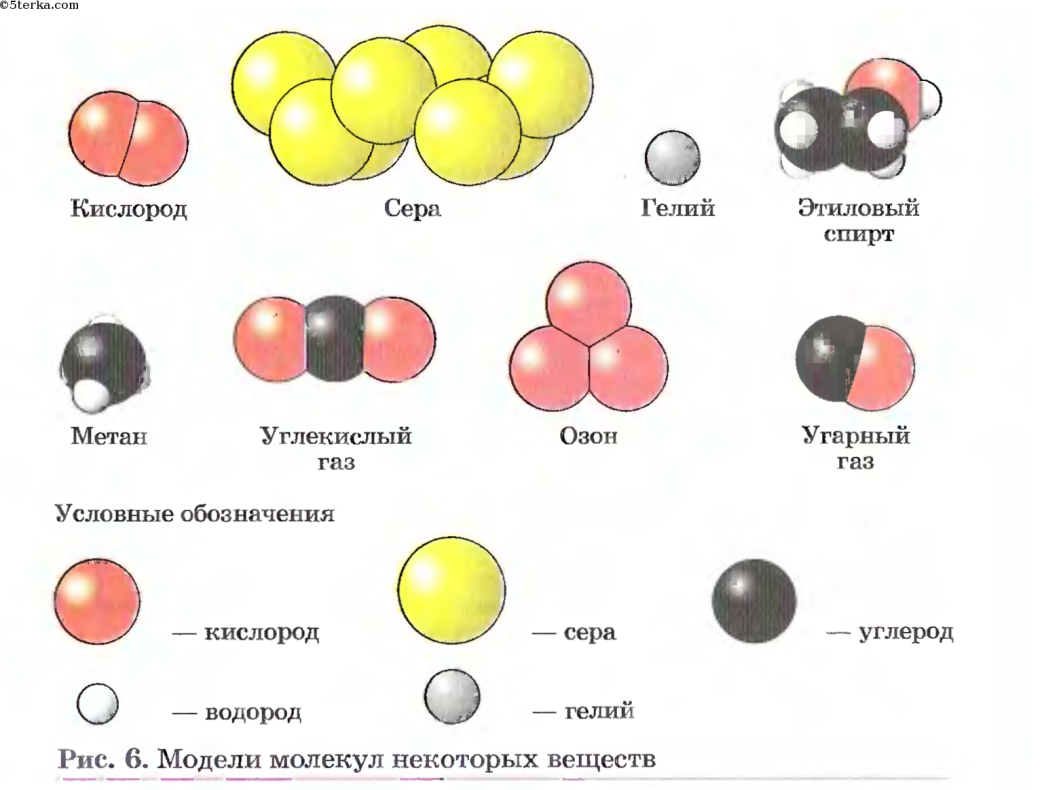 Так, для углеводородов применимы те же соотношения, но число атомов кислорода принимается равным нулю. Для соединений, содержащих серу, азот, фосфор, в уравнении (VI,1) постоянство суммы теплот образования и теплот сгорания сохраняется, но в правую часть уравнения входит новый член, представляющий теплоту сгорания перечисленных элементов (точнее говоря — соответствующих простых веществ). Конечное состояние продуктов сгорания в этом случае принимается иногда условно. Здесь важно лишь, чтобы это состояние было одинаковым конечным состоянием, принятым при определении теплоты сгорания данного соединения. Одинаковыми должны быть и исходные состояния данного элемента в реакции, к которой относится теплота сгорания простого вещества, и в реакции образования рассматриваемого соединения нз простых веществ. Практически это замечание относится главным образом к сере, так как для нее параметры реакций образования и, в частности, теплоту образования -в настоящее время часто относят к исходному состоянию ее в виде газа с двухатомными молекулами, 5г(г).
Так, для углеводородов применимы те же соотношения, но число атомов кислорода принимается равным нулю. Для соединений, содержащих серу, азот, фосфор, в уравнении (VI,1) постоянство суммы теплот образования и теплот сгорания сохраняется, но в правую часть уравнения входит новый член, представляющий теплоту сгорания перечисленных элементов (точнее говоря — соответствующих простых веществ). Конечное состояние продуктов сгорания в этом случае принимается иногда условно. Здесь важно лишь, чтобы это состояние было одинаковым конечным состоянием, принятым при определении теплоты сгорания данного соединения. Одинаковыми должны быть и исходные состояния данного элемента в реакции, к которой относится теплота сгорания простого вещества, и в реакции образования рассматриваемого соединения нз простых веществ. Практически это замечание относится главным образом к сере, так как для нее параметры реакций образования и, в частности, теплоту образования -в настоящее время часто относят к исходному состоянию ее в виде газа с двухатомными молекулами, 5г(г). Хотя стандартное состояние такого газа в обычных условиях физически нереализуемо, термодинамически оно определено достаточно хорошо, а использование параметров его в качестве вспомогательных расчетнь1х величин дает возможность при выражении влияния температуры на параметры реакций образования избежать искажающего влия ния изменений агрегатного состояния серы при повышенных температурах. К тому же при сопоставлении серусодержащих соединений с аналогичными кислородными соединениями параметры реакций образования с участием 5г(г), естественно, показывают более закономерные соотношения, чем параметры реакций образования с участием серы ромбической. [c.210]
Хотя стандартное состояние такого газа в обычных условиях физически нереализуемо, термодинамически оно определено достаточно хорошо, а использование параметров его в качестве вспомогательных расчетнь1х величин дает возможность при выражении влияния температуры на параметры реакций образования избежать искажающего влия ния изменений агрегатного состояния серы при повышенных температурах. К тому же при сопоставлении серусодержащих соединений с аналогичными кислородными соединениями параметры реакций образования с участием 5г(г), естественно, показывают более закономерные соотношения, чем параметры реакций образования с участием серы ромбической. [c.210]
Подобные же определения были выполнены этими исследователями для кислородных соединений (спиртов и простых эфиров). Полученные значения инкрементов для ЛЯа. 298 и АЯ . 293 рассматриваемых соединений в газообразном и жидком состояниях приведены в табл. VI,29, причем для алкантиолов, тиаалканов и ди-тиаалканов теплоты образования из простых веществ относятся к состоянию серы в виде ромбической [а не S2 (г)]. При использовании инкрементов для теплот атомизации надо учитывать, что они рассчитаны при следующих значениях теплот атомизации (в ккал) простых веществ (они большей частью отличаются от значений, приведенных в табл. VI, 1) [c.256]
При использовании инкрементов для теплот атомизации надо учитывать, что они рассчитаны при следующих значениях теплот атомизации (в ккал) простых веществ (они большей частью отличаются от значений, приведенных в табл. VI, 1) [c.256]
В этом смысле прогноз скорости химического превращепия оказывается в радиационно-химической кинетике несравпоппо бо.ние простым и определенным, чем при любом другом способе возбуждения химических реакций. Однако предсказание того, какие вещества образуются в результате радиолиза, значительно более трудно. Это связано с том, что наряду с возбуждением и диссоциацией, на нейтральные осколки прп радиационно-химическом воздействии происходят ионизация и диссоциативная ионизация, а при вторичных процессах — еще и ионно-молекулярные реакции и рекомбинация ионов. [c.184]
Из экспериментов известно, что, несмотря на огромное число компонентов, в различных процессах МСС ведут себя удив1ггельно просто. Подобные факты часто приводят к неоправданному распространению закономерностей химии и физики простых веществ на сложные многокомпонентные системы, даже без введения соответствующих поправок. Несмотря на определенный успех данных моделей, в них имеет место детерминированность элементарных стадий процессов, не учитываются их сопряжение и стохастический характер процесса во времени. Единственно возможным в таких случаях является статистический термодинамический и синергетический недетерминистиче-скии подход, который эффективно используется в естественных науках, в том числе в исследовании систем далеких от равновесия [35-45].Но в синергетике очень часто изучаются не самые главные компоненты и процессы, так как не достаточно информации о системе в це юм. Таким образом, в синергетике не хватает определенного макроуровня для описания сложных многокомпонентных объектов. Непрерывный подход к веществу, родившийся в древности, воплотился в XIX веке в термодинамику, для которой важен не состав, а начальное и конечное усредненное энергетическое состояние вещества. Кибернетика также оперирует начальным и конечным состоянием системы, которая является черным ящиком Из обширного эмпирического материала известно, что МСС, несмотря на огромное число компонентов, в ряде случаев ведут себя удивительно просто. Например, кинетика деструктивных процессов превращения нефтяных фракций и твердого топлива описывается простыми уравнениями первого или второго порядка [17-20]. Кроме того, пре- [c.11]
Со времени Лавуазье все вещества разделяют на простые вещества, сложные вещества (соединения) и смеси. Простое вещество состоит из атомов какого-нибудь одного элемента, соединения— из химически связанных атомов двух или более элементов. Простые вещества и соединения представляют собой химические иудивиды или индивидуальные вещества. Каждое из них обладает определенным составом, строением и только ему одному присущим набором свойств, обусловленных этим составом и строением. Химические индивиды отличаются от механических смесей однородностью, т. е. в их массе нет включений иного состава н строения. [c.12]
Приемная комиссия БГМУ
Программы вступительных испытаний
ПРОГРАММЫ ВСТУПИТЕЛЬНЫХ ЭКЗАМЕНОВ ДЛЯ ПОСТУПАЮЩИХ В БГМУ
ПРОГРАММА ПО ХИМИИ
Общие указания
На экзамене по химии поступающий в ВУЗ должен:
— показать знание основных теоретических положений химии как одной из важнейших естественных наук, лежащих в основе научного понимания природы;
— уметь применять теоретические положения химии при рассмотрении классов неорганических и органических веществ и их соединений;
— уметь раскрывать зависимость свойств веществ от их состава и строения;
— знать свойства важнейших веществ, применяемых в народном хозяйстве и в быту;
— понимать научные принципы важнейших химических производств (не углубляясь в детали устройства различной аппаратуры)
— решать типовые и комбинированные задачи по основным разделам химии.
На экзамене можно пользоваться следующими таблицами:
— «Периодическая система химических элементов Д.И.Менделеева»,
— «Растворимость оснований, кислот и солей в воде»,
— «Электрохимический ряд стандартных электродных потенциалов».
При решении задач разрешается пользоваться калькулятором.
Теоретические основы химии.
Предмет и задачи химии. Место химии среди естественных наук.
1. Основные понятия химии.
Основы атомно-молекулярного учения. Понятие атома, элемента, вещества. Простое вещество, сложное вещество. Понятие об аллотропных модификациях. Относительная атомная и относительная молекулярная масса. Стехиометрия: закон сохранения массы вещества, постоянство состава. Моль. Молярная масса. Закон Авогадро и его следствие. Уравнение Менделеева-Клапейрона. Явления физические и химические. Валентность и степень окисления.
2. Периодический закон и периодическая система элементов Д.И. Менделеева. Строение атома. Химическая связь. Строение вещества.
Строение ядер и электронных оболочек атомов химических элементов (s-, p-, d-элементов). Периодический закон химических элементов Д.И. Менделеева и строение периодической системы. Изотопы. Характеристика отдельных химических элементов главных подгрупп на основании положения в периодической системе и строения атома. Значение периодического закона для понимания научной картины мира, развития науки и техники.
Виды химической связи: Ковалентная (полярная и неполярная), ионная, металлическая, водородная. Механизм образования и примеры соединений. Модель гибридизации орбиталей. Агрегатные состояния веществ, вещества аморфные и кристаллические. Типы кристаллических решеток.
3. Основные закономерности протекания химических реакций.
Классификация химических реакций: реакции соединения, разложения, замещения, ионного обмена. Окислительно–восстановительные реакции, важнейшие окислители и восстановители. Электролиз. Тепловые эффекты химических реакций. Термохимические уравнения. Закон Гесса и следствия из него. Скорость химических реакций. Зависимости скорости от природы реагирующих веществ, концентрации, температуры. Катализ. Обратимость химических реакций. Химическое равновесие и условия его смещения.
4. Растворы. Электролитическая диссоциация.
Растворы. Растворимость веществ. Зависимость растворимости веществ от их природы, температуры, давления. Типы растворов. Выражение состава раствора (массовая доля, объемная доля, молярная концентрация). Значение растворов в промышленности, медицине, быту. Электролитическая диссоциация. Степень диссоциации. Сильные и слабые электролиты. Ионные уравнения реакций.
Неорганическая химия.
1. Основные классы неорганических соединений.
Оксиды, кислоты, гидроксиды, соли: классификация, номенклатура, способы получения и свойства. Амфотерность. Гидролиз солей.
2. Неметаллы.
Водород, его химические и физические свойства.
Вода. Физические, химические свойства. Кристаллогидраты. Значение воды в промышленности, сельском хозяйстве, быту, природе. Охрана водоемов от загрязнения.
Общая характеристика элементов YII группы главной подгруппы. Хлор. Физические, химические свойства. Свойства и способы получения галогеноводородов, галогенидов, кислородсодержащих соединений хлора.
Общая характеристика элементов главной подгруппы YI группы. Кислород, его получение, сравнение физических и химических свойств кислорода и озона. Окислительно–восстановительные реакции с участием пероксида водорода. Сера, ее физические и химические свойства. Соединения серы: сероводород, оксиды серы (IY, YI). Серная и сернистая кислоты, их свойства, соли серной и сернистой кислот. Производство серной кислоты.
Общая характеристика элементов Y группы главной подгруппы. Азот. Физические и химические свойства. Свойства аммиака и солей аммония, оксидов азота (I, II, IY), азотистой кислоты и нитритов, азотной кислоты и нитратов. Производство аммиака и азотной кислоты. Фосфор, его физические и химические свойства. Свойства соединений фосфора: фосфороводорода, фосфидов, оксида фосфора (Y), фосфорной кислоты и фосфатов.
Общая характеристика элементов IY группы главной подгруппы. Углерод, его аллотропные модификации, физические и химические свойства.. Свойства соединений углерода: оксидов (II, IY), угольной кислоты и ее солей. Свойства кремния, оксида кремния, кремниевой кислоты и силикатов.
3. Металлы.
Положение в периодической системе. Особенности строения атомов металлов. Металлическая связь. Характерные физические и химические свойства. Электрохимический ряд напряжений металлов. Коррозия металлов.
Общая характеристика IА- и IIА- групп периодической системы. Свойства натрия, калия, кальция и магния и их соединений. Жесткость воды и способы ее устранения. Свойства алюминия и его соединений. Свойства железа, оксидов, гидроксидов и солей железа (II и III). Природные соединения железа. Свойства перманганата калия: восстановление перманганат иона в кислой, нейтральной и щелочной средах.
Медико-биологическое значение соединений указанных металлов.
Органическая химия.
1. Теоретические положения органической химии.
Основные положения теории химического строения А.М. Бутлерова. Зависимость свойств веществ от химического строения. Виды изомерии. Электронная природа химических связей в молекулах органических соединений, способы разрыва связей, понятие о свободных радикалах.
2. Основные классы органических соединений.
Углеводороды.
Гомологический ряд предельных углеводородов, их электронное и пространственное строение (sp3-гибридизация). Номенклатура, физические и химические свойства, способы получения предельных углеводородов. Циклоалканы.
Гомологический ряд этиленовых углеводородов. Двойная связь: σ– и p – связи, sp2–гибридизация. Изомерия углеродного скелета и положение двойной связи. Номенклатура этиленовых углеводородов. Физические и химические свойства, способы получения. Природный каучук, его строение и свойства.
Гомологический ряд ацетиленовых углеводородов. Тройная связь, sp–гибридизация. Номенклатура, физические и химические свойства, способы получения. Получение ацетилена карбидным способом и из метана.
Ароматические углеводороды (арены). Бензол, электронное и пространственное строение, химические свойства. Гомологи бензола. Понятие о взаимном влиянии атомов на примере толуола.
Природные источники углеводородов: нефть, природный газ и попутные нефтяные газы, уголь. Фракционная перегонка нефти. Крекинг. Ароматизация нефтепродуктов. Охрана окружающей среды при нефтепереработке.
Кислородсодержащие соединения.
Спирты, их строение. Номенклатура, химические свойства, способы получения спиртов. Многоатомные спирты, номенклатура, особые свойства (этиленгликоль, глицерин). Ядовитость спиртов, их губительное действие на организм человека. Фенол, его строение, физические и химические свойства фенола.
Альдегиды, их строение. Номенклатура, физические и химические свойства. Получение и применение муравьиного и уксусного альдегидов. Понятие о кетонах.
Карбоновые кислоты, их строение. Карбоксильная группа, взаимное влияние карбоксильной группы и углеводного радикала. Физические и химические свойства карбоновых кислот. Муравьиная, уксусная, стеариновая, олеиновая, бензойная кислоты. Получение и применение карбоновых кислот. Сложные эфиры. Строение, химические свойства. Реакция этерификации.
Азотсодержащие соединения.
Амины алифатические и ароматические, их строение. Номенклатура, химические свойства, способы получения аминов.
Аминокислоты. Строение, химические свойства, изомерия.
Понятие об азотсодержащих гетероциклических соединениях на примере пиридина и пиррола.
3. Важнейшие природные соединения.
Жиры, строение, химические свойства, их роль в природе.
Углеводы: строение и свойства глюкозы, рибозы, дезоксирибозы, сахарозы, крахмала и целлюлозы. Применение целлюлозы и её производных. Понятие об искусственных волокнах.
Синтез пептидов, их строение. Строение, структура и свойства белков. Успехи в изучении и синтезе белков. Значение микробиологической промышленности. Строение нуклеотидов и полинуклеотидов. Различие в строении РНК и ДНК. Биологическая роль указанных классов соединений.
Типовые расчетные задачи
1. Вычисление массовой или объемной доли компонента.
2. Вычисление молярной концентрации.
3. Вычисление относительных плотностей веществ в газообразном состоянии.
4. Вычисление объема газообразного вещества известной массы или известного количества при нормальных условиях.
5. Установление молекулярной формулы вещества по массовой доле элементов или по массам продуктов сгорания.
6. Вычисление массы (объема, количества вещества) одного из участников реакции по известной массе (объему, количеству вещества) другoгo участника реакции.
7. То же, с предварительным нахождением, какое из веществ вступает в реакцию полностью.
8. То же, с учетом выхода продукции реакции в процентах от теоретически возможного.
9. То же, с учетом массовой доли примесей в реагенте.
10. Определение состава соли (кислая или средняя) по массам веществ, вступающих в реакцию.
11. Определение состава двухкомпонентной смеси по массам веществ, образующихся в ходе одной или нескольких реакций.
Все расчетные задачи могут быть как в прямом, так и в обратном вариантах (например, расчет массовой доли вещества по его массе и известной массе раствора или же расчет массы вещества по известной массовой доле и массе раствора). Сложные задачи включают в себя две или больше перечисленных типовых задач.
Рекомендуемая литература:
1. Рудзитис Г.Е., Фельдман Ф.Г. Химия для 8–11 классов. М.: «Просвещение», 2011.
- Гузей Л.С. и др. Химия для 8-11 классов. М., «Дрофа», 2004.
- В.В. Еремин, Н.Е. Кузьменко, А.А. Дроздов, В.В. Лунин. Химия для 8-11 классов. М.: Дрофа, 2008
- Габриелян О.С. Химия для 8-11 классов. М., «Дрофа», 2005.
- Гольдфарб Я.Л., Ходаков Ю.Б., Додонов Ю.Б. Сборник задач и упражнений по химии. — М.: «Дрофа», 2005.
- Е.А. Еремина, О.Н. Рыжова Справочник школьника по химии. Еремина М.: Издательство «Экзамен», 2006.
Дополнительная литература:
1. Хомченко Г.П. Химия для поступающих в ВУЗы. М.: «Высшая школа», 2003.
2. Хомченко Г.П., Хомченко И.Г. Задачи по химии для поступающих в ВУЗы. М., «Высшая школа», 2005.
3. Кузьменко Н.Е., Магдесиева Н.Н., Еремин В.В. Задачи по химии для абитуриентов. Курс повышенной сложности. – М: «Высшая школа», 2004.
4. Кузьменко Н.Е., Еремин В.В., Попков В.А. Химия для школьников старших классов и поступающих в ВУЗы. М., «Дрофа», 2008.
5. Егоров А.С., Дионисьев В.Д., Ермакова В.К. и др. Химия. Пособие – репетитор. Ростов-на-Дону, «Феникс», 2006.
Программа вступительных испытаний по биологии
1. Биология как наука.
Биология — наука о живой природе. Вклад биологии в формирование современной научной картины мира и общей культуры личности. Значение биологической науки для сельского хозяйства, промышленности, медицины, охраны природы. Методы биологии. Уровни организации живого: молекулярный, клеточный, организменный, популяционно-видовой, экосистемный, биосферный. Свойства живых систем: особенности химического состава, обмен веществ и энергии, открытость, рост, самовоспроизведение, наследственность и изменчивость, раздражимость, саморегуляция; их проявление уживотных, растений, грибов и бактерий.
2. Строение и функционирование клетки.
Основные положения клеточной теории, ее значение в современной науке. Клетка — структурная и функциональная единица живого. Клеточное строение организмов как отражение единства живой природы.
Химический состав клеток. Содержание химических элементов в клетке. Вода, минеральные соли и другие неорганические вещества, их роль в жизнедеятельности. Особенности структуры и функции органических веществ: белков, углеводов, липидов, нуклеиновых кислот в связи с их функциями. Строение и функции органоидов клетки; взаимосвязь этих компонентов как основа ее целостности.
Многообразие клеток. Прокариотные и эукариотные клетки. Особенности строения клеток растений, животных и грибов. Вирусы — неклеточные формы. Роль вирусов как возбудителей заболеваний, их профилактика.
Клеточный метаболизм и его составляющие — ассимиляция (анаболизм) и диссимиляция (катаболизм). Пластический и энергетический обмен. Ферменты, их свойства и роль в метаболизме. Основные этапы пластического обмена. Репликация ДНК. Гены. Генетический код и его свойства. Транскрипция. Трансляция. Роль матричных процессов в реализации наследственной информации. Автотрофные и гетеротрофные организмы. Этапы фотосинтеза и роль хлорофилла в этом процессе. Биосферное значение фотосинтеза. Хемосинтез. Основные этапы энергетического обмена. Брожение и клеточное дыхание, метаболическая роль кислорода. Роль АТФ в энергетическом и пластическом обмене. Взаимосвязь энергетического и пластического обмена.
3. Размножение и индивидуальное развитие организмов.
Деление клетки — основа роста, развития и размножения организмов. Митоз и мейоз — основные способы деления эукариотной клетки. Интерфаза. Этапы митоза и мейоза. Значение митоза и мейоза. Половое и бесполое размножение, их роль в природе. Способы бесполого размножения у животных, растений и грибов. Развитие половых клеток. Оплодотворение у животных и растений. Двойное оплодотворение — особенность цветковых растений. Чередование полового и бесполого поколений (гаметофита и спорофита) у растений.
Онтогенез – индивидуальное развитие организма, основные этапы онтогенеза. Эмбриональное и постэмбриональное развитие. Основные этапы развития зародыша (на примере животных). Прямое развитие и развитие с метаморфозом (непрямое). Понятие жизненного цикла.
4. Основы генетики и селекции.
Генетика — наука о наследственности и изменчивости организмов. Основные методы генетики. Гибридологический анализ, моно-, ди- и полигибридное скрещивание. Основные понятия генетики: ген, аллель, признак, гомозигота и гетерозигота, доминантность и рецессивность, генотип, фенотип и норма реакции. Законы наследственности, установленные Г. Менделем, и условия их выполнения. Цитологические основы выполнения законов Г.Менделя. Полное и неполное доминирование.
Хромосомная теория наследственности. Сцепленное наследование и его цитологические основы, нарушение сцепления. Кроссинговер (перекрест хромосом) и его значение. Генетическое определение пола, половые хромосомы и аутосомы, наследование признаков, сцепленных с полом. Генотип как целостная исторически сложившаяся система. Понятие о взаимодействии и множественном действии генов. Роль генотипа и факторов внешней среды в формировании фенотипа.
Формы изменчивости организмов: модификационная и наследственная изменчивость, мутационная и комбинативная изменчивость, их роль в природе. Причины мутаций. Влияние окружающей среды на мутационный процесс, мутагены. Главные источники комбинативной изменчивости: независимое поведение гомологичных хромосом в мейозе, кроссинговер, оплодотворение. Значение генетики для здравоохранения. Наследственные заболевания человека и меры их профилактики. Влияние радиоактивного излучения и химических мутагенов (в том числе никотина, алкоголя и наркотических веществ) на наследственность человека.
Генетика — теоретическая основа селекции. Порода животных и сорт растений. Основные методы селекции растений и животных: мутагенез, полиплоидия, гибридизация, искусственный отбор. Современные биотехнологии: генная и клеточная инженерия, микробиологический синтез, их роль в развитии здравоохранения, промышленности, сельского хозяйства и охраны природы.
5. Многообразие живой природы.
5.1. Система органического мира
Классификация организмов и роль К.Линнея как основоположника научной систематики. Основные систематические категории: вид, род, семейство, отряд (порядок), класс, тип (отдел), царство. Особенности строения и функционирования представителей основных царств живой природы: бактерий, растений, животных и грибов.
5.2. Царство бактерий
Основные черты строения и жизнедеятельности бактерий, их размножение. Споры. Роль бактерий в биосфере. Значение бактерий для сельского хозяйства, промышленности и медицины. Болезнетворные бактерии и борьба с ними.
5.3. Царство грибов.
Формы вегетативного тела грибов. Шляпочные грибы, их строение, питание, размножение. Плесневые грибы. Дрожжи. Экологические группы грибов. Грибы-паразиты, вызывающие болезни растений, животных и человека. Микориза. Роль грибов в биосфере и значение для человека.
Лишайники – организмы симбиотического происхождения, образованные микобионтом (гриб) и фикобионтом (цианобактерия или зеленая одноклеточная водоросль). Строение лишайников. Экологические и морфологические группы. Питание. Размножение. Роль лишайников в биосфере и значение для человека.
5.4. Царство растений.
Общая характеристика растений. Роль растений в структуре экосистемы и значение для человека. Классификация растений. Низшие и высшие растения. Жизненный цикл у растений, чередование поколений спорофита и гаметофита. Эволюция жизненного цикла у растений.
Низшие растения (Водоросли). Эволюция и формы вегетативного тела. Основные отделы водорослей – Зеленые, Бурые и Красные. Строение и жизнедеятельность одноклеточных водорослей (хламидомонада). Нитчатые водоросли (Улотрикс) и водоросли с пластинчатым слоевищем. Размножение водорослей и жизненные циклы. Роль водорослей в биосфере и значение для человека.
Выход растений на сушу. Понятие о тканях и органах у растений. Характеристика отдела Риниевых (Псилофитов).
Отдел Моховидные. Зеленые мхи. Строение, размножение и жизненный цикл кукушкина льна. Мох сфагнум, особенности его строения. Образование торфа, его значение.
Отделы Плауновидные, Хвощевидные, Папоротниковидные: характеристика, основные представители, их строение и биология. Жизненный цикл и размножение папоротника.
Отдел Голосеменные: характеристика строения и размножения. Распространение хвойных. Биологическое значение семени. Роль голосеменных в биосфере и значение для человека.
Отдел Покрытосеменные (цветковые). Строение цветка. Семезачаток. Двойное оплодотворение. Образование семян и плодов. Роль покрытосеменных в биосфере и значение для человека. Классификация Покрытосеменных: классы Двудольных и Однодольных, их особенности. Отличительные признаки растений основных семейств; их биологические особенности (семейства Крестоцветные, Розоцветные, Бобовые, Пасленовые, Сложноцветные, Лилейные, Злаки). Основные группы тканей растений (образовательные, покровные, механические, проводящие, основные). Вегетативные органы высших растений. Строение и функции корня, виды корней, типы корневой системы, видоизменения (метаморфозы) корня. Побег. Почки. Стебель. Ветвление побега. Строение и функции стебля, видоизменения побегов (корневище, клубень, луковица). Строение и функции листа, типы листьев, листорасположение, типы жилкования.
Генеративные органы цветковых растений. Строение цветка в связи со способами опыления. Цветки однополые и обоеполые. Формула цветка. Соцветия и их биологическое значение. Строение и классификация семян (на примере однодольного и двудольного растения) и плодов. Типы прорастания семян, питание и рост проростка. Распространение плодов и семян. Значение цветков, плодов и семян в природе и жизни человека. Происхождение растений. Основные этапы эволюции растительного мира: возникновение фотосинтеза, возникновение одноклеточных и многоклеточных водорослей, выход растений на сушу (псилофиты), появление споровых и семенных растений. Филогенетические связи в растительном мире.
5.5. Царство животных
Простейшие животные. Общая характеристика простейших: строение клеток, питание, дыхание, выделение, движение, поведение и размножение. Разнообразие простейших: обыкновенная амеба, эвглена зеленая и гетеротрофные жгутиконосцы, инфузория-туфелька и другие. Отличия простейших от многоклеточных животных. Их значение в природе и жизни человека. Паразитические простейшие – возбудители заболеваний человека и животных.
Многоклеточные животные. Особенности строения многоклеточных животных. Основные ткани, органы и их системы. Типы симметрии тела животных. Двухслойные и трехслойные животные.
Типы Кишечнополостные, Плоские черви, Круглые черви, Кольчатые черви. Характеристика их строения и основных процессов жизнедеятельности (внешнее строение, система покровов, движение и мускулатура, питание и пищеварительная система, дыхание, выделение и выделительная система, распределение веществ в организме, полость тела, нервная система, особенности поведения, половая система и способы размножения). Жизненные циклы важнейших представителей. Характеристика основных классов. Роль в экосистемах и жизни человека. Паразитические представители плоских и круглых червей, их значение для здравоохранения и сельского хозяйства. Профилактика паразитарных заболеваний.
Тип Членистоногие. Характеристика строения и основных процессов
жизнедеятельности. Классы: Ракообразные, Паукообразные, Насекомые. Особенности членистоногих в связи с освоением наземно-воздушной среды обитания. Основные отряды насекомых: Прямокрылые, Жесткокрылые, Чешуекрылые, Двукрылые, Перепончатокрылые. Насекомые с полным и неполным превращением. Многообразие насекомых, их роль в экосистемах и жизни человека. Методы борьбы с насекомыми — вредителями сельскохозяйственных культур и переносчиками заболеваний. Охрана насекомых.
Тип Моллюски. Характеристика строения и основных процессов жизнедеятельности, основные классы (Брюхоногие, Двустворчатые, Головоногие). Роль моллюсков в водных и наземных экосистемах.
Тип Хордовые. Общая характеристика типа. Основные классы хордовых: Ланцетники, Хрящевые рыбы, Костные рыбы, Земноводные, Пресмыкающиеся, Птицы, Млекопитающие. Характеристика их строения и основных процессов жизнедеятельности в связи с особенностями среды обитания и образа жизни. Происхождение основных классов и эволюция позвоночных. Выход позвоночных на сушу и освоение ими наземно-воздушной среды обитания. Характеристика основных отрядов. Роль различных хордовых в экосистемах и жизни человека, охрана и регуляция численности. Основные домашние и сельскохозяйственные животные: происхождение, биологические основы их содержания, кормления, разведения.
Эволюция животного мира.
Происхождение Простейших и Многоклеточных животных. Происхождение основных типов животного царства. Усложнение строения и жизнедеятельности животных в процессе эволюции. Положение человека в системе царства животных, доказательства его систематической принадлежности.
6. Человек и его здоровье.
Общий обзор организма человека: основные ткани и системы органов. Значение знаний о строении, жизнедеятельности организма и гигиене человека для охраны его здоровья.
Органы и системы органов человека.
Система покровов. Строение и функции кожи. Производные кожи: волосы и ногти. Роль кожи в терморегуляции, закаливание организма. Гигиена кожи, профилактика и первая помощь при ожогах, обморожениях, и механических травмах.
Опорно-двигательная система и движение. Основные элементы опорно-двигательной системы человека. Части скелета: осевой скелет, скелет конечностей и их поясов. Строение костей и их функции. Основные типы костей и их соединений. Суставы. Хрящи, сухожилия, связки. Строение мышц и их функции. Основные группы мышц человека. Первая помощь при ушибах, растяжении связок, переломах и вывихах.
Кровь и кровообращение. Понятие внутренней среды организма, значение постоянства внутренней среды. Кровь, лимфа и тканевая жидкость. Состав крови человека: плазма крови и различные форменные элементы, их строение и функции. Иммунитет и его типы. Антигены и антитела. Роль И.И. Мечникова в создании учения об иммунитете. Инфекционные заболевания и борьба с ними. Прививки и их роль в профилактике инфекционных заболеваний. Группы крови. Переливание крови, донорство. Свертывание крови. Строение системы кровообращения: сердце и сосуды (артерии, капилляры, вены). Большой и малый круги кровообращения. Предупреждение сердечно-сосудистых заболеваний. Первая помощь при кровотечениях. Вредное влияние курения, употребления алкоголя и наркотиков на сердечно-сосудистую систему.
Дыхательная система и газообмен. Основные компоненты дыхательной системы. Строение легких, механизм вдоха и выдоха, газообмен. Значение дыхания. Гигиена органов дыхания. Заболевания органов дыхания и их профилактика. Предупреждение распространения инфекционных заболеваний. Чистота атмосферного воздуха как фактор здоровья. Приемы первой помощи при отравлении угарным газом и спасении утопающего.
Органы пищеварения и питание. Строение и функции пищеварительной системы. Отделы пищеварительного тракта и их функции. Пищеварительные железы. Роль ферментов в пищеварении. Регуляция пищеварения, исследования И.П. Павлова. Пищевые продукты и питательные вещества: белки, липиды, углеводы, минеральные вещества, вода, витамины. Гигиена органов пищеварения, рациональное питание. Значение питания и пищеварения. Обмен веществ и энергии в организме человека, профилактика нарушений метаболизма. Роль витаминов в организме, их содержание в пищевых продуктах. Профилактика пищевых отравлений, кишечных инфекций и паразитарных заболеваний.
Выделение. Строение мочевыделительной системы человека. Органы мочевыделительной системы и их функции. Образование первичной и вторичной мочи. Профилактика заболеваний. Роль других систем органов в выделении продуктов метаболизма.
Размножение и развитие. Мужская и женская половая система, их строение и функция. Образование половых клеток. Основные этапы индивидуального развития человека. Причины нарушения индивидуального развития; наследственные болезни, их причины и предупреждение. Инфекции, передающиеся половым путем, их профилактика.
Нервная и гуморальная регуляция процессов жизнедеятельности. Основные железы внутренней секреции и их значение для роста, развития и регуляции функций организма. Основные гормоны человека. Строение нервной системы, ее отделы: центральная и периферическая нервная система. Строение и функции головного и спинного мозга. Соматическая и вегетативная нервная система. Органы чувств, их строение и функции. Анализаторы. Нарушения работы анализаторов и их профилактика. Условные и безусловные рефлексы, рефлекторные дуги. Высшая нервная деятельность, речь и мышление. Сознание как функция мозга. Социальная и биологическая обусловленность поведения человека. Роль И.М. Сеченова и И.П. Павлова в создании учения о высшей нервной деятельности. Нарушения деятельности нервной системы и их предупреждение. Сон, его значение и гигиена. Взаимосвязь процессов нервной и гуморальной регуляции.
7. Эволюция органического мира.
Доказательства эволюции живой природы. История эволюционного учения; К. Линней, Ж.Кювье, Ж.-Б.Ламарк и их роль в развитии науки. Основные положения теории Ч. Дарвина, ее значение. Популяции и их структура. Численность популяций, возрастной и половой состав, формы совместного существования особей. Изменчивость в популяциях. Факторы (движущие силы) эволюции. Естественный отбор — направляющий фактор эволюции. Формы естественного отбора (движущий, стабилизирующий, разрывающий). Борьба за существование. Роль экологии в изучении механизмов эволюционных преобразований. Возникновение приспособленности, ее относительный характер. Вид и его критерии. Механизмы видообразования. Изоляция и ее типы, роль географической изоляции. Микроэволюция и макроэволюция, соотношение их механизмов. Роль изучения онтогенеза в познании механизмов эволюции органического мира. Биогенетический закон. Биологический прогресс и регресс. Ароморфоз, идиоадаптация, общая дегенерация; соотношение путей эволюции. Эволюционные параллелизмы и конвергенция, их причины. Гомологичные и аналогичные органы. Основные этапы эволюции жизни. Происхождение жизни на Земле. Наиболее важные ароморфозы в эволюции живой природы. Происхождение и эволюция человека. Доказательства происхождения человека от животных. Этапы эволюции человека. Движущие силы антропогенеза. Возникновение человеческих рас. Биологическое и социальное в природе человека.
8. Организм и окружающая среда. Экосистемы. Биосфера.
Экология — наука о взаимоотношении организмов и окружающей среды, значение экологии. Понятие окружающей среды и экологического фактора, классификация экологических факторов. Действие экологических факторов. Ограничивающие факторы. Понятие экологической ниши. Основные абиотические факторы: свет, температура, влажность, их роль в жизни организмов. Периодические явления в жизни природы: биологические ритмы, фотопериодизм. Типы межвидовых взаимоотношений: конкуренция, хищничество, паразитизм, симбиоз. Разнообразие популяций, их возрастная и половая структура. Динамика численности популяций и ее причины. Биологические сообщества — многовидовые системы, взаимосвязь организмов в сообществе. Экосистема и биогеоценоз. Видовая и пространственная структура экосистем. Роль редких видов в природе и меры по их охране. Трофическая структура экосистем: продуценты, консументы, редуценты. Правило экологической пирамиды. Пищевые цепи и сети. Круговорот веществ и превращение энергии в экосистемах. Саморегуляция — одно из важнейших свойств экосистем. Внешние и внутренние причины изменения экосистем, экологическая сукцессия. Влияние человека на природные экосистемы, специфика действия антропогенных факторов. Сравнение естественных и искусственных экосистем. Агроэкосистемы и экосистемы городов. Значение биологического разнообразия для нормального функционирования естественных экосистем, сохранение биологического разнообразия. Значение природоохранных мероприятий и рационального природопользования. Биосфера как глобальная экосистема, ее границы. Вклад В.И.Вернадского в разработку учения о биосфере. Функции живого вещества. Особенности распределения биомассы в биосфере. Биологический круговорот. Эволюция биосферы. Глобальные изменения в биосфере и их причины. Влияние деятельности человека на эволюцию биосферы.
Общие указания
На экзамене по биологии поступающий в высшее учебное заведение должен показать:
- знание главнейших понятий, закономерностей и законов, касающихся строения, жизни и развития растительного, животного и человеческого организмов, развития живой природы;
- знание строения и жизни растений, животных, человека, основных групп растений и классификации животных;
- умение обосновывать выводы, оперировать понятиями при объяснении явлений природы с приведением примеров из практики сельскохозяйственного и промышленного производства, здравоохранения и т.д. Этому умению придается особое значение, так как оно будет свидетельствовать об осмысленности знаний, о понимании излагаемого материала экзаменующимся.
Рекомендуемая литература:
1. Каменский А.А. Общая биология 10-11 класс. М.: Дрофа, 2013г.
2. Пономарева И.Н. Биология 10 класс. Профильный уровень. М.: Вентана-Граф, 2013.
3. Трайтак Д.И. Биология 5-6 класс. М.: Мнемозина, 2013. ФГОС.
4. Пасечник В.В. Биология 7 класс. М.: Просвещение, 2015 г. ФГОС.
5. Рохлов В.С. Биология. Человек 8 класс. М.: Дрофа, 2010 г.
6. Пасечник В.В. Биология. Человек 8 класс. М.: Просвещение, 2011.
7. Каменский А.А. Биология. Введение в экологию. М.: Дрофа, 2011.
8. Бородин П.М., Высоцкая Л.В., Дымшиц Г.М. и др. Биология (профильный уровень). 10-11 класс. В 2-х частях. М.: Просвещение, 2014.
9. Дубинина Н.В., Пасечник В.В. Биология. Бактерии, грибы, растения. 6 класс. М.: Дрофа, 2014.
10. Каменский А.А., Криксунов Е.А., Пасечник В.В. Биология. Общая биология. 10-11 класс. М.: Дрофа, 2014.
11. Колесов Д.В., Маш Р.Д., Беляев И.Н. Биология. Человек. 8 класс. М.: Дрофа, 2014.
12. Пасечник В.В. Биология. 7 класс (серия «Линия жизни»). М.: Просвещение, 2013.
13. Пасечник В.В., Каменский А.А., Швецов Г.Г. (под ред. Пасечника В.В.) Биология. 8 класс. М.: Просвещение, 2013.
14. Пасечник В.В., Суматохин С.В., Калинова Г.С. (под ред. Пасечника В.В.) Биология. 7 кл. М.: Просвещение, 2013.
ПРОГРАММЫ ПО РУССКОМУ ЯЗЫКУ
Программы по русскому языку составлена в соответствии со школьной программой.
Цель: выявить наиболее грамотных абитуриентов, знающих орфографические и пунктуационные правила, культуру речи, умеющих точно выражать мысли, используя разнообразную лексику и различные грамматические конструкции.
ПРОГРАММА ПО РУССКОМУ ЯЗЫКУ
1. Орфография
1. Правописание гласных в корне. Проверяемые безударные гласные. Непроверяемые безударные гласные. Чередующиеся гласные а-о, и-е. Гласные после шипящих. Гласные после ц. Буквы э — е. Буква й..
2. Правописание согласных в корне. Звонкие и глухие согласные. Двойные согласные в корне и на стыке приставки и корня. Непроизносимые согласные.
3. Употребление прописных букв. Прописные буквы в начале текста. Собственные имена лиц. Клички животных, наименования видов растений, сортов вин. Имена действующих лиц в произведениях. Названия документов, памятников старины, произведений искусства. Наименование должностей и званий. Названия литературных произведений и органов печати и др.
4. Разделительныеъ и ь. Употребление ъ. Употребление ь.
5. Правописание приставок. Приставки на з~. Приставка с-. Приставки пре- и при-. Гласные ы и и после приставок.
6. Гласные после шипящих и ц в суффиксах и окончаниях. Гласные о и епосле шипящих. Гласные после ц.
7. Правописание имен существительных. Окончания имен существительных. Суффиксы имен существительных. О и Е после шипящих в корне.
8. Правописание имен прилагательных. Окончания имен прилагательных. Суффиксы имен прилагательных.
9. Правописание сложных слов. Соединительные гласные о и е. Сложные слова без соединительной гласной. Правописание сложных существительных. Правописание сложных прилагательных.
10. Правописание имен числительных. Числительные количественные, порядковые, собирательные, дробные. Числительное пол-.
11. Правописание местоимений. Отрицательные местоимения.
12. Правописание глаголов. Личные окончания глаголов. Употребление ь в глагольных формах. Суффиксы глаголов.
13. Правописание причастий. Гласные в суффиксах причастий. Правописание н и нн в причастиях и отглагольных прилагательных.
14. Правописание наречий. Гласные на конце наречий. Наречия на шипящую. Отрицательные наречия. Слитное написание наречий. Дефисное написание наречий. Раздельное написание наречных сочетаний.
15. Правописание предлогов. Сложные предлоги. Слитное написание предлогов и предложных словосочетаний.
16. Правописание союзов. Слитное написание союзов. Раздельное написание союзов.
17. Правописание частиц.
2. Пунктуация
1. Знаки препинания в конце предложения и при перерыве речи.
2. Тире между членами предложения.
3. Знаки препинания в предложениях с однородными членами.
4. Знаки препинания при повторяющихся словах.
5. Знаки препинания в предложениях с обособленными членами.
6. Знаки препинания в предложениях с уточняющими, пояснительными и присоединительными членами предложения.
7. Знаки препинания при словах, грамматически не связанных с членами предложения.
8. Знаки препинания при междометиях, частицах, утвердительных, отрицательных и вопросительно-отрицательных словах.
9. Знаки препинания в сложносочиненных предложениях.
10. Знаки препинания в сложноподчиненных предложениях.
11. Знаки препинания при оборотах, не являющихся придаточными предложениями.
12. Знаки препинания в бессоюзных сложных предложениях.
13. Знаки препинания при прямой речи.
14. Знаки препинания при цитатах.
15. Употребление кавычек.
3. Культура речи.
1. Нормативный аспект культуры речи. Языковые нормы: орфоэпические (произношение), акцентологические (ударение), орфографические (написание), словообразовательные, лексические, морфологические, синтаксические, пунктуационные.
2. Функциональные стили русского языка: научный, официально-деловой, газетно-публицистический, художественный, разговорный.
Примеры тестов.
Задание 1. Укажите номер слова, в котором пропущена буква А.
1. Р…птание
2. Раств…рить
3. Г…ворливый
4. Утв…рь
Задание 2. Укажите номер слова, в котором пропущена И.
1. Об…скивать
2. Пред…нфарктный.
3. Спорт…гра.
4. С…скной.
Задание 3. Укажите номер предложения, в котором между подлежащим и сказуемым на месте подчеркнутого пробела тире не ставится.
1. Самое большое счастье для человека _ приносить людям радость.
2. Офицер этот _ не чета вам.
3. Любить тайгу _ значит восстанавливать ее богатства.
4. Трижды пять _ пятнадцать.
Задание 4. Укажите номер предложения с обстоятельством, в котором на месте подчеркнутого пробела запятая не ставится.
1. Очнувшись _ я некоторое время не мог опомниться.
2. Ворча и оглядываясь _ Каштанка вошла в комнату.
3. Он знал, что бросается _ очертя голову _ в омут, куда и заглядывать не стоило.
4. Отправляя Метелицу в разведку _ Левинсон наказал ему вернуться той же ночью.
Задание 5. Ударение неправильно поставлено в слове:
1) цепочка
2) оптовый
3) каталог
4) афиняне
5) свекла
Задание 6. Нормы сочетаемости слов нарушены в словосочетании:
1) основать выводы
2) разъяснять ошибки
3) беспокоиться за родителей
4) оплатить за проезд
5) мириться с недостатками
Литература
1. Баранов М.Т. Русский язык. Справочные материалы: пособие для учащихся общеобразовательных организаций / М.Т. Баранов, Т.А. Костяева, А.В. Прудникова; под ред. Н.М. Шанского. – 13-е изд.- М.: Просвещение, 2014. — 285 с.
2. Введенская Л.А. Русский язык и культура: учебное пособие/ Л.А. Введенская, М.Н. Черкасова. = Изд. 14-е, стер. — Ростов н/Д.: Феникс, 2013. – 38, [1] c.
3. Голуб И.Б. Русский язык: справочник/ И.Б. Голуб. – М.: КНОРУС, 2014. — 190 с.
4. Греков В.Ф. Пособие для занятий по русскому языку в старших классах/ В.Ф. Греков, С.Е. Крючков, Л.А. Чешко. — М., Просвещение, любое издание.
5. Розенталь Д.Э. Русский язык. Сборник правил и упражнений/ Д.Э. Розенталь. – М.: ЭКСМО. 2014. – 432 с.
ПРОГРАММА ПО ИСТОРИИ
История с древности до конца XV в.
Народы и государства на территории нашей страны в древности.
Древние люди на территории нашей страны. Города-государства Северного Причерноморья. Кочевые скотоводческие племена. Тюркский и Хазарский каганаты.
Восточные славяне в VI-VIII вв.: расселение, занятия, быт, верования. Родоплеменные отношения. Взаимоотношения с соседями. Зарождение государственности: внутренние и внешние факторы. Города. Становление территориальных общин.
Формирование древнерусского государства в IX-X вв. Новгород и Киев. Норманнская теория. Древнерусские города. Ремесло. Торговля, Первые русские князья. Князь и дружина. Славяне, финно-угры и тюрки. Русь и Волжская Булгария. Византия и Русь. Владимир Святославович. Крещение Руси. «Повесть временных лет».
Русь в конце X — первой половине XII в. Формирование крупной земельной собственности. Категории свободного и зависимого населения. Специфика общинного строя. Древнерусские города, ремесла, торговля. Ярослав Мудрый. «Русская Правда». Княжеские усобицы. Владимир Мономах. Русь и государства Европы. Русь и Степь.
Культура и быт Древней Руси. Устное народное творчество, письменность, литература, художественное ремесло, зодчество. Повседневная жизнь и обычаи древних русичей.
Русь в XII — первой половине XV вв. Политическая раздробленность Руси. Причины раздробленности. Формирование политических центров и становление трех социокультурных моделей развития древнерусского общества и государства: Новгород Великий; Владимиро-Суздальское княжество; Галицко-Волынское княжество. Особенности развития хозяйства, политических институтов, культуры русских земель удельного периода. Последствия раздробленности.
Борьба Руси против агрессоров в XIII в. Нашествие Батыя, сопротивление завоевателям. Зависимость Руси от Орды, ее последствия. Обособление Юго-Западной Руси. Борьба Северо-Западной Руси против экспансии с Запада. Невская битва. Ледовое побоище. Александр Невский.
Русь в середине ХIII — XIV вв. Борьба за политическое лидерство на Руси. Княжеская власть и Орда. Московские князья и их политика. Иван Калита. Москва — центр объединения русских земель. Княжеская власть и церковь. Монастыри. Сергий Радонежский. Русь и Литва. Золотая Орда и XIII-XIV вв. Куликовская битва, ее значение. Дмитрий Донской. Особенности культурного развития, Феофан Грек. Андрей Рублев.
Московское государство во второй половине XV в. Иван III. Прекращение зависимости Руси от Орды. Завершение политического объединения русских земель. Иван III. Изменение системы управления государством. Боярская Дума. Приказы. Вотчинно-поместное землевладение и формы зависимости крестьян. Судебник 1497 г. Начало закрепощения крестьян.
Государство и церковь. Ереси. Московское государство и Великое княжество Литовское в XV — XVI вв. Тюрко-татарские ханства в XV-XVI вв.
Культура и быт Московского государства во второй половине XV в. Фольклор. Книжное дело. Летописание. Литература. Общественно-политическая мысль. Зодчество. Фрески и иконы. Повседневная жизнь.
История в XVI в.
Московское государство в XVI в. Сословно-представительная монархия. Иван IV. Реформы 50-х гг. XVI в. «Избранная рада». Земские соборы. Опричнина. Становление самодержавия.
Внешняя политика Ивана IV. Завоевание Поволжья и Западной Сибири. Отношения с Крымским ханством. Ливонская война. Народы России в XVI в. Итоги внешней политики Ивана Грозного.
Культура и быт в XVI в. Фольклор. Просвещение. Начало книгопечатания. Общественно-политическая мысль. Литература. Развитие публицистики. Зодчество. Иконопись, Дионисий. Быт. Обычаи. «Домострой».
Россия в XVII-XVIII вв.
Россия на рубеже XVI-XVII вв. Обострение социальных и политических противоречий. Династический кризис. Разрушение удельно-вотчинной системы. Борис Годунов. Смута. Феномен самозванства. Власть и казачество. Восстание Ивана Болотникова. Власть и земщина: противоборство и взаимодействие. Социальный и национальный факторы в Смуте.
Освободительная борьба против польских и шведских интервентов; ополчение Козьмы Минина и Дмитрия Пожарского. Начало правления династии Романовых.
Россия в XVII в. Политический строй. Начало становления элементов абсолютизма. Система приказов. Судьбы сословно-представительных институтов. Местное управление. Законы. Соборное уложение 1649 г.
Экономическое и социальное развитие. Формирование единого экономического пространства России. Рост товарно-денежных отношений. Ремесло. Развитие мелкотоварного производства. Возникновение мануфактур и наемного труда. Рост городов и торговли. Освоение Сибири и Дальнего Востока. Ярмарки. Окончательное закрепощение крестьянства.
Народы России в XVII в. Новые территории в составе России. Национальный состав населения страны. Государственный статус присоединенных территорий Поволжья, Украины, Сибири и Дальнего Востока. Хозяйство. Религия. Культура.
Самодержавие и церковь. Церковь после Смуты. Реформа патриарха Никона. Церковный раскол. Протопоп Аввакум. Усиление разногласий между церковной и царской властью.
Народные движения. Причины и особенности народных выступлений. Городские восстания. Восстание под предводительством Степана Разина. Выступления старообрядцев.
Внешняя политика. Россия и Речь Посполитая. Присоединение Левобережной Украины и Киева к России. Русско-турецкие отношения. Крымские походы. Русские первопроходцы в Сибири и на Дальнем Востоке.
Культура и быт в XVII в. Усиление светского характера культуры. Образование. Научные знания. Литература. Зодчество и живопись. Театр. Крупнейшие представители духовной и художественной культуры. Сословный быт. Обычаи и нравы.
Россия в первой половине XVIII в. Преобразования Петра I. Предпосылки преобразований. Реформы в экономике, административно-государственной сфере, армии. Утверждение абсолютизма. Формирование чиновничье-бюрократического аппарата. Оппозиция реформам. Экономическая и социальная политика. Значение преобразований.
Внешняя политика Петра I. Северная война (основные сражения, итоги). Петербург — новая столица. Прутский и Каспийский походы. Образование Российской империи. Россия и Европа в первой четверти XVIII в.
Изменения в культуре и быту. Наука. Становление системы образования. Создание Академии наук. Литература и искусство. Архитектура. Изменения в быту. Значение культурного наследия петровской эпохи.
Дворцовые перевороты. Причины и сущность дворцовых переворотов. Внутренняя политика. Расширение привилегий дворянства. Основные направления и итоги внешней политики.
Россия во второй половине XVIII в. Внутренняя политика Екатерины II. «Просвещенный абсолютизм». Проекты реформ. Уложенная комиссия. «Золотой век» российского дворянства. Жалованные грамоты дворянству и городам. Губернская (областная) реформа. Ужесточение внутренней политики. Борьба с вольнодумством. Н.И. Новиков. А.Н. Радищев.
Социально-экономическое развитие. Рост мануфактур и промыслов. Предпринимательство, торгово-промышленные компании. Начало разложения крепостнической системы. Социальная политика. Ужесточение крепостничества.
Народы Российской империи в XVIII в. Национальный состав населения. Национальная политика. Хозяйство. Религия. Культура. Обычаи и нравы.
Восстание под предводительством Емельяна Пугачева: причины, цели, состав участников, основные этапы, итоги, значение.
Внутренняя политика Павла I. Изменение порядка престолонаследия. Комиссия для составления законов Российской империи. Политика в отношении крестьянства. Дискуссии о личности и политике Павла I.
Внешняя политика. Основные направления. Русско-турецкие войны. Русское военное искусство. А.В.Суворов, Ф.Ф.Ушаков. Присоединение Крыма, Северного Причерноморья. Георгиевский трактат.
Участие России в разделах Речи Посполитой. Присоединение Правобережной Украины, Белоруссии, Литвы, части Латвии. Борьба с революционной Францией. Итоги и последствия внешней политики.
Культура и быт во второй половине XVIII в. Развитие системы образования. Становление отечественной науки. Академические экспедиции. М.В.Ломоносов. Русские просветители. Архитектура, скульптура, живопись, музыка: стили и направления. Крупнейшие деятели культуры, выдающиеся техники и изобретатели. Дворцы и усадьбы. Изменения в быту и обычаях дворянства, крестьян и горожан.
Россия в XIX в.
Россия в первой четверти XIX в. Внутренняя политика Александра I. «Негласный комитет». Реформа высших органов управления. М.М. Сперанский. Н.Н. Новосильцев. Польская конституция. Политическая реакция начала 20-х гг. Итоги внутренней политики.
Внешняя политика. Международное положение России и основные направления внешней политики в начале века. Русско-французские отношения. Тильзитский мир. Россия на Кавказе. Польский вопрос. Войны с Турцией, Ираном, Швецией. Присоединение Финляндии и Бессарабии.
Отечественная война 1812 г. Причины войны. Планы и силы сторон. Смоленское и Бородинское сражения. М.И.Кутузов. Партизанское движение. Итоги войны. Заграничный поход 1812-1814 гг. Роль России в европейской и мировой политике.
Социально-экономическое развитие. Указ о «вольных хлебопашцах». Отмена крепостного права в Прибалтике. Экономический кризис: 1812-1815 гг. Аграрный проект А.А. Аракчеева. Развитие промышленности и торговли.
Движение декабристов. Южное и Северное общества: участники, программы, цели, главные события, значение.
Россия во второй четверти XIX в. Внутренняя политика Николая I. Укрепление роли государственного аппарата. Централизация, бюрократизация государственного управления. Ужесточение контроля над обществом (полицейский надзор, цензура). Укрепление социальной базы самодержавия. «Свод законов» Российской империи. Усиление борьбы с революционными настроениями.
Социально-экономическое развитие. Противоречия хозяйственного развития. Начало промышленного переворота. Новые явления в промышленности и сельском хозяйстве. Реформа управления государственными крестьянами. Торговля. Города. Итоги социально-экономического развития.
Общественное движение 30-60-х гг. XIX в. Консерваторы. Либералы. Западники и славянофилы. Социалисты.
Народы России в первой половине XIX в. Национальные отношения. Польский вопрос. Польское восстание 1830-1831 гг. Национальная политика самодержавия.
Кавказская война. Народы Кавказа. Причины и основные этапы войны. Мюридизм. Имамат. Движение Шамиля. Итоги войны.
Внешняя политика. Россия в европейской и мировой политике второй четверти XIX в. Войны с Ираном и Турцией. Россия и Центральная Азия. Обострение Восточного вопроса. Крымская война (участники, их цели, основные сражения). Оборона Севастополя. П.С. Нахимов, В.А. Корнилов. Итоги войны.
Культура и быт в первой половине XIX в. Развитие системы образования, его сословный характер. Научные открытия. Русские первооткрыватели и путешественники. Основные стили в художественной культуре (романтизм, классицизм, реализм). Литература, «золотой век» русской поэзии. Становление русской национальной музыкальной школы. Театр. Музыка. Живопись. Архитектура. Быт и обычаи.
Россия во второй половине XIX в. Внутренняя политика Александра II. Реформы 60-70-х гг. XIX в. Предпосылки и проекты реформ. Александр II. Отмена крепостного права. Сохранение крепостнических пережитков в пореформенной деревне. Судебная, земская, городская, военные реформы. Д.А. Милютин. М.Т. Лорис-Меликов. Историческое значение и последствия реформ.
Общественное движение 60-70-х гг. XIX в. Консервативные, либеральные, радикальные течения в общественной мысли, их представители. Земский конституционализм. Революционное народничество: теория, организации, лидеры, тактика.
Внутренняя политика Александра III. Политика в крестьянском вопросе. Рабочее законодательство. Укрепление позиций дворянства. Национальная и религиозная политика. К.П. Победоносцев.
Социально-экономическое развитие в пореформенный период. Завершение промышленного переворота, его последствия. Сельское хозяйство. Промышленность. Железнодорожное строительство. Промышленный подъем. Развитие внутреннего рынка. Формирование буржуазии и пролетариата. Изменение положения дворянства. Расслоение крестьянства.
Начало индустриализации. Н.Х. Бунге. С.Ю. Витте. «Золотое десятилетие» русской промышленности. Итоги социально-экономического развития.
Общественное движение в 80-90-е гг. XIX в. «Модернизаторы» и традиционалисты. Кризис революционного народничества. Либеральное движение. Распространение марксизма в России. Консервативный лагерь.
Внешняя политика. Основные направления внешней политики. Европейская политика. Присоединение Средней Азии. Дальневосточная политика. Продажа Аляски. Русско-турецкая война 1877-1878 гг. Участие России в военных союзах. Итоги внешней политики в 60-90-х гг. XIX в.
Народы Российской империи во второй половине XIX в. Национальный вопрос и пути его решения при Александре II. Национальная политика Александра III. Положение народов Средней Азии.
Культура и быт во второй половине XIX в. Достижения российских ученых, их вклад в мировую науку и технику. Развитие образования. Расширение издательского дела. Демократизация культуры. Направления в литературе и искусстве. Реалистическое искусство (литература, театр, живопись). Художественные промыслы. Деятели российской культуры. Российские меценаты. Культурные достижения народов империи. Вклад российской культуры XIX в. в мировую культуру.
Рост населения. Изменение облика городов. Развитие связи и городского транспорта. Перемены в жизни и быте горожан и крестьян.
Россия в XX в.
Россия в начале XX в. (1900-1916 гг.). Социально-экономическое развитие в начале XX в. Продолжение индустриализации. Первые монополии. Экономический кризис и его последствия. Российские предприниматели. Роль иностранных капиталов. Специфика аграрного строя России. Помещичье землевладение. Община. Противоречия социально-экономического развития.
Внутренняя политика Николая II на рубеже веков. Самодержавная власть в начале века. Идеи народного представительства в общественном сознании и внутренней политике. В.К. Плеве. П.Д. Святополк-Мирский.
Внешняя политика России в конце XIX — начале XX вв. Русско-японская война. Инициативы России по всеобщему разоружению.
Дальневосточная политика. Русско-японская война: причины, основные сражения, результаты. Сближение России с Англией. Обострение русско-германских отношений. Нарастание угрозы мировой войны,
Общественное движение на рубеже веков. Идеи консерватизма, либерализма, социализма, национализма в общественной жизни. Генезис политических партий. Особенности российской многопартийности.
Революция 1905-1907 гг.: причины, характер, движущие силы, основные этапы и события. Манифест 17 октября 1905 г. Вооруженное восстание в Москве. Основные Законы Российской империи 1906 г. Думская монархия. Итоги революции.
Реформы П.А. Столыпина. Эволюция политической системы. Аграрная реформа: основные положения, ход реализации, итоги. Проекты реформ в области религиозной и национальной политики, местного самоуправления, системы образовании, улучшения быта рабочих. Политика в области кооперации. Промышленный подъем. Перестройка аграрных отношений.
Культура в начале XX в. Развитие естественных и общественных наук. Стили и течения в искусстве. «Серебряный рек» русской поэзии. Русский авангард. Меценаты. Российская культура начала XX в. — составная часть мировой культуры.
Россия в Первой мировой войне. Роль Восточного фронта в войне. Война и российское общество. Кризис режима.
Россия в 1917-1920 гг. Февральская революция. Причины, характер, движущие силы, особенности Февральской революции. Падение монархии. Двоевластие. Временное правительство, его внутренняя и внешняя политика. Советы.
Россия в феврале-октябре 1917 г. Основные политические партии (кадеты, эсеры, большевики, меньшевики) в 1917 г. Кризисы власти. Выступление генерала Л.Г. Корнилова.
Октябрьское восстание в Петрограде. II Всероссийский съезд Советов, его декреты. Создание правительства во главе с В.И. Лениным.
Установление советской власти в стране. Создание Советского государства. Экономическая и социальная политика новой власти. Национализация банков, промышленности, земли. Созыв и роспуск Учредительного собрания. Выход Советской России из мировой войны. Брестский мир. Утверждение однопартийной системы.
Гражданская война: сущность, предпосылки, участники, этапы, основные фронты. Красные и белые. «Военный коммунизм»: идеология, политика, экономика. Красный и белый террор. Положение крестьянства. «Зеленые». Интервенция. Национальный фактор в войне. Причины и цена победы большевиков в войне. Итоги войны. Последствия гражданской войны. Российская эмиграция.
Советская Россия. СССР в 1920-1930-е гг. Экономический и политический кризис начала 1920-х г.: истоки, сущность, последствия. Крестьянские восстания. Восстание в Кронштадте. Голод 1921 г.
НЭП: сущность, мероприятия, противоречия, итоги.
Образование СССР. Национальная политика в 1920-30-е гг. Дискуссии в партийном руководстве о принципах образования союзного государства. Политика выравнивания экономического и культурного уровня союзных республик. Этнические и социально-культурные изменения. Межнациональные отношения. Противоречия советской национальной политики.
Внешняя политика советского государства в 1920-е гг.: от концепции «мировой революции» к концепции построения социализма в отдельно взятой стране. Начало осознания национально-государственных интересов руководством страны. Прорыв международной изоляции
Политическая жизнь в 1920-1930-е гг. Обострение внутрипартийной борьбы. Смерть В.И. Ленина. Сосредоточение власти в руках И.В. Сталина. Формирование тоталитарной системы. Массовые репрессии. ГУЛАГ. Политические процессы 1930-х гг. Конституция 1936 г.
Социалистическая индустриализация: предпосылки, источники накопления, метод, темпы. Полное огосударствление промышленности. Пятилетние планы. Трудовой энтузиазм масс. Итоги и цена индустриализации.
Политика сплошной коллективизации сельского хозяйства, ее экономические и социальные последствия. Раскулачивание. Установление колхозного строя. Голод 1932-1933 гг.: причины и масштабы. Полное огосударствление экономики.
Политика в области культуры. Насаждение коммунистической идеологии. Ликвидация неграмотности. Развитие общего и профессионального образования. Положение науки, литературы, искусства: достижения, трудности, противоречия. Идеологические запреты. Выдающиеся деятели отечественной науки и культуры 1920-30-х гг.
Международные отношения и внешняя политика СССР в 1930-е гг. Вступление СССР в Лигу Наций, борьба за создание системы коллективной безопасности. Советско-германские договоры 1939 г., их последствия. Изменение внешнеполитического курса советского государства в 1939 г. Начало Второй мировой войны. Включение в состав СССР новых территорий в 1939-1940 гг. Советско-финская война, ее последствия.
Великая Отечественная война 1941-1945 гг. Периоды, основные фронты войны. Причины поражений в начальный период войны. Крупнейшие сражения, их значение (битва за Москву, Сталинградская битва, сражение на Курской дуге, Белорусская, Берлинская операции и др.) Национально-патриотический подъем. Массовый героизм на фронте и в тылу. Полководцы и герои войны. Г.К. Жуков. К.К. Рокоссовский. A.M. Василевский. И.С. Конев.
СССР и антигитлеровская коалиция.
Нацистский «новый порядок» на оккупированной территории, массовое уничтожение людей. Борьба в тылу врага; партизанское движение.
Советский тыл в годы войны. Военная экономика. Трудовой героизм народа.
Особенности национальной политики в годы войны. Депортация ряда народов.
Итоги и уроки Великой Отечественной войны. Величие и цена победы советского народа.
СССР с середины 1940-х до середины 1980-х гг. СССР в системе послевоенных международных отношений. «Холодная война», ее причины и последствия. Формирование военно-политических блоков. Биполярное мироустройство. Внешняя политика СССР в 1945- начале 1950 гг. СССР и мировое коммунистическое движение. Война в Корее и позиция советского руководства.
Послевоенное восстановление хозяйства. Потери СССР в войне. Экономические дискуссии. Восстановление и развитие промышленности. Трудности и проблемы сельского хозяйства. Жизнь и быт людей.
Политическое развитие СССР в 1945-1952 гг. Реорганизация властных структур. Идеологические кампании второй половины 1940-х гг. Новая волна репрессий. СССР в середине 1950-х — середине 1960-х гг. Борьба за власть после смерти И.В. Сталина.
XX съезд КПСС, его значение. «Оттепель», ее влияние на духовную атмосферу общества. Советская наука в эпоху научно-технической революции. Начало освоения космоса. Реформа образования. Противоречия культурной политики. Деятельность Н.С. Хрущева.
Внешняя политика СССР в середине 1950-х — середине 1960-х гг.; политика мирного сосуществования; отношения со странами «восточного» и «западного» блоков, «третьего мира». СССР и венгерские события 1956 г. Берлинский кризис 1961 г. Карибский кризис. Итоги внешней политики. СССР в середине 1960-х — середине 1980-х гг. Консервативный поворот во второй половине 1960-х гг. Л.И. Брежнев. Усиление партийно-государственной номенклатуры. Экономические реформы 1965 г.: содержание, реализация, причины свертывания. Нарастание кризисных явлений в экономике и социальной сфере, политике и идеологии. Достижения и проблемы науки. Судьбы научной и творческой интеллигенции. Движение диссидентов. Идеология и культура. Конституция 1977 г. Кризис тоталитарной системы.
Внешняя политика. Достижение военно-стратегического паритета с США, его цена. Поворот к разрядке напряженности в 1970-е гг. Хельсинкские соглашения. Ввод советских войск в Афганистан, его последствия.
СССР в середине 1980-х — начале 1990-х гг. Перестройка в СССР. М.С. Горбачев. Попытки обновления системы. Гласность. Возрождение многопартийности. Новый внешнеполитический курс. Вывод войск из Афганистана. Распад «восточного блока».
Кризисная ситуация в экономике. Обострение межнациональных противоречий. Провозглашение союзными республиками суверенитета.
Августовские события 1991 г. Роспуск КПСС. Распад СССР. Образование СНГ.
Россия в 1990-е гг. Становление суверенного российского государства. Б.Н. Ельцин. Начало перехода к рыночной экономике. Противоречия и социальные последствия реформ.
События октября 1993 г. Конституция 1993 г. Демонтаж системы власти Советов.
Национально-региональная политика. Федеративный Договор.
Отношения центра и регионов. Война в Чечне, ее последствия. Образование, наука и культура в условиях рынка.
Внешняя политика Российского государства. Россия и СНГ. Россия и мировое сообщество.
Литература:
- История России. Учебник / Под ред. Г.Б. Поляка. — М.: Юнити, 2018. — 128 c.
- Куксин, А.И. История России / А.И. Куксин. — М.: АСТ, 2018. — 317 c.
- Сафразьян, А. История России. Конспект лекций с иллюстрациями / А. Сафразьян. — М.: РГ-Пресс, 2019. — 112 c.
- Сахаров, А.Н. История России с древнейших времен до наших дней / А.Н. Сахаров. — М.: АСТ, 2018. — 64 c.
- Семин, В.П. История России: Учебник / В.П. Семин. — М.: КноРус, 2019. — 304 c.
- Сёмин, В.П. История России: конспект лекций / В.П. Сёмин. — М.: КноРус, 2019. — 304 c.
- Соловьев, С.М. История России с древнейших времен / С.М. Соловьев. — М.: АСТ, 2018. — 368 c.
ПРОГРАММА ПО ОБЩЕСТВОЗНАНИЮ
Общество
Общество как сложная динамическая система. Влияние человека на окружающую среду. Общество и природа. Правовая защита природы. Общество и культура. Причинные и функциональные связи в обществе. Взаимосвязь основных сфер общественной жизни. Важнейшие институты общества. Общественные отношения.
Объективные и субъективные факторы развития общества. Деятельность как способ существования общества. Ступени человеческой истории. Многообразие путей и форм общественного развития. Эволюция и революция. Революция и реформы. Возможность альтернативности общественного развития.
Культура и цивилизации. Типы цивилизации. Современные цивилизации. НТР и ее социальные последствия. Перспективы постиндустриальной цивилизации. Проблема общественного прогресса и его критериев. Противоречивость прогресса. Цена прогресса. Проблема смысла и направленности исторического процесса.
Человечество как социальная общность. Многообразие. Взаимосвязь и целостность современного мира. Противоречия современного общественного развития. Глобальные проблемы человечества. Стратегия выживания человечества в условиях обострения глобальных проблем.
Человек.
Человек как продукт биологической, социальной и культурной эволюции. Взаимоотношение духовного и телесного, биологического и социального начал в человеке. Сознание. Разум. Сознательное и бессознательное.
Бытие человека. Потребности человека: материальные и духовные, подлинные и мнимые. Способности человека. Человеческая деятельность. Ее многообразие. Творческая природа человека. Предназначение человека. Цель и смысл жизни человека. Объективное и субъективное содержание смысла жизни. Ценность жизни человека.
Основные социальные феномены жизни человека. Труд и трудовая деятельность. Игра в жизни человека. Общение и коммуникация. Многообразие видов общения. Функции общения.
Личность как субъект общественной жизни. Социализация и воспитание личности. Поведение. Самореализация личности. Саморегуляция. Свобода и ответственность личности.
Общая характеристика межличностных отношений. Конфликтные ситуации и способы их разрешения.
Духовный мир человека. Мировоззрение человека. Ценности. Основные типы жизненных стратегий в современном обществе: стратегии благополучия, успеха и самореализации. Проблема смерти в духовном опыте человечества.
Познание
Познание мира. Чувственное и рациональное познание. Интуиция. Истина и заблуждение. Критерии истины. Истина абсолютная и относительная.
Научное познание. Познание и творчество. Знание и вера. Формы и методы современного научного познания.
Особенности социального познания. Факты, теории, оценки. Науки, изучающие общество. Проблема социального прогнозирования.
Науки, изучающие человека, их система. Развитие взглядов на человека. Целостное постижение человека.
Многообразие путей познания и форм человеческого знания. Социальное и гуманитарное знание. Самопознание.
Духовная жизнь общества.
Культура и духовная жизнь. Духовная культура. Формы и разновидности культуры: народная, массовая, элитарная культуры. Средства массовой информации. Тенденции духовной жизни современной России. Особенности развития национальных культур в Российской Федерации.
Наука как часть культуры. Наука и общество. Наука как система, знаний и вид духовного производства. Особенности современной науки. Дифференциация и интеграция наук. Научная картина мира и ценностно-мировоззренческие формы знания. Возрастание роли науки в условиях НТР.
Сущность морали. Мораль как регулятор социального поведения. Категории морали. Высшие духовные ценности. Истина, добро и красота. Моральный идеал. Нравственная оценка деятельности. Моральный выбор.
Религия как феномен культуры. Функции религии. Религиозное сознание. Религиозный культ. Религиозные организации. Религия и мораль. Религия в современном мире. Свобода совести и вероисповеданий.
Искусство как вид духовного производства. Сущность искусства, его происхождение и основные формы. Искусство как эстетическая деятельность. Формы и основные направления искусства. Значение искусства для человека и человечества.
Образование в системе духовного производства. Цели и функции образования в современном мире. Основные элементы системы образования. Образование как ценность. Самообразование. Значение образования для самореализации.
Экономика.
Экономика: наука и хозяйство, теория и практика. Потребности и ресурсы: проблемы выбора. Роль экономики в жизни общества. Типы экономических систем, их отличительные признаки. Виды экономических отношений. Экономический цикл, его основные фазы. Экономический рост.
Экономическое содержание собственности. Формы и отношения собственности. Разгосударствление и приватизация. Частная собственность на землю и ее экономическое значение.
Экономическая деятельность. Общая характеристика сферы производства и сферы услуг. Производство: структура, факторы, виды. Измерители экономической деятельности. Экономика производителя. Предпринимательство: сущность, функции, виды.
Рынок как особый институт, организующий социально-экономическую систему общества. Многообразие рынков. Конкуренция. Спрос и предложение. Обмен. Специализация. России в условиях рыночных отношений.
Деньги, их функции. Банки, инфляция.
Государство и экономика. Экономические функции и задачи государства. Экономическая политика. Государственный бюджет. Государственный долг. Бюджетно-налоговое и денежно-кредитное регулирование экономики. Налоги, их виды и функции.
Мировая экономика. Россия в системе международных экономических отношений. Международное разделение труда и международная торговля. Экономическое сотрудничество и интеграция.
Экономика потребителя. Права потребителя, их защита. Уровень жизни. Прожиточный минимум. Рынок труда. Занятость и безработица.
Экономическая культура. Экономическая свобода и социальная ответственность. Культура производства и потребления. Нравственно-правовые основы экономических отношений.
Экономический интерес, экономическая свобода и социальная ответственность хозяйственного субъекта.
Социальные отношения.
Социальная структура общества, ее элементы. Социальные отношения и взаимодействия. Социальные изменения. Многообразие социальных групп. Неравенство и социальная стратификация. Личный и социальный статус. Социальные роли. Социальная мобильность. Социальные процессы в современной России.
Понятие о малой группе. Групповые нормы и санкции.
Социальные нормы. Элементы социального поведения. Отклоняющееся поведение. Социальный контроль и самоконтроль.
Этнические общности. Межнациональные отношения. Национализм. Межнациональные конфликты и пути их преодоления. Национальная политика.
Семья как социальный институт и малая группа. Тенденции развития семьи в современном обществе. Семейно-демографическая структура общества. Брак. Правовые основы семьи и брака. Правовой статус ребенка.
Молодежь как социальная группа. Молодежная субкультура. Проблемы молодежи в условиях социальных перемен. Молодежь как субъект социального развития.
Социальный конфликт и пути его разрешения. Экстремизм. Компромисс. Толерантность.
Социальное законодательство. Социальная политика.
Политика.
Политика, ее роль в жизни общества. Структура политической сферы.
Власть, ее происхождение и виды. Политический режим. Типы политических режимов: тоталитарный, авторитарный, демократический.
Политическая система общества. Государство, его признаки, формы, функции. Государственный аппарат. Избирательные системы. Политическая жизнь современной России.
Гражданское общество, его основные черты. Правовое государство, его сущность и основные принципы. Верховенство права. Местное самоуправление. Соотношение правового государства и гражданского общества.
Политическая идеология и ее структура. Функции политической идеологии. Различия и взаимодействие политической идеологии и политической психологии. Политическая идеология и политическая деятельность.
Политическая культура. Типы политической культуры. Функции политической культуры. Пути и формы политической социализации личности.
Право.
Право в системе социальных норм. Роль права в жизни человека, общества, государства. Система права: основные отрасли, институты, отношения. Источник права. Правовые акты. Публичное и частное право. Правоотношения. Правонарушения. Юридическая ответственность и ее виды. Правовая культура.
Международные документы по правам человека. Всеобщая декларация прав человека. Социально-экономические, политические и личные права и свободы. Система судебной защиты прав человека. Международное гуманитарное право.
Государственное право. Конституция в иерархии нормативных актов. Конституция Российской Федерации об основах конституционного строя. Закрепление в Конституции общепринятых международных стандартов прав человека.
Структура высшей государственной власти в Российской Федерации.
Федерация и ее субъекты.
Гражданин, гражданство и государство. Участие граждан в политике и управлении. Политические организации. Многопартийность. Правовая культура.
Основные признаки и значение юридической ответственности.
Признаки и виды правонарушений. IIроступок и преступление.
Административное право. Органы государственного управления. Административная ответственность.
Гражданское право. Право собственности юридических и физических лиц. Обязательства в гражданском праве. Трудовое право. Трудовой договор. Формы и виды оплаты труда. Заработная плата. Трудовая дисциплина. Трудовые споры и порядок их разрешения.
Уголовное право. Преступление и наказание в уголовном праве. Ответственность за преступления против личности. Уголовная ответственность за другие виды преступлений. Правоохранительные органы.
Литература:
- Обществознание: Учебное пособие / Под ред. Опалева А.В.. — М.: Юнити, 2018. — 478 c.
- Баранов, П.А. ЕГЭ. Обществознание. Новый полный справочник для подготовки к ЕГЭ / П.А. Баранов, А.В. Воронцов, С.С. Шевченко. — М.: АСТ, 2019. — 544 c.
- Баранов, П.А. Обществознание. Краткий справочник в таблицах и схемах для подготовки к ЕГЭ / П.А. Баранов. — М.: АСТ, 2019. — 288 c.
- Важенин, А.Г. Обществознание для профессий и специальностей технического, естественно-научного, гуманитарного профилей: Учебник / А.Г. Важенин. — М.: Academia, 2018. — 256 c.
- Важенин, А.Г. Обществознание для профессий и специальностей технического, естественно-научного, гуманитарного профилей. Контрольные задания / А.Г. Важенин. — М.: Academia, 2019. — 352 c.
- Касьянов, В.В. Обществознание в схемах и таблицах: готовимся к ЕГЭ / В.В. Касьянов. — РнД: Феникс, 2019. — 318 c.
- Касьянов, В.В. Обществознание: Учебное пособие / В.В. Касьянов. — Рн/Д: Феникс, 2019. — 128 c.
- Мушинский, В.О. Обществознание: Учебник / В.О. Мушинский. — М.: Форум, 2019. — 256 c.
Бериллий
| Бериллий | |
|---|---|
| Атомный номер | 4 |
| Внешний вид простого вещества |
мягкий металл серебристо-белого цвета |
| Свойства атома | |
|
Атомная масса (молярная масса) |
9,01218 а.е.м. (г/моль) |
| Радиус атома | 112 пм |
|
Энергия ионизации (первый электрон) |
898,8 (9,32) кДж/моль (эВ) |
| Электронная конфигурация | [He] 2s2 |
| Химические свойства | |
| Ковалентный радиус | 90 пм |
| Радиус иона | 35 (+2e) пм |
|
Электроотрицательность (по Полингу) |
1.57 |
| Электродный потенциал | −1,69 В |
| Степени окисления | 2; 1 |
| Термодинамические свойства простого вещества | |
| Плотность | 1,848 г/см³ |
| Молярная теплоёмкость | 16,44 Дж/(K·моль) |
| Теплопроводность | 201 Вт/(м·K) |
| Температура плавления | 1551 K |
| Теплота плавления | 12,21 кДж/моль |
| Температура кипения | 3243 K |
| Теплота испарения | 309 кДж/моль |
| Молярный объём | 5,0 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | гексагональная |
| Параметры решётки | a=2,286; c=3,584 Å |
| Отношение c/a | 1,567 |
| Температура Дебая | 1000 K |
| Be | 4 |
| 9,012182 | |
| [He]2s2 | |
| Бериллий | |
Бериллий химический элемент главной подгруппы второй группы, второго периода периодической системы химических элементов Д.И.Менделеева, с атомным номером 4. Обозначается символом Be (Beryllium). Простое вещество бериллий (CAS-номер: 7440-41-7)— мягкий высокотоксичный металл серого цвета, имеет весьма высокую стоимость.
История
Воклен, Луи НиколаОткрыт в 1798г. французским химиком Луи Никола Вокленом. Большую работу по установлению состава соединений бериллия и его минералов провёл русский химик И.В.Авдеев (1818—1865). Именно он доказал, что оксид бериллия имеет состав BeO, а не Be2O3, как считалось ранее.
Происхождение названия
Схема строения атома бериллияОпределение элемента бериллий произошло от названия минерала берилла (beryllos) (силикат бериллия и алюминия, Be3Al2Si6O18), которое восходит к названию города Белур (Веллуру) в Южной Индии, недалеко от Мадраса; с древних времён в Индии были известны месторождения изумрудов— разновидности берилла. Из-за сладкого вкуса растворимых в воде соединений бериллия элемент вначале называли «глюциний» (от греч. glykys— сладкий).
Нахождение в природе
Изотоп 8Be отсутствует в природе, поскольку является крайне нестабильным и имеет период полураспада 10−18 с. Стабильным является 9Be. Кроме 9Be в природе встречаются радиоактивные изотопы 7Be и 10Be.
Содержание бериллия в земной коре— около 3,5 г/т, обычно он встречается как примесь к различным минералам. Известно более 30 собственно бериллиевых минералов, но только 6 из них считаются более-менее распространёнными: берилл, хризоберилл, бертрандит, фенакит, гельвин, даналит. Промышленное значение имеет в основном берилл, в РФ (Республика Бурятия) разрабатывается фенакит-бертрандитовое Ермаковское месторождение.
Разновидности берилла считаются драгоценными камнями: аквамарин — голубой, зеленовато-голубой, голубовато-зеленый; изумруд— густо-зеленый, ярко-зеленый; гелиодор — желтый; известны ряд других разновидностей берилла, различающихся окраской (темно-синие, розовые, красные, бледно-голубые, бесцветные и др.). Цвет бериллу придают примеси различных элементов.
Физические свойства
Бериллий— мягкий, но не пластичный (легко разрушается) металл серебристо-белого цвета. Имеет высокий (в связи с чем ему ошибочно приписывается высокая твёрдость) модуль упругости— 300 ГПа (у сталей— 200—210 ГПа). На воздухе активно покрывается стойкой оксидной плёнкой BeO.
Модуль продольной упругости (модуль Юнга) 300 ГПа (312кгс/мм2). Механические свойства Бериллия зависят от чистоты металла, величины зерна и текстуры, определяемой характером обработки. Предел прочности Бериллия при растяжении 200—550 Мн/м2(20-55 кгс/мм2), удлинение 0,2-2%, что при таком высоком модуле упругости обеспечивает его хрупкость. Обработка давлением приводит к определенной ориентации кристаллов. Возникает анизотропия, становится возможным значительное улучшение свойств. Предел прочности в направлении вытяжки доходит до 400—800 Мн/м2(40-80 кгс/мм2), предел текучести 250—600 Мн/м2(25-60 кгс/мм2), а относительное удлинение до 4-12%. Механические свойства в направлении, перпендикулярном вытяжке, почти не меняются. Бериллий— хрупкий металл; его ударная вязкость 10-50 кДж/м2 (0,1-0,5 кгс·м/см2). Температура перехода Бериллия из хрупкого состояния в пластическое 200—400°C.
Химические свойства
Получение
В виде простого вещества в XIX веке бериллий получали действием калия на безводный хлорид бериллия:
В настоящее время бериллий получают, восстанавливая его фторид магнием:
,
либо электролизом расплава смеси хлоридов бериллия и натрия. Исходные соли бериллия выделяют при переработке бериллиевой руды.
Применение Бериллия
Легирование сплавов
Бериллий в основном используют как легирующую добавку к различным сплавам. Добавка бериллия значительно повышает твёрдость и прочность сплавов, коррозионную устойчивость поверхностей изготовленных из этих сплавов изделий. В технике довольно широко распространены бериллиевые бронзы типа BeB (пружинные контакты). Добавка 0,5% бериллия в сталь позволяет изготовить пружины, которые пружинят при красном калении.
Рентгенотехника
Бериллий слабо поглощает рентгеновское излучение, поэтому из него изготавливают окошки рентгеновских трубок (через которые излучение выходит наружу).
Ядерная энергетика
В атомных реакторах из бериллия изготовляют отражатели нейтронов, его используют как замедлитель нейтронов. В смесях с некоторыми α-радиоактивными нуклидами бериллий используют в ампульных нейтронных источниках, так как при взаимодействии ядер бериллия-9 и α-частиц возникают нейтроны: 9Ве + α → n + 12C. Оксид бериллия является наиболее теплопроводным из всех оксидов и служит высокотеплопроводным высокотемпературным изолятором, и огнеупорным материалом(тигли), а кроме того наряду с металлическим бериллием служит в атомной технике как более эффективный замедлитель и отражатель нейтронов чем чистый бериллий, кроме того оксид бериллия в смеси с окисью урана применяется в качестве очень эффективного ядерного топлива. Фторид бериллия в сплаве с фторидом лития применяется в качестве теплоносителя и растворителя солей урана, плутония, тория в высокотемпературных жидкосолевых атомных реакторах.
Фторид бериллия используется в атомной технике для варки стекла применяемого для регулирования небольших потоков нейтронов. Самый технологичный и качественный состав такого стекла -(BeF2−60%,PuF4−4%,AlF3−10%, MgF2−10%, CaF2−16%). Этот состав наглядно показывает один из примеров применения соединений плутония в качестве конструкционного материала (частичное).
Лазерные материалы
В лазерной технике находит применение алюминат бериллия для изготовления твердотельных излучателей (стержней, пластин).
Аэрокосмическая техника
В производстве тормозов для аэрокосмической техники, тепловых экранов и систем наведения с бериллием не может конкурировать практически ни один конструкционный материал. Конструкционные материалы на основе бериллия обладают одновременно и лёгкостью, и прочностью, и стойкостью к высоким температурам. Будучи в 1,5 раз легче алюминия, эти сплавы в то же время прочнее многих специальных сталей. Налажено производство бериллидов применяемых как конструкционные материалы для двигателей и обшивки ракет и самолетов, а так же в атомной технике.
Ракетное топливо
Теоретические характеристики топлив, образованных бериллием с различными окислителями
| Окислитель | Удельная тяга(Р1,сек) | Температура сгорания °С | Плотность топлива г/см³ | Прирост скорости, ΔVид,25, м/сек | Весовое содерж.горючего% |
|---|---|---|---|---|---|
| Фтор | 323,3 сек | 4328°C | 1,547 | 5014 м/сек | 13% |
| Тетрафторгидразин | 310,8 сек | 4234°C | 1,19 | 4204 м/сек | 11% |
| ClF3 | 277,4 сек | 4075°C | 1,85 | 4696 м/сек | 13% |
| ClF5 | 289,6 сек | 4176°C | 1,762 | 4791 м/сек | 13% |
| Перхлорилфторид | 242,6 сек | 3593°C | 1,709 | 3953 м/сек | 13% |
| Окись фтора | 308,6 сек | 4177°C | 1,561 | 4986 м/сек | 13% |
| Кислород | 235,4 сек | 3637°C | 1,21 | 3213 м/сек | 15% |
| Перекись водорода | 276,8 сек | 3472°C | 1,503 | 4231 м/сек | 18% |
| Азотная кислота | 256 сек | 2728°C | 1,574 | 4005 м/сек | 24% |
Стоит отметить высокую токсичность и высокую стоимость металлического бериллия, и в этой связи приложены значительные усилия для выявления бериллийсодержащих топлив имеющих значительно меньшую общую токсичность и стоимость. Одним из таких соединений бериллия является гидрид бериллия.
Теоретические характеристики топлив, образованных гидридом бериллия с различными окислителями
| Окислитель | Удельная тяга(Р1,сек) | Температура сгорания °С | Плотность топлива г/см³ | Прирост скорости, ΔVид,25, м/сек | Весовое содерж.горючего% |
|---|---|---|---|---|---|
| Фтор | 354,9 сек | 4244°C | 1,298 | 5029 м/сек | 13% |
| Тетрафторгидразин | 335,6 сек | 4133°C | 1,065 | 4270 м/сек | 10% |
| ClF3 | 298,8 сек | 3885°C | 1,573 | 4674 м/сек | 10% |
| ClF5 | 314,5 сек | 3979°C | 1,481 | 4773 м/сек | 11,25% |
| Перхлорилфторид | 309,5 сек | 2932°C | 1,114 | 4037 м/сек | 34% |
| Окись фтора | 342,9 сек | 3027°C | 1,054 | 4338 м/сек | 35% |
| Кислород | 331,4 сек | 3079°C | 0,867 | 3744 м/сек | 45% |
| Перекись водорода | 353,1 сек | 2932°C | 0,98 | 4285 м/сек | 41% |
| N2O4 | 316,1 сек | 2558°C | 0,93 | 3721 м/сек | 48% |
| Азотная кислота | 322,1 сек | 3085°C | 1,047 | 4060 м/сек | 35% |
Огнеупорные материалы
Оксид бериллия 99,9%(изделие)Оксид бериллия применяется в качестве очень важного огнеупорного материала в специальных случаях. Считается одним из лучших огнеупорных материалов и при этом это самый теплопроводный огнеупорный материал.
Биологическая роль и физиологическое действие
В живых организмах бериллий не несёт какой-либо значимой биологической функции. Однако бериллий может замещать магний в некоторых ферментах, что приводит к нарушению их работы. Нормальное содержание бериллия в организме взрослого человека (при массе тела 60 кг) составляет 0,031мг, ежедневное поступление с пищей— около 0,01мг.
Бериллий— ядовит: Летучие (и растворимые) соединения бериллия, в том числе и пыль, содержащая соединения бериллия, высокотоксичны. Для воздуха ПДК (предельно допустимые концентрации) вещества в пересчёте на бериллий составляет 0,001 мг/м³. Бериллий обладает ярко выраженным аллергическим и канцерогенным действием. Вдыхание атмосферного воздуха содержащего бериллий приводит к тяжёлому заболеванию органов дыхания — бериллиозу.
Дополнительная информация по Бериллию
Соединения бериллия
Бериллий, Beryllium, Be (4)
Содержащие бериллий минералы (драгоценные камни) — берилл, смарагд, изумруд, аквамарин и др.- известны с глубокой древности. Некоторые из них добывались на Синайском полуострове еще в XVII в. до н. э. В Стокгольмском папирусе (III в.) описываются способы изготовления поддельных камней. Название берилл встречается у греческих и латинских (Beryll) античных писателей и в древнерусских произведениях, например в «Изборнике Святослава» 1073 г., где берилл фигурирует под названием вируллион. Исследование химического состава драгоценных минералов этой группы началось, однако, лишь в конце XVIII в. с наступлением химико-аналитического периода.
Первые анализы (Клапрот, Биндгейм и др.) не обнаружили в берилле ничего особенного.
В конце XVIII в. известный минералог аббат Гаюи обратил внимание на полное сходство кристаллического строения берилла из Лиможа и смарагда из Перу. Вокелен произвел химический анализ обоих минералов (1797) и обнаружил в обоих новую землю, отличную от алюмины. Получив соли новой земли, он установил, что некоторые из них обладают сладким вкусом, почему и назвал новую землю глюцина (Glucina) от греческого — сладкий. Новый элемент, содержащийся в этой земле, был назван соответственно глюцинием (Glucinium). Это название употреблялось во Франции в XIX в., существовал даже символ — Gl.
Клапрот, будучи противником наменования новых элементов по случайным свойствам их соединений, предложил именовать глюциний бериллием (Beryllium), указав, что сладким вкусом обладают соединения и других элементов. Металлический бериллий был впервые получен Велером и Бусси в 1728 г. путем восстановления хлорида бериллия металлическим калием. Отметим здесь выдающиеся исследования русского химика И.В.Авдеева по атомному весу и составу окисла бериллия (1842). Авдеев установил атомный вес бериллия 9,26 (совр.9,0122), тогда как Берцелиус принимал его равным 13,5, и правильную формулу окисла.
О происхождении названия минерала берилл, от которого образовано слово бериллий, существует несколько версий. А. М. Васильев (по Диргарту) приводит следующее мнение филологов: латинское и греческое названия берилла могут быть сопоставлены с практритским veluriya и санскритским vaidurya. Последнее является названием некоторого камня и происходит от слова vidura (очень далеко), что, по-видимому, означает какую-то страну или гору. Мюллер предложил другое объяснение: Vaidurya произошло от первоначального vaidarya или vaidalya, а последнее от vidala (кошка). Иначе говоря, vaidurya означает приблизительно «кошачий глаз». Рай указывает, что в санскрите топаз, сапфир и коралл считались кошачьим глазом. Третье объяснение дает Липпман, который считает, что слово берилл обозначало какую-то северную страну (откуда поступали драгоценные камни) или народ. В другом месте Липпман отмечает, что Николай Кузанский писал, что немецкое Brille (очки) происходит от варварско-латинского berillus. Наконец, Лемери, объясняя слово берилл (Beryllus), указывает, что Berillus, или Verillus, означает «мужской камень».
В русской химической литературе начала XIX в. глюцина называлась — сладимая земля, сладозем (Севергин, 1815), сладкозем (Захаров, 1810), глуцина, глицина, основание глицинной земли, а элемент именовался глицинием, глицинитом, глицием, сладимцем и пр. Гизе предложил название бериллий (1814). Гесс, однако,придерживался названия глиций; его употреблял в качестве синонима и Менделеев (1-е изд. «Основ химии»).
Материалы для организации дистанционного обучения. Химия (8-9 классы)
| Класс | Название урока | Ссылка на учебные материалы |
| 8 | Предмет химии. Тела и вещества. Основные методы познания. Вводный инструктаж по технике безопасности | https://resh.edu.ru/subject/lesson/1521/main/ |
| 8 | Чистые вещества и смеси. Способы разделения смесей | https://resh.edu.ru/subject/lesson/1522/main/ |
| 8 | Физические и химические явления | https://resh.edu.ru/subject/lesson/1485/main/ |
| 8 | Атом. Молекула | https://resh.edu.ru/subject/lesson/1486/main/ |
| 8 | Химический элемент. Знаки химических элементов | https://resh.edu.ru/subject/lesson/1486/main/ |
| 8 | Простые и сложные вещества | https://resh.edu.ru/subject/lesson/1486/main/ |
| 8 | Валентность. Составление химических формул бинарных соединений | https://resh.edu.ru/subject/lesson/1520/main/ |
| 8 | Химические уравнения. Коэффициенты. Закон сохранения массы веществ | https://resh.edu.ru/subject/lesson/1519/main/ |
| 8 | Вычисления по химическим уравнениям количества и массы вещества по количеству вещества, массе реагентов или продуктов реакции | https://resh.edu.ru/subject/lesson/2448/main/ |
| 8 | Обобщение и систематизация знаний по теме «Первоначальные химические понятия» | https://resh.edu.ru/subject/lesson/2448/main/ |
| 8 | Кислород – химический элемент и простое вещество. Озон. Состав воздуха | https://resh.edu.ru/subject/lesson/2447/main/ |
| 8 | Физические и химические свойства кислорода | https://resh.edu.ru/subject/lesson/2447/main/ |
| 8 | Получение и применение кислорода | https://resh.edu.ru/subject/lesson/2447/main/ |
| 8 | Озон. Аллотропия кислорода. Состав воздуха. Горение | https://resh.edu.ru/subject/lesson/2446/main/ |
| 8 | Водород – химический элемент и простое вещество. Физические и химические свойства водорода | https://resh.edu.ru/subject/lesson/3119/main/ |
| 8 | Получение и применение водорода | https://resh.edu.ru/subject/lesson/3119/main/ |
| 8 | Объёмные отношения газов при химических реакциях | https://resh.edu.ru/subject/lesson/2731/main/ |
| 8 | Вода в природе. Круговорот воды в природе. Физические свойства воды | https://resh.edu.ru/subject/lesson/2062/main/ |
| 8 | Химические свойства воды. Взаимодействие с металлами | https://resh.edu.ru/subject/lesson/2062/main/ |
| 8 | Химические свойства воды. Взаимодействие воды с оксидами металлов | https://resh.edu.ru/subject/lesson/2062/main/ |
| 8 | Растворы. Растворимость веществ в воде. Массовая доля растворённого вещества в растворе | https://resh.edu.ru/subject/lesson/2062/main/ |
| 8 | Расчёт массовой доли растворённого вещества в растворе | https://resh.edu.ru/subject/lesson/2062/main/ |
| 8 | Оксиды. Классификация. Номенклатура | https://resh.edu.ru/subject/lesson/2445/main/ |
| 8 | Амфотерные оксиды и гидроксиды | https://resh.edu.ru/subject/lesson/2684/main/ |
| 8 | Физические и химические свойства оксидов | https://resh.edu.ru/subject/lesson/2444/main/ |
| 8 | Получение и применение оксидов | https://resh.edu.ru/subject/lesson/2444/main/ |
| 8 | Основания. Классификация. Номенклатура | https://resh.edu.ru/subject/lesson/2442/main/ |
| 8 | Получение и применение оснований | https://resh.edu.ru/subject/lesson/2442/main/ |
| 8 | Кислоты. Классификация. Номенклатура | https://resh.edu.ru/subject/lesson/2055/main/ |
| 8 | Физические и химические свойства кислот. Индикаторы. Изменение окраски индикаторов в различных средах | https://resh.edu.ru/subject/lesson/3120/main/ |
| 8 | Получение и применение кислот | https://resh.edu.ru/subject/lesson/3120/main/ |
| 8 | Соли. Классификация. Номенклатура. Получение и применение солей | https://resh.edu.ru/subject/lesson/2054/main/ |
| 8 | Физические и химические свойства солей | https://resh.edu.ru/subject/lesson/2441/main/ |
| 8 | Генетическая связь между классами неорганических соединений | https://resh.edu.ru/subject/lesson/2440/main/ |
| 8 | Строение атома: ядро, энергетический уровень |
https://resh.edu.ru/subject/lesson/2051/main/ https://mosobr.tv/release/7883 |
| 8 | Состав ядра атома: протоны, нейтроны. Изотопы | https://resh.edu.ru/subject/lesson/2051/main/ |
| 8 | Периодический закон Д. И. Менделеева. Периодическая система химических элементов Д. И. Менделеева | https://resh.edu.ru/subject/lesson/2050/main/ |
| 8 | Физический смысл атомного (порядкового) номера химического элемента, номера группы и периода периодической системы | https://resh.edu.ru/subject/lesson/2050/main/ |
| 8 | Закономерности изменения свойств атомов химических элементов и их соединений на основе положения в периодической системе Д. И. Менделеева и строения атома |
https://resh.edu.ru/subject/lesson/2049/main/ |
| 8 | Электроотрицательность атомов химических элементов | https://resh.edu.ru/subject/lesson/2439/main/ |
| 8 | Ковалентная химическая связь: неполярная и полярная. Ионная связь | https://resh.edu.ru/subject/lesson/2048/main/ |
| 8 | Металлическая связь. Понятие о водородной связи и её влиянии на физические свойства веществ на примере воды | https://resh.edu.ru/subject/lesson/2438/main/ |
| 8 | Валентность и степень окисления. Правила определения степеней окисления | https://resh.edu.ru/subject/lesson/3121/main/ |
| 8 | Окислительно-восстановительные реакции | https://resh.edu.ru/subject/lesson/3122/main/ |
| 8 | Повторение и обобщение по теме «Строение атома. Строение вещества. Химическая связь» | https://resh.edu.ru/subject/lesson/3093/main/ |
| 8 | Химические формулы. Индексы. Закон постоянства состава вещества | https://interneturok.ru/lesson/chemistry/8-klass/bpervonachalnye-himicheskie-predstavleniyab/himicheskaya-formula-veschestva?seconds=0 |
| 8 | Относительная атомная и молекулярная массы. Массовая доля химического элемента в соединении |
Относительная+атомная+и+молекулярная+массы |
| 8 | Вычисление массовой доли химического элемента по формуле соединения | Вычисление+массовой+доли+химического+элемента |
| 8 | Моль – единица количества вещества. Молярная масса | Моль+-+единица+количества+вещества.+Молярная+масса |
| 8 | Тепловой эффект химических реакций. Понятие об экзо- и эндотермических реакциях | Тепловой+эффект+химических+реакций.+Понятие+об +экзо-+и+эндотермических+реакциях |
| 8 | Физические и химические свойства оснований | Физические+и+химические+свойства+оснований |
| 9 | Окислительно-восстановительные реакции. Реакции соединения, разложения, замещения и обмена с точки зрения окисления и восстановления | https://resh.edu.ru/subject/lesson/2104/main/ |
| 9 | Тепловой эффект химических реакций. Понятие об экзо- и эндотермических реакциях | https://resh.edu.ru/subject/lesson/2437/main/ |
| 9 | Скорость химических реакций. Первоначальные представления о катализе | https://resh.edu.ru/subject/lesson/2102/main/ |
| 9 | Обратимые и необратимые реакции. Понятие о химическом равновесии | https://resh.edu.ru/subject/lesson/2103/main/ |
| 9 | Сущность процесса электролитической диссоциации. Диссоциация кислот, оснований и солей. Слабые и сильные электролиты. Степень диссоциации | https://resh.edu.ru/subject/lesson/1518/main/ |
| 9 | Реакции ионного обмена и условия их протекания | https://resh.edu.ru/subject/lesson/1603/main/ |
| 9 | Гидролиз солей | https://resh.edu.ru/subject/lesson/3123/main/ |
| 9 | Химические свойства основных классов неорганических соединений в свете представлений об электролитической диссоциации и окислительно-восстановительных реакциях | https://resh.edu.ru/subject/lesson/1606/main/ |
| 9 | Обобщение и систематизация знаний по теме «Химические реакции» | https://resh.edu.ru/subject/lesson/2101/main/ |
| 9 | Общая характеристика элементов VIIA группы. Галогены в природе. Физические свойства галогенов | https://resh.edu.ru/subject/lesson/2075/main/ |
| 9 | Химические свойства и применение галогенов | https://resh.edu.ru/subject/lesson/2075/main/ |
| 9 | Хлороводород. Соляная кислота и её соли | https://resh.edu.ru/subject/lesson/2075/main/ |
| 9 | Общая характеристика элементов VIA группы. Сера в природе. Физические и химические свойства серы | https://resh.edu.ru/subject/lesson/2434/main/ |
| 9 | Сероводород. Сульфиды | https://resh.edu.ru/subject/lesson/2434/main/ |
| 9 | Оксиды серы (IV). Сернистая кислота и её соли | https://resh.edu.ru/subject/lesson/2076/main/ |
| 9 | Оксиды серы (VI). Серная кислота и её соли | https://resh.edu.ru/subject/lesson/2077/main/ |
| 9 | Общая характеристика элементов VA группы. Азот в природе. Физические и химические свойства азота | https://resh.edu.ru/subject/lesson/2078/main/ |
| 9 | Аммиак: строение молекулы, физические и химические свойства | https://resh.edu.ru/subject/lesson/2078/main/ |
| 9 | Аммиак: химические свойства, получение, применение | https://resh.edu.ru/subject/lesson/2078/main/ |
| 9 | Соли аммония | https://resh.edu.ru/subject/lesson/2078/main/ |
| 9 | Азотная кислота и её соли | https://resh.edu.ru/subject/lesson/2078/main/ |
| 9 | Фосфор. Оксид фосфора (V) | https://resh.edu.ru/subject/lesson/2073/main/ |
| 9 | Фосфорная кислота и её соли | https://resh.edu.ru/subject/lesson/2073/main/ |
| 9 | Характеристика элементов IVA группы. Углерод и кремний в природе. Физические и химические свойства углерода. Аллотропия углерода | https://resh.edu.ru/subject/lesson/2072/main/ |
| 9 | Оксиды углерода | https://resh.edu.ru/subject/lesson/2071/main/ |
| 9 | Угольная кислота и её соли | https://resh.edu.ru/subject/lesson/2070/main/ |
| 9 | Кремний и его соединения | https://resh.edu.ru/subject/lesson/2069/main/ |
| 9 | Обобщение и систематизация знаний по теме «Неметаллы IV и V групп и их соединения» | https://resh.edu.ru/subject/lesson/2068/main/ |
| 9 | Положение металлов в Периодической системе химических элементов Д. И. Менделеева. Общие физические свойства металлов |
https://resh.edu.ru/subject/lesson/1607/main/ https://mosobr.tv/release/7942 |
| 9 | Общие химические свойства металлов |
https://resh.edu.ru/subject/lesson/1607/main/ https://mosobr.tv/release/7974 |
| 9 | Получение и применение металлов | https://resh.edu.ru/subject/lesson/1607/main/ |
| 9 | Положение щелочных и щелочноземельных металлов в Периодической таблице химических элементов Д. И. Менделеева и строение их атомов. Свойства | https://resh.edu.ru/subject/lesson/1602/main/ |
| 9 | Соединения щелочных и щелочноземельных металлов | https://resh.edu.ru/subject/lesson/3124/main/ |
| 9 | Положение алюминия в Периодической таблице химических элементов Д. И. Менделеева и строение атома. Физические и химические свойства алюминия | https://resh.edu.ru/subject/lesson/1604/main/ |
| 9 | Соединения алюминия | https://resh.edu.ru/subject/lesson/1604/main/ |
| 9 | Положение железа в Периодической таблице химических элементов Д. И. Менделеева и строение атома. Нахождение в природе. Физические и химические свойства железа | https://resh.edu.ru/subject/lesson/1605/main/ |
| 9 | Соединения железа и их свойства | https://resh.edu.ru/subject/lesson/1605/main/ |
| 9 | Получение и применение соединений железа | https://resh.edu.ru/subject/lesson/1605/main/ |
| 9 | Обобщение и систематизация знаний по теме «Металлы и их соединения» | https://resh.edu.ru/subject/lesson/2067/main/ |
| 9 | Углеводороды | https://resh.edu.ru/subject/lesson/1608/main/ |
| 9 | Спирты: метанол, этанол, глицерин | https://resh.edu.ru/subject/lesson/2066/main/ |
| 9 | Карбоновые кислоты: уксусная, стеариновая, олеиновая, аминоуксусная кислоты | https://resh.edu.ru/subject/lesson/2065/main/ |
| 9 | Биологически важные вещества: жиры, углеводы, белки | https://resh.edu.ru/subject/lesson/1609/main/ |
| 9 | Полимеры | https://resh.edu.ru/subject/lesson/2435/main/ |
| 9 | Обобщающий урок по теме «Важнейшие органические соединения» | https://resh.edu.ru/subject/lesson/2064/main/ |
| 9 | Степень окисления атомов и её определение в соединениях | Степень+окисления+атомов+и+её+определение+в+соединениях |
| 9 | Положение неметаллов в Периодической системе химических элементов Д. И. Менделеева | https://www.youtube.com/watch?v=ohFd4lJ9RcE&feature=emb_logo |
| 9 | Химические свойства металлов. Взаимодействие металлов с неметаллами | https://www.youtube.com/watch?v=qgzo40bfL1o |
| 9 | Оксиды азота | https://www.youtube.com/watch?time_continue=130&v=JmbTPhygCdk&feature=emb_logo |
| 9 | Общие химические свойства металлов | https://www.youtube.com/watch?time_continue=217&v=3O_1UupZ71E&feature=emb_logo |
| 9 | Получение и применение металлов | https://www.youtube.com/watch?time_continue=347&v=ZmgAo8Q3jFI&feature=emb_logo |
| 9 | Природные источники углеводородов: природный газ, нефть, уголь | https://www.youtube.com/watch?time_continue=206&v=O9e6ORyASjI&feature=emb_logo |
| 9 | Свойства металлов, неметаллов и их соединений. Генетическая связь между классами неорганических соединений | Свойства+металлов+неметаллов+и+их+соединений |
| 9 | Вычисления по химическим уравнениям количества, объёма, массы вещества по количеству, объёму, массе реагентов или продуктов реакции | https://www.youtube.com/watch?time_continue=8&v=nwIVA6XBq5w&feature=emb_logo |
Феромоны: секрет сексуальной привлекательности или заблуждение?
- Алекс Райли
- BBC Future
Автор фото, Getty
Действительно ли запах человека несет в себе феромоны, которые действуют как афродизиаки, привлекая потенциальных сексуальных партнеров? Обозреватель BBC Future решил выяснить всю правду.
В 2010 году несколько десятков человек собрались в арт-галерее в нью-йоркском Бруклине, чтобы понюхать грязные футболки.
Вечеринка фетишистов? Вовсе нет — собравшиеся лишь хотели проверить, можно ли использовать обоняние для завоевания симпатий противоположного пола.
Правила на «феромонной вечеринке» были простыми: человек открывал запечатанный пакет с номерком, где лежала футболка, которую другой участник успел поносить.
Если запах открывшему нравился, с владельцем футболки можно было организовать свидание.
Необычное мероприятие имело успех, и с тех пор подобные встречи уже проходили в Лос-Анджелесе и Лондоне. Как писал один журнал, это отличный вариант для тех, кто «ищет любовь, полагаясь на свой нюх и святую веру во всесилие науки».
Представление о том, что феромоны могут помочь человеку найти сексуального партнера и спутника жизни, прочно укоренилось в массовой культуре. Некоторые даже покупают духи, которые рекламируются как «приворотное зелье».
В некоторых таких духах содержится андростенон — самое мощное вещество из тех, которые призваны повышать сексуальное влечение.
Как заявляют продавцы, оно усиливает женское либидо, а мужчин делает более привлекательными.
Другое вещество — андростенол — как утверждается, облегчает переход к более близкому общению.
Если верить рекламе различных феромонов, они могут сделать человека более раскованным, подчеркнуть мужественность или помочь расслабиться во время сексуальной близости.
Что же думает по этому поводу наука? Могут ли феромоны сделать нас сексуальнее? Действительно ли любовь витает в воздухе — или же это просто банальный запах человеческого тела?
Автор фото, Getty
Подпись к фото,Термин «феромон» появился в 1959 году, когда ученых увлекло новое направление науки
Термин «феромон» появился в 1959 году, когда Петер Карлсон и Мартин Люшер из Института биохимии имени Макса Планка в Мюнхене предположили, что в облаке молекул, испускаемых животными, есть те, которые играют особую роль.
Эти вещества чем-то похожи на гормоны, однако они не циркулируют в крови, а выбрасываются наружу, чтобы влиять на поведение и физиологию других животных.
В отличие от обычных пахучих веществ, молекулы которых могут вызывать самую различную реакцию, механизм выделения феромонов развился в ходе эволюции для достижения вполне определенной цели при взаимодействии представителей одного вида.
В том же году был открыт первый феромон — бомбикол. Это вещество, которое выделяется самками тутового шелкопряда (Bombyx mori) и привлекает самцов на расстоянии многих километров.
Таким образом, бомбикол стал первым известным сексуальным феромоном — природным афродизиаком, переносимым по воздуху.
Бомбикол идеально подошел под определение феромона: во-первых, это простое вещество, состоящее всего из одной молекулы. Во-вторых, его действие узконаправленно — он действует только на один вид бабочек.
А в-третьих, он стабильно вызывает одну и ту же реакцию: самцы устремляются на источник этого вещества, даже когда поблизости нет ни одной самки.
Научную общественность охватил ажиотаж. Гормоны сразу были забыты как прошлый век, все бросились на изучение феромонов.
Вскоре после публикации пары сенсационных исследований один автор писал: «Последние 40 лет были поистине блестящим временем для эндокринологии; теперь же мы стоим на пороге расцвета экзокринологии».
Автор фото, Thinkstock
Подпись к фото,Рецепторы мышей могут улавливать целый ряд химических сигналов, людям же этого не дано
И расцвет действительно начался. Упоминания о феромонах все чаще стали встречаться на страницах научных журналов.
Оказалось, что все формы жизни, от микробов до мышей, используют эти химические регуляторы, чтобы изменять поведение своих соплеменников.
Феромонами пронизаны воздух, земля и Мировой океан. Некоторые из них даже передаются напрямую, от особи к особи, как персональные молекулярные сообщения.
Кроме того, сексуальные феромоны были лишь началом. Ученые стали находить молекулы со всё новыми функциями: от регулирования репродуктивных циклов потенциальных партнеров до участия в механизме памяти.
И вот в 1971 году исследователи феромонов добрались и до людей.
Сначала было сделано открытие, которым в наше время никого уже не удивишь: у женщин, долго находящихся в одном пространстве, синхронизируются менструальные циклы.
Эта закономерность была отмечена в знаменитом исследовании Марты Макклинток, опубликованном в журнале Nature, когда она была еще студенткой Колледжа Уэллсли в штате Массачусетс.
Макклинток обратила внимание на то, что у 135 девушек, живших в одном пригородном студенческом общежитии в течение полугода, менструальные циклы сдвигались в сторону синхронизации.
С тех пор на это исследование многократно ссылались как на доказательство существования человеческих феромонов, способных синхронизировать репродуктивный период у женщин.
«Всем, кто рассказывает подобные истории, хочется, чтобы это было правдой, — говорит Тристрам Уайатт из Оксфордского университета. — Но на поверку оказывается, что это, скорее всего, не так».
Многочисленные исследователи, пытавшиеся воспроизвести результаты Макклинток, так и не смогли этого сделать, и в какой-то момент один из ее научных сотрудников, внимательно изучив данные, пришел к выводу, что наблюдаемый феномен мог быть не более чем статистическим артефактом.
Автор фото, SPL
Подпись к фото,Обонятельные рецепторы в нашем носу отлично воспринимают запахи, но феромоны — совсем другое дело
Иными словами, к одному и тому же результату могла с равной вероятностью привести как химическая коммуникация, так и банальная случайность.
Длина и периодичность менструального цикла (5 дней из 28), а также его нерегулярность делают подобную синхронизацию весьма вероятной.
Однако в 70-е это предполагаемое открытие вскружило многим голову. Основываясь на исследовании Макклинток, британский врач Алекс Камфорт написал статью под названием «Вероятность обнаружения человеческих феромонов», где выразил уверенность в том, что до открытия феромонов homo sapiens осталось совсем немного.
В том же году в журнале New Scientist было опубликовано письмо Х. Кука, где автор рассказывал о том, что ему удалось обнаружить как минимум два феромона — в человеческом дыхании и поту.
Один, насколько автор мог судить, имел чесночный запах.
«Он содержится в воздухе, выдыхаемом женщиной, которая находится в состоянии полового возбуждения, и при этом не связан с поеданием чеснока», — уверял Кук.
Он также предположил, что этот феромон оказывает на мужчин возбуждающее действие, и именно поэтому женщины издревле добавляют чеснок в пищу.
«Второй человеческий феромон — это запах страха, который, безусловно, ощущают собаки», — продолжал автор, забыв о том, что феромоны по определению действуют в рамках одного вида.
Разумеется, такие заявления научным сообществом не принимались всерьез.
Однако были и другие, которые оставили более существенный след. Так, если попытаться проследить, откуда появилась современная идея о сексуальных феромонах человека, то наши поиски приведут нас на конференцию, которая состоялась в 1991 году в Париже.
Автор фото, Thinkstock
Подпись к фото,У нас мало фактов, которые могли бы подтвердить, что люди или их братья-приматы могут чувствовать наличие химических веществ в воздухе так же, как, например, мыши
В начале того же года биохимики Линда Бак и Ричард Эксел из Колумбийского университета в Нью-Йорке обнаружили у мышей группу рецепторов, отвечающих за обоняние, каждый из которых кодируется отдельным геном.
Было доказано, что рецепторы, расположенные в носу млекопитающего, связываются с определенными пахучими веществами, запуская каскад сигналов, идущих по нейронам в мозг.
В зависимости от объема и соотношения веществ возникают различные запахи — мозг в некотором смысле считывает обонятельный штрихкод.
«Тогда мы впервые увидели, как работает обоняние», — говорит Уайатт. В 2004 году Бак и Экселу за эту работу присудили Нобелевскую премию.
Вместе с тем на конференции 1991 года внимание публики привлекло еще одно исследование. Двое психиатров из Университета Юты заявили о том, что нашли у людей два сексуальных феромона.
«Они тогда наделали шуму, — вспоминает Ричард Доти, директор Центра исследования обоняния и вкуса при Пенсильванском университете в Филадельфии. — Хотя всем и показалось, что это довольно странная история».
Исследователи заявили, что у 49 добровольных участников эксперимента «предполагаемые человеческие феромоны» увеличивали интенсивность электрических сигналов между вомероназальным органом и головным мозгом.
У мышей, а также многих других млекопитающих, этот орган, который также называют «вторичным носом», улавливает ряд химических сигналов — независимо от первичной обонятельной системы.
Исследование 2000 года, автором которого была Марта Макклинток, подтвердило эти выводы, что и привело к росту популярности идеи о человеческих феромонах.
Автор фото, Getty
Подпись к фото,Запах, особенно знакомый, может привлекать, но к феромонам это не имеет никакого отношения
Тем не менее нет никаких доказательств того, что приматы, к которым относится и человек, умеют различать химические сигналы так же, как мыши.
У людей вомероназальный орган — это лишь рудимент, оставшийся от животных предков. Он состоит всего из нескольких пор внутри носовой полости, а нейронные связи между ним и мозгом у приматов почти отсутствуют.
«У людей ничего подобного нет», — говорит Джордж Прети из Центра исследования органов химического чувства в Филадельфии.
Но и сегодня на рынке можно найти все те же человеческие феромоны.
На самом деле некоторые исследователи, среди которых Ричард Доти, директор Центра исследований обоняния и вкуса в Филадельфии, считают, что феромоны не имеют существенного влияния ни на один из видов млекопитающих.
«Нет никаких фактов, подтверждающих наличие сигналов, которые воздействуют на поведение так, как нам хотелось бы думать», — говорит ученый.
Эта точка зрения была наиболее популярна в 1970-е годы, и Доти был одним из ее главных сторонников.
Млекопитающие, по мнению многих исследователей, слишком сложно организованы, чтобы такие простые молекулы могли влиять на их поведение.
Как писал один автор в 1976 году, «вероятно, не стоит извращать понятие феромона, столь полезное в исследовании поведения и физиологии насекомых, используя его для описания поведения млекопитающих».
Возьмем, к примеру, копулины — молекулы, обнаруженные в конце 1960-х у лабораторных макак-резусов.
Копулины, представляющие собой вагинальный секрет самок, вызывают сексуальное возбуждение, позывы к мастурбации и активное сексуальное поведение у самцов.
Автор фото, Thinkstock
Подпись к фото,Проверить действие феромонов можно только на новорожденных младенцах
Тем не менее они не являются феромонами. Самцы, принимавшие участие в исследовании, уже встречали тех самок раньше и возбуждались, поскольку узнавали их по характерному запаху.
Таким образом, копулин представляет собой скорее ароматическое вещество, чем феромон. И действительно, его часто используют в производстве духов.
И таких примеров много, отмечает Доти, — многие исследования страдают от такой неточности в терминологии.
«Феромоном называют все что угодно — это слово уже давно перестало быть научным термином», — констатирует ученый.
Значительная часть так называемых феромонов содержит множество химических веществ, поэтому не удовлетворяют критерию простоты.
Некоторые из них «работают» лишь на отдельных испытуемых и не оказывают никакого эффекта на других.
И так же, как в случае с копулинами, их действие в основном объясняется наличием предыдущего опыта общения особей и распознаванием знакомого запаха.
Несколько лет назад Джейн Херст из Ливерпульского университета была согласна с Доти: млекопитающие и тем более люди слишком сложны, чтобы феромоны могли сыграть в их жизни сколько-нибудь значимую роль.
Однако в 2010 году она обнаружила новый вид белка — дарцин, который содержится в моче самцов мышей.
Этот белок, названный в честь любимца всех женщин мистера Дарси из романа «Гордость и предубеждение», не только привлекает самок, но и выступает в качестве стимулятора памяти, помогая им запомнить специфический запах самца и место встречи с ним.
Таким образом, белок функционирует и как аттрактант (вещество, привлекающее противоположный пол), и как усилитель памяти.
Интересно, что без дарцина — одного-единственного вида сигнального белка — самка перестает испытывать интерес к противоположному полу и не помнит предыдущих отношений.
«Я изменила свое мнение, — говорит Херст, ранее решительно опровергавшая идею существования феромонов у человека. — Есть определенные химические вещества, которые имеют право называться феромонами».
Для того чтобы выделить дарцин, Херст и ее коллегам пришлось вернуться к истокам. Они выделили активное вещество из мочи при помощи метода, взятого из первоначального исследования бомбикола 1959 года.
Выделенный феромон испытали на мышах. Оказалось, что чистый дарцин вызывает у животных ту же реакцию, что и моча.
Для того чтобы исключить фактор знакомого запаха, самок растили отдельно от самцов — они не видели, не слышали и не чувствовали запах самца ни разу в жизни.
В таких условиях реакция может быть только врожденной — обусловленной генами и нормальным развитием, а не опытом, полученным в течение жизни.
Вопрос в том, можем ли мы сделать то же самое с людьми? Ответ ученых: маловероятно.
«У людей практически невозможно проверить действие феромонов изолированно», — объясняет Херст.
Многолетний опыт общения с противоположным полом, личные предпочтения и отсутствие рефлекторных реакций — это помехи, влияние которых неизбежно исказит результаты исследования, как бы тщательно оно ни было организовано.
Поведение человека определяется столь огромным количеством внешних факторов, что однозначных выводов из эксперимента сделать будет нельзя.
Тем не менее это, возможно, не касается новорожденных. «С детьми работать гораздо проще, чем со взрослыми, — они еще не накопили опыта и не подверглись воздействию культуры», — говорит Уайатт.
Исследование, проведенное в 2009 году, указало возможный путь вперед.
При грудном вскармливании железы возле соска матери набухают и выделяют вместе с молоком дополнительный секрет.
Когда сосок оказывается возле лица младенца, это неизменно вызывает стереотипное поведение: дети открывают рот, высовывают язык и начинают сосать. Они так пытаются получить питание.
Важным фактом оказалось то, что секрет, взятый у других матерей, вызывает у детей точно такую же рефлекторную реакцию.
Следовательно, можно исключить вероятность того, что дети просто опознавали запах своей матери.
Как говорит Тристрам Уайатт, ученые надеются найти первый человеческий феромон именно при помощи этого ареолярного секрета.
Если искомое вещество удастся выделить и синтезировать в лаборатории, оно сможет помочь детям, имеющим проблемы с захватом груди — одной из основных причин детской смертности во многих развивающихся странах.
В сельских районах Ганы, например, по имеющимся оценкам, один час задержки в кормлении грудью после рождения является причиной 22% детской смертности.
Это также способствовало бы изучению феромонов в целом.
«Если мы обнаружим феромон молочных желез, то с большей уверенностью сможем вести поиск и других феромонов, способных воздействовать уже на взрослый организм», — отмечает Уайатт.
«Хотя в конечном итоге мы можем прийти к выводу, что человеческих феромонов не существует: ведь ни одна молекула такого рода до сих пор не найдена».
Получается, единственное, что можно с уверенностью сказать на данный момент, — это то, что у людей есть запах…
3.5: Чистые вещества и смеси
Учебная цель
- Различают чистые вещества и смеси
- Определять смеси как однородные или неоднородные
Чистые вещества
Когда мы говорим о чистой субстанции , мы говорим о чем-то, что содержит только один вид материи. Это может быть один-единственный элемент или одно-единственное соединение, но каждый образец этого вещества, который вы исследуете, должен содержать в точности одно и то же с фиксированным, определенным набором свойств.
| Чистое вещество | Элемент или соединение? | Состоит из: |
|---|---|---|
| Свинец (Pb) | элемент | атома свинца |
| Газообразный кислород (O 2 ) | элемент | молекулы кислорода * |
| Вода (H 2 O) | соединение | молекулы воды |
| Аммиак (NH 3 ) | соединение | молекулы аммиака |
* Примечание: чистый газообразный кислород состоит из молекул, но по-прежнему считается элементом, а не соединением, поскольку молекулы состоят из элементов одного типа.Соединения состоят из одного или нескольких элементов.
Смеси
Если мы берем два или более чистых вещества и смешиваем их вместе, мы называем это смесью . Смеси всегда можно снова разделить на составляющие чистые вещества, потому что связывание между атомами составляющих веществ не происходит в смеси. В то время как соединение может иметь свойства, сильно отличающиеся от свойств составляющих его элементов, в смесях вещества сохраняют свои индивидуальные свойства.Например, натрий — мягкий блестящий металл, а хлор — едкий зеленый газ. Эти два элемента могут объединяться с образованием соединения, хлорида натрия (поваренная соль), которое представляет собой белое кристаллическое твердое вещество, не обладающее свойствами натрия или хлора , ни . Если, однако, вы смешали поваренную соль с молотым перцем, вы все равно могли бы видеть отдельные зерна каждого из них, и, если бы вы были терпеливы, вы могли бы взять пинцет и осторожно разделить их обратно на чистую соль и чистый перец. .
Гетерогенная смесь
Гетерогенная смесь представляет собой смесь, состав которой неоднороден по всей смеси. Овощной суп — это неоднородная смесь. Любая данная ложка супа будет содержать различное количество различных овощей и других компонентов супа.
Гомогенная смесь / раствор
Гомогенная смесь представляет собой комбинацию двух или более веществ, которые настолько тщательно перемешаны, что смесь ведет себя как единое вещество.Еще одно слово для обозначения однородной смеси — раствор. Таким образом, комбинация соли и стальной ваты представляет собой гетерогенную смесь, поскольку легко увидеть, какие частицы вещества являются кристаллами соли, а какие — стальной ватой. С другой стороны, если вы возьмете кристаллы соли и растворите их в воде, очень трудно определить наличие более одного вещества, просто взглянув, даже если вы используете мощный микроскоп. Соль, растворенная в воде, представляет собой гомогенную смесь или раствор (Рисунок \ (\ PageIndex {3} \)).
Рисунок \ (\ PageIndex {3} \): Типы смесей © Thinkstock Слева комбинация двух веществ представляет собой гетерогенную смесь, поскольку частицы двух компонентов выглядят по-разному. Справа кристаллы соли растворились в воде настолько тонко, что вы не можете сказать, присутствует ли соль. Гомогенная смесь выглядит как единое вещество.
Пример \ (\ PageIndex {3} \)
Определите следующие комбинации как гетерогенные смеси или гомогенные смеси.
- газированная вода (углекислый газ растворен в воде.)
- смесь металлической стружки железа и порошка серы (и железо, и сера являются элементами.)
Рисунок \ (\ PageIndex {4} \): Смесь железной стружки и порошка серы ( Asoult, смесь Fe-S 03, CC BY 4.0)
Решение
- Поскольку диоксид углерода растворен в воде, мы можем сделать вывод из поведения кристаллов соли, растворенных в воде, что диоксид углерода, растворенный в воде, является (также) гомогенной смесью.
- Если предположить, что железо и сера просто смешаны вместе, должно быть легко увидеть, что такое железо, а что такое сера, так что это гетерогенная смесь.
Упражнение \ (\ PageIndex {3} \)
Являются ли следующие комбинации гомогенными смесями или гетерогенными смесями?
- человеческое тело
- амальгама, комбинация некоторых других металлов, растворенных в небольшом количестве ртути
Ответы
- гетерогенная смесь
- однородная смесь
Классификация материалов
Рисунок \ (\ PageIndex {1} \): Взаимосвязь между типами веществ и методами, используемыми для разделения смесейОбычная поваренная соль называется хлоридом натрия.Его считают веществом , потому что оно имеет однородный и определенный состав. Все образцы хлорида натрия химически идентичны. Вода также является чистым веществом. Соль легко растворяется в воде, но соленую воду нельзя классифицировать как вещество, поскольку ее состав может варьироваться. Вы можете растворить небольшое или большое количество соли в определенном количестве воды. Смесь представляет собой физическую смесь двух или более компонентов, каждый из которых сохраняет свою индивидуальность и свойства в смеси .Меняется только форма соли, когда она растворяется в воде. Он сохраняет свой состав и свойства.
Этап
Фаза — это любая часть образца, имеющая однородный состав и свойства. По определению, чистое вещество или гомогенная смесь состоит из одной фазы. Гетерогенная смесь состоит из двух или более фаз. Когда масло и вода смешиваются, они не смешиваются равномерно, а образуют два отдельных слоя. Каждый из слоев называется фазой.
Пример \ (\ PageIndex {1} \)
Определите каждое вещество как соединение, элемент, гетерогенную смесь или гомогенную смесь (раствор).
- фильтрованный чай
- свежевыжатый апельсиновый сок
- компакт-диск
- оксид алюминия, белый порошок с соотношением атомов алюминия и кислорода 2: 3
- селен
Дано : химическое вещество
Запрошено : его классификация
Стратегия:
- Определите, является ли вещество химически чистым.Если оно чистое, это либо элемент, либо соединение. Если вещество можно разделить на элементы, это соединение.
- Если вещество не является химически чистым, это либо гетерогенная смесь, либо гомогенная смесь. Если его состав однороден во всем, это однородная смесь.
Решение:
- A) Чай представляет собой раствор соединений в воде, поэтому он не является химически чистым. Обычно его отделяют от чайных листьев фильтрацией.
B) Поскольку состав раствора однороден повсюду, это однородная смесь . - A) Апельсиновый сок содержит твердые частицы (мякоть), а также жидкость; он не является химически чистым.
B) Поскольку его состав неоднороден, апельсиновый сок представляет собой гетерогенную смесь . - A) Компакт-диск — это твердый материал, содержащий более одного элемента, с видимыми по краю участками разного состава.Следовательно, компакт-диск не является химически чистым.
B) Области разного состава указывают на то, что компакт-диск представляет собой гетерогенную смесь. - A) Оксид алюминия представляет собой единое химически чистое соединение .
- A) Селен — один из известных элементов .
Упражнение \ (\ PageIndex {1} \)
Определите каждое вещество как соединение, элемент, гетерогенную смесь или гомогенную смесь (раствор).
- белое вино
- ртуть
- заправка для салата в стиле ранчо
- сахар столовый (сахароза)
- Ответ:
- гомогенная смесь (раствор)
- Ответ b:
- элемент
- Ответ c:
- гетерогенная смесь
- Ответ d:
- соединение
Пример \ (\ PageIndex {2} \)
Как химик классифицирует каждый образец вещества?
- соленая вода
- почва
- вода
- кислород
РЕШЕНИЕ
- Соленая вода действует как единое целое, даже если содержит два вещества — соль и воду.Морская вода — это однородная смесь или раствор.
- Почва состоит из маленьких кусочков различных материалов, поэтому представляет собой неоднородную смесь.
- Вода — это вещество; более конкретно, поскольку вода состоит из водорода и кислорода, она представляет собой соединение.
- Кислород, вещество, это элемент.
Упражнение \ (\ PageIndex {2} \)
Как химик классифицирует каждый образец вещества?
- кофе
- водород
- яйцо
- Ответ:
- однородная смесь (раствор), предположим, это фильтрованный кофе
- Ответ b:
- элемент
- Ответ c:
- смесь гетерогенная.
- Чистые вещества состоят из одного элемента или соединений.
- Комбинации различных веществ называются смесями.
- Гомогенные смеси — это смеси двух или более соединений (или элементов), которые не отличаются друг от друга визуально.
- Гетерогенные смеси — это смеси двух или более соединений (или элементов), которые визуально отличимы друг от друга.
- обычных веществ, таких как воздух, вода, дерево и ткань, представляют собой смеси материалов и могут быть химически или физически разложены на более простые вещества.
- чистое или элементарное вещество не может быть разбито на более мелкие или простые составляющие без потери всех своих первоначальных свойств; такие чистые вещества называются элементами .
- Каждый элемент состоит из идентичных частиц материи, называемых атомами .
- все атомы в чистом веществе или элементе идентичны друг другу, но отличаются от атомов в другом элементе.
- 92 природных элемента и еще 13 созданы в лаборатории.
- Уникальные химические свойства всего нескольких атомов определяют форму и функции всего живого.
- Физические и химические свойства всех элементов являются результатом возникновения субструктуры их атомов.
- протоны представляют собой небольшие положительно заряженные частицы с массой, по определению, равной одной единице (одна а.е.м.).
- нейтроны — нейтральные частицы без электрического заряда, также с массой, равной одной единице (одна а.е.м.).
- электронов очень маленькие отрицательно заряжают частицу с очень малой массой, которой можно пренебречь.
- протонов всегда находятся в атомном центре.
- нейтронов всегда находятся в атомном центре.
- электронов всегда находятся в быстро движущихся диффузных облаках или орбиталях определенного объема и формы на разных расстояниях от центра атома.
- в сбалансированном нейтральном атоме количество протонов всегда равно количеству электронов.
- большая часть атома — это пустое пространство.
- сумма масс всех протонов и нейтронов в атоме называется атомной массой .
- число протонов в атоме называется атомным номером
- масса или вес атома зависит от количества протонов и нейтронов, которые он содержит.
- атомов элементов, содержащих больше протонов и нейтронов, имеют большую общую массу.
- некоторые элементы имеют диапазон или ряд атомных масс, в которых число протонов всегда постоянно, но число нейтронов меняется.
- некоторые из этих устройств нестабильны, и атомы самопроизвольно взрываются и испускают излучение; это радиоактивных форм элемента.
- водород — элемент с тремя изотопами.
- самая распространенная форма водорода (записанная в химической нотации как H ) имеет единственный протон в центре и не имеет нейтронов.
- другая форма водорода, называемая дейтерий, состоит из одного протона и одного нейтрона.
- третья форма водорода, называемая тритием, имеет один протон и два нейтрона.
- атомная субструктура трития нестабильна и радиоактивна.
- баланс всех сил содержания энергии и зарядов определяет объем или форму пространства, которое электрон может занимать вокруг атомного центра атома.
- электронов находятся в зонах, называемых энергетическими уровнями , на увеличивающихся расстояниях от атомного центра.
- ближайший к центру атома энергетический уровень является самым маленьким и самым низким по энергии. Электроны с низкой энергией занимают этот уровень.
- следующий энергетический уровень по большей части находится дальше от атомного центра. Электроны на этом уровне энергии содержат больше энергии, чем на первом.
- только два электрона могут занимать первый энергетический уровень одновременно.
- максимум восемь электронов могут занимать второй энергетический уровень одновременно.
- только максимум два электрона могут находиться на любой орбитали или занимать ее одновременно.
- самый низкий энергетический уровень имеет только одну орбиталь в форме сферы, называемую орбиталью 1s .
- два электрона — максимальное количество, обнаруживаемое в любой момент времени на этой орбитали.
- второй энергетический уровень имеет четыре орбитали.
- Орбиталь 2s имеет форму сферы и удерживает максимум два электрона.
- есть три 2p-орбитали, которые имеют форму гантели и снова содержат максимум два электрона каждая.
- , имеющий только один электрон на первом уровне энергии, является химически реактивным.
- гелий с двумя электронами на первом уровне энергии инертен и имеет незначительные химические или реактивные свойства или не имеет их вообще (первый энергетический уровень не полон).
- Натрий имеет один электрон на внешнем уровне энергии, он очень реактивен.
- Хлор имеет семь электронов на внешнем энергетическом уровне, он тоже очень реактивен.
- Химические свойства элемента очень сильно зависят от количества электронов, которые атомы этого элемента имеют на своем внешнем энергетическом уровне.
- атом водорода может отдать свой один электрон со своего первого энергетического уровня.
- этот энергетический уровень теперь свободен от электронов, и полученная атомная форма более стабильна.
- оставшаяся атомная частица теперь состоит из одного протона с положительным зарядом, который больше не нейтрализуется электроном.
- эта атомная частица теперь называется ионом .
- атомов элемента хлора имеют семь электронов на внешнем энергетическом уровне.
- эти атомы хлора легко принимают пожертвованные электроны, чтобы заполнить этот энергетический уровень.
- новая атомная частица теперь имеет дополнительный отрицательно заряженный электрон, который не нейтрализуется протоном в атомном центре, но это более стабильное атомное расположение.
- эта атомная частица теперь является отрицательно заряженным ионом хлорида.
- ионизация — это термин, используемый для такого обмена электронами и образования положительно или отрицательно заряженных атомных частиц.
- , когда два атома водорода приближаются друг к другу, их положительно заряженные центры притягиваются к отрицательно заряженным электронным облакам, окружающим противоположный атом.
- на определенном расстоянии друг от друга два крайних энергетических уровня (и орбитали) сливаются вместе и образуют единую сложную молекулярную орбиталь .
- эта новая орбиталь теперь содержит два электрона, по одному от каждого атома в рамках общих отношений.
- эта новая компоновка более устойчива, чем исходная.
- требуется энергия, чтобы разделить эти атомы, поэтому атомы остаются вместе, как если бы они были связаны энергетическим клеем .
- эти силы, удерживающие атомы вместе, называются ковалентными связями .
- одинарная ковалентная связь удерживает два атома вместе, в то время как они разделяют два электрона.
- имеет только четыре электрона на внешнем энергетическом уровне. Углерод
- может разделять эти четыре электрона и получать четыре электрона от других атомов, образуя, таким образом, четыре ковалентные связи.
- водород имеет только один электрон на внешнем энергетическом уровне.
- водород может разделять этот электрон, образуя одну ковалентную связь.
- один атом углерода и четыре атома водорода могут объединяться.
- каждый атом водорода имеет два общих электрона (один от атома водорода, один от атома углерода) с атомом углерода, образуя ковалентную связь.
- полученная молекула имеет один атом углерода в центре и четыре атома водорода, прикрепленных к нему четырьмя ковалентными связями.
- это молекула под названием метан .
- молекул, состоящих из углерода и водорода, скрепленных ковалентными связями, часто называют органическими молекулами , потому что они впервые были обнаружены в живых организмах.
- является электроотрицательным элементом .
- электронов плотно прижаты к атому кислорода.
- в схеме совместного использования между атомом кислорода и атомом водорода (ковалентная связь) электроны проводят больше времени рядом с атомом кислорода или вокруг него, чем атом водорода.
- атом кислорода приобретает небольшой отрицательный заряд (из-за наличия дополнительных электронов).
- атомы водорода развивают небольшой положительный заряд (от оставшегося протона, который не полностью нейтрализуется отсутствующими электронами).
- молекула воды, следовательно, имеет небольшое, очень слабое распределение электрического заряда; положительный по атомам водорода и отрицательный по атому кислорода.
- вода — это полярная молекула .
- вода — это небольшая молекула, меньшая, чем молекулярный кислород.
- кислород — это газ при комнатной температуре, а вода — жидкость.
- Вода полярна, с небольшими положительными и отрицательными зарядами на водородном и кислородном компонентах молекулы.
- положительный заряд одной молекулы воды притягивает отрицательный заряд соседней молекулы воды, и они ненадолго удерживаются вместе.
- эта крошечная сила притяжения называется водородной связью .
- миллиардов и миллиардов водородных связей образуются и разрываются между молекулами воды каждую секунду.
- сумма всех этих притяжений удерживает молекулы воды ближе друг к другу, чем они не образовывались.
- состояние вещества, занимаемого совокупностью молекул воды, — это состояние жидкости, а не газа.
- нагревание молекул воды вызывает увеличение кинетической энергии, большее движение и разрыв водородных связей.
- при достаточно высоких температурах вода превращается в газ (пар).
- вода может растворять больше веществ, чем любой другой растворитель.
- a растворенное вещество — растворенное вещество.
- Степень растворения растворенного вещества в воде зависит от природы и распределения электрических зарядов, которые оно имеет или может образовывать. Ионы
- , которые имеют сильный положительный или отрицательный заряд, легко растворяются в воде.Электрические заряды на молекулах растворенного вещества притягиваются к полярным зарядам на молекулах воды.
- такие вещества называются гидрофильными , что означает водолюбивых .
- молекул, таких как метан и другие подобные молекулы (например, содержащиеся в углеводородах — см. Ниже), не имеют зарядов на своей поверхности и не являются полярными.
- нет притяжения между водой и этими типами молекул, поэтому они образуют границу на границе раздела, в которой один тип молекулы остается на одной стороне, а другой тип молекулы остается на другой стороне.
- все такие вещества гидрофобны означает водобоязнь
- Глава:
- (стр.32) 2 От простого вещества к химическому элементу
- Источник:
- Что такое химический элемент?
- Автор (ы):
Бернадетт Бенсауд-Винсент
- Издатель:
- Oxford University Press
- Облегченная диффузия — Распределение вещества через клеточную мембрану с использованием специализированных встроенных транспортных белков.
- Пассивный транспорт — Использование белков для облегчения диффузии растворенного вещества по его градиенту через клеточную мембрану.
- Активный транспорт — Использование белков и энергии для транспортировки вещества, даже против их градиента через мембрану.
- Осмос — Простая диффузия воды по градиенту в растворе или через мембрану.
- Теории вещества XVII века: общий фон
- Декарт
- Рассказ Декарта о субстанции
- Какие вещества есть?
- Являются ли воплощенные человеческие существа субстанциями?
- Насколько независимы вещества?
- Сколько материальных веществ?
- Спиноза
- Счет вещества Спинозы
- Какие вещества есть?
- Почему Спиноза не создает субстанцию?
- Как может вещество иметь более одного атрибута?
- Расширенная и неделимая субстанция?
- Лейбниц
- Счет веществ Лейбница
- Какие вещества есть?
- Опыт и реальность
- Что не так с составными существами?
- Лейбниц и Спиноза
- Теории вещества XVII века в перспективе
- Ссылки и дополнительная литература
- Основные тексты на английском языке
- Дополнительные тексты
- Декарт
- Джон Коттингем, Роберт Стоутхофф, Дугальд Мердок и Энтони Кенни изд.и пер. Философские сочинения Декарта , 3 тома, Кембридж: Издательство Кембриджского университета, 1984–1991.
- Это стандартное английское издание работы Декарта.
- Спиноза
- Эдвин Керли, пер. и изд. Собрание сочинений Спинозы Vol. 1. Princeton: Princeton University Press, 1985.
- Это стандартный английский перевод.
- Лейбниц
- Роджер Арью и Дэниел Гарбер пер.и изд. г. Лейбниц: Философские очерки. Индианаполис: Хакетт, 1989.
- Это большая коллекция многих наиболее важных работ Лейбница.
- Leroy L. Loemker пер. и изд. Философские статьи и письма 2-е изд . Дордрехт: Рейдель, 1969.
- Это гораздо более широкое собрание работ Лейбница, чем тексты Ариев и Гарбера.
- Адамс, Роберт Меррихью. Лейбниц: детерминист, теист, идеалист . Нью-Йорк: Издательство Оксфордского университета, 1994.
- Это одна из самых влиятельных книг, написанных о Лейбнице за последние годы. Книга Адамса включает подробные обсуждения Лейбница модальности и идентичности, онтологического аргумента и места тел в зрелой метафизике Лейбница, среди других тем.
- Карриеро, Джон. «О взаимосвязи между модусом и субстанцией в метафизике Спинозы», Journal of the History of Philosophy , vol.33, нет. 2 (1995), стр. 245-273.
- В этой статье Карриеро утверждает, что представление Спинозы о субстанции является традиционным, согласно которому субстанции являются конечными субъектами.
- Коттингем, Джон. Декарт . Нью-Йорк: Блэквелл, 1986.
- Это хорошее введение в мысль Декарта и поднимает вопрос о триалистической интерпретации.
- Коттингем, Джон. Рационалисты . Оксфорд: Издательство Оксфордского университета, 1988.
- Это четко написанное резюме и сравнение философий Декарта, Спинозы и Лейбница. Рекомендуется глава 3 по существу.
- Делла Рокка, Майкл. «Субстанциальный монизм Спинозы», Спиноза: Метафизические темы . Эд. Олли Койстинен и Джон Биро. Оксфорд: Издательство Оксфордского университета, 2002.
- В этой статье Делла Рокка рассматривает официальный аргумент Спинозы о том, что существует только одна субстанция, и защищает его от ряда возражений, включая утверждение о том, что Спиноза не имеет права утверждать, что эта субстанция может иметь более одного атрибута.
- Делла Рокка, Майкл. Спиноза. Рутледж: 2008.
- Эта книга — отличный обзор жизни и философии Спинозы; Особенно хорошо рассуждения Делла Рокка о содержании Спинозы в отличие от Декарта.
- Хуенеманн, Чарльз. «Предикативные интерпретации божественного расширения Спинозы», History of Philosophy Quarterly , vol. 14, вып. 1 (1997), стр. 53-76.
- В этой статье Хенеманн предлагает описание расширенной субстанции Спинозы, которое во многом отличается от других влиятельных интерпретаций.При этом он поднимает вопрос о делимости субстанции и аргумент Спинозы о вакууме.
- Хоффман, Пол. «Единство человека Декарта», Philosophical Review , vol. 95, нет. 3 (1986), стр. 339-370.
- В этой часто цитируемой статье Хоффман приводит доводы в пользу триалистического прочтения Декарта и попутно предлагает ряд критических замечаний в отношении монистических интерпретаций субстанции.
- Хоффман, Джошуа и Розенкранц, Гэри С. Субстанция: ее природа и существование . Рутледж, 1997.
- В этой книге Хоффман и Розенкранц опираются на идеи философов прошлого (в том числе Декарта, Спинозу и Лейбница), а также на современные философские достижения, чтобы разработать и защитить концепцию субстанции, основанную на независимости.
- Джолли, Николас . Лейбниц. Рутледж: 2005.
- Эта книга — отличный обзор жизни и философии Лейбница.Книга написана для неспециалистов и будет хорошим началом для человека без предварительных знаний.
- Кауфман, Дан. «Декарт о композитах, неполных веществах и видах единства», Archiv für Geschichte der Philosophie , vol. 90, нет. 1 (2008), стр. 39-73.
- В этой прекрасной статье Кауфман утверждает, что Декарт — дуалист, и что триалистическая интерпретация, поддерживаемая Хоффманом (см. Выше) и другими, ошибочна.
- Линь, Мартин.«Аргументы Спинозы в пользу существования Бога», Философские и феноменологические исследования , том. 75, нет. 2 (2007), стр. 269-297.
- В этой статье Лин по-новому взглянул на аргументы Спинозы в пользу существования Бога и попытался защитить Спинозу от обвинения в бессвязной мысли о том, что Бог имеет более одного (а тем более всех) атрибутов.
- Леб, Луи Э. От Декарта до Юма: континентальная метафизика и развитие современной философии .Итака: Издательство Корнельского университета, 1981.
- Эта книга является одним из эталонов в данной области, и в главе 2 Леб предлагает сравнение Декарта, Спинозы и Лейбница по существу.
- Марки, Питер. «Декартовские концепции субстанции», «Разум, воля и ощущение: исследования по метафизике Декарта», . Эд. Джон Коттингем. Оксфорд: Clarenden Press, 1994.
- В этой влиятельной статье Марки утверждает, что обнаружил не два, а три описания существа работы Декарта.
- Робинсон, Таддеус С. «Спиноза о вакууме и простоте телесной субстанции», History of Philosophy Quarterly , vol. 26, № 1 (2009), стр. 63-81.
- В этой статье Робинсон предлагает новую интерпретацию аргумента Спинозы о вакууме и утверждает, что представление Декарта о протяженной субстанции, по крайней мере в свете Спинозы, непоследовательно.
- Родригес-Перейра, Гонсало. «Субстанциальный дуализм Декарта и его независимая концепция субстанции», , Журнал истории философии, , том.46, нет. 1 (2008), стр. 69-90.
- В этой статье Родригес-Перейра сосредотачивается на прояснении аспектов, в которых субстанции Декарта независимы, и утверждает, что другие характерные черты концепции субстанции Декарта вытекают из независимости, понимаемой таким образом.
- Резерфорд, Дональд. Лейбниц и рациональный порядок природы . Кембридж: Издательство Кембриджского университета, 1995a.
- Хотя эта влиятельная книга написана для специалистов, она удобочитаема.Резерфорд предлагает отчет о метафизике Лейбница, который отводит теодицею Лейбница особенно важную роль.
- Резерфорд, Дональд. «Метафизика: поздний период». Кембриджский компаньон Лейбница . Эд. Николас Джолли. Кембридж: Издательство Кембриджского университета, 1995b.
- Эта статья представляет собой превосходное резюме и обсуждение метафизики Лейбница от Новой Системы Природы 1695 года до Монадологии 1714 года, и фокусируется на учении Лейбница о материи в этот период.
- Скирри, Джастин. Декарт и метафизика человеческой природы . Нью-Йорк: Континуум, 2005.
- В этой книге прослеживаются схоластические влияния Декарта и развиваются плюралистические и триалистические интерпретации его представления о сущности.
- Сани, R.C. Лейбниц и Арно: комментарий к их переписке . Нью-Хейвен: издательство Йельского университета, 1990.
- Это чрезвычайно влиятельная книга, которая предлагает прочтение одного из самых важных философских обменов Лейбница.
- Словик, Эдвард. «Декарт и индивидуальная телесная субстанция», Британский журнал истории философии, , вып. 9 нет. 1 (2001) стр. 1-15.
- Словик продолжает с того места, где Хоффман заканчивает, выдвигая несколько аргументов против монистической интерпретации Декарта.
- Woolhouse, R.S. «Спиноза, Декарт и существование расширенной субстанции», Центральные темы в ранней современной философии . Эд. J.A. Обложка и Марк Кульстад.Индианаполис: Хакетт, 1990.
- В этой статье Вулхаус предлагает новое прочтение расширенной субстанции Спинозы, утверждая, что она относится к сущности, а не к фактически существующему бесконечному расширению.
- Woolhouse, R.S. Понятие субстанции в метафизике семнадцатого века . Нью-Йорк: Рутледж, 1993.
- Это хороший общий труд по существу за 17 -е годы века. Вдобавок Вулхаус предлагает новые прочтения Декарта и Спинозы (см. Выше) по расширенной субстанции.Эта работа предлагает особенно хороший взгляд на отношения между механикой, причинностью и субстанцией в течение этого периода.
Сводка
Вещество можно разделить на две большие категории: чистые вещества и смеси. Чистое вещество — это форма вещества, имеющая постоянный состав и постоянные свойства во всем образце. Смеси представляют собой физические комбинации двух или более элементов и / или соединений. Смеси можно разделить на однородные и гетерогенные. Элементы и соединения являются примерами чистых веществ. Соединения — это вещества, состоящие из более чем одного типа атомов.Элементы — это простейшие вещества, состоящие только из одного типа атомов.
Основные выводы
Определение вещества по Merriam-Webster
суть | \ ˈSəb-stən (t) s \б : основная или характерная часть или качество
2а : высшая реальность, лежащая в основе всех внешних проявлений и изменений
б : практическое значение : значение, полезность … законопроект, который будет лишен содержания в том смысле, что он будет санкционировать не что иное, как набор идей — Ричард Ривз3а : физический материал, из которого что-то сделано или который существует дискретно.
б : вещество определенного или определенного химического состава
c : что-то (например, наркотики или алкогольные напитки) считается вредным и обычно подлежит правовому ограничению. хранение контролируемых веществ, злоупотребление психоактивными веществами
4 : материальное имущество : имущество семейство материальных ценностейНаука на расстоянии
Наука на расстоянии Наука на расстоянииКонспект лекций
проверка
Используйте этот раздел, чтобы проверить точность ваших лекционных заметок.Убедитесь, что вы записали следующие определения, объяснения и важные концепции в своих заметках.
Физическая структура — Часть первая
Атомы
Атом — это наименьшая единица чистого вещества или элемента, которая может существовать и при этом сохранять свойства исходного вещества или элемента.- Ключевые идеи:
Атомы жизни
Три самых распространенных элемента на Земле — это кислород, кремний и алюминий; В живых организмах шесть наиболее распространенных элементов — это углерод, водород, азот, кислород, фосфор и сера.- Ключевые идеи:
Субатомные частицы
Есть три типа субатомных частиц, которые находятся в атомах всех элементов, кроме одного.- Ключевые идеи:
Атомная подструктура
Каждый атом имеет одинаковую субструктуру с плотным положительно заряженным центром (иногда называемым атомным ядром ), окруженным рассеянным, быстро движущимся числом отрицательно заряженных частиц.- Ключевые идеи:
Физические свойства атомов
Два важных физических свойства всех атомов зависят от их атомной массы и относительного количества протонов и нейтронов в атомном центре.- Ключевые идеи:
Изотопы
Изотопы — это семейства атомов, которые имеют одинаковый атомный номер, но разные атомные массы.- Ключевые идеи:
Электронные устройства
Электроны заряжены отрицательно и поэтому притягиваются к положительно заряженным протонам в центре атома. Они также отталкиваются отрицательными зарядами других электронов. Электроны удерживают фиксированное количество энергии, и этот уровень энергии определяет, насколько близко или далеко от атомного центра они расположены.- Ключевые идеи:
Орбитали
По мере того, как они диффундируют и перемещаются по ядру, электроны ограничены определенными объемами или формами пространства, называемыми орбиталями .- Ключевые идеи:
Атомная стабильность
Атомы наиболее стабильны и наименее реактивны, когда их внешний энергетический уровень либо полностью заполнен электронами, либо полностью лишен электронов.- Ключевые идеи:
Водород
Стабильность I: ионы
Один из способов перехода атома в более стабильное состояние состоит в том, чтобы набирать или терять электроны с его внешнего энергетического уровня до тех пор, пока этот энергетический уровень не станет полным или пустым.- Ключевые идеи:
Stability II: совместное использование
Атомы могут объединяться вместе и обмениваться электронами между собой.Атомы с общими электронами связаны друг с другом в форме, называемой молекулой , которая находится в более низком энергетическом состоянии, чем любой из отдельных атомов в отдельности.- Ключевые идеи:
Метан: органическая молекула
Атомы разных элементов могут обмениваться электронами, образовывать между собой ковалентные связи и создавать сложные молекулы.- Ключевые идеи:
Углерод
Молекула воды
Молекула воды состоит из одного атома кислорода, связанного двумя ковалентными связями с двумя атомами водорода. Электроны в этих связях не распределяются между атомами поровну. Этот тип ковалентной связи называется полярной .- Ключевые идеи:
Кислород
Особые свойства воды I: жидкость
Полярность молекулы воды придает ей некоторые особые свойства, первое из которых состоит в том, что вода является жидкостью при комнатной температуре.- Ключевые идеи:
Особые свойства воды II: растворитель
Растворитель — это жидкость, в которой растворяются другие твердые вещества и жидкости.Вода — почти универсальный растворитель, в котором до некоторой степени растворяется большинство других веществ.- Ключевые идеи:
Наука на расстоянии
© 1997, 1998, 1999, 2000, профессор Джон Бламир
От простого вещества к химическому элементу
Страница из
НАПЕЧАТАНО ИЗ ОНЛАЙН-СТИПЕНДИИ ОКСФОРДА (oxford.universitypressscholarship.com). (c) Авторские права Oxford University Press, 2021. Все права защищены. Отдельный пользователь может распечатать одну главу монографии в формате PDF в OSO для личного использования.дата: 28 апреля 2021 г.
DOI: 10.1093 / oso / 97801
784.003.0003
Современные представления о химическом элементе приписывается Лавуазье. Я буду утверждать, что, несмотря на значительное влияние определения элементов как неразложившихся тел в «Элементах химии» Лавуазье, это утверждение вводит в заблуждение по крайней мере по трем причинам.Во-первых, элементы уже были определены как остатки анализа до Лавуазье. Во-вторых, Лавуазье не отказался полностью от традиционного взгляда на элементы как на составные части всех тел. В-третьих, современное определение химического элемента подразумевает четкое различие между простыми телами и элементами, которое позже ввел Дмитрий Менделеев. Я обрисую роль этого концептуального различия в процессе классификации элементов Менделеева и симметрично подчеркну, как периодическая система способствовала стабилизации его представления об элементе как отдельном человеке, определяемом его положением в системе.Таким образом, понятие элемента выступает как предварительное условие, так и продукт построения периодической системы.
Ключевые слова: анализ, атомы, изотопы, Лавуазье, молекулы, вещества
Для получения доступа к полному тексту книг в рамках службы для получения стипендииOxford Online требуется подписка или покупка. Однако публичные пользователи могут свободно искать на сайте и просматривать аннотации и ключевые слова для каждой книги и главы.
Пожалуйста, подпишитесь или войдите для доступа к полному тексту.
Если вы считаете, что у вас должен быть доступ к этому заголовку, обратитесь к своему библиотекарю.
Для устранения неполадок, пожалуйста, проверьте наш FAQs , и если вы не можете найти там ответ, пожалуйста свяжитесь с нами .
Что такое элемент? | Особенность
Из химических концепций нет ничего более фундаментального, чем элемент.Это одна из первых идей, с которыми сталкивается студент-химик, часто в знаковой таблице этих основных компонентов природы, которую Дмитрий Менделеев впервые описал 150 лет назад и которая отмечается в этом году. И все же никто не может точно сказать, что такое элемент. Этот вопрос обсуждался с большой энергией и время от времени во время встречи Международного общества философии химии в Бристоле в июле 2018 года, но до сих пор без единого мнения.
Это неудивительно.Некоторые из лучших умов химии, в том числе Антуан Лавуазье, сам Менделеев и пионер ядерной химии Фредерик Содди, боролись с этим, но все же краткое и исчерпывающее определение остается неуловимым. И некоторые участники встречи дали понять, что это может быть к лучшему.
Для других это показатель того, что химия требует серьезных философских размышлений. «Химия не воспринимает себя как дисциплину», — говорит философ Фарзад Махотян из Нью-Йоркского университета в США.Это не просто определение элемента; такие понятия, как молекулы, связи и даже характер самой таблицы Менделеева, остаются нечеткими: обманчиво знакомыми из регулярного использования практиками, но не имеющими никакого значения, с которым все согласны. «Существует потребность в философских размышлениях об аспектах химии, которые мы склонны преподавать довольно механически», — говорит Эрик Скерри из Калифорнийского университета в Лос-Анджелесе, США, редактор журнала «Философия науки» Foundations of Chemistry.
Кажется разумным ожидать, что химия даст однозначное определение
Значение «элемента» — излюбленная тема для споров среди химиков, не работающих на дежурстве. Мы согласны (верно?), Что водород — это элемент, но что мы подразумеваем под этим? Является ли газообразный молекулярный водород элементом? Или изолированный атом водорода? Или мы имеем в виду не какое-то реальное вещество, а «трансцендентное» понятие водорода, реальные атомы и молекулы которого являются лишь материальными представителями?
Кто-то может сказать: а кого это волнует? Мы знаем, что имеем в виду на практике.Если я скажу: «Сера — это элемент, который образует желтое твердое вещество с резким запахом», я не ожидаю возражений. Точно так же, если я скажу: «Сера — второй элемент в группе 16 Периодической таблицы». Но это две совершенно разные вещи.
По словам химика-теоретика Ойгена Шварца из Университета Зигена в Германии, типичное отношение — сказать: «Я знаю, как я говорю об элементах, — это не совсем правильно, но все это делают, и студенты в конце концов поймут это». «Но« лично я как химик считаю, что не следует усваивать эту привычку », — добавляет он.
Елена Гибауди из Туринского университета в Италии обеспокоена тем, что отсутствие точного определения элемента порождает проблемы понимания, общения и доверия при обучении. «Когда два специалиста по химии обсуждают элементы, они могут отличить значение от контекста, но в классе это не так», — говорит она.
Могут возникнуть проблемы и с общественным пониманием химии. Шварц указывает на то, что из-за того, что некоторые элементы становятся связанными с токсичными веществами — например, газообразным хлором или серой в диоксиде серы, выделяющейся при сжигании угля и нефти, — сам элемент может считаться токсичным по своей природе и уязвимым для химически безграмотных запретов.«Я не знаю, как дать понять общественности, что только некоторые соединения данного элемента токсичны, и даже только в концентрациях, превышающих определенную конкретную, а слишком мало того же элемента может даже вызвать проблемы со здоровьем», — говорит он. .
«Понятие элемента занимает центральное место в химии и служит ряду целей», — говорит Гибади. «Например, он определяет, что остается неизменным в системе, подвергающейся химическому преобразованию, и различает химические и ядерные изменения.Поэтому кажется разумным ожидать, что химия даст однозначное определение ». Но может ли это?
Земля, ветер и огонь?
Подобно идее атомов, элементы скорее страдают, чем выигрывают от иллюзии непрерывности в давней традиции мышления. Популярная история гласит, что древние греки думали, что существует только четыре элемента — земля, воздух, огонь и вода, — но примерно с восемнадцатого века мы начали понимать, что их больше, чем четыре, и что ни один из них не соответствует этим древним элементам. элементы.На самом деле все сложнее. Во-первых, четыре элемента, приписываемые Эмпедоклу и закрепленные в философии Аристотеля, ни в коем случае не были единственной схемой основных строительных блоков материи в греческой мысли. А до золотого века химии в эпоху позднего Просвещения системы «элементов» были довольно туманными. Швейцарский врач 16 века Парацельс предложил три основных «принципа» — серу, соль и ртуть, в то время как несколько других схем (включая такие фиктивные элементы, как флогистон) получили временную поддержку.
Должен ли каждый изотоп занимать свое место в периодической таблице?
Кроме того, это не обязательно были конкурирующие альтернативы. Идея элемента, такого как атом, имела довольно разнообразный оттенок и не обязательно означала первичный тип материи. Например, три принципа Парацельса рассматривались больше как свойства, чем ингредиенты: сера, представляющая горючесть, твердость соли и текучесть ртути.
Роберт Бойль справедливо прославился тем, что внес некоторую ясность в концепцию, когда в своей книге « Скептический химик » 1665 года он предположил, что элементом является субстанция, которую нельзя свести («проанализировать») к чему-то более простому.Но определение Бойля говорит вам только , когда у вас есть элемент, а не то, что это за элемент и что отличает один от другого. И это весьма условно, в заложниках ваших аналитических способностей. Как вы могли быть уверены, что у вас есть элемент, а не просто соединение, которое еще никто не нашел способ разделить на его ингредиенты? В самом деле, нельзя, поэтому трудно расщепляемые оксиды, такие как оксид алюминия и кремнезем, фигурируют как элементы в списках 18-го века, как в влиятельной книге Антуана Лавуазье 1789 Traité Élémentaire de Chimie .Лавуазье вслед за Бойлем утверждал, что элемент представляет собой заключительную стадию анализа.
Джон Дальтон внес нечто более фундаментальное в определение Лавуазье, когда в 1808 году он утверждал, что специфические свойства элементов происходят от свойств составляющих их атомов, представленных в виде крошечных твердых сферических частиц. Ко времени Менделеева в середине того века было признано, что разные элементы имеют разный атомный вес, и при составлении своей периодической таблицы Менделеев использовал упорядочение элементов на основе их атомного веса.(Он сам использовал термин «элементарный вес», поскольку не верил в атомы.)
Открытия радиохимиков, таких как Содди, и физиков, таких как Эрнест Резерфорд и Генри Мозли, к 1920-м годам привели к пониманию того, что более фундаментальным свойством атомов элемента является их атомный номер Z — количество протонов в их ядрах, которое составляет то же самое для всех атомов данного элемента. Фрэнсис Астон открыл изотопы в 1922 году, которые имеют одинаковый Z , но разную атомную массу.Но если Z отличается для двух атомов, это разные элементы.
Что мы подразумеваем под «углеродом»? Алмаз, атом с Z = 6 или C 60
Но сначала изотопы выбросили кошку среди голубей. «Их открытие было проблемой для определения элемента», — говорит Гибади. «Среди химиков и физиков разгорелись оживленные дебаты о концепции химического элемента. Вопрос заключался в том, должен ли каждый изотоп занимать свое место в периодической таблице.В 1923 году международный комитет согласился основывать идентификацию химического элемента на атомном номере, а не на атомном весе.
На этом, как вы могли подумать, мог бы и конец: элементы определены Z . Проблема в том, что химики используют это слово не совсем так. В основополагающей статье об определении элементов в 1932 году немецкий химик Фридрих Панет допустил два разных определения, которые он назвал Einfacher Stoff — обычно переводится как «простое вещество» — и Grundstoff , или «первичное / основное вещество». .Первый относится к понятию Лавуазье реального, физического вещества, которое не может быть сокращено химическими методами до более основных ингредиентов, второй — к абстрактному понятию: «кислород», скажем, как тип атома с Z = 8.
Гибади сомневается, что мы уже сейчас вышли за пределы дуализма Панета. В настоящее время Iupac дает двойное определение «элементу» в своей «Золотой книге» химической терминологии, в которой говорится, что это слово может относиться либо к «разновидности атома» (которую Гибади считает родственной «основной субстанции» Панета), либо, скорее тавтологически, к «чистой элементарной субстанции».
Это двойное значение неудобно. Найдите слово «кислород» на веб-сайте, посвященном элементам, и вам, вероятно, скажут, что он имеет Z = 8 и, возможно, определенную электронную конфигурацию и положение в периодической таблице, но также и что это очень реактивное вещество с формула O 2 и температура кипения –183 ° C. По словам химика Марка Лича, который управляет веб-сайтом химических ресурсов meta-synthesis.com, это небрежное объединение двух совершенно разных типов данных: одно относится к «основной субстанции» Панета (абстрактный идеал), а другое — к его «основной субстанции» (абстрактный идеал). простая субстанция »(реальная субстанция).Конечно, это не может быть хорошо?
Более того, говорит Лич, все наше представление о таблице Менделеева неуклюже смешивает эти два понятия. Мы можем представить себе, что это таблица «основных веществ» — именно так ее видел Менделеев. Но само понятие периодичности относится к реальным химическим свойствам реального вещества: валентности химических соединений, таким свойствам, как энергия ионизации, металлический характер и так далее. «Если основное вещество имеет только свойство Z , то это просто простой список», — говорит Лич.«Откуда же тогда взялась структура периодической таблицы Менделеева?»
В некоторых популярных версиях таблицы Менделеева даже показаны фотографии «простых» материальных форм элементов: алмаз или графит вместо углерода и так далее. Так что это запутанная смесь — и, возможно, так и должно быть. «Для его создания нужен разумный компромисс как основных, так и простых свойств», — говорит Скерри.
Это нетривиальный вопрос. Например, до сих пор не утихают споры о том, должны ли элементы ниже иттрия в группе 3 быть лантаном и актинием или лютецием и лоуренсием.Спор сводится к тому, считаете ли вы, что таблица должна отражать «фундаментальные» характеристики, такие как электронная конфигурация, или наблюдаемые, такие как химическое поведение. Эти аргументы становятся еще более неоднозначными, когда релятивистские эффекты (из-за очень высоких скоростей электронов внутренней оболочки) начинают разрушать химическую периодичность среди созданных человеком сверхтяжелых элементов.
Становится тяжелее
Это не единственное осложнение, которое создают супертяжелые машины.Заблуждение относительно того, является ли элемент «материалом» или «концепцией», происходит из-за того, что в прошлом они были обоими. Но действительно ли новый элемент имеет такие же претензии на реальность, когда он существует только в виде горстки атомов, которые стабильны менее секунды, как в случае с некоторыми новейшими искусственными элементами, такими как теннессин? Если элементы частично определяются их химическими свойствами, то где же тогда элементы, которые не существуют достаточно долго, чтобы вступить в какое-либо значимое химическое взаимодействие, и которые в любом случае состоят только из сильно заряженных ионов, которые никогда не приобретают полный набор электронов? ? «В каком смысле они элементы, если они длятся всего одну-две миллисекунды?» — спрашивает Скерри.«Я не думаю, что мы когда-нибудь сможем разливать их в бутылки».
В каком смысле они элементы, если они существуют всего одну-две миллисекунды?
Радиохимия всегда была немного тревожной в пределах химической стойкости. Один из распространенных способов мышления о химических элементах — это «сохраненные количества» химии. Точно так же, как масса и энергия никогда не разрушаются в физике (хотя, конечно, они могут взаимно преобразовываться), фундаментальное правило сохранения химии состоит в том, что элементы сохраняются: вы никогда не выйдете из реакции с меньшим количеством углерода, чем вы начали.Но в радиохимии, где один элемент может распадаться на другой, вы это делаете. Вопрос о том, делает ли это радиохимию частью химии вообще, обсуждался с первых дней ее существования, когда Нобелевские комитеты по физике и химии соревновались за то, кто должен присуждать призы таким, как Кюри и Резерфорд (оба они теперь «претендовали» на звание химии в названия элементов).
Эта война за территорию так и не закончилась, о чем свидетельствуют недавние ссоры между Международными союзами теоретической и прикладной физики и химии (Iupap и Iupac) по поводу того, кто должен говорить об утверждении новых элементов.Физики говорят, что только у них достаточно опыта, чтобы судить об утверждениях, сделанных в экспериментах по разрушению атомов с помощью ускорителей частиц. Но химики не рады позволить другой группе определять, что входит в их самый ценный символ — таблицу Менделеева.
Кто бы ни выносил решение, эти новые элементы нельзя держать в руках. Они подчеркивают новую актуальность сроков. Возможно, любое слияние ядер, которое длится дольше, чем типичный временной масштаб ядерного рассеяния, около 10 –10 с, можно квалифицировать как образование другого элемента.Но действительно ли объединение, измеряемое в наносекундах, оправдывает это, или это просто своего рода резонанс? Вот почему, говорит Шварц, «когда мы говорим об элементах, мы должны также говорить о временных рамках». Он задается вопросом, должен ли «элемент» быть по крайней мере сущностью, способной в принципе образовывать молекулы. «Химия — это искусство и наука о реальных материалах, — добавляет он, — но для физиков ядро - это элемент». Между тем, Iupac недавно объявил о новых критериях открытия сверхтяжелых элементов, которые подтверждают, что временной масштаб существования, соответствующий статусу элемента, составляет всего
10 –14 с.
Сама по себе вещь
Проблема элементов показывает, что, как говорит Скерри, химии нужна философия. «Проблема« химического элемента », как и некоторые другие проблемы в химии, такие как понятия вещества и структуры, поднимает философские вопросы, и поэтому не может быть решена, не полагаясь на идеи из философии», — говорит Гибади. В некотором смысле этот вопрос восходит к Платону, чье понятие «идеальных» нематериальных форм лежало в основе его взглядов на реальные физические сущности.Абстрактная «основная субстанция» Панета также иногда обсуждается с точки зрения концепции Иммануила Канта Ding an sich — «вещи в себе» или фундаментального аспекта реальности, недоступного для наших (подверженных ошибкам) чувств.
Содержит ли «базовое» определение элемента все «простые» характеристики внутри него?
Но если это философский вопрос, который не может быть решен с помощью эмпиризма, может быть, нам просто нужно сделать выбор между «основной субстанцией» Панета и «простой субстанцией» в качестве определения элемента? Некоторые исследователи так считают.Тем временем Скерри предполагает, что природа элемента не просто двойственна, а тройственна: в веществе элемента важны не только свойства сырья, но и свойства его соединений. В конце концов, одно из непреходящих чудес химии заключается в том, что в хлориде натрия не остается следов реактивного серого металла и ядовитого зеленого газа.
Введение отдельной номенклатуры для «простого» и «основного» определений, чтобы молекулы дигидрогена больше не рассматривались как «элемент водород», потребует реформирования глубоко укоренившегося химического языка.Но Сара Хиджманс из Университета Париж-Дидро во Франции сомневается в том, нужно ли нам так далеко идти. Возможно, предлагает она, мы могли бы рассматривать слово «элемент» как понятие, содержащееся в обоих определениях. Она говорит, что во времена Лавуазье не было другого выбора, кроме как обратиться к аналитическому определению, потому что мы почти ничего не понимали в том, что отличает элементы на фундаментальном уровне. Постепенно баланс склонился к «фундаментальному» определению в терминах Z . Но очевидно, что эмпирическая, «химическая» точка зрения все же имеет значение, как показывает таблица Менделеева.
Возможно, вопрос в том, действительно ли эти двое вообще конфликтуют. В каком-то смысле в Z для химиков нет ничего особенно значимого для химиков, поскольку ядро практически не играет прямой роли в химическом поведении. Число протонов — это всего лишь косвенный показатель того, что имеет значение для химии: числа электронов, а также их конфигурации и энергии.
Но они, учитывая конкретный Z , предопределены правилами квантовой механики.Их можно предсказать. А из этой информации , в свою очередь, мы можем в принципе предсказать многие химические реакции, например, какие соединения будут образовывать элемент. Мы даже можем предсказать физические свойства некоторых элементов: аллотропные формы, точки плавления и так далее. Итак, содержит ли «базовое» определение элемента все «простые» характеристики внутри него, которые будут раскрыты по мере того, как наши вычислительные возможности улучшатся?
Может быть, мы должны признать, что понятие элемента всегда будет окружать некоторую неопределенность.И, возможно, это не так уж и плохо. В конце концов, химики привыкли к этому — как отметил лауреат Нобелевской премии Роальд Хоффманн, они всегда используют концепции, не имеющие однозначного и точного определения, такие как электроотрицательность и ионный радиус, без уменьшения их ценности для поля. «Неопределенность сыграла полезную роль в мышлении», — говорит Махотян. Он утверждает, что, возможно, дело не в самой расплывчатости, а в том, чтобы убедиться, что это не просто небрежность.
Так что же такое углерод? Ответ, говорит Шварц, может зависеть от того, с кем мы говорим.Для разной аудитории и для разных целей это может быть сажа; это может быть шестой элемент, природная смесь изотопов или компонент метана. Элементарно, правда.
Филип Болл — научный писатель из Лондона, Великобритания
Простая диффузия — определение и примеры
Определение простой диффузии
Простая диффузия — это процесс, при котором растворенные вещества перемещаются по градиенту концентрации в растворе или через полупроницаемый мембрана.Простая диффузия осуществляется за счет водородных связей, образующихся между молекулами воды и растворенными веществами. Молекулы воды движутся внутрь, чтобы окружить отдельные молекулы растворенного вещества, что максимизирует водородные связи. Однако водородные связи чрезвычайно временны, и в результате раствор постоянно перемешивается. Это помогает равномерно распределить растворенное вещество по всему раствору. Если молекулы достаточно малы, эта простая диффузия может происходить через клеточные мембраны между отдельными фосфолипидами, составляющими мембрану.Таким образом, вода может двигаться по градиенту своей концентрации через клеточную мембрану, это форма простой диффузии, известная как осмос , .
В отличие от простой диффузии, клеточные мембраны часто содержат специализированные мембранные белки, которые помогают транспортировать вещества через мембрану. Это известно как облегченная диффузия . Облегченная диффузия включает в себя как активных , так и пассивных транспортных растворенных веществ через мембрану. Активный транспорт использует АТФ для обеспечения энергией белков, обеспечивающих транспорт.В отличие от простой диффузии, молекулы могут перемещаться против своего градиента с помощью активных транспортных систем. Простая диффузия присутствует в ряде биологических систем, включая доставку кислорода, воды и других небольших молекул к клеткам тела. Хотя многие растворенные вещества обладают способностью проходить через мембрану посредством простой диффузии, в клетках часто есть белковые каналы, которые помогают ускорить этот процесс.
Примеры простой диффузии
Двуокись углерода
Двуокись углерода — это небольшая молекула, которая может растворяться в воде.Если вам когда-нибудь нравилась газированная вода, вы знаете это. Однако вы можете не знать, что тот же механизм транспортирует углекислый газ, который создают ваши клетки, в кровоток и из организма через легкие. Двуокись углерода достаточно мала, чтобы легко распространяться через ткани и выходить из организма. Если вы задержите дыхание на короткое время, вы начнете чувствовать жгучее «желание дышать». Это вызвано накоплением углекислого газа в чувствительных нервных тканях кровотока, легких и головного мозга.Когда вы снова начинаете дышать, углекислый газ выходит из вашего организма. Многие газы способны делать это через легкие, включая кислород, азот и многие другие газы в атмосфере.
Бактерии
Так как бактерии представляют собой простые организмы, они не могут потреблять питательные вещества, кроме диффузии их через клеточную мембрану. Хотя они действительно используют облегченную диффузию для транспортировки большинства питательных веществ, они полагаются на простую диффузию для доставки кислорода, воды и небольших питательных веществ в цитоплазму.Внутри их клеток нет специализированных органелл, удерживающих или транспортирующих вещества, поэтому бактерии полагаются на простую диффузию материала внутри своих клеток, чтобы обеспечить присутствие материалов для реакции, которая контролирует их жизненные процессы.
Викторина
1. Кубик соли опускают в стакан с водой. Через час куб исчез. Что из следующего произошло?
A. Простая диффузия
B. Облегченная диффузия
C. Осмос
Ответ на вопрос № 1
A правильный. Это случай простой диффузии. Поваренная соль состоит из матрицы двух ионов: натрия (Na + ) и хлорида (Cl — ). Вода в стакане сразу же начала выводить молекулы из блока, как только она попадала в стакан. Водородные связи, образованные между молекулами воды и ионами соли, разделяют ионы соли и равномерно распределяют их между молекулами воды.Когда вода проникает в блок, молекулы соли в конечном итоге полностью окружаются молекулами воды. Водородные связи продолжают перемещать молекулы воды и полностью окружают каждый ион соли, пока соль не перестанет быть видимой в растворе.
2. В клеточных мембранах некоторых организмов есть белки, называемые аквапоринами, которые обеспечивают легкий путь для воды, проходящей через мембрану. Однако вода будет проходить через мембрану путем осмоса без этих белков.Если клетка подвергается воздействию высокогипотонической среды, вода устремляется через аквапорины и клеточную мембрану в клетку. Что из следующего происходит?
A. Простая диффузия
B. Осмос
C. Осмос и облегченная диффузия
Ответ на вопрос № 2
C правильный. Простая диффузия воды известна как осмос. У него есть отдельное название, чтобы различать, когда вода движется без растворенных веществ, как в случае, когда вода проходит через клеточную мембрану.Растворенные вещества, первоначально распределенные в воде, остаются, поскольку вода устремляется, чтобы уравновесить концентрацию растворенных веществ в ячейке. Аквапорин — это особые мембранные белки, которые способствуют диффузии воды в клетку.
3. Кислород, используемый для дыхания, представляет собой очень маленькую молекулу. У некоторых мелких организмов органы дыхания не нужны, потому что кислород проходит непосредственно через клеточную мембрану в каждую клетку. Какой процесс за это отвечает?
А. Облегченная диффузия
B. Осмос
C. Простая диффузия
Ответ на вопрос № 3
C правильный. Кислород перемещается по морской среде благодаря простой диффузии. Кислород обычно образует связь со второй молекулой кислорода и движется как O 2 . Эти небольшие молекулы могут образовывать водородные связи, а также достаточно малы, чтобы диффундировать напрямую через клеточные мембраны. Даже в больших организмах не нужны специальные белки для перемещения кислорода в клетки, он диффундирует прямо из легких в клетки крови и по всему телу.Теории субстанции XVII века
В современном повседневном языке слово «субстанция», как правило, является общим термином, используемым для обозначения различных видов материальных вещей («Нам нужно очистить эту липкую субстанцию с пола») или как прилагательное, относящееся к массе чего-либо, размер или важность («Это солидный книжный шкаф»). Однако в философских дискуссиях 17, и веков значение этого термина лишь косвенно связано с нашим повседневным использованием этого термина.Для 17 философов -го и -го века этот термин зарезервирован для основных составляющих реальности, от которых зависит все остальное. В этой статье обсуждаются наиболее важные теории субстанции 17 – веков: теории Декарта, Спинозы и Лейбница. Хотя эти философы были в высшей степени оригинальными мыслителями, они разделяли базовую концепцию субстанции, унаследованную от схоластически-аристотелевской традиции, из которой возникло философское мышление. В общем смысле каждая из этих теорий представляет собой способ выработки двойных обязательств: приверженность субстанции как конечному предмету и приверженность существованию Бога как субстанции.Несмотря на это систематическое сходство между теориями, в конечном итоге они предлагают очень разные объяснения природы субстанции. Учитывая основополагающую роль, которую субстанция играет в метафизических схемах этих мыслителей, неудивительно, что эти теории субстанции лежат в основе совершенно разных представлений о природе и структуре реальности.
Содержание
1.Теории вещества XVII века: общий фон
Размышляя о 17 отчетах о веществе -го -го века, мы должны помнить, что озабоченность веществом и его природой не была новостью для того периода. Фактически, философское мышление о природе вещества восходит к древней Греции. В то время как новые философы 17, и века стремились порвать с прошлым и решать философские и научные проблемы на новых основаниях, их взгляды развивались не в интеллектуальном вакууме.Действительно, схоластически-аристотелевская традиция того времени сообщала их размышлениям о субстанции разными способами и способствовала ряду общих черт в их мышлении. Прежде чем рассматривать конкретные теории субстанции, важно отметить четыре общие черты.
Вещество, Режим, Присутствие
Для философов, которых мы будем обсуждать, на самом глубоком уровне вселенная содержит только два вида или категорий сущностей: субстанции и формы.Вообще говоря, режимы — это способы существования вещей; таким образом, форма (например, прямоугольник), цвет (например, краснота) и размер (например, длина) являются парадигмальными режимами. Как способ есть вещь, мода находится в особых отношениях с тем, для чего она является способом. Согласно традиции, восходящей к Аристотелевской Категории , говорится, что модусы существуют в субъекте или присущи ему. Точно так же считается, что у субъекта есть годы или нет. Таким образом, мы можем сказать, что дверь — это объект, в котором присутствует форма прямоугольности.Один режим может существовать в другом режиме (например, цвет может иметь определенный оттенок), но в конечном итоге все режимы существуют в чем-то, что само по себе не является режимом, то есть в веществе. Таким образом, субстанция — это высший предмет.
Независимость и приоритет
Новые философы 17, -го, -го века следуют традиции, связывая наследственность с зависимостью. Все они согласны с тем, что существование режима зависит не так, как существование субстанции.Идея состоит в том, что модусы, как способы существования вещей, зависят в своем существовании от того, модами они являются, например не существует режима «быть длиной 8’0» без субъекта , имеющего длину 8’0. Иначе говоря, точка зрения состоит в том, что существование режима в конечном итоге требует или предполагает существование субстанции. Иногда об этом говорят, говоря, что субстанции как субъекты метафизически предшествуют модусам.
Градусов реальности
В отличие от современных философов, большинство философов -го и -го веков считали, что реальность проявляется поэтапно — что некоторые существующие вещи более или менее реальны, чем другие существующие.По крайней мере, часть того, что диктует реальность существа, согласно этим философам, — это степень, в которой его существование зависит от других вещей: чем менее зависима вещь от других вещей в своем существовании, тем она более реальна. Учитывая, что существуют только субстанции и модусы и что способы существования зависят от субстанций, отсюда следует, что субстанции являются наиболее реальными составляющими реальности.
Бог существует и является субстанцией
Более того, каждый из философов, которых мы будем обсуждать, утверждает (и предлагает аргументы в пользу этого утверждения), что Бог существует, и что существование Бога абсолютно независимо.Поэтому неудивительно, учитывая вышесказанное, что каждый из этих философов считает, что Бог является субстанцией par excellence .
2. Декарт
Философская система Декарта, включая его понимание сущности, имела огромное влияние в течение 17, -го, -го века. Дополнительные сведения см. В статье IEP «Рене Декарт: Обзор». Однако, в отличие от Спинозы и Лейбница, теория субстанции Декарта не была центральным элементом его философской системы. Тем не менее Декарт предложил новую теорию субстанции, которая во многом расходилась с схоластико-аристотелевской традицией.
а. Рассказ Декарта о субстанции
Иногда говорят, что Декарт дает два разных определения субстанции, и действительно, в Принципах и Вторых ответах он определяет субстанцию по-разному. Однако мы не должны рассматривать это как свидетельство того, что Декарт изменил свое мнение. Напротив, очевидно, что для Декарта эти определения выражают две стороны единого представления о субстанции.
Давайте начнем с определения, которое он предлагает в его Принципах философии (I.51-52). Здесь он определяет «сущность» с точки зрения независимости. Он начинает с того, что разъясняет, что на самом деле существует два разных философских значения этого термина (соответствующих двум степеням независимости). По причинам, которые станут понятны через мгновение, давайте различим два чувства, назвав одно вещество , а другое — созданное вещество . Определения Декарта можно перефразировать следующим образом:
Вещество : Вещь, существование которой не зависит ни от чего.
Созданная субстанция : Вещь, существование которой не зависит ни от чего, кроме Бога.
Строго говоря, для Декарта существует только одна Субстанция (в отличие от Созданная Субстанция ), поскольку есть только одна вещь, существование которой независимо от всех других вещей: Бог. Однако во вселенной, которую создал Бог, есть сущности, существование которых зависит только от Бога. Эти меньшие субстанции являются основными составляющими сотворенного мира.
Определение субстанции, которое Декарт предлагает в Second Replies (и в других местах), игнорирует различие между Богом и творением и определяет субстанцию гораздо более традиционным способом, утверждая, что субстанция — это субъект, который имеет или несет модусы, но сам по себе не является проявлением чего-либо другого. Это согласуется с другими его комментариями по существу в Принципах . Таким образом, он говорит нам, что каждая сотворенная субстанция имеет ровно один атрибут (Принципы , I.53). Атрибут субстанции, как объясняет Декарт, — это ее «основное свойство, которое составляет ее природу и сущность и к которому относятся все ее другие свойства» (Там же). Следовательно, атрибут субстанции определяет ее вид, поскольку атрибуты «составляют» природу субстанции, и все и только предметы одной и той же природы относятся к одному и тому же виду. Более того, заявляя, что все свойства вещества передаются через атрибут вещества, Декарт утверждает, что атрибут вещества определяет свойства, которыми оно может обладать.
Декарт определяет два атрибута: мысль и протяженность. Следовательно, существует по крайней мере два вида сотворенных субстанций — протяженные субстанции и мыслящие субстанции. Под «протяженностью» Декарт просто имел в виду длину, ширину и глубину. В более разговорной речи мы могли бы сказать, что быть расширенным — это просто занять место или иметь объем. Тогда как под «мыслящей субстанцией» Декарт имел в виду просто «ум». Хотя Декарт обсуждает только эти два атрибута, он никогда явно не исключает возможности других атрибутов.Тем не менее, традиция интерпретировала Декарта как утверждающего, что существует только два вида сотворенной субстанции, и именно по этой причине Декарта часто называют субстанциальным дуалистом .
Имея эту спецификацию в руках, мы лучше понимаем, что имеет в виду Декарт, когда говорит, что все свойства субстанции передаются через атрибут субстанции или «основное свойство». Рассмотрим протяженное вещество, скажем, конкретный камень. Среди свойств этой породы — форма и размер; но наличие этих свойств предполагает свойство протяженности.Иначе говоря, что-то не может иметь форму или размер без расширения. Более того, свойства, которыми может обладать камень, ограничиваются модификациями растяжения — например, камень не может обладать свойством испытывать боль, поскольку свойство испытывать боль не является способом расширения. В общем, мы можем сказать, что для Декарта: i) атрибут субстанции является ее наиболее общим свойством, и что ii) любое другое свойство субстанции является просто спецификацией, способом существования или способом этого атрибута.
г. Какие есть вещества?
Какие существуют вещества с учетом этого объяснения природы вещества? В своей работе Meditation Six Декарт утверждает, что человеческий разум и тело действительно различны, то есть что все они являются субстанциями. В самом деле, каждое индивидуальное сознание или ум — это мыслящая субстанция. Кроме того, Декарт рассматривает тела, включая предметы нашего повседневного опыта (стулья, деревья, ложки и т. Д.), Как протяженные субстанции. Это имеет смысл.Расширение — это атрибут субстанции, поэтому из этого следует, что все, что расширяется (имеет атрибут расширения), само по себе является субстанцией. Более того, части протяженных субстанций, как сами протяженные, кажутся Декарту протяженными субстанциями (см. Принципы I. 60). Учитывая, что Декарт считает материю бесконечно делимой (Принципы , II. 20) — что каждая часть материи простирается до самого низа — отсюда следует, что существует бесконечное число протяженных субстанций.
Таким образом, мы получаем следующую картину реальности. Самая реальная вещь — это Бог, от которого зависит все остальное. Однако в созданном мире есть сущности, которые независимы от всего, кроме Бога. Это созданные субстанции. Созданные субстанции бывают двух видов — расширенные субстанции и умы, и того и другого существует множество.
Это краткое изложение концепции субстанции Декарта поднимает ряд более глубоких вопросов и противоречий. Естественно возникает один центральный вопрос: почему Декарт считает протяженность и мышление наиболее общими свойствами субстанций.Подробное обсуждение причин Декарта см. В статье IEP Рене Декарт: Различие между разумом и телом. В этой статье будет кратко рассмотрена роль воплощенных человеческих существ в метафизике Декарта, что Декарт имел в виду, называя субстанции независимыми, и связанные с этим споры относительно количества материальных субстанций, на которые Декарт имеет право.
г. Являются ли воплощенные человеческие существа субстанциями?
Воплощенные люди плохо вписываются в метафизику Декарта.В воплощении люди — составные существа; воплощенный человек состоит из ментальной субстанции (наш разум) и физической субстанции (наше тело) для Декарта. Однако Декарт думает, что это составное существо есть нечто сверх простого агрегирования. Он пишет в Mediation Six : «Природа также учит меня … что я не просто присутствую в моем теле, как моряк, находящийся на корабле, но что я очень тесно связан и как бы смешан с ним, поэтому что я и корпус образуют единицу »(курсив мой).В целом ясно, что Декарт считает воплощенных людей исключительными существами в некотором отношении, но то, как мы должны понимать этот союз разума и тела и его место в метафизике Декарта, было предметом некоторых разногласий среди ученых. Один из наиболее заметных споров был между теми учеными, которые, по мнению Декарта, считали воплощенные человеческие существа отдельным видом сотворенной субстанции, и теми учеными, которые этого не делали. Первые видят в Декарте исследователя субстанций , тогда как вторые интерпретируют его в традиционном смысле как субстанциального дуалиста.Для ознакомления с судебным процессом см. Hoffman 1986 и Skirry 2005: Chapter 4). О недавних аргументах в защиту субстанциального дуализма от толкований триалистов см. Kaufman 2008 и Zaldivar 2011.
г. Насколько независимы от вещества?
Как мы видели, Декарт определяет субстанцию в терминах независимости. Однако это лишь очень общее утверждение. Чтобы лучше понять концепцию субстанции Декарта, нам нужно иметь лучшее представление о том, как субстанции независимы. С одной стороны, в своих размышлениях о субстанции Декарт работает с традиционной концепцией независимости, согласно которой существование субстанции является независимым, в отличие от существования модуса, поскольку субстанции являются конечными субъектами.Соответственно, допустим, что субстанции независимы от субъектов. С другой стороны, в своем описании субстанции Декарт также работает с причинным чувством независимости. В конце концов, причина того, что Бог является единственной Субстанцией (в отличие от Созданной Субстанции ), заключается в том, что все остальное «может существовать только с помощью Божьего согласия» (Принципы I.51), и Декарт понимает это как причинное утверждение, что все остальное — творение Бога и требует его постоянного сохранения.Следовательно, ученые считают, что Декарт утверждал, что в целом: 1) Бог является как причинно, так и субъективно независимым (в конце концов, Бог не является модулем чего-либо еще), 2) сотворенные субстанции причинно независимы от всего, кроме Бога, и субъективно независимы, и iii) способы как причинно, так и субъективно зависят в том смысле, что они оба зависят от постоянного сохранения Богом и от сотворенных субстанций как субъектов. (См., Например, Markie 1994: 69; Rodriguez-Pereyra 2008: 79-80)
e.Сколько материальных веществ?
Что сотворенные субстанции причинно независимы от всего, но Бог предлагает поразительный вывод: несмотря на то, что, кажется, говорит Декарт, тела не являются материальными субстанциями, поскольку они недостаточно независимы. Тела причинно зависят от других тел множеством разных способов. Например, тела возникают и уничтожаются другими телами: человек является продуктом своих родителей и может умереть в результате удара автомобилем.Действительно, согласно одной научной традиции, есть только одна материальная вещь, которая удовлетворяет определению сотворенной субстанции Декартом — материальная вселенная в целом (см., Например, Cottingham 1986: 84-85). Опять же, следуя традиции, мы можем назвать эту точку зрения Монистической Интерпретацией , а противоположную точку зрения, что существует много материальных субстанций, Плюралистической Интерпретацией (для отдельной точки зрения см. Woolhouse 1993: 22-23). Таким образом, может показаться, что существует философское свидетельство монизма; Другими словами, может показаться, что взгляды Декарта на сотворенную субстанцию заставляют его думать, что материальная субстанция может быть только одна.Сторонники этой интерпретации утверждают, что есть также текстовые свидетельства, указывающие на отрывок в Синопсисе к Медитациям . Декарт пишет:
.[Нам] нужно признать, что тело, взятое в общем смысле, является субстанцией, чтобы оно тоже никогда не погибло. Но человеческое тело, поскольку оно отличается от других тел, просто состоит из определенной конфигурации конечностей и других случайностей такого рода; тогда как человеческий разум таким образом не состоит из каких-либо случайностей, а представляет собой чистую субстанцию.
Монисты читают «тело в общем смысле» как относящееся к материальной вселенной в целом. Следовательно, они рассматривают этот отрывок как утверждение, что материальная вселенная является субстанцией, а человеческое тело — нет, поскольку оно состоит из конфигурации конечностей и случайностей. Если предположить, что монисты правы, сразу возникают два вопроса. Во-первых, если тела не являются субстанциями, тогда что же они такое? Монисты обычно заявляют, что тела — это моды. В этом есть смысл: если тела не являются субстанциями, они должны быть модами, учитывая онтологию Декарта.Во-вторых, если Декарт не считает тела субстанциями, почему он так часто говорит так, как будто они есть? Монисты отвечают, что Декарт свободно говорит в этих контекстах, используя термин «субстанция» во вторичном или производном смысле этого слова.
Плюралисты высказали возражения по ряду причин. Во-первых, плюралисты оспорили текстовые свидетельства мониста, предложив альтернативные интерпретации Синопсиса. Во-вторых, они подвергли сомнению мотивацию монизма, указав, что монистическая интерпретация требует очень сильной концепции каузальной независимости и что не совсем ясно, придерживается ли это точка зрения Декарта.В-третьих, плюралисты отмечают, что, хотя Декарт во многих случаях пишет о телах как о субстанциях, он никогда четко не называет их модусами. Наконец, плюралисты отрицают, что Декарт мог утверждать, что тела являются модами, отмечая, что для Декарта: 1) части вещей не являются их модусами и 2) тела являются частями материальной вселенной. Хоффман 1986 кратко высказывает каждое из этих возражений. Для более продолжительных обсуждений см. Skirry 2005: Chapter 3 и Slowik 2001.
3. Спиноза
Самая важная работа Спинозы — это его «Этика , продемонстрированная в геометрическом порядке » — далее «Этика ».Спиноза работал над текстом на протяжении 1660–70-х годов. К этому времени философия Декарта стала широко читаемой, и действительно, на мышление Спинозы она оказала сильное влияние, в том числе и на его понимание субстанции. Тем не менее, взгляды Спинозы во многом расходятся и приводят к совершенно иной картине мира.
а. Отчет Спинозы о субстанции
Спиноза предлагает определение сущности на самой первой странице Ethics . Он пишет: «Под субстанцией я понимаю то, что есть в себе и задумано через себя…» (E1d3).Спиноза следует Декарту (и традиции) в определении субстанции как «самой по себе» или как конечного субъекта. Соответственно, он следует традиции, определяя «модус» как то, что принадлежит или переносится другим; как выразился Спиноза, режим — это «то, что есть в другом…» (E1d5). Обсуждение схоластико-аристотелевских корней определения Спинозы см. В Carriero 1995. Спиноза также следует Декарту, считая, что i) атрибуты являются основными свойствами субстанции, ii) среди этих атрибутов есть мышление и расширение, iii) все другие свойства сущности. субстанции передаются через этот атрибут или являются способами бытия; iv) Бог существует и является субстанцией.На этом соглашение заканчивается.
Первое очевидное отклонение от Декарта обнаружено в E1P5. Для Декарта существует множество расширенных субстанций (по крайней мере, в плюралистической интерпретации) и множество умов. Однако Спиноза считает, что это в корне неверно. На E1P5 Спиноза утверждает, что субстанция уникальна в своем роде — может быть только одна субстанция для каждого атрибута. Этот факт о субстанции (в сочетании с рядом других метафизических тезисов) имеет далеко идущие последствия для его понимания субстанции.
Отсюда следует, как утверждает Спиноза в E1P6, что быть субстанцией — значит быть причинно изолированным, на том основании, что i) существует только одна субстанция для каждого вида или атрибута и ii) причинные отношения могут иметь место только между вещами одного и того же вида. Однако причинная изоляция не влечет за собой причинную импотенцию. Существующая субстанция должна иметь причину в некотором смысле, но, будучи причинно изолированной, ее причина не может лежать ни в чем вне себя. Спиноза заключает, что субстанция «будет причиной самой себя… она относится к природе существующей субстанции» (E1P7).Не только субстанция является причиной самой себя, но Спиноза позже говорит нам, что это имманентная причина всего, что в ней есть (E1P18). Спиноза продолжает в E1P8, заявляя, что «каждая субстанция обязательно бесконечна». В целом Спиноза утверждает, что если существует только одна субстанция для каждого атрибута, то субстанция не может быть ограничена, поскольку ограничение — это причинное понятие, а субстанции причинно изолированы. Наконец, Спиноза утверждает, что субстанции неделимы. В E1P12-13 он утверждает, что если бы субстанция была делимой, то она делилась бы либо на части одной природы, либо на части другой природы.Если первое, то было бы более одного вещества одной и той же природы, что исключается E1P5. В последнем случае вещество может прекратить свое существование, что исключается E1P7; следовательно, субстанция не может быть разделена.
г. Какие есть вещества?
Какие существуют вещества с учетом этого объяснения природы вещества? Из того, что было сказано до сих пор в «Этике », было бы разумно предположить, что для Спинозы реальность состоит из следующих субстанций: Бог, одна расширенная субстанция, одна мыслящая субстанция и одна субстанция для каждого последующего атрибута. быть любым.Однако, как выясняется, это верно лишь отчасти. Верно, что Спиноза в конечном итоге считает, что Бог существует, что существует одна протяженная субстанция и одна мыслящая субстанция. Однако Спиноза отрицает, что это различных веществ. Одна мыслящая субстанция численно идентична одной расширенной субстанции, которая численно идентична Богу. Иначе говоря, существует только одна субстанция, Бог, и эта субстанция одновременно протяженная и мыслящая.
Официальный аргумент Спинозы в пользу этого вывода находится на E1P14.Он рассуждает так: Бог существует (что было доказано на E1P11). Учитывая, что Бог определяется как существо, обладающее всеми атрибутами (E1d6) и что существует только одна субстанция на атрибут (E1P5), из этого следует, что Бог является только субстанцией . Подробное обсуждение этого аргумента см. В статье IEP «Спиноза: метафизика».
Учитывая, что Бог — единственная субстанция, и онтология субстанции / моды Спинозы, отсюда следует, что материальные объекты нашего опыта не являются независимо существующими субстанциями, а, напротив, являются формами одной расширенной субстанции.Точно так же и умы, которые Декарт считал мыслящими субстанциями, согласно Спинозе, являются формами атрибута мышления.
Таким образом, мы получаем следующую картину реальности. Как и Декарт, Спиноза считает, что самое реальное — это Бог, от которого зависит все остальное. Однако нет никаких созданных веществ. Бог как единая субстанция обладает всеми атрибутами и, следовательно, является одновременно расширенной субстанцией и мыслящей. То, что Декарт принял за сотворенные субстанции, на самом деле являются гунами Бога.Тем не менее Спиноза соглашается с Декартом в том, что содержание реальности бывает двух видов — способы расширения и способы мышления, и существует множество обоих.
Это представление о природе субстанции дает картину метафизической структуры мира, совершенно отличную от Декарта (и от здравого смысла). В этой статье особое внимание уделяется трем вопросам: (i) Почему Спиноза не принимает созданные субстанции, (ii) Как субстанция может иметь более одного атрибута, и (iii) Как субстанция может быть неделимой, как предлагает Спиноза?
г.Почему Спиноза не создает субстанцию?
Спиноза не будет поддерживать различие Декарта между Substance и Created Substance по ряду причин. Во-первых, сотворенные субстанции — это причинные продукты Бога. Однако вещества причинно изолированы, и поэтому даже если бы было несколько веществ, одно не могло быть причинным продуктом другого. Во-вторых, как мы видели, Декарт считает, что, несмотря на их причинную зависимость от Бога, конечные умы и тела оправдывают название «субстанция», по крайней мере частично, потому что такие существа являются конечными субъектами.Спиноза соглашается, что быть конечным субъектом — неотъемлемая часть бытия субстанции; проблема в том, что конечные тела и умы не являются конечными субъектами. Официальные основания Спинозы для этого тезиса находятся в аргументах в пользу E1P4 и 5. В целом Спиноза утверждает, что от субстанций как конечных субъектов отличает то, что они могут быть индивидуализированы только с помощью атрибута. Согласно Спинозе, существует только два вида признаков, по которым объекты могут быть индивидуализированы — по атрибуту и по способу.Субстанции как конечные субъекты не могут быть индивидуализированы модами, поскольку субъекты метафизически предшествуют модам. Например, два конечных тела не индивидуализированы по атрибутам (поскольку оба они протяженные) и поэтому не могут быть субстанциями.
г. Как у вещества может быть более одного атрибута?
Как мы видели, для Декарта каждая субстанция имеет один — и только один — атрибут. С другой стороны, аргумент Спинозы в пользу субстанциального монизма утверждает, что существует субстанция, обладающая всеми атрибутами.Спиноза оправдывает этот шаг защитой; на E1P10s Спиноза утверждает, что ничто, что мы знаем об атрибутах, влечет за собой их принадлежность к разным субстанциям, и, следовательно, нет ничего незаконного в утверждении, что субстанция может иметь более одного атрибута. Хотя это заявленная защита Спинозы, ряд ученых заявили, что у Спинозы есть философские ресурсы, чтобы привести более веские аргументы. В частности, они утверждают, что у него есть положительный случай, что на самом деле субстанция, обладающая чем-то меньшим, чем все атрибуты (и, следовательно, только одним), невозможна.Вкратце, Лин 2007 просит нас предположить, что Спиноза ошибается и что может существовать субстанция, которая имеет меньше, чем все атрибуты (но по крайней мере, один). Спиноза является ярым сторонником принципа достаточного разума (см., Например, E1P8s2), согласно которому каждому факту есть объяснение. Из PSR следует, что существует объяснение того, почему рассматриваемое вещество не обладает всеми атрибутами. Однако любое такое объяснение должно апеллировать к существующим атрибутам (или атрибутам) вещества.Однако атрибуты концептуально независимы, и, следовательно, нельзя обращаться к существующему атрибуту для объяснения отсутствия другого. Для другой, но тесно связанной версии этого аргумента см. Della Rocca 2002.
e. Расширенная и неделимая субстанция?
В отличие от Декарта, Спиноза считает, что субстанция неделима, и это поднимает ряд вопросов о непротиворечивости спинозовской концепции субстанции. Например, как неделимость субстанции согласуется с утверждениями Спинозы о том, что (i) субстанция имеет множество атрибутов, составляющих ее сущность, и (ii) эта субстанция протяжена? Для обсуждения (i) см. Статью IEP «Спиноза: метафизика».Здесь основное внимание уделяется (ii).
Расширенная субстанция Спинозы, или Бог, рассматриваемый как атрибут протяженности, обычно понимается как охватывающая всю расширенную реальность (хотя альтернативу см. Woolhouse 1990). Согласно философской традиции, восходящей, по крайней мере, к «Федону » Платона , быть протяженным или телесным — значит иметь части, быть делимым и, следовательно, быть тленным. Спиноза, однако, считает, что «это относится к природе существования субстанции.Следовательно, из этого следует, что Спиноза не может последовательно утверждать, что субстанция расширена. Спиноза был хорошо осведомлен об этом аргументе, и его официальный ответ можно найти в E1P15s. Проблема с аргументом в том, что он «основан только на предположении, что телесная субстанция состоит из частей». На первый взгляд, это утверждение сбивает с толку: если протяженная или телесная субстанция — это всего лишь вся расширенная реальность, у нее обязательно есть части. Например, есть часть расширения, которая составляет индивидуальное человеческое тело, часть, которая составляет Атлантический океан, часть, которая составляет Землю, и т. Д.Несмотря на свою формулировку, Спиноза не отрицает, что расширенная субстанция имеет части во всех смыслах этого слова. Скорее, Спиноза особенно озабочен тем, чтобы противостоять идее о том, что его расширенная субстанция является составной субстанцией, построенной из частей, которые сами по себе являются субстанциями, и на которые она может быть разделена или разделена. Это имеет смысл, так как а) проблема заключается в отсутствии частей, а в том, что они подвержены искажению, и б) это представление о расширенной субстанции как делимой на дальнейшие расширенные субстанции — это как раз то, что Декарт (одно из главных влияний на мысль Спинозы). провести.
Спиноза в E1P15s аргументирует свою позицию двумя способами. Во-первых, Спиноза возвращает нас к аргументам E1P12 и 13 в пользу неделимости субстанции. Во-вторых, Спиноза предлагает новый аргумент, сфокусированный конкретно на расширенной субстанции, который, что интересно, не предполагает предшествующего аппарата Ethics . Отложив в сторону свои собственные предыдущие выводы, очевидная цель Спинозы состоит в том, чтобы показать, что точка зрения Декарта, согласно которой любая протяженная субстанция имеет части, которые сами являются протяженными субстанциями, не работает сама по себе.В целом он рассуждает следующим образом. Рассмотрим расширенное вещество, скажем, сырное колесо. Если части этого колеса сами являются протяженными субстанциями, то, по крайней мере в принципе, возможно, чтобы одна или несколько частей были уничтожены без каких-либо последствий для других частей. Идея здесь в том, что, поскольку субстанции являются независимыми субъектами, уничтожение одного субъекта не может иметь никаких последствий для других. Предположим, что середина нашего сырного колеса уничтожена; Таким образом, у нас остается «пончик» из сыра.Проблема в том, что отверстие в сыре измеримо — оно имеет диаметр, окружность и т. Д. Короче говоря, оно увеличено. Однако мы предположили, что протяженная субстанция — предмет расширения — в середине была разрушена. Таким образом, мы остаемся с примером атрибута, протяженности, без субстанции в качестве субъекта — что невозможно по стандартам как Декарта, так и Спинозы. Подробное обсуждение этого аргумента см. В Huenemann 1997 и Robinson 2009.
4.Лейбниц
Взгляды Лейбница основывались на отчетах Декарта и Спинозы. Фактически, Лейбниц переписывался со Спинозой в начале 1670-х годов и ненадолго встречался со Спинозой в 1676 году. В отличие от Спинозы, Лейбниц не написал ни одного авторитетного описания своей метафизической системы. Не только это, но и его метафизические взгляды значительно изменились за время его жизни. Тем не менее, можно выделить базовое объяснение природы субстанции, которое проходит через его средние и более поздние работы (от Discourse on Metaphysics 1686 до Monadology 1714).
а. Отчет Лейбница о веществах
Вещества независимы и являются окончательными предметами .
Подобно Декарту, Лейбниц думает, что Бог — единственная абсолютно независимая вещь, и что, кроме того, существуют сотворенные субстанции, которые «подобны отдельному миру, независимому от всех других вещей, кроме Бога» ( Discourse on Metaphysics § 8). Во-вторых, Лейбниц явно соглашается с Декартом, Спинозой и традицией в утверждении, что субстанции являются конечными носителями модусов или свойств.Он пишет: «Когда несколько предикатов приписываются одному субъекту и этот субъект не приписывается никакому другому, это называется индивидуальной субстанцией» (Там же).
Вещества являются единицами .
Для Лейбница быть единым целым — значит быть простым и лишенным частей, и поэтому основные составляющие реальности не являются составными или агрегированными существами. То, что субстанции просты, имеет метафизически важные последствия; Лейбниц заключает в «Принципах природы » и «Изящество» и других местах, что «Поскольку монады не имеют частей, они не могут быть ни сформированы, ни разрушены.Они не могут ни начаться, ни закончиться естественным образом, и, следовательно, они длятся столько же, сколько и вселенная ». Существо возникает естественно только в результате композиции; сущность уничтожается естественным образом только в результате распада или коррупции. Таким образом, только составные объекты можно естественным образом генерировать или разрушать. Лейбниц, однако, подчеркивает, что единство субстанций и вытекающая из этого простота полностью согласуются с наличием и изменением способов или свойств.
Вещества активные .
Сказать, что вещество является активным, значит сказать не только, что оно причинно эффективно, но и что оно является конечным (созданным) источником своих собственных действий. Так, он пишет: «Каждая субстанция обладает совершенной спонтанностью… что все, что с ней происходит, является следствием ее идеи или ее бытия, и что ничто не определяет ее, кроме одного Бога» (DM §32). Вещества, в некотором смысле, имеют всю свою историю, запечатленную в самой их природе. История каждой субстанции разворачивается последовательно, каждое состояние причинно вытекает из предыдущего состояния согласно законам.Из этого следует, что если бы мы в совершенстве знали состояние вещества в определенный момент и законы причинной последовательности, мы могли бы предвидеть всю жизнь вещества. Как изящно сформулировал Лейбниц в «Принципах природы и благодати », «настоящее чревато будущим; будущее можно прочитать в прошлом; дальнее выражается в ближайшем ».
Вещества причинно изолированы .
Как и Спиноза, Лейбниц считает, что вещества причинно эффективны, и что их эффективность не распространяется на другие вещества.Другими словами, хотя существует внутрисубстанциальная причинность (поскольку субстанции вызывают свои собственные состояния), межсубстанциональной причинности нет. Лейбниц предлагает несколько различных аргументов в пользу этого утверждения. В некоторых случаях он утверждает, что причинная изоляция следует из природы субстанции. Если состояние вещества может быть причинным эффектом другого вещества, то спонтанность и независимость вещества будут поставлены под угрозу. В другом месте он утверждает, что межсубстанциальная причинность сама по себе невозможна, утверждая, что единственный способ, которым одна субстанция может вызывать другую, — это фактическая передача акциденций или свойств.Так, Лейбниц классно пишет, что вещества «не имеют окон, через которые что-то может войти или выйти. Несчастные случаи не могут быть отделены, и они не могут происходить вне субстанций »( Monadology §7). Более подробное обсуждение взглядов Лейбница на причинно-следственную связь см. В статье IEP «Лейбниц: причинно-следственная связь».
г. Какие есть вещества?
Хотя Лейбниц соглашается с Декартом в том, что Бог — бесконечная субстанция, которая создала и сохраняет конечный мир, он не согласен с фундаментальными составляющими этого мира.По мнению Декарта, существует два основных типа конечных субстанций — мыслящие субстанции или умы и протяженные субстанции или тела. Лейбниц не согласен; согласно Лейбницу (и это особенно ясно в более поздних работах) не существует протяженных субстанций. Ничто расширенное не может быть субстанцией, поскольку ничто расширенное не является единством. Согласно Лейбницу, быть расширенным — значит быть фактически разделенным на части и, следовательно, быть совокупностью. Предельно созданные субстанции для Лейбница гораздо больше похожи на декартово мыслящие субстанции, и действительно, Лейбниц называет простые субстанции «разумом» или «душой».Эта терминология может сбивать с толку, и важно четко понимать, что, используя эти термины, Лейбниц не утверждает, что все простые субстанции являются индивидуальными человеческими сознаниями (хотя человеческие сознания — простые субстанции для Лейбница). Скорее, существует целый спектр простых веществ, особенно сложным примером которых является человеческий разум.
Таким образом, мы получаем следующую картину реальности. Бог существует и несет ответственность за создание и постоянное сохранение всего остального.Конечные составляющие реальности — это монады, которые являются неделимыми и непротяженными умами или подобными разуму субстанциями. Хотя монады причинно изолированы, у них есть свойства или качества, которые постоянно меняются, и эти изменения продиктованы самой природой монады. Изучение Лейбница субстанции и его метафизики в целом вызывает ряд вопросов. В этой статье речь пойдет, в частности, о трех. Во-первых, представление Лейбница о субстанции дает (в сочетании с рядом других метафизических обязательств) картину реальности, которая существенно расходится как со здравым смыслом, так и с Декартом и Спинозой.Как наш опыт расширенного мира причинных взаимодействий вписывается в метафизическую картину Лейбница? Во-вторых, то, что субстанции представляют собой единства, является ключевой чертой теории Лейбница, и важно понять, почему Лейбниц так противостоит составным субстанциям. Наконец, Спиноза и Лейбниц предлагают очень похожие описания сущности, но в итоге получают очень разные метафизические картины, и поэтому в этой статье мы рассмотрим, в чем разница между мнениями Лейбница и Спинозы.
г. Опыт и реальность
Как мир, в котором мы живем, вписывается в концепцию реальности Лейбница? Наш повседневный опыт — это причинно-следственные взаимодействия протяженных объектов, но для Лейбница на фундаментальном уровне нет межсубстанциальной причинности и нет протяженных субстанций.Как же тогда мир нашего опыта связан с миром таким, какой он есть на самом деле?
Начнем с очевидных причинно-следственных связей между вещами. Напомним, что для Лейбница монады активны и спонтанны. Каждый отдельный человеческий разум — это монада, а это означает, что весь человеческий опыт, включая его ощущения мира, является следствием его собственных предыдущих состояний. Например, ощущение того, что книга лежит на столе, вызвано не книгой (или светом, отражающимся от книги, попаданием в глаза и т. Д.).), а скорее прогресс в развитии истории, вписанной в природу человека. Хотя жизнь монады проистекает только из ее природы, Бог создал мир таким образом, чтобы жизни сотворенных монад полностью соответствовали друг другу. Лейбниц пишет в A New System of Nature ,
Бог изначально создал душу (и любое другое реальное единство) таким образом, что все должно возникать для нее из ее собственных глубин … но с совершенным соответствием по отношению к внешним вещам … Между всеми этими субстанциями будет совершенное согласие, производящее тот же эффект, который был бы замечен, если бы они передавались посредством передачи видов или качеств, как это делают обычные философы.
Таким образом, когда Кэти выходит из-за угла и видит Беатриче, а Беатрис видит Кэти, они делают это, потому что в самой природе Кэти было записано, что она будет видеть Беатриче, и в природе Беатрис, что она увидит Кэти. Это известная доктрина предустановленной гармонии Лейбница. Для получения дополнительной информации см. Статью IEP «Лейбниц: метафизика».
Как возникает наш опыт расширенного мира тел? Начнем с того, что Лейбниц определенно не считает, что тела построены из монад или составлены из них.Так, в своих заметках о комментариях Мишеля Анджело Фарделлы «» он пишет: «Как точка не является частью линии… так и душа не является частью материи». Вместо этого во многих случаях Лейбниц характеризует тела как явления или явления. Он пишет в часто цитируемом отрывке к ДеВольдеру:
.[М] Атлет и движение не являются субстанциями или вещами, а являются феноменами воспринимающих, реальность которых находится в гармонии воспринимающих с самими собой (в разное время) и с другими воспринимающими.
Лейбниц, кажется, говорит здесь и где-либо еще, что тела — это просто видимости (хотя и общие видимости), которые не соответствуют какой-либо независимой от разума реальности, и действительно, ряд ученых заявили, что это — рассмотренная точка зрения Лейбница (см., Например, Loeb 1981: 299-309). Однако в других текстах Лейбниц утверждает, что тела возникают из совокупностей монад или основаны на них, и это предполагает, что тела являются чем-то сверх простого восприятия монад. В целом, ученые предлагают интерпретации, которые пытаются учесть оба набора текстов и рассматривают тела как совокупность монад, которые воспринимаются как как расширенные.Однако ведется много споров о том, как такие агрегаты могут в конечном итоге быть связаны с телами и их восприятием (например, см. Rutherford 1995b: 143-153).
г. Что не так с составными существами?
Лейбниц считает, что составные существа исключены как возможные субстанции по ряду причин. Во-первых, никакая композиция не является (или не может быть) единством, поскольку, согласно Лейбницу, невозможно объединить два или более объекта в одно. Он классно иллюстрирует это утверждение, обращаясь к двум бриллиантам.Он пишет в своих письмах к Арно :
.Можно было бы навязать им одно и то же собирательное название… хотя они далеки друг от друга; но нельзя сказать, что эти два алмаза составляют субстанцию … Даже если бы они были сближены и соприкасались, они не были бы существенно объединены в какой-либо большей степени … контакт, общее движение и участие в общем плане не имеют никакого эффекта о субстанциальном единстве.
В общем, не существует отношения, в которое могут быть введены две или более сущности, которые объединяли бы их в одно существо.
Вторая и, возможно, еще более серьезная проблема с композитами состоит в том, что, согласно Лейбницу, они не могут быть конечными объектами. Он пишет, снова в « письмах к Арно »: «Также кажется, что то, что составляет сущность существа путем агрегирования, — это только способ вещей, из которых оно состоит. Например, то, что составляет сущность армии, — это всего лишь образ людей, составляющих ее ». Утверждение Лейбница состоит в том, что никакая совокупность не является субстанцией, потому что совокупности являются модами или состояниями своих частей, и никакая мода не является конечным субъектом.Однако это оставляет нас с вопросом: почему Лейбниц думает, что совокупности — это просто моды или состояния своих частей? В своей влиятельной книге R.C. Sleigh (1990: 123–124) утверждает, что основание Лейбница рассматривать агрегаты как модусы состоит в том, что агрегаты семантически и онтологически необязательны. То есть все, что верно в отношении совокупности, может быть выражено путем приписывания различных форм частям, и все это без обращения к самой совокупности. Это говорит нам о том, что все предполагаемые модусы совокупности на самом деле являются модами частей и, следовательно, совокупность не является конечным субъектом.Из онтологии субстанции / моды следует, что в той степени, в которой агрегаты существуют, они должны быть модами.
e. Лейбниц и Спиноза
Хотя Спиноза и Лейбниц предлагают очень разные картины структуры реальности, их соответствующие представления о субстанции во многом пересекаются: оба согласны с тем, что быть субстанцией должно быть по крайней мере i) конечным субъектом, ii) причинно изолированным, но причинно эффективным. , и iii) неделимы. Действительно, ряд ученых предположили, что Лейбниц на короткое время принял или, по крайней мере, был соблазнен спинозистской метафизикой в начале своей философской карьеры (см., Например, обсуждение в Adams 1994: 123–130).Даже в более позднем возрасте Лейбниц, кажется, высоко ценил взгляды Спинозы, говоря в письме Луи Бурге , что «[А] согласно Спинозе … существует только одна субстанция. Он был бы прав, если бы не было монад ». Учитывая это, стоит задуматься о том, где Лейбниц порывает со Спинозой и почему.
Хотя они различаются по ряду важных аспектов, возможно, наиболее заметное различие между метафизикой Спинозы и Лейбница состоит в том, что Лейбниц считает, что реальность разделена на две части: Бога и творение.Бог — это субстанция, и Он производит конечные субстанции — сотворенные монады. Это сигнализирует о разрыве со Спинозой по крайней мере по двум важным причинам. Во-первых, это означает, что соглашение Лейбница со Спинозой о причинной изоляции субстанций применимо только к сотворенным субстанциям; Хотя для Лейбница Бог — это субстанция, он не изолирован причинно. Напомним, что, по крайней мере, одна из причин, по которой Лейбниц отрицает межсущественную причинную связь, заключается в том, что для этого потребуется фактическая передача собственности или несчастных случаев, и что такая передача невозможна.Джолли (2005) утверждает, что для Лейбница причинная деятельность Бога имеет другой вид. Бог не производит эффектов метафизически невыносимым образом, и, следовательно, Бог не должен быть причинно изолирован.
Во-вторых, Лейбниц считает, в отличие от Спинозы, что созданные субстанции являются конечными субъектами. Лейбниц очень недвусмысленно возражает Спинозе по этому поводу. Хотя он согласен с тем, что субстанции требуют индивидуализации, он считает, что доказательство Спинозы на E1P5 того, что может быть только одна субстанция для каждой природы или атрибута, необоснованно.Кроме того, Лейбниц считает, что Монады могут быть индивидуализированы, в конечном счете утверждая в Монадологии , что «Монады… различаются по степени их различного восприятия».
5. Теории вещества XVII века в перспективе
Оглядываясь назад, мы можем увидеть Декарта, но особенно Спинозу и Лейбница, работающих над метафизическими последствиями утверждения, что субстанции являются конечными объектами. В более общем плане мы можем рассматривать эти теории субстанции как разные способы попытаться примирить понятие субстанции как конечного субъекта с приверженностью к существованию и независимости Бога.
Эпистемологические соображения заставили выдающихся философов конца 17 годов и 18 веков отказаться от таких вопросов и отвести субстанции гораздо более скромное место в своих метафизических системах. Джон Локк, например, считает, что существуют субстанции и что они являются конечными объектами, но опасается делать какие-либо дальнейшие выводы. Как известно Локк, «если кто-нибудь исследует себя относительно своего Понятия чистой Субстанции в целом , он обнаружит, что у него нет никакой другой Идеи об этом, а есть только предположение, что он не знает, какая поддержка таких качеств… обычно называемые несчастными случаями »( EHU 2.23.2). Дэвид Хьюм идет дальше, утверждая, что это не в наших силах знать окончательную структуру реальности, и что наше представление о субстанции как субъекте является просто результатом нашего воображения: «Воображение склонно симулировать нечто неизвестное и невидимое. , который, как предполагается, останется таким же при всех этих вариациях; и это непонятное нечто она называет субстанцией »( Трактат 1.4.3). Юмовский скептицизм по поводу субстанции (и метафизики в целом) в той или иной форме сохранился до наших дней.
Конечно, не все согласны с этой традицией, и природа субстанции была вопросом, которым занялись многие современные философы, хотя и с иных отправных точек, чем Декарт, Спиноза и Лейбниц. В отличие от 17, -го и -го века, в современном философском использовании термин «субстанция» не обязательно предназначен для обозначения основных составляющих реальности (хотя может). Скорее, этот термин обычно используется для обозначения того, что иногда называют «конкретными деталями», то есть отдельных материальных вещей или объектов.Более того, среди современных философов нет ничего похожего на консенсус, который мы находим среди 17 философов -го -го века относительно онтологии, зависимости, реальности и Бога. Таким образом, обычно считается, что существуют категории реальности за пределами субстанции и режима (или свойства), возможно, наиболее заметные из них — это события или процессы. Многие философы ставят под сомнение как отношение наследственности, так и связь между наследственностью и онтологической зависимостью. Например, теории связок субстанции отрицают, что субстанции вообще являются субъектами — они просто совокупности или совокупности свойств.Более того, большинство современных философов отрицают, что имеет смысл говорить о степенях реальности: вещи либо реальны, либо нет. Наконец, и, возможно, наиболее очевидно, современные философы больше не согласны с тем, что Бог существует и является субстанцией. О современных попытках предложить отчет по существу в духе дискуссий 17 -го -го века см. Hoffman and Rosenkrantz 1997.