Конспект «Основания (названия, получение, свойства)»
«Основания (названия, получение, свойства)»
Ключевые слова конспекта: названия оснований, получение оснований, химические свойства.
Основаниями или гидроксидами называют соединения металлов с гидроксогруппами ОН (одна или несколько групп ОН на каждый атом металла М, т.е. МОН или М(ОН)n). Гидроксогруппа ОН – это ион, ее заряд равен 1–, валентность I.
Названия оснований
В названии основания два слова: КОН – гидроксид калия. Если металл имеет переменную валентность, то ее указывают римской цифрой в скобках: Сг(ОН)3 – гидроксид хрома(III).
Чтобы составить формулу гидроксида по названию соединения, надо знать заряд катиона металла Мn+. Число гидроксогрупп в формуле равно величине этого заряда: М(ОН)n. Заряды катионов металлов можно узнать из таблицы растворимости.
Например, в гидроксиде калия заряд иона калия 1+, К+, поэтому формула КОН. В гидроксиде бария ион бария Ва2+, формула Ва(ОН)
Щелочи – это растворимые в воде основания (LiOH, NaOH, КОН, Ва(ОН)2, Са(ОН)2 ). Щелочи – очень едкие вещества, вызывают ожоги. При работе с ними надо особенно тщательно соблюдать правила техники безопасности, надевать очки и перчатки.
Для распознавания растворов щелочей используют индикаторы.

Индикаторы – это органические красители, изменяющие окраску в зависимости от состава раствора. Так, бесцветный раствор фенолфталеина в растворе щелочи становится малиновым. Фиолетовый раствор лакмуса в растворах щелочей становится синим, а оранжевый раствор метилоранжа приобретает интенсивно желтый цвет.
Нерастворимые основания – это практически нерастворимые в воде вещества, например гидроксид железа(III), гидроксид меди(II), гидроксид магния.
Основные оксиды
– это оксиды, которым соответствуют основания. Если элемент образует несколько оксидов, то оксид, соответствующий низшей степени окисления, является основным оксидом. Например, СrО и МnО – основные оксиды.Формулы основных оксидов можно вывести, вычитая необходимое число молекул воды из формулы основания. Например, для формул основных оксидов Na2O, СаО, Fe2O3:
а) 2NaOH – Н2O = Na2O;
б) Са(ОН)2 – Н2O = СаО;
в) 2Fe(OH)3 – ЗН2O = Fe2O3.

Получение оснований
Растворимые основания получают:
а) реакцией оксидов щелочных и щелочноземельных металлов с водой: ВаО + Н2O = Ва(ОН)2;
б) взаимодействием активных металлов (электроотрицательность которых 1,2 и меньше) с водой:
в) электролизом водного раствора соли, например хлорида натрия; при пропускании постоянного электрического тока через раствор на катоде выделяется водород, на аноде – хлор, а в растворе остается гидроксид натрия:
2NaCl + 2Н2O →электролиз→ Н2 ↑ + 2NaOH + Cl2 ↑.
Нерастворимые основания получают по реакции обмена растворимых солей со щелочами:
CuCl2 + 2NaOH = Cu(OH)2 ↓ + 2NaCl.
Химические свойства оснований
Нерастворимые основания – довольно неустойчивые соединения. Нагревание (300–400 °С) приводит к потере ими воды. Например, голубой гидроксид меди(II) при нагревании отщепляет воду и превращается в черный оксид меди(II):
Сu(ОН)2 → t → СuО + Н2O.


Конспект урока «Основания».
Следующая тема: «».
uchitel.pro
5.Опишите способы получения оснований
1. Реакции активных металлов ( щелочных и щелочноземельных металлов) с водой:
2Na + 2h3O = 2NaOH + h3
Ca + 2h3O = Ca(OH)2 + h3
2. Взаимодействие оксидов активных металлов с водой:
BaO + h3O = Ba(OH)2
3. Электролиз водных растворов солей:
2NaCl + 2h3O = 2NaOH + h3 + Cl2
6.Опишите химические свойства оснований
Щелочи
1. Действие на индикаторы.
лакмус – синий
метилоранж — жёлтый
Нерастворимые основания
—-
фенолфталеин — малиновый
2. Взаимодействие с кислотными оксидами.
2KOH + CO2 = K2CO3 + h3O —-
KOH + CO2 = KHCO3
3. Взаимодействие с кислотами (реакция нейтрализации)
NaOH + HNO3 = NaNO3 + h3 Cu(OH)2 + 2HCl = CuCl2 + 2h3O
4. Обменная реакция с солями
Ba(OH)2 + K2SO4 = 2KOH + BaSO4↓ —-3KOH+Fe(NO3)3 = Fe(OH)3 ↓ + 3KNO3
5. Термический распад.
— Cu(OH)2 t°= Cu2O + h3O
7. Опишите классификацию и номенклатуру кислот, приведите примеры
НОМЕНКАТУРА КИСЛОТ
1. БЕСКИСЛОРОДНЫЕ КИСЛОТЫ (Н+1 n Э -n )
Э + [o] + водородная кислота
HCl – хлороводородная кислота
HF – фтороводороная кислота
h3S – сероводородная кислота
h3Se – селеноводородная
2. КИСЛОРОДСОДЕРЖАЩИЕ КИСЛОТЫ (Н +1 Э +n
а) Степень окисления Э = № группы
Э + [ная] кислота
[овая]
б) Степень окисления Э < № группы
Э + [истая] кислота
H2S+6O4 — cерная кислота
H2S+4O3 – сернистая кислота
H3As+5O4 – мышьяковая кислота
H3As+3O3 – мышьяковистая кислота
8.Опишите способы получения кислот
Получение кислот
1. Взаимодействие кислотного оксида с водой (для кислородсодержащих кислот):
SO3 + h3O = h3SO4
P2O5 + 3h3O =2h4PO4
2. Взаимодействие водорода с неметаллом и последующим растворением полученного продукта в воде (для бескислородных кислот):
h3 + Cl2 = 2HCl
h3 + S = h3S
3. Реакциями обмена соли с кислотой
Ba(NO3)2 + h3SO4 = BaSO4↓ + 2HNO3
в том числе, вытеснение слабых, летучих или малорастворимых кислот из солей более сильными кислотами:
Na2SiO3 + 2HCl = h3SiO3↓ + 2NaCl
2NaCl(тв.) + h3SO4(конц.) t°= Na2SO4 + 2HCl
9.Опишите химические свойства кислот

10.Опишите классификацию и номенклатуру солей, приведите примеры
КЛАССИФИКАЦИЯ
1. Средние (нормальные) – продукт полного замещения атомов водорода в кислоте на металл
а) соли кислородсодержащих кислот
Н2SO4 → Na2SO4 – сульфат натрия
Н2SO3 → Na2SO3 – сульфит натрия
б) соли бескислородных кислот
HCl → KCl — хлорид калия

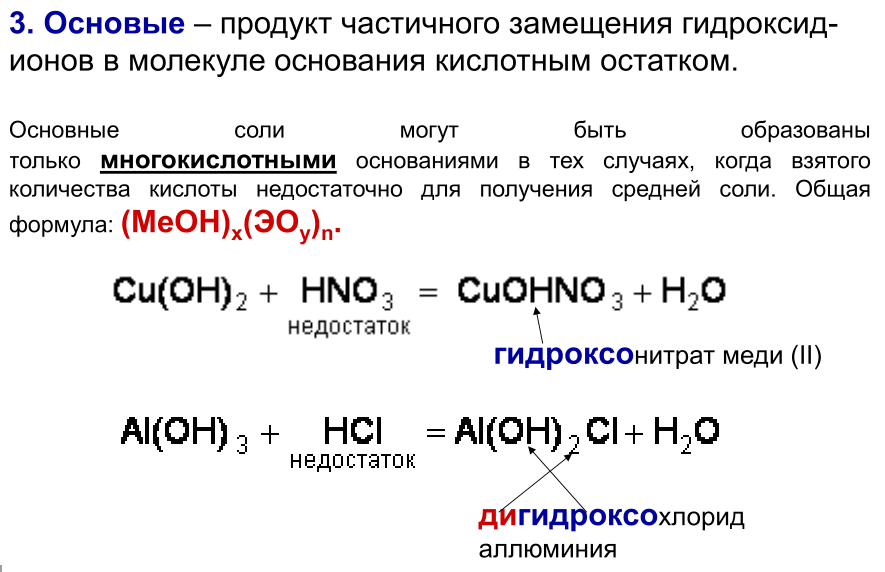
4. Двойные соли состоят из ионов двух разных металлов и кислотного остатка.
KNaCO3 – калий натрий карбонат
5. Смешанные соли – содержат один ион металла и анионы двух кислот.
AlCl(SO4) – алюминий хлорид сульфат.
6. Комплексные соли состоят из сложных (комплексных) ионов
[Ag(NH3)2] Cl
studfile.netХимические свойства
1. Основные оксиды взаимодействуют с водой с образованием оснований. Непосредственно в реакцию соединения с водой вступают только оксиды щелочных и щелочноземельных металлов:
Na2O + H2O → 2NaOH,
CaO + H2O → Ca(OH)2.
2. Взаимодействие с кислотами с образованием соли и воды:
CaO + H2SO4 → CaSO4 + H2O.
3. Взаимодействие с кислотными оксидами с образованием соли:
СaO + SiO2 
4. Взаимодействие с амфотерными оксидами:
СaO
+ Al2O3  Сa
(AlO2)2.
Сa
(AlO2)2.
3 Билет
Основания.
Основания — это сложные вещества, состоящие из атома металла, связанного с одной или несколькими гидроксильными группами — ОН. Общая формула:

Основаниями называются вещества, в которых атомы металла связаны с гидрокси-группами.
Химические свойства оснований
Химические свойства оснований характеризуются отношением их к кислотам, ангидридам кислот и солям.
1. Действуют на индикаторы. Индикаторы меняют свою окраску в зависимости от взаимодействия с разными химическими веществами. В нейтральных растворах – они имеют одну окраску, в растворах кислот – другую. При взаимодействии с основаниями они меняют свою окраску: индикатор метиловый оранжевый окрашивается в жёлтый цвет, индикатор лакмус – в синий цвет, а фенолфталеин становится цвета фуксии.
2. Взаимодействуют с кислотными оксидами с образованием соли и воды:
2NaOH + SiO2 → Na2SiO3 + H2O.
3. Вступают в реакцию с кислотами, образуя соль и воду. Реакция взаимодействия основания с кислотой называется реакцией нейтрализации, так как после её окончания среда становится нейтральной:
2KOH + H2SO4 → K2SO4 + 2H2O.
4. Реагируют с солями, образуя новые соль и основание:
2NaOH + CuSO4 → Cu(OH)2 + Na2SO4.
5. Способны при нагревании разлагаться на воду и основной оксид:
Cu(OH)2 = CuO + H2O.
Классификация:
По кислотности : одно кислотные и много кислотные
По растворимости: растворимые и нерастворимые
По силе: (не) сильно растворимые
По получению: прямые и косвенные
Получение оснований:
Взаимодействие активных металлов с водой только щелочи:
2Na+2h3O=2NaOH+h3
Взаимодействие основных оксидов с водой только щелочи :
Na2O+h3O=2NaOH
Взаимодействие солей со щелочами(малорастворимые основания):
Cu(+2)+2OH(-)=CuOh3
Электролиз водных растворов солей:
2NaCl+2h3O=2NaOH+h3+Cl2
Применение оснований:
Основания находят широкое применение в промышленности и быту.
Гидрокисд кальция «Ca(OH)2», или гашеная известь – он белый порошок. Если смешивать его с водой образуется известковое молоко. Так как гидроксид кальция совсем чуть чуть растворяется в воде, то после отфильтровывания известкового молока получается прозрачный раствор – известковая вода, она мутнеет при пропускании через неё оксида углерода. Вот такая реакция происходит: Ca(OH)2 + CO2 CaCO3+ h3O. Эта же реакция происходит при затвердении строительного раствора.
Гашеную известь могут применить в приготовления бордоской смеси — это средства борьбы с болезнями и насекомыми.
Известковое молоко могут использовать в химической промышленности например в производстве сахара, соды и тд
studfile.net
Основание (химия) — это… Что такое Основание (химия)?
У этого термина существуют и другие значения, см. Основание.Основа́ния — класс химических соединений.
В статье смысл термина «основание» раскрывается в первом, наиболее широко используемом значении — осно́вные гидрокси́ды.
Получение


Классификация
Основания классифицируются по ряду признаков.
- По растворимости в воде.
- Растворимые основания (щёлочи): гидроксид натрия NaOH, гидроксид калия KOH, гидроксид бария Ba(OH)2, гидроксид стронция Sr(OH)2, гидроксид цезия CsOH, гидроксид рубидия RbOH.
- Практически нерастворимые основания: Mg(OH)2, Ca(OH)2, Zn(OH)2, Cu(OH)2, Al(OH)3, Fe(OH)3, Be(OH)2.
- Другие основания: NH3·H2O
Деление на растворимые и нерастворимые основания практически полностью совпадает с делением на сильные и слабые основания, или гидроксиды металлов и переходных элементов
- По летучести.
- Летучие: NH3, CH3-NH2
- Нелетучие: щёлочи, нерастворимые основания.
- По стабильности.
- По наличию кислорода.
- По типу соединения:
- Неорганические основания: содержат одну или несколько групп -OH.
- Органические основания: органические соединения, являющиеся акцепторами протонов: амины, амидины и другие соединения.
Номенклатура
По номенклатуре IUPAC неорганические соединения, содержащие группы -OH, называются гидроксидами. Примеры систематических названий гидроксидов:
- NaOH — гидроксид натрия
- TlOH — гидроксид таллия(I)
- Fe(OH)2 — гидроксид железа(II)
Если в соединении есть оксидные и гидроксидные анионы одновременно, то в названиях используются числовые приставки:
- TiO(OH)2 — дигидроксид-оксид титана
- MoO(OH)3 — тригидроксид-оксид молибдена
Для соединений, содержащих группу O(OH), используют традиционные названия с приставкой мета-:
- AlO(OH) — метагидроксид алюминия
- CrO(OH) — метагидроксид хрома
Для оксидов, гидратированных неопределённым числом молекул воды, например Tl2O3•n H2O, недопустимо писать формулы типа Tl(OH)3. Называть такие соединениями гидроксидами также не рекомендуется. Примеры названий:
- Tl2O3•n H2O — полигидрат оксида таллия(III)
- MnO2•n H2O — полигидрат оксида марганца(IV)
Особо следует именовать соединение NH3•H2O, которое раньше записывали как NH4OH и которое в водных растворах проявляет свойства основания. Это и подобные соединения следует именовать как гидрат:
Химические свойства
- В водных растворах основания диссоциируют, что изменяет ионное равновесие:
- это изменение проявляется в цветах некоторых кислотно-основных индикаторов:
- При взаимодействии с кислотой происходит реакция нейтрализации и образуется соль и вода:
- Примечание: реакция не идёт, если и кислота и основание слабые.
- При избытке кислоты или основания реакция нейтрализации идёт не до конца и образуются кислые или осно́вные соли, соответственно:
- Амфотерные основания могут реагировать с щелочами с образованием гидроксокомплексов:
- Основания реагируют с кислотными или амфотерными оксидами с образованием солей:
- Основания вступают в обменные реакции (реагируют с растворами солей):
- Слабые и нерастворимые основания при нагреве разлагаются на оксид и воду:
- Некоторые основания (Cu(I), Ag, Au(I)) разлагаются уже при комнатной температуре.
См. также
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8
- Лидин Р.А. и др. Номенклатура неорганических веществ. — М.: КолосС, 2006. — 95 с. — ISBN 5-9532-0446-9
dic.academic.ru
Химическое основание — это… Что такое Химическое основание?
Основа́ния — класс химических соединений.
- Основания — (осно́вные гидрокси́ды) — вещества, молекулы которых состоят из ионов металлов или иона аммония и одной (или нескольких) гидроксогруппы (гидроксида) -OH. В водном растворе диссоциируют с образованием катионов и анионов ОН—. Название основания обычно состоит из двух слов: «гидроксид металла/аммония». Хорошо растворимые в воде основания называются щелочами.
- Согласно другому определению, основания — один из основных классов химических соединений, вещества, молекулы которых являются акцепторами протонов.
- В органической химии по традиции основаниями называют также вещества, способные давать аддукты («соли») с сильными кислотами, например, многие алкалоиды описывают как в форме «алкалоид-основание», так и в виде «солей алкалоидов».
- В статье смысл термина основание раскрывается в первом, наиболее широко используемом значении — осно́вные гидрокси́ды.
Способы получения оснований
- Получение щелочи при реакции сильноосновного оксида с водой
Так как только сильноосновные оксиды способны реагировать с водой, этот способ можно использовать исключительно для получения сильных оснований или щелочей.
CaO(т) + H2O(ж) → Ca(OH)2(p)Слабоосновные и амфотерные оксиды с водой не реагируют, и поэтому соответствующие им гидроксиды таким способом получить нельзя.
- Косвенное получение основания (гидроксида) при реакции соли со щелочью
Гидроксиды малоактивных металлов получают при добавлении щелочи к растворам соответствующих солей. Так как растворимость слабоосновных гидроксидов в воде очень мала, гидроксид выпадает из раствора в виде студнеобразной массы.
CuSO4(p) + 2NaOH(p) → Cu(OH)2(т)↓ + Na2SO4(p)- Получение щелочи при реакции замещения типичного металла с водой.
Ca+2H2O=Ca(OH)2+H2
Классификация оснований
- Растворимые в воде основания (щёлочи)
LiOH, NaOH, KOH, Ca(OH)2 , Ba(OH)2 , Sr(OH)2 , Ra(OH)2, CsOH, RbOH, FrOH
- Практически нерастворимые в воде гидрооксиды
Mg(OH)2, Zn(OH)2, Cu(OH)2, Al(OH)3, Fe(OH)3 , Be(OH)2
- Другие основания
NH3 × H2O
Деление на растворимые и нерастворимые основания практически полностью совпадает с делением на сильные и слабые, или гидроксиды типичных металлов и не типичных.
Химические свойства
1. Действие на индикаторы: лакмус — синий, метилоранж — жёлтый, фенолфталеин — малиновый,
2. Основание + кислота = Соли + вода Примечание:реакция не идёт, если и кислота, и щёлочь слабые. NaOH + HCl = NaCl + H2O
3. Щёлочь + кислотный или амфотерный оксид = соли + вода 2NaOH + SiO2 = Na2SiO3 + H2O
4. Щёлочь + соли = (новое)основание + (новая) соль прим-е:исходные вещества должны быть в растворе, а хотя бы 1 из продуктов реакции выпасть в осадок или мало растворяться. Ba(OH)2 + Na2SO4 = BaSO4+ 2NaOH
5.Слабые основания при нагреве разлагаются: Cu(OH)2+Q=CuO + H2O
6.При нормальных условиях невозможно получить гидроксиды серебра и ртути, вместо них в реакции появляются вода и соответствующий оксид: AgNO3 + 2NaOH(p) → NaNO3+Ag2O+H2O
См. также
Гидроксид
Wikimedia Foundation. 2010.
dic.academic.ru
Урок 38. Получение и применение оснований – HIMI4KA
В уроке 38 «Получение и применение оснований» из курса «Химия для чайников» рассмотрим способы получения щелочей и нерастворимых оснований, а ещё узнаем где в каких отраслях они применяются.


Поскольку растворимые и нерастворимые основания отличаются по свойствам, эти вещества получают разными способами.
Получение щелочей
Для получения щелочей можно использовать следующие реакции.
Взаимодействие активных металлов (Li, Na, К, Ca, Ba) с водой
Например:


Поскольку эти реакции протекают очень бурно (рис. 121), на практике их используют редко.


Взаимодействие оксидов активных металлов с водой
Например:


Некоторые щелочи (NaOH, KOH) получают, пропуская электрический ток через водные растворы солей NaCl или KCl. При этом наряду со щелочами образуются и другие ценные вещества — водород H2 и хлор Сl2.
Получение нерастворимых оснований
Нерастворимые основания получают взаимодействием растворимых оснований (щелочей) с солями. Образующиеся нерастворимые основания выделяются из растворов в виде осадков.


Применение оснований
Из всех оснований наиболее широкое применение находят щелочи. Раствор одной из них вы наверняка сможете найти дома. Эту жидкость под названием «Крот» используют в быту для промывания труб, идущих от кухонных раковин. Дело в том, что эти трубы постепенно засоряются остатками жира, которые мешают стоку воды. А щелочи обладают способностью растворять жиры. Поэтому достаточно в засоренную трубу влить небольшое количество «Крота», и через некоторое время проблема будет решена.
В последнее время в быту получили широкое распространение щелочные гели — густые жидкости, содержащие гидроксид натрия. Они предназначены для быстрого удаления остатков пригоревшего жира с поверхности кухонных плит и СВЧ- печей.
Большое количество гидроксида кальция используется в производстве сахара из сахарной свеклы. Некоторые области применения оснований показаны на рисунке 122.
Из нерастворимых оснований применение находят гидроксиды алюминия Al(OH)3 и магния Mg(OH)2. Они входят в состав медицинского препарата «Алмагель», который используют при заболеваниях пищеварительной системы.


Поскольку щелочи оказывают разрушающее действие на кожу, при их практическом использовании следует соблюдать правила безопасности.
Краткие выводы урока:
- Щелочи образуются при взаимодействии некоторых металлов и их оксидов с водой.
- Нерастворимые основания получаются в результате взаимодействия щелочей с солями.
Надеюсь урок 38 «Получение и применение оснований» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
himi4ka.ru
Основания — это… Что такое Основания?
Основа́ния — класс химических соединений.
- Основания — (осно́вные гидрокси́ды) — вещества, молекулы которых состоят из ионов металлов или иона аммония и одной (или нескольких) гидроксогруппы (гидроксида) -OH. В водном растворе диссоциируют с образованием катионов и анионов ОН—. Название основания обычно состоит из двух слов: «гидроксид металла/аммония». Хорошо растворимые в воде основания называются щелочами.
- Согласно другому определению, основания — один из основных классов химических соединений, вещества, молекулы которых являются акцепторами протонов.
- В органической химии по традиции основаниями называют также вещества, способные давать аддукты («соли») с сильными кислотами, например, многие алкалоиды описывают как в форме «алкалоид-основание», так и в виде «солей алкалоидов».
- В статье смысл термина основание раскрывается в первом, наиболее широко используемом значении — осно́вные гидрокси́ды.
Способы получения оснований
- Получение щелочи при реакции сильноосновного оксида с водой
Так как только сильноосновные оксиды способны реагировать с водой, этот способ можно использовать исключительно для получения сильных оснований или щелочей.
CaO(т) + H2O(ж) → Ca(OH)2(p)Слабоосновные и амфотерные оксиды с водой не реагируют, и поэтому соответствующие им гидроксиды таким способом получить нельзя.
- Косвенное получение основания (гидроксида) при реакции соли со щелочью
Гидроксиды малоактивных металлов получают при добавлении щелочи к растворам соответствующих солей. Так как растворимость слабоосновных гидроксидов в воде очень мала, гидроксид выпадает из раствора в виде студнеобразной массы.
CuSO4(p) + 2NaOH(p) → Cu(OH)2(т)↓ + Na2SO4(p)- Получение щелочи при реакции замещения типичного металла с водой.
Ca+2H2O=Ca(OH)2+H2
Классификация оснований
- Растворимые в воде основания (щёлочи)
LiOH, NaOH, KOH, Ca(OH)2 , Ba(OH)2 , Sr(OH)2 , Ra(OH)2, CsOH, RbOH, FrOH
- Практически нерастворимые в воде гидрооксиды
Mg(OH)2, Zn(OH)2, Cu(OH)2, Al(OH)3, Fe(OH)3 , Be(OH)2
- Другие основания
NH3 × H2O
Деление на растворимые и нерастворимые основания практически полностью совпадает с делением на сильные и слабые, или гидроксиды типичных металлов и не типичных.
Химические свойства
1. Действие на индикаторы: лакмус — синий, метилоранж — жёлтый, фенолфталеин — малиновый,
2. Основание + кислота = Соли + вода Примечание:реакция не идёт, если и кислота, и щёлочь слабые. NaOH + HCl = NaCl + H2O
3. Щёлочь + кислотный или амфотерный оксид = соли + вода 2NaOH + SiO2 = Na2SiO3 + H2O
4. Щёлочь + соли = (новое)основание + (новая) соль прим-е:исходные вещества должны быть в растворе, а хотя бы 1 из продуктов реакции выпасть в осадок или мало растворяться. Ba(OH)2 + Na2SO4 = BaSO4+ 2NaOH
5.Слабые основания при нагреве разлагаются: Cu(OH)2+Q=CuO + H2O
6.При нормальных условиях невозможно получить гидроксиды серебра и ртути, вместо них в реакции появляются вода и соответствующий оксид: AgNO3 + 2NaOH(p) → NaNO3+Ag2O+H2O
См. также
Гидроксид
Wikimedia Foundation. 2010.
dic.academic.ru