Соли — это сложные вещества, которые состоят из ионов металла и кислотного остатка
Задание1На какие группы и по каким признакам можно
разделить вещества , формулы которых
приведены ниже?
Na2O ; h3CO3; ;
Ca(NO3)2 CaCO3
h3SiO3
NaCl
Cr2S3
NaOH ; О2; Al2O3 ; Ca (OH)2 ; С
СаO ;
Аl; N2 ; Al(OH)3 ;
h3SO3 ; SO2 ; Ca; Na
формулы запишите в схему:
S ; СО2 ;
Соли
— это сложные
вещества, которые
состоят из ионов металла
и кислотного остатка
3 задание.
Определить : почему у солей разное
количество кислотных остатков
Дайте обоснованный ответ.
NaNO3
Ca (NO3 )2
Al (NO3 )3
3 задание.
Na+1
Ca+2
Al+3
Имеют разную степень окисления.
(см. таблицу растворимости)
задание 4.
Определить : почему у солей разное
количество ионов металла? Дайте
обоснованный ответ.
NaNO3
Na 2СO3
Na 3 Р-O4
Так как кислотные остатки имеют свою
степень окисления:
(см.

NO2-1- нитрит
NO3-1 — нитрат
SO3-2- сульфит
SO4-2 — сульфат
СO3-2-карбонат
Р-O4-3 — фосфат
Cl-1 — хлорид
SiO3-2 -силикат
Выведем общую
формулу солей?
+n
Ме
(К.
-m
О. )
n
11. Алгоритм названия солей
8Алгоритм названия солей
Название
Соли
Название
кислотного
остатка
Кислотные остатки
NO2-1- нитрит
NO3-1 — нитрат
SO3-2- сульфит
SO4-2 — сульфат
СO3-2-карбонат
Р-O4-3 — фосфат
Cl-1 — хлорид
SiO3-2 -силикат
Стр. 76 таблица
Название
металла в
родительном
падеже
С.О.
римскими
цифрами
12. Алгоритм названия солей
НазваниеСоли
Название
кислотного
остатка
Название
металла в
родительном
падеже
С.О.
римскими
цифрами
Fe+2(NO3-1)2 – нитрат железа (II)
Fe +3(NO3-1)3 – нитрат железа (III)
-2
ZnSO
AlCl
3
-14)
Cu (NO
3 2
13.
 задание 5. НАЗОВИТЕ СОЛИ NaCl
задание 5. НАЗОВИТЕ СОЛИ NaClFe +2SO4
Al3(PO4)3
Ca(NO3)2
Cu+2CO3
Cr2+3S3
Na2SO4
Ba(NO3 )2
14. задание 5. НАЗОВИТЕ СОЛИ
NaCl — хлорид натрияFe +2SO4 — сульфат железа (II)
Al3(PO4)3 – фосфат алюминия
Ca(NO3)2 — нитрат кальция
Cu+2CO3 – карбонат меди (II)
Cr2+3S3 – сульфид хрома (III)
Na2SO4 – сульфат натрия
Ba(NO3 )2 — нитрат бария
15. Контрольное задание1 Установите соответствие между формулой вещества и его названием
ФОРМУЛА ВЕЩЕСТВА1
2
3
Na2SO4
Cu2S
CuS
НАЗВАНИЕ ВЕЩЕСТВА
А
Сульфид меди (I)
Б
Сульфид меди (II)
В
Сульфат натрия
1
2
3
В
А
Б
2. Составление формул
солей по их названиям.
17. 1. Запиши рядом знаки химических элементов, которые входят в состав вещества.
Алгоритм составления формул солей:Составить химическую формулу
сульфата железа (III ) (первый способ)
Первый пункт выполнили переходим ко второму
Соли — это
сложные
вещества,
которые состоят
из ионов
металла и
остатка
Fe SO4
1.
 Запиши рядом знаки химических элементов,
Запиши рядом знаки химических элементов,которые входят в состав вещества.
17
18. 2. Над знаками химических элементов поставь их степень окисления.
Пример:Второй пункт выполнили переходим к третьему
+3
-2
Fe SO4
2. Над знаками химических элементов
поставь их степень окисления.
18
19. 3. Определи Н.О.К. чисел выражающих степень окисления этих элементов. Запиши Н.О.К. в квадратике над формулой.
Пример: Составить химическуюформулу сульфата железа (III).
Третий пункт выполнили переходим ко четвертому
Н.О.К. (наименьшее
общее кратное) –
это число,
которое делится
на исходные
числа без
остатка.
Таблица для
определения Н.О.К.
+3 -2
Fe SO4
1
2
3
4
5
6
7
1
1
2
3
4
5
6
7
2
2
2
6
4
10
6
14
3
3
6
3
12
15
6
21
4
4
4
12
4
20
24
28
5
5
10
15
20
5
30
35
6
6
6
6
12
30
6
42
7
7
14
21
28
35
42
7
6
3.
 Определи Н.О.К. чисел выражающих степень
Определи Н.О.К. чисел выражающих степеньокисления этих элементов.
Запиши Н.О.К. в квадратике над формулой.
19
20. 4. Раздели Н.О.К. на степень окисления каждого элемента. Запиши полученный индекс.
Пример: Составить химическуюформулу сульфата железа (III )..
Формула составлена
6
+3
-2
Fe (SO4)
2
6 : 3 =2
3
6 : 2 = 3
4. Раздели Н.О.К. на степень окисления каждого
элемента.
Запиши полученный индекс.
20
21. Составить формулу сульфата алюминия: (второй способ)
9Составить формулу сульфата алюминия:
(второй способ)
Составьте
формулы:
Упр. 3 стр. 78
Контрольное задание 2
Составьте формулу
хлорида кальция
СаCl2
Составьте формулу
нитрата натрия
NaNO3
Составьте формулу
Zn(SO4)2
Составьте формулу
нитрата меди (I)
Cu NO3
Составьте формулу
хлорида свинца (II)
PbCl2
3. Отдельные
Представители
стр.
 77 в таблицу
77 в таблицу2 хлорид натрия
название
хлорид
натрия
формула
Нахождение
в природе
Значение и применение
25. «Среди всех природных минеральных солей, самая главная та, которую мы называем просто “соль” А.Е.Ферсман
«Среди всех природных минеральных солей,самая главная та, которую мы называем просто
“соль”
А.Е.Ферсман
26. За 4 года человек съедает пуд соли
(в год человек с пищейпотребляет 3-5,5 кг
соли)
27. Соль в геральдике российских городов
Герб БахмутаГерб Энгельса
Герб Сольвычегодска
Герб Усолья-Сибирского
Герб Солигалича
Герб Дрогобыча
28. Добыча соли
из соляных шахтиз соленых озер
29. На озере Баскунчак ежегодно добывается около 5 млн. тонн соли
30. Применение NaCl
31. Д/З: CaCO3
32. Моллюски, раки, радиолярии, кораллы – все имеют известковый скелет
33. Большой Барьерный риф в Австралии
34. Меловые горы
35.
 Минералы карбоната кальция находятся в горных породах: Известняк
Минералы карбоната кальция находятся в горных породах: ИзвестнякМел
Мрамор
Мрамор
Мрамор
Мрамор
Травертин
36. Мрамор – строительный материал
Единственное в России здание, полностью построенное изнешлифованного мрамора — железнодорожный вокзал в
городе Слюдянка Иркутской области
37. Д/З: Фосфат кальция
— основа минераловфосфоритов
и апатитов
38. 3.КЛАССИФИКАЦИЯ: а)по растворимости
СОЛИЛабораторный опыт. №1
Определите растворимость солей
Для этого:
-прибавьте в первую пробирку к хлориду
натрия 5-10 мл воды ;
-прибавьте во вторую пробирку к карбонату кальция
5-10 мл воды
-Что произошло?
Вывод:
40. 3.КЛАССИФИКАЦИЯ: а)по растворимости
СОЛИРастворимые
NaCl
Нерастворимые
CaCO3
таблица растворимости
41. а)по составу
СОЛИ?
?
?
Лабораторный опыт. №2
Определите в какой из трех пробирок
находятся кислота, в какой щелочь, в
какой соль, хлорид натрия.

-прибавьте в пробирку №1
универсальный лакмус
-прибавьте в пробирку №2
универсальный лакмус
-прибавьте в пробирку №3
-универсальный лакмус
Что произошло?
таблицу:
Изменение окраски индикатора
Для кислот, также как и для щелочей, существуют
качественные реакции с помощью которых растворы
кислот можно распознать среди растворов других веществ.
Это реакции с индикаторами.
Название индикатора
В кислой среде
(H+1)
В нейтральной среде
(H+1 = ОH-1 )
В щелочной среде
(ОH-1 )
Окраска индикатора
универсального лакмуса
Контрольное задание3
Что сделали
Что наблюдали
Вывод
Ответте на вопросы:
1.Какая окраска индикатора в растворе хлорида
натрия. Почему?
2.Раствор хлорида натрия. является : кислым,
щелочным или нейтральным?
3. Следовательно соль хлорид натрия какая?
45. а)по составу
СОЛИсредние
NaCl
Ba(NO3)2
Кислые
?
Основные
?
Подведем итоги?
Контрольное задание — итоговое
Часть А (задания с выбором ответа)
1.
 Соли – это сложные вещества:
Соли – это сложные вещества:А) состоящие из ионов металлов и связанных с ними
одного или нескольких гидроксид- ионов.
Б) состоящие из ионов металлов и кислотных
остатков;
В) состоящие из двух химических элементов, один из
которых – кислород со степенью окисления -2;
Г) молекулы, которых состоят из ионов водорода и
кислотных остатков.
2. Хлорид железа (III) имеет формулу:
А) FeCl3;
B) Fe2O3;
Б) FeCl2;
Г) FeO.
Контрольное задание — итоговое
Часть В
Выбери лишнее вещество и объясни почему?
Игра « Третий лишний»
1. BaSO4; CaCO3; NaCl.
2. NaCl, Na2SO4, NaOH
3Al2(SO4)3, h3SO4, CaSO4
4. Cu(NO3)2, CuO, CuCl2
5. CaCl2, PbS, BaSO4.
Контрольное задание — итоговое
Часть А
1. Г
2. А
Часть В
объясни почему?
1. NaCl. т.к…
2. NaOH т.к…
3 h3SO4, т.к…
4. CuO, т.к…
5. CaCl т.к…
50. Домашнее задание
§,21 упр.3 стр. 78Составить презентацию фосфата
кальция или опорный конспект в форме
таблицы
Рефлексия
1.
 Сегодня я узнал…
Сегодня я узнал…2. Было интересно…
3. Было трудно…
4. Я выполнял задания…
5. Я понял, что…
6. Теперь я могу…
7. Я почувствовал, что…
8. Я приобрёл…
9. Я научился…
10. У меня получилось…
11. Я смог…
12. Попробую…
13. Меня удивило…
14.Урок мне дал для
жизни…
15. Мне захотелось…
Соли
Кроме катионов металлов в солях могут находиться катионы аммония Nh5+, фосфония Ph5+ и их органические производные, а также комплексные катионы и т. д
Если рассматривать соли как продукты протонов в кислотах или гидроксогрупп в основаниях, то можно выделить следующие типы солей:
— Средние (нормальные) соли — продукты замещения всех катионов водорода в молекулах кислоты на катионы металла (Na 2CO3, K3PO4).
— Кислые соли
—
продукты частичного замещения катионов водорода в кислотах на катионы металла (NaHCO3, K2HPO4). Они образуются при нейтрализации основания избытком кислоты (то есть в условиях недостатка основания или избытка кислоты).
Они образуются при нейтрализации основания избытком кислоты (то есть в условиях недостатка основания или избытка кислоты).
— Основные соли — продукты неполного замещения гидроксогрупп основания (OH—) кислотными остатками ((CuOH)2CO3). Они образуются в условиях избытка основания или недостатка кислоты.
— Простые соли — соли, состоящие из одного вида катионов и одного вида анионов (NaCl).
— Двойные соли — соли, содержащие два различных катиона (KAl(SO4)2·12 H2O).
— Смешанные соли — соли, в составе которых присутствует два различных аниона (Ca(OCl)Cl).
Также различают гидратные соли (кристаллогидраты), в состав которых входят молекулы кристаллизационной воды, например, Na2SO4·10 H2O, и комплексные соли, содержащие комплексный катион или комплексный анион (K4[Fe(CN)6], [Cu(NH3)4](OH)2. Внутренние соли образованы биполярными ионами, то есть молекулами, содержащими как положительно заряженный, так и отрицательно заряженный атом.
Названия солей, как правило, связаны с названиями соответствующих кислот. Поскольку многие кислоты в русском языке носят тривиальные, или традиционные, названия, подобные названия (нитраты, фосфаты, карбонаты и др.) также сохраняются и для солей.
Традиционные названия солей состоят из названий анионов в именительном падеже и названий катионов в родительном падеже[10]. Названия анионов строятся на основе русских или латинских названий кислотообразующих элементов. Если кислотообразующий элемент может иметь одну степень окисления, то к его названию добавляют суффикс — ат:
CO32- — карбонат,
GeO32- — германат.
Если кислотообразующий элемент может принимать две степени окисления, то для аниона, образованного этим элементом в более высокой степени окисления, применяют суффикс -ат, а для аниона с элементов в меньшей степени окисления — суффикс -ит:
SO42- — сульфат,
SO32- — сульфит.
Если элемент может принимать три степени окисления, то для высшей, средней и низшей степени окисления используют соответственно суффиксы -ат, -ит и суффикс -ит с приставкой гипо-:
NO3- — нитрат,
NO2— — нитрит,
NO22- — гипонитрит.
Наконец, в случае элементов, принимающих четыре степени окисления, для высшей степени окисления применяют приставку пер- и суффикс -ат, далее (в порядке понижения степени окисления) суффикс -ат, суффикс -ит и суффикс -ит с приставкой гипо-:
ClO4— — перхлорат,
ClO3— — хлорат,
ClO2— — хлорит,
ClO— — гипохлорит.
Приставки мета-, орто-, поли-, ди-, три-, пероксо- и т. п., традиционно присутствующие в названиях кислот, сохраняются также и в названиях анионов.
Названия катионов соответствуют названиям элементов, от которых они образованы: при необходимости указывается число атомов в катионе (катион диртути(2+) Hg22+, катион тетрамышьяка(2+) As42+) и степень окисления атома, если она переменная.
Названия кислых солей образуются путём добавления приставки гидро- к названию аниона. Если на один анион приходится больше одного атома водорода, то его количество указывают при помощи умножающей приставки (NaHCO3 — гидрокарбонат натрия, NaH2PO4 — дигидрофосфат натрия). Аналогично, для образования названий основных солей используются приставки гидроксо- ((FeOH)NO3 — гидроксонитрат железа(II)).
Кристаллогидратам дают названия, добавляя слово гидрат к традиционному или систематическому названию соли (Pb(BrO3)2·H2O — гидрат бромата свинца(II), Na2CO3·10H2O — декагидрат карбоната натрия). Если известна структура кристаллогидрата, то может применяться номенклатура комплексных соединений ([Be(h3O)4]SO4 — сульфат тетрааквабериллия(II)).
Для некоторых классов солей существуют групповые названия, например, квасцы — для двойных сульфатов общего вида MIMIII(SO4)2·12H2O, где MI — катионы натрия, калия, рубидия, цезия, таллия или аммония, а MIII — катионы алюминия, галлия, индия, таллия, титана, ванадия, хрома, марганца, железа, кобальта, родия или иридия.
Для более сложных или редких солей применяются систематические названия, образующиеся по правилам номенклатуры комплексных соединений. Согласно данной номенклатуре, соль подразделяется на внешнюю и внутреннюю сферы (катион и анион): последняя состоит из центрального атома и лигандов — атомов, связанных с центральным атомом. Название соли формируют следующим образом. Вначале записывают название внутренней сферы (аниона) в именительном падеже, состоящее из названий лигандов (приставок) и центрального элемента (корня) с суффиксом -ат и указанием его степени окисления. Затем к названию добавляют названия атомов внешней сферы (катионов) в родительном падеже.
LiBO3 — триоксоборат(III) лития
Na2Cr2O7 — гептаоксодихромат(VI) натрия
NaHSO4 — тетраоксосульфат(VI) водорода-натрия
Для образования названий солей бескислородных кислот пользуются общими правилами составления названий бинарных соединений: применяются либо универсальные номенклатурные правила с указанием числовых приставок, либо способ Штока с указанием степени окисления, причём второй способ является предпочтительным.
Названия галогенидов составляются из названия галогена с суффиксом -ид и катиона (NaBr — бромид натрия, SF6 — фторид серы(VI), или гексафторид серы, Nb6I11 — ундекаиодид гексаниобия). Кроме того, существует класс псевдогалогенидов — солей, которые содержат анионы с галогенидоподобными свойствами. Их названия образуются подобным образом (Fe(CN)2 — цианид железа(II), AgNCS — тиоцианат серебра(I)).
Названия галогенидов составляются из названия галогена с суффиксом -ид и катиона (NaBr — бромид натрия, SF6 — фторид серы(VI), или гексафторид серы, Nb6I11 — ундекаиодид гексаниобия). Кроме того, существует класс псевдогалогенидов — солей, которые содержат анионы с галогенидоподобными свойствами. Их названия образуются подобным образом (Fe(CN)2 — цианид железа(II), AgNCS — тиоцианат серебра(I)).
Халькогениды, содержащие в качестве аниона серу, селен и теллур, называют сульфидами, селенидами и теллуридами. Сероводород и селеноводород могут образовывать кислые соли, которые называют гидросульфидами и гидроселенидами соответственно (ZnS — сульфид цинка, SiS2 — дисульфид кремния, NaHS — гидросульфид натрия). Двойные сульфиды называют, указывая два катиона через дефис: (FeCu)S2 — дисульфид железа-меди.
Сероводород и селеноводород могут образовывать кислые соли, которые называют гидросульфидами и гидроселенидами соответственно (ZnS — сульфид цинка, SiS2 — дисульфид кремния, NaHS — гидросульфид натрия). Двойные сульфиды называют, указывая два катиона через дефис: (FeCu)S2 — дисульфид железа-меди.
Практически все соли являются сильными электролитами, т.е. в водных растворах полностью диссоциируют на ионы. Характер диссоциации зависит от типа соли.
Нормальные (средние) соли:
NaCl → Na+ + Сl— хлорид натрия
Al2(SO4)3 → 2Al3++ 3SO42- сульфат алюминия
NH4NO3 → NH4+ + NO3— нитрат аммония
Кислые соли:
KHCO3 → К+ + НСО3— гидрокарбонат калия
Ca(H2PO4)2 → Са2+ + 2Н2РO42- дигидрофосфат кальция
NH4HS → NH4+ + HS— гидросульфид аммония
Основные соли:
CuOHBr → CuOH+ + Br—гидроксобромид меди (II) (бромид гидроксомеди (II))
Fe(OH)2NO3 → Fe(OH)2+ + NO3— дигмдроксонитрат железа (III)
(Ni(OH))2SO4 → 2NiOH+ + SO42- гидроксосульфат никеля (II)
Двойные соли:
K2SO4 • Al2(SO4)3 → 2K+ + 2Al3+ + 4SO42- сульфат калия-алюминия
или:
KAl(SO4)2 → K+ + Al3+ + 2SO42-
Комплексные соли:
[Ag(NH3)2]Cl → [Ag(NH3)2]+ + Cl— хлорид диаммин серебра (I)
K3[Fe(CN)6] → 3K+ + [Fe(CN)6]3- гексацианоферрат (III) калия
Большинство солей являются твердыми веществами с ионной кристаллической решеткой. Соли s- и р-металпов, как правило, бесцветны. Многие соли d- элементов окрашены.
Соли s- и р-металпов, как правило, бесцветны. Многие соли d- элементов окрашены.
Растворимость солей в воде варьируется в широких пределах. (См. таблицу растворимости.) Хорошо растворимыми являются практически все соли натрия, калия, аммония; соли азотной кислоты (нитраты), соляной кислоты (хлориды), уксусной кислоты (ацетаты). Плохо растворимы в воде многие фосфаты (соли Н3РO4), карбонаты (соли Н2СO3), сульфиды (соли H2S).
Характерными для солей являются следующие типы реакций:
1) реакции ионного обмена, в ходе которых катионы или анионы солей образуют малодиссоциирующие или малорастворимые вещества при связывании с ионами реагентов;
2) окислительно-восстановительные реакции, в ходе которых катионы или (и) анионы солей выступают либо в роли окислителей, либо в роли восстановителей;
3) реакции разложения солей, происходящие без переноса электронов.
Реакции данного типа возможны, если хотя бы один из продуктов реакции представляет собой:
а) слабый электролит;
б) осадок;
в) газообразное вещество.
— Взаимодействие с растворами щелочей (возможны для растворимых солей)
(1) CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4
Сu2+ + 2OH— = Cu(OH)2
(2) NH4NO3 + KOH = KNO3 + NH3↑ + H2O
NH4+ +OH— = NH3↑ + H2O
(3) Na2CO3 + Ba(OH)2 = 2NaOH + BaCO3↓
CO32- + Ba2+ = BaCO3↓
(4) KHCO3 + KOH = K2CO3 + H2O
HCO3— + OH— = CO32- + H2O
(5) Fe(OH)2Cl + NaOH = Fe(OH)3↓ + NaCl
Fe(OH)2+ + OH— = Fe(OH)3↓
— Взаимодействие с кислотами
(6) Na2CO3 + 2HCl = 2NaCl + CO2↑ + H2O
CO32- + 2H+ = CO2↑ + H2O
(7) CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O
CaCO3 + 2H+ = Ca2+ + CO2↑ + H2O
(8) NaHCO3 + HCl = NaCl + CO2↑ + H2O
HCO3— + H+ = CO2↑ + H2O
(9) Na2S + H2S = 2NaHS
S2- + H2S = 2HS—
(10) MgOHCl + HCl = MgCl2 + H2O
MgOH+ + Н+ = Mg2+ + H2O
(11) AgNO3 + HCl = AgCl↓ + HNO3
Ag+ + Сl— = AgCl↓
(12) BaCl2 + H2SO4 = BaSO4↓ + 2HCl
Ba2+ + SO42- = BaSO4↓
(13) Pb(NO3)2 + H2S = PbS↓ + 2HNO3
Pb2+ + H2S = PbS↓ + 2H+
— Взаимодействие солей друг с другом (возможны для растворимых солей)
(14) AgNO3 + NaCl = AgCl↓ + NaNO3
Ag+ + Сl— = AgCl↓
(15) Ba(NO3)2 + K2SO4 = BaSO4↓ + 2K(NO3
Ba2+ + SO42- = BaSO4↓
(16) CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl
Ca2+ + CO32- = CaCO3↓
(17) Zn(NO3)2 + K2S = ZnS↓ + 2KNO3
Zn2+ + S2- = ZnS↓
(18) NH4HCO3 + NaCl = NaHCO3↓ + NH4CI
HCO3— + Na+ = NaHCO3↓
(19) 2К3[Fe(CN)6] + 3FeSO4 = Fe3[Fe(CN)6]2 + 3K2SO4,
2[Fe(CN)6]3- + 3Fe2+ = Fe3[Fe(CN)6]2
(20) FeCl3 + 3NH4SCN ↔ Fe(SCN)3 + 3NH4Cl
Fe3+ + 3SCN— ↔ Fe(SCN)3 (слабый электролит)
Многие обменные реакции являются качественными реакциями на катионы и анионы:
реакция (2) — на катион Nh5+; реакции (6, 7, 8) — на анион СO32- ; реакции (11,14) — на катион Аg+ и анион Сl—; реакции (12,15) — на катион Ва2+ и анион SO42- ; реакция (13) — на анион S2-; реакция (19) — на катион Fe2+; реакция (20) — на катион Fe3+.
Реакции, в которых катион соли играет роль окислителя
а) взаимодействие растворов солей с металлами (более активные металлы восстанавливают менее активные металлы из растворов их солей):
Cu+2SO4 + Fe = Сu0 + FeSO4
Hg+2(NO3)2 + Сu = Hg0 + Cu(NO3)2
б) взаимодействие растворов солей с другими восстановителями:
2Fe+3Cl3 + 2KI = 2Fe+2Cl2 + l2 + 2KCl
8AgNO3 + PH3 + 4H2O = 8Ag + h4PO4 + 8 HNO3
— Реакции, в которых катион соли играет роль восстановителя
2Fe+2Cl2 + Cl2 = 2Fe+3Cl3
4Cr+2Cl2 + 4HCl + O2 = 4Cr+3Cl3 + 2H2O
10Fe+2SO4 + 2KMnO4 + 8H2SO4 = 5Fe+32(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
2Cr+3Cl3 + 3NaBiO3 + 7NaOH + H2 = 2Na2CrO4 + 3Bi(OH)3 + 6NaCl
— Реакции, в которых анион соли играет роль окислителя
2KMn+7O4 + 16HCl = 2Mn+2Cl2 + 5Cl2↑ + 2KCl + 8H2O
K2Cr+72O7 + 3H2O2 + 4H2SO4 = Cr+32(SO4)3 + 3O2 + K2SO4 + 7H2O
2KMn+7O4 + 3C2H4 + 4H2O = 2Mn+4O2↓ + 3C2H4(OH)2 + 2KOH
2KN+5O3 + 3C + S = N02↑ + 3CO2↑ + K2S
2KN+5O3 + 3C + S — черный порох
— Реакции, в которых анион соли играет роль восстановителя
2KI-1 + Cl2 = I02 + 2KCl
3PbS-2+ 8HNO3 = 3PbS+6O4 + 8NO + 4Н2O
Na2S+4O3 + I2 + Н2O = Na2S+6O4 + 2HI
2КСr+3O2 + ЗPbO2 + 2КОН = 2K2Cr+6O4 + ЗРbО + Н2O
5KN+3O2 + 2КМnO4 + 3H2SO4 = 5KN+5O3 + 2MnSO4 + K2SO4 + 3H2O
— Реакции, в которых и катион и анион соли играют роль восстановителей
4Fe+2S-12 + 11O2 = 2Fe+32O3 + 8S+4O2
10Fe+2S-1 + 36HNO3(разб. ) = 10Fe+3(NO3)3 + 10S0/sup> + 3N2 + 18H2O
) = 10Fe+3(NO3)3 + 10S0/sup> + 3N2 + 18H2O
— Реакции внутримолекулярного окисления-восстановления
N-3H4N+3O2 = N02↑ + 2H2O
N-3H4N+5O3 = N+12O↑+ 2H2O
2KCl+5O-23 = 2KCl-1 + 3O02↑
2KN+5O-23 = 2KN+3O2 + O02↑
2Cu(N+5O-23)2 = 2CuO + 4N+4O2↑ + O02↑
Ag+1N+5O-23 = 2Ag0 + 2N+4O2↑ + O02↑
2KMn+7O-24 = K2MnO4 + Mn+4O2 + O02↑
Если анион соли не проявляет окислительных свойств, то такие соли, как правило, разлагаются без изменения степеней окисления:
СаСО3 = CaO + CO2↑
Са(HCO3)2 = СаСО3↓ + H2O + CO2↑
Mg(HCO3)2 = Mg(ОH)2↓ + 2CO2↑
(CuOH)2CO3 = 2CuO + CO2↑ + H2O
ZnSO4 = ZnO + SO3↑
(NH4)2SO4 = NH3↑ + NH4HSO4
NH4Cl = NH3↑ + HCl↑
Ниже представлены способы получения солей на примере растворимой соли бескислородной кислоты (хлорид натрия) и нерастворимой соли кислородсодержащей кислоты (сульфат бария).
1) основание + кислота: NaOH + HCl = NaCl + H2O
2) основной оксид + кислота: Na2O + 2HCl = 2NaCl + H2O
3) металл + кислота: 2Na + 2HCl = 2NaCl + H2↑
4) щелочь + соль: 2NaOH + CuCl2 = 2NaCl + Cu(OH2)↓
5) соль + кислота: Na2CO3 + 2HCl = 2NaCl + CO2↑ + H2O
6) соль + соль: Na2SO4 + BaCl2 = 2NaCl + BaSO4↓
7) металл + неметалл: 2Na + Cl2 = 2NaCl
8) гидрид + кислота: NaH + HCд = NaCд + H2↑
1) основание + кислота: Ba(OH)2 + H2SO4 = BaSO4↓ + 2H2O
2) основной оксид + кислота: BaO + H2SO4 = BaSO4↓ + H2O
3) металл + кислота: Ba + H2SO4(разб.) = BaSO4↓ + H2↑
4) щелочь + соль: Ba(OH)2 + Na2SO4 = BaSO4↓ + 2NaOH
5) соль + кислота: BaCl2 + H2SO4 = BaSO4↓ + 2HCl
6) соль + соль: Ba(NO3)2 + Na2SO4 = BaSO4↓ + 2NaNO3
7) основной оксид + кислотный оксид: BaO + SO3 = BaSO4↓
8) щелочь + кислотный оксид: Ba(OH)2 + SO3 = BaSO4↓ + H2O
Первые 6 способов получения являются идентичными для обеих солей.
Почему в клинике все без соли? -Питание
Почему в клинике все без соли?Мы с малых лет привыкаем солить еду во время ее приготовления, а иногда еще и в тарелке. А в сущности соль состоит из хлористого натрия, который сам по себе не приносит пользы организму. В составе соли нет органических веществ, она не содержит витаминов и, при этом, она входит в список трудноперевариваемых продуктов, поэтому это неорганическое вещество в виде пищевых добавок не только не оказывает питательного эффекта, но к тому же еще и может принести немалый вред. Поваренная соль наносит вред человеческому организму одновременно по двум системам пищеварительной и кровеносной.
Пищеварительная система страдает от разъедающих способностей соли. Легко сделать вывод, что первый удар выпадает на желудок, в который хлорид натрия направляется прямо из пищевода, а затем страдают и почки. Здоровый желудок с перевариванием соли обычно справляется достаточно хорошо, растворяя ее желудочным соком. А вот при различного рода заболеваниях этого внутреннего органа употребление данного продукта необходимо прекратить. Одним из примеров является гастрит. Эта болезнь вызывает острое воспаление слизистой оболочки желудка. У человека начинается отрыжка, рвота, сильная боль. И если к этому вдобавок происходит попадание в воспаленный орган большого количества поваренной соли, то рискнем предположить, что подобный процесс вряд ли окажет на организм целебное воздействие. Скорее, как раз произойдет наоборот – соль послужит катализатором для дальнейшего обострения.
А вот при различного рода заболеваниях этого внутреннего органа употребление данного продукта необходимо прекратить. Одним из примеров является гастрит. Эта болезнь вызывает острое воспаление слизистой оболочки желудка. У человека начинается отрыжка, рвота, сильная боль. И если к этому вдобавок происходит попадание в воспаленный орган большого количества поваренной соли, то рискнем предположить, что подобный процесс вряд ли окажет на организм целебное воздействие. Скорее, как раз произойдет наоборот – соль послужит катализатором для дальнейшего обострения.
Почкам поваренная соль причиняет вреда гораздо больше, так как это фильтр тела с очень нежной структурой и чутким восприятием, поэтому неорганический химический элемент – соль, почки переносят тяжело. Если человек употребляет пищевой соли больше, чем могут переработать почки, то «белая смерть» частично остается в организме, становясь причиной различных видов опухолей. Влияние поваренной соли на почки ведет к различным почечным заболеваниям, например нефриту (поражение почечных клубочков и как следствие воспалительный процесс), нефрозу ( повреждение почечных канальцев).
Проникая в организм человека через кровеносную систему, соль становится участником разрушительного процесса, где поражает систему кровоснабжения и наносит вред водно-солевому обмену организма. Между кровяной и тканевой жидкостями происходит регулярный обмен, тем самым происходит постоянный выход влаги из кровяных сосудов в ткани организма (процесс транссудации). В случаях, когда количество выделяемой жидкости кровеносными сосудами больше, обратно ими всасываемой, образуется скопление воды в тканях, и получается отек. Внешние признаки отека это набухание кожных покровов, наиболее ярко выражены, как правило на лице, руках и ногах. Очень часто отеки возникают в качестве спутников ряда болезней.
Скопление соли в кровеносных сосудах благоприятствует возникновению тромбов (сгустков крови, образующие наросты на стенках сосудов, состоящие из соединительной ткани, замедляющие кровообращение). Сейчас уже каждый может легко себе представить разрушительные возможности подобных образований. Следствием тромбов становятся многие заболевания, некоторые из которых могут иметь смертельный исход: тромбоз, тромбофлебит, коронарная недостаточность, ишемия миокарда, стенокардия, инфаркт миокарда, гангрена.
Следствием тромбов становятся многие заболевания, некоторые из которых могут иметь смертельный исход: тромбоз, тромбофлебит, коронарная недостаточность, ишемия миокарда, стенокардия, инфаркт миокарда, гангрена.
Повышенное содержание в крови хлорида натрия способствует развитию атеросклероза – еще одного вида заболеваний кровеносных сосудов. При его действии стенки сосудов набухают, становятся неровными. Внутри артерий разрастается соединительная ткань, появляются атеросклеротические бляшки. В итоге сосуды забиваются, сужается просвет, и происходит недостаточное питание сердца кровью. Употребление большого количества поваренной соли во время атеросклероза – путь, целенаправленно ведущий на уничтожение собственного здоровья. Этот продукт необходимо исключить из своего рациона. Следствием атеросклероза мозговых сосудов может явиться инсульт.
Конечно не следует приписывать мощную разрушительную силу только соли, иначе она бы была ядом и на нее наложили бы запрет использования еще в древности первые алхимики. Однако поваренная соль в совокупности с другими факторами способна нанести немалый вред здоровью. А к уже имеющимся болезням хлорид натрия может добавить серьезные осложнения. «Белая смерть» служит хорошим помощником алкоголизму, курению, наркомании, нервным перегрузкам в деле разрушения нормальной работы человеческого организма.
Однако поваренная соль в совокупности с другими факторами способна нанести немалый вред здоровью. А к уже имеющимся болезням хлорид натрия может добавить серьезные осложнения. «Белая смерть» служит хорошим помощником алкоголизму, курению, наркомании, нервным перегрузкам в деле разрушения нормальной работы человеческого организма.
Вред, наносимый человеку поваренной солью, приводит к убеждению о необходимости удаления этого продукта из ежедневного рациона не только заболевшего человека, но и здоровому такая мера так же не будет вредна. А ведь есть целые народы которые не используют часто поваренную соль, например народы Севера: чукчи, скажем, едят морскую мороженую рыбу, не добавляя туда ни грамма соли и на вкус такое блюдо, между прочим, очень даже неплохое.
Следует учитывать и то, что природа мудра, и во всех «живых» продуктах она распределила те пропорции компонентов, которые были им необходимы. То же касается и соли. Она содержится и в моркови, и в капусте, и в мясе. Причем объемы этого элемента отвечают тем требованиям, которые диктует нам наше здоровье. Следовательно, добавлять соль нет никакой надобности – она и так есть везде.
Следовательно, добавлять соль нет никакой надобности – она и так есть везде.
Таким образом, практически всем пациентам нашей клиники необходима бессолевая диета и гипертоникам (людям, страдающим нарушением кровообращения), и беременным (у которых из-за отеков увеличивается и без того немалая нагрузка на ноги), и с проблемами почек, и курящим (этот процесс заставляет вены сужаться, заметно повышая давление), и даже если Вы молоды и восстанавливаетесь после операции на аппендицит.
Если необходимость бессолевой диеты сомнения у вас не вызывает, то это не значит, что следует забыть о блюдах, ставших давно привычными.
Есть множество возможностей подсолить, например, бессолевой борщ, НО ЕСЛИ В ВАШЕМ КОНКРЕТНОМ СЛУЧАЕ ЭТО НЕ ЗАПРЕЩЕНО ВРАЧОМ.
Придать супу соленый вкус можно, если добавить лимонный сок или петрушку. Солоновато-горький вкус любистка так же поможет выйти из положения. Имеют слегка горьковатый вкус и, тем самым, прекрасно заменяют соль: тмин, кумин, розмарин, семена сельдерея. Одновременно с этим, в травах содержится множество нужных нам витаминов и минералов. Тем самым, замена соли травами или соком лимона позволяет не только снизить риск ряда болезней, например, сердечно-сосудистых заболеваний или болезней почек, но и улучшить свой иммунитет, повысить жизненный тонус.
Одновременно с этим, в травах содержится множество нужных нам витаминов и минералов. Тем самым, замена соли травами или соком лимона позволяет не только снизить риск ряда болезней, например, сердечно-сосудистых заболеваний или болезней почек, но и улучшить свой иммунитет, повысить жизненный тонус.
Сколько соли не вредит вашему организму?
- Джессика Браун
- BBC Future
Автор фото, Getty Images
По мнению некоторых ученых, диета с низким содержанием соли может так же вредить организму, как и ее чрезмерное ее потребление. Так сколько соли на самом деле должно быть в сбалансированном питании?
В прошлом году сексапильный турецкий шеф-повар Нусрет Гекче стал звездой соцсетей благодаря своей оригинальной манере готовить стейк. Гекче театральным жестом через локоть посыпал мясо солью, за что и получил прозвище Salt bae.
Впрочем, внимание привлекло не только его поварское мастерство.
Несмотря на регулярные предупреждения о вреде чрезмерного потребления соли, большинство из нас одержимы ею.
В последнее время, однако, становится более популярным противоположное мнение.
Оно ставит под сомнение десятки лет исследований, но при этом проливает свет на некоторые особенности нашей любимой приправы.
Хлорид натрия, основное вещество в составе соли, имеет важное значение для нашего организма.
Он необходим для поддержания баланса жидкости, транспортировки кислорода и питательных веществ, а также передачи электрических импульсов нашей нервной системой.
Автор фото, Getty Images
Підпис до фото,В 100 г голубого сыра содержится 2,7 г соли — это больше, чем в морской воде
Впрочем, человечество потребляет заметно больше соли, чем рекомендуют специалисты, которым приходится без устали напоминать нам об опасности «белой смерти».
Суточная норма соли для взрослого — не более 6 граммов. Британцы в среднем потребляют около 8, американцы — 8,5.
Впрочем, три четверти нашего ежедневного потребления соли происходится на покупные продукты, в частности, хлеб, соусы и злаки.
Добавляет путаницы и тот факт, что производители на этикетках часто указывают содержание натрия, а не соли, а это значит, что соли мы потребляем больше, чем думаем.
Соль состоит из ионов натрия и хлорида. В 2,5 г соли содержится около 1 г натрия.
«Широкой общественности это неизвестно, мы думаем, что натрий и соль — одно и то же. Никто вам этого не объясняет», — говорит диетолог Мэй Симпкин.
Как показывают исследования, чрезмерное потребление соли влияет на артериальное давление, риск развития инсульта и сердечных заболеваний. В целом эксперты соглашаются, что показания о вреде чрезмерного количества соли являются убедительными.
Потребление соли заставляет наш организм удерживать жидкость, повышая артериальное давление, пока организм не удалит ее излишки вместе с мочой.
Автор фото, Getty Images
Підпис до фото,Большое ведро соленого попкорна (примерно 250 г) содержит почти суточную норму соли — 5 г
По данным Всемирной организации здравоохранения, в 62% случаев это является причиной инсульта и в 49% — сердечной недостаточности.
Метаанализ 13 исследований, опубликованных в течение 35 лет, показал, что 5 г соли сверх нормы ежедневно повышают суммарный риск сердечно-сосудистых заболеваний на 17%, а риск инсульта — на 23%.
Было бы логичным предположить, что сокращение дневной нормы соли иметь обратный эффект.
Это подтверждает ряд исследований, в ходе которых снижение ежедневного потребления соли на 1,4 г, способствовало падению артериального давления и, следовательно, снижению до 42% риска смерти от инсульта и до 40% — смертности от сердечных заболеваний.
Впрочем, в таких исследованиях, когда ученые наблюдают за последствиями определенных изменений в диете людей, очень трудно отделить, что именно повлияло на положительный результат: уменьшение потребления соли или общие изменение системы питания и образа жизни.
Те, кто следят за потреблением соли, обычно также уделяют большее внимание здоровой пище, занимаются спортом, меньше курят и не употребляют алкоголь.
Автор фото, Getty Images
Підпис до фото,Тарелка супа мисо содержит 2,7 г соли
Долгосрочные исследования, в которых можно было бы сравнить последствия переедания с диетой с низким содержанием соли, проводятся нечасто из-за недостаточного финансирования и этических вопросов.
«Провести рандомизированное контролируемое исследование влияния соли на организм практически невозможно», — отмечает Франческо Капуччио, профессор кардиологии и эпидемиологии в медицинской школе Университета Уорвика.
«Впрочем подобных исследований ожирения или курения также нет, что нам не мешает осознавать их опасность».
Повышенная чувствительность к соли
Осложняет ситуацию еще один фактор — влияние потребления соли на артериальное давление и здоровье сердечно-сосудистой системы заметно отличается у отдельно взятых людей.
Исследования показывают, что чувствительность нашего организма к соли варьируется у разных людей и зависит от многих факторов, например этнической принадлежности, возраста, индекса массы тела, состояния здоровья и семейной история гипертонии.
Автор фото, MARCELOKRELLING
Підпис до фото,Два кусочка суши нигири содержат около 0,5 г соли, а столовая ложка соевого соуса еще 2,2 г
Некоторые исследования обнаружили связь между повышенной чувствительностью к соли и риском развития высокого кровяного давления.
С другой стороны, некоторые ученые теперь утверждают, что диета с низким содержанием соли может так же вызвать гипертонию.
Иными словами, зависимость между потреблением соли и высоким артериальным давлением напоминает по форме букву U, нижняя часть которой является порогом нормы.
Так, в ряде исследований было обнаружено, что негативные последствия для здоровья имеет как потребление более 12,5 г, так и менее 5,6 г соли в день.
В ходе другого исследования при участии более 170 тысяч человек были сделаны похожие выводы.
«Низкое» потреблением соли, то есть менее 7,5 г, было связано с высоким риском сердечно-сосудистых заболеваний и смерти у людей как с гипертонией, так и без, против «умеренного» потребления — до 12,5 г (от 1,5 до 2,5 чайных ложек соли) в сутки.
Автор фото, Getty Images
Підпис до фото,Мясные деликатесы, например индейка, ветчина и жареная говядина, содержат около 1,5 г соли на порцию, а два ломтика цельнозернового пшеничного хлеба — еще 0,6 г
Интересно, что это «умеренное» потребление почти вдвое превышает рекомендованную в Великобритании суточную норму.
«Такой оптимальный уровень потребления определен для любых жизненно важных питательных веществ», — отмечает Эндрю Менте, диетолог-эпидемиолог из Университета Макмастера в Онтарио.
«То есть опасно, как чрезмерное потребление, когда вещество оказывает токсическое воздействие на организм, так и низкое потребление, что приводит к развитию дефицита», — объясняет специалист.
Не все с этим согласны.
По мнению Франческо Капуччио, исследований в данной области все еще недостаточно.
К тому же некоторые из них имеют существенные недостатки в объективности данных.
Автор фото, Getty Images
Підпис до фото,Хоть кекс на вкус и сладкий, он также содержит около 1 г соли
В частности, исследование Менте, в ходе которого использовали единственный анализ мочи натощак, вместо «золотого стандарта», то есть сбора мочи в течение 24 часов.
Сара Стеннер, директор по научным исследованиям благотворительной организации British Nutrition Foundation, соглашается, что положительный результат уменьшения потребления соли у людей с гипертонией доказан.
Кроме того, довольно мало людей потребляют 3 или меньше грамма соли в день. Этот уровень некоторые из исследователей называют опасно низким.
Достичь этого очень сложно, по крайней мере учитывая содержание соли в готовых продуктах, которые мы потребляем.
Не существует единого мнения и по поводу того, может ли здоровое питание и физическая активность компенсировать высокое потребление соли.
Автор фото, Getty Images
Підпис до фото,100 г пиццы пепперони может содержать 1,9 г соли
Некоторые исследователи, как например Сара Стеннер, утверждают, что диета, богатая калием, который содержится в фруктах, овощах, орехах и молочных продуктах, помогает компенсировать вредное воздействие соли на артериальное давление.
Сеу Матеус, старший преподаватель кафедры экономики здравоохранения в Ланкастерском университете, советует прежде всего обратить внимание на содержание скрытой соли в пищевых продуктах, чем пытаться исключить ее потребление.
«Мы должны помнить, что чрезмерное потребление соли является очень вредным, но полностью исключать ее из рациона не надо», — объясняет специалист.
Сейчас точно известно только то, что чрезмерное потребление соли повышает артериальное давление.
А последние исследования, предупреждающие об опасности низкого содержания соли в диете и индивидуальной чувствительности к ней, нужно воспринимать с долей скепсиса.
Или, как говорят англичане, «со щепоткой соли».
Прочитать оригинал этой статьи на английском языке вы можете на сайте BBC Future.
Хотите поделиться с нами своими жизненными историями? Напишите о себе по адресу [email protected], и наши журналисты с вами свяжутся.
Российские ученые выяснили, почему «жидкие соли» проводят ток
https://ria.ru/20190610/1555447481.html
Российские ученые выяснили, почему «жидкие соли» проводят ток
Российские ученые выяснили, почему «жидкие соли» проводят ток — РИА Новости, 10.06.2019
Российские ученые выяснили, почему «жидкие соли» проводят ток
Ученые из «Сколтеха» и зарубежных научных центров выяснили, как так называемые ионные жидкости, жидкие соли, могут проводить электрический ток. Их выводы и… РИА Новости, 10.06.2019
Их выводы и… РИА Новости, 10.06.2019
2019-06-10T15:20
2019-06-10T15:20
2019-06-10T15:20
наука
москва
открытия — риа наука
сколковский институт науки и технологий
химия
физика
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/150834/40/1508344063_0:3:1036:586_1920x0_80_0_0_c87168730dc7aa80130e729bd5a39cf8.jpg
МОСКВА, 10 июн – РИА Новости. Ученые из «Сколтеха» и зарубежных научных центров выяснили, как так называемые ионные жидкости, жидкие соли, могут проводить электрический ток. Их выводы и возможные применения подобных соединений были представлены в журнале Physical Review X.Ионные жидкости, по сути, представляют собой жидкие соли. В то время как их обычные «кузены», такие как вода или бензин, состоят из электрически нейтральных молекул, молекулы ионных жидкостей несут электрические заряды.Неорганические соли переходят в подобное состояние только при высоких температурах, однако в последние годы химики открыли сразу несколько сложных органических веществ с подобным устройством, которые остаются жидкими при комнатной температуре. Ионные жидкости обладают массой интересных свойств, которые позволят в будущем использовать их для создания нетоксичных, но при этом жидких проводников, экзотических растворителей, суперконденсаторов и различных компонентов электроники и электрических сетей, в том числе движущихся частей роботов.Проблема, как отмечает Бриллиантов, заключается в том, что ученые до сих пор не до конца понимают и спорят о том, как именно ионные жидкости проводят ток. Дело в том, что подобные соединения должны содержать в себе равное число положительно и отрицательно заряженных ионов, нейтрализующих друг друга при сближении.Иными словами, свободных носителей заряда в подобной жидкости не должно быть и она должна быть изолятором, а не проводником, однако в реальности наблюдается совершенно обратная картина. Российские физики и их зарубежные коллеги, как сообщает пресс-служба «Сколтеха», нашли объяснение этому, создав математическую модель «жидкой соли».Как оказалось, механизм электропроводности в таких жидкостях весьма необычен.
Ионные жидкости обладают массой интересных свойств, которые позволят в будущем использовать их для создания нетоксичных, но при этом жидких проводников, экзотических растворителей, суперконденсаторов и различных компонентов электроники и электрических сетей, в том числе движущихся частей роботов.Проблема, как отмечает Бриллиантов, заключается в том, что ученые до сих пор не до конца понимают и спорят о том, как именно ионные жидкости проводят ток. Дело в том, что подобные соединения должны содержать в себе равное число положительно и отрицательно заряженных ионов, нейтрализующих друг друга при сближении.Иными словами, свободных носителей заряда в подобной жидкости не должно быть и она должна быть изолятором, а не проводником, однако в реальности наблюдается совершенно обратная картина. Российские физики и их зарубежные коллеги, как сообщает пресс-служба «Сколтеха», нашли объяснение этому, создав математическую модель «жидкой соли».Как оказалось, механизм электропроводности в таких жидкостях весьма необычен. Большую часть времени ионы внутри них действительно проводят в нейтральном состоянии, объединяясь в пары с носителями противоположного заряда или в более крупные структуры.С другой стороны, как показали расчеты ученых, почти незаметные тепловые флуктуации, неизбежно возникающие в разных частях жидкости, заставляют подобные структуры распадаться на очень короткое время и потом заново соединяться.В результате этого, электричество движется через «жидкие соли», подобно атлетам, участвующим в своеобразном многоборье. Пока ионы находятся в свободном состоянии, они поддерживают электрический ток, а затем «передают эстафету» следующей партии частиц. Нечто похожее, как отмечают ученые, происходит в полупроводниках, через которые электричество движется благодаря взаимодействию «дырок» и электронов.С другой стороны, как отмечает Бриллиантов, эта идея не может объяснить всех парадоксов ионных жидкостей. Дело в том, что число свободных ионов, которые фиксируются внутри жидких солей во время экспериментов с ними, значительно ниже, чем предсказывает данная теория.
Большую часть времени ионы внутри них действительно проводят в нейтральном состоянии, объединяясь в пары с носителями противоположного заряда или в более крупные структуры.С другой стороны, как показали расчеты ученых, почти незаметные тепловые флуктуации, неизбежно возникающие в разных частях жидкости, заставляют подобные структуры распадаться на очень короткое время и потом заново соединяться.В результате этого, электричество движется через «жидкие соли», подобно атлетам, участвующим в своеобразном многоборье. Пока ионы находятся в свободном состоянии, они поддерживают электрический ток, а затем «передают эстафету» следующей партии частиц. Нечто похожее, как отмечают ученые, происходит в полупроводниках, через которые электричество движется благодаря взаимодействию «дырок» и электронов.С другой стороны, как отмечает Бриллиантов, эта идея не может объяснить всех парадоксов ионных жидкостей. Дело в том, что число свободных ионов, которые фиксируются внутри жидких солей во время экспериментов с ними, значительно ниже, чем предсказывает данная теория. Почему это так, ученым еще предстоит выяснить.
Почему это так, ученым еще предстоит выяснить.
https://ria.ru/20190418/1552813187.html
https://ria.ru/20190530/1555114436.html
москва
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2019
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdnn21.img.ria.ru/images/150834/40/1508344063_127:0:911:588_1920x0_80_0_0_89b069094b73f65c85a42e2b260520d8.jpgРИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og. xn--p1ai/awards/
xn--p1ai/awards/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
москва, открытия — риа наука, сколковский институт науки и технологий, химия, физика
МОСКВА, 10 июн – РИА Новости. Ученые из «Сколтеха» и зарубежных научных центров выяснили, как так называемые ионные жидкости, жидкие соли, могут проводить электрический ток. Их выводы и возможные применения подобных соединений были представлены в журнале Physical Review X.«Мы с коллегами ожидаем, что явления, наблюдаемые в полупроводниках, будут обнаружены в ионных жидкостях комнатной температуры. Нам кажется, что они найдут множество важных применений», — заявил Николай Бриллиантов, профессор Сколковского института науки и технологий.
Ионные жидкости, по сути, представляют собой жидкие соли. В то время как их обычные «кузены», такие как вода или бензин, состоят из электрически нейтральных молекул, молекулы ионных жидкостей несут электрические заряды.
Неорганические соли переходят в подобное состояние только при высоких температурах, однако в последние годы химики открыли сразу несколько сложных органических веществ с подобным устройством, которые остаются жидкими при комнатной температуре.
18 апреля 2019, 14:24НаукаРоссийские физики подобрали идеальный материал для создания лазеровИонные жидкости обладают массой интересных свойств, которые позволят в будущем использовать их для создания нетоксичных, но при этом жидких проводников, экзотических растворителей, суперконденсаторов и различных компонентов электроники и электрических сетей, в том числе движущихся частей роботов.
Проблема, как отмечает Бриллиантов, заключается в том, что ученые до сих пор не до конца понимают и спорят о том, как именно ионные жидкости проводят ток. Дело в том, что подобные соединения должны содержать в себе равное число положительно и отрицательно заряженных ионов, нейтрализующих друг друга при сближении.
Иными словами, свободных носителей заряда в подобной жидкости не должно быть и она должна быть изолятором, а не проводником, однако в реальности наблюдается совершенно обратная картина. Российские физики и их зарубежные коллеги, как сообщает пресс-служба «Сколтеха», нашли объяснение этому, создав математическую модель «жидкой соли».
Российские физики и их зарубежные коллеги, как сообщает пресс-служба «Сколтеха», нашли объяснение этому, создав математическую модель «жидкой соли».
Как оказалось, механизм электропроводности в таких жидкостях весьма необычен. Большую часть времени ионы внутри них действительно проводят в нейтральном состоянии, объединяясь в пары с носителями противоположного заряда или в более крупные структуры.
С другой стороны, как показали расчеты ученых, почти незаметные тепловые флуктуации, неизбежно возникающие в разных частях жидкости, заставляют подобные структуры распадаться на очень короткое время и потом заново соединяться.
30 мая 2019, 16:40НаукаУченые из МФТИ превратили кинескоп телевизора в «вечную» лампочкуВ результате этого, электричество движется через «жидкие соли», подобно атлетам, участвующим в своеобразном многоборье. Пока ионы находятся в свободном состоянии, они поддерживают электрический ток, а затем «передают эстафету» следующей партии частиц. Нечто похожее, как отмечают ученые, происходит в полупроводниках, через которые электричество движется благодаря взаимодействию «дырок» и электронов.
С другой стороны, как отмечает Бриллиантов, эта идея не может объяснить всех парадоксов ионных жидкостей. Дело в том, что число свободных ионов, которые фиксируются внутри жидких солей во время экспериментов с ними, значительно ниже, чем предсказывает данная теория. Почему это так, ученым еще предстоит выяснить.
Синтетические катиноны («соли для ванн») DrugFacts
Что такое синтетические катиноны?
Синтетические катиноны, более известные как соли для ванн, представляют собой искусственные стимуляторы, химически связанные с катиноном, веществом, содержащимся в растении кат. Кат — это кустарник, выращиваемый в Восточной Африке и на юге Аравии, где некоторые люди жуют его листья из-за их мягкого стимулирующего действия. Созданные человеком версии катинона могут быть намного сильнее, чем натуральный продукт, а в некоторых случаях очень опасны. 1
Только наименование
Продукты с синтетическим катиноном, продаваемые как соли для ванн, не следует путать с такими продуктами, как английская соль, которую люди используют во время купания. Эти средства для купания не содержат ингредиентов, изменяющих сознание.
Эти средства для купания не содержат ингредиентов, изменяющих сознание.
Синтетические катиноны обычно имеют форму белого или коричневого кристаллоподобного порошка и продаются в небольших пластиковых или фольгированных упаковках с пометкой «не для употребления в пищу». Они могут быть помечены как соль для ванн, растительная пища, средство для чистки ювелирных изделий или средство для чистки экрана телефона.
Синтетические катиноны входят в группу лекарств, которые беспокоят чиновников здравоохранения, которые называются новыми психоактивными веществами (НПВ). НПВ — это нерегулируемые психоактивные вещества, изменяющие сознание, не имеющие законного медицинского использования и созданные для копирования эффектов контролируемых веществ. Они вводятся и повторно выводятся на рынок в быстрой последовательности, чтобы уклоняться или препятствовать усилиям правоохранительных органов по их производству и продаже.
Синтетические катиноны продаются как дешевые заменители других стимуляторов, таких как амфетамины и кокаин. Продукты, продаваемые как Молли, часто содержат синтетические катиноны вместо МДМА (см. Синтетические катиноны и Молли (экстази)).
Продукты, продаваемые как Молли, часто содержат синтетические катиноны вместо МДМА (см. Синтетические катиноны и Молли (экстази)).
Как люди используют синтетические катиноны?
Люди обычно глотают, фыркают, курят или вводят синтетические катиноны.
Как синтетические катиноны влияют на мозг?
Многое еще неизвестно о том, как синтетические катиноны влияют на человеческий мозг. Исследователи действительно знают, что синтетические катиноны химически похожи на такие наркотики, как амфетамины, кокаин и МДМА.
Исследование показало, что 3,4-метилендиоксипировалерон (MDPV), обычный синтетический катинон, воздействует на мозг аналогично кокаину, но по крайней мере в 10 раз сильнее. МДПВ является наиболее распространенным синтетическим катиноном, обнаруживаемым в крови и моче пациентов, поступивших в отделения неотложной помощи после приема солей для ванн. 2
Синтетические катиноны могут вызывать следующие эффекты:
- паранойя — крайнее и необоснованное недоверие к другим
- галлюцинаций — переживание ощущений и образов, которые кажутся реальными, но не являются
- повышенное дружелюбие
- Повышенное половое влечение
- панические атаки
- возбужденный делирий — крайнее возбуждение и агрессивное поведение
Синтетические катиноны и Молли (экстази)
«Молли» — сленг «молекулярный» — относится к наркотикам, которые, как предполагается, представляют собой чистую кристаллическую порошкообразную форму МДМА.
Молли, которую обычно покупают в капсулах, за последние несколько лет стала более популярной. Некоторые люди используют Молли, чтобы избегать таких добавок, как кофеин, метамфетамин и других вредных наркотиков, которые обычно содержатся в таблетках МДМА, продаваемых как экстази. Но те, кто принимает то, что, по их мнению, является чистой Молли, могут подвергать себя такому же риску.
Источники в правоохранительных органах сообщили, что капсулы Молли содержат вредные вещества, в том числе синтетические катиноны. Например, сотни капсул Молли, протестированных в двух криминалистических лабораториях Южной Флориды в 2012 году, содержали метилон, опасный синтетический катинон.
Каковы другие эффекты синтетических катинонов на здоровье?
Повышенная частота сердечных сокращений, артериальное давление и боль в груди — это некоторые другие эффекты синтетических катинонов для здоровья. Люди, страдающие делирием, часто страдают от обезвоживания, разрушения скелетных мышц и почечной недостаточности.
Худшие исходы связаны с вдыханием или инъекцией через иглу. Отравление синтетическими катинонами привело к смерти.
Вызывают ли синтетические катиноны зависимость?
Да, синтетические катиноны могут вызывать привыкание.Исследования на животных показывают, что крысы компульсивно самостоятельно вводят синтетические катиноны. Люди, употребляющие наркотики, сообщают, что наркотики вызывают сильное неконтролируемое желание снова употребить наркотик. Прием синтетических катинонов может вызвать сильные симптомы отмены, в том числе:
- депрессия
- тревога
- толчки
- проблемы со сном
- паранойя
Как лечить от зависимости от синтетических катинонов?
Поведенческая терапия может использоваться для лечения зависимости от синтетических катинонов.Примеры включают:
- когнитивно-поведенческая терапия
- Управление непредвиденными обстоятельствами или мотивационные стимулы — поощрение пациентов, не употребляющих психоактивные вещества
- терапия повышения мотивации
- Поведенческие процедуры для подростков
Как и в случае со всеми видами зависимости, поставщики медицинских услуг должны проверять сопутствующие психические расстройства. Хотя не существует одобренных FDA лекарств от зависимости от синтетического катинона, существуют лекарства от распространенных сопутствующих состояний.
Хотя не существует одобренных FDA лекарств от зависимости от синтетического катинона, существуют лекарства от распространенных сопутствующих состояний.
Что следует помнить
- Синтетические катиноны, более известные как соли для ванн, представляют собой лекарства, содержащие один или несколько антропогенных химических веществ, связанных с катиноном, стимулятором, содержащимся в растении кат.
- Синтетические катиноны продаются как дешевые заменители других стимуляторов, таких как метамфетамин и кокаин. Вместо этого продукты, продаваемые как Молли (МДМА), могут содержать синтетические катиноны.
- Люди обычно глотают, фыркают, курят или вводят синтетические катиноны.
- Многое еще неизвестно о том, как химические вещества в синтетических катинонах влияют на человеческий мозг.
- Синтетические катиноны могут вызывать:
- паранойя
- повышенная коммуникабельность
- Повышенное половое влечение
- галлюцинации
- панические атаки
- Отравление синтетическими катинонами привело к смерти.

- Синтетические катиноны могут вызывать привыкание.
- Поведенческая терапия может использоваться для лечения зависимости от синтетических катинонов.
- В настоящее время нет доступных лекарств для лечения зависимости от синтетических катинонов.
Узнать больше
Для получения дополнительной информации о синтетических катинонах посетите:
Список литературы
- Baumann MH. Омывается в море «солей для ванн»: значение для биомедицинских исследований и общественного здравоохранения. Наркоман Абингдон, англ. 2014; 109 (10): 1577-1579. DOI: 10.1111 / add.12601.
- Baumann MH, Partilla JS, Lehner KR, et al. Мощное кокаиноподобное действие 3,4-метилендиоксипировалерона (МДПВ), основного компонента психоактивных «солей для ванн». Нейропсихофармакология. 2013; 38 (4): 552-562. DOI: 10.1038 / Npp.2012.204.
Эта публикация доступна для вашего использования и может быть воспроизведена полностью без разрешения NIDA. Приветствуется цитирование источника, если используется следующий язык: Источник: Национальный институт по борьбе со злоупотреблением наркотиками; Национальные институты здоровья; Министерство здравоохранения и социальных служб США.
Приветствуется цитирование источника, если используется следующий язык: Источник: Национальный институт по борьбе со злоупотреблением наркотиками; Национальные институты здоровья; Министерство здравоохранения и социальных служб США.
Химические, физико-химические и биологические аспекты
Реферат
Физико-химические и биологические свойства активных фармацевтических ингредиентов (АФИ) в значительной степени зависят от их солевых форм.Выбор конкретного солевого состава основан на многочисленных факторах, таких как химический состав API, предполагаемая лекарственная форма, фармакокинетика и фармакодинамика. Подходящая соль может улучшить общие терапевтические и фармацевтические эффекты API. Однако неправильная форма соли может иметь противоположный эффект и может быть весьма пагубной для общей разработки лекарства. В этом обзоре обобщены несколько критериев выбора подходящих солевых форм, а также влияние солевых форм на фармацевтические свойства API.В дополнение к всестороннему обзору критериев выбора, этот обзор также дает краткую историческую перспективу процессов выбора соли.
Ключевые слова: химия, соль, растворимость в воде, пути введения, физико-химические, стабильность, разложение
1. Введение
Специфические соли активных фармацевтических ингредиентов (API) часто образуются для достижения желаемых свойств рецептуры. Хотя решение проблемы плохой растворимости в воде является одной из наиболее важных причин для использования образования солей, фармацевтические компании также используют образование уникальных солевых продуктов для решения других физико-химических и биологических проблем, таких как стабильность, токсичность, плохая абсорбция и вопросы, связанные с производством. процессы.На важность солей указывают примерно 50% разрешений Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (US FDA), состоящих из API в солевой форме [1]. Более того, половина из 200 лучших рецептурных препаратов в США состоит из фармацевтических солей [2]. Выбор подходящей формы соли продиктован различными факторами. Формирование потенциально товарной соли требует согласованных усилий и глубокого понимания физических и химических характеристик используемых API и противоионов.Для выбора лучшей соли наиболее экономичным способом следует придерживаться рационального дерева решений. Более того, все необходимые испытания следует проводить на ранних этапах процесса разработки лекарств, чтобы свести к минимуму неудачи. Соли могут значительно изменить физические / химические свойства API, так что это может ускорить процесс разработки лекарств.
Формирование потенциально товарной соли требует согласованных усилий и глубокого понимания физических и химических характеристик используемых API и противоионов.Для выбора лучшей соли наиболее экономичным способом следует придерживаться рационального дерева решений. Более того, все необходимые испытания следует проводить на ранних этапах процесса разработки лекарств, чтобы свести к минимуму неудачи. Соли могут значительно изменить физические / химические свойства API, так что это может ускорить процесс разработки лекарств.
Пригодность кандидата для выбора соли определяется физическими и химическими свойствами API; различные противоионы могут использоваться для устранения одного или нескольких недостатков API.Прогнозирование качественных и / или количественных свойств соли на основе используемого противоиона является важной областью исследований. Несколько исследований описали связь между солевыми свойствами и используемыми противоионами [3,4,5,6,7,8]. Хотя прогнозы могут быть сделаны с некоторой степенью точности, нет надежного способа точно исследовать свойства соли на основе используемого противоиона. В настоящее время доступен широкий спектр проверенных противоионов для приготовления солей API () [9]. Одним из важных критериев при выборе противоионов является использование агентов, которые ранее использовались в одобренных FDA лекарствах и поэтому признаны безопасными (GRAS) [7].
В настоящее время доступен широкий спектр проверенных противоионов для приготовления солей API () [9]. Одним из важных критериев при выборе противоионов является использование агентов, которые ранее использовались в одобренных FDA лекарствах и поэтому признаны безопасными (GRAS) [7].
Таблица 1
Список имеющихся в настоящее время противоионов для солеобразования [9].
| Химия (тип иона) | Примеры противоионов | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Катионы | Алюминий Аргинин Бензатин Кальций Хлорпрокаин Бензатин Кальций Хлорпрокаин Гистаноламин Гистанолин Этанолин Этанол Этанол Холин Дитаноламин Холин литий Меглумин Калий Прокаин натрия триэтиламин Цинк | ||||||||||||||||||||||||
| Анионы | ацетат аспартаты бензолсульфонат Бензоит безилат Бикарбонат битартрат Бромид камзилат Карбонат хлорид цитрат деканоит эдетат эзилат Фумарат Глюцепат Глюконат Глутамат Гликолат Гексаноат Гидроксинафтоат Йодид Изетионат Лактат | Лактобионат Малат Малеат Манделат Манделат этилсульфат Мукат Напсилат Нитрат Октаноат Олеат Памоат Пантотенат Фосфат Полигалактуронат Пропионат Салицилат Стеарат Ацетат Токцинат Сукцинат Сукцинат Сукцинат Сукцинат Рассмотрение различных критериев Этот анализ будет рассматриваться подборка солевых форм, а также подходящие примеры для каждой категории.  Включение всех примеров по каждому критерию выходит за рамки этого обзора; поэтому включены только несколько репрезентативных примеров. Следует отметить, что были опубликованы различные учебники, посвященные солевым формам API; Основная часть литературы сосредоточена на повышении растворимости API за счет образования солей. Этот обзор уникален и направлен на то, чтобы предложить краткий отчет о критериях выбора соли, основанных на химическом, фармацевтическом, биологическом и экономическом применении различных составов солей. Включение всех примеров по каждому критерию выходит за рамки этого обзора; поэтому включены только несколько репрезентативных примеров. Следует отметить, что были опубликованы различные учебники, посвященные солевым формам API; Основная часть литературы сосредоточена на повышении растворимости API за счет образования солей. Этот обзор уникален и направлен на то, чтобы предложить краткий отчет о критериях выбора соли, основанных на химическом, фармацевтическом, биологическом и экономическом применении различных составов солей.2. Соображения химии лекарств2.1. Функциональные группы API Присутствие кислотных или основных функциональных групп является важным требованием для образования солей. Большинство обнаруженных API являются подходящими кандидатами для образования солей во время разработки лекарств, поскольку они либо имеют слабокислую, либо слабощелочную природу. Скрининг соли начинается с определения кислотных или основных функциональных групп. В зависимости от наличия этих групп и фармацевтических потребностей можно выбрать потенциальный противоион. 2.2. pKa лекарства Выбор противоиона основан на правиле pK a , которое учитывает степень ионизации кислотных или основных функциональных групп, присутствующих в лекарстве [11]. Согласно правилу pK a , когда pK a разница между кислотой и основанием больше двух или трех, ожидается образование соли [11,12]. В идеале для основных лекарств pK a должен быть как минимум на две единицы pH выше, чем pK a противоиона, а для кислых лекарств pK a лекарства должен быть как минимум на две единицы pH ниже. чем pK a выбранного противоиона.Эта разница обеспечивает сильную энергию связи между противоположными ионными частицами, так что образованные комплексы не будут легко распадаться на отдельные частицы, когда они не требуются. Например, фенитоин — хорошо известное кислое лекарство со значением pK , равным , равным 8,4; однако он имеет ограниченную растворимость. 2.3. Липофильность Солеобразование — это широко используемый метод увеличения растворимости лекарства в воде. Однако иногда считается, что подходы с использованием гидрофобных солей увеличивают липофильность молекулы лекарства [14,15].Было обнаружено, что снижение растворимости в воде является полезным подходом для обеспечения большей химической стабильности, особенно при высокой влажности и высокой температуре. Таблица 2 Противоионы ибупрофена и их соответствующие значения log P и значения мембранного поглощения.
2,4. Гигроскопичность Гигроскопичность определяется как способность материала поглощать и удерживать влагу при различных температурах и условиях влажности. Низкая гигроскопичность является предпочтительной характеристикой лекарств, так как содержание влаги может значительно повлиять на стабильность. В зависимости от степени водопоглощения API можно классифицировать как негигроскопичные, слегка гигроскопичные и гигроскопичные твердые вещества [18].Негигроскопичное вещество может впитывать влагу из влажной среды, что, в свою очередь, может изменять механические свойства и свойства растворимости, влияя на эффективность лекарственного средства. 2,5. Гидратная вода Соль с связанной кристаллизационной водой считается гидратной формой. Эти формы содержат молекулу (ы) воды в кристаллической решетке API. Гидратные формы API-интерфейсов довольно распространены; по оценкам, примерно одна треть API может образовывать гидраты при воздействии условий, способствующих образованию гидратов [20].Фармацевтические гидраты образуются, когда API вступает в контакт с водой во время кристаллизации, лиофилизации, влажной грануляции, нанесения водной пленки, сушки распылением и хранения [21]. 2.6. Полиморфизм Полиморфизм — это способность твердого соединения существовать более чем в одной кристаллической форме. Большинство лекарств проявляют структурный полиморфизм или множественные кристаллические формы. Чтобы молекула превратилась в потенциальное лекарство, необходимо установить существование стабильного полиморфа или подходящего псевдополиморфа. 2.7. Химическая стабильностьКислотные или основные противоионы могут изменять pH микросреды в жидких лекарственных формах. В свою очередь, изменения pH могут влиять на реактивность API с наполнителями и могут привести либо к улучшенной стабильности, либо к деградации API. Нежелательные взаимодействия могут привести к образованию значительных примесей в лекарственном препарате [29]. Например, амлодипин — это свободное основание, которое изначально было выбрано для разработки малеатной соли. Реакция разложения амлодипина в присутствии малеиновой кислоты. 2,8. Растворимость и скорость растворения Подходы к образованию солей широко используются для увеличения растворимости и, следовательно, скорости растворения лекарственного средства. 3. Фармацевтические соображения3.1. Желаемая лекарственная форма3.1.1. A Жидкости (суспензии) Суспензии являются наиболее распространенным типом жидких лекарственных форм для перорального применения. Маскировка вкуса горьких лекарств — одно из важных соображений при разработке лекарственных препаратов. Использование различных противоионов для получения подходящих солевых форм было эффективно использовано либо для приготовления суспензий, либо для снижения растворимости, так что лекарства не растворяются хорошо при нанесении на язык. Например, эритромицин (свободное основание) — хорошо известный макролидный антибиотик, легко растворимый в воде.Однако более высокая растворимость приводит к более быстрому растворению на языке, что приводит к горькому вкусу. Аналогичным образом подсластители, такие как цикламовая кислота или сахарин, могут быть полезны для получения солей основных лекарственных средств. 3.1.2. B Растворы Растворимость лекарства в водных системах является важным фактором при разработке парентеральных препаратов. Таким образом, чтобы увеличить растворимость, солевые формы часто используются для приготовления концентрированных парентеральных растворов. Соответствующие противоионы могут быть легко проверены на основе экспериментов по растворимости, которые служат важным инструментом для поиска лучшего кандидата.В большинстве случаев растворимость можно повысить, изменив pH раствора. Одним из хорошо известных примеров является фенитоин натрия, растворимость которого значительно повышается при добавлении гидроксида натрия (NaOH), чтобы обеспечить парентеральное введение в желаемой концентрации [33]. Химическая стабильность — еще один важный фактор, поскольку лекарства в растворе обычно менее стабильны, чем в твердых лекарственных формах. 3.1.3. Кремы / мази / гели Кремы, мази и гели являются обычно используемыми лекарственными формами для трансдермальной доставки. Высокополярные трансдермальные препараты-кандидаты обычно демонстрируют неэффективное чрескожное проникновение [34]. Это ограничивает использование некоторых важных лекарств. В прошлом для увеличения трансдермальной проницаемости использовали образование соли. 3.1.4. Аэрозоли Ингаляционный путь направлен в первую очередь на бронхиолы и легкие для местной доставки лекарств, но для эффективной доставки следует учитывать различные физико-химические и механические факторы.Ограниченное время пребывания препарата в месте действия является одним из наиболее распространенных и важных препятствий на пути эффективного использования API. 3.2. Легкость синтеза и масштабирования3.2.1. Сыпучесть Как правило, API с хорошими характеристиками текучести считается хорошим кандидатом для разработки коммерчески успешных твердых пероральных лекарственных форм.Сыпучесть лекарственного средства может иметь значительное влияние на операции смешивания, сжатия, наполнения, транспортировки и увеличения масштаба производства твердых доз. 3.2.2. Коррозионная активность противоионов Лекарство с очень агрессивной природой может стать серьезным препятствием для успешного производственного процесса. Хотя использование противоионного подхода для маскировки коррозионной группы может решить проблему в большей степени, если отбор не будет проведен должным образом, это может привести к большему количеству проблем на последних этапах разработки лекарственного средства. Например, слабоосновные препараты с низкими значениями константы диссоциации (pKa) требуют, чтобы соли гораздо более сильных противоионов были физически стабильными [38]. 3.2.3. Совместимость с наполнителями В литературе есть многочисленные примеры выбора подходящих солевых форм для минимизации взаимодействия API с различными наполнителями, что делает лекарственный продукт химически пригодным для развития. Например, форма свободного основания соединения CGP6085 изначально была разработана как антидепрессант.Однако его нежелательные взаимодействия с наполнителем таблетки, лактозой, привели к значительной деградации API (). Таким образом, форма свободного основания оказалась нежизнеспособной. Позднее была разработана форма гидрохлоридной соли CGP6085, которая значительно улучшила стабильность API и в конечном итоге подавила взаимодействие с лактозой [12]. Этот пример показывает, как солевые формы могут оказывать значительное влияние на стабильность лекарственного средства, а уникальные противоионы могут увеличивать стабильность лекарственного средства в выбранной лекарственной форме. Свободное основание и форма соли CGP6085. 3.3. Путь введения Пути введения лекарственного средства диктуют использование свободной формы (кислота / основание) лекарственного средства или необходимость использования подходящей солевой формы. Различные солевые формы одного и того же лекарственного средства также могут подходить для разных путей введения. Например, диклофенак, содержащий натрий, калий и свободные кислоты, был одобрен в качестве пероральных препаратов. 1% гель диклофенака натрия (Voltaren Gel ® ) и 1,5% раствор диклофенака натрия для местного применения w / w (Pennsaid ® ) также доступны в качестве продуктов для местного применения; однако его соль эполамина (Flector ® ) одобрена в качестве трансдермального пластыря из-за его лучшего проникновения через кожу, чем соли натрия или калия [41]. 3.4. Лекарственные формы с контролируемым высвобождением API демонстрируют различные свойства растворения и высвобождения при присоединении к различным противоионам; это свойство было использовано для создания лекарственных форм с контролируемым высвобождением. Клинически одна форма соли может быть предпочтительнее другой по желаемым характеристикам высвобождения. Например, из хорошо растворимого лекарственного средства можно создать лекарственную форму с контролируемым высвобождением с использованием труднорастворимых солей. Это снижение растворимости лекарства может при желании замедлять высвобождение лекарства.Следовательно, выбор подходящего противоиона для замедления высвобождения лекарственного средства может быть полезным в составах с замедленным высвобождением (SR). Например, имипрамин, который является трициклическим антидепрессантом, изначально был разработан в виде гидрохлоридной соли в виде препарата с немедленным высвобождением (IR) (). Однако композиция с контролируемым высвобождением более желательна для поддержания устойчивых терапевтических эффектов. Другой пример, который иллюстрирует важность растворения, — это различные солевые формы диклофенака. Fini et al. исследовали растворение 30 различных солевых форм диклофенака [42]. Хотя в настоящее время в США для лекарственной формы с немедленным высвобождением используются как форма калия, так и форма свободной кислоты, для лекарственной формы с пролонгированным высвобождением используется только форма натриевой соли. Таким образом, разные противоионы, присоединенные к одному и тому же лекарству, могут влиять на скорость растворения и, следовательно, могут влиять на лекарственные формы, желаемые в клинической практике. 4. Фармакокинетика (PK), фармакодинамика (PD) и соображения безопасности4.1. Токсикологические соображения Когда лекарство вводится перорально, оно может взаимодействовать со слизистой оболочкой желудочно-кишечного тракта (ЖКТ), вызывая нежелательные побочные эффекты. 4.2. Распространение и клиренс Было показано, что солевые образования, хотя обычно не используются, влияют на распределение и клиренс молекулы лекарственного средства. 4.3. Начало и прекращение терапевтического эффекта Исходя из терапевтических показаний, некоторые лекарственные формы требуют более медленного начала и прекращения терапевтического эффекта. 4.4. Противодействие побочным эффектам Иногда противоионы используются таким образом, что побочные эффекты исходного лекарственного средства могут быть уменьшены используемым противоионом. 4.5. Лекарственные взаимодействия Присутствие свободных кислотных / основных форм или конкретного противоиона может иметь некоторые клинически значимые лекарственные взаимодействия, особенно когда он производится совместно или вводится совместно с другими лекарствами. 5. Экономические соображенияСоображения интеллектуальной собственности (ИС)На протяжении многих лет различные производители фармацевтических препаратов-дженериков пытались представить различные солевые формы утвержденного АФИ, чтобы выйти на рынок, даже до истечения срока действия первоначального патента.Напротив, инновационные солевые составы помогли первоначальным патентообладателям расширить права собственности или предоставить исключительные права на рынок производителю дженериков. Некоторые из преимуществ, предлагаемых инновационными солевыми формами, которые могут заслуживать патентной защиты, — это упрощенные производственные процедуры, более стабильные аналоги, новые способы введения или совершенно иное терапевтическое применение [53]. Одним из хорошо известных примеров является просьба компании Dr. Reddy’s Laboratories получить одобрение на рынок малеата амлодипина еще до истечения срока действия патента на безилат амлодипина. Для ясности суммированы все факторы, влияющие на процесс выбора соли. Различные факторы, влияющие на процесс выбора соли. 6. Скрининг, приготовление и характеристика солей Существуют различные статьи, посвященные скринингу, приготовлению и характеристике солей [55,56,57]. Цель этого раздела не в том, чтобы дать исчерпывающий отчет о задействованных процессах, а в том, чтобы предложить краткое изложение с целью связать концы с концами между отбором, скринингом, приготовлением и характеристикой солей.Процесс отбора солей начинается с выбора возможных противоионов для образования соли [9]. Соли исходных соединений (PC) идентифицируют путем скрининга большого количества солевых форм (SF) в различных условиях кристаллизации. Традиционно проводятся обширные скрининги в различных условиях для выявления солей с идеальными свойствами для разработки рецептур [55]. Лекарство должно быть полностью ионизировано в единственном состоянии ионизации, чтобы допустить образование соли, поскольку неполная ионизация может привести к осаждению неионизированной формы. Безопасно ли запах соли? Как они работают, польза и риски Соли с запахом используются в качестве лечебного средства с 13 века. Несмотря на то, что они вышли из обихода, спортсмены начали использовать нюхательные соли для улучшения своих спортивных результатов. Это принесло нюхательной соли сомнительную репутацию. Однако нюхательные соли безопасны в использовании. Как действуют нюхательные солиНюхательные соли состоят из химического вещества, обычно аммиака, имеющего очень сильный запах. Когда пахнущая соль подносится к носу человеку, который потерял сознание, резкий запах заставляет его снова просыпаться. Пары нюхательной соли резкие (подумайте о едком запахе отбеливателя, когда что-то чистите).При поднесении к носу пары раздражают внутреннюю часть носа. Раздражение заставляет легкие быстро дышать глубоко, чтобы очистить носовой ход. Пары вызывают дыхательный рефлекс, который помогает перезапустить дыхательный ритм и отправить кислород в мозг. Дозировка и применение. Количество, частота и продолжительность использования нюхательных солей во многом зависят от того, почему вы их используете, и от силы соли.Проконсультируйтесь с инструкциями к продукту или рекомендациями врача для правильного использования. Хранилище. Поскольку нюхательные соли основаны на аммиаке, их довольно легко хранить. Храните их при комнатной температуре в закрытом контейнере вдали от влаги. Преимущества нюхательной солиОсновным преимуществом нюхательной соли является реанимация потерявшего сознание человека. Хотя они больше не используются врачами широко, нюхательные соли по-прежнему эффективны. Спортивные кроссовки нашли альтернативное применение нюхательной соли. Одно из применений — лечение травм головы. Спортсмен может потерять сознание из-за травмы головы или испытать «затуманенное сознание» из-за травмы головы, а запах соли может использоваться в качестве временного самолечения. Спортсмены обратились к нюхательной соли для прилива энергии и концентрации. Однако нет никаких доказательств того, что они имеют такую пользу, а нюхательная соль даже была запрещена некоторыми лигами. Риски и побочные эффектыПри правильном использовании нюхательные соли не имеют побочных эффектов.Некоторые необычные побочные эффекты включают:
Чрезмерное употребление нюхательной соли может привести к повреждению носовых ходов. Острые пары аммиака могут обжечь мембраны в ноздрях, но для этого потребуется частое и интенсивное употребление нюхательных солей. Соблюдайте осторожность при использовании нюхательной соли для лечения травм головы. Использование нюхательной соли для лечения сотрясения мозга или аналогичной травмы головы дает немедленные преимущества, но может усложнить дальнейшее лечение. Когда человека реанимируют с помощью нюхательной соли, он может рефлекторно дергать головой и шеей, пытаясь уйти от паров аммиака. Это может еще больше травмировать человека, если он потеряет сознание из-за травмы головы. Соли с запахом могут плохо реагировать с ранее существовавшими условиями. Люди с заболеваниями дыхательной системы могут испытывать побочные реакции.Эти условия включают:
Избегайте контакта с кожей и глазами. Аммиак — это едкое химическое вещество, которое может раздражать и сжигать все, с чем соприкасается. Если запах соли попадет в глаза, осторожно промойте глаза водой и обратитесь в токсикологический центр, к врачу или в отделение неотложной помощи. Если соли попали на кожу, промойте кожу водой.Не используйте мазь для снятия раздражения. Если раздражение не исчезнет, обратитесь к врачу. Проблемы безопасности, связанные с нюхательной сольюРастущей проблемой в некоторых профессиональных спортивных лигах является неправильное использование нюхательной соли. Спортсмены узнали, что тряска от запаха солей дает им прилив энергии перед большой игрой или решающей игрой, или когда они начинают уставать во время игры. Спортсмены, у которых наблюдаются симптомы сотрясения мозга, могут обращаться к нюхательным солям для их лечения.Повторное использование нюхательных солей таким образом может подвергнуть их риску получения травм в будущем. Хотя нюхательные соли не имеют зарегистрированных отрицательных эффектов, их вызывающее привыкание использование для стимуляции занятий спортом может быть опасным и открыть дверь для злоупотребления психоактивными веществами в будущем. Морская соль и поваренная соль: в чем разница? Основные различия между морской солью и поваренной солью заключаются во вкусе, текстуре и обработке. Поваренная соль — это гранулированная белая соль, которую используют в большинстве солонцев.Поваренную соль обычно добывают из подземных месторождений. Его обрабатывают для удаления других минералов. Поваренная соль обычно обогащена йодом, который важен для здоровья щитовидной железы. Морская соль — это общий термин для обозначения соли, образующейся при испарении океанской воды или воды из соленых озер. Она менее обработана, чем поваренная соль, и сохраняет микроэлементы. Эти минералы придают аромат и цвет. Морская соль доступна в виде мелких зерен или кристаллов. Морская соль часто считается более полезной для здоровья, чем поваренная соль.Но основная пищевая ценность морской и поваренной соли одинакова. Морская соль и поваренная соль содержат сопоставимые количества натрия по весу. Какой бы сорт соли вы ни любили, делайте это в умеренных количествах. Диетические рекомендации для американцев рекомендуют ограничивать потребление натрия до уровня менее 2300 миллиграммов в день. Получите самую свежую информацию о здоровье от экспертов Mayo Clinic.Зарегистрируйтесь бесплатно и будьте в курсе достижений в области исследований, советов по здоровью и актуальных тем, связанных со здоровьем, таких как COVID-19, а также опыта в области управления здоровьем. Узнайте больше об использовании данных Mayo Clinic. Чтобы предоставить вам наиболее актуальную и полезную информацию и понять, какие
информация полезна, мы можем объединить вашу электронную почту и информацию об использовании веб-сайта с
другая имеющаяся у нас информация о вас. Подписаться! Спасибо за подписку Наш электронный информационный бюллетень Housecall будет держать вас в курсе самой последней информации о здоровье. Извините, что-то пошло не так с вашей подпискойПовторите попытку через пару минут Повторить
. Что такое каменная соль?Галит, более известный как каменная соль, представляет собой минерал, образованный из хлорида натрия.Его химическая формула — NaCl, и это также включает другие вариации соли, такие как поваренная соль и поваренная соль. Промышленное название галита — каменная соль. Он образует изометрические кристаллы и обычно бесцветный или белый, но также может быть другого цвета в зависимости от количества и типа содержащихся в нем примесей. Соль встречается в пластах осадочных минералов эвапоритов. Это вызвано высыханием крупных озер и морей. Глубина этих соляных пластов может достигать сотен метров. Кристаллы галита образуются очень быстро в некоторых быстро испаряющихся озерах. Англия была покрыта внутренними морями более 200 миллионов лет назад, что помогло создать слои соли, которые добываются сегодня. Когда очень высокие температуры в этом районе испаряли воду очень медленно, они оставляли большие солевые отложения под землей. В Великобритании, когда вода испарилась и начали формироваться кристаллы соли, они приобрели свой коричневатый цвет из-за песка, принесенного из восточных пустынь. Однако из-за других геологических факторов цвет каменной соли иногда может меняться от прозрачного, до розового, до темно-коричневого. Большая часть каменной соли, используемой для грунтования дорог в Великобритании, поступает из шахт древних подземных соляных месторождений в Кливленде, графстве Антрим и Винсфорд. Уинсфорд находится в Чешире, и четыре из окружающих его городов — Мидлвич, Нантвич, Нортвич и Лэфтвич — исторически связаны с производством соли. «Wich» (или иногда «wych») в их названии часто ассоциируется с соляными источниками или колодцами. Соляная ассоциация, занимающаяся торговлей производителями соли, считает, что соляные шахты Великобритании имеют около 225 км (140 миль) туннелей.Если вы думали, что запасы соли в ближайшее время будут исчерпаны, вы будете удивлены, узнав, что доказанные запасы соли в Великобритании обширны, с расчетной мощностью 500 лет при текущих темпах добычи. Основное отличие каменной соли от обычной поваренной соли — это размер и цвет. Каменная соль образует очень большие массивные кристаллы, в отличие от мелких кристаллов, которые можно увидеть в поваренной соли. Как и поваренная соль, каменная соль также содержит ряд микроэлементов, которые могут влиять на ее химическое поведение.Большой размер кристаллов каменной соли означает, что ее обычно не используют в кулинарии, так как она слишком долго растворяется. Есть и другие различия между двумя наиболее распространенными типами соли. Отложения каменной соли обычно представляют собой остатки внутренних морей, испарившихся тысячи или миллионы лет назад. Человек, осужденный за распространение «соли для ванн» по всей территории штата ЮтаСОЛТ-ЛЕЙК-СИТИ — Мужчина из штата Юта был приговорен к 51 месяцу лишения свободы в федеральной тюрьме за хранение наркотика Списка 1 Альфа-пирролидиногексанофенон, широко известного как «Альфа-PHP», с намерение распространить наркотик. Исполняющий обязанности прокурора США Андреа Мартинес. от округа Юта и Стивен Каген, ответственный специальный агент отдела расследований внутренней безопасности, Денвер. 63-летний Брент Ортон из Солт-Лейк-Сити признал себя виновным по однозначной уголовной информации, поданной федеральными прокурорами по обвинению его в хранении с целью распространения Alpha PHP в июне 2021 года. В соглашении о признании вины Ортон признал, что получил пакет Alpha PHP с целью распространения запрещенного наркотического средства. «Опасным синтетическим наркотикам, таким как соли для ванн, нет места в нашем сообществе, и HSI будет расследовать дела тех, кто импортирует и распространяет эти смертоносные вещества», — сказал Стивен Кейген, ответственный специальный агент отдела расследований национальной безопасности Денверского полевого отделения. Прокуроры утверждали, что Ортон импортировал и распространял большое количество Alpha-PHP в течение двух лет, и что Ортон распространил от 575 000 до 4 600 000 доз этого препарата в Юте, которые продавались по цене от 300 до 500 долларов за грамм.Прокуратура также утверждала, что Ортон использовал друзей своей дочери в качестве клиентов, а также использовал их для проникновения в бизнес по торговле наркотиками. Alpha-PHP, контролируемое вещество Списка 1, представляет собой соединение химического класса замещенный катинон и замещенный пирролидин, представляет собой синтетический вариант препарата, более часто называемого «солями для ванн». В целом интенсивность воздействия этого вещества сравнима с сильными стимуляторами, такими как метамфетамин, МДПВ и альфа-ПВП. «Синтетические наркотики, такие как Alpha-PHP, представляют собой смертельные соединения, представляющие опасность для наших сообществ», — сказала и.о. прокурора США Андреа Мартинес. «Прокуратура Соединенных Штатов сосредоточена на преследовании преступников, которые ввозят и распространяют эти незаконные наркотики в нашем сообществе.” помощника прокурора США из прокуратуры США в штате Юта и специальный помощник прокурора США из Министерства внутренней безопасности США ведут дело. Расследование проводили специальные агенты службы внутренней безопасности и сотрудники таможни и пограничной службы. HSI — это управление иммиграционной и таможенной службы США (ICE) и главное следственное подразделение Министерства внутренней безопасности США (DHS), ответственное за расследование транснациональных преступлений и угроз, особенно тех преступных организаций, которые используют глобальную инфраструктуру, через которую торговля, путешествия и финансы. Штат HSI, насчитывающий более 10 400 сотрудников, состоит из более 7 100 специальных агентов, работающих в 220 городах США и 80 заграничных точках в 53 странах. Международное присутствие HSI представляет собой крупнейшее следственное присутствие правоохранительных органов DHS за рубежом и одно из крупнейших международных следственных действий правоохранительных органов США. соли и натрия — в чем разница?Если вы думаете, что соль и натрий — одно и то же, вы не одиноки.Но вы также не обязательно правы. Это распространенное заблуждение сбивает с толку многих людей, но разница может сильно повлиять на качество вашей диеты. Натрий против солиВот четкий способ отличить натрий от соли, как мы ее обычно знаем.
В идеале нам нужны непереработанные продукты, потому что чем больше времени они обрабатываются, тем больше натрия добавляется в процессе. Соль — это химическое соединение, состоящее из натрия и хлорида. На самом деле именно натрий вредит вашему здоровью. (Следовательно, именно хлорид придает пище «соленый» вкус.) Сколько натрия слишком много?Средняя американская диета требует не более 2300 мг натрия в день, а для людей с высоким кровяным давлением или состояниями здоровья — даже меньше. Но среднее количество натрия, которое мы фактически потребляем, ближе к 3400 мг в день.Чтобы представить это в контексте, пол чайной ложки соли эквивалентен 500 мг натрия. Советы по сокращению потребления натрия Итак, какие шаги вы можете предпринять, чтобы свести к минимуму потребление натрия? Прежде всего, обратите внимание на этикетки. Если количество натрия кажется высоким, поищите вариант с более низким содержанием натрия или сделайте практическую замену. Многие продукты доступны сегодня для людей с особыми диетическими потребностями, но вам, возможно, придется проконсультироваться с вашим местным бакалейщиком. | |||||||||||||||||||||||

 Низкомолекулярные основания и кислоты имеют больше шансов оказаться жидкостью с низкой температурой плавления. Образование соли можно использовать для увеличения их точек плавления и преобразования и поддержания твердого состояния. Например, Bozigian et al. сообщили, что соединение NBI-75043, которое является исследуемым соединением для лечения бессонницы, представляет собой кристаллическое свободное основание с низкой температурой плавления (64 ° C) [10]. Одним из важных фармацевтических требований для этого соединения было создание соли с более высокой температурой плавления.Поскольку слабоосновным лекарствам для образования ионных связей требуются кислотные противоионы, в качестве возможных противоионов было выбрано 14 кислот. Поскольку низкая температура плавления была одной из проблем этого препарата, первоначальные подходы к характеристике солевых форм включали дифференциальную сканирующую калориметрию (ДСК), которая является важным инструментом для определения температуры плавления, а также кристалличности, сольватов и наличия или отсутствия полиморфы.
Низкомолекулярные основания и кислоты имеют больше шансов оказаться жидкостью с низкой температурой плавления. Образование соли можно использовать для увеличения их точек плавления и преобразования и поддержания твердого состояния. Например, Bozigian et al. сообщили, что соединение NBI-75043, которое является исследуемым соединением для лечения бессонницы, представляет собой кристаллическое свободное основание с низкой температурой плавления (64 ° C) [10]. Одним из важных фармацевтических требований для этого соединения было создание соли с более высокой температурой плавления.Поскольку слабоосновным лекарствам для образования ионных связей требуются кислотные противоионы, в качестве возможных противоионов было выбрано 14 кислот. Поскольку низкая температура плавления была одной из проблем этого препарата, первоначальные подходы к характеристике солевых форм включали дифференциальную сканирующую калориметрию (ДСК), которая является важным инструментом для определения температуры плавления, а также кристалличности, сольватов и наличия или отсутствия полиморфы. Они смогли успешно найти солевую форму NBI-75043, сосредоточив внимание на химии препарата [10].
Они смогли успешно найти солевую форму NBI-75043, сосредоточив внимание на химии препарата [10]. Одним из важных фармацевтических свойств этого лекарства, на которое необходимо было обратить внимание, было улучшение его растворимости в воде. Из-за кислой природы препарата основные противоионы с pK и имеют значения> 10.4, вероятно, будут образовывать фармацевтически приемлемые соли. Следовательно, для образования желаемой соли фенитоина необходим сильный основной противоион, такой как NaOH. Слабоосновные противоионы не могут образовывать соли с фенитоином, поскольку эти противоионы не могут повышать pH выше требуемого значения pH max , равного 11 [13].
Одним из важных фармацевтических свойств этого лекарства, на которое необходимо было обратить внимание, было улучшение его растворимости в воде. Из-за кислой природы препарата основные противоионы с pK и имеют значения> 10.4, вероятно, будут образовывать фармацевтически приемлемые соли. Следовательно, для образования желаемой соли фенитоина необходим сильный основной противоион, такой как NaOH. Слабоосновные противоионы не могут образовывать соли с фенитоином, поскольку эти противоионы не могут повышать pH выше требуемого значения pH max , равного 11 [13]. Одним из хорошо известных примеров является образование сульфата, а также гидрофобных солей ксилобама. Сульфатная соль этого препарата полностью ионизирована. Фактически, было обнаружено, что наличие арильных групп в сульфатном противоионе этого лекарственного средства защищает основание от легкого гидролиза в присутствии высокой влажности и высоких температур.Образование гидрофобных солей позволяет фармацевтическим компаниям готовить более стабильные лекарства, не влияя на их биодоступность [16]. Образование солей приводит к повышенной липофильности в результате нейтрализации общего электростатического заряда, тем самым повышая проницаемость гидрофильных молекул через мембрану. Как показано в Sarveiya et al. сопоставили влияние нескольких противоионов ибупрофена на значение log P и мембранную абсорбцию [17] и четко продемонстрировали влияние различных противоионов на эти свойства.
Одним из хорошо известных примеров является образование сульфата, а также гидрофобных солей ксилобама. Сульфатная соль этого препарата полностью ионизирована. Фактически, было обнаружено, что наличие арильных групп в сульфатном противоионе этого лекарственного средства защищает основание от легкого гидролиза в присутствии высокой влажности и высоких температур.Образование гидрофобных солей позволяет фармацевтическим компаниям готовить более стабильные лекарства, не влияя на их биодоступность [16]. Образование солей приводит к повышенной липофильности в результате нейтрализации общего электростатического заряда, тем самым повышая проницаемость гидрофильных молекул через мембрану. Как показано в Sarveiya et al. сопоставили влияние нескольких противоионов ибупрофена на значение log P и мембранную абсорбцию [17] и четко продемонстрировали влияние различных противоионов на эти свойства.
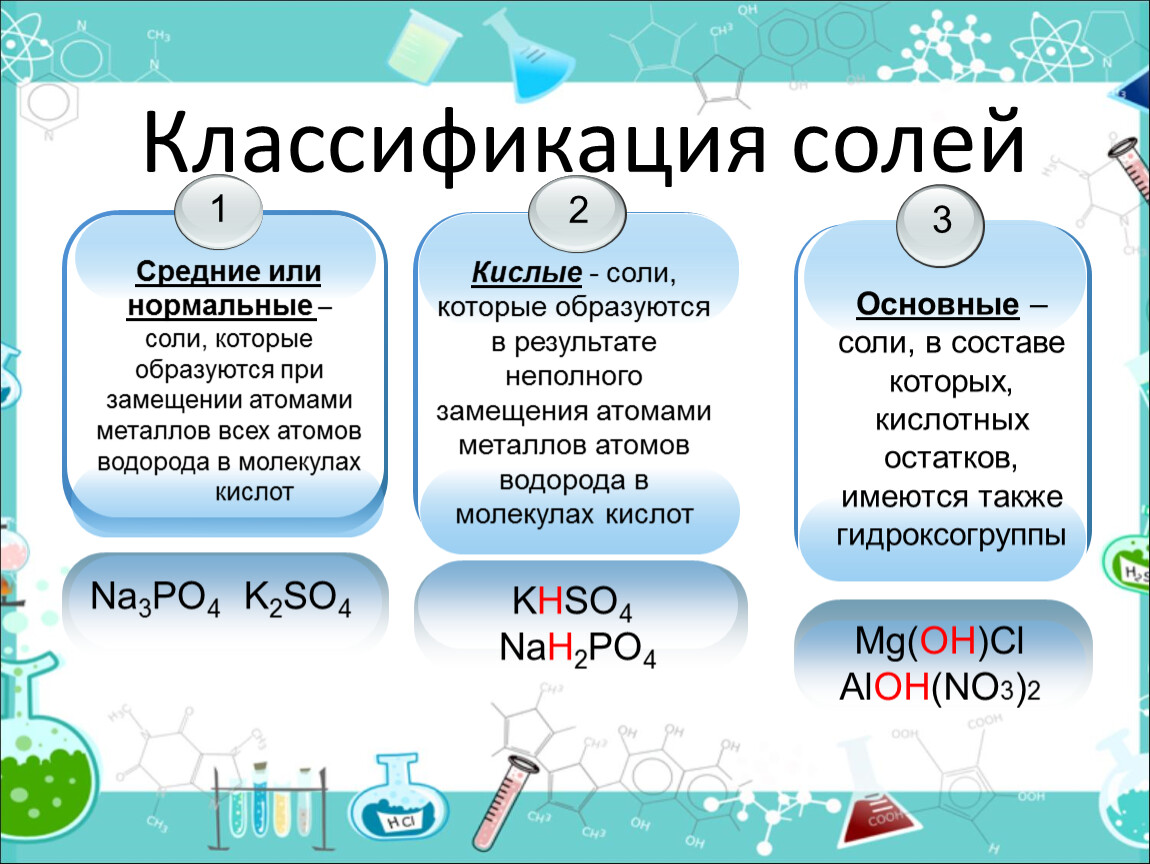 31
31 Легко гидролизуемые лекарственные средства легче разлагаются из-за присутствия воды и изменений pH в микросреде соли. Таким образом, при разработке солевой формы лекарственного средства необходимо тщательно контролировать гигроскопичность. Например, соли минеральных кислот имеют тенденцию быть очень полярными, что приводит к повышенной гигроскопичности и низкому pH в микросреде.Эти факторы могут влиять на стабильность некоторых лекарств из-за последующего увеличения скорости гидролиза [19].
Легко гидролизуемые лекарственные средства легче разлагаются из-за присутствия воды и изменений pH в микросреде соли. Таким образом, при разработке солевой формы лекарственного средства необходимо тщательно контролировать гигроскопичность. Например, соли минеральных кислот имеют тенденцию быть очень полярными, что приводит к повышенной гигроскопичности и низкому pH в микросреде.Эти факторы могут влиять на стабильность некоторых лекарств из-за последующего увеличения скорости гидролиза [19]. Если гидрат подвергается воздействию сухой окружающей среды, он может потерять кристаллизационную воду, чтобы достичь более низкого состояния гидратации или безводной формы. Обмен воды между лекарственным средством и вспомогательными веществами, такими как крахмал или целлюлоза, также может влиять на растворимость и механические свойства лекарственного препарата [22,23]. Молекулы воды в фармацевтических гидратах влияют на внутреннюю энергию, термодинамическую активность, гигроскопичность, растворимость, скорость растворения и стабильность [23].Следовательно, понимание гидратной формы имеет решающее значение для лучшего понимания этих свойств и решения серьезных проблем, если возникнет необходимость.
Если гидрат подвергается воздействию сухой окружающей среды, он может потерять кристаллизационную воду, чтобы достичь более низкого состояния гидратации или безводной формы. Обмен воды между лекарственным средством и вспомогательными веществами, такими как крахмал или целлюлоза, также может влиять на растворимость и механические свойства лекарственного препарата [22,23]. Молекулы воды в фармацевтических гидратах влияют на внутреннюю энергию, термодинамическую активность, гигроскопичность, растворимость, скорость растворения и стабильность [23].Следовательно, понимание гидратной формы имеет решающее значение для лучшего понимания этих свойств и решения серьезных проблем, если возникнет необходимость. Полиморфы (или псевдополиморфы) лекарств обладают разной химической стабильностью; Обычно наблюдается, что более термодинамически стабильный полиморф более химически устойчив, чем метастабильный полиморф [24]. Оптимизированная ориентация молекул, водородных и неводородных связей в кристаллической решетке играет важную роль в придании термодинамической стабильности кристаллическим структурам. Даже небольшие изменения в упаковке кристаллов могут привести к значительным различиям в химической активности двух полиморфов одного и того же лекарства [24].Между кристаллической формой и аморфными формами одного и того же лекарства аморфная форма менее стабильна из-за отсутствия трехмерной кристаллической структуры, свободного объема и большей молекулярной подвижности [24]. Аморфная форма пенициллина G менее стабильна, чем кристаллические соли натрия и калия [25]. Существует несколько примеров влияния полиморфизма лекарственного средства на его фармацевтическую судьбу. Рассмотрение всех примеров выходит за рамки предполагаемого объема данного обзора.
Полиморфы (или псевдополиморфы) лекарств обладают разной химической стабильностью; Обычно наблюдается, что более термодинамически стабильный полиморф более химически устойчив, чем метастабильный полиморф [24]. Оптимизированная ориентация молекул, водородных и неводородных связей в кристаллической решетке играет важную роль в придании термодинамической стабильности кристаллическим структурам. Даже небольшие изменения в упаковке кристаллов могут привести к значительным различиям в химической активности двух полиморфов одного и того же лекарства [24].Между кристаллической формой и аморфными формами одного и того же лекарства аморфная форма менее стабильна из-за отсутствия трехмерной кристаллической структуры, свободного объема и большей молекулярной подвижности [24]. Аморфная форма пенициллина G менее стабильна, чем кристаллические соли натрия и калия [25]. Существует несколько примеров влияния полиморфизма лекарственного средства на его фармацевтическую судьбу. Рассмотрение всех примеров выходит за рамки предполагаемого объема данного обзора. Однако стоит упомянуть полиморфизм ритонавира (Norvir ® ), открытие которого послужило тревожным сигналом для фармацевтических компаний. Ритонавир — противовирусный препарат, продаваемый Abbott Laboratories в 1996 году в форме полутвердых гелевых капсул для лечения синдрома приобретенного иммунодефицита (СПИД) [26]. Капсулы содержали единственную известную кристаллическую форму, форму I, которая была обнаружена в процессе разработки. Однако в 1998 году новый и значительно менее растворимый полиморф ритонавира осаждался в полутвердых гелевых капсулах [27,28], которые стали известны как форма II.Эта форма продемонстрировала значительно более низкую растворимость в водно-спиртовых растворах, чем имеющаяся на рынке Форма I [28]. Производство полутвердых капсул с ритонавиром состояло из водно-спиртового раствора лекарственного средства, который, как было обнаружено, был насыщен формой II. Внезапное появление и преобладание этой менее растворимой формы сделало состав непригодным для производства [27], а также повлияло на хранение перорального раствора Норвир ® в условиях охлаждения, поскольку более низкие температуры хранения приводили к кристаллизации Формы II [27].
Однако стоит упомянуть полиморфизм ритонавира (Norvir ® ), открытие которого послужило тревожным сигналом для фармацевтических компаний. Ритонавир — противовирусный препарат, продаваемый Abbott Laboratories в 1996 году в форме полутвердых гелевых капсул для лечения синдрома приобретенного иммунодефицита (СПИД) [26]. Капсулы содержали единственную известную кристаллическую форму, форму I, которая была обнаружена в процессе разработки. Однако в 1998 году новый и значительно менее растворимый полиморф ритонавира осаждался в полутвердых гелевых капсулах [27,28], которые стали известны как форма II.Эта форма продемонстрировала значительно более низкую растворимость в водно-спиртовых растворах, чем имеющаяся на рынке Форма I [28]. Производство полутвердых капсул с ритонавиром состояло из водно-спиртового раствора лекарственного средства, который, как было обнаружено, был насыщен формой II. Внезапное появление и преобладание этой менее растворимой формы сделало состав непригодным для производства [27], а также повлияло на хранение перорального раствора Норвир ® в условиях охлаждения, поскольку более низкие температуры хранения приводили к кристаллизации Формы II [27]. Эти факторы, наряду с ограниченным инвентарем, привели к тому, что Abbot Laboratories отозвали это лекарство, в результате чего десятки тысяч пациентов со СПИДом во всем мире остались без лекарств [26]. Ритонавир был изменен и одобрен в 1999 году перед выпуском на рынок; При этом компания Abbot потеряла доход в размере более 250 миллионов долларов США [26]. Следовательно, понимание солевых составов и их корреляции с полиморфизмом на ранней стадии разработки лекарств является обязательным для сведения к минимуму неэффективности лекарств на более поздних стадиях разработки лекарств.
Эти факторы, наряду с ограниченным инвентарем, привели к тому, что Abbot Laboratories отозвали это лекарство, в результате чего десятки тысяч пациентов со СПИДом во всем мире остались без лекарств [26]. Ритонавир был изменен и одобрен в 1999 году перед выпуском на рынок; При этом компания Abbot потеряла доход в размере более 250 миллионов долларов США [26]. Следовательно, понимание солевых составов и их корреляции с полиморфизмом на ранней стадии разработки лекарств является обязательным для сведения к минимуму неэффективности лекарств на более поздних стадиях разработки лекарств. Однако присутствие малеиновой кислоты изменило микросреду лекарственного продукта, и это изменение привело к образованию производного аспарагиновой кислоты (UK-57269) путем добавления Майкла, как показано на рис.Было обнаружено, что этот продукт разложения обладает различной биологической активностью, и поэтому малеат амлодипина оказался непригодным для дальнейшей разработки. Хотя такие реакции можно свести к минимуму путем тщательного выбора вспомогательных веществ и избегания щелочных условий [30], безилат (бензолсульфонат) был выбран в качестве подходящей солевой формы со значительно меньшими проблемами [12]. Этот пример ясно демонстрирует, как может быть нарушена стабильность лекарственного средства, если противоион не будет тщательно выбран.
Однако присутствие малеиновой кислоты изменило микросреду лекарственного продукта, и это изменение привело к образованию производного аспарагиновой кислоты (UK-57269) путем добавления Майкла, как показано на рис.Было обнаружено, что этот продукт разложения обладает различной биологической активностью, и поэтому малеат амлодипина оказался непригодным для дальнейшей разработки. Хотя такие реакции можно свести к минимуму путем тщательного выбора вспомогательных веществ и избегания щелочных условий [30], безилат (бензолсульфонат) был выбран в качестве подходящей солевой формы со значительно меньшими проблемами [12]. Этот пример ясно демонстрирует, как может быть нарушена стабильность лекарственного средства, если противоион не будет тщательно выбран. Это один из наиболее распространенных методов повышения растворимости слабокислых и основных лекарств. Гидрохлорид, мезилат, гидробромид, ацетат и фумарат являются наиболее распространенными противоионами, которые используются для основных химических соединений за последние 20 лет [31], в то время как натрий, кальций и калий продолжают оставаться наиболее распространенными противоионами для слабокислых лекарств.Большинство этих противоионов увеличивают растворимость в воде. Slater et al. изучили возможность образования соли для RPR2000765, имеющего pKa 5,3 и собственную растворимость свободного основания 10 мкг / мл [32]. Плохая растворимость в воде привела к низкой биодоступности у животных. В то время как все солевые формы (гидрохлорид, гидробромид, метансульфонат, мезилат и камфорсульфонат) увеличивали растворимость исходного лекарственного средства, мезилатная соль постоянно давала более высокую растворимость, составляющую 39 мг / мл при 25 ° C.Также были учтены другие факторы, такие как гигроскопичность, чистый полиморфный профиль, размер частиц и свойства текучести, и все эти факторы способствовали образованию мезилатной соли для дальнейшего развития [32].
Это один из наиболее распространенных методов повышения растворимости слабокислых и основных лекарств. Гидрохлорид, мезилат, гидробромид, ацетат и фумарат являются наиболее распространенными противоионами, которые используются для основных химических соединений за последние 20 лет [31], в то время как натрий, кальций и калий продолжают оставаться наиболее распространенными противоионами для слабокислых лекарств.Большинство этих противоионов увеличивают растворимость в воде. Slater et al. изучили возможность образования соли для RPR2000765, имеющего pKa 5,3 и собственную растворимость свободного основания 10 мкг / мл [32]. Плохая растворимость в воде привела к низкой биодоступности у животных. В то время как все солевые формы (гидрохлорид, гидробромид, метансульфонат, мезилат и камфорсульфонат) увеличивали растворимость исходного лекарственного средства, мезилатная соль постоянно давала более высокую растворимость, составляющую 39 мг / мл при 25 ° C.Также были учтены другие факторы, такие как гигроскопичность, чистый полиморфный профиль, размер частиц и свойства текучести, и все эти факторы способствовали образованию мезилатной соли для дальнейшего развития [32]. Это показывает, что выбор подходящего противоиона не должен быть изолированным подходом, который сосредотачивается на одном соображении за раз, а должен быть целостным подходом, включающим одновременно дополнительные важные соображения.
Это показывает, что выбор подходящего противоиона не должен быть изолированным подходом, который сосредотачивается на одном соображении за раз, а должен быть целостным подходом, включающим одновременно дополнительные важные соображения. Было обнаружено, что эта уникальная характеристика является большим сдерживающим фактором для педиатрических составов. Позже были найдены солевые составы для снижения растворимости. Было обнаружено, что из различных отобранных форм солей соль стеариновой кислоты имеет пониженную растворимость и, кроме того, позволяет приготовить суспензию, которая эффективно подавляет горький вкус свободного основания. Это делает кислую солевую форму эритромицина гораздо более фармацевтически приемлемой, особенно для педиатрических пациентов.Подобно эритромицину, чтобы снизить растворимость кислотного или основного лекарственного средства, можно синтезировать соли, позволяющие разработать композицию в виде суспензии. Для кислых лекарств могут быть рассмотрены соли кальция или анионный обмен. Для основных лекарственных средств хорошим выбором могут быть соли длинноцепочечных жирных кислот (например, лауратов и памоатов) и катионообменные резонаты [12].
Было обнаружено, что эта уникальная характеристика является большим сдерживающим фактором для педиатрических составов. Позже были найдены солевые составы для снижения растворимости. Было обнаружено, что из различных отобранных форм солей соль стеариновой кислоты имеет пониженную растворимость и, кроме того, позволяет приготовить суспензию, которая эффективно подавляет горький вкус свободного основания. Это делает кислую солевую форму эритромицина гораздо более фармацевтически приемлемой, особенно для педиатрических пациентов.Подобно эритромицину, чтобы снизить растворимость кислотного или основного лекарственного средства, можно синтезировать соли, позволяющие разработать композицию в виде суспензии. Для кислых лекарств могут быть рассмотрены соли кальция или анионный обмен. Для основных лекарственных средств хорошим выбором могут быть соли длинноцепочечных жирных кислот (например, лауратов и памоатов) и катионообменные резонаты [12]. В случае кислых лекарств для улучшения вкуса могут быть полезны основные соли, такие как триэтаноламины [12].Эти примеры демонстрируют, что солевые стратегии могут быть эффективным методом маскировки вкуса горьких лекарств.
В случае кислых лекарств для улучшения вкуса могут быть полезны основные соли, такие как триэтаноламины [12].Эти примеры демонстрируют, что солевые стратегии могут быть эффективным методом маскировки вкуса горьких лекарств. Например, цефалоспориновые антибиотики представляют собой нейтральные цвиттерионы и не очень стабильны в растворе.Соли моно-противоионов не обладали большой стабильностью, и, хотя соли ди-противоионов давали стабильные растворы, они были довольно кислыми с pH <2. Эта проблема с pH была решена путем приготовления дигидрохлоридной соли для восстановления 2 мл аргинина при температуре время инъекции. Это привело к стабильному раствору лекарства в желаемом диапазоне pH [12]. Это ясно свидетельствует о том, что солевые составы можно использовать для приготовления подходящих парентеральных растворов для достижения желаемого терапевтического результата.
Например, цефалоспориновые антибиотики представляют собой нейтральные цвиттерионы и не очень стабильны в растворе.Соли моно-противоионов не обладали большой стабильностью, и, хотя соли ди-противоионов давали стабильные растворы, они были довольно кислыми с pH <2. Эта проблема с pH была решена путем приготовления дигидрохлоридной соли для восстановления 2 мл аргинина при температуре время инъекции. Это привело к стабильному раствору лекарства в желаемом диапазоне pH [12]. Это ясно свидетельствует о том, что солевые составы можно использовать для приготовления подходящих парентеральных растворов для достижения желаемого терапевтического результата. Противоионы действуют как нейтрализующие агенты, связываясь с API через кулоновские силы, чтобы обеспечить пассивное поглощение. Например, образование пар салицилатов с алкиламинами и ионами четвертичного аммония показало увеличение чрескожного проникновения лекарственного средства.Увеличенное проникновение было успешно достигнуто с помощью диэтиламиновой соли диклофенака в качестве геля для местного применения, в то время как натриевая соль доступна для перорального всасывания [35]. Следовательно, может быть разработан подходящий состав для увеличения трансдермальной проницаемости для желаемых системных эффектов.
Противоионы действуют как нейтрализующие агенты, связываясь с API через кулоновские силы, чтобы обеспечить пассивное поглощение. Например, образование пар салицилатов с алкиламинами и ионами четвертичного аммония показало увеличение чрескожного проникновения лекарственного средства.Увеличенное проникновение было успешно достигнуто с помощью диэтиламиновой соли диклофенака в качестве геля для местного применения, в то время как натриевая соль доступна для перорального всасывания [35]. Следовательно, может быть разработан подходящий состав для увеличения трансдермальной проницаемости для желаемых системных эффектов. Солевые составы сыграли важную роль в обеспечении местной доставки лекарств с гораздо более длительным периодом полураспада. Например, сальметерол является бета-адренергическим агонистом длительного действия, который используется в терапии хронической обструктивной болезни легких (ХОБЛ). Пониженная растворимость была необходима, чтобы обеспечить более продолжительное время на месте действия, и была достигнута за счет образования соли ксинафоата.Это медленно растворяющееся соединение усиливает длительный период полувыведения сальметерола. Таким образом, ксинафоатная соль салметерола служила важным препаратом и ярким примером, демонстрирующим, как свойства API могут быть изменены для достижения желаемых результатов [36].
Солевые составы сыграли важную роль в обеспечении местной доставки лекарств с гораздо более длительным периодом полураспада. Например, сальметерол является бета-адренергическим агонистом длительного действия, который используется в терапии хронической обструктивной болезни легких (ХОБЛ). Пониженная растворимость была необходима, чтобы обеспечить более продолжительное время на месте действия, и была достигнута за счет образования соли ксинафоата.Это медленно растворяющееся соединение усиливает длительный период полувыведения сальметерола. Таким образом, ксинафоатная соль салметерола служила важным препаратом и ярким примером, демонстрирующим, как свойства API могут быть изменены для достижения желаемых результатов [36]. API-интерфейсы с плохими характеристиками текучести могут привести к получению конечных продуктов с неприемлемым содержанием однородности, вариациями веса и физической несогласованностью. Кристаллическая природа API в основном предпочтительна, так как она поддается методам, улучшающим свойства текучести [37]. Таким образом, аморфное лекарственное средство может быть приготовлено в виде подходящей солевой формы, которая улучшает его свойства в твердом состоянии, способствуя кристаллической структуре.
API-интерфейсы с плохими характеристиками текучести могут привести к получению конечных продуктов с неприемлемым содержанием однородности, вариациями веса и физической несогласованностью. Кристаллическая природа API в основном предпочтительна, так как она поддается методам, улучшающим свойства текучести [37]. Таким образом, аморфное лекарственное средство может быть приготовлено в виде подходящей солевой формы, которая улучшает его свойства в твердом состоянии, способствуя кристаллической структуре. Это может привести к кислым водным растворам соли. Сильнокислые водные растворы могут вызывать коррозию металлических контейнеров, производственных инструментов и другого оборудования. Следовательно, детали, используемые для таблетирования, такие как пуансоны, матрицы и столы для штампов, более уязвимы для повреждений, вызванных корродирующими твердыми частицами, поскольку они находятся в постоянном контакте со смесями таблеток под высоким давлением и трением. Металлическая поверхность машин для наполнения капсул и механические силы, задействованные при наполнении лекарств, также могут подвергнуться коррозии.Коррозионные соли могут сделать таблетирование технически невозможным и, если они используются, могут привести к образованию следов металла в таблетках во время прессования. Следовательно, эти типы коррозионных противоионов не следует использовать для создания солевых составов или, в качестве альтернативы, их следует в достаточной степени разбавлять вспомогательными веществами, чтобы избежать серьезных коррозионных свойств [39].
Это может привести к кислым водным растворам соли. Сильнокислые водные растворы могут вызывать коррозию металлических контейнеров, производственных инструментов и другого оборудования. Следовательно, детали, используемые для таблетирования, такие как пуансоны, матрицы и столы для штампов, более уязвимы для повреждений, вызванных корродирующими твердыми частицами, поскольку они находятся в постоянном контакте со смесями таблеток под высоким давлением и трением. Металлическая поверхность машин для наполнения капсул и механические силы, задействованные при наполнении лекарств, также могут подвергнуться коррозии.Коррозионные соли могут сделать таблетирование технически невозможным и, если они используются, могут привести к образованию следов металла в таблетках во время прессования. Следовательно, эти типы коррозионных противоионов не следует использовать для создания солевых составов или, в качестве альтернативы, их следует в достаточной степени разбавлять вспомогательными веществами, чтобы избежать серьезных коррозионных свойств [39]. Кроме того, соли лекарственных препаратов со значениями pH 2,5 или ниже для насыщенных водных растворов обычно оказываются агрессивными. Испытания на коррозионную активность следует проводить, если значение pH насыщенного водного раствора меньше или равно четырем.Например, слабоосновные лекарственные средства (pKa = 4,7), как упоминалось Stahl et al., Считались разработанными либо в виде свободных оснований, либо в виде гидрохлоридных / метансульфонатных солей. Однако позже от хлористоводородной соли отказались из-за сильной коррозии. Метансульфонат не вызывает коррозии нержавеющей стали и лишь незначительно вызывает коррозию серого чугуна и сплавов инструментальной стали. Поэтому в качестве предпочтительного противоиона был выбран метансульфонат, за которым последовали дальнейшие разработки [12]. Таким образом, необходимо изучить уникальные свойства противоионов, чтобы правильно производить некоррозионные лекарственные препараты.
Кроме того, соли лекарственных препаратов со значениями pH 2,5 или ниже для насыщенных водных растворов обычно оказываются агрессивными. Испытания на коррозионную активность следует проводить, если значение pH насыщенного водного раствора меньше или равно четырем.Например, слабоосновные лекарственные средства (pKa = 4,7), как упоминалось Stahl et al., Считались разработанными либо в виде свободных оснований, либо в виде гидрохлоридных / метансульфонатных солей. Однако позже от хлористоводородной соли отказались из-за сильной коррозии. Метансульфонат не вызывает коррозии нержавеющей стали и лишь незначительно вызывает коррозию серого чугуна и сплавов инструментальной стали. Поэтому в качестве предпочтительного противоиона был выбран метансульфонат, за которым последовали дальнейшие разработки [12]. Таким образом, необходимо изучить уникальные свойства противоионов, чтобы правильно производить некоррозионные лекарственные препараты. Выбор противоиона должен основываться на понимании типов химического взаимодействия с вспомогательными веществами.
Выбор противоиона должен основываться на понимании типов химического взаимодействия с вспомогательными веществами. Фактически, для некоторых типов лекарственных форм даже более важно иметь солевую форму, чем несолевую форму. Одной из основных проблем для инъекционных лекарственных форм является ограниченная растворимость лекарственного средства в нескольких носителях, подходящих для инъекций. Например, образование солевых композиций гораздо более важно для инъекционных лекарственных форм, чем для пероральных или трансдермальных лекарственных форм.Это связано с тем, что инъекционные препараты, которые в основном вводятся внутривенно (IV), требуют растворимых продуктов, чтобы избежать флебита или раздражения тканей из-за нерастворимых терапевтических агентов [40]. Исторически было одобрено больше форм солей для инъекций, чем любых других форм солей. Обзорная статья Paulekuhn et al. описали, как более 70% инъекционных лекарственных форм содержат соли по сравнению только с 50–60% пероральных лекарственных форм. Большая потребность в хорошо растворимой соли для инъекционных лекарственных форм является одной из важных движущих сил, стоящих за солевыми формами [1].
Фактически, для некоторых типов лекарственных форм даже более важно иметь солевую форму, чем несолевую форму. Одной из основных проблем для инъекционных лекарственных форм является ограниченная растворимость лекарственного средства в нескольких носителях, подходящих для инъекций. Например, образование солевых композиций гораздо более важно для инъекционных лекарственных форм, чем для пероральных или трансдермальных лекарственных форм.Это связано с тем, что инъекционные препараты, которые в основном вводятся внутривенно (IV), требуют растворимых продуктов, чтобы избежать флебита или раздражения тканей из-за нерастворимых терапевтических агентов [40]. Исторически было одобрено больше форм солей для инъекций, чем любых других форм солей. Обзорная статья Paulekuhn et al. описали, как более 70% инъекционных лекарственных форм содержат соли по сравнению только с 50–60% пероральных лекарственных форм. Большая потребность в хорошо растворимой соли для инъекционных лекарственных форм является одной из важных движущих сил, стоящих за солевыми формами [1]. Наиболее часто используемые анионы для пероральных лекарственных форм — это хлорид, сульфат и малеат; хлорид, сульфат и ацетат были тремя главными анионами, используемыми для инъекционных лекарственных форм. В то время как натрий, калий и кальций были тремя наиболее предпочтительными катионами, используемыми как для пероральных, так и для парентеральных составов. В последнее время противоион лизина стал популярным выбором для инъекционных препаратов, появляясь примерно в 15% инъекционных солей, которые были одобрены в период с 2002 по 2006 год [1]. Таким образом, солеобразование является одним из важных способов достижения желаемых характеристик лекарственного средства, таких как повышенная растворимость при парентеральном пути введения.
Наиболее часто используемые анионы для пероральных лекарственных форм — это хлорид, сульфат и малеат; хлорид, сульфат и ацетат были тремя главными анионами, используемыми для инъекционных лекарственных форм. В то время как натрий, калий и кальций были тремя наиболее предпочтительными катионами, используемыми как для пероральных, так и для парентеральных составов. В последнее время противоион лизина стал популярным выбором для инъекционных препаратов, появляясь примерно в 15% инъекционных солей, которые были одобрены в период с 2002 по 2006 год [1]. Таким образом, солеобразование является одним из важных способов достижения желаемых характеристик лекарственного средства, таких как повышенная растворимость при парентеральном пути введения.
 По той же причине был разработан памоат имипрамина, и было обнаружено, что его растворимость значительно ниже, чем у гидрохлоридной соли.Эта задержка скорости высвобождения лекарственного средства подходила для желаемого препарата SR [12].
По той же причине был разработан памоат имипрамина, и было обнаружено, что его растворимость значительно ниже, чем у гидрохлоридной соли.Эта задержка скорости высвобождения лекарственного средства подходила для желаемого препарата SR [12]. Проблема токсичности АФИ имеет решающее значение и может способствовать ограничению эффективного использования лекарств. Иногда солевые подходы использовались для уменьшения желудочно-кишечной (ЖКТ) токсичности исходного лекарственного средства.Различные примеры [43,44,45] демонстрируют такое использование противоионов, которые легко метаболизируются и выводятся из организма при минимальной токсичности. Таким образом, эти подходы были полезны в решении проблем токсичности ЖКТ. Например, известно, что салицилаты вызывают желудочно-кишечные кровотечения и связанные с ними нарушения, включая язвы. Холин — важный противоион с минимальной токсичностью; Сообщалось, что салицилат холина продемонстрировал более низкую частоту токсичности желудочно-кишечного тракта и лучше переносился при более высоких дозах [43].Таким образом, токсичность API-интерфейсов для желудочно-кишечного тракта может быть эффективно снижена путем выбора подходящих солевых форм.
Проблема токсичности АФИ имеет решающее значение и может способствовать ограничению эффективного использования лекарств. Иногда солевые подходы использовались для уменьшения желудочно-кишечной (ЖКТ) токсичности исходного лекарственного средства.Различные примеры [43,44,45] демонстрируют такое использование противоионов, которые легко метаболизируются и выводятся из организма при минимальной токсичности. Таким образом, эти подходы были полезны в решении проблем токсичности ЖКТ. Например, известно, что салицилаты вызывают желудочно-кишечные кровотечения и связанные с ними нарушения, включая язвы. Холин — важный противоион с минимальной токсичностью; Сообщалось, что салицилат холина продемонстрировал более низкую частоту токсичности желудочно-кишечного тракта и лучше переносился при более высоких дозах [43].Таким образом, токсичность API-интерфейсов для желудочно-кишечного тракта может быть эффективно снижена путем выбора подходящих солевых форм. Malek et al. продемонстрировали, что свойства распределения некоторых антибиотиков можно значительно изменить с помощью макромолекулярных противоионов [45]. Макромолекулы, такие как полисахариды, полиакриловые кислоты, сульфоновые кислоты и полиуроновые кислоты, были объединены с популярными антибиотиками, такими как стрептомицин и неомицин.По сравнению с сульфатной солью стрептомицина эти высокомолекулярные противоионные соли со стрептомицином показали более высокое распределение лекарства в лимфатических узлах и меньшее присутствие лекарства в плазме. Селективное распределение затем привело к замедленному выведению стрептомицина [46]. Это открывает широкие возможности для исследований по поиску уникальных форм макромолекулярных солей, позволяющих изменять распределение лекарства в зависимости от желаемых терапевтических результатов.
Malek et al. продемонстрировали, что свойства распределения некоторых антибиотиков можно значительно изменить с помощью макромолекулярных противоионов [45]. Макромолекулы, такие как полисахариды, полиакриловые кислоты, сульфоновые кислоты и полиуроновые кислоты, были объединены с популярными антибиотиками, такими как стрептомицин и неомицин.По сравнению с сульфатной солью стрептомицина эти высокомолекулярные противоионные соли со стрептомицином показали более высокое распределение лекарства в лимфатических узлах и меньшее присутствие лекарства в плазме. Селективное распределение затем привело к замедленному выведению стрептомицина [46]. Это открывает широкие возможности для исследований по поиску уникальных форм макромолекулярных солей, позволяющих изменять распределение лекарства в зависимости от желаемых терапевтических результатов. Различные солевые формы эффективно используются для изменения начала и продолжительности действия лекарств. Например, было замечено, что амфетамин с одной солью в препаратах декстроамфетамина не является хорошим выбором для получения быстрых и устойчивых психостимулирующих эффектов. Вместо этого Adderall XR ® был разработан как комбинация аспартатной и сульфатной солей амфетамина, а также сахаратной и сульфатной солей декстроамфетамина. Эти разные соли в одном лекарственном препарате допускали разную скорость метаболизма и обладали разным началом действия.Это привело к более быстрой индукции терапевтического эффекта при сохранении этого эффекта в течение достаточно длительного времени [47]. Этот пример показывает, как можно использовать соль для изменения начала и продолжительности действия лекарственного средства для достижения желаемых результатов.
Различные солевые формы эффективно используются для изменения начала и продолжительности действия лекарств. Например, было замечено, что амфетамин с одной солью в препаратах декстроамфетамина не является хорошим выбором для получения быстрых и устойчивых психостимулирующих эффектов. Вместо этого Adderall XR ® был разработан как комбинация аспартатной и сульфатной солей амфетамина, а также сахаратной и сульфатной солей декстроамфетамина. Эти разные соли в одном лекарственном препарате допускали разную скорость метаболизма и обладали разным началом действия.Это привело к более быстрой индукции терапевтического эффекта при сохранении этого эффекта в течение достаточно длительного времени [47]. Этот пример показывает, как можно использовать соль для изменения начала и продолжительности действия лекарственного средства для достижения желаемых результатов. Например, в литературе описаны антигистаминные соли пенициллина, поскольку пенициллин может вызывать аллергический ответ у некоторых пациентов.Основная идея заключалась в том, чтобы смягчить этот аллергический ответ на пенициллин с помощью хорошо задокументированных противоаллергических препаратов [48]. Точно так же внутримышечная (IM) инъекция бензилпенициллина была приготовлена совместно с бензатиновым противоионом. Бензатин — это хорошо известный местный анестетик, обезболивающий место внутримышечной инъекции. Этот совместный препарат уменьшает боль, связанную с очень высокой внутримышечной депо дозой бензилпенициллина, которая требуется для лечения определенных состояний, таких как сифилис [49]. Другой известный пример, отражающий использование противоионов для минимизации побочных эффектов, — это Драмамин ® (дифенгидрамин + 8-хлортеофиллин), где 8-хлортеофиллин действует как стимулятор, нейтрализующий сонливость, вызванную дифенгидрамином [50,51].
Например, в литературе описаны антигистаминные соли пенициллина, поскольку пенициллин может вызывать аллергический ответ у некоторых пациентов.Основная идея заключалась в том, чтобы смягчить этот аллергический ответ на пенициллин с помощью хорошо задокументированных противоаллергических препаратов [48]. Точно так же внутримышечная (IM) инъекция бензилпенициллина была приготовлена совместно с бензатиновым противоионом. Бензатин — это хорошо известный местный анестетик, обезболивающий место внутримышечной инъекции. Этот совместный препарат уменьшает боль, связанную с очень высокой внутримышечной депо дозой бензилпенициллина, которая требуется для лечения определенных состояний, таких как сифилис [49]. Другой известный пример, отражающий использование противоионов для минимизации побочных эффектов, — это Драмамин ® (дифенгидрамин + 8-хлортеофиллин), где 8-хлортеофиллин действует как стимулятор, нейтрализующий сонливость, вызванную дифенгидрамином [50,51]. Прасугрел представляет собой важный пример лекарственного взаимодействия при совместном применении с ингибиторами протонной помпы (ИПП) [52]. Прасугрель доступен в виде гидрохлоридной соли, которая, как было обнаружено, обеспечивает лучшую абсорбцию при более высоком pH желудочного сока по сравнению с формой свободного основания.Однако во время производства лекарства было обнаружено, что кислотно-основная реакция может преобразовывать солевую форму в форму свободного основания, что влияет на фармакокинетику. Это дополнительно осложняется одновременным применением ИПП с прасугрелом, а совместное введение может изменить pH желудочного сока, а также соотношение соли и основания. Таким образом, исследования биоэквивалентности с ИПП или без них стали клинически актуальными. Было обнаружено, что когда прасугрел в различных соотношениях соль / основание вводился совместно с лансопразолом, все формы демонстрировали одинаковую степень абсорбции; однако скорость абсорбции оказалась иной [52].Это был очень важный клинический результат, поскольку высокая конверсия соли в основание значительно задерживала максимальную агрегацию тромбоцитов, достигаемую прасугрелом, что является важной терапевтической целью после инфаркта миокарда.
Прасугрел представляет собой важный пример лекарственного взаимодействия при совместном применении с ингибиторами протонной помпы (ИПП) [52]. Прасугрель доступен в виде гидрохлоридной соли, которая, как было обнаружено, обеспечивает лучшую абсорбцию при более высоком pH желудочного сока по сравнению с формой свободного основания.Однако во время производства лекарства было обнаружено, что кислотно-основная реакция может преобразовывать солевую форму в форму свободного основания, что влияет на фармакокинетику. Это дополнительно осложняется одновременным применением ИПП с прасугрелом, а совместное введение может изменить pH желудочного сока, а также соотношение соли и основания. Таким образом, исследования биоэквивалентности с ИПП или без них стали клинически актуальными. Было обнаружено, что когда прасугрел в различных соотношениях соль / основание вводился совместно с лансопразолом, все формы демонстрировали одинаковую степень абсорбции; однако скорость абсорбции оказалась иной [52].Это был очень важный клинический результат, поскольку высокая конверсия соли в основание значительно задерживала максимальную агрегацию тромбоцитов, достигаемую прасугрелом, что является важной терапевтической целью после инфаркта миокарда. Таким образом, различные солевые формы, а также лекарственные взаимодействия могут иметь важное клиническое значение [52].
Таким образом, различные солевые формы, а также лекарственные взаимодействия могут иметь важное клиническое значение [52]. Это заявление было отклонено в пользу оригинального патента. Однако некоторым производителям удалось изменить определенные характеристики дозировки, поскольку они продемонстрировали уникальные преимущества. Одним из хорошо известных примеров является диклофенак эполамин (Flector ® ), который был одобрен и запатентован как трансдермальный пластырь, в то время как его соли натрия и калия уже были доступны в виде общих таблеток, капсул, гелей для местного применения и растворов. Первоначальный патент на традиционный состав был выдан 4 марта 1997 года.Institut Biochimique SA (IBSA) получил новый патент на Flector ® , который был одобрен FDA 31 января 2007 г. и действителен до 13 апреля 2019 г. [54]. Инновационная формула оправдывала расширенные патентные и маркетинговые эксклюзивные права. Это демонстрирует, что патентование инновационных солевых форм может придать некоторым продуктам исключительность на рынке и помочь компаниям защитить свою интеллектуальную собственность.
Это заявление было отклонено в пользу оригинального патента. Однако некоторым производителям удалось изменить определенные характеристики дозировки, поскольку они продемонстрировали уникальные преимущества. Одним из хорошо известных примеров является диклофенак эполамин (Flector ® ), который был одобрен и запатентован как трансдермальный пластырь, в то время как его соли натрия и калия уже были доступны в виде общих таблеток, капсул, гелей для местного применения и растворов. Первоначальный патент на традиционный состав был выдан 4 марта 1997 года.Institut Biochimique SA (IBSA) получил новый патент на Flector ® , который был одобрен FDA 31 января 2007 г. и действителен до 13 апреля 2019 г. [54]. Инновационная формула оправдывала расширенные патентные и маркетинговые эксклюзивные права. Это демонстрирует, что патентование инновационных солевых форм может придать некоторым продуктам исключительность на рынке и помочь компаниям защитить свою интеллектуальную собственность.
 Как упоминалось в разделе pK a , идеальная разница pK a должна поддерживаться в системе растворителей, которая используется для кристаллизации; Проблема с этим требованием состоит в том, что часто для кристаллизации используются неводные или смешанные системы растворителей, которые могут повлиять на pK a . Последние достижения, такие как микрожидкостная платформа, могут преодолеть ограничение несовместимости растворителей. Микрожидкостная платформа состоит из 48 лунок, каждая — примерно 87 лунок.Объем 5 нл. Уменьшение объема позволяет проводить скрининг образцов с концентрацией соли до 1 мг [55]. Соль API получают с использованием одного из четырех методов: термического, антирастворителя, испарения и превращения суспензии [9]. Независимо от используемого метода, на кристаллизацию влияют тип добавки, концентрация, pH и ионная сила [9]. Полученная соль характеризуется порошковой дифракцией рентгеновских лучей, которая дает информацию о том, является ли образец кристаллическим или аморфным.
Как упоминалось в разделе pK a , идеальная разница pK a должна поддерживаться в системе растворителей, которая используется для кристаллизации; Проблема с этим требованием состоит в том, что часто для кристаллизации используются неводные или смешанные системы растворителей, которые могут повлиять на pK a . Последние достижения, такие как микрожидкостная платформа, могут преодолеть ограничение несовместимости растворителей. Микрожидкостная платформа состоит из 48 лунок, каждая — примерно 87 лунок.Объем 5 нл. Уменьшение объема позволяет проводить скрининг образцов с концентрацией соли до 1 мг [55]. Соль API получают с использованием одного из четырех методов: термического, антирастворителя, испарения и превращения суспензии [9]. Независимо от используемого метода, на кристаллизацию влияют тип добавки, концентрация, pH и ионная сила [9]. Полученная соль характеризуется порошковой дифракцией рентгеновских лучей, которая дает информацию о том, является ли образец кристаллическим или аморфным. Кроме того, инфракрасная (ИК), рамановская спектроскопия и спектроскопия ядерного магнитного резонанса (ЯМР) предоставляет информацию о взаимодействии между исходным соединением и противоионом [9].Термические методы, такие как дифференциальная сканирующая калориметрия (ДСК), используются для определения температуры плавления и энтальпии плавления. Оба эти свойства помогают прогнозировать растворимость и стабильность солей [9]. Чистоту и кристалличность образца можно оценить по резкости эндотермы. Природа эндотермы также может дать информацию о гидратах и сольватах в кристаллической структуре [9]. Нивергельт и др. недавно сообщили о высокопроизводительном скрининге солей катионных API с использованием полуавтоматической техники.В их методе для кристаллизации использовались только нанолитры раствора аналита, что давало монокристаллы подходящего размера для определения характеристик с помощью определения рентгеновской структуры монокристаллов [56].
Кроме того, инфракрасная (ИК), рамановская спектроскопия и спектроскопия ядерного магнитного резонанса (ЯМР) предоставляет информацию о взаимодействии между исходным соединением и противоионом [9].Термические методы, такие как дифференциальная сканирующая калориметрия (ДСК), используются для определения температуры плавления и энтальпии плавления. Оба эти свойства помогают прогнозировать растворимость и стабильность солей [9]. Чистоту и кристалличность образца можно оценить по резкости эндотермы. Природа эндотермы также может дать информацию о гидратах и сольватах в кристаллической структуре [9]. Нивергельт и др. недавно сообщили о высокопроизводительном скрининге солей катионных API с использованием полуавтоматической техники.В их методе для кристаллизации использовались только нанолитры раствора аналита, что давало монокристаллы подходящего размера для определения характеристик с помощью определения рентгеновской структуры монокристаллов [56]. Их часто использовали для предотвращения или лечения обморока, но нюхательные соли вышли из моды в большинстве медицинских кругов. Нюхательные соли все еще можно купить без рецепта для личного пользования.
Их часто использовали для предотвращения или лечения обморока, но нюхательные соли вышли из моды в большинстве медицинских кругов. Нюхательные соли все еще можно купить без рецепта для личного пользования. Может показаться чудесным видеть, как немного соли пробуждает бессознательного человека, но резкий запах и выброс кислорода просто запускают ваше сознание.
Может показаться чудесным видеть, как немного соли пробуждает бессознательного человека, но резкий запах и выброс кислорода просто запускают ваше сознание.
 Обоняние солей может маскировать более серьезную травму или скрывать ухудшение симптомов, затрудняя надлежащее неврологическое обследование.
Обоняние солей может маскировать более серьезную травму или скрывать ухудшение симптомов, затрудняя надлежащее неврологическое обследование. 
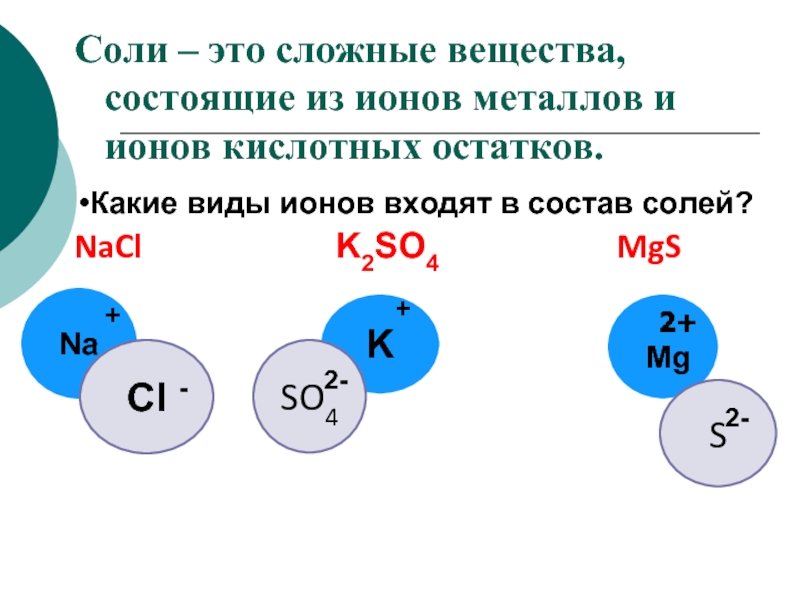
 Примерно столько натрия содержится в 1 чайной ложке поваренной соли.
Примерно столько натрия содержится в 1 чайной ложке поваренной соли. Если вы пациент клиники Мэйо, это может
включать защищенную медицинскую информацию. Если мы объединим эту информацию с вашими защищенными
информация о здоровье, мы будем рассматривать всю эту информацию как защищенную
информацию и будет использовать или раскрывать эту информацию только в соответствии с нашим уведомлением о
политика конфиденциальности. Вы можете отказаться от рассылки по электронной почте в любое время, нажав на
ссылку для отказа от подписки в электронном письме.
Если вы пациент клиники Мэйо, это может
включать защищенную медицинскую информацию. Если мы объединим эту информацию с вашими защищенными
информация о здоровье, мы будем рассматривать всю эту информацию как защищенную
информацию и будет использовать или раскрывать эту информацию только в соответствии с нашим уведомлением о
политика конфиденциальности. Вы можете отказаться от рассылки по электронной почте в любое время, нажав на
ссылку для отказа от подписки в электронном письме.
 https: // www.foodaryguidelines.gov. По состоянию на 29 июня 2021 г.
https: // www.foodaryguidelines.gov. По состоянию на 29 июня 2021 г.

 Поваренная соль, напротив, поступает почти исключительно из прудов-испарителей, которые удаляют соль из морской воды.
Поваренная соль, напротив, поступает почти исключительно из прудов-испарителей, которые удаляют соль из морской воды. «Мы благодарны нашим партнерам из правоохранительных органов за их помощь в расследовании и прокуратуре США за судебное преследование по делу. Дистрибьюторам вроде Ортона, которые наживаются на этом яде, нет места в нашем сообществе ».
«Мы благодарны нашим партнерам из правоохранительных органов за их помощь в расследовании и прокуратуре США за судебное преследование по делу. Дистрибьюторам вроде Ортона, которые наживаются на этом яде, нет места в нашем сообществе ». Сообщается, что Alpha-PHP имитирует эффекты кокаина и метамфетамина. Побочные эффекты, связанные со злоупотреблением альфа-PHP, включали рвоту, возбуждение, паранойю, гипертонию, потерю сознания, тахикардию, судороги, остановку сердца, рабдомиолиз или смерть.
Сообщается, что Alpha-PHP имитирует эффекты кокаина и метамфетамина. Побочные эффекты, связанные со злоупотреблением альфа-PHP, включали рвоту, возбуждение, паранойю, гипертонию, потерю сознания, тахикардию, судороги, остановку сердца, рабдомиолиз или смерть.

