Квантово-механическая модель атома
Современная модель атома является развитием планетарной модели. Согласно этой модели, ядро атома состоит из положительно заряженных протонов и не имеющих заряда нейтронов и окружено отрицательно заряженными электронами. Однако представления квантовой механики не позволяют считать, что электроны движутся вокруг ядра по сколько-нибудь определённым траекториям (неопределённость координаты электрона в атоме может быть сравнима с размерами самого атома).
Квантовые числа (К.ч.)
Набор К. ч., исчерпывающе определяющий состояние квантовой системы, называется полным. Совокупность состояний, отвечающих всем возможным значениям К. ч. из полного набора, образует полную систему состояний. Состояние электрона в атоме определяется четырьмя К. ч. соответственно четырём степеням свободы электрона (3 степени свободы связаны с тремя координатами, определяющими пространственное положение электрона, а четвёртая, внутренняя, степень свободы — с его спином). Для атома водорода и водородоподобных атомов эти К. ч., образующие полный набор, следующие.
Главное К. ч. n = 1, 2, 3,… определяет уровни энергии электрона.
Азимутальное
(или орбитальное) К. ч. l
= 0, 1, 2,…, n
—1
задаёт спектр возможных значений
квадрата орбитального момента количества
движения электрона: 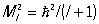
Магнитное
К. ч. ml характеризует
возможные значения проекции Mlz орбитального
момента Ml на
некоторое, произвольно выбранное,
направление (принимаемое за ось z):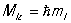 l
до + l (всего 2 l + 1 значений).
l
до + l (всего 2 l + 1 значений).
Магнитное спиновое К, ч., или просто спиновое К. ч., m
s характеризует возможные значения проекции спина электрона и может принимать 2 значения:ms = ± 1/2.
Задание состояния электрона с помощью К. ч. n, l, ml и ms не учитывает так называемой тонкой структуры энергетических уровней — расщепления уровней с данным n (при n ≥ 2) в результате влияния спина на орбитальное движение электрона.
При́нцип Па́ули(принцип запрета) — один из фундаментальных принципов квантовой механики, согласно которому два и более тождественных фермиона (частиц с полуцелым спином) не могут одновременно находиться в одном квантовом состоянии.
Принцип Паули можно сформулировать следующим образом: в пределах одной квантовой системы в данном квантовом состоянии может находиться только одна частица, состояние другой должно отличаться хотя бы одним квантовым числом
Правило Хундаопределяет порядок заполнения орбиталей определённого подслоя и формулируется следующим образом: модуль суммарного значения спинового квантового числа электронов данного подслоя должен быть максимальным. Сформулировано Фридрихом Хундом в 1925 году.
Это означает, что в каждой из орбиталей подслоя заполняется сначала один электрон, а только после исчерпания незаполненных орбиталей на эту орбиталь добавляется второй электрон. При этом на одной орбитали находятся два электрона с полуцелыми спинами противоположного знака, которые спариваются (образуют двухэлектронное облако) и, в результате, суммарный спин орбитали становится равным нулю.
Химические свойства атомов определяются конфигурацией электронной оболочки и описываются квантовой механикой. Положение атома в таблице Менделеева определяется электрическим зарядом его ядра (то есть количеством протонов), в то время как количество нейтронов принципиально не влияет на химические свойства; при этом нейтронов в ядре, как правило, больше, чем протонов (см.: атомное ядро). Если атом находится в нейтральном состоянии, то количество электронов в нём равно количеству протонов. Основная масса атома сосредоточена в ядре, а массовая доля электронов в общей массе атома незначительна (несколько сотых процента массы ядра).
Квантово-механическая модель строения атома — МегаЛекции
Модели строения атома
Модель Томсона
Первая модель строения атома была предложена Дж. Томсоном в 1904 г.,
согласно которой атом – положительно заряженная сфера с вкрапленными в нее электронами. Несмотря на свое несовершенство томсоновская модель
позволяла объяснить явления испускания, поглощения и рассеяния света атомами, а также установить число электронов в атомах легких элементов.
Модель Резерфорда
Модель Томсона была опровергнута Э. Резерфордом (1911 г.), который доказал, что положительный заряд и практически вся масса атома сконцентрированы в малой части его объема – ядре, вокруг которого двигаются электроны. Эта модель строения атома известна как планетарная,
т. к. электроны вращаются вокруг ядра подобно планетам солнечной системы.
Согласно законам классической электродинамики, движение электрона по окружности вокруг ядра будет устойчивым, если сила кулоновского притяжения будет равна центробежной силе. Однако, в соответствии с теорией электромагнитного поля, электроны в этом случае должны двигаться по спирали, непрерывно излучая энергию, и падать на ядро. Однако атом устойчив.
К тому же при непрерывном излучении энергии у атома должен наблюдаться непрерывный, сплошной спектр. На самом деле спектр атома состоит из отдельных линий и серий.
Таким образом, данная модель противоречит законам электродинамики и не объясняет линейчатого характера атомного спектра.
Модель Бора
В 1913 г. Н. Бор предложил свою теорию строения атома, не отрицая при этом полностью предыдущие представления. В основу своей теории Бор положил два постулата.
Первый постулат говорит о том, что электрон может вращаться вокруг ядра только по определенным стационарным орбитам. Находясь на них, он не излучает и не поглощает энергию. При движении по любой стационарной орбите запас энергии электрона (Е1, Е2 …) остается постоянным. Чем ближе к ядру расположена орбита, тем меньше запас энергии электрона Е1 ˂ Е2 …˂ Еn .
Энергия электрона на орбитах определяется уравнением:

где m – масса электрона, h – постоянная Планка, n – 1, 2, 3… (n=1 для 1-ой орбиты, n=2 для 2-ой и т.д.).
Второй постулат говорит о том, что при переходе с одной орбиты на другую электрон поглощает или выделяет квант (порцию) энергии.
Если подвергнуть атомы воздействию (нагреванию, облучению и др.), то электрон может поглотить квант энергии и перейти на более удаленную от ядра орбиту. В этом случае говорят о возбужденном состоянии атома. При обратом переходе электрона (на более близкую к ядру орбиту) энергия выделяется в виде кванта лучистой энергии – фотона. В спектре это фиксируется определенной линией. На основании формулы
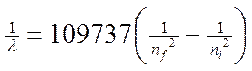 ,
,
где λ – длина волны, n = квантовые числа, характеризующие ближнюю и дальнюю орбиты, Бор рассчитал длины волн для всех серий в спектре атома водорода. Полученные результаты соответствовали экспериментальным данным. Стало ясным происхождение прерывистых линейчатых спектров. Они – результат излучения энергии атомами при переходе электронов из возбужденного состояния в стационарное. Переходы электронов на 1-ю орбиту образуют группу частот серии Лаймана, на 2-ю – серию Бальмера, на 3-ю серию Пашена (табл. 1).
Таблица 1
Проверка формулы Бора для серий водородного спектра
| Название серии | λ, А Экспериментальная | λ, А Вычисленная Бором |
| Пашена | 18751,3 12817,5 10938,0 10049,8 | |
| Бальмера | 6564,66 4862,71 4102,91 3971,20 3799,00 3712,70 | 6564,70 4862,80 4341,70 4102,93 3971,23 3799,01 3712,62 |
| Лаймана | 1215,68 1025,73 972,5 |
Однако, теория Бора не смогла объяснить расщепление линий в спектрах многоэлектронных атомов. Бор исходил из того, что электрон – это частица, и использовал для описания электрона законы, характерные для частиц. Вместе с тем накапливались факты, свидетельствующие о том, что электрон способен проявлять и волновые свойства. Классическая механика оказалась не в состоянии объяснить движение микрообъектов, обладающих одновременно свойствами материальных частиц и свойствами волны. Эту задачу позволила решить квантовая механика – физическая теория, исследующая общие закономерности движения и взаимодействия микрочастиц, обладающих очень малой массой (табл. 2).
Таблица 2
Свойства элементарных частиц, образующих атом
| Частица | Заряд | Масса | ||
| Кл | Условн.ед. | г | А.е.м. | |
| Электрон | — 1,6·10-19 | -1 | 9,10·10-28 | 0,00055 |
| Протон | 1,6·10-19 | +1 | 1,67·10-24 | 1,00728 |
| Нейтрон | 1,67·10-24 | 1,00866 |
Квантово-механическая модель строения атома
В основе современной теории строения атома лежат следующие основные положения:
1. ЭЛЕКТРОН ИМЕЕТ ДВОЙСТВЕНУЮ (корпускулярно-волновую) ПРИРОДУ.
Электрон, как и другие элементарные частицы (протон, нейтрон), обладает определенной массой и зарядом, т.е. ведет себя как частица. В то же время, движущийся электрон проявляет волновые свойства, например характеризуется способностью к дифракции (рассеяние световых лучей) и интерференции (наложение световых волн). Для любой элементарной частицы справедливо уравнение (Луи де Бройль), связывающее параметры волны и частицы
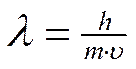 ,
,
где λ – длина волны электрона, h — постоянная Планка, m – масса электрона,
υ – скорость движения электрона.
2. ДЛЯ ЭЛЕКТРОНА НЕВОЗМОЖНО ОДНОВРЕМЕННО ТОЧНО ИЗМЕРИТЬ КООРДИНАТУ И СКОРОСТЬ.
В силу наличия у микрочастиц волновых свойств невозможно в каждый момент времени точно фиксировать их положение в пространстве и определять
с любой точностью скорость их движения. Чем точнее мы измеряем один параметр, тем больше неопределенность в другом. Принцип неопределенности сформулирован Гейзенбергом (1927 г.) и имеет математическое выражение
 ,
,
где Δх – неопределенность положения частицы по оси х, ΔРх = Δ(m·υ) – неопределенность составляющей импульса по оси х.
Из формулы видно, что чем меньше значение Δх , т.е. чем определеннее положение частицы, тем больше ΔРх, т.е. тем неопределеннее ее импульс. Неопределенность в свойствах микрообъектов проявляется тем в большей степени, чем в большей степени выражена его волновая функция (чем меньше его масса). Поэтому неопределенность в положении электрона значительно больше, чем неопределенность в положении ядра атома.
2. ЭЛЕКТРОН В АТОМЕ НЕ ДВИЖЕТСЯ ПО ОПРЕДЕЛЕННЫМ
ТРАЕКТОРИЯМ, А МОЖЕТ НАХОДИТСЯ В ЛЮБОЙ ЧАСТИ ОКОЛОЯДЕРНОГО ПРОСТРАНСТВА, однако вероятность его нахождения в разных частях этого пространства неодинакова.
Вероятность нахождения электрона в разных местах околоядерного пространства можно определить с помощью уравнения Шредингера
 ,
,
где h – постоянная Планка, m – масса электрона, U – потенциальная энергия,
Е – полная энергия, ψ – волновая (пси) функция. Первый член уравнения
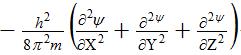
соответствует кинетической энергии частицы (Ек) с массой m. При короткой записи Ек описывается оператором Лапласа
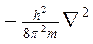
где  — оператор Лапласа.
— оператор Лапласа.
Упрощенный вид уравнения Шредингера
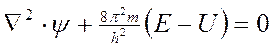 .
.
Решение этого уравнения связано с большими математическими трудностями. Точное решение оно имеет для атома водорода и для одноэлектронных частиц. Для сложных атомов уравнение Шредингера может быть решено только приблизительно. Решая его находят энергию электрона, а также функцию координат электрона X, Y, Z и времени τ:  . Волновая функция ψ представляет собой амплитуду трехмерной электронной волны. Причем она имеет как положительные, так и отрицательные значения. Квадрат модуля волновой функции
. Волновая функция ψ представляет собой амплитуду трехмерной электронной волны. Причем она имеет как положительные, так и отрицательные значения. Квадрат модуля волновой функции 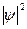 характеризует вероятность нахождения электрона в некотором объеме. Эту величину называют также электронной плотностью. Если в соответствии с Ур авнением Шредингера получим, что
характеризует вероятность нахождения электрона в некотором объеме. Эту величину называют также электронной плотностью. Если в соответствии с Ур авнением Шредингера получим, что  , где
, где 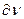 — определенный объем, то это значит, что в данном объеме электрон находится 0,1 времени, а 0,9 – в другом месте, т.е. можно утверждать, что электронная плотность в данном объеме равна 0,1. Совокупность мест пространства, где
— определенный объем, то это значит, что в данном объеме электрон находится 0,1 времени, а 0,9 – в другом месте, т.е. можно утверждать, что электронная плотность в данном объеме равна 0,1. Совокупность мест пространства, где 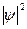 имеет максимальное значение называют электронной орбиталью.
имеет максимальное значение называют электронной орбиталью.
Таким образом, электронной орбиталью или электронным облаком называется часть околоядерного пространства, в котором вероятность пребывания электрона максимальна.
Поверхность, охватывающая ядро атома, за пределами которой вероятность пребывания электрона исчезающее мала, называют граничной поверхностью орбитали, которая и передает форму самой орбитали.
4. ЯДРА АТОМОВ СОСТОЯТ ИЗ ПРОТОНОВ И НЕЙТРОНОВ
(общее название — нуклоны).
Число протонов в ядре равно порядковому номеру элемента в таблице Д.И. Менделеева, а сумма протонов и нейтронов его атомному числу. Массовое число (А), заряд ядра (Z), равный числу протонов, и число нейтронов (N)
связаны соотношениями: Z = А – N, N = А – Z, А = Z + N.
Атомы с одинаковыми Z, но разными А и N, называют изотопами.
Квантовые числа
Решение уравнения Шредингера позволяет найти волновые функции, при этом выяснено, что для полного определения каждого решения необходимы три целых числа – квантовые числа. Можно сказать, что квантовые числа описывают совокупность движений электронов в атоме.
ГЛАВНОЕ КВАНТОВОЕ ЧИСЛО (n) определяет общую энергию электрона на данной орбитали и принимает значения n = 1, 2, 3, 4….
Чем больше n, тем больше объем внутреннего пространства атомной орбитали, т.е. растет удаленность электрона от ядра атома. Все электроны с одинаковым значением главного квантового числа образуют электронный слой. Приняты следующие обозначения электронных слоев:
Значение n ……………………………. 1 2 3 4 5 6 7
Обозначение слоя (уровня) ………….. K L M N O P Q.
Зная главное квантовое число можно определить максимальное число электронов, которое может находиться на этом уровне по формуле Nе = 2n2.
Возможное число подуровней для каждого электронного уровня численно равно значению n– первый уровень (n = 1) состоит из одного подуровня, второй уровень (n = 2) – из двух и т.д. (табл.3).
ОРБИТАЛЬНОЕ КВАНТОВОЕ ЧИСЛО ( 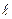 ), которое иногда называют побочным квантовым числом, определяет форму электронного облака и принимает значения от нуля до n-1. Область электронного уровня, в котором содержатся орбитали определенной формы называется энергетическим подуровнем. Подуровень, содержащий s-орбитали, называется s-подуровнем,
), которое иногда называют побочным квантовым числом, определяет форму электронного облака и принимает значения от нуля до n-1. Область электронного уровня, в котором содержатся орбитали определенной формы называется энергетическим подуровнем. Подуровень, содержащий s-орбитали, называется s-подуровнем,
р-орбитали — р-подуровнем и т.д. Например, при n = 1, 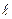 = 0 (на первом уровне существуют только s-электроны). При n = 3,
= 0 (на первом уровне существуют только s-электроны). При n = 3, 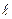 = 0, 1, 2 (на третьем уровне содержит 3s-, 3р- и 3d-электроны).
= 0, 1, 2 (на третьем уровне содержит 3s-, 3р- и 3d-электроны).
Таблица 3
Максимальное число подуровней и орбиталей на энергетических уровнях
| Энергетический уровень | Число подуровней | Типы орбиталей | Орбитали, 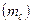 |
| К (n = 1) | 1s | ||
| L (n = 2) | 2s 2p | -1, 0, +1 | |
| M (n = 3) | 3s 3p 3d | -1, 0, +1 -2, -1, 0, +1, +2 | |
| N (n = 4) | 4s 4p 4d 4f | -1, 0, +1 -2, -1, 0, +1, +2 -3, -2, -1, 0, +1, +2, +3 |
Если 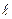 = 0, электронное облако имеет сферическую форму;
= 0, электронное облако имеет сферическую форму;
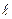 = 1 — электронное облако имеет форму симметричной восьмерки (гантель).
= 1 — электронное облако имеет форму симметричной восьмерки (гантель).
С ростом численного значения орбитального квантового числа форма электронного облака усложняется.
МАГНИТНОЕ КВАНТОВОЕ ЧИСЛО 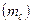 характеризует ориентацию данной орбитали в пространстве. Магнитное квантовое число принимает целочисленные значения от —
характеризует ориентацию данной орбитали в пространстве. Магнитное квантовое число принимает целочисленные значения от — 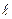 до +
до + 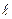 , включая ноль. Например, для
, включая ноль. Например, для 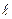 = 2, магнитные квантовые числа имеют значения -2, -1, 0, +1, +2, т.е. в данной подоболочке (d-подуровень) существует пять орбиталей. Соответственно на
= 2, магнитные квантовые числа имеют значения -2, -1, 0, +1, +2, т.е. в данной подоболочке (d-подуровень) существует пять орбиталей. Соответственно на
s-подуровне ( 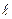 = 0) имеется одна орбиталь; на р-подуровне (
= 0) имеется одна орбиталь; на р-подуровне ( 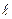 = 1) – три орбитали; на f-подуровне – семь орбиталей. Атомную орбиталь обозначают в виде клеточки □. Тогда число орбиталей на соответствующих подуровнях будет равно: s-подуровень — □; р-подуровнь — □□□; d-подуровень — □□□□□;
= 1) – три орбитали; на f-подуровне – семь орбиталей. Атомную орбиталь обозначают в виде клеточки □. Тогда число орбиталей на соответствующих подуровнях будет равно: s-подуровень — □; р-подуровнь — □□□; d-подуровень — □□□□□;
f-подуровнь — □□□□□□□.
Вышерассмотренные квантовые числа полностью характеризуют три определяющих свойства электрона-волны: длину, направление и амплитуду. Однако у электрона-частицы имеется особое свойство, называемое спином. Упрощенно спин можно рассматривать как вращение электрона вокруг собственной оси. Поэтому в теорию строения атома введено еще одно
СПИНОВОЕ КВАНТОВОЕ ЧИСЛО (ms), которое может принимать два значения в соответствии с двумя возможными направлениями вращения:
ms = + ½ (электрон вращается по часовой стрелке вокруг своей оси и имеет обозначение), ms = — ½ (электрон вращается против часовой стрелки вокруг своей оси и имеет обозначение).
Многоэлектронные атомы
В многоэлектронном атоме на электрон действует не только сила притяжения со стороны положительного заряженного ядра, но и отталкивание со стороны других электронов. Электроны внутренних электронных уровней атома ослабляют притяжение внешнего электрона ядром – экранируют внешний электрон от ядра. Это экранирование оказывается различным для электронов с разной формой электронного облака. Поэтому в многоэлектронных атомах энергия электрона зависит не только от главного квантового числа, но и от орбитального квантового числа, которое определяет форму электронной орбитали.
Распределение электронов в атоме по уровням и орбиталям происходит в соответствии с принципами Паули, Хунда, наименьших энергий.
Принцип Паули
Принцип (запрет) Паули гласит: в атоме не может быть двух электронов, имеющих одинаковыезначения всех четырех квантовых чисел. Отсюда следует, что на каждой орбитали может быть не более двух электронов, причем они должны иметь антипараллельные спины.
Правило Гунда
В соответствии с этим правилом заполнение орбиталей данного подуровня происходит таким образом, чтобы достигалось максимальное значение суммарного спинового числа (∑ms).
Рекомендуемые страницы:
Воспользуйтесь поиском по сайту:
Квантово-механическая модель строения атома
Квантовая механика (КМ)– это раздел физики, который изучает состояние и движение объектов микромира, к которому нельзя применить классическую механику Ньютона.
Электрон
Лекция 3. Периодический закон и электронные конфигурации атомов.
Д.И.Менделеев: Свойства элементов, а потому свойства образуемых ими простых и сложных тел, стоят в периодической зависимости т их атомного веса. Д.И.Менделеев предсказал существование трех элементов и дал характеристику их свойств исходя из периодической зависимости свойств известных к тому времени элементов на основе составленной им ПТ. Это элементы галлий (аналог известного к тому времени алюминия), германий (аналог кремния) и скандий (эка-бор).
Современная формулировка. Свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от зарядов ядер их атомов.
Физический смысл ПЗ заключается в периодической зависимости изменения свойств элементов, т.к. периодически повторяются электронные конфигурации валентных электронов в атоме при последовательном возрастании значений главного квантового числа.
Периодическая система элементов – система классификации химических элементов, созданная Д.И.Менделеевым. ПС позволяет выявить связи между химическими элементами, отражающие их сходство и различие. Она основана на периодической зависимости физических и химических свойств элементов от зарядов их ядер. Периодическая таблица – это графическое представление периодического закона. Структура ПТ с ее группами, подгруппами, периодами может рассматриваться как проявление определенной последовательности заполнения электронами энергетических уровней.
Период – совокупность химических элементов, горизонтально и последовательно расположенных в ПТ в порядке возрастания зарядов ядра их атомов.
Группы – совокупность элементов, образующих вертикальные столбцы и обладающих сходными свойствами, потому что они имеют одинаково заполненные внешние электронные слои.
Различают короткую и длинную форму ПТ. Короткая – это форма, при которой большие периоды записываются в две строки. При записи образуются главные (А) и побочные (В) подгруппы (элементы главной подгруппы смещены обычно влево, а побочной – вправо). Первый, второй и третий называют малыми (короткими) периодами, а четвертый- седьмой – большими (длинными) периодами. Декада (вставная декада) – совокупность десяти элементов одного периода, характеризующихся последовательным заполнением в их атомах d- подуровня.
Номер периода численно равен максимальному значению главного квантового числа внешних электронов элементов рассматриваемого периода.
Номер группы численно равен максимальной положительной степени окисления элемента или стехиометрической валентности. Аналоги ( электронные аналоги)– элементы, близкие по свойствам, входящие в состав одной подгруппы ПС.
Большинство химических элементов – это металлы (их более 90). Характерным свойством металлов является способность их атомов отдавать внешние электроны и превращаться в положительно заряженные ионы: Ме = Меn+ + nе.
Характерным свойством неметаллов является способность их атомов присоединять электроны и образовывать отрицательно заряженные ионы. В том и другом случаях атомы стремятся образовать устойчивую электронную конфигурацию, характерную для инертных (благородных) газов, расположенных в VIII группе.
Рассмотрим электронные конфигурации всех элементов ПС в основном состоянии (состояние с наименьшей энергией электронов данного атома). Электроны, находящиеся на орбиталях внешнего электронного уровня, называются валентными и играют основную роль в образовании химической связи. Элементы, у которых заполняется s,p,d,f подуровни называют соответственно s,p,d,f –элементами.
Внутренняя горизонтальная периодичность элементов обусловлена двухэтапным заполнением электронами p,d,f орбиталей. Первый этап заполнения заключается заполнением электронами с одинаковым спином, а второй – с противоположным.
Электронная конфигурация
s–элементы ns1-2 IA,IIA (щелочные и щелочно-земельные металлы)
p –элементы ns2np1-6 IIIA-VIIIA (металлы-неметаллы-благородные газы)
d – элементы ns2 (n-1)d1-10 IB- VIIIB (металлы)
f — элементы ns2 (n-1)d1 (n-2)f1-14 IIIB (лантаноиды и актиноиды).
Изменение свойств в периодах и группах:
Усиление немет. свойств (увеличение П.И., ЭО, умен. радиуса атомов)
__________________________________ (в периодах)
Усиление мет. свойств
(умен.П.И.,ЭО, увел. радиуса атома)
(в группах)
Названия вновь открытых элементов: 110- дармштадтиум Ds/ 111 – ренгениум Rg/ 112 – копернициум Сn/
3. Квантово-механическая модель атома, квантовые числа, типы атомных орбиталей.
Квантово-механическая модель атома
Движение е— в атоме нельзя представить определенной траекторией (линейной или плоской). Движение е— в атоме принято изображать с помощью атомной орбитали (АО).
Атомная орбиталь (АО) — трехмерная область пространства, нахождение электрона в которой наиболее вероятно (90%-98%). Для каждого атома существует целый набор атомных орбиталей, отличающихся друг от друга значениями энергии. Каждая атомная орбиталь (ее энергия, форма, размер, ориентация в пространстве) описывается 4 квантовыми числами (n,l,m,s). Первые три соответствуют трем степеням свободы электрона в трехмерном пространстве, а четвертое соответсвует вероятности вращения электрона вокруг воображаемой собственной оси.
Квантовые числа:
“n” – главное квантовое число. Характеризует уровень энергии электрона в поле атома, удаленность от ядра.Совпадает с номером периода. Принимает значения n=1,…,7. Есвязи=-21,76∙*1/n2
Каждый энергетический уровень имеет сложное строение, и в поле ядра разделяется на подуровни. Число подуровней совпадает с уровнем т.е. на 1 уровне один подуровень, …, на третьем –три..
“l” – орбитальное квантовое число. Характризует тип энергетического подуровня (форма электронного облака). l=0,1,2,…,(n-1). Обозначается буквами s, p, d, f, q, h. При этом нулю соответствует 0-s, 1-p, 2-d, 3-f, 4-q, 5-h.
Число АО на подуровне определяется числом возможных ориентаций этой орбитали, т.е магнитным квантовым числом m.
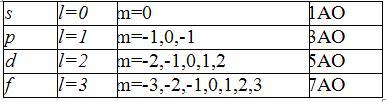 “m” – магнитное квантовое число. Определяет
пространственное расположение АО. m=0,
1,
2,…,
l.
Cумма
орбиталей на подуровне: =2l+1.
“m” – магнитное квантовое число. Определяет
пространственное расположение АО. m=0,
1,
2,…,
l.
Cумма
орбиталей на подуровне: =2l+1.
“s” – спиновое квантовое число. Характеризует вероятность вращения электрона вокруг своей оси в двух противоположенных направлениях. s=1/2. “+” – по часовой стрелке, “-“ – против часовой стрелке, собственная характеристика электрона, которая не может быть уничтожена. Вращение сообщает электрону собственный магнитный момент, который называется спином электрона.
Вывод: Квантовые числа дают полную характеристику состояния электрона в атоме: энергия, форма, ориентация электронов в пространстве и спиновые характеристик.
4. Основные принципы заполнения Атомных Орбиталей электронами. Принцип Паули, правило Хунда.
Принцип
Паули:
у атомов, имеющих больше одного электрона,
не может быть 2х электронов с одинаковыми значениями
всех 4х квантовых чисел. Следствие:
на каждой АО максимально может находится
только два электрона с антипараллельными
спинами  .
.
Подуровни p, d и f состоят из нескольких орбиталей, энергия которых одинакова, поэтому эти подуровни называются «вырожденными»: p подуровень вырожден трехкратно, d пятикратно и f семикратно. Для электронов этих подуровней соблюдается правило Хунда.
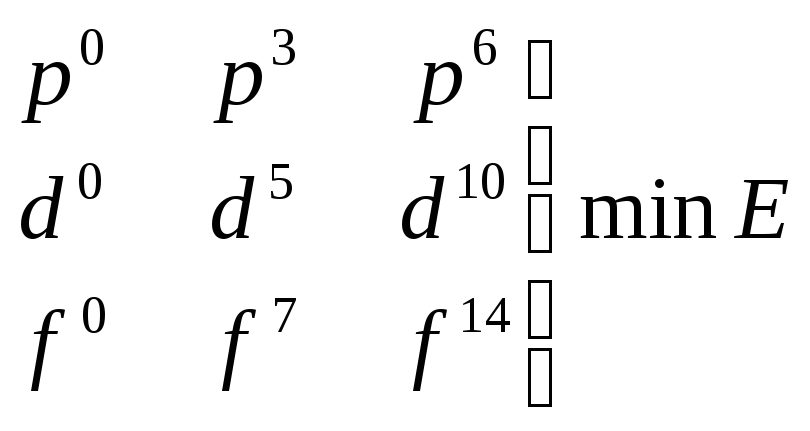 Правило
Хунда: в основном (невозбужденном) состоянии
атома на подуровнях np,
nd
и nf
всегда имеется максимальное количество
неспаренных электронов (максимальный
неспаренный спин).
Правило
Хунда: в основном (невозбужденном) состоянии
атома на подуровнях np,
nd
и nf
всегда имеется максимальное количество
неспаренных электронов (максимальный
неспаренный спин).
Правило Хунда. Минимумом энергии обладает конфигурация с максимальным сумм. спином.
Особенности формирования d- и f-подуровней
Принцип минимума энергии: состояние электрона должно отвечать основному принципу – принципу минимума энергии. Энергия задается: Е= n+l. Минимум энергии соответствует максимуму устойчивости. На внешнем уровне не может быть более 8 электронов.
Правило Кличковского: Энергетические подуровни заполняются в порядке увеличения суммы квантовых чисел (n+l). При равных значениях суммы сначала заполняется подуровень с меньшим n.
Особенности заполнения и формирования многоэлектронных подуровней
S  — max 2e
— max 2e
P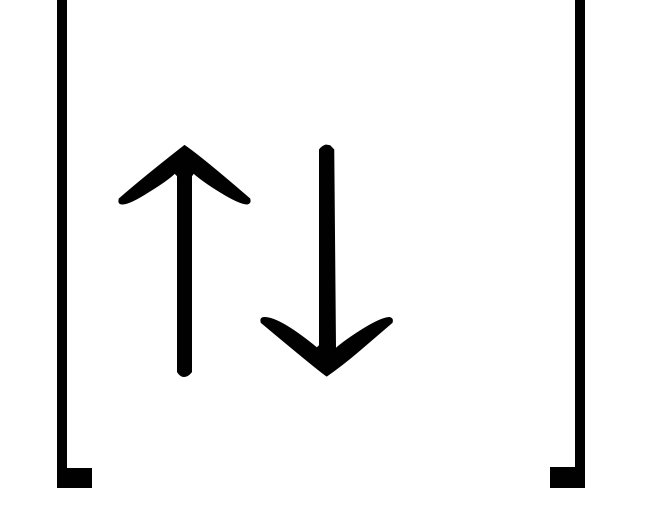

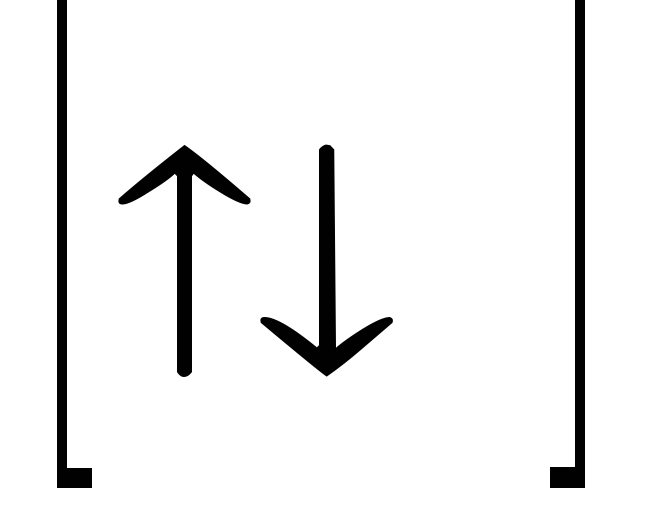 —
max 6e
—
max 6e
D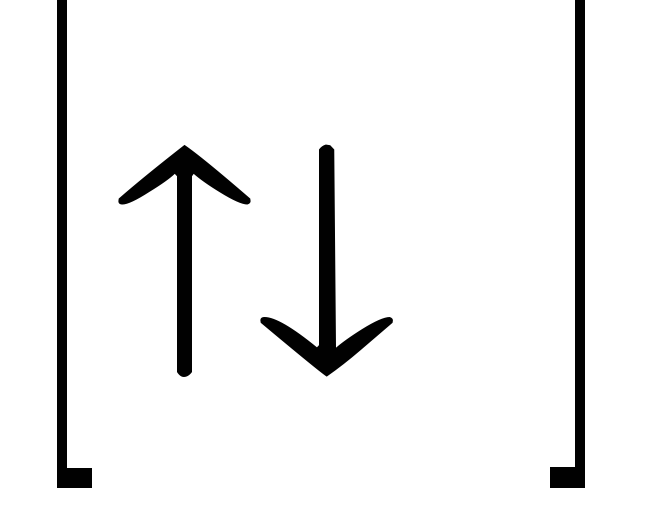

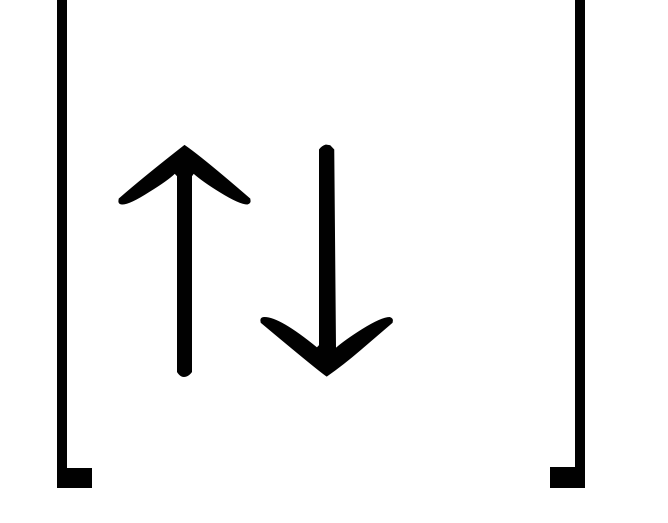

 —
max 10e
—
max 10e
F



 -max
14 e
-max
14 e
Квантово-механическая модель атома и его строение :: SYL.ru
Планетарная квантово-механическая модель атома Бора часто запоминается за счет аккуратной и знакомой картины электронов. Они вращаются вокруг центрального ядра, подобно планетам вокруг Солнца. Из-за этого может быть сложно заменить картину той, которая более точно представляет квантово-механическую модель атома, используемую современными физиками.
Как располагается и движется атом?
Атом обладает крошечным ядром и волнами острых орбит. Расположение и движение электронов описывается волнами их материи. Эти структуры предсказывают вероятность нахождения электрона в данной области атома. Но откуда появилась квантово механическая модель атома Бора?
Планетарная модель положила начало процессу введения квантовой теории в структуру атома. Бор ввел идею стационарных состояний, в которых атом был устойчив. Переходы между этими состояниями объясняли существование спектральных линий. В случае водорода он смог получить энергетические уровни:
- Переходы между его энергетическими уровнями соответствовали линиям в водородном спектре.
- Его модель не могла предсказать уровни энергии для любых других атомов (хотя уровни водородоподобных щелочных металлов можно было бы приблизить к истине).
Отдельно проводились работы Гейзенберга и Шредингера, чтобы придумать способы более полного описания квантованных энергетических уровней атомов.
Аналогии Гейзенберга и Шредингера: как они привели уравнение к доказательству волны
Квантово-механическая модель строения атома обладает уникальным набором свойств. Гейзенберг использовал матрицы, а Шредингер разработал волновое уравнение, чтобы доказать абсолютность разницы в поведении кванта. Детальнее двоякость частицы показана на видео.

Уравнения Шредингера обеспечивают представление плотности картины вероятности электронов вокруг ядра атома. Большинство определений квантовой теории и квантовой механики предлагают одинаковое описание для обоих. Они по существу описывают квантовую теорию, в которой и энергия, и материя имеют характеристики волн в одних условиях и характеристики частиц — в других.
Чтобы идея была понятней, люди стали проводить эксперименты в условиях мысленного посыла.

- Квантовая теория предполагает, что энергия приходит в дискретных пакетах, называемых квантами (или — в случае электромагнитного излучения — фотонами).
- Квантовая теория имеет некоторое математическое развитие, часто называемое квантовой механикой, которая предлагает объяснения поведения электронов внутри электронных облаков атомов.
Основные положения квантово механической модели строения атома — это двойственность волн электронов в электронном облаке, которая ограничивает нашу способность одновременно измерять энергию и положение электрона.
Скрытые особенности электронов
Чем точнее мы измеряем энергию или положение электрона, тем меньше мы знаем о другом. Мы не можем точно отметить одновременно положение и импульс электрона. Это приводит к невозможности предсказать траекторию для частицы. Следовательно, поведение электрона описывается иначе, чем поведение частиц нормального размера. Необходимо знать:
- Наиболее распространенным способом описания электронов в атомах в соответствии с квантовой механикой является решение уравнения Шредингера для энергетических состояний электронов этом облаке.
- Когда электрон находится в этих состояниях, его энергия четко определена, а положение — нет.
- Положение описывается картой распределения вероятностей, называемой орбитальной.
Траектория, которую мы обычно связываем с макроскопическими объектами, заменяется электронами в облаках электронов, причем в статистических описаниях указывается не путь, а область, в которой он найден. Поскольку именно электрон в облаке электронов атома определяет его химическое поведение, для понимания химии необходимо описание конфигурации электронов в ключе квантово-механической модели атома.
Принцип неопределенности Гейзенберга: область внутри атома
Луи де Бройль предложил, чтобы все частицы можно было рассматривать, как материальные волны с длиной волны — лямбда, определяемая следующим уравнением:
Лямбда = фактическое время (час) + милливольтчас
Эрвин Шредингер предложил квантово-механическую модель атома. Кратко: она рассматривает электроны, как волны вещества.
Квадрат волновой функции представляет вероятность нахождения электрона в данной области внутри атома. Атомная орбита определяется, как область внутри атома, которая находится там, где электрон.
Принцип неопределенности Гейзенберга гласит, что мы не можем знать ни энергию, ни положение электрона. Поэтому, когда мы больше узнаем о положении электрона, мы меньше знаем о его энергии, и наоборот. Электроны имеют внутреннее свойство, называемое спином. Любые два электрона, занимающие одну и ту же орбиту, должны иметь противоположные спины.
Светоносный эфир в квантовом мире
Природа света была предметом исследования с древности. В семнадцатом веке Исаак Ньютон провел эксперименты с линзами и призмами. Он смог продемонстрировать, что белый свет состоит из отдельных цветов радуги, объединенных вместе. Ньютон объяснил результаты своей оптики «корпускулярным» взглядом на свет, в котором свет состоял из потоков чрезвычайно мелких частиц, движущихся на высоких скоростях в соответствии с законами движения Ньютона. Стоит заметить:
Кристиан Гюйгенс показал, что оптические явления такие, как отражение и преломление, могут быть одинаково хорошо объяснены с точки зрения света как волны, движущиеся с высокой скоростью через среду, называемую «светоносный эфир». Она пронизывает все пространство.
В начале девятнадцатого века Томас Янг продемонстрировал, что свет, проходящий через узкие, близко расположенные щели, создает интерференционные картины, которые не могут быть объяснены с точки зрения ньютоновских частиц, но могут быть легко растолкованы с точки зрения волн.
- Позже, в девятнадцатом веке после того, как Джеймс Клерк Максвелл разработал свою теорию электромагнитного излучения и показал, что свет является видимой частью огромного спектра электромагнитных волн, взгляд частиц на свет стал полностью дискредитирован.
Сегодня эти области называют классической механикой и классической электродинамикой (или классическим электромагнетизмом).
Как прогрессировала идея о внедрении новых понятий в физике

К концу девятнадцатого века ученые рассматривали физическую вселенную как приблизительно состоящую из двух отдельных областей:
- материи, сформированной из частиц, движущихся согласно законам движения Ньютона;
- электромагнитного излучения, состоящего из волн, управляемых уравнениями Максвелла.
Парадоксы привели к современной структуре квантово-механической модели атома Шредингера, которая тесно связывает частицы и волны на фундаментальном уровне, называемом дуальностью волны-частицы, которая заменила классический взгляд.
Дискретная волна Бора: как ведут себя спектры излучения водорода
Согласно модели Бора, спектры излучения различных элементов содержат дискретные линии. Представить видимую область спектров излучения водорода можно при помощи таблицы.
| Основное квантовое число | Количество подуровней | Количество электронов |
| 1 | 1 | 2 |
| 2 | 2 | 8 |
| 3 | 3 | 18 |
| 4 | 4 | 32 |
Это схематическое представление квантов, где известно число электронов и уровней. В жизни в условиях вакуума точно нельзя сказать ограничение по подуровням, но их не может быть больше 7. Квантованные спектры излучения указывали Бору, что электроны могут существовать внутри атома только при определенных атомных радиусах и энергиях.

Построив модель, Бор вывел уравнение, которое правильно предсказывало различные уровни энергии в атоме водорода. Квантовая механическая модель подходила только для представления этого конкретного случая. Уровни соответствовали линиям излучения в спектре вещества.
Модель Бора, которая доказала одноэлектронные системы водорода
Скорость электрона на уровне энергии основного состояния водорода составляет 2,2×106 s÷m, где s — длина, m — масса. Мы можем подставить постоянную, а также массу и скорость электрона в уравнение де Бройля. Но при этом он не смог объяснить электронную структуру в атомах, которые содержали более одного электрона.
Если обратиться к химии, квантово-механическая модель атома водорода должна состоять только из протонов. При встрече с электронами или нейтронами частица начинает себя вести, как волна. В остальных случаях атомы другого вещества могут независимо от структуры вести себя подобно волнам или частицам. Если сказать кратко, квантово-механическая модель атома водорода представляет собой материальный дуализм волны, но не частицы.
Наложение волн одну на другую: как не смешиваются пути пересечения атомов
Радиоволны от мобильного телефона, рентгеновские снимки, используемые стоматологами, энергия, используемая для приготовления пищи в вашей микроволновой печи, лучистое тепло от раскаленных предметов и свет от экрана телевизора — все это формы электромагнитного излучения, которые проявляют волнообразное поведение. Необходимо запомнить:
- Волна — это колебание или периодическое движение, которое может переносить энергию из одной точки пространства в другую.
- Встряхивание конца веревки передает энергию от вашей руки к другому концу веревки; падение гальки в пруд приводит к волнам, распространяющимся вдоль поверхности воды; расширение воздуха, сопровождающее удар молнии, генерирует звуковые волны (гром), которые могут путешествовать наружу на несколько миль.
- В каждом из этих случаев кинетическая энергия передается через вещество (веревку, воду или воздух), в то время как вещество остается на месте.
Волны не должны быть ограничены, чтобы путешествовать сквозь материю. Как показал Максвелл, электромагнитные волны состоят из электрического поля, колеблющегося в такт с перпендикулярным магнитным полем. Они перпендикулярны направлению движения. Эти волны могут проходить через вакуум с постоянной скоростью 2,998 × 108 м/с, где с — скорость света.
1.2. Квантово-механическая модель атома водорода
Двойственная природа электрона. В 1905 г. А. Эйнштейн предсказал, что любое излучение представляет собой поток квантов энергии, называемых фотонами. Из теории Эйнштейна следует, что свет имеет двойственную (корпускулярно-волновую) природу.
В 1924 г. Луи де Бройль (Франция) выдвинул предположение, что электрон также характеризуется корпускулярно-влновым дуализмом. Позднее это было подтверждено на опытах по дифракции на кристаллах. Де Бройль предложил уравнение, связывающее длину волны λ электрона или любой другой частицы с массой m и скоростью ν,
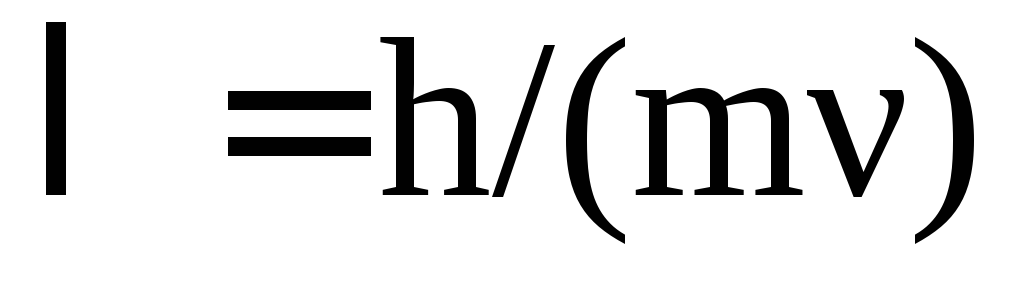 .
(1.5)
.
(1.5)
Волны частиц материи де Бройль назвал материальными волнами. Они свойственны всем частицам или телам. Однако, как следует уравнения (1.5), для макротел длина волны настолько мала, что в настоящее время не может быть обнаружена. Так, для тела с массой 1000 кг, двигающегося со скоростью 108 км/ч (30 м/с) λ = 2,21·10-38 м.
В 1927 г. В. Гейзенберг (Германия) постулировал принцип неопределенности, согласно которому положение и импульс движения субатомной частицы (микрочастицы) принципиально невозможно определить в любой момент времени с абсолютной точностью. В каждый момент времени можно определить только лишь одно из этих свойств. Э. Шредингер (Австрия) в 1926 г. вывел математическое описание поведения электрона в атоме.
Работы Планка, Эйнштейна, Бора, де Бройля, Гейзенберга, а также Шредингера, предложившего волновое уравнение, заложили основу квантовой механики, изучающей движение и взаимодействие микрочастиц.
Орбиталь. В соответствие с квантово-механическими представлениями невозможно точно определить энергию и положение электрона, поэтому в квантово-механической модели атома используют вероятностный подход для характеристики положения электрона. Вероятность нахождения электрона в определенной области пространства описывается волновой функцией ψ, которая характеризует амплитуду волны, как функцию координат электрона. В наиболее простом случае эта функция зависит от трех пространственных координат и называется орбиталью. В соответствии с определением ψ, орбиталью называется область пространства, в котором наиболее вероятно нахождение электрона. Необходимо заметить, что понятие орбиталь существенно отличается от понятия орбита, которая в теории Бора означала путь электрона вокруг ядра атома. Величина области пространства, которую занимает орбиталь, обычно такова, чтобы вероятность нахождения электрона внутри нее составляла не менее 95 %.
Так как электрон несет отрицательный заряд, то его орбиталь представляет собой определенное распределение заряда, которое получило название электронного облака.
Квантовые числа. Для характеристики поведения электрона в атоме введены квантовые числа: главное, орбитальное, магнитное и спиновое.
Главное квантовое число n определяет энергию и размеры электронных орбиталей. Главное квантовое число принимает значения 1,2,3,4,5,… и характеризует оболочку или энергетический уровень. Чем больше n, тем выше энергия. Оболочки (уровни) имеют буквенные обозначения: К (n = 1), L (n = 2), M (n = 3), N (n = 4), Q (n = 5), переходы электронов с одной оболочки (уровня) на другую сопровождаются выделение квантов энергии, которые могут проявиться в виде спектров (см. рис. 1.1).
Орбитальное квантовое число l определяет форму атомной орбитали. Электронные оболочки расщеплены на подоболочки, поэтому орбитальное квантовое число также характеризует энергетические подуровни в электронной оболочке атома.
Орбитальные квантовые числа принимают целочисловое значение от 0 до (n-1). Подоболочки также обозначаются буквами:
Подоболочка (подуровень)…………………s p d f
Орбитальное квантовое число, l……………0 1 2 3
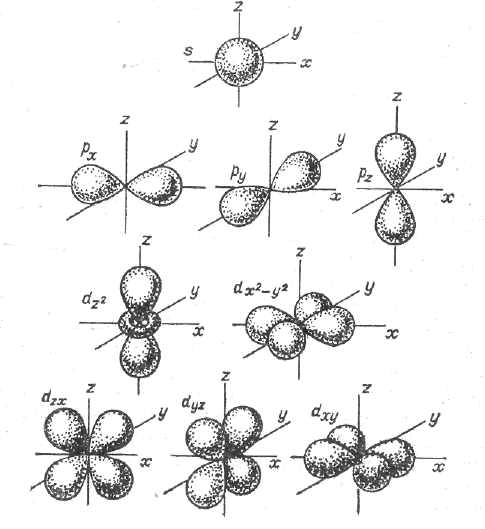
Электроны с орбитальным квантовым числом 0, называются s — электронами. Орбитали и соответственно электронные облака имеют сферическую форму (рис. 1.2).
Электроны с орбитальным квантовым числом 1 называются p — электронами. Орбитали и соответственно электронные облака имеют форму, напоминающую гантель (рис. 1.2).
Электроны с орбитальным квантовым числом 2 называют d – электронами. Орбитали имеют форму четырехлепестковой розетки (рис. 1.2).
Электроны с орбитальным квантовым числом 3 получили название f – электронов. Форма их орбиталей еще сложнее, чем форма d – орбиталей.
В первой оболочке (n=1) может быть одна (s–), во второй (n=2) две (s- и p-), в третьей (n=3) – три (s-, p-, d-), в четвертой (n=4) – четыре (s-, p-, d-, f-)-подоболочки.
Магнитное квантовое число ml характеризует положение орбитали в пространстве (см. рис. 1.2).
Рис. 1.2. Фрмы электронных облаков различных атомных орбиталей | В отсутствие внешнего магнитного поля все орбитали одного подуровня (подоболочки) имеют одинаковое значение энергии. Под воздействием внешнего магнитного поля происходит расщепление энергии подоболочек. Магнитное квантовое число принимает целочисленные значения от –l до +l, включая ноль. Например, для l = 3, магнитные квантовые числа имеют значения -3, -2, -1, 0, +1, +2, +3. Таким образом, в данной подоболочке (f-подоболочке) существует семь орбиталей. |
Соответственно в подоболочке s (l = 0) имеется одна орбиталь (ml = 0), в подоболочке р (l = 1) – три орбитали (ml = -1, 0, +1), в подоболочке d (l = 2) пять орбиталей (ml = -2, -1, 0, +1, +2).
Атомная орбиталь. Каждая электронная орбиталь в атоме (атомная орбиталь, АО) может характеризоваться тремя квантовыми числами n, l и ml.
Условно атомную
орбиталь обозначают в виде клеточки  .
.
Соответственно
для s-подоболочки имеется одна АО  ,
для р-подоболочки – три АО
,
для р-подоболочки – три АО 

 ,
для d-подоболочки – пять АО
,
для d-подоболочки – пять АО 



 ,
для f-подоболочки – семь АО
,
для f-подоболочки – семь АО 





 .
.
Спиновое квантовое
число 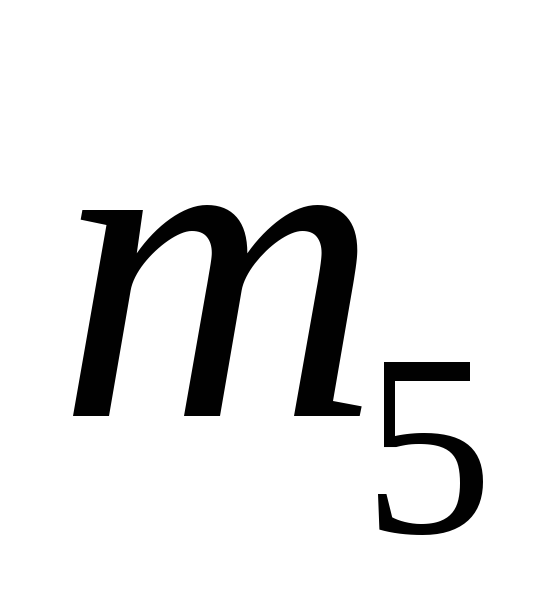 .
Каждый электрон характеризуется
собственным механическим моментом
движения, который получил названиеспина. Соответствующие спину квантовое число
имеет только 2 значения: +1/2 и -1/2.
Положительные и отрицательные значения
спина связаны с его направлением.
Электроны с разными спинами обычно
обозначаются противопложно напрвленными
стрелками
.
Каждый электрон характеризуется
собственным механическим моментом
движения, который получил названиеспина. Соответствующие спину квантовое число
имеет только 2 значения: +1/2 и -1/2.
Положительные и отрицательные значения
спина связаны с его направлением.
Электроны с разными спинами обычно
обозначаются противопложно напрвленными
стрелками  .
.
2.4. Квантово-механическая модель строения атома
В основе современной теории строения атома лежат следующие основные положения:
1. ЭЛЕКТРОН ИМЕЕТ ДВОЙСТВЕННУЮ (корпускулярно-волновую) ПРИРОДУ.
Электрон, как и другие элементарные частицы (протон, нейтрон), обладает определенной массой и зарядом, т.е. ведет себя как частица. В то же время, движущийся электрон проявляет волновые свойства, например характеризуется способностью к дифракции (рассеяние световых лучей) и интерференции (наложение световых волн). Для любой элементарной частицы справедливо уравнение (Луи де Бройль), связывающее параметры волны и частицы
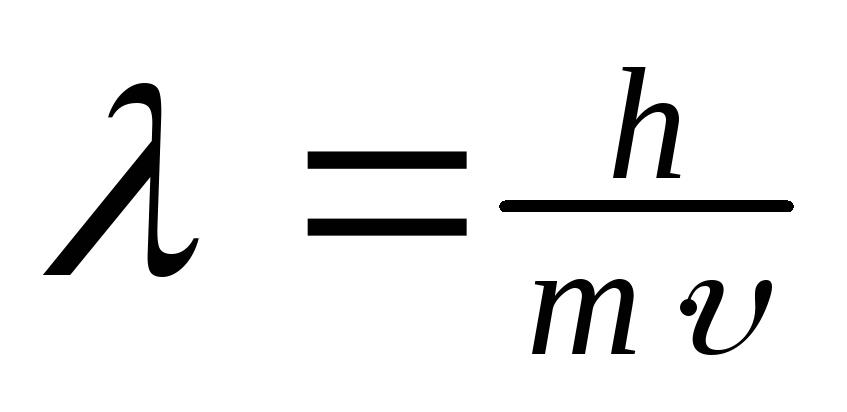 ,
,
где λ – длина волны электрона, h – постоянная Планка, m – масса электрона,
υ – скорость движения электрона.
2. ДЛЯ ЭЛЕКТРОНА НЕВОЗМОЖНО ОДНОВРЕМЕННО ТОЧНО ИЗМЕРИТЬ КООРДИНАТУ И СКОРОСТЬ
В силу наличия у микрочастиц волновых свойств невозможно в каждый момент времени точно фиксировать их положение в пространстве и определять
с любой точностью скорость их движения. Чем точнее мы измеряем один параметр, тем больше неопределенность в другом. Принцип неопределенности сформулирован Гейзенбергом (1927 г.) и имеет математическое выражение
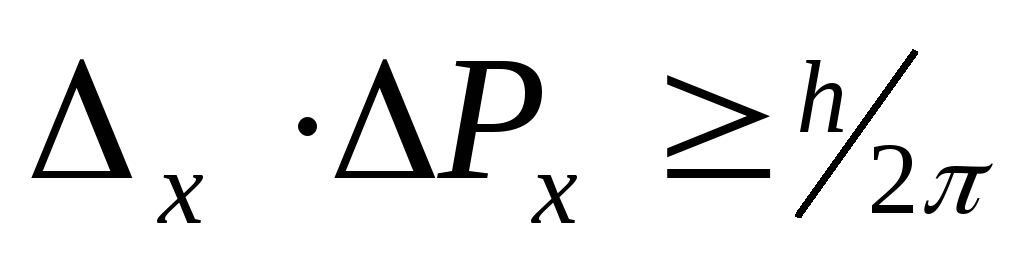 ,
,
где Δх – неопределенность положения частицы по оси х, ΔРх = Δ(m·υ) – неопределенность составляющей импульса по оси х.
Из формулы видно, что чем меньше значение Δх , т.е. чем определеннее положение частицы, тем больше ΔРх, т.е. тем неопределеннее ее импульс. Неопределенность в свойствах микрообъектов проявляется тем в большей степени, чем в большей степени выражена его волновая функция (чем меньше его масса). Поэтому неопределенность в положении электрона значительно больше, чем неопределенность в положении ядра атома.
ЭЛЕКТРОН В АТОМЕ НЕ ДВИЖЕТСЯ ПО ОПРЕДЕЛЕННЫМ
ТРАЕКТОРИЯМ, А МОЖЕТ НАХОДИТЬСЯ В ЛЮБОЙ ЧАСТИ ОКОЛОЯДЕРНОГО ПРОСТРАНСТВА, однако вероятность его нахождения в разных частях этого пространства неодинакова.
Вероятность нахождения электрона в разных местах околоядерного пространства можно определить с помощью уравнения Шредингера
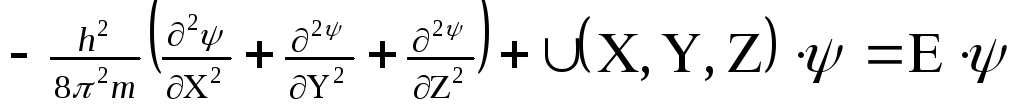 ,
,
где h – постоянная Планка, m – масса электрона, U – потенциальная энергия,
Е – полная энергия, ψ – волновая (пси) функция. Первый член уравнения
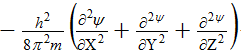
соответствует кинетической энергии частицы (Ек) с массой m. При короткой записи Ек описывается оператором Лапласа
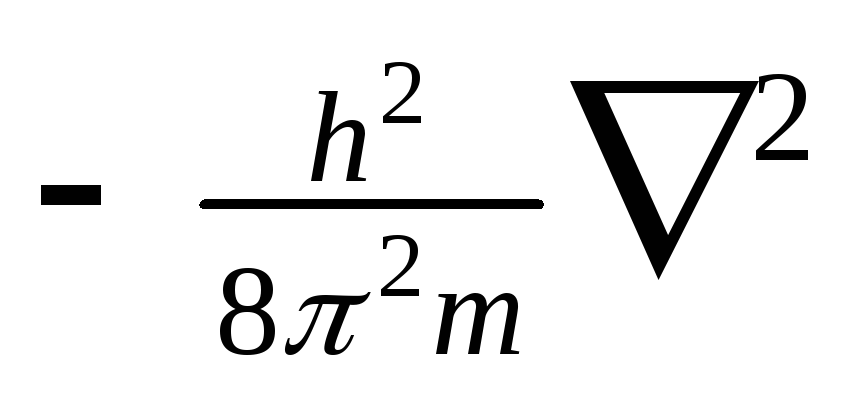 ,
,
где 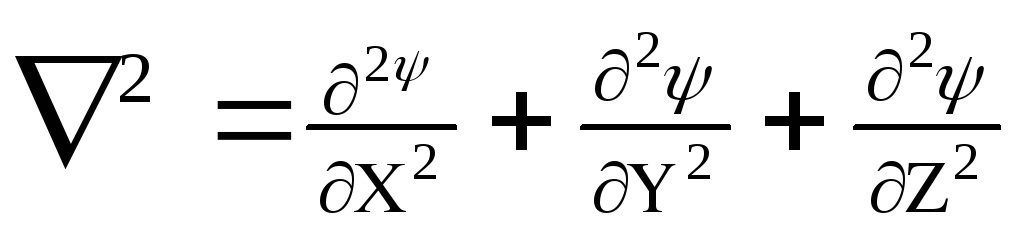 — оператор Лапласа.
— оператор Лапласа.
Упрощенный вид уравнения Шредингера
 .
.
Решение этого
уравнения связано с большими математическими
трудностями. Точное решение оно имеет
для атома водорода и для одноэлектронных
частиц. Для сложных атомов уравнение
Шредингера может быть решено только
приблизительно. Решая его, находят
энергию электрона, а также функцию
координат электрона X, Y, Z и времени τ: 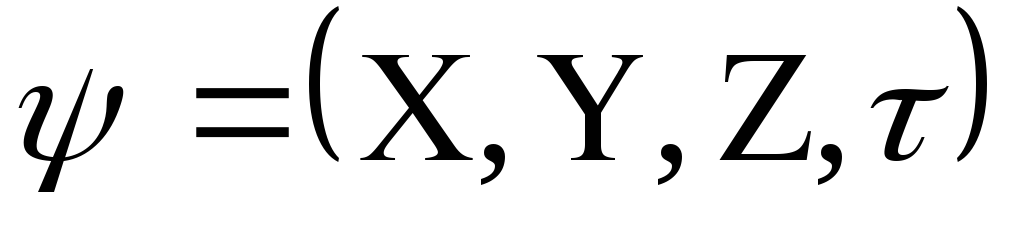 .
Волновая функция ψ представляет собой
амплитуду трехмерной электронной волны.
Причем она имеет как положительные, так
и отрицательные значения. Квадрат модуля
волновой функции
.
Волновая функция ψ представляет собой
амплитуду трехмерной электронной волны.
Причем она имеет как положительные, так
и отрицательные значения. Квадрат модуля
волновой функции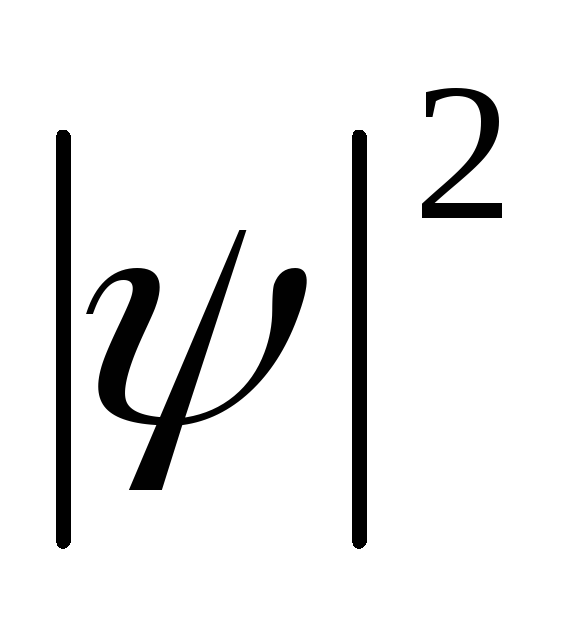 характеризует вероятность нахождения
электрона в некотором объеме. Эту
величину называют также электронной
плотностью. Если в соответствии с
уравнением Шредингера получим, что
характеризует вероятность нахождения
электрона в некотором объеме. Эту
величину называют также электронной
плотностью. Если в соответствии с
уравнением Шредингера получим, что ,
где
,
где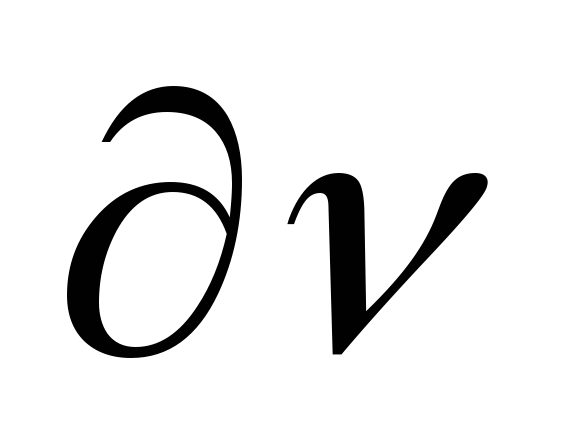 – определенный объем, то это значит,
что в данном объеме электрон находится
0,1 времени, а 0,9 – в другом месте, т.е.
можно утверждать, что электронная
плотность в данном объеме равна 0,1.
Совокупность мест пространства, где
– определенный объем, то это значит,
что в данном объеме электрон находится
0,1 времени, а 0,9 – в другом месте, т.е.
можно утверждать, что электронная
плотность в данном объеме равна 0,1.
Совокупность мест пространства, где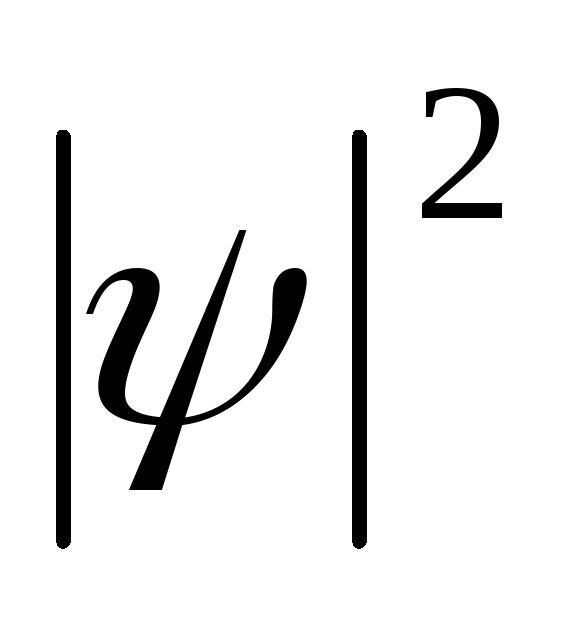 имеет максимальное значение называют
электронной орбиталью.
имеет максимальное значение называют
электронной орбиталью.
Таким образом, электронной орбиталью или электронным облаком называется часть околоядерного пространства, в котором вероятность пребывания электрона максимальна.
Поверхность, охватывающая ядро атома, за пределами которой вероятность пребывания электрона исчезающе мала, называют граничной поверхностью орбитали, которая и передает форму самой орбитали.
4. ЯДРА АТОМОВ СОСТОЯТ ИЗ ПРОТОНОВ И НЕЙТРОНОВ
(общее название – нуклоны).
Число протонов в ядре равно порядковому номеру элемента в таблице Д.И. Менделеева, а сумма протонов и нейтронов его атомному числу. Массовое число (А), заряд ядра (Z), равный числу протонов, и число нейтронов (N)
связаны соотношениями: Z = А – N, N = А – Z, А = Z + N.
Атомы с одинаковыми Z, но разными А и N, называют изотопами.