«Способы изменения внутреннеи энергии тела. Теплопроводность.»
Физика 8 класс Волик Н.Н.
Дата проведения |
Тема: Способы изменения внутренней энергии тела. Теплопроводность.
Цели (ожидаемый результат):
Образовательная:
сформировать понятия теплопередачи и изменения внутренней энергии путём совершения механической работы;
отработка и закрепление умений учащихся применять свои знания для объяснения конкретных явлений.
Развивающая:
развивать интерес к физике, мотивировать необходимость изучения тепловых явлений, раскрывать на интересных и важных примерах их широкое проявление в природе, показывать применение знаний о тепловых явлениях в быту и технике;
развитие умений применять полученные знания при решении расчетных и качественных задач;
развитие логического мышления.

Воспитательная:
Тип урока: урок изучения нового материала.
Методы урока: словесный, наглядный.
Оборудование: термометр, цилиндр металлический (заранее нагретый)
УМК: презентация «Изменение внутренней энергии тела».
Ход урока
Орг. момент.
Приветствует учащихся, создает доброжелательный настрой
Отмечает отсутствующих
Актуализация опорных знаний
Мы продолжаем изучать вопросы тепловых явлений. Сегодня рассматриваем способы изменения внутренней энергии. А прежде чем мы начнем говорить о способах изменения внутренней энергии, давайте вспомним материал предыдущего урока:
Физический диктант (заполнить пропуски): (слайд)
1. Нас окружают физические…
2. Они состоят из…
3. … движутся непрерывно.
4. Кинетическая энергия движущихся молекул и потенциальная энергия их взаимодействия образуют… энергию.
5. Об изменении внутренней энергии тела мы судим по…
Проверим ваши ответы (учащиеся обменивают своими ответами в парах и осуществляют взаимопроверку).
Пять правильных ответов это «5», четыре правильных ответа- «4» и так далее.
1. Нас окружают физические тела
2. Они состоят из молекул.
3. Молекулы движутся непрерывно.
4. Кинетическая энергия движущихся молекул и потенциальная энергия их взаимодействия образуют внутреннюю энергию.
5. Об изменении внутренней энергии тела мы судим по изменению температуры тела и деформации.
Все тела состоят из молекул, которые непрерывно движутся и взаимодействуют друг с другом. Они обладают одновременно кинетической и потенциальной энергией.
(слайд)
Таким образом, внутренняя энергия — это энергия движения и взаимодействия частиц, из которых состоит тело.
Сообщение темы и целей урока
Поговорим подробнее о способах изменения внутренней энергии тела. Запишите тему урока. Способы изменения внутренней энергии тела. Теплопроводность.
Запишите тему урока. Способы изменения внутренней энергии тела. Теплопроводность.
Изучение нового материала
Объяснение нового материала с помощью презентации.
Внутренняя энергия не является величиной постоянной.
Если температура тела увеличивается, увеличивается и внутренняя энергия тела. Это означает, что молекулы этого тела начинают быстрее двигаться, чаще взаимодействовать друг с другом, и, соответственно расстояние между частицами увеличивается. Следовательно, энергия этого тела тоже увеличивается.
Если же температура понижается, тело остывает, то это означает, что молекулы начинают двигаться медленнее, их кинетическая энергия и расстояние между ними уменьшается, и, следовательно, энергия тела тоже убывает.
Можно сказать, что температура является главной характеристикой внутренней энергии тела.
Итак, от каких величин зависит внутренняя энергия тела?
Когда мы говорим об изменении внутренней энергии тела, то необходимо отметить, что не сразу сложилась теория, связывающая внутреннюю энергию и движение частиц. Почти до конца 19 века считалось, что существует так называемая субстанция – тепла, которая, втекая в тело, увеличивает его внутреннюю энергию, температуру; течением этой жидкости считалась его внутренняя энергия. А если тело остывает, то это тепло вытекает из тела, соответственно, внутренняя энергия его уменьшается.
Почти до конца 19 века считалось, что существует так называемая субстанция – тепла, которая, втекая в тело, увеличивает его внутреннюю энергию, температуру; течением этой жидкости считалась его внутренняя энергия. А если тело остывает, то это тепло вытекает из тела, соответственно, внутренняя энергия его уменьшается.
Демонстрация: опыт по сгибанию и разгибанию медной проволоки. Место сгиба быстро становится теплым.
— Почему проволока в месте сгиба нагревается?
Обсуждая ответ на поставленный вопрос, учащиеся приходят к выводу, что, сгибая и разгибая кусок проволоки, мы совершаем механическую работу. Так как температура сгиба увеличилась, то увеличилась и средняя кинетическая энергия молекул, а значит и внутренняя энергия. Следовательно, механическая работа превратилась во внутреннюю энергию.
Рассмотрим опыт, описанный в учебнике на стр.8 (рис.4). (слайд)
Что мы совершали, натирая трубку шнуром? (Механическую работу).
Этот способ увеличения внутренней энергии тела при трении был известен людям с глубокой древности. Именно таким способом люди добывали огонь.
Сделаем общий вывод: как можно увеличить внутреннюю энергию тела? (Совершая над ним механическую работу).
В своей жизненной практике вы также не раз сталкивались с увеличением внутренней энергии тела при совершении над ним механической работы. Работая в мастерских, например, обтачивая детали напильником, что вы замечали? (Детали нагревались).
Если мы будем совершать работу, то тем самым будем изменять энергию тела.
То же самое можно сказать о внутренней энергии: если мы будем совершать работу над телом какими -либо внешними силами, то соответственно, внутренняя энергия этого тела будет изменяться.
(слайд)
Первые опыты по изменению внутренней энергии провел английский инженер и физик Румфорт, который в 18 веке при изготовлении пушек занимался сверлением ствола. Когда происходило сверление, Румфорт заметил, что и сверло, и сам ствол очень сильно нагреваются. В результате эксперимента он убедился, что при движении-вращении сверла можно нагреть даже воду, т.е. на вершине сверла укрепляли ведро с водой, которое в результате движения сверла, закипало, выделялась огромная энергия. Это доказывало, что внутренняя энергия тела может быть изменена при помощи совершения работы.
В технике, промышленности, повседневной практике мы постоянно встречаемся с изменением внутренней энергии тела при совершении работы: нагревание тел при ковке, при ударе; совершение работы сжатым воздухом или паром и др. (слайд)
Демонстрация: Проведём еще один опыт. В стакан с водой, имеющей температуру 20⁰С опустим цилиндр с температурой 100⁰С. Через некоторое время температура воды станет равна 60⁰С. Но и температура цилиндра также станет 60⁰С. За счёт чего повышается температура воды в стакане? (Цилиндр передаёт часть тепла воде. При этом температура (внутренняя энергия) воды становится выше, а температура (внутренняя энергия) цилиндра уменьшается). Такое явление, когда одно тело отдает энергию, а другое принимает, называется теплообменом. При теплообмене температура взаимодействующих тел становятся одинаковой. (слайд)
В стакан с водой, имеющей температуру 20⁰С опустим цилиндр с температурой 100⁰С. Через некоторое время температура воды станет равна 60⁰С. Но и температура цилиндра также станет 60⁰С. За счёт чего повышается температура воды в стакане? (Цилиндр передаёт часть тепла воде. При этом температура (внутренняя энергия) воды становится выше, а температура (внутренняя энергия) цилиндра уменьшается). Такое явление, когда одно тело отдает энергию, а другое принимает, называется теплообменом. При теплообмене температура взаимодействующих тел становятся одинаковой. (слайд)
Изменение внутренней энергии способом теплопередачи: нагревание чайника на плите, или, если вы вдруг опустили ложку чайную в стакан с чаем, то увидите, что эта ложка нагревается, т. е. как происходит этот нагрев, без совершения работы.
е. как происходит этот нагрев, без совершения работы.
Внутренняя энергия тела изменяет свою энергию и за счет теплопередачи, и за счет совершения работы.
(слайд)
Внутренняя энергия изменяется при помощи работы и теплопередачи. Необходимо отметить, что теплопередача может происходить тремя способами, это:
1) Процесс конвекции;
2)Процесс излучения;
3) Процесс теплопроводности.
Внутреннюю энергию можно изменить двумя способами.
Об этом мы будем говорить на последующих уроках.
Физкультминутка
Раз, два – встать пора,
Три, четыре – руки шире,
Пять, шесть – тихо сесть,
Семь, восемь – лень отбросим.
Закрепление изученного материала
Вопрос 1. Если кусок алюминиевой проволоки расклепать на наковальне или быстро изгибать в одном и том же месте то в одну, то в другую сторону, то это место сильно нагревается. Объясните явление.
Объясните явление.
Ответ: Над проволокой совершается механическая работа. Механическая энергия превращается во внутреннюю.
Вопрос №2. Чем объясняется сильный нагрев покрышек автомобиля во время длительной езды?
Ответ. Покрышки нагреваются а счёт работы трения при частичном проскальзывании из по полотну дороги, и за счёт работы деформации покрышки при качении.
Вопрос №3. Когда автомобиль расходует больше горючего: при езде без остановки или с остановками? Почему?
Ответ: При остановке кинетическая энергия автомобиля превращается во внутреннюю энергию тормозных колодок. Чтобы каждый раз после остановки приобрести необходимую скорость, в двигателе должно быть израсходовано дополнительно некоторое количество горючего.
Рефлексия
Итак, внутренняя энергия тела – это суммарная потенциальная и кинетическая энергия всех молекул тела. Молекулы обладают потенциальной энергией, т. к. взаимодействуют друг с другом. Потенциальная энергия молекул зависит от расстояния между молекулами. Расстояние между молекулами можно изменить деформацией или нагреванием. При нагревании и охлаждении расстояние между молекулами изменяется не очень сильно. Значительно расстояние между молекулами изменяется при переходе вещества из одного агрегатного состояния в другое. Молекулы обладают кинетической энергией, т.к. находятся в непрерывном движении. Кинетическая энергия молекул зависит от скорости движения молекул. Скорость движения молекул зависит от температуры. Следовательно, внутренняя энергия тела изменяется при деформации и изменении температуры тела.
к. взаимодействуют друг с другом. Потенциальная энергия молекул зависит от расстояния между молекулами. Расстояние между молекулами можно изменить деформацией или нагреванием. При нагревании и охлаждении расстояние между молекулами изменяется не очень сильно. Значительно расстояние между молекулами изменяется при переходе вещества из одного агрегатного состояния в другое. Молекулы обладают кинетической энергией, т.к. находятся в непрерывном движении. Кинетическая энергия молекул зависит от скорости движения молекул. Скорость движения молекул зависит от температуры. Следовательно, внутренняя энергия тела изменяется при деформации и изменении температуры тела.
Внутреннюю энергию тела можно изменить двумя способами: совершая над телом механическую работу и способом теплопередачи. Теплопередача совершается несколькими способами.
Задает вопросы учащимся:
Все ли было понятно на уроке? Что вызвало трудности?
Почему при обработке детали напильником деталь и напильник нагреваются?
Каким способом и как изменяется внутренняя энергия продуктов, положенных в холодильник?
Молоток будет нагреваться, когда им забивают гвозди, а также когда он лежит на солнце.

Каким образом меняется внутренняя энергия молотка в каждом случае?
Как древние люди добывали огонь? Как сегодня в походных условиях получают огонь?
Каким образом происходит нагревание двигателя и его охлаждение при движении автомобиля?
Оценивание
Как вы работали на уроке? Как вы себя оцениваете?
Выставляет оценки за урок, с комментариями
Домашнее задание: прочитать параграф 3, 4 — выучить основные понятия, упр.1. стр.13.
Физика — 8
ПРИМЕНЕНИЕ ПОЛУЧЕННЫХ ЗНАНИЙИССЛЕДОВАНИЕ-2
- Решите задачу
Если в процессе закачивания воздуха в толстостенный сосуд совершается работа, равная
2 · 107 Дж, пробка выбивается из сосуда.
В это время:
- за счет чего изменилась внутренняя энергия воздуха в сосуде: механической работы или теплопередачи?
- на сколько джоулей изменилась внутренняя энергия воздуха в сосуде?
- как изменилась внутренняя энергия воздуха в сосуде: увеличилась или
уменьшилась? Ответы обоснуйте.

КЛЮЧЕВЫЕ СЛОВА
Изменение внутренней энергии
Сохранение энергии
Количество теплоты
Совершение механической работы
ЧТО ВЫ УЗНАЛИ?
Если внутренняя энергия системы изменяется одновременно в результате __ и
теплопередачи, то __ равна сумме совершенной работы и переданному __.
Это выражение закона __ в тепловом
процессе.
- В каком случае может уменьшиться внутренняя энергия тела?
- Как выражается закон сохранения энергии для тепловых процессов?
- Газ сжимается путем совершения 5,5 кДж механической работы. В процессе сжатия окружающей среде было передано количество теплоты в 3,3 кДж. Вычислите изменение внутренней энергии газа. Внутренняя энергия газа в этом процессе увеличилась или уменьшилась?
- Что выражают формулы∇U = A или ∇U = —A? Приведите примеры для этих процессов.

- Что выражают формулы ∇U = Q или ∇U = —Q? Приведите примеры для этих процессов.
Расчет изменения внутренней энергии — презентация онлайн
Уроки физики в 8 классеУчитель физики МОУ «Новокулындинская СОШ»
Ваганова Елена Равкатовна
2010 год
1
Вам уже известно,
что внутренняя
энергия тела может
изменяться как
путем совершения
работы, так и путем
теплопередачи.
2
Энергия, которую
получает или теряет
тело при
теплопередаче,
называется
количеством
теплоты
3
Количество
теплоты,
которое
необходимо
для
нагревания
тела,
зависит от
его массы.
4
Количество
теплоты, которое
необходимо для
нагревания,
зависит от того, на
сколько градусов
нагревается тело.
Это значит, что
количество теплоты
зависит от разности
температур тела.

5
Количество
теплоты,
которое
необходимо
для
нагревания
тела, зависит
от того, из
какого
вещества оно
состоит.
6
Количество теплоты,
которое необходимо
для нагревания тела
(или выделяемое при
остывании), зависит от
массы этого тела, от
изменения его
температуры и рода
вещества.
7
1 ккал = 1000 кал.
1 кДж = 1000 Дж
1 кал = 4,19 Дж =
4,2 Дж.
1 ккал = 4190 Дж =
4200 Дж = 4,2 кДж
8
Обозначим изменение
внутренней энергии через
(«дельта U»).
Под изменением внутренней
энергии будем понимать разность
между конечным и начальным
значением энергии: U U 2 U1
Очевидно, что если
U > О,
то внутренняя энергия
увеличивается, если U
то энергия уменьшается.
U
9
Если при
теплообмене
Если внешние
силы
система
получила
работу А
Uсовершили
Q
количество
над системой, то:
теплоты Q, то
U UÀ Q
Если система отдает при
теплообмене количество
теплоты Q, то внутренняя
энергия системы
уменьшается,
c
10
U A Q
Изменение внутренней
энергии системы равно
работе внешних сил
над системой и
количеству теплоты,
полученному системой.

11
Работа, теплота и внутренняя энерги
Теплота, работа и внутренняя энергия участвуют в термодинамических процессах, т. е. являются термодинамическими функциями. Ранее мы изложили основные свойства последних, а теперь покажем проявление этих свойств в конкретных термодинамических процессах изохорическом, изобарическом, изотермическом и адиабатическом. [c.57]
Приведенные понятия опираются на представления о молекулярной структуре вещества, что соответствует современным взглядам. Однако эти определения не являются термодинамическими, так как классическая термодинамика не использует каких-либо сведений о строении вещества и вводит иные, формальные понятия теплоты, работы и внутренней энергии. С ними мы познакомимся в дальнейшем. [c.61]
Аналогичную связь между теплотой, работой и внутренней энергией газа характеризует первый закон термодинамики, который можно записать в виде [c. 26]
26]
Как связаны между собой теплота, работа и внутренняя энергия [c.59]
Единицей измерения количества теплоты, внутренней энергии, работы и других энергетических величин в системе СИ является Дж или Дж/моль. [c.19]
Однако такая запись требует некоторых уточнений. Не следует думать, что тепло, работа и внутренняя энергия могут быть подвергнуты одинаковой оценке. Обладая способностью измеряться в одинаковых единицах, эти величины значительно отличаются друг от друга по своей физической сущности. Теплота и работа не являются формой энергии, они представляют собой лишь форму перехода энергии от одного тела к другому. Кроме того, тепло и работа являются абсолютными величинами и в уравнении (4) связаны с разностной величиной — внутренней энергией. Поэтому часто для того, чтобы более выпукло представить различие свойств энергии, теплоты и работы, первое начало термодинамики в интегральной форме записывается иначе [c. 19]
19]
Все величины в приведенных формулах измеряются в джоулях (Дж). В качестве иллюстрации, дающей представление о применении первого начала термодинамики, удобно рассмотреть связь между теплотой, работой и внутренней энергией при многократном поднятии груза человеком (рис. 1.3). [c.14]
Несколько слов следует сказать о систем знаков рассматриваемых величин. В настояш ее время общепринятой является система знаков относительно системы, в которой знак минус присваивается какому-либо свойству (например, внутренней энергии), если его количество убывает, и наоборот. Аналогично, если теплота или внешняя работа увеличивают внутреннюю энергию системы (например, в эндотермических процессах или при совершении внешней работы над системой от наружного источника), их считают положительными, а если уменьшают (в экзотермических процессах или при совершении системой работы против внешних сил), то отрицательными. К сожалению, в отечественной литературе пока нет единообразия в решении этого вопроса. В химической литературе можно увидеть запись тепловых эффектов в так называемой химической системе знаков, обратной термодинамической, о которой идет речь. Знак работы, совершаемой системой, принимается положительным в большинстве отечественных учебников и отрицательным — в зарубежных. Первое начало в учебниках обычно представляют в виде [ср. с уравнением (103)] [c.325]
В химической литературе можно увидеть запись тепловых эффектов в так называемой химической системе знаков, обратной термодинамической, о которой идет речь. Знак работы, совершаемой системой, принимается положительным в большинстве отечественных учебников и отрицательным — в зарубежных. Первое начало в учебниках обычно представляют в виде [ср. с уравнением (103)] [c.325]
Если привести в соприкосновение два тела, то молекулы этих тел, сталкиваясь между собой, передают друг другу энергию. При этом энергия передается от более нагретого тела к менее нагретому, т. е. от тела, имеющего большую среднюю кинетическую энергию молекул, к телу с меньшей кинетической энергией молекул. Тело, которое отдает энергию, охлаждается, а тело, которое ее получает, нагревается. Меру изменения внутренней энергии, перешедшей от одного тела к другому в результате энергетического взаимодействия молекул без видимого движения самих тел, называют количеством теплоты.
 Внутренняя энергия тела может изменяться также в процессе его расширения с преодолением сопротивления внешних сил и в процессе сжатия, под воздействием внешних сил. При расширении сжатого тела и совершении им внешней работы за счет внутренней энергии температура тела понижается, а при сжатии повышается. [c.7]
Внутренняя энергия тела может изменяться также в процессе его расширения с преодолением сопротивления внешних сил и в процессе сжатия, под воздействием внешних сил. При расширении сжатого тела и совершении им внешней работы за счет внутренней энергии температура тела понижается, а при сжатии повышается. [c.7]ГИИ, перешедшей от одного тела к другому в результате энергетического взаимодействия молекул без видимого движения самих тел, называют количеством теплоты. Внутренняя энергия тела может изменяться также в процессе его расширения с преодолением сопротивления внешних сил и в процессе сжатия, под воздействием внешних сил. При расширении сжатого тела и совершении им внешней работы за счет внутренней энергии температура тела понижается, а при сжатии повышается. [c.6]
Первый закон отражает энергетический и тепловой баланс протекающих процессов и включает принцип эквивалентности между видами энергий. Он определяет взаимосвязь между работой, теплотой и различными видами энергии. Согласно одной из формулировок теплота, подведенная к рабочему телу, расходуется на производство работы, повышение внутренней энергии рабочего тела и потерь в окружающую среду. [c.54]
Согласно одной из формулировок теплота, подведенная к рабочему телу, расходуется на производство работы, повышение внутренней энергии рабочего тела и потерь в окружающую среду. [c.54]
Здесь можно упомянуть о волнующей умы проблеме источника энергии для дальнейшего развития земной цивилизации. Казалось бы, в распоряжении человечества имеется огромный запас энергии в виде теплоты (внутренней энергии) тропических морей. Ведь охлаждение 1 л воды на Г эквивалентно 1 ккал и 427 кгм работы. Однако второй закон ограничивает возможность использования этой энергии — если даже найти необходимый второй тепловой резервуар с более низкой температурой в более низко расположенных слоях воды, то разность Tl — Т2 оказывается малой и получаемая работа дорогой. Попытки в этом направлении все же делаются. [c.79]
Если рассматриваем бесконечно малые термодинамические процессы, т. е. когда система обменивается с окружающей средой бесконечно малыми количествами теплоты и работы и внутренняя энергия претерпевает бесконечно малое изменение, уравнение первого закона термодинамики запишем в виде [c. 13]
13]
Итак, любая система характеризуется внутренней энергией, мерами измерения которой служат теплота и работа. Приращение внутренней энергии системы в любом процессе равно сумме теплоты, подведенной к системе, и работы, которую совершают внешние силы над системой. [c.119]
Теплота и работа, Согласно молекулярно-кинетической теории каждое тело располагает определенным запасом внутренней энергии, который слагается из энергии движения молекул (поступательного и вращательного), называемой внутренней кинетической энергией, и энергии взаимного притяжения молекул — внутренней потенциальной энергии (в идеальных газах отсутствует). [c.25]
Для конечных (не диференциально малых) количеств теплоты, внутренней энергии и работы [c.56]
Существует другой способ интерпретации первого закона, имеющий особо важное значение для химии. Будем рассматривать уравнение (15-1) просто как определение некоторой функции, называемой внутренней энергией Е. Напомним, что при нагревании газа он может совершать работу (см. подпись к рис. 15-2), но можно и обратить этот процесс, т.е. совершать работу над газом, сжимая его, и при этом отводить теплоту, выделяемую газом. Наконец, если нагревать газ, не давая ему выполнять работу, то в этом случае происходит повышение температуры газа. И наоборот, если позволить газу, находящемуся под высоким давлением, расширяться и совершать работу, не нагревая его, то в таком процессе обнаруживается охлаждение газа. Подбирая требуемые условия, удается манипулировать величинами дат независимо. За тем, что происходит в каждом случае, удобно следить, если определять изменение внутренней энергии, АЕ, как разность между добавляемым в систему количеством теплоты и выполненной системой работой, как это следует из уравнения (15-1). Если при добавлении в систему некоторого количества теплоты система выполняет в точности эквивалентную работу, внутренняя энергия системы остается неизменной. Когда мы нагреваем газ, но ограничиваем его объем, лишая газ возможности расширяться и вьшолнять работу, внутренняя энергия газа возрастает на величину, равную поступившему в него количеству теплоты.
Напомним, что при нагревании газа он может совершать работу (см. подпись к рис. 15-2), но можно и обратить этот процесс, т.е. совершать работу над газом, сжимая его, и при этом отводить теплоту, выделяемую газом. Наконец, если нагревать газ, не давая ему выполнять работу, то в этом случае происходит повышение температуры газа. И наоборот, если позволить газу, находящемуся под высоким давлением, расширяться и совершать работу, не нагревая его, то в таком процессе обнаруживается охлаждение газа. Подбирая требуемые условия, удается манипулировать величинами дат независимо. За тем, что происходит в каждом случае, удобно следить, если определять изменение внутренней энергии, АЕ, как разность между добавляемым в систему количеством теплоты и выполненной системой работой, как это следует из уравнения (15-1). Если при добавлении в систему некоторого количества теплоты система выполняет в точности эквивалентную работу, внутренняя энергия системы остается неизменной. Когда мы нагреваем газ, но ограничиваем его объем, лишая газ возможности расширяться и вьшолнять работу, внутренняя энергия газа возрастает на величину, равную поступившему в него количеству теплоты. Наконец, если мы используем газ для совершения работы, не поставляя в него теплоту, внутренняя энергия газа уменьшается на величину, равную выполненной работе. Наши обьщенные наблюдения относительно того, что в одних из этих случаев газ нагревается, а в других охлаждается, указывают на связь внутренней энергии и температуры газа. [c.15]
Наконец, если мы используем газ для совершения работы, не поставляя в него теплоту, внутренняя энергия газа уменьшается на величину, равную выполненной работе. Наши обьщенные наблюдения относительно того, что в одних из этих случаев газ нагревается, а в других охлаждается, указывают на связь внутренней энергии и температуры газа. [c.15]
Принцип эквивалентности теплоты и работы. Внутренняя энергия тела может изменяться как путем теплопередачи (нагревание или охлаждение), так и путем совершения работы. По закону сохранения энергии, открытому М. В. Ломоносовым, теплота и работа эквивалентны друг другу и могут переходить одна в другую. Впервые опытные определения соотношения между механической работой й внутренней энергией тела были осуществлены английским физиком Джоулем в период с 1840 по 1849 г. [c.11]
Каждый процесс, в котором происходит расширение или сжатие газа, следует рассматривать как процесс перехода теплоты в механическую работу и внутреннюю энергию или обратно. Для того чтобы теп- [c.29]
Для того чтобы теп- [c.29]
Предположим, что некоторая система за счет поглощения теплоты Q переходит из состояния 1 в состояние 2. В общем случае эта теплота расходуется на изменение внутренней энергии системы ДО и на совершение работы претив внешних сил Л Q = Ai/ + Л. [c.159]
Приведенное уравнение выражает закон сохранения энергии, т. е. означает, что сумма изменения внутренней энергии и совершенной системой (или над нею) работы равна сообщенной (или выделенной ею) теплоте. Так, если теплота сообщается газу в цилиндре, закрытом поршнем, то газ, во-первых, нагрев.ается, т. е. его внутренняя энергия и возрастает, а во-вторых, расширяется, т. е. производит работу подъема поршня А. [c.159]
Направление расходования подводимой тепловой энергии определяется условиями, при которых она передается системе. Если теплота подводится, например, к газу при постоянном объеме, то газ, не имея возможности расширяться, не может совершить работу расширения и вся теплота расходуется на приращение внутренней энергии.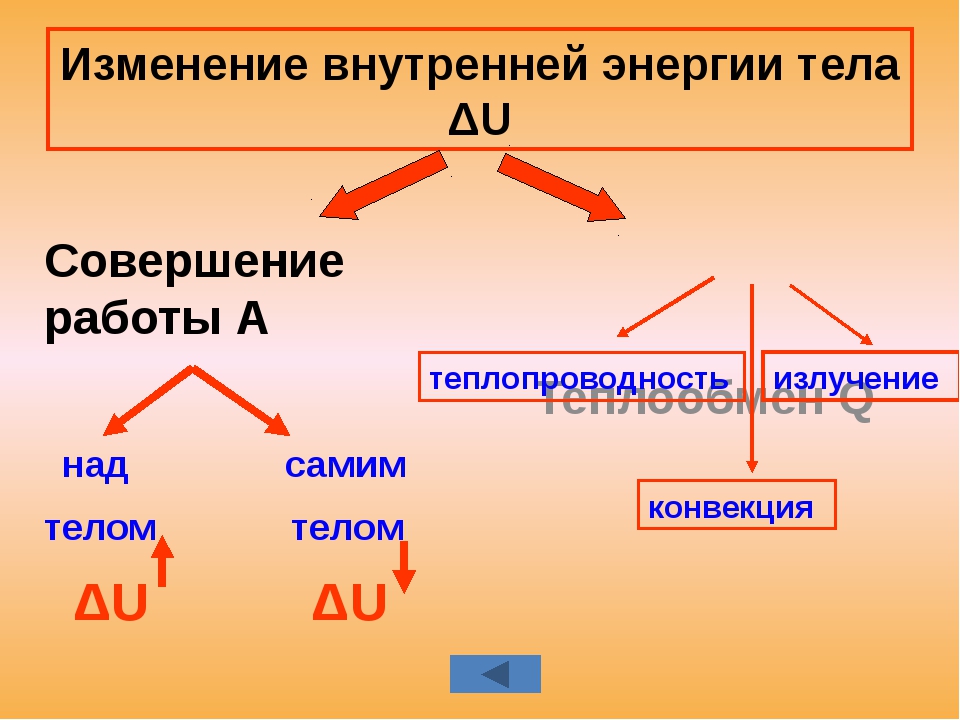 [c.37]
[c.37]
Коэффициент активного тепловыделения % представляет собой относительную долю теплоты, использованной на нагревание рабочего тела (на повышение его внутренней энергии АС/) и на совершение внешней работы J PdV, от общей теплоты Q, введенной в цикл [c.155]
Между выделяемым или поглощаемым системой количеством теплоты aQ, количеством производимой или потребляемой системой работы dA и изменением внутренней энергии системы du, согласно первому закону термодинамики, существует зависимость [c.127]
Выше было показано, что теплота, поглош аемая системой при постоянном давлении, затрачивается на изменение ее внутренней энергии и внешнюю работу (4) [c.13]
В термодинамических процессах осуществляется передача внутренней энергии от одних тел к другим. Эта энергия может передаваться в виде теплоты и в виде работы. Различие состоит в том, что при передаче энергии путем теплоты отсутствует видимое движение тел относительно друг друга, а взаимодействие между телами выражается в переходе энергии от молекул одного тела к молекулам другого. Передача энергии в виде работы связана с видимым перемещением тел, в частности с изменением их объема. Поэтому про работу говорят, что она совершается, а про теплоту — что она подводится (или отводится). [c.25]
Передача энергии в виде работы связана с видимым перемещением тел, в частности с изменением их объема. Поэтому про работу говорят, что она совершается, а про теплоту — что она подводится (или отводится). [c.25]
В изотермическом процессе нет изменения температуры газа, поэтому его внутренняя энергия не изменяется, а вся подводимая теплота расходуется на совершение внешней работы [c.29]
Следует отметить, что первый закон термодинамики не дает возможности найти полное значение внутренней энергии системы в каком-либо состоянии, так как уравнения, выражающие первый закон, приводят к вычислению только изменения энергии системы в различных процессах. Точно так же нельзя непосредственно измерить изменения внутренней энергии в макроскопических процессах можно лишь вычислить эти изменения с помощью уравнения (I, 26), учитывая измеримые величины—теплоту и работу данного процесса. [c.33]
Отметим, что теплота и работа (каждая в отдельности) не обладают свойством функции состояния, выражаемым уравнением (I, 3) или (I, 5) и присущим внутренней энергии. Теплота и работа процесса, переводящего систему из состояния 1 в состояние 2, зависят, в общем случае, от пути процесса, и величины SQ и оЛ не являются дифференциалами функции состояния, а суть просто бесконечно малые величины, которые мы будем называть элементарной теплотой и элементарной работой. [c.33]
Теплота и работа процесса, переводящего систему из состояния 1 в состояние 2, зависят, в общем случае, от пути процесса, и величины SQ и оЛ не являются дифференциалами функции состояния, а суть просто бесконечно малые величины, которые мы будем называть элементарной теплотой и элементарной работой. [c.33]
Таким образом, дифференциал внутренней энергии dll имеет иные математические свойства, чем элементарные теплота 3Q и работа 8Л. Это имеет существенное значение при построении системы термодинамики. [c.33]
Перед тем, как поступить в реактор, пары пропана предварительно подогреваются от 25 до 427 С, Определить теплоту, работу, изменение внутренней энергии, изменение энтальпии, если давление в нагревателе поддерживаехса постоянным (необходимые сведения см. в 12]). [c.67]
В терм0дина1мике принято считать теплоту, поглощаемую системой, положительной. За счет поглощения теплоты внутренняя энергия увеличивается. Работу считают положительной, если она совершается системой против внешних сил. В противном случае эти величины берутся с отрицательным знаком [c.12]
Работу считают положительной, если она совершается системой против внешних сил. В противном случае эти величины берутся с отрицательным знаком [c.12]
В этом уравнении 17, названная Клаузиусом внутренней энергией, выступает как мера материального движешта во всех его превращениях из одной формы в другую, в пределах термодинамики внутренняя энергия выступает как общая мера работы и теплоты. Внутренней энергией мы называем энергию, заключенную в системе. При этом обычно не учитывается кинетическая энергия системы в целом и потенциальная энергия системы во внешнем поле. При микроскопическом рассмотрении это означает, что внутренняя энергия равна сумме кинетической энергии отдельных молекул и энергии вза одействия между ними. Другими словами, внутренняя энергия системы является функцией лишь внутренних параметров состояния (температуры, массы отдельных элементов системы и т. д.) и является экстенсивной величиной (17 = X] 17 , где 17 — внутренняя энергия г-й области системы).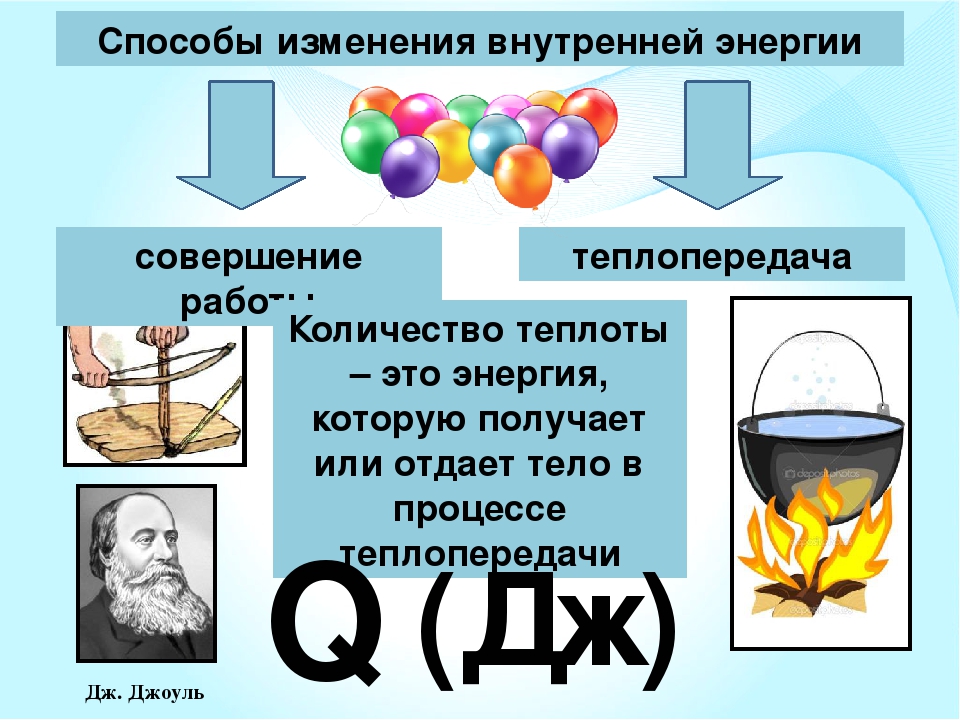 [c.12]
[c.12]
Третий пример -т расширение газа в пустоту. В данном случае вопрос об-обратимости сводится к тому, возможен ли процесс, единственный результат которого заключался бы в сжатии газа без изменения его внутренней энергии. На сжатиетела надо затратить работу чтобы внутренняя энергия тела не увеличилась, надо отнять от него эквивалентное количество тепла наконец, чтобы никаких изменений в окружающем мире не произошло,, надо было бы эту отнятую у газа теплоту некомпенсированно превратить в работу, что невозможно. Значит, расширение газа в пустоту необратимо. [c.73]
Каждый вид энергии, как это следует и из (6) — (9), можно представить в виде произведения двух параметров (или факторов) — параметра (фактора) интенсивности и параметра (фактора) экстенсивности или емкости. Первый из них показывает уровень энергии, второй — ее количество, меру. При установлении равновесия между системами однотипные параметры интенсивности нивелируются, выравниваются, а однотипные параметры экстенсивности суммируются. Уровень нивелированных факторов интенсивности зависит при этом от соотношения соответствующих экстенсивных факторов в исходных, изолированных системах (до установления равновесия между ними). Пусть, например, в двух коленах и-образного сосуда, разделенного в его нижней части закрытым краном, находится одна и та же жидкость при одной и тон же температуре. В одном, более узком, например в левом, колене ее объем равен Уд и высота Йл этой высоте пропорционально давление Ря. В другом (правом), более широком колене эти величины равны соответственно Кш Лд и Рп, причем Рл>Рп. Если, открыть кран, то жидкость в обоих коленах сосуда установится на одном и том же уровне, а давления сделаются одинаковыми и равными некоторой величине Рр(Рпобъем системы Ур будет равен при этом сумме исходных объемов 1 р= У л-Н п. Очевидно, что смещение уровней (изменение давлений) в процессе установления равновесия от их первоначальных значений до конечного определяется соотношением объемов. Таким образом, в случае объемномеханической работы (энергии) давление Р — это фактор интенсивности, а объем V — фактор экстенсивности.
Уровень нивелированных факторов интенсивности зависит при этом от соотношения соответствующих экстенсивных факторов в исходных, изолированных системах (до установления равновесия между ними). Пусть, например, в двух коленах и-образного сосуда, разделенного в его нижней части закрытым краном, находится одна и та же жидкость при одной и тон же температуре. В одном, более узком, например в левом, колене ее объем равен Уд и высота Йл этой высоте пропорционально давление Ря. В другом (правом), более широком колене эти величины равны соответственно Кш Лд и Рп, причем Рл>Рп. Если, открыть кран, то жидкость в обоих коленах сосуда установится на одном и том же уровне, а давления сделаются одинаковыми и равными некоторой величине Рр(Рпобъем системы Ур будет равен при этом сумме исходных объемов 1 р= У л-Н п. Очевидно, что смещение уровней (изменение давлений) в процессе установления равновесия от их первоначальных значений до конечного определяется соотношением объемов. Таким образом, в случае объемномеханической работы (энергии) давление Р — это фактор интенсивности, а объем V — фактор экстенсивности. Аналогично, температура Т представляет собой параметр интенсивности, а энтропия 5— параметр экстенсивности тепловой энергии (теплоты).. Внутренняя энергия и как функция энтропии и объема — факторов экстенсивности сама также является экстенсивным параметром внутренние энергии систем, приведенных в равновесие, суммируются. [c.12]
Аналогично, температура Т представляет собой параметр интенсивности, а энтропия 5— параметр экстенсивности тепловой энергии (теплоты).. Внутренняя энергия и как функция энтропии и объема — факторов экстенсивности сама также является экстенсивным параметром внутренние энергии систем, приведенных в равновесие, суммируются. [c.12]
Таким образом, величина i подобна pVT, а также и и характеризует состояние тела. В физическом смысле di есть элементарное количество тепла, сообщаемое телу при р = onst. Иными словами, энтальпию можно определить как количество тепла, которое нужно затратить для перехода тела, имеющего бесконечно малый объем, к данному состоянию при постоянном давлении. В связи с изменением можно сказать, что энтальпия есть та теплота, которая будет затрачена на увеличение внутренней энергии и соверщение работы в системе. [c.71]
Первый закон термодинамики, который называется также законом эквивалентности теплоты и работы, является одним из частых случаев закона сохранения энергии и служит основой всех тепловых и энергегических расчетов. Этот закон формулируют следующим образом тепловая энергия не может ни исчезнуть бесследно, ни возникнуть вновь из ничего она момэквивалентное количество энергии другого рода. При этом установлено, что если система поглощает извне или отдает в окружающее пространство тепло, то последнее расходуется только на изменение внутренней энергии данной системы и на совершение ею внешней работы (если таковая имеет место в данном процессе). Таким образом, если внутре1шяя энергия какой-либо системы (например, газа в сосуде и т. п.) после сообщения этой системе некоторого количества тепла (ЛQ) изменилась на Д(7, то, согласно первому закону термодинамики, имеем [c.66]
Этот закон формулируют следующим образом тепловая энергия не может ни исчезнуть бесследно, ни возникнуть вновь из ничего она момэквивалентное количество энергии другого рода. При этом установлено, что если система поглощает извне или отдает в окружающее пространство тепло, то последнее расходуется только на изменение внутренней энергии данной системы и на совершение ею внешней работы (если таковая имеет место в данном процессе). Таким образом, если внутре1шяя энергия какой-либо системы (например, газа в сосуде и т. п.) после сообщения этой системе некоторого количества тепла (ЛQ) изменилась на Д(7, то, согласно первому закону термодинамики, имеем [c.66]
Из этого соотношения следует, что работа сил трения йА для выделенного элементарного объема системы превраш,ается в теплоту dQ, а кроме того, расходуется на увеличение внутренней энергии на химическое взаимодействие (%1с1п1г) и некоторые другие виды превращений. Указанные параметры тесно связаны между собой. Исходя из энергетической гипотезы, изнашивание (отделение) материала наступает тогда, когда внутренняя энергия 7 достигает критического значения.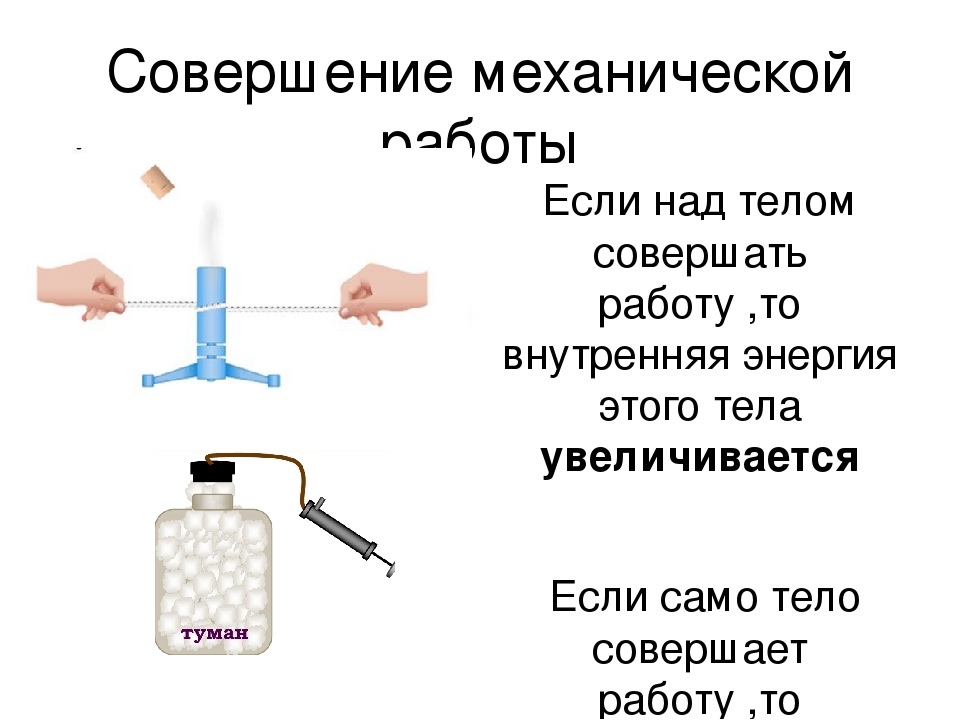 Однако в общем случае в присутствии химически активных компонентов износ определяется также глубиной химических превращений. В свою очередь, оба перечисленных фактора зависят от dQ. [c.250]
Однако в общем случае в присутствии химически активных компонентов износ определяется также глубиной химических превращений. В свою очередь, оба перечисленных фактора зависят от dQ. [c.250]
В изохорпом процессе газ не совершает внешней работы, потому что пе изменяется его объем. Поэтому вся подведенная теплота идет на увеличение внутренней энергии газа. Из уравнения состояния идеального газа р-о=ЯТ следует, что [c.28]
Данное рассуждение обосновывает 01И) тным путем наличие определенной функции состояния системы, имеющей смысл суммарной меры всех движений, которыми система oблaдaeт Предположим, что циклический процесс удалось провести так, что после того как система вернулась к исходному состоянию, внутренняя энергия системы не приняла начального значения, а увеличилась. В этом случае повторение круговых процессов вызвало бы накопление энергии в системе. Создалась бы возможность превращения этой энергии в работу и получения таким путем работы не за счет теплоты, а из ничего , так как в круговом процессе работа и теплота эквивалентны друг другу, что показано прямыми опытами. [c.31]
[c.31]
Страница не найдена |
Страница не найдена |404. Страница не найдена
Архив за месяц
ПнВтСрЧтПтСбВс
21222324252627
28
12
12
1
3031
12
15161718192021
25262728293031
123
45678910
12
17181920212223
31
2728293031
1
1234
567891011
12
891011121314
11121314151617
28293031
1234
12
12345
6789101112
567891011
12131415161718
19202122232425
3456789
17181920212223
24252627282930
12345
13141516171819
20212223242526
2728293031
15161718192021
22232425262728
2930
Архивы
Мар
Апр
Май
Июн
Июл
Авг
Сен
Окт
Ноя
Дек
Метки
Настройки
для слабовидящих
Изменение внутренней энергии происходит при
Внутренняя энергия системы может изменяться за счет энергии, сообщаемой системе извне.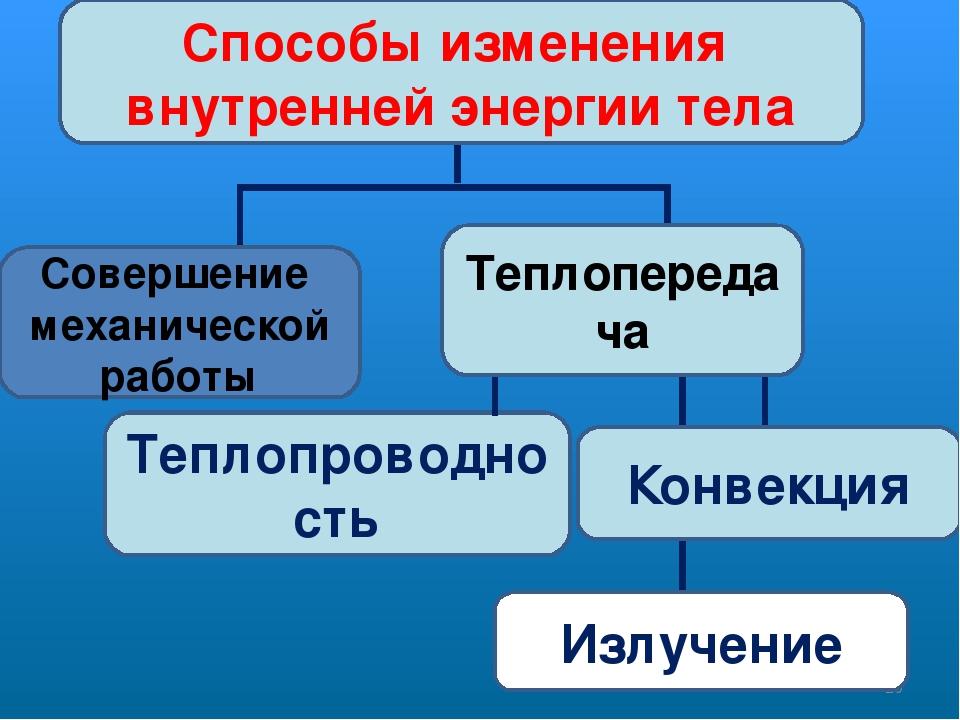 Эта энергия может сообщаться системе посредством двух процессов: либо за счет работы, производимой внешними силами над системой, либо за счет передачи ей тепла. Рассмотрим газ, сжимаемый в сосуде поршнем под действием силы F (рис.). Пусть под действием этой силы поршень переместился на расстояние dh, сжав газ. Работа силы на пути dh ‑ dA = Fdh.
Эта энергия может сообщаться системе посредством двух процессов: либо за счет работы, производимой внешними силами над системой, либо за счет передачи ей тепла. Рассмотрим газ, сжимаемый в сосуде поршнем под действием силы F (рис.). Пусть под действием этой силы поршень переместился на расстояние dh, сжав газ. Работа силы на пути dh ‑ dA = Fdh.
Разделив величину силы на площадь поршня, получим давление P, а умножив на S, получим изменение объема газа dV . Таким образом, производимая над газом работа
dA= PdV. (2.30)
Такую же по величине работу совершает газ при расширении, перемещая поршень. При этом dV положительно, если газ расширяется, и отрицательно при сжатии газа. Соответственно работа dA положительна или отрицательна: в первом случае система производит работу сама, во втором — внешние силы производят работу над системой.
Графически процесс изменения состояния газа при его расширении или сжатии изображается на кривой P, V участком 1-2 на рис. Полная работа, совершаемая газом, при расширении от V1до V2:
Полная работа, совершаемая газом, при расширении от V1до V2:
. (2.31)
Эта работа численно равна заштрихованной площади, заключенной под кривой P(V).
Рассмотрим способы передачи телу тепла. При соприкосновении тел либо при взаимодействии тел через излучение, изменение внутренней энергии происходит за счет передачи энергии хаотически движущихся частиц одного тела частицам другого.
Энергия, передаваемая от одного тела другому, представляет собой теплоту. Обозначим ее через Q. Теплота измеряется в тех же единицах, что и энергия.
Связь между переданным теплом, изменением внутренней энергии системы и произведенной работой выражается уравнением
dQ = dE + dA = dE + PdV. (2.32)
Это уравнение представляет собой закон сохранения энергии применительно к механической и тепловой энергии макроскопических тел. Он получил название первого начала термодинамики.
Важно учесть, что в выражении (2. 32) работа и количество тепла не есть полные дифференциалы каких-либо величин, в то время как внутренняя энергия является таковой. Можно говорить о внутренней энергии в данном состоянии, а не о количестве тепла или работы, которыми обладает тело. Нельзя делить энергию тела на тепловую и механическую, речь идет лишь об изменении внутренней энергии тела за счет количества тепла, переданного ему или отданного им, и количества совершенной работы. Это разделение неоднозначно и зависит от начального и конечного состояний тела и от характера совершаемого процесса. Поэтому, например, в процессе перехода из состояния 1 в состояние 2 изменение внутренней энергии может быть равно нулю, а тело при этом может приобрести или потерять энергию.
32) работа и количество тепла не есть полные дифференциалы каких-либо величин, в то время как внутренняя энергия является таковой. Можно говорить о внутренней энергии в данном состоянии, а не о количестве тепла или работы, которыми обладает тело. Нельзя делить энергию тела на тепловую и механическую, речь идет лишь об изменении внутренней энергии тела за счет количества тепла, переданного ему или отданного им, и количества совершенной работы. Это разделение неоднозначно и зависит от начального и конечного состояний тела и от характера совершаемого процесса. Поэтому, например, в процессе перехода из состояния 1 в состояние 2 изменение внутренней энергии может быть равно нулю, а тело при этом может приобрести или потерять энергию.
Дата добавления: 2015-08-08; просмотров: 307;
ПОСМОТРЕТЬ ЕЩЕ:
На предыдущем уроке мы уже узнали, от чего зависит внутренняя энергия. Теперь попытаемся разобраться, как её можно изменить. При повышении температуры увеличивается скорость движения молекул, следовательно, возрастает их кинетическая энергия и внутренняя энергия тела. И, наоборот: при понижении температуры, внутренняя энергия уменьшается.
И, наоборот: при понижении температуры, внутренняя энергия уменьшается.
Проведем маленький эксперимент. Возьмем деревянные палочки и потрём их друг о друга. Через некоторое время они нагреются, а, следовательно, их внутренняя энергия увеличится. То же самое произойдёт и при ударе. Нетрудно догадаться, что при деформации тело тоже нагревается, так как деформация может являться следствием удара. Во всех этих случаях, над телом совершалась та или иная работа. Значит, увеличение внутренней энергии происходит при совершении работы над телом.
Рассмотрим другой пример. В стеклянный сосуд бросим несколько горящих спичек, а на горлышко сосуда положим варёное яйцо. Через некоторое время спички потухнут, в результате чего воздух начнёт остывать. Из-за этого яйцо засосет внутрь. Это произойдет из-за того, что давление внутри сосуда понизится и будет не достаточным, чтобы сдерживать давление снаружи. Из этого можно сделать вывод, что внутренняя энергия воздуха внутри сосуда уменьшилась. Заметим, что понижение давления произошло из-за сжатия воздуха при понижении температуры, то есть, воздух совершил работу. Следовательно, уменьшение внутренней энергии происходит, когда тело само совершает работу.
Заметим, что понижение давления произошло из-за сжатия воздуха при понижении температуры, то есть, воздух совершил работу. Следовательно, уменьшение внутренней энергии происходит, когда тело само совершает работу.
Однако, изменить внутреннюю энергию можно и путём теплопередачи.
Нальём воду в чайник, и нагреем.
Для того, чтобы вода закипела, мы должны сообщить ей некоторое количество теплоты, то есть, произвести теплопередачу. Чем дольше продолжается теплопередача, тем больше становится температура воды и её внутренняя энергия. Через некоторое время вода закипит, а, значит, её внутренняя энергия увеличится.
Проведем ещё один эксперимент. Нальем в кружку горячий чай. Через некоторое время кружка нагреется, а чай, напротив, остынет, а, значит, его внутренняя энергия уменьшится.
Дело в том, что в этом случае, чай сам совершил теплопередачу, а именно, — нагрел кружку и часть окружающего воздуха.
Как видим, теплопередача всегда происходит от тела с более высокой температурой к телу с более низкой температурой. Когда температуры тел выравниваются, теплопередача прекращается. Способами теплопередачи являются теплопроводность, конвекция и излучение. О них мы поговорим на следующих уроках.
Когда температуры тел выравниваются, теплопередача прекращается. Способами теплопередачи являются теплопроводность, конвекция и излучение. О них мы поговорим на следующих уроках.
Итак, изменить внутреннюю энергию тела можно с помощью механической работы или теплопередачи.
Упражнения.
Изменится ли внутренняя энергия мяча, если, находясь в комнате, его подбросить в воздух?
Нет, потому что бросок не изменил ни температуру мяча, ни его агрегатное состояние. Над мячом не была совершена работа, и сам мяч не совершал работы. Теплопередача тоже отсутствовала, поэтому внутренняя энергия меча не изменилась.
Изменится ли внутренняя энергия мяча, если, находясь в комнате, его подбросить так, чтоб он отскочил от потолка?
Да, потому что при ударе о потолок мяч на время деформируется, а, следовательно, его внутренняя энергия возрастёт, так как над мячом была совершена работа.
Изменится ли внутренняя энергия льда, если его растопить?
Конечно. Ведь растопить лед — значит, превратить его в воду, а это изменение агрегатного состояния, да и температуры тоже. Кроме того, чтобы растопить лёд нужно осуществить теплопередачу.
Ведь растопить лед — значит, превратить его в воду, а это изменение агрегатного состояния, да и температуры тоже. Кроме того, чтобы растопить лёд нужно осуществить теплопередачу.
Изменится ли внутренняя энергия кусочка мела, если провести им по доске? Конечно. Ведь мел пишет только тогда, когда трение достаточно велико, а трение, как мы помним из примера, совершает работу над телом. Кроме того, часть мела останется на доске. Это изменит количество молекул, содержащихся в данном кусочке, а, как мы помним, внутренняя энергия тела — это суммарная энергия всех молекул этого тела.
676. Является ли тепловым движением вращение искусственного спутника вокруг Земли?
Нет, не является. Тепловое движение – это беспорядочное движение молекул и атомов, из которых состоит тело.
677. Движение молекул газа можно назвать тепловым движением? Тепловое движение – это процесс хаотичного движения частиц. Молекулы газа движутся хаотично, поэтому их движение можно назвать тепловым.
678. Можно ли сказать, что явление диффузии вызвано тепловым движением? Тепловое движение – это процесс хаотичного движения частиц в веществе. Диффузия – процесс взаимного проникновения атомов и молекул одного вещества в другое. Процесс взаимного проникновения вызван хаотичным движением атомов и молекул, следовательно, явление диффузии вызвано тепловым движением.
679. Что происходит с тепловым движением при повышении температуры?
При повышении температуры скорость движения молекул увеличивается.
680. Изменится ли кинетическая и потенциальная энергии молекул воды в плотно закупоренной банке с холодной водой, если ее погрузить в горячую воду?
Температура в банке будет увеличиваться за счет явления теплообмена, тем самым увеличивая кинетическую энергию. Потенциальная энергия останется неизменной, так как она зависит от расстояния между молекулами, а оно не изменяется.
681. Свободно падающий мяч, ударившись об асфальт, опять подскакивает, но никогда не поднимается до начальной высоты, с которой упал. Почему?
Почему?
Потому что кинетическая энергия мяча тратится на преодоление сопротивления воздуха и сил земного тяготения.
682. Вверх подбрасывают монетку. Какие превращения энергии происходят при подъеме монетки? при ее падении? в момент удара об асфальт?
При увеличении высоты подъема монетки возрастает ее потенциальная энергия, а кинетическая убывает. В наивысшей точке потенциальная энергия максимальна, а кинетическая минимальна. При начале падения кинетическая энергия возрастает, а потенциальная убывает. В момент перед ударом кинетическая энергия максимальна, а потенциальная минимальна. При ударе происходит преобразование части энергии в тепло, а также в энергию деформации.
683. Почему при ударе об асфальт монетка нагревается?
Потому что часть энергии монетки переходит в тепловую.
Видео удалено.
| Видео (кликните для воспроизведения). |
684. В один стакан налита горячая вода, в другой – холодная вода той же массы. В каком стакане вода обладает большей внутренней энергией?
В каком стакане вода обладает большей внутренней энергией?
В стакане с горячей водой молекулы двигаются быстрее, чем в холодной. Поэтому горячая вода обладает большей внутренней энергией.
685. Приведите примеры изменения внутренней энергии тел при их сжатии.
Нагревание воздуха в поршне насоса.
686. Как меняется внутренняя энергия тел при трении? Приведите примеры.
Увеличивается. Заточка ножа на точильном камне; трение шин автомобиля при торможении.
687. Меняется ли внутренняя энергия тел при ударе? Приведите примеры.
При ударе внутренняя энергия тел увеличивается. Работа молотка; отскок мяча от пола.
688. Почему происходит изменение внутренней энергии пружины при ее сжатии?
При сжатии пружины возрастает ее потенциальная энергия. Следовательно, внутренняя энергия возрастает.
689. Происходит ли изменение внутренней энергии газа при его расширении?
При расширении газ производит работу против внешних сил, внутренняя энергия его при этом уменьшается.
690. Что происходит с внутренней энергией жидких и твердых тел при их нагревании?
Происходит увеличение внутренней энергии за счет увеличения скорости движения частиц.
691. Меняется ли внутренняя энергия льда при его таянии?
При таянии льда внутренняя энергия увеличивается за счет подвода теплоты излучением и теплопередачей.
692. Сила трения совершает над телом работу. Какие признаки свидетельствуют об изменении внутренней энергии тела?
При совершении работы трения тело нагревается, кинетическая энергия увеличивается и вызывает увеличение внутренней энергии.
Внутренняя энергия газа Основы термодинамики
Внутренняя энергия газа Первая научная теория тепловых процессов — термодинамическая Возникла при изучении оптимальных условий использования теплоты для совершения работы в середине XIX века, еще задолго до признания МКТ. В настоящее время Тепловые явления Термодинамика Молекулярно-кинетическая теория
Внутренняя энергия газа Молекулярно-кинетическая теория Термодинамика изучают — раздел физики, изучающий возможности использования внутренней энергии тел для совершения механической работы. Различными методами Одни и те же явления
Различными методами Одни и те же явления
Внутренняя энергия газа Термодинамика главное содержание выражается Устанавливается опытным путем Касаются поведения энергии два основных законах Справедливы для всех видов веществ независимо от их внутреннего строения
Внутренняя энергия газа Тепловые явления изучение МКТ Термодинамика Статистический метод Статистическая механика Термодинамический метод Использование законов термодинамики
Внутренняя энергия газа XIX век Макроскопические тела Механическая энергия Энергия, заключенная внутри самих тел Внутренняя энергия
Внутренняя энергия газа Внутренняя энергия Шайба, скользящая по льду Нагрев воды в пробирке, закрытой пробкой Переход Ek -> Eвнутренняя Переход Eвнутренняя -> Eк
Внутренняя энергия газа МКТ Внутренняя энергия Макроскопического тела Суммарная кинетическая энергия беспорядочного движения всех молекул относительно центра масс тела Потенциальная энергия взаимодействия всех молекул друг с другом (но не с молекулами других тел!!!).
Внутренняя энергия газа Внутренняя энергия Вычислить – невозможно! Одноатомный газ – газ, состоящий из отдельных атомов, а не из молекул. Инертные газы: гелий, неон, аргон и другие. Определяют значение внутренней энергии или ее изменение в зависимости от макроскопических параметров, которые можно непосредственно измерить
Внутренняя энергия газа Внутренняя энергия одноатомного идеального газа Идеальный газ – газ, молекулы которого не взаимодействуют друг с другом, то есть их Eп = 0 Для 1 атома: Число атомов: Получаем: U = Ek — универсальная газовая постоянная
Внутренняя энергия газа Внутренняя энергия одноатомного идеального газа пропорциональна абсолютной температуре: Не зависит от объема и других макроскопических параметров!!!
Внутренняя энергия газа Изменение внутренней энергии происходит только при изменении температуры:
Внутренняя энергия газа Увеличение массы m газа приводит к увеличению его внутренней энергии Зависит от рода газа, так как чем больше M, тем меньше атомов содержится в газе данной массы
Внутренняя энергия газа Если идеальный газ состоит из более сложных молекул, чем одноатомный, то: Изменяется лишь коэффициент пропорциональности между U и T. i – число степеней свободы молекулы Число степеней свободы – число возможных независимых направлений движения молекулы.
i – число степеней свободы молекулы Число степеней свободы – число возможных независимых направлений движения молекулы.
Внутренняя энергия газа Реальные газы, жидкости и твердые тела: — зависит от объема вещества, так как при изменении объема изменяется среднее расстояние между молекулами Внутренняя энергия в термодинамике в общем случае зависит не только от температуры (T), но и от объема (V). Внутренняя энергия (U) макроскопических тел однозначно определяется параметрами, характеризующими состояние этих тел: температурой (T) и объемом (V)
Задание Моль какого газа (водорода или гелия) имеет большую внутреннюю энергию при одинаковой температуре?
Внутренняя энергия газа Может изменяться: При деформации При тепловых процессах Тепловые процессы – процессы, связанные с изменением как температуры тела, так и его агрегатного состояния – плавлением или отвердеванием, испарением или конденсацией. При химических реакциях Силы взаимодействия между атомами изменяются Энергии взаимодействия атомов Характер движения и взаимодействия молекул При ядерных реакциях
Внутренняя энергия газа Способы изменения Совершение работы Теплопередача (теплообмен) Теплообмен – процесс передачи энергии от одного тела к другому без совершения работы. мера передачи энергии количество теплоты — это энергия, передаваемая телу извне в результате теплообмена.
мера передачи энергии количество теплоты — это энергия, передаваемая телу извне в результате теплообмена.
Задачи 1. В одном стакане находится горячая вода, в другом – холодная. В каком случае вода обладает большей внутренней энергией? 2. Спичка воспламеняется при трении ее головки о коробок. Объяснить это явление. 3. Объяснить возрастание скорости диффузии с повышением температуры. 4. Почему радиаторы центрального отопления ставят обычно под окнами? 5. Почему зимой на улице металл на ощупь кажется холоднее дерева? 6. В стакан налит горячий чай. Как осуществляется теплообмен между чаем и стенками стакана? 7. Приведите примеры изменения внутренней энергии тела в процессе теплообмена 8. Почему в безветрие пламя свечи устанавливается вертикально? 9. Зачем канализационные и водопроводные трубы зарывают в землю на значительную глубину? 5. 1. 1 Найдите внутреннюю энергию 5 моль водорода при 20 °С. 5. 1. 2. Как изменится внутренняя энергия 500 г кислорода при его нагревании на 15 °С.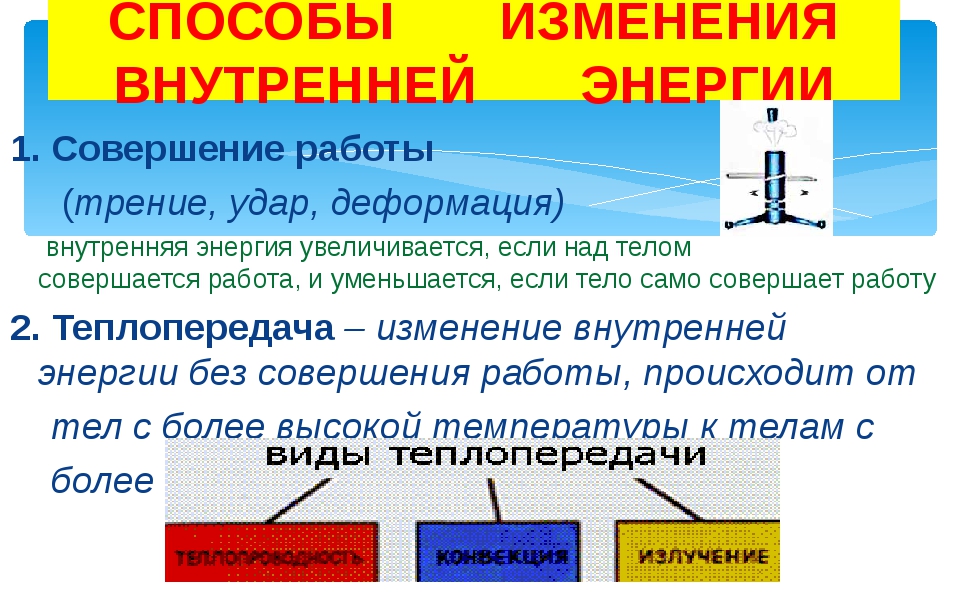
Работа как мера изменения внутренней энергии системы Древние времена человек теплота Возникла наука — термодинамика ТЕПЛОВЫЕ МАШИНЫ работа
Работа как мера изменения внутренней энергии системы Тепловая машина Джеймс Уатт (Ватт) – шотландский изобретатель, создатель универсального парового двигателя. Джеймс Уатт 19. 01. 1736 г. – 19. 08. 1819 г. Исследовал свойства водяного пара, в частности зависимость температуры насыщенного пара от давления. Детальное изучение паровой машины Ньюкомена привело его к введению в неё многих усовершенствований.
Работа как мера изменения внутренней энергии системы Схема уаттовской паровой машины двойного действия
Работа как мера изменения внутренней энергии системы Работа в механике A = F∙∆l∙cosα A – работа ∆l – перемещение тела F — сила α – угол между силой и направлением перемещения Работа совершается при действии силы на движущееся тело и равна изменении его кинетической энергии.
Работа как мера изменения внутренней энергии системы Работа в термодинамике Движение тела как целого не рассматривается, речь идет о перемещении частей макроскопического тела относительно друга. Меняется объем тела, его скорость остается равной нулю Работа в термодинамике равна изменению внутренней энергии тела
Меняется объем тела, его скорость остается равной нулю Работа в термодинамике равна изменению внутренней энергии тела
Работа как мера изменения внутренней энергии системы Работа в термодинамике F’ – сила, с которой сам газ действует на поршень; F – сила, с которой поршень действует на газ; По 3 закону Ньютона: F’=-F А’–работа, совершаемая газом; A-работа, совершаемая внешними телами над газом.
Работа как мера изменения внутренней энергии системы Работа в термодинамике A’ = p∙∆V – работа, совершаемая газом. Положительная. A = — p∙∆V – работа, совершаемая внешними телами над газом. Отрицательная.
Домашнее задание
Видео удалено.| Видео (кликните для воспроизведения). |
Источники:
- Марченко, М.Н. Проблемы теории государства и права. Учебник / М.Н. Марченко. — М.: Норма, 2017. — 415 c.
Изменение внутренней энергии происходит при
Оценка 5 проголосовавших: 1Приветствую Вас на нашем сайте. Я Артем Черных. Я уже более 6 лет работаю юрисконсультом. В настоящее время являюсь специалистом в этом направлении, хочу подсказать всем посетителям сайта как решать сложные и не очень задачи.
Я Артем Черных. Я уже более 6 лет работаю юрисконсультом. В настоящее время являюсь специалистом в этом направлении, хочу подсказать всем посетителям сайта как решать сложные и не очень задачи.
Все материалы для сайта собраны и тщательно переработаны с целью донести как можно доступнее всю нужную информацию. Однако чтобы применить все, описанное на сайте всегда необходима консультация с профессионалами.
Изменение внутренней энергии — Энциклопедия по машиностроению XXL
Какая доля теплоты, подведенной к I кг кислорода в изобарном процессе, затрачивается на изменение внутренней энергии [c.19]Общий метод расчета по Л, s-диаграмме состоит в следующем. По известным параметрам наносится начальное состояние рабочего тела, затем проводится линия процесса и определяются его параметры в конечном состоянии. Далее вычисляется изменение внутренней энергии, определяются количества теплоты и работы в заданном процессе. [c.38]
[c.38]
Перегретый пар расширяется в турбине по адиабате от начального давления 8 МПа и температуры 500 °С до р2= 100 кПа. Определить конечное состояние пара, изменение внутренней энергии и работу расширения. [c.43]
Для идеального газа изменение внутренней энергии в адиабатном процессе ui — ui = l вычисляется по формуле (4.20), поэтому [c.46]
Таким процессом является, например, изотермическое расширение идеального газа, находящегося в тепловом контакте с горячим источником. Так как в этом процессе изменение внутренней энергии равно нулю, то согласно первому закону термодинамики, работа, совершенная при расширении газа, равна количеству теплоты, переданной от горячего источника. Таким образом, имеет место полное превращение теплоты в работу. Но это не противоречит второму закону термодинамики, который утверждает, что невозможен процесс, единственным конечным результатом которого будет превращение в работу теплоты, извлеченной от горячего источника. Действительно, в конце изотермического процесса газ занимает объем больше, чем он занимал вначале. Изменение состояния газа и является компенсацией превращения теплоты в работу.
[c.209]
Действительно, в конце изотермического процесса газ занимает объем больше, чем он занимал вначале. Изменение состояния газа и является компенсацией превращения теплоты в работу.
[c.209]
Изменение внутренней энергии [c.210]
С макроскопической точки зрения энергию системы, соответствующую ее массе, называют внутренней энергией. Внутренняя энергия — это свойство системы, которое полностью определяется ее состоянием и известно как функция состояния . Изменение внутренней энергии при переходе системы из одного состояния [c.30]
Так как измеряет скорость изменения внутренней энергии с изменением температуры при постоянном объеме, то приближенное значение С может быть получено прямым дифферент рованием значения внутренней энергии (табл. 1) по температуре Теплоемкости идеальных газов при постоянном объеме и постоянном давлении приведены в табл. 2. [c.33]
Изменение внутренней энергии системы удобнее всего определять с помощью теплоемкости при постоянном объеме, вычисляемой по уравнению (1-1). Для процесса при постоянном объеме
[c.40]
Для процесса при постоянном объеме
[c.40]
Работа, выполненная при течении процесса в закрытой системе при постоянном объеме, равна О, так как любые перемещения отсутствуют. Следовательно, теплота, добавленная системе при течении процесса при постоянном объеме, равна изменению внутренней энергии. Путем сочетания уравнений (1-5) и (1-14) получаем [c.40]
Для жидкостей и твердых тел величина v/ p обычно бывает незначительна по отношению к изменению внутренней энергии, тогда [c.41]
Так как изменение внутренней энергии при течении изотермического процесса в системе из твердого тела, жидкости или идеального газа практически равно нулю, то теплота, сообщенная системе, равна произведенной работе. [c.43]
Работу и изменение внутренней энергии можно легко вычислить, определив отношение конечной температуры к начальной с помощью уравнения (1-47) и подставив его численное значение в уравнение (1-31). [c.45]
[c.45]
Пример 2. Вычислить произведенную работу, передачу теплоты и изменение внутренней энергии для каждого из следующих процессов. [c.46]
Для идеального газа с независимой от температуры С, = = 3 брит. тепл. ед./(фунт-моль °R) [3 тл1 моль ° ] изменение внутренней энергии составит [c.49]
В процессе при постоянном объеме не происходит никаких перемещений и работа равна нулю. Перенесенная теплота в этом случае равна изменению внутренней энергии [c.51]
Определить количество переданной теплоты, выполненной работы, изменение внутренней энергии и изменение энтальпии при сжатии 1 моля идеального газа от давления 1 атм при следующих условиях [c.67]
Изменение внутренней энергии может быть выражено в функции изменения и Z путем нахождения частных производных [c.130]
Согласно первому закону термодинамики, замкнутая система может испытывать изменение внутренней энергии только в результате обмена теплотой и работой с окружающей средой.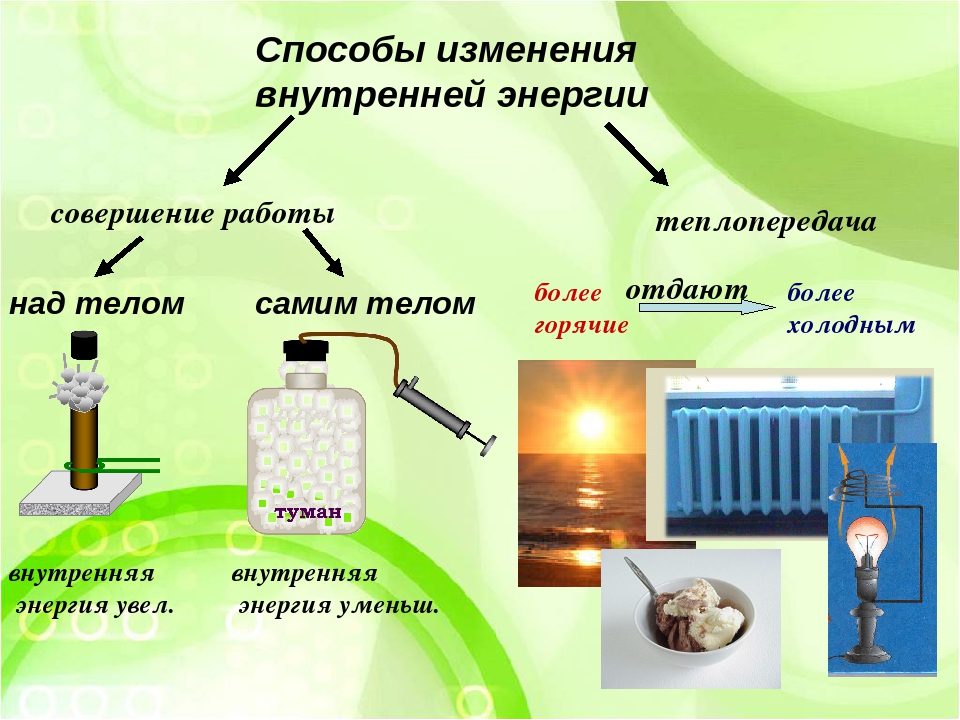 Так как для этой системы изменение объема указывает на передачу энергии в форме работы, то второе слагаемое уравнения (4-33) можно отождествить с работой, обратимо выполненной системой. Ограничение в виде обратимости необходимо, так как коэффициент при dv представляет собой свойство системы, а именно — давление системы
[c.131]
Так как для этой системы изменение объема указывает на передачу энергии в форме работы, то второе слагаемое уравнения (4-33) можно отождествить с работой, обратимо выполненной системой. Ограничение в виде обратимости необходимо, так как коэффициент при dv представляет собой свойство системы, а именно — давление системы
[c.131]
Общее изменение внутренней энергии замкнутой системы постоянного состава может быть выражено в функции изменений температуры и объема с помощью уравнения (5-2) для полного дифференциала [c.152]
Окончательно выражение для общего изменения внутренней энергии в функции р, V, Т я Со может быть получено подстановкой уравнений (5-4) и (5-10) в уравнение (5-3) [c.153]
При использовании закона идеального газа для вычисления изменений термодинамических функций получаются простые соотношения, которые выражают внутренние свойства, обусловленные незначительностью межмолекулярных сил и молекулярного объема.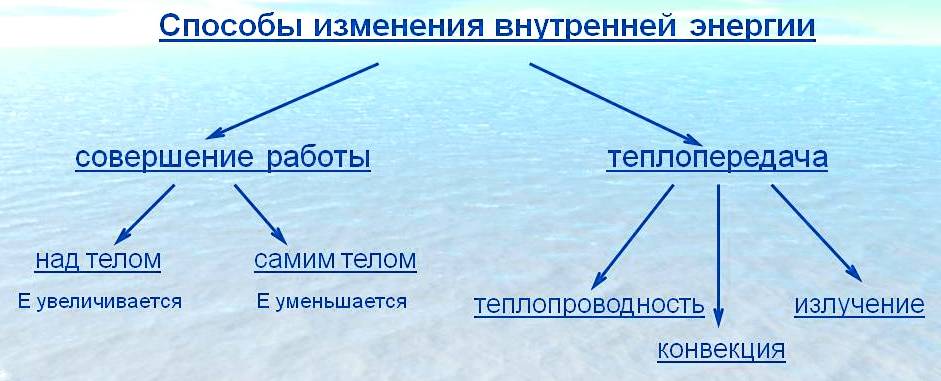 Например, чтобы вычислить изменение внутренней энергии, согласно уравнению (5-11), необходимо вычислить частную др
[c.164]
Например, чтобы вычислить изменение внутренней энергии, согласно уравнению (5-11), необходимо вычислить частную др
[c.164]
Таким образом, изменение внутренней энергии идеального газа не зависит от давления и объема и является функцией только температуры. [c.164]
Изменение внутренней энергии может быть вычислено из определения энтальпии [c.175]
В начальный момент тело А имеет внутреннюю энергию температуру и величина W для него будет Wa тело В имеет внутреннюю энергию Eg, температуру Гд и величина W для него будет Wq. Для бесконечно малого количества теплоты, переданного от тела А к телу В, изменение внутренней энергии тела А может быть вычислено согласно уравнению (6-1) [c.190]
Изменение внутренней энергии тела В [c.190]
Изменение внутренней энергии части А может быть выражено с помощью уравнения (6-1) [c.192]
Термодинамическая эффективность такого цикла определяется отношением совершенной работы к поглош,енной теплоте. После каждого полного цикла система возвращается к своему первоначальному состоянию, так что изменение внутренней энергии работающего газа для одного цикла равно нулю. Баланс энергии для одного цикла примет вид
[c.197]
После каждого полного цикла система возвращается к своему первоначальному состоянию, так что изменение внутренней энергии работающего газа для одного цикла равно нулю. Баланс энергии для одного цикла примет вид
[c.197]
Для получения численных значений эмпирических температур следует обратиться к первому и второму законам термодинамики. Первый закон термодинамики просто констатирует сохранение энергии при условии, что учитывается не только работа, совершаемая над системой, но и обмен теплом через стенки с окружающей средой. Если система в остальных отношениях изолирована, то внутренняя энергия и, представляющая собой экстенсивную величину, может только увеличиваться при совершении над системой некоторой работы. Однако если система термически не изолирована и в результате некоторого процесса переходит из термодинамического состояния А в другое состояние В, то работа совершаемая над системой, разумеется, зависит от того, каким способом система осуществляет переход из состояния А в состояние В. С другой стороны, увеличение внутренней энергии равно и в—и А независимо от способа совершения работы. Следовательно, для термически не изолированной системы увеличение внутренней энергии и в — и а отлично от Разность Q мы назовем количеством теплоты, которая, таким образом, служит мерой отклонения от адиабатических условий. Следовательно, для любого термодинамического процесса, начинающегося в состоянии А и завершающегося в состоянии В, изменение внутренней энергии определяется выражением
[c.15]
С другой стороны, увеличение внутренней энергии равно и в—и А независимо от способа совершения работы. Следовательно, для термически не изолированной системы увеличение внутренней энергии и в — и а отлично от Разность Q мы назовем количеством теплоты, которая, таким образом, служит мерой отклонения от адиабатических условий. Следовательно, для любого термодинамического процесса, начинающегося в состоянии А и завершающегося в состоянии В, изменение внутренней энергии определяется выражением
[c.15]
При незначительных объемных изменениях тепловой эффект полиморфизма L можно считать следствием изменения внутренней энергии [c.14]
Изменение внутренней энергии тела не зависит от пути процесса и целиком определяется начальным и конечным состоянием, т. е. [c.54]
Это наглядно иллюстрируется рис. 5-1. Во всех процессах 1а2, 1Ь2, 1с2 изменение внутренней энергии будет одно и то же. [c.55]
[c.55]
В круговых процессах изменение внутренней энергии будет равно нулю [c.55]
Если в ру-диаграмме (рис. 5-3) между изотермами Г) и Гг изобразить ряд произвольных процессов 1-2, 3-4, 5-6, которые имеют различные начальные и конечные объемы и давления, то изменение внутренней энергии идеального газа у всех этих процессов будет одинаковым [c.56]
Сумма изменений внутренней кинетической и внутренней потенциальной энергии представляет полное изменение внутренней энергии du. [c.62]
Полученное уравнение является математическим выражением первого закона термодинамики. Оно формулируется так изменение внутренней энергии термодинамической системы равно алгебраической сумме полученной системой энергии в форме теплоты dq и совершенной ею внешней работы dl, или подведенная к рабочему телу энергия в форме теплоты расходуется на изменение внутренней энергии тела и на совершение телом внешней работы. [c.63]
[c.63]
Изменение внутренней энергии водяного пара при 11 = onst [c.39]
Из уравнений (1-14) и (1-25) видно, что изменение внутренней энергии идеального газа всегда равно j jiT и не зависит от какого-либо изменения объема или давления оно равно нулю, если начальная и конечная температуры одинаковы. Другими словами, внутренняя энергия идеального газа является функцией только температуры. [c.42]
Численные значения поступательных, вращательных, колебательных и электронных энергетических уровней, определенных по спектроскопическим данным или вычисленных с помощью квантовой механики, обычно выражают относительно самого низкого или основного уровня молекулы. Если такие значения используют для вычисления внутренней энергии, полученная внутренняя энергия представляет собой избыточную энергию относительно основного состояния системы, когда все частицы находятся на самом низком энергетическом уровне при температуое абсолютного нуля. Для процессов, в которых общее число частиц данных молекулярных объектов остается постоянным, изменения внутренней энергии могут быть вычислены без сведений об основном состоянии. Однако если число частиц данных молекулярных объектов изменяется, как в химической реакции, то для вычисления изменения внутренней энергии процесса должна быть известна разность между основными состояниями различных соединений.
[c.115]
Для процессов, в которых общее число частиц данных молекулярных объектов остается постоянным, изменения внутренней энергии могут быть вычислены без сведений об основном состоянии. Однако если число частиц данных молекулярных объектов изменяется, как в химической реакции, то для вычисления изменения внутренней энергии процесса должна быть известна разность между основными состояниями различных соединений.
[c.115]
Согласно правилу фаз Гиббса, состояние замкнутой однофазной системы фиксированного состава может быть полностью определено двумя независимыми переменными. Следовательно, изменение внутренней энергии такой H TeNibi можно выразить мате-матетически как функцию изменения температуры и объема [c.130]
Для полностью обратимых процессов в замкнутой системе одна часть изменения внутренней энергии, представленная полезной работой и работой, выполненной против атмосферного давления Poi o — способна совершить работу над окружающей средой, в то время как другая часть, представленная произведением ГдД5, переходит в виде теплоты к теплоприемнику и полностью непригодна для совершения работы любого вида. Поэтому произведение Tf,AS иногда называют рассеянной энергией .
[c.203]
Поэтому произведение Tf,AS иногда называют рассеянной энергией .
[c.203]
Изменение энергии выделенного элементарного объема ЛУп возникает ib связи с притоком тепла и работой внешних сил (массовых и поверхностных). Причем это изменение проявится в увеличении кинетической энергии среднего и пульсационного движения и в изменении внутренней энергии элемента. Учитывая, что для дисперсных потоков теплоносителей характерны в основном умеренные скорости течения, пренебрегаем изменением давления и кинетической энергии компонетов. Полагая также, что внутренние источники или стоки энергий отсутствуют, в соответствии с первым законом термодинамики для изобарных процессов получим, что количество переданного элементу ДУц за время Лт тепла AQa равно изменению энтальпии его компонентов [c.40]
15.1 Первый закон термодинамики – College Physics
Метаболизм человека и первый закон термодинамики
Метаболизм человека — это преобразование пищи в теплопередачу, работу и накопление жира. Метаболизм — интересный пример действия первого закона термодинамики. Теперь мы еще раз взглянем на эти темы через первый закон термодинамики. Рассматривая тело как интересующую нас систему, мы можем использовать первый закон для изучения теплопередачи, выполнения работы и внутренней энергии в различных видах деятельности, от сна до тяжелых упражнений.Каковы некоторые из основных характеристик теплообмена, совершения работы и энергии в организме? Во-первых, температура тела обычно поддерживается постоянной за счет передачи тепла в окружающую среду. Это означает отрицательное значение. Другой факт заключается в том, что тело обычно воздействует на внешний мир. Это означает положительное значение. В таких ситуациях тело теряет внутреннюю энергию, т.к. оно отрицательное.
Метаболизм — интересный пример действия первого закона термодинамики. Теперь мы еще раз взглянем на эти темы через первый закон термодинамики. Рассматривая тело как интересующую нас систему, мы можем использовать первый закон для изучения теплопередачи, выполнения работы и внутренней энергии в различных видах деятельности, от сна до тяжелых упражнений.Каковы некоторые из основных характеристик теплообмена, совершения работы и энергии в организме? Во-первых, температура тела обычно поддерживается постоянной за счет передачи тепла в окружающую среду. Это означает отрицательное значение. Другой факт заключается в том, что тело обычно воздействует на внешний мир. Это означает положительное значение. В таких ситуациях тело теряет внутреннюю энергию, т.к. оно отрицательное.
Теперь рассмотрим последствия еды. Прием пищи увеличивает внутреннюю энергию тела за счет добавления химической потенциальной энергии (это неромантичный взгляд на хороший стейк).Тело усваивает всю пищу, которую мы потребляем. По сути, обмен веществ представляет собой процесс окисления, при котором высвобождается химическая потенциальная энергия пищи. Это означает, что потребление пищи осуществляется в форме работы. Энергия пищи сообщается в специальной единице, известной как калория. Эта энергия измеряется путем сжигания пищи в калориметре, так определяются единицы измерения.
По сути, обмен веществ представляет собой процесс окисления, при котором высвобождается химическая потенциальная энергия пищи. Это означает, что потребление пищи осуществляется в форме работы. Энергия пищи сообщается в специальной единице, известной как калория. Эта энергия измеряется путем сжигания пищи в калориметре, так определяются единицы измерения.
В химии и биохимии одна калория ( пишется строчной буквой с) определяется как энергия (или теплопередача), необходимая для повышения температуры одного грамма чистой воды на один градус Цельсия.Диетологи и люди, следящие за весом, обычно используют диетических калорий, которые часто называют калориями (пишется с большой буквы C). Одна пищевая калория — это энергия, необходимая для повышения температуры одного килограммов воды на один градус Цельсия. Это означает, что для химика одна диетическая калория равна одной килокалории, и нужно быть осторожным, чтобы не путать их.
Опять же, рассмотрим внутреннюю энергию, потерянную телом. Эта внутренняя энергия может быть использована в трех направлениях: для теплопередачи, для выполнения работы и для накопления жира (крошечная часть также идет на восстановление и рост клеток).Теплообмен и совершение работы забирают внутреннюю энергию из организма, а пища возвращает ее. Если вы едите только нужное количество пищи, то ваша средняя внутренняя энергия остается постоянной. Все, что вы теряете при теплопередаче и выполнении работы, заменяется едой, так что в долгосрочной перспективе, если вы постоянно переедаете, это всегда положительно, и ваше тело сохраняет эту дополнительную внутреннюю энергию в виде жира. Обратное верно, если вы едите слишком мало. Если он отрицательный в течение нескольких дней, то организм усваивает собственный жир для поддержания температуры тела и выполнения работы, требующей энергии от тела.Этот процесс заключается в том, как диета приводит к потере веса.
Эта внутренняя энергия может быть использована в трех направлениях: для теплопередачи, для выполнения работы и для накопления жира (крошечная часть также идет на восстановление и рост клеток).Теплообмен и совершение работы забирают внутреннюю энергию из организма, а пища возвращает ее. Если вы едите только нужное количество пищи, то ваша средняя внутренняя энергия остается постоянной. Все, что вы теряете при теплопередаче и выполнении работы, заменяется едой, так что в долгосрочной перспективе, если вы постоянно переедаете, это всегда положительно, и ваше тело сохраняет эту дополнительную внутреннюю энергию в виде жира. Обратное верно, если вы едите слишком мало. Если он отрицательный в течение нескольких дней, то организм усваивает собственный жир для поддержания температуры тела и выполнения работы, требующей энергии от тела.Этот процесс заключается в том, как диета приводит к потере веса.
Жизнь не всегда так проста, как знает любой сидящий на диете. Организм накапливает жир или усваивает его, только если потребление энергии изменяется в течение нескольких дней. После того, как вы сели на основную диету, следующая будет менее успешной, потому что ваше тело меняет реакцию на низкое потребление энергии. Ваш основной уровень метаболизма (BMR) — это скорость, с которой пища преобразуется в теплопередачу и совершается работа, когда тело находится в полном покое. Организм регулирует скорость основного обмена, чтобы частично компенсировать переедание или недоедание.Тело снизит скорость метаболизма, а не устранит собственный жир, чтобы заменить потерянное потребление пищи. Вы будете легче остывать и чувствовать себя менее энергичным в результате более низкой скорости метаболизма, и вы не будете терять вес так быстро, как раньше. Упражнения помогают похудеть, потому что они производят как теплопередачу от вашего тела, так и работу, а также повышают скорость метаболизма, даже когда вы находитесь в состоянии покоя. Похудению способствует также довольно низкая эффективность преобразования внутренней энергии тела в работу, так что потеря внутренней энергии в результате выполнения работы намного больше, чем выполненная работа.
После того, как вы сели на основную диету, следующая будет менее успешной, потому что ваше тело меняет реакцию на низкое потребление энергии. Ваш основной уровень метаболизма (BMR) — это скорость, с которой пища преобразуется в теплопередачу и совершается работа, когда тело находится в полном покое. Организм регулирует скорость основного обмена, чтобы частично компенсировать переедание или недоедание.Тело снизит скорость метаболизма, а не устранит собственный жир, чтобы заменить потерянное потребление пищи. Вы будете легче остывать и чувствовать себя менее энергичным в результате более низкой скорости метаболизма, и вы не будете терять вес так быстро, как раньше. Упражнения помогают похудеть, потому что они производят как теплопередачу от вашего тела, так и работу, а также повышают скорость метаболизма, даже когда вы находитесь в состоянии покоя. Похудению способствует также довольно низкая эффективность преобразования внутренней энергии тела в работу, так что потеря внутренней энергии в результате выполнения работы намного больше, чем выполненная работа. Однако следует отметить, что живые системы не находятся в тепловом равновесии.
Однако следует отметить, что живые системы не находятся в тепловом равновесии.
Тело дает нам прекрасное указание на то, что многие термодинамические процессы необратимы . Необратимый процесс может идти в одном направлении, но не в обратном, при заданном наборе условий. Например, хотя телесный жир может быть преобразован для выполнения работы и передачи тепла, работа, совершаемая телом, и теплопередача в него не могут быть преобразованы в телесный жир.В противном случае мы могли бы пропустить обед, загорая или спускаясь по лестнице. Другим примером необратимого термодинамического процесса является фотосинтез. Этот процесс представляет собой поглощение растениями одной формы энергии — света — и преобразование ее в химическую потенциальную энергию. Оба приложения первого закона термодинамики проиллюстрированы на рис. 4. Большое преимущество законов сохранения, таких как первый закон термодинамики, состоит в том, что они точно описывают начало и конец сложных процессов, таких как метаболизм и фотосинтез, безотносительно к осложнения между ними. В таблице 1 представлено краткое описание терминов, относящихся к первому закону термодинамики.
В таблице 1 представлено краткое описание терминов, относящихся к первому закону термодинамики.
Первый закон термодинамики – Основы тепла, света и звука
Люмен Обучение
Цели обучения
К концу этого раздела вы сможете:
- Дайте определение первому закону термодинамики.
- Опишите, как сохранение энергии связано с первым законом термодинамики.
- Определить случаи применения первого закона термодинамики в повседневных ситуациях, включая биологический метаболизм.

- Рассчитайте изменения внутренней энергии системы после учета теплопередачи и выполненной работы.
Если нас интересует, как теплопередача преобразуется в работу, то важным является принцип сохранения энергии.Первый закон термодинамики применяет принцип сохранения энергии к системам, в которых передача тепла и совершение работы являются методами передачи энергии в систему и из нее. Первый закон термодинамики гласит, что изменение внутренней энергии системы равно чистому переносу тепла в систему за вычетом чистой работы, выполненной системой. В форме уравнения первый закон термодинамики выглядит так: Δ U = Q − Вт .
Здесь Δ U — изменение внутренней энергии U системы. Q — это чистая теплота, переданная в систему , то есть Q — это сумма всей теплопередачи в систему и из нее. W — это чистая работа, выполненная системой. Мы используем следующие соглашения о знаках: если Q положительно, то в систему идет чистый теплообмен; если W положительно, то система совершает чистую работу.Таким образом, положительный Q добавляет энергию в систему, а положительный W забирает энергию из системы. Таким образом, Δ U = Q − W . Обратите также внимание, что если в систему передается больше тепла, чем совершается работа, разница сохраняется в виде внутренней энергии. Хорошим примером этого являются тепловые двигатели — в них происходит передача тепла, чтобы они могли совершать работу. (См. рис. 2.) Теперь мы рассмотрим Q , W и Δ U .
Установление связей: закон термодинамики и закон сохранения энергии
Первый закон термодинамики на самом деле является законом сохранения энергии, сформулированным в форме, наиболее полезной в термодинамике. Первый закон устанавливает связь между теплопередачей, выполненной работой и изменением внутренней энергии системы.
Тепло
Q и Работа Вт Теплопередача ( Q ) и выполнение работы ( W ) – это два повседневных способа подачи энергии в систему или ее вывода из системы. Процессы совсем другие. Теплопередача, менее организованный процесс, обусловлена разницей температур. Работа, вполне организованный процесс, включает в себя действие макроскопической силы на расстоянии. Тем не менее, теплота и работа могут давать одинаковые результаты. Например, и то, и другое может вызвать повышение температуры.Передача тепла в систему, например, когда солнце нагревает воздух в велосипедной шине, может повысить его температуру, и, таким образом, над системой может совершаться работа, например, когда велосипедист накачивает воздух в шину. После того, как произошло повышение температуры, невозможно сказать, было ли оно вызвано теплопередачей или совершением работы. Эта неопределенность является важным моментом. Теплопередача и работа — это энергия в пути — ни одна из них не хранится как таковая в системе. Однако и то, и другое может изменить внутреннюю энергию U системы.Внутренняя энергия — это форма энергии, совершенно отличная от теплоты или работы.
Однако и то, и другое может изменить внутреннюю энергию U системы.Внутренняя энергия — это форма энергии, совершенно отличная от теплоты или работы.
Внутренняя энергия
U Мы можем думать о внутренней энергии системы двумя разными, но непротиворечивыми способами. Первый — это атомно-молекулярный взгляд, который исследует систему в атомном и молекулярном масштабе. Внутренняя энергия U системы представляет собой сумму кинетической и потенциальной энергий ее атомов и молекул. Напомним, что кинетическая плюс потенциальная энергия называется механической энергией.Таким образом, внутренняя энергия представляет собой сумму атомной и молекулярной механической энергии. Поскольку невозможно уследить за всеми отдельными атомами и молекулами, мы должны иметь дело со средними значениями и распределениями. Второй способ представления внутренней энергии системы — ее макроскопические характеристики, которые очень похожи на средние атомные и молекулярные значения.
Макроскопически мы определяем изменение внутренней энергии Δ U как соответствующее первому закону термодинамики: Δ U = Q − Вт .
Многие детальные эксперименты подтвердили, что Δ U = Q − W , где Δ U — это изменение полной кинетической и потенциальной энергии всех атомов и молекул в системе. Экспериментально установлено также, что внутренняя энергия U системы зависит только от состояния системы, а не от того, как она достигла этого состояния . В частности, установлено, что U является функцией нескольких макроскопических величин (например, давления, объема и температуры), не зависящих от прошлой истории, например, от наличия теплопередачи или выполненной работы.Эта независимость означает, что если мы знаем состояние системы, мы можем рассчитать изменения ее внутренней энергии U по нескольким макроскопическим переменным.
Создание связей: макроскопические и микроскопические
В термодинамике мы часто используем макроскопическую картину при расчетах поведения системы, в то время как атомарная и молекулярная картина дает основные объяснения в терминах средних значений и распределений. Мы еще увидим это в следующих разделах этой главы.Например, в теме энтропии расчеты будут производиться с использованием атомарно-молекулярного представления.
Мы еще увидим это в следующих разделах этой главы.Например, в теме энтропии расчеты будут производиться с использованием атомарно-молекулярного представления.
Чтобы получить лучшее представление о внутренней энергии системы, давайте рассмотрим систему, переходящую из состояния 1 в состояние 2. Система имеет внутреннюю энергию U 1 в состоянии 1, и она имеет внутреннюю энергия U 2 в состоянии 2, независимо от того, как она попала в любое состояние. Таким образом, изменение внутренней энергии Δ U = U 2 − U 1 не зависит от того, что вызвало изменение.Другими словами, Δ U не зависит от пути . Под путем мы подразумеваем способ добраться из начальной точки в конечную. Почему важна эта независимость? Обратите внимание, что Δ U = Q − Вт . И Q , и W зависят от пути , а Δ U — нет. Эта независимость от пути означает, что внутреннюю энергию U легче учитывать, чем передачу тепла или выполненную работу.
Пример 1.Расчет изменения внутренней энергии: одно и то же изменение в
U производится двумя разными процессами- Предположим, что системе передается теплота 40,00 Дж, в то время как система совершает работу 10,00 Дж. Затем из системы передается 25,00 Дж тепла, а над системой совершается работа 4,00 Дж. Каково чистое изменение внутренней энергии системы?
- Как изменится внутренняя энергия системы, если из (из) системы будет передано 150,00 Дж теплоты и 159.00 Дж работы совершается в системе? (См. рис. 3).

Стратегия
В части 1 мы должны сначала найти чистую теплопередачу и чистую работу, выполненную по данной информации. Затем можно использовать первый закон термодинамики (Δ U = Q − Вт ), чтобы найти изменение внутренней энергии. В части (b) даны чистая теплопередача и проделанная работа, поэтому уравнение можно использовать напрямую.
Решение для части 1
Чистая теплопередача представляет собой теплопередачу в систему за вычетом теплопередачи из системы, или
Q = 40.00 Дж − 25,00 Дж = 15,00 Дж.
Аналогично, общая работа равна работе, выполненной системой, за вычетом работы, выполненной системой, или
.Вт = 10,00 Дж − 4,00 Дж = 6,00 Дж.
Таким образом, изменение внутренней энергии определяется первым законом термодинамики:
Δ U = Q − Вт = 15,00 Дж − 6,00 Дж = 9,00 Дж.
Мы также можем найти изменение внутренней энергии для каждого из двух шагов. Сначала рассмотрим 40,00 Дж теплопередачи в и 10.00 Дж работы, или Δ U 1 = Q 1 − Вт 1 = 40,00 Дж — 10,00 Дж = 30,00 Дж.
Сначала рассмотрим 40,00 Дж теплопередачи в и 10.00 Дж работы, или Δ U 1 = Q 1 − Вт 1 = 40,00 Дж — 10,00 Дж = 30,00 Дж.
Теперь рассмотрим 25,00 Дж теплопередачи на выходе и 4,00 Дж работы на входе, или
.Δ U 2 = Q 2 − Вт 2 = –25,00 Дж −(−4,00 Дж) = –21,00 Дж. 7 9000 Дж.
Общее изменение представляет собой сумму этих двух шагов, или Δ U = Δ U 1 + Δ U 2 = 30.00 Дж + (-21,00 Дж) = 9,00 Дж.
Обсуждение первой части
Независимо от того, смотрите ли вы на процесс в целом или разбиваете его на этапы, изменение внутренней энергии одинаково.
Решение для части 2
Здесь чистая теплопередача и полная работа даны непосредственно как Q = –150,00 Дж и Вт = –159,00 Дж, так что
Δ U = Q – Вт = –150,00 Дж –(−159,00 Дж) = 9,00 Дж.
Обсуждение части 2
Совершенно другой процесс в части 2 дает те же 9.00-Дж изменение внутренней энергии, как в части 1. Обратите внимание, что изменение в системе в обеих частях связано с Δ U , а не с отдельными вовлеченными Q с или Вт с. Система заканчивается в том же состоянии в обеих частях. Части 1 и 2 представляют два разных пути, по которым система должна следовать между одними и теми же начальной и конечной точками, и изменение внутренней энергии для каждого одинаково — оно не зависит от пути.
Метаболизм человека и первый закон термодинамики
Метаболизм человека — это превращение пищи в теплопередачу, работу и накопление жира.Метаболизм — интересный пример действия первого закона термодинамики. Теперь мы еще раз взглянем на эти темы через первый закон термодинамики. Рассматривая тело как интересующую нас систему, мы можем использовать первый закон для изучения теплопередачи, выполнения работы и внутренней энергии в различных видах деятельности, от сна до тяжелых упражнений. Каковы некоторые из основных характеристик теплообмена, совершения работы и энергии в организме? Во-первых, температура тела обычно поддерживается постоянной за счет передачи тепла в окружающую среду.Это означает, что Q является отрицательным. Другой факт заключается в том, что тело обычно воздействует на внешний мир. Это означает, что W положительный. В таких ситуациях тело теряет внутреннюю энергию, поскольку Δ U = Q − Вт отрицательно.
Каковы некоторые из основных характеристик теплообмена, совершения работы и энергии в организме? Во-первых, температура тела обычно поддерживается постоянной за счет передачи тепла в окружающую среду.Это означает, что Q является отрицательным. Другой факт заключается в том, что тело обычно воздействует на внешний мир. Это означает, что W положительный. В таких ситуациях тело теряет внутреннюю энергию, поскольку Δ U = Q − Вт отрицательно.
Теперь рассмотрим последствия еды. Прием пищи увеличивает внутреннюю энергию тела за счет добавления химической потенциальной энергии (это неромантичный взгляд на хороший стейк). Тело усваивает всю пищу, которую мы потребляем.По сути, обмен веществ представляет собой процесс окисления, при котором высвобождается химическая потенциальная энергия пищи. Это означает, что потребление пищи осуществляется в форме работы. Энергия пищи сообщается в специальной единице, известной как калория. Эта энергия измеряется путем сжигания пищи в калориметре, так определяются единицы измерения.
Эта энергия измеряется путем сжигания пищи в калориметре, так определяются единицы измерения.
В химии и биохимии одна калория ( пишется строчной буквой с) определяется как энергия (или теплопередача), необходимая для повышения температуры одного грамма чистой воды на один градус Цельсия.Диетологи и люди, следящие за весом, обычно используют диетических калорий, которые часто называют калориями (пишется с большой буквы C). Одна пищевая калория — это энергия, необходимая для повышения температуры одного килограммов воды на один градус Цельсия. Это означает, что для химика одна диетическая калория равна одной килокалории, и нужно быть осторожным, чтобы не путать их.
Опять же, рассмотрим внутреннюю энергию, потерянную телом. Эта внутренняя энергия может быть использована в трех направлениях: для теплопередачи, для выполнения работы и для накопления жира (крошечная часть также идет на восстановление и рост клеток).Теплообмен и совершение работы забирают внутреннюю энергию из организма, а пища возвращает ее. Если вы едите только нужное количество пищи, то ваша средняя внутренняя энергия остается постоянной. Все, что вы теряете при теплопередаче и выполнении работы, заменяется пищей, так что в долгосрочной перспективе Δ U = 0. Если вы постоянно переедаете, то Δ U всегда положительна, и ваше тело откладывает эту дополнительную внутреннюю энергию в виде жира. Обратное верно, если вы едите слишком мало. Если Δ U отрицателен в течение нескольких дней, то организм метаболизирует собственный жир для поддержания температуры тела и выполнения работы, забирающей энергию у организма.Этот процесс заключается в том, как диета приводит к потере веса.
Если вы едите только нужное количество пищи, то ваша средняя внутренняя энергия остается постоянной. Все, что вы теряете при теплопередаче и выполнении работы, заменяется пищей, так что в долгосрочной перспективе Δ U = 0. Если вы постоянно переедаете, то Δ U всегда положительна, и ваше тело откладывает эту дополнительную внутреннюю энергию в виде жира. Обратное верно, если вы едите слишком мало. Если Δ U отрицателен в течение нескольких дней, то организм метаболизирует собственный жир для поддержания температуры тела и выполнения работы, забирающей энергию у организма.Этот процесс заключается в том, как диета приводит к потере веса.
Жизнь не всегда так проста, как знает любой сидящий на диете. Организм накапливает жир или усваивает его, только если потребление энергии изменяется в течение нескольких дней. После того, как вы сели на основную диету, следующая будет менее успешной, потому что ваше тело меняет реакцию на низкое потребление энергии. Ваш основной уровень метаболизма (BMR) — это скорость, с которой пища преобразуется в теплопередачу и совершается работа, когда тело находится в полном покое. Организм регулирует скорость основного обмена, чтобы частично компенсировать переедание или недоедание.Тело снизит скорость метаболизма, а не устранит собственный жир, чтобы заменить потерянное потребление пищи. Вы будете легче остывать и чувствовать себя менее энергичным в результате более низкой скорости метаболизма, и вы не будете терять вес так быстро, как раньше. Упражнения помогают похудеть, потому что они производят как теплопередачу от вашего тела, так и работу, а также повышают скорость метаболизма, даже когда вы находитесь в состоянии покоя. Похудению способствует также довольно низкая эффективность преобразования внутренней энергии тела в работу, так что потеря внутренней энергии в результате выполнения работы намного больше, чем выполненная работа.Однако следует отметить, что живые системы не находятся в тепловом равновесии.
Ваш основной уровень метаболизма (BMR) — это скорость, с которой пища преобразуется в теплопередачу и совершается работа, когда тело находится в полном покое. Организм регулирует скорость основного обмена, чтобы частично компенсировать переедание или недоедание.Тело снизит скорость метаболизма, а не устранит собственный жир, чтобы заменить потерянное потребление пищи. Вы будете легче остывать и чувствовать себя менее энергичным в результате более низкой скорости метаболизма, и вы не будете терять вес так быстро, как раньше. Упражнения помогают похудеть, потому что они производят как теплопередачу от вашего тела, так и работу, а также повышают скорость метаболизма, даже когда вы находитесь в состоянии покоя. Похудению способствует также довольно низкая эффективность преобразования внутренней энергии тела в работу, так что потеря внутренней энергии в результате выполнения работы намного больше, чем выполненная работа.Однако следует отметить, что живые системы не находятся в тепловом равновесии.
Тело дает нам прекрасное указание на то, что многие термодинамические процессы необратимы . Необратимый процесс может идти в одном направлении, но не в обратном, при заданном наборе условий. Например, хотя телесный жир может быть преобразован для выполнения работы и передачи тепла, работа, совершаемая телом, и теплопередача в него не могут быть преобразованы в телесный жир. В противном случае мы могли бы пропустить обед, загорая или спускаясь по лестнице.Другим примером необратимого термодинамического процесса является фотосинтез. Этот процесс представляет собой поглощение растениями одной формы энергии — света — и преобразование ее в химическую потенциальную энергию. Оба приложения первого закона термодинамики проиллюстрированы на рис. 4. Большое преимущество законов сохранения, таких как первый закон термодинамики, состоит в том, что они точно описывают начало и конец сложных процессов, таких как метаболизм и фотосинтез, безотносительно к осложнения между ними. В Таблице 1 представлена сводка терминов, относящихся к первому закону термодинамики.
В Таблице 1 представлена сводка терминов, относящихся к первому закону термодинамики.
| Таблица 1. Сводка терминов для первого закона термодинамики, ΔU = Q − W | |
|---|---|
| Срок | Определение |
| У | Внутренняя энергия — сумма кинетической и потенциальной энергий атомов и молекул системы.Можно разделить на множество подкатегорий, таких как тепловая и химическая энергия.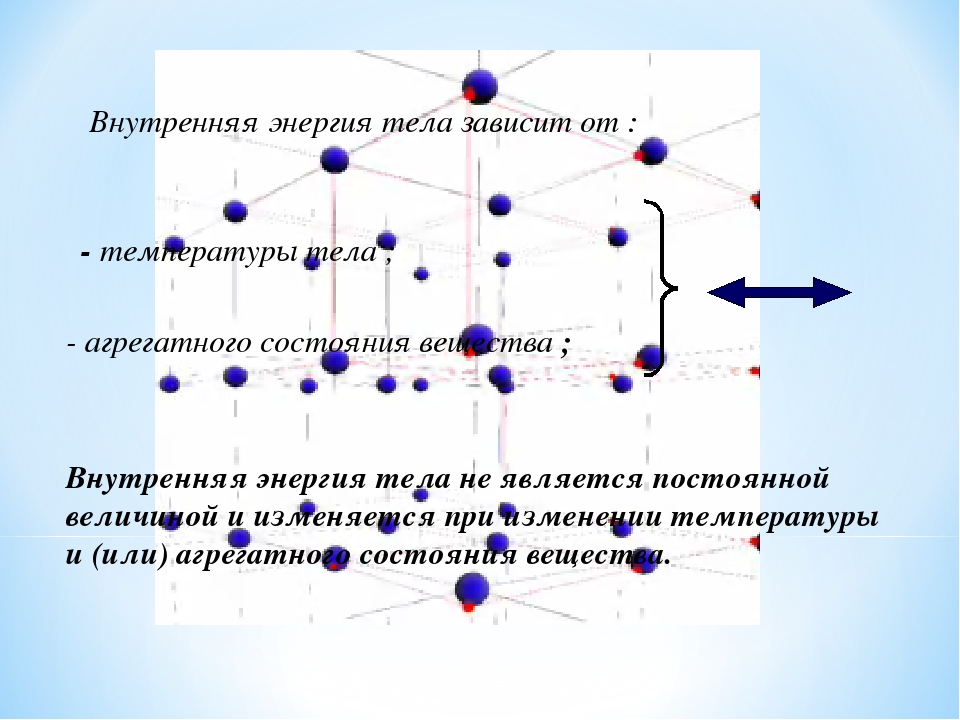 Зависит только от состояния системы (например, ее P , V и T ), а не от того, как энергия попала в систему. Изменение внутренней энергии не зависит от пути. Зависит только от состояния системы (например, ее P , V и T ), а не от того, как энергия попала в систему. Изменение внутренней энергии не зависит от пути. |
| К | Тепло — энергия, передаваемая из-за разницы температур. Характеризуется беспорядочным движением молекул. Сильно зависит от пути. Q вход в систему положительный. |
| Ш | Работа — энергия, переданная силой, движущейся на расстояние. Организованный, упорядоченный процесс. Зависит от пути. W , совершаемое системой (либо против внешней силы, либо для увеличения объема системы), положительна. |
Резюме раздела
- Первый закон термодинамики выражается как вся теплопередача в систему и из нее), а Вт является чистой выполненной работой (сумма всей работы, выполненной системой или системой).
- Оба Q и W являются энергией в пути; только Δ U представляет собой независимую величину, которую можно хранить.

- Внутренняя энергия U системы зависит только от состояния системы, а не от того, как она достигла этого состояния.
- Обмен веществ живых организмов и фотосинтез растений являются специализированными видами теплообмена, совершения работы и внутренней энергии систем.
Концептуальные вопросы
- Опишите фотографию чайника в начале этого раздела с точки зрения передачи тепла, выполненной работы и внутренней энергии.Как передается тепло? Какая работа сделана и что она делает? Как чайник сохраняет свою внутреннюю энергию?
- Первый закон термодинамики и закон сохранения энергии, как обсуждалось в Законе о сохранении энергии, явно связаны. Чем они различаются по рассматриваемым видам энергии?
- Теплопередача Q и выполненная работа Вт всегда представляют собой энергию в пути, тогда как внутренняя энергия U является энергией, хранящейся в системе. Приведите пример каждого типа энергии и конкретно укажите, как она либо находится в пути, либо находится в системе.

- Чем отличаются теплопередача и внутренняя энергия? В частности, что можно хранить как таковое в системе, а что нельзя?
- Если вы сбежите по лестнице и остановитесь, что произойдет с вашей кинетической энергией и вашей начальной гравитационной потенциальной энергией?
- Объясните, как можно рассматривать энергию пищи (калории) как молекулярную потенциальную энергию (в соответствии с атомарным и молекулярным определением внутренней энергии).
- Определите тип энергии, передаваемой вашему телу в каждом из следующих случаев: внутренняя энергия, теплопередача или выполнение работы: (а) купание в солнечных лучах; б) прием пищи; в) подняться на лифте на верхний этаж.
Задачи и упражнения
- Как изменится внутренняя энергия автомобиля, если в его бак залить 12,0 галлонов бензина? Энергоемкость бензина составляет 1,3 × 10 8 Дж/галлон. Все остальные факторы, например температура автомобиля, постоянны.
- Какой объем теплоты передается от системы, если ее внутренняя энергия уменьшилась на 150 Дж при совершении работы 30,0 Дж?
- Система совершает 1,80 × 10 8 Дж работы, в то время как 7,50 × 10 8 Дж теплопередачи происходит в окружающую среду.
 Каково изменение внутренней энергии системы при отсутствии других изменений (например, температуры или добавления топлива)?
Каково изменение внутренней энергии системы при отсутствии других изменений (например, температуры или добавления топлива)? - Как изменится внутренняя энергия системы, которая совершает работу 4,50×10 5 Дж при теплопередаче в систему 3,00×10 6 Дж и теплопередаче 8,00×10 6 Дж к окружающей среде?
- Предположим, что женщина совершает работу 500 Дж и при этом в окружающую среду передается 9500 Дж теплоты.а) Каково уменьшение ее внутренней энергии при условии отсутствия изменения температуры или потребления пищи? (То есть другого переноса энергии нет.) (б) Каков ее КПД?
- (а) Сколько энергии пищи усвоит человек в процессе выполнения работы в 35,0 кДж с КПД 5,00%? б) Какой объем теплоты передается окружающей среде, чтобы поддерживать ее температуру постоянной?
- (a) Какова средняя скорость метаболизма в ваттах у человека, который усваивает 10 500 кДж пищевой энергии за один день? б) Какую максимальную работу в джоулях он может выполнить, не расщепляя жир, при условии, что максимальный КПД равен 20.
 0%? (c) Сравните производительность его работы с дневной мощностью двигателя мощностью 187 Вт (0,250 л.с.).
0%? (c) Сравните производительность его работы с дневной мощностью двигателя мощностью 187 Вт (0,250 л.с.). - (a) Как долго хватит энергии чашки йогурта 1470 кДж (350 ккал) на женщину, выполняющую работу мощностью 150 Вт с эффективностью 20,0% (например, при неторопливом подъеме по лестнице)? (б) Означает ли время, указанное в части (а), что легко потреблять больше энергии пищи, чем вы можете обоснованно ожидать от работы с помощью физических упражнений?
- (a) Женщина, взбирающаяся на Монумент Вашингтона, метаболизирует 6.00 × 10 2 кДж энергии пищи. Если ее КПД составляет 18,0%, сколько тепла передается окружающей среде, чтобы поддерживать ее температуру постоянной? (b) Обсудите величину теплопередачи, найденную в (a). Соответствует ли это тому, что вы быстро разогреваетесь во время тренировки?
Глоссарий
первый закон термодинамики: утверждает, что изменение внутренней энергии системы равно чистой передаче тепла в систему за вычетом чистой работы, выполненной системой
внутренняя энергия: сумма кинетической и потенциальной энергий атомов и молекул системы
метаболизм человека: преобразование пищи в теплопередачу, работу и накопление жира
Избранные решения задач и упражнений
1. 1,6 × 10 9 Дж
1,6 × 10 9 Дж
3. −9,30 × 10 8 Дж
5. (а) -1,0 × 10 4 Дж или -2,39 ккал; (б) 5,00%
7. (а) 122 Вт; (б) 2,10 × 10 6 Дж; в) работа, совершаемая двигателем, равна 1,61 × 10 7 Дж; таким образом, двигатель производит работу, в 7,67 раз превышающую работу человека
9. (а) 492 кДж; (б) Это количество тепла соответствует тому факту, что вы быстро согреваетесь во время тренировки. Поскольку тело неэффективно, избыточное тепло должно рассеиваться через потоотделение, дыхание и т. д.
1. Введение.
Энергия. Мы все это используем. Мы все говорим об этом. Мы все платим за это. Правительства формулируют энергетическую политику и имеют огромные отделы для управления энергетической политикой. Мы беспокоимся о том, что наши естественные источники энергии «иссякают». В некоторые дни у нас мало энергии, и мы принимаем таблетки, чтобы повысить ее. Мы наблюдаем за играющими детьми и говорим: «Хотел бы я, чтобы ты смог собрать всю эту энергию в бутылки».
Тем не менее, если спросить: «Что такое 90 599 — это энергия 90 600?», большинство людей не в состоянии дать связный ответ.Студент-первокурсник-физик может ответить, указав различные «виды» или «формы» энергии: кинетическую энергию, потенциальную энергию, тепловую энергию, химическую энергию, ядерную энергию и электрическую энергию. Но это не ответ; это список покупок.
|
Мы говорим об энергии на языке, который предполагает, что энергия — это «нечто, содержащееся в материальных вещах». Мы говорим об «извлечении» энергии из угля и нефти. Мы говорим, что энергия может быть «преобразована из одной формы в другую». Такой язык предполагает, что мы думаем об энергии как о «веществе». Но идея хранения чистой энергии абсурдна. Кто-нибудь когда-нибудь прикасался или видел чистую энергию?
Такой язык предполагает, что мы думаем об энергии как о «веществе». Но идея хранения чистой энергии абсурдна. Кто-нибудь когда-нибудь прикасался или видел чистую энергию?
Научное образование убедило большинство людей в том, что энергия, доступная из природных ресурсов Земли, конечна, но понимание конечность ресурса не мешает нам растрачивать его небрежно и без нужды.Тем не менее, если бы обычного человека спросили, возможно ли, что мы когда-нибудь создадим машины, производящие больше энергии, чем потребляют, он бы отверг эту идею как абсурдную, сказав: «Нельзя получить что-то из ничего» или «Есть бесплатного обеда не будет».
В ранней истории техники даже такое поверхностное понимание энергии не было известно. Сама идея энергии является недавно разработанной концепцией. Историю физики можно разделить на несколько периодов: 1) Античность до XVII в., когда понятие силы еще не было точно сформулировано.(2) 17–18 века, когда сила и крутящий момент были достаточно хорошо изучены, а классическая ньютоновская механика превратилась в очень успешную модель. (3) 19 век, когда работа, энергия и импульс стали достаточно хорошо понятны (по крайней мере, физиками и инженерами) и были сформулированы законы термодинамики. (4) с 1900 г. по настоящее время, когда атомная теория и квантовая механика достигли огромных успехов.
(3) 19 век, когда работа, энергия и импульс стали достаточно хорошо понятны (по крайней мере, физиками и инженерами) и были сформулированы законы термодинамики. (4) с 1900 г. по настоящее время, когда атомная теория и квантовая механика достигли огромных успехов.
Но несмотря на все эти достижения, современный студент-физик должен по-прежнему продвигаться в изучении физических концепций каждого из этих периодов, но ускоренными темпами.Этот процесс обычно начинается с аристотелевских понятий, которые необходимо заменить: сначала пониманием ускорения, затем пониманием понятия силы как векторной величины, изучением теоремы о работе-энергии, борьбой с одновременным применением законов сохранения импульса и сохранения энергии, а затем к тонкостям законов термодинамики. Для тех, кто не отходит на второй план, святой Грааль квантовой механики и теории относительности угрожающе вырисовывается как последнее препятствие на пути к тому, чтобы стать физиком.
Учителя математики говорят, что многие ученики «теряют сознание» на уроках математики, когда вводят дроби, обычно в 4-м классе. Учителя физики знают, что многие студенты «теряют сознание», когда вводят векторы и силы. Те, кто преодолевает эти препятствия, часто добиваются успеха (едва ли) за счет зубрежки, писанины и подхода к решению проблем по принципу «подключи и пыхни», но без подлинного понимания. Они достигают только хрупкого и поверхностного понимания предмета, часто достаточного для низкоуровневой функциональности в технической области.Они могут не до конца осознать, что они упустили.
Учителя физики знают, что многие студенты «теряют сознание», когда вводят векторы и силы. Те, кто преодолевает эти препятствия, часто добиваются успеха (едва ли) за счет зубрежки, писанины и подхода к решению проблем по принципу «подключи и пыхни», но без подлинного понимания. Они достигают только хрупкого и поверхностного понимания предмета, часто достаточного для низкоуровневой функциональности в технической области.Они могут не до конца осознать, что они упустили.
1. Энергия.
Современные учебники отбрасывают в сторону извилистую историю нашей борьбы за понимание энергии, импульса и силы и представляют эти предметы в аккуратно организованном логическом изложении формул и процедур для решения физических задач. Обычно сначала вводятся законы Ньютона и понятие силы, затем кинетическая и потенциальная энергия, работа и импульс. Студенты, однако, часто не в состоянии понять основные понятия и логические связи.Давайте подойдем к теме немного по-другому — не то, чтобы в обычном представлении было что-то не так. Считайте это всего лишь «обзором с другой точки зрения» для человека, который прошел обычную презентацию и у которого остались нерешенные вопросы. Я буду избегать математических выводов, поскольку их можно найти в стандартных учебниках. Но не заблуждайтесь, математика необходима для понимания. Одни только слова могут лишь намекнуть на силу логических связей.
Считайте это всего лишь «обзором с другой точки зрения» для человека, который прошел обычную презентацию и у которого остались нерешенные вопросы. Я буду избегать математических выводов, поскольку их можно найти в стандартных учебниках. Но не заблуждайтесь, математика необходима для понимания. Одни только слова могут лишь намекнуть на силу логических связей.Сколько видов энергии существует? Это зависит от того, как вы определяете «виды».Я бы ответил: «Два — кинетический и потенциальный». Кинетическая энергия — это энергия движения тела, выраженная как мв 2 /2 . Потенциальная энергия — это энергия, обусловленная конфигурацией системы в пространстве в ситуациях, когда компоненты системы могут воздействовать друг на друга.
Я уже слышу возражения некоторых читателей. «А тепло? Ядерная энергия? Психическая энергия?» Давайте возьмем их один за другим. Психическая энергия есть не что иное, как псевдонаучный самогон, недостойный здесь дальнейшего комментария. Нет никаких доказательств его существования. «Тепло» — это разговорный термин, обозначающий то, что физики называют «тепловой энергией». Это не что иное, как суммарная неупорядоченная кинетическая энергия частиц тела, молекул и атомов. Ядерная энергия – это форма потенциальной энергии элементарных частиц, сжатых в ядра. Так оно и есть. Любая энергия, которую вы можете назвать, является либо кинетической, либо потенциальной энергией, либо их смесью.
Нет никаких доказательств его существования. «Тепло» — это разговорный термин, обозначающий то, что физики называют «тепловой энергией». Это не что иное, как суммарная неупорядоченная кинетическая энергия частиц тела, молекул и атомов. Ядерная энергия – это форма потенциальной энергии элементарных частиц, сжатых в ядра. Так оно и есть. Любая энергия, которую вы можете назвать, является либо кинетической, либо потенциальной энергией, либо их смесью.
Мы давно изучили, как тела обмениваются энергией друг с другом.Мы уже должны быть осторожны с языком. Слово «обмен» предполагает перенос чего-то материального из одного тела в другое, как купцы обменивают деньги. Это заблуждение, поскольку энергия не является материальной субстанцией. Мы говорим о ситуациях, когда два тела каким-то образом взаимодействуют друг с другом, и одно получает столько же энергии, сколько теряет другое. Мы избегаем явных разъяснений о том, как это происходит. Принято считать, что посредником процесса является сила, действующая со стороны одного тела на другое. Эта сила отвечает за обмен энергией, который мы называем работой . Но являются ли силы «реальными»? Является ли энергия «реальной»? Мы наблюдаем, что поведение каждого тела изменяется транзакцией. Одно или оба тела могут быть вынуждены изменить свою скорость (изменение кинетической энергии), или одно или оба тела могут быть перемещены в другое место, где их потенциальная энергия отличается от той, что была раньше.
Эта сила отвечает за обмен энергией, который мы называем работой . Но являются ли силы «реальными»? Является ли энергия «реальной»? Мы наблюдаем, что поведение каждого тела изменяется транзакцией. Одно или оба тела могут быть вынуждены изменить свою скорость (изменение кинетической энергии), или одно или оба тела могут быть перемещены в другое место, где их потенциальная энергия отличается от той, что была раньше.
Обратите внимание на общую черту изменения энергии. Меняете ли вы кинетическую или потенциальную энергию тела, в любом случае вы перемещаете тело.Когда вы используете язык силы, вы заключаете, что для того, чтобы изменить энергию тела, сила, действующая для этого изменения, должна сдвинуть тело .
Кинетическая энергия является хорошей отправной точкой, так как кинетическую энергию тела можно легко определить, измерив массу и скорость тела. В начале истории машин была изобретена пружинная шкала, которая является удобным способом измерения силы. Когда мы сокращаем числа, вычисляя величину изменения энергии тела из-за силы, действующей на него, мы обнаруживаем, что изменение равно величине силы, умноженной на расстояние, на которое тело было перемещено.Мы называем это «работой силы над телом». В этом есть уточнение, когда направление силы и расстояние, на которое движется тело, не параллельны. Тогда работа должна быть определена как произведение силы и расстояния, умноженное на косинус угла между векторами силы и расстояния. Когда направление расстояния важно физически, мы называем его смещением и рассматриваем с помощью векторной математики.
Когда мы сокращаем числа, вычисляя величину изменения энергии тела из-за силы, действующей на него, мы обнаруживаем, что изменение равно величине силы, умноженной на расстояние, на которое тело было перемещено.Мы называем это «работой силы над телом». В этом есть уточнение, когда направление силы и расстояние, на которое движется тело, не параллельны. Тогда работа должна быть определена как произведение силы и расстояния, умноженное на косинус угла между векторами силы и расстояния. Когда направление расстояния важно физически, мы называем его смещением и рассматриваем с помощью векторной математики.
Теперь, когда мы определили работу полезным способом, мы заключаем, что если сила и перемещение тела расположены под прямым углом друг к другу, эта сила не совершает работы над телом .Если сила, действующая на тело, равна нулю, то оно не совершает никакой работы. А если силы, действующие на тело, не производят перемещения, то никакой работы эти силы не совершали. Наконец, если над телом не совершается результирующая работа, его энергия не меняется. Они подтверждены экспериментом.
Наконец, если над телом не совершается результирующая работа, его энергия не меняется. Они подтверждены экспериментом.
Вернемся к некоторым повседневным примерам, с которыми может столкнуться каждый.
- Предположим, вы изо всех сил толкаете твердую каменную стену здания. Какую бы силу вы ни прикладывали к ней, вы не совершаете никакой работы со стеной, потому что стена не двигается.Вы можете почувствовать усталость от усилий, вы можете «вспотеть» и сказать: «Это была работа!» Вы действительно израсходовали энергию, но почти полностью она была внутри вашего тела. Это работа, выполняемая силой мышечного сокращения и расслабления, результатом которой является внутренний нагрев ваших мышц и окружающих тканей. Некоторая работа была также затрачена на сопутствующие химические изменения в ваших мышцах. И очень небольшое количество может быть потрачено впустую на легкое сжатие и изгибание объекта, который вы пытаетесь толкнуть.
- Натяните обычную резинку. Сила ваших пальцев раздвигает концы резины дальше друг от друга, временно делая ленту длиннее.
 Вы проделали работу с каучуком, и в растянутом состоянии он обладает потенциальной энергией из-за пространственной реконфигурации его материальных компонентов. Некоторая работа, которую вы проделали, также заставила резину «нагреться», что вы можете подтвердить, повторяя это несколько раз, а затем быстро прижимая резину к губам. Резина чувствует себя теплее после многократного растяжения.(Губы более чувствительны к небольшим изменениям температуры, чем другие части тела.) Итак, в этом эксперименте проделанная вами работа изменяет как потенциальную энергию, так и кинетическую энергию (молекулярного движения) резиновой ленты.
Вы проделали работу с каучуком, и в растянутом состоянии он обладает потенциальной энергией из-за пространственной реконфигурации его материальных компонентов. Некоторая работа, которую вы проделали, также заставила резину «нагреться», что вы можете подтвердить, повторяя это несколько раз, а затем быстро прижимая резину к губам. Резина чувствует себя теплее после многократного растяжения.(Губы более чувствительны к небольшим изменениям температуры, чем другие части тела.) Итак, в этом эксперименте проделанная вами работа изменяет как потенциальную энергию, так и кинетическую энергию (молекулярного движения) резиновой ленты. - Отпустите один конец сшитой ленты. Он отскакивает назад (движение имеет кинетическую энергию), вероятно, со слышимым звуком. Эта звуковая волна уносит часть накопленной энергии полосы, остальная часть увеличивает ее тепловую энергию, увеличивая ее температуру.
- Поднимите книгу с пола и положите ее на стол.Работа, которую вы проделали над книгой, равна произведению веса книги на вертикальное расстояние от пола до стола.
 Вы также проделали некоторую дополнительную работу в своем теле из-за мышечной активности (как отмечалось выше). Таким образом, неправильно говорить, что общая работа 90 599, которую вы сделали 90 600, была только работой, проделанной над книгой. Ваше тело действует как машина, а машины всегда тратят впустую часть энергии, которую они потребляют. Под «отходами» мы подразумеваем, что не вся энергия машины идет на выполнение задачи, для которой она предназначена; это не то, что мы называем «полезной работой».
Вы также проделали некоторую дополнительную работу в своем теле из-за мышечной активности (как отмечалось выше). Таким образом, неправильно говорить, что общая работа 90 599, которую вы сделали 90 600, была только работой, проделанной над книгой. Ваше тело действует как машина, а машины всегда тратят впустую часть энергии, которую они потребляют. Под «отходами» мы подразумеваем, что не вся энергия машины идет на выполнение задачи, для которой она предназначена; это не то, что мы называем «полезной работой». - Толкните книгу, чтобы она упала со стола. При движении вниз его потенциальная энергия уменьшается, а кинетическая энергия увеличивается по мере увеличения скорости. При падении сумма его кинетической и потенциальной энергий постоянна. Когда книга падает на пол, ее потенциальная энергия уменьшается до того же значения, что и до того, как вы ее подняли. В момент перед приземлением его кинетическая энергия равна работе, которую вы совершили над ним, поднимая его на поверхность стола.
 После столкновения он покоится, и его кинетическая энергия движения равна нулю.Но его внутренняя энергия движения увеличилась (тепловая энергия), но это хаотическое движение миллионов частиц, движущихся во всех возможных направлениях. Это неорганизованное движение не способствует какому-либо движению книги в целом.
После столкновения он покоится, и его кинетическая энергия движения равна нулю.Но его внутренняя энергия движения увеличилась (тепловая энергия), но это хаотическое движение миллионов частиц, движущихся во всех возможных направлениях. Это неорганизованное движение не способствует какому-либо движению книги в целом.
Наконец, мы отметили, что взаимодействие тел может привести к изменению энергии обоих тел из-за сил, которые они действуют друг на друга. Но материальные тела могут взаимодействовать и другими способами, и один из наиболее важных способов — тепловое взаимодействие.Когда два тела находятся в контакте, эти хаотично движущиеся частицы в каждом теле взаимодействуют там, где тела соприкасаются. Это силовые взаимодействия, но это микроскопическая версия того, что мы описали выше, настолько малая, что она не оказывает заметного влияния на движение тел в целом. Но при этом одно тело может получить тепловую энергию, а другое такое же количество ее потерять. Количество обмениваемой энергии называется «тепло». Итак, в физике мы признаем два способа обмена телами энергией: через 90 599 работы 90 600 или через 90 599 тепла 90 600.Мы избегаем использовать термин «тепло» как нечто «внутри» или «одержимое» телом. Точно так же мы никогда не говорим о «работе в теле». И «тепло», и «работа» являются мерами энергии 90 599 изменений 90 600, возникающих в результате силовых взаимодействий.
Но материальные тела могут взаимодействовать и другими способами, и один из наиболее важных способов — тепловое взаимодействие.Когда два тела находятся в контакте, эти хаотично движущиеся частицы в каждом теле взаимодействуют там, где тела соприкасаются. Это силовые взаимодействия, но это микроскопическая версия того, что мы описали выше, настолько малая, что она не оказывает заметного влияния на движение тел в целом. Но при этом одно тело может получить тепловую энергию, а другое такое же количество ее потерять. Количество обмениваемой энергии называется «тепло». Итак, в физике мы признаем два способа обмена телами энергией: через 90 599 работы 90 600 или через 90 599 тепла 90 600.Мы избегаем использовать термин «тепло» как нечто «внутри» или «одержимое» телом. Точно так же мы никогда не говорим о «работе в теле». И «тепло», и «работа» являются мерами энергии 90 599 изменений 90 600, возникающих в результате силовых взаимодействий.
Ради обсуждения мы должны различать две области: микроскопические и макроскопические явления. Микроскопические физические явления — это явления размером с молекулу и меньше. Тепловая энергия является микроскопическим явлением. Объемное движение твердых объектов, таких как механизмы или планеты, является макроскопическим.
Микроскопические физические явления — это явления размером с молекулу и меньше. Тепловая энергия является микроскопическим явлением. Объемное движение твердых объектов, таких как механизмы или планеты, является макроскопическим.
Во всем этом есть фундаментальная асимметрия. Поскольку тепловая энергия представляет собой хаотическую (неорганизованную) кинетическую энергию, ее нельзя полностью преобразовать в макроскопическую работу. Некоторая работа должна быть выполнена при преобразовании тепловой энергии в работу, и существуют ограничения на то, сколько может быть преобразовано. Однако в другом направлении работа может быть полностью преобразована в тепловую энергию. Это вполне разумно, если учесть, что для превращения тепловой энергии покоящегося тела в движение тела в целом мы должны совершить работу, чтобы перенаправить хаотическое движение множества частиц со скоростями во всех возможных направлениях так, чтобы они двигались в одном направлении. .
Как можно сохранить энергию? Вопрос вводит в заблуждение, поскольку энергия не является материальной субстанцией. Конечно, мы можем собирать и хранить материалы, которые 90 599 имеют энергию 90 600, например, хранить бензин, который имеет химическую потенциальную энергию в своей молекулярной структуре. Мы можем хранить тепловую энергию, скажем, нагретой воды, часть которой может быть извлечена тепловыми двигателями (с учетом ограничений термодинамических законов). Сама материя представляет собой накопленную энергию, и в некоторых случаях часть ее может быть передана другим формам посредством ядерных реакций.
Конечно, мы можем собирать и хранить материалы, которые 90 599 имеют энергию 90 600, например, хранить бензин, который имеет химическую потенциальную энергию в своей молекулярной структуре. Мы можем хранить тепловую энергию, скажем, нагретой воды, часть которой может быть извлечена тепловыми двигателями (с учетом ограничений термодинамических законов). Сама материя представляет собой накопленную энергию, и в некоторых случаях часть ее может быть передана другим формам посредством ядерных реакций.
Но было бы ошибкой предполагать, как это делают некоторые, что все, что может проявлять силу, представляет собой «источник» энергии. Выше мы были осторожны, чтобы не рассматривать «силу» как нечто большее, чем удобный способ выражения и количественной оценки энергетических взаимодействий между материальными телами. Я получаю вопросы о возможности «извлечения энергии из гравитации». Для физика это абсурдная идея, но нелегко объяснить почему тому, кто не занимается физикой каждый день.
Пересмотрите приведенные выше примеры.В примере с книгой и столом потенциальная энергия книги на столе была обусловлена тем фактом, что мы работали над книгой, чтобы увеличить ее расстояние от земли. Вес книги был обусловлен силой земного притяжения, действовавшей на книгу. Итак, когда книга упала со стола, ее кинетическая энергия увеличилась и в конце концов превратилась в тепловую энергию. Откуда взялась эта энергия? Не из-за гравитации, а из-за того, что кто-то поднял книгу с пола. Вся последовательность процессов не извлекла ничего из гравитации и не уменьшила гравитационное поле Земли.Оно исходило от человека или машины, выполнявших подъем.
Ни одна когда-либо созданная машина, ни один естественный процесс никогда не извлекали энергию из гравитации.
У меня были люди, которые говорили мне, что в магнитном поле есть бесконечная энергия. В качестве «доказательства» они приводят магнит холодильника, цепляющийся за вертикальную стенку холодильника и поддерживающий собственный вес против силы тяжести, предположительно навсегда. Некоторые добавляют, что он упадет только тогда, когда «запасенная энергия» в магните будет исчерпана.Итак, говорят они, в магните должно храниться неограниченное количество энергии. Эти люди медленно учатся. Магнит, покоящийся на стенке холодильника, совершает 90 612, но не 90 614 работы, и затрачивает 90 612, а не 90 614 энергии, поскольку его сила притяжения не вызывает движения ни магнита, ни холодильника. У магнита есть небольшое количество накопленной энергии (от работы, необходимой для его намагничивания), но он ничего из этого не использует. Он также не крадет энергию гравитации. Он просто не расходует энергию ни в какой форме.Рассмотрим аналогичную ситуацию. Используйте клей, чтобы прикрепить деревянный брусок к стене холодильника. Никакой магнетизм не задействован. Блок останется там, поддерживая собственный вес, на неопределенный срок. Стал бы человек, который использовал пример с магнитом, теперь утверждать, что клей обладает неограниченным запасом энергии? А как насчет гвоздя, вбитого в стену, чтобы повесить картину? Или крючок в шкафу? Люди, которые до сих пор используют аргумент магнита холодильника в качестве аргумента в пользу извлечения неограниченной энергии из магнитов, совершают не только ошибку физики, но и ошибку критического мышления и исключительное отсутствие здравого смысла.
Некоторые добавляют, что он упадет только тогда, когда «запасенная энергия» в магните будет исчерпана.Итак, говорят они, в магните должно храниться неограниченное количество энергии. Эти люди медленно учатся. Магнит, покоящийся на стенке холодильника, совершает 90 612, но не 90 614 работы, и затрачивает 90 612, а не 90 614 энергии, поскольку его сила притяжения не вызывает движения ни магнита, ни холодильника. У магнита есть небольшое количество накопленной энергии (от работы, необходимой для его намагничивания), но он ничего из этого не использует. Он также не крадет энергию гравитации. Он просто не расходует энергию ни в какой форме.Рассмотрим аналогичную ситуацию. Используйте клей, чтобы прикрепить деревянный брусок к стене холодильника. Никакой магнетизм не задействован. Блок останется там, поддерживая собственный вес, на неопределенный срок. Стал бы человек, который использовал пример с магнитом, теперь утверждать, что клей обладает неограниченным запасом энергии? А как насчет гвоздя, вбитого в стену, чтобы повесить картину? Или крючок в шкафу? Люди, которые до сих пор используют аргумент магнита холодильника в качестве аргумента в пользу извлечения неограниченной энергии из магнитов, совершают не только ошибку физики, но и ошибку критического мышления и исключительное отсутствие здравого смысла.
Ни одна когда-либо созданная машина, ни один естественный процесс никогда не извлекали из магнита больше энергии, чем то небольшое количество энергии, которое используется для намагничивания магнита.
Одна из причин, по которой мы слышим такие возмутительные искажения физики, заключается в том, что многие люди не занимаются математикой, даже простыми расчетами количества работы, проделанной в процессах, и количества обмениваемой энергии. Магнит в двигателе с постоянными магнитами может длиться годами непрерывной работы, а небольшое снижение его магнитных свойств представляет собой крошечное изменение энергии, незначительное по сравнению с объемом работы, выполняемой двигателем во время его работы.
2. Потенциальная энергия.
Давайте более внимательно посмотрим на потенциальную энергию, о которой мы упоминали. Как мы это измеряем. До сих пор мы предполагали, что можем измерять массу (с помощью любого из нескольких древних измерительных инструментов) и силу (с помощью пружинных весов или датчиков силы). Скорость измеряется мерными рейками и секундомерами. (Именно сложность измерения коротких временных интервалов задержала наше понимание движения в ранней истории физики.) Итак, у нас есть инструменты для измерения кинетической энергии, а также для измерения работы.С ними мы можем проводить эксперименты для изучения того, как тела обмениваются энергиями посредством силовых взаимодействий.
Скорость измеряется мерными рейками и секундомерами. (Именно сложность измерения коротких временных интервалов задержала наше понимание движения в ранней истории физики.) Итак, у нас есть инструменты для измерения кинетической энергии, а также для измерения работы.С ними мы можем проводить эксперименты для изучения того, как тела обмениваются энергиями посредством силовых взаимодействий.Потенциальная энергия системы равна работе, необходимой для сборки компонентов системы, работающих против взаимодействующих сил ее компонентов и любых внешних сил, действующих на них. Есть сложности с измерением этого из-за потери энергии в диссипативных процессах, производстве тепловой энергии, звука и т. Д., Но мы не должны позволять этому отвлекать нас от важных вопросов.
Предположим, мы растягиваем или сжимаем пружину весов-пружин. Мы должны работать, чтобы добиться этого. После того, как струна сжата, мы фиксируем ее в сжатом положении. Где энергия равна проделанной нами работе? Мы говорим, что это «потенциальная энергия, запасенная в пружине». Мы можем убедиться в этом, разблокировав пружину и позволив ей воздействовать на что-то еще, пока она расширяется. Потенциальная энергия сжатой пружины как раз равна работе, которую мы совершали против силы упругости пружины, когда мы ее сжимали.
Мы можем убедиться в этом, разблокировав пружину и позволив ей воздействовать на что-то еще, пока она расширяется. Потенциальная энергия сжатой пружины как раз равна работе, которую мы совершали против силы упругости пружины, когда мы ее сжимали.
Когда мы подняли книгу с пола на стол, мы говорим, что книга на столе получила потенциальную энергию, и мы можем рассчитать эту энергию как мгч , где м — ее масса, г — константа, а h — вертикальное расстояние, на которое он был поднят. Мы можем убедиться в этом, позволив ему упасть и измерив его кинетическую энергию непосредственно перед тем, как он упадет на пол. Потенциальная энергия книги на столе как раз равна работе, которую мы совершили против силы гравитации, поднимая книгу с пола на стол.
3. Гравитация.
Мы называем это «гравитационной потенциальной энергией». Но это имя может ввести нас в заблуждение, если мы не рассмотрим, что оно представляет. Итак, давайте более внимательно посмотрим на гравитацию.
Исаак Ньютон задавался вопросом «Почему тела падают». История рассказывалась много раз, но суть в том, что он постулировал, что Земля оказывает силу на тела рядом с ней, и не только вблизи, но эта гравитационная сила распространяется даже на Луну и дальше, хотя и уменьшается в силе с расстояние от земли, изменяющееся как 1/R 2 , где R — расстояние от центра Земли.Это была идея, которую в то время подозревали многие другие люди, но именно Ньютон провел необходимые математические расчеты, чтобы подтвердить, что она действительно согласуется с тем, что мы знали о падающих телах и с орбитой Луны. Тем не менее, эта идея потрясла многих, поскольку она предполагала, что существует сила «влияния», которая может действовать на тела даже на расстоянии, без каких-либо других доказательств, кроме того факта, что она влияет на их наблюдаемое движение. Гравитация не «наблюдается», она «выводится» из наблюдений за движением тел.И гравитация — это не только результат действия Земли, Ньютон сказал, что 90 599 любое тело массой 90 600 влияет на любое другое тело с массой в количестве, пропорциональном произведению их масс.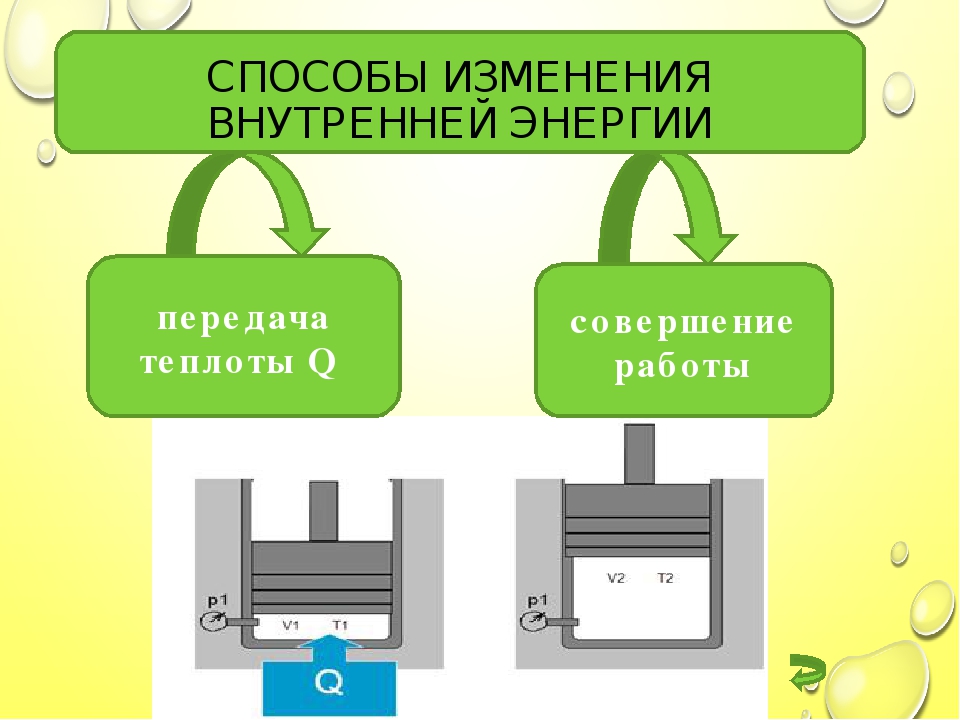 Окончательное уравнение гласило, что сила, с которой каждое тело действует на другое, имеет величину F = GmM/R 2 , где m и M — массы, G — универсальная гравитационная постоянная и R . — расстояние разноса тел.
Окончательное уравнение гласило, что сила, с которой каждое тело действует на другое, имеет величину F = GmM/R 2 , где m и M — массы, G — универсальная гравитационная постоянная и R . — расстояние разноса тел.
Мы говорим, что гравитация ответственна за изменение наблюдаемого движения тел таким же образом, как если бы на два тела воздействовали силы из-за соприкосновения тел.Контакт с гравитацией не нужен. Хотя мы легко воспринимаем контактные силы, будучи чем-то, что мы «чувствуем», когда толкаем или поднимаем объект, мы не можем чувствовать силу, которую Земля и Луна воздействуют друг на друга. Однако в обоих случаях мы не измеряем силу напрямую. Сила предполагается, выводится из изменения движения, которое мы наблюдаем. В каком-то смысле ни одна из сил не является «реальной». В другом смысле оба одинаково «реальны». Мы оставляем обсуждение того, «что действительно реально», для другого документа. Реально это или нет, но мы можем измерить движение и вычислить величины и направления сил, и все это образует непротиворечивую картину.
4. Сила.
Один экспериментальный факт возникает, когда мы начинаем точно и точно измерять вещи. Когда два тела взаимодействуют, и в результате этого процесса одно из них приобретает энергию, другое теряет такое же количество энергии. Такие факты привели физиков к закону сохранения энергии. Теперь этот закон применяется, когда взаимодействие является таким, когда одно тело действует на другое, а также когда одно тело нагревает другое. Оба являются обменом из-за силы (сил), действующих на расстоянии, будь то на макроскопическом уровне или на микроскопическом уровне (тепло). Когда сила и перемещение имеют одно и то же направление, мы говорим, что сила совершает положительную работу над телом, на которое она действует. Когда сила и перемещение направлены в противоположные стороны, мы говорим, что сила совершает отрицательную работу над телом, на которое она действует. Другими словами, если тело А воздействует на В с силой F, причем сила и перемещение направлены в одном направлении, то А совершает положительную работу над В. Если тело А действует на В с силой F, а сила и перемещение направлены в противоположном направлении, то А совершает отрицательную работу над В.Это то же самое, что сказать, что если тело A действует на тело B, то B совершает работу равной величины и с противоположным знаком по отношению к A. Отсюда можно вернуться к третьему закону Ньютона: «Если тело A действует на тело B, то тело В действует на А с равной и противоположно направленной силой».
Если тело А действует на В с силой F, а сила и перемещение направлены в противоположном направлении, то А совершает отрицательную работу над В.Это то же самое, что сказать, что если тело A действует на тело B, то B совершает работу равной величины и с противоположным знаком по отношению к A. Отсюда можно вернуться к третьему закону Ньютона: «Если тело A действует на тело B, то тело В действует на А с равной и противоположно направленной силой».
Итак, работая в обратном направлении от концепции энергии и сохранения энергии, мы приходим к законам Ньютона. Исторически порядок открытия этих понятий был обратным. Но в каком бы направлении вы ни следовали логике, закон сохранения энергии и законы Ньютона неразрывно связаны.Если одно верно, то верно и другое. А если бы одно из них было неверным, оба были бы неверными. У нас нет абсолютно никаких доказательств того, что любой из них ошибочен на макроскопическом уровне классической физики.
Последняя редакция, декабрь 2017 г.
Первый закон термодинамики — обзор
5.1 Введение
Обычно считается, что первый закон термодинамики наименее труден для понимания, поскольку он является расширением закона сохранения энергии. это означает, что энергия не может быть ни создана, ни уничтожена.Сколько бы энергии ни было в начале Вселенной, столько же будет и в конце. Однако термодинамика — предмет тонкий, и первый закон гораздо интереснее, чем может показаться из этого замечания. Более того, подобно нулевому закону, давшему толчок к введению свойства «температура» и его уточнению, первый закон мотивирует введение и помогает прояснить смысл неуловимого понятия «энергия».
Энергетический баланс, основанный на первом законе термодинамики, разработан для лучшего понимания любого процесса, облегчения проектирования и управления, выявления потребностей в улучшении процесса и возможной оптимизации.Степень совершенства использования энергии процесса или его отдельных частей позволяет сравнить степень совершенства и связанные параметры процесса с параметрами других подобных процессов. Особенно важно сравнение с достижимыми в настоящее время значениями в наиболее эффективных системах. Можно установить приоритеты для необходимых попыток оптимизации системы или ее компонентов. Такие приоритеты могут осуществляться на основании либо чрезмерного энергопотребления, либо особо низкой степени совершенства.
Особенно важно сравнение с достижимыми в настоящее время значениями в наиболее эффективных системах. Можно установить приоритеты для необходимых попыток оптимизации системы или ее компонентов. Такие приоритеты могут осуществляться на основании либо чрезмерного энергопотребления, либо особо низкой степени совершенства.
Однако энергетический подход имеет некоторые недостатки. Как правило, энергообмен не чувствителен к предполагаемому направлению процесса, например, энергетический анализ допускает самопроизвольную передачу тепла в направлении повышения температуры. Энергия также не различает своего качества, например, 1 Вт тепла равен 1 Ватт работы или электроэнергии.
Первый закон термодинамики гласит, что полная энергия системы остается постоянной, даже если она переходит из одной формы в другую.Например, кинетическая энергия — энергия, которой обладает объект при движении, — преобразуется в тепловую энергию, когда водитель нажимает на тормоз автомобиля, чтобы замедлить его. Первый закон термодинамики связывает различные формы кинетической и потенциальной энергии в системе с работой, которую система может совершить, и с передачей тепла. Этот закон иногда принимается за определение внутренней энергии , а также вводит дополнительную переменную состояния, энтальпию . Первый закон термодинамики допускает существование множества возможных состояний системы.Однако опыт показывает, что имеют место только определенные состояния. В конечном итоге это приводит ко второму закону термодинамики и определению другой переменной состояния, называемой энтропией .
Первый закон термодинамики связывает различные формы кинетической и потенциальной энергии в системе с работой, которую система может совершить, и с передачей тепла. Этот закон иногда принимается за определение внутренней энергии , а также вводит дополнительную переменную состояния, энтальпию . Первый закон термодинамики допускает существование множества возможных состояний системы.Однако опыт показывает, что имеют место только определенные состояния. В конечном итоге это приводит ко второму закону термодинамики и определению другой переменной состояния, называемой энтропией .
Работа есть движение против противодействующей силы. Поднятие веса против противодействующей силы тяжести требует работы. Величина работы зависит от массы объекта, силы притяжения к нему и высоты, на которую он поднят. Работа является основной основой термодинамики и, в частности, первого закона.Любая система способна выполнять работу. Например, сжатая или растянутая пружина может совершать работу, подобную той, которая используется для подъема груза.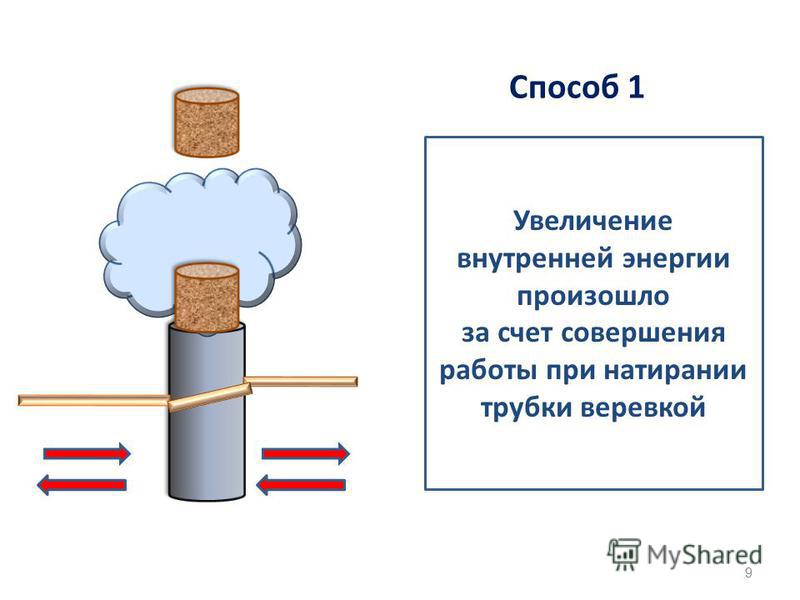 Электрическая батарея способна выполнять работу, так как ее можно подключить к электродвигателю, который, в свою очередь, можно использовать для подъема груза. Это не совсем очевидный момент, но когда электрический ток проходит через нагреватель, он совершает работу над нагревателем, так как тот же самый ток можно использовать для подъема груза, пропуская его через электродвигатель, а не через нагреватель.Тогда почему обогреватель называется « обогреватель », а не « рабочий », очевидно из понятия теплоты, которое было определено в главе 4.
Электрическая батарея способна выполнять работу, так как ее можно подключить к электродвигателю, который, в свою очередь, можно использовать для подъема груза. Это не совсем очевидный момент, но когда электрический ток проходит через нагреватель, он совершает работу над нагревателем, так как тот же самый ток можно использовать для подъема груза, пропуская его через электродвигатель, а не через нагреватель.Тогда почему обогреватель называется « обогреватель », а не « рабочий », очевидно из понятия теплоты, которое было определено в главе 4.
Первый закон термодинамики обычно называют законом сохранения энергии. В начальных курсах физики изучение сохранения энергии делает упор на изменения механической кинетической и потенциальной энергии и их связь с работой. Более общая форма сохранения энергии включает в себя эффекты теплопередачи и изменения внутренней энергии.Эта более общая форма обычно называется первым законом термодинамики . Также могут быть включены другие формы энергии, такие как электростатическая, магнитная, деформационная и поверхностная энергия.
Чтобы понять и иметь лучшее представление о работе с точки зрения термодинамики, необходим термин, обозначающий способность системы выполнять работу. Этот термин равен энергии . Полностью растянутая пружина совершает большую работу, чем та же пружина, только слегка растянутая. Литр горячей воды обладает большей энергетической ценностью, чем литр холодной воды.Следовательно, понятие энергии — это всего лишь мера способности системы совершать работу.
Первый закон термодинамики гласит, что энергия е не может быть ни создана, ни уничтожена, а только изменена в форме . Для любой системы перенос энергии связан с переходом массы через границу управления, внешней работой или передачей тепла через границу. Они производят изменение накопленной энергии в пределах контрольного объема. Массовый расход жидкости связан с кинетической, потенциальной, внутренней и «потоковой» энергиями, влияющими на общий энергетический баланс системы.Обмен внешней работой и теплотой завершает энергетический баланс. Вот почему первый закон термодинамики называется принципом сохранения энергии , что означает, что энергия не может быть ни создана, ни уничтожена , а преобразована в различные формы по мере изменения жидкости в контрольном объеме. Система – это область пространства (контрольный объем), через которую может проходить или не проходить рабочая жидкость. Затем наблюдают за различными энергиями, связанными с жидкостью, по мере того, как они пересекают границы системы, и устанавливается баланс.Как обсуждалось в главе 1, система может быть одного из трех типов:
Вот почему первый закон термодинамики называется принципом сохранения энергии , что означает, что энергия не может быть ни создана, ни уничтожена , а преобразована в различные формы по мере изменения жидкости в контрольном объеме. Система – это область пространства (контрольный объем), через которую может проходить или не проходить рабочая жидкость. Затем наблюдают за различными энергиями, связанными с жидкостью, по мере того, как они пересекают границы системы, и устанавливается баланс.Как обсуждалось в главе 1, система может быть одного из трех типов:
- 1.
Изолированная система;
- 2.
Закрытая система;
- 3.
Открытая система.
Открытая система, самая общая из трех, позволяет массе, теплу и внешней работе пересекать контрольную границу. Равновесие выражается в работе, поскольку все энергии, поступающие в систему, равны всем энергиям, покидающим систему, плюс изменение накопления энергий внутри системы.
Система может быть механическим устройством, биологическим организмом или определенным количеством материала, например, хладагентом в кондиционере или паром, расширяющимся в турбине. Термодинамическая система — это система, которая может взаимодействовать (и обмениваться энергией) со своим окружением или окружающей средой как минимум двумя способами, одним из которых является передача тепла. Знакомый пример — количество зерен попкорна в кастрюле с крышкой (рис. 5.1). Когда горшок ставится на плиту, к попкорну добавляется энергия за счет теплопроводности; когда попкорн лопается и расширяется, он действительно работает, поскольку оказывает восходящее усилие на крышку и смещает ее.
Рисунок 5.1. Попкорн в кастрюле — это термодинамическая система. В термодинамическом процессе, показанном здесь, к системе добавляется тепло, и система работает над своим окружением, поднимая крышку кастрюли.
В этом процессе изменяется состояние попкорна, поскольку объем, температура и давление попкорна изменяются по мере того, как он лопается. Процесс, подобный этому, при котором происходят изменения состояния термодинамической системы, называется термодинамическим процессом. В термодинамических системах важно с самого начала четко определить, что именно входит в систему, а что нет.Только тогда можно однозначно описать переносы энергии. Например, в примере с попкорном система включала попкорн, но не кастрюлю, крышку или плиту.
Процесс, подобный этому, при котором происходят изменения состояния термодинамической системы, называется термодинамическим процессом. В термодинамических системах важно с самого начала четко определить, что именно входит в систему, а что нет.Только тогда можно однозначно описать переносы энергии. Например, в примере с попкорном система включала попкорн, но не кастрюлю, крышку или плиту.
Три закона термодинамики | ОРЕЛ
Все дело в термодинамике. Это не просто концепция, зарезервированная для области физики, и это не набор законов, которые вы найдете только в электронике, холодильниках, автомобилях, самолетах и т. д. Это научная концепция, которая вплетается в саму ткань. жизни.Проблема в том, что термодинамика — это именно то, как работает энергия, поэтому ее легко упустить. Когда вы неделю за неделей убираете свой офис, который с каждым днем становится все более грязным, это работает второй закон термодинамики, где все приводит к усилению состояния дезорганизации. Или когда вы готовите этот вкусный стейк на гриле в эти выходные, это первый закон термодинамики в действии, передающий энергию в виде тепла вашей еде. Термодинамика — это не просто изучение тепла и работы; это изучение того, как работает энергия, материал, из которого сделаны вы, я и все вокруг вас. Термодинамика изучает жизнь.
Или когда вы готовите этот вкусный стейк на гриле в эти выходные, это первый закон термодинамики в действии, передающий энергию в виде тепла вашей еде. Термодинамика — это не просто изучение тепла и работы; это изучение того, как работает энергия, материал, из которого сделаны вы, я и все вокруг вас. Термодинамика изучает жизнь.
Системы и окружение
Мы все живем в системе, где происходит непрерывный обмен веществом и энергией; это бесконечный поток. Возьмем, к примеру, процесс еды: вы поглощаете химическую энергию пищи и преобразуете ее в форму, пригодную для использования вашим телом. Теперь, когда ваше тело получает энергию из пищи, оно может работать в мире.
Этот процесс обмена, при котором энергия переходит из одного состояния в другое, происходит в наборе систем и окружения .Когда вы включаете свой электрический чайник утром, у вас есть вода, заключенная в металлическом контейнере, это ваша система. Остальная кухня, даже остальная часть дома — это окружение.
Когда ваш чайник начинает кипеть, он превращает часть воды в пар, который выходит из носика в верхней части. Эта преобразованная энергия пересекает границу из системы внутри металлического контейнера в окружающую среду за его пределами. Это термодинамика в действии, перенос энергии и материи между системами и окружающей средой.
Каждая термодинамическая система окружена границей и окружением. (Источник изображения)
Системы определяются наблюдателем, поэтому для одного человека чайник может быть системой. Для другого весь дом может быть системой, а окрестности — окрестностями, все зависит от вашей точки зрения. Дело в том, что каждая система в термодинамике содержится в пределах определенной границы, а по другую сторону границы находится окружение. В термодинамике различают три типа систем:
- Открытая система , в которой может происходить обмен энергией и веществом между системой и ее окружением.
- Замкнутая система , в которой между системой и ее окружением возможен обмен только энергией, а не материей.

- Изолированная система , в которой не происходит обмена энергией или материей между системой и ее окружением. По-настоящему изолированная система встречается редко.
На высоком уровне вся наша вселенная считается системой, но каковы границы нашей вселенной и каково ее окружение? Это одни из самых важных вопросов, на которые нам еще предстоит ответить.Для разработчика электроники термодинамика представляет собой более личную реальность в повседневных устройствах, которые вы проектируете. Вы обнаружите, что многие из принципов, с которыми вы уже работаете для расчета и анализа цепей, таких как закон Кирхгофа, основаны на основах термодинамики.
Первый закон термодинамики
Первый закон термодинамики, также известный как закон сохранения энергии, гласит, что энергия не может быть создана или уничтожена, она может только изменять форму.Энергия бывает разных форм, в том числе:
Энергия бывает разных форм. (Источник изображения)
Энергия не создается и не уничтожается; он просто переходит из одной формы в другую. Включение выключателя света не создает энергию, оно просто преобразует электрическую энергию в лучистую энергию (свет) и тепловую энергию (тепло).
Включение выключателя света не создает энергию, оно просто преобразует электрическую энергию в лучистую энергию (свет) и тепловую энергию (тепло).
Практические примеры преобразования энергии в действии. (Источник изображения)
В Первом Законе есть три взаимосвязанных понятия – работа, теплота и внутренняя энергия. Тепло – это передача тепловой энергии между двумя системами. Работа — это сила, передающая энергию между системой и ее окружением. Производя работу либо внутри системы, либо вне ее, вы создаете тепло. Затем есть внутренняя энергия , то есть вся энергия внутри системы. Когда теплота, работа и внутренняя энергия взаимодействуют друг с другом, происходит преобразование энергии. Вы можете выразить это отношение математически как:
Здесь ΔU — полное изменение внутренней энергии в системе, Q — теплообмен между системой и ее окружением, а W — работа, совершаемая системой или системой.
Когда система выделяет тепло или совершает какую-либо работу, внутренняя энергия системы уменьшается. Точно так же, если в систему добавляется тепло или в систему совершается работа, внутренняя энергия системы увеличивается. Любой вид энергии, который высвобождается системой, поглощается ее окружением, и любой вид энергии, потерянный окружением, поглощается системой. Во всех этих примерах вы не создаете и не уничтожаете энергию; это просто перемещение из одного места в другое. Выражаясь математически, это выглядит так:
Точно так же, если в систему добавляется тепло или в систему совершается работа, внутренняя энергия системы увеличивается. Любой вид энергии, который высвобождается системой, поглощается ее окружением, и любой вид энергии, потерянный окружением, поглощается системой. Во всех этих примерах вы не создаете и не уничтожаете энергию; это просто перемещение из одного места в другое. Выражаясь математически, это выглядит так:
Здесь ΔU с система — это полная внутренняя энергия в системе, которая всегда равна ΔU с окружения — полная энергия в окружении.
Одна важная вещь, которую следует помнить о Первом законе, заключается в том, что преобразование энергии не является эффективным на 100%. В нашем примере с лампочкой вы можете преобразовать электрическую энергию в пригодную для использования форму световой энергии, но при этом вы создаете бесполезную энергию в виде тепла.
Применительно к электронике Первый закон термодинамики похож на Текущий закон Кирхгофа. Этот хорошо известный закон гласит, что количество тока, входящего в узел, равно количеству тока, выходящего из узла.Неважно, сколько у вас узлов, что входит, то и выходит.
Этот хорошо известный закон гласит, что количество тока, входящего в узел, равно количеству тока, выходящего из узла.Неважно, сколько у вас узлов, что входит, то и выходит.
На изображении ниже у нас есть два тока, входящие в узел, и три потока, выходящие из узла. В соответствии с текущим законом Кирхгофа отношение между текущими входами и выходами узлов может быть представлено как:
Текущий закон Кирхгофа. (Источник изображения)
Разве это не выглядит странно знакомым для нашего уравнения баланса между системами и окружающей средой?
Второй закон термодинамики
Второй закон термодинамики, также известный как закон возрастающей энтропии, гласит, что с течением времени состояние дезорганизации или энтропия в системе всегда будет увеличиваться.Что мы подразумеваем под этим? Возьмем этот пример — почему ваш стол всегда становится все более грязным в течение недели? Или, что более важно, почему ваш офис не превращается из грязного в чистый без вашего участия? Это стрела времени в термодинамике. Со временем увеличивается и дезорганизация.
Со временем увеличивается и дезорганизация.
Это явление происходит в любой системе. Со временем полезная энергия в конечном итоге уступит место бесполезной энергии. Хотя энергия не может быть создана или уничтожена в соответствии с Первым законом, она может перейти из полезного состояния в менее полезное состояние, например тепловую энергию (тепло).
Со временем каждая система переходит из состояния низкой энтропии в состояние высокой. (Источник изображения)
Снова в нашем примере с лампочкой: чем дольше мы оставляем лампочку включенной, преобразовывая электрическую энергию в энергию излучения, тем больше полезной энергии мы продолжаем преобразовывать в бесполезную энергию в виде тепла. Поскольку полезная энергия внутри системы уменьшается, а неиспользуемая энергия увеличивается, мы говорим, что энтропия системы увеличилась. Математически заявлено:
Здесь общая энтропия ΔS Universe внутри Вселенной равна общей энтропии внутри системы ΔS sys плюс полная энергия всего окружения ΔS surr , каждая из которых не может быть меньше 0. Почему? Потому что во все времена, в любое время суток вся энергия трансформируется из одной формы в другую, и одна из этих форм является непригодной для использования энергией. Вождение автомобиля использует механическую энергию для производства кинетической энергии движения, но при этом вы также превращаете массу энергии в тепло. Это неизбежный побочный продукт.
Почему? Потому что во все времена, в любое время суток вся энергия трансформируется из одной формы в другую, и одна из этих форм является непригодной для использования энергией. Вождение автомобиля использует механическую энергию для производства кинетической энергии движения, но при этом вы также превращаете массу энергии в тепло. Это неизбежный побочный продукт.
Еще один способ представить энтропию — это вероятности. Возьмем, к примеру, коробку, наполненную кусочками головоломки. Какова вероятность того, что вы выбросите все части головоломки из коробки, и одна из них случайно приземлится там, где идеально соединяется с другой частью? Это низкая вероятность.Какова вероятность того, что в той же коробке фигура окажется случайным образом там, где она не подходит к другой фигуре? Это высокая вероятность.
Полный хаос! Энтропия берет верх над вероятностью. (Источник изображения)
В этом примере головоломки случайно расположенная часть головоломки представляет собой высшую форму беспорядка или энтропии. Вот почему шины выпускают воздух при проколе, или почему льдинки, оставленные при комнатной температуре, в конце концов тают, или почему электроны в цепи перетекают от отрицательного к положительному.Конечно, все эти действия могут происходить в обратном порядке, но вероятность того, что они произойдут, настолько мала, а карты с возрастающей вероятностью сложены так высоко, что они просто никогда не происходят.
Вот почему шины выпускают воздух при проколе, или почему льдинки, оставленные при комнатной температуре, в конце концов тают, или почему электроны в цепи перетекают от отрицательного к положительному.Конечно, все эти действия могут происходить в обратном порядке, но вероятность того, что они произойдут, настолько мала, а карты с возрастающей вероятностью сложены так высоко, что они просто никогда не происходят.
В электронике мы видим второй закон термодинамики в сочетании с эффектом Зеебека. Это явление возникает, когда к одному из двух проводников прикладывается тепло, что заставляет нагретые электроны течь к более холодному проводнику. Если вы соедините эту пару нагретых проводников вместе в цепи, то эффект нагрева вызовет постоянный ток (DC), протекающий через цепь.В этой ситуации у нас есть электроны в более низком состоянии энтропии в холодном проводнике, достигающие более высокого состояния энтропии за счет приложения тепла, и поэтому беспорядок увеличивается.
Эффект Зеебека с использованием тепла для создания постоянного тока. (Источник изображения)
(Источник изображения)
Третий закон термодинамики
Третий закон термодинамики гласит, что идеальная кристаллическая структура при абсолютном нуле температуры будет иметь нулевой беспорядок или энтропию. Однако если в этой кристаллической структуре есть хоть малейший намек на несовершенство, то и энтропия будет минимальной.Однако этот закон становится немного странным, потому что даже при нуле Кельвина все еще происходит некоторое движение атомов, поэтому он немного теоретический. Несмотря на это, этот закон позволяет нам понять, что по мере того, как энтропия системы приближается к температуре абсолютного нуля, энтропия, присутствующая в системе, уменьшается.
Третий закон термодинамики. (Источник изображения)
Нулевой закон термодинамики
Нулевой закон термодинамики гласит, что если две системы находятся в тепловом равновесии с третьей системой, то первые две системы также находятся в тепловом равновесии друг с другом. Используя наше старое доброе транзитивное свойство равенства:
Используя наше старое доброе транзитивное свойство равенства:
- Если система A находится в равновесии с системой C
- И Система B находится в балансе с Системой C
- Тогда Система А и Система Б также находятся в равновесии друг с другом.
Этот закон позволяет определить направление теплового потока между системами. Если вы знаете температуру набора связанных систем, то вы будете знать, в каком направлении будет перемещаться тепло, исходя из основ теплового равновесия.
Установлено тепловое равновесие между системами. (Источник изображения)
Обратите внимание: хоть мы и рассматриваем нулевой закон в последнюю очередь, на самом деле он идет первым. В 18 веке, когда были определены законы термодинамики, были включены только первые три. Однако ученые поняли, что им необходим четвертый закон, определяющий движение температуры. Вместо того чтобы перенумеровывать все существующие законы и вносить путаницу в существующую литературу, английский ученый Роберт Фаулер придумал название Нулевой закон.
Кто открыл эти законы?
Законы термодинамики не были открыты одним человеком. Развитие восходит к 1600-м годам, когда впервые была сформулирована основная идея тепла и температуры. В 1824 году французский физик Сади Карно первым сформулировал основные принципы термодинамики в своих рассуждениях об эффективности идеальной машины. Первоначально Сади использовал калорическую систему для описания тепла, теряемого во время движения двигателя, которое позже было заменено энтропией во втором законе термодинамики.
Отец термодинамики Сади Карно. (Источник изображения)
В 1850 году немецкий физик Рудольф Клаузиус разработал утверждение Клаузиуса, в котором говорилось, что «тепло обычно не может самопроизвольно переходить от материала с более низкой температурой к материалу с более высокой температурой». Примерно в то же время Уильям Томсон (лорд Кельвин) разработал утверждение Кельвина, в котором говорилось, что «невозможно полностью преобразовать тепло в циклическом процессе [без потери энергии]. Оба эти утверждения легли в основу Первого и Второго законов термодинамики. Третий закон термодинамики был позже разработан немецким химиком Вальтером Нернстом и часто упоминается как теорема Нернста.
Оба эти утверждения легли в основу Первого и Второго законов термодинамики. Третий закон термодинамики был позже разработан немецким химиком Вальтером Нернстом и часто упоминается как теорема Нернста.
Лорд Кельвин, один из великих умов, разработавших законы термодинамики. (Источник изображения)
Собираем все вместе
Посмотрите вокруг себя на этот удивительный мир энергии в движении, и вы увидите законы термодинамики в действии.Будь то процесс преобразования химической энергии пищи в полезную энергию в вашем теле или преобразования механической энергии в кинетическую энергию в автомобиле или самолете. Термодинамика — это образ жизни. Вы даже обнаружите, что законы термодинамики работают в ваших электронных проектах. Такие принципы, как Закон тока Кирхгофа, идеально согласуются с Первым законом термодинамики, утверждающим, что ток, который входит в набор узлов, должен выйти, точно так же, как энергия не может быть создана или уничтожена, а только преобразована. Что касается второго закона термодинамики, у нас есть эффект Зеебека, который можно наблюдать в электрических цепях, где нагретая электроника будет течь к более холодному проводнику, создавая при этом ток в цепи. Здесь мы имеем энтропию в действии, создающую нарастающие состояния беспорядка, куда бы она ни пошла.
Что касается второго закона термодинамики, у нас есть эффект Зеебека, который можно наблюдать в электрических цепях, где нагретая электроника будет течь к более холодному проводнику, создавая при этом ток в цепи. Здесь мы имеем энтропию в действии, создающую нарастающие состояния беспорядка, куда бы она ни пошла.
Что бы вы ни проектировали, вы проектируете в соответствии с законами термодинамики. Примените эти принципы на практике: попробуйте Autodesk EAGLE бесплатно уже сегодня!
Что такое тепловая энергия? — Определение и примеры — Видео и стенограмма урока
Применение тепловой энергии
Давайте рассмотрим простой пример тепловой энергии.Нагревательный элемент печи содержит тепловую энергию, и чем больше вы включаете печь, тем больше внутренней энергии содержит печь. На самом базовом уровне эта тепловая энергия представляет собой движение молекул, из которых состоит металл элемента печи. Я знаю, что вы не можете видеть, как движутся молекулы, но они движутся. Чем быстрее молекулы, тем больше внутренней тепловой энергии они содержат.
Чем быстрее молекулы, тем больше внутренней тепловой энергии они содержат.
Теперь поставим кастрюлю с водой на нагревательный элемент. Что просходит? Печка работает, да? Ну, не так, как мы обычно думаем об этом.Здесь «работа» относится к «движению чего-либо при приложении силы». В частности, тепловая энергия печи заставляет частицы кастрюли и, в конечном итоге, воду двигаться быстрее. Внутренняя энергия нагревательного элемента передается кастрюле и, в конечном счете, воде внутри кастрюли. Эта передача тепловой энергии от плиты к кастрюле и к воде называется теплотой . Очень важно соблюдать эти термины. В этом контексте тепло — это термин, который мы используем для обозначения передачи тепловой энергии от одного объекта или системы к другому, причем передача является ключевой.Тепловая энергия — это энергия, которой обладает объект или система вследствие движения частиц. Они разные — тепло и тепловая энергия.
Вы почувствуете жар, если подержите руку над плитой. Тепло, в свою очередь, ускоряет молекулы внутри кастрюли и воды. Если вы поместите термометр в воду, по мере того, как вода нагревается, вы можете наблюдать, как температура поднимается. Опять же, увеличение внутренней энергии приведет к увеличению температуры.
Тепло, в свою очередь, ускоряет молекулы внутри кастрюли и воды. Если вы поместите термометр в воду, по мере того, как вода нагревается, вы можете наблюдать, как температура поднимается. Опять же, увеличение внутренней энергии приведет к увеличению температуры.
Геотермальная энергия
Геотермальная энергия — еще один пример тепловой энергии. Слово « геотермальный » происходит от греческих слов « гео », что означает «Земля», и « терм », что означает «тепло». Следовательно, геотермальная энергия — это тепловая энергия, содержащаяся в нашей Земле. Большая часть этой геотермальной энергии исходит от быстро движущихся частиц внутри ядра Земли, где температура может достигать 5000 градусов по Цельсию (9000 градусов по Фаренгейту).Тепловая энергия в центре Земли передается на поверхность Земли. Этот теплообмен приводит к тому, что поверхность Земли имеет относительно постоянную температуру, будь то зима или лето.
Этот теплообмен приводит к тому, что поверхность Земли имеет относительно постоянную температуру, будь то зима или лето.
Мы пользуемся этим, используя тепловые насосы. Эти тепловые насосы используют геотермальную энергию для обогрева воздуха зимой и охлаждения летом. В гораздо большем масштабе мы используем геотермальную энергию для производства электроэнергии. Геотермальная энергия является источником возобновляемой энергии , так как это энергия, полученная из природного ресурса, и ее можно восполнить.Другие примеры возобновляемых источников энергии включают ветер и воду.
Итоги урока
Подведем итоги. Тепловая энергия — это энергия, которой обладает объект или система из-за движения частиц внутри этого объекта или системы. Энергия — это просто способность выполнять работу, а работа совершается, когда сила перемещает объект. В этом контексте система представляет собой набор объектов в пределах границ, таких как горшок с водой. Тепловая энергия является примером кинетической энергии , поскольку она возникает из-за движения частиц, причем движение является ключевым.
Тепловая энергия является примером кинетической энергии , поскольку она возникает из-за движения частиц, причем движение является ключевым.
Тепловая энергия приводит к тому, что объект или система имеют температуру, которую можно измерить. Тепловая энергия может передаваться от одного объекта или системы к другому в виде теплоты . Геотермальная энергия — это тепловая энергия внутри Земли, возникающая в результате движения земных частиц. Большая часть этой геотермальной энергии содержится в ядре Земли. Эта геотермальная энергия является возобновляемой энергией , так как это энергия, полученная из природного ресурса, и ее можно восполнить.
Результаты обучения
В конце этого урока вы сможете:
- Давать определение тепловой энергии, энергии, работе, системной и возобновляемой энергии
- Объясните, почему тепловая энергия является кинетической энергией
- Различие между теплом и тепловой энергией
- Опишите, что такое геотермальная энергия, где она находится и как мы ее используем
Теплота, работа и энергия
Теплота (энергия)
Единицей СИ для теплоты или энергии является джоуль (Дж) .
С разностью температур Калория (количество тепла, необходимое для нагревания 1 грамма воды на 1 o C ( или 1 K )).
калорий определяется как количество тепла, необходимое для изменения температуры одного грамма жидкой воды на один градус Цельсия (или один градус Кельвина).
1 Cal = 4.184 J
1 J = 1 WS
= (1 WS) (1/3600 H / S)
= 2.78 10 -4 wh
= 2,78 10 -7 кВт·ч
Тепловой поток (мощность)
Теплопередача только в результате разницы температур называется тепловым потоком. Единицы СИ для теплового потока: Дж/с или ватт (Вт) — то же, что и мощность. Один ватт определяется как 1 Дж/с .
Удельная энтальпия
Удельная энтальпия является мерой полной энергии в единице массы. Обычно используемой единицей СИ является Дж/кг или кДж/кг .
Термин относится к полной энергии, обусловленной как давлением, так и температурой жидкости (такой как вода или пар) в любое заданное время и при любых условиях. В частности, энтальпия представляет собой сумму внутренней энергии и работы, совершаемой приложенным давлением.
Теплоемкость
Теплоемкость системы
- количество тепла, необходимое для изменения температуры всей системы на один градус .
Удельная теплоемкость
Удельная теплоемкость (= удельная теплоемкость) – это количество тепла, необходимое для изменения температуры одной единицы массы вещества на один градус .
Удельная теплоемкость может быть измерена в Дж/г К, Дж/кг К , кДж/кг К, кал/г К или БТЕ/фунт 9 0 9 0 F 9 0 0 2 9 o 9 и более .
Никогда не используйте табличные значения теплоемкости без проверки единиц измерения фактических значений!
Удельную теплоемкость для обычных продуктов и материалов можно найти в разделе «Свойства материала».
Удельная теплоемкость — постоянное давление
Энтальпия — или внутренняя энергия — вещества зависит от его температуры и давления.
Изменение внутренней энергии по отношению к изменению температуры при фиксированном давлении равно Удельной теплоемкости при постоянном давлении — c p .
Удельная теплоемкость — постоянный объем
Изменение внутренней энергии по отношению к изменению температуры при фиксированном объеме — это удельная теплоемкость при постоянном объеме — c v .
Если давление не очень высокое, работой, совершаемой давлением на твердые и жидкие тела, можно пренебречь, а энтальпию можно представить только компонентом внутренней энергии. Можно сказать, что теплоты постоянного объема и постоянного давления равны.
для твердых веществ и жидкостей
C P = C V (1)
Удельное тепло представляет собой количество энергии, необходимую для повышения 1 кг вещества на 1 o C (или 1 K) , и его можно рассматривать как способность поглощать тепло.Единицы удельной теплоемкости в СИ равны Дж/кгК (кДж/кг o Кл) . Вода имеет большую удельную теплоемкость по сравнению со многими другими жидкостями и материалами.
- Вода — хороший теплоноситель!
Количество тепла, необходимое для повышения температуры
количество тепла, необходимое для нагрева субъекта от одного температурного уровня к другому, может быть выражено как:
Q = C P M DT ( 2)
, где
Q = количество тепла (KJ)
C P = Удельная тепловая температура (KJ / KGK)
M = Масса (кг )
dT = разница температур между горячей и холодной стороной (K)
Пример Отопительная вода
Рассмотрим энергию, необходимую для нагрева 1.
0 кг воды от 0 O C до 100 O C до 100 o C , когда удельная температура воды составляет 4,19
9 кДж / кг o C : Q = (4.19 KJ / кг O C ) (1,0 кг) ((100 O C) — (0 O C))
= 419 (KJ)
Работа
Работа и энергия с технической точки зрения — одно и то же, но работа — это результат, когда направленная сила (вектор) перемещает объект в одном и том же направлении.
Количество выполненной механической работы может быть определено уравнением, полученным из ньютоновской механики
Работа = Приложенная сила x Расстояние, пройденное в направлении силы (3)
Откуда
W = Работа (NM, J)
F = Приложенная сила (N)
L = Длина или расстояние перемещены (M)
Работа Также быть описан как продукт приложенного давления и перемещенного объема:
Работа = приложенное давление x перемещенного объема
или
W = P A L (3b)
, где
p = приложенное давление (Н/м 2 , Па)
A = под давлением площадь (м 2 )
l = длина или расстояние, на которое область под давлением перемещается под действием приложенной силы (м)
Пример — Работа, совершаемая силой
Работа, совершаемая силой 100 Н Перемещение тела 50 м можно рассчитать как
W = (100 N) (50 м)
= 9067
= 5000 (NM, J)
Устройство работы Джоуль, Дж, который определяется как количество работы, совершаемой, когда сила 1 ньютон действует на расстоянии 1 м в направлении силы.
1 Дж = 1 Нм
Пример. Работа силы тяжести F
G H г H= MGH
= (100 кг) (9,81 м / с 2 ) (10 м)
= 9810 (NM, J)
где
F г = сила тяжести — или вес (Н)
г = ускорение свободного падения 9.81 (м/с 2 )
h = высота над уровнем моря (м)
В британских единицах единица работы выполняется, когда вес 1 фунт f (0-сила равна 1) поднят вертикально против силы тяжести на расстояние 1 фут . Единица называется lb ft .
Объект массой 10 слагов поднят 10 футов . Совершенную работу можно рассчитать как
W = F г ч
= мг ч
= (10 2 слагов)17405 FT / S 2 ) (10 футов)
= 3217 фунт Ft FT
Пример — Работа из-за изменения скорости
Работа, выполненная, когда масса 100 кг ускоряется из Скорость 10 м / с до скорости 20 м / с может быть рассчитана как
= ((20 м / с) 2 — (10 м / с) 2 ) (100 кг) / 2
= 15000 (NM, J)
, где
V 2 = конечная скорость (м / с)
V 1 = начальная скорость (м / с)
Energy
Energy — это способность делать работа (перевод с греческого — «работа внутри»). Единицей СИ для работы и энергии является джоуль, определяемый как 1 Нм .
Единицей СИ для работы и энергии является джоуль, определяемый как 1 Нм .
Движущиеся объекты могут совершать работу, потому что они обладают кинетической энергией. («кинетический» в переводе с греческого означает «движение»).
Количество кинетической энергии, одержимого объектом, можно рассчитать как
E K = 1/2 MV 2 (4)
00, где
м = масса объекта (кг)
v = скорость (м/с)
Энергия положения уровня (запасенная энергия) называется потенциальной энергией.Это энергия, связанная с силами притяжения и отталкивания между объектами (гравитацией).
Полная энергия системы состоит из внутренней, потенциальной и кинетической энергии. Температура вещества напрямую связана с его внутренней энергией. Внутренняя энергия связана с движением, взаимодействием и соединением молекул внутри вещества. Внешняя энергия вещества связана с его скоростью и местоположением и представляет собой сумму его потенциальной и кинетической энергии.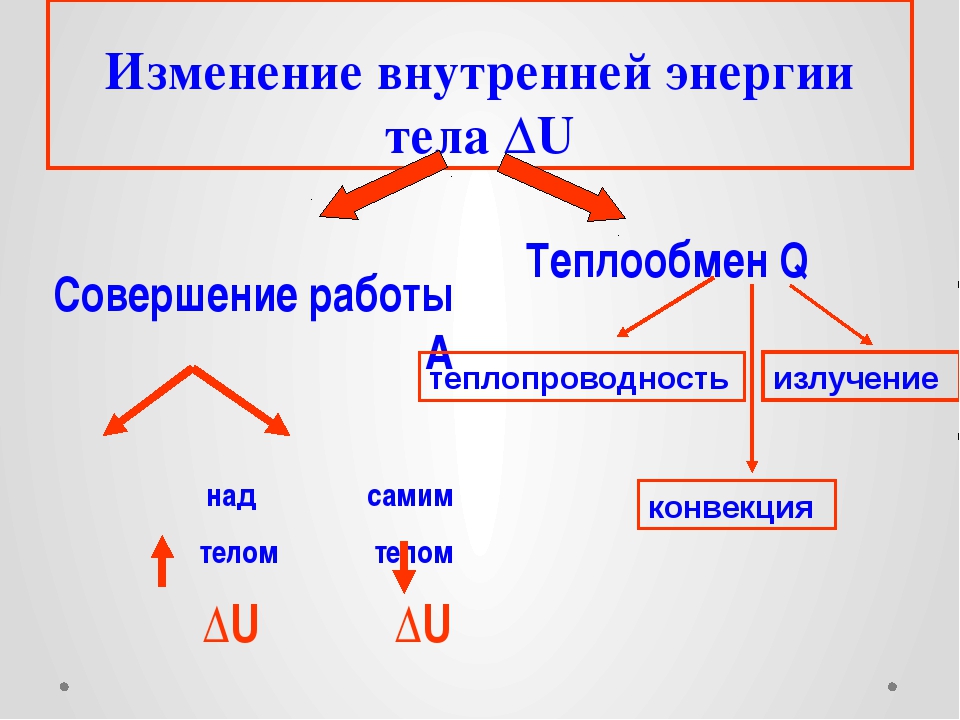

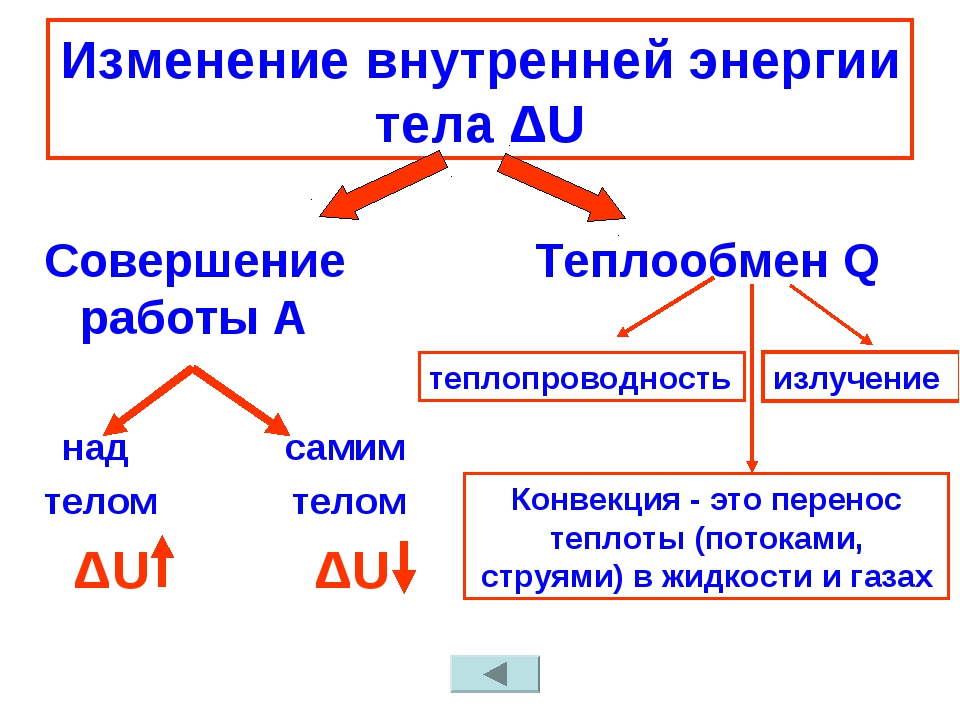





 Каково изменение внутренней энергии системы при отсутствии других изменений (например, температуры или добавления топлива)?
Каково изменение внутренней энергии системы при отсутствии других изменений (например, температуры или добавления топлива)?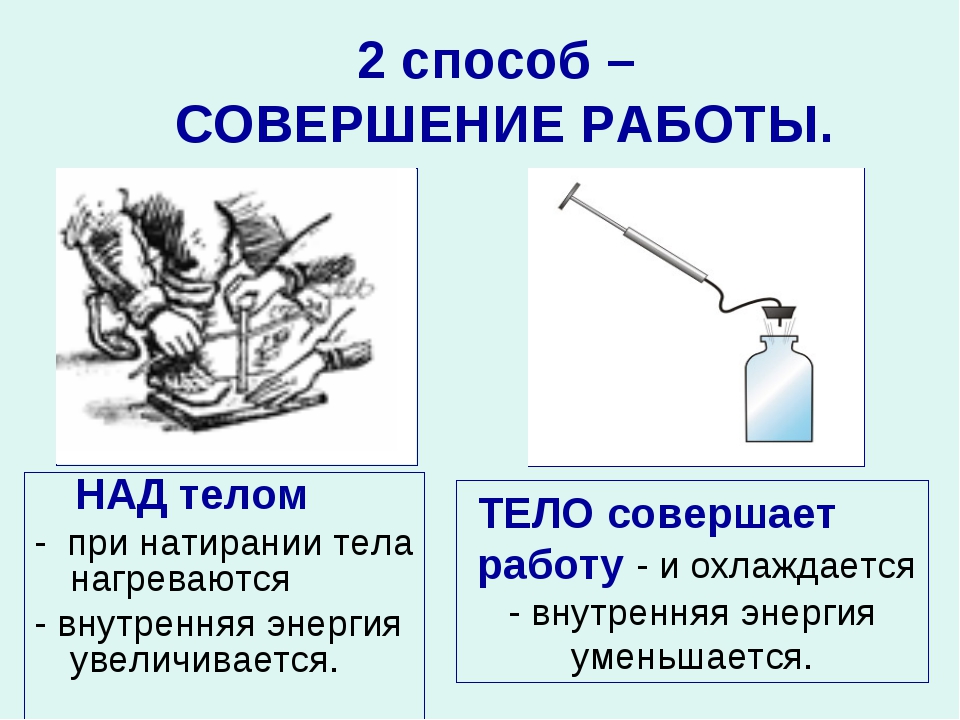 0%? (c) Сравните производительность его работы с дневной мощностью двигателя мощностью 187 Вт (0,250 л.с.).
0%? (c) Сравните производительность его работы с дневной мощностью двигателя мощностью 187 Вт (0,250 л.с.).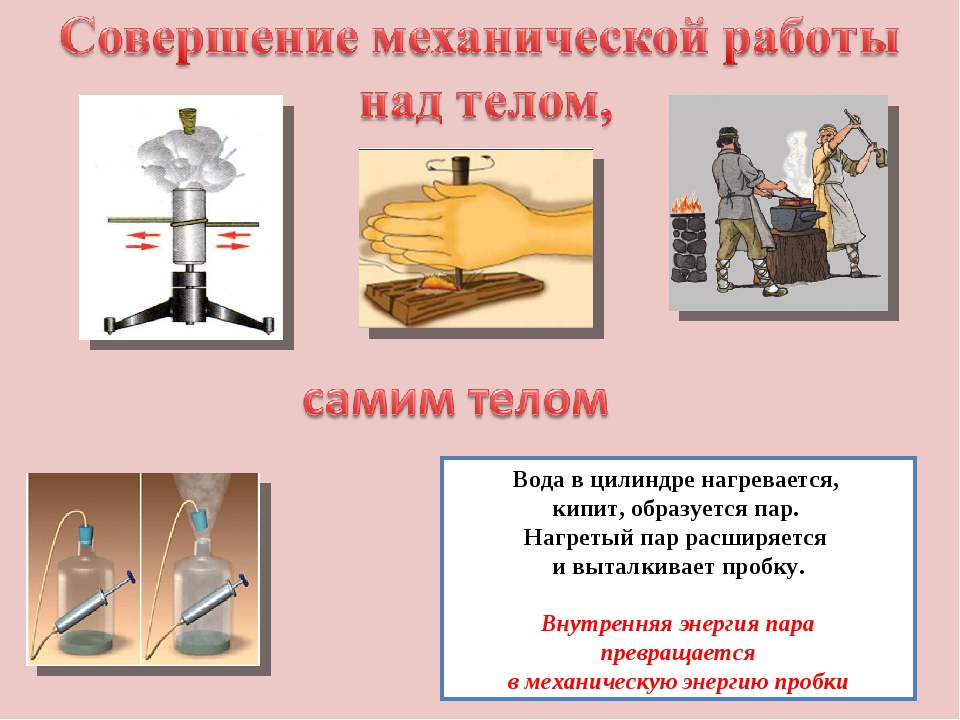 Вы проделали работу с каучуком, и в растянутом состоянии он обладает потенциальной энергией из-за пространственной реконфигурации его материальных компонентов. Некоторая работа, которую вы проделали, также заставила резину «нагреться», что вы можете подтвердить, повторяя это несколько раз, а затем быстро прижимая резину к губам. Резина чувствует себя теплее после многократного растяжения.(Губы более чувствительны к небольшим изменениям температуры, чем другие части тела.) Итак, в этом эксперименте проделанная вами работа изменяет как потенциальную энергию, так и кинетическую энергию (молекулярного движения) резиновой ленты.
Вы проделали работу с каучуком, и в растянутом состоянии он обладает потенциальной энергией из-за пространственной реконфигурации его материальных компонентов. Некоторая работа, которую вы проделали, также заставила резину «нагреться», что вы можете подтвердить, повторяя это несколько раз, а затем быстро прижимая резину к губам. Резина чувствует себя теплее после многократного растяжения.(Губы более чувствительны к небольшим изменениям температуры, чем другие части тела.) Итак, в этом эксперименте проделанная вами работа изменяет как потенциальную энергию, так и кинетическую энергию (молекулярного движения) резиновой ленты. Вы также проделали некоторую дополнительную работу в своем теле из-за мышечной активности (как отмечалось выше). Таким образом, неправильно говорить, что общая работа 90 599, которую вы сделали 90 600, была только работой, проделанной над книгой. Ваше тело действует как машина, а машины всегда тратят впустую часть энергии, которую они потребляют. Под «отходами» мы подразумеваем, что не вся энергия машины идет на выполнение задачи, для которой она предназначена; это не то, что мы называем «полезной работой».
Вы также проделали некоторую дополнительную работу в своем теле из-за мышечной активности (как отмечалось выше). Таким образом, неправильно говорить, что общая работа 90 599, которую вы сделали 90 600, была только работой, проделанной над книгой. Ваше тело действует как машина, а машины всегда тратят впустую часть энергии, которую они потребляют. Под «отходами» мы подразумеваем, что не вся энергия машины идет на выполнение задачи, для которой она предназначена; это не то, что мы называем «полезной работой». После столкновения он покоится, и его кинетическая энергия движения равна нулю.Но его внутренняя энергия движения увеличилась (тепловая энергия), но это хаотическое движение миллионов частиц, движущихся во всех возможных направлениях. Это неорганизованное движение не способствует какому-либо движению книги в целом.
После столкновения он покоится, и его кинетическая энергия движения равна нулю.Но его внутренняя энергия движения увеличилась (тепловая энергия), но это хаотическое движение миллионов частиц, движущихся во всех возможных направлениях. Это неорганизованное движение не способствует какому-либо движению книги в целом.
 0 кг воды от 0 O C до 100 O C до 100 o C , когда удельная температура воды составляет 4,19
0 кг воды от 0 O C до 100 O C до 100 o C , когда удельная температура воды составляет 4,19