Расширенная периодическая таблица элементов — Википедия
Материал из Википедии — свободной энциклопедии
Расши́ренная периоди́ческая табли́ца элеме́нтов была предложена Гленом Сиборгом в 1969 году. Она явилась логическим продолжением принципов периодической системы химических элементов Д. И. Менделеева, также призвана включить возможные необнаруженные химические элементы.
Все необнаруженные элементы названы Международным союзом теоретической и прикладной химии (ИЮПАК) по стандарту образования кодового наименования, существующего до тех пор, пока не будет открыт соответствующий элемент, подтверждён, и официальное название не будет утверждено.
Синий символ в заголовке каждой колонки показывает размещение каждого элемента в каждом блоке в расширенной периодической таблице элементов. Однако, он не всегда показывает количество электронов на орбитали (например, меди).
Красный номер с левой стороны каждой строки показывает период.
Гелий помещён после водорода потому, что является частью группы
| № | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 | 1 H | 2 He | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 | 3 Li | 4 Be | 5 B | 6 C | 7 N | 8 O | 9 F | 10 Ne | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 | 11 Na | 12 Mg | 13 Al | 14 Si | 15 P | 16 S | 17 Cl | 18 Ar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 | 19 K | 20 Ca | 21 Sc | 22 Ti | 23 V | 24 Cr | 25 Mn | 26 Fe | 27 Co | 28 Ni | 29 Cu | 30 Zn | 31 Ga | 32 Ge | 33 As | 34 Se | 35 Br | 36 Kr | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5 | 37 Rb | 38 Sr | 39 Y | 40 Zr | 41 Nb | 42 Mo | 43 Tc | 44 Ru | 45 Rh | 46 Pd | 47 Ag | 48 Cd | 49 In | 50 Sn | 51 Sb | 52 Te | 53 I | 54 Xe | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6 | 55 Cs | 56 Ba | 57 La | 58 Ce | 59 Pr | 60 Nd | 61 Pm | 62 Sm | 63 Eu | 64 Gd | 65 Tb | 66 Dy | 67 Ho | 68 Er | 69 Tm | 70 Yb | 71 Lu | 72 Hf | 73 Ta | 74 W | 75 Re | 76 Os | 77 Ir | 78 Pt | 79 Au | 80 Hg | 81 Tl | 82 Pb | 83 Bi | 84 Po | 85 At | 86 Rn | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7 | 87 Fr | 88 Ra | 89 Ac | 90 Th | 91 Pa | 92 U | 93 Np | 94 Pu | 95 Am | 96 Cm | 97 Bk | 98 Cf | 99 Es | 100 Fm | 101 Md | 102 No | 103 Lr | 104 Rf | 105 Db | 106 Sg | 107 Bh | 108 Hs | 109 Mt | 110 Ds | 111 Rg | 112 Cn | 113 | 114 Fl | 115 Mc | 116 Lv | 117 Ts | 118 Og | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 8 | 119 Uue | 120 Ubn | 121 Ubu | 122 Ubb | 123 Ubt | 124 Ubq | 125 Ubp | 126 Ubh | 127 Ubs | 128 Ubo | 129 Ube | 130 Utn | 131 Utu | 132 Utb | 133 Utt | 134 Utq | 135 Utp | 136 Uth | 137 Uts | 138 Uto | 139 Ute | 140 Uqn | 141 Uqu | 142 Uqb | 143 Uqt | 144 Uqq | 145 Uqp | 146 Uqh | 147 Uqs | 148 Uqo | 149 Uqe | 150 Upn | 151 Upu | 152 Upb | 153 Upt | 154 Upq | 155 Upp | 156 Uph | 157 Ups | 158 Upo | 159 Upe | 160 Uhn | 161 Uhu | 162 Uhb | 163 Uht | 164 Uhq | 165 Uhp | 166 Uhh | 167 Uhs | 168 Uho | ||||||||||||||||||||||||||||||||||||||||||||||||
| 9 | 169 Uhe | 170 Usn | 171 Usu | 172 Usb | 173 Ust | 174 Usq | 175 Usp | 176 Ush | 177 Uss | 178 Uso | 179 Use | 180 Uon | 181 Uou | 182 Uob | 183 Uot | 184 Uoq | 185 Uop | 186 Uoh | 187 Uos | 188 Uoo | 189 Uoe | 190 Uen | 191 Ueu | 192 Ueb | 193 Uet | 194 Ueq | 195 Uep | 196 Ueh | 197 Ues | 198 Ueo | 199 Uee | 200 Bnn | 201 Bnu | Bnb | 203 Bnt | 204 Bnq | 205 Bnp | 206 Bnh | 207 Bns | 208 Bno | 209 Bne | 210 Bun | 211 Buu | 212 Bub | 213 But | 214 Buq | 215 Bup | 216 Buh | 217 Bus | 218 Buo | ||||||||||||||||||||||||||||||||||||||||||||||||
Альтернативные периодические таблицы — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 16 июля 2019; проверки требуют 2 правки. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 16 июля 2019; проверки требуют 2 правки.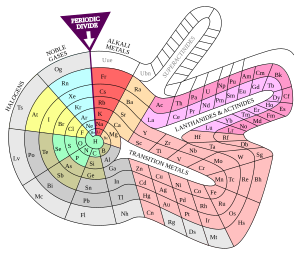 Альтернативная система элементов Теодора Бенфея
Альтернативная система элементов Теодора БенфеяАльтернативные периодические таблицы
являются табличным представлением химических элементов, которое значительно отличаются от организации элементов в Периодической таблице Менделеева. В настоящее время различными авторами предложено множество вариантов, которые в основном нацелены на дидактическое преподнесение материала, так как не все корреляции между химическими элементами видны из стандартной Периодической системы.Альтернативные периодические таблицы часто разрабатываются для того, чтобы выделить или подчеркнуть различные химические или физические свойства элементов, которые неочевидны для традиционной периодической таблицы. Цели некоторых таблиц заключаются в том, чтобы подчеркнуть структуру электронного и ядерного строения атомов. В других элементы расположены во временной шкале по мере их открытия человеком.
Хотя сам Д. И. Менделеев в течение своей жизни публиковал различные варианты периодической таблицы, и интерес к её форме и структуре сохранялся и впоследствии, тем не менее считается, что первая научная работа, целиком посвященная форме периодической таблицы, вышла лишь в 1988 году.
Левосторонняя система Жанета (1928) считается наиболее значительной альтернативой традиционному описанию периодической системы. В ней элементы расположены согласно заполнению атомных орбиталей и она часто используется физиками. Её современная версия, известная как ADOMAH Periodic Table (2006), удобна для написания электронной конфигурации атомов.
В периодической системе Теодора Бенфея (1960) элементы образуют двухмерную спираль, которая, раскручиваясь, опоясывает острова с переходными металлами, лантаноидами и актиноидами. В данной модели появляются ещё не открытые, но предсказанные g-элементы (с атомными числами от 121 до 138). Подобное строение имеет так называемая Химическая Галактика (англ.)русск. [источник не указан 117 дней] , предложенная Филиппом Стюартом.
В расширенной версии Периодической таблицы, предложенной Г. Т. Сиборгом в 1969 году, зарезервированы места до элемента с атомным номером 218.
 Цветок Менделеева
Цветок МенделееваФизическая периодическая система, предложенная Тиммоти Стове, является трёхмерной с тремя осями, на которых отложены главное, орбитальное и магнитное квантовые числа.
Другой подход основан на том, что кластеры атомов одного элемента имеют свойства единственного атома другого элемента. На этом основано предложение расширить периодическую таблицу вторым слоем, где будут представлены такие кластерные соединения. Самое последние добавление к такой «многоэтажной» таблице — это отрицательно заряженный кластер атомов алюминия Al
В таблице Рональда Рича химический элемент может появляться в таблице при необходимости несколько раз.
Вариант, названный «Цветком Менделеева», по мнению авторов, является эстетической версией таблицы химических элементов и представляет собой трехмерный многолепестковый цветок, в котором каждый лепесток представлен атомами с определенным орбитальным квантовым числом.[3][4]
Короткая форма периодической системы элементов — Википедия
Материал из Википедии — свободной энциклопедии
 Таблица Менделеева по изданию 1871 года с прочерками у предсказанных, но ещё не открытых элементов
Таблица Менделеева по изданию 1962 года
Таблица Менделеева по изданию 1871 года с прочерками у предсказанных, но ещё не открытых элементов
Таблица Менделеева по изданию 1962 годаКороткая форма периодической системы элементов — один из способов изображения периодической системы химических элементов, восходящий к первоначальной версии таблицы Д. И. Менделеева[1]. Короткая форма таблицы Менделеева основана на параллелизме степеней окисления элементов главных и побочных подгрупп: например, максимальная степень окисления ванадия равна +5, как у фосфора и мышьяка, максимальная степень окисления хрома равна +6, как у серы и селена, и т. д. В таком виде таблица была опубликована Менделеевым в 1871 году[2].
Короткая форма таблицы была широко распространена и популяризовывалась. Так, например, будущий академик Б. М. Кедров писал в своей книге «Периодический закон Д. И. Менделеева и его философское значение» (1947 г.)
 | Тот факт, что результаты электронной теории так легко и естественно уложились в как бы специально предназначенные для них Менделеевым подвижные табличные формы, еще раз доказывает, что именно короткая таблица и именно с точки зрения электронного строения атома является наиболее совершенной для выражения периодической системы как естественной системы элементов. |  |
Короткая форма таблицы отменена ИЮПАК в 1989 году. Из современной иностранной литературы короткая форма исключена полностью, вместо неё используется длинная форма, однако, благодаря своей привычности и распространённости, она все ещё периодически встречается в российских справочниках и пособиях[3], а также используется в школах для изучения, поскольку стехиометрическая (формальная) валентность элемента связана с номером его группы именно в короткой форме таблицы Менделеева . Такую ситуацию некоторые исследователи связывают в том числе с кажущейся рациональной компактностью короткой формы таблицы, а также с инерцией, стереотипностью мышления и невосприятием современной (международной) информации[4].
Водород в короткой форме таблицы иногда помещают в 7-ю группу[6].
- ↑ «Химическая энциклопедия», статья ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ: Структура периодической системы, изд. «Советская энциклопедия», М., 1988.
- ↑ Scerri 2007, p. 112
- ↑ Р. САЙФУЛЛИН, А. САЙФУЛЛИН Современная форма таблицы Менделеева // Наука и жизнь № 7 , 2004
- ↑ Р. С. Сайфуллин, А. Р. Сайфуллин, «Новая таблица Менделеева», Химия и жизнь, 2003, № 12, стр. 14—17. (В виде PDF-файла (недоступная ссылка) — 6,0 МБ — на сайте «Единой Коллекции цифровых образовательных ресурсов… Архивная копия от 18 марта 2016 на Wayback Machine».)
- ↑ Для облегчения восприятия символы элементов главных и побочных подгрупп выравниваются в ячейках таблицы в разные стороны. В первом варианте таблицы символы элементов главных подгрупп выровнены влево, а символы элементов побочных подгрупп — вправо. Приводимый здесь вариант отличается тем, что в первой строке каждого периода символы элементов выровнены влево, а во второй строке — вправо. Таким образом выравнивание оказывается одинаковым, но ради этого подгруппы перемешиваются. Во втором и третьем периоде, которые состоят только из одной строки, используется смешанное выравнивание
- ↑ Некрасов Б. В., Основы общей химии, т. 1, 1973, с. 238.
- Scerri, Eric. The periodic table: Its story and its significance (англ.). — Oxford: Oxford University Press, 2007. — ISBN 0-19-530573-6.
- Mazurs, E.G. Graphical Representations of the Periodic System During One Hundred Years (англ.). — Alabama: University of Alabama Press (англ.)русск., 1974. — ISBN 978-0-8173-3200-6.
- Некрасов Б.В. Основы общей химии. — 3-е изд. — М.: Химия, 1973. — Т. 1. — 656 с.
- Советский энциклопедический словарь. — М.: Издательство Советская Энциклопедия, 1980. — С. 1000. — 1600 с., с илл.
Короткая форма периодической системы химических элементов Д. И. Менделеева
Период (химия) — Википедия
Материал из Википедии — свободной энциклопедии
Период — строка периодической системы химических элементов, последовательность атомов по возрастанию заряда ядра и заполнению электронами внешней электронной оболочки.
Периодическая система имеет семь периодов. Первый период, содержащий 2 элемента, а также второй и третий, насчитывающие по 8 элементов, называются малыми. Остальные периоды, имеющие 18 и более элементов — большими. Номер периода, к которому относится химический элемент, определяется числом его электронных оболочек (энергетических уровней).
Каждый период (за исключением первого) начинается типичным металлом (Li, Nа, К, Rb, Cs, Fr) и заканчивается благородным газом (Ne, Ar, Kr, Хе, Rn, Og), которому предшествует типичный неметалл.
В первом периоде, кроме гелия, имеется только один элемент — водород, сочетающий свойства, типичные как для металлов, так и (в большей степени) для неметаллов. У этих элементов заполняется электронами 1s-подоболочка.
У элементов второго и третьего периода происходит последовательное заполнение s— и р-подоболочек. Для элементов малых периодов характерно достаточно быстрое увеличение электроотрицательности с увеличением зарядов ядер, ослабление металлических свойств и усиление неметаллических.
Четвёртый и пятый периоды содержат декады переходных d-элементов (от скандия до цинка и от иттрия до кадмия), у которых после заполнения электронами внешней s-подоболочки заполняется, согласно правилу Клечковского, d-подоболочка предыдущего энергетического уровня.
1s
2s 2p
3s 3p
4s 3d 4p
5s 4d 5p
6s 4f 5d 6p
7s 5f 6d 7p
6f 7d 7f
...
В шестом и седьмом периоде происходит насыщение 4f— и 5f-подоболочек, вследствие чего они содержат ещё на 14 элементов больше по сравнению с 4-м и 5-м периодами (лантаноиды в шестом и актиноиды в седьмом периоде).
Вследствие различия периодов по длине и другим признакам существуют разные способы их относительного расположения в периодической системе. В короткопериодном варианте, малые периоды содержат по одному ряду элементов, большие имеют по два ряда. В длиннопериодном варианте все периоды состоят из одного ряда. Ряды лантаноидов и актиноидов обычно записывают отдельно внизу таблицы.
| Малые периоды | Большие периоды | |
| Количество элементов | 2 или 8 | 18 и более |
| Распределение электронов | заполняются только s— и р-подоболочки | заполняются также предвнешние d-подоболочки и предпредвнешние f-подоболочки |
| Изменение свойств элементов | металлические свойства быстро убывают | медленный переход от металлических свойств к неметаллическим |
Элементы одного периода имеют близкие значения атомных масс, но разные физические и химические свойства, в отличие от элементов одной группы. С возрастанием заряда ядра у элементов одного периода уменьшается атомный радиус и увеличивается количество валентных электронов, вследствие чего происходит ослабление металлических и усиление неметаллических свойств элементов, ослабление восстановительных и усиление окислительных свойств образуемых ими веществ.
Группа периодической системы — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 21 сентября 2018; проверки требуют 7 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 21 сентября 2018; проверки требуют 7 правок.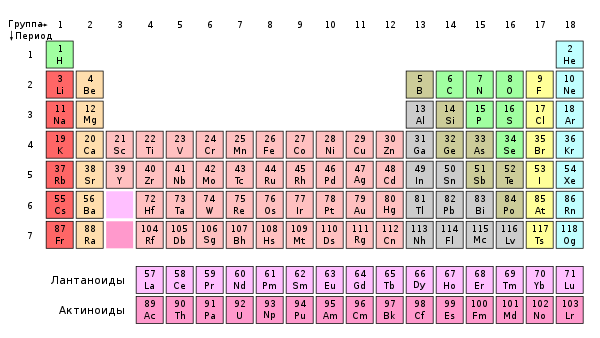
Гру́ппа периодической системы химических элементов — последовательность атомов по возрастанию заряда ядра, обладающих однотипным электронным строением.
Номер группы определяется количеством электронов на внешней оболочке атома (валентных электронов) и, как правило, соответствует высшей валентности атома.
В короткопериодном варианте периодической системы группы подразделяются на подгруппы — главные (или подгруппы A), начинающиеся с элементов первого и второго периодов, и побочные (подгруппы В), содержащие d-элементы. Подгруппы также имеют названия по элементу с наименьшим зарядом ядра (как правило, по элементу второго периода для главных подгрупп и элементу четвёртого периода для побочных подгрупп). Элементы одной подгруппы обладают сходными химическими свойствами.
С возрастанием заряда ядра у элементов одной группы из-за увеличения числа электронных оболочек увеличиваются атомные радиусы, вследствие чего происходит снижение[источник не указан 1019 дней]электроотрицательности, усиление[источник не указан 1019 дней]металлических и ослабление[источник не указан 1019 дней]неметаллических свойств элементов, усиление восстановительных и ослабление окислительных свойств образуемых ими веществ.
С 1989 года Международным союзом теоретической и прикладной химии (IUPAC) в качестве основного варианта периодической системы утверждена длиннопериодная форма[1]. В связи с этим IUPAC рекомендует сплошную нумерацию групп: арабскими цифрами от 1 до 18.
Несмотря на это, продолжают применяться ставшие традиционными системы нумерации с использованием римских цифр и латинских букв, отличающиеся для Америки и Европы.
Современная система нумерации содержит следующие группы (старые системы, европейская и американская, приведены в скобках):
- Группа 1 (IA, IA): щелочные металлы
- Группа 2 (IIA, IIA): щёлочноземельные металлы
- Группа 3 (IIIB, IIIA): подгруппа скандия
- Группа 4 (IVB, IVA): подгруппа титана
- Группа 5 (VB, VA): подгруппа ванадия
- Группа 6 (VIB, VIA): подгруппа хрома
- Группа 7 (VIIB, VIIA): подгруппа марганца
- Группа 8 (VIIIВ, VIIIA): подгруппа железа
- Группа 9 (VIIIВ, VIIIA): подгруппа кобальта
- Группа 10 (VIIIВ, VIIIA): подгруппа никеля
- Группа 11 (IB, IB): подгруппа меди
- Группа 12 (IIB, IIB): подгруппа цинка
- Группа 13 (IIIA, IIIB): подгруппа бора
- Группа 14 (IVA, IVB): подгруппа углерода
- Группа 15 (VA, VB): подгруппа азота (пниктогены)
- Группа 16 (VIA, VIB): подгруппа кислорода (халькогены)
- Группа 17 (VIIA, VIIB): галогены
- Группа 18 (VIIIA, VIIIB)[2]: инертные газы
- ↑ Сайфуллин Р. С., Сайфуллин А. Р. Новая таблица Менделеева // Химия и жизнь.— 2003.— № 12.— С. 14—17.
- ↑ Подгруппа гелия (инертные газы) иногда, особенно в старых изданиях, обозначается цифрой 0.
Седьмой период периодической системы — Википедия
Материал из Википедии — свободной энциклопедии
К седьмо́му пери́оду периоди́ческой систе́мы относятся элементы седьмой строки (или седьмого периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов в химических свойствах элементов при увеличении атомного числа: новая строка начинается тогда, когда химические свойства повторяются, что означает, что элементы с аналогичными свойствами попадают в один и тот же вертикальный столбец. Седьмой период содержит 32 элемента (столько же, сколько и предыдущий), в том числе включает особую группу элементов — актиноиды. В него входят: франций, радий, актиний, торий, протактиний, уран, нептуний, плутоний, америций, кюрий, берклий, калифорний, эйнштейний, фермий, менделеевий, нобелий, лоуренсий, резерфордий, дубний, сиборгий, борий, хассий, мейтнерий, дармштадтий, рентгений, коперниций, нихоний, флеровий, московий, ливерморий, теннессин и оганесон.
Все элементы седьмого периода являются радиоактивными. Этот период содержит самый тяжёлый элемент, встречающийся на Земле в естественном виде — уран. Большинство последующих элементов были синтезированы искусственно. Хотя некоторые из них (например, плутоний) теперь доступны в многотонных количествах, большинство из них крайне редки и получены лишь в количествах несколько микрограмм или даже меньше. Некоторые из последних элементов синтезированы в лабораториях совсем недавно в количестве нескольких атомов.
Хотя редкость многих из этих элементов означает, что экспериментальных результатов накоплено не так много, но уже сейчас можно сказать, что тенденции в поведении по группам в 7 периоде, по всей видимости, менее выражены по сравнению с другими периодами. Хотя франций и радий действительно показывают типичные (и даже наиболее резко выраженные) свойства групп 1 и 2 соответственно, актиноиды демонстрируют гораздо большее разнообразие поведения и степени окисления, чем лантаноиды. Предварительные исследования показывают, что элемент группы 14 флеровий (находящийся в таблице Менделеева под свинцом), по-видимому, является инертным газом, а не чистым металлом, а элемент группы 18 оганесон, вероятно, не является инертным газом. Эти особенности периода 7 могут быть связаны с рядом факторов, в том числе значительным влиянием спин-орбитального взаимодействия и релятивистских эффектов, в конечном счёте вызванных очень высоким положительным электрическим зарядом их массивных атомных ядер.
Этот период имеет большое количество исключений из правила Клечковского, к ним относятся: актиний (Ac), торий (Th), протактиний (Pa), уран (U), нептуний (Np), кюрий (Cm) и, возможно, лоуренсий (Lr), дармштадтий (Ds), берклий (Bk) и резерфордий (Rf) (исследования по некоторым элементам не завершены).
Обсуждение:Периодическая система химических элементов — Википедия
Материал из Википедии — свободной энциклопедии
внезапно — исследователи из Сибирского федерального университета (СФУ) развеяли миф о том, что Дмитрию Менделееву приснилась периодическая таблица химических элементов // 6 февраля 2019
113-й химический элемент таблицы Дмитрия Менделеева называется рикений. Стоит ли обновить таблицу? 94.180.100.9 16:09, 21 января 2016 (UTC)
- АИ есть? —exlex 12:17, 6 января 2016 (UTC)
Недавно элементам под номерами 113-118 даны новые названия. Надо бы внести изменения в таблицу. 217.76.1.22 09:19, 7 декабря 2016 (UTC)
Названия для новых элементов[править код]
- 113-й элемент — Нихоний (Nihonium), символ Nh
- 115-й элемент — Московий (Moscovium), символ Mc
- 117-й элемент — Теннессин (Tennessine), символ Ts
- 118-й элемент — Оганессон (Oganesson), символ Og
https://iupac.org/iupac-is-naming-the-four-new-elements-nihonium-moscovium-tennessine-and-oganesson/ —195.3.129.182 07:33, 9 ноября 2016 (UTC)
119 и 120 элементы[править код]
Свежая и очень важная информация по данным и другим элементам от АИ (ТАСС). Оставляю данную информацию как резерв, так как я сейчас на работе, нет времени на редактирование статьи. Так что можете приложить руку к редактированию, освежить, так сказать, данные. —Sheih82 14:52, 5 апреля 2016 (UTC)
А почему короткую форму постеснялись изобразить? 185.150.154.127 15:38, 22 июня 2016 (UTC)
- Кстати, ссылка 6 вовсе на короткую форму не указывает.185.150.154.127 15:41, 22 июня 2016 (UTC)
Физические и химические свойства неоткрытых элементов[править код]
В некоторых статья о неоткрытых либо искусственно синтезированных элементах (например, Унбинилий, Унуненний, etc) присутствует раздел «Физические и химические свойства». У единичных атомов, которые получены (или возможно, когда-нибудь будут получены), нет и не может быть ни физических, ни химических свойств — ибо это свойства макроскопические. Таковыми свойствами обладает простое вещество, но не элемент. Как-то с этим надо определиться, дабы не вводить читателей в заблуждение. S Levchenkov 15:35, 2 сентября 2016 (UTC)
Последний рисунок («Свойства элементов. Стрелки указывают на повышение») неправильно переведён с английского. Там, где на русском подписано «атомное число», должен быть «атомный радиус». Атомное число не растёт справа налево.Румата Эсторский (обс.) 03:12, 3 января 2018 (UTC)
Обновить ссылку на интерактивную таблицу[править код]
Предлагаю обновить ссылку на ресурс с интерактивной таблицей Менделеева (ссылка «Интерактивная таблица Менделеева») в виду устаревшего оформления. https://periodicable.com считаю более релевантным.