В 1748 году Ломоносов впервые формулирует «всеобщий закон природы» — закон сохранения материи и движения
Ученый-энциклопедист (физик и астроном, историк и филолог) Михаил Васильевич Ломоносов работал в самых различных отраслях науки, но наибольших успехов достиг в области физики и химии.
Он сформулировал самый общий закон естествознания – закон сохранения материи и движения. До Ломоносова закон сохранения движения был выведен Декартом и Лейбницем, которые считали, что при всех явлениях в природе неизменным остается только количество механического движения.
Ломоносов же сформулировал свой закон в 1748 году в следующем виде: «Все перемены, в натуре случающиеся, такого суть состояния, что сколько у одного тела отнимается, столько присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте. Сей всеобщий естественный закон простирается и в самые правила движения: ибо тело, движущее своею силою другое, столько же оные у себя теряет, сколько сообщает другому, которое от него движение получает». Его обоснование закона было дано в письме Ломоносова от 16 (5 ст.ст.) июля 1748 года, адресованном великому математику Леонарду Эйлеру.
Замечательно, что под движением Ломоносов понимал не только механическое перемещение, но и тепловое; по сути дела он высказывал мысль о переходе одних форм движения в другие.
Ломоносов не только сформулировал свой закон, но и применял его. Так, пользуясь этим законом, он объяснил процесс перехода энергии при теплопередаче, процессы, происходящие в охлаждающих смесях, и другие случаи перехода энергии.
Открытый Ломоносовым закон получил более полное обоснование в его работах: «Об отношении количества материи и веса» (1758) и в «Рассуждении о твердости и жидкости тел» (1760). Обе эти работы были опубликованы на латинском языке и, следовательно, получили известность за пределами России. Но осознать значение открытия, сделанного Ломоносовым, многие ученые тех лет так и не смогли.
Однако с развитием физики и техники формулировка закона сохранения энергии все более и более уточняется. Необходимость улучшения тепловых машин и их коэффициента полезного действия заставила более обстоятельно заняться изучением тепловых процессов. Это привело к окончательному выяснению того, что теплота является формой энергии, и к установлению впоследствии Майером, Джоулем, Гельмгольцем и Ленцом механического эквивалента теплоты. Таким образом, Ломоносов является прямым предшественником этих ученых.
www.molgvardia.ru
Закон сохранения вещества — это… Что такое Закон сохранения вещества?
Закон сохранения массы — исторический закон физики, согласно которому масса как мера количества вещества сохраняется при всех природных процессах, то есть несотворима и неуничтожима. С точки зрения современной физики, этот закон неверен. Например, при радиоактивном распаде совокупная масса вещества уменьшается.
Исторический очерк
Закон сохранения массы исторически понимался как одна из формулировок закона сохранения материи. Одним из первых его сформулировал древнегреческий философ Эмпедокл (V век до н. э.):
Ничто не может произойти из ничего, и никак не может то, что есть, уничтожиться.
Позже аналогичный тезис высказывали Демокрит, Аристотель и Эпикур (в пересказе Лукреция Кара). Средневековые учёные также не высказывали никаких сомнений в истинности этого закона.
С появлением понятия массы как меры количества вещества, пропорциональной весу, формулировка закона сохранения материи была уточнена: масса есть инвариант, то есть при всех процессах общая масса не уменьшается и не увеличивается. В 1630 году Жан Рэ (Jean Rey, 1583-1645), доктор из Перигора, писал Мерсенну
Вес настолько тесно привязан к веществу элементов, что, превращаясь из одного в другой, они всегда сохраняют тот же самый вес.
В середине XVIII века опыты Роберта Бойля поставили закон сохранения массы под сомнение — у него при химической реакции вес вещества увеличился. Однако Ломоносов и другие физики вскоре указали Бойлю на его ошибку: увеличение веса происходило за счёт воздуха, а в запаянном сосуде вес сохранялся неизменным. Ломоносов писал Эйлеру:
Все встречающиеся в природе изменения происходят так, что если к чему-либо нечто прибавилось, то это отнимается у чего-то другого. Так, сколько материи прибавляется к какому-либо телу, столько же теряется у другого, сколько часов я затрачиваю на сон, столько же отнимаю от бодрствования и т. д.
В дальнейшем, вплоть до создания физики микромира, закон сохранения массы считался истинным и очевидным. Лавуазье в «Начальном учебнике химии» (1789), приводит точную количественную формулировку закона сохранения массы вещества, однако не объявляет его каким-то новым и важным законом, а просто упоминает мимоходом как о хорошо известном и давно установленном факте. Для химических реакций Лавуазье сформулировал закон так: «Масса всех веществ, вступивших в химическую реакцию, равна массе всех продуктов реакции».
Современное состояние
Как выяснилось, в общефизическом смысле закон сохранения массы, строго говоря, неверен. Ведь, например, электрон и позитрон, каждый из которых обладает массой, могут аннигилировать в фотоны, не имеющие массы покоя. Другой пример: масса дейтрона, состоящего из одного протона и одного нейтрона, не равна сумме масс своих составляющих, поскольку следует учесть энергию взаимодействия частиц.
Таким образом, закон сохранения массы в физике работает с известными оговорками, а на самом деле является ограниченным и частным случаем закона сохранения энергии, с учётом известного соотношения для энергии массы покоя частиц: E=mc².
Примечания
Литература
- Спасский Б. И.. История физики. М., «Высшая школа», 1977.
- Том 1, часть 1-я [1]
- Том 1, часть 2-я [2]
- Том 2, часть 1-я [3]
- Том 2, часть 2-я [4]
Wikimedia Foundation. 2010.
dic.academic.ru
Формулировка закона сохранения массы — урок. Химия, 8–9 класс.
Закон сохранения массы веществ в химических реакциях был сформулирован на основе работ по прокаливанию металлов.
В XVII в. английский учёный Р. Бойль проводил опыты по прокаливанию свинца. После окончания опытов он взвешивал полученные продукты и сравнивал их массу с массой исходного металла. Масса окалины всегда была больше массы свинца.
Русский учёный М. В. Ломоносов повторил опыты Р. Бойля. Но металлы он прокаливал в запаянных стеклянных сосудах — ретортах. Взвешивание сосудов до и после реакции показало, что их масса остаётся неизменной.
В \(1748\) г. М. В. Ломоносов сделал вывод: «Все перемены, в натуре случающиеся, суть такого состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому. Так ежели где убудет материи, то умножится в другом месте».
В \(1789\) г. французский химик А. Лавуазье объяснил причину разных результатов взвешивания веществ в открытых и закрытых сосудах. Он доказал, что образование окалины происходит за счёт присоединения к металлу кислорода, содержащегося в воздухе.
На основе работ М. В. Ломоносова и А. Лавуазье был сформулирован закон сохранения массы.
Масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ.
При химических реакциях атомы не исчезают и не появляются. Продукты реакции образуются из атомов, содержащихся в исходных веществах. Поэтому масса и остаётся неизменной.
Пример:
реакция горения природного газа (метана):
метан \(+\) кислород \(=\) углекислый газ \(+\) вода.
Исходные вещества — метан Ch5 и кислород O2:
Продукты реакции — углекислый газ CO2 и вода h3O:
В молекулах исходных веществ и в молекулах продуктов реакции содержатся атомы углерода, водорода и кислорода. Их число не меняется, поэтому и масса веществ остаётся неизменной.
масса метана \(+\) масса кислорода \(=\) масса углекислого газа \(+\) масса воды,
m(Ch5)+m(O2)=m(CO2)+m(h3O).
www.yaklass.ru
Закон сохранения массы (закон Ломоносова)
Экспериментальное доказательство закона сохранения массы при химических взаимодействиях явилось первым примером количественного химического анализа. Гениальный русский ученый М. В. Ломоносов (1711— 1765), впервые применивший весы и взвешивание для количественного контроля химических превращений и открывший закон сохранения массы, является основоположником количественного анализа. [c.7]Закон сохранения массы и энергии. В 1760 г. Ломоносов, по существу, сформулировал единый закон сохранения массы и энергии «Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимается, столько же присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте… Сей всеобщий естест венный закон распространяется и в самые правила движения, ибо тело, движущее своею силою другое, столько же оныя у себя теряет, сколько сообщает другому, которое от него движение получает». Однако до начала XX в. эти законы обычно рассматривались независимо друг от друга. Химия в основном имела дело с законом сохранения массы вещества, а физика — с законом сохранения энергии. В 1905 г. основоположник современной физики А.Эйнштейн показал, что между массой и энергией существует взаимосвязь, выражаемая уравнением
М. Б. Ломоносов (1711 — 1765) впервые стал систематически применять весы при изучении химических реакций. Б 1756 г. он экспериментально установил один из основных законов природы — закон сохранения массы вещества, составивший основу количественного анализа и имеющий огромное значение для всей науки. М. В. Ломоносов разработал многие приемы химического анализа и исследования, не потерявшие значения до наших дней [c.8]
Химия как точная наука зародилась еще в эпоху полного господства теории флогистона Более определенным временем ее возникновения можно условно считать середину XVIII в., когда М. В. Ломоносов (1711 — 1765) сформулировал закон сохранения массы вещества в химических процессах и доказал его экспериментально. Он же первый высказал мысль, что при нагревании металл соединяется, как он говорил, с частичками воздуха. Заслуга полного и окончательного ниспровержения флогистонной теории принадлежит великому французскому химику А. Лавуазье (1743—1794), который, изучая горение и обжиг металлов, не только выяснил и сделал очевидной для других роль кислорода в этих явлениях, разрушив тем самым теорию флогистона, но также внес ясность в понятия химического элемента, простого и сложного вещества и независимо от Ломоносова экспериментально установил закон сохранения массы в химических реакциях. Начиная с Лавуазье химия заговорила на современном нам языке. Именно его трудами завершился процесс превращения химии в науку. Если Бойль начал этот процесс, то Лавуазье довел его до конца. [c.22]
Закон сохранения массы. На основании молекулярно-атомистических представлений М. В. Ломоносов сделал вывод Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько же присовокупится к другому. Так, ежели где убудет несколько материи, то умножится в другом месте . Позднее, применяя точные методы исследования, ученые подтвердили опытным путем, что при химических превращениях общая масса веществ остается неизменной. Этот закон — закон сохранения массы — в настоящее время формулируется так
В связи со сказанным необходимо реабилитировать гения русской науки — Михаила Васильевича Ломоносова. До сих пор приходится встречаться с ложным утверждением о том, что закон сохранения энергии открыт Ломоносовым. Это утверждение основывается не на каких-либо работах Ломоносова, а на одной фразе в его письме Эйлеру 5 июля 1748 года Так, сколько материи прибавляется какому-либо телу, столько же теряется у другого… Так как это всеобщий закон природы, то он распространяется и на правила движения тело, которое своим толчком возбуждает другое к движению, столько же теряет от своего движения, сколько сообщает другому, им двинутому . Слова очень содержательные. Но, во-первых, они касаются не энергии, а движения — понятия неопределенного, и, во-вторых, сходные мысли были высказаны еще в XVH веке Декартом, утверждавшим, что во Вселенной в.сегда сохраняется одно и то же количество движения. Закона сохранения энергии здесь нет, да и невозможно было открыть его до наступления века пара и электричества. Ломоносов, открывший закон сохранения массы, обосновавший кинетическую теорию тепла, так много сделавший в науке и искусстве, не нуждается в том, чтобы ему приписывали мнимые открытия. [c.16]
Закон сохранения массы и э н е р г и и. Несмотря на то что еще в 1760 г. Ломоносов, по существу, сформулировал единый закон сохранения массы и энергии , до начала XX в. эти законы обычно рассматривались независимо друг от друга. Химия в основном имела дело с законом сохранения массы вещества, а физика — с законом сохранения энергии. В 1905 г. основоположник современной физики А. Эйнштейн показал, что между массой и энергией существует взаимосвязь, количественно выражаемая уравнением [c.9]
На основе достижений современной атомной физики и теории относительности было установлено, что закон сохранения массы тесно связан с законом сохранения энергии (Ломоносов, 1748 г., Мейер, 1842 г.). Соотношение между массой и энергией было установлено Эйнштейном, который показал, что изменение энергии системы прямо пропорционально изменению массы
Закон сохранения массы вещества. Впервые его высказал М. В. Ломоносов в письме к Эйлеру от 5 июня 1748 г., опубликованном на русском языке в 1760 г. Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому… Это определение, за исключением архаичности языка, не устарело. [c.13]
Закон сохранения массы при химических реакциях. В 1756 г. Ломоносов, применяя количественные методы при исследовании химических процессов, установил, что при химических превращениях масса веществ остается неизменной. Это открытие Ломоносова стало одним из основных законов химии, который в настоящее время формулируется следующим образом масса веществ, вступивших в реакцию, всегда равна массе вешаете, образовавшихся в результате реакции. [c.8]
Творческая деятельность Ломоносова отличается исключительной широтой интересов и глубиной проникновения в тайны природы. Его исследования относятся к области физики, химии, астрономии и др. Результаты этих работ заложили основы современного естествознания. Ломоносов указал (1765) на основополагающее значение закона сохранения массы вещества в химических реакциях изложил (1741 —1750) основы корпускулярного (атомно-молекулярного) учения выдвинул (1744—1748) кинетическую теорию теплоты. Был зачинателем применения математических и физических методов исследования в химии и первым начал читать в Пет
www.chem21.info
Закон сохранения массы веществ (м.В.Ломоносов, 1748 г.; а.Лавуазье, 1789 г.).
В начале 20 века формулировка закона сохранения массы подверглась пересмотру в связи с появлением теории относительности (А.Эйнштейн, 1905 г.), согласно которой масса тела зависит от его скорости и, следовательно, характеризует не только количество материи, но и ее движение. Полученная телом энергия DE связана с увеличением его массы Dm соотношением DE = Dm · c2 , где с — скорость света. Это соотношение не используется в химических реакциях, т.к. 1 кДж энергии соответствует изменению массы на ~10-11 г и Dm практически не может быть измерено. В ядерных реакциях, где DЕ в ~106 раз больше, чем в химических реакциях, Dm следует учитывать.
Исходя из закона сохранения массы, можно составлять уравнения химических реакций и по ним производить расчеты. Он является основой количественного химического анализа.
Закон постоянства состава. Впервые сформулировал ж.Пруст (1808 г).
Все индивидуальные химические вещества имеют постоянный качественный и количественный состав и определенное химическое строение, независимо от способа получения. Из закона постоянства состава следует, что при образовании сложного вещества элементы соединяются друг с другом в определенных массовых соотношениях.
Пример.
CuS — сульфид меди. m(Cu) : m(S) = Ar(Cu) : Ar(S) = 64 : 32 = 2 : 1 Чтобы получить сульфид меди (CuS) необходимо смешать порошки меди и серы в массовых отношениях 2 : 1. Если взятые количества исходных веществ не соответствуют их соотношению в химической формуле соединения, одно из них останется в избытке.
Например, если взять 3 г меди и 1 г серы, то после реакции останется 1 г меди, который не вступил в химическую реакцию. Вещества немолекулярного строения не обладают строго постоянным составом. Их состав зависит от условий получения.
Массовая доля элементаw(Э) показывает, какую часть составляет масса данного элемента от всей массы вещества: где n — число атомов; Ar(Э) — относительная атомная масса элемента; Mr — относительная молекулярная масса вещества.
w(Э) = (n · Ar(Э)) / Mr
Зная количественный элементный состав соединения можно установить его простейшую молекулярную формулу:
Обозначают формулу соединения Ax By Cz
Рассчитывают отношение X: Y: Z через массовые доли элементов:
w(A) = (х · Ar(А)) / Mr(AxByCz) w(B) = (y · Ar(B)) / Mr(AxByCz) w(C) = (z · Ar(C)) / Mr(AxByCz)
X = (w(A) · Mr) / Ar(А) Y = (w(B) · Mr) / Ar(B) Z = (w(C) · Mr) / Ar(C)
x : y : z = (w(A) / Ar(А)) : (w(B) / Ar(B)) : (w(C) / Ar(C))
Полученные цифры делят на наименьшее для получения целых чисел X, Y, Z.
Записывают формулу соединения.
studfile.net
Закон сохранения массы веществ (М.В.Ломоносов, 1748 г.; А.Лавуазье, 1756 г.)
Основные химические понятия и законы.
1.Место и значение химии в системе наук.
Современная химия представляет собой систему научных дисциплин: общей,
неорганической, аналитической, органической физической, коллоидной химии,… Как всякая наука, химия изучает некоторую часть явлений окружающего мира. Химия играет значительную роль в научно-техническом прогрессе. Нет ни одной отрасли не связанной в той или иной мере с применением химии.
Основные понятия и законы химии
Химия – наука о свойствах вещества и его превращениях, она включает в себя законы и принципы, описывающие эти превращения, а так же представления и теории, позволяющие дать им объяснение.
Атомно-молекулярное учение заключается в следующем:
1. Все вещества состоят из молекул.
2. Молекулы состоят из атомов.
3. Молекулы и атомы находятся в непрерывном движении; между ними существуют силы притяжения и отталкивания.
Рассмотрим следующие определения:
Вещество – вид материи, которая обладает массой покоя.
Состоит из элементарных частиц: электронов, протонов, нейтронов, мезонов и др. Химия изучает главным образом вещество, организованное в атомы, молекулы, ионы и радикалы. Такие вещества принято подразделять на простые и сложные (хим. соединения). Простые вещества образованы атомами одного хим. элемента и потому являются формой его существования в свободном состоянии, напр. Сера, железо, озон, алмаз. Сложные вещества образованы разными элементами и могут иметь состав постоянный (стехиометрические соединения или дальтониды) или меняющийся в некоторых пределах (нестехиометрические соединения или бертоллиды).
Молекула — наименьшая частица вещества, обладающая его химическими свойствами.
Атом — наименьшая частица химического элемента, сохраняющая все его химические свойства.
Различным элементам соответствуют различные атомы, обозначаемые символом данного элемента (Ag, Fe, Mg).
Химический элемент — это вид атомов, характеризующийся определенными зарядами ядер и строением электронных оболочек.
В настоящее время известно 118 элементов: 89 из них найдены в природе (на Земле), остальные получены искусственным путем. Атомы существуют в свободном состоянии, в соединениях с атомами того же или других элементов, образуя молекулы. Способность атомов вступать во взаимодействие с другими атомами и образовывать химические соединения определяется его строением. Атомы состоят из положительно заряженного ядра и отрицательно заряженных электронов, движущихся вокруг него, образуя электронейтральную систему, которая подчиняется законам, характерным для микросистем.
Ионы (от греч. ion – идущий), одноатомные или многоатомные частицы, несущие электрический заряд.
Положительные ионы называют катионами, отрицательные – анионами. Валентность (от лат. valentia – сила), способность атома присоединять или замещать определенное число других атомов или атомных групп с образованием химической связи.
Реакции химические (от лат. re- – приставка, означающая обратное действие, и actio –действие), превращения одних веществ (исходных соединений) в другие (продукты реакции) при неизменяемости ядер атомов.
Исходные вещества иногда называют реагентами, однако чаще (особенно в органической химии) термин «реагент» используют по отношению к одному, наиболее активному исходному соединению, определяющему направление химической реакции.
Химическая формула — это условная запись состава вещества с помощью химических знаков (предложены в 1814 г. Й. Берцелиусом) и индексов (индекс — цифра, стоящая справа внизу от символа. Обозначает число атомов в молекуле).
Химическая формула показывает, атомы каких элементов и в каком отношении соединены между собой в молекуле.
Простые вещества— молекулы, состоят из атомов одного и того же элемента.
Cложные вещества — молекулы, состоят из атомов различных химических элементов.
Аллотропия — явление образования химическим элементом нескольких простых веществ, различающихся по строению и свойствам.
Международная единица атомных масс равна 1/12 массы изотопа 12C — основного изотопа природного углерода.
1 а.е.м = 1/12 • m (12C) = 1,66057 • 10-27 кг
Относительная атомная масса (Ar) — безразмерная величина, равная отношению средней массы атома элемента (с учетом процентного содержания изотопов в природе) к 1/12 массы атома 12C.
Средняя абсолютная масса атома (m) равна относительной атомной массе, умноженной на а.е.м. Ar(Mg) = 24,312
m(Mg) = 24,312 • 1,66057 • 10-24 = 4,037 • 10-23 г
Относительная молекулярная масса (Mr) — безразмерная величина, показывающая, во сколько раз масса молекулы данного вещества больше 1/12 массы атома углерода 12C.
Mг = mг / (1/12 mа(12C))
mr — масса молекулы данного вещества;
mа(12C) — масса атома углерода 12C.
Mг = S Aг(э). Относительная молекулярная масса вещества равна сумме относительных
атомных масс всех элементов с учетом индексов.
Абсолютная масса молекулы равна относительной молекулярной массе, умноженной на а.е.м.
Число атомов и молекул в обычных образцах веществ очень велико, поэтому при характеристике количества вещества используют специальную единицу измерения — моль.
Количество вещества, моль. Означает определенное число структурных элементов (молекул, атомов, ионов).
Обозначается n, измеряется в моль. Моль — количество вещества, содержащее столько же частиц, сколько содержится атомов в 12 г углерода.
Число Авогадро ди Кваренья (NA). Количество частиц в 1 моль любого вещества одно и то же и равно 6,02 • 1023. (Постоянная Авогадро имеет размерность — моль-1).
Молярная масса показывает массу 1 моля вещества (обозначается M).
M = m / υ
Молярная масса вещества равна отношению массы вещества к соответствующему количеству вещества и численно равна его относительной молекулярной массе, однако первая величина имеет размерность г/моль, а вторая — безразмерная.
Это означает, что если масса некоторой молекулы равна, например, 80 а.е.м. (SO3), то масса одного моля молекул равна 80 г. Постоянная Авогадро является коэффициентом пропорциональности, обеспечивающим переход от молекулярных соотношений к молярным. Все утверждения относительно молекул остаются справедливыми для молей (при замене, в случае необходимости, а.е.м. на г)
Например, уравнение реакции: 2Na + Cl2 = 2NaCl, означает, что два атома натрия реагируют с одной молекулой хлора или, что одно и то же, два моль натрия реагируют с одним молем хлора.
3. Основные законы
Закон сохранения массы веществ (М.В.Ломоносов, 1748 г.; А.Лавуазье, 1756 г.)
Масса всех веществ, вступивших в химическую реакцию, равна массе всех продуктов реакции.
Атомно-молекулярное учение этот закон объясняет следующим образом: в результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка (т.е. химическое превращение- это процесс разрыва одних связей между атомами и образование других, в результате чего из молекул исходных веществ получаются молекулы продуктов реакции). Поскольку число атомов до и после реакции остается неизменным, то их общая масса также изменяться не должна. Под массой понимали величину, характеризующую количество материи. Исходя из закона сохранения массы, можно составлять уравнения химических реакций и по ним производить расчеты. Он является основой количественного химического анализа.
studopedia.net
Закон сохранения массы веществ м.в.ломоносова. Закон сохранения массы
Закон сохранения массы является основой для расчета физических процессов во всех сферах человеческой деятельности. Его справедливость не оспаривается ни физиками, ни химиками, ни представителями других наук. Этот закон, как строгий бухгалтер, следит за соблюдением точной массы вещества до и после его взаимодействия с другими веществами. Честь открытия этого закона принадлежит русскому ученому М. В. Ломоносову.
Первоначальные представления о составе веществ
Строение вещества на протяжении многих веков оставалось тайной для любого человека. Различные гипотезы будоражили ученые умы и подвигали мудрецов на длительные и бессмысленные споры. Один утверждал, что все состоит из огня, другой отстаивал совершенно иную точку зрения. В массе теорий промелькнула и была незаслуженно забыта теория древнегреческого мудреца Демокрита о том, что все вещества состоят из крошечных, невидимых глазу мельчайших частиц вещества. Демокрит назвал их «атомами», что значит «неделимые». К сожалению, в течение целых 23 веков его предположение было забыто.
Алхимия
В основном научные данные средних веков базировались на предрассудках и различных домыслах. Возникает и широко распространяется алхимия, которая представляла собой свод скромных практических познаний, тесно сдобренных самыми фантастическими теориями. Например, известные умы того времени старались превратить свинец в золото и найти неведомый философский камень, исцеляющий от всех болезней. В процессе поисков постепенно накапливался научный опыт, состоящий из многих необъясненных реакций химических элементов. Например, было выяснено, что многие вещества, названные впоследствии простыми, не распадаются. Таким образом возродилась древняя теория о неделимых частичках материи. Понадобился великий ум, чтобы превратить этот склад информации в стройную и логичную теорию.
Теория Ломоносова
Точным количественным методом исследования химия обязана русскому ученому М. В. Ломоносову. За блестящие способности и упорный труд он получил звание профессора химии и стал членом Российской академии наук. При нем была организованна первая в стране современная химическая лаборатория, в которой и был открыт знаменитый закон сохранения массы веществ.

В процессе изучения течения химических реакций Ломоносов взвешивал исходные химические вещества и продукты, появившиеся после проведения реакции. При этом он открыл и сформулировал закон сохранения массы вещества. В 17 веке понятие массы часто путали с термином «вес». Поэтому массы веществ часто называли «весами». Ломоносов определил, что строение вещества находится в прямой зависимости от частичек, из которых оно построено. Если содержит частички одного сорта, то такое вещество ученый называл простым. При разнородном составе корпускул получается сложное вещество. Эти теоретические данные позволили Ломоносову сформулировать закон сохранения массы.
Определение закона
После многочисленных экспериментов М. В. Ломоносов установил закон, суть которого сводилась к следующему: вес веществ, которые вступили в реакцию, равен весу веществ, которые получились в итоге реакции.

В русской науке данный постулат носит название «Закон сохранения массы веществ Ломоносова».
Это закон был сформулирован в 1748 году, а самые точные эксперименты с реакцией обжига металлов в запаянных сосудах были проведены в 1756 году.
Опыты Лавуазье
Европейская наука открыла закон сохранения массы после публикации описания работ великого французского химика Антуана Лавуазье.

Этот ученый смело применял в своих экспериментах теоретические представления и физические методы того времени, что позволило ему разработать химическую номенклатуру и создать реестр всех известных на то время химических веществ.
Своими экспериментами Лавуазье доказал, что в процессе любой химической реакции соблюдается закон сохранения массы веществ, вступающих в соединение. Кроме этого, он расширил распространение закона сохранения на массу каждого из элементов, которые принимали участие в реакции в составе сложных веществ.
Таким образом, на вопрос, кто открыл закон сохранения массы веществ, можно ответить двояко. М. В. Ломоносов первым провел эксперименты, наглядно демонстрирующие закон сохранения, и подвел его под теоретическую базу. А. Лавуазье в 1789 году независимо от русского ученого самостоятельно открывает закон сохранения масс и распространяет его принцип на все элементы, участвующие в химической реакции.
Масса и энергия
В 1905 году великий А. Эйнштейн показал связь между массой вещества и его энергией. Она выражалась формулой:
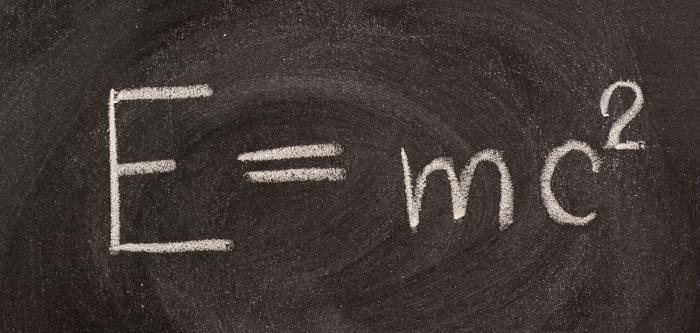
Уравнение Эйнштейна подтверждает закон сохранения массы и энергии. Данная теория утверждает, что всякая энергия имеет массу и изменение этой энергии несет изменение массы тела. Потенциальная энергия любого тела очень велика, и высвободиться она может лишь в особых условиях.
Закон сохранения массы справедлив для любых тел микро- и макромира. Любая химическая реакция принимает участие в преобразовании внутренней энергии вещества. Поэтому при расчете массы веществ, участвующих в химических реакциях, нужно было бы учитывать прирост или убыль массы, вызванных выделением или поглощением энергии в данной реакции. На самом деле в макромире этот эффект настолько незначителен, что такие изменения можно не принимать во внимание.
Знаменитый английский химик Роберт Бойль при выполнении различных опытов с металлами заметил, что при сильном нагревании металлов на воздухе их масса увеличивается. В итоге ученый предположил, что в результате химической реакции, протекающей при нагревании, масса веществ должна меняться. Роберт Бойль считал, что при нагревании металлы реагируют с некоей «огненной материей», содержащейся в пламени. «Огненную материю» называли флогистоном.
Русский ученый Михаил Васильевич Ломоносов, изменил постановку эксперимента, и нагревал металлы не на открытом воздухе, а в герметично запаянных стеклянных ретортах. При постановке эксперимента таким способом, масса реторты с металлом до и после нагревания оставалась прежней.
При вскрытии такой реторты оказалось, что металл частично превратился в другое вещество, которое покрывало поверхность металла. Следовательно, металл прореагировал с воздухом, который находился в реторте. М.В. Ломоносов сделал очень важный вывод. Если общая масса реторты до и после прокаливания не изменялась, значит, масса содержащегося в сосуде воздуха уменьшилась на столько же, на сколько увеличилась масса металла (за счет образования нового вещества на его поверхности).
Масса воздуха в реторте действительно уме
gvozdec.ru