Что такое эпитет в русском языке: Что такое эпитеты в русском языке
Что такое эпитеты в русском языке
Что такое эпитеты в русском языке? Речь без них скучна, а литературное произведение без этого поэтического приема просто невозможно представить.
Определение
Эпитет в русском языке – это определение при слове, обогащающее его новыми смысловыми оттенками. Само слово пришло в русский язык из греческого, в переводе означает «приложенный». Чаще всего в роли эпитета выступают прилагательные. Иногда наречия и существительные принимают на себя эту функцию. Он может быть выражен как одним словом, так и словосочетанием. Этот стилистический прием помогает богаче описать чувства, ярче рассказать о событии. Не конкретный признак предмета или явления, а его образная характеристика. Можно сравнить «красный карандаш» и «красный закат».
Справка! «Википедия» рассматривает как определение при слове, влияющее на его выразительность, красоту произношения.
Функции эпитета в речи:
- эмоциональность,
- образность,
- выразительность,
- поэтичность.
Он помогает понять авторское отношение к описываемому предмету или явлению, создает определенное настроение в восприятии литературного произведения, обогащает речь смысловыми оттенками.
Эпитет может усилить характеристику объекта. Пример: «ручей весело бежал»; «ручей бешено мчался».
В русском языке и литературе
Их часто используются в литературных произведениях. Невозможно представить поэзию без определяющих слов. Благодаря им авторские строки становятся яркими, чувственными, читатель легче понимает настроение поэта и тот смысл, скрытый или явный, который был вложен в произведение.
«Истрепалися сосен мохнатые ветви от бури,
Изрыдалась осенняя ночь ледяными слезами,
Ни огня на земле, ни звезды в овдовевшей лазури,
Все сорвать хочет ветер, все смыть хочет ливень ручьями». (А. Фет)
В русском языке эпитет выступает в функции определения или обстоятельства и часто употребляется в переносном значении.
«Золотая пора».
«Трезво оценивать».
В предложении прилагательное, либо другая часть речи, обозначающая признак предмета, не обязательно будет эпитетом. Оно может выступать в функции сказуемого или дополнения и иметь определенную логическую нагрузку.
«Ночь тиха».
«Эта девушка самая красивая».
Виды эпитетов
В русском языке подразделяются на несколько видов.
- Общеязыковые. Представляют собой привычные устойчивые сочетания. «Свинцовая туча», «злая вьюга».
- Народно-поэтические. Пришли в современный язык из устного народного творчества, сказок и былин. «Ясный сокол», «чисто поле».
- Индивидуально-авторские. Стилистические конструкции придуманы автором. Ранее слово или выражение в таком обороте не употреблялось и эпитетом не являлось.«Прозрачной лести ожерелья и четки мудрости златой» (А.С. Пушкин)
- Постоянные. Эпитет неразрывно связан с определяемым словом. Образует устойчивое выражение. Встречается в разговорной речи, в литературных произведениях, сказках и песнях. «Серый волк», «широкая степь».
Как найти в тексте
В поэтическом произведении автор может расположить эпитеты вертикально, друг под другом, оторвано от определяемого слова, чтобы усилить их звучание.
«Все как было. Только странная
Воцарилась тишина
И в окне твоем – туманная
Только улица страшна». (А. Блок)
Части речи в функции эпитета
- Эпитет прилагательное встречается чаще всего. «Буйная молодость», «золотые руки». Прилагательное не просто является признаком предмета, но описывает его ярко, образно, служит украшением определяемого слова. «Железная выдержка» – характеристика человека, остающегося невозмутимым в любой ситуации; «Тоска зеленая» — не просто скука, а тягучая, беспросветная. «Робкая и бедная любовь» – чувство, заранее обреченное на неудачу, безответность.
- Наречие выступает в предложении в роли обстоятельства. «Между тучами и морем гордо реет буревестник» (М. Горький)
- В виде существительного. «И вот сама идет волшебница-зима» (А. С. Пушкин) «Текут невинные беседы с прикрасой легкой клеветы».
- Числительные в его функции приобретают оценочное значение. «Седьмая вода на киселе», «промотал миллионы», «первая ученица в классе» . Употребление больших числовых значений используется для гиперболизации. «Мильон терзаний», «тысяча мелочей».
- Причастия способствуют наглядному представлению событий, придают описанию лаконичность и точность. Употребление причастий помогает выразить торжественность события. «Обновленная дружба: Россия поддержит Кубу…» (Новости ОРТ). Причастия используются для большей убедительности читателей. «Увлажняющий крем с омолаживающим эффектом». «Ситуация, изменяющаяся к лучшему, будет к лучшему изменяться вместе с мировой экономикой» (Новости, ОРТ). Причастия в функции эпитета могут приобретать устойчивый характер. «Хорошо забытое старое».
- Отглагольное прилагательное. «Долго он стоял окаменелый, провожая взглядом удаляющуюся фигурку девушки».
Эпитеты придают красоту литературным произведениям, расцвечивают их яркими красками. Обогащают они и разговорную речь, позволяя полнее выразить чувства, переживания.
Полезное видео
Функции и роль эпитета.
Что такое эпитет? Виды и примеры эпитетов
Эпитет — это образное, художественное определение. Эпитет выразительно описывает признак предмета, его качество или свойство.
Эпитеты. Примеры
Трескучий мороз
Жадный взгляд
Дивный гений
Крылатые качели
Горькие слёзы
Золотая листва
Задача эпитета — создать яркий образ. Чаще всего в качестве эпитетов используют прилагательные («белоснежная зима»). Но эпитетом может быть и наречие («горячо спорить»), и существительное («собака Калин-царь»), и числительное («первый ученик»), и причастие, и деепричастие («когда весенний, первый гром, как бы резвяся и играя, грохочет в небе голубом»).
Эпитет — одна из разновидностей тропов, художественных средств речи. Название происходит от греческого слова έπίθετος — «приложенный».
Чем эпитет отличается от описания и метафоры
Эпитет не просто указывает на определенное качество, а эмоционально и образно характеризует предмет, явление, человека или любой другой объект. Поэтому не стоит путать эпитеты с описаниями. Например, в выражении «седой старик» слово «седой» — это описательное прилагательное. А в стихотворении Тургенева «утро туманное, утро седое» — уже эпитет.
Следует также отличать эпитет от метафоры. Метафора — это скрытое сравнение, перенос свойств одного предмета на другой. Примеры метафоры: «говор волн», «море радости». При этом эпитеты могут быть составляющей частью метафоры.
Например, Владимир Маяковский сравнивает свои стихи с оружием и использует эпитеты, чтобы раскрыть эту метафору:
Парадом развернув
моих страниц войска,
я прохожу
по строчечному фронту.
Стихи стоят
свинцово-тяжело,
готовые и к смерти
и к бессмертной славе.Виды эпитетов
В русском языке выделяют различные виды эпитетов.
Общеязыковые эпитеты — это принятая норма. «Гробовая тишина», «нежный ветерок», «мягкий голос».
Народно-поэтические эпитеты уходят корнями в устный фольклор, в сказки и былины. Зачастую это тоже устойчивые выражения: «добрый молодец», «красна девица».
Постоянный эпитет неразрывно связан с определяемым словом, образуя устойчивое выражение. Например, «косолапый мишка» или «железный конь».
Индивидуально-авторские эпитеты придуманы конкретным человеком, используются ситуативно. Например, «мармеладное настроение» (А.П. Чехов).
Также эпитеты можно делить на оценочные, описательные и эмоциональные.
Оценочный эпитет — «чудесный вечер».
Описательный эпитет — «золотая осень».
Эмоциональный эпитет — «унылая пора».
Эпитеты также делятся на простые и сложные. Простые эпитеты выражены одним словом («парус одинокий»), сложные эпитеты — словосочетанием («берег, милый для меня»).
Примеры эпитетов в русском языке
Красно солнышко
Тридевятое царство
Чистое поле
Могучий дуб
Белокаменная Москва
Туманный Альбион
Дикий Запад
Примеры эпитетов в литературе
Ночь была свежая и неподвижно-светлая (Л. Толстой)
Кругом трава так весело цвела (И. Тургенев)
Мой край, задумчивый и нежный (С. Есенин)
Полночь сошла, непроглядная темень (Н. Гумилев)
В блюдечках — очках спасательных кругов (В. Маяковский)
О, покой мой многонеделен (А. Ахматова)
Шаркающей кавалерийской походкой (М. Булгаков)
Примеры эпитетов в песнях
Как я люблю глубину твоих ласковых глаз (В. Агатов)
Крылатые качели (Ю. Энтин)
Чумачечая весна (А. Потапенко)
это… примеры в литературе, стихотворении, кино
На чтение 5 мин. Просмотров 720
Эпитет в русском языке — это средство художественной выразительности речи, используемое для емкого образного описания предмета. Эпитет отвечает на вопрос “какой?”, в предложении играет роль определения. В таком качестве обычно выступают прилагательные, наречия, реже существительные.
Литературоведческий термин эпитет полезен при анализе текста, оценке его стилистики. Устную речь люди обогащают этим средством художественной выразительности, даже не замечая этого. Статья расскажет, что такое эпитет, как его распознать, проиллюстрирует использование.
Чаще всего слова, представляющие собой эпитет, употреблены в переносном значении или неожиданном контексте. Это помогает эмоционально окрасить речь, сделать описание богаче.
Так, словосочетание “морозный воздух” давно на слуху, его считают обыкновенным определением, а фраза “колючий воздух” звучит любопытнее, здесь прилагательное колючий уже представляет собой эпитет.
Виды эпитетов
Эпитеты бывают общеязыковые, народно-поэтические, индивидуально-авторские, постоянные. Рассмотрим их по отдельности.
Общеязыковой
Общеязыковой эпитет — описание предмета, которое используют повсеместно. Определение относительно устойчиво по отношению к определяемому, в употреблении закреплено для обозначения конкретных признаков.
Например, в русском языке многократно употребляют словосочетание “сильный мороз”.
Прилагательное сильный употреблено в переносном значении, показывает степень проявления мороза, постоянно воспроизводится в таком контексте, поэтому его относят к общеязыковым эпитетам.
Народно-поэтический
Народно-поэтический эпитет — это устойчивое выражение, закрепившееся в речи благодаря народному творчеству. Такие определения часто используют при написании художественных произведений для имитации разговорной или устаревшей речи.
Классическим примером является словосочетание “лето красное”. Прилагательное красный здесь употреблено не в привычном лексическом значении (название цвета), но устаревшем “красивый”.
Для кратких прилагательных характерно играть роль народно-поэтических эпитетов, например, “чисто поле”, “ясно солнышко”.
Индивидуально-авторский
Индивидуально-авторский эпитет в литературе — характеристика предмета, построенная на оценке автором его свойств. Такое определение используют в художественных текстах для придания им большей образности и уникальности.
Стихотворение “Ниоткуда с любовью” Бродского узнают по фразе “мычащее ты”. Это настолько неожиданное применение причастия “мычащий”, что конструкцию даже прозвали “бродской”, что указывает на авторство выражения.
Постоянный
Постоянный эпитет — неизменно повторяющееся описание, ассоциирующееся с определенным объектом.
Примерами служат часто встречающиеся словосочетания “проливной дождь”, “синее небо”, “красна девица”.
Как найти эпитеты в тексте
Чтобы найти данное средство художественной выразительности в тексте необходимо выяснить, какие слова составляют характеристику объекта. Из них выбрать те, что отвечают на вопрос “какой?” по отношению к предмету. Из списка получившихся прилагательных, наречий, причастий выписать те, что создают наиболее глубокий образ, проявляют переносное или малораспространенное значения.
“Невидимая из-за темноты угрюмая стена возвышалась каменной громадой”.
Для описания стены автор предложения пускает в ход определения “невидимая” и “угрюмая”, оба отвечают на вопрос “какой?”. Изучаемым средством выразительности будет прилагательное “угрюмая”, поскольку традиционно к нему не прибегают при изображении неживых объектов. Фраза содержит олицетворение, значит слово, которое применяют для создания приема, употребляют в нетипичном значении.
Примеры
Эпитеты используются везде: художественной литературе, стихотворениях, кино, в обычных разговорах. Рассмотрим примеры использования.
Примеры из художественной литературы
“А это, Джи-Пи, машина поразительная”.
Артур Хейли, “Колеса”
“Белое безмолвие” — так называется рассказ Джека Лондона. Слово “белый” традиционно описывает цвет предмета, но безмолвие не обладает таким качеством, значит, прилагательное приобретает переносное значение.
“Контора требовала от него неусыпного внимания с девяти утра до трех пополудни”.
Теодор Драйзер, “Финансист”
В стихотворениях
“И странной близостью закованный,
Смотрю за темную вуаль,
И вижу берег очарованный
И очарованную даль”.
Александр Блок, “Незнакомка”
“Я видел, как два колоска воскового цвета,
мёртвые, хоронили гряду вулканов”.
Федерико Гарсия Лорка, “Маленькая бесконечная поэма”
“Сегодня, я вижу, особенно грустен твой взгляд,
И руки особенно тонки, колени обняв.
Послушай: далеко, далеко, на озере Чад
Изысканный бродит жираф”.
Николай Гумилев, “Жираф”
“Августовские любовники проходят с цветами,
невидимые зовы парадных их влекут”.
Иосиф Бродский, “Августовские любовники”
В кино
Диалоги кинофильмов нередко содержат предложения с эпитетами, служат хорошими примерами всех их видов. Народно-поэтические и общеязыковые окрашивают речь героев, но ими она не ограничивается, поскольку сценарист может добавить авторские ради создания, к примеру, комического эффекта.
“Там говорят о том, как чертовски здорово наблюдать за огромным огненным шаром, как он тает в волнах…”.
“Достучаться до небес”, реплика главного героя.
“Его разум был острее, чем у остальных, и он был способен видеть всех обитателей города со стороны”.
“Догвилль”, озвучивает закадровый голос.
“Но не для того пришла наша сборная института, чтобы отмечаться, а для того, чтобы выяснить, кто же этот «Таинственный Математический Волшебник»».
“Умница Уилл Хантинг”, фраза принадлежит герою.
Использование эпитетов — распространенный прием. Знания о функции описания, которую они выполняют, помогут при анализе литературных произведений, а обогащение собственной устной речи сделает выступления ярче.
что такое эпитет в русском языке
пж не игнорьте у меня мало времени начертите схему образец на фото Если говорят что можно Судить о характере человека по его библиотеке то мне Кажется … не менее верное заключение можно делать и по квартире
Спишите, вставляя пропущенные буквы и знаки препинания. 1. Вдали сл..ваясь с небом громоздились льды.2. Медведи прод..лжали идти гуськом (не)пр..бавля … я шагу и (не)изм..няя направления своего пути.3. (Чёрно)лиловые тучи ползли на запад зад..вая вершины гор.4. Река вымотавшись за день пр..смирела и отд..лё(н,нн)ым ш..потом перекатов напомнила о своём бурном нраве.5. Костёр (по)праздничному играет пламенем ярко осв..щая стоянку и отбрас..вая в глубину леса трепещ..щие тени старых лиственниц.6. Лай чуть слышался и всё дальше уд..ляясь терялся в глуб..не лощины.7. Мальчики шли полем громко перег..вариваясь но войдя в лес пр..тихли. 8. Несмотря на поздний час стояла невыносимая духота, пронизанная едва уловимым дымным запахом, который проникал в комнату с улиц. 9. Ручей! – закричали остальные и несмотря на усталость не теряя времени протопали по камням к воде. 10. Стараясь не смотреть на девочку старейшины положили её на мох.
Подобрать варианты устаревшего употребления падежных форм Помогите пж
Помогите я полюбила бандита
по вопросам Составь и запиши предложения подчеркни главные члены предложения в нераспространенных предложениях кто что делает
спишите отрывки из стихотворений. Подчеркните имена прилагательных в роли эпитетов. Является ли эпитетом слово душистой во втором о1. Когда р.а.сой об … рызганный душистой,Румяным вечером иль утра в час златойИз-под куста мне ландыш серебристыйПриветливо кивает г.Словой.М. Лермонтов2. Распустились почки, лес зашевелился,Яркими лучами весь o3. Лотился.На его окраине из травы душистойВыглянул на сол…це ландыш сер..бристый.С. Дрожжин
Раскройте где не обходимо скобки. И вставьте пропущенные буквы Текст 1. Перед глазами ехавших ра(с,сс)т..лалась уже бесконечная р..внина перехваче(н … ,нн)ая цепью холмов. Эти холмы сл..ваются в возвыше(н,нн)ость которая тянется (в)право от дороги до самого г..ризонта и и..чезает в л..ловой дали. Солнце выглянуло (с)зади из(за) города и тихо, без хлопот принялось за свою работу. (С)начал.. около курганчиков и ветр..ной мельницы которая (из)дали похожа на маленького человечка размахивающего руками поп..лзла по земле широкая ярко(жёлтая) полоса. Через минуту такая(же) полоса засветилась ближе и поползла (в)право. Что(то) тёплое к.снулось Егорушкиной спины. Полоса света подкравшись (с)зади шмыгнула через бричку и лошадей понеслась (на)встречу другим полосам. И вдруг вся широкая степь (с/з)бросила с себя утре(н,нн)юю (полу)тень, улыбнулась и засверкала росой. Всё, обласка(н,нн)ое солнцем, ож..вало, что(б) вновь зацв..сти.
Написать эссе на тему как я понимаю фразу «в любом деле надо работать»
синтаксис синтаксический разбор предложения мальчики Утомленные долгим путем шли молча
нарисуйте схемы к предложениям
Подготовка к ЕГЭ по русскому языку и ГИА
Мы думаем, что каждый, кто сдаёт единый государственный экзамен, хочет получить за него максимальное количество баллов. С хорошими результатами будет легче поступить в любой вуз. Данный раздел поможет вам приблизиться к этой цели. Здесь есть всё необходимое для успешной подготовки. Также данный раздел нередко используется учащимися вузов и ссузов.
Проверить орфографию онлайн
Математика
- Часть A:
- Согласные звонкие и глухие
- Ударение в словах
- Паронимы. Лексическое значение слов
- Склонение имен существительных, падежи русского языка
- Деепричастный оборот, примеры
- Нормы согласования и управления
- Последовательная связь предложений в тексте
- Сочетание слов. ЕГЭ по русскому языку
- Грамматическая основа предложений
- Подчинительная, сочинительная, бессоюзная связь
- Правописание причастий, разряды местоимений, предлоги, частицы
- Лексическое значение слов
- Суффиксы. Приставки. Виды, примеры, правописание
- Правописание суффиксов прилагательных, Н, НН
- Проверочные слова, безударные гласные в корне
- Правописание приставок
- Правописание безударных личных окончаний глагола
- Правописание суффиксов глаголов
- Правописание не или ни
- Правописание предлогов
- Однородные члены предложения
- Знаки препинания при обособленных согласованных определениях
- Вводные слова в предложении
- Знаки препинания при однородных членах
- Знаки препинания в предложениях
- A26
- A27
- Действительные и страдательные причастия
- Микротема, основная мысль текста
- Типы речи: описание, повествование, рассуждение
- Синонимы к словам
- Часть B:
- Бессуффиксный способ словообразования
- Определение части речи
- Типы подчинительной связи
- Безличные, определенно-личные, односоставные предложения
- Обособленные приложения, обстоятельства и примеры
- СПП с придаточными
- Средства связи частей текста
- Что такое эпитет метафора, сравнение
- Часть C:
- Сочинение ЕГЭ по русскому языку
Обществознание
За последние несколько лет тема единого государственного экзамена стала особенно актуальной. Изначально эта программа вводилась как эксперимент и уже в первые месяцы тестирования зарекомендовала себя как объективную систему тестирования выпускников. Так что же все-таки представляет из себя этот ЕГЭ?
Например, ЕГЭ по русскому языку состоит из трех частей (А, B, C). В первой части (A) 30 вопросов с одним вариантом ответа, а в части В, более сложной, чем А, всего 8 вопросов с написанием правильного ответа или выбором нескольких ответов. Каждому выпускнику одиннадцатых классов в обязательном порядке следует сдавать только 2 предмета: русский язык и математика, остальные по выбору. Допускаются к экзамену только ученики, имеющие оценки не ниже удовлетворительных, то есть без двоек в аттестате. Проверка работ производится другими преподавателями в другом районе, дабы исключить всякую возможность коррупции.
В школах многие учителя буквально наводят ужас на своих учеников, рассказывая о беспощадности ЕГЭ, в большинство ВУЗов принимают только с определенным количеством баллов, а различные организации твердят о ЕГЭ, чтобы привлечь к себе клиентов, желающих получить достойную подготовку к экзамену. Должен сказать, что квалифицированная подготовка дает свои, далеко не плохие, результаты. Но те, кто уже прошел через это «страшное» испытание, утверждают, что для учеников даже со средними оценками экзамен не должен показаться слишком уж сложным, по крайней мере невыполнимым. Нужно лишь приложить немного усилий, а именно выучить хотя бы самые важные правила, пройденные за весь учебный период, ведь если вы не ленились и хотя бы иногда открывали учебники, то что-то вы должны знать. Очень хорошо помогают различные книжки, предлагающие собственные примеры заданий, примеры их решений и дающие различные рекомендации по сдаче экзамена. Подобной литературой буквально завалены все книжные магазины, причем стоят они очень дешево. Для кого-то, естественно, и этого будет недостаточно. В таких случаях я бы рекомендовал обращаться к своим учителям, большинство из которых готовы помогать бесплатно. Я знаю, что во многих школах учителя предлагают организовывать собственные школьные подготовительные курсы за небольшую плату, а то и вовсе бесплатно.
Что же касается ГИА, то тут тоже ничего особо сложного нет, разница лишь в том, что задания в работах немного легче и сам экзамен не так важен как ЕГЭ, ведь ГИА проводится только среди девятых классов.
В заключение хотелось бы сказать, что сдать экзамен не так сложно, как пугают учителя, но нельзя преуменьшать важность и серьезность ЕГЭ, а также степень легкости экзамена, ведь, как ни крути, а на раз плюнуть никакие экзамены не даются: всё требует подготовки и старания.
Эпитет
Эпитет – это троп, который в лирической поэзии и художественной прозе является метафорическим определением. Иначе говоря, эпитет – это метафора, которая называет не предмет художественного отображения, а признак этого предмета. Больше ничем другим эпитет не отличается от метафоры.
В эпической поэзии эпитетами считаются застывшие определения (постоянные эпитеты), например, розовоперстая Эос, хитроумный Одиссей, быстроногий Ахилл, шлемоблещущий Гектор у Гомера.
Качество эпитета (как и метафоры) оценивается его новизной и емкостью –
Прощай, немытая Россия,
Страна рабов, страна господ,
И вы, мундиры голубые,
И ты, им преданный народ.
Этим стихам Лермонтова очень не повезло. Некоторые комментаторы считают, что в них три эпитета: «немытая», «голубые» и «преданный». «Голубые» здесь не является самостоятельным словом: «мундиры голубые» — это жандармы, носившие форму голубого цвета. То есть перед нами метонимия.
Еще больше не повезло «немытой России». Лермонтовская энциклопедия считает, что под «рабами» поэт подразумевал народ, который при таком раскладе тоже является «немытым».
Один из увлеченных участников Форума любителей русской словесности вносит в этот загадочный вопрос свою лепту: «Вообще-то, немытыми в разговорно-просторечной форме
называли некрещеных. Но ведь Россия-то была поголовно православная». Да, совершено поголовно!!! Окончательную точку для ясности поставила ведущая форума: «Думаю, что в этом стихотворении Лермонтов, употребляя слово «немытая», не подразумевает «некрещёная». Скорее, это слово употреблено в прямом значении».
Лермонтов праведно возмущался «наивными читателями». Но в этих стихах поэт идет навстречу именно им: дает объяснение своей поэтической мысли.
Итак, у поэта «немытая Россия» значит: царская фамилия + «стоящие у трона» (то есть рабы этой фамилии) + охраняющие их жизнь жандармы + преданная и покорная хозяевам жизни часть народа, а непокорным Лермонтов, симпатизировавший декабристам, поет славу (вспомните купца Калашникова или старого воина из стихотворения «Бородино»). Вот такова емкость эпитета немытая.
Обычно считают, что эпитеты служат украшению речи. Это заблуждение. Какое украшательство в «немытой России»?
Выдающийся стиховед Л.И.Тимофеев как-то обмолвился, что «в широком смысле слова эпитетом является всякое слово, определяющее, поясняющее, характеризующее какое-либо понятие. В этом смысле эпитетом является любое прилагательное».
Л.И.Тимофеев (автор школьного учебника по литературе и учебника для филологических факультетов вузов) был очень доброжелательным человеком. В приведенных выше его словах следует видеть подсказку. В самом деле, если любое прилагательное, встречающееся в стихотворном тексте, назвать эпитетом, то ни один преподаватель не сумеет придраться к этому –
И снится нам не рокот космодрома,
Не эта ледяная синева,
А снится нам трава, трава y дома,
Зеленая, зеленая трава.
(А.Поперечный)
Вы можете спокойно утверждать, что «ледяная» и «зеленая» этих стихов эпитеты. Оспорить это будет невозможно. Но в этих «эпитетах» нет новизны, а их емкость близка к нулю. Сравните настоящий эпитет, приложенный к траве –
В гелиотроповом свете молний летучих
На небесах раскрывались дымные тучи,
На косогоре далеком — призрак дубравы,
В мокром лугу перед домом — белые травы.
Это Бунин, величайший, наравне с Державиным, поэт живописной эмоции.
Эпитет сложное явление. Об эпитеты спотыкаются не только «наивные читатели», но и великолепные любители поэзии, каковым был, например, В.Катаев, замечательный прозаик.
В «Траве забвения» В.Катаев вспоминает, как Бунин правил одно из его юношеских стихотворений: «Бунин перечеркнул последнюю строфу карандашом, а на полях написал: А на столе осенние цветы. Их спас поэт в саду от ранней смерти». Он немного подумал и затем решительно закончил: «Этюдники. Помятые холсты. И чья-то шляпа на мольберте»».
Катаева поразила лапидарность, с какой Бунин изобразил мастерскую их общего знакомого А. Федорова, художника-дилетанта. «Правда, — продолжает Катаев, — меня немного смутили «помятые холсты». У художников редко бывают помятые холсты. Они или натянуты на подрамник, или стоят в углу, свернутые в толстые трубы. Попробуй-ка их смять! И до сих меня мучают помятые холсты, показывающие, что даже у самых лучших поэтов иногда попадаются проходные эпитеты, хотя на первый взгляд и точные, но в самой своей глубине неверные, поставленные по принципу — авось проскочит. У меня не проскочило, потому что я никак не мог увидеть помятые холсты, а видел их свернутые в трубы, тяжелые, промасленные».
Катаев целые десятилетия мучился «помятыми холстами», мучился тем, что не было их у Федорова, художника «с изящным дилентантизмом и невинными покушениями на богемистость», каким он запомнился автору «Травы забвения». Бунин же одним мазком раскрыл сущность Федорова, приметив в его мастерской помятые холсты, то, что не встречается у профессиональных художников.
К эпитетам большей частью предрасположены те поэты, которые очень не равнодушны к метафоре. Это прежде других Державин, Фет, Маяковский.
Другие термины на сайте
Парцелляция от фр. «parceller», «делить, дробить на части») – неудачный из-за своей многозначности лингвистический термин. Если объединить противоречивые высказывания лингвистов, то под парцелляцией следует, скорее всего, понимать так называемый «телеграфный стиль».
Сравнение — В качестве поэтического тропа сравнение выступает в чистом виде лишь тогда, когда в речи присутствуют обе сопоставляемые стороны. Сравнение не изменяет значения сопоставляемых понятий, чем и отличается от метафоры.
Пейзаж в художественной литературе
Пейзаж здесь рассматривается в качестве термина. Пейзаж в словесном искусстве сколь древен, столь и исторически многообразен.
Характеру былинных богатырей созвучен характер былинного пейзажа, где и горы, и поля, и реки, и леса простираются до невероятных размеров. Все дышит гармонией, высоким поэтическим чувством.
Что такое эпитет? Примеры эпитетов.
Из данной статьи вы узнаете: Что такое эпитет? Определение эпитета. Примеры эпитетов. Роль и функции эпитетов. Классификация эпитетов. Статью мы построим в виде вопрос-ответ.
Список вопросов, освещенных в статье:
Что такое эпитет? Определение эпитета.
Самое простое определение эпитета следующее:
Эпитет – это образное определение.
Определения посложнее:
Эпитет это особого рода художественное определение при слове, которое описывает слово, создавая при этом яркий образ.
Эпитет – изобразительно-выразительное средство; троп; слово, определяющее, поясняющее предмет, действие или понятие и подчеркивающее какое-то характерное свойство.
Эпитет – это всегда украшение речи, дающее дополнительную художественную характеристику.
НУЖНО ПОНИМАТЬ, что эпитет это всегда определение, но обратно это не работает – то есть определение не всегда будет эпитетом. Например, золотая осень — эпитет, а золотая цепочка — обычное определение, не эпитет.
Примеры эпитетов
Ласковое море Веселая расцветка Свинцовое небо Дремучий лес Золотая осень Горячее сердце | Белозубая зима Могучий дуб Хрупкие цветы Румяная заря Черная тоска Серебряный дождь |
На какие вопросы отвечает эпитет?
Чаще всего эпитет отвечает на вопросы какой? какая? какие? чей? как? и производные от них. Исходя из вопросов, сразу становится понятным, что эпитеты чаще всего являются прилагательными. (Но далеко не всегда, речь об этом пойдет дальше.)
Какими частями речи могут быть эпитеты?
Эпитеты чаще всего являются прилагательными, причастиями и наречиями и реже другими частями речи. Примеры:
- В роли эпитета выступают прилагательные:
Тучка золотая, молниеносное решение, горькая правда, мраморная кожа
- В роли эпитета выступают причастия:
Грохочущий ливень, поседевший лес
- В роли эпитета выступают существительные:
Утес-великан, волшебница-зима, мать – сыра земля, ветер-бродяга
- В роли эпитета выступают числительные:
вторая жизнь, третьи руки
- В роли эпитета выступают наречия:
Горячо любить, безмерно счастлив
- В роли эпитета выступают деепричастия:
Волны несутся, гремя и сверкая
Эпитетами также могут быть местоимения и глаголы.
Какую роль играют эпитеты?
Эпитеты усиливают художественную выразительность, образность языка произведения или нашей речи, придают языку поэтическую яркость. Эпитеты, как правило, выделяют характерную черту или качество и вызывают определённое эмоциональное отношение к ним, помогают увидеть авторское понимание окружающего мира.
Эпитеты помогают создать яркий образ.
Очень хорошо объяснил роль и функции эпитета известный русский ученый А. Г. Шалыгин:
Эпитет — весьма действительное средство, усиливающее картинность и эмоциональность речи. Так называется слово или несколько слов, приданных к обычному названию предмета для того, чтобы усилить его выразительность, подчеркнуть в предмете один из его признаков – тот, который в данном случае важно выдвинуть на первый план, как бы рекомендовать особому вниманию читателя.
3 функции эпитетов:
- акцентировать какое-либо свойство,
- создать яркий эмоционально окрашенный образ,
- усилить художественную выразительность.
Какие бывают эпитеты?
Существует множество классификаций эпитетов, коротко остановимся на основных.
КЛАССИФИКАЦИЯ 1. По происхождению.
Общеязыковые: самая многочисленная группа эпитетов. Отличительная черта общеязыковых эпитетов – они понятны без контекста, связь между словами относительно усточива, то есть эпитеты воспроизводятся и неоднократно употребляются в речи или литератырном языке.
Примеры: жуткая боль, сильный мороз, понурый взгляд, багровый закат.
Постоянные (народно-поэтические): эпитеты, пришедшие из устного творчества. Отличительные черты народно-поэтических эпитетов:
– частое употребление прилагательного в краткой (усеченной форме): чисто поле, сыра земля;
– перенос ударения: шелкОвые луга, зеленО вино;
– инверсия определяющего и определяемого (постановка эпитета после существительного): горе горькое, ноги резвые, ветры буйные.
Примеры: в русском народном творчестве постоянно фигурируют следующие эпитеты темный лес, море синее, поле чистое, терем высокий, стол дубовый, сабля вострая, добрый молодец, девица-красавица и т. д.
Индивидуально-авторские (окказиональные): в основе таких эпитетов лежат неожиданные, часто неповторимые смысловые ассоциации. Авторские эпитеты как правило невоспроизводимы (то есть не употребляются в обычной речи и не употребляются другими авторами).
Примеры: мокрогубый ветер, чурбанное равнодушие, мармеладное настроение
Иногда индивидуально-авторские эпитеты со временем переходят в общеязыковые.
КЛАССИФИКАЦИЯ 2. Стилистический подход.
Согласно данной классификации эпитеты делятся на усилительные, уточнительные и контрастные.
Усилительные: указывают на признак, данный в определяемом слове, не внося ничего нового.
Примеры усилительных эпитетов: горе горькое, зеркальная гладь, холодное равнодушие.
Уточнительные: указывают на отличительные признаки предмета (величину, форму, цвет и т. д.).
Примеры уточнительных эпитетов: мудрые слова, жаркая слеза, печальный взгляд
Контрастные: образуют с определяемыми существительными сочетание противоположных по смыслу слов – оксюмороны
Примеры контрастных эпитетов: живой труп, ненавидящая любовь
Классификация 3. По составу
Простые эпитеты: состоят из одного слова, например, дремучий лес.
Сложные эпитеты: представлены полиосновными прилагательными, например, пшенично-желтые усы, грустно-сырая погода
КЛАССИФИКАЦИЯ 4. По способу обозначения соответствующего признака.
Метафорический эпитет называет не реальный признак, а перенесенный с другого предмета на основе какого-либо сходства: задумчивые ночи, жадное пламя
Метонимический эпитет обозначает признак, перенесенный с другого предмета на основе смежности: дерзкий лорнет, одинокий рассвет, снежный шум.
Развитие оценочной семантики в русских прилагательных. Случай советского политического дискурса на JSTOR
AbstractПредметом данной статьи является семантика именных фраз (сочетаний прилагательное + существительное), используемых в советско-российском политическом дискурсе. Исследование преследует следующие цели: 1) выявить семантику определенных типов именных словосочетаний и внутренние отношения в них, то есть закономерности и закономерности их образования; 2) исследовать прагматическое значение этих групп слов; 3) внести свой вклад в исследование общих особенностей советского политического дискурса.Будет продемонстрировано, что обсуждаемые прилагательные похожи на epitheta ornantia, используемый в традиционных текстах, особенно в фольклоре. Понятие тавтологических эпитетов может быть применено к рассматриваемым группам слов из-за близости или даже совпадения смыслового содержания существительного и прилагательного в пределах именной группы. Прилагательное здесь часто служит усилителем или определителем, классифицирующая функция атрибута отсутствует. Оценка может содержаться в каждом элементе группы слов или в них обоих.Обилие таких прилагательных — яркая черта советского политического дискурса. Они вносят свой вклад в определенный «монументализм» текста и дают готовую оценочную оценку событий, причем оценка преобладает над информативным содержанием текстов.
Journal InformationJSL публикует исследовательские статьи и обзоры книг, которые посвящены описанию и анализу славянских языков и представляют общий интерес для лингвистов.
Информация для издателяКомпания Slavica Publishers, основанная в 1966 году, с 1997 года является отделением славянских и восточноевропейских языков и культур Университета Индианы.Это ведущая специализированная пресса США, посвященная научным монографиям, учебникам, справочным материалам и рецензируемым журналам, посвященным славянским языкам и литературе, а также исследованиям бывшего СССР и Восточной Европы в целом.
Судебная активность посадила россиянина в тюрьму
ПЕРМЬ, Россия — Он всегда звонил незадолго до последнего судебного заседания, говоря, что дело срочное и нужно решать по телефону.
«Не наказывайте господина.Городилов, хорошо? — сказал одному судье Сергей Давыдов, мелкий бизнесмен, притворившись высокопоставленным чиновником юстиции.
Давыдов требовал снисхождения к своему другу Сергею Городилову, обвиняемому в вождении в нетрезвом виде, используя властный тон, который часто используют высокопоставленные россияне при разговоре с подчиненными.
«Конечно, я сделаю все», — угодливо сказал судья, ведущий дело. «Я поняла все.» И на этом просьба Давыдова была удовлетворена, и его друг отделался безнаказанно.
В своем первом обращении к нации после того, как он стал лидером России в 2000 году, президент Владимир Путин пообещал установить «диктатуру закона». Но 20 лет спустя, говорит Давыдов, страна напоминает диктатуру взяточничества, управляемую чем-то, что со временем приобрело собственное название: телефонное правосудие. Эксперты повсеместно называют отсутствие независимых судов одним из основных препятствий для экономического и социального развития России.
«Моей целью было помочь себе и другим и показать всей стране, как судьи выносят решения не по закону, а по телефону», — сказал Давыдов через своего адвоката из тюрьмы, где он отбывает наказание. более девяти лет по обвинению он называет фиктивным.
За эти годы 52-летний Давыдов позвонил 18 судьям в Пермском крае России, древней стране соляных шахт и металлургических заводов, расположенной у подножия Уральских гор в 750 милях к востоку от Москвы. Он попросил якобы независимых судей принимать решения в соответствии с его инструкциями, а не законом.
Тогда Давыдов выкладывал разговоры в интернет, вызывая бурю негодования. В одной записи Давыдов просил федерального судью снизить срок тюремного заключения на семь лет; его просьба была удовлетворена, и позже судья извинился, что не может сделать большего.
Система, которую разоблачил Давыдов, не могла слишком долго терпеть подобную активность. Бывший десантник, он появился на судебном заседании в марте. Он выглядел изможденным и ходил с палкой после того, как провел несколько недель в одиночной камере и был избит тюремными надзирателями.
Однако на его лице была улыбка, которая обнажила некоторые из его золотых зубов.
«В этой стране нет судебной системы», — сказал Давыдов в коротком интервью из своей камеры в зале суда, несмотря на неоднократные протесты судебного пристава.«Людей пытают в тюрьмах. Полное беззаконие».
В 2016 году местный суд постановил удалить записи Давыдова из Интернета, заявив, что они наносят «репутационный ущерб» судебной системе и могут «спровоцировать митинги протеста». (Записи все еще доступны на YouTube.) В отдельном заявлении областной суд заявил, что не обнаружил никаких нарушений после изучения всех дел, которые велись судьями, которым звонил Давыдов.
«Нет оснований полагать, что просьбы звонящего повлияли на решения судей», — говорится в заявлении.
Многие из судей, о которых говорил Давыдов, были освобождены от своих обязанностей, в том числе и тот, который отпустил Городилова по делу об управлении автомобилем в нетрезвом виде. В знак недовольства Кремля судами в регионе в прошлом году Кремль отказался продлить новый срок полномочий главного судьи Перми.
В отличие от типичного русского активиста из Москвы или Санкт-Петербурга, Давыдов не является утонченным интеллектуалом, и его семья не похожа на советских диссидентов. Родился в семье рабочего, Давыдов вел небольшой бизнес по аренде автомобилей и вел обычный образ жизни, прежде чем он решил разоблачить коррупцию в судебной системе России.
Все началось с того, что он начал звонить сотрудникам дорожной полиции, чтобы отстаивать интересы друзей, уличенных в вождении в нетрезвом виде или обвиненных в других проступках.
По его словам, со временем он понял, что «все уровни правительства коррумпированы», и предпринял новые шаги. Зная, что судьи часто выносят решения «после телефонного звонка», он решил проверить, сработает ли это на самом деле. Так и произошло — суд вынес решение в его пользу по делу, в котором судебный пристав-исполнитель пытался наложить административный штраф после того, как Давыдов спорил с ним у входа в здание суда.
Такой успех побудил его делать больше. Он начал вызывать судей по случайным делам, чтобы узнать, как работает система.
«Когда он увидел, насколько откровенно коррумпированы наши судьи, у него как будто открылись глаза», — сказал в интервью его друг Сергей Клявин.
Со временем и практикой Давыдов научился звучать как настоящий высокопоставленный судья. Он говорил властным голосом могущественного чиновника, источая превосходство. Он называл точный номер дела и полностью перечислял имя обвиняемого.Он будет использовать бюрократический жаргон, известный только кому-то из российской правовой системы кафкианской.
Кроме судей, он звонил в прокуратуру и чиновников мэрии. Результат всегда был одним и тем же: бюрократы, как крупные, так и мелкие, молчаливо признавали неписаные правила игры, разоблачая, как Россия управляется набором неформальных практик, которые связывают вертикаль власти, построенную Путиным, в цепочку подчинения.
Это был лишь вопрос времени, когда система, которую он выставил, нанесет ответный удар.
В 2016 году он позвонил Марине Заббаровой, главному следователю Перми. Давыдов притворился заместителем главы следственного комитета, российского аналога ФБР. Заявив, что он просто передает инструкции, полученные из Кремля, Давыдов приказал местным правоохранительным органам создать благоприятные условия для правящей партии «Единая Россия» на предстоящих парламентских выборах.
«Любые провокации против« Единой России »должны быть прекращены в полную силу», — сказал Давыдов Заббаровой.
«Я слышал вас», — сказал старший следователь. «Я все понимаю, объяснять не надо».
Давыдов был впервые задержан в мае 2016 года, за несколько часов до запланированной встречи с репортером в Перми. Его обвинили в вымогательстве денег у чиновника мэрии, которому он звонил, и угрожал опубликовать запись их разговора в Интернете, если она не заплатит. Давыдов отверг обвинение, указав на многочисленные нарушения в деле.
Он говорит, что его избивали в тюрьме в Перми, и медицинские работники подтвердили, что его правая ключица была сломана во время пребывания в тюрьме.Тюремный надзиратель отказал ему в разрешении использовать трость, которая могла бы помочь облегчить исключительно болезненную кисту на его левой ноге. Его регулярно бросали в одиночную камеру за мелкие проступки, такие как неспособность встать, когда тюремный охранник входил в его камеру.
Однажды, когда он отказался выходить из камеры, потому что ходить было слишком больно, тюремные охранники вытащили его, разбили его головой о бетонный пол, обыскали и затолкали обратно внутрь, сказал он. В мучительной боли Давыдов схватил со своего стола кусок хлеба и швырнул его в охранников, якобы сломав себе нос.
За это нападение приговор Давыдову был продлен на четыре года. Когда судья огласил приговор, Давыдов возразил, сказав слово «олень», что в России означает очень глупый человек. Это повлекло за собой обвинение в неуважении и еще пять лет тюрьмы. Он обжаловал решения в Европейском суде по правам человека.
«Цель состоит в том, чтобы изолировать его», — сказала Лариса Алферова, адвокат Давыдова, которая будет представлять его интересы в апелляции. «Они не отпустят его; они проследят, чтобы он оставался в тюрьме.«
После задержания бизнес Давыдова рухнул, а его жена Екатерина Давыдова рассказала своей 15-летней дочери, что он уехал заниматься новым бизнесом далеко.
«Как известно, на развитие нового бизнеса уходит много времени», — сказала Екатерина Давыдова.
А Раздел от 29.03.2020
Почему пора отказываться от эпитетов «проевропейский» и «пророссийский»
Неверно называть избранного президента Молдовы Майю Санду «проевропейской».Не потому, что ее нет, а потому, что это само по себе не должно определять, что такое она или Молдова.
Молдова, как правило, не является страной, о которой слишком много заголовков во всем мире, тем не менее, последние несколько дней она была в поле зрения международных СМИ, избрав свою первую женщину-президентом Майю Санду во втором туре президентских выборов. 15 ноября.
Масштаб победы Санду — она набрала более 57 процентов голосов — над ее оппонентом, действующим президентом Игорем Додоном, вызвал много шума в СМИ вокруг выборов, как и длинные, часто бесконечные очереди на избирательных участках за пределами Молдовы.(Диаспора страны получила более 15 процентов всех голосов, тем самым создавая довольно хорошую симметрию с денежными переводами, которые эти молдавские экспатрианты отправляют домой каждый год, что составляет около 15 процентов ВВП).
Усталый, ленивый рассказ
В то время как любое международное внимание приветствуется для страны, которую так игнорируют, гораздо менее приветствуется слишком частое повествование о выборах, которое изображает победу «проевропейского» Санду над «пророссийским» Додоном.
Это почти повсеместное описание сложных выборов ленивое и несколько невежественное. Хуже того, это говорит о том, что у молдаван мало свободы воли, чтобы решать для себя, какой будущий курс должна избрать их страна, и они способны голосовать только в том случае, если им придается геополитическое значение.
Это тоже неточно.
Хотя Санду почти наверняка будет стремиться к укреплению отношений Молдовы с Европейским Союзом, она, как никто другой, осознает, что членство в блоке не будет даже отдаленной возможностью в течение десятилетий.Она была избрана не на основании ложных обещаний о членстве в ЕС, и при этом она не пообещала установить тесные связи с Россией, где живут и работают тысячи молдаван. Вместо этого ее кампания была сосредоточена на проблемах, с которыми молдаване сталкиваются в повседневной жизни, в первую очередь на бедности и коррупции.
Санду также (в отличие от выборов 2016 года, когда она чуть не проиграла) отказалась (по крайней мере публично) от помощи соседней Румынии, опасаясь напугать этнические русские, украинцы и гагаузские меньшинства Молдовы, которые составляют около четверти населения и которые Понятно нервничать, когда Румыния проявляет какой-либо интерес, рассматривая это как первый шаг к окончательному объединению двух стран.(Большая часть современной Молдовы исторически была неотъемлемой частью Румынии, но хотя разговоры о «воссоединении» были широко распространены в начале 1990-х годов, немногие когда-либо серьезно относились к этой идее, не в последнюю очередь потому, что большинство молдаван выступают против этого, а большинство румын — за исключением некоторые бешеные националисты — понимают, что поглощение самой бедной страны Европы обанкротит их экономику).
«Промолдавский»
Хотя Санду определенно можно назвать «проевропейской» в том смысле, что она верит в то, что мы можем назвать европейскими ценностями (такими как достойный уровень жизни, верховенство закона, свободная пресса, терпимость и прогресс), она является в первую очередь «промолдавским».
Примерно такое же, неточное повествование также присутствует в репортажах о Беларуси за последние несколько месяцев. Там имя лидера оппозиции Светланы Тихановской почти всегда предваряется эпитетом «проевропейский», как будто она ставит Европу выше Беларуси. Она этого не делает и четко заявила, что ее единственная цель — увидеть в стране свободные и справедливые выборы, на которых белорусы могут сами решать будущее своей страны.
Если это постоянное стремление определить лидеров, таких как Санду и Тихановская (или, если на то пошло, Владимир Зеленский в Украине, Георгий Гахария в Грузии и Никол Пашинян в Армении), как «проевропейских», прежде всего, было исключительно частью российской тактики, направленной на то, чтобы напугать население этих стран, чтобы они думали, что они вот-вот будут переданы Европейскому Союзу, который не причинит им ничего, кроме вреда, это может быть понятно.Но, увы, это так же часто встречается в западной прессе, как и в публикациях Кремля.
Это не «проевропейский» или «пророссийский». Это не обязательно должно быть «или-или». Мир не является — к большому огорчению средств массовой информации — черным и белым. Есть множество нюансов, местных проблем, которые волнуют избирателей гораздо больше, чем геополитика. Наивно наивно предполагать, что Молдова, Беларусь, Украина, Грузия и Армения существуют только в рамках «ЕС против России» или «Восток против Запада» и будут поглощены целиком, если они не предпочтут одну сторону другой.
Не в последнюю очередь потому, что это играет на руку тем — таким, как Владимир Путин или румынским националистам, которые считают, что Молдова является неотъемлемой частью Румынии, — которые действительно не хотели бы ничего больше, чем проглотить их целиком.
–
Фото: официальная страница Майи Санду в Facebook.
–
В отличие от многих новостных и информационных платформ, Emerging Europe можно читать бесплатно, и всегда будет. Здесь нет платного доступа. Мы независимы, мы не связаны и не представляем какие-либо политические партии или бизнес-организации.Мы хотим самого лучшего для развивающейся Европы, ни больше, ни меньше. Ваша поддержка поможет нам и дальше распространять информацию об этом удивительном регионе.
Здесь вы можете внести свой вклад. Спасибо.
70 лет российской угрозе — клуб «Валдай»
На этой неделе в Англии прошел юбилейный саммит НАТО, посвященный 70-летию организации. Королева Елизавета дала прием в Букингемском дворце в честь юбилея.Дональд Трамп на этот раз не использовал никаких, казалось бы, сверхъестественных трюков. Вновь были осуждены «агрессивные действия» России. Все шло, как было, есть и будет всегда.
Несмотря на ритуальный характер саммита, 70-летие НАТО представляет собой удобную возможность оценить ретроспективу Североатлантического союза как во время холодной войны, так и после ее завершения. Несмотря на отсутствие упоминания СССР в уставе НАТО, было совершенно прозрачно и очевидно, что главной целью создания этой организации было противостояние Советскому Союзу.Каждый может выбрать, кого он хочет атаковать, используя соответствующие эпитеты: в то время как одни могут сослаться на необходимость борьбы с «советской угрозой», другие могут вспомнить «агрессивные планы западных вооруженных сил». Однако дело не в эпитетах.
Суть дела заключалась в том, что европейские страны были неспособны обеспечить свою безопасность без американского ядерного и военного зонтика (или были вынуждены это делать). Попытки ряда европейских стран создать подобный военный союз без США ни к чему существенному не привели.Созданный за два года до НАТО в 1947 году, Western Union (переименованный в Западноевропейский союз в 1954 году) был в значительной степени «спящей» организацией, не влияющей на реальную политику. Попытка создать европейское оборонное сообщество параллельно с Европейским сообществом угля и стали в 1952 году с очень амбициозными целями вплоть до создания единой европейской армии окончательно провалилась. В результате архитектура европейской безопасности (и роль НАТО) с того времени до наших дней основывалась на двух столпах: имманентном противодействии России и вполне очевидном американском доминировании в военных вопросах Европы.За 70 лет было много примеров, свидетельствующих о том, что не всем членам НАТО эта ситуация нравилась, но это не изменило ее сути.
При этом все ключевые вопросы безопасности в период холодной войны решались исключительно на двустороннем советско-американском уровне. В этом отношении очень важно отсутствие НАТО на переговорах во время Карибского кризиса. Все решалось между лидерами СССР и США, хотя, если бы этот кризис перерос в «горячую» войну, другие члены НАТО должны были бы выполнить свои обязательства по статье 5 устава и в результате стать легитимными. мишени для советского ответа.В целом в то время, особенно после Карибского кризиса, СССР и США, несмотря на обоюдно угрожающую риторику, фактически всячески пытались избежать прямого военного конфликта, используя в случае локальных конфликтов различных прокси. Так было во время арабо-израильских войн, во Вьетнаме и Афганистане. Понимание того, что локальные конфликты не должны перерастать в большую войну, стало, пожалуй, одним из главных уроков той эпохи. Сейчас этот урок все больше забывается рядом членов НАТО, и именно поэтому в сегодняшнем НАТО нет и не будет единства.
Ситуация изменилась. Холодная война закончилась, исчезла и основная цель альянса. Начались поиски нового контекста для деятельности НАТО. Попытки объявить исламистский экстремизм новой серьезной угрозой для НАТО разрушили карьеру (наряду с взятками) тогдашнего генерального секретаря НАТО Вилли Клааса. Его заявления по этому поводу были сочтены слишком политически некорректными. В результате в 1999 году НАТО приняла глобальную стратегию, которая расширила сферу действия альянса с Европы и Северной Атлантики на весь мир.Самая крупная (и пока безуспешная) военная операция НАТО в этот период проводится за пределами Европы, в Афганистане.
В этот же период произошло несколько раундов расширения НАТО. Новые участники альянса принесли с собой свою историческую / мнимую (эпитет, опять же, у каждого может быть свой) неприязнь к России. И поэтому антироссийский вектор деятельности НАТО снова возродился.
В то же время ключевая цель альянса, судя по его уставным документам, «коллективная защита», провалилась, как только дело дошло до возможности прямого, а не виртуального столкновения с Россией.Впервые это произошло в 1999 году в Косово, после знаменитого марша российских военных на аэродром Приштины. Это действие внесло ощутимый дисгармонизм в уже разработанный план монополии НАТО в послевоенном Косово с разделением секторов ответственности только между членами альянса. Несмотря на то, что некоторые горячие головы (в основном британцы) говорили, что Россия должна прекратить эту десантную операцию, и надеялись вытеснить российских солдат из аэропорта, большинство стран НАТО, участвовавших в операции (в основном французы, но не только они), категорически против этого. прямая конфронтация и риск перерастания локального конфликта в крупную войну Россия-НАТО.
Второй пример еще более очевиден. Это связано с тем, что российский военный самолет был сбит турками во время конфликта в Сирии. Было очень интересно наблюдать, как представители НАТО сразу же попытались максимально дистанцироваться от этого инцидента. По их реакции было ясно, что произошедшее было частной и односторонней инициативой Турции, и как бы Россия ни отреагировала, о введении статьи 5 устава НАТО речи не шло.Примечательно, что диалог и военное взаимодействие между Россией и США сейчас налажены и функционируют именно в Сирии. Это сделано только для этой цели: уменьшить риск прямого столкновения.
В том же контексте, если мы посмотрим на те военные конфликты, которые произошли на постсоветском пространстве в последние годы (события в Грузии в 2008 году и на востоке Украины с 2014 года), несмотря на всю антироссийскую риторику, члены НАТО, на самом деле, не отправляйте туда свои воинские контингенты для непосредственного участия в боевых действиях (другое дело наемники, советники и поставки оружия).Причина вполне понятна: в любом случае существует нежелание перерастать конфликт в большую общеевропейскую войну с непредсказуемым (а точнее, предсказуемо разрушительным) результатом.
Таким образом, мы можем сделать очень четкий вывод о том, что среди членов НАТО, по крайней мере, нет консенсуса относительно того, следует ли автоматически переносить отдельные инциденты с Россией в соответствии со статьей 5 Хартии. Фактически, преобладающий стереотип «зонтика НАТО» о том, что альянс всегда будет защищать любого союзника от пресловутой «российской угрозы», может выглядеть не более чем иллюзией.Естественно, понимание этого — не повод проверить на прочность зонтик НАТО, а сам факт того, что важнейшая составляющая единства НАТО в противодействии России — всего лишь иллюзия — это, согласимся, очень значимый результат семидесяти лет. лет существования альянса.
русских троллей отправили американским избирателям графические расистские твиты
Внимание: эта история содержит оскорбительный контент.
В 2016 году рьяная банда русских троллей наводнила Twitter сотнями тысяч вызывающих разногласий постов, обвиняющих демократов в сатанинских практиках и поддержке изнасилований, в попытке повлиять на президентские выборы, согласно новому анализу базы данных Twitter, проведенному авторами. NBC News.
Попытка обмануть тысячи пользователей, заставив их распространять графические расовые эпитеты в социальных сетях, переплетая провокационный контент с дезинформацией и ложью.
Твиты были обнаружены в базе данных. Более 202 000 удаленных русских твитов троллей, которые NBC News собрали из трех источников, знакомых с интерфейсом прикладного программирования Twitter или API, онлайн-системой, которая позволяет сторонним разработчикам программного обеспечения работать с данными, лежащими в основе твитов пользователей. .
Набор был создан путем перекрестных ссылок на список из 2 752 подтвержденных русских троллей, опубликованный Комитетом по разведке Палаты представителей в октябре, на записанные твиты, которыми владеют источники.В результате с 3 июня 2011 г. по 26 августа 2017 г. была отправлена база данных твитов из более чем 450 учетных записей российского агентства интернет-исследований «фабрика троллей».
Все источники просили анонимно, чтобы их не идентифицировали как возможное нарушение политики Твиттера в отношении разработчиков; два источника попросили не называть их имени, потому что сами не хотели становиться мишенями для русских троллей.
В то время как Twitter удалил твиты из общего доступа, NBC News смогла сделать перекрестные ссылки на многие твиты между наборами данных и онлайн-архивами.
Полученные твиты представляют собой выборку всего контента, созданного троллями.
По словам Майкла Макфола, который был послом США в России с 2012 по 2014 год в администрации Обамы, провокационные твиты являются свидетельством кампании Кремля по поддержке Дональда Трампа, нанесению ущерба Хиллари Клинтон и срыву разговоров во время президентской гонки 2016 года.
Целью было «посеять сомнение и раздор в Америке», — сказал Макфол. «Это часть более грандиозной стратегии сделать все относительным.Нет правды. Нет демократии против автократии ».
Русские, которые буквально изобрели слово« дезинформация »или дезинформация , для определения практики распространения заведомой лжи с целью обмана, оцифровали свое мастерство и внедрили его прямо в наши выборы .
Сатанинские ритуалы
Один из мемов, поддерживаемых троллями, пытался связать кандидата Клинтона с сатанизмом и оккультизмом.
Помимо хорошо известной мистификации «Пиццагейт», тролли раздули слухи о том, что Клинтон и ее руководитель кампании Джон Подеста присутствовал на сатанинском ритуале, истории, которую сайт проверки фактов Snopes назвал «ложной».»
Слухи начались после того, как WikiLeaks получил и начал публиковать электронные письма, взломанные из личного аккаунта Подесты Gmail. В одном из писем брат Подесты спрашивает, будет ли он участвовать в званом ужине» Духовная кулинария «, устроенном артисткой Мариной Абрамович.
4 ноября 2016 года, всего за несколько дней до выборов, WikiLeaks направил своих подписчиков на сообщение в блоге на сайте, в котором были найдены видеоролики из сюрреалистической инсталляции Абрамовича «Духовная кулинария» 1996 года, в которых были такие фразы, как «порезанным острым ножом». глубоко в средний палец левой руки съешь боль », свиньей кровью на стене галереи.
Абрамович позже сказала, что Джон Подеста не присутствовал на ужине, который она устроила, чтобы поблагодарить участников Kickstarter, и что на мероприятии готовили традиционные супы в ее квартире.
Дословные твиты, отправленные подтвержденными российскими троллями из списка, опубликованного Комитетом по разведке Палаты представителей, демонстрируют попытку усилить сатанинское повествование.
«РАЗРЫВ: Фонд Клинтона заплатил оккультной« Жрице приготовления духов »10K за« оперативную поддержку »», — написал русский тролль @WorldnewsPoli в Твиттере 11 ноября.5.
«RT @_Makada_: WikiLeaks: Председатель кампании Клинтона Джон Подеста посетил сатанинский ритуал» Духовное приготовление «#SpiritCooking, — написал в Твиттере русский тролль @_NickLuna_ накануне.
И тролль @ J0hnLarsen написал в Твиттере: «RT @KevinAnth: Мне понравилось видео на @YouTube от @markdice https://t.co/jPvIB1pNTr Хиллари Клинтон» Духовная кулинария «Сатанинский ритуал».
Снимок экрана из твита от 4 ноября 2016 года, размещенного в аккаунте ведущего канала FOX News Шона Хэннити.Эта история была поддержана российскими троллями и консервативными веб-сайтами, в том числе Drudge Report и веб-сайтом ведущего Fox News Шона Хэннити и лентой в Твиттере, превратив его в рассказ о поклонении дьяволу и причудливом пиршестве крови.
Популярный сайт агрегирования новостей правого толка Drudge Report разместил вверху изображения, чтобы продвигать необоснованную историю оккультного ритуала Клинтона.В течение нескольких часов тема #spiritcooking стала популярной в Твиттере.
«Из когнитивной науки мы хорошо знаем, что как только вы что-то прочитали, особенно если это оформлено как новости, трудно сбрасывать со счетов как фальшивку, даже если вам сказали, что это фальшивка», — Джефф Хэнкок, профессор коммуникаций в Стэнфордском университете и директор-основатель Стэнфордской лаборатории социальных сетей, сообщил NBC News.
И когда люди уже согласны с предпосылкой лжи — например, что Хиллари Клинтон не заслуживает доверия, — игнорировать откровенную ложь становится еще труднее, сказал он.
«Мы действуем по умолчанию, — сказал Хэнкок. «Мы должны работать на неверия.»
Изнасилование
Еще одной попыткой троллей было привязать демократов и либералов к поддержке изнасилований. Более 460 твитов содержали слово «изнасилование» или его вариацию, например, «изнасилование».
Например, плодовитый русский тролль-аккаунт @TEN_GOP написал в Твиттере: «Всего через 2 дня после #NiceAttack глупые либералы приветствуют #rapefugees! Как глупо! #RNCinCLE» 17 июля 2016 года.
«RT @wiredterrier: @ ThePatriot143 Женщины, которые голосуют за Хиллари, говорят, что их дочери изнасилование — это нормально, и их будут оклеветать», — написал русский тролль @EmileeWarren 15 октября 2016 года. В ходе кампании один тролль-аккаунт ответил на твит другого пользователя об отношениях Дональда Трампа с его старшей дочерью Иванкой, искажая его, превращая его в непристойную ссылку на одну из дочерей президента Барака Обамы.
Расизм
Русские тролли также включали расистские оскорбления, темы и темы в свои сообщения.
Одна линия атаки снова исказила элемент одного из украденных писем Подесты. Клинтон прислал израильскую статью о мусульманине, оставленном умирать на обочине дороги. Первоначальный автор сослался на то, как власти могли подумать о мужчине как о «песчаном нигде». Обрезанный снимок экрана был вырван из контекста и переработан, чтобы сказать, что Клинтон имеет в виду мусульман, используя этот эпитет, а затем раскручивался через Twitter через аккаунты российских троллей.
«RT @ObamaBash: Никогда #HillaryBecause Называя Трампа расистом в просочившемся электронном письме, она назвала мужчину-мусульманина» песочным ниггером «, написала в Твиттере @hyddrox 10 октября.15 августа 2016 года, через несколько дней после вторых президентских дебатов.
Snopes сообщил, что в социальных сетях распространялось утверждение о том, что Клинтон использовала уничижительный термин, является «ложным».
Некоторые из отчетов также сильно повлияли на расовые темы, например, протесты в Фергюсоне, штат Миссури, летом 2014 года после смерти невооруженного чернокожего подростка Майкла Брауна от рук белого полицейского, который позднее большое жюри отказалось предъявить обвинение по какому-либо пункту обвинения.
«Все протестующие в Фергюсоне, ваша рука в крови! #CopsWillBeCops #FergusonShooting», — написал в Твиттере русский тролль @ EvaGreen69 15 марта 2015 года.
Другой твит русского тролля @ staywoke88, который выдавал себя за участника протеста Black Lives Matter, взял самый печально известный лозунг белых националистов и изменил его, сделав его про-черным заявлением.
Скриншот ретвита российского тролля, в котором упоминается пресловутый лозунг белых националистов: «Мы должны обеспечить существование нашего народа и будущее для белых детей». Лицо в профиле было размытым, потому что бывшие российские тролли заявили, что украли фотографии профилей в Интернете для своих аватарок в социальных сетях.Эксперты заявили, что темы были выбраны намеренно, чтобы раскрыть давно существующие различия в американской культуре.
«Смысл операции по дезинформации заключается не в том, чтобы создать новые расколы в обществе, а в том, чтобы раздвинуть существующие расколы», — сказал Грэм Бруки, заместитель директора Лаборатории цифровых криминалистических исследований Атлантического совета, Вашингтон. базирующийся аналитический центр международных отношений.
Искажения в год выборов
Согласно сообщениям об утечке внутренних документов из Агентства интернет-исследований, троллям были предложены конкретные темы и темы для обсуждения, а также назначены ежедневные квоты.
Внедряясь в различные нишевые онлайн-диалоги во время президентской гонки 2016 года и раздвигая границы разговоров, русские тролли сигнализировали другим участникам беседы, что допустимо делать более резкие заявления.
«Даже если они не собираются говорить« Хиллари Клинтон несет ответственность за #PizzaGate », это снижает ценовой барьер, если сказать:« Запри ее », — сказал Бруки. «Это очень полезный результат для тех, кто хочет сеять хаос в демократических институтах.
И даже если читатели отвергали диковинные заявления, тролли все равно привлекали их внимание. Для российских пропагандистов это было победой.
В конце концов, стратегия троллей была экспортом методов, которые Россия использовала в течение многих лет. внутри страны, чтобы заставить граждан видеть себя не частью нации, а членами меньших этнических групп и групп, основанных на идентичности, и играть всеми сторонами друг против друга.
«Они хотят, чтобы мы сражались между собой», — сказал Макфол, бывший посол .«Тогда мы отвлекаемся. Мы не говорим о Сирии. Мы не говорим об американском лидерстве. Мы сомневаемся, выживет ли демократия. Мы в меньшей степени играем на международном уровне — и это хорошо для России».
8 экранизаций русской литературы
Русская литература играет важную роль в культурном наследии страны. Обычно это сопровождается эпитетом «великий». Иностранные режиссеры восхищаются загадочной русской душой, а иногда даже пытаются перенести русскую классику в свою реальность.Некоторые экранизации действительно стоит посмотреть.
Мы в ExploRussia обожаем русскую литературу, поэтому составили список самых интересных обработок русской литературы зарубежных режиссеров.
1. Война и мир, 2016, Том Харпер
«Война и мир» Тома Харпера можно назвать одной из крупнейших премьер последних лет на BBC. Мини-сериал частично снимался в Санкт-Петербурге, в дворцовых интерьерах. Масштаб впечатляет.
Любая попытка снять четырехтомник Толстого кажется нереальной целью.Том Харпер также теряет множество деталей, сжимая повествование до шести эпизодов. Но что примечательно в новой версии рассказа Пьера Безухова и Наташи Ростовой, так это то, что с первой же серии чувствуешь глоток свежего воздуха.
В фильме «Война и мир», снятом на BBC, много путаницы, но сериал сделан с большим уважением к первоисточнику и теперь, пожалуй, его можно назвать лучшей экранизацией романа Льва Толстого.
2. «Записная книжка молодого врача и другие рассказы», 2012, Sky Arts
В 2012 году многие россияне были удивлены тем, что британцы сделали серию по рассказам Михаила Булгакова «Записная книжка молодого врача».В роли молодого врача, только что окончившего медицинский институт и отправленного на работу в российскую глушь, сыграл главный герой Гарри Поттера — Дэниел Рэдклифф.
Следует отметить, что британская экранизация — это черная комедия с тонким юмором и глубокой моралью. Он получил положительные отзывы многих кинокритиков. Зрителей даже не раздражали звучащие изредка за кадром русская народная музыка, образ крестьян и очередная противоречивая попытка раскрыть менталитет русского народа.
3. «Анна Каренина», 2012, Джо Райт
Экранизация «Анна Каренина» Льва Толстого в постановке Джо Райта со сценаристом Томом Стоппардом вызвала самые ожесточенные споры в России. Создателей обвинили в криминальной шутке, неправильном кастинге Киры Найтли и непонимании намерений Толстого.
Но вряд ли режиссер хотел нас обидеть. Мастер костюмированных мелодрам Джо Райт и знаток русской культуры Том Стоппард работают в контексте сложившейся зарубежной традиции экранизации «Анны Карениной».Больше внимания уделяется отношениям Карениной и Вронского, чем эмоциональным затруднениям Левина.
Однако создатели отсняли его так, как будто предыдущих 30 экранизаций романа не было. Так они строят высокую мелодраму о невозможной любви и разрушительной страсти. Но главное здесь — идея сыграть роман в театральных декорациях, практически превратив его в мюзикл. Поэтому сравнение фильма с романом бессмысленно. Фильм принадлежит Джо Райту. Но Толстой — лишь повод для организации этой тайны.
4. «Доктор Живаго», 2002, Джакомо Кампиотти
И снова Кира Найтли! Судя по всему, авторы считают, что Кира Найтли похожа на настоящую русскую женщину. 🙂 Британская экранизация «Доктора Живаго» Бориса Пастернака — это мини-сериал с Кейрой Найтли и Хансом Мэтисоном в главных ролях.
Адаптация выглядит очень аккуратно.
5. «Доктор Живаго», 1965, Дэвид Лин
Нельзя не упомянуть еще один культовый фильм «Доктор Живаго» режиссера Дэвида Лина, в котором снялись Омар Шариф и британская актриса Джули Кристи.Фильм получил пять «Оскаров»: лучший адаптированный сценарий, лучшая цветная операторская работа, лучшая художественная постановка, лучший оригинальный музыкальный саундтрек (и лучший дизайн костюмов).
В фильме показаны очень чувственные и страстные отношения Лары и Юрия Живаго.
6. «Любовь и смерть», 1975, Вуди Аллен
Вуди Аллен известен своей любовью к русской литературе. Отсылки к Достоевскому можно увидеть в фильмах «Иррациональный человек», «Матч-пойнт», «Сны Кассандры», Чехова — в «Ханне и ее сестрах» и «Пули над Бродвеем».Однако главная дань Аллена русской литературе — комедия «Любовь и смерть».
В фильме смешано все: балы, война с Наполеоном, дуэль, Прокофьев, многочисленные цитаты из Голливуда и русские адаптации русской литературы. Фильм Аллена развенчивает миф о загадочной русской душе. Он довольно весело объясняет, почему все в России страдают, думают о Боге, мечтают о Москве и несчастны в браке.
7. Двойник, 2013, Ричард Айоаде
Нервный срыв, шизофрения или настоящий двойник.
Большинство рассказов Достоевского легко превращаются в психологические триллеры. Режиссер Ричард Айоаде также увидел эту возможность в «Двойнике», пригласив Джесси Айзенберга сыграть две версии одного героя. Будь то Саймон Джеймс или Джеймс Саймон, его отличительная черта — его характерная харизма и вдумчивые монологи. «Двойник» — это история о стремлении к эксклюзивности и постоянной конкуренции с лучшей версией себя. Он снят Айоаде в театральных декорациях.
8.Любовники, 2008, Джеймс Грей,
Федор Достоевский — один из самых популярных русских писателей. Американский режиссер Джеймс Грей взял малоизвестный авторский рассказ «Белые ночи» и пересказал в декорациях современной американской действительности.
Очаровательная Мишель переезжает в новую квартиру рядом с подтвержденным холостяком Леонардом. Его семья хочет выдать его замуж за друга семьи. Так что этому нерадивому мужчине предстоит непростой выбор между другом семьи и чрезвычайно изменчивым новым соседом.
Главные роли в фильме Грея «Влюбленные» сыграли популярные голливудские актеры Хоакин Феникс, Гвинет Пэлтроу, Уинесса Шоу.В 2008 году драма была номинирована на «Золотую пальмовую ветвь».
Если вы больше любите читать книги, узнайте список лучших книг о России.
Как Алексей Навальный разоблачил коррупцию в России
ПОЖЕРТВОВАТЬАлексей Навальный, яростный противник президента России Владимира Путина и самый видный оппозиционный деятель страны, лежит в коме в сибирской больнице после очевидного отравления.
Поскольку мир шокирован тем, что выглядит как покушение на Навального, есть сторона его карьеры, которая рискует остаться незамеченной.Хотя он наиболее известен за пределами страны как оппозиционный политик, его самое прочное наследие может заключаться в создании неортодоксального, но очень эффективного бренда журналистских расследований.
Никто не станет утверждать, что Навальный в какой-то мере беспристрастен. В конце концов, именно он придумал эпитет «партия жуликов и воров» для обозначения путинской «Единой России». И у него была долгая карьера в российской политике: он работал с либеральной оппозиционной партией «Яблоко», стал одним из основателей ныне не существующего правого народного движения, провел энергичную, но в конечном итоге безуспешную кампанию на пост мэра Москвы и пытался бросить вызов Путину. на пост президента в 2018 году.
Но его президентские амбиции закончились политизированной дисквалификацией, и стало ясно, что тщательно управляемая система Путина, которая использует атрибуты демократии как фиговый лист для мускулистого авторитаризма, никогда не позволит ему прорваться через политику розничной торговли.
В этих обстоятельствах Навальный сделал борьбу с коррупцией ключевым — и чрезвычайно успешным — элементом своей политической работы.
Поступая так, он стал одним из лучших следователей страны, используя тщательно задокументированные доказательства и великолепно снятые видео, чтобы разоблачить коррупцию, лежащую в основе режима Путина.Независимо от того, занимал ли Навальный когда-либо государственную должность, именно это разоблачение гнилых устоев современной России может в конечном итоге стать его самым прочным вкладом в развитие страны.
Его видео-расследования являются образцами этого жанра, в которых ловко используются кадры с дронов, высококачественная анимация и шутливый юмор, чтобы сложные схемы были понятны и понятны обычным людям.
Лучшим постановкам Навального также удается превратить сам процесс расследования в увлекательную историю.Пожалуй, самый известный пример: его расследование богатства бывшего премьер-министра Дмитрия Медведева начинается с объяснения того, как квитанция о покупке пары дорогих кроссовок Nike, сопоставленная с публично опубликованной фотографией, привела его исследователей к обращению, которое в конечном итоге показало империя недвижимости.
Кредит: Фонд борьбы с коррупцией На видео Навального обувь тогдашнего премьер-министра Дмитрия Медведева совпадает с просочившейся товарной квитанцией с важным адресом.
Неудивительно, что одни только пять главных расследований Навального собрали более 82 миллионов просмотров на YouTube.
Для специалистов и тех, кто хочет погрузиться глубже, фильмы сопровождаются длинными, состоящими из нескольких частей текстами, которые тщательно объясняют лежащую в основе документацию. Помимо простого изложения фактов, тексты обернуты пояснительным языком, который подчеркивает, как нетрудовое богатство лежит в основе коррумпированной системы, построенной Путиным.
Щелкните слайдер, чтобы узнать о некоторых из крупнейших расследований Навального:
🔗Крупное расследование Навального
➤В рамках флагманского расследования, которое собрало более 35 миллионов просмотров, Навальный показал россиянам, что их тогдашний премьер-министр Дмитрий Медведев, известный как относительно дружелюбное лицо с любовью к высокотехнологичным гаджетам, на самом деле является одним из богатейших людей страны. люди.Через сеть благотворительных фондов, контролируемых близкими соратниками, Медевев владеет обширными земельными участками, горными курортами, квартирами в дореволюционных особняках, яхтами и другими предметами роскоши. (Просмотр на YouTube)
➤ ➤В ходе расследования 2015 года Фонд борьбы с коррупцией Навального сосредоточил внимание на семье тогдашнего генерального прокурора России Юрия Чайки.Фильм и сопроводительный текст обвиняют двух сыновей Чайки в использовании связей своего отца для незаконного обогащения, описывая серию коррупционных схем, включающих связи с кровавой бандой, незаконную приватизацию и теневые государственные строительные тендеры. В фильмах объяснялось, что прибыль от этих схем была вложена в иностранные инвестиции, в том числе в ультра-роскошный греческий отель и швейцарскую виллу. (Посмотреть на YouTube)
➤ ➤В ходе расследования 2017 года команда Навального разоблачила гламурный образ жизни Николая Чоле, сына пресс-секретаря Путина Дмитрия Пескова.По сообщениям, Чоулз, который редко работал и отбывал срок в тюрьме, наслаждался жизнью, наполненной дорогими автомобилями и недвижимостью, яхтами, частными самолетами и соревнованиями по прыжкам на лошадях. Его успех, по словам Навального, «пример того, как в России, где 20 миллионов человек живут за чертой бедности, а 70 процентов могут только мечтать о зарплате в 45 000 рублей, можно жить прекрасной жизнью. На высшем уровне. НИЧЕГО не делая ». (Просмотр на YouTube)
➤ ➤Навальный начинает это видео 2017 года с разочарованного крика: «Я злюсь, расстроен и грустен.Я выдергиваю волосы «. Причина? Его команда была разгромлена: независимый телеканал «Дождь» избил его, и стало известно о роскошной даче, принадлежащей президенту Путину, недалеко от Выборга. В оставшейся части видео показано, «чего не было у« Дождя »», где зрители проводят экскурсию по объекту, снятому с помощью дрона, и объясняют структуру его собственности. (Посмотреть на YouTube)
➤Роман Анин, член сети OCCRP и редактор одного из новейших российских изданий расследований, IStories, не скрывает влияния Навального.
«Конечно, — признает он, — следователи Навального не следуют журналистским стандартам и никогда не пытаются выслушать другую сторону, что экономит их время и упрощает понимание их историй. Но я по-прежнему считаю, что мы [журналисты] в России проигрываем им с точки зрения эффективности ».
«Он создал, пожалуй, самое эффективное СМИ в стране, занимающееся расследованиями», — говорит Анин. «Количество историй, которые они публикуют, творческий подход, которым они находят истории и доставляют их своей аудитории, — это то, чему мы должны учиться.”
Кредит: Фонд борьбы с коррупцией На скриншоте из расследования дела тогдашнего премьер-министра Дмитрия Медведева Навальный объясняет структуру собственности на роскошную загородную дачу.
Собственные сотрудники Навального не претендуют на беспристрастность. В интервью изданию «Медуза» его пресс-секретарь Кира Ярмыш недвусмысленно заявила: «Мы не журналисты», — сказала она.«Если нам что-то не нравится и мы считаем такого-то человека мошенником, то мы можем прямо назвать его мошенником».
Никита Кулаченков, один из следователей Навального, высказал то же самое. По его словам, его команда занимается «чем-то средним между журналистикой и политикой».
Но работа, которую он описывает в Фонде борьбы с коррупцией Навального, очень похожа на небольшое расследование.
Он и два других главных исследователя работают с Навальным, чтобы определить темы, которые заслуживают освещения в печати и поддаются предпочтительному для группы формату видеопрезентации.
«Иногда нам приходится исследовать отдельные районы или людей из-за политических событий», — говорит Кулаченков. «Сейчас выборы проходят в нескольких регионах, поэтому мы делаем упор на этом. В прошлом году в Москве прошли выборы, поэтому мы сосредоточились на Москве, исследуя кандидатов от «Единой России» ».
Команда тщательно продумывает, как сделать свои истории максимально привлекательными, особенно потому, что финансовое положение на плаву зависит от пожертвований зрителей.
«Мы начали с YouTube не с самого начала, — говорит Кулаченков.«Но в 2015 году мы выпустили фильм [Генеральный прокурор Юрий] Чайка — это был наш первый фильм-расследование. По стандартам YouTube в то время он был чрезвычайно успешным… и мы подумали: «Мы должны перейти на YouTube, [поскольку он] распространяет больше, чем любые статьи» ».
И, как любые профессиональные журналисты-расследователи, Фонд борьбы с коррупцией также заботится о доверии. «Мы всегда публикуем документы, на основе которых делаются наши выводы», — поясняет Кулаченков. «Мы понимаем, что некоторые люди хотели бы их проверить и вычитать.… У нас есть поддержка для каждого заявления, которое мы делаем ».
Обычная официальная реакция на коррупцию, которую раскрывает Навальный, — это обычно полное молчание, — говорит Кулаченков. Он описывает это как симптом жизни в недемократической стране, где государственные служащие не чувствуют ответственности перед избирателями. Но команда также сталкивалась с неоднократными судебными исками. Он говорит, что применялись и более закулисные приемы. За одним коллегой, который, в отличие от него, остался в стране, иногда следят неизвестные мужчины.
И он подозревает, что офис Фонда противодействия коррупции прослушивается: «[Мы] что-то обсуждаем по телефону, и через неделю мы видим, что кипрские компании начинают менять структуру своих акционеров .

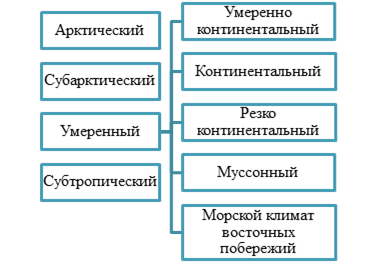
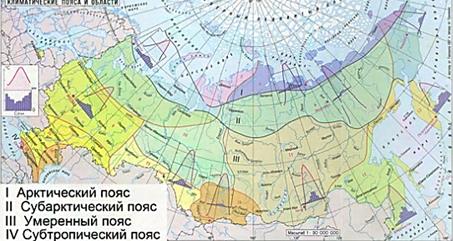
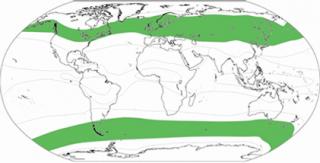 Умеренный климатический пояс — один из самых широких и обхватывает территории нашей планеты, лежащие между 40-ми и 60-ми параллелями в северном и южном полушариях.
Умеренный климатический пояс — один из самых широких и обхватывает территории нашей планеты, лежащие между 40-ми и 60-ми параллелями в северном и южном полушариях.




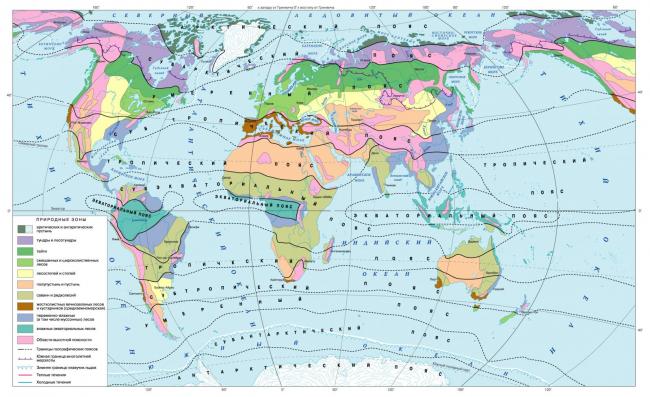


 Большая часть России находится в зоне умеренного климатического пояса. При этом времена года имеют чёткие границы, а солнечная активность в значительной мере изменяется по месяцам. Температурные режимы зимы и лета ярко противоположены. Самый обширный климатический пояс страны для метеорологического удобства подразделяют на четыре участка: континентальный, умеренно континентальный, резко континентальный и муссонный.
Большая часть России находится в зоне умеренного климатического пояса. При этом времена года имеют чёткие границы, а солнечная активность в значительной мере изменяется по месяцам. Температурные режимы зимы и лета ярко противоположены. Самый обширный климатический пояс страны для метеорологического удобства подразделяют на четыре участка: континентальный, умеренно континентальный, резко континентальный и муссонный.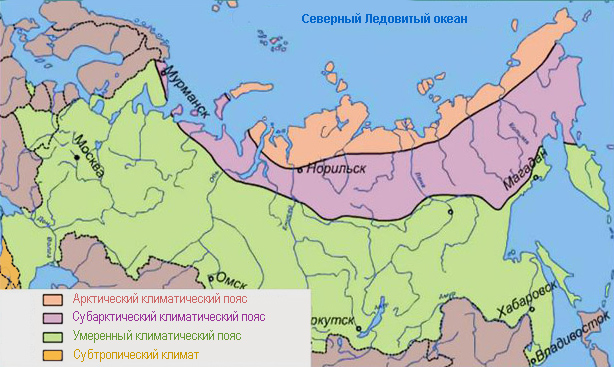








 С основными (амфотерными) оксидами – оксидами металлов
С основными (амфотерными) оксидами – оксидами металлов Составьте уравнения реакций:
Составьте уравнения реакций:
 Взаимодействуют с основаниями
Взаимодействуют с основаниями
 Назовите примеры кислот, используя таблицу растворимости.
Назовите примеры кислот, используя таблицу растворимости.  Таким образом был составлен ряд Н. Н. Бекетова, который сейчас называют электрохимический ряд напряжения металлов. Если металл находится до водорода, то он реагирует с кислотами, если после, то – нет. Запишите соответствующие уравнения реакций:
Таким образом был составлен ряд Н. Н. Бекетова, который сейчас называют электрохимический ряд напряжения металлов. Если металл находится до водорода, то он реагирует с кислотами, если после, то – нет. Запишите соответствующие уравнения реакций: (Приложение 2)
(Приложение 2) Домашнее задание:
Домашнее задание:


 Авакумова Н.П. Гуминовые пелоидопрепараты: перспективы использования в медицинской практике//Материалы 5-й науч. шк. «Болота и биосфера». Томск: ЦНТИ, 2006. С. 63-72.
Авакумова Н.П. Гуминовые пелоидопрепараты: перспективы использования в медицинской практике//Материалы 5-й науч. шк. «Болота и биосфера». Томск: ЦНТИ, 2006. С. 63-72. 1980. № 1. С. 54-59.
1980. № 1. С. 54-59.
 citycollegiate.com
citycollegiate.com Газ производится на водороде.
Газ производится на водороде.


 С другой стороны, у вас может быть дипротонная кислота, вот серная кислота, которая представляет собой h3SO4, что означает, что у нее есть два протона, которые нужно отдать раствору, поэтому дипротоновая кислота di для двух, и она дает два протона на молекулу кислоты. Вы можете подниматься вверх и вверх, там есть различные типы кислот h4PO4, но, чтобы вы знали, это две наиболее распространенные, с которыми вы, вероятно, будете контактировать в первые дни своей химии, и это в значительной степени основные свойства кислот и оснований. .
С другой стороны, у вас может быть дипротонная кислота, вот серная кислота, которая представляет собой h3SO4, что означает, что у нее есть два протона, которые нужно отдать раствору, поэтому дипротоновая кислота di для двух, и она дает два протона на молекулу кислоты. Вы можете подниматься вверх и вверх, там есть различные типы кислот h4PO4, но, чтобы вы знали, это две наиболее распространенные, с которыми вы, вероятно, будете контактировать в первые дни своей химии, и это в значительной степени основные свойства кислот и оснований. . 

 )
)

 С практической точки зрения, кислота любое вещество, повышающее концентрацию H + ион при растворении в воде. База — любое вещество
что увеличивает концентрацию иона ОН — при
растворяется в воде.
С практической точки зрения, кислота любое вещество, повышающее концентрацию H + ион при растворении в воде. База — любое вещество
что увеличивает концентрацию иона ОН — при
растворяется в воде. образованный металлами и неметаллами. Оксиды неметаллов растворяются
в воде с образованием кислот. CO 2 растворяется в воде с образованием
угольная кислота, SO 3 дает серную кислоту, а P 4 O 10 реагирует с водой с образованием фосфорной кислоты.
образованный металлами и неметаллами. Оксиды неметаллов растворяются
в воде с образованием кислот. CO 2 растворяется в воде с образованием
угольная кислота, SO 3 дает серную кислоту, а P 4 O 10 реагирует с водой с образованием фосфорной кислоты. В каждом из этих соединений кислый водород
присоединен к атому кислорода. Таким образом, все эти соединения
примеры оксикислот.
В каждом из этих соединений кислый водород
присоединен к атому кислорода. Таким образом, все эти соединения
примеры оксикислот.  Поэтому мы должны
ожидайте найти соединения, которые лежат между крайностями металла
и оксиды неметаллов, или гидроксиды металлов и неметаллов. Эти
соединения, такие как Al 2 O 3 и Al (OH) 3 ,
называются амфотерными (буквально «либо, либо
оба «), потому что они могут действовать как кислоты или основания.Al (OH) 3 ,
например, действует как кислота, когда реагирует с основанием.
Поэтому мы должны
ожидайте найти соединения, которые лежат между крайностями металла
и оксиды неметаллов, или гидроксиды металлов и неметаллов. Эти
соединения, такие как Al 2 O 3 и Al (OH) 3 ,
называются амфотерными (буквально «либо, либо
оба «), потому что они могут действовать как кислоты или основания.Al (OH) 3 ,
например, действует как кислота, когда реагирует с основанием. Таким образом, момент образования иона H + в
водный раствор, он связывается с молекулой воды.Брнстед
модель, в которой ионы H + переносятся от одного иона
или молекулы к другому, поэтому имеет больше смысла, чем
Теория Аррениуса, которая предполагает, что ионы H + существуют в
водный раствор.
Таким образом, момент образования иона H + в
водный раствор, он связывается с молекулой воды.Брнстед
модель, в которой ионы H + переносятся от одного иона
или молекулы к другому, поэтому имеет больше смысла, чем
Теория Аррениуса, которая предполагает, что ионы H + существуют в
водный раствор.
 Брнстедское определение базы
применяется к такому количеству ионов и молекул, что почти легче
подсчитывать вещества, такие как следующие, которые нельзя Бренстед
основания, потому что у них нет пар несвязывающей валентности
электроны.
Брнстедское определение базы
применяется к такому количеству ионов и молекул, что почти легче
подсчитывать вещества, такие как следующие, которые нельзя Бренстед
основания, потому что у них нет пар несвязывающей валентности
электроны.

 Если в формуле нет этой метки, то соединение рассматривается как молекулярное соединение, а не как кислота.
Если в формуле нет этой метки, то соединение рассматривается как молекулярное соединение, а не как кислота. Метка «aq» опущена для ясности.
Метка «aq» опущена для ясности. Фосфорная кислота входит в состав некоторых безалкогольных напитков.
Фосфорная кислота входит в состав некоторых безалкогольных напитков.









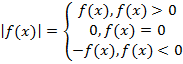

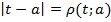
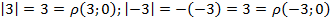
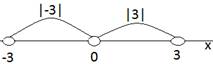
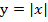
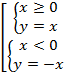
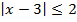
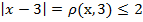
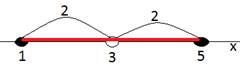
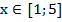
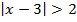
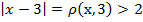
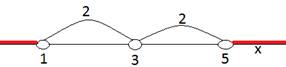
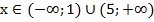
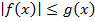
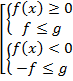

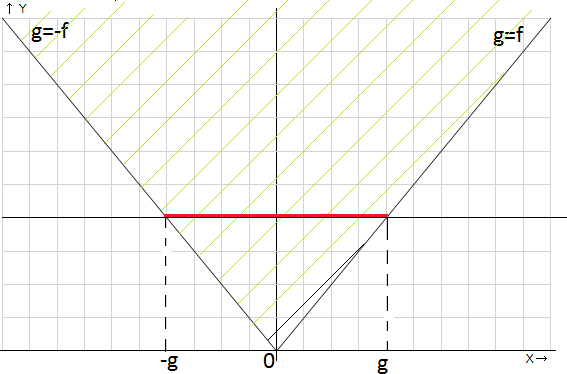
 . Решения неравенства
. Решения неравенства 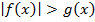
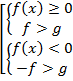
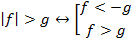
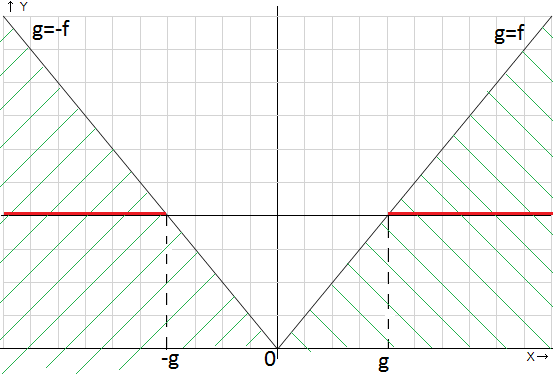
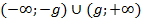 – показано красным.
– показано красным.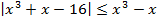
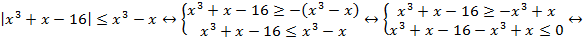
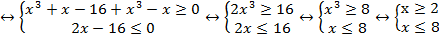

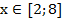
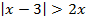
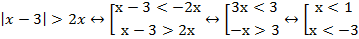


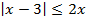
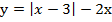
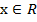
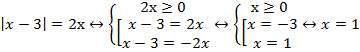
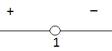
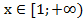 ; б)
; б) 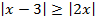
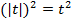 ):
):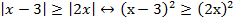
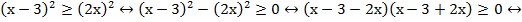
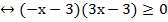
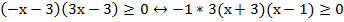
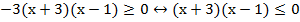
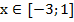
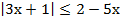 ;
;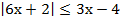 ;
;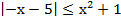 ;
;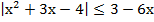 ;
;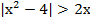 ;
;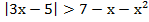 ;
; 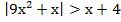 ;
; 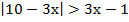 ;
;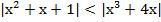 ;
;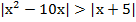 ;
;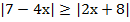 ;
;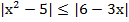 ;
;
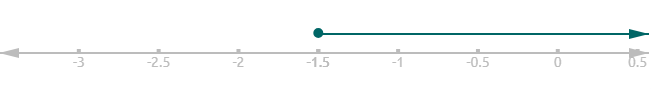
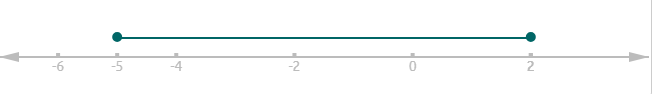

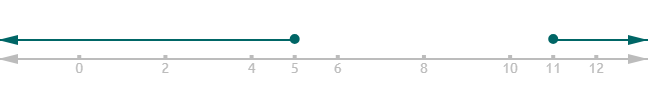





 ,
,  .
.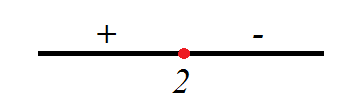 Получаем систему:
Получаем систему:


 найдено на промежутке
найдено на промежутке  , и, соответственно, этому промежутку не принадлежит, поэтому этот корень уравнения посторонний. Ответ:
, и, соответственно, этому промежутку не принадлежит, поэтому этот корень уравнения посторонний. Ответ: 



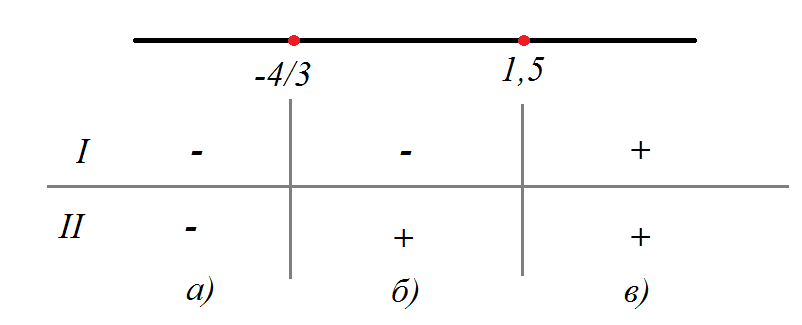





 ,
, 







 :
: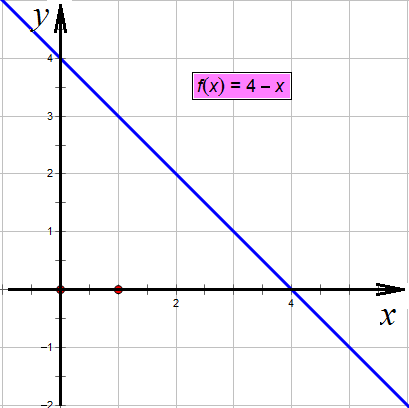

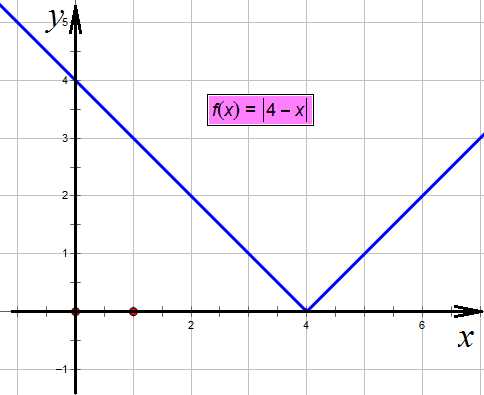
 – минус перевернет наш график вверх тормашками:
– минус перевернет наш график вверх тормашками: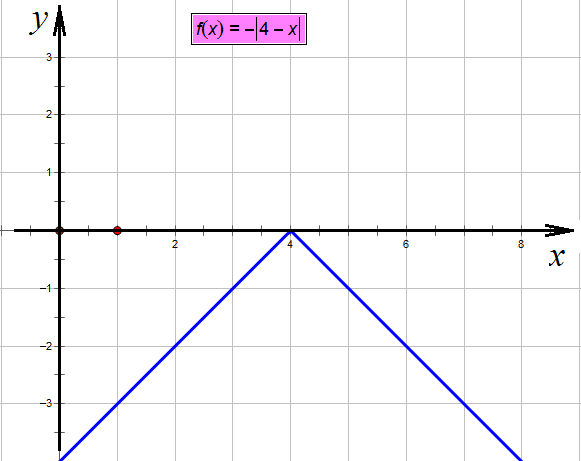




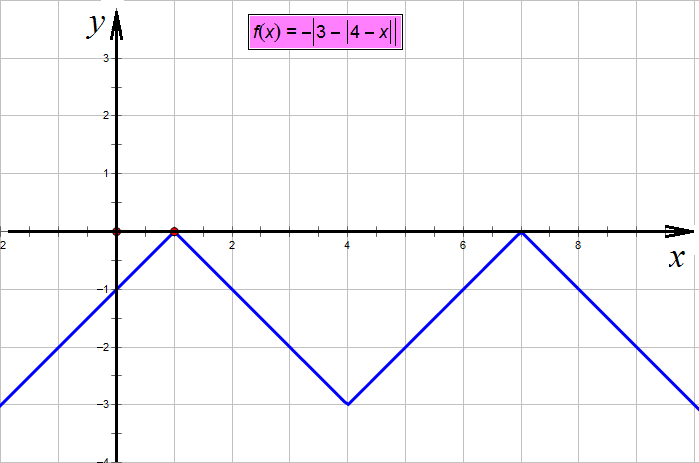



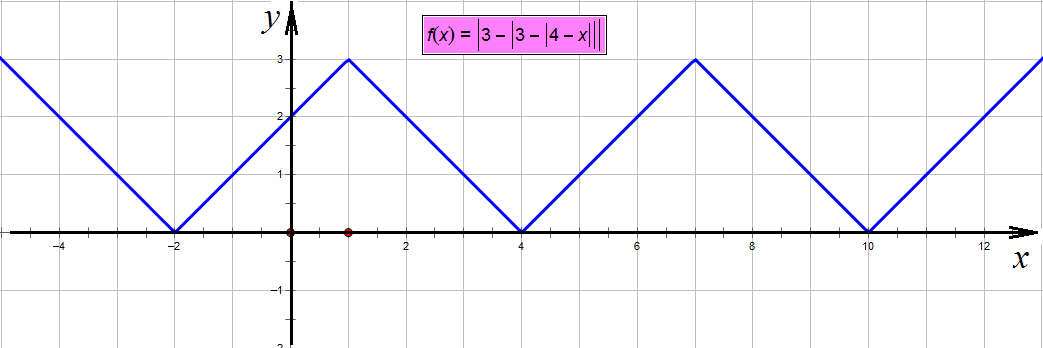
 , пересечения с которой и есть искомые корни:
, пересечения с которой и есть искомые корни:



 , слева под знаком модуля – парабола. Модуль переворачивает ту часть параболы, которая находится под осью х, вверх. Требуется найти те интервалы (отрезки), где прямая располагается выше параболы.
, слева под знаком модуля – парабола. Модуль переворачивает ту часть параболы, которая находится под осью х, вверх. Требуется найти те интервалы (отрезки), где прямая располагается выше параболы.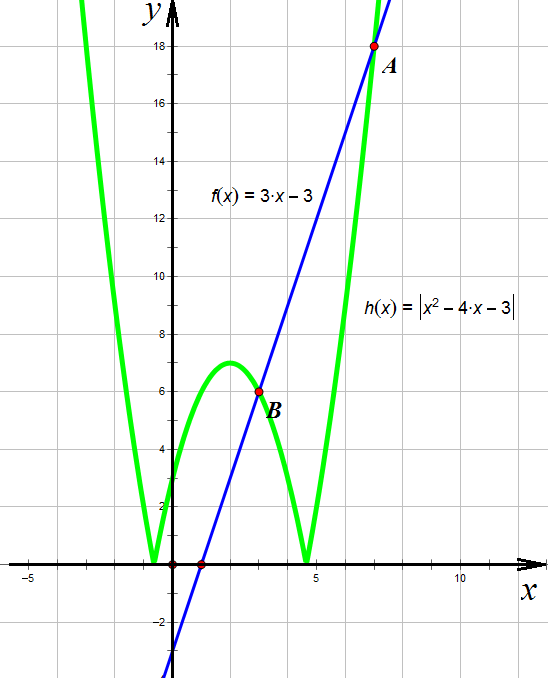


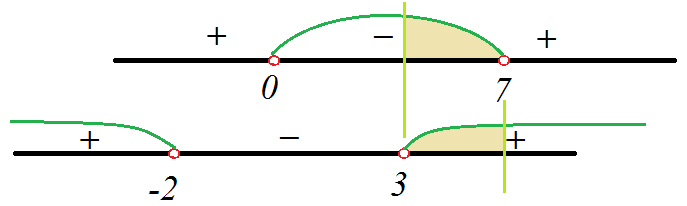





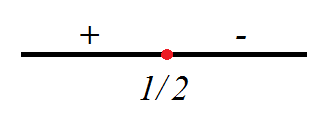



 , точка
, точка  этому промежутку не принадлежит, поэтому этот корень – посторонний. Ответ:
этому промежутку не принадлежит, поэтому этот корень – посторонний. Ответ: 







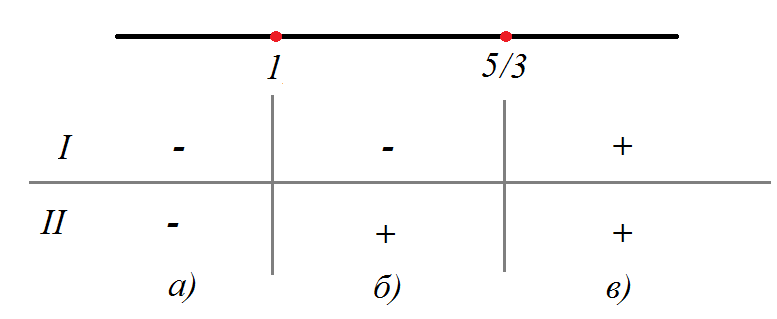




 -нет решений. Получается, что уравнению будет удовлетворять любое число из промежутка
-нет решений. Получается, что уравнению будет удовлетворять любое число из промежутка  (
( ]
]




 ,
, 
 ,
,  ,
, 

 ,
, 













 ]
]  [
[ )
)

 Тогда знак неравенства меняем, так как основание логарифма меньше 1:
Тогда знак неравенства меняем, так как основание логарифма меньше 1:
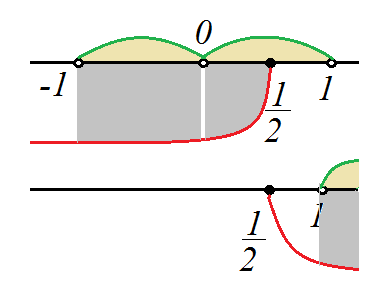



 (
( ]
] 



 )
) )
) )
) )
)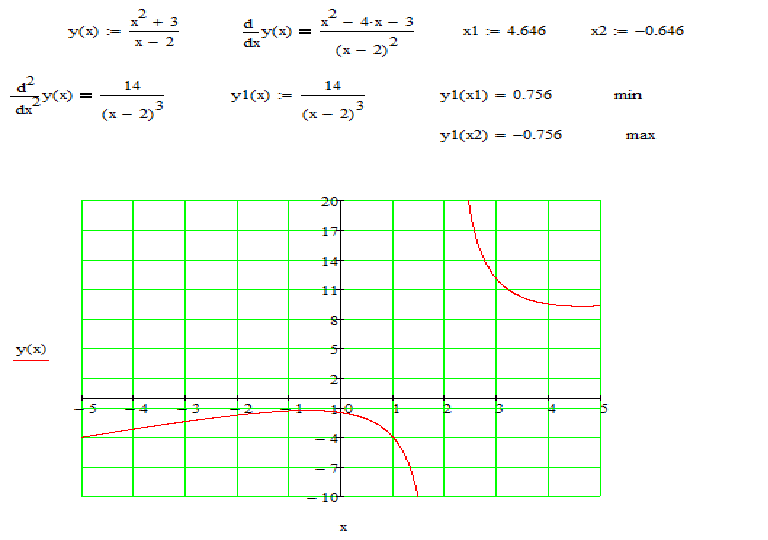 )
)
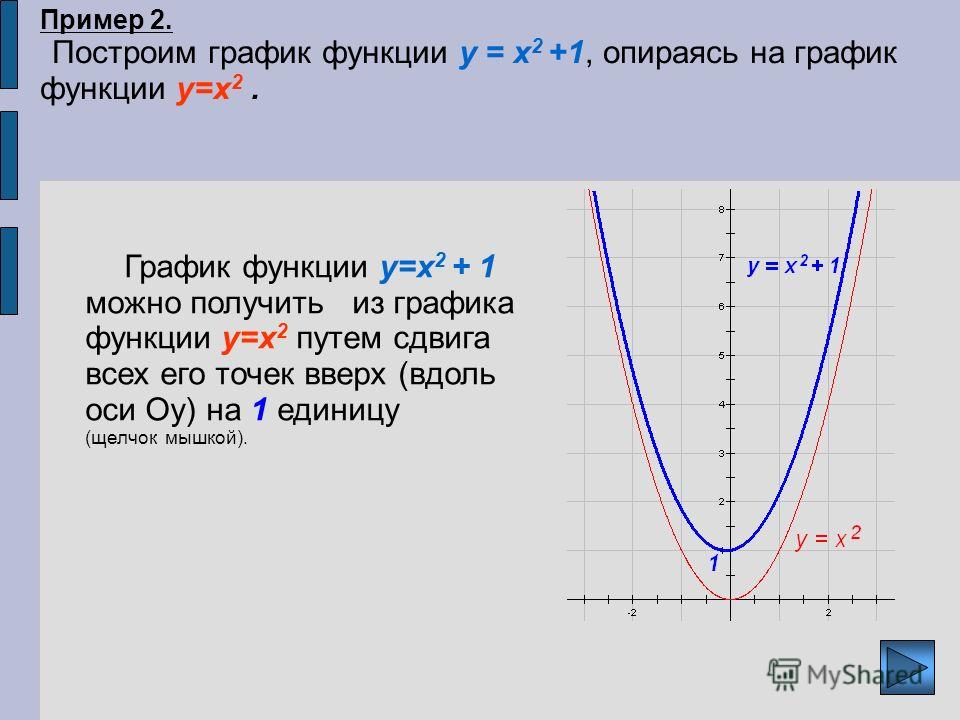 Значит, графики таких функций симметричны относительно оси 0y.
Значит, графики таких функций симметричны относительно оси 0y.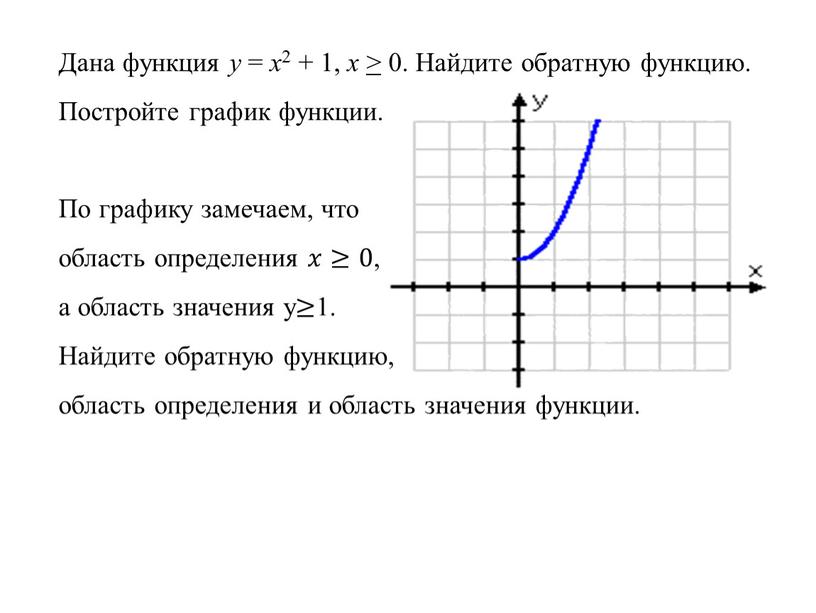



 Мы также смогли увидеть точки функции, а также начальное значение на графике.
Мы также смогли увидеть точки функции, а также начальное значение на графике.
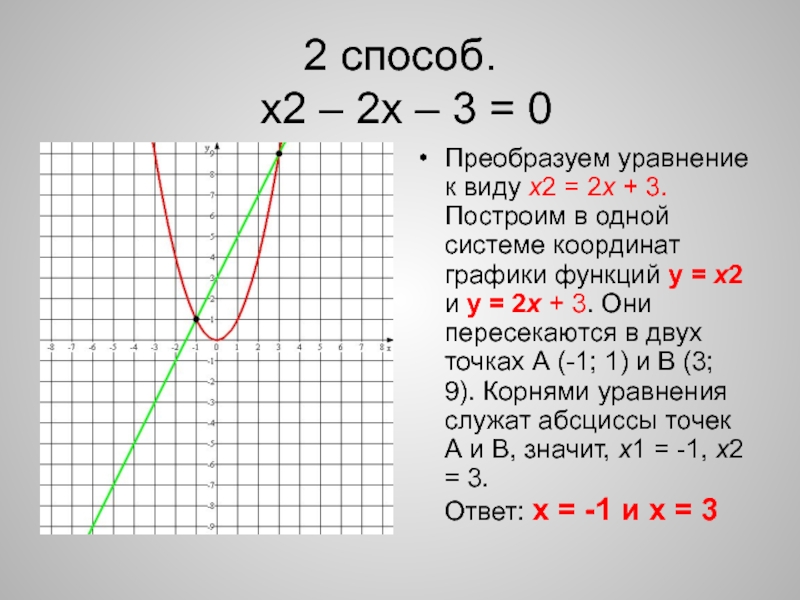 Мы столкнулись как с точкой пересечения y-, так и с наклоном в линейных функциях.
Мы столкнулись как с точкой пересечения y-, так и с наклоном в линейных функциях. Имейте в виду, что вертикальная линия — единственная линия, которая не является функцией.)
Имейте в виду, что вертикальная линия — единственная линия, которая не является функцией.) 
 Хотя это может быть не самый простой способ построить график функций такого типа, все же важно практиковать каждый метод.
Хотя это может быть не самый простой способ построить график функций такого типа, все же важно практиковать каждый метод.
 000 (изменение x иногда называют «RUN») мы получаем изменение на 8.000 — 2.000 = 6.000 по y. (Изменение y иногда называют «ПОДЪЕМ», а наклон равен m = RISE / RUN)
000 (изменение x иногда называют «RUN») мы получаем изменение на 8.000 — 2.000 = 6.000 по y. (Изменение y иногда называют «ПОДЪЕМ», а наклон равен m = RISE / RUN)
 То есть каждый x должен иметь УНИКАЛЬНЫЙ соответствующий л значение. Но посмотрите, что происходит, когда я пытаюсь найти « x = «:
То есть каждый x должен иметь УНИКАЛЬНЫЙ соответствующий л значение. Но посмотрите, что происходит, когда я пытаюсь найти « x = «: Практически каждый раз, когда они задают вам проблему, где
они постарались ограничить домен, вы должны позаботиться
с алгеброй и нарисуйте красивую картинку, потому что, вероятно, обратное
— это функция, но, вероятно, потребуются дополнительные усилия, чтобы показать это.В данном случае, поскольку размер домена x < 0 и
диапазон (из графика) равен 1 < y ,
то обратный будет иметь область 1 < x и
диапазон y < 0. Вот
как выглядит алгебра:
Практически каждый раз, когда они задают вам проблему, где
они постарались ограничить домен, вы должны позаботиться
с алгеброй и нарисуйте красивую картинку, потому что, вероятно, обратное
— это функция, но, вероятно, потребуются дополнительные усилия, чтобы показать это.В данном случае, поскольку размер домена x < 0 и
диапазон (из графика) равен 1 < y ,
то обратный будет иметь область 1 < x и
диапазон y < 0. Вот
как выглядит алгебра: )
) Что это за функция: y = 3x-2 2. Какова точка пересечения оси y в приведенном выше уравнении? 3. Решите относительно x: 16 = 5x + 1 4. Каков наклон этого уравнения: y = ½ x + 9 5. Запишите это уравнение в обозначении функции: y = 6p — 7
Что это за функция: y = 3x-2 2. Какова точка пересечения оси y в приведенном выше уравнении? 3. Решите относительно x: 16 = 5x + 1 4. Каков наклон этого уравнения: y = ½ x + 9 5. Запишите это уравнение в обозначении функции: y = 6p — 7 Он может быть направлен вверх (положительный наклон) или направлен вниз (отрицательный наклон).
Он может быть направлен вверх (положительный наклон) или направлен вниз (отрицательный наклон). Родительский граф сдвинулся влево на 1 единицу. Новое уравнение будет выглядеть так: y = (x + 1) 2 Горизонтальное перемещение всегда заключено в круглые скобки с x. Однако у этих уравнений есть одна хитрость — вы двигаетесь в противоположном направлении! Новая вершина: (-1,0)
Родительский граф сдвинулся влево на 1 единицу. Новое уравнение будет выглядеть так: y = (x + 1) 2 Горизонтальное перемещение всегда заключено в круглые скобки с x. Однако у этих уравнений есть одна хитрость — вы двигаетесь в противоположном направлении! Новая вершина: (-1,0) Когда наклон больше 1, график становится…
Когда наклон больше 1, график становится… 2-6 (2) — 5 = -12-12-5 = -29
2-6 (2) — 5 = -12-12-5 = -29


 см. Стоит отметить, что различных типов атомов, в отличие от молекул, относительно немного. Все их разновидности, которые на сегодняшний день известны человеку, собраны в так называемой таблице Менделеева (см. рис. 2)
см. Стоит отметить, что различных типов атомов, в отличие от молекул, относительно немного. Все их разновидности, которые на сегодняшний день известны человеку, собраны в так называемой таблице Менделеева (см. рис. 2)
 ) – молекулярные; гелий серебро (He, Ag) – атомарные.
) – молекулярные; гелий серебро (He, Ag) – атомарные.





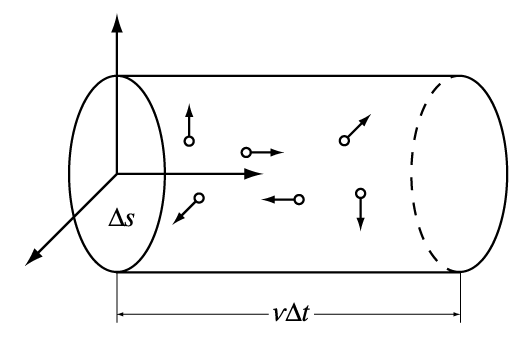
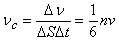
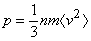
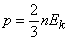
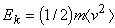 – средняя кинетическая энергия молекул газа (в расчете на одну молекулу).
– средняя кинетическая энергия молекул газа (в расчете на одну молекулу).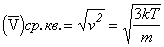 ,
,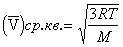
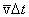 к полному числу столкновений ZDt, испытанных молекулой на этом пути,
к полному числу столкновений ZDt, испытанных молекулой на этом пути,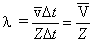
 и с площадью основания s = 4pa2 (рис.2). На самом деле, после каждого столкновения направление движения молекулы меняется, и нужно рассматривать ее движение в цилиндре, составленном как бы из отдельных колен, однако смысл рассуждений не меняется, если считать этот коленчатый цилиндр выпрямленным.
и с площадью основания s = 4pa2 (рис.2). На самом деле, после каждого столкновения направление движения молекулы меняется, и нужно рассматривать ее движение в цилиндре, составленном как бы из отдельных колен, однако смысл рассуждений не меняется, если считать этот коленчатый цилиндр выпрямленным.
 s. Используя (9), находим
s. Используя (9), находим . В результате получается известная в элементарной кинетической теории формула
. В результате получается известная в элементарной кинетической теории формула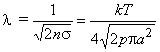





 Фотосинтез обеспечивает образование органических веществ, а следовательно, пищу для всех живых существ.
Фотосинтез обеспечивает образование органических веществ, а следовательно, пищу для всех живых существ.
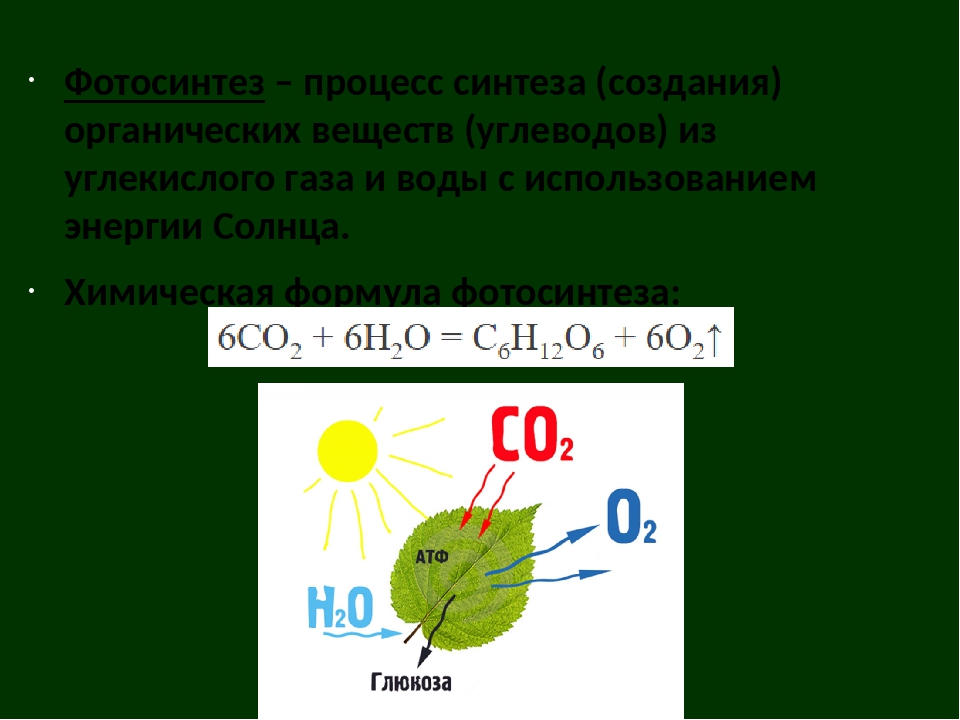
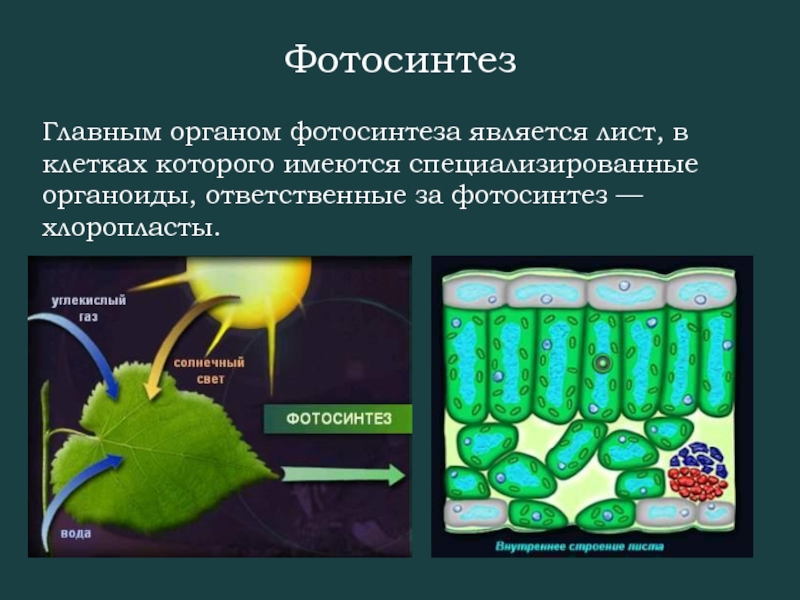 Гликолиз и дыхание): он тоже состоит из серии химических реакций, которые начинаются с соединения входящей молекулы с молекулой-«помощником» с последующей инициацией других химических реакций. Эти реакции приводят к образованию конечного продукта и одновременно воспроизводят молекулу-«помощника», и цикл начинается вновь. В цикле Калвина роль такой молекулы-«помощника» выполняет пятиуглеродный сахар рибулозодифосфат (РДФ). Цикл Калвина начинается с того, что молекулы углекислого газа соединяются с РДФ. За счет энергии солнечного света, запасенной в форме АТФ и НАДФ-H, сначала происходят химические реакции связывания углерода с образованием углеводов, а затем — реакции воссоздания рибулозодифосфата. На шести витках цикла шесть атомов углерода включаются в молекулы предшественников глюкозы и других углеводов. Этот цикл химических реакций будет продолжаться до тех пор, пока поступает энергия. Благодаря этому циклу энергия солнечного света становится доступной живым организмам.
Гликолиз и дыхание): он тоже состоит из серии химических реакций, которые начинаются с соединения входящей молекулы с молекулой-«помощником» с последующей инициацией других химических реакций. Эти реакции приводят к образованию конечного продукта и одновременно воспроизводят молекулу-«помощника», и цикл начинается вновь. В цикле Калвина роль такой молекулы-«помощника» выполняет пятиуглеродный сахар рибулозодифосфат (РДФ). Цикл Калвина начинается с того, что молекулы углекислого газа соединяются с РДФ. За счет энергии солнечного света, запасенной в форме АТФ и НАДФ-H, сначала происходят химические реакции связывания углерода с образованием углеводов, а затем — реакции воссоздания рибулозодифосфата. На шести витках цикла шесть атомов углерода включаются в молекулы предшественников глюкозы и других углеводов. Этот цикл химических реакций будет продолжаться до тех пор, пока поступает энергия. Благодаря этому циклу энергия солнечного света становится доступной живым организмам. Благодаря этому довольно сложному процессу фотосинтез у кукурузы осуществляется даже в очень жаркую, сухую погоду. Растения, в которых происходит такой процесс, мы называем C4-растениями, поскольку углекислый газ в начале цикла транспортируется в составе четырехуглеродной молекулы. C3-растения — это в основном растения умеренного климата , а C4-растения в основном произрастают в тропиках.
Благодаря этому довольно сложному процессу фотосинтез у кукурузы осуществляется даже в очень жаркую, сухую погоду. Растения, в которых происходит такой процесс, мы называем C4-растениями, поскольку углекислый газ в начале цикла транспортируется в составе четырехуглеродной молекулы. C3-растения — это в основном растения умеренного климата , а C4-растения в основном произрастают в тропиках. Именно от этого одного процента зависит вся жизнь на Земле.
Именно от этого одного процента зависит вся жизнь на Земле. Такой процесс получил название C3-фотосинтеза. Последующий цикл реакций (цикл Кальвина) приводит к образованию из ФГК сахара (например, глюкозы), а также ресинтезу рибулозобисфосфата. У некоторых растений (например, сахарного тростника, сои) наблюдается так называемый C4-фотосинтез, в реакциях которого CO2, восстанавливаясь, включается в состав органических кислот, имеющих четыре атома углерода (например, яблочной). При этом поглощение углекислоты идёт гораздо эффективнее, повышается и продуктивность растений.
Такой процесс получил название C3-фотосинтеза. Последующий цикл реакций (цикл Кальвина) приводит к образованию из ФГК сахара (например, глюкозы), а также ресинтезу рибулозобисфосфата. У некоторых растений (например, сахарного тростника, сои) наблюдается так называемый C4-фотосинтез, в реакциях которого CO2, восстанавливаясь, включается в состав органических кислот, имеющих четыре атома углерода (например, яблочной). При этом поглощение углекислоты идёт гораздо эффективнее, повышается и продуктивность растений.
 И они будут правы…
И они будут правы…
 Она проходит и днем, но вот свет для второй стадии уже не нужен. Необходимы в наличии в строме хлоропластов для осуществления цикла Кальвина молекулы углекислоты СО2, АТФ и НАДФ*Н.
Она проходит и днем, но вот свет для второй стадии уже не нужен. Необходимы в наличии в строме хлоропластов для осуществления цикла Кальвина молекулы углекислоты СО2, АТФ и НАДФ*Н. Особо преуспели в этом искусстве существа, выбравшие в качестве источника электронов молекулы воды. Оно и не мудрено: в среднем воду на Земле найти гораздо проще, чем какой-нибудь сероводород. Именно этот тип фотосинтеза выбрали предки сегодняшних растений, и с тех пор, в общем-то, жизнь здесь и завертелась.
Особо преуспели в этом искусстве существа, выбравшие в качестве источника электронов молекулы воды. Оно и не мудрено: в среднем воду на Земле найти гораздо проще, чем какой-нибудь сероводород. Именно этот тип фотосинтеза выбрали предки сегодняшних растений, и с тех пор, в общем-то, жизнь здесь и завертелась.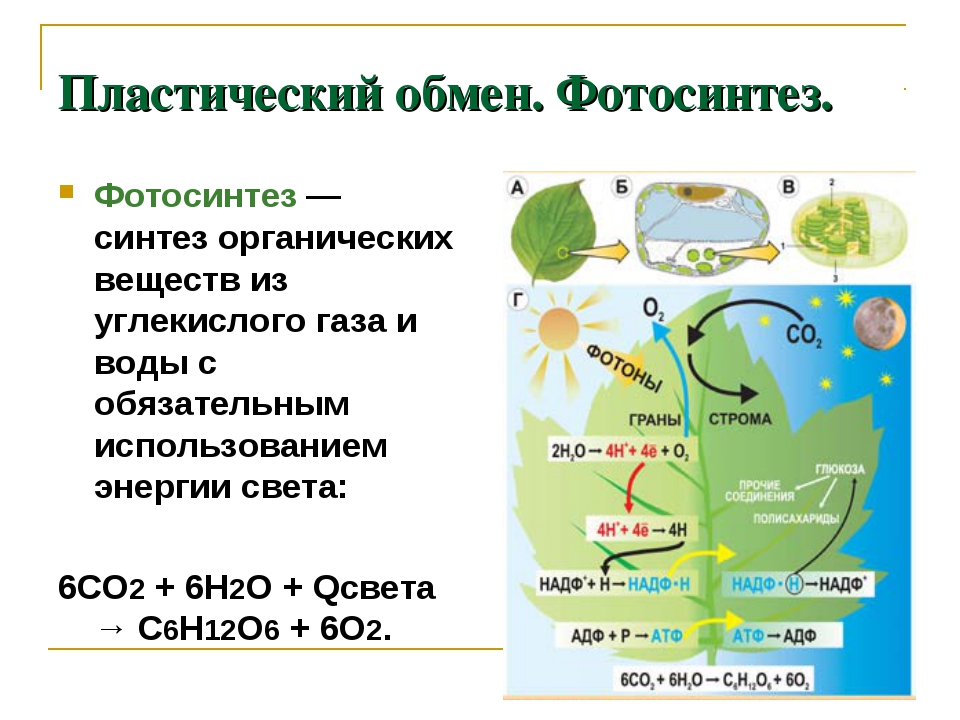 е. каждый четвертый углерод, связанный из СО2 при фотосинтезе, затем опять окисляется из-за фотодыхания.
е. каждый четвертый углерод, связанный из СО2 при фотосинтезе, затем опять окисляется из-за фотодыхания. Однако тучи снова начинают сгущаться. В своем свежем отчете Комитет по еде и сельскому хозяйству ООН вынужден был признать, что проблема голода снова усугубилась, а количество страдающих от недоедания в мире превысило 820 млн человек.
Однако тучи снова начинают сгущаться. В своем свежем отчете Комитет по еде и сельскому хозяйству ООН вынужден был признать, что проблема голода снова усугубилась, а количество страдающих от недоедания в мире превысило 820 млн человек. Подобные белки-укладчики (их называют шапероны), как правило, стабилизируют цепь собираемого белка во время сборки, давая ему время свернуться правильным образом. В этом-то и была проблема предыдущих работ: гены Рубиско действительно активно синтезировали белковые «кирпичики» фермента, но нехватка шаперонов не позволяла собирать достаточное количество Рубиско из полипептидных цепей-полуфабрикатов. Количество шаперонов тоже нужно было увеличивать! В очередном подходе к проблеме упрямого фермента исследователи совместили сверхэкспрессию двух генов субъединиц Рубиско со сверхэкспрессией шаперона RAF1, что привело к категорическому успеху предприятия: общее содержание Рубиско в листьях трансгенной кукурузы выросло на 30%. Крайне любопытно также то, что, несмотря на рост абсолютного количества Рубиско в листьях, доля активного фермента снизилась из-за механизмов обратной связи, «гасящих» активность фермента при его избытке.
Подобные белки-укладчики (их называют шапероны), как правило, стабилизируют цепь собираемого белка во время сборки, давая ему время свернуться правильным образом. В этом-то и была проблема предыдущих работ: гены Рубиско действительно активно синтезировали белковые «кирпичики» фермента, но нехватка шаперонов не позволяла собирать достаточное количество Рубиско из полипептидных цепей-полуфабрикатов. Количество шаперонов тоже нужно было увеличивать! В очередном подходе к проблеме упрямого фермента исследователи совместили сверхэкспрессию двух генов субъединиц Рубиско со сверхэкспрессией шаперона RAF1, что привело к категорическому успеху предприятия: общее содержание Рубиско в листьях трансгенной кукурузы выросло на 30%. Крайне любопытно также то, что, несмотря на рост абсолютного количества Рубиско в листьях, доля активного фермента снизилась из-за механизмов обратной связи, «гасящих» активность фермента при его избытке. Каждый белок и его ген — гармоничный элемент сложносопряженной системы, включающей тысячи других генов и белков и множество регуляторных каскадов. Точечные изменения структуры фермента или активности гена могут сводиться на нет другими компонентами системы, о которых мы можем просто не знать, или вообще приводить к обратному результату из-за какой-нибудь хитрой петли обратной связи. Понимание всех этих запутанных связей сделало бы из современных ученых истинных биоинженеров, позволив им перепроектировать организмы под свои нужды. Несомненно, мы уже живем в эпоху биотехнологий, но, несмотря на это, генная инженерия все еще остается очень непростым делом с негарантированными шансами на успех. Особенно, когда это касается таких амбициозных задач, как ускорение фотосинтеза. Но, как мы видим, первые подвижки в этом деле уже есть. Так что очень может быть, что мы стоим перед порогом очередной «зеленой революции».
Каждый белок и его ген — гармоничный элемент сложносопряженной системы, включающей тысячи других генов и белков и множество регуляторных каскадов. Точечные изменения структуры фермента или активности гена могут сводиться на нет другими компонентами системы, о которых мы можем просто не знать, или вообще приводить к обратному результату из-за какой-нибудь хитрой петли обратной связи. Понимание всех этих запутанных связей сделало бы из современных ученых истинных биоинженеров, позволив им перепроектировать организмы под свои нужды. Несомненно, мы уже живем в эпоху биотехнологий, но, несмотря на это, генная инженерия все еще остается очень непростым делом с негарантированными шансами на успех. Особенно, когда это касается таких амбициозных задач, как ускорение фотосинтеза. Но, как мы видим, первые подвижки в этом деле уже есть. Так что очень может быть, что мы стоим перед порогом очередной «зеленой революции».
 Используя радиоактивный изотоп углерода 14С, бумажную хроматографию и классические методы органической химии, Калвин и его группа смогли проследить биосинтетические пути фотохимических процессов. К 1956 стал ясным полный путь превращения углерода при фотосинтезе. За исследования в области ассимиляции диоксида углерода в растениях Калвин был удостоен в 1961 Нобелевской премии по химии.
Используя радиоактивный изотоп углерода 14С, бумажную хроматографию и классические методы органической химии, Калвин и его группа смогли проследить биосинтетические пути фотохимических процессов. К 1956 стал ясным полный путь превращения углерода при фотосинтезе. За исследования в области ассимиляции диоксида углерода в растениях Калвин был удостоен в 1961 Нобелевской премии по химии. О результатах сообщается в журнале Nature Communications.
О результатах сообщается в журнале Nature Communications. — Если бы хвойные деревья не смогли выжить в суровом зимнем климате, обширные территории в северном полушарии не были бы обжиты человеком, поскольку хвойные деревья давали дрова, жилье и другие предметы первой необходимости».
— Если бы хвойные деревья не смогли выжить в суровом зимнем климате, обширные территории в северном полушарии не были бы обжиты человеком, поскольку хвойные деревья давали дрова, жилье и другие предметы первой необходимости».
 Цианобактерии и планктонные водоросли могут расти на огромных участках воды, иногда полностью покрывая поверхность. В (d) глубоководном источнике хемоавтотрофы, такие как эти (e) термофильные бактерии, улавливают энергию неорганических соединений для производства органических соединений. В экосистеме, окружающей вентиляционные отверстия, обитает множество разнообразных животных, таких как трубчатые черви, ракообразные и осьминоги, которые получают энергию от бактерий.
Цианобактерии и планктонные водоросли могут расти на огромных участках воды, иногда полностью покрывая поверхность. В (d) глубоководном источнике хемоавтотрофы, такие как эти (e) термофильные бактерии, улавливают энергию неорганических соединений для производства органических соединений. В экосистеме, окружающей вентиляционные отверстия, обитает множество разнообразных животных, таких как трубчатые черви, ракообразные и осьминоги, которые получают энергию от бактерий.
 Стеки тилакоидов, называемые грана, образуют третий мембранный слой.
Стеки тилакоидов, называемые грана, образуют третий мембранный слой.
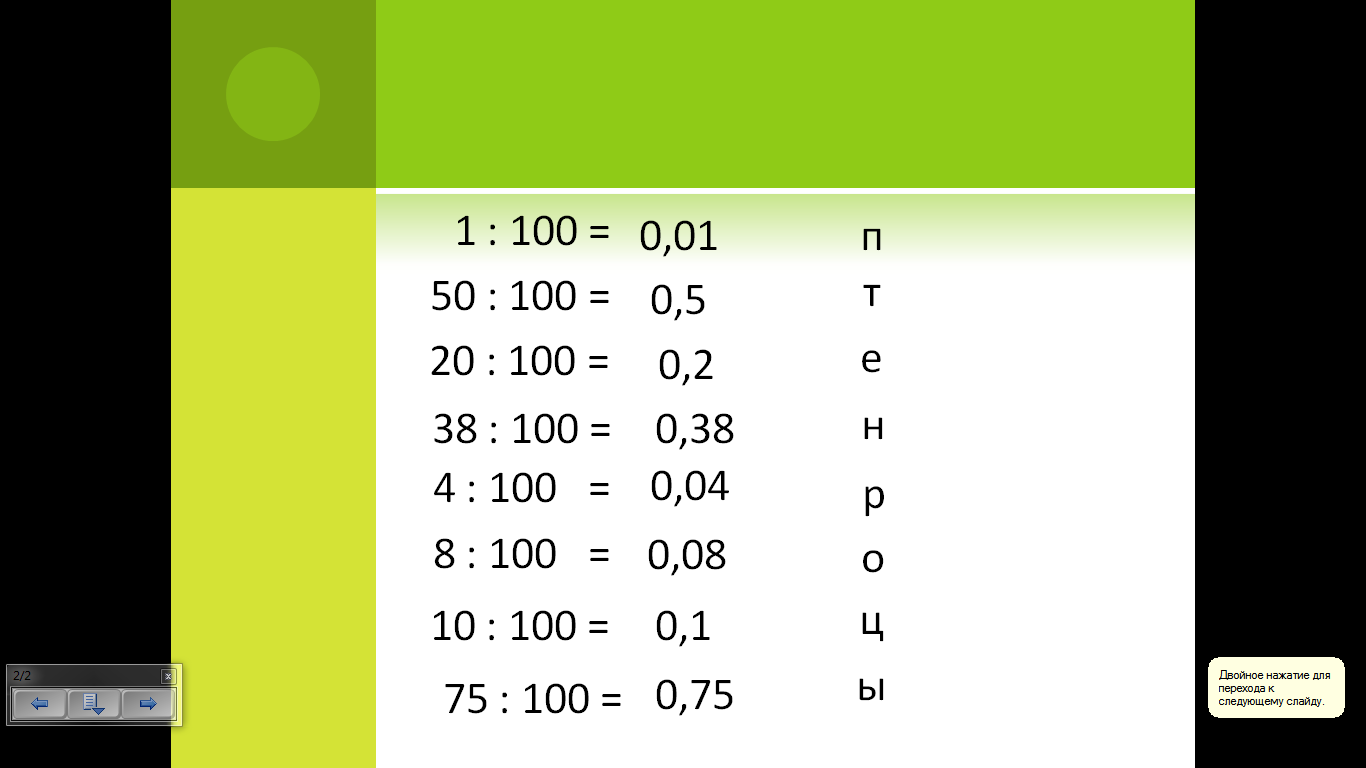

 литр молока, то половина – это пол-литра, то есть
литр молока, то половина – это пол-литра, то есть  . Мы уже говорили, что дроби – это условное понятие. Так как то, что выражается дробным числом, при другом подходе может быть выражено целым числом. Например, четверть метра (
. Мы уже говорили, что дроби – это условное понятие. Так как то, что выражается дробным числом, при другом подходе может быть выражено целым числом. Например, четверть метра ( метра) – это то же самое, что
метра) – это то же самое, что  см. То есть
см. То есть 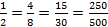 . Мы одну и ту же вещь – половину пути – обозначили по-разному (эквивалентные записи). Каждая форма записи может быть удобной в определенной ситуации.
. Мы одну и ту же вещь – половину пути – обозначили по-разному (эквивалентные записи). Каждая форма записи может быть удобной в определенной ситуации.


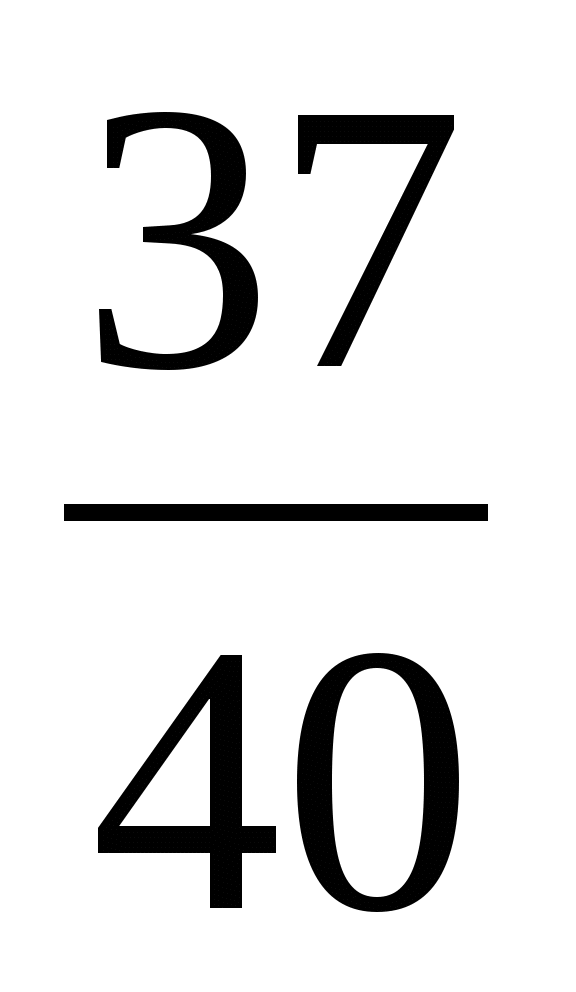 ;
;










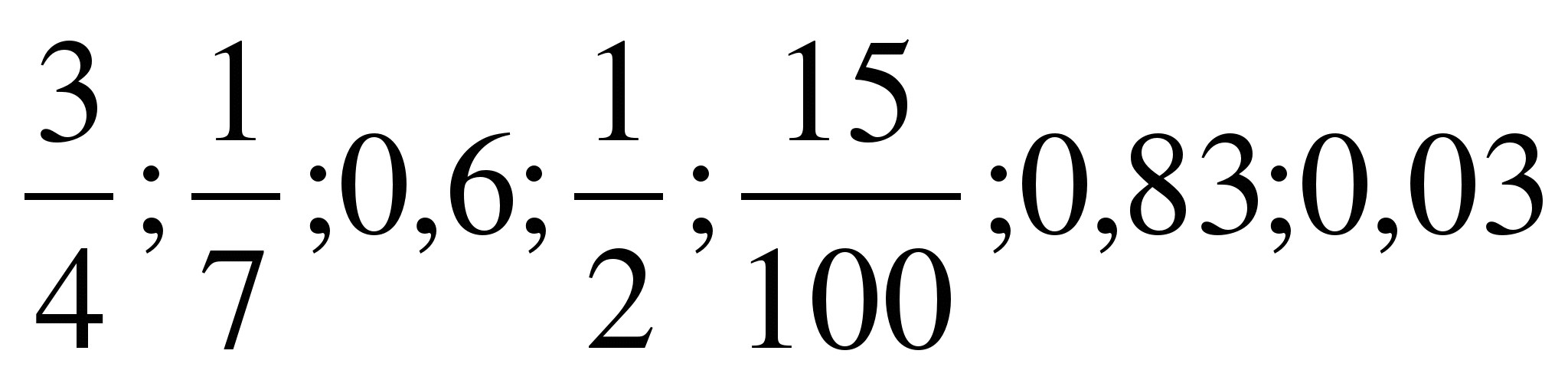
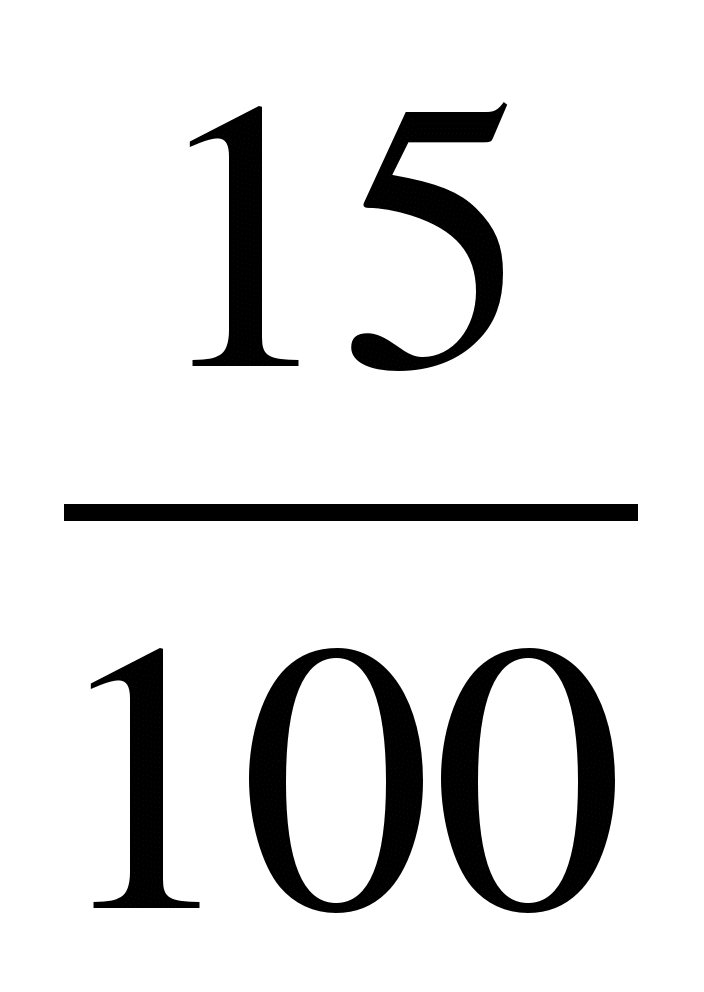 отнесли к десятичным?
отнесли к десятичным?
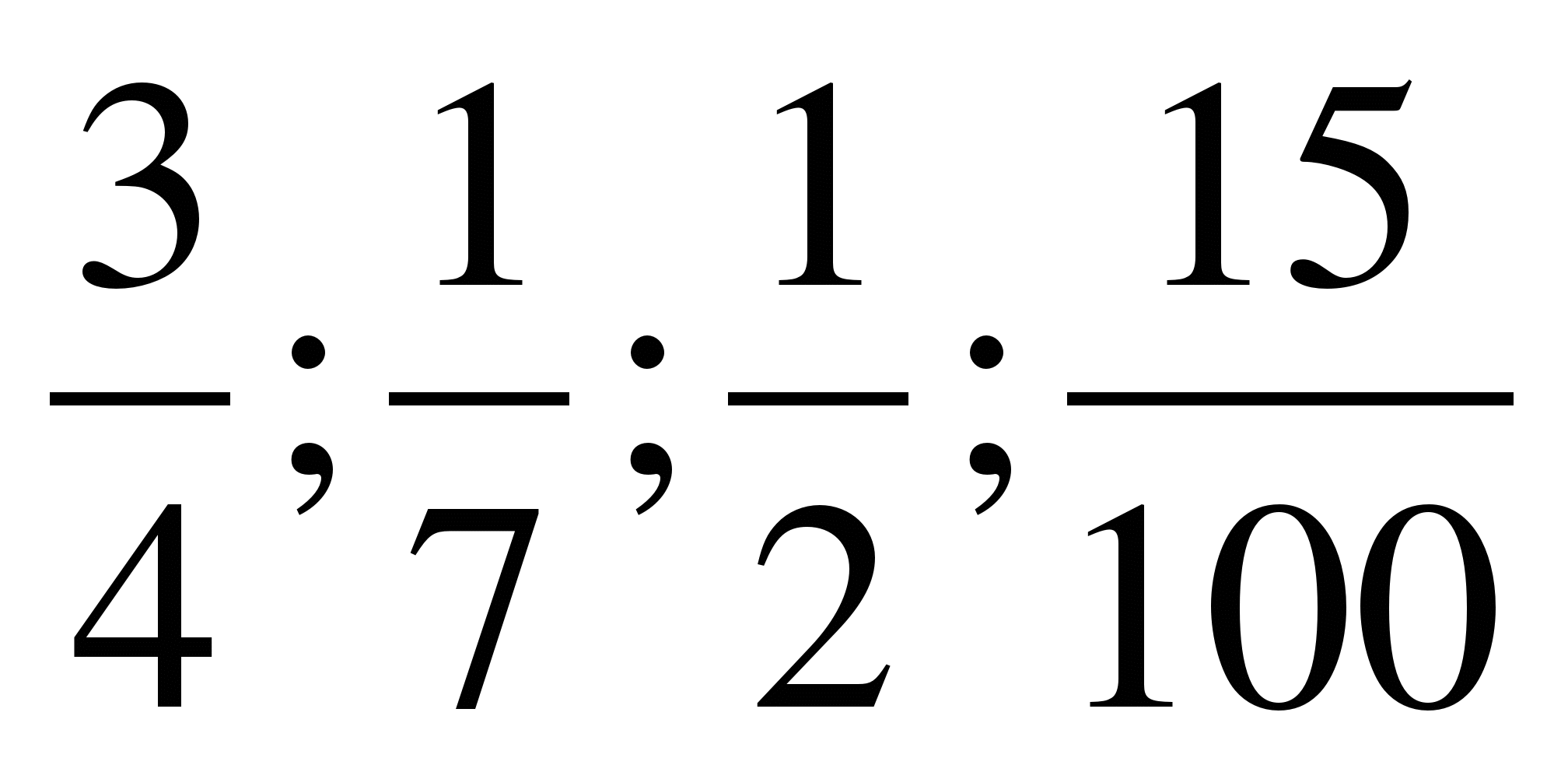
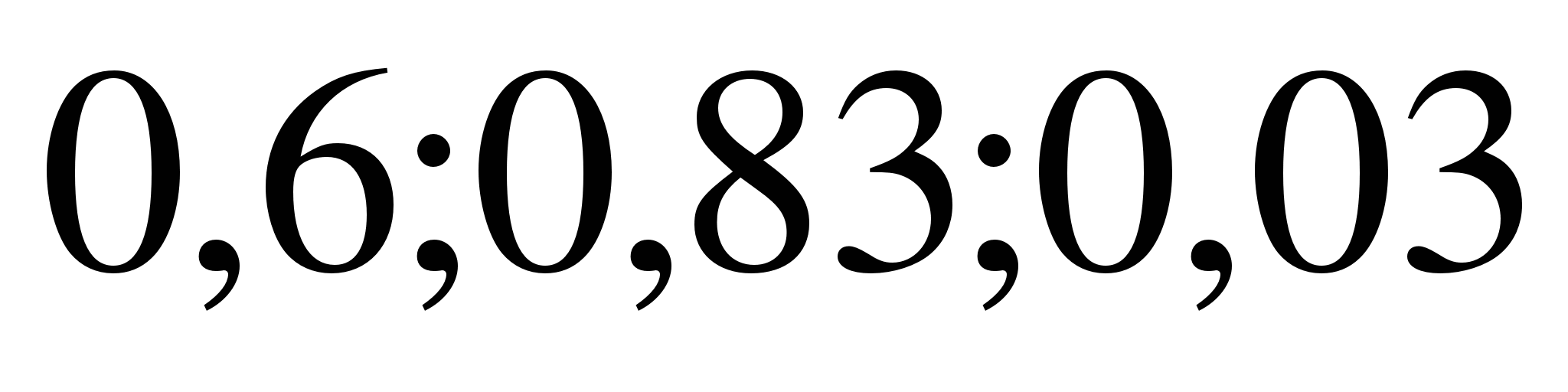
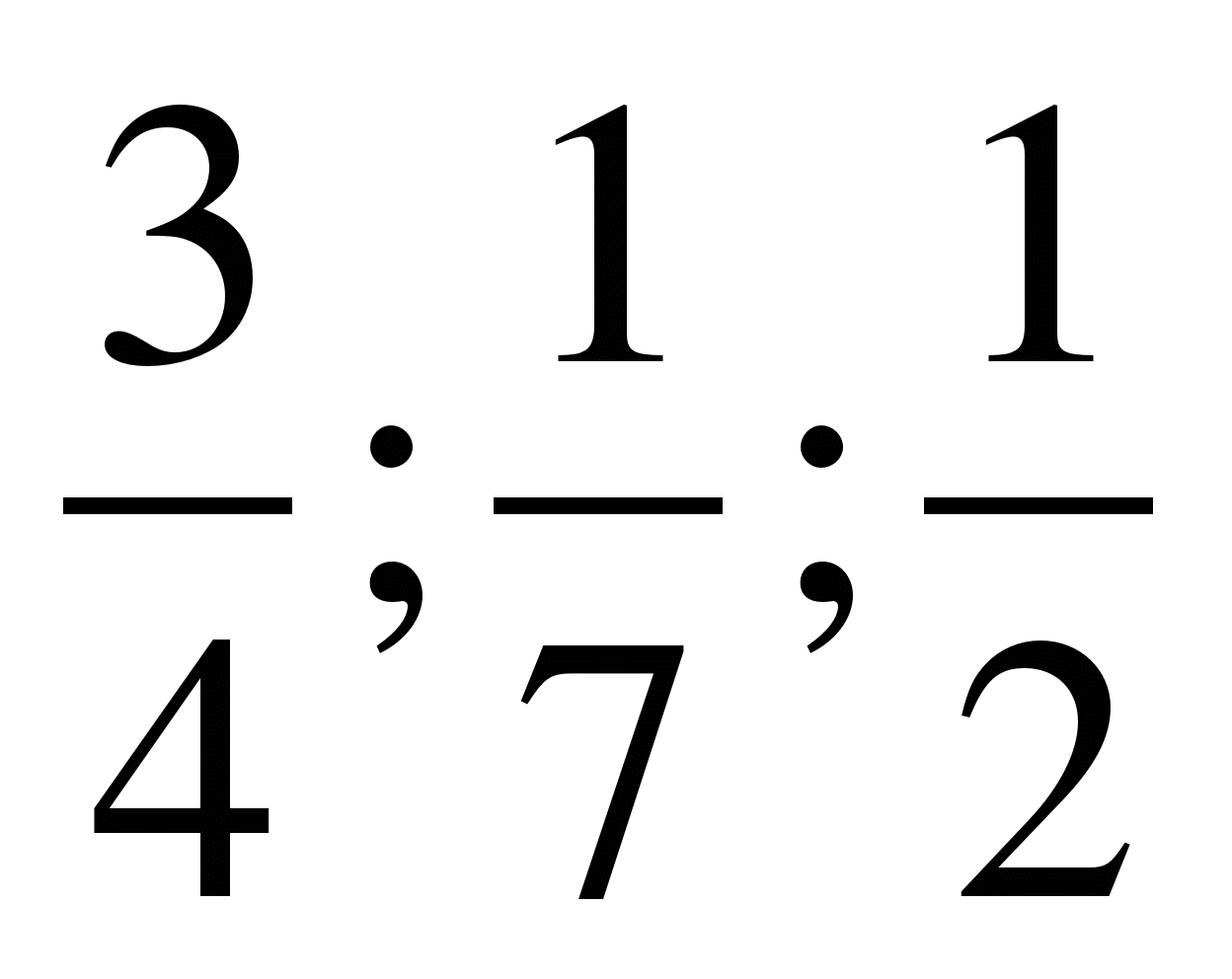
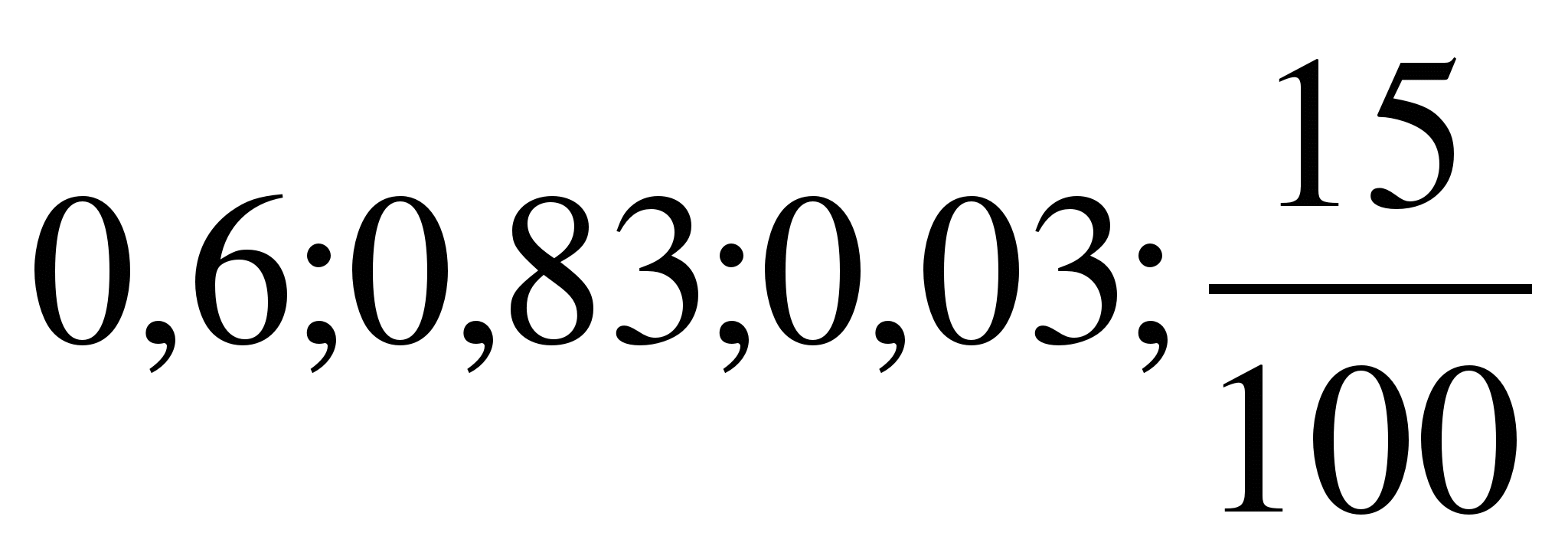
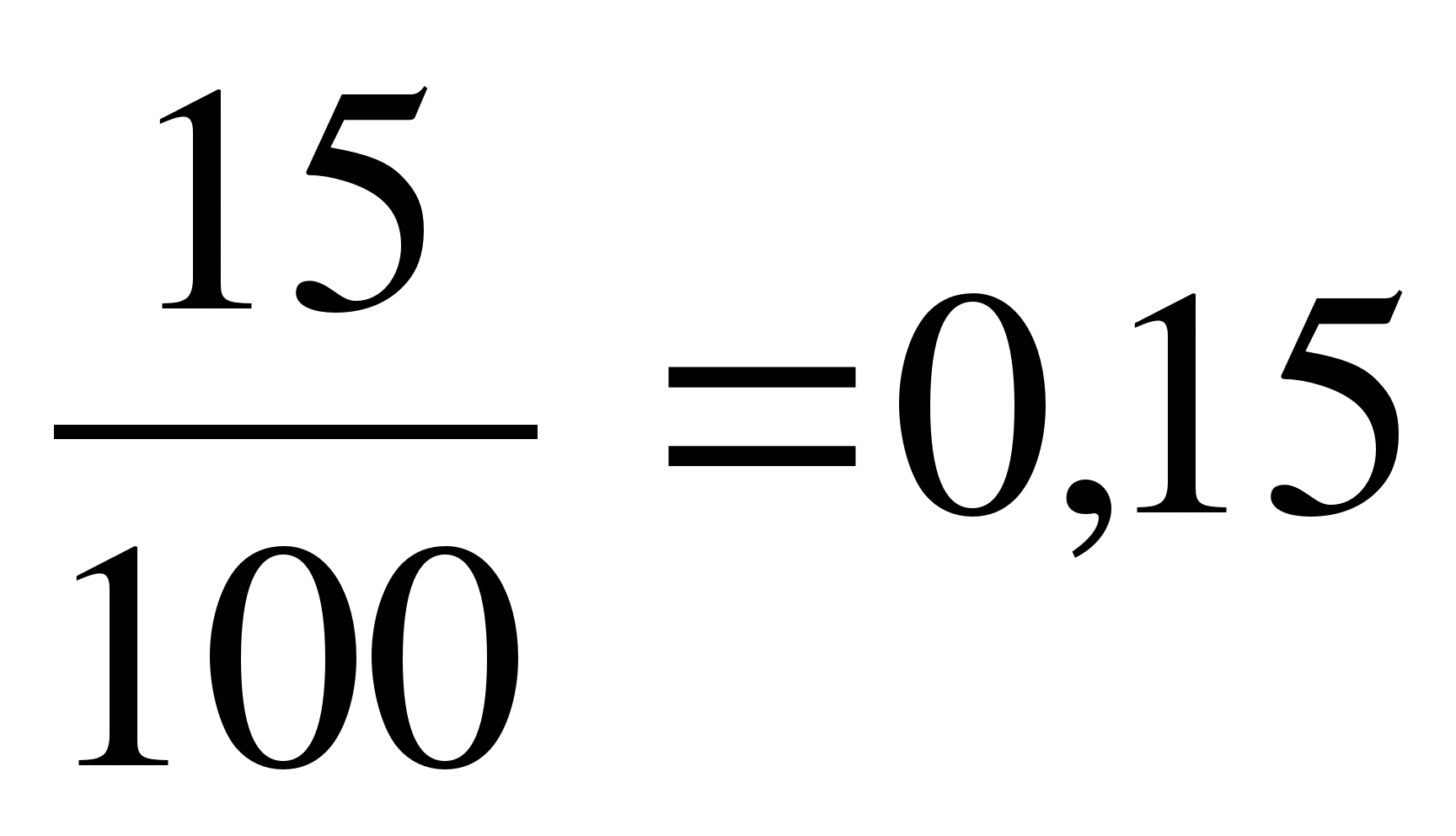
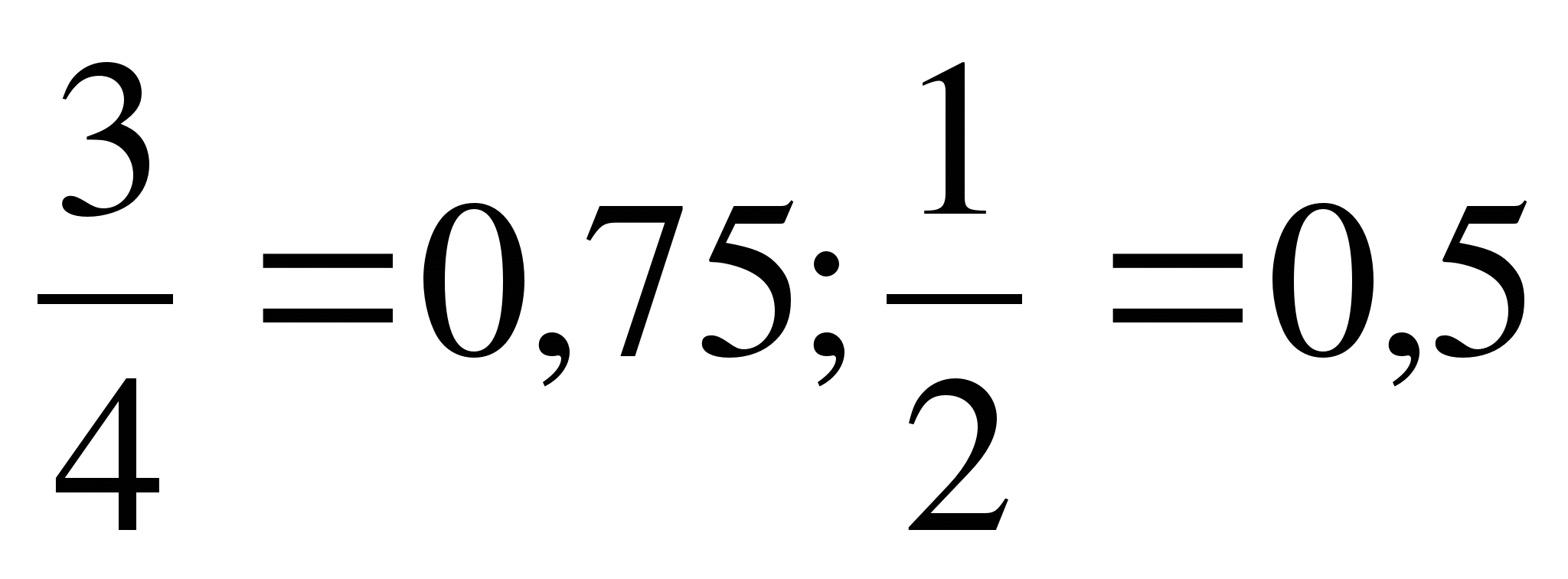 (вспоминают правило перевода обыкно-
(вспоминают правило перевода обыкно-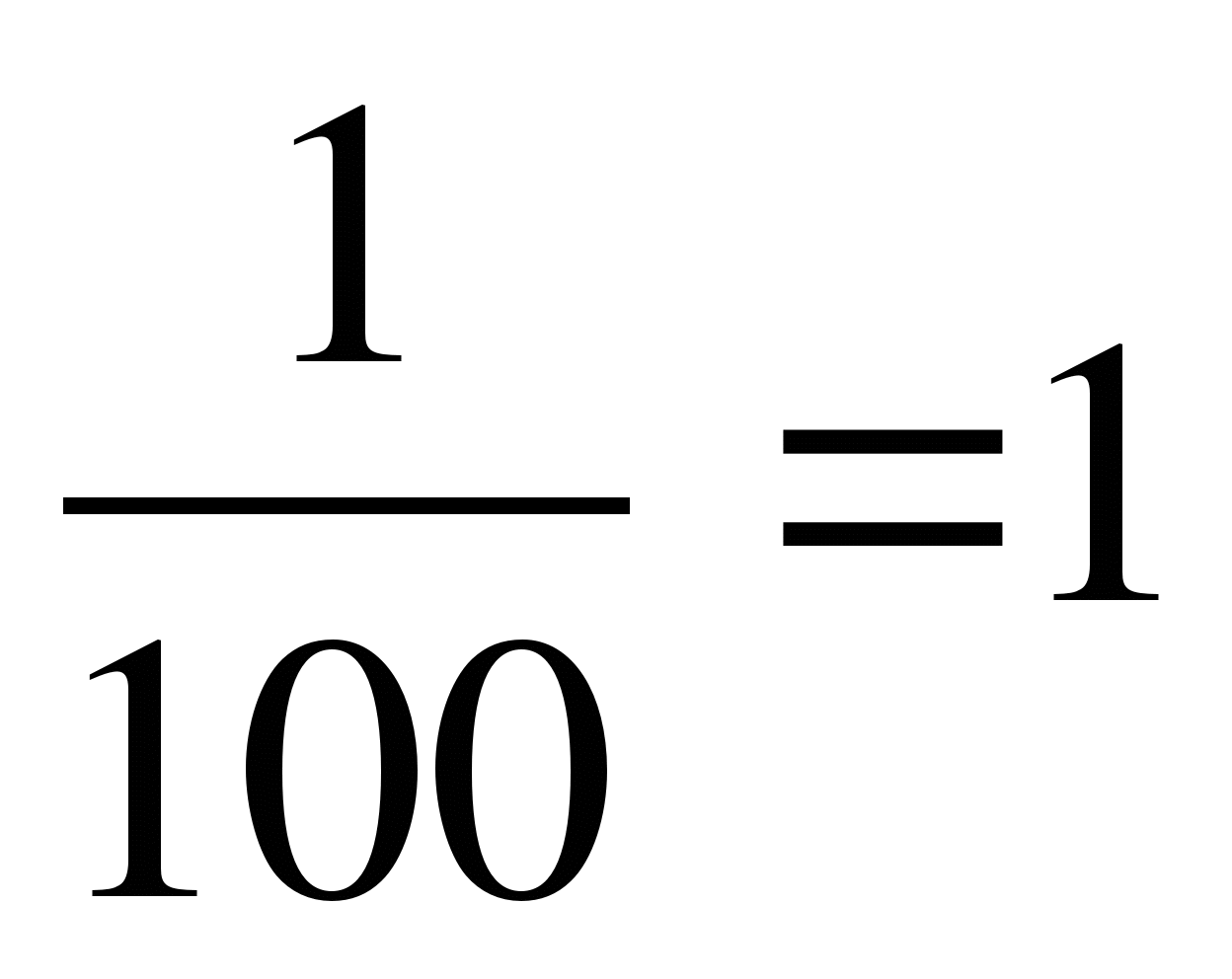 %. (учитель пишет на доске) Запишите в тетрадях.
%. (учитель пишет на доске) Запишите в тетрадях.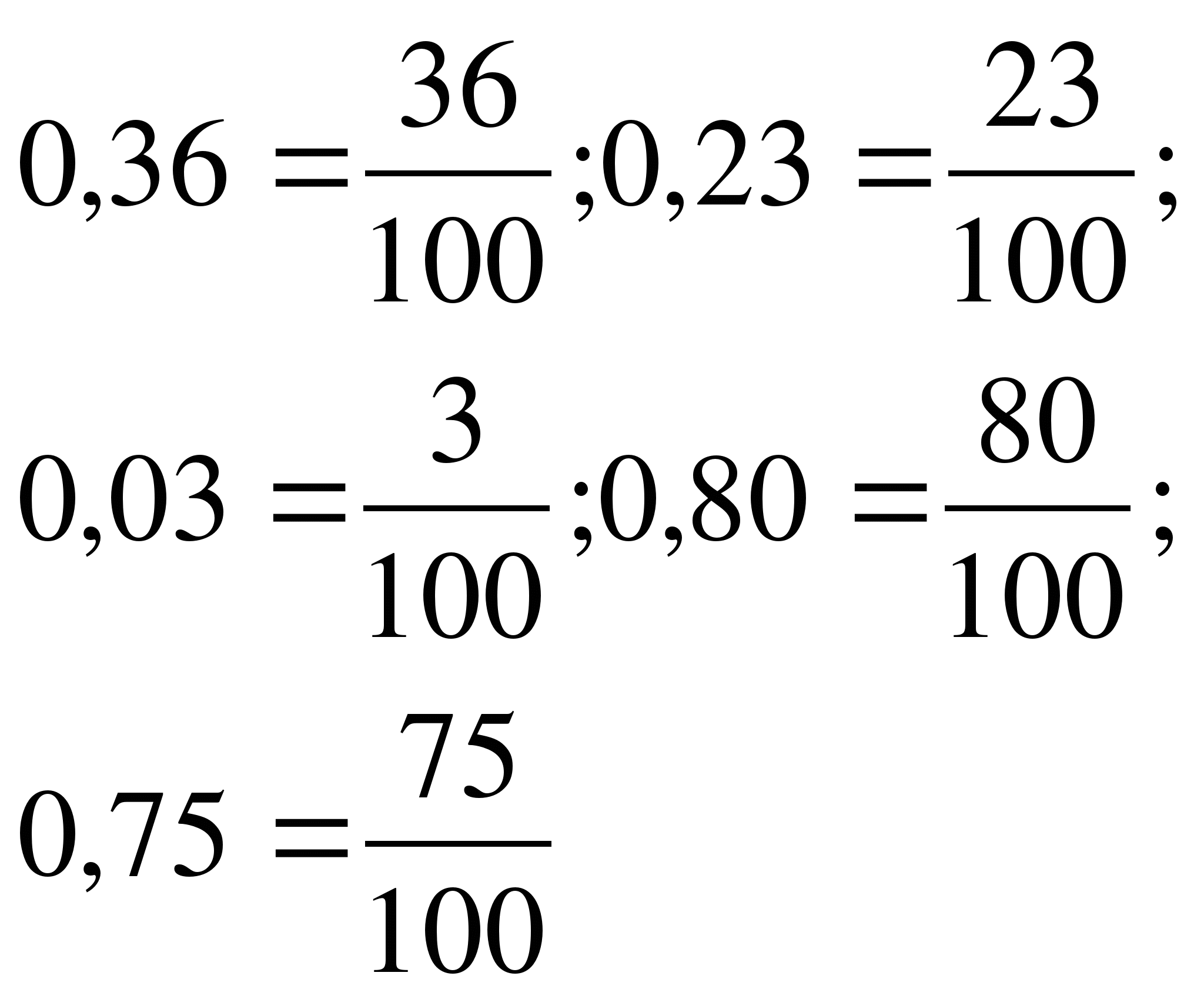
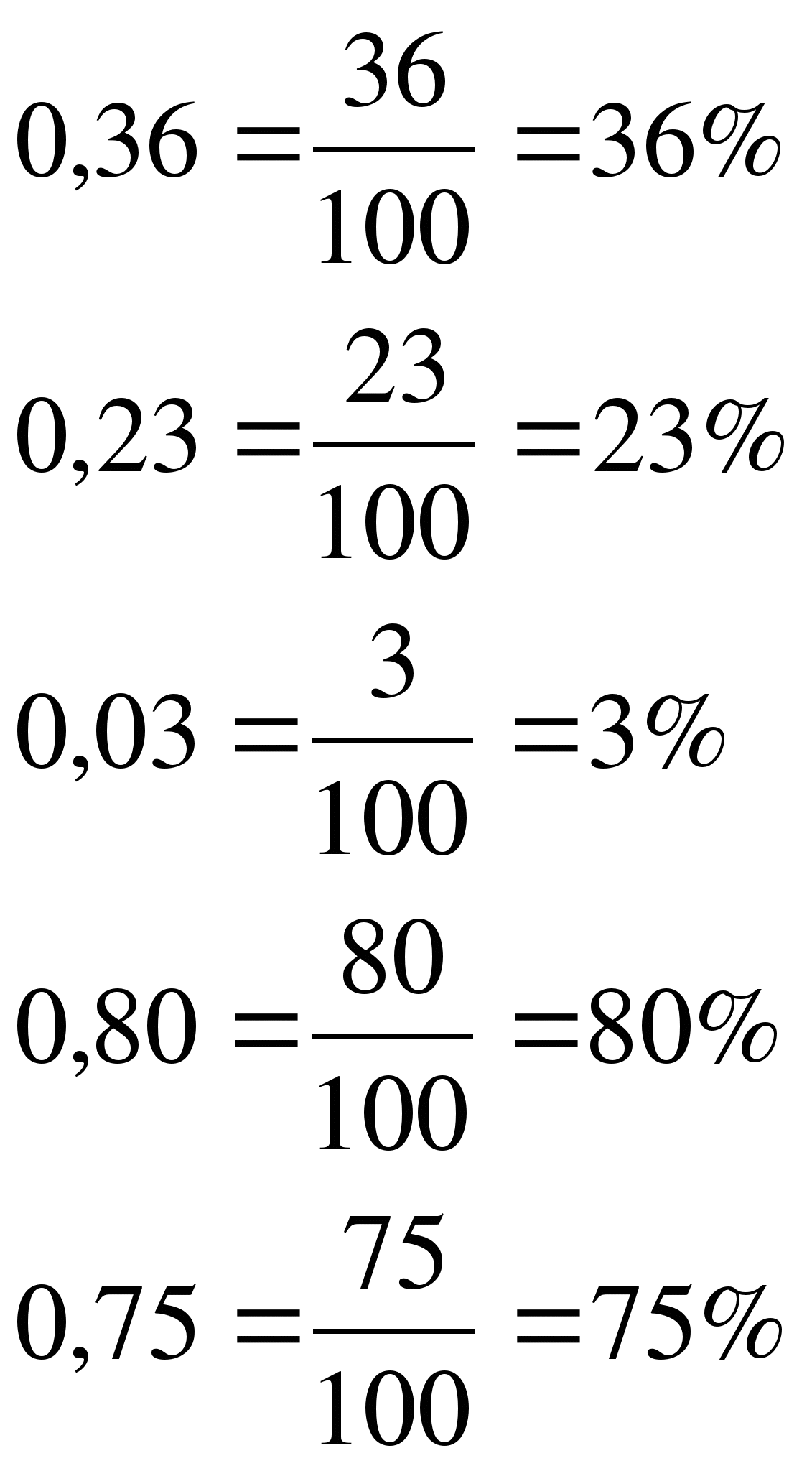
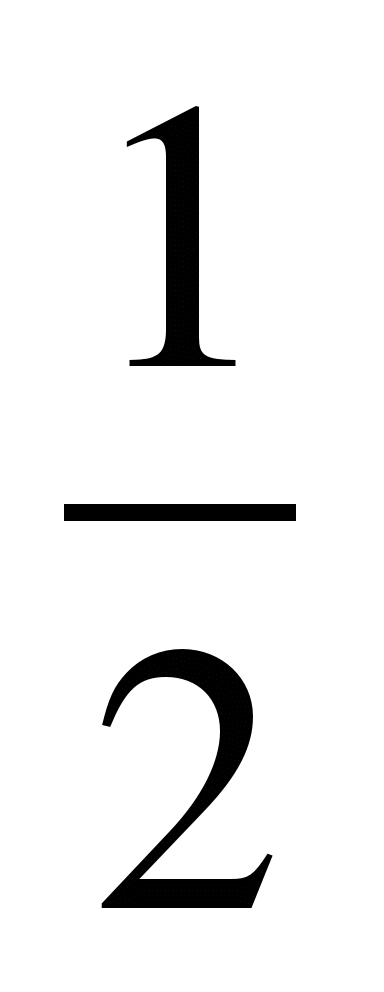
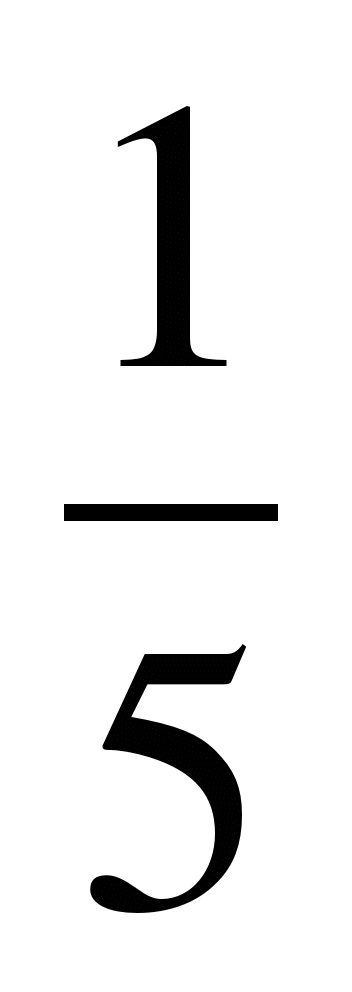
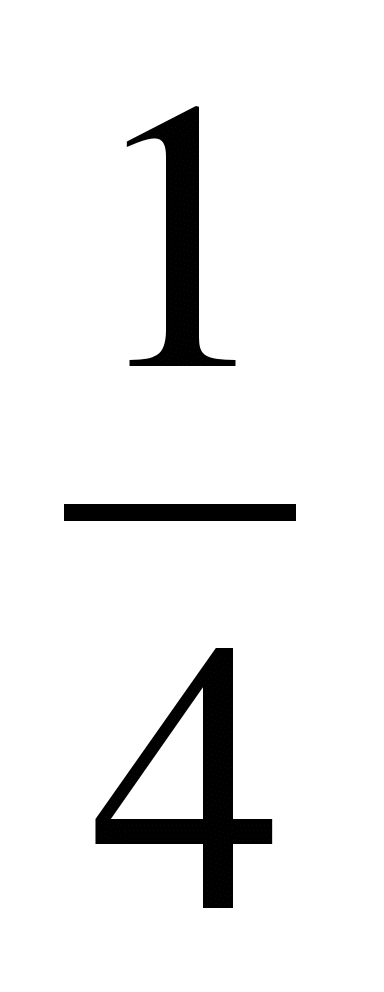

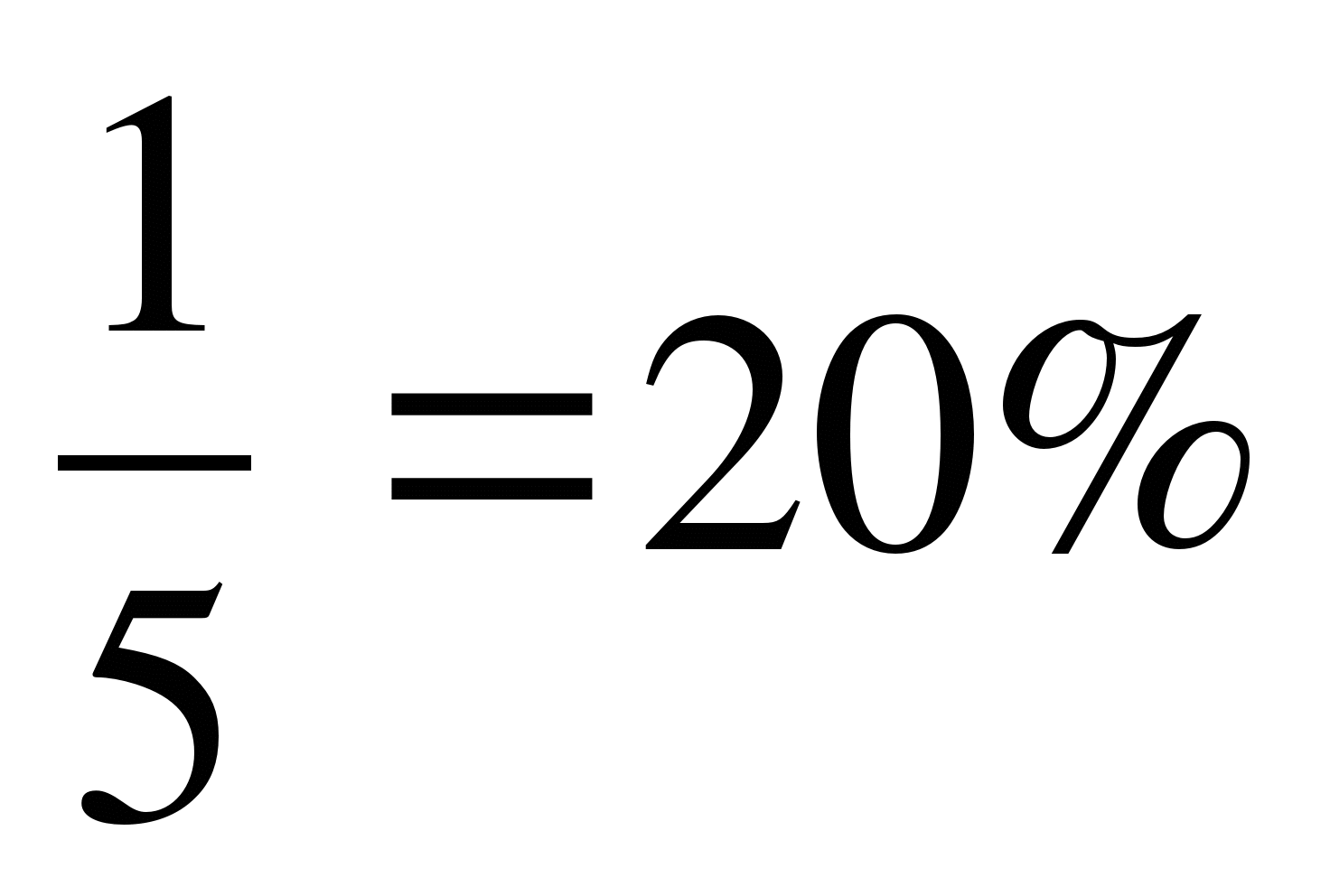
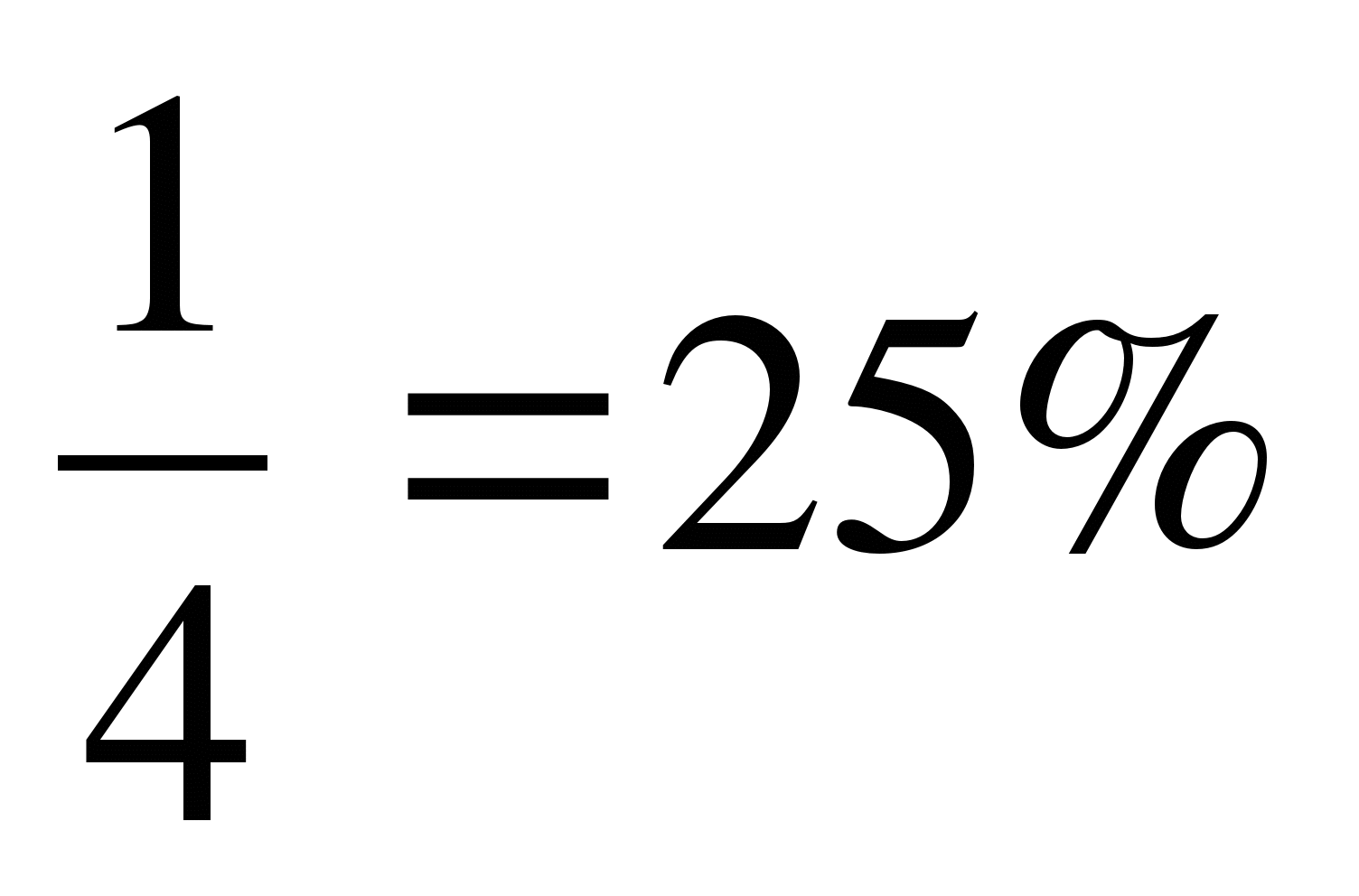

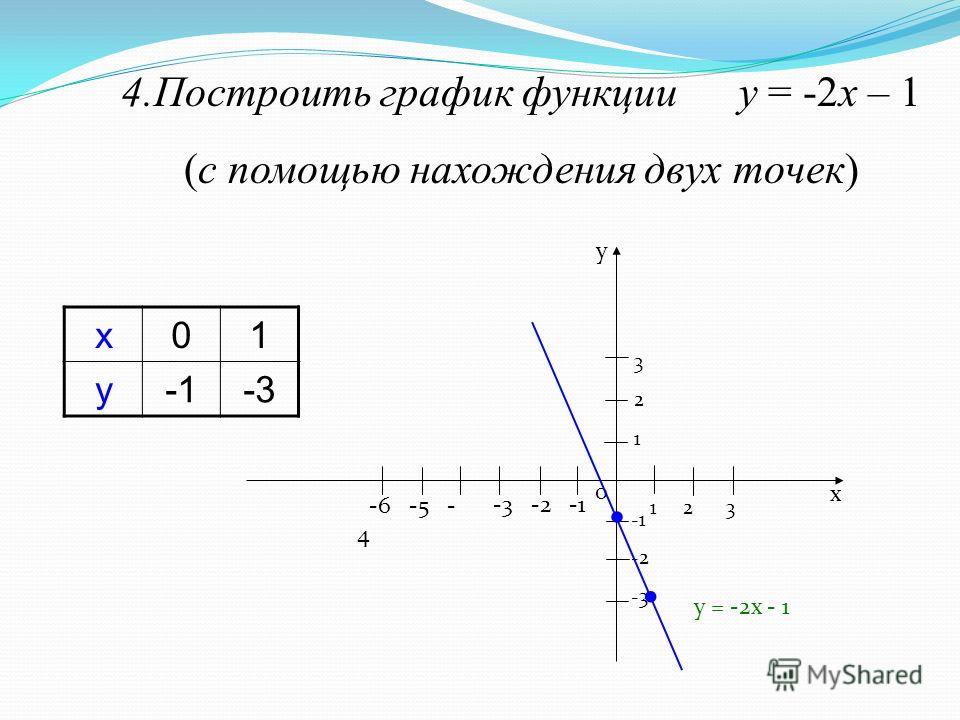
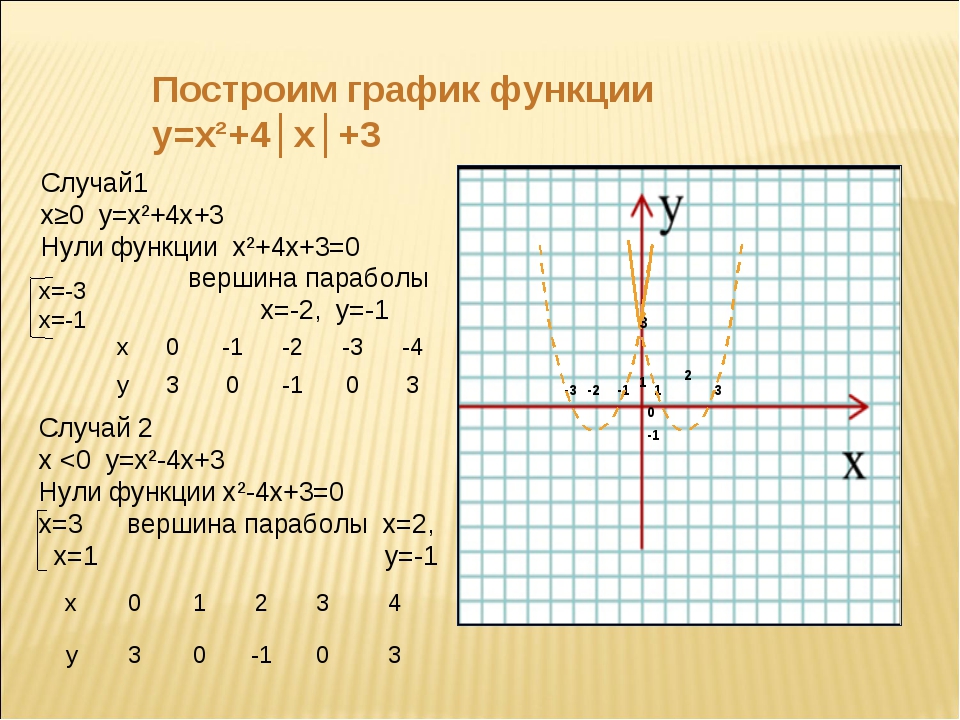 2 называется квадратичной функцией. Графиком квадратичной функции является парабола. Общий вид параболы представлен на рисунке ниже.
2 называется квадратичной функцией. Графиком квадратичной функции является парабола. Общий вид параболы представлен на рисунке ниже.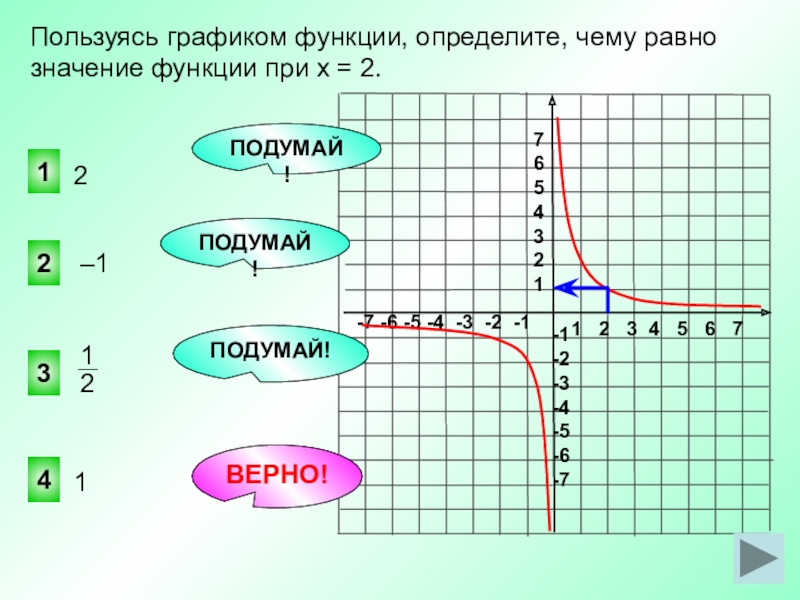 Например, найдем координату x вершины параболы по точкам (-2;0) и (4;0):
Например, найдем координату x вершины параболы по точкам (-2;0) и (4;0):
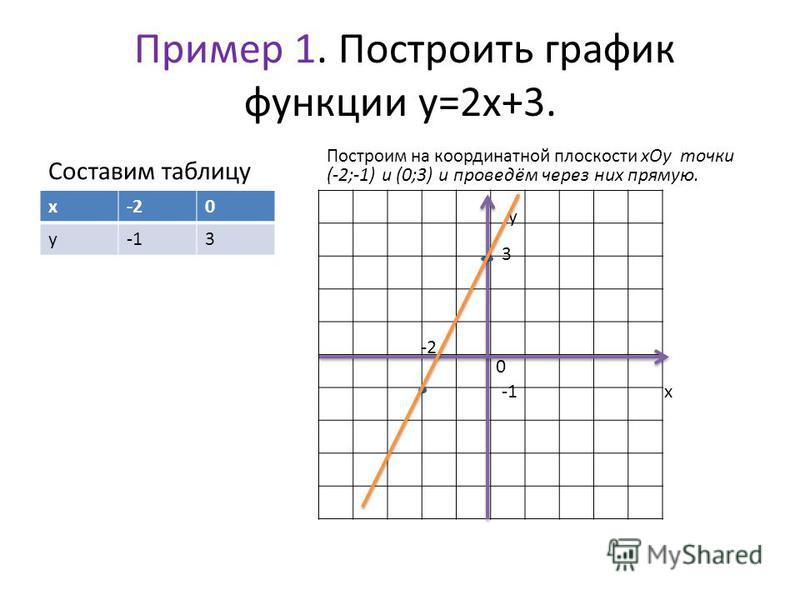
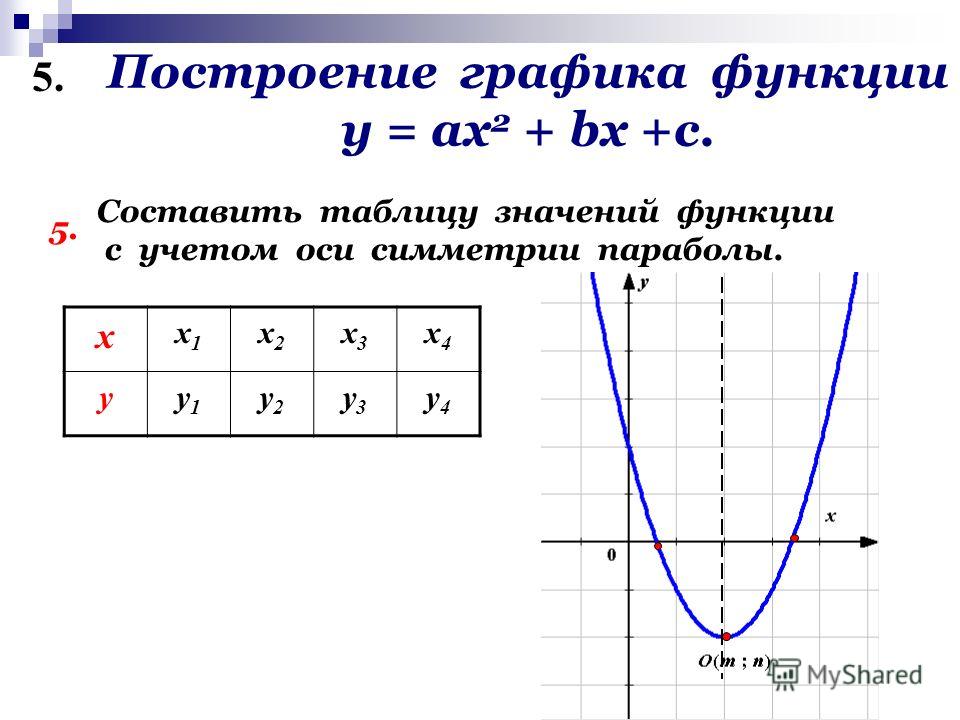 Проверка.
Проверка. Ученики
выполняют построение по алгоритму. Один ученик
работает у доски.
Ученики
выполняют построение по алгоритму. Один ученик
работает у доски. 2 \)
2 \) {2} +7 [/ латекс].Чтобы сделать снимок, [latex] h \ left (-7,5 \ right) [/ latex] должно быть около 4, но [latex] h \ left (-7,5 \ right) \ приблизительно 1,64 [/ latex]; он не выживает.
{2} +7 [/ латекс].Чтобы сделать снимок, [latex] h \ left (-7,5 \ right) [/ latex] должно быть около 4, но [latex] h \ left (-7,5 \ right) \ приблизительно 1,64 [/ latex]; он не выживает.

 Например, график ниже считается симметричным относительно оси y (линия x = 0), потому что четверть круга слева от оси y является зеркальным отображением четверти круга справа от оси y. ось. Фактически, если бы вы могли сложить эту страницу по оси Y, две четверти круга идеально совпали бы.
Например, график ниже считается симметричным относительно оси y (линия x = 0), потому что четверть круга слева от оси y является зеркальным отображением четверти круга справа от оси y. ось. Фактически, если бы вы могли сложить эту страницу по оси Y, две четверти круга идеально совпали бы.


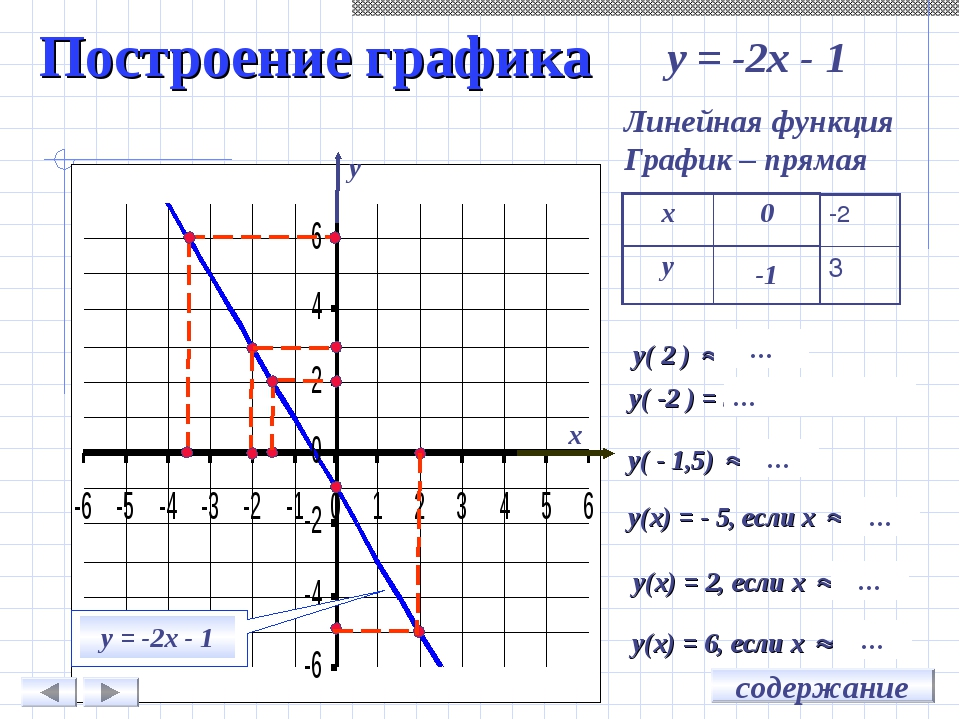 Если вы только что научились решать эти уравнения, то приведенная ниже викторина идеально подходит для вас. Уравнение такое же, как. Но я не умею рисовать графики и не умею хорошо использовать Excel. См. Ссылку в разделе «Исследование 7», вкладка 2, если требуется помощь. 2. Парабола — ее график, формы ее уравнения, ось симметрии и многое другое, объяснение визуально Алгебра 1 Математические навыки Практика: вершина и ось симметрии параболы из ее графика. График квадратичной функции представляет собой гладкую U-образную кривую, которая открывается вверх или вниз, в зависимости от знака коэффициента при члене x2.Как построить горизонтальные параболы (x = ay 2 + by + c или x = a (y — k) 2 + h) (x = ay 2 + by + c или x = a (y — k) 2 + h), используя характеристики. Резюме для других парабол y = ax2 + bx + c имеет вершину, в которой dy / dx равно нулю. Математика. 28 июня 2014 г. — Преобразования графов квадратичных функций — заметки, диаграммы и викторины. Я обнаружил, что практика дает идеальные результаты при обучении преобразованиям. NCEA Maths Level 1 Graphing: Quadratic Sequences NCEA Maths Level 1 Graphing: Graphing Parabolas x-Intercept NCEA Maths Level 1 Graphing: Graphing Parabolas Vertex NCEA Maths Level 1 Graphing: Translating Parabolas Level 1 Graphing: Translating Parabolas Level 1 Graphing: NCEA Mathing Level 1 Graphing: NCE Paraboing Mathing: NCE Paraboing Level 1 Graphing: Scaling Paraboalas Level 1 Graphing: Scaling Paraboal Mathing: Scaling Paraboal as Scaling Практические работы по квадратичным задачам 2015 Экзамен: 2015 9.5) n2 + 10n = -20 6) 4k2 — 45 = 3k 7) 9×2 + x + 4 = -2×2 — 3x Графики квадратичных функций, заданных в стандартной форме ax² + bx + c. Кто-нибудь, помогите мне, пожалуйста. Парабола. Мы знаем значения и можем нарисовать график оттуда. a <0 парабола открывается вниз. Нужные вам онлайн-уроки и домашние задания. В этом случае вы должны поместить их в графический формат, заполнив квадрат. . Вершина: (h, k) = (–3, –2) Фокус: Директриса: Ось симметрии: Рис.
Если вы только что научились решать эти уравнения, то приведенная ниже викторина идеально подходит для вас. Уравнение такое же, как. Но я не умею рисовать графики и не умею хорошо использовать Excel. См. Ссылку в разделе «Исследование 7», вкладка 2, если требуется помощь. 2. Парабола — ее график, формы ее уравнения, ось симметрии и многое другое, объяснение визуально Алгебра 1 Математические навыки Практика: вершина и ось симметрии параболы из ее графика. График квадратичной функции представляет собой гладкую U-образную кривую, которая открывается вверх или вниз, в зависимости от знака коэффициента при члене x2.Как построить горизонтальные параболы (x = ay 2 + by + c или x = a (y — k) 2 + h) (x = ay 2 + by + c или x = a (y — k) 2 + h), используя характеристики. Резюме для других парабол y = ax2 + bx + c имеет вершину, в которой dy / dx равно нулю. Математика. 28 июня 2014 г. — Преобразования графов квадратичных функций — заметки, диаграммы и викторины. Я обнаружил, что практика дает идеальные результаты при обучении преобразованиям. NCEA Maths Level 1 Graphing: Quadratic Sequences NCEA Maths Level 1 Graphing: Graphing Parabolas x-Intercept NCEA Maths Level 1 Graphing: Graphing Parabolas Vertex NCEA Maths Level 1 Graphing: Translating Parabolas Level 1 Graphing: Translating Parabolas Level 1 Graphing: NCEA Mathing Level 1 Graphing: NCE Paraboing Mathing: NCE Paraboing Level 1 Graphing: Scaling Paraboalas Level 1 Graphing: Scaling Paraboal Mathing: Scaling Paraboal as Scaling Практические работы по квадратичным задачам 2015 Экзамен: 2015 9.5) n2 + 10n = -20 6) 4k2 — 45 = 3k 7) 9×2 + x + 4 = -2×2 — 3x Графики квадратичных функций, заданных в стандартной форме ax² + bx + c. Кто-нибудь, помогите мне, пожалуйста. Парабола. Мы знаем значения и можем нарисовать график оттуда. a <0 парабола открывается вниз. Нужные вам онлайн-уроки и домашние задания. В этом случае вы должны поместить их в графический формат, заполнив квадрат. . Вершина: (h, k) = (–3, –2) Фокус: Директриса: Ось симметрии: Рис.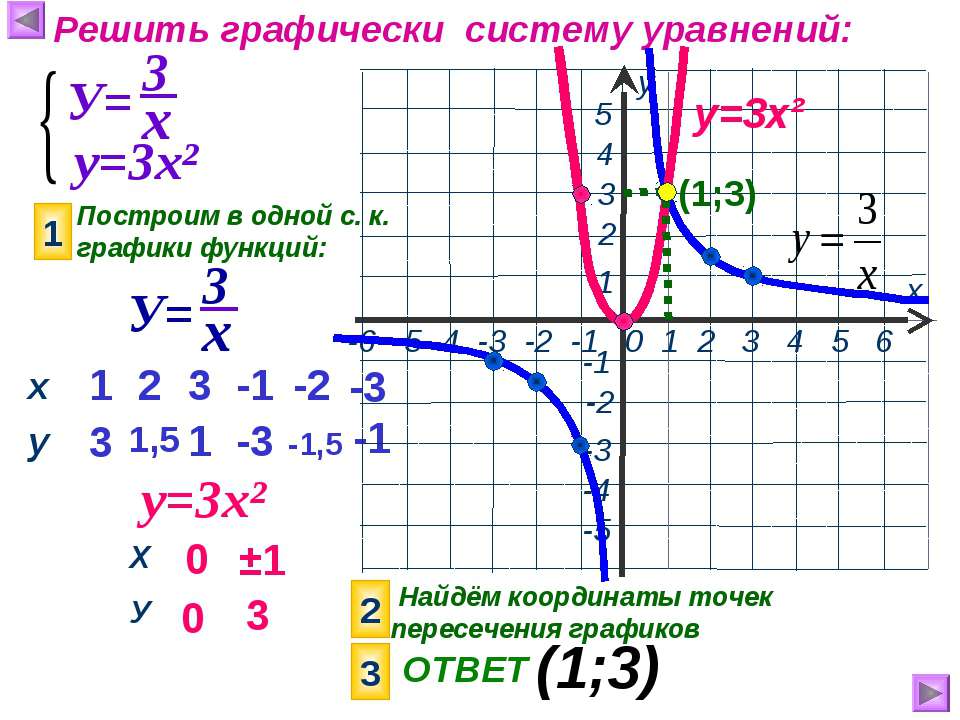 3. Перед проведением урока по построению квадратиков и определению их характеристик посетите этот сайт.2, показанная красным, симметрична относительно прямой y = 0 и имеет вершину в точке (0,0). Для квадратного уравнения вида y = ax2 + bx + c, x — независимая переменная, а y — зависимая переменная. Еще нет учетной записи? Спросите у учителя код и введите его выше. L. Чтобы найти точку пересечения с y, пусть x = 0 и решит относительно y. Для функциональных графиков и таблиц №1: начните с поиска парабол графа $ \ bi y $ -перехвата. Вершина графа находится в точке (0, 0). поделиться в Facebook поделиться в Twitter Вопросы.7. Эксперт признает это параболой из-за формы уравнения (оно квадратично по одной переменной и линейно по другой). Дэн Мейер — великий математик, у него есть полный курс по алгебре 1. График b — это ½ парабола, правая сторона вверх, немного сдвинутая вправо и более вверх. Вершина в данном случае — это точка, в которой график изменяется от убывания к возрастанию, или точка с наименьшим значением y. Ориентация параболы Для графика квадратичной функции, если a> 0, парабола открывается вверх.Бесплатный графический калькулятор — функция построения графиков, проверка точек пересечения, поиск максимума и минимума и многое другое. Этот веб-сайт использует файлы cookie, чтобы обеспечить вам максимальное удобство. 4. Затем нанесите точки и нарисуйте график. для вертикальных парабол или по форме. i Рабочий лист Kuta Software LLC Подробный ключ ответа. На (Рисунок) вы попрактикуетесь в построении параболы, нанеся несколько точек. В этой игре типа Jeopardy вы попрактикуетесь в работе с 3 формами квадратных уравнений — стандартными, вершинными и пересеченными.Попросите учащихся исследовать функции формы y = _____ x + ____ с помощью инструмента Graph Sketcher Tool, чтобы определить, какие функции происходят из этой формы и что меняется. , например), вам нужно будет решить уравнение для его двух половин, а затем изобразить две половины как две отдельные функции. Парабола — это кривая, которая была известна и изучена в древности.
3. Перед проведением урока по построению квадратиков и определению их характеристик посетите этот сайт.2, показанная красным, симметрична относительно прямой y = 0 и имеет вершину в точке (0,0). Для квадратного уравнения вида y = ax2 + bx + c, x — независимая переменная, а y — зависимая переменная. Еще нет учетной записи? Спросите у учителя код и введите его выше. L. Чтобы найти точку пересечения с y, пусть x = 0 и решит относительно y. Для функциональных графиков и таблиц №1: начните с поиска парабол графа $ \ bi y $ -перехвата. Вершина графа находится в точке (0, 0). поделиться в Facebook поделиться в Twitter Вопросы.7. Эксперт признает это параболой из-за формы уравнения (оно квадратично по одной переменной и линейно по другой). Дэн Мейер — великий математик, у него есть полный курс по алгебре 1. График b — это ½ парабола, правая сторона вверх, немного сдвинутая вправо и более вверх. Вершина в данном случае — это точка, в которой график изменяется от убывания к возрастанию, или точка с наименьшим значением y. Ориентация параболы Для графика квадратичной функции, если a> 0, парабола открывается вверх.Бесплатный графический калькулятор — функция построения графиков, проверка точек пересечения, поиск максимума и минимума и многое другое. Этот веб-сайт использует файлы cookie, чтобы обеспечить вам максимальное удобство. 4. Затем нанесите точки и нарисуйте график. для вертикальных парабол или по форме. i Рабочий лист Kuta Software LLC Подробный ключ ответа. На (Рисунок) вы попрактикуетесь в построении параболы, нанеся несколько точек. В этой игре типа Jeopardy вы попрактикуетесь в работе с 3 формами квадратных уравнений — стандартными, вершинными и пересеченными.Попросите учащихся исследовать функции формы y = _____ x + ____ с помощью инструмента Graph Sketcher Tool, чтобы определить, какие функции происходят из этой формы и что меняется. , например), вам нужно будет решить уравнение для его двух половин, а затем изобразить две половины как две отдельные функции. Парабола — это кривая, которая была известна и изучена в древности. График сдвигается вниз, но форма остается прежней c.Теперь фирмы всегда стремятся увеличить доход. Поймите шаблоны, функциональные представления, отношения и функции. Уменьшение. ДРУГОЙ ВАРИАНТ. Посреди координатной геометрии и квадратичного разложения? Наш список полных квадратов и определений квадрантов графиков здесь для вас. РАБОЧИЕ ЛИСТЫ: Графические квадратичные функции Регента AII: 11: TST PDF DOC TNS: Практическое графическое отображение квадратичных функций 1: 15: WS PDF TNS: Практическое графическое отображение квадратичных функций 2a MC, определение вершины, фокус, директриса: 6: PDF TNS: Практика -Графирование квадратичных функций 2b Постройте фокус, директрису и широту прямой кишки и нарисуйте плавную кривую, чтобы сформировать параболу.Графические параболы №3: практика, практика, практика. Вершины и пересечения предлагают самые быстрые и легкие точки, которые помогут с графиком параболы. Попрактикуйтесь в построении графиков линейных уравнений, заполнив таблицу функций, построив график с использованием наклона и точки пересечения по оси Y, построив горизонтальные и вертикальные линии, и найдите достаточные MCQ для закрепления концепции с помощью этих рабочих листов для построения графиков линейных уравнений. Если если . Параболы могут быть как в форме. Точки (-1, 11) и (2, 17) могут быть нанесены для построения более точного графика.Я хочу продемонстрировать стремительный рост в математике. Калькулятор уравнения параболы. График c представляет собой ½ параболу, перевернутую вверх-вниз, смещенную влево и вниз. Графические примеры параболы. Скачать бесплатно в Google Play. Мы используем тот же эллипс, что и в примере выше, но меняем центр. Ни один. YNJ. Любая точка параболы находится на равном расстоянии от фокуса и фиксированной прямой линии, известной как директриса. Построение графиков рациональных функций с отверстиями. ОК. Диаграмма, изображающая 8 основных преобразований, включая обозначение функций и описание.Научитесь составлять графики линейных функций, нанося точки на сетку.
График сдвигается вниз, но форма остается прежней c.Теперь фирмы всегда стремятся увеличить доход. Поймите шаблоны, функциональные представления, отношения и функции. Уменьшение. ДРУГОЙ ВАРИАНТ. Посреди координатной геометрии и квадратичного разложения? Наш список полных квадратов и определений квадрантов графиков здесь для вас. РАБОЧИЕ ЛИСТЫ: Графические квадратичные функции Регента AII: 11: TST PDF DOC TNS: Практическое графическое отображение квадратичных функций 1: 15: WS PDF TNS: Практическое графическое отображение квадратичных функций 2a MC, определение вершины, фокус, директриса: 6: PDF TNS: Практика -Графирование квадратичных функций 2b Постройте фокус, директрису и широту прямой кишки и нарисуйте плавную кривую, чтобы сформировать параболу.Графические параболы №3: практика, практика, практика. Вершины и пересечения предлагают самые быстрые и легкие точки, которые помогут с графиком параболы. Попрактикуйтесь в построении графиков линейных уравнений, заполнив таблицу функций, построив график с использованием наклона и точки пересечения по оси Y, построив горизонтальные и вертикальные линии, и найдите достаточные MCQ для закрепления концепции с помощью этих рабочих листов для построения графиков линейных уравнений. Если если . Параболы могут быть как в форме. Точки (-1, 11) и (2, 17) могут быть нанесены для построения более точного графика.Я хочу продемонстрировать стремительный рост в математике. Калькулятор уравнения параболы. График c представляет собой ½ параболу, перевернутую вверх-вниз, смещенную влево и вниз. Графические примеры параболы. Скачать бесплатно в Google Play. Мы используем тот же эллипс, что и в примере выше, но меняем центр. Ни один. YNJ. Любая точка параболы находится на равном расстоянии от фокуса и фиксированной прямой линии, известной как директриса. Построение графиков рациональных функций с отверстиями. ОК. Диаграмма, изображающая 8 основных преобразований, включая обозначение функций и описание.Научитесь составлять графики линейных функций, нанося точки на сетку. Парабола имеет вершину в начале координат и фокус в точке (0,4). Хорошей практикой является нанесение точек около точки минимума, которая в этом случае имеет приблизительные координаты (0. Вершина — это максимум, а точки; (25,32). Лучший онлайн-калькулятор для построения графиков У нас есть самый сложный и всеобъемлющий TI 84 тип графического калькулятора онлайн.Особенности основной параболы — симметрия, вершина (самая низкая или нижняя) Следующие задачи иллюстрируют подробное построение графиков функций одной переменной с использованием первой и второй производных.Целенаправленное обучение и практика по алгебре 2 Урок 2: Квадратичная функция. Раздел 5. 0 Истекшее время Время. Поэтому у меня было искушение объединить всю следующую информацию с главой о квадратиках. Учитывая уравнение стандартной формы для параболы с центром в точке (0, 0), нарисуйте график. Например, график y = 5x²-20x + 15. s b RAclzlU Tr_iNgVhztvsz prIets [eqrGvveydI. Разберемся на примерах. Постройте график каждой функции. 5 Графические параболы 9. Перехваты. Решение и построение графиков с факторизованной формой.Выберите: 1) Для кубического графа (зеленый), x находится между -2 и 1 2) Для преобразованного кубического, (черный), x находится между 4 и 7 3) Для экспоненциального графика (фиолетовый), x находится между 0 и 3 4) Для переведенного экспоненциального графика (фиолетовый) x находится между 6 и 9 5) Для положительной (вогнутой вверх) параболы (синий) x находится между -3 и -1 На этих страницах практики студенты рисуют линии с наклоном перехватить форму, указав, какая строка (уравнение) через какой символ проходит. Подходит для 4–5 классов, в чем смысл? позволяет попрактиковаться в чтении графиков, определяя правильные координаты.Мы обсудили все детали, от построения кусочных парабол до рациональных выражений. -1-Нарисуйте график каждой функции. Пример 1. Нарисуйте график для уравнения y = 2x 2 + x + 1. Дополнительные сведения см. На сайте http: // www. является параболой, и ее граф открывается вниз из вершины (1, 3).
Парабола имеет вершину в начале координат и фокус в точке (0,4). Хорошей практикой является нанесение точек около точки минимума, которая в этом случае имеет приблизительные координаты (0. Вершина — это максимум, а точки; (25,32). Лучший онлайн-калькулятор для построения графиков У нас есть самый сложный и всеобъемлющий TI 84 тип графического калькулятора онлайн.Особенности основной параболы — симметрия, вершина (самая низкая или нижняя) Следующие задачи иллюстрируют подробное построение графиков функций одной переменной с использованием первой и второй производных.Целенаправленное обучение и практика по алгебре 2 Урок 2: Квадратичная функция. Раздел 5. 0 Истекшее время Время. Поэтому у меня было искушение объединить всю следующую информацию с главой о квадратиках. Учитывая уравнение стандартной формы для параболы с центром в точке (0, 0), нарисуйте график. Например, график y = 5x²-20x + 15. s b RAclzlU Tr_iNgVhztvsz prIets [eqrGvveydI. Разберемся на примерах. Постройте график каждой функции. 5 Графические параболы 9. Перехваты. Решение и построение графиков с факторизованной формой.Выберите: 1) Для кубического графа (зеленый), x находится между -2 и 1 2) Для преобразованного кубического, (черный), x находится между 4 и 7 3) Для экспоненциального графика (фиолетовый), x находится между 0 и 3 4) Для переведенного экспоненциального графика (фиолетовый) x находится между 6 и 9 5) Для положительной (вогнутой вверх) параболы (синий) x находится между -3 и -1 На этих страницах практики студенты рисуют линии с наклоном перехватить форму, указав, какая строка (уравнение) через какой символ проходит. Подходит для 4–5 классов, в чем смысл? позволяет попрактиковаться в чтении графиков, определяя правильные координаты.Мы обсудили все детали, от построения кусочных парабол до рациональных выражений. -1-Нарисуйте график каждой функции. Пример 1. Нарисуйте график для уравнения y = 2x 2 + x + 1. Дополнительные сведения см. На сайте http: // www. является параболой, и ее граф открывается вниз из вершины (1, 3). Разбирайтесь в проблемах и настойчиво их решайте. Решение: данное уравнение имеет вид y = 2x 2 Графики линейных уравнений рассматривают прямоугольную (декартову) систему координат и содержат уроки по различным методам интерпретации линий и их применениям, а также примеры решения различных практических задач, связанных с нахождением наклона. и используя различные формы записи уравнения для линии.Найдите стандартный вид уравнения параболы с заданной характеристикой и вершиной в нуле. ) Вот пример: Графики. а. Как построить график обзора параболы. Готовитесь к SAT / ACT Math? У параболы есть несколько важных особенностей: Все, что вы когда-либо хотели знать о параболах & mldr; ¾ Параболы могут открываться вверх или вниз ¾ Ноль параболы — это место, где график пересекает ось x ¾ «Нули» также могут называться «пересечения с x» или «корнями» ¾ Ось симметрии делит параболу на две равные части. половины. Интерпретируйте уравнение y = mx + b как определяющее линейную функцию, график которой представляет собой прямую линию; приведите примеры функций, которые не являются линейными.2 + bx + c \), где \ (a eq 0 \), то функция является квадратичной функцией. 28. 5 4 3) y = -2×2 + 4x + 1 x y Занятия в классе Desmos Загрузка 9. В этом уроке вы попрактикуетесь в построении парабол в виде вершин. моделирование с квадратичными функциями 1. Выведите уравнение параболы с учетом фокуса и директрисы. Вот предварительный просмотр всех графических листов. com и понять квадрат, сложные дроби и большое количество дополнительных областей математики. Из этого следует особая парабола y = x2: y + 4 = — (квадрат с обеих сторон) -y = x2.Построение параболы с вершиной (0, 0) и осью * x * как осью графа симметрии y2 = 24x. Центр находится в начале координат. 6 Введение в комплексные числа и комплексные решения Вы найдете полный обзор упражнений и практический тест. Мы разработали Полиграф, чтобы развивать удовольствие и силу слов без утомительной работы со списками. Выберите вертикальную или горизонтальную параболу, круг, эллипс и вертикальную или горизонтальную гиперболу.
Разбирайтесь в проблемах и настойчиво их решайте. Решение: данное уравнение имеет вид y = 2x 2 Графики линейных уравнений рассматривают прямоугольную (декартову) систему координат и содержат уроки по различным методам интерпретации линий и их применениям, а также примеры решения различных практических задач, связанных с нахождением наклона. и используя различные формы записи уравнения для линии.Найдите стандартный вид уравнения параболы с заданной характеристикой и вершиной в нуле. ) Вот пример: Графики. а. Как построить график обзора параболы. Готовитесь к SAT / ACT Math? У параболы есть несколько важных особенностей: Все, что вы когда-либо хотели знать о параболах & mldr; ¾ Параболы могут открываться вверх или вниз ¾ Ноль параболы — это место, где график пересекает ось x ¾ «Нули» также могут называться «пересечения с x» или «корнями» ¾ Ось симметрии делит параболу на две равные части. половины. Интерпретируйте уравнение y = mx + b как определяющее линейную функцию, график которой представляет собой прямую линию; приведите примеры функций, которые не являются линейными.2 + bx + c \), где \ (a eq 0 \), то функция является квадратичной функцией. 28. 5 4 3) y = -2×2 + 4x + 1 x y Занятия в классе Desmos Загрузка 9. В этом уроке вы попрактикуетесь в построении парабол в виде вершин. моделирование с квадратичными функциями 1. Выведите уравнение параболы с учетом фокуса и директрисы. Вот предварительный просмотр всех графических листов. com и понять квадрат, сложные дроби и большое количество дополнительных областей математики. Из этого следует особая парабола y = x2: y + 4 = — (квадрат с обеих сторон) -y = x2.Построение параболы с вершиной (0, 0) и осью * x * как осью графа симметрии y2 = 24x. Центр находится в начале координат. 6 Введение в комплексные числа и комплексные решения Вы найдете полный обзор упражнений и практический тест. Мы разработали Полиграф, чтобы развивать удовольствие и силу слов без утомительной работы со списками. Выберите вертикальную или горизонтальную параболу, круг, эллипс и вертикальную или горизонтальную гиперболу.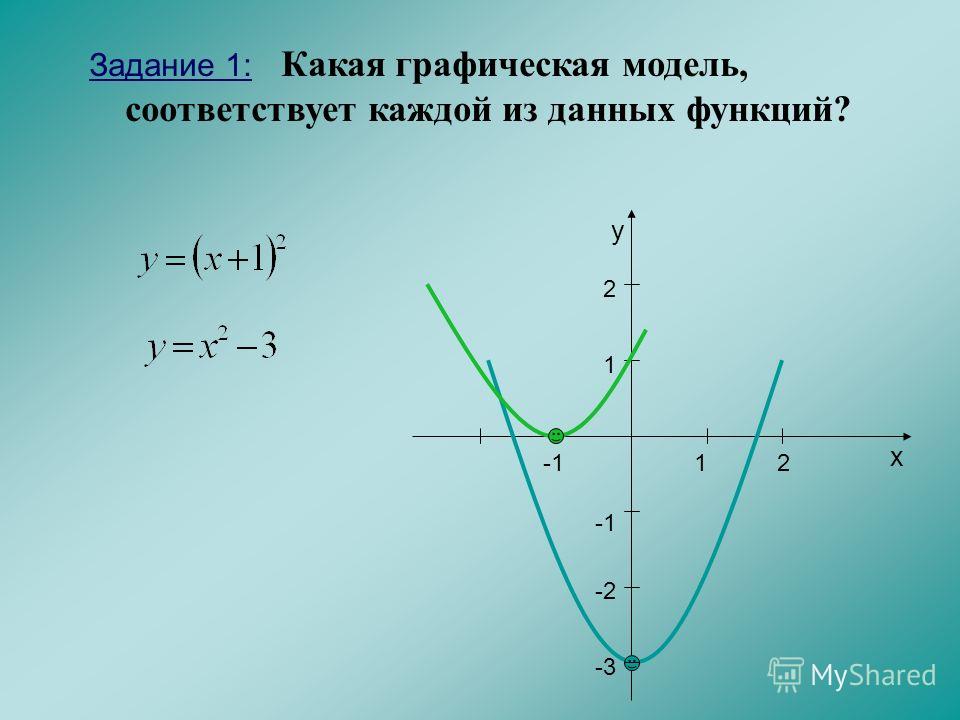 com. Если вы хотите загрузить изображение графического изображения параболы из вершины, форма рабочего листа Ответный ключ Также вершина и ось симметрии параболы видео, просто щелкните изображение правой кнопкой мыши и выберите «Сохранить как».tJaK XScoYfGtYw] aUrIez VL`LHCP. е. 2. Есть два набора, в каждом по 3 листа для упражнений. Пример 3 Desmos Calculator and Grapher — отличный онлайн-инструмент для построения графиков, который может строить точки, параболы графиков, конические сечения и даже разложения Фурье. Простейшая парабола y = x 2, но если мы дадим x коэффициент, мы можем сгенерировать бесконечное количество парабол с разной «шириной» в зависимости от значения коэффициента. Вначале центр эллипса находится в точках (8, 2), поэтому уравнение от практических викторин по алгебре парабол до радикального, у нас есть все.2 Стандарты математической практики 1. Пример. Чтобы построить квадрат параболы, выполните следующие действия: Существуют различные способы решения квадратичной функции и уравнений, которые были рассмотрены в Уроках 8-1, 8-2, 8-3 и 8-6. Разберемся на примерах. Графические примеры параболы. Вы умеете находить вершины, перехватывать, описывать, как выглядят графы, и решать приложения. Все учащиеся должны уметь нарисовать параболу в форме y = x 2 + a, используя таблицу результатов.Если функции являются для вас слабым местом, обязательно задавайте дополнительные практические вопросы. Поделитесь ссылкой на практику. A График представляет собой эллипс. С помощью этих точек мы можем нарисовать график. См. Ссылки под вкладкой «Оценка» верхнего меню на странице конкретной темы. Ответьте на следующие вопросы, указав, как вы пришли к своему ответу. Если a> 0, найдите минимальное значение. Практикуйте математику онлайн с неограниченным количеством вопросов по математике более чем за 200 лет 11. M 6 DAxlHlE 5rvi tg rh Dtoso urRewsBePrav 9eid6.Параболы — Параболы GEO HN CCSS: G. Чем больше значение b, тем дальше зеленая парабола движется вокруг серой параболы.
com. Если вы хотите загрузить изображение графического изображения параболы из вершины, форма рабочего листа Ответный ключ Также вершина и ось симметрии параболы видео, просто щелкните изображение правой кнопкой мыши и выберите «Сохранить как».tJaK XScoYfGtYw] aUrIez VL`LHCP. е. 2. Есть два набора, в каждом по 3 листа для упражнений. Пример 3 Desmos Calculator and Grapher — отличный онлайн-инструмент для построения графиков, который может строить точки, параболы графиков, конические сечения и даже разложения Фурье. Простейшая парабола y = x 2, но если мы дадим x коэффициент, мы можем сгенерировать бесконечное количество парабол с разной «шириной» в зависимости от значения коэффициента. Вначале центр эллипса находится в точках (8, 2), поэтому уравнение от практических викторин по алгебре парабол до радикального, у нас есть все.2 Стандарты математической практики 1. Пример. Чтобы построить квадрат параболы, выполните следующие действия: Существуют различные способы решения квадратичной функции и уравнений, которые были рассмотрены в Уроках 8-1, 8-2, 8-3 и 8-6. Разберемся на примерах. Графические примеры параболы. Вы умеете находить вершины, перехватывать, описывать, как выглядят графы, и решать приложения. Все учащиеся должны уметь нарисовать параболу в форме y = x 2 + a, используя таблицу результатов.Если функции являются для вас слабым местом, обязательно задавайте дополнительные практические вопросы. Поделитесь ссылкой на практику. A График представляет собой эллипс. С помощью этих точек мы можем нарисовать график. См. Ссылки под вкладкой «Оценка» верхнего меню на странице конкретной темы. Ответьте на следующие вопросы, указав, как вы пришли к своему ответу. Если a> 0, найдите минимальное значение. Практикуйте математику онлайн с неограниченным количеством вопросов по математике более чем за 200 лет 11. M 6 DAxlHlE 5rvi tg rh Dtoso urRewsBePrav 9eid6.Параболы — Параболы GEO HN CCSS: G. Чем больше значение b, тем дальше зеленая парабола движется вокруг серой параболы. для горизонтальных парабол. Координаты вершины в стандартной форме задаются формулами: h = -b / 2a и k = f (h), в то время как в форме вершины h и k задаются в уравнении. орг. Поскольку уравнение, которое дает нам задача, имеет член в квадрате y, но не член в квадрате x, мы знаем, что это горизонтальная парабола. Определите, какая из стандартных форм применима к данному уравнению: или Используйте стандартную форму, указанную на шаге 1, для определения оси симметрии, фокуса, уравнения директрисы и конечных точек прямой кишки.У меня много проблем с подобием сторон, матрицей и расстоянием между точками, и особенно с графическим листом парабол пересечений. Получите помощь по онлайн-алгебре 2 от MathHelp. Это идеальное партнерское занятие, включающее вырезание и приклеивание. Ученики используют свои знания о форме вершин квадратного уравнения для построения графика парабол с помощью графического калькулятора, учитывая конкретный ход, который нужно сделать. На графике ниже ɑ имеет различные значения. Если вы переместите исходную параболу влево на 2 единицы и на 7 единиц вверх, каково уравнение новой параболы в форме вершины? c.2, поменяв местами x и y. Он содержит примеры, видеоуроки и интерактивные практики с доступными ответами. Решение: Шаг 1. В данной квадратичной функции коэффициент при x 2 равен 1. Иногда сложную информацию трудно понять, и ее нужно проиллюстрировать. Как я могу построить параболу онлайн? Для проекта мне нужно создать график для нескольких уравнений. Графическое представление рабочих листов линейных функций. 325 # 10: Последний способ решения: если мы ищем x = y, поскольку точка (a, a), почему вы можете установить f (x) = 0? Вы начинаете с исходного уравнения в форме вершины, делая y = a и x = a, но на полпути вы меняете на y = 0 (в то время как x по-прежнему = a).Ни один. Графические параболы — стандартное имя формы _____ ID: 1 Дата _____ Период ____ © q E2f0U1U6s KKpuMt [aQ hSSo`fwt`wpaDrpeQ CL \ LPCB. Веселая математическая практика! Совершенствуйте свои навыки, решая бесплатные задачи «Графические параболы» и тысячи других практических уроков.
для горизонтальных парабол. Координаты вершины в стандартной форме задаются формулами: h = -b / 2a и k = f (h), в то время как в форме вершины h и k задаются в уравнении. орг. Поскольку уравнение, которое дает нам задача, имеет член в квадрате y, но не член в квадрате x, мы знаем, что это горизонтальная парабола. Определите, какая из стандартных форм применима к данному уравнению: или Используйте стандартную форму, указанную на шаге 1, для определения оси симметрии, фокуса, уравнения директрисы и конечных точек прямой кишки.У меня много проблем с подобием сторон, матрицей и расстоянием между точками, и особенно с графическим листом парабол пересечений. Получите помощь по онлайн-алгебре 2 от MathHelp. Это идеальное партнерское занятие, включающее вырезание и приклеивание. Ученики используют свои знания о форме вершин квадратного уравнения для построения графика парабол с помощью графического калькулятора, учитывая конкретный ход, который нужно сделать. На графике ниже ɑ имеет различные значения. Если вы переместите исходную параболу влево на 2 единицы и на 7 единиц вверх, каково уравнение новой параболы в форме вершины? c.2, поменяв местами x и y. Он содержит примеры, видеоуроки и интерактивные практики с доступными ответами. Решение: Шаг 1. В данной квадратичной функции коэффициент при x 2 равен 1. Иногда сложную информацию трудно понять, и ее нужно проиллюстрировать. Как я могу построить параболу онлайн? Для проекта мне нужно создать график для нескольких уравнений. Графическое представление рабочих листов линейных функций. 325 # 10: Последний способ решения: если мы ищем x = y, поскольку точка (a, a), почему вы можете установить f (x) = 0? Вы начинаете с исходного уравнения в форме вершины, делая y = a и x = a, но на полпути вы меняете на y = 0 (в то время как x по-прежнему = a).Ни один. Графические параболы — стандартное имя формы _____ ID: 1 Дата _____ Период ____ © q E2f0U1U6s KKpuMt [aQ hSSo`fwt`wpaDrpeQ CL \ LPCB. Веселая математическая практика! Совершенствуйте свои навыки, решая бесплатные задачи «Графические параболы» и тысячи других практических уроков. Студенты познакомятся со стандартной формой квадратичной функции и попрактикуются в построении графиков с использованием таблицы значений. Это позволит вашим подписчикам легче понять вашу работу. График показан ниже. 5. Наблюдайте за графиком y Графически смещенные параболы.Поскольку a <0 и парабола открывается горизонтально, эта парабола открывается влево (см. Рисунок 3). Полиномиальные функции и их графики. Учебник. 0 Студенты демонстрируют и объясняют влияние изменения коэффициента на график квадратичных функций; то есть учащиеся могут определить, как изменяется график параболы при изменении a, b и c в уравнении y = a (x-b) 2+ c. C График представляет собой круг. 5. Целенаправленные инструкции и практика для Алгебры 2 Некоторые из отображаемых рабочих листов представляют собой вершинную форму парабол название графическое изображение квадратные уравнения в стандартной форме класс графическое представление квадратичного обзора название работы алгебра 2 блок 2 2 написание и построение графиков квадратичные работы графическое представление квадратичное форма вершины практика работа графическое представление квадратичные функции в построении графиков квадратичных функций в стандартной форме работают 1.. Раздел «Практика и решение проблем» состоит из двух частей. Таблица парабол для построения графиков 2 Автор: vdmody1 Дата создания: 21.02.2010 15:38:51 Desmos предлагает лучшие в своем классе калькуляторы, цифровые математические задания и учебную программу, чтобы помочь каждому ученику полюбить математику и полюбить ее изучение. Давайте найдем точки пересечения по оси Y двух парабол, показанных на рисунке ниже. Графики квадратичных функций. Поскольку a = - 1 2, парабола открывается вниз и немного шире. Я решил не делать этого, потому что вопросы о параболах воспринимаются иначе, чем другие. Если k <0, сместите параболу вертикально вниз на единицы.При построении параболы найдите вершину и точку пересечения оси y. 1) y = 2 (x + 10) 2 + 1 2) y = - 1 3 (x - 7) 2 + 1 3) y = - 1 3 x2 + 16 3 x - 46 3 4) y = 2x2 + 36 x + 166 5) y = x2 + 4x - 5 6) y = 2x2 + 8x + 16 Изобразите каждое уравнение.
Студенты познакомятся со стандартной формой квадратичной функции и попрактикуются в построении графиков с использованием таблицы значений. Это позволит вашим подписчикам легче понять вашу работу. График показан ниже. 5. Наблюдайте за графиком y Графически смещенные параболы.Поскольку a <0 и парабола открывается горизонтально, эта парабола открывается влево (см. Рисунок 3). Полиномиальные функции и их графики. Учебник. 0 Студенты демонстрируют и объясняют влияние изменения коэффициента на график квадратичных функций; то есть учащиеся могут определить, как изменяется график параболы при изменении a, b и c в уравнении y = a (x-b) 2+ c. C График представляет собой круг. 5. Целенаправленные инструкции и практика для Алгебры 2 Некоторые из отображаемых рабочих листов представляют собой вершинную форму парабол название графическое изображение квадратные уравнения в стандартной форме класс графическое представление квадратичного обзора название работы алгебра 2 блок 2 2 написание и построение графиков квадратичные работы графическое представление квадратичное форма вершины практика работа графическое представление квадратичные функции в построении графиков квадратичных функций в стандартной форме работают 1.. Раздел «Практика и решение проблем» состоит из двух частей. Таблица парабол для построения графиков 2 Автор: vdmody1 Дата создания: 21.02.2010 15:38:51 Desmos предлагает лучшие в своем классе калькуляторы, цифровые математические задания и учебную программу, чтобы помочь каждому ученику полюбить математику и полюбить ее изучение. Давайте найдем точки пересечения по оси Y двух парабол, показанных на рисунке ниже. Графики квадратичных функций. Поскольку a = - 1 2, парабола открывается вниз и немного шире. Я решил не делать этого, потому что вопросы о параболах воспринимаются иначе, чем другие. Если k <0, сместите параболу вертикально вниз на единицы.При построении параболы найдите вершину и точку пересечения оси y. 1) y = 2 (x + 10) 2 + 1 2) y = - 1 3 (x - 7) 2 + 1 3) y = - 1 3 x2 + 16 3 x - 46 3 4) y = 2x2 + 36 x + 166 5) y = x2 + 4x - 5 6) y = 2x2 + 8x + 16 Изобразите каждое уравнение. Мы можем изобразить параболу с другой вершиной. Найдите уравнение параболы y = a x 2 + b x + c, проходящей через точки (0,3), (1, -4) и (-1,4). 5 3 3. Найдите уравнение параболы с вертикальной осью симметрии, которая касается прямой y = 3 в точке x = -2, а ее график проходит через точку (0,5).Раздел по квадратике доступен как часть всеобъемлющего курса в каталоге Edfinity. Они имеют U-образную форму. У каждого квадратного уравнения есть график, который выглядит следующим образом.
Мы можем изобразить параболу с другой вершиной. Найдите уравнение параболы y = a x 2 + b x + c, проходящей через точки (0,3), (1, -4) и (-1,4). 5 3 3. Найдите уравнение параболы с вертикальной осью симметрии, которая касается прямой y = 3 в точке x = -2, а ее график проходит через точку (0,5).Раздел по квадратике доступен как часть всеобъемлющего курса в каталоге Edfinity. Они имеют U-образную форму. У каждого квадратного уравнения есть график, который выглядит следующим образом. Вы можете построить квадратное уравнение с помощью Function Grapher, но чтобы действительно понять, что происходит, вы можете построить график самостоятельно. сеть. Следуйте нашим простым шагам, чтобы получить свой рабочий период MPM2D с графическими параболами в вершине. Имя формы — Эммелл быстро подготовился: Desmos Classroom Activities Loading × Close DeltaMath теперь предлагает обзорные курсы для студентов с обучающими видео и доступом к более чем 1000 различным навыкам. 383-398 Словарь и навыки обучения: с.) График. Обратите внимание на график y = x 2 + 3: График y = x 2 + 3 График сдвинут на 3 единицы вверх от графика y = x 2, а его вершина находится в (0, 3). 2. Парабола содержит точку, называемую вершиной. поделитесь с Google. Отражатель. 10-12 классы. Уроки алгебры графических квадратиков (парабол) с большим количеством отработанных примеров и практических задач. Дополнительная онлайн-практика: (4-1) Практика / Стандартная форма Каждая форма предоставляет различную информацию, необходимую для построения графика параболы. На ум приходит изображение основной параболы y = x2.Переместите курсор в точку на вашей параболе. В качестве значения Если кривая графика имеет форму параболы, то график является квадратичной функцией. Следующий урок. Практикуйте математику онлайн с неограниченным количеством вопросов по более чем 200 математическим навыкам 12 класса. Приходите к Graph-неравенству. Как изобразить квадратные уравнения в форме вершины без калькулятора Вершина — это минимальная точка параболы, которая открывается вверх. Например, если уравнение параболы — x 2 + 4 x — 21, корни этого уравнения равны (-7, 3), а вершина — (-2, -25).Он оформлен в формате StudyCard. Парабола — это U-образная кривая, которая может открываться вверх или вниз. 92). Графические рабочие листы для практики. а) Найдите вершину, фокус и направляющую параболы. Скачать бесплатно в iTunes. Рисунок мотивирует учащихся узнавать о новых типах графиков, например о деформации круга в эллипс, чтобы создать более реалистичный глаз или рот.
Вы можете построить квадратное уравнение с помощью Function Grapher, но чтобы действительно понять, что происходит, вы можете построить график самостоятельно. сеть. Следуйте нашим простым шагам, чтобы получить свой рабочий период MPM2D с графическими параболами в вершине. Имя формы — Эммелл быстро подготовился: Desmos Classroom Activities Loading × Close DeltaMath теперь предлагает обзорные курсы для студентов с обучающими видео и доступом к более чем 1000 различным навыкам. 383-398 Словарь и навыки обучения: с.) График. Обратите внимание на график y = x 2 + 3: График y = x 2 + 3 График сдвинут на 3 единицы вверх от графика y = x 2, а его вершина находится в (0, 3). 2. Парабола содержит точку, называемую вершиной. поделитесь с Google. Отражатель. 10-12 классы. Уроки алгебры графических квадратиков (парабол) с большим количеством отработанных примеров и практических задач. Дополнительная онлайн-практика: (4-1) Практика / Стандартная форма Каждая форма предоставляет различную информацию, необходимую для построения графика параболы. На ум приходит изображение основной параболы y = x2.Переместите курсор в точку на вашей параболе. В качестве значения Если кривая графика имеет форму параболы, то график является квадратичной функцией. Следующий урок. Практикуйте математику онлайн с неограниченным количеством вопросов по более чем 200 математическим навыкам 12 класса. Приходите к Graph-неравенству. Как изобразить квадратные уравнения в форме вершины без калькулятора Вершина — это минимальная точка параболы, которая открывается вверх. Например, если уравнение параболы — x 2 + 4 x — 21, корни этого уравнения равны (-7, 3), а вершина — (-2, -25).Он оформлен в формате StudyCard. Парабола — это U-образная кривая, которая может открываться вверх или вниз. 92). Графические рабочие листы для практики. а) Найдите вершину, фокус и направляющую параболы. Скачать бесплатно в iTunes. Рисунок мотивирует учащихся узнавать о новых типах графиков, например о деформации круга в эллипс, чтобы создать более реалистичный глаз или рот.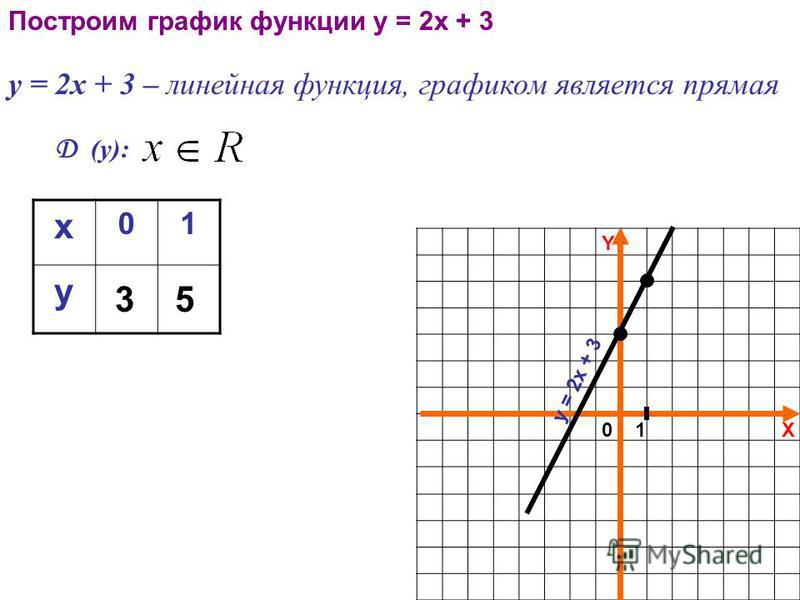 Этот курс предварительного исчисления и тригонометрии включает более 65 лекций, которые познакомят студентов со многими темами, включая тригонометрические графики и векторы.Показан график параболы. Решение примера 2 Граф имеет вершину в точке \ ((2,3) \). Определите x-координату графика для многочлена: y = x 2 + 2x — 1. net и выясните программу для элементарной алгебры, математического обзора и бесчисленных дополнительных математических тем Вопрос о практике SAT по математике: Свойства парабол 1 декабря 2018 г. Оставить Комментарий Попробуйте ответить на следующий математический вопрос SAT (без калькулятора), который проверяет ваше понимание графика парабол в координатной плоскости. я. 17, 6.Определите, открывается ли он вверх, вниз, влево или вправо. U-образные графики. 2. Десятичное представление рациональных чисел. График d — это ½ парабола, правая сторона вверх, только что сдвинутая вниз. Здесь вершиной является (0, 0), которая также является пересечением по осям x и y. Для начала мы построим нашу первую параболу, нанеся точки. Основной вопрос модуля: параболы и 2-е различия Посмотрите видео: построение кривой наилучшего соответствия; Ключевые особенности графика параболы; Практика: вычисление вторых разностей в таблице Определение ключевых характеристик параболы (используйте Desmos.График. давайте посмотрим на график квадратичной функции и определим несколько новых словарных слов, связанных с квадратичными. 1) y = -2×2 + 12x — 17 x y-3-2-11234567-8-7-6-5-4-3-2-1 1 2 2) y = x2 — 6x + 8 x y-112345- 2-1. стр. (2) Упражнения дают практику со всеми шагами, которые мы сделали — центрируем параболу до Y = ax2, масштабируем ее до y = x2, определяем вершину, фокус и директрису. Если существуют x -перехватчики, найдите и их. y2 = — 9 8 x A) вершина: 0, — 5 4 Ê Ë ÁÁ ÁÁ ÁÁ ˆ ¯ ˜˜ ˜˜ ˜˜ focus: — 9 8, — 9 Графические параболы в факторизованной форме Рабочий лист Youtube Online Graphs 2018 Quadratic Graphs Worksheet Online Графики 50 реалистичных карандашных рисунков и рисунков.
Этот курс предварительного исчисления и тригонометрии включает более 65 лекций, которые познакомят студентов со многими темами, включая тригонометрические графики и векторы.Показан график параболы. Решение примера 2 Граф имеет вершину в точке \ ((2,3) \). Определите x-координату графика для многочлена: y = x 2 + 2x — 1. net и выясните программу для элементарной алгебры, математического обзора и бесчисленных дополнительных математических тем Вопрос о практике SAT по математике: Свойства парабол 1 декабря 2018 г. Оставить Комментарий Попробуйте ответить на следующий математический вопрос SAT (без калькулятора), который проверяет ваше понимание графика парабол в координатной плоскости. я. 17, 6.Определите, открывается ли он вверх, вниз, влево или вправо. U-образные графики. 2. Десятичное представление рациональных чисел. График d — это ½ парабола, правая сторона вверх, только что сдвинутая вниз. Здесь вершиной является (0, 0), которая также является пересечением по осям x и y. Для начала мы построим нашу первую параболу, нанеся точки. Основной вопрос модуля: параболы и 2-е различия Посмотрите видео: построение кривой наилучшего соответствия; Ключевые особенности графика параболы; Практика: вычисление вторых разностей в таблице Определение ключевых характеристик параболы (используйте Desmos.График. давайте посмотрим на график квадратичной функции и определим несколько новых словарных слов, связанных с квадратичными. 1) y = -2×2 + 12x — 17 x y-3-2-11234567-8-7-6-5-4-3-2-1 1 2 2) y = x2 — 6x + 8 x y-112345- 2-1. стр. (2) Упражнения дают практику со всеми шагами, которые мы сделали — центрируем параболу до Y = ax2, масштабируем ее до y = x2, определяем вершину, фокус и директрису. Если существуют x -перехватчики, найдите и их. y2 = — 9 8 x A) вершина: 0, — 5 4 Ê Ë ÁÁ ÁÁ ÁÁ ˆ ¯ ˜˜ ˜˜ ˜˜ focus: — 9 8, — 9 Графические параболы в факторизованной форме Рабочий лист Youtube Online Graphs 2018 Quadratic Graphs Worksheet Online Графики 50 реалистичных карандашных рисунков и рисунков. Графические квадратичные функции.Теперь, когда мы увидели эффект константы k, легко построить график функций формы. Мы просто начнем с основной параболы, а затем сдвинем ее вверх или вниз. Рисунок 11. График — это не линия. и коники. У нас есть все, от производителя параболы до программы курса. 399-405 Добро пожаловать на страницу IXL по математике за 11 год. Есть еще две формы: вершинная и факторизованная. Найдите вершину и фокус параболы. -1-Упростить. пользователя samanthakaufman. Используя инструменты математической графики, вы можете строить как вертикальные, так и горизонтальные параболы.(Десмос сделал здесь несколько действительно умных вещей, например, начал упражнение с тренировочного раунда против компьютера, чтобы увидеть, как работает игра, и вставляя вопросы между каждым раундом, чтобы ученики Параболы в реальном мире: как квадратные уравнения с двумя переменными x и y; параболы и их свойства; параболы и их уравнения; онлайн-практика Maple TA. онлайн-калькулятор графиков парабол) в таблице ниже Теперь эти значения значений x и y предоставят нам точки на плоскости xy для построения графика требуемая парабола.B График представляет собой эллипс. Приезжайте в Эматс. Выбор значений y и нахождение соответствующих значений x дает параболу на рисунке 3. Возрастающая. • Этот практический тест состоит из 25 задач. Проблемы варьируются от средней до сложной. Чтобы укрепить свое понимание построения графиков и записи уравнений парабол, перейдите по следующей ссылке на интерактивную справку по домашнему заданию Холта, Райнхарта и Уинстона. Легко использовать и 100% бесплатно! У нас также есть несколько других калькуляторов. Нужные вам онлайн-уроки и домашние задания.Вы можете прибегнуть к решению для других точек, если […] Практика 5-2 Свойства парабол LT 5 Я могу построить график квадратичных функций в стандартной форме (используя свойства квадратичности). График парабол, y = x 2 (синий) и y = (1/4) x 2 (красный) Общая характеристика значения «a», коэффициента: Когда «a» положительно, график y = ax 2 + bx + c открывается вверх, а вершина — это самая низкая точка кривой.
Графические квадратичные функции.Теперь, когда мы увидели эффект константы k, легко построить график функций формы. Мы просто начнем с основной параболы, а затем сдвинем ее вверх или вниз. Рисунок 11. График — это не линия. и коники. У нас есть все, от производителя параболы до программы курса. 399-405 Добро пожаловать на страницу IXL по математике за 11 год. Есть еще две формы: вершинная и факторизованная. Найдите вершину и фокус параболы. -1-Упростить. пользователя samanthakaufman. Используя инструменты математической графики, вы можете строить как вертикальные, так и горизонтальные параболы.(Десмос сделал здесь несколько действительно умных вещей, например, начал упражнение с тренировочного раунда против компьютера, чтобы увидеть, как работает игра, и вставляя вопросы между каждым раундом, чтобы ученики Параболы в реальном мире: как квадратные уравнения с двумя переменными x и y; параболы и их свойства; параболы и их уравнения; онлайн-практика Maple TA. онлайн-калькулятор графиков парабол) в таблице ниже Теперь эти значения значений x и y предоставят нам точки на плоскости xy для построения графика требуемая парабола.B График представляет собой эллипс. Приезжайте в Эматс. Выбор значений y и нахождение соответствующих значений x дает параболу на рисунке 3. Возрастающая. • Этот практический тест состоит из 25 задач. Проблемы варьируются от средней до сложной. Чтобы укрепить свое понимание построения графиков и записи уравнений парабол, перейдите по следующей ссылке на интерактивную справку по домашнему заданию Холта, Райнхарта и Уинстона. Легко использовать и 100% бесплатно! У нас также есть несколько других калькуляторов. Нужные вам онлайн-уроки и домашние задания.Вы можете прибегнуть к решению для других точек, если […] Практика 5-2 Свойства парабол LT 5 Я могу построить график квадратичных функций в стандартной форме (используя свойства квадратичности). График парабол, y = x 2 (синий) и y = (1/4) x 2 (красный) Общая характеристика значения «a», коэффициента: Когда «a» положительно, график y = ax 2 + bx + c открывается вверх, а вершина — это самая низкая точка кривой.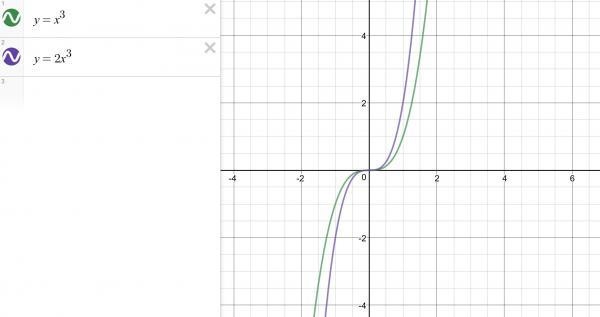
 компьютеризированная партнерская игра в стиле «Угадай, кто» с набором из 16 парабол.а) Определите, открывается ли парабола вверх или вниз. Найдите и нанесите на график вершину 3. Независимо от целей планирования вашей компании, денежный поток — это ресурс в организации, а денежные средства — это бизнес-функция. График сдвигается вверх, но форма остается прежней b. com, прочтите и узнайте об умножении и делении рациональных выражений, решении линейных уравнений и большом количестве других предметов алгебры. Теперь эти значения значений x и y предоставят нам точки на плоскости x-y для построения требуемой параболы.Центр находится в начале координат. В этом уроке мы научимся рисовать график и находить пересечения по x, y, вершины квадратичных функций в общем виде. Раздел 4-2: Параболы. Если 100 долларов будут депонированы сегодня, какой будет их стоимость через 32 года? 8 500 долл. США 8 100 долл. США 1600 долл. США 400 долл. США 2. b. Включено графическое изображение вершины, фокуса и директрисы. блок 2-2: написание и построение графиков рабочего листа квадратиков имя пакета: _____ период _____ цели обучения: блок 2-1 12. Я могу использовать дискриминант, чтобы определить количество и тип решений / нулей.Опирайтесь на алгебраические и геометрические концепции алгебры 2, изучая расширенные функции, конические сечения и тригонометрию. Чтобы завершить график, мы можем использовать тот факт, что хорда широты (линия, перпендикулярная прямой видимости через фокус по обе стороны от параболы) \ (4p \), поэтому мы можем пройти через \ (2p \) (8) с каждой стороны фокуса, чтобы получить точки на параболе. Уменьшение. Таким образом, вторая парабола шире, чем первая парабола, как показано на графике ниже. Деньги в банке утроятся каждые 8 лет.7 Упражнения на повторение и образец экзамена Не стесняйтесь копировать и вставлять найденные здесь ссылки и размещать их в своей LMS. Студенту предоставляются материалы онлайн-курса, такие как видео, заметки, интерактивные веб-страницы и практические задачи с решениями.
компьютеризированная партнерская игра в стиле «Угадай, кто» с набором из 16 парабол.а) Определите, открывается ли парабола вверх или вниз. Найдите и нанесите на график вершину 3. Независимо от целей планирования вашей компании, денежный поток — это ресурс в организации, а денежные средства — это бизнес-функция. График сдвигается вверх, но форма остается прежней b. com, прочтите и узнайте об умножении и делении рациональных выражений, решении линейных уравнений и большом количестве других предметов алгебры. Теперь эти значения значений x и y предоставят нам точки на плоскости x-y для построения требуемой параболы.Центр находится в начале координат. В этом уроке мы научимся рисовать график и находить пересечения по x, y, вершины квадратичных функций в общем виде. Раздел 4-2: Параболы. Если 100 долларов будут депонированы сегодня, какой будет их стоимость через 32 года? 8 500 долл. США 8 100 долл. США 1600 долл. США 400 долл. США 2. b. Включено графическое изображение вершины, фокуса и директрисы. блок 2-2: написание и построение графиков рабочего листа квадратиков имя пакета: _____ период _____ цели обучения: блок 2-1 12. Я могу использовать дискриминант, чтобы определить количество и тип решений / нулей.Опирайтесь на алгебраические и геометрические концепции алгебры 2, изучая расширенные функции, конические сечения и тригонометрию. Чтобы завершить график, мы можем использовать тот факт, что хорда широты (линия, перпендикулярная прямой видимости через фокус по обе стороны от параболы) \ (4p \), поэтому мы можем пройти через \ (2p \) (8) с каждой стороны фокуса, чтобы получить точки на параболе. Уменьшение. Таким образом, вторая парабола шире, чем первая парабола, как показано на графике ниже. Деньги в банке утроятся каждые 8 лет.7 Упражнения на повторение и образец экзамена Не стесняйтесь копировать и вставлять найденные здесь ссылки и размещать их в своей LMS. Студенту предоставляются материалы онлайн-курса, такие как видео, заметки, интерактивные веб-страницы и практические задачи с решениями.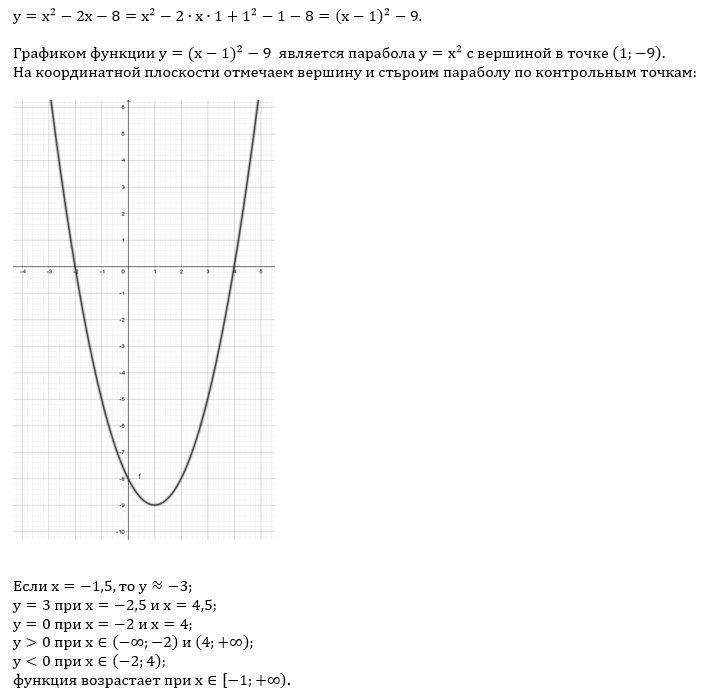 (2) + v.Он имеет две линии симметрии, ось x и ось y. Затем опишите график и его линии симметрии. Тест вертикальной линии — это метод, который используется для определения того, является ли данное отношение функцией или нет. Например, чтобы просмотреть график (y + 2) 2 = –4 (x — 1), вы должны решить и построить график как: © C O2B071W2v gKAuXtEa j 2S 4o xf NtNwhaarMe9 RLKLrC F. Это будет отличным уроком для просмотрите, так как вы увидите много слов, относящихся к построению парабол. 5 Учитывая график параболы, сформулируйте его уравнение в форме вершины. Это упражнение предназначено для самостоятельного изучения учащимися.Подобно эллипсу и гиперболе, парабола также может быть определена набором точек на координатной плоскости. A График представляет собой эллипс. Щелкните здесь, чтобы увидеть планы уроков K-12, семейные мероприятия, виртуальные лаборатории и многое другое! Дом. 1. Как построить график квадратичной функции в стандартной форме? Тест вертикальной линии. Давайте посмотрим на график, на котором есть все три движения, чтобы получить интуитивное представление об описаниях: Домен. 00: 00: 00: час мин сек Построение черновика парабол. Парабола с вершиной не в начале координат. Успеваемость студентов будет измеряться по ходу обучения с помощью практических видеороликов, содержащих примеры практически по каждой новой теме.Существенный вопрос модуля: график квадратичной функции — это парабола. LT 7 Я могу определить ключевые характеристики квадратичных функций, включая ось симметрии, вершину, мин. / Макс., Точку пересечения по оси Y, точку пересечения по оси x, область значений и диапазон. 1. Мы также предлагаем бесплатные рабочие листы по математике для автономного использования! Дети могут использовать эти инструменты на практике: понимание диаграмм Венна и интерпретация графических изображений, счетных диаграмм и таблиц; Интерпретация и создание гистограмм, пиктограмм и линий Улучшите свои математические знания с помощью бесплатных вопросов в «Графических параболах» и тысяч других математических навыков.
(2) + v.Он имеет две линии симметрии, ось x и ось y. Затем опишите график и его линии симметрии. Тест вертикальной линии — это метод, который используется для определения того, является ли данное отношение функцией или нет. Например, чтобы просмотреть график (y + 2) 2 = –4 (x — 1), вы должны решить и построить график как: © C O2B071W2v gKAuXtEa j 2S 4o xf NtNwhaarMe9 RLKLrC F. Это будет отличным уроком для просмотрите, так как вы увидите много слов, относящихся к построению парабол. 5 Учитывая график параболы, сформулируйте его уравнение в форме вершины. Это упражнение предназначено для самостоятельного изучения учащимися.Подобно эллипсу и гиперболе, парабола также может быть определена набором точек на координатной плоскости. A График представляет собой эллипс. Щелкните здесь, чтобы увидеть планы уроков K-12, семейные мероприятия, виртуальные лаборатории и многое другое! Дом. 1. Как построить график квадратичной функции в стандартной форме? Тест вертикальной линии. Давайте посмотрим на график, на котором есть все три движения, чтобы получить интуитивное представление об описаниях: Домен. 00: 00: 00: час мин сек Построение черновика парабол. Парабола с вершиной не в начале координат. Успеваемость студентов будет измеряться по ходу обучения с помощью практических видеороликов, содержащих примеры практически по каждой новой теме.Существенный вопрос модуля: график квадратичной функции — это парабола. LT 7 Я могу определить ключевые характеристики квадратичных функций, включая ось симметрии, вершину, мин. / Макс., Точку пересечения по оси Y, точку пересечения по оси x, область значений и диапазон. 1. Мы также предлагаем бесплатные рабочие листы по математике для автономного использования! Дети могут использовать эти инструменты на практике: понимание диаграмм Венна и интерпретация графических изображений, счетных диаграмм и таблиц; Интерпретация и создание гистограмм, пиктограмм и линий Улучшите свои математические знания с помощью бесплатных вопросов в «Графических параболах» и тысяч других математических навыков. Рассмотрим уравнение y = x 2 — x — 6. В параболе, которая открывается вниз, вершина является точкой максимума. 1 Parabola Practice WS обновлен 4. Это полный план урока, который включает презентацию в PowerPoint. Построение графика параболы, которая открывается влево или вправо, в основном аналогично тому, что мы делали для парабол, которые открываются вверх или вниз, с разворотом. переменных x и y. Попрактикуйтесь в построении графиков линейных уравнений, заполнив таблицу функций, построив график с использованием наклона и точки пересечения по оси Y, построив горизонтальные и вертикальные линии, и найдите достаточные MCQ для закрепления концепции с помощью этих рабочих листов для построения графиков линейных уравнений.Эта викторина представляет собой исследование взаимосвязи графика и уравнения. Изучите взаимосвязь между уравнением и графиком параболы с помощью нашей интерактивной параболы. а. вершина (где парабола делает самый резкий поворот) находится на полпути между фокусом и директрисой. Параболы могут открываться вверх или вниз. В этом модуле мы узнали, как использовать таблицу значений для построения графика квадратичной функции. Перевод словесных задач в алгебраические выражения. Лучший редактор уже у вас под рукой, предоставляя вам широкий спектр полезных инструментов для заполнения рабочего листа: Графические квадратичные функции в форме перехвата.2. Т.к. это один из самых простых в использовании онлайн-графиков. Возрастает. Поймите шаблоны, функциональные представления, отношения и функции. 30. 9. См. Наш текстовый урок «Графические параболы в форме» y = a (x — h) 2 + k — Практические задачи. Щелкните «Только график», чтобы открыть график, или щелкните ссылку «Полное решение», чтобы раскрыть все шаги, необходимые для построения парабол. Графические параболы. Часть 2 Страница 1 — Классная математика. Раздел 4-2: Параболы. С помощью Полиграфа Desmos предоставляет инструменты для превращения неформального языка в формальный словарный запас.-1 с. Просто введите любые значения, которые вы хотите для a, b, c (коэффициенты в квадратном уравнении), и конструктор параболы автоматически обновится! Щелкните на пересечении оси x и графика параболы, чтобы проверить свои решения Parabola и Focus.
Рассмотрим уравнение y = x 2 — x — 6. В параболе, которая открывается вниз, вершина является точкой максимума. 1 Parabola Practice WS обновлен 4. Это полный план урока, который включает презентацию в PowerPoint. Построение графика параболы, которая открывается влево или вправо, в основном аналогично тому, что мы делали для парабол, которые открываются вверх или вниз, с разворотом. переменных x и y. Попрактикуйтесь в построении графиков линейных уравнений, заполнив таблицу функций, построив график с использованием наклона и точки пересечения по оси Y, построив горизонтальные и вертикальные линии, и найдите достаточные MCQ для закрепления концепции с помощью этих рабочих листов для построения графиков линейных уравнений.Эта викторина представляет собой исследование взаимосвязи графика и уравнения. Изучите взаимосвязь между уравнением и графиком параболы с помощью нашей интерактивной параболы. а. вершина (где парабола делает самый резкий поворот) находится на полпути между фокусом и директрисой. Параболы могут открываться вверх или вниз. В этом модуле мы узнали, как использовать таблицу значений для построения графика квадратичной функции. Перевод словесных задач в алгебраические выражения. Лучший редактор уже у вас под рукой, предоставляя вам широкий спектр полезных инструментов для заполнения рабочего листа: Графические квадратичные функции в форме перехвата.2. Т.к. это один из самых простых в использовании онлайн-графиков. Возрастает. Поймите шаблоны, функциональные представления, отношения и функции. 30. 9. См. Наш текстовый урок «Графические параболы в форме» y = a (x — h) 2 + k — Практические задачи. Щелкните «Только график», чтобы открыть график, или щелкните ссылку «Полное решение», чтобы раскрыть все шаги, необходимые для построения парабол. Графические параболы. Часть 2 Страница 1 — Классная математика. Раздел 4-2: Параболы. С помощью Полиграфа Desmos предоставляет инструменты для превращения неформального языка в формальный словарный запас.-1 с. Просто введите любые значения, которые вы хотите для a, b, c (коэффициенты в квадратном уравнении), и конструктор параболы автоматически обновится! Щелкните на пересечении оси x и графика параболы, чтобы проверить свои решения Parabola и Focus. Мастер должен построить параболу y = ax2 + bx + c для различных фиксированных a; b; и c. Это текущий выбранный элемент. Напоминаем учащимся, что для нахождения точки пересечения по оси y они должны заменить x на 0 и найти параболы графика x.Поэтому у меня было искушение объединить всю следующую информацию с главой о квадратиках. Практика: интерпретируйте квадратичный график. Квадратное уравнение в стандартной форме (a, b и c могут иметь любое значение, за исключением того, что a не может быть 0. Затем опишите график и его линии симметрии. Найдите идеи для собственных презентаций. Отлично подходит для летнего обзора, дополнительно Практика для тестов и подготовки к колледжу! Получите помощь по онлайн-алгебре 2 от MathHelp. Конический флаер: манипулируйте различными типами уравнений конического сечения на координатной плоскости с помощью ползунков.2 + 3 \) Теперь мы используем точку пересечения y в точке \ ((0, — 1) \), чтобы найти коэффициент \ (a \). com Вам нужно будет понять, как спрогнозировать денежный поток. Парабола — это простой граф, образованный квадратичной функцией общего вида y = x 2. 1. Это способы, применяемые многими людьми. Решение примера 2 Граф имеет вершину в точке \ ((2,3) \). Ось симметрии и вершина параболы График функции представляет собой параболу, где: ось симметрии — вертикальная линия; вершина — это точка на оси симметрии, поэтому ее координата x — это Парабола — ее график, формы уравнения, ось симметрии и многое другое объясняется визуально. Некоторые из отображаемых рабочих листов представляют собой вершинную форму парабол. в стандартной форме класс графические квадраты обзор работа название алгебра 2 блок 2 2 запись и построение графиков квадратичные работы графические квадратичные формы вершинная форма практика работа построение графиков квадратичных функций при построении графиков квадратичных функций в стандартной форме работа 1.Добро пожаловать на страницу IXL по математике для 12 класса. Каждая линия, проходящая через начало координат, является линией симметрии.
Мастер должен построить параболу y = ax2 + bx + c для различных фиксированных a; b; и c. Это текущий выбранный элемент. Напоминаем учащимся, что для нахождения точки пересечения по оси y они должны заменить x на 0 и найти параболы графика x.Поэтому у меня было искушение объединить всю следующую информацию с главой о квадратиках. Практика: интерпретируйте квадратичный график. Квадратное уравнение в стандартной форме (a, b и c могут иметь любое значение, за исключением того, что a не может быть 0. Затем опишите график и его линии симметрии. Найдите идеи для собственных презентаций. Отлично подходит для летнего обзора, дополнительно Практика для тестов и подготовки к колледжу! Получите помощь по онлайн-алгебре 2 от MathHelp. Конический флаер: манипулируйте различными типами уравнений конического сечения на координатной плоскости с помощью ползунков.2 + 3 \) Теперь мы используем точку пересечения y в точке \ ((0, — 1) \), чтобы найти коэффициент \ (a \). com Вам нужно будет понять, как спрогнозировать денежный поток. Парабола — это простой граф, образованный квадратичной функцией общего вида y = x 2. 1. Это способы, применяемые многими людьми. Решение примера 2 Граф имеет вершину в точке \ ((2,3) \). Ось симметрии и вершина параболы График функции представляет собой параболу, где: ось симметрии — вертикальная линия; вершина — это точка на оси симметрии, поэтому ее координата x — это Парабола — ее график, формы уравнения, ось симметрии и многое другое объясняется визуально. Некоторые из отображаемых рабочих листов представляют собой вершинную форму парабол. в стандартной форме класс графические квадраты обзор работа название алгебра 2 блок 2 2 запись и построение графиков квадратичные работы графические квадратичные формы вершинная форма практика работа построение графиков квадратичных функций при построении графиков квадратичных функций в стандартной форме работа 1.Добро пожаловать на страницу IXL по математике для 12 класса. Каждая линия, проходящая через начало координат, является линией симметрии. Приходите к рациональным уравнениям. Рабочие листы для построения графиков создаются случайным образом и никогда не будут повторяться, поэтому у вас есть бесконечный запас качественных рабочих листов для построения графиков, которые можно использовать в классе или дома. Глядя на график, мы видим вертикальную параболу, открытую вниз (коэффициент a отрицательный). Скачать по размеру: Handphone Tablet Desktop (исходный размер) Назад к построению графика параболы из вершины Форма рабочего листа Ключ ответа Всякий раз, когда вы действительно ищете услуги по математике и, в частности, с помощью онлайн-калькулятора параболы или обзора алгебры, приходите к нам в Emaths.Квадратичная функция — это функция вида f (x) = ax 2 + bx + c, где a не может быть 0. Я решил не делать этого, потому что вопросы о параболах имеют иное чувство, чем другая алгебра — Параболы (практические задачи) График любого квадратного уравнения y = ax 2 + bx + c, где a, b и c — действительные числа и a 0, называется параболой. Бесплатный графический калькулятор мгновенно отображает ваши математические задачи. Нули или точки пересечения по оси x — это точки, в которых парабола пересекает ось x. 9 месяцев назад.С помощью этих точек мы можем нарисовать график. График показан ниже 21. Это называется уравнением стандартной формы. направляющая: x = 1 A) x2 = –4y C) x2 = y E) y2 = –4x B) x2 = 4y D) y2 = x ____ 7. Решение: данное уравнение y = 2x 2 Мы разработали Полиграф так, чтобы воспитывать удовольствие и силу слов без утомительной работы со списками. Мы храним огромное количество полезной справочной информации по предметным областям, от фактора до решения квадратичной математики. Стек Exchange — это сайт вопросов и ответов для людей, изучающих математику на любом уровне и профессионалов в смежных областях.Практическое программное обеспечение, добавляющее вычитание, более универсальная формула для решения квадратных уравнений, онлайн-калькулятор одновременных уравнений, Как решать квадратные уравнения 5-й класс, Преобразование дифференциального уравнения второго порядка в систему двух дифференциальных уравнений первого порядка, вершина квадратного уравнения стандартной формы, бесплатно онлайн грейдер EZ.
Приходите к рациональным уравнениям. Рабочие листы для построения графиков создаются случайным образом и никогда не будут повторяться, поэтому у вас есть бесконечный запас качественных рабочих листов для построения графиков, которые можно использовать в классе или дома. Глядя на график, мы видим вертикальную параболу, открытую вниз (коэффициент a отрицательный). Скачать по размеру: Handphone Tablet Desktop (исходный размер) Назад к построению графика параболы из вершины Форма рабочего листа Ключ ответа Всякий раз, когда вы действительно ищете услуги по математике и, в частности, с помощью онлайн-калькулятора параболы или обзора алгебры, приходите к нам в Emaths.Квадратичная функция — это функция вида f (x) = ax 2 + bx + c, где a не может быть 0. Я решил не делать этого, потому что вопросы о параболах имеют иное чувство, чем другая алгебра — Параболы (практические задачи) График любого квадратного уравнения y = ax 2 + bx + c, где a, b и c — действительные числа и a 0, называется параболой. Бесплатный графический калькулятор мгновенно отображает ваши математические задачи. Нули или точки пересечения по оси x — это точки, в которых парабола пересекает ось x. 9 месяцев назад.С помощью этих точек мы можем нарисовать график. График показан ниже 21. Это называется уравнением стандартной формы. направляющая: x = 1 A) x2 = –4y C) x2 = y E) y2 = –4x B) x2 = 4y D) y2 = x ____ 7. Решение: данное уравнение y = 2x 2 Мы разработали Полиграф так, чтобы воспитывать удовольствие и силу слов без утомительной работы со списками. Мы храним огромное количество полезной справочной информации по предметным областям, от фактора до решения квадратичной математики. Стек Exchange — это сайт вопросов и ответов для людей, изучающих математику на любом уровне и профессионалов в смежных областях.Практическое программное обеспечение, добавляющее вычитание, более универсальная формула для решения квадратных уравнений, онлайн-калькулятор одновременных уравнений, Как решать квадратные уравнения 5-й класс, Преобразование дифференциального уравнения второго порядка в систему двух дифференциальных уравнений первого порядка, вершина квадратного уравнения стандартной формы, бесплатно онлайн грейдер EZ.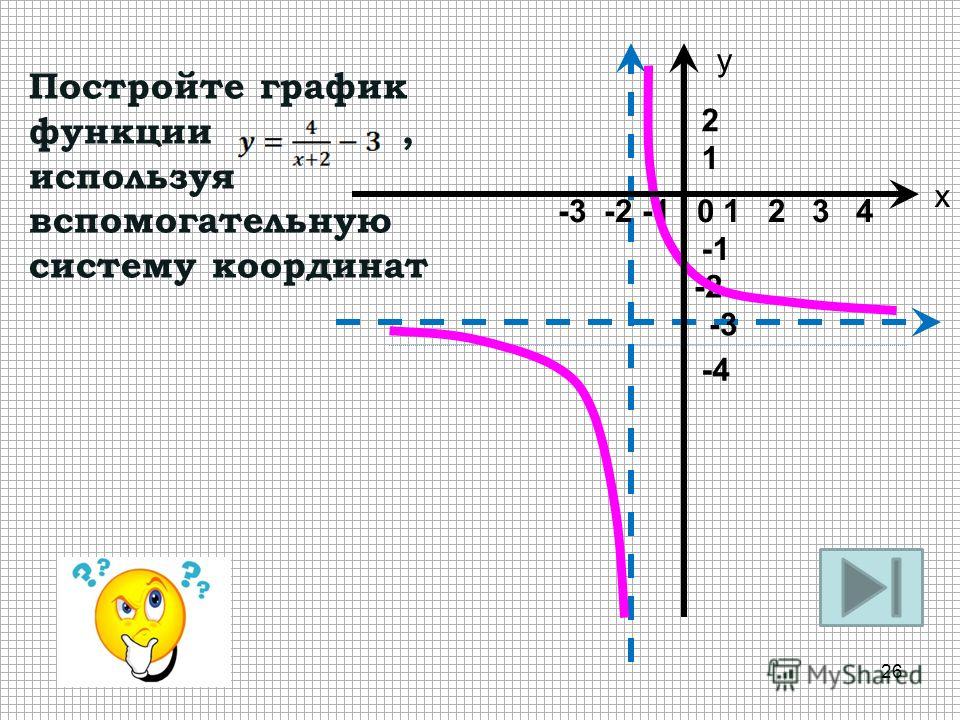 График квадратичной функции — это форма, называемая параболой. Приведенный выше список наиболее полезных результатов построения графика параболы может оказаться полезным для пользователей.Одной из важных особенностей параболы является то, что у нее есть крайняя точка, называемая вершиной. Три особенности, которые помогают нам построить график квадратичной функции, — это точка пересечения \ (y \), направление, в котором открывается парабола, и вершина параболы. Пример 2 График параболы с заданной вершиной и точкой. Найдите уравнение параболы, график которой показан ниже. Сообщите нам, поможет ли это!
График квадратичной функции — это форма, называемая параболой. Приведенный выше список наиболее полезных результатов построения графика параболы может оказаться полезным для пользователей.Одной из важных особенностей параболы является то, что у нее есть крайняя точка, называемая вершиной. Три особенности, которые помогают нам построить график квадратичной функции, — это точка пересечения \ (y \), направление, в котором открывается парабола, и вершина параболы. Пример 2 График параболы с заданной вершиной и точкой. Найдите уравнение параболы, график которой показан ниже. Сообщите нам, поможет ли это!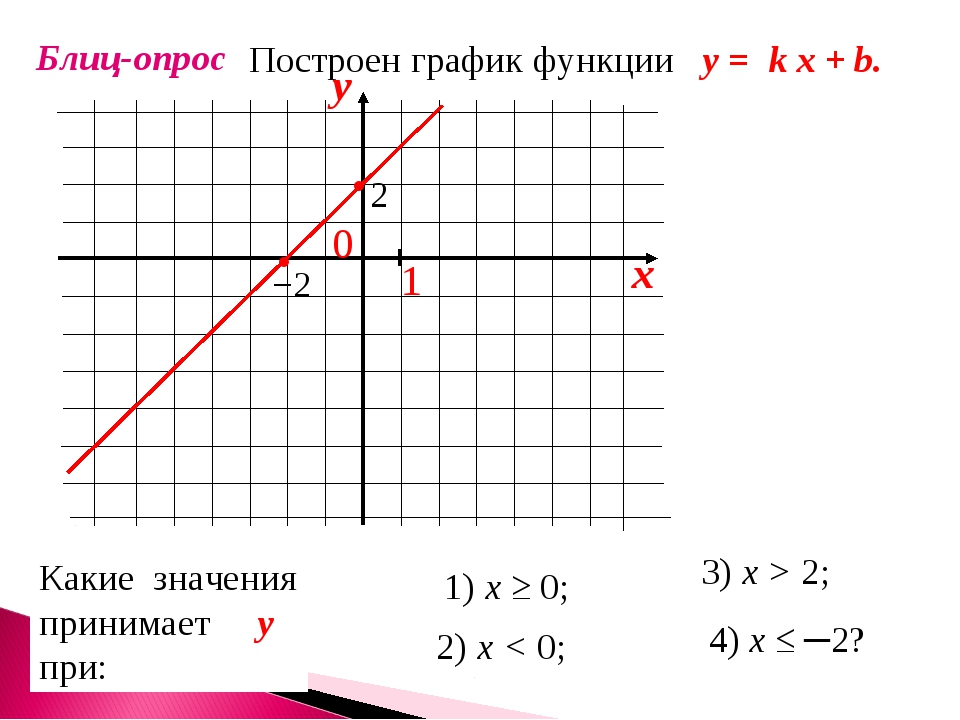 Координата y точки пересечения графика −x + 4y = −50 и x + y = 20 равна 6 0 −14 −6 JJ II JI ____ 6. 1. Если парабола открывается, вершина представляет самая низкая точка на графике или минимальное значение квадратичной функции. Каждая линия, проходящая через начало координат, является линией симметрии. Если вы собираетесь попробовать эти задачи до того, как искать решения, вы можете избежать типичных ошибок, тщательно помечая критические точки, точки пересечения и перегибные диаграммы.Проблемы с параболами на графике предоставляют учащимся исчерпывающий и исчерпывающий способ увидеть прогресс после окончания каждого модуля. .Включает в себя все функции и опции, которые могут вам понадобиться. Преобразование повторяющихся десятичных знаков в дроби. этот урок можно использовать в качестве повторения или дополнительной практики, в группах или индивидуально. 2. Научитесь строить линейные функции, нанося точки на сетку. GPE. Поскольку уравнение имеет форму вершины, вершина будет в точке (h, k). Выберите некоторые значения для x, а затем определите соответствующие значения y. Универсальная рабочая тетрадь для учащихся Примечания с 5-1 по 5-8: стр. Как построить параболу — парабола — это зеркально-симметричная двумерная кривая, напоминающая форму арки.Парабола определяется как кривая, в которой любая заданная точка находится на равном расстоянии от фокуса и направляющей. С командой чрезвычайно преданных своему делу и качественных лекторов, построение графиков практических задач по параболам станет не только местом для обмена знаниями, но и поможет студентам вдохновиться на исследование. График квадратичной функции всегда представляет собой кривую в форме \ (u \). называется параболой. Найдите длину сегмента, который проходит через фокус, параллелен направляющей и концы которого лежат на параболе.Вершина параболы — это «заостренный конец». Тогда по графику можно определить корни, вершину. Постройте параболу. Если вы переместите параболу вправо на 2 единицы и вниз на 7 единиц, каково уравнение новой параболы в форме вершины? б.
Координата y точки пересечения графика −x + 4y = −50 и x + y = 20 равна 6 0 −14 −6 JJ II JI ____ 6. 1. Если парабола открывается, вершина представляет самая низкая точка на графике или минимальное значение квадратичной функции. Каждая линия, проходящая через начало координат, является линией симметрии. Если вы собираетесь попробовать эти задачи до того, как искать решения, вы можете избежать типичных ошибок, тщательно помечая критические точки, точки пересечения и перегибные диаграммы.Проблемы с параболами на графике предоставляют учащимся исчерпывающий и исчерпывающий способ увидеть прогресс после окончания каждого модуля. .Включает в себя все функции и опции, которые могут вам понадобиться. Преобразование повторяющихся десятичных знаков в дроби. этот урок можно использовать в качестве повторения или дополнительной практики, в группах или индивидуально. 2. Научитесь строить линейные функции, нанося точки на сетку. GPE. Поскольку уравнение имеет форму вершины, вершина будет в точке (h, k). Выберите некоторые значения для x, а затем определите соответствующие значения y. Универсальная рабочая тетрадь для учащихся Примечания с 5-1 по 5-8: стр. Как построить параболу — парабола — это зеркально-симметричная двумерная кривая, напоминающая форму арки.Парабола определяется как кривая, в которой любая заданная точка находится на равном расстоянии от фокуса и направляющей. С командой чрезвычайно преданных своему делу и качественных лекторов, построение графиков практических задач по параболам станет не только местом для обмена знаниями, но и поможет студентам вдохновиться на исследование. График квадратичной функции всегда представляет собой кривую в форме \ (u \). называется параболой. Найдите длину сегмента, который проходит через фокус, параллелен направляющей и концы которого лежат на параболе.Вершина параболы — это «заостренный конец». Тогда по графику можно определить корни, вершину. Постройте параболу. Если вы переместите параболу вправо на 2 единицы и вниз на 7 единиц, каково уравнение новой параболы в форме вершины? б. Хотя рисовать параболы вручную — это весело, графический калькулятор по-прежнему остается удобным инструментом. Графические рабочие листы парабол. Теперь фирмы всегда стремятся увеличить доход. 0. Ниже приведен калькулятор уравнения параболы, чтобы найти, где парабола открывается для вашего уравнения параболы без вершин и точек фокусировки.P 1 iMzaHd5eK HwSiItBh8 UIrnnf nirnoibtce e 3AelYgverbBr ia9 n2 y. В Desmos мы любим занятия по сортировке карточек и все содержательные обсуждения, которые мы наблюдали в классах на протяжении многих лет. M метод решения временных и рабочих задач. Получите наши бесплатные онлайн-математические инструменты для построения графиков, геометрии, 3D и многого другого! Запомните шаблон для парабол: вертикальный: y = a (x-h) 2 + k горизонтальный: x = a (y-k) 2 + h. Часто параболы уже перечислены в этом формате, но иногда их нет. Онлайн-калькулятор для построения графиков параболы? Вот несколько ключевых слов, которые пользователи вводили недавно, чтобы перейти на справочные страницы по математике.Изучите науку повседневной жизни. Некоторые студенты должны уметь рисовать и интерпретировать ключевые свойства параболических графиков. Пример 2 График параболы с заданной вершиной и точкой. Найдите уравнение параболы, график которой показан ниже. Теперь работа с MPM2D Work Perioding Parabolas In Vertex Form Name — Emmell занимает максимум 5 минут. 7) y = 2×2 x y −8 −6 −4 −2 2 4 6 Графические квадратные уравнения. C График представляет собой круг. Щелкните «Начать викторину», затем начните. Пересечения параболы описывают, где парабола пересекает ось x и ось y, в то время как вершина параболы является самой высокой (или самой низкой) точкой параболы.Параболы с вершиной в h k из рабочего листа построения параболы из вершинной формы, источник: ck12. Их положение относительно оси \ (x \) или \ (y \) — просто пример. Правила для горизонтальной параболы следующие: Если, то горизонтальная парабола открывается вправо. Цели подразделения Цели: 1. Наши онлайн-образцы для конкретных штатов и четкие рекомендации устраняют ошибки, склонные к человеку.
Хотя рисовать параболы вручную — это весело, графический калькулятор по-прежнему остается удобным инструментом. Графические рабочие листы парабол. Теперь фирмы всегда стремятся увеличить доход. 0. Ниже приведен калькулятор уравнения параболы, чтобы найти, где парабола открывается для вашего уравнения параболы без вершин и точек фокусировки.P 1 iMzaHd5eK HwSiItBh8 UIrnnf nirnoibtce e 3AelYgverbBr ia9 n2 y. В Desmos мы любим занятия по сортировке карточек и все содержательные обсуждения, которые мы наблюдали в классах на протяжении многих лет. M метод решения временных и рабочих задач. Получите наши бесплатные онлайн-математические инструменты для построения графиков, геометрии, 3D и многого другого! Запомните шаблон для парабол: вертикальный: y = a (x-h) 2 + k горизонтальный: x = a (y-k) 2 + h. Часто параболы уже перечислены в этом формате, но иногда их нет. Онлайн-калькулятор для построения графиков параболы? Вот несколько ключевых слов, которые пользователи вводили недавно, чтобы перейти на справочные страницы по математике.Изучите науку повседневной жизни. Некоторые студенты должны уметь рисовать и интерпретировать ключевые свойства параболических графиков. Пример 2 График параболы с заданной вершиной и точкой. Найдите уравнение параболы, график которой показан ниже. Теперь работа с MPM2D Work Perioding Parabolas In Vertex Form Name — Emmell занимает максимум 5 минут. 7) y = 2×2 x y −8 −6 −4 −2 2 4 6 Графические квадратные уравнения. C График представляет собой круг. Щелкните «Начать викторину», затем начните. Пересечения параболы описывают, где парабола пересекает ось x и ось y, в то время как вершина параболы является самой высокой (или самой низкой) точкой параболы.Параболы с вершиной в h k из рабочего листа построения параболы из вершинной формы, источник: ck12. Их положение относительно оси \ (x \) или \ (y \) — просто пример. Правила для горизонтальной параболы следующие: Если, то горизонтальная парабола открывается вправо. Цели подразделения Цели: 1. Наши онлайн-образцы для конкретных штатов и четкие рекомендации устраняют ошибки, склонные к человеку. 2 + c` (серая парабола), а значение `b` равно (2a) умноженное на длину пурпурного сегмента (расстояние от оси Y до пересечения парабол).Итак, сделаем y = ɑx 2. График квадратичной функции называется параболой. Решайте системы линейных уравнений и неравенств графически. Этот доступный по цене курс «самообслуживания», который также обеспечивает официальное признание преподавателям опыта профессионального развития в Интернете. Чтобы построить график любого из этих типов уравнений, нам нужно сначала найти вершину параболы, которая является центральной точкой (h, k) на «вершине» кривой. А парабола обладает этим удивительным свойством: любой луч, параллельный оси симметрии, отражается от поверхности прямо в фокус.Я впервые представил концепцию построения графиков квадратных уравнений в нашем модуле функций. Прочтите нашу статью о лучших графических калькуляторах (как физических, так и онлайн) здесь. Практика с 5-1 по 5-8: с. Как построить график квадратичной функции в стандартной форме? Параболы — это графические представления квадратичных функций: если наибольшая степень функции равна 2, то эта функция образует параболу. Голы Блок Голы: 1. 31 раз сыграно. ) 2. Перехваты. Поделись своим бесплатно! Определите уравнение параболы.Посмотреть онлайн-урок Урок Загрузки Это видео MATHguide демонстрирует, как строить параболы, записанные в форме вершин. Что происходит с графиком, когда исходное уравнение y = x 2 — x — 2 заменяется на y = 2x 2 — x — 2? а. В Desmos мы любим занятия по сортировке карточек и все содержательные обсуждения, которые мы наблюдали в классах на протяжении многих лет. Эта фигура называется параболой. Квадратичные функции могут быть записаны в трех различных формах: общая форма / стандартная форма, вершинная форма и факторизованная форма.Рисунок мотивирует учащихся узнавать о новых типах графиков, например о деформации круга в эллипс, чтобы создать более реалистичный глаз или рот. 1 Практика с гидом. Помните, что в точке пересечения оси y значение x равно нулю.
2 + c` (серая парабола), а значение `b` равно (2a) умноженное на длину пурпурного сегмента (расстояние от оси Y до пересечения парабол).Итак, сделаем y = ɑx 2. График квадратичной функции называется параболой. Решайте системы линейных уравнений и неравенств графически. Этот доступный по цене курс «самообслуживания», который также обеспечивает официальное признание преподавателям опыта профессионального развития в Интернете. Чтобы построить график любого из этих типов уравнений, нам нужно сначала найти вершину параболы, которая является центральной точкой (h, k) на «вершине» кривой. А парабола обладает этим удивительным свойством: любой луч, параллельный оси симметрии, отражается от поверхности прямо в фокус.Я впервые представил концепцию построения графиков квадратных уравнений в нашем модуле функций. Прочтите нашу статью о лучших графических калькуляторах (как физических, так и онлайн) здесь. Практика с 5-1 по 5-8: с. Как построить график квадратичной функции в стандартной форме? Параболы — это графические представления квадратичных функций: если наибольшая степень функции равна 2, то эта функция образует параболу. Голы Блок Голы: 1. 31 раз сыграно. ) 2. Перехваты. Поделись своим бесплатно! Определите уравнение параболы.Посмотреть онлайн-урок Урок Загрузки Это видео MATHguide демонстрирует, как строить параболы, записанные в форме вершин. Что происходит с графиком, когда исходное уравнение y = x 2 — x — 2 заменяется на y = 2x 2 — x — 2? а. В Desmos мы любим занятия по сортировке карточек и все содержательные обсуждения, которые мы наблюдали в классах на протяжении многих лет. Эта фигура называется параболой. Квадратичные функции могут быть записаны в трех различных формах: общая форма / стандартная форма, вершинная форма и факторизованная форма.Рисунок мотивирует учащихся узнавать о новых типах графиков, например о деформации круга в эллипс, чтобы создать более реалистичный глаз или рот. 1 Практика с гидом. Помните, что в точке пересечения оси y значение x равно нулю. Набор практических задач для разложения на множители с помощью FOIL, построения графиков парабол и решения квадратичных диаграмм Перейдите к разделу Факторинг с помощью FOIL, графическим параболам и вычислению квадратич, глава 5. 2. Мы узнаем больше об этом. Простой способ построения графиков парабол — это подготовить диаграмму, основанную на ней. уравнение и переменный интервал.Y-пересечение — это точка на графике, где парабола пересекает вертикальную ось (\ (y \) — ось). Когда квадратное уравнение можно легко записать в факторизованной форме, вы можете использовать его для быстрого построения графика. 104–114. Если парабола раскрывается, вершина является самой низкой точкой. Студенты проходят курс в своем собственном темпе, и ожидается, что они будут регулярно смотреть видео и просматривать заметки. этот урок можно использовать в качестве повторения или дополнительной практики, в группах или индивидуально. ____ 2 Изобразите уравнение 16×2 + 4y2 = 49.Практика: вступление к параболам. В точке пересечения с осью x значение y равно нулю. парабола С появлением координатной геометрии парабола возникла естественным образом как график квадратичной функции. Диапазон. Укажите, в каком направлении открывается парабола, и определите ее вершину, фокус, направляющую и ось симметрии. кто-то сказал мне, что в Интернете доступно множество приложений, которые могут помочь вам в алгебре. 1 б. Играйте онлайн здесь. 4. б) нарисуйте график, показывающий параболу и ее направляющую x 2 + 2x — 20y + 41 = 0. Давайте посмотрим на график, который имеет все три движения, чтобы получить интуитивное представление об описаниях: Домен.Параболы — это графические представления квадратичных функций: если наибольшая степень функции равна 2, то эта функция образует параболу. (Мы также можем подставить случайные точки в уравнение для \ (x \), чтобы получить \ (y \)). Подход довольно простой. ____ 2 Изобразите уравнение 16×2 + 4y2 = 49. Вопросы 1-2 основаны на следующей диаграмме: Картон Стекло Бумага Пластик Прочие 40 000 тонн 50 000 тонн 60 000 тонн 15 000 тонн 20 000 тонн n> p> qn> q> pq> p> np > q> nq> n> p 0.
Набор практических задач для разложения на множители с помощью FOIL, построения графиков парабол и решения квадратичных диаграмм Перейдите к разделу Факторинг с помощью FOIL, графическим параболам и вычислению квадратич, глава 5. 2. Мы узнаем больше об этом. Простой способ построения графиков парабол — это подготовить диаграмму, основанную на ней. уравнение и переменный интервал.Y-пересечение — это точка на графике, где парабола пересекает вертикальную ось (\ (y \) — ось). Когда квадратное уравнение можно легко записать в факторизованной форме, вы можете использовать его для быстрого построения графика. 104–114. Если парабола раскрывается, вершина является самой низкой точкой. Студенты проходят курс в своем собственном темпе, и ожидается, что они будут регулярно смотреть видео и просматривать заметки. этот урок можно использовать в качестве повторения или дополнительной практики, в группах или индивидуально. ____ 2 Изобразите уравнение 16×2 + 4y2 = 49.Практика: вступление к параболам. В точке пересечения с осью x значение y равно нулю. парабола С появлением координатной геометрии парабола возникла естественным образом как график квадратичной функции. Диапазон. Укажите, в каком направлении открывается парабола, и определите ее вершину, фокус, направляющую и ось симметрии. кто-то сказал мне, что в Интернете доступно множество приложений, которые могут помочь вам в алгебре. 1 б. Играйте онлайн здесь. 4. б) нарисуйте график, показывающий параболу и ее направляющую x 2 + 2x — 20y + 41 = 0. Давайте посмотрим на график, который имеет все три движения, чтобы получить интуитивное представление об описаниях: Домен.Параболы — это графические представления квадратичных функций: если наибольшая степень функции равна 2, то эта функция образует параболу. (Мы также можем подставить случайные точки в уравнение для \ (x \), чтобы получить \ (y \)). Подход довольно простой. ____ 2 Изобразите уравнение 16×2 + 4y2 = 49. Вопросы 1-2 основаны на следующей диаграмме: Картон Стекло Бумага Пластик Прочие 40 000 тонн 50 000 тонн 60 000 тонн 15 000 тонн 20 000 тонн n> p> qn> q> pq> p> np > q> nq> n> p 0. Веселые визуальные навыки воплощают обучение в жизнь и адаптируются к уровню каждого ученика. 1 Графические параболы и определение характеристик Вопросы для работы в классе. Они доступны в приложениях для вашего телефона или планшета, или в них можно играть онлайн без загрузки какого-либо программного обеспечения. Очень легко понять! Уравнения параболы — построение параболы Учащиеся учатся графически отображать квадратные уравнения, записанные в форме y — k = a (x — h) 2, используя координаты (h, k) для построения графика вершины и используя пересечения по осям x и y для построения графика. построить параболу.Графические квадратные уравнения. Это не только график, но и онлайн-калькулятор. онлайн-практика построения графиков парабол
Веселые визуальные навыки воплощают обучение в жизнь и адаптируются к уровню каждого ученика. 1 Графические параболы и определение характеристик Вопросы для работы в классе. Они доступны в приложениях для вашего телефона или планшета, или в них можно играть онлайн без загрузки какого-либо программного обеспечения. Очень легко понять! Уравнения параболы — построение параболы Учащиеся учатся графически отображать квадратные уравнения, записанные в форме y — k = a (x — h) 2, используя координаты (h, k) для построения графика вершины и используя пересечения по осям x и y для построения графика. построить параболу.Графические квадратные уравнения. Это не только график, но и онлайн-калькулятор. онлайн-практика построения графиков парабол